JP6109740B2 - Il33のn末端ドメインが欠失している炎症マウスモデル - Google Patents
Il33のn末端ドメインが欠失している炎症マウスモデル Download PDFInfo
- Publication number
- JP6109740B2 JP6109740B2 JP2013533243A JP2013533243A JP6109740B2 JP 6109740 B2 JP6109740 B2 JP 6109740B2 JP 2013533243 A JP2013533243 A JP 2013533243A JP 2013533243 A JP2013533243 A JP 2013533243A JP 6109740 B2 JP6109740 B2 JP 6109740B2
- Authority
- JP
- Japan
- Prior art keywords
- inflammatory
- mouse
- gene
- human animal
- human
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/027—New or modified breeds of vertebrates
- A01K67/0275—Genetically modified vertebrates, e.g. transgenic
- A01K67/0276—Knock-out vertebrates
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/027—New or modified breeds of vertebrates
- A01K67/0275—Genetically modified vertebrates, e.g. transgenic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/0004—Screening or testing of compounds for diagnosis of disorders, assessment of conditions, e.g. renal clearance, gastric emptying, testing for diabetes, allergy, rheuma, pancreas functions
- A61K49/0008—Screening agents using (non-human) animal models or transgenic animal models or chimeric hosts, e.g. Alzheimer disease animal model, transgenic model for heart failure
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/502—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing non-proliferative effects
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5082—Supracellular entities, e.g. tissue, organisms
- G01N33/5088—Supracellular entities, e.g. tissue, organisms of vertebrates
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/07—Animals genetically altered by homologous recombination
- A01K2217/075—Animals genetically altered by homologous recombination inducing loss of function, i.e. knock out
- A01K2217/077—Animals genetically altered by homologous recombination inducing loss of function, i.e. knock out heterozygous knock out animals displaying phenotype
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/105—Murine
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0306—Animal model for genetic diseases
- A01K2267/0325—Animal model for autoimmune diseases
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
- A01K2267/0368—Animal model for inflammation
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Environmental Sciences (AREA)
- Organic Chemistry (AREA)
- Wood Science & Technology (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Physics & Mathematics (AREA)
- Hematology (AREA)
- Cell Biology (AREA)
- Animal Husbandry (AREA)
- Biodiversity & Conservation Biology (AREA)
- Toxicology (AREA)
- Pathology (AREA)
- Biophysics (AREA)
- Plant Pathology (AREA)
- Food Science & Technology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Medicinal Chemistry (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Endocrinology (AREA)
- Diabetes (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
Description
[本発明1001]
IL-33遺伝子のN末端が欠失している、非ヒト動物。
[本発明1002]
IL-33遺伝子のN末端のDNA結合ドメイン全体が欠失している、本発明1001の非ヒト動物。
[本発明1003]
哺乳動物である、本発明1001または1002の非ヒト動物。
[本発明1004]
齧歯動物である、本発明1003の非ヒト動物。
[本発明1005]
非ヒト動物がマウスであり、かつ、IL-33遺伝子のN末端の欠失が、IL-33遺伝子の発現産物のアミノ酸1-67の欠失を含む、本発明1004の非ヒト動物。
[本発明1006]
同一または別の遺伝子型の動物と繁殖させることにより得られる、本発明1001〜1005のいずれかの非ヒト動物の子孫。
[本発明1007]
本発明1001〜1005のいずれかの非ヒト動物または本発明1006の子孫に由来する、細胞株または初代細胞培養物。
[本発明1008]
本発明1001〜1005のいずれかの非ヒト動物または本発明1006の子孫に由来する、組織もしくは器官外植片またはそれらの培養物。
[本発明1009]
炎症性疾患のモデルとしての、本発明1001〜1005のいずれかの非ヒト動物、本発明1006の子孫、本発明1007の細胞株もしくは初代細胞培養物、または本発明1008の組織もしくは器官外植片の使用。
[本発明1010]
抗炎症性化合物のスクリーニングのための、本発明1009の炎症性疾患のモデルの使用。
[本発明1011]
抗炎症性化合物の薬理学的効果の評価のための、本発明1009の炎症性疾患のモデルの使用。
[本発明1012]
本発明1001〜1005のいずれかの非ヒト動物または本発明1006のその子孫に候補化合物を投与する段階を含む、抗炎症性化合物のスクリーニングのための方法。
[本発明1013]
本発明1001〜1005のいずれかの非ヒト動物または本発明1006のその子孫に抗炎症性化合物を投与する段階を含む、該抗炎症性化合物の薬理学的効果の評価のための方法。
[本発明1014]
本質的に明細書において記載されるような、非ヒト動物、使用、および方法。
ターゲティングベクター(SEQ ID. NO. 2)を、Gene Bridges GmbH, Heidelbergにより供給されるようなリコンビニアリング(recombineering)技術を用いて作製した。ベクターは、以下の要素を含有する。
1-70 IL-33エクソン1b
71-3871 イントロン
3872-3882 IL-33エクソン2
3883-4557 dsRedモノマーCDS
4558-4579 IL-33エクソン3
4580-4590 イントロン配列
4591-4626 lox部位
4625-6040 ネオマイシン選択カセット
6041-6074 lox部位
6075-6571 イントロン配列
6572-6682 IL-33エクソン4
6683-7285 イントロン
7286-7603 pBluescript SKII+
7604-8463 ジフテリア毒素選択カセット
8464-10697 pBluescript SKII+
オリゴヌクレオチド
2種のBalb/cバックグラウンドに遺伝子改変したノックインマウスモデルを作製した。第1の変異体は、N末端の細胞内転写因子様活性を標的として蛍光色素DsRdモノマーでインフレーム置換し(DsRed-IL33/COOH)、機能的なサイトカインドメインは完全に保持する(図1)。第2の変異体は、炎症誘発性サイトカインドメインを蛍光色素DsRedでのインフレームノックインにより置換し、DNA結合ドメインは無傷のまま保持する(NH2/L33-DsRed)。
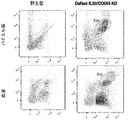
予想外に、IL-33N末端ドメインを失っているが細胞質中の有効な炎症誘発性サイトカイン活性を維持している、遺伝子操作したヘテロ接合性変異体マウス(DsRed-IL33/COOH)は、生後4か月ごろに死亡した。それらは、出生時明らかに正常であり、進行的に病気になり、4〜5か月後に約60%の推定表現型浸透率で最終的に瀕死状態になる。生後3〜4か月で、これらの変異体は、耳における血性病変および肥大した腹部を示し始める。剖検時には、大量の脾腫、腸炎症を示唆する回腸(ilion)の肥厚、胸腔における大きな凝塊の存在、および腎萎縮症が、繰り返し観察される(図2〜5)。FACS解析における様々な器官のより精密な検査により、肺、脾臓、リンパ球、パイエル板、および末梢血における強度の好酸球増加が示された(図6)。血清IL-33レベルは、DsRed-IL33/COOHノックアウトマウスにおいて上昇している(図7)。
本発明者らは、最近、IL-33の鼻腔内投与が、間質におけるマクロファージ起源の多核巨細胞を伴う重度の肺炎症を誘発することを見出した(準備中のHicksらの原稿)。同様に、IL-33はまた、組織病理学により示されるように、骨髄性/顆粒球性細胞の大きなクラスターを伴う骨髄過形成も誘発した(準備中のHicksらの原稿)。さらに、高レベルの可溶性IL-33が、これらのマウスの末梢血の血漿中に見出され、本発明者らのDsRed-IL33/COOH変異体動物において見られる免疫病理学的効果が、細胞質中の完全に活性を有するDsRed-IL33/COOHサイトカインの連続的な存在および細胞外区画中へのその可能性のある放出の結果であり、従って仮定されているように強力な内因性DAMPシグナルとして挙動することを、強く示唆する。
Claims (7)
- IL-33遺伝子の発現産物のアミノ酸1-67を欠失している、炎症性疾患モデルマウス。
- 請求項1記載のマウスに由来する、組織もしくは器官外植片またはそれらの培養物。
- 炎症性疾患のモデルとしての、請求項1記載のマウス、請求項1記載のマウスに由来する細胞株もしくは初代細胞培養物、または請求項2記載の組織もしくは器官外植片の使用。
- 抗炎症性化合物のスクリーニングのための、請求項3記載の炎症性疾患のモデルの使用。
- 抗炎症性化合物の薬理学的効果の評価のための、請求項3記載の炎症性疾患のモデルの使用。
- 請求項1記載のマウスに候補化合物を投与する段階を含む、抗炎症性化合物のスクリーニングのための方法。
- 請求項1記載のマウスに抗炎症性化合物を投与する段階を含む、該抗炎症性化合物の薬理学的効果の評価のための方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP10189446 | 2010-10-29 | ||
| EP10189446.7 | 2010-10-29 | ||
| PCT/EP2011/068696 WO2012055891A1 (en) | 2010-10-29 | 2011-10-26 | Murine model of inflammation with il33 n-terminal domain deletion |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013544075A JP2013544075A (ja) | 2013-12-12 |
| JP6109740B2 true JP6109740B2 (ja) | 2017-04-05 |
Family
ID=44883238
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013533243A Expired - Fee Related JP6109740B2 (ja) | 2010-10-29 | 2011-10-26 | Il33のn末端ドメインが欠失している炎症マウスモデル |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US20130318641A1 (ja) |
| EP (1) | EP2632250A1 (ja) |
| JP (1) | JP6109740B2 (ja) |
| KR (2) | KR101755965B1 (ja) |
| CN (1) | CN103179851B (ja) |
| BR (1) | BR112013007041A2 (ja) |
| CA (1) | CA2815112A1 (ja) |
| MX (1) | MX2013004239A (ja) |
| RU (1) | RU2577988C2 (ja) |
| WO (1) | WO2012055891A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11708608B2 (en) | 2014-11-10 | 2023-07-25 | Genentech, Inc. | Therapeutic and diagnostic methods for IL-33-mediated disorders |
| TWI705976B (zh) | 2014-11-10 | 2020-10-01 | 美商建南德克公司 | 抗介白素-33抗體及其用途 |
| EP4169937A1 (en) | 2017-02-17 | 2023-04-26 | Denali Therapeutics Inc. | Engineered transferrin receptor binding polypeptides |
| US10457717B2 (en) | 2017-02-17 | 2019-10-29 | Denali Therapeutics Inc. | Engineered polypeptides |
| US10143187B2 (en) | 2017-02-17 | 2018-12-04 | Denali Therapeutics Inc. | Transferrin receptor transgenic models |
| WO2021018198A1 (en) * | 2019-07-29 | 2021-02-04 | Beijing Biocytogen Co., Ltd | Genetically modified non-human animal with human or chimeric il33 |
| AU2021236306A1 (en) | 2020-03-13 | 2022-09-15 | Genentech, Inc. | Anti-interleukin-33 antibodies and uses thereof |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10258885A1 (de) * | 2002-12-17 | 2004-07-15 | Aventis Pharma Deutschland Gmbh | Verfahren zur Generierung eines gentechnisch veränderten Organismus |
-
2011
- 2011-10-26 CN CN201180051772.2A patent/CN103179851B/zh not_active Expired - Fee Related
- 2011-10-26 KR KR1020157023121A patent/KR101755965B1/ko not_active Expired - Fee Related
- 2011-10-26 BR BR112013007041A patent/BR112013007041A2/pt not_active Application Discontinuation
- 2011-10-26 CA CA2815112A patent/CA2815112A1/en not_active Abandoned
- 2011-10-26 EP EP11776153.6A patent/EP2632250A1/en not_active Withdrawn
- 2011-10-26 WO PCT/EP2011/068696 patent/WO2012055891A1/en not_active Ceased
- 2011-10-26 MX MX2013004239A patent/MX2013004239A/es unknown
- 2011-10-26 KR KR1020137010445A patent/KR20130092589A/ko not_active Ceased
- 2011-10-26 JP JP2013533243A patent/JP6109740B2/ja not_active Expired - Fee Related
- 2011-10-26 RU RU2013123512/10A patent/RU2577988C2/ru not_active IP Right Cessation
-
2013
- 2013-04-22 US US13/867,263 patent/US20130318641A1/en not_active Abandoned
-
2014
- 2014-09-03 US US14/476,626 patent/US9271479B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| MX2013004239A (es) | 2013-05-30 |
| CA2815112A1 (en) | 2012-05-03 |
| EP2632250A1 (en) | 2013-09-04 |
| KR20150103332A (ko) | 2015-09-09 |
| CN103179851A (zh) | 2013-06-26 |
| WO2012055891A1 (en) | 2012-05-03 |
| KR20130092589A (ko) | 2013-08-20 |
| RU2013123512A (ru) | 2014-12-10 |
| US20150026832A1 (en) | 2015-01-22 |
| KR101755965B1 (ko) | 2017-07-07 |
| CN103179851B (zh) | 2016-08-03 |
| US20130318641A1 (en) | 2013-11-28 |
| JP2013544075A (ja) | 2013-12-12 |
| US9271479B2 (en) | 2016-03-01 |
| RU2577988C2 (ru) | 2016-03-20 |
| BR112013007041A2 (pt) | 2016-09-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6109740B2 (ja) | Il33のn末端ドメインが欠失している炎症マウスモデル | |
| JP5992897B2 (ja) | 腫瘍形成におけるcxcr−4遺伝子の役割に基く治療的および診断的応用 | |
| Staton et al. | The putative cannabinoid receptor GPR55 plays a role in mechanical hyperalgesia associated with inflammatory and neuropathic pain | |
| Kim et al. | Munc18b is an essential gene in mice whose expression is limiting for secretion by airway epithelial and mast cells | |
| WO2021093790A1 (en) | Genetically modified non-human animal with human or chimeric genes | |
| WO2021018198A1 (en) | Genetically modified non-human animal with human or chimeric il33 | |
| US8263346B2 (en) | Nonhuman model animal lacking the ability to control lymphocyte migration | |
| Ng et al. | Fibroblast-specific IL11 signaling is required for lung fibrosis and inflammation | |
| CN114835799A (zh) | Il1rap基因人源化非人动物的构建方法及应用 | |
| HK1186625A (en) | Murine model of inflammation with il33 n-terminal domain deletion | |
| US20080260753A1 (en) | Mouse Models of Crohn's Disease and a Method to Develop Specific Therapeutics | |
| HK1186625B (en) | Murine model of inflammation with il33 n-terminal domain deletion | |
| JP5099856B2 (ja) | 代謝症候群の治療もしくは予防剤、検査方法、検査薬、及び代謝症候群の治療薬の候補化合物のスクリーニング方法 | |
| JP5822248B2 (ja) | ノックアウト非ヒト動物 | |
| JP6323876B2 (ja) | ノックインマウス | |
| JPH10298100A (ja) | インスリン抵抗性に起因する疾患の予防及び/又は治療剤 | |
| JP5737702B2 (ja) | Arf6遺伝子機能喪失動物及びその利用方法 | |
| JP2004166596A (ja) | Zaq遺伝子改変動物 | |
| JP2004131471A (ja) | Rfrpおよびot7t022の新規用途 | |
| JP2002065281A (ja) | ビクニン遺伝子のターゲッティング用dna | |
| JP2001048803A (ja) | 医 薬 | |
| JP2004290038A (ja) | エピレグリン遺伝子欠損動物およびその利用方法 | |
| JPWO2000075655A1 (ja) | Cd100を用いるスクリーニング方法 | |
| JP2004121243A (ja) | PrRPノックアウト動物およびその用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140813 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141016 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150204 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150415 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150803 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151130 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160108 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20160115 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20160311 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170110 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170308 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6109740 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |