JP6097388B2 - インフルエンザにおけるリスクの階層化 - Google Patents
インフルエンザにおけるリスクの階層化 Download PDFInfo
- Publication number
- JP6097388B2 JP6097388B2 JP2015520775A JP2015520775A JP6097388B2 JP 6097388 B2 JP6097388 B2 JP 6097388B2 JP 2015520775 A JP2015520775 A JP 2015520775A JP 2015520775 A JP2015520775 A JP 2015520775A JP 6097388 B2 JP6097388 B2 JP 6097388B2
- Authority
- JP
- Japan
- Prior art keywords
- ifi27
- gene product
- patient
- level
- influenza
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/70—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving virus or bacteriophage
- C12Q1/701—Specific hybridization probes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/6851—Quantitative amplification
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6863—Cytokines, i.e. immune system proteins modifying a biological response such as cell growth proliferation or differentiation, e.g. TNF, CNF, GM-CSF, lymphotoxin, MIF or their receptors
- G01N33/6866—Interferon
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/112—Disease subtyping, staging or classification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/136—Screening for pharmacological compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/005—Assays involving biological materials from specific organisms or of a specific nature from viruses
- G01N2333/08—RNA viruses
- G01N2333/11—Orthomyxoviridae, e.g. influenza virus
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/46—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans from vertebrates
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/52—Assays involving cytokines
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2469/00—Immunoassays for the detection of microorganisms
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
Description
インフルエンザ/肺炎は、米国における死因の上位10位中8位にランクすると報告されている。インフルエンザウイルス感染症は、毎年、世界全体で最も多くの人々に罹患する最も一般的な感染疾患を表す。インフルエンザは、季節性の流行時には世界全体に急速に広がって、入院という相当な負荷を課す。世界全体で評価することは難しいが、世界保健機構(WHO)は、年間の流行時の有病率が、重度の疾患で300万から500万例であり、および世界全体での死亡率は年間250,000から500,000例であると推定している。WHOによれば、アメリカにおいて、インフルエンザの流行は、上気道感染症を有するアメリカ人集団の5〜15%に影響を及ぼし、入院および死亡は主に高リスク群(高齢者および慢性疾患を有する人など)で起こり、結果としてアメリカ経済が被るその費用は年間710〜1670億ドルに上ると推定されている。先進国におけるインフルエンザによる死亡の多くは年齢65歳以上の高齢者に起こっている。結果として起こる経済的費用と共に、感染症が流行すること、および患者の苦痛に関するその潜在的重症度により、感染症を検出して処置することは、医療制度の中でも優先順位が高い。
本発明者らは、患者が重度の疾患のいかなる徴候も示す前に、病院または臨床環境での医学的介入をおそらく必要とするインフルエンザ患者(患者が確認されているおよび/または症候性であるか否かによらず)と、おそらく安全に自宅に戻ることができる患者とを識別することができる方法があれば、医師がより良い処置の決定を下すのを大きく補助するであろうと認識している。
のプライマー配列、または同じ標的配列を増幅することができるその配列変種の1つまたは両方を利用してもよい。1つの態様において、ポリメラーゼ連鎖反応は、
のプライマー配列、または同じ標的配列を増幅することができるその配列変種の1つまたは両方を利用してもよい。
に結合する。
略語RSVは、本明細書においてRSウイルスに関して用いられる。
本明細書において用いられる、単数形「1つの」、「1つの(an)」、および「その」は、本文が明らかにそれ以外であることを示している場合を除き、複数形を含む。
インフルエンザ感染症を有するまたは有することが疑われる患者における臨床的リスクを同定するための方法であって、該患者由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子の発現レベルを決定する段階、および決定されたIFI27遺伝子産物レベルを標準レベルと比較する段階を含む、方法。
[本発明1002]
IFI27遺伝子産物の標準レベルが臨床的リスクなしを示しており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、本発明1001の方法。
[本発明1003]
標準レベルが、健康な対象、インフルエンザに感染した無症候性の対象、またはインフルエンザに感染しているが重度の疾患を発症していない対象におけるIFI27遺伝子産物レベルに基づく、本発明1002の方法。
[本発明1004]
IFI27遺伝子産物の標準レベルが臨床的リスクを示しており、標準レベルと比較して患者の試料中の同等であるかまたは高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、本発明1001の方法。
[本発明1005]
標準レベルが、健康な対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、本発明1001の方法。
[本発明1006]
標準レベルが、インフルエンザウイルスに感染した無症候性の対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、本発明1001の方法。
[本発明1007]
標準レベルが、患者由来の生物試料中のIFI27遺伝子の発現レベルの決定と同時に調製される、本発明1001〜1006のいずれかの方法。
[本発明1008]
標準レベルより少なくとも40倍から60倍高いIFI27遺伝子産物レベルが臨床的リスクを示す、本発明1005または1006の方法。
[本発明1009]
標準レベルより少なくとも40倍高いIFI27遺伝子産物レベルが臨床的リスクを示す、本発明1008の方法。
[本発明1010]
標準レベルより少なくとも50倍高いIFI27遺伝子産物レベルが臨床的リスクを示す、本発明1008の方法。
[本発明1011]
標準レベルより少なくとも60倍高いIFI27遺伝子産物レベルが臨床的リスクを示す、本発明1008の方法。
[本発明1012]
標準レベルが、IFI27遺伝子産物の1つまたは複数の既知試料を、患者由来の生物試料と同じIFI27遺伝子発現レベルの決定法に供することによって調製され、IFI27遺伝子産物の1つまたは複数の既知試料が、臨床的リスクを示すある既定量または複数の既定量の試料であり、標準レベルと比較して患者の試料中の同等であるかまたは高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、本発明1001の方法。
[本発明1013]
標準レベルが、IFI27遺伝子産物の1つまたは複数の既知試料を、患者由来の生物試料と同じIFI27遺伝子発現レベルの決定法に供することによって調製され、IFI27遺伝子産物の1つまたは複数の既知試料が、臨床的リスクなしを示すある既定量または複数の既定量の試料であり、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、本発明1001の方法。
[本発明1014]
患者由来の第一の生物試料中のIFI27遺伝子の発現レベルを決定する段階、および患者由来の第二の生物試料中のIFI27遺伝子の発現レベルを決定する段階であって、第一および第二の試料が異なる時期に患者から得られる、段階、ならびに
第一および第二の試料中のIFI27の相対的発現レベルに基づいて患者の状態を評価する段階
を含む、インフルエンザを有する患者の進行をモニターする方法
を提供する、本発明1001の方法。
[本発明1015]
第一の生物試料と比較した第二の生物試料中のIFI27遺伝子の発現レベルの増加が、患者における臨床的リスクの増加を示す、本発明1014の方法。
[本発明1016]
第一の生物試料と比較した第二の生物試料中のIFI27遺伝子の発現レベルの低下が、患者における臨床的リスクの低下を示す、本発明1014の方法。
[本発明1017]
患者由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子の発現レベルを決定する段階、および決定されたIFI27遺伝子産物レベルを標準レベルと比較する段階を含む、患者におけるインフルエンザまたはウイルス性肺炎を同定するための方法。
[本発明1018]
標準レベルが、健康な対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27レベルが、患者におけるインフルエンザまたはウイルス性肺炎を示す、本発明1017の方法。
[本発明1019]
患者がウイルス性肺炎または細菌性肺炎を有することが疑われる、本発明1017の方法。
[本発明1020]
標準レベルが、細菌性肺炎を有する対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎を有する患者であることを示す、本発明1017の方法。
[本発明1021]
標準レベルより少なくとも10倍高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎を示す、本発明1018〜1020のいずれかの方法。
[本発明1022]
標準レベルより少なくとも40倍から60倍高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎および臨床的リスクを有する患者を示す、本発明1018〜1020のいずれかの方法。
[本発明1023]
標準レベルより少なくとも40倍高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎および臨床的リスクを有する患者を示す、本発明1022の方法。
[本発明1024]
標準レベルより少なくとも50倍高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎および臨床的リスクを有する患者を示す、本発明1022の方法。
[本発明1025]
標準レベルより少なくとも60倍高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎および臨床的リスクを有する患者を示す、本発明1022の方法。
[本発明1026]
生物試料中の少なくとも1つの追加の遺伝子の発現レベルを決定する段階をさらに含む、本発明1001〜1025のいずれかの方法。
[本発明1027]
少なくとも1つの追加の遺伝子が、その発現が構成的である遺伝子である、本発明1026の方法。
[本発明1028]
少なくとも1つの追加の遺伝子がGAPDH遺伝子である、本発明1027の方法。
[本発明1029]
生物試料が、血液、または血球サブセットなどその成分である、本発明1001〜1028のいずれかの方法。
[本発明1030]
生物試料に、IFI27遺伝子産物に結合することができる物質を接触させる段階、および該物質とIFI27遺伝子産物との結合を検出する段階を含む、本発明1001〜1029のいずれかの方法。
[本発明1031]
生物試料がRNA、mRNA、cDNA、またはタンパク質である、本発明1001〜1030のいずれかの方法。
[本発明1032]
IFI27遺伝子産物が、IFI27 mRNAまたはその断片である、本発明1001〜1031のいずれかの方法。
[本発明1033]
IFI27遺伝子産物が、SEQ ID NO:1の核酸配列またはその断片もしくは変種、またはSEQ ID NO:2の核酸配列またはその断片もしくは変種を含む、本発明1001〜1032のいずれかの方法。
[本発明1034]
IFI27遺伝子産物が、IFI27ポリペプチドまたはその断片もしくは変種である、本発明1001〜1031のいずれかの方法。
[本発明1035]
IFI27遺伝子産物が、SEQ ID NO:3の配列を含むアミノ酸配列またはその断片もしくは変種、またはSEQ ID NO:4の配列を含むアミノ酸配列またはその断片もしくは変種を含む、本発明1034の方法。
[本発明1036]
mRNAのcDNAへの逆転写を含む、本発明1001〜1033のいずれかの方法。
[本発明1037]
試料のIFI27核酸配列の増幅および増幅された配列の検出を含む、本発明1001〜1033または1036のいずれかの方法。
[本発明1038]
定量的ポリメラーゼ連鎖反応(qPCR)を含む、本発明1001〜1033、1036、または1037のいずれかの方法。
[本発明1039]
ポリメラーゼ連鎖反応が、(i)SEQ ID NO:1、(ii)SEQ ID NO:2、(iii)SEQ ID NO:5、(iv)SEQ ID NO:6の配列、および(v)またはSEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:5、SEQ ID NO:6のいずれかの断片または変種から選択される核酸配列を増幅することができる1つまたは複数のプライマーを利用する、本発明1038の方法。
[本発明1040]
ポリメラーゼ連鎖反応が、
のプライマー配列の1つまたは両方、または同じ標的配列を増幅することができるその配列変種を利用する、本発明1038の方法。
[本発明1041]
ポリメラーゼ連鎖反応が、
のプライマー配列の1つまたは両方、または同じ標的配列を増幅することができるその配列変種を利用しうる、本発明1038の方法。
[本発明1042]
IFI27遺伝子産物またはその断片もしくは変種に特異的に結合することができる1つまたは複数のプローブを試料に接触させる段階を含む、本発明1001または1017の方法。
[本発明1043]
1つまたは複数のプローブが、
(i)SEQ ID NO:1に示される配列と相補的である配列、または(ii)SEQ ID NO:2に示される配列と相補的である配列、または(i)もしくは(ii)の断片もしくは変種
を含む核酸である、本発明1042の方法。
[本発明1044]
1つまたは複数のプローブが、
(i)SEQ ID NO:5に示される配列と相補的である配列、または(ii)SEQ ID NO:6に示される配列と相補的である配列、または(i)もしくは(ii)の断片もしくは変種
を含む核酸である、本発明1042の方法。
[本発明1045]
核酸プローブが10から50塩基を含む、本発明1042の方法。
[本発明1046]
核酸プローブが30から600塩基を含む、本発明1042の方法。
[本発明1047]
(i)インフルエンザ感染症を有するまたは有することが疑われる患者から血液試料を得る段階;(ii)血液試料から総RNA単離体を調製する段階;(iii)総RNA単離体の逆転写によってcDNAを調製する段階;(iv)ポリメラーゼ連鎖反応によってIFI27核酸配列を増幅する段階;(v)増幅されたIFI27核酸配列のレベルを標準と比較する段階;(vi)比較に基づいて該患者が該患者に対する臨床的リスクを有するか否かを決定する段階
を含む、本発明1001または1017の方法。
[本発明1048]
ポリメラーゼ連鎖反応が定量的ポリメラーゼ連鎖反応である、本発明1047の方法。
[本発明1049]
IFI27ポリペプチドまたはその断片のレベルを決定する段階を含む、本発明1001または1017の方法。
[本発明1050]
(i)SEQ ID NO:3のアミノ酸配列もしくは(ii)SEQ ID NO:4のアミノ酸配列を含むIFI27ポリペプチドまたは(i)もしくは(ii)の抗原性断片もしくは変種のレベルを決定する段階を含む、本発明1049の方法。
[本発明1051]
SEQ ID NO:3またはSEQ ID NO:4に示されるアミノ酸配列を含むIFI27ポリペプチド、またはその抗原性断片もしくは変種に選択的に結合することができる抗体を試料に接触させる段階を含む、本発明1049の方法。
[本発明1052]
ゲル電気泳動、核酸シークエンシング、およびアミノ酸シークエンシングの1つまたは複数を含む、本発明1001または1017の方法。
[本発明1053]
全体的にエクスビボで行われる、本発明1001または1017の方法。
[本発明1054]
生物試料中の決定されたIFI27遺伝子産物レベルを標準レベルと比較する段階が、コンピュータープログラムの補助によって行われる、本発明1001または1017の方法。
[本発明1055]
比較に基づいて患者における臨床的リスクを同定する段階が、コンピュータープログラムの補助によって行われる、本発明1001〜1030のいずれかの方法。
[本発明1056]
生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物レベルを決定するためのキットであって、IFI27遺伝子産物の存在を検出するための少なくとも1つの物質を含む、キット。
[本発明1057]
少なくとも1つの物質が、プライマー、抗体、またはプローブである、本発明1056のキット。
[本発明1058]
プライマーまたはプローブが、SEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:5、SEQ ID NO:6に示される配列から選択される核酸配列、またはその変種もしくは断片に対して特異的である、本発明1056のキット。
[本発明1059]
SEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:5、SEQ ID NO:6に示される配列から選択される核酸配列またはその変種もしくは断片を選択的に増幅することができるフォワードおよびリバースプライマーを含む、本発明1056のキット。
[本発明1060]
からなる群より選択される1つまたは複数の核酸配列、または同じ標的配列に特異的に結合することができるその配列変種を含む、本発明1056のキット。
[本発明1061]
生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物の存在を検出することができる多数の物質を含む、本発明1056のキット。
[本発明1062]
IFI27遺伝子配列によってコードされるポリペプチドまたはその断片もしくは変種に特異的に結合することができる抗体を含む、本発明1056のキット。
[本発明1063]
抗体がIFI27に対して特異的なコンジュゲート抗体である、本発明1062のキット。
[本発明1064]
抗体がポリクローナル抗体である、本発明1062のキット。
[本発明1065]
ポリクローナル抗体がウサギポリクローナル抗体である、本発明1064のキット。
[本発明1066]
抗体がモノクローナル抗体である、本発明1062のキット。
[本発明1067]
抗体が、エピトープ配列:
に結合する、本発明1062のキット。
[本発明1068]
抗体が、(i)SEQ ID NO:3に示されるアミノ酸配列を含むIFI27ポリペプチド、または(ii)SEQ ID NO:4に示されるアミノ酸配列を含むIFI27ポリペプチド、または(iii)(i)もしくは(ii)の抗原性断片もしくは変種に選択的に結合することができる、本発明1062のキット。
[本発明1069]
前記方法の正規化のための1つまたは複数の物質を含む、本発明1056のキット。
[本発明1070]
正規化のための物質が、構成的に発現される遺伝子産物を検出するための1つまたは複数の物質からなる群より選択される、本発明1056のキット。
[本発明1071]
構成的に発現される遺伝子産物がGAPDHである、本発明1056のキット。
[本発明1072]
前記キットが1つまたは複数の較正された標準を含み、該標準がIFI27遺伝子産物の既知濃度を含む、本発明1056のキット。
[本発明1073]
(i)1つまたは複数の参照試料;(ii)1つまたは複数の検出可能な部分;(iii)固相支持体上にIFI27遺伝子産物を検出するための物質を固定するための1つまたは複数の物体;(iv)固相支持体材料;(v)生物試料を採取および/または保存するための1つまたは複数の容器;(vi)生物試料の調製に用いるための1つまたは複数の試薬;(vii)核酸配列を増幅するための1つまたは複数の物質;ならびに(viii)生物試料中のIFI27遺伝子産物レベルを決定するための方法におけるキットまたはその成分の使用説明書
からなる群より選択される1つまたは複数の追加の成分を含む、本発明1056のキット。
[本発明1074]
インフルエンザを処置するための物質の有効性を評価するための方法であって、
インフルエンザ感染症を有する個体に該物質を投与する段階、および該個体由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物レベルを決定する段階、および決定されたIFI27遺伝子産物レベルを標準レベルと比較する段階
を含む、方法。
[本発明1075]
インフルエンザウイルスに曝露された個体における疾患の重症度を低下させるための物質の有効性を評価するための方法であって、
該物質を該個体に投与する段階、該個体由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物レベルを決定する段階、および決定されたレベルを標準レベルと比較する段階
を含む、方法。
[本発明1076]
個体が、前記物質の投与前にインフルエンザウイルスに曝露される、本発明1074または1075の方法。
[本発明1077]
個体が、前記物質の投与時にインフルエンザ感染症を有している、本発明1074または1075の方法。
[本発明1078]
個体が、前記物質の投与後にインフルエンザウイルスに曝露される、本発明1074または1075の方法。
[本発明1079]
前記物質を投与する前の個体から得られた生物試料中のIFI27遺伝子産物のレベルを決定する段階をさらに含む、本発明1074または1075の方法。
[本発明1080]
投与前のレベルと比較して前記物質の投与後の個体由来の生物試料中の低いIFI27遺伝子産物レベルが、インフルエンザウイルスに曝露されたまたはインフルエンザ感染症を有する患者における疾患の重症度を前記物質が低下させることができることを示す、本発明1074または1075の方法。
[本発明1081]
インフルエンザの予防または処置のために候補抗ウイルス剤の研究試験または臨床試験の一部として行われる、本発明1074または1075の方法。
記載の目的に関して、本明細書において言及した全ての文書は、それ以外であると明記している場合を除き、その全体が参照により本明細書に組み入れられる。
SEQ ID NO:1:IFI27 mRNA配列、アイソフォーム1;665塩基;NM_001130080.1から。
本発明は、少なくとも部分的に、対象におけるIFI27の発現レベルがその対象におけるインフルエンザ感染症によって引き起こされる疾患の重症度と相関することを本発明者らが同定したことに基づいている。本発明は、重篤な疾患を発症する可能性がより高く、入院または臨床環境での医学的介入を必要とすることとして定義される臨床的リスクを、どの個体が有するかを決定することによって、インフルエンザに感染した患者を評価するために用いられうる。この決定は、患者がインフルエンザ感染症の症状を示す前に、および患者が重度の疾患を示す症状を示す前になされうる。医学的介入は、入院または生命維持治療を含みうるがこれらに限定されるわけではない。本発明は、医療において、たとえばインフルエンザ感染症の初期の管理、疾患に対する患者の免疫応答のモニタリング、およびそうでなければ従来の診断アプローチでは見逃されうる有リスク者に対する生命維持介入を可能にすることにおいて応用を有する。
IFI27は、未知機能の低分子インターフェロンα誘導遺伝子ファミリーの1つのメンバーである。IFI27は、またはインターフェロンα誘導11.5 kDaタンパク質、インターフェロン刺激遺伝子12aタンパク質として、および代わりの略語ISG12、ISG12(a)、FAM14D、およびP27としても知られる。IFI27のcDNAは、当初、ヒト上皮細胞株MCF-7においてエストロゲン誘導遺伝子としてクローニングされ、p27と命名された3。IFI27は、乾癬表皮病巣における病巣性および非病巣性乾癬皮膚においてアップレギュレートされ4、ならびに定量的RT-PCR試験において非病巣性ケラチノサイトにおいて検出可能である5と報告されている。同じ試験により、扁平苔癬、慢性湿疹、皮膚扁平上皮癌などの他の皮膚疾患においても発現されることが報告され、ケラチノサイトをIFN-γ、TNF-α、またはTGF-β1によって刺激すると発現のアップレギュレーションを示した。その結果、IFI27は、上皮増殖および癌のマーカーであると仮定されている。IFI27はまた、変形性関節炎およびリウマチ性関節炎の滑膜組織と比較して全身性紅斑性狼瘡の滑膜組織において有意に過剰発現されていると報告されている6。
本発明の方法は、IFI遺伝子産物の存在および定量に関する患者の試料の分析を含む。このようにして、試料中のIFI27遺伝子産物レベルを定量してもよく、それによって患者における臨床的リスクを同定することができる。同様に、本発明の方法は、細菌性肺炎などの類似の臨床症状を有しうる状態とは異なるインフルエンザまたはウイルス性肺炎の存在に関して患者を評価することができる。
態様において、本発明の方法は、患者から生物試料を得る段階を含む。生物試料は典型的に、血液試料である。生物試料は、血球サブセット、タンパク質分画、または総RNAもしくはmRNAなどの核酸分画などの、選択された血液成分でありうる。生物試料は、白血球などの1つもしくは複数の成分、またはpDCなどのその特異的成分の存在に関して分画または濃縮するために処理されうる。
本発明者らは、インフルエンザを有する対象におけるIFI27遺伝子の発現レベルが、疾患の重症度と相関すること、それゆえ臨床的リスクの指標として利用することができることを特定した。したがって、本発明の作業において、試料はIFI27遺伝子産物の存在に関して試験されうる。遺伝子産物は、IFI27 mRNAまたは転写物でありうる。IFI27 mRNAの完全なポリヌクレオチド配列が決定されており、たとえばEnsembl/Havanaマージ: ENSG00000165949で報告されている。本明細書において示されるように、既に記述されたIFI27転写物の変種が存在する。1つの態様において、IFI27遺伝子の存在に関して試料を分析する段階は、SEQ ID NO:1またはSEQ ID NO:2に示される配列、またはその断片もしくは変種などのIFI27 mRNA配列の存在に関して試料を分析する段階を含む。
本発明は、対象におけるインターフェロンα誘導タンパク質27(IFI27)遺伝子の発現レベルが、その対象におけるインフルエンザの重症度と相関することを本発明者らが同定したことに少なくとも部分的に基づいている。このように、本発明は、関心対象の対象から得られた試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子の発現レベルの検出および決定を通して、インフルエンザ感染症の際の宿主応答を検出する方法に関する。本方法の作業において、IFI27ポリヌクレオチドの配列またはその断片もしくは変種に基づくヌクレオチドおよび断片は、インターフェロンα誘導タンパク質27(IFI27)遺伝子産物のレベルを検出および決定するためのプライマーおよびプローブとして用いられうる。
(フォワードプライマー;SEQ ID NO:7)、または配列
(リバースプライマー;SEQ ID NO:8)である。本発明の方法の特異的態様において、PCRは、187 bpの配列(SEQ ID NO:11)を増幅するプライマー対
および配列
を用いて行われうる。
または配列
である。本発明の方法の特異的態様において、PCRは、プライマー対
(フォワードプライマー;SEQ ID NO:9)および配列
(リバースプライマー;SEQ ID NO:10)を用いて行われうる5。当業者は、本発明の方法においてそのような核酸配列を用いるための適切な条件を決定することができるであろう。当業者はまた、その内容が参照により本明細書に組み入れられる、Suomelaら5において、IFI27遺伝子産物の増幅および検出のためにそのような核酸配列を用いるための指針を見いだすであろう。
または配列
である。本発明の方法の特異的態様において、PCRは、プライマー対
および配列
を用いて行われうる8。ISG12fおよびISG12rに記載される配列において、大文字はcDNA配列に対応する。当業者は、本発明の方法においてそのような核酸配列を用いるための適切な条件を決定することができるであろう。当業者は、その内容が参照により本明細書に組み入れられるGjermandsen et al (1999)8において、IFI27遺伝子産物を増幅および検出するためのそのような核酸配列の使用に関する指針を見いだすであろう。
IFI27遺伝子によってコードされるポリペプチドまたはその断片もしくは変種に特異的に結合することができる抗体もまた、本発明の方法によって企図される。抗体または複数の抗体は、所定の試料における1つまたは複数のポリペプチド、詳しくはIFI27遺伝子によってコードされるポリペプチドまたは断片を定性的または定量的に検出および分析するために用いられうる。アッセイの対照または正規化の目的のために、追加のポリペプチドの抗体検出および定量も同様に行われうる。「特異的に結合する」とは、無関係なタンパク質に結合する場合より高い親和性で抗体が標的ポリペプチドまたはその断片に結合することができると理解されるであろう。たとえば、抗体は、少なくとも約10-4 Mから約10-10 Mの範囲の結合定数でポリペプチドまたはその断片に結合しうる。好ましくは、結合定数は、少なくとも約10-5 M、または少なくとも約10-6 Mであり、より好ましくは関心対象のポリペプチドまたはその断片に対する抗体の結合定数は、少なくとも約10-7 M、少なくとも約10-8 M、または少なくとも約10-9 Mであるか、またはそれより高い。
本明細書において用いられるように、インターフェロンα誘導タンパク質27(IFI27)遺伝子産物のレベルを決定する段階は、様々な態様において、試料中の遺伝子産物の存在、非存在、または量を決定する段階を含み、試料中の遺伝子産物の量を定量する段階を含みうる。好ましい態様において、本発明の方法の全ての段階は、対象のヒトの体または動物の体などの対象の体の外部で起こり、本方法は体において実践されない。そのため、好ましい態様において、本発明は、ヒトまたは動物の体において実践されるいかなる物理的介入も伴わない。
本発明は、IFI27遺伝子産物の存在を検出するための少なくとも1つの物質を含む、生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物のレベルを決定するためのキットを提供する。物質は、ポリヌクレオチドまたはポリペプチドでありうるIFI27遺伝子産物を検出することができる物質でありうる。本明細書において記述される配列を検出することができる任意の適した物質がキットに含まれうる。非制限的な例には、プライマー、プローブ、および抗体が挙げられる。
試験参加者
実験は、実験セットおよびバリデーションセットからなる試験試料に基づいて行った。実験セット(n=54)は、インフルエンザ感染症のための候補バイオマーカーを同定するために用いられた。これには、患者のいくつかのコホートが含まれた;インフルエンザ感染症(n=8)、細菌感染症(n=16)、非感染状態を有する重篤な患者(n=12)、および健康なボランティア(n=18)。バリデーションセット(n=33)は、実験セットから生成されたバイオマーカーを試験するために用いた。試験参加者は全員、書面での同意書を提出しており、試験参加者の詳細は表1に示す。
(COPD、慢性閉塞性肺疾患;APACHE II、急性生理学的慢性健康評価スコア;SIRS、全身性炎症反応症候群。プラスマイナスの値は、平均値±標準偏差である)。
可能性がある候補マーカーに関してスクリーニングするために、インフルエンザ感染症が確認された個体の全血について、トランスクリプトームマイクロアレイ分析を行った。標準プロトコール(PAXgene(商標) Blood RNA kit - Qiagen, Germany)を用いてRNA抽出を行った。Agilent Bioanalyserを用いてRNAの品質を分析したところ、全ての試料が、高品質試料を示す6.5より大きいRNA完全性数値を有した。 試料の増幅および標識は、Illumina TotalPrep増幅キット(Ambion, Austin, TX)を用いて、総RNA 200 ngについて一度に試料24個のバッチで行った。満足できる増幅が確実に得られるように、増幅されたcRNAをAgilent Bioanalyserを用いて評価した。
定量的リアルタイムPCRを、実験試料セットおよびバリデーション試料セットにおける全ての試料について行った。Qiagen RNeasyミニキットによって製造元の説明書(Qiagen, Germany)に従って総RNAを調製した。RNAの収量をUV吸収によって決定した。
であった。PCRサイクリング条件は:95℃で10分間の保持、95℃で30秒、64℃で30秒、次に72℃で30秒を5サイクル、95℃で30秒、59℃で30秒、次に72℃で30秒を35サイクル、75℃から99℃での融解であった。IFI27の発現レベルを、ヒトハウスキーピング遺伝子、GAPDH
を用いて正規化した。アッセイは、Rotor-Gene 2000リアルタイムPCRマシン(Corbett Research, NSW, Australia)において行った。シングルPCR産物を、融解曲線分析と、エチジウムブロマイド染色2%アガロースゲル(Sigma-Aldrich)上で泳動させてUV透視により可視化した場合の単一産物の観察との両方によって確認した。遺伝子発現データの可視化は、GraphPad PRISM(バージョン6)を用いて行った。
ヒト免疫細胞において行った実験に関して、10%ウシ胎児血清(FBS; SAFC Biosciences, Victoria, Australia)、50 IU/mlペニシリン、50 μg/mlストレプトマイシン、および2 mM L-グルタミンを添加したGibco RPMI 1640培地(Life Technologies, Australia Pty Ltd)からなる培養培地を用いた。培養細胞は全て、5%CO2の湿潤大気中で37℃で維持した。
ヒト細胞タイプ(単球、NK細胞、B細胞、pDC、mDC、CD4+、CD8+ T細胞、および好中球)を、全末梢血単核球(PBMC)から精製した。
細胞を、表2に示すように表面マーカーの異なる発現に基づいて分離した。各実験において、細胞(>104個/試料)を培地に懸濁し、新しく単離した細胞(細胞表面表現型)の純度を直ちに決定したか、またはフローサイトメトリーBD LSR-II(BD Biosciences)による後の分析のために1%パラホルムアルデヒド中で固定した。FlowJoソフトウェアプログラム(Tree Star, USA)を用いて分析を行った。
単離された免疫細胞を、インターフェロン-α、インターフェロン-β、インターフェロン-λ、インフルエンザウイルス抗原、toll様受容体(TLR1、TLR2、TLR3、TLR4、TLR5、TLR6、TLR7、TLR8、およびTLR9)のアゴニスト、ならびに生きたインフルエンザウイルス(H1N1、H3N2、B型インフルエンザ)を含む内因性のリガンドによって刺激した。純粋な細胞集団を、10%FBS、2 mM L-グルタミン、50 IU/mlペニシリン、および50μg/mlストレプトマイシンを含むRPMI 1640に、細胞1〜2×106個/mlの密度で懸濁した。異なる濃度の刺激物質がIFI27発現に及ぼす効果を決定するために、細胞を、培地中で表記の濃度の刺激物質と共に37℃で6、12、および24時間インキュベートした。全ての処置に関して、最適な刺激条件を定義するために、用量反応を行った。刺激の前後での細胞生存率を、トリパンブルー排除法(Sigma-Aldrich, St Louis, MO, USA)によって測定した。
2つの群の比較を、必要に応じて、対応のない両側のスチューデントt-検定またはノンパラメトリックマン・ホイトニーU検定を用いて計算した。多群比較は、必要に応じて、一元配置ANOVAまたはクラスカル-ウォリス検定を用いて計算した。遺伝子発現データは、健康な対照と比較した変化倍率として表記する(平均値±SD)。統計分析は全て、GraphPad Prismバージョン6(GraphPad Software, La Jolla, CA)を用いて行った。p値は全て両側であり、有意性の閾値はp<0.05であると考えられる。
可能性がある候補マーカーをスクリーニングするために、インフルエンザ感染症が確認された患者の全血についてトランスクリプトームマイクロアレイ分析を行った。この分析により、重度のインフルエンザ感染症のマーカーとして、インターフェロン刺激遺伝子、インターフェロンα誘導タンパク質27(IFI27)が同定された(図1)。実験セットにおいて、IFI27遺伝子は、インフルエンザ感染症による重度の疾患を有する個体において高度に発現された。この知見をバリデーションセットにおいて確認した(図2)。
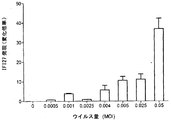
IFI27発現のメカニズムを明らかにするために、内因性のリガンド(インターフェロン-α、インターフェロン-β、およびインターフェロン-λ)を用いて末梢血細胞におけるインターフェロン経路を刺激する実験を行った。インターフェロンα(IFNα)は、IFI27発現の最大の増加を生じること(図9)およびこの増加は用量依存的に起こる(図10)ことが観察された。
IFI27発現の経時的変化を調べるために、pDCにおけるIFI27発現の縦断的分析を行った。pDCをインフルエンザウイルスに曝露して、IFI27遺伝子発現を4日間毎日測定した(図16)。この実験から、pDCが24時間以内にIFI27発現を急速に増加させた後、48および72時間で低下することが示された。遺伝子発現の低下は、アポトーシスアッセイによって証明される生存細胞数が48および72時間で比較的一定のままであることから(図16)、pDC数の減少によるものではなかった。この知見は、IFI27が感染の初期相において急速にアップレギュレートされることを証明した。
他の病原体(たとえば、細菌)も同様にIFI27発現を増加させうるか否かもまた調べた。この目的のため、PBMCをリポ多糖類(LPS)と共に培養した。LPSは、無視できる程度のIFI27遺伝子発現を引き起こすことが見いだされた(図17)。このことは、IFI27発現がインフルエンザ肺炎を有する患者と比較して有意に少ない細菌性肺炎患者のコホートにおいて確認された(図18)。これを、ウイルス性および細菌性肺炎の両方の患者(n=37)からなる独立したデータセット(GSE6269)においてさらに検証した。この場合も、この分析から、IFI27発現が、細菌性肺炎と比較してインフルエンザ感染症において有意に高いことが示された(図19)。
重度の疾患は、宿主において全身性の炎症応答を誘発することから、重度の疾患が同様にIFI27発現を増加させうるか否かを試験した。全身炎症反応症候群(外傷、膵炎、および高リスク手術によって引き起こされた)の患者のコホートにおいて、IFI27遺伝子発現は有意に増加しないことが見いだされた(図20)。このことは、IFI27発現が最少であるSIRS患者(n=167)の独立したデータセット(GSE11375)において確認された(図21)。
インフルエンザのパンデミックは、感受性集団を通しての新規ウイルス株の急速な蔓延を特徴とする。大流行の際には感染者が指数的に増加することにより、疑われるあらゆる症例を検査および検疫することは論理的に不可能となる。公衆衛生の対応は、大流行の封じ込めから、最も重篤な個体への医療資源の割付へと急速にシフトするであろう。それゆえ、多数の感染者を迅速にトリアージできること、および悪化のリスクが高い個体を同定できることは、パンデミックの管理にとって極めて重要である。この目的に関して、IFI27は、インフルエンザ感染症に関連する信頼できる疾患重症度バイオマーカーとして確立されている。
Claims (23)
- インフルエンザ感染症を有するまたは有することが疑われる患者における臨床的リスクの同定を補助する方法であって、該患者由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子の発現レベルを決定する段階、および決定されたIFI27遺伝子産物レベルを標準レベルと比較する段階を含む、方法。
- (i) IFI27遺伝子産物の標準レベルが臨床的リスクなしを示しており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、または
(ii) 標準レベルが、健康な対象、インフルエンザに感染した無症候性の対象、またはインフルエンザに感染しているが重度の疾患を発症していない対象におけるIFI27遺伝子産物レベルに基づく、または
(iii) IFI27遺伝子産物の標準レベルが臨床的リスクを示しており、標準レベルと比較して患者の試料中の同等であるかまたは高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、または
(iv) 標準レベルが、健康な対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、または
(v) 標準レベルが、インフルエンザウイルスに感染した無症候性の対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、
請求項1記載の方法。 - (i) 標準レベルが、IFI27遺伝子産物の1つまたは複数の既知試料を、患者由来の生物試料と同じIFI27遺伝子発現レベルの決定法に供することによって調製され、IFI27遺伝子産物の1つまたは複数の既知試料が、臨床的リスクを示すある既定量または複数の既定量の試料であり、標準レベルと比較して患者の試料中の同等であるかまたは高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、または
(ii) 標準レベルが、IFI27遺伝子産物の1つまたは複数の既知試料を、患者由来の生物試料と同じIFI27遺伝子発現レベルの決定法に供することによって調製され、IFI27遺伝子産物の1つまたは複数の既知試料が、臨床的リスクなしを示すある既定量または複数の既定量の試料であり、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、患者における臨床的リスクを示す、
請求項1記載の方法。 - インフルエンザを有する患者の経過をモニターする方法であって、患者由来の第一の生物試料中のIFI27遺伝子の発現レベルを決定する段階、および患者由来の第二の生物試料中のIFI27遺伝子の発現レベルを決定する段階であって、第一および第二の試料が異なる時期に患者から得られる、段階、ならびに
第一および第二の試料中のIFI27の相対的発現レベルに基づいて患者の状態の評価を補助する段階を含む、方法。 - 第一の生物試料と比較した第二の生物試料中のIFI27遺伝子の発現レベルの増加が、患者における臨床的リスクの増加を示す、請求項4記載の方法。
- 第一の生物試料と比較した第二の生物試料中のIFI27遺伝子の発現レベルの低下が、患者における臨床的リスクの低下を示す、請求項4記載の方法。
- 患者由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子の発現レベルを決定する段階、および決定されたIFI27遺伝子産物レベルを標準レベルと比較する段階を含む、患者におけるインフルエンザまたはウイルス性肺炎の臨床的リスクの同定を補助する方法。
- (i) 標準レベルが、健康な対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27レベルが、患者におけるインフルエンザまたはウイルス性肺炎を示す、または
(ii) 標準レベルが、細菌性肺炎を有する対象におけるIFI27遺伝子産物レベルに基づいており、標準レベルと比較して患者の試料中の高いIFI27遺伝子産物レベルが、インフルエンザまたはウイルス性肺炎を有する患者であることを示す、
請求項7記載の方法。 - 患者がウイルス性肺炎または細菌性肺炎を有することが疑われる、請求項7記載の方法。
- (i) 生物試料中の少なくとも1つの追加の遺伝子、または
(ii) その発現が構成的である遺伝子である、少なくとも1つの追加の遺伝子、または
(iii) GAPDH遺伝子である、少なくとも1つの追加の遺伝子
の発現レベルを決定する段階をさらに含む、請求項1〜9のいずれか一項記載の方法。 - 生物試料が、血液、または血球サブセット、RNA、mRNA、cDNA、もしくはタンパク質などその成分である、請求項1〜10のいずれか一項記載の方法。
- 決定する段階が、生物試料に、IFI27遺伝子産物に結合することができる物質を接触させる段階、および該物質とIFI27遺伝子産物との結合を検出する段階を含み、
(i) IFI27遺伝子産物が、IFI27 mRNAまたはその断片である、または
(ii) IFI27遺伝子産物が、SEQ ID NO:1の核酸配列またはその断片もしくは変種、またはSEQ ID NO:2の核酸配列またはその断片もしくは変種を含む、または
(iii) IFI27遺伝子産物が、IFI27ポリペプチドまたはその断片もしくは変種である、または
(iv) IFI27遺伝子産物が、SEQ ID NO:3の配列を含むアミノ酸配列またはその断片もしくは変種を含むか、またはSEQ ID NO:4の配列を含むアミノ酸配列またはその断片もしくは変種を含む、
請求項1〜11のいずれか一項記載の方法。 - SEQ ID NO:3またはSEQ ID NO:4に示されるアミノ酸配列を含むIFI27ポリペプチド、またはその抗原性断片もしくは変種に選択的に結合することができる抗体を試料に接触させる段階を含む、請求項12記載の方法。
- ELISAを行う段階を含む、請求項12または13記載の方法。
- 生物試料中の決定されたIFI27遺伝子産物レベルを標準レベルまたは第二の生物試料と比較する段階が、コンピュータープログラムの補助によって行われる、請求項1〜14のいずれか一項記載の方法。
- 生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物レベルを決定するための、請求項1〜15のいずれか一項記載の方法において使用されるキットであって、IFI27遺伝子産物の存在を検出するための少なくとも1つの物質を含む、キット。
- 少なくとも1つの物質が、以下からなる群から選択される、請求項16記載のキット、
(i) プライマー、抗体、またはプローブ、または
(ii) SEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:5、SEQ ID NO:6に示される配列から選択される核酸配列またはその変種もしくは断片に対して特異的なプライマーまたはプローブ、
(iii) SEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:5、SEQ ID NO:6に示される配列から選択される核酸配列またはその変種もしくは断片を選択的に増幅することができるフォワードおよびリバースプライマー、または
(iv)
からなる群より選択される1つまたは複数の核酸配列、または同じ標的配列に特異的に結合することができるその配列変種、または
(v) IFI27遺伝子配列によってコードされるポリペプチドまたはその断片もしくは変種に特異的に結合することができる抗体。 - 抗体が、IFI27に対して特異的なコンジュゲート抗体、ポリクローナル抗体、またはモノクローナル抗体からなる群から選択される、請求項17記載のキット。
- 前記キットが1つまたは複数の較正された標準を含み、該標準がIFI27遺伝子産物の既知濃度を含む、請求項17〜19のいずれか一項記載のキット。
- (i)1つまたは複数の参照試料;(ii)1つまたは複数の検出可能な部分;(iii)固相支持体上にIFI27遺伝子産物を検出するための物質を固定するための1つまたは複数の物体;(iv)固相支持体材料;(v)生物試料を採取および/または保存するための1つまたは複数の容器;(vi)生物試料の調製に用いるための1つまたは複数の試薬;(vii)核酸配列を増幅するための1つまたは複数の物質;ならびに(viii)生物試料中のIFI27遺伝子産物レベルを決定するための方法におけるキットまたはその成分の使用説明書
からなる群より選択される1つまたは複数の追加の成分を含む、請求項17〜20のいずれか一項記載のキット。 - 個体におけるインフルエンザを処置するための物質の有効性またはインフルエンザウイルスに曝露された個体における疾患の重症度を低下させるための物質の有効性を評価するための方法であって、
該物質を投与された個体由来の生物試料中のインターフェロンα誘導タンパク質27(IFI27)遺伝子産物レベルを決定する段階、および決定されたレベルを標準レベルと比較する段階
を含む、方法。 - (i) 前記個体が、前記物質の投与前にインフルエンザウイルスに曝露された個体である、または
(ii) 前記個体が、前記物質の投与時にインフルエンザ感染症を有している個体である、または
(iii)前記個体が、前記物質の投与後にインフルエンザウイルスに曝露された個体である、または
(iv) 方法が、前記物質を投与する前の前記個体から得られた生物試料中のIFI27遺伝子産物のレベルを決定する段階をさらに含む、または
(v) 前記物質を投与する前の前記個体から得られた生物試料中のIFI27遺伝子産物のレベルと比較して、前記物質を投与された個体由来の生物試料中の低いIFI27遺伝子産物レベルが、インフルエンザウイルスに曝露されたまたはインフルエンザ感染症を有する患者における疾患の重症度を前記物質が低下させることができることを示す、または
(vi) 方法が、インフルエンザの予防または処置のための候補抗ウイルス剤の研究試験または臨床試験の一部として行われる、
請求項22記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2012902954 | 2012-07-10 | ||
| AU2012902954A AU2012902954A0 (en) | 2012-07-10 | Risk stratification in influenza | |
| PCT/AU2013/000765 WO2014008545A1 (en) | 2012-07-10 | 2013-07-10 | Risk stratification in influenza |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2015530868A JP2015530868A (ja) | 2015-10-29 |
| JP2015530868A5 JP2015530868A5 (ja) | 2016-06-16 |
| JP6097388B2 true JP6097388B2 (ja) | 2017-03-15 |
Family
ID=49915252
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015520775A Active JP6097388B2 (ja) | 2012-07-10 | 2013-07-10 | インフルエンザにおけるリスクの階層化 |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US10036075B2 (ja) |
| EP (1) | EP2872891B1 (ja) |
| JP (1) | JP6097388B2 (ja) |
| KR (1) | KR20150040289A (ja) |
| CN (1) | CN104769430B (ja) |
| AU (1) | AU2013289854B2 (ja) |
| BR (1) | BR112015000685A2 (ja) |
| CA (1) | CA2877400A1 (ja) |
| DK (1) | DK2872891T3 (ja) |
| WO (1) | WO2014008545A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015103664A1 (en) * | 2014-01-09 | 2015-07-16 | Nepean Blue Montains Local Health District | Risk stratification in influenza |
| EP3180621B1 (en) | 2014-08-14 | 2020-04-01 | Memed Diagnostics Ltd. | Computational analysis of biological data using manifold and a hyperplane |
| EP3146974A1 (en) | 2015-09-25 | 2017-03-29 | Universite Claude Bernard - Lyon 1 | Biomarkers for early determination of severity of influenza related disease |
| WO2017149548A1 (en) | 2016-03-03 | 2017-09-08 | Memed Diagnostics Ltd. | Rna determinants for distinguishing between bacterial and viral infections |
| US20190085378A1 (en) | 2016-03-03 | 2019-03-21 | Memed Diagnostics Ltd. | Analyzing rna for diagnosing infection type |
| US20210230694A1 (en) * | 2018-06-05 | 2021-07-29 | University Of Rochester | Nasal genes used to identify, characterize, and diagnose viral respiratory infections |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5792626A (en) * | 1996-09-18 | 1998-08-11 | Incyte Pharmaceuticals, Inc. | Human interferon-inducible protein |
| US6821724B1 (en) * | 1998-09-17 | 2004-11-23 | Affymetrix, Inc. | Methods of genetic analysis using nucleic acid arrays |
| US7214498B2 (en) * | 2001-03-23 | 2007-05-08 | Benaroya Research Institute At Virginia Mason | Tumor associated antigens and methods of using the same |
| JP2004121218A (ja) * | 2002-08-06 | 2004-04-22 | Jenokkusu Soyaku Kenkyusho:Kk | 気管支喘息または慢性閉塞性肺疾患の検査方法 |
| JP2008504803A (ja) * | 2004-01-09 | 2008-02-21 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 遺伝子発現の細胞型特異的パターン |
| US20050244851A1 (en) * | 2004-01-13 | 2005-11-03 | Affymetrix, Inc. | Methods of analysis of alternative splicing in human |
| WO2007034280A2 (en) * | 2005-09-19 | 2007-03-29 | Moshe Amihood Blay | Composition and method for prevention of influenza |
| AU2007286915B2 (en) * | 2006-08-11 | 2014-05-15 | Baylor Research Institute | Gene expression signatures in blood leukocytes permit differential diagnosis of acute infections |
| US20110129816A1 (en) * | 2008-06-06 | 2011-06-02 | National University Corporation University Of Toyama | Device for detection of influenza virus |
| EP2376653A2 (en) * | 2008-12-29 | 2011-10-19 | Yissum Research Development Company of The Hebrew University of Jerusalem | Methods of predicting responsiveness to interferon treatment and treating hepatitis c infection |
| WO2011008349A2 (en) * | 2009-05-26 | 2011-01-20 | Duke University | Methods of identifying infectious disease and assays for identifying infectious disease |
| WO2011005793A1 (en) | 2009-07-06 | 2011-01-13 | Alnylam Pharmaceuticals, Inc. | Cell-based bioprocessing |
| US20120214705A1 (en) * | 2009-09-28 | 2012-08-23 | The Regents Of The University Of California Office of Technology, | Beta-defensin 2 genetic variation predicts h. pylori susceptibility |
| WO2013030841A1 (en) * | 2011-09-04 | 2013-03-07 | Yissum Research Development Company Of The Hebrew Universitiy Of Jerusalem Ltd. | Prognostic methods and compositions for predicting interferon treatment eficacy in a subject |
-
2013
- 2013-07-10 JP JP2015520775A patent/JP6097388B2/ja active Active
- 2013-07-10 CN CN201380046905.6A patent/CN104769430B/zh active Active
- 2013-07-10 US US14/410,367 patent/US10036075B2/en active Active
- 2013-07-10 AU AU2013289854A patent/AU2013289854B2/en active Active
- 2013-07-10 CA CA2877400A patent/CA2877400A1/en not_active Abandoned
- 2013-07-10 WO PCT/AU2013/000765 patent/WO2014008545A1/en active Application Filing
- 2013-07-10 DK DK13817599.7T patent/DK2872891T3/da active
- 2013-07-10 BR BR112015000685A patent/BR112015000685A2/pt not_active Application Discontinuation
- 2013-07-10 EP EP13817599.7A patent/EP2872891B1/en active Active
- 2013-07-10 KR KR20157003223A patent/KR20150040289A/ko not_active Application Discontinuation
-
2018
- 2018-06-25 US US16/017,197 patent/US20180298455A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN104769430A (zh) | 2015-07-08 |
| EP2872891A4 (en) | 2016-01-20 |
| US20180298455A1 (en) | 2018-10-18 |
| US10036075B2 (en) | 2018-07-31 |
| AU2013289854A2 (en) | 2015-02-26 |
| EP2872891B1 (en) | 2019-03-13 |
| CA2877400A1 (en) | 2014-01-16 |
| EP2872891A1 (en) | 2015-05-20 |
| US20150322538A1 (en) | 2015-11-12 |
| DK2872891T3 (da) | 2019-05-13 |
| AU2013289854B2 (en) | 2016-03-24 |
| BR112015000685A2 (pt) | 2017-11-28 |
| KR20150040289A (ko) | 2015-04-14 |
| WO2014008545A1 (en) | 2014-01-16 |
| JP2015530868A (ja) | 2015-10-29 |
| CN104769430B (zh) | 2018-12-14 |
| AU2013289854A1 (en) | 2015-01-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20180298455A1 (en) | Risk stratification in influenza | |
| Puccetti et al. | Gene expression profiling in Behcet’s disease indicates an autoimmune component in the pathogenesis of the disease and opens new avenues for targeted therapy | |
| US20190367984A1 (en) | Methods for predicting response to anti-tnf therapy | |
| JP2016526888A (ja) | 敗血症バイオマーカー及びそれらの使用 | |
| US20140205613A1 (en) | Anti-tnf and anti-il 17 combination therapy biomarkers for inflammatory disease | |
| ES2959778T3 (es) | Método para detectar tuberculosis activa | |
| WO2011065168A1 (ja) | 関節リウマチに対するヒト型抗TNFα抗体薬の薬効予測方法、及び薬効予測装置 | |
| WO2012169887A2 (en) | Use of new markers in a diagnostic assay for determining severity of rsv infection | |
| US20140221235A1 (en) | Biomarker algorithm for determining the time of stroke symptom onset and method | |
| WO2015103664A1 (en) | Risk stratification in influenza | |
| Karabacak et al. | Is microRNA 1910-3p (miR-1910-3p) a really distinctive marker for psoriasis? | |
| EP4230749A1 (en) | In vitro method for predicting a risk of post-chikungunya chronic inflammatory joint disease | |
| US20230003719A1 (en) | Materials and methods for inflammatory molecular markers | |
| US20230014092A1 (en) | Materials and methods for monitoring inflammation | |
| RU2639122C1 (ru) | Способ прогнозирования дыхательной недостаточности у больных бронхиальной астмой | |
| Koptan et al. | Evaluation of serum microRNA-30e-5p expression in systemic lupus erythematosus and its association with clinical manifestations: A cross-sectional study | |
| US20170342495A1 (en) | Markers of preterm birth | |
| Mesko et al. | Research article Peripheral blood gene expression patterns discriminate among chronic inflammatory diseases and healthy controls and identify novel targets |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160418 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160418 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20160418 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20160518 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160601 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160830 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161019 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20161114 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161228 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170119 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170217 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6097388 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |