JP6087604B2 - 医用画像処理装置 - Google Patents
医用画像処理装置 Download PDFInfo
- Publication number
- JP6087604B2 JP6087604B2 JP2012265233A JP2012265233A JP6087604B2 JP 6087604 B2 JP6087604 B2 JP 6087604B2 JP 2012265233 A JP2012265233 A JP 2012265233A JP 2012265233 A JP2012265233 A JP 2012265233A JP 6087604 B2 JP6087604 B2 JP 6087604B2
- Authority
- JP
- Japan
- Prior art keywords
- blood vessel
- stent graft
- medical image
- stent
- unit
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Measuring And Recording Apparatus For Diagnosis (AREA)
- Media Introduction/Drainage Providing Device (AREA)
- Medical Treatment And Welfare Office Work (AREA)
- Apparatus For Radiation Diagnosis (AREA)
- Magnetic Resonance Imaging Apparatus (AREA)
- Prostheses (AREA)
Description
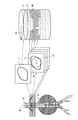
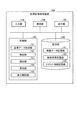
図1は、第1の実施形態に係る医用画像処理装置100の構成の一例を示す図である。図1に示すように、医用画像処理装置100は、入力部110と、表示部120と、通信部130と、記憶部140と、制御部150とを有する。例えば、医用画像処理装置100は、ワークステーションや、任意のパーソナルコンピュータなどであり、図示しない医用画像診断装置や、画像保管装置などとネットワークを介して接続される。医用画像診断装置は、例えば、X線CT(Computed Tomography)装置、MRI(Magnetic Resonance Imaging)装置、X線診断装置などである。また、医用画像診断装置は、3次元の医用画像データ(例えば、大動脈などの血管の3次元画像データなど)を生成可能である。なお、以下、3次元画像データをボリュームデータと記す場合がある。画像保管装置は、医用画像を保管するデータベースである。具体的には、画像保管装置は、医用画像診断装置から送信された3次元の医用画像データを記憶部に格納し、これを保管する。
上述した第1の実施形態においては、1時点(例えば、ステントグラフト留置直後)のボリュームデータを用いてエンドリークを予測する場合について説明した。第2の実施形態では、複数の時点で収集されたボリュームデータを用いてエンドリークを予測する場合について説明する。なお、第2の実施形態に係る医用画像処理装置100においては、第1の実施形態に係る医用画像処理装置と比較して、算出部154による処理内容が異なる。以下、これを中心に説明する。
上述した実施形態では、ステントグラフト内挿術が施術された後に収集されたボリュームデータを用いて血管とステントグラフトとの接触領域を抽出して境界距離を算出する場合について説明した。第3の実施形態では、ステントグラフトのサイズを用いて仮想的に接触領域の抽出と境界距離の算出を実行する場合について説明する。
さて、これまで第1、第2及び第3の実施形態について説明したが、上述した第1、第2及び第3の実施形態以外にも、種々の異なる形態にて実施されてよいものである。
150 制御部
151 画像データ取得部
152 検出部
153 抽出部
154 算出部
155 表示制御部
Claims (6)
- 3次元の医用画像データに含まれる血管とステントグラフトとを検出する機能を有する検出手段と、
前記3次元の医用画像データにおける座標に基づいて、前記検出手段によって検出された血管とステントグラフトとの接触領域を抽出する抽出手段と、
前記ステントグラフトの端部と前記抽出手段によって抽出された接触領域との相対的な位置関係を示す表示画像を所定の表示部にて表示させるように制御する表示制御手段と、
を備え、
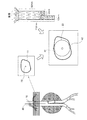
前記抽出手段は、前記血管の長手方向において前記血管の全周囲に渡って前記血管と前記ステントグラフトとが接触している位置のうち、前記ステントグラフトの中央側の位置をエンドリークが発生する境界であるエンドリーク境界位置として抽出することを特徴とする医用画像処理装置。 - 前記抽出手段は、前記血管の芯線に沿って前記芯線に直交する複数の断面を抽出し、抽出した複数の断面にそれぞれ含まれる血管壁の断面と前記ステントグラフトの断面との接触部分を、前記血管壁及び前記ステントグラフトの断面それぞれの座標に基づいて抽出し、抽出した接触部分を結合することで前記接触領域を抽出することを特徴とする請求項1に記載の医用画像処理装置。
- 前記抽出手段は、前記血管壁の断面上の点から前記ステントグラフトの断面までの距離、又は、前記ステントグラフトの断面上の点から前記血管壁の断面までの距離が、所定の閾値を下回った部分を前記接触部分として抽出することを特徴とする請求項2に記載の医用画像処理装置。
- 前記血管と前記ステントグラフトとの境界であるステント境界位置と前記エンドリーク境界位置との間の距離を算出する算出手段をさらに備えたことを特徴とする請求項1〜3のいずれか1項に記載の医用画像処理装置。
- 前記抽出手段は、同一被検体から収集された時相の異なる3次元の医用画像データから前記ステント境界位置及び前記エンドリーク境界位置をそれぞれ抽出し、
前記算出手段は、前記抽出手段によって時相の異なる3次元の医用画像データからそれぞれ抽出された前記ステント境界位置及び前記エンドリーク境界位置の間の距離をそれぞれ算出し、算出した距離の変化に基づいて、エンドリークの時期を推定することを特徴とする請求項4に記載の医用画像処理装置。 - 前記抽出手段は、前記検出手段によって検出された血管に対してステントグラフトを仮想的に留置した場合に、前記血管と前記仮想的に留置したステントグラフトとの仮想的な接触領域である仮想接触領域を抽出し、
前記表示制御手段は、前記仮想的に留置したステントグラフトの端部と前記抽出手段によって抽出された仮想接触領域との相対的な位置関係を示す表示画像を所定の表示部にて表示させるように制御することを特徴とする請求項1に記載の医用画像処理装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012265233A JP6087604B2 (ja) | 2012-12-04 | 2012-12-04 | 医用画像処理装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012265233A JP6087604B2 (ja) | 2012-12-04 | 2012-12-04 | 医用画像処理装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2014108313A JP2014108313A (ja) | 2014-06-12 |
| JP6087604B2 true JP6087604B2 (ja) | 2017-03-01 |
Family
ID=51029296
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012265233A Active JP6087604B2 (ja) | 2012-12-04 | 2012-12-04 | 医用画像処理装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6087604B2 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7262923B2 (ja) * | 2017-12-27 | 2023-04-24 | キヤノンメディカルシステムズ株式会社 | 医用画像処理装置、その制御方法、及びプログラム |
| JP7286380B2 (ja) | 2019-04-01 | 2023-06-05 | 国立大学法人 東京大学 | 医用画像処理装置及び医用画像処理プログラム |
| JP7513495B2 (ja) * | 2020-10-30 | 2024-07-09 | キヤノン株式会社 | 医用情報処理装置、医用情報処理方法及び医用情報処理プログラム |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6702847B2 (en) * | 2001-06-29 | 2004-03-09 | Scimed Life Systems, Inc. | Endoluminal device with indicator member for remote detection of endoleaks and/or changes in device morphology |
| JP5358841B2 (ja) * | 2008-03-10 | 2013-12-04 | 学校法人東海大学 | ステント形状最適化シミュレータ |
| EP2344020B1 (en) * | 2008-10-14 | 2020-05-20 | Lightlab Imaging, Inc. | Stent strut detection and related measurement and display using optical coherence tomography |
| JP2011045449A (ja) * | 2009-08-25 | 2011-03-10 | Toshiba Corp | 画像処理装置及び画像診断装置 |
-
2012
- 2012-12-04 JP JP2012265233A patent/JP6087604B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2014108313A (ja) | 2014-06-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11694330B2 (en) | Medical image processing apparatus, system, and method | |
| ES2940439T3 (es) | Sistema de obtención de imágenes intravasculares y métodos para determinar el ángulo de visión del plano de corte de la rama lateral | |
| RU2595805C2 (ru) | Аннотатор сосудов | |
| CN102917647B (zh) | 对象的特定取向的确定 | |
| US20180345581A1 (en) | Living body tissue three-dimensional model and production method therefor | |
| EP3308710B1 (en) | Blood vessel image processing apparatus, blood vessel image processing program, and blood vessel image processing method | |
| CN105899138B (zh) | 部署建模 | |
| JP2018527964A (ja) | 画像位置合わせ | |
| US8768436B2 (en) | Coronary artery angiography image processing method to detect occlusion and degree effect of blood vessel occlusion to an organ | |
| JP2014188323A (ja) | 血流解析装置及び血流解析プログラム | |
| US11723721B2 (en) | Apparatus and method for manufacturing surgical guide, and surgical guide | |
| CN111317566A (zh) | 用于介入式手术的规划支持 | |
| WO2013156546A2 (en) | Endoprosthesis leakage analysis | |
| JP6087604B2 (ja) | 医用画像処理装置 | |
| Kobayashi et al. | Development of an image-based modeling system to investigate evolutional geometric changes of a stent graft in an abdominal aortic aneurysm | |
| EP3238626A1 (en) | Image processing device and image processing method | |
| Wilson et al. | A novel approach to calculating small intestine length based on magnetic resonance enterography | |
| US9642535B2 (en) | Medical image processing apparatus and medical image processing method | |
| JP2015023997A (ja) | 診断支援装置および診断支援方法並びに診断支援プログラム | |
| JP5957409B2 (ja) | 領域抽出装置および方法並びにプログラム | |
| CN112294435B (zh) | 对内置假体的部署的改进的实时模拟 | |
| JP2015536750A (ja) | 対象内の目標要素の空間的寸法を決定する空間的寸法決定装置 | |
| WO2025070105A1 (ja) | 画像処理装置、画像処理システム、画像処理方法、及び画像処理プログラム | |
| US20220180511A1 (en) | Analysis device, analysis system, and analysis method | |
| JP6554335B2 (ja) | 医用画像処理装置、及びそれを用いた医用画像誘導装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20151027 |
|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7421 Effective date: 20151102 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20160513 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20160831 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20160928 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20161004 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20161021 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161202 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170104 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170202 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6087604 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |