JP5677752B2 - アルカリ水電解用電極、その製造方法及び水素発生装置 - Google Patents
アルカリ水電解用電極、その製造方法及び水素発生装置 Download PDFInfo
- Publication number
- JP5677752B2 JP5677752B2 JP2010041130A JP2010041130A JP5677752B2 JP 5677752 B2 JP5677752 B2 JP 5677752B2 JP 2010041130 A JP2010041130 A JP 2010041130A JP 2010041130 A JP2010041130 A JP 2010041130A JP 5677752 B2 JP5677752 B2 JP 5677752B2
- Authority
- JP
- Japan
- Prior art keywords
- electrode
- alloy
- alkaline water
- hydrogen
- water electrolysis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 title claims description 98
- 239000001257 hydrogen Substances 0.000 title claims description 96
- 229910052739 hydrogen Inorganic materials 0.000 title claims description 96
- 238000005868 electrolysis reaction Methods 0.000 title claims description 87
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 title claims description 69
- 238000004519 manufacturing process Methods 0.000 title description 23
- 229910018104 Ni-P Inorganic materials 0.000 claims description 129
- 229910018536 Ni—P Inorganic materials 0.000 claims description 129
- 229910045601 alloy Inorganic materials 0.000 claims description 129
- 239000000956 alloy Substances 0.000 claims description 129
- 238000004070 electrodeposition Methods 0.000 claims description 87
- 230000003746 surface roughness Effects 0.000 claims description 41
- 239000000758 substrate Substances 0.000 claims description 36
- 239000000463 material Substances 0.000 claims description 32
- 238000007788 roughening Methods 0.000 claims description 16
- 239000000203 mixture Substances 0.000 claims description 7
- 238000005192 partition Methods 0.000 claims description 4
- 238000005260 corrosion Methods 0.000 description 33
- 230000007797 corrosion Effects 0.000 description 33
- 239000002585 base Substances 0.000 description 25
- 238000007747 plating Methods 0.000 description 17
- 239000000243 solution Substances 0.000 description 13
- 239000010935 stainless steel Substances 0.000 description 13
- 229910001220 stainless steel Inorganic materials 0.000 description 13
- 239000007772 electrode material Substances 0.000 description 10
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 10
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 7
- 239000001301 oxygen Substances 0.000 description 7
- 229910052760 oxygen Inorganic materials 0.000 description 7
- 239000007864 aqueous solution Substances 0.000 description 6
- 230000007423 decrease Effects 0.000 description 6
- 238000010586 diagram Methods 0.000 description 5
- 239000003792 electrolyte Substances 0.000 description 5
- 238000000034 method Methods 0.000 description 5
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 4
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 3
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 3
- 239000004327 boric acid Substances 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- LAIZPRYFQUWUBN-UHFFFAOYSA-L nickel chloride hexahydrate Chemical compound O.O.O.O.O.O.[Cl-].[Cl-].[Ni+2] LAIZPRYFQUWUBN-UHFFFAOYSA-L 0.000 description 3
- RRIWRJBSCGCBID-UHFFFAOYSA-L nickel sulfate hexahydrate Chemical compound O.O.O.O.O.O.[Ni+2].[O-]S([O-])(=O)=O RRIWRJBSCGCBID-UHFFFAOYSA-L 0.000 description 3
- 229940116202 nickel sulfate hexahydrate Drugs 0.000 description 3
- 229910052698 phosphorus Inorganic materials 0.000 description 3
- 239000011574 phosphorus Substances 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 230000005611 electricity Effects 0.000 description 2
- 238000005530 etching Methods 0.000 description 2
- 125000001475 halogen functional group Chemical group 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- 229910052697 platinum Inorganic materials 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-N Fluorane Chemical compound F KRHYYFGTRYWZRS-UHFFFAOYSA-N 0.000 description 1
- 229910000990 Ni alloy Inorganic materials 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 229910001096 P alloy Inorganic materials 0.000 description 1
- 229910021607 Silver chloride Inorganic materials 0.000 description 1
- 229910001069 Ti alloy Inorganic materials 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 229910000808 amorphous metal alloy Inorganic materials 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000003486 chemical etching Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 229910001882 dioxygen Inorganic materials 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 229910000040 hydrogen fluoride Inorganic materials 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 239000007769 metal material Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000005498 polishing Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 229960000999 sodium citrate dihydrate Drugs 0.000 description 1
- KOUDKOMXLMXFKX-UHFFFAOYSA-N sodium oxido(oxo)phosphanium hydrate Chemical compound O.[Na+].[O-][PH+]=O KOUDKOMXLMXFKX-UHFFFAOYSA-N 0.000 description 1
- 238000004381 surface treatment Methods 0.000 description 1
- ISIJQEHRDSCQIU-UHFFFAOYSA-N tert-butyl 2,7-diazaspiro[4.5]decane-7-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCCC11CNCC1 ISIJQEHRDSCQIU-UHFFFAOYSA-N 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/36—Hydrogen production from non-carbon containing sources, e.g. by water electrolysis
Landscapes
- Electrodes For Compound Or Non-Metal Manufacture (AREA)
- Electrolytic Production Of Non-Metals, Compounds, Apparatuses Therefor (AREA)
Description
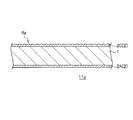
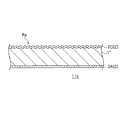
本発明に係るアルカリ水電解用電極11(11a,11b)は、図1及び図2に示すように、基材1の両面にアモルファス相のNi−P合金電析膜2C,2Aが設けられ、少なくともカソード電極となる側のNi−P合金電析膜2Cの表面が微細凹凸面になっていることを特徴とする。なお、アノード電極側Ni−P合金電析膜2Aの表面は微細凹凸面であってもなくてもよい。
基材1、1’は電極としての導電性とアルカリ水溶液に対する耐食性を有するものであればその種類は特に限定されないが、導電性と耐食性に優れた金属材料で構成されたものであることが好ましい。通常、低価格で耐食性のよいステンレス鋼が好ましく用いられる。ステンレス鋼の種類については特に限定されず、アルカリ水電解用溶液に対する耐食性を考慮して任意に選択される。また、チタン又はチタン合金、ニッケル又はニッケル合金、等であってもよい。
Ni−P合金電析膜2は、図1及び図2に示すように、カソード電極となるNi−P合金電析膜2Cと、アノード電極となるNi−P合金電析膜2Aとで構成される。これらのNi−P合金電析膜2はいずれもアモルファス相である。アモルファス相は、Ni−P合金中のP(リン)の含有率が通常、約7質量%以上で見られる。本願では、P含有率10質量%〜20質量%であることが好ましく、15質量%〜20質量%以下がより好ましい。Ni−P合金電析膜2中のP含有率をこの範囲内とすることにより、アルカリ水電解用溶液中でアノード電極及びカソード電極として用いても、良好な耐食性を示すことができる。また、基材1の両面に設けられたNi−P合金電析膜2C,2Aの組成が同じであるので、例えば単一のNi−P合金めっき液で基材1の両面にNi−P合金電析膜2C,2Aを析出させることができ、得られるアルカリ水電解用電極のより一層の低コスト化を図ることができる。また、耐食性のある安定した特性は、P含有率が10質量%〜20重量%の範囲で実現できる。なお、アモルファス相は、X線回折装置によりいわゆるハロー又はハロー形態が現れることにより同定することができる。
本発明に係るアルカリ水電解用電極の製造方法は、上記本発明に係るアルカリ水電解用電極を製造する方法であって、基材1の両面にNi−P合金めっき液を接触させてアモルファス相のNi−P合金を形成する工程を有し、少なくともカソード電極となる側のNi−P合金電析膜2Cの表面を微細凹凸面にすることを特徴とする。
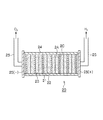
本発明に係る水素発生装置20は、図5に示すように、アルカリ水電解用電極板21と、隔壁22とを交互に複数配置した電解セル27を有する。具体的には、一方の面をアノード電極とし、他方の面をカソード電極とする複数の電極板21と、その複数の電極板21,…,21間に設けられた隔膜22とで構成された電解セル27を有している。その複数の電極板21,…,21は、既述した第1形態から第4形態のアルカリ水電解用電極を好ましく用いることができる。具体的には、図1及び図2に示すように、基材1,1’上にアモルファス相のNi−P合金電析膜2(2C,2A)が両面に設けられているアルカリ水電解用電極11a,11bを好ましく用いることができる。
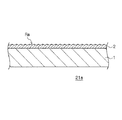
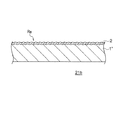
上記においては、基材の両面にNi−P合金電析膜を設けた例を説明したが、図3及び図4に示すように、Ni−P合金電析膜は基材の片面のみに形成されていてもよい。具体的には、基材面にアモルファス相のNi−P合金電析膜が設けられ、その電析膜の表面が微細凹凸面であることに特徴がある。なお、その微細凹凸面の表面粗さRaは0.3μm〜3μmであることが好ましい。この発明によれば、その微細凹凸面では、発生した水素の離脱が容易であることから、水素発生量が増し、水素発生効率と電流効率が良好なものとなる。また、上記と同様、Ni−P合金電析膜のP含有率が10質量%以上20質量%以下であることが好ましく、耐食性のある安定した特性は、P含有率が10質量%〜20重量%の範囲で実現できる。
(電極の作製)
基材1として、SUS304ステンレス鋼板(株式会社ニラコ製、厚さ0.5mm)を用い、めっき面の有効表面積が3cm2となるようにマスキングした。そのステンレス鋼板の表面をアセトン脱脂し、FeCl2を340〜380g/Lとした水溶液中に35〜37%塩酸を10〜50mLを入れて40〜50℃にしたエッチング液中に5分間浸漬した。エッチング後の電極表面に黒色皮膜の不純物が残るため、これを除去するために、15〜40%硝酸に軽く浸漬し、その後1〜10%のフッ化水素溶液に軽く浸漬した。このときのステンレス鋼板の表面粗さRaをAFM(原子間力顕微鏡、株式会社島津製作所製、SPM−9500J3、測定面積100μm×100μm)で測定し、付属のコンピュータ及びソフトウエアで算出した結果、表面粗さRaは0.11μmであった。
(2)Ni−P合金電析膜A:硫酸ニッケル六水和物200g/L、塩化ニッケル六水和物45g/L、ホウ酸35g/L、次亜リン酸ナトリウム一水和物15g/L
(3)Ni−P合金電析膜B:硫酸ニッケル六水和物100g/L、塩化ニッケル六水和物100g/L、ホウ酸30g/L、亜リン酸82g/L、クエン酸ナトリウム二水和物145g/L
上記(1)〜(3)で得られたアルカリ水電解用電極アルカリ水電解用電極を用い、アルカリ水電解を行った。水電解には、20質量%のNaOH水溶液を電解液として使用し、試験試料を陰極とし、SUS304ステンレス鋼板を陽極とし、電解電位を−2Vとし、常温で60分間電解を行った。この水電解に伴う電流値を計測して電流効率を測定し、また、発生した水素の捕集を行った。図6は、電流効率の測定装置と、発生した水素と酸素の捕集装置の模式的な構成図である。図6に示す測定装置40は、水槽47内に水酸化ナトリウム溶液(電解質46)を充填した測定セル44を配置し、その測定セル44内にNi−P合金電極41,42を隔壁45を介して配置している。各電極41,42に配線43を取り付け、その配線43はポテンシオスタット48に接続され、そのポテンシオスタット48はパソコン49に接続されている。
電流効率は、図6に示す装置を用い、[(ポテンシオスタット48から与えた電気量)/(観測された電気量)×100](%)を電流効率として得た。また、カソード電極の電解前後の表面状態をSEMとEDXより観察した。また、電気化学的特性を考察するために、−1.5〜0.6Vの範囲でCVを行った。電位走査速度は100mV/sec、参照電極にはAg/AgClを用い、対極にはNi電極を使用した。また、LSV(電位走査法)を用いて交換電流密度を測定した。
水素発生量は、P含有率の異なるNi−P合金電析膜A,Bのいずれも8mL前後であり大差はなかった。なお、ブランクとして用いたステンレス鋼板(Ni−P合金電析膜を設ける前のものと同じもの)は、水素発生量がかなり小さく、半分の4mL程度であった。このときの交換電流密度は、純Ni電析膜で−4.44A/cm2、Ni−P合金電析膜1で−4.27A/cm2、Ni−P合金電析膜2で−4.48A/cm2、であった。なお、ブランクとして用いたステンレス鋼板の表面粗さRaは0.12μm程度であったのに対し、Ni−P合金電析膜1,2の表面粗さRaはそれより大きく、0.3μm〜0.5μmであった。
表面粗さRaと水素発生量との関係について検討した。基材であるステンレス鋼板を、(i)粗面化処理しない基材1、(ii)粗面化処理した基材1’、を準備し、その水素発生量と表面粗さRaと電流効率の関係を検討した。粗面化処理は、各種の研磨紙を試して行い、表面粗さRaが0.5μm、1μm、2μm、5μmの範囲で各種作製した。なお、粗面化処理していない基材1の表面粗さRaは0.12μmである。各基材1,1’上に、Ni−P合金電析膜1,2を形成した。Ni−P合金電析膜1,2を形成した後の表面粗さRaは、粗面化した基材1’上に形成したものは、それぞれ0.3μm、0.6μm、1μm、3μm程度になり、めっきする前より少し小さくなった。
この実験例3では、耐食性の実験を行った。Ni−P合金電析膜の耐食性は、実験例1の条件、すなわち、20質量%のNaOH水溶液を電解液として使用し、試験試料を陰極とし、SUS304ステンレス鋼板を陽極とし、電解電位を−2Vとし、常温で電解を継続して行った。その結果、ステンレス鋼板や純Niめっき板では交換しなければならない時期が来ても、アノード電極とカソード電極のいずれも交換しなくてもよい程度の耐食性であった。
両面とも粗面化処理をした。実験例2と同様の表面粗さ条件を作り、アノード電極側とカソード電極側の両方のNi−P合金電析膜の表面を微細凹凸面とした。実験例2では、カソード電極での水素の離脱が効果的に行われていたが、アノード電極側でも酸素の離脱が効果的に行われているのが確認された。両面へのNi−P合金電析膜の形成は、めっき液に入れて電解するだけで簡単に行えるので、コスト低減には極めて有望である。
1’ 予め粗面化された基材
2 Ni−P合金電析膜
2A アノード電極側の電析膜
2C カソード電極側の電析膜
11(11a,11b) アルカリ水電解用電極
21a,21b アルカリ水電解用電極
20 水素発生装置
21 両面電極タイプのNi−P合金電極板
22 隔膜
23 電解質(アルカリ水溶液)
24,25 電解セルを構成する保持プレート
26 ガス配管
27 電解セル
40 測定装置
41,42 Ni−P合金電極
43 配線
44 測定セル
45 隔壁
46 電解質(アルカリ水溶液)
47 水槽
48 ポテンシオスタット
49 コンピュータ
Claims (3)
- アルカリ水電解用電極と、隔壁とを交互に複数配置した電解セルを有する水素発生装置であって、
前記アルカリ水電解用電極は、基材の両面にアモルファス相のNi−P合金電析膜が設けられ、少なくともカソード電極となる側のNi−P合金電析膜の表面が、表面粗さRaが0.3μm〜3μmの微細凹凸面になっており、
前記基材の両面に設けられたNi−P合金電析膜の組成が同じであって、かつそのP含有率が10質量%以上20質量%以下であることを特徴とする水素発生装置。 - 前記カソード電極側の基材面が予め粗面化処理され、粗面化処理された基材面にNi−P合金電析膜が形成されている、請求項1に記載の水素発生装置。
- 前記カソード電極側の基材面は粗面化処理されておらず、粗面化処理されていない基材面にNi−P合金電析膜が形成されている、請求項1に記載の水素発生装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010041130A JP5677752B2 (ja) | 2010-02-25 | 2010-02-25 | アルカリ水電解用電極、その製造方法及び水素発生装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010041130A JP5677752B2 (ja) | 2010-02-25 | 2010-02-25 | アルカリ水電解用電極、その製造方法及び水素発生装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011174162A JP2011174162A (ja) | 2011-09-08 |
| JP5677752B2 true JP5677752B2 (ja) | 2015-02-25 |
Family
ID=44687273
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010041130A Expired - Fee Related JP5677752B2 (ja) | 2010-02-25 | 2010-02-25 | アルカリ水電解用電極、その製造方法及び水素発生装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5677752B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5908372B2 (ja) * | 2012-08-21 | 2016-04-26 | 住友金属鉱山エンジニアリング株式会社 | 電気分解用電極 |
| CN115418687A (zh) * | 2021-05-14 | 2022-12-02 | 中国科学院金属研究所 | 一种电镀溶液及碱性电解水制氢用电极板的制备方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5344485A (en) * | 1976-10-05 | 1978-04-21 | Asahi Glass Co Ltd | Electrode |
| JPS5845388A (ja) * | 1981-09-09 | 1983-03-16 | Chlorine Eng Corp Ltd | 電解槽 |
| JPS61264187A (ja) * | 1986-01-22 | 1986-11-22 | Showa Denko Kk | 水溶液電解方法 |
| JP3426937B2 (ja) * | 1997-10-27 | 2003-07-14 | 三菱重工業株式会社 | 高分子水電解用セル製造方法及び高分子水電解用セル |
-
2010
- 2010-02-25 JP JP2010041130A patent/JP5677752B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2011174162A (ja) | 2011-09-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Zhao et al. | Electrochemical reduction of CO2 to formate in aqueous solution using electro-deposited Sn catalysts | |
| Wang et al. | The enhanced electrocatalytic activity and stability of NiW films electrodeposited under super gravity field for hydrogen evolution reaction | |
| Zhang et al. | Effect of CeO2 and graphite powder on the electrochemical performance of Ti/PbO2 anode for zinc electrowinning | |
| González-Buch et al. | Study of the catalytic activity of 3D macroporous Ni and NiMo cathodes for hydrogen production by alkaline water electrolysis | |
| Abdel-Karim et al. | Surface morphology and electrochemical characterization of electrodeposited Ni–Mo nanocomposites as cathodes for hydrogen evolution | |
| JP5008043B1 (ja) | 塩素発生用陽極 | |
| JP5616633B2 (ja) | 電解用陽極 | |
| EP3101159A1 (en) | Method for manufacturing aluminum plate, aluminum plate, current collector for electric storage device, and electric storage device | |
| Shetty et al. | Magnetically induced electrodeposition of Ni-Mo alloy for hydrogen evolution reaction | |
| Seetharaman et al. | Electrochemical behaviour of nickel-based electrodes for oxygen evolution reaction in alkaline water electrolysis | |
| JP5701080B2 (ja) | アルカリ水電解用電極、その製造方法及び水素発生装置 | |
| Boudjehem et al. | Effect of deposition conditions on the properties of Ni–Mo–W coatings as electrocatalysts for hydrogen evolution reaction | |
| CN102899682A (zh) | 氯碱工业用纳米结构镍钼活性阴极及其制备方法 | |
| JP5677752B2 (ja) | アルカリ水電解用電極、その製造方法及び水素発生装置 | |
| Belhani et al. | Enhanced electrocatalytic activity of Ni-Mn-Co-Fe alloys for efficient hydrogen and oxygen evolution reactions: A study on the effects of electrodeposition parameters | |
| Wang et al. | Fabrication of micro/nano wettability MoS2 hydrogen evolution electrocatalyst based on femtosecond laser | |
| JP6803069B2 (ja) | アルカリ水電解用電極、その製造方法及び水素発生装置 | |
| CN101717950A (zh) | 电解煤浆的阳极催化电极的制备方法 | |
| Yan et al. | Microrod structure and properties of Sb-doped Ti/SnO2 anodes prepared by magnetron sputtering | |
| CN114622238B (zh) | 一种过渡金属基析氢析氧双功能电极的制备及应用 | |
| JP5802085B2 (ja) | アルカリ水電解用電極の製造方法 | |
| JP5600011B2 (ja) | 水素ガス製造方法 | |
| CN101717948B (zh) | 氯碱工业用纳米结构镍钨磷活性阴极及其制备方法 | |
| Zhang et al. | Electrocatalytic properties of nickel foam-based Ni-Mo, Ni+ Mo and Ni+ Mo/Ni-Mo electrodes for hydrogen evolution reaction | |
| CN102363892A (zh) | 一种活性阴极的制造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130206 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130520 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130528 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130729 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140415 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140616 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20141202 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150105 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5677752 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |