JP5483023B2 - がん細胞運動およびがん細胞浸潤抑制剤 - Google Patents
がん細胞運動およびがん細胞浸潤抑制剤 Download PDFInfo
- Publication number
- JP5483023B2 JP5483023B2 JP2010505602A JP2010505602A JP5483023B2 JP 5483023 B2 JP5483023 B2 JP 5483023B2 JP 2010505602 A JP2010505602 A JP 2010505602A JP 2010505602 A JP2010505602 A JP 2010505602A JP 5483023 B2 JP5483023 B2 JP 5483023B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- par1
- cells
- seq
- present
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 206010028980 Neoplasm Diseases 0.000 title claims description 68
- 201000011510 cancer Diseases 0.000 title claims description 50
- 230000009087 cell motility Effects 0.000 title description 23
- 230000004709 cell invasion Effects 0.000 title description 16
- 239000003112 inhibitor Substances 0.000 title description 2
- 210000004027 cell Anatomy 0.000 claims description 100
- 230000000694 effects Effects 0.000 claims description 48
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 37
- 239000012634 fragment Substances 0.000 claims description 30
- 238000000034 method Methods 0.000 claims description 28
- 230000002401 inhibitory effect Effects 0.000 claims description 20
- 210000004408 hybridoma Anatomy 0.000 claims description 16
- 210000004881 tumor cell Anatomy 0.000 claims description 16
- 239000008194 pharmaceutical composition Substances 0.000 claims description 14
- 230000004899 motility Effects 0.000 claims description 9
- 239000000203 mixture Substances 0.000 claims description 8
- 238000003384 imaging method Methods 0.000 claims description 7
- 238000004519 manufacturing process Methods 0.000 claims description 7
- 239000003814 drug Substances 0.000 claims description 6
- 238000005516 engineering process Methods 0.000 claims description 5
- 239000012216 imaging agent Substances 0.000 claims description 5
- 108010070519 PAR-1 Receptor Proteins 0.000 description 154
- 102100037136 Proteinase-activated receptor 1 Human genes 0.000 description 154
- 108090000765 processed proteins & peptides Proteins 0.000 description 79
- 238000003776 cleavage reaction Methods 0.000 description 24
- 230000007017 scission Effects 0.000 description 24
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 23
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 23
- 239000000243 solution Substances 0.000 description 21
- 241000699666 Mus <mouse, genus> Species 0.000 description 19
- 239000000523 sample Substances 0.000 description 19
- 230000027455 binding Effects 0.000 description 17
- 239000000427 antigen Substances 0.000 description 14
- 102000036639 antigens Human genes 0.000 description 14
- 108091007433 antigens Proteins 0.000 description 14
- 230000000890 antigenic effect Effects 0.000 description 12
- 206010003445 Ascites Diseases 0.000 description 9
- 150000001413 amino acids Chemical class 0.000 description 9
- 102000004196 processed proteins & peptides Human genes 0.000 description 9
- 239000002246 antineoplastic agent Substances 0.000 description 8
- 108010082117 matrigel Proteins 0.000 description 8
- 108090000631 Trypsin Proteins 0.000 description 7
- 102000004142 Trypsin Human genes 0.000 description 7
- 230000001419 dependent effect Effects 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- 239000012588 trypsin Substances 0.000 description 7
- 102000014914 Carrier Proteins Human genes 0.000 description 6
- 108010078791 Carrier Proteins Proteins 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 108010045069 keyhole-limpet hemocyanin Proteins 0.000 description 6
- 230000033001 locomotion Effects 0.000 description 6
- 238000011579 SCID mouse model Methods 0.000 description 5
- 108090000190 Thrombin Proteins 0.000 description 5
- 239000012228 culture supernatant Substances 0.000 description 5
- 238000001514 detection method Methods 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 230000037023 motor activity Effects 0.000 description 5
- 229960004072 thrombin Drugs 0.000 description 5
- 102000000380 Matrix Metalloproteinase 1 Human genes 0.000 description 4
- 108010016113 Matrix Metalloproteinase 1 Proteins 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- XOJVVFBFDXDTEG-UHFFFAOYSA-N pristane Chemical compound CC(C)CCCC(C)CCCC(C)CCCC(C)C XOJVVFBFDXDTEG-UHFFFAOYSA-N 0.000 description 4
- 238000004445 quantitative analysis Methods 0.000 description 4
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- 206010006187 Breast cancer Diseases 0.000 description 3
- 208000026310 Breast neoplasm Diseases 0.000 description 3
- 108091006027 G proteins Proteins 0.000 description 3
- 102000030782 GTP binding Human genes 0.000 description 3
- 108091000058 GTP-Binding Proteins 0.000 description 3
- 101000741967 Homo sapiens Presequence protease, mitochondrial Proteins 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 102100038632 Presequence protease, mitochondrial Human genes 0.000 description 3
- 102000003790 Thrombin receptors Human genes 0.000 description 3
- 108090000166 Thrombin receptors Proteins 0.000 description 3
- 229940125644 antibody drug Drugs 0.000 description 3
- 229940098773 bovine serum albumin Drugs 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 230000009545 invasion Effects 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000009870 specific binding Effects 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 108010088751 Albumins Proteins 0.000 description 2
- 102000009027 Albumins Human genes 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 108010058846 Ovalbumin Proteins 0.000 description 2
- 108090000901 Transferrin Proteins 0.000 description 2
- 102000004338 Transferrin Human genes 0.000 description 2
- 210000000683 abdominal cavity Anatomy 0.000 description 2
- 238000001261 affinity purification Methods 0.000 description 2
- 239000005667 attractant Substances 0.000 description 2
- 210000004204 blood vessel Anatomy 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000031902 chemoattractant activity Effects 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 238000002372 labelling Methods 0.000 description 2
- 238000013507 mapping Methods 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 229940092253 ovalbumin Drugs 0.000 description 2
- 230000010118 platelet activation Effects 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 230000001629 suppression Effects 0.000 description 2
- 239000012581 transferrin Substances 0.000 description 2
- 239000004475 Arginine Substances 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 229920002684 Sepharose Polymers 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 238000002073 fluorescence micrograph Methods 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000011503 in vivo imaging Methods 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 208000030776 invasive breast carcinoma Diseases 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 208000037819 metastatic cancer Diseases 0.000 description 1
- 208000011575 metastatic malignant neoplasm Diseases 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000002823 phage display Methods 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 238000002603 single-photon emission computed tomography Methods 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/502—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing non-proliferative effects
- G01N33/5029—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing non-proliferative effects on cell motility
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/02—Screening involving studying the effect of compounds C on the interaction between interacting molecules A and B (e.g. A = enzyme and B = substrate for A, or A = receptor and B = ligand for the receptor)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
Description
(1)PAR1(プロテアーゼ活性化受容体1)に特異的に結合してMMP1(マトリックスメタロプロテアーゼ1)による切断を阻害し、がん細胞の運動活性および浸潤活性を阻害する抗体、または該抗体と同様の性質を保持する該抗体のフラグメント;
(2)PAR1(プロテアーゼ活性化受容体1)のMMP1(マトリックスメタロプロテアーゼ1)による切断部位(Arg41とSer42の間)を含む領域をエピトープとして特異的に結合し、がん細胞の運動活性および浸潤活性を阻害する(1)記載の抗体、または該抗体と同様の性質を保持する該抗体のフラグメント;
(3)該エピトープのアミノ酸配列が配列番号:1で示されるものである(2)記載の抗体、または該抗体と同様の性質を保持する該抗体のフラグメント;
(4)独立行政法人産業技術総合研究所 特許生物寄託センターから受託番号FERM BP−11105を付与されたハイブリドーマにより産生されるモノクローナル抗体である、(3)記載の抗体、または該抗体と同様の性質を保持する該抗体のフラグメント;
(5)キメラ化またはヒト化されている、(1)〜(4)のいずれかに記載の抗体、または該抗体と同様の性質を保持する該抗体のフラグメント;
(6)モノクローナル抗体である(1)〜(5)いずれかに記載の抗体;
(7)ポリクローナル抗体である(1)〜(3)または(5)のいずれかに記載の抗体;
(8)(1)〜(7)のいずれかに記載の抗体またはフラグメントを含む、がん細胞の運動活性および浸潤活性を阻害するための組成物;
(9)(1)〜(7)のいずれかに記載の抗体またはフラグメントを含む、がん治療用医薬組成物;
(10)(1)〜(7)のいずれかに記載の抗体またはフラグメントを含む、医薬組成物の有効量を治療を必要とする対象に投与することを含むがんの治療方法;
(11)がんを治療するための医薬の製造における(1)〜(7)のいずれかに記載の抗体またはフラグメントの使用;
(12)(1)〜(7)のいずれかに記載の抗体またはフラグメントを、対象から得た試料と接触させ、試料中の腫瘍細胞と結合させることを特徴とする、試料中の腫瘍細胞のイメージング方法または腫瘍の検出方法;
(13)(1)〜(7)のいずれかに記載の抗体またはフラグメントを含む、腫瘍細胞イメージング剤;
(14)(1)〜(7)のいずれかに記載の抗体または抗体フラグメントを対象に投与して、体内の腫瘍組織と本発明の抗体または抗体フラグメントとの結合を調べることを特徴とする、腫瘍の診断方法;
(15)配列番号:1で示されるアミノ酸配列からなるペプチド;
(16)配列番号:1で示されるアミノ酸配列からなるペプチドおよびキャリア蛋白からなる抗原性ペプチド;
(17)(15)記載のペプチドまたは(16)記載の抗原性ペプチドを用いることを特徴とする、PAR1に特異的に結合してMMP1による切断を阻害する抗体、または該抗体と同様の性質を保持する該抗体のフラグメントの作製方法;
(18)(15)記載のペプチドまたは(16)記載の抗原性ペプチドを用いることを特徴とする、PAR1に特異的に結合してMMP1による切断を阻害する抗体、または該抗体と同様の性質を保持する該抗体のフラグメントの精製方法;
(19)(15)記載のペプチドまたは(16)記載の抗原性ペプチドを含む、がん細胞の運動活性および浸潤活性を阻害するための組成物
を提供するものである。
(A)PAR1の切断部位(R41とS42の間)をまたぐような配列(N35ATLDPRSFLL45)(配列番号:1)、および(B)PAR1の切断部位(R41とS42の間)よりも内側に位置する配列(45LRNPNDKYEPFWEDEEKKNES64)(配列番号:22)を標的として選択し、(A)配列のN末および(B)配列のC末にCを付加したC−N35ATLDPRSFLL45(配列番号:2)ペプチドおよびL45RNPNDKYEPFWEDEEKKNES64−C(配列番号:23)ペプチドを合成した。CのSH基を用いて合成ペプチドをKLHと架橋し、これを抗原としてマウスを免疫し、11種のハイブリドーマを得た。これらのハイブリドーマを、それぞれPAR1 N2−1〜PAR1 N2−11およびPAR1 N3−1〜PAR1 N3−11と命名し、そのうち、ハイブリドーマの培養上清を用いたマトリゲルアッセイから効果が最も強力であったPAR1 N2−11および配列番号:23に非常に強い結合活性を示したPAR1 N3−1を選択し、抗体特異性および抗体効果の解析を行った。PAR1 N2−11により産生される抗体をN2−11、PAR1 N3−1により産生される抗体をN3−1と命名した。このうち、N2−11抗体を産生するハイブリドーマは、PAR1 N2−11と命名し、ブタペスト条約の下、平成20年(2008年)3月18日より、日本国茨城県つくば市東1丁目1番地1中央第6の、独立行政法人産業技術総合研究所 特許生物寄託センターにFERM BP−11105の受託番号で寄託してある。N2−11抗体およびN3−1抗体のクラス決定を行った結果、IgG1のクラスに属することが判明した。
本発明のN2−11抗体の抗原認識部位を以下のように決定した。PAR1の部分アミノ酸配列A26RRPESKATNATLDPRSFLLRNPNDKYEP54(配列番号:3)に基づき12個のアミノ酸のペプチドを18種類作製し(以下、本明細書においてペプチド(1)〜(18)という)、ELISA法によるエピトープマッピングを行った。ペプチド(1)〜(18)のアミノ酸配列は以下のとおりであった。
ペプチド(1)ARRPESKATNAT(配列番号:4)
ペプチド(2)RRPESKATNATL(配列番号:5)
ペプチド(3)RPESKATNATLD(配列番号:6)
ペプチド(4)PESKATNATLDP(配列番号:7)
ペプチド(5)ESKATNATLDPR(配列番号:8)
ペプチド(6)SKATNATLDPRS(配列番号:9)
ペプチド(7)KATNATLDPRSF(配列番号:10)
ペプチド(8)ATNATLDPRSFL(配列番号:11)
ペプチド(9)TNATLDPRSFLL(配列番号:12)
ペプチド(10)NATLDPRSFLLR(配列番号:13)
ペプチド(11)ATLDPRSFLLRN(配列番号:14)
ペプチド(12)TLDPRSFLLRNP(配列番号:15)
ペプチド(13)LDPRSFLLRNPN(配列番号:16)
ペプチド(14)DPRSFLLRNPND(配列番号:17)
ペプチド(15)PRSFLLRNPNDK(配列番号:18)
ペプチド(16)RSFLLRNPNDKY(配列番号:19)
ペプチド(17)SFLLRNPNDKYE(配列番号:20)
ペプチド(18)FLLRNPNDLYEP(配列番号:21)
本発明のN3−1抗体の抗原認識部位を以下のように決定した。PAR1の部分アミノ酸配列A36TLDPRSFLLRNPWEDEEKNESGLTEYRLVS73(配列番号:24)に基づき12個のアミノ酸のペプチドを27種類作製し(以下、本明細書においてPAR1−N3−(1)〜(27)という)、ELISA法によるエピトープマッピングを行った。PAR1−N3−(1)〜(27)のアミノ酸配列は以下のとおりであった。
PAR1−N3−(1)ATLDPRSFLLRN(配列番号:25)
PAR1−N3−(2)TLDPRSFLLRNP(配列番号:26)
PAR1−N3−(3)LDPRSFLLRNPN(配列番号:27)
PAR1−N3−(4)DPRSFLLRNPND(配列番号:28)
PAR1−N3−(5)PRSFLLRNPNDK(配列番号:29)
PAR1−N3−(6)RSFLLRNPNDKY(配列番号:30)
PAR1−N3−(7)SFLLRNPNDKYE(配列番号:31)
PAR1−N3−(8)FLLRNPNDKYEP(配列番号:32)
PAR1−N3−(9)LLRNPNDKYEPF(配列番号:33)
PAR1−N3−(10)LRNPNDKYEPFW(配列番号:34)
PAR1−N3−(11)RNPNDKYEPFWE(配列番号:35)
PAR1−N3−(12)NPNDKYEPFWED(配列番号:36)
PAR1−N3−(13)PNDKYEPFWEDE(配列番号:37)
PAR1−N3−(14)NDKYEPFWEDEE(配列番号:38)
PAR1−N3−(15)DKYEPFWEDEEK(配列番号:39)
PAR1−N3−(16)KYEPFWEDEEKN(配列番号:40)
PAR1−N3−(17)YEPFWEDEEKNE(配列番号:41)
PAR1−N3−(18)EPFWEDEEKNES(配列番号:42)
PAR1−N3−(19)PFWEDEEKNESG(配列番号:43)
PAR1−N3−(20)FWEDEEKNESGL(配列番号:44)
PAR1−N3−(21)WEDEEKNESGLT(配列番号:45)
PAR1−N3−(22)EDEEKNESGLTE(配列番号:46)
PAR1−N3−(23)DEEKNESGLTEY(配列番号:47)
PAR1−N3−(24)EEKNESGLTEYR(配列番号:48)
PAR1−N3−(25)EKNESGLTEYRL(配列番号:49)
PAR1−N3−(26)KNESGLTEYRLV(配列番号:50)
PAR1−N3−(27)NESGLTEYRLVS(配列番号:51)
N2−11抗体およびN3−1抗体が、トロンビンに依存する細胞浸潤活性をどの程度阻害できるのかを調べるために、マトリゲルアッセイを用いて、抗体の浸潤阻害効果を試験した。第1に、アッセイを用いる細胞を調製するため、低浸潤性乳がん培養細胞KPL−4(PAR1低発現株)にPAR1−GFPを安定発現させた細胞株(以下、本明細書においてPAR1発現KPL−4という)を作製した。1.5x105細胞のPAR1発現KPL−4細胞をトリプシン処理により浮遊させ、PBSで洗浄した。3および10μMのN2−11抗体または10μMのN3−1抗体またはコントロール抗体である3および10μMのマウスIgGを添加し、37℃で90分間保温した。次いで、セルカルチャーインサート(BD バイオサイエンス社)に細胞を蒔き、37℃で45時間培養した。インサートを浸す誘引物質溶液には、10%FBS含有2.5U/mlトロンビン(WAKO社)溶液を用い、45時間後にメンブレンフィルターの底面に移動してきた浸潤細胞をHE染色し、浸潤細胞数をカウントした。浸潤細胞数のカウントは、フィルター内のランダムな地点を0.66mmX0.66mmの大きさでスキャンし、その平均細胞数を算出した。次いで、マウスIgGで処理した場合の浸潤細胞数を100%としたときのN2−11抗体およびN3−1抗体処理時の浸潤細胞数の割合を図3に示す。なお、10μMのマウスIgGで処理した場合の浸潤細胞数は、約2.4x103細胞であった。図3において、(a)は3μM N2−11抗体(n=30)処理時、(b)は10μM N2−11抗体(n=80)処理時、および(c)は10μM N3−1抗体(n=40)処理時の細胞数の割合を示す。
10μMの抗体濃度において、N2−11抗体は40%の阻害効果を有することが判明したが、N3−1抗体にはこのような活性はみられなかった(図3(b)および(c)参照)。このため、PAR1の52番目のTyrから56番目のTrpを含む配列をエピトープとする抗体は、細胞浸潤能を阻害しないことが分かる。
N2−11抗体が細胞表面のPAR1を特異的に認識できるかを評価するため、PAR1発現KPL−4を作製し、次いで、KPL−4およびPAR1発現KPL−4に対するN2−11抗体の特性について以下の(A)〜(D)により検討した:
(A)KPL−4細胞をトリプシン処理により浮遊させ、FBS不含L−15溶液(GIBCO社)で洗浄した。2μM マウスIgG(SIGMA社)含有L−15培地を添加し、37℃で15分間保温し、ブロッキングを行い、さらに40nMのN2−11抗体−QDプローブを添加し、37℃で30分間保温した。次いで、N2−11抗体−QDプローブをL−15培地で洗浄し、0.5%FBS含有L−15培地を添加し、ガラスボトムディシュに細胞を蒔き、細胞の観察および解析を行った。なお、N2−11抗体−QDプローブは、N2−11抗体と高輝度の蛍光性ナノ粒子(QD705(Invitrogen社))を結合させたプローブである。
(B)PAR1発現KPL−4をトリプシン処理により浮遊させ、FBS不含L−15溶液(GIBCO社)で洗浄した。2μM マウスIgG(SIGMA社)含有L−15培地を添加し、37℃で15分間保温し、ブロッキングを行い、さらに40nMのN2−11抗体−QDプローブを添加し、37℃で30分間保温した。次いで、N2−11抗体−QDプローブをL−15培地で洗浄し、0.5%FBS含有L−15培地を添加し、ガラスボトムディシュに細胞を蒔き、細胞の観察および解析を行った。
(C)PAR1発現KPL−4をトリプシン処理により浮遊させ、FBS不含L−15溶液(GIBCO社)で洗浄した。50nM MMP1(SIGMA社)を添加し、37℃で60分間保温した。2μM マウスIgG(SIGMA社)含有L−15培地を添加し、37℃で15分間保温し、ブロッキングを行い、さらに40nMのN2−11抗体−QDプローブを添加し、37℃で30分間保温した。次いで、N2−11抗体−QDプローブをL−15培地で洗浄し、0.5%FBS含有L−15培地を添加し、ガラスボトムディシュに細胞を蒔き、細胞の観察および解析を行った。
(D)PAR1発現KPL−4をトリプシン処理により浮遊させ、FBS不含L−15溶液(GIBCO社)で洗浄した。2μM マウスIgG(SIGMA社)含有L−15を添加し、37℃で15分間保温し、ブロッキングを行い、さらに40nMのN2−11抗体−QDプローブを添加し、37℃で30分間保温した。次いで、N2−11抗体−QDプローブをL−15培地で洗浄し、50nM MMP1を添加し、37℃で60分間保温した。さらに、L−15培地で洗浄し、0.5%FBS含有L−15培地を添加し、ガラスボトムディシュに細胞を蒔き、細胞の観察および解析を行った。
上記(A)〜(D)により得られた細胞およびそのデータに基づく定量的解析結果を図4に示す。なお、(A)〜(D)の結果は図中のカラム1〜4にそれぞれ対応している。細胞を観察した結果、KPL−4細胞ではPAR1の発現量が少ないことから、N2−11抗体−QDが僅かしか反応していなかったこと(カラム1)、PAR1発現KPL−4ではN2−11抗体−QDによる標識により、「細胞膜上のPAR1」および「細胞内に取り込まれたPAR1」がドット状に強く標識されていたこと(カラム2)、MMP1で細胞膜上のPAR1が切断されているため、N2−11抗体がPAR1を認識できず、N2−11抗体−QDで標識されなかったこと(カラム3)、ならびにPAR1発現KPL−4をN2−11抗体−QDで標識した後にMMP1で処理した場合には、N2−11抗体がカラム2と同程度細胞に結合していたこと(カラム4)が示された。また、定量的解析の右パネルにより、PAR1発現KPL−4に結合するN2−11抗体の量はKPL−4に結合する量の約6倍であること、PAR1発現KPL−4を50nM MMP1で処理した場合には、N2−11抗体の結合量はKPL−4と同レベルになること、ならびにN2−11抗体で標識後にMMP1処理した場合には、N2−11抗体がMMP1未処理の場合とほぼ同程度結合していることが示された。
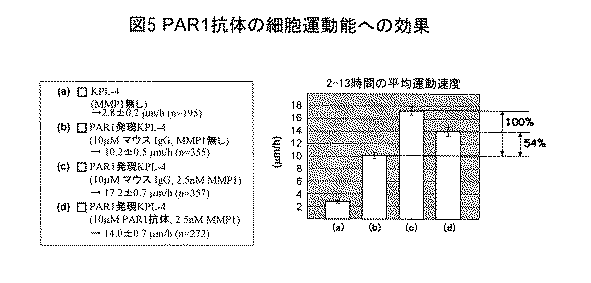
PAR1発現KPL−4細胞は、MMP1処理によりPAR1が活性化し、細胞浸潤能が促進される。そこで、PAR1発現KPL−4の細胞運動の経時的コマ撮り撮影(Time−laps)観察およびその運動軌跡解析を行い、N2−11抗体がMMP1依存的な細胞運動能を阻害するかを検討した。7x104細胞のPAR1発現KPL−4細胞をトリプシン処理により浮遊させ、PBSで洗浄した。10μMのN2−11抗体またはコントロール抗体であるマウスIgGを添加し、37℃で60分間保温した。次いで、2.5nM MMP1を含む10%FBS含有L−15培地を添加し、ガラスボトムデッシュに細胞を蒔いた。細胞運動の経時的コマ撮り撮影画像を2分ごとに取得し、細胞運動の軌跡を追跡した。経時的コマ撮り撮影観察開始後、2−13時間の間の1時間当たりの平均運動速度を算出した。細胞運動の軌跡では、核の重心位置を指標とし、データに偏りが出ないように追跡可能な全ての細胞を解析した。また、コントロール実験として、KPL−4細胞およびMMP1未処理のPAR1発現KPL−4細胞についても同様に解析を行った。
N2−11抗体の算出された平均運動速度を図5に示し、その算出値を表1に示す。
PAR1発現KPL−4細胞は、MMP1処理によりPAR1が活性化し、細胞浸潤能が促進される。そこで、N2−11抗体存在下でPAR1発現KPL−4のマトリゲルアッセイを行い、N2−11抗体がMMP1依存的な細胞浸潤能を阻害するかを検討した。1.5x105細胞のPAR1発現KPL−4細胞をトリプシン処理により浮遊させ、PBSで洗浄した。3および10μMのN2−11抗体またはコントロール抗体であるマウスIgGを添加し、37℃で90分間保温した。次いで、セルカルチャーインサートに細胞を蒔き、37℃で45時間培養した。インサートを浸す誘引物質溶液には、10%FBS含有2.5nM MMP1溶液を用い、45時間後にメンブレンフィルターの底面に移動してきた浸潤細胞をHE染色し、浸潤細胞数をカウントした。浸潤細胞数のカウントは、フィルター内のランダムな地点を0.66mmX0.66mmの大きさでスキャンし、その平均細胞数を算出した。次いで、マウスIgGで処理した場合の浸潤細胞数を100%としたときのN2−11抗体処理時の浸潤細胞数の割合を求めた。
実施例5と同様のN2−11抗体−QDをプローブに用いて、独自のインビボイメージング法により腫瘍組織の生体染色を行い、上記により調製された抗体が腫瘍組織のPAR1に対し特異的であるかを検討した。SCIDマウスに1x106細胞のPAR1発現KPL−4細胞を皮下注入した。次いで、4週間飼育しPAR1発現KPL−4細胞由来の腫瘍を作製した。腫瘍を露出させて観察用の小窓を作製した後、N2−11抗体−QDプローブを血中濃度10nMで尾静脈より注入した。次いで、独自のイメージング装置を用いて、生きたマウスの腫瘍組織を観察した。
N2−11抗体−QDが腫瘍細胞に特異的に反応している像を図7に示す。図7より、マウス生体内において、N2−11抗体が腫瘍細胞に対し特異的であることが示された。したがって、濃度や結合能(結合定数)を高めることにより、N2−11抗体が生きた腫瘍細胞のPAR1活性を阻害する可能性を示唆している。
PAR1の切断部位(R41とS42の間)をまたぐような配列(N35ATLDPRSFLL45)(配列番号:1)を標的として選択し、この配列のN末にCを付加したCN35ATLDPRSFLL45(配列番号:2)ペプチドを合成した。CのSH基を利用して合成ペプチドをKLHと架橋し、これを抗原としてウサギを免役し、PAR1に対する抗血清を調製した。次いで、抗血清のアフィニティー精製を行うため、抗原に用いたペプチドとSulfoLinkカップリングゲル(PIERCE社)を用いてカラムを作製した。カラムに抗血清をアプライした後、カラム体積の5倍以上のPBS(pH7.2)でカラムの洗浄を行った。その後、3M MgCl2でPAR1ポリクローナル抗体の溶出を行った。溶出後はPBSにて透析を行い、精製PAR1抗体とした(10mlの抗血清から約0.4mgの精製抗体を得た)。ポリクローナル抗体の細胞浸潤活性を、モノクローナル抗体のアッセイと同様の方法でマトリゲルを用いて検討した。コントロールとして300nMのウサギIgGを用いた。
条件(a)の平均浸潤細胞数を100%とした場合におけるPAR1ポリクローナル抗体処理時の浸潤細胞数割合を図8に示し、その算出値を以下の表3に示す。
Claims (7)
- 独立行政法人産業技術総合研究所 特許生物寄託センターから受託番号FERM BP−11105を付与されたハイブリドーマにより産生されるモノクローナル抗体、またはアミノ酸配列が配列番号:1で示されるものであるエピトープに特異的に結合する該抗体のフラグメント。
- キメラ化またはヒト化されている、請求項1記載の抗体、またはアミノ酸配列が配列番号:1で示されるものであるエピトープに特異的に結合する該抗体のフラグメント。
- 請求項1または2記載の抗体またはフラグメントを含む、がん細胞の運動活性および浸潤活性を阻害するための組成物。
- 請求項1または2記載の抗体またはフラグメントを含む、がん治療用医薬組成物。
- がんを治療するための医薬の製造における請求項1または2記載の抗体またはフラグメントの使用。
- 請求項1または2記載の抗体またはフラグメントを、対象から得た試料と接触させ、試料中の腫瘍細胞と結合させることを特徴とする、試料中の腫瘍細胞のイメージング方法または腫瘍細胞の検出方法。
- 請求項1または2記載の抗体またはフラグメントを含む、腫瘍細胞イメージング剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010505602A JP5483023B2 (ja) | 2008-03-27 | 2009-03-19 | がん細胞運動およびがん細胞浸潤抑制剤 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008083588 | 2008-03-27 | ||
| JP2008083588 | 2008-03-27 | ||
| JP2010505602A JP5483023B2 (ja) | 2008-03-27 | 2009-03-19 | がん細胞運動およびがん細胞浸潤抑制剤 |
| PCT/JP2009/055479 WO2009119455A1 (ja) | 2008-03-27 | 2009-03-19 | がん細胞運動およびがん細胞浸潤抑制剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2009119455A1 JPWO2009119455A1 (ja) | 2011-07-21 |
| JP5483023B2 true JP5483023B2 (ja) | 2014-05-07 |
Family
ID=41113650
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010505602A Active JP5483023B2 (ja) | 2008-03-27 | 2009-03-19 | がん細胞運動およびがん細胞浸潤抑制剤 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8674079B2 (ja) |
| EP (1) | EP2267125B1 (ja) |
| JP (1) | JP5483023B2 (ja) |
| WO (1) | WO2009119455A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012523438A (ja) * | 2009-04-10 | 2012-10-04 | タフツ メディカル センター インコーポレイテッド | メタロプロテイナーゼ−1(mmp−1)によるpar−1活性化 |
| WO2011102483A1 (ja) * | 2010-02-19 | 2011-08-25 | 独立行政法人理化学研究所 | ヒトTGF-βのLAPに結合する抗体 |
| CN103168242B (zh) * | 2010-09-02 | 2016-02-03 | 国立大学法人东北大学 | 癌症发病或癌症发病风险的判定方法 |
| WO2012090207A2 (en) * | 2010-12-30 | 2012-07-05 | Hadasit Medical Research Services & Development Limited | Par1 and par2 c-tail peptides and peptide mimetics |
| TWI549997B (zh) | 2014-10-14 | 2016-09-21 | 財團法人工業技術研究院 | 木質素生質環氧樹脂的形成方法與木質素生質環氧樹脂組合物 |
| SG10201906471PA (en) | 2015-01-14 | 2019-09-27 | Brigham & Womens Hospital Inc | Treatment of cancer with anti-lap monoclonal antibodies |
| WO2019075090A1 (en) | 2017-10-10 | 2019-04-18 | Tilos Therapeutics, Inc. | ANTI-LAP ANTIBODIES AND USES THEREOF |
| WO2020076969A2 (en) | 2018-10-10 | 2020-04-16 | Tilos Therapeutics, Inc. | Anti-lap antibody variants and uses thereof |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5776700A (en) | 1996-09-05 | 1998-07-07 | Trustees Of The University Of Pennsylvania | Thrombine receptor activation assay for use in identifying thrombin receptor antagonists |
| IL125698A (en) | 1998-08-07 | 2007-03-08 | Hadasit Med Res Service | Use of molecules associated with protease activated receptors for the preparation of pharmaceutical compositions and pharmaceutical compositions comprising them |
| JP4469467B2 (ja) | 2000-06-29 | 2010-05-26 | 帝人株式会社 | 細胞増殖抑制剤 |
| US7074765B2 (en) * | 2003-05-01 | 2006-07-11 | The Regents Of The University Of Michigan | Synthetic peptide analogs of Arg-Pro-Pro-Gly-Phe as selective inhibitors of thrombin and thrombin activation of protease activated receptors 1 and 4 |
| US7888483B2 (en) | 2006-07-18 | 2011-02-15 | Irm Llc | Antagonists of protease activated receptor-1 (PAR1) |
| JP4861115B2 (ja) | 2006-09-28 | 2012-01-25 | サントリーホールディングス株式会社 | ラベル、ラベルの製造方法、ラベルの線剥離強度の経時安定化方法、及び容器 |
-
2009
- 2009-03-19 JP JP2010505602A patent/JP5483023B2/ja active Active
- 2009-03-19 WO PCT/JP2009/055479 patent/WO2009119455A1/ja active Application Filing
- 2009-03-19 US US12/934,133 patent/US8674079B2/en active Active
- 2009-03-19 EP EP09726307.3A patent/EP2267125B1/en not_active Not-in-force
Non-Patent Citations (4)
| Title |
|---|
| JPN6009016591; Cell, 2005, Vol.120, No.3, p.303-313 * |
| JPN6009016592; The Journal of biological chemistry, 1994, Vol.269, No.4, p.2943-2952 * |
| JPN6013024397; Cancer research. 1990, Vol.50, No.15, p.4485-4496 * |
| JPN6013040635; Biological chemistry. 2006, Vol.387, No.6, p.817-824 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2267125B1 (en) | 2015-09-02 |
| EP2267125A1 (en) | 2010-12-29 |
| US8674079B2 (en) | 2014-03-18 |
| EP2267125A4 (en) | 2011-09-07 |
| WO2009119455A1 (ja) | 2009-10-01 |
| JPWO2009119455A1 (ja) | 2011-07-21 |
| US20110070163A1 (en) | 2011-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5483023B2 (ja) | がん細胞運動およびがん細胞浸潤抑制剤 | |
| EP2723377B1 (en) | Anti-axl antibodies and uses thereof | |
| US9249228B2 (en) | Anti-Axl antibodies and uses thereof | |
| CN101573382B (zh) | 针对人抗苗勒激素ⅱ型受体(amhr-ⅱ)的单克隆抗体 | |
| EP3419674A1 (en) | Targeting immunotherapy for amyloidosis | |
| CN105037551A (zh) | 治疗试剂 | |
| CN103890010A (zh) | 抗-人-her3抗体及其用途 | |
| US20160185856A1 (en) | Anti-Claudin 1 Antibodies and Uses Thereof | |
| CN107849138B (zh) | 抗Aggrus单克隆抗体及其应用 | |
| EP1956032B1 (en) | Monoclonal antibody directed against cd166 and method for production thereof | |
| US20220389113A1 (en) | Binding proteins to cub domain-containing protein (cdcp1) | |
| Harrington et al. | Anti-CDCP1 immuno-conjugates for detection and inhibition of ovarian cancer | |
| CN111201244A (zh) | 特异性结合到水通道蛋白3(aqp3)的细胞外域的抗aqp3单克隆抗体及其用途 | |
| US8586042B2 (en) | Hybridomas producing monoclonal anti-mortalin peptide antibodies | |
| CN101864398A (zh) | 一种抗促性腺激素释放激素受体的单克隆抗体与应用 | |
| US20220227882A1 (en) | Anti-adam8 antibodies and uses of the same | |
| WO2020158959A1 (ja) | 抗mc16抗体 | |
| WO2022056329A1 (en) | Snx9 subfamily-targeting antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120119 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120119 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130528 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130723 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130820 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131015 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20131105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131118 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20140106 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140121 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140204 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5483023 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |