JP5167149B2 - 白血病の診断および治療ターゲット - Google Patents
白血病の診断および治療ターゲット Download PDFInfo
- Publication number
- JP5167149B2 JP5167149B2 JP2008551261A JP2008551261A JP5167149B2 JP 5167149 B2 JP5167149 B2 JP 5167149B2 JP 2008551261 A JP2008551261 A JP 2008551261A JP 2008551261 A JP2008551261 A JP 2008551261A JP 5167149 B2 JP5167149 B2 JP 5167149B2
- Authority
- JP
- Japan
- Prior art keywords
- calm
- hoxa5
- fusion protein
- dot1l
- polypeptide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5011—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing antineoplastic activity
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1135—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against oncogenes or tumor suppressor genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6897—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids involving reporter genes operably linked to promoters
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/136—Screening for pharmacological compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/154—Methylation markers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/14—Heterocyclic carbon compound [i.e., O, S, N, Se, Te, as only ring hetero atom]
- Y10T436/142222—Hetero-O [e.g., ascorbic acid, etc.]
- Y10T436/143333—Saccharide [e.g., DNA, etc.]
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Analytical Chemistry (AREA)
- Biomedical Technology (AREA)
- Microbiology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- General Engineering & Computer Science (AREA)
- Pathology (AREA)
- Biophysics (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Hospice & Palliative Care (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Toxicology (AREA)
- Medicinal Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
本願は、2006年1月20日に出願された米国仮特許出願第60/760,709号の利益を主張し、その開示は引用することにより本明細書の一部をなすものとする。
本発明は、米国国立衛生研究所によって交付された助成金番号GM68804の下に、連邦政府の支援を受けてなされた。米国政府は本発明に一定の権利を有する。
本発明は、ヒストンメチル化に基づく、白血病治療用の候補化合物を識別する方法および診断方法に関する。
DOT1LポリペプチドがCALM−AF10融合タンパク質に結合するのに十分な条件下で、試験化合物の存在下で、DOT1LポリペプチドをCALM−AF10融合タンパク質と接触させるステップと、DOT1LポリペプチドとCALM−AF10融合タンパク質の間の相互作用を検出するステップとを含み、該試験化合物の非存在下での相互作用のレベルと比較した、該試験化合物存在下での、DOT1LポリペプチドとCALM−AF10融合タンパク質の間の相互作用の減少が、前記試験化合物が白血病の予防および/または治療のための候補化合物であることを示す方法を提供する。
試験化合物がCALM−AF10融合タンパク質に結合するのに十分な条件下で、CALM−AF10融合タンパク質を試験化合物と接触させるステップと、試験化合物とCALM−AF10融合タンパク質の間の結合を検出するステップとを含み、CALM−AF10融合タンパク質への試験化合物の結合は、前記試験化合物が白血病の予防および/または治療のための候補化合物であることを示す方法も提供する。
・CALMに結合しかつ/またはCAMLの一つ以上の生物学的活性、例えば、限定するわけではないが、白血病誘発活性および/または他の任意の興味ある生物学的活性を調整する(例えば増加または減少させる)化合物、
・AF10に結合しかつ/またはAF10の一つ以上の生物学的活性、例えば、限定するわけではないが、白血病誘発活性および/または他の任意の興味ある生物学的活性を調整する(例えば増加または減少させる)化合物、
・CALM−AF10に結合しかつ/またはCALM−AF10の一つ以上の生物学的活性、例えば、限定するわけではないが、白血病誘発活性、HoxA5プロモーター活性のアップレギュレーション(例えば、ネイティブであるか異種であるかを問わず、HoxA5プロモーターと作動可能に関連する核酸の転写の増加)および/または他の任意の興味ある生物学的活性を調整する(例えば増加または減少させる)化合物、
・DOT1LのAF10またはCALM−AF10との相互作用を調整する(例えば増加または減少させる)化合物、
・CALM−AF10の核局在化を調整する(例えば増加または減少させる)化合物;
・DOT1LまたはDOT1L/CALM−AF10によるHoxA5遺伝子のH3−K79メチル化を調整する(例えば増加または減少させる)化合物、
・HoxA5遺伝子におけるDOT1L/CALM−AF10、CALM−AF10またはCALM結合を調整する(例えば増加または減少させる)化合物、および/または、
・DOT1L/CALM−AF10、CALM−AF10またはCALMによるHoxA5プロモーター活性(例えば、ネイティブであるか異種であるかを問わず、HoxA5プロモーターと作動可能に関連する核酸の転写)の調節を調整する(例えば増加または減少させる)化合物、
・HoxA5プロモーター活性に結合しかつ/またはHoxA5プロモーター活性をダウンレギュレートする(例えばHoxA5遺伝子発現またはレポーター遺伝子などの導入遺伝子と作動可能に関連するHoxA5プロモーターを含むキメラコンストラクトを減少させる)化合物。
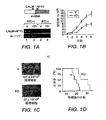
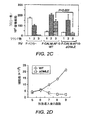
U937細胞におけるCALM−AF10ノックダウンおよび移植.CALMとAF10の接合部をターゲットとする21bp−shRNA(5’−ATC AGG AGC ACA GAG CTG TGA−3’;配列番号3)をコードするDNAを、H1 RNAプロモーターと共に、pMSCV−puroにサブクローニングした。形質導入細胞をピューロマイシン(0.5μg/ml)によって選択し、限界希釈法によってクローニングした。ノックダウン効率をRT−PCRによって評価した。5〜10週齢のNOD/SCIDマウスに照射(300rad)した。6時間後に、CALM−AF10ノックダウン(KD)U937細胞およびベクター形質導入(V)U937細胞を、眼窩内注射した(1×107細胞/マウス、各群n=6)。マウスを監視し、組織学的検査およびFACS解析のために、末期に屠殺した。KD群のマウス数匹については、対照実験用に、末期に至る前に屠殺した。
CALM−AF10融合タンパク質は、白血病性形質転換を媒介するのに必要である。本発明者らは最近、ヒストンH3−K79メチルトランスフェラーゼであるhDOT1L(Feng et al.,(2002)Curr.Biol.12:1052−1058)がMLL−AF10による白血病誘発に重要な役割を果たすことを証明した(Okada et al.,(2005)Cell 121:167−78)。本発明者らは、MLL−AF10によるHoxa9遺伝子へのhDOT1LのミスターゲティングがH3−K79メチル化およびHoxa9アップレギュレーションをもたらし、それが白血病性形質転換の一因になることを示した(Okada et al.,(2005)Cell 121:167−78)。さらに本発明者らは、MLL−AF10による白血病性形質転換に必要なAF10のOM−LZモチーフが、hDOT1LとMLL−AF10の相互作用に関与することも証明した(DiMartino et al.,(2002)Blood 99,3780−5)。OM−LZ領域がCALM−AF10融合タンパク質に保たれているという事実から、hDOT1LはCALM−AF10による白血病にも重要な役割を果たしうる可能性が考えられる。CALM−AF10による白血病におけるhDOT1Lの潜在的役割を検討するために、本発明者らは、まず、CALM−AF10融合タンパク質と白血病の間の因果関係を確証しようと試みた。
Claims (19)
- 白血病の予防および/または治療のための候補化合物を識別する方法であって、
DOT1LポリペプチドがCALM−AF10融合タンパク質に結合するのに十分な条件下で、試験化合物の存在下で、DOT1LポリペプチドをCALM−AF10融合タンパク質と接触させるステップと、
DOT1LポリペプチドとCALM−AF10融合タンパク質の間の相互作用を検出するステップと
を含み、
前記試験化合物の非存在下での相互作用のレベルと比較した、前記試験化合物存在下での、DOT1LポリペプチドとCALM−AF10融合タンパク質の間の相互作用の減少が、前記試験化合物が白血病の予防および/または治療のための候補化合物であることを示す、方法。 - DOT1LポリペプチドのCALM−AF10融合タンパク質との相互作用が、
(i)DOT1LポリペプチドとCALM−AF10の間の結合を決定すること、
(ii)CALM−AF10の核局在化を決定すること、
(iii)HoxA5のヒストンH3リジン79(H3−K79)メチル化を決定すること、もしくは前記HoxA5プロモーターの前記H3−K79メチル化が決定されること、または
(iv)HoxA5プロモーター活性を決定すること
によって評価される、請求項1に記載の方法。 - 白血病の予防および/または治療のための候補化合物を識別する方法であって、
試験化合物がCALM−AF10融合タンパク質に結合するのに十分な条件下で、CALM−AF10融合タンパク質を前記試験化合物と接触させるステップと、
前記試験化合物とCALM−AF10融合タンパク質の間の結合を検出するステップとを含み、
CALM−AF10融合タンパク質への前記試験化合物の結合が、前記試験化合物が白血病の予防および/または治療のための候補化合物であることを示す方法。 - 白血病の予防および/または治療のための候補化合物を識別する方法であって、
(i)CALM−AF10融合タンパク質がHoxA5プロモーターに結合するのに十分な条件下、または(ii)DOT1LポリペプチドとCALM−AF10融合タンパク質が複合体を形成し、前記複合体がHoxA5プロモーターに結合するのに十分な条件下で、試験化合物の存在下で、HoxA5プロモーター領域を含む核酸を(i)CALM−AF10融合タンパク質、または(ii)DOT1LポリペプチドおよびCALM−AF10融合タンパク質と接触させるステップと、
(i)CALM−AF10融合タンパク質の前記HoxA5プロモーターとの相互作用、または(ii)前記DOT1L/CALM−AF10複合体の前記HoxA5プロモーターとの相互作用を検出するステップと
を含み、
前記試験化合物の非存在下での相互作用のレベルと比較した、前記試験化合物存在下での、(i)CALM−AF10融合タンパク質とHoxA5プロモーターとの相互作用、または(ii)前記DOT1L/CALM−AF10複合体の前記HoxA5プロモーターとの相互作用の減少が、前記試験化合物が白血病の予防および/または治療のための候補化合物であることを示す方法。 - 前記核酸が前記HoxA5遺伝子のエクソン1をさらに含む、請求項4に記載の方法。
- 前記核酸が前記HoxA5遺伝子のエクソン1とエクソン2の間のイントロンをさらに含む、請求項4または5に記載の方法。
- 前記核酸が前記HoxA5遺伝子のエクソン2をさらに含む、請求項4〜6のいずれかに記載の方法。
- 前記DOT1L/CALM−AF10複合体の前記HoxA5プロモーターとの相互作用が、前記HoxA5プロモーターへの前記DOT1L/CALM−AF10複合体の結合を決定することによって評価される、請求項4に記載の方法。
- DOT1L/CALM−AF10複合体の前記HoxA5プロモーターとの相互作用が、前記HoxA5プロモーターのヒストンH3リジン79(H3−K79)メチル化を決定することによって評価される、請求項4に記載の方法。
- 前記DOT1L/CALM−AF10複合体の前記HoxA5プロモーターとの相互作用が、前記HoxA5プロモーター活性を決定することによって評価される、請求項4に記載の方法。
- 前記HoxA5プロモーターがレポーター分子をコードするヌクレオチド配列と作動可能に関連し、HoxA5プロモーター活性が前記レポーター分子を検出することによって決定される、請求項2または4に記載の方法。
- 前記レポーター分子がポリペプチドである、請求項11に記載の方法。
- 前記ポリペプチドが酵素である、請求項12に記載の方法。
- 無細胞アッセイとして行われる、請求項1〜4のいずれかに記載の方法。
- 細胞に基づくアッセイとして行われる、請求項1〜4のいずれかに記載の方法。
- 前記DOT1Lポリペプチドおよび/またはCALM−AF10融合タンパク質が核酸から発現される、請求項1〜4のいずれかに記載の方法。
- 前記白血病がT細胞急性リンパ性白血病(T−ALL)または急性骨髄性白血病サブタイプM0/1(AML−M0/1)である、請求項1〜4のいずれかに記載の方法。
- 前記DOT1Lポリペプチドが哺乳類DOT1Lポリペプチドであり、前記CALM−AF融合タンパク質が哺乳類CALM−AF10融合タンパク質である、請求項1〜4のいずれかに記載の方法。
- 前記DOT1LポリペプチドがヒトDOT1Lポリペプチドであり、前記CALM−AF10融合タンパク質がヒトCALM−AF10融合タンパク質である、請求項18に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US76070906P | 2006-01-20 | 2006-01-20 | |
| US60/760,709 | 2006-01-20 | ||
| PCT/US2006/046612 WO2007087015A1 (en) | 2006-01-20 | 2006-12-06 | Diagnostic and therapeutic targets for leukemia |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2009524051A JP2009524051A (ja) | 2009-06-25 |
| JP2009524051A5 JP2009524051A5 (ja) | 2010-01-28 |
| JP5167149B2 true JP5167149B2 (ja) | 2013-03-21 |
Family
ID=38309541
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008551261A Expired - Fee Related JP5167149B2 (ja) | 2006-01-20 | 2006-12-06 | 白血病の診断および治療ターゲット |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US8524467B2 (ja) |
| EP (2) | EP1974055A4 (ja) |
| JP (1) | JP5167149B2 (ja) |
| AU (1) | AU2006336552B2 (ja) |
| CA (1) | CA2623271A1 (ja) |
| WO (1) | WO2007087015A1 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130102477A1 (en) | 2010-06-23 | 2013-04-25 | Ryan D. Morin | Biomarkers for non-hodgkin lymphomas and uses thereof |
| PL2614369T3 (pl) | 2010-09-10 | 2016-08-31 | Epizyme Inc | Sposób określania przydatności inhibitorów ludzkiego ezh2 w leczeniu |
| US9175331B2 (en) | 2010-09-10 | 2015-11-03 | Epizyme, Inc. | Inhibitors of human EZH2, and methods of use thereof |
| JO3438B1 (ar) | 2011-04-13 | 2019-10-20 | Epizyme Inc | مركبات بنزين مستبدلة بأريل أو أريل غير متجانس |
| TWI598336B (zh) | 2011-04-13 | 2017-09-11 | 雅酶股份有限公司 | 經取代之苯化合物 |
| NZ700761A (en) | 2012-04-13 | 2016-09-30 | Epizyme Inc | Salt form of a human histone methyltransferase ezh2 inhibitor |
| US10092572B2 (en) | 2012-10-15 | 2018-10-09 | Epizyme, Inc. | Substituted benzene compounds |
| AU2014295980B2 (en) | 2013-08-02 | 2020-08-27 | Memorial Sloan-Kettering Cancer Center | Methods for the detection and treatment of leukemias that are responsive to DOT1L inhibition |
| ES2960953T3 (es) | 2013-10-16 | 2024-03-07 | Epizyme Inc | Forma de sal de clorhidrato para la inhibición de EZH2 |
| JP7428717B2 (ja) * | 2019-01-15 | 2024-02-06 | ピーティーシー セラピューティクス, インコーポレイテッド | 急性骨髄性白血病の治療方法 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5420328A (en) | 1992-09-11 | 1995-05-30 | Affymax Technologies, N.V. | Methods for the synthesis of phosphonate esters |
| US5288514A (en) | 1992-09-14 | 1994-02-22 | The Regents Of The University Of California | Solid phase and combinatorial synthesis of benzodiazepine compounds on a solid support |
| US5525735A (en) | 1994-06-22 | 1996-06-11 | Affymax Technologies Nv | Methods for synthesizing diverse collections of pyrrolidine compounds |
| US5525734A (en) | 1994-06-22 | 1996-06-11 | Affymax Technologies N.V. | Methods for synthesizing diverse collections of pyrrolidine compounds |
| US5817751A (en) | 1994-06-23 | 1998-10-06 | Affymax Technologies N.V. | Method for synthesis of diketopiperazine and diketomorpholine derivatives |
| AU7829398A (en) | 1997-06-09 | 1998-12-30 | University Of Southern California | A cancer diagnostic method based upon dna methylation differences |
| US6555329B2 (en) | 2000-06-09 | 2003-04-29 | Boehringer Ingelheim International Gmbh | Method for identifying compounds altering higher-order chromatin-dependent chromosome stability |
| WO2003016497A2 (en) | 2001-08-17 | 2003-02-27 | Incyte Genomics, Inc. | Molecules for disease detection and treatment |
| US7485414B2 (en) | 2002-08-30 | 2009-02-03 | Rigel Pharmaceuticals, Inc. | Modulators of angiogenesis |
| US7442685B2 (en) * | 2003-06-13 | 2008-10-28 | The University Of North Carolina At Chapel Hill | DOT1 histone methyltransferases as a target for identifying therapeutic agents for leukemia |
| EP1791973B1 (en) | 2004-08-31 | 2009-10-21 | University Of North Carolina At Chapel Hill | Dot1 histone methyltransferases as a target for identifying therapeutic agents for leukemia |
-
2006
- 2006-12-06 EP EP06839119A patent/EP1974055A4/en not_active Withdrawn
- 2006-12-06 JP JP2008551261A patent/JP5167149B2/ja not_active Expired - Fee Related
- 2006-12-06 EP EP13177872.2A patent/EP2730661A1/en not_active Withdrawn
- 2006-12-06 AU AU2006336552A patent/AU2006336552B2/en not_active Ceased
- 2006-12-06 US US12/161,482 patent/US8524467B2/en not_active Expired - Fee Related
- 2006-12-06 CA CA002623271A patent/CA2623271A1/en not_active Abandoned
- 2006-12-06 WO PCT/US2006/046612 patent/WO2007087015A1/en active Application Filing
-
2013
- 2013-07-29 US US13/953,190 patent/US20140044740A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| EP2730661A1 (en) | 2014-05-14 |
| AU2006336552B2 (en) | 2012-12-20 |
| WO2007087015A1 (en) | 2007-08-02 |
| US8524467B2 (en) | 2013-09-03 |
| JP2009524051A (ja) | 2009-06-25 |
| AU2006336552A1 (en) | 2007-08-02 |
| EP1974055A1 (en) | 2008-10-01 |
| US20140044740A1 (en) | 2014-02-13 |
| CA2623271A1 (en) | 2007-08-02 |
| EP1974055A4 (en) | 2010-01-27 |
| US20090061443A1 (en) | 2009-03-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5167149B2 (ja) | 白血病の診断および治療ターゲット | |
| US9534259B2 (en) | DOT1 histone methyltransferases as a target for identifying therapeutic agents for leukemia | |
| Sessa et al. | SETD5 regulates chromatin methylation state and preserves global transcriptional fidelity during brain development and neuronal wiring | |
| Zhao et al. | Identification of transcription factor KLF8 as a downstream target of focal adhesion kinase in its regulation of cyclin D1 and cell cycle progression | |
| Vogl et al. | Neddylation inhibition impairs spine development, destabilizes synapses and deteriorates cognition | |
| EP1791973B1 (en) | Dot1 histone methyltransferases as a target for identifying therapeutic agents for leukemia | |
| JP2010531662A (ja) | P53のモジュレータ及び癌の標的であるtrim24(tif−1a) | |
| Munnur et al. | NR4A nuclear receptors target poly-ADP-ribosylated DNA-PKcs protein to promote DNA repair | |
| JP2002516577A (ja) | 哺乳動物chk1エフェクター細胞周期チェックポイントタンパク質キナーゼ物質及び方法 | |
| JP2003532428A (ja) | 抗癌剤をスクリーニングするための酵素的アッセイ | |
| US20040180349A1 (en) | Diagnosis and treatment of cancer involving the notch pathway | |
| JP2007282628A (ja) | 抗癌剤のスクリーニング方法 | |
| KR20140046991A (ko) | 메틸 데그론 펩타이드 및 이를 이용한 단백질 수명 조절 방법 | |
| JP2003511022A (ja) | 単離されたディシュベルド(Dishevelled)関連キナーゼ、該キナーゼをコードするポリヌクレオチド、およびそれらの用途 | |
| Cho et al. | S-nitrosylation-mediated unfolded protein response maintains hematopoietic progenitors | |
| Sarkar | Bookending the Germ Cell to Maternal Transition: Dynamics of Gene Regulation in Drosophila Oogenesis | |
| JP2003533226A (ja) | 神経細胞のセリンスレオニンプロテインキナーゼ | |
| US20040235001A1 (en) | Regulatory poly(A) polymerase and uses thereof | |
| WO2023230564A2 (en) | Palmitoylation of the alternative amino terminus of the btk-c isoform controls subcellular distribution and signaling | |
| EP2250195B1 (en) | Sulfatase enzymes | |
| Kilpatrick | Elucidating the role of GODZ-mediated palmitoylation in controlling GABAergic inhibition | |
| WO2004031731A2 (en) | Methods for controlling proliferation of cells | |
| Peng | Regulation and mechanism of NFBD1 and 53BP1 in mediating DNA damage responses | |
| de Almeida Dantas | The roles of centrins/caltractins at the centrosome and in genome maintenance | |
| Stairs | Discovery, characterization and functional analysis of the serine/threonine kinase Krct |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091201 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091201 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110608 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110708 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111007 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111017 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111108 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111115 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111208 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111215 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111215 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120424 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120724 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120731 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120824 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120831 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120924 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20121001 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121023 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121221 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151228 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |