JP4976851B2 - 脂質レベルを哺乳動物において低下させる方法 - Google Patents
脂質レベルを哺乳動物において低下させる方法 Download PDFInfo
- Publication number
- JP4976851B2 JP4976851B2 JP2006538169A JP2006538169A JP4976851B2 JP 4976851 B2 JP4976851 B2 JP 4976851B2 JP 2006538169 A JP2006538169 A JP 2006538169A JP 2006538169 A JP2006538169 A JP 2006538169A JP 4976851 B2 JP4976851 B2 JP 4976851B2
- Authority
- JP
- Japan
- Prior art keywords
- diabetic
- age
- rats
- acid
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 150000002632 lipids Chemical class 0.000 title claims description 39
- 241000124008 Mammalia Species 0.000 title claims description 6
- 238000000034 method Methods 0.000 title description 26
- 206010012601 diabetes mellitus Diseases 0.000 claims description 250
- 150000001875 compounds Chemical class 0.000 claims description 106
- KJQWSJOVJCOZBD-UHFFFAOYSA-N 2-quinolin-8-yloxypropanoic acid Chemical compound C1=CN=C2C(OC(C)C(O)=O)=CC=CC2=C1 KJQWSJOVJCOZBD-UHFFFAOYSA-N 0.000 claims description 45
- WJDMCXSGUCNRPZ-UHFFFAOYSA-N 2-[4-[[4-[[4-[[4-(2-carboxypropan-2-yloxy)phenyl]carbamoylamino]-3-chlorophenyl]methyl]-2-chlorophenyl]carbamoylamino]phenoxy]-2-methylpropanoic acid Chemical compound C1=CC(OC(C)(C)C(O)=O)=CC=C1NC(=O)NC(C(=C1)Cl)=CC=C1CC(C=C1Cl)=CC=C1NC(=O)NC1=CC=C(OC(C)(C)C(O)=O)C=C1 WJDMCXSGUCNRPZ-UHFFFAOYSA-N 0.000 claims description 38
- -1 8-quinolinoxy Chemical group 0.000 claims description 20
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 claims description 16
- KGRVJHAUYBGFFP-UHFFFAOYSA-N 2,2'-Methylenebis(4-methyl-6-tert-butylphenol) Chemical compound CC(C)(C)C1=CC(C)=CC(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=C1O KGRVJHAUYBGFFP-UHFFFAOYSA-N 0.000 claims description 9
- ILPUOPPYSQEBNJ-UHFFFAOYSA-N 2-methyl-2-phenoxypropanoic acid Chemical compound OC(=O)C(C)(C)OC1=CC=CC=C1 ILPUOPPYSQEBNJ-UHFFFAOYSA-N 0.000 claims description 9
- 235000019260 propionic acid Nutrition 0.000 claims description 8
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 claims description 8
- 150000003839 salts Chemical class 0.000 claims description 5
- 239000008194 pharmaceutical composition Substances 0.000 claims 10
- JVXXKQIRGQDWOJ-UHFFFAOYSA-N naphthalene-2-carboxamide Chemical compound C1=CC=CC2=CC(C(=O)N)=CC=C21 JVXXKQIRGQDWOJ-UHFFFAOYSA-N 0.000 claims 4
- 241000700159 Rattus Species 0.000 description 130
- 241001465754 Metazoa Species 0.000 description 60
- 210000003734 kidney Anatomy 0.000 description 59
- NHZMQXZHNVQTQA-UHFFFAOYSA-N pyridoxamine Chemical compound CC1=NC=C(CO)C(CN)=C1O NHZMQXZHNVQTQA-UHFFFAOYSA-N 0.000 description 52
- 238000011282 treatment Methods 0.000 description 50
- 230000000694 effects Effects 0.000 description 45
- 238000004519 manufacturing process Methods 0.000 description 42
- 238000007254 oxidation reaction Methods 0.000 description 41
- 239000010949 copper Substances 0.000 description 39
- 102000008186 Collagen Human genes 0.000 description 38
- 108010035532 Collagen Proteins 0.000 description 38
- 229920001436 collagen Polymers 0.000 description 38
- 230000003647 oxidation Effects 0.000 description 38
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 36
- 208000001930 Autoimmune limbic encephalitis Diseases 0.000 description 35
- 235000015107 ale Nutrition 0.000 description 34
- 238000003877 atomic layer epitaxy Methods 0.000 description 34
- UCTWMZQNUQWSLP-VIFPVBQESA-N (R)-adrenaline Chemical compound CNC[C@H](O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-VIFPVBQESA-N 0.000 description 33
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 26
- 229910052802 copper Inorganic materials 0.000 description 26
- 235000008151 pyridoxamine Nutrition 0.000 description 26
- 239000011699 pyridoxamine Substances 0.000 description 26
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 25
- 239000008103 glucose Substances 0.000 description 25
- 230000003859 lipid peroxidation Effects 0.000 description 24
- 102000007330 LDL Lipoproteins Human genes 0.000 description 22
- 108010007622 LDL Lipoproteins Proteins 0.000 description 22
- DDRJAANPRJIHGJ-UHFFFAOYSA-N creatinine Chemical compound CN1CC(=O)NC1=N DDRJAANPRJIHGJ-UHFFFAOYSA-N 0.000 description 22
- XCYPSOHOIAZISD-MLWJPKLSSA-N N(6)-(1-carboxyethyl)-L-lysine Chemical compound OC(=O)C(C)NCCCC[C@H](N)C(O)=O XCYPSOHOIAZISD-MLWJPKLSSA-N 0.000 description 20
- 239000003112 inhibitor Substances 0.000 description 19
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 18
- 108090000623 proteins and genes Proteins 0.000 description 18
- 230000002829 reductive effect Effects 0.000 description 18
- HAMNKKUPIHEESI-UHFFFAOYSA-N aminoguanidine Chemical compound NNC(N)=N HAMNKKUPIHEESI-UHFFFAOYSA-N 0.000 description 16
- 239000000047 product Substances 0.000 description 16
- 235000018102 proteins Nutrition 0.000 description 16
- 102000004169 proteins and genes Human genes 0.000 description 16
- 210000002966 serum Anatomy 0.000 description 16
- 238000010186 staining Methods 0.000 description 16
- GIANIJCPTPUNBA-QMMMGPOBSA-N (2s)-3-(4-hydroxyphenyl)-2-nitramidopropanoic acid Chemical compound [O-][N+](=O)N[C@H](C(=O)O)CC1=CC=C(O)C=C1 GIANIJCPTPUNBA-QMMMGPOBSA-N 0.000 description 14
- 230000037396 body weight Effects 0.000 description 14
- 201000001421 hyperglycemia Diseases 0.000 description 14
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 13
- 210000004369 blood Anatomy 0.000 description 13
- 239000008280 blood Substances 0.000 description 13
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- ZSJLQEPLLKMAKR-UHFFFAOYSA-N Streptozotocin Natural products O=NN(C)C(=O)NC1C(O)OC(CO)C(O)C1O ZSJLQEPLLKMAKR-UHFFFAOYSA-N 0.000 description 12
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 12
- 150000003254 radicals Chemical class 0.000 description 12
- 239000000523 sample Substances 0.000 description 12
- 229960001052 streptozocin Drugs 0.000 description 12
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 11
- WSMYVTOQOOLQHP-UHFFFAOYSA-N Malondialdehyde Chemical compound O=CCC=O WSMYVTOQOOLQHP-UHFFFAOYSA-N 0.000 description 11
- 235000012000 cholesterol Nutrition 0.000 description 11
- 229940109239 creatinine Drugs 0.000 description 11
- 201000010099 disease Diseases 0.000 description 11
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 11
- 235000020778 linoleic acid Nutrition 0.000 description 11
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 11
- 229940118019 malondialdehyde Drugs 0.000 description 11
- 230000036542 oxidative stress Effects 0.000 description 11
- 108010088751 Albumins Proteins 0.000 description 10
- 102000009027 Albumins Human genes 0.000 description 10
- 239000004472 Lysine Substances 0.000 description 10
- OUUQCZGPVNCOIJ-UHFFFAOYSA-M Superoxide Chemical compound [O-][O] OUUQCZGPVNCOIJ-UHFFFAOYSA-M 0.000 description 10
- 239000000872 buffer Substances 0.000 description 10
- 238000004132 cross linking Methods 0.000 description 10
- 238000000338 in vitro Methods 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 9
- 239000002253 acid Substances 0.000 description 9
- 235000010323 ascorbic acid Nutrition 0.000 description 9
- 239000011668 ascorbic acid Substances 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 9
- 238000001727 in vivo Methods 0.000 description 9
- 230000005764 inhibitory process Effects 0.000 description 9
- 239000006228 supernatant Substances 0.000 description 9
- 210000002435 tendon Anatomy 0.000 description 9
- 150000003626 triacylglycerols Chemical class 0.000 description 9
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 9
- 210000005239 tubule Anatomy 0.000 description 9
- 201000001320 Atherosclerosis Diseases 0.000 description 8
- 208000002249 Diabetes Complications Diseases 0.000 description 8
- 229960005070 ascorbic acid Drugs 0.000 description 8
- 206010061989 glomerulosclerosis Diseases 0.000 description 8
- 230000002401 inhibitory effect Effects 0.000 description 8
- 208000017169 kidney disease Diseases 0.000 description 8
- 230000004048 modification Effects 0.000 description 8
- 238000012986 modification Methods 0.000 description 8
- 208000007342 Diabetic Nephropathies Diseases 0.000 description 7
- 206010012655 Diabetic complications Diseases 0.000 description 7
- 208000031226 Hyperlipidaemia Diseases 0.000 description 7
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 7
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 7
- 239000000524 Thiobarbituric Acid Reactive Substance Substances 0.000 description 7
- 238000004458 analytical method Methods 0.000 description 7
- 210000004027 cell Anatomy 0.000 description 7
- 230000007423 decrease Effects 0.000 description 7
- 238000000151 deposition Methods 0.000 description 7
- 238000011161 development Methods 0.000 description 7
- 230000018109 developmental process Effects 0.000 description 7
- 208000033679 diabetic kidney disease Diseases 0.000 description 7
- 238000011534 incubation Methods 0.000 description 7
- 235000018977 lysine Nutrition 0.000 description 7
- 230000004060 metabolic process Effects 0.000 description 7
- 235000000346 sugar Nutrition 0.000 description 7
- 229910052723 transition metal Inorganic materials 0.000 description 7
- 150000003624 transition metals Chemical class 0.000 description 7
- 230000002485 urinary effect Effects 0.000 description 7
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 6
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 6
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 6
- 208000034189 Sclerosis Diseases 0.000 description 6
- 238000009825 accumulation Methods 0.000 description 6
- 230000003078 antioxidant effect Effects 0.000 description 6
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 6
- 230000036252 glycation Effects 0.000 description 6
- TUJKJAMUKRIRHC-UHFFFAOYSA-N hydroxyl Chemical compound [OH] TUJKJAMUKRIRHC-UHFFFAOYSA-N 0.000 description 6
- 238000002347 injection Methods 0.000 description 6
- 239000007924 injection Substances 0.000 description 6
- 239000000543 intermediate Substances 0.000 description 6
- 230000001404 mediated effect Effects 0.000 description 6
- 230000037361 pathway Effects 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 239000012086 standard solution Substances 0.000 description 6
- 239000011550 stock solution Substances 0.000 description 6
- 102000057297 Pepsin A Human genes 0.000 description 5
- 108090000284 Pepsin A Proteins 0.000 description 5
- 239000003963 antioxidant agent Substances 0.000 description 5
- 210000002469 basement membrane Anatomy 0.000 description 5
- 238000007385 chemical modification Methods 0.000 description 5
- 239000007795 chemical reaction product Substances 0.000 description 5
- 230000001054 cortical effect Effects 0.000 description 5
- 230000001419 dependent effect Effects 0.000 description 5
- 230000008021 deposition Effects 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 230000000678 effect on lipid Effects 0.000 description 5
- 230000029142 excretion Effects 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 238000011532 immunohistochemical staining Methods 0.000 description 5
- 230000008595 infiltration Effects 0.000 description 5
- 238000001764 infiltration Methods 0.000 description 5
- 230000003907 kidney function Effects 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 210000000440 neutrophil Anatomy 0.000 description 5
- 230000001590 oxidative effect Effects 0.000 description 5
- 229940111202 pepsin Drugs 0.000 description 5
- 241000894007 species Species 0.000 description 5
- 208000011580 syndromic disease Diseases 0.000 description 5
- 210000002700 urine Anatomy 0.000 description 5
- JVJFIQYAHPMBBX-UHFFFAOYSA-N 4-hydroxynonenal Chemical compound CCCCCC(O)C=CC=O JVJFIQYAHPMBBX-UHFFFAOYSA-N 0.000 description 4
- 108010075016 Ceruloplasmin Proteins 0.000 description 4
- 102100023321 Ceruloplasmin Human genes 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- AIJULSRZWUXGPQ-UHFFFAOYSA-N Methylglyoxal Chemical compound CC(=O)C=O AIJULSRZWUXGPQ-UHFFFAOYSA-N 0.000 description 4
- MWUXSHHQAYIFBG-UHFFFAOYSA-N Nitric oxide Chemical compound O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 4
- YIQKLZYTHXTDDT-UHFFFAOYSA-H Sirius red F3B Chemical compound C1=CC(=CC=C1N=NC2=CC(=C(C=C2)N=NC3=C(C=C4C=C(C=CC4=C3[O-])NC(=O)NC5=CC6=CC(=C(C(=C6C=C5)[O-])N=NC7=C(C=C(C=C7)N=NC8=CC=C(C=C8)S(=O)(=O)[O-])S(=O)(=O)[O-])S(=O)(=O)O)S(=O)(=O)O)S(=O)(=O)[O-])S(=O)(=O)[O-].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+] YIQKLZYTHXTDDT-UHFFFAOYSA-H 0.000 description 4
- 229960000583 acetic acid Drugs 0.000 description 4
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 4
- 230000006378 damage Effects 0.000 description 4
- 230000003247 decreasing effect Effects 0.000 description 4
- 230000029087 digestion Effects 0.000 description 4
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 4
- 229940088598 enzyme Drugs 0.000 description 4
- UFFSXJKVKBQEHC-UHFFFAOYSA-N heptafluorobutyric anhydride Chemical compound FC(F)(F)C(F)(F)C(F)(F)C(=O)OC(=O)C(F)(F)C(F)(F)C(F)(F)F UFFSXJKVKBQEHC-UHFFFAOYSA-N 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 230000002503 metabolic effect Effects 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 238000005502 peroxidation Methods 0.000 description 4
- 239000008363 phosphate buffer Substances 0.000 description 4
- 235000020777 polyunsaturated fatty acids Nutrition 0.000 description 4
- 230000003389 potentiating effect Effects 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 230000008085 renal dysfunction Effects 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 230000000451 tissue damage Effects 0.000 description 4
- 231100000827 tissue damage Toxicity 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 0 CC(*)(*)C(CC=*1)C=C1[U] Chemical compound CC(*)(*)C(CC=*1)C=C1[U] 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 102000017011 Glycated Hemoglobin A Human genes 0.000 description 3
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 235000006708 antioxidants Nutrition 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 230000002238 attenuated effect Effects 0.000 description 3
- 230000008721 basement membrane thickening Effects 0.000 description 3
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 3
- 238000012754 cardiac puncture Methods 0.000 description 3
- 239000002738 chelating agent Substances 0.000 description 3
- 239000007979 citrate buffer Substances 0.000 description 3
- 210000000805 cytoplasm Anatomy 0.000 description 3
- 235000005911 diet Nutrition 0.000 description 3
- 230000037213 diet Effects 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 3
- 239000003651 drinking water Substances 0.000 description 3
- 235000020188 drinking water Nutrition 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 150000004665 fatty acids Chemical class 0.000 description 3
- 235000013305 food Nutrition 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 230000001434 glomerular Effects 0.000 description 3
- 108091005995 glycated hemoglobin Proteins 0.000 description 3
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 3
- 230000033444 hydroxylation Effects 0.000 description 3
- 238000005805 hydroxylation reaction Methods 0.000 description 3
- 229960002591 hydroxyproline Drugs 0.000 description 3
- 238000003364 immunohistochemistry Methods 0.000 description 3
- 229910052742 iron Inorganic materials 0.000 description 3
- 230000003902 lesion Effects 0.000 description 3
- 239000002858 neurotransmitter agent Substances 0.000 description 3
- 230000004792 oxidative damage Effects 0.000 description 3
- 230000008506 pathogenesis Effects 0.000 description 3
- 230000009145 protein modification Effects 0.000 description 3
- 239000002516 radical scavenger Substances 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 230000002000 scavenging effect Effects 0.000 description 3
- JUJBNYBVVQSIOU-UHFFFAOYSA-M sodium;4-[2-(4-iodophenyl)-3-(4-nitrophenyl)tetrazol-2-ium-5-yl]benzene-1,3-disulfonate Chemical compound [Na+].C1=CC([N+](=O)[O-])=CC=C1N1[N+](C=2C=CC(I)=CC=2)=NC(C=2C(=CC(=CC=2)S([O-])(=O)=O)S([O-])(=O)=O)=N1 JUJBNYBVVQSIOU-UHFFFAOYSA-M 0.000 description 3
- FGMPLJWBKKVCDB-UHFFFAOYSA-N trans-L-hydroxy-proline Natural products ON1CCCC1C(O)=O FGMPLJWBKKVCDB-UHFFFAOYSA-N 0.000 description 3
- 230000004584 weight gain Effects 0.000 description 3
- 235000019786 weight gain Nutrition 0.000 description 3
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 description 2
- AOFUBOWZWQFQJU-SNOJBQEQSA-N (2r,3s,4s,5r)-2,5-bis(hydroxymethyl)oxolane-2,3,4-triol;(2s,3r,4s,5s,6r)-6-(hydroxymethyl)oxane-2,3,4,5-tetrol Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O.OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@@H]1O AOFUBOWZWQFQJU-SNOJBQEQSA-N 0.000 description 2
- MUGOTNWCTZMBLV-UHFFFAOYSA-N 2-[4-oxo-2-(2-propan-2-ylidenehydrazinyl)-1,3-thiazol-5-yl]-n-phenylacetamide Chemical compound S1C(NN=C(C)C)=NC(=O)C1CC(=O)NC1=CC=CC=C1 MUGOTNWCTZMBLV-UHFFFAOYSA-N 0.000 description 2
- CWBPXSZASLMQHN-UHFFFAOYSA-N 2-hydroxyheptanal Chemical compound CCCCCC(O)C=O CWBPXSZASLMQHN-UHFFFAOYSA-N 0.000 description 2
- BURIBGPOZBIZEK-UHFFFAOYSA-N 3-[(2-chlorophenyl)carbamoylamino]-2-methyl-2-phenoxypropanoic acid Chemical compound ClC1=C(C=CC=C1)NC(NCC(C(=O)O)(C)OC1=CC=CC=C1)=O BURIBGPOZBIZEK-UHFFFAOYSA-N 0.000 description 2
- ZGCHLOWZNKRZSN-NTSWFWBYSA-N 3-deoxyglucosone Chemical compound OC[C@@H](O)[C@@H](O)CC(=O)C=O ZGCHLOWZNKRZSN-NTSWFWBYSA-N 0.000 description 2
- UHPMJDGOAZMIID-UHFFFAOYSA-N 3-deoxyglucosone Natural products OCC1OC(O)C(=O)CC1O UHPMJDGOAZMIID-UHFFFAOYSA-N 0.000 description 2
- 239000005541 ACE inhibitor Substances 0.000 description 2
- 206010001580 Albuminuria Diseases 0.000 description 2
- ATRRKUHOCOJYRX-UHFFFAOYSA-N Ammonium bicarbonate Chemical compound [NH4+].OC([O-])=O ATRRKUHOCOJYRX-UHFFFAOYSA-N 0.000 description 2
- 229910000013 Ammonium bicarbonate Inorganic materials 0.000 description 2
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 2
- 102000014914 Carrier Proteins Human genes 0.000 description 2
- 108010078791 Carrier Proteins Proteins 0.000 description 2
- 102000012437 Copper-Transporting ATPases Human genes 0.000 description 2
- JPVYNHNXODAKFH-UHFFFAOYSA-N Cu2+ Chemical compound [Cu+2] JPVYNHNXODAKFH-UHFFFAOYSA-N 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 208000032928 Dyslipidaemia Diseases 0.000 description 2
- 108010067770 Endopeptidase K Proteins 0.000 description 2
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical compound [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- WGCNASOHLSPBMP-UHFFFAOYSA-N Glycolaldehyde Chemical compound OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 2
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 2
- 102000001554 Hemoglobins Human genes 0.000 description 2
- 108010054147 Hemoglobins Proteins 0.000 description 2
- 208000002972 Hepatolenticular Degeneration Diseases 0.000 description 2
- 101000610640 Homo sapiens U4/U6 small nuclear ribonucleoprotein Prp3 Proteins 0.000 description 2
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 2
- 208000017170 Lipid metabolism disease Diseases 0.000 description 2
- 102000004895 Lipoproteins Human genes 0.000 description 2
- 108090001030 Lipoproteins Proteins 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- 208000008948 Menkes Kinky Hair Syndrome Diseases 0.000 description 2
- 208000012583 Menkes disease Diseases 0.000 description 2
- 102000010909 Monoamine Oxidase Human genes 0.000 description 2
- 108010062431 Monoamine oxidase Proteins 0.000 description 2
- 102000003992 Peroxidases Human genes 0.000 description 2
- 230000002292 Radical scavenging effect Effects 0.000 description 2
- 208000017442 Retinal disease Diseases 0.000 description 2
- 206010038923 Retinopathy Diseases 0.000 description 2
- 101001110823 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-A Proteins 0.000 description 2
- 101000712176 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-B Proteins 0.000 description 2
- 239000002262 Schiff base Substances 0.000 description 2
- 150000004753 Schiff bases Chemical class 0.000 description 2
- 102000019197 Superoxide Dismutase Human genes 0.000 description 2
- 108010012715 Superoxide dismutase Proteins 0.000 description 2
- 102100040374 U4/U6 small nuclear ribonucleoprotein Prp3 Human genes 0.000 description 2
- 206010053649 Vascular rupture Diseases 0.000 description 2
- 208000018839 Wilson disease Diseases 0.000 description 2
- 210000001766 X chromosome Anatomy 0.000 description 2
- GPKUGWDQUVWHIC-UHFFFAOYSA-N [4-(4-hydrazinylphenyl)phenyl]hydrazine tetrahydrochloride Chemical compound Cl.Cl.Cl.Cl.NNC1=CC=C(C=C1)C1=CC=C(NN)C=C1 GPKUGWDQUVWHIC-UHFFFAOYSA-N 0.000 description 2
- 238000005903 acid hydrolysis reaction Methods 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 235000012538 ammonium bicarbonate Nutrition 0.000 description 2
- 239000001099 ammonium carbonate Substances 0.000 description 2
- 229940044094 angiotensin-converting-enzyme inhibitor Drugs 0.000 description 2
- 229940114079 arachidonic acid Drugs 0.000 description 2
- 235000021342 arachidonic acid Nutrition 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000031018 biological processes and functions Effects 0.000 description 2
- 239000000090 biomarker Substances 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 238000011088 calibration curve Methods 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 230000003915 cell function Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000013522 chelant Substances 0.000 description 2
- 230000009920 chelation Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 229910001431 copper ion Inorganic materials 0.000 description 2
- 210000000695 crystalline len Anatomy 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 230000007850 degeneration Effects 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000004807 desolvation Methods 0.000 description 2
- 239000012470 diluted sample Substances 0.000 description 2
- 229960003638 dopamine Drugs 0.000 description 2
- 238000001647 drug administration Methods 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 210000000585 glomerular basement membrane Anatomy 0.000 description 2
- LEQAOMBKQFMDFZ-UHFFFAOYSA-N glyoxal Chemical compound O=CC=O LEQAOMBKQFMDFZ-UHFFFAOYSA-N 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 229960002725 isoflurane Drugs 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 238000012417 linear regression Methods 0.000 description 2
- 230000037356 lipid metabolism Effects 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 229910021645 metal ion Inorganic materials 0.000 description 2
- 238000000386 microscopy Methods 0.000 description 2
- 238000002552 multiple reaction monitoring Methods 0.000 description 2
- 229960002748 norepinephrine Drugs 0.000 description 2
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000004783 oxidative metabolism Effects 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 239000008188 pellet Substances 0.000 description 2
- KHIWWQKSHDUIBK-UHFFFAOYSA-N periodic acid Chemical compound OI(=O)(=O)=O KHIWWQKSHDUIBK-UHFFFAOYSA-N 0.000 description 2
- 108040007629 peroxidase activity proteins Proteins 0.000 description 2
- CMFNMSMUKZHDEY-UHFFFAOYSA-N peroxynitrous acid Chemical compound OON=O CMFNMSMUKZHDEY-UHFFFAOYSA-N 0.000 description 2
- 230000000750 progressive effect Effects 0.000 description 2
- 230000006318 protein oxidation Effects 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 239000007845 reactive nitrogen species Substances 0.000 description 2
- 230000008707 rearrangement Effects 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 229960004889 salicylic acid Drugs 0.000 description 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 2
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 2
- 239000004299 sodium benzoate Substances 0.000 description 2
- 235000010234 sodium benzoate Nutrition 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000013222 sprague-dawley male rat Methods 0.000 description 2
- 230000035882 stress Effects 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000008719 thickening Effects 0.000 description 2
- 208000037816 tissue injury Diseases 0.000 description 2
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 2
- ALXLJPPLHFRKEJ-MLWJPKLSSA-N (2s)-2,6-diaminononanedioic acid Chemical compound OC(=O)CCC(N)CCC[C@H](N)C(O)=O ALXLJPPLHFRKEJ-MLWJPKLSSA-N 0.000 description 1
- FJIGLGLZNXQEDE-GDVGLLTNSA-N (2s)-2,6-diaminooctanedioic acid Chemical compound OC(=O)CC(N)CCC[C@H](N)C(O)=O FJIGLGLZNXQEDE-GDVGLLTNSA-N 0.000 description 1
- FYKWFMBIZQSDMP-VUWPPUDQSA-N (2s)-6-amino-2-(2-hydroxyheptanoylamino)hexanoic acid Chemical compound CCCCCC(O)C(=O)N[C@H](C(O)=O)CCCCN FYKWFMBIZQSDMP-VUWPPUDQSA-N 0.000 description 1
- HRGCAZUYBJZUHM-GDVGLLTNSA-N (6S)-2-amino-6-(methylamino)heptanedioic acid Chemical compound CN[C@H](C(O)=O)CCCC(N)C(O)=O HRGCAZUYBJZUHM-GDVGLLTNSA-N 0.000 description 1
- 229930182837 (R)-adrenaline Natural products 0.000 description 1
- KVJHGPAAOUGYJX-UHFFFAOYSA-N 1,1,3,3-tetraethoxypropane Chemical compound CCOC(OCC)CC(OCC)OCC KVJHGPAAOUGYJX-UHFFFAOYSA-N 0.000 description 1
- XHTYQFMRBQUCPX-UHFFFAOYSA-N 1,1,3,3-tetramethoxypropane Chemical compound COC(OC)CC(OC)OC XHTYQFMRBQUCPX-UHFFFAOYSA-N 0.000 description 1
- HXJZEGBVQCRLOD-UHFFFAOYSA-N 1-triethoxysilylpropan-2-amine Chemical compound CCO[Si](CC(C)N)(OCC)OCC HXJZEGBVQCRLOD-UHFFFAOYSA-N 0.000 description 1
- XOHUEYCVLUUEJJ-UHFFFAOYSA-I 2,3-Diphosphoglycerate Chemical compound [O-]P(=O)([O-])OC(C(=O)[O-])COP([O-])([O-])=O XOHUEYCVLUUEJJ-UHFFFAOYSA-I 0.000 description 1
- STRVVRPNBAHXRJ-UHFFFAOYSA-N 2-hydroxynon-2-enal Chemical compound CCCCCCC=C(O)C=O STRVVRPNBAHXRJ-UHFFFAOYSA-N 0.000 description 1
- RVBUGGBMJDPOST-UHFFFAOYSA-N 2-thiobarbituric acid Chemical compound O=C1CC(=O)NC(=S)N1 RVBUGGBMJDPOST-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UHFFFAOYSA-N 2-{[3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy}-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound OCC1OC(CO)(OC2OC(CO)C(O)C(O)C2O)C(O)C1O CZMRCDWAGMRECN-UHFFFAOYSA-N 0.000 description 1
- KJDSORYAHBAGPP-UHFFFAOYSA-N 4-(3,4-diaminophenyl)benzene-1,2-diamine;hydron;tetrachloride Chemical compound Cl.Cl.Cl.Cl.C1=C(N)C(N)=CC=C1C1=CC=C(N)C(N)=C1 KJDSORYAHBAGPP-UHFFFAOYSA-N 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 102100030988 Angiotensin-converting enzyme Human genes 0.000 description 1
- 102000006410 Apoproteins Human genes 0.000 description 1
- 108010083590 Apoproteins Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 208000024172 Cardiovascular disease Diseases 0.000 description 1
- QRYRORQUOLYVBU-VBKZILBWSA-N Carnosic acid Natural products CC([C@@H]1CC2)(C)CCC[C@]1(C(O)=O)C1=C2C=C(C(C)C)C(O)=C1O QRYRORQUOLYVBU-VBKZILBWSA-N 0.000 description 1
- 108010087806 Carnosine Proteins 0.000 description 1
- 102000016938 Catalase Human genes 0.000 description 1
- 108010053835 Catalase Proteins 0.000 description 1
- 102000000844 Cell Surface Receptors Human genes 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- 230000010736 Chelating Activity Effects 0.000 description 1
- 102000000634 Cytochrome c oxidase subunit IV Human genes 0.000 description 1
- 108090000365 Cytochrome-c oxidases Proteins 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 108010015720 Dopamine beta-Hydroxylase Proteins 0.000 description 1
- 102100033156 Dopamine beta-hydroxylase Human genes 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 108010067306 Fibronectins Proteins 0.000 description 1
- 102000016359 Fibronectins Human genes 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 208000035150 Hypercholesterolemia Diseases 0.000 description 1
- 206010020880 Hypertrophy Diseases 0.000 description 1
- 235000019766 L-Lysine Nutrition 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- 102000007547 Laminin Human genes 0.000 description 1
- 108010085895 Laminin Proteins 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 206010027525 Microalbuminuria Diseases 0.000 description 1
- 102000006386 Myelin Proteins Human genes 0.000 description 1
- 108010083674 Myelin Proteins Proteins 0.000 description 1
- VEYYWZRYIYDQJM-ZETCQYMHSA-N N(2)-acetyl-L-lysine Chemical compound CC(=O)N[C@H](C([O-])=O)CCCC[NH3+] VEYYWZRYIYDQJM-ZETCQYMHSA-N 0.000 description 1
- NUXSIDPKKIEIMI-LURJTMIESA-N N(6)-carboxymethyl-L-lysine Chemical compound OC(=O)[C@@H](N)CCCCNCC(O)=O NUXSIDPKKIEIMI-LURJTMIESA-N 0.000 description 1
- QPCDCPDFJACHGM-UHFFFAOYSA-N N,N-bis{2-[bis(carboxymethyl)amino]ethyl}glycine Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(=O)O)CCN(CC(O)=O)CC(O)=O QPCDCPDFJACHGM-UHFFFAOYSA-N 0.000 description 1
- CQOVPNPJLQNMDC-UHFFFAOYSA-N N-beta-alanyl-L-histidine Natural products NCCC(=O)NC(C(O)=O)CC1=CN=CN1 CQOVPNPJLQNMDC-UHFFFAOYSA-N 0.000 description 1
- SPMDNGMGZSHTLL-ZSCHJXSPSA-N NCCCC[C@H](N)C(O)=O.CCCCCC(O)C=CC=O Chemical compound NCCCC[C@H](N)C(O)=O.CCCCCC(O)C=CC=O SPMDNGMGZSHTLL-ZSCHJXSPSA-N 0.000 description 1
- DHDHEPWUWIWXOG-BAPYBRSISA-N NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.CCCCCC(=O)N[C@H](C(O)=O)CCCCN Chemical compound NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.CCCCCC(=O)N[C@H](C(O)=O)CCCCN DHDHEPWUWIWXOG-BAPYBRSISA-N 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000013901 Nephropathies and tubular disease Diseases 0.000 description 1
- 206010029164 Nephrotic syndrome Diseases 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 241000520330 Otomys irroratus Species 0.000 description 1
- 102000004669 Protein-Lysine 6-Oxidase Human genes 0.000 description 1
- 108010003894 Protein-Lysine 6-Oxidase Proteins 0.000 description 1
- 208000031074 Reinjury Diseases 0.000 description 1
- 206010038468 Renal hypertrophy Diseases 0.000 description 1
- 206010061481 Renal injury Diseases 0.000 description 1
- 101710172711 Structural protein Proteins 0.000 description 1
- ISWQCIVKKSOKNN-UHFFFAOYSA-L Tiron Chemical compound [Na+].[Na+].OC1=CC(S([O-])(=O)=O)=CC(S([O-])(=O)=O)=C1O ISWQCIVKKSOKNN-UHFFFAOYSA-L 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 102000004243 Tubulin Human genes 0.000 description 1
- 108090000704 Tubulin Proteins 0.000 description 1
- 108091000117 Tyrosine 3-Monooxygenase Proteins 0.000 description 1
- 102000048218 Tyrosine 3-monooxygenases Human genes 0.000 description 1
- 108010061168 Ultralente Insulin Proteins 0.000 description 1
- COQLPRJCUIATTQ-UHFFFAOYSA-N Uranyl acetate Chemical compound O.O.O=[U]=O.CC(O)=O.CC(O)=O COQLPRJCUIATTQ-UHFFFAOYSA-N 0.000 description 1
- 206010053648 Vascular occlusion Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- KTXWMXPGLVNFQF-UHFFFAOYSA-N [W].[P].P(=O)(=O)[Mo] Chemical compound [W].[P].P(=O)(=O)[Mo] KTXWMXPGLVNFQF-UHFFFAOYSA-N 0.000 description 1
- 230000003187 abdominal effect Effects 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 108010055267 advanced glycation end products-bovine serum albumin Proteins 0.000 description 1
- 239000012637 allosteric effector Substances 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 210000003484 anatomy Anatomy 0.000 description 1
- 239000000400 angiotensin II type 1 receptor blocker Substances 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 230000006851 antioxidant defense Effects 0.000 description 1
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- DCPBQSFZQHFSMR-QMMMGPOBSA-N argpyrimidine Chemical compound CC1=NC(NCCC[C@H](N)C(O)=O)=NC(C)=C1O DCPBQSFZQHFSMR-QMMMGPOBSA-N 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 230000003143 atherosclerotic effect Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000008236 biological pathway Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- HOQPTLCRWVZIQZ-UHFFFAOYSA-H bis[[2-(5-hydroxy-4,7-dioxo-1,3,2$l^{2}-dioxaplumbepan-5-yl)acetyl]oxy]lead Chemical compound [Pb+2].[Pb+2].[Pb+2].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O.[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O HOQPTLCRWVZIQZ-UHFFFAOYSA-H 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 230000006931 brain damage Effects 0.000 description 1
- 231100000874 brain damage Toxicity 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 239000007978 cacodylate buffer Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- LEMUFSYUPGXXCM-JNEQYSBXSA-N caninsulin Chemical compound [Zn].C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H]1CSSC[C@H]2C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC3N=CN=C3)NC(=O)[C@H](CO)NC(=O)CNC1=O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)O)C(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O)=O)CSSC[C@@H](C(N2)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C1C=NC=N1 LEMUFSYUPGXXCM-JNEQYSBXSA-N 0.000 description 1
- 230000023852 carbohydrate metabolic process Effects 0.000 description 1
- 235000021256 carbohydrate metabolism Nutrition 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 150000001728 carbonyl compounds Chemical class 0.000 description 1
- 230000009084 cardiovascular function Effects 0.000 description 1
- CQOVPNPJLQNMDC-ZETCQYMHSA-N carnosine Chemical compound [NH3+]CCC(=O)N[C@H](C([O-])=O)CC1=CNC=N1 CQOVPNPJLQNMDC-ZETCQYMHSA-N 0.000 description 1
- 229940044199 carnosine Drugs 0.000 description 1
- 230000001925 catabolic effect Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 210000004671 cell-free system Anatomy 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 206010008118 cerebral infarction Diseases 0.000 description 1
- 238000002655 chelation therapy Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 108010034748 copper-binding protein Proteins 0.000 description 1
- 208000029078 coronary artery disease Diseases 0.000 description 1
- 208000031513 cyst Diseases 0.000 description 1
- OESHPIGALOBJLM-REOHCLBHSA-N dehydroascorbate Chemical compound OC[C@H](O)[C-]1OC(=O)C(=O)C1=O OESHPIGALOBJLM-REOHCLBHSA-N 0.000 description 1
- 235000020960 dehydroascorbic acid Nutrition 0.000 description 1
- 239000011615 dehydroascorbic acid Substances 0.000 description 1
- 229910003460 diamond Inorganic materials 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 125000004989 dicarbonyl group Chemical group 0.000 description 1
- 230000010339 dilation Effects 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 238000000132 electrospray ionisation Methods 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000008753 endothelial function Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 238000001976 enzyme digestion Methods 0.000 description 1
- 229960005139 epinephrine Drugs 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 210000001508 eye Anatomy 0.000 description 1
- 229910001448 ferrous ion Inorganic materials 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- VZCCETWTMQHEPK-QNEBEIHSSA-N gamma-linolenic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/CCCCC(O)=O VZCCETWTMQHEPK-QNEBEIHSSA-N 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 108091005996 glycated proteins Proteins 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 229940015043 glyoxal Drugs 0.000 description 1
- 210000004884 grey matter Anatomy 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 238000002173 high-resolution transmission electron microscopy Methods 0.000 description 1
- 230000001744 histochemical effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002349 hydroxyamino group Chemical group [H]ON([H])[*] 0.000 description 1
- 208000006575 hypertriglyceridemia Diseases 0.000 description 1
- 238000013115 immunohistochemical detection Methods 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Substances N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 230000010438 iron metabolism Effects 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 201000008627 kidney hypertrophy Diseases 0.000 description 1
- 208000037806 kidney injury Diseases 0.000 description 1
- 210000000738 kidney tubule Anatomy 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000029226 lipidation Effects 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical compound CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 description 1
- 229960003105 metformin Drugs 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 206010062198 microangiopathy Diseases 0.000 description 1
- 210000004088 microvessel Anatomy 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 238000013425 morphometry Methods 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 210000005012 myelin Anatomy 0.000 description 1
- 210000003007 myelin sheath Anatomy 0.000 description 1
- VEYYWZRYIYDQJM-UHFFFAOYSA-N n-α-acetyllysine Chemical compound CC(=O)NC(C(O)=O)CCCCN VEYYWZRYIYDQJM-UHFFFAOYSA-N 0.000 description 1
- 210000000885 nephron Anatomy 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 230000001019 normoglycemic effect Effects 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 238000010525 oxidative degradation reaction Methods 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- AYEKKSTZQYEZPU-RYUDHWBXSA-N pentosidine Chemical compound OC(=O)[C@@H](N)CCCCN1C=CC=C2N=C(NCCC[C@H](N)C(O)=O)N=C12 AYEKKSTZQYEZPU-RYUDHWBXSA-N 0.000 description 1
- YPJUNDFVDDCYIH-UHFFFAOYSA-N perfluorobutyric acid Chemical compound OC(=O)C(F)(F)C(F)(F)C(F)(F)F YPJUNDFVDDCYIH-UHFFFAOYSA-N 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- DHRLEVQXOMLTIM-UHFFFAOYSA-N phosphoric acid;trioxomolybdenum Chemical compound O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.OP(O)(O)=O DHRLEVQXOMLTIM-UHFFFAOYSA-N 0.000 description 1
- 208000005833 pili torti Diseases 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000034190 positive regulation of NF-kappaB transcription factor activity Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000004853 protein function Effects 0.000 description 1
- 201000001474 proteinuria Diseases 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 210000005234 proximal tubule cell Anatomy 0.000 description 1
- 150000003224 pyridoxamines Chemical class 0.000 description 1
- 238000000275 quality assurance Methods 0.000 description 1
- 238000003908 quality control method Methods 0.000 description 1
- HDACQVRGBOVJII-JBDAPHQKSA-N ramipril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](C[C@@H]2CCC[C@@H]21)C(O)=O)CC1=CC=CC=C1 HDACQVRGBOVJII-JBDAPHQKSA-N 0.000 description 1
- 229960003401 ramipril Drugs 0.000 description 1
- 239000003642 reactive oxygen metabolite Substances 0.000 description 1
- 210000005084 renal tissue Anatomy 0.000 description 1
- 230000001084 renoprotective effect Effects 0.000 description 1
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000009919 sequestration Effects 0.000 description 1
- 229940076279 serotonin Drugs 0.000 description 1
- 239000012064 sodium phosphate buffer Substances 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 210000002536 stromal cell Anatomy 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 229950003937 tolonium Drugs 0.000 description 1
- HNONEKILPDHFOL-UHFFFAOYSA-M tolonium chloride Chemical compound [Cl-].C1=C(C)C(N)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 HNONEKILPDHFOL-UHFFFAOYSA-M 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 208000037978 tubular injury Diseases 0.000 description 1
- 230000010024 tubular injury Effects 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 238000012762 unpaired Student’s t-test Methods 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 208000021331 vascular occlusion disease Diseases 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XOSXWYQMOYSSKB-LDKJGXKFSA-L water blue Chemical compound CC1=CC(/C(\C(C=C2)=CC=C2NC(C=C2)=CC=C2S([O-])(=O)=O)=C(\C=C2)/C=C/C\2=N\C(C=C2)=CC=C2S([O-])(=O)=O)=CC(S(O)(=O)=O)=C1N.[Na+].[Na+] XOSXWYQMOYSSKB-LDKJGXKFSA-L 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4706—4-Aminoquinolines; 8-Aminoquinolines, e.g. chloroquine, primaquine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/02—Muscle relaxants, e.g. for tetanus or cramps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/06—Free radical scavengers or antioxidants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/14—Vasoprotectives; Antihaemorrhoidals; Drugs for varicose therapy; Capillary stabilisers
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Physical Education & Sports Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Vascular Medicine (AREA)
- Hematology (AREA)
- Toxicology (AREA)
- Rheumatology (AREA)
- Heart & Thoracic Surgery (AREA)
- Urology & Nephrology (AREA)
- Obesity (AREA)
- Cardiology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Dermatology (AREA)
- Biochemistry (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Pain & Pain Management (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Quinoline Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
背景技術
1.技術分野
[0002] 本出願は、生物医科学の分野に関し、そして特に、脂質レベルを哺乳動物において低下させる方法に関する。ある態様は、4−(2−ナフチルカルボキサミド)フェノキシイソ酪酸;2−(8−キノリノキシ)プロピオン酸;及びメチレンビス(4,4’−(2−クロロフェニルウレイドフェノキシイソ酪酸))のような化合物を投与することを含んでなる阻害へ向けられる。
[0003] 糖尿病の制御及び合併症試験(The Diabetic Control and Complications Trial)(DCCT)とUKPDS研究により、高血糖症は、糖尿病性合併症の発症の主たる危険因子として同定された。糖尿病の制御及び合併症試験研究グループ(The Diabetes Control and Complications Trial Research Group)N. Engl. J. Med. 329: 977-986, 1993; 英国後向き糖尿病研究グループ(UK Prospective Diabetes Study Group)Lancet 352: 837-853, 1998。糖化最終産物(AGE)の生成は、高血糖症と糖尿病の長期合併症の間の重要な病原性のつながりとして同定された。Makita et al., N. Eng. J. Med. 325: 836-842, 1993; Bucala and Cerami, Adv. Pharmacol 23: 1-33, 1992; Browlee, Nature 414: 813-820, 2001; Sheetz and King, J. A. M. A. 288: 2579-2588, 2002; Stith et al., Expert Opin. Invest. Drugs 11: 1205-1223, 2002。
[0013] 故に、1つの態様において、本発明は、脂質レベルを哺乳動物において低下させる方法を提供し、該方法は、以下の化合物又はその医薬的に許容される塩:LR−9[4−(2−ナフチルカルボキサミド)フェノキシイソ酪酸];LR−74[2−(8−キノリノキシ)プロピオン酸];及びLR−90[メチレンビス(4,4’−(2−クロロフェニルウレイドフェノキシイソ酪酸))]のいずれかの有効量を哺乳動物へ投与することを含んでなる。
[0017] 本明細書に考察するLR化合物(図2を参照のこと)は、LR−16より誘導される一群の新規芳香族化合物に属する。LR−16は、ヘモグロビン分子の酸素アフィニティーを高めることにおいて2,3−ビスホスホグリセリン酸塩と相乗的なアロステリックエフェクターとして作用して、そしてそれは、コレステロールの豊富な食餌で飼育したラットにおいて血清コレステロールと低密度リポタンパク質(LDL)を低下させることが示された。Lalezari et al., Proc. Natl. Acad. Sci. USA 85: 6117-6121, 1988。
実施例1.糖尿病及び対照ラットの処置
[0034] 雄性スプリーグ・ドーリーラット(約175〜200g)を処置前の1週間馴化してから、一晩絶食の後でSTZ(クエン酸緩衝液(pH4.5)中65mg/kg)の腹腔内注射により糖尿病にした。対照(非糖尿病)動物には緩衝液だけを注射した。ストレプトゾトシン(STZ)注射から7日後に血漿グルコース濃度を測定することによって糖尿病を確認した。20ミリモルより高い血漿グルコース濃度のある動物だけを糖尿病として分類して、本試験に使用した。これらの糖尿病ラットを未処置糖尿病対照群と糖尿病処置群へ無作為に分けた。処置群には、本試験の期間(LR−90では32週;LR−9及びLR−74では30週)を通して、LR化合物をその飲料水中50mg/lで与えた。すべての動物を個別に収容して、食餌と水を自由に摂取させた。
b 非糖尿病対照ラットに対してp<0.05
c 糖尿病ラットに対してp<0.05
表II.STZ糖尿病ラットの体重及び血糖に対するLR−9及びLR−74の効果(30週の処置)
b 非糖尿病対照ラットに対してp<0.05
c 糖尿病ラットに対してp<0.05
実施例2.脂質代謝に対する効果
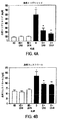
[0039] 糖尿病ラットは、非糖尿病ラットと比較して、全血漿/血清トリグリセリドとコレステロールの両方の上昇レベルを示した(p<0.001)。図3を参照のこと。LR化合物のいずれかで処置した糖尿病ラットは、トリグリセリド及びコレステロールの両方の濃度において有意な低下を示した。LR−90は、血清トリグリセリドと血清コレステロールを非糖尿病動物のレベルの方へ50%低下させた(図3)。同様に、糖尿病ラットの血漿トリグリセリド及びコレステロールのレベルも、LR−9とLR−74の両方によりそれぞれ60%及び50%より多く低下した(図4)。
[0040] 腎機能の指標として、尿アルブミン、血漿クレアチニン濃度、及び尿アルブミン/クレアチニン比を使用した。非糖尿病対照ラットと比べて、尿アルブミン排出、血漿クレアチニン濃度、及びUA/Crは、糖尿病動物において有意に増加した。表III及びIVを参照のこと。糖尿病ラットのLR化合物での処置は、尿アルブミン排出及びUA/Crの上昇を阻害して、未処置糖尿病ラットに比較して約50%の濃度の低下を伴った。さらに、糖尿病動物において観察される血漿クレアチニン濃度の上昇は、LR−9、LR−74、又はLR−90のいずれの処置でも50%ほど有意に減少した。
b 非糖尿病対照ラットに対してp<0.05
c 糖尿病ラットに対してp<0.05
表IV.STZ糖尿病ラットの腎機能パラメータに対するLR−9及びLR−74の効果
b 非糖尿病対照ラットに対してp<0.05
c 糖尿病ラットに対してp<0.05
実施例4.血清AGEに対する効果
[0041] Al-Abed et al., Meth. Enzymol 309: 152-172, 1999 の方法に従って血清AGEを測定して、Rahbar et al., Biochem. Biophys. Res. Commun. 262: 651-656, 1999 の方法を使用して、ポリクローナルR6/9抗AGE RNAアーゼ抗体で定量した。1AUを1μg/ml AGE−BSAに等しいと仮定した。
[0043] Kochakian et al., Diabetes 45: 1694-1700, 1996 に従って、尾腱コラーゲンの単離及び調製を実施した。コラーゲン中の架橋結合及びAGE生成の相対度をペプシン消化と酸溶解性により評価した。ペプシン消化は、Stefek et al., Biochim. Biophys. Acta 1502: 398-404, 2000 により既報のように実施した。簡潔に言えば、個々のラットからの10mgのコラーゲン試料を37℃で24時間、ペプシン(酢酸0.5モル/L中50μg/mL)で消化した。消化後、試料を4℃で30分間、3000rpmで遠心分離して、消化されたコラーゲンを含有する澄明な上清を採取した。上清の100マイクロリットルのアリコートを、365nm励起と418nm放射での試料の蛍光の測定のために、900μL PBS緩衝液と混合した。酸加水分解に続いて既知の方法(Creemers et al., Biotechniques 22: 656-658, 1997)によるマイクロアッセイ法を使用して、上清のヒドロキシプロリン含量を算出した。
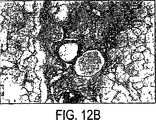
[0046] 糸球体硬化症(糸球体基底膜の肥厚化、糸球体間質肥大、及び毛細管閉塞として定義される)を定量するために、腎臓切片を過ヨウ素酸シッフ(PAS)試薬で染色した。各ラット腎臓(各処置につき4つの異なる腎臓)より全部で150の糸球体を無作為に選択して、盲検の評価者により、硬化症を慎重に等級付けた。各糸球体における硬化症の度合いは、以下のように、1〜4のスケールで主観的に等級付けた:等級1、硬化症領域が25%未満;等級2、硬化症領域が25〜50%;等級3、硬化症領域が51〜75%;及び、等級4、硬化症領域が75%より多い。次いで、以下の式を使用して、糸球体硬化症指標(GSI)を算出した:GSI=Σ4 i=1Fi(i)(ここでFiは、(I)のスコアを与えられたラットにおける糸球体の百分率である)。Wilkinson-Berka et al., Diabetes 51: 3283-3289, 2002 を参照のこと。糸球体硬化症を定量するために、腎臓切片を過ヨウ素酸シッフ(PAS)試薬で染色した。
[0052] 免疫組織化学的なAGE染色のために、ホルマリン固定したパラフィルム埋込み切片(厚さ2μm)を、2−アミノプロピルトリエトキシシランでコートしたスライドに載せて、58℃で3時間焼き、脱パラフィン化し、3%過酸化水素水で濯いで、プロテイナーゼK(0.5mg/mL)とともに室温で5分間インキュベートした。上記の切片をリンス緩衝液で洗浄し、タンパク遮断剤で5分間遮断して、引き続き、CMLに特異的な6D12抗AGEマウスモノクローナル抗体とともに室温で30分間インキュベートした。リンス緩衝液で洗浄後、この切片を標識ポリマーペルオキシダーゼ共役マウス抗IgGのあるEnVisionTMとともに室温で30分間インキュベートし、続いて色素原としての3,3’−ジアミノベンチジン四塩酸塩溶液と対比染色としての50%ヘマトキシリンで検出した。
[0053] タンパク酸化のマーカーであるニトロチロシンを、反応性窒素種により引き起こされる酸化的組織傷害の指標として使用した。ニトロチロシンの免疫組織化学的な検出は、既報(Forbes et al., Diabetes 51: 3274-3282, 2002)のように実施して、本研究では、ほとんど変更を加えずに従った。簡潔に言えば、各処置群からの代表的なラットより32週で採取した、ホルマリン固定した腎臓切片(厚さ5μm)をスライドに載せて、脱ワックスして、水和させた。プロテイナーゼKと10分間のインキュベーション後、切片を3%過酸化水素水において20分間インキュベートし、ブタ正常血清で20分間遮断してから、市販のウサギポリクローナル抗ニトロチロシン抗体で1時間染色した。DAKOリンス緩衝液で濯いだ後で、切片をビオチニル化抗ウサギIgGとともに25分間インキュベートし、アビジン−ビオチン西洋ワサビペルオキシダーゼ複合体との25分間のインキュベーションを続けた。ペルオキシダーゼコンジュゲートの位置決定は、ジアミノベンチジン四塩酸塩(DAB)溶液を色素原として、50%ヘマトキシリンを対比染色として使用して明らかにした。
[0055] アスコルビン酸の銅触媒酸化の阻害の動態の in vitro 測定を、Price et al. J. Biol. Chem. 276: 48967-48972, 2001 の方法に従って実施した。簡潔に言えば、CuCl2と様々な濃度の阻害化合物を、Chelex処理した20ミリモル/Lリン酸緩衝液(pH7.4)において5分間プレインキュベートした。次いで、アスコルビン酸(水中10ミリモル/Lの50μL)を加えて、反応を開始させた(全体の反応量:1mL)。CuCl2とアスコルビン酸の反応物中での最終濃度は、それぞれ500ナノモル/Lと500マイクロモル/Lであった。アリコート(135μL)を0及び60分で取り出して、15μLの10ミリモル/l DTPAを含有する自動注入バイアルへ移した。自動注入器とMillenium(登録商標)32ソフトウェアが装備したWaters(登録商標)2690 Separator Moduleを使用して、XTerraTM RP18 5μmガードカラム付きXTerraTM RP18カラム(250mm x 4.6mm,5μm)での逆相HPLCにより試料を分析した。溶媒と勾配液は、いずれも Dillon et al., Life Sci. 72: 1583-1594, 2003 に記載のように使用した。アスコルビン酸の吸光度を244nmで測定し、ピーク面積を得て、時間に対して残存するアスコルビン酸の百分率を推定した。それぞれの阻害化合物について、AA酸化の速度を50%阻害する濃度(IC50)を、PrismTMソフトウェアを使用して、対照に関連して計算した。
[0062] 雄性スプリーグ・ドーリーラットにおいて、一晩絶食後のSTZ(65mg/kg,クエン酸緩衝液(pH4.5)中)の単回i.p.注射により、糖尿病を誘導した。非糖尿病動物には、クエン酸緩衝液だけを注射した。STZ注射の1週後、>20ミリモル/Lの血漿グルコースを有する動物だけを糖尿病として分類して、本試験に含めた。糖尿病ラットを以下の処置群:糖尿病未処置(D);及び、LR−9(D+LR−9)又はLR−74(D+LR−74)のいずれかを飲料水中50mg/Lで摂取する2つの糖尿病処置群へ無作為に分けた。3つの非糖尿病群:1つの未処置非糖尿病群(ND)と、飲料水中50mg/LのLR−9(ND+LR−9)又はLR−74(ND+LR−74)のいずれかで処置する2つの非糖尿病群も同時に試験した。
*NDに対してP<0.05;**Dに対してP<0.05;***Dに対してP<0.01。
[0066] 本試験の32週目に、イソフルレンでの過剰麻酔と心臓穿刺によりラットを殺した。各動物より血液試料を採取し、ヘパリン添加した Vaculainer 管へ移してから、血漿単離のために遠心分離した。これら血漿試料のアリコートを分析のときまで−70℃で保存した。すぐに腎臓を取り出し、被膜剥離して、PBS緩衝液中で濯いだ。左腎臓の切片を後続の顕微鏡検査とAGE免疫組織化学のために10%中性緩衝化ホルマリンに保存した。各個別ラットの腹皮及び尾の切片を取り出し、PBS緩衝液中で濯ぎ、後続のAGE定量と架橋結合分析のために−70℃で保存した。
[0068] 実施例11の各ラットより尾腱コラーゲンを単離して、コラーゲン中のAGE生成の度合いを、酵素消化後の蛍光AGEの測定により評価した。Figarola et al., Diabetologia 46: 1140-1152。皮膚コラーゲンの単離及び還元は、Shaw et al., Methods Mol. Biol. 186: 129-137, 2002 に記載のように実施した。AGE/ALEのレベルをコラーゲン試料のリジン含量に対して正規化した。
[0070] Micromass QuatroTM Ultima三重四重極(Triple Quadripole)質量分析計へインターフェース連結したAgilent TechnologiesTM LC1100シリーズシステムを使用して、イオン対逆相液体クロマトグラフィー/タンデム質量分析法の分析を実施した。Phenomenex C18ガードカラムを先付けしたPhenomenex SynergiTM Hydro−RP 4μm 80A 150x2.0mmカラムを使用して、HPLC分離を行った。カラム温度を25℃に維持して、流速は、0.2mL/分であった。一定比の移動相は、水中10%アセトニトリル及び0.1%ヘプタフルオロ酪酸からなった。全ランタイムは、12分であり;注入量は、20μLであった。自動注入器の温度は、5℃であった。質量分光光度計のエレクトロスプレーイオン化源は、190L/時間のコーンガス流速と550L/時間の脱溶媒和ガス流速の陽イオンモードで操作した。毛管電圧は2.7kVへ設定した。コーン電圧及び衝突槽電圧は、それぞれ、CMLについて25V及び13eV、d4CMLについて33V及び12eV、CELについて24V及び14eV、d8CELについて29kV及び14eV、そしてリジンについて29kV及び16eVへ最適化した。電源温度は、125℃であった。脱溶媒和温度を300℃へ高めて、溶媒遅延プログラムを0〜3分と10〜20分に使用した。上記化合物の断片化は、衝突解離条件下の酸性移動相で誘導することができる。前駆体→生成物イオンのm/zでの組合せ(CMLについて205.1→130.11、d4CMLについて209.12→134.12、CELについて219.11→130.11、d8CELについて227.18→138.16、リジンについて147.15→84.21、そしてDL−d4リジンについて151.27→88.23)を多重反応モニタリング(MRM)モードで使用して、上記の化合物を定量した。データの獲得及び処理には、MassLynxTMバージョン3.5ソフトウェアを使用した。
[0074] 糖尿病ラットは、非糖尿病ラットと比較して、上昇レベルの血漿脂質を示した。図21を参照のこと。血漿トリグリセリドは、未処置非糖尿病対照の86±14mg/dLに比較して、糖尿病ラットでは598±110mg/dLへ増加した(P<0.001)。血漿コレステロール濃度は、糖尿病動物において同様の増加を示した(非糖尿病の61±7mg/dLに対して、糖尿病ラットでは136±13mg/dL)(P<0.001)。非糖尿病動物の脂質代謝には、いずれの化合物も効果がなかった。しかしながら、いずれかのLR化合物で処置した糖尿病ラットは、トリグリセリド及びコレステロールの両方の濃度で有意な低下を示した。LR−9は、血漿トリグリセリド及びコレステロールをそれぞれ60%及び30%ほど低下させた(それぞれ、239±50及び96±5mg/dLの平均/SEM)。LR−74処置は、未処置糖尿病動物と比較して、血漿グリセリドのほとんど70%の低下(161±29mg/dL)とコレステロールレベルのほぼ30%の減少(93±2mg/dL)をもたらした。血漿脂質ヒドロペルオキシド濃度は、非糖尿病動物と比較して、糖尿病対照ラットでほぼ5倍高かった(5.6±0.5μMに対して26.3±2.7μM)。図21を参照のこと。LR−9又はLR−74での処置は、糖尿病動物の血漿脂質ヒドロペルオキシドをそれぞれ35%と45%実質的に低下させた。図21を参照のこと。
[0075] 実施例10に記載のようにラットを処置して、処置群へ分けた。薬物の投与前に血漿グルコースと体重をともに検査したが、3つの糖尿病処置群の間にも、3つの非糖尿病群の間にも差を検出しなかった。動物はすべて個別に収容して、食餌と水を自由に摂らせた。血糖コントロールと体重を定期的にモニタリングした。高血糖症を制限して、動物が体重を維持することを確実にするために、糖尿病動物には、3IUのUltralenteインスリンを週2〜3回与えた。本試験は、32週にわたって行った。
* NDラットに対してP<0.05を示す
実施例15.糖尿病ラットでは、ニトロチロシン生成が増加する
[0077] ホルマリン固定したパラフィルム埋込み腎臓切片(厚さ2μm)をスライドに載せて、既知の方法に従って、ポリクローナル抗ニトロチロシン抗体で染色した。Figarola et al., Diabetologia 46; 1140-1152, 2003 を参照のこと。ニトロチロシン生成は、反応性窒素種より生じるタンパク質の酸化傷害の指標であり、糖尿病動物において、具体的には近位尿細管細胞において亢進していた。図22を参照のこと。この増加した染色は、いずれかのLR化合物の処置によって減弱した。
[0078] 健常ドナーの血漿より、1回の垂直スピン遠心分離によりヒトLDLを単離し(Chung et al., Methods Enzymol. 128: 181-209, 1986 を参照のこと)、調製の24〜48時間以内に使用した。50mM Chelex処理リン酸塩緩衝液(pH7.4)単独、又は5μM CuCl2、又は5μM CuCl2+様々な濃度のLR化合物の存在下にLDL(50μg/mL)を37℃でインキュベートした。5時間のインキュベーション後、各反応混合物からのアリコートを、Satoh, Clin. Chim. Acta 90: 37-43, 1978 に記載のようなチオバルビツール酸反応性物質(TBARS)の測定のために取り出した。簡潔に言えば、500μLの試料アリコートへ250μLの20%トリクロロ酢酸に続いて、750μLの1% TBARSを加えた。次いで、この試料を激しく撹拌し、沸騰水浴において10分間インキュベートした。冷却後、試料を5000rpmで5分間遠心分離した。上清の吸光度を532nmで読み取り、1,1,3,3−テトラメトキシプロパンを標準品として使用して、MDA当量として表した。脂肪酸酸化の試験では、リノール酸(5mM)を200nMリン酸塩緩衝液(pH7.4)において単独で、又は1mM LR化合物の存在下に37℃で7日間インキュベートした。上記のようなTBARSの測定のために、各反応混合物よりアリコートを定期的に吸引した。アミノグアニジン(AG)とピリドキサミン(PM)を比較対照として250μMで使用した。
Claims (8)
- 哺乳動物において脂質レベルを低下させる化合物又は前記化合物の医薬的に許容される塩の有効量を含む医薬組成物であって、前記化合物が:
LR-9[4-(2-ナフチルカルボキサミド)フェノキシイソ酪酸];
LR-74[2-(8-キノリノキシ)プロピオン酸];及び
LR-90[メチレンビス(4,4'-(2-クロロフェニルウレイドフェノキシイソ酪酸))]からなる群より選択される、前記医薬組成物。 - 前記化合物がLR-9[4-(2-ナフチルカルボキサミド)フェノキシイソ酪酸]である、請求項1の医薬組成物。
- 前記化合物がLR-74[2-(8-キノリノキシ)プロピオン酸]である、請求項1の医薬組成物。
- 前記化合物がLR-90[メチレンビス(4,4'-(2-クロロフェニルウレイドフェノキシイソ酪酸))]である、請求項1の医薬組成物。
- 哺乳動物の糖尿病より生じる合併症を治療するための化合物又は前記化合物の医薬的に許容される塩の有効量を含む医薬組成物であって、ここで前記合併症は、脂質の上昇レベルより生じ、前記化合物は:
LR-9[4-(2-ナフチルカルボキサミド)フェノキシイソ酪酸];
LR-74[2-(8-キノリノキシ)プロピオン酸];及び
LR-90[メチレンビス(4,4'-(2-クロロフェニルウレイドフェノキシイソ酪酸))]からなる群より選択される、前記医薬組成物。 - 前記化合物がLR-9[4-(2-ナフチルカルボキサミド)フェノキシイソ酪酸]である、請求項5の医薬組成物。
- 前記化合物がLR-74[2-(8-キノリノキシ)プロピオン酸]である、請求項5の医薬組成物。
- 前記化合物がLR-90[メチレンビス(4,4'-(2-クロロフェニルウレイドフェノキシイソ酪酸))]である、請求項5の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US51447603P | 2003-10-27 | 2003-10-27 | |
| US60/514,476 | 2003-10-27 | ||
| PCT/US2004/035440 WO2005044251A2 (en) | 2003-10-27 | 2004-10-27 | Methods of lowering lipid levels in a mammal |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2007509946A JP2007509946A (ja) | 2007-04-19 |
| JP2007509946A5 JP2007509946A5 (ja) | 2007-11-22 |
| JP4976851B2 true JP4976851B2 (ja) | 2012-07-18 |
Family
ID=34572758
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006538169A Expired - Lifetime JP4976851B2 (ja) | 2003-10-27 | 2004-10-27 | 脂質レベルを哺乳動物において低下させる方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US7320988B2 (ja) |
| EP (2) | EP2269601A1 (ja) |
| JP (1) | JP4976851B2 (ja) |
| AU (1) | AU2004287434B2 (ja) |
| CA (1) | CA2543611A1 (ja) |
| WO (1) | WO2005044251A2 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2269601A1 (en) * | 2003-10-27 | 2011-01-05 | City of Hope | LR-9, LR-74 and LR-90 for use in treating complications resulting from diabetes |
| WO2007044309A2 (en) * | 2005-10-05 | 2007-04-19 | Vasix Corporation | Device and method for inhibiting age complex formation |
| US8580854B2 (en) * | 2005-11-09 | 2013-11-12 | City Of Hope | Methods of suppression of rage gene expression and rage triggered inflammatory genes by selected age-inhibitors |
| US8124655B2 (en) * | 2007-06-15 | 2012-02-28 | City Of Hope | Use of LR-90 and LR-102 to overcome insulin resistance |
| WO2012103523A2 (en) | 2011-01-27 | 2012-08-02 | Samuel Rahbar | Novel modulators of development of adipocyte and cancer cells |
| US9808434B2 (en) | 2011-01-27 | 2017-11-07 | City Of Hope | Compound for treating cancer and diabetes |
| US11471497B1 (en) | 2019-03-13 | 2022-10-18 | David Gordon Bermudes | Copper chelation therapeutics |
| US20230048576A1 (en) * | 2019-03-19 | 2023-02-16 | City Of Hope | Compounds for the treatment of neuropathic pain |
Family Cites Families (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US514476A (en) | 1894-02-13 | Minnow-bucket | ||
| JPS57500432A (ja) | 1980-03-20 | 1982-03-11 | ||
| US5700447A (en) * | 1992-05-21 | 1997-12-23 | The Picowder Institute For Medical Research | Methods and materials for the diagnosis and treatment of conditions such as stroke |
| US5100919A (en) | 1984-03-19 | 1992-03-31 | The Rockefeller University | Biguanides and derivatives thereof as inhibitors of advanced glycosylation of a target protein |
| US5272176A (en) | 1984-03-19 | 1993-12-21 | The Rockefeller University | Advanced glycation inhibitors containing amino-benzoic acids and derivatives, and methods of use |
| DE3410927A1 (de) | 1984-03-24 | 1985-10-03 | Hoechst Ag, 6230 Frankfurt | Vollaromatische polyester, verfahren zu ihrer herstellung und entsprechende formkoerper |
| US4801610A (en) | 1984-05-21 | 1989-01-31 | G. D. Searle & Co. | Phenolic ester derivatives as elastase inhibitors |
| US4603144A (en) | 1984-08-16 | 1986-07-29 | G. D. Searle & Co. | Kojic acid ether-ester derivatives |
| US5268500A (en) | 1987-06-15 | 1993-12-07 | Montefiore Medical Center | Compound, composition and method for the reduction of lipids the modification of the affinity of hemoblogin for oxygen and the prevention of platelet aggregation |
| US4921997A (en) | 1988-06-15 | 1990-05-01 | Montefiore Medical Center | Method of synthesis and novel compounds for pharmaceutical uses |
| US5093367A (en) | 1988-06-15 | 1992-03-03 | Montefiore Medical Center | Method of synthesis and novel compounds for pharmaceutical uses |
| US5677330A (en) * | 1990-02-12 | 1997-10-14 | The Center For Innovative Technology | Medical uses of allosteric hemoglobin modifier compounds in patient care |
| US6046222A (en) | 1993-09-15 | 2000-04-04 | Warner-Lambert Company | Use of thiazolidinedione derivatives in the treatment of polycystic ovary syndrome, gestational diabetes and disease states at risk for progressing to noninsulin-dependent diabetes mellitus |
| US5833700A (en) | 1995-03-15 | 1998-11-10 | Ethicon Endo-Surgery, Inc. | Sterile occlusion fasteners and instrument and method for their placement |
| WO1995031192A1 (en) | 1994-05-16 | 1995-11-23 | Thomas Jefferson University | Method and use of agents to inhibit protein polymerization and methods of identifying these agents |
| US5661139A (en) | 1995-01-13 | 1997-08-26 | Alteon Inc. | Bis-(2-aryl) hydrazones |
| US5962651A (en) | 1995-01-27 | 1999-10-05 | Montefiore Medical Center | Modified hemoglobin and its use as a component of an artificial blood substitute |
| US5602277A (en) | 1995-03-30 | 1997-02-11 | Biocryst Pharmaceuticals, Inc. | Substituted benzene derivatives useful as neuraminidase inhibitors |
| US5667330A (en) | 1995-11-28 | 1997-09-16 | Case Corporation | Quick-connect mechanism for releasably retaining a power take-off shaft within an output shaft hub |
| US5716987A (en) | 1996-06-21 | 1998-02-10 | Bristol-Myers Squibb Company | Prophylactic and therapeutic treatment of skin sensitization and irritation |
| ATE241982T1 (de) * | 1998-10-22 | 2003-06-15 | Univ South Carolina | Verfahren zur hemmung von diabetischen komplikationen |
| US6787566B2 (en) | 1999-04-05 | 2004-09-07 | City Of Hope | Breakers of advanced glycation endproducts |
| US6605642B2 (en) | 1999-04-05 | 2003-08-12 | City Of Hope | Inhibitors of formation of advanced glycation endproducts (AGES) |
| US6589944B1 (en) | 1999-04-05 | 2003-07-08 | City Of Hope | Breakers of advanced glycation endproducts |
| US7030133B2 (en) | 1999-04-05 | 2006-04-18 | City Of Hope | Inhibitors of formation of advanced glycation endproducts (AGEs) |
| AU763750B2 (en) | 1999-04-05 | 2003-07-31 | City Of Hope | Novel inhibitors of formation of advanced glycation endproducts (AGE's) |
| EP1210087A2 (en) | 1999-04-29 | 2002-06-05 | City of Hope | Pentoxifylline, pioglitazone and metformin are inhibitors of formation of advanced glycation endproducts (age's) |
| CA2393722A1 (en) | 1999-12-13 | 2002-06-14 | President And Fellows Of Harvard College | Methods for treating cell death diseases and inflammation |
| FR2836474B1 (fr) | 2002-02-22 | 2004-12-24 | Synt Em | Composes, compositions et methode pour le transport des molecules de cyclosporine a travers la barriere hemato-encephalique |
| EP2269601A1 (en) * | 2003-10-27 | 2011-01-05 | City of Hope | LR-9, LR-74 and LR-90 for use in treating complications resulting from diabetes |
-
2004
- 2004-10-27 EP EP20100183235 patent/EP2269601A1/en not_active Withdrawn
- 2004-10-27 WO PCT/US2004/035440 patent/WO2005044251A2/en active Application Filing
- 2004-10-27 JP JP2006538169A patent/JP4976851B2/ja not_active Expired - Lifetime
- 2004-10-27 CA CA002543611A patent/CA2543611A1/en not_active Abandoned
- 2004-10-27 EP EP04796420A patent/EP1682114A2/en not_active Ceased
- 2004-10-27 US US10/974,028 patent/US7320988B2/en not_active Expired - Lifetime
- 2004-10-27 AU AU2004287434A patent/AU2004287434B2/en not_active Ceased
-
2007
- 2007-11-30 US US11/948,574 patent/US7652037B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2005044251A3 (en) | 2005-08-25 |
| WO2005044251A2 (en) | 2005-05-19 |
| EP1682114A2 (en) | 2006-07-26 |
| AU2004287434B2 (en) | 2011-04-07 |
| US20050171150A1 (en) | 2005-08-04 |
| JP2007509946A (ja) | 2007-04-19 |
| US7652037B2 (en) | 2010-01-26 |
| US20080200502A1 (en) | 2008-08-21 |
| EP2269601A1 (en) | 2011-01-05 |
| AU2004287434A1 (en) | 2005-05-19 |
| US7320988B2 (en) | 2008-01-22 |
| CA2543611A1 (en) | 2005-05-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7652037B2 (en) | Methods of lowering lipid levels in a mammal | |
| Pérez-Torres et al. | Beneficial effects of the amino acid glycine | |
| Abdel-Wahab et al. | Renal protective effect of SGLT2 inhibitor dapagliflozin alone and in combination with irbesartan in a rat model of diabetic nephropathy | |
| Smit et al. | The clinical relevance of advanced glycation endproducts (AGE) and recent developments in pharmaceutics to reduce AGE accumulation | |
| Monnier | Intervention against the Maillard reaction in vivo | |
| Radika et al. | Nitric oxide mediates the insulin sensitizing effects of β-sitosterol in high fat diet-fed rats | |
| CA2439791C (en) | Use of breakers of advanced glycation endproducts for treating deleterious effects of aging and debilitating diseases | |
| JP4860906B2 (ja) | 心疾患および/または関連心不全の予防および/または治療 | |
| del Carmen Contini et al. | Adverse effects in kidney function, antioxidant systems and histopathology in rats receiving monosodium glutamate diet | |
| Sourris et al. | Inhibitors of advanced glycation end product (AGE) formation and accumulation | |
| Duan et al. | Ferroptosis and its potential role in metabolic diseases: a curse or revitalization? | |
| Ott et al. | Effects of stimulation of soluble guanylate cyclase on diabetic nephropathy in diabetic eNOS knockout mice on top of angiotensin II receptor blockade | |
| JP2005533003A5 (ja) | ||
| Méndez et al. | Inhibition by L-arginine and spermidine of hemoglobin glycation and lipid peroxidation in rats with induced diabetes | |
| Mishra et al. | Inhibition of phosphodiesterase type 9 reduces obesity and cardiometabolic syndrome in mice | |
| Hamdy et al. | Modulatory effects of curcumin and green tea extract against experimentally induced pulmonary fibrosis: a comparison with N‐acetyl cysteine | |
| Samadi-Noshahr et al. | trans-Anethole attenuated renal injury and reduced expressions of angiotensin II receptor (AT1R) and TGF-β in streptozotocin-induced diabetic rats | |
| Kostoglou-Athanassiou et al. | Oxytocin release is inhibited by the generation of carbon monoxide from the rat hypothalamus–further evidence for carbon monoxide as a neuromodulator | |
| JP3864050B2 (ja) | 糖尿病合併症を治療または予防するための医薬組成物 | |
| Nagareddy et al. | N-acetylcysteine prevents nitrosative stress-associated depression of blood pressure and heart rate in streptozotocin diabetic rats | |
| Noa et al. | A comparative study of policosanol vs lovastatin on intimal thickening in rabbit cuffed carotid artery | |
| US8580854B2 (en) | Methods of suppression of rage gene expression and rage triggered inflammatory genes by selected age-inhibitors | |
| KR100785375B1 (ko) | 중금속중독 예방을 위한 사료. | |
| WO2000066101A2 (en) | Method of inhibiting glycation product formation | |
| Basaran et al. | Effect of curcumin on ipsilateral and contralateral testes after unilateral testicular torsion in a rat model |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071004 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20071004 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110609 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20110906 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110908 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110915 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111007 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111017 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111108 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111209 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120316 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120413 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4976851 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150420 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |