JP4441121B2 - 新規トリプシンファミリーセリンプロテアーゼ - Google Patents
新規トリプシンファミリーセリンプロテアーゼ Download PDFInfo
- Publication number
- JP4441121B2 JP4441121B2 JP2000579724A JP2000579724A JP4441121B2 JP 4441121 B2 JP4441121 B2 JP 4441121B2 JP 2000579724 A JP2000579724 A JP 2000579724A JP 2000579724 A JP2000579724 A JP 2000579724A JP 4441121 B2 JP4441121 B2 JP 4441121B2
- Authority
- JP
- Japan
- Prior art keywords
- protein
- pro
- testec
- dna
- present
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
- C12N9/50—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25)
- C12N9/64—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from animal tissue
- C12N9/6421—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from animal tissue from mammals
- C12N9/6424—Serine endopeptidases (3.4.21)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Enzymes And Modification Thereof (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Detergent Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
本発明は新規トリプシンファミリーセリンプロテアーゼ、その遺伝子、並びにそれらの製造及び用途に関する。
背景技術
雄性配偶子である精子は、雄の生殖器官である精巣において、主に(1)生殖幹細胞である精原細胞の自己増殖と精子への分化の開始、(2)精母細胞の減数分裂と遺伝子の組み換え、(3)半数体精子細胞の精子への形態形成、の3段階の過程を経て生産される。こうして形成された精子は交尾により雌体に排出され、卵管を通過し、雌性配偶子である卵子と結合し受精に至る(K.YomogidaおよびY.Nishimune(1998)蛋白質核酸酵素,511−521)。
受精において、精子は卵管を通り卵子表面の透明帯と結合し、その透明帯を通過し、さらに卵子と融合する必要がある。これら受精の過程にはさまざまなプロテアーゼが関与している。例えば精子型アンジオテンシン変換酵素(testis ACE)は、そのノックアウトマウスの解析(J.H.Kregeら(1995)Nature375,146−148;C.R.Esther Jrら(1996)Lab.Invest.74,953−965)から、精子が卵管を通る際に重要な役割を果たしていることが示されており(J.R.Hagamanら,1998,Proc.Natl.Acad.Sci.USA 95:2552−2557)、また、前駆体タンパク質変換酵素4(PC4)も、雄のノックアウトマウスでは受精が著しく低下する(M.Mbikayら(1997)Proc.Natl.Acad.Sci.USA 94,6842−6846)。
セリンプロテアーゼに関しては、in vitroの受精が各種のトリプシンインヒビターにより阻害されることから、精子が透明帯を通過する際、精子(特に先端)に含まれるトリプシン様セリンプロテアーゼが透明帯を消化することが示唆されている(P.M.Saling(1981)Proc.Natl.Acad.Sci.USA78,6231−6235;D.A.BenauおよびB.T.Storey(1987)Biol.Reprod.36,282−292;D.Y.LiuおよびH.W.Baker(1993)Biol.Reprod.48,340−348)。従来は精子先端に存在するトリプシンファミリーセリンプロテアーゼであるアクロシン(acrosin)がこの働きを担っていると考えられていた(C.R.Brown(1983)J.Reprod.Fertil.69,289−295;H.Kremlingら(1991)Genomics 11,828−834;U.Klemmら(1990)Differentiation 42,160−166)。しかしそのノックアウトマウスがほぼ正常な受精をすることが判明し、アクロシン以外の精子に存在するセリンプロテアーゼが透明帯の消化を行っていることが示唆されている(T.Babaら(1994)J.Biol.Chem.269,31845−31849;I.M.Adhamら(1997)Mol.Reprod,Dev.46,370−376)。ホヤではスペルモシン(spermosin)というトリプシンファミリーセリンプロテアーゼが精子で発現しており(H.Sawadaら(1984)J.Biol.Chem.259,2900−2904)、この特異抗体がホヤの受精を濃度依存的に阻害することが判明している(H.Sawadaら(1996)Biochem.Biophys.Res.Commun.222,499−504)。また、最近マウスの精子先端に特異的に発現しているトリプシンファミリーセリンプロテアーゼであるTESP1、TESP2のcDNAがクローニングされた(N.Kohnoら(1998)Biochem.Biophys.Res.Commun.245,658−665)。しかし、この遺伝子が有する受精の際の役割はいまだ判明していない。これまでに透明帯を消化する働きを持つ、精子に存在するセリンプロテアーゼは報告されていない。
発明の開示
本発明は、精子の形成や機能に関連する新規トリプシンファミリーセリンプロテアーゼおよびそれらをコードする遺伝子、並びにそれらの製造方法および用途を提供することを課題とする。
本発明者らは、76A5sc2と命名された遺伝子のポリメラーゼ連鎖反応による増幅の結果、76A5sc2遺伝子とは異なる配列を有する遺伝子断片を見出した。本発明者らは、この遺伝子断片を基に、成体マウス精巣に特異的に発現する2つの新規トリプシンファミリーセリンプロテアーゼ(「Tespec PRO−1」及び「Tespec PRO−2」)の全オープンリーディングフレーム(ORF)を含むcDNAをクローニングし、さらにこれら遺伝子の組織における発現について解析した。
単離された「Tespec PRO−1」(Testis specific expressed serine proteinase−1)は321アミノ酸をコードすると予想され、その予想アミノ酸配列はトリプシンファミリーセリンプロテアーゼモチーフである「Trypsin−His」および「Trypsin−Ser」活性部位を有し、また他のトリプシンファミリーセリンプロテアーゼであるアクロシンやプロスタシン、トリプシンなどと、この2つのモチーフおよびその近傍において非常に高い相同性を示した。しかし、それ以外の領域においては核酸およびアミノ酸レベルで高い相同性を示す既知遺伝子は存在せず、新規なトリプシンファミリーセリンプロテアーゼであることが判明した。
一方、「Tespec PRO−2」は319アミノ酸をコードすると予想され、「Trypsin−His」活性部位を保持していた。[Trypsin−Ser」活性部位については12アミノ酸よりなるモチーフ中、2アミノ酸がモチーフとは異なるが、他の既知トリプシンファミリーセリンプロテアーゼにおいてもこのような例は存在するため、「Tespec PRO−2」はプロテアーゼとして機能すると考えられる。「Tespec PRO−2」もまた、核酸およびアミノ酸レベルで高い相同性を示す既知遺伝子は存在せず、新規なトリプシンファミリーセリンプロテアーゼであることが判明した。
「Tespec PRO−2」には、興味深いことに「Tespec PRO−2」の前半領域と「Tespec PRO−1」の後半領域がつながったスプライシングアイソフォームが存在した。このため、これら2つのプロテアーゼは染色体上で非常に近い位置に存在することが示唆された。「Tespec PRO−2」には種々のスプライシングアイソフォームが存在するが、「Tespec PRO−2」以外のアイソフォームは長いORFが開かず、プロテアーゼをコードしていなかった。「Tespec PRO−1」および「Tespec PRO−2」は核酸レベル、アミノ酸レベルでそれぞれ52.2%、33.1%の相同性を有していた。
本発明者らは、また、マウス「Tespec PRO−2」の核酸配列を基に、RT−PCR及びRACEを用いて、ヒト「Tespec PRO−2」のcDNAのクローニングを行った。これにより取得されたヒト「Tespec PRO−2」とマウス「Tespec PRO−2]は核酸レベル、アミノ酸レベルでそれぞれ74.2%、69.8%の相同性を有することが判明した。また、ヒト「Tespec PRO−2」は第8染色体にコードされていることが判明した。
本発明者らはさらに、マウス「Tespec PRO−1」の核酸配列を基に、RT−PCR及びRACEを用いて、ヒト「Tespec PRO−3」のcDNAのクローニングに成功した。また、ヒト「Tespec PRO−3」のカウンターパートであるマウス「Tespec PRO−3」のcDNAのクローニングにも成功した。
「Tespec PRO−1」をコードする領域をプローブとしたマウスノーザンブロットの解析より、この遺伝子は成体マウス精巣でのみ発現が見られ、他の組織や胎児期ではその発現は確認されなかった。同様にRT−PCRによる解析からも、「Tespec PRO−1」の発現は成体精巣で非常に高いことが判明した。また、「Tespec PRO−1」は生後18日目以降の精巣で発現の上昇が確認できたが、生後12日目以前の精巣や精子形成不全の変異体マウス精巣ではその発現が全く見られなかった。同様な解析を「Tespec PRO−2」でも行ったところ、「Tespec PRO−1」と同様の発現パターンであることが判明した。これら事実は「Tespec PRO−1]及び「Tespec PRO−2」が、精子の分化・熟成または精子の機能(受精)に関与していることを示唆する。一方、トリプシンファミリーセリンプロデアーゼに関しては、受精の際に重要な役割を担っていることが示唆されている。
従って、本発明者らは、見出した遺伝子によりコードされるタンパク質が、受精の鍵となるセリンプロテアーゼである可能性があり、新しい不妊症の治療薬や不妊症診断薬の開発、あるいは新しい避妊薬の開発に有用であると考えた。
本発明は、精子の形成や機能に関連すると考えられる新規トリプシンファミリーセリンプロテアーゼ、それらをコードする遺伝子、並びにそれらの製造方法および用途に関し、より具体的には、
1. 配列番号:2、4、6、8、10のいずれかに記載のアミノ酸配列からなるタンパク質、
2. 配列番号:2、4、6、8、10のいずれかに記載のアミノ酸配列からなるタンパク質と機能的に同等な、下記(a)または(b)に記載のタンパク質、
(a) 配列番号:2、4、6、8、10のいずれかに記載のアミノ酸配列において1若しくは複数のアミノ酸が欠失、付加、挿入および/または他のアミノ酸による置換により修飾されたアミノ酸配列からなるタンパク質、
(b) 配列番号:1、3、5、7、9のいずれかに記載の塩基配列からなるDNAとハイブリダイズするDNAがコードするタンパク質、
3. (1)または(2)に記載のタンパク質の部分ペプチド、
4. (1)または(2)に記載のタンパク質と他のペプチドとからなる融合タンパク質、
5. (1)〜(3)のいずれかに記載のタンパク質をコードするDNA、
6. (5)に記載のDNAが挿入されたベクター、
7. (5)に記載のDNAを発現可能に保持する形質転換体、
8. (7)に記載の形質転換体を培養し、該形質転換体またはその培養上清から発現させたタンパク質を回収する工程を含む、(1)〜(3)のいずれかに記載のタンパク質の製造方法、
9. (1)または(2)に記載のタンパク質の基質をスクリーニングする方法であって、
(a)該タンパク質に被検試料を接触させる工程、
(b)該タンパク質の被検試料に対するプロテアーゼ活性を検出する工程、および
(c)該プロテアーゼ活性により分解または切断を受ける化合物を選択する工程、を含む方法、
10. (9)に記載の方法により単離されうる、(1)または(2)に記載のタンパク質の基質、
11. (1)または(2)に記載のタンパク質の活性を阻害する化合物をスクリーニングする方法であって、
(a)被検試料の存在下で該タンパク質に(10)に記載の基質を接触させる工程、
(b)該タンパク質による該基質に対するプロテアーゼ活性を検出する工程、および
(c)被検試料非存在下において検出した場合と比較して、該プロテアーゼ活性を低下させる化合物を選択する工程、を含む方法、
12. (11)に記載の方法により単離されうる、(1)または(2)に記載のタンパク質の活性を阻害する化合物、
13. (1)または(2)に記載のタンパク質に結合する抗体、
14. (13)に記載の抗体と、(1)または(2)に記載のタンパク質が含まれると予想される試料とを接触させ、該抗体と該タンパク質との免疫複合体の生成を検出又は測定することを含んでなる、該タンパク質を検出又は測定する方法、
15. 配列番号:1、3、5、7または9のいずれかに記載の塩基配列からなるDNAと特異的にハイブリダイズし、少なくとも15塩基の鎖長を有するヌクレオチド、を提供するものである。
本発明は、新規トリプシンファミリーセリンプロテアーゼを提供する。本発明のタンパク質に含まれる「Tespec PRO−1」と命名されたマウスタンパク質のアミノ酸配列を配列番号:2に、「Tespec PRO−2」と命名されたマウスおよびヒトタンパク質のアミノ酸配列をそれぞれ配列番号:4および6に、また「Tespec PRO−3」と命名されたマウスおよびヒトタンパク質のアミノ酸配列をそれぞれ配列番号:8および10に示し、それらのタンパク質をコードするcDNAの塩基配列をそれぞれ配列番号:1、3、5、7および9に示す。
本発明のタンパク質に含まれる[Tespec PRO−1」及び「Tespec PRO−2」は、マウス精巣において高い発現が観察された(実施例5および6)。これらのタンパク質は精子、特にその先端領域に存在するならば、精子が透明帯を消化し受精を成立させる際の鍵となるプロテアーゼである可能性がある。従って、本発明のタンパク質は、不妊症治療薬や不妊症診断薬あるいは避妊薬の開発に有用であると考えられる。
また、本発明のタンパク質にはマウス「Tespec PRO−1」タンパク質、マウス「Tespec PRO−2」タンパク質、ヒト「Tespec PRO−2」タンパク質、マウス「Tespec PRO−3」タンパク質、またはヒト「Tespec PRO−3」タンパク質と機能的に同等なタンパク質を包含する。ここで「機能的に同等」とは、マウス「Tespec PRO−1」タンパク質、マウス「Tespec PRO−2」タンパク質、ヒト「Tespec PRO−2」タンパク質、マウス「Tespec PRO−3」タンパク質、またはヒト「Tespec PRO−3」タンパク質と同等の生物学的特性を有していることを意味する。生物学的特性としては、例えば、▲1▼活性の特性として、トリプシンファミリーセリンプロテアーゼ活性を有すること、▲2▼配列の構造的特性として、トリプシンファミリーセリンプロテアーゼモチーフ(「Trypsin−His(PROSITE PS00134)」、「Trypsin−Ser(PROSITE PS00135)」)および/またはそれと類似した配列を有することや、マウス「Tespec PRO−1」タンパク質、マウス「Tespec PRO−2」タンパク質、ヒト「Tespec PRO−2」タンパク質、マウス[Tespec PRO−3]タンパク質、もしくはヒト「Tespec PRO−3」タンパク質のアミノ酸配列と高い相同性が見られること(後述)、▲3▼発現特性として、精巣に発現すること、などが挙げられる。
このようなタンパク質を得るための方法としては、例えば、タンパク質のアミノ酸配列に変異を導入する方法が用いられている。アミノ酸配列に変異が導入されたタンパク質を得るためには、例えば、合成オリゴヌクレオチドプライマーを利用した部位特異的変異誘発法(Kramer,W.and Fritz,H.J.Methods in Enzymol.(1987)154,350−367)やPCRによる部位特異的変異誘発システム(GIBCO−BRL社)、Kunkel法(Methods Enzymol.85,2763−2766(1988))を使用することができる。これらの方法により、配列番号:2、4、6、8または10に示されたアミノ酸配列からなるタンパク質において、その生物学的特性に影響を与えないよう、1若しくは複数個のアミノ酸の欠失、付加、挿入及び/又は他のアミノ酸による置換により修飾されたタンパク質を得ることができる。
変異するアミノ酸の個数は、配列番号:2、4、6、8または10に示されたアミノ酸配列からなるタンパク質の生物学的特性を保持しつる限り特に制限はない。配列番号:2、4、6、8または10のいずれかに示されるアミノ酸配列中の1又は2個以上、好ましくは、2個以上30個以下、より好ましくは2個以上10個以下のアミノ酸が欠失したもの、配列番号:2、4、6、8または10のいずれかに示されるアミノ酸配列に1又は2個以上、好ましくは、2個以上30個以下、より好ましくは2個以上10個以下のアミノ酸が付加したもの、配列番号:2、4、6、8または10のいずれかに示されるアミノ酸配列中の1又は2個以上、好ましくは、2個以上30個以下、より好ましくは2個以上10個以下のアミノ酸が他のアミノ酸で置換されたものが挙げられる。また、アミノ酸の変異部位も、配列番号:2、4、6、8または10に示されたアミノ酸配列からなるタンパク質の生物学的特性を保持しうる限り特に制限はない。
あるアミノ酸配列に対する1または複数個のアミノ酸残基の欠失、付加および/または他のアミノ酸による置換により修飾されたアミノ酸配列を有するタンパク質がその生物学的活性を維持することはすでに知られている(Mark,D.F.et al.,Proc.Natl.Acad.Sci.USA(1984)81,5662−5666、Zoller,M.J.& Smith,M.Nucleic Acids Research(1982)10,6487−6500、Wang,A.et al.,Science224,1431−1433、Dalbadie−McFarland,G.et al.,Proc.Natl.Acad.Sci.USA(1982)79,6409−6413)。
例えば、本発明のタンパク質に1または複数個のアミノ酸残基が付加されたタンパク質として、融合タンパク質が挙げられる。融合タンパク質は、本発明のタンパク質と他のペプチドとが融合したものである。融合タンパク質は人為的に作製することもできる。例えば、本発明のタンパク質をコードするDNAと他のペプチドをコードするDNAをフレームが一致するように連結してこれを発現ベクターに導入し、宿主で発現させればよく、すでに公知の手法を用いることができる。本発明のタンパク質との融合に付される他のペプチドとしては、特に限定されない。例えば、ペプチドとしては、FLAG(Hopp,T.P.et al.,BioTechnology(1988)6,1204−1210)、6個のHis(ヒスチジン)残基からなる6×His、10×His、インフルエンザ凝集素(HA)、ヒトc−mycの断片、VSV−GPの断片、p18HIVの断片、T7−tag、HSV−tag、E−tag、SV40T抗原の断片、lck tag、α−tubulinの断片、B−tag、ProteinCの断片等、すでに公知であるペプチドが使用される。またタンパク質としては、例えばGST(グルタチオン・S・トランスフェラーゼ)、HA(インフルエンザ凝集素)、イムノグロブリン定常領域、β−ガラクトシダーゼ、MBP(マルトース結合タンパク質)等が挙げられる。市販されているこれらをコードするDNAを融合させたものを用いることができる。
また、当業者にとっては、周知技術であるハイブリダイゼーション技術(Sambrook,J et al.,Molecular Cloning 2nd ed.9.47−9.58,Cold Spring Harbor Lab.press,1989)を用いて、上記本発明のタンパク質をコードするDNA(配列番号:1、3、5、7または9に記載のDNA)またはその一部を基に、これと相同性の高いDNAを単離して、該DNAから上記本発明のタンパク質と機能的に同等なタンパク質を得ることも当業者が通常行い得ることである。本発明のタンパク質には、ストリンジェントな条件下で上記本発明のタンパク質をコードするDNAまたはその一部とハイブリダイズするDNAがコードし、上記本発明のタンパク質と機能的に同等なタンパク質が含まれる。ハイブリダイズするDNAを他の生物から単離する場合、生物種に制限はないが、例えば、ヒト、マウス、ラット、ウシ、サル、ブタなどを挙げることができる。「ストリンジェントな条件」とは、通常、「42℃、2xSSC、0.1% SDS」程度であり、好ましくは「50℃、2xSSC、0.1% SDS」程度であり、さらに好ましくは「65℃、2xSSC、0.1% SDS」程度である。これらの条件において、温度を上げる程に高い相同性を有するDNAを得ることができる。
ハイブリダイズ技術により得られたDNAがコードするタンパク質は、通常、配列番号:2、4、6、8または10に記載のアミノ酸配列と高い相同性を有する。「高い相同性」とは、少なくとも60%以上の相同性、好ましくは70%以上の相同性、さらに好ましくは80%以上の相同性、さらに好ましくは95%以上の相同性を指す。タンパク質の相同性を決定するには、文献(Wilbur,W.J.and Lipman,D.J.Proc.Natl.Acad.Sci.USA(1983)80,726−730)に記載のアルゴリズムにしたがえばよい。
本発明のタンパク質は、該タンパク質を産生する細胞や宿主あるいは精製方法により、アミノ酸配列、分子量、等電点又は糖鎖の有無や形態が異なっていてもよい。得られたタンパク質が配列番号:2、4、6、8または10に記載のアミノ酸配列からなるタンパク質の生物学的特性を保持している限り、本発明のタンパク質に含まれる。
本発明のタンパク質は、天然のタンパク質として、また遺伝子組換技術を利用して組み換えタンパク質として製造することが可能である。天然のタンパク質は、本発明のタンパク質が存在すると考えられる組織若しくは細胞(例えば精巣)からタンパク質を抽出し、後述する本発明の抗体を利用したアフィニティークロマトグラフィーを行うことにより調製することができる。
また、組み換えタンパク質を製造するには、本発明のタンパク質をコードするDNAを発現制御領域、例えばエンハンサー、プロモーターの制御のもとで発現可能なように発現ベクターに組み込み、この発現ベクターにより宿主細胞を形質転換し、タンパク質を発現させることができる。
具体的には、例えば、哺乳類細胞を使用する場合、常用される有用なプロモーター/エンハンサー、本発明のタンパク質をコードするDNA、その3’側下流にポリAシグナルを機能的に結合させたDNAあるいはそれを含むベクターを構築することができる。例えばプロモーター/エンハンサーとしては、ヒトサイトメガロウイルス前期プロモーター/エンハンサー(human cytomegalovirus immediateearly promoter/enhancer)を挙げることができる。
また、その他にタンパク質発現に使用できるプロモーター/エンハンサーとして、レトロウイルス、ポリオーマウイルス、アデノウイルス、シミアンウイルス40(SV40)等のウイルスプロモーター/エンハンサーやヒトエロンゲーションファクター1α(HEF1α)の哺乳類細胞由来のプロモーター/エンハンサー等を用いることができる。
例えば、SV40プロモーター/エンハンサーを使用する場合、Mulliganらの方法(Nature(1979)277,108)、また、HEF1αプロモーター/エンハンサーを使用する場合、Mizushimaらの方法(Nucleic Acids Res.(1990)18,5322)に従えば容易に実施することができる。
複製開始点としては、SV40、ポリオーマウイルス、アデノウイルス、ウシパピローマウイルス(BPV)等の由来のものを用いることもできる。さらに、宿主細胞系で遺伝子コピー数増幅のため、発現ベクターは選択マーカーとして、アミノグリコシドトランスフェラーゼ(APH)遺伝子、チミジンキナーゼ(TK)遺伝子、大腸菌キサンチングアニンホスホリポシルトランスフェラーゼ(Ecogpt)遺伝子、ジヒドロ葉酸還元酵素(dhfr)遺伝子等を含むことができる。
大腸菌を使用する場合、常用される有用なプロモーター、ポリペプチド分泌のためのシグナル配列、発現させる遺伝子を機能的に結合させて発現させることができる。例えばプロモーターとしては、lacZプロモーター、araBプロモーターを挙げることができる。lacZプロモーターを使用する場合、Wardらの方法(Nature(1098)341,544−546;FASEB J.(1992)6,2422−2427)、araBプロモーターを使用する場合、Betterらの方法(Science(1988)240,1041−1043)に従えばよい。
タンパク質分泌のためのシグナル配列としては、大腸菌のペリプラズムに産生させる場合、pelBシグナル配列(Lei,S.P.et al J.Bacteriol.(1987)169,4379)を使用すればよい。
本発明のタンパク質を製造するための発現ベクターは、本発明に好適に使用される発現ベクターであればいかなる発現ベクターであってよい。本発明の発現ベクターとしては、例えば、アデノウイルスベクター「pAdexLcw」やレトロウイルスベクター「pZIPneo」などが挙げられる。また哺乳動物由来の発現ベクター、例えばpEF、pCDM8、昆虫細胞由来の発現ベクター、例えばpBacPAK8、植物由来の発現ベクター、例えばpMH1、pMH2、動物ウイルス由来の発現ベクター、例えばpHSV、pMV、pAdexLcw、レトロウイルス由来の発現ベクター。例えばpZIpneo、酵母由来の発現ベクター、例えばpNV11、SP−Q01、枯草菌由来の発現ベクター、例えばpPL608、pKTH50、大腸菌由来の発現ベクター、例えばpQE、pGEAPP、pGEMEAPP、pMALp2、pREP4が挙げられる。
本発明において、タンパク質の製造のために、任意の産生系を使用することができる。タンパク質製造のための産生系は、in vitroおよびin vivoの産生系がある。in vitroの産生系としては、真核細胞を使用する産生系や原核細胞を使用する産生系が挙げられる。
真核細胞を使用する場合、動物細胞、植物細胞、真菌細胞を用いる産生系がある。動物細胞としては、哺乳類細胞、例えばCHO(J.Exp.Med.(1995)108,945)、COS、ミエローマ、BHK(baby hamster kidney)、HeLa、Vero、両生類細胞、例えばアフリカツメガエル卵母細胞(Valle,et al.,Nature(1981)291,358−340)、あるいは昆虫細胞、例えばsf9、sf21、Tn5が知られている。CHO細胞としては、特にDHFR遺伝子を欠損したCHO細胞であるdhfr−CHO(Proc.Natl.Acad.Sci.USA(1980)77,4216−4220)やCHO K−1(Proc.Natl.Acad.Sci.USA(1968)60,1275)を好適に使用することができる。
植物細胞としては、ニコチアナ・タバカム(Nicotiana tabacum)由来の細胞が知られており、これをカルス培養すればよい。真菌細胞としては、酵母、例えばサッカロミセス(Saccharomyces)属、例えばサッカロミセス・セレビシエ(Saccharomyces cerevisiae)、糸状菌、例えばアスペルギルス属(Aspergillus)属、例えばアスペルギルス・ニガー(Aspergillus niger)が知られている。
原核細胞を使用する場合、細菌細胞を用いる産生系がある。細菌細胞としては、大腸菌(E.coli)、枯草菌が知られている。
これらの細胞を目的とするDNAにより形質転換し、形質転換された細胞をin vitroで培養することによりタンパク質が得られる。培養は、公知の方法に従い行う。真核細胞であれば例えば、培養液としてDMEM、MEM、RPMI1640、IMDMを使用することができる。その際、牛胎児血清(FCS)等の血清補液を併用することもできるし、無血清培養してもよい。培養時のpHは約6〜8であるのが好ましい。培養は通常約30〜40℃で約15〜200時間行い、必要に応じて培地の交換、通気、攪拌を加える。
一方、in vivoの産生系としては、動物を使用する産生系や植物を使用する産生系が挙げられる。これらの動物又は植物に目的とするDNAを導入し、動物又は植物の体内でタンパク質を産生させ、回収する。本発明における「宿主」とは、これらの動物、植物を包含する。
動物を使用する場合、哺乳類動物、昆虫を用いる産生系がある。哺乳類動物としては、ヤギ、ブタ、ヒツジ、マウス、ウシを用いることができる(VickiGlaser,SPECTRUM Biotechnology Applications,1993)。また、哺乳類動物を用いる場合、トランスジェニック動物を用いることができる。例えば、目的とするDNAをヤギβカゼインのような乳汁中に固有に産生されるタンパク質をコードする遺伝子の途中に挿入して融合遺伝子として調製する。このDNAが挿入された融合遺伝子を含むDNA断片をヤギの胚へ注入し、この胚を雌のヤギへ導入する。胚を受容したヤギから生まれるトランスジェニックヤギ又はその子孫が産生する乳汁からタンパク質を得る。トランスジェニックヤギから産生されるタンパク質を含む乳汁量を増加させるために、適宜ホルモンをトランスジェニックヤギに使用してもよい(Ebert,K.M.et al.,Bio/Technology(1994)12,699−702)。
また、昆虫としては、例えばカイコを用いることができる。カイコを用いる場合、目的とするDNAを挿入したバキュロウイルスをカイコに感染させ、このカイコの体液より所望のタンパク質を得る(Susumu,M.et al.,Nature(1985)315,592−594)。
さらに植物を使用する場合、例えばタバコを用いることができる。タバコを用いる場合、目的とするDNAを植物発現用ベクター、例えばpMON530に挿入し、このベクターをアグロバクテリウム・ツメファシエンス(Agrobacterium tumefaciens)のようなバクテリアに導入する。このバクテリアをタバコ、例えばニコチアナ・タバカム(Nicotiana tabacum)に感染させ、本タバコの葉より所望のポリペプチドを得る(Julian,K.−C.Ma et al.,Eur.J.Immunol.(1994)24,131−138)。
上記で得られた本発明のタンパク質は、細胞内外、宿主から単離し実質的に純粋で均一なタンパク質として精製することができる。タンパク質の分離、精製は、通常のタンパク質の精製で使用されている分離、精製方法を使用すればよく、何ら限定されるものではない。例えば、クロマトグラフィーカラム、フィルター、限外濾過、塩析、溶媒沈殿、溶媒抽出、蒸留、免疫沈降、SDS−ポリアクリルアミドゲル電気泳動、等電点電気泳動法、透析、再結晶等を適宜選択、組み合わせればタンパク質を分離、精製することができる。
クロマトグラフィーとしては、例えばアフィニティークロマトグラフィー、イオン交換クロマトグラフィー、疎水性クロマトグラフィー、ゲル濾過、逆相クロマトグラフィー、吸着クロマトグラフィー等が挙げられる(Strategies for Protein Purification and Characterization:A Laboratory Course Manual.Ed Daniel R.Marshak et al.,Cold Spring Harbor Laboratory Press,1996)。これらのクロマトグラフィーは、液相クロマトグラフィー、例えばHPLC、FPLC等の液相クロマトグラフィーを用いて行うことができる。本発明は、これらの精製方法を用い、高度に精製されたタンパク質も包含する。
なお、タンパク質を精製前又は精製後に適当なタンパク修飾酵素を作用させることにより、任意に修飾を加えたり部分的にペプチドを除去することもできる。タンパク修飾酵素としては、トリプシン、キモトリプシン、リシルエンドペプチダーゼ、プロテインキナーゼ、グルコシダーゼ、プロテインキナーゼ、グルコシダーゼが用いられる。
本発明は、また、本発明のタンパク質の部分ペプチドも含む。このようなペプチドは、例えば、本発明のタンパク質に結合する抗体を得るための免疫原として利用しうる。この場合、ペプチドは、少なくとも12アミノ酸以上の鎖長を有し、好ましくは、20アミノ酸以上の鎖長を有する。本発明のタンパク質の部分ペプチドは、遺伝子工学的手法、公知のペプチド合成法、あるいは本発明のタンパク質を適切なペプチダーゼで切断することによって製造することができる。ペプチド合成法としては、たとえば固相合成法、液相合成法のいずれによっても良い。
遺伝子工学的手法を利用して宿主内で発現させた本発明のタンパク質若しくはその部分ペプチドは、細胞内外から単離し実質的に純粋で均一なタンパク質として精製することができる。タンパク質の分離、精製は、通常のタンパク質の精製で使用されている分離、精製方法を使用すればよく、何ら限定されるものではない。例えば、クロマトグラフィーカラム、フィルター、限外濾過、塩析、溶媒沈殿、溶媒抽出、蒸留、免疫沈降、SDS−ポリアクリルアミドゲル電気泳動、等電点電気泳動法、透析、再結晶等を適宜選択、組み合わせればタンパク質を分離、精製することができる。
クロマトグラフィーとしては、例えばアフィニティークロマトグラフィー、イオン交換クロマトグラフィー、疎水性クロマトグラフィー、ゲル濾過、逆相クロマトグラフィー、吸着クロマトグラフィー等が挙げられる(Strategies for Protein Purification and Characterization:A Laboratory Course Manual.Ed Daniel R.Marshak et al.,Cold Spring Harbor Laboratory Press,1996)。これらのクロマトグラフィーは、液相クロマトグラフィー、例えばHPLC、FPLC等の液相クロマトグラフィーを用いて行うことができる。本発明は、これらの精製方法を用い、高度に精製されたタンパク質も包含する。
なお、タンパク質を精製前又は精製後に適当なタンパク修飾酵素を作用させることにより、任意に修飾を加えたり部分的にペプチドを除去することもできる。タンパク修飾酵素としては、トリプシン、キモトリプシン、リシルエンドペプチダーゼ、プロテインキナーゼ、グルコシダーゼ、プロテインキナーゼ、グルコシダーゼが用いられる。
また、本発明は、上記本発明のタンパク質をコードするDNAを提供する。本発明のDNAは、in vivo、in vitroで本発明のタンパク質を製造するのみならず、例えば、哺乳動物、例えばヒトの遺伝子治療に用いることもできる。特に、本発明の遺伝子は、不妊症の遺伝子治療への応用が期待される。遺伝子治療に用いる場合には、本発明のDNAが挿入されたベクターを生体内の標的部位へ投与する。投与方法は、ex vivo法であっても、in vivo法であってもよい。なお、本発明のベクターには、このように遺伝子治療に用いられるベクターも含まれる。
本発明のタンパク質をコードするゲノムDNA又はcDNAは、当業者に周知のハイフリダイゼーション技術を用いて、それぞれゲノムライブラリーまたはcDNAライブラリー等をスクリーニングして得ることができる。
得られたDNA又はDNA断片をプローブとして、さらにゲノムライブラリーやcDNAライブラリーをスクリーニングすることにより、異なる細胞、組織、臓器又は種から遺伝子を得ることができる。ゲノムライブラリーまたはcDNAライブラリーは、例えばSambrook,J.et al.,Molecular Cloning、Cold Spring Harbor Laboratory Press(1989)に記載の方法により調製してもよいし、市販のDNAライブラリーを用いてもよい。
また、得られたcDNAの塩基配列を決定することにより、それがコードする翻訳領域を決定でき、本発明のタンパク質のアミノ酸配列を得ることができる。
具体的には、例えば次のようにすればよい。まず、本発明のタンパク質を発現する細胞、組織、臓器からmRNAを単離する。mRNAの単離は公知の方法、例えば、グアニジン超遠心法(Chirgwin,J.M.et al.,Biochemistry(1979)18,5294−5299)、AGPC法(Chomczynski,P.and Sacchi,N.,Anal.Biochem.(1987)162,156−159)等により全RNAを調製し、mRNA Purification Kit(Pharmacia)等を使用して全RNAからmRNAを精製する。また、QuickPrep mRNA Purification Kit(Pharmacia)を用いることによりmRNAを直接調製することもできる。
得られたmRNAから逆転写酵素を用いてcDNAを合成する。cDNAの合成は、AMVReverse Transcriptase First−strand cDNA Synthesis Kit(生化学工業)等を用いて行うこともできる。また、本明細書に記載されたプローブを用いて、5’−Ampli FINDER RACE Kit(Clontech製)およびポリメラーゼ連鎖反応(polymerase chainreaction;PCR)を用いた5’−RACE法(Frohman,M.A.et al.,Proc.Natl.Acad.Sci.U.S.A.(1988)85,8998−9002;Belyavsky,A.et al.,Nucleic Acids Res.(1989)17,2919−2932)に従い、cDNAの合成および増幅を行うことができる。
得られたPCR産物から目的とするDNA断片を調製し、ベクターDNAと連結する。さらに、これより組換えベクターを作製し、大腸菌等に導入してコロニーを選択して所望の組換えベクターを調製する。目的とするDNAの塩基配列を公知の方法、例えば、ジデオキシヌクレオチドチェインターミネーション法により確認すればよい。
また、本発明のDNAは、発現に使用する宿主のコドン使用頻度を考慮して、より発現効率の高い配列を設計することができる(Grantham,R.et al.,Nucelic Acids Research(1981)9,r43−r74)。また、本発明のDNAを市販のキットや公知の方法によって改変することができる。例えば、制限酵素による消化、合成オリゴヌクレオチドや適当なDNAフラグメントの挿入、リンカーの付加、開始コドン(ATG)及び/又は終始コドン(TAA、TGA 又はTAG)の挿入等が挙げられる。
本発明のDNAは、具体的には例えば配列番号:1の塩基配列において48位の塩基Aから1010位の塩基CからなるDNA、配列番号:3の塩基配列において69位の塩基Aから1025位の塩基CからなるDNA、配列番号:5の塩基配列において73位の塩基Aから867位の塩基AからなるDNA、配列番号:7の塩基配列において38位の塩基Aから1000位の塩基AからなるDNA、配列番号:9の塩基配列において41位の塩基Aから1096位の塩基CからなるDNAを包含する。
本発明のDNAはまた、配列番号:1、3、5、7または9のいずれかに記載の塩基配列からなるDNAとストリンジェントな条件下でハイブリダイズするDNAであり、且つ本発明のタンパク質と機能的に同等なタンパク質をコードするDNAを含む。
「ストリンジェントな条件」とは、通常、「42℃、2xSSC、0.1% SDS」程度であり、好ましくは「50℃、2xSSC、0.1%SDS」程度であり、さらに好ましくは「65℃、2xSSC、0.1%SDS」程度である。これらの条件において、温度を上げる程に高い相同性を有するDNAを得ることができる。
上記のハイブリダイズするDNAは、例えば天然由来のDNA(例えばcDNA又はゲノムDNA)であってよい。天然由来のDNAの場合、機能的に同等なタンパク質をコードするDNAを単離するための生物としては、例えば、ヒト、マウス、ラット、ウシ、サル、ブタなどが挙げられる。例えばこれらの生物において、実施例において本発明のタンパク質をコードするcDNAとハイブリダイズするmRNAが検出される組織(例えば精巣)由来のcDNAを用いて本発明のDNAを単離することができる。また、本発明のタンパク質をコードするDNAはcDNAやゲノムDNAの他、合成DNAであってもよい。
また、本発明は、本発明のタンパク質の基質のスクリーニング方法を提供する。本発明のタンパク質の「基質」とは、本発明のタンパク質が結合することにより特定の部位で分解または切断を受ける化合物を指す。
基質となる化合物としては、タンパク質に制限されない。例えば、トリプシン(trypsin)やキモトリプシン(Chymotrypsin)は、タンパク質のみならず、ペプチド化合物の誘導体のアミド結合やエステル結合も切断することが知られている(Farmer,D.A.,et al.,J Biol Chem.(1975)250,7366−7371;del Castillo,L.M.,et al.,Biochim Biophys Acta.(1971)235,358−69)。従って、本発明において、基質としては本発明のタンパク質が結合することにより特定の部位で分解または切断を受ける限り限定されず、ペプチドやその類縁体、誘導体(ペプチド性化合物)、または非ペプチド性化合物などでもよい。
本発明の基質のスクリーニング方法は、(a)本発明のタンパク質に被検試料を接触させる工程、(b)本発明のタンパク質の被検試料に対するプロテアーゼ活性を検出する工程、および(c)本発明のタンパク質のプロテアーゼ活性により分解若しくは切断を受ける化合物を選択する工程、を含む。
スクリーニングに使用される被検試料としては、本発明のタンパク質の基質を含むことが期待される試料であれば特に制限はなく、例えば、細胞抽出液、動物組織抽出液、遺伝子ライブラリーの発現産物、精製若しくは粗精製タンパク質、ペプチド、ペプチドの類縁体若しくは誘導体、非ペプチド性化合物、合成化合物、天然化合物などが挙げられる。
本発明のタンパク質に結合する基質のスクリーニングにおいては、例えば、本発明のタンパク質と被検試料とを混合し、インキュベートした後、被検試料の変化(切断、分解)を測定する。例えば、タンパク質を被検試料とする場合、被検試料を直接、またはアジド化したり、蛍光物質と結合させ、反応前後の試料の変化をUVスペクトル(R.J.Beynon and J.S.Bond,Proteolytic enzymes(1989)IRL press 25−55)や、HPLC(Maier M,et al.(1988)FEBS Lett.232,395−398,Gau W,et al.Adv Exp Med Biol.(1983)156,483−494)で検出し、プロテアーゼ活性を測定することができる。
また、ペプチド(及び類縁体、誘導体)を被検試料とする場合、数アミノ酸(1〜5アミノ酸の場合が多いが、特に制限はない)からなるペプチド(及び類縁体、誘導体)を本発明のタンパク質と混合し、インキュベート後被検試料の変化を測定する。例えば、被検試料のカルボキシル末端に蛍光性化合物(MEC;Kawabata S,et al.(1988)Eur.J.Biochem.172,17−25,AMC; Morita T,et al.(1977)JBiochem(Tokyo).82,1495−1498,AFC;Garrett JR,et al.(1985)Histochem.J.17,805−817,など)を導入しておき、被検試料が切断を受けた際に生じる蛍光性化合物のスペクトル変化を指標にプロテアーゼ活性を測定すればよい。また、その他の蛍光標識ペプチド基質を用いたスクリーニング方法を用いることもできる(R.J.Beynon and J.S.Bond,Proteolytic enzymes(1989)IRL press25−55,Gossrau R,et al.(1984)Adv Exp Med Biol.167,191−207,Yu JX,et al.(1994)J Biol Chem.269,18843−18848)。
また、上記方法の原理を利用して、被検化合物として合成化合物、または天然物バンク、ランダムファージペプチドディスプレイライブラリー、もしくはピンペプチド合成物等を用いてスクリーニングすることや、コンビナトリアルケミストリー技術によるハイスループットスクリーニングも可能である(Wrighton NC;Farrell FX; Chang R;Kashyap AK;Barbone FP;Mulcahy LS;Johnson DL;Barrett RW;Jolliffe LK;Dower WJ.,Small peptides as potent mimetics of the protein hormone erythropoietin,Science(UNITED STATES)Jul 26 1996,273 p458−64、Verdine GL.,The combinatorial chemistry of nature.Nature(ENGLAND)Nov7 1996,384 p11−13、Hogan JC Jr.,Directed combinatorial chemistry.Nature(ENGLAND)Nov 7 1996,384 p17−9)。
上記スクリーニング方法を利用して、本発明のタンパク質の基質が単離されれば、本発明のタンパク質の該基質に対するプロテアーゼ活性を阻害する活性を指標に、本発明のタンパク質の阻害剤をスクリーニングすることができる。従って、本発明は、また、本発明のタンパク質の活性を阻害する化合物をスクリーニングする方法を提供する。
この方法は、(a)被検試料の存在下で本発明のタンパク質にその基質を接触させる工程、(b)本発明のタンパク質の該基質に対するプロテアーゼ活性を検出する工程、および(c)被検試料が非存在下において検出した場合と比較して、該プロテアーゼ活性を低下させる化合物を選択する工程、を含む。
スクリーニングに使用される本発明のタンパク質としては、天然のタンパク質、組換えタンパク質、またはそれらの部分ペプチドであってもよい。また、スクリーニングに使用される被検試料としては、特に制限はなく、例えば、細胞培養上清、遺伝子ライブラリーの発現産物、ペプチド、ペプチドの類縁体若しくは誘導体、精製若しくは粗精製タンパク質(抗体を含む)、非ペプチド性化合物、合成化合物、微生物発酵生産物、海洋生物抽出液、植物抽出液、細胞抽出液、動物組織抽出液、が挙げられる。
本発明のタンパク質の阻害剤のスクリーニングは、例えば、上記文献「R.J.Beynon and J.S.Bond,Proteolytic enzymes(1989)IRL press25−55;Maier M,et al.(1988)FEBS Lett.232,395−398;Gau W,et al.Adv Exp Med Biol.(1983)156,483−494);Kawabata S,et al.(1988)Eur.J.Biochem.172,17−25,;MoritaT,et al.(1977)J Biochem(Tokyo).82,1495−1498;Garrett JR,et al.(1985)Histochem.J.17,805−817;Gossrau R,et al.(1984)Adv Exp Med Biol.167,191−207,Yu JX,et al.(1994)J Biol Chem.269,18843−18848」に記載の系を利用して行なうことができる。また、ペプチド性基質をリード化合物とし、その構造の一部を修飾したり置換した化合物を、本発明のタンパク質の阻害剤スクリーニングにおける被検化合物として用いることも可能である(Okamoto S,et al.(1993)Methods Enzymol.222,328−340)。
上述したように、本発明のタンパク質は、その発現特性等から、精子の分化・熟成または精子の機能(受精)に関与していることが示唆される。本発明のスクリーニング方法により単離される上記阻害剤は、本発明のタンパク質の受精への関与を解析するために利用しうる。例えば、本発明のタンパク質の阻害剤を用いて、インビトロ受精解析(Y.Toyoda et al.,1971,Jpn.J.Anim.Reprod.16:147−151;Y.Kuribayashi et al.,1996,Fertil.Steril.66:1012−1017)を行い、該阻害剤が受精を阻害するか否かを検討することにより、本発明のタンパク質の受精への関与を判定することができる。受精を阻害しうる本発明のタンパク質の阻害剤には、例えば、新たな避妊薬としての利用が考えられる。
本発明のスクリーニング方法を利用して得られる化合物をヒトや他の哺乳動物、例えばマウス、ラット、モルモット、ウサギ、ニワトリ、ネコ、イヌ、ヒツジ、ブタ、ウシ、サル、マントヒヒ、チンパンジーの医薬として使用する場合、常用される手段に従って実施することができる。
例えば、必要に応じて糖衣を施した錠剤、カプセル剤、エリキシル剤、マイクロカプセル剤として経口的に、あるいは水もしくはそれ以外の薬学的に許容し得る液との無菌性溶液、又は懸濁液剤の注射剤の形で非経口的に使用できる。例えば本発明のタンパク質と結合活性を有する化合物を生理学的に認められる担体、香味剤、賦形剤、ベヒクル、防腐剤、安定剤、結合剤とともに一般に認められた製薬実施に要求される単位用量形態で混和することによって製造することができる。これら製剤における有効成分量は指示された範囲の適当な容量が得られるようにするものである。
錠剤、カプセル剤に混和することができる添加剤としては、例えばゼラチン、コーンスターチ、トラガントガム、アラビアゴムのような結合剤、結晶性セルロースのような賦形剤、コーンスターチ、ゼラチン、アルギン酸のような膨化剤、ステアリン酸マグネシウムのような潤滑剤、ショ糖、乳糖又はサッカリンのような甘味剤、ペパーミント、アカモノ油又はチェリーのような香味剤が用いられる。調剤単位形態がカプセルである場合には、上記の材料にさらに油脂のような液状担体を含有することができる。注射のための無菌組成物は注射用蒸留水のようなベヒクル中の活性物質、胡麻油、椰子油のような天然産出植物油を溶解又は懸濁させるための通常の製剤実施に従って処方することができる。
注射用の水溶液としては、例えば生理食塩水、ブドウ糖やその他の補助薬を含む等張液、例えばD−ソルビトール、D−マンノース、D−マンニトール、塩化ナトリウムが挙げられ、適当な溶解補助剤、例えばアルコール、具体的にはエタノール、ポリアルコール、例えばプロピレングリコール、ポリエチレングリコール、非イオン性界面活性剤、例えばポリソルベート80(TM)、HCO−50と併用してもよい。
油性液としてはゴマ油、大豆油があげられ、溶解補助剤として安息香酸ベンジル、ベンジルアルコールと併用してもよい。また、緩衝剤、例えばリン酸塩緩衝液、酢酸ナトリウム緩衝液、無痛化剤、例えば塩化ペンザルコニウム、塩酸プロカイン、安定剤、例えばベンジルアルコール、フェノール、酸化防止剤と配合してもよい。調製された注射液は通常、適当なアンプルに充填させる。
本発明のスクリーニング方法により得られる化合物の投与量は、症状により差異はあるが、経口投与の場合、一般的に成人(体重60kgとして)においては、1日あたり約0.1から100mg、好ましくは約1.0から50mg、より好ましくは約1.0から20mgである。
非経口的に投与する場合は、その1回の投与量は投与対象、対象臓器、症状、投与方法によっても異なるが、例えば注射剤の形では通常成人(体重60kgとして)においては、1日あたり約0.01から30mg、好ましくは約0.1から20mg、より好ましくは約0.1から10mg程度を静脈注射により投与するのが好都合である。他の動物の場合も、体重60kg当たりに換算した量を投与することができる。
また、本発明は、本発明のタンパク質に結合する抗体を提供する。このような抗体は、本発明のタンパク質の検出や精製などに利用しうる。また、上述したin vitro受精解析において利用しうる。抗体は、公知の手段を用いてモノクローナル抗体又はポリクローナル抗体として得ることができる。
本発明のタンパク質に対して特異的に結合する抗体は、タンパク質を感作抗原として使用して、これを通常の免疫方法にしたがって免疫し、得られる免疫細胞を通常の細胞融合法によって公知の親細胞と融合させ、通常のスクリーニング法により、抗体産生細胞をスクリーニングすることによって作製できる。
具体的には、本発明のタンパク質に対して特異的に結合するモノクローナル抗体又はポリクローナル抗体を作製するには次のようにすればよい。
例えば、抗体取得の感作抗原として使用される本発明のタンパク質は、その由来となる動物種に制限されないが哺乳動物、例えばヒト、マウス又はラット由来のタンパク質が好ましく、特にヒト由来のタンパク質が好ましい。ヒト由来のタンパク質は、本明細書に開示される遺伝子配列又はアミノ酸配列を用いて得ることができる。
本発明において、感作抗原として使用されるタンパク質は、本発明のタンパク質またはその部分ペプチドを用いることができる。タンパク質の部分ペプチドとしては、例えばタンパク質のアミノ基(N)末端断片やカルボキシ(C)末端断片が挙げられる。本発明における「抗体」とはタンパク質の全長又は断片に結合する抗体を意味する。
本発明のタンパク質又はその断片をコードする遺伝子を公知の発現ベクター系に挿入して本明細書で述べた宿主細胞を形質転換させた後、その宿主細胞内外又は、宿主から目的のタンパク質又はその断片を公知の方法で得、このタンパク質を感作抗原として用いればよい。また、タンパク質を発現する細胞又はその溶解物あるいは化学的に合成した本発明のタンパク質またはその部分ペプチドを感作抗原として使用してもよい。
感作抗原で免疫される哺乳動物としては、特に限定されるものではないが、一般的にはげっ歯目、ウサギ目、霊長目の動物が使用される。モノクローナル抗体を作成する場合は、細胞融合に使用する親細胞との適合性を考慮して選択するのが好ましい。
げっ歯目の動物としては、例えば、マウス、ラット、ハムスター等が使用される。ウサギ目の動物としては、例えば、ウサギが使用される。霊長目の動物としては、例えばサルが使用される。サルとしては、狭鼻下目のサル(旧世界ザル)、例えば、カニクイザル、アカゲザル、マントヒヒ、チンパンジー等が使用される。
感作抗原を動物に免疫するには、公知の方法にしたがって行われる。例えば、一般的方法として、感作抗原を哺乳動物の腹腔内又は、皮下に注射することにより行われる。具体的には、感作抗原をPBS(Phosphate−Buffered Saline)や生理食塩水等で適当量に希釈、懸濁したものを所望により通常のアジュバント、例えば、フロイント完全アジュバントを適量混合し、乳化後、哺乳動物に投与し、以降フロイント不完全アジュバントに適量混合した感作抗原を、4〜21日毎に数回投与するのが好ましい。また、感作抗原免疫時に適当な担体を使用することができる。このように免疫し、血清中に所望の抗体レベルが上昇するのを常法により確認する。
ここで、本発明のタンパク質に対するポリクローナル抗体を得るには、血清中の所望の抗体レベルが上昇したことを確認した後、抗原を感作した哺乳動物の血液を取り出す。この血液から公知の方法により血清を分離する。ポリクローナル抗体としてポリクローナル抗体を含む血清を使用してもよいし、必要に応じこの血清からポリクローナル抗体を含む画分をさらに単離してもよい。
モノクローナル抗体を得るには、上記抗原を感作した哺乳動物の血清中に所望の抗体レベルが上昇するのを確認した後に、哺乳動物から免疫細胞を取り出し、細胞融合に付せばよい。この際、細胞融合に使用される好ましい免疫細胞として、特に脾細胞が挙げられる。前記免疫細胞と融合される他方の親細胞としては、好ましくは哺乳動物のミエローマ細胞が挙げられる。
前記免疫細胞とミエローマ細胞の細胞融合は基本的には公知の方法、例えば、ミルステインらの方法(Galfre,G.and Milstein,C.,Methods Enzymol.(1981)73,3−46)等に準じて行うことができる。
細胞融合により得られたハイブリドーマは、通常の選択培養液、例えばHAT培養液(ヒポキサンチン、アミノプテリンおよびチミジンを含む培養液)で培養することにより選択される。当該HAT培養液での培養は、目的とするハイブリドーマ以外の細胞(非融合細胞)が死滅するのに十分な時間、通常数日〜数週間継続する。ついで、通常の限界希釈法を実施し、目的とする抗体を産生するハイブリドーマのスクリーニングおよびクローニングが行われる。
また、ヒト以外の動物に抗原を免疫して上記ハイブリドーマを得る他に、ヒトリンパ球、例えばEBウイルスに感染したヒトリンパ球をin vitroでタンパク質、タンパク質発現細胞又はその溶解物で感作し、感作リンパ球をヒト由来の永久分裂能を有するミエローマ細胞、例えばU266と融合させ、タンパク質への結合活性を有する所望のヒト抗体を産生するハイブリドーマを得ることもできる(特開昭63−17688号公報)。
さらに、ヒト抗体遺伝子のレパートリーを有するトランスジェニック動物に抗原となるタンパク質、タンパク質発現細胞又はその溶解物を免疫して抗体産生細胞を取得し、これをミエローマ細胞と融合させたハイブリドーマを用いてタンパク質に対するヒト抗体を取得してもよい(国際公開92−03918号、国際公開93−2227号、国際公開94−02602号、国際公開94−25585号、国際公開96−33735号および国際公開96−34096号参照)。
ハイブリドーマを用いて抗体を産生する以外に、抗体を産生する感作リンパ球等の免疫細胞を癌遺伝子(oncogene)により不死化させた細胞を用いてもよい。
このように得られたモノクローナル抗体はまた、遺伝子組換え技術を用いて産生させた組換え型抗体として得ることができる(例えば、Borrebaeck,C.A.K.and Larrick,J.W.,THERAPEUTIC MONOCLONAL ANTIBODIES Published in the United Kingdom by MACMILLAN PUBLISHERS LTD,1990参照)。組換え型抗体は、それをコートするDNAをハイブリドーマ又は抗体を産生する感作リンパ球等の免疫細胞からクローニングし、適当なベクターに組み込んで、これを宿主に導入し産生させる。本発明は、この組換え型抗体を包含する。
本発明の抗体は、本発明のタンパク質に結合するかぎり、その抗体断片や抗体修飾物であってよい。例えば、抗体断片としては、Fab、F(ab’)2、Fv又はH鎖とL鎖のFvを適当なリンカーで連結させたシングルチェインFv(scFv)(Huston,J.S.et al.,Proc.Natl.Acad.Sci.U.S.A.(1988)85,5879−5883)が挙げられる。具体的には、抗体を酵素、例えば、パパイン、ペプシンで処理し抗体断片を生成させるか、又は、これら抗体断片をコードする遺伝子を構築し、これを発現ベクターに導入した後、適当な宿主細胞で発現させる(例えば、Co,M.S.et al.,J.Immunol.(1994)152,2968−2976;Better,M.and Horwitz,A.H.,MethodsEnzymol.(1989)178,476−496;Pluckthun,A.and Skerra,A.,Methods Enzymol.(1989)178,497−515;Lamoyi,E.,Methods Enzymol.(1986)121,652−663;Rousseaux,J.et al.,Methods Enzymol.(1986)121,663−669;Bird,R.E.and Walker,B.W.,Trends Biotechnol.(1991)9,132−137参照)。
抗体修飾物として、ポリエチレングリコール(PEG)等の各種分子と結合した抗体を使用することもできる。本発明における「抗体」にはこれらの抗体修飾物も包含される。このような抗体修飾物を得るには、得られた抗体に化学的な修飾を施すことによって得ることができる。これらの方法はこの分野において既に確立されている。
また、本発明の抗体は、公知の技術を使用して非ヒト抗体由来の可変領域とヒト抗体由来の定常領域からなるキメラ抗体又は非ヒト抗体由来のCDR(相補性決定領域)とヒト抗体由来のFR(フレームワーク領域)及び定常領域からなるヒト型化抗体として得ることができる。
前記のように得られた抗体は、均一にまで精製することができる。本発明で使用される抗体の分離、精製は通常のタンパク質で使用されている分離、精製方法を使用すればよく、何ら限定されるものではない。上記で得られた抗体の濃度測定は吸光度の測定又は酵素結合免疫吸着検定法(Enzyme−linked immunosorbentassay;ELISA)等により行うことができる。
また、本発明の抗体の抗原結合活性を測定する方法として、ELISA、EIA(酵素免疫測定法)、RIA(放射免疫測定法)あるいは蛍光抗体法を用いることができる。例えば、ELISAを用いる場合、本発明の抗体を同相化したプレートに本発明のタンパク質を添加し、次いで目的の抗体を含む試料、例えば、抗体産生細胞の培養上清や精製抗体を加える。酵素、例えばアルカリフォスファターゼ等で標識した抗体を認識するに次抗体を添加し、プレートをインキュベーション、洗浄した後、p−ニトロフェニル燐酸などの酵素基質を加えて吸光度を測定することで抗原結合活性を評価することができる。タンパク質としてタンパク質の断片、例えばそのC末端からなる断片あるいはN末端からなる断片を使用してもよい。本発明の抗体の活性評価には、BIAcore(Pharmacia製)を使用することができる。
これらの手法を用いることにより、本発明の抗体と試料中に含まれる本発明のタンパク質が含まれると予想される試料とを接触させ、前記抗体とタンパク質との免疫複合体を検出又は測定することからなる本発明のタンパク質の検出又は測定方法を実施することができる。本発明のタンパク質の検出又は測定方法は、タンパク質を特異的に検出又は測定することができるため、タンパク質を用いた種々の実験等に有用である。
また、本発明は、配列番号:1、3、5、7または9に示される塩基配列からなるDNA(その相補鎖を含む)と特異的にハイブリダイズし、少なくとも15塩基の鎖長を有するヌクレオチドを提供する。ここで「特異的にハイブリダイズする」とは、通常のハイブリダイゼーション条件下、好ましくは上記したストリンジェントなハイブリダイゼーション条件下で、他のタンパク質をコードするDNAとクロスハイブリダイゼーションが有意に生じないことを指す。このようなヌクレオチドは、本発明のタンパク質をコードするDNAを検出、単離するためのプローブとして、また増幅するためのプライマーとして利用可能である。特異的なハイブリダイゼーションのためのストリンジェンシーは、ハイブリダイズ反応の温度、反応時間、プローブ又はプライマー濃度、プローブ又はプライマーの長さ、塩強度などを考慮することにより、当業者であれば適宜選択することができる。
本発明のマウス「Tespec PRO−1」および「Tespec PRO−2」遺伝子は精巣に特異的に発現し、またマウスにおいて生後18日以降、生殖細胞に特異的に発現していると考えられる。このため、これらのDNAは生殖細胞のマーカー(検査薬)としても利用することが可能である。また、本発明の遺伝子は、精子の分化・成熟、および/または受精の成立を含む精子の機能に関与している可能性が考えられるため、これらDNAは、不妊症の検査に利用することも考えられる。
また、「配列番号:1、3、5、7または9に示される塩基配列からなるDNA(その相補鎖を含む)と特異的にハイブリダイズし、少なくとも15塩基の鎖長を有するヌクレオチド」には、例えばアンチセンスオリゴヌクレオチドやリボザイムも含まれる。アンチセンスオリゴヌクレオチドは、本発明のタンパク質の産生細胞に作用して、該タンパク質をコードするDNA 又はmRNAに結合することにより、その転写又は翻訳を阻害したり、mRNAの分解を促進したりして、本発明のタンパク質の発現を抑制することにより、結果的に本発明のタンパク質の作用を抑制する効果を有する。アンチセンスオリゴヌクレオチドとしては、例えば、配列番号:1、3、5、7または9に示される塩基配列中のいずれかの箇所にハイブリダイズするアンチセンスオリゴヌクレオチドを含む。アンチセンスオリゴヌクレオチドは、好ましくは配列番号:1、3、5、7または9に示される塩基配列中の連続する少なくとも15個以上のヌクレオチドに対するアンチセンスオリゴヌクレオチドである。さらに好ましくは、前記連続する少なくとも15個以上のヌクレオチドが翻訳開始コドンを含む、前記のアンチセンスオリゴヌクレオチドである。
アンチセンスオリゴヌクレオチドとしては、それらの誘導体や修飾体を使用することができる。このような修飾体として、例えばメチルホスホネート型又はエチルホスホネート型のような低級アルキルホスホネート修飾体、ホスホロチオエート修飾体又はホスホロアミデート修飾体等が挙げられる。
アンチセンスオリゴヌクレオチドとしては、DNA又はmRNAの所定の領域を構成するヌクレオチドに対応するヌクレオチドが全て相補的であるもののみならず、DNA又はmRNAとオリゴヌクレオチドとが配列番号:1、3、5、7または9に示される塩基配列に選択的に安定にハイブリダイズできる限り、1又は複数個のヌクレオチドのミスマッチが存在していてもよい。このようなオリゴヌクレオチドとしては、少なくとも15個の連続したヌクレオチド配列領域で、少なくとも70%、好ましくは少なくとも80%、より好ましくは90%、さらに好ましくは95%以上の塩基配列上の相同性を有するものを示す。なお、相同性を決定するためのアルゴリズムは、上記した文献に記載のアルゴリズムを使用すればよい。
本発明のアンチセンスオリゴヌクレオチドは、それらに対して不活性な適当な基剤と混和して塗布剤、パップ剤等の外用剤とすることができる。また、必要に応じて、賦形剤、等張化剤、溶解補助剤、安定化剤、防腐剤、無痛化剤等を加えて錠剤、散財、顆粒剤、カプセル剤、リポソームカプセル剤、注射剤、液剤、点鼻剤など、さらに凍結乾燥剤とすることができる。これらは常法にしたがって調製することができる。
本発明のアンチセンスオリゴヌクレオチド誘導体はin vivoでもin vitroでも適用できる。また、患者の患部に直接適用するか、又は血管内に投与するなどして結果的に患部に到達し得るように患者に適用してもよい。さらには、持続性、膜透過性を高めるアンチセンス封入素材を用いることもできる。例えば、リポソーム、ポリ−L−リジン、リピッド、コレステロール、リポフェクチン又はこれらの誘導体が挙げられる。
本発明のアンチセンスオリゴヌクレオチド誘導体の投与量は、患者の状態に応じて適宜調整し、好ましい量を用いることができる。例えば、0.1〜100mg/kg好ましくは0.1〜50mg/kgの範囲で投与することができる。
発明を実施するための最良の形態
次に、本発明を実施例によりさらに具体的に説明するが、本発明は下記実施例に限定されるものではない。
[実施例1]「Tespec PRO−1」遺伝子断片の単離
Mouse heart cDNA plasmid library(GIBCO社,5×109cfu/ml)から、5×104クローンからなるプラスミドを単離、精製し、これを鋳型として、本発明者らが「76A5sc2」と命名した遺伝子に由来する遺伝子特異的プライマー「76A5sc2−B」とベクタープライマー「SPORT RV」を用いて以下の様にPCRをおこなった。
SuperScript Mouse heart cDNA library及びSuperScript Mouse testis cDNA library(GIBCO社,5×109cfu/ml)を100倍に希釈したものを、16本の3ml LB−Amp培地に1μlずつ加え、30℃で培養したのちQIAspin mini prep kit(QIAGEN社)でプラスミドを得た(このプラスミドにはそれぞれ5×104の独立なクローンが存在する)。マウス心臓由来のプラスミドを鋳型とし、76A5sc2−B(配列番号:11/5’GAT CMA CAG GTG CCA GTC ATC A 3’)とSPORT SP6(配列番号:12/5’ATT TAG GTG ACA CTA TAG AA3’)のプライマーで、Ampli Taq Gold(Perkin Elmer社)をポリメラーゼとして用い、95℃12分の後、「96℃,20秒、55℃,20秒、72℃,2分」×40サイクル、続いて72℃3分の条件でPCRをおこなった。
PCR反応液を1.5%アガロースゲルで電気泳動を行い約0.7KbのPCR生成物を切り出し、QIAquick Gel Extraction Kit(QIAGEN社)でPCR生成物を回収した。このPCR生成物をpGEM T easy vector(PROMEGA社)にT4 DNA ligase(PROMEGA社)を用いてTAクローニングした。
出現したコロニーから8つを選択し、コロニーPCRにより挿入断片を以下のようにして増幅した。
SPORT FW(配列番号:13/5’TGT AAA ACG ACG GCC AGT 3’)、SPORT RV(配列番号:14/5’CAG GAA ACA GCT ATG ACC 3’)及びKOD dashポリメラーゼを含む20μlのPCR反応溶液に組み替え体を持つコロニーを直接懸濁し、94℃1分の後、「96℃ 15秒、55℃ 5秒、72℃ 25秒」を32サイクルの条件でPCRをおこなった。
増幅されたPCR生成物はアガロースゲル電気泳動で確認し、必要に応じてPCR生成物をMicrospin S−300あるいはS−400ゲルろ過(Pharmacia社)で精製した。
シークエンス反応のテンプレートとして、上記のコロニーPCRやRT−PCRなどのPCR産物を用いてシークエンスを行った。PCR反応後アガロースゲル電気泳動で生成物を確認し、夾雑物が混入している場合はアガロースゲルより目的PCR産物を切り出し、そうでない場合は上記のゲルろ過で精製した。シークエンス反応はDye Terminator Cycle Sequencing FS Ready Reaction Kit、dRhodamine Terminator Cycle Sequencing FS ready Reaction Kit、またはBigDye Terminator Cycle Sequencing FS ready Reaction Kit(Perkin−Elmer社)を用いたサイクルシークエンシングを行った。プライマーには、SPORT FWおよびSPORT RVを用いた。未反応のプライマー、ヌクレオチド等を96 well precipitation HL kit(AGTC社)で除去し、ABI 377あるいはABI 377XL DNA Sequencer(Perkin−Elmer社)で塩基配列を決定した。
その結果、7つは76A5sc2由来の塩基配列であったが、1つは(インサートサイズ約0.5Kb)異なる塩基配列を持っていた。そこでこの塩基配列をGCGのデータベースサーチで解析した。また、この塩基配列はORFが開いていたのでアミノ酸に翻訳し、アミノ酸配列もGCGのデータベースで解析した。その結果、この遺伝子断片は核酸及びアミノ酸レベルで多数の既知トリプシンファミリーセリンプロテアーゼ(trypsin family serine proteinase)と一部の領域で相同性を持っていることが判明した。しかしこの遺伝子断片の全領域において高い相同性を示す既知遺伝子はなく、新規な遺伝子であることが判明した。また、このアミノ酸配列はトリプシンファミリーセリンプロテアーゼモチーフである「Trypsin−His(PROSITE PS00134)」モチーフを有することが判明し、新規なプロテアーゼの断片であることが示唆された。
[実施例2][Tespec PRO−1」遺伝子の全長cDNAのクローニング
実施例1においてSuperScript Mouse heart cDNA libraryより得たプラスミドをテンプレートとし、実施例1で単離された遺伝子断片より新たにデザインしたNo9−C(配列番号:15/5’ATG CTT CTG CTA TCG TGG AAG G3’)とベクタープライマーSPORT FWあるいはSPORTT7(配列番号:16/5’TAA TAC GAC TCA CTA TAG GG3’)のプライマーセット、及び該遺伝子断片より新たにデザインしたNo9−B(配列番号:17/5’CTT TGT GCT GAG GTC TTC AGT G3’)とベクタープライマーSPORT RVのプライマーセットでAmpli Taq Goldをポリメラーゼとして用いてplasmid library BACEをおこなった。PCR反応は95℃12分の後、「96℃20秒、55℃20秒、72℃5分」×42サイクル、次いで72℃3分の条件でおこなった。
PCR反応液をアガロースゲルで電気泳動し、PCR産物の確認を行った。さらにこれらPCR産物について、直接またはpGEM T easy vectorにクローニングしたのち塩基配列を決定した。
3’RACEをおこなったところ、2つのPCRバンドが得られたのでその塩基配列を決定した。一方のバンドの塩基配列は他方のバンドの塩基配列の途中にpoly Aが付加したものであった。
一方、5’RACEの結果も同様に、PCR産物は長短2つのバンドを与えたので、それぞれのバンドをサブクローニングした後、塩基配列を決定した。その結果、この両者の3’側の塩基配列は同一であり、スプライシングアイソフォーム(splicing isoform)であることが判明した。
5’RACEで出現した短い方のバンドと、3’RACEの長い方のバンドの塩基配列をつなぎあわせることによりプロテアーゼをコードする塩基配列が得られたので、これを「Tespec PRO−1」(Testis specific expressed serine proteinase−1)と名付けた。
得られた「Tespec PRO−1」cDNAは1033塩基で、321アミノ酸をコードしていると予想される(図1)。その塩基配列を配列番号:1に、アミノ酸配列を配列番号:2に示す。アミノ酸配列にはN末端にシグナルペプチドと思われる疎水性アミノ酸領域が存在し、またC末端にも疎水性アミノ酸に富む領域が存在していた。このアミノ酸配列はGCGでの解析結果からトリプシンファミリーセリンプロテアーゼモチーフである「Trypsin−His(PROSITE PS00134)」および「Trypsin−Ser(PROSITE PS00135)」を持つことが判明した。PROSITEによれば、「あるタンパク質がセリンおよびヒスチジン活性化部位の両方を有している場合は、そのタンパク質がトリプシンファミリーセリンプロテアーゼである確率は100%である(”if a protein includes both the serine and histidine active site signatures,the probability of it being a trypsin famiy serine protease is 100%”)」とされている(S.Brenner,1988,Nature 334:528−530;N.D.Rawlings and A.J.Barrett,1994,Meth.Enzymol.244:19−61)ため、「Tespec PRO−1」はトリプシンファミリーセリンプロテアーゼであると考えられる。この遺伝子について塩基配列及びアミノ酸配列についてGCGのデータベースサーチをおこなった。その結果上述の2つのモチーフとその近傍ではアクロシンやプロスタシン、トリプシンなど既知のトリプシンファミリーセリンプロテアーゼと高い相同性を示し、またプロテアーゼ活性に必要なアスパラギン酸残基や、プロテアーゼ活性に必要と思われる分子内ジスルフィド結合に必要なシステインの位置も他のプロテアーゼと比較してよく保存されていた(図3)。しかしそれ以外の領域においては、核酸およびアミノ酸レベルで高い相同性を示す既知の遺伝子、タンパク質は存在せず、新規なトリプシンファミリーセリンプロテアーゼであることが判明した。
[実施例3]「Tespec PRO−2」遺伝子の全長cDNAのクローニング
実施例2において「Tespec PRO−1」のクローニングの際の5’RACEで取得できた分子量の大きいバンド(5’側で「Tespec PRO−1」ではない塩基配列を持つ)について、その塩基配列より新たに合成したプライマー(No9−GあるいはNo9−J)を用いて、実施例1に示したSuperScript Mouse testis cDNA libraryから得たプラスミドをテンプレートとし、更に3’及び5’RACEをおこなった。
具体的には、No9−G(配列番号:18/5’CAG TCA ATG TCA CTG TGG TCA T3’)とSPORT FW、及びNo9−J(配列番号:19/5’ACT TGC CGT TGG TGC CCA CTT C3’)とSPORT RVのプライマーセットでAmpli Taq Goldをポリメラーゼとして用い、95℃12分の後、「96℃ 20秒、55℃ 20秒、72℃ 5分」×42サイクル、次いで72℃3分の条件でPCRをおこなった。
PCR産物について、直接またはpGEM T easy vectorにクローニングしたのち塩基配列を決定した。
3’RACEをおこない、2つの3’RACE産物を得た。両者の塩基配列を決定したところ、両者とも5’側の塩基配列は同一であるが、3’側の塩基配列が異なっていた。一方は上述した「Tespec PRO−1」の塩基配列の途中にpoly Aが付加したものと同一であった。他方の3’側の塩基配列は「Tespec PRO−1」のものとは異なる配列を持っていた。
5’RACEをおこなうと、マルチバンドを与えたのでサブクローニングをした後、それらの塩基配列を決定した。その結果これらはすべて3’側の配列が共通であり、スプライシングアイソフォームであることが判明した。その内の1つは長いORFが開いており、この5’RACE産物と、先に述べた3’側の塩基配列が「Tespec PRO−1」のものとは異なる3’RACE産物をつなぎあわせることにより、プロテアーゼをコードすると思われる塩基配列が得られたので、これを「Tespec PRO−2」と名付けた。その塩基配列を配列番号:3に、アミノ酸配列を配列番号:4に示す。
得られた「Tespec PRO−2」cDNAは1034塩基で(図2)、5’非コード領域は68塩基であるのに対し3’非コード領域が9塩基と非常に短かく、またpoly AシグナルもGATAAAと一般のmRNA(AAUAAA)よりも弱いと思われる。このcDNAより「Tespec PRO−2」は319アミノ酸をコードすると予想され、そのアミノ酸配列はN末端にシグナルペプチドと思われる領域が存在するが、「Tespec PRO−1」とは異なりC末端には疎水性アミノ酸に富む領域は存在しない。またこのアミノ酸配列はトリプシンファミリーセリンプロテアーゼモチーフである「Trypsin−His」を持つが、「Trypsin−Ser」については12アミノ酸よりなるモチーフ([DNSTAGC]−[GSTAPIMVQH]−X−X−G−[DE]−S−G−[GS]−[SAPHV]−[LIVMFYWH]−[LIVMFYSTANQH])中、2アミノ酸がこのコンセンサスから外れている(GKCQGDSGAPMV)。しかし既知のトリプシンファミリーセリンプロテアーゼにおいても、コンセンサス配列から数アミノ酸異なった配列を持つものも存在するため、取得した「Tespec PRO−2」も、プロテアーゼとして機能するものと思われる。
「Tespec PRO−2」についても塩基配列及びアミノ酸配列について、GCGのデータベースサーチをおこなった。その結果、「TespecPRO−1」同様上述の2つのモチーフとその近傍では、既知のトリプシンファミリーセリンプロテアーゼと高い相同性を示し、またプロテアーゼ活性に必要なアスパラギン酸残基や、プロテアーゼ活性に必要と思われる分子内ジスルフィド結合に必要なシステインの位置も他のプロテアーゼと比較してよく保存されていたが(図3)、それ以外の領域においては、核酸およびアミノ酸レベルで高い相同性を示す既知の遺伝子、タンパク質は存在せず、新規なトリプシンファミリーセリンプロテアーゼであることが判明した。
[実施例4]「Tespec PRO−1」および「Tespec PRO−2」のスプライシングアイソフォーム
「Tespec PRO−1」と「Tespec PRO−2」の核酸及びアミノ酸レベルでの相同性はそれぞれ52.2%、33.1%であった。これらの値は他の既知トリプシンファミリーセリンプロテアーゼに対する相同性と同程度である。
実施例3の5’RACEで取得できた「Tespec PRO−2」のスプライシングアイソフォームは、スプライシングジャンクション部分や「Tespec PRO−2」では使用されない領域の塩基配列に終止コドンが現れ、長いORFを見出すことはできずプロテアーゼをコードしていないと考えられた。スプライシングアイソフォームを、RT−PCRを用いて以下の様により詳しく解析した。
cDNAクローニングによって得られた塩基配列を基に、No9−P(配列番号:20/5’GCA CTG GAA TGA CAA CAT GAT GC3’)、No9−Q(配列番号:21/5’ATT GGCGTG GCA AGT AGG AGC A3’)、No9−N(配列番号:22/5’CGA GTC TCC CAG TTA GCACAG A 3’)、No9−M’(配列番号:23/5’CGG TGA CTT GGT CAT GTC TGT G 3’)、No9−K(配列番号:24/5’GGA TCC ATG AAA CGA TGG AAG GAC AGA AG 3’)、No9−G、No9−J、No9−0(配列番号:25/5’CGC AGA GTT CTG CTC ATA CAT A 3’)の各プライマーを合成した。これらを用い、マウスの組織より調製したcDNAをテンプレートとして、Ampli Taq Goldをポリメラーゼとして、95℃12分の後、「96℃ 20秒、60℃ 20秒、72℃ 1分」を40サイクル、次いで72℃3分の条件でRT−PCRをおこなった。PCR反応液は1.5%Seakem GTGアガロース(TaKaRa社)で電気泳動を行った。
RT−PCRによる解析の結果(図4および5)、「Tespec PRO−2」のスプライシングアイソフォームのうち、5’側がBox2−I〜2−III〜2−VIというアイソフォームが主要であると思われ、「Tespec PRO−2」よりその存在は多いと思われる。また、Box2−Iを使用したアイソフォームとしては、Box2−VIを経てBox2−VIIあるいはBox1−IIへとつながっていくcDNA(後者は「Tespec PRO−1」とのキメラcDNAと思われる)がRT−PCRで確認できたが、Box2−IIHbを使用したアイソフォームとしては、Box2−VIを経てBox 1−IIへとつながっていく「Tespec PRO−1」とのキメラ型のcDNAのみが確認できた(図4および5)。このことは、「Tespec PRO−2」と「Tespec PRO−1」が染色体上で非常に接近しており、また「Tespec PRO−2」のpolyAシグナルが弱いために起きているものと思われる。また、このような一見無意味と思われるような(短いタンパク質しかコードできない)スプライシングアイソフォームが存在する意義は不明であるが、「Tespec PRO−2」の発現が転写時のみならずスプライシングによっても制御されている可能性も考えられる。
[実施例5]「Tespec PRO−1」及び「TespecPRO−2」遺伝子発現の組織分布
「Tespec PRO−1」と[Tespec PRO−2」の発現がどの組織で見られるかをRT−PCRで確認した。成体マウスの10種の組織(肝臓、脳、胸腺、心臓、肺、脾臓、精巣、子宮、腎臓、10〜11日目胎児)より単離した全RNA(Ambion社)をSuperScript II(GIBCO社)を逆転写酵素として用い、(dT)30VNプライマーでcDNA合成をしRT−PCRのテンプレートとした。また、QUICK−Clone cDNA mouse 7day embryo,17day embryo(CLONTECH社)もRT−PCRのテンプレートとして用いた。
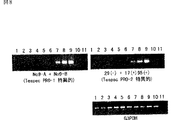
「Tespec PRO−1」特異的プライマーとしてNo9−A(配列番号:26/5’GGC ATG TAG CTC ACT GGC ATG 3’)とNo9−Bを、「Tespec PRO−2」特異的プライマーとして29(−)(配列番号:27/5’GGA CCA GCA AGA ATC AGT TCT G3’)と17(+)95(+)(配列番号:28/5’CTG CTA CCA GTT CTA ATT TGC C 3’)を用いた。G3PDHのコントロールプライマーとしてG3PDH5’(配列番号:29/5’GAG ATT GTT GCC ATC AAC GAC C3’)とG3PDH3’(配列番号:30/5’GTT GAA GTC GCA GGA GAC AAC C3’)を用いた。Ampli Taq Goldをポリメラーゼとして、95℃ 12分の後、「96℃ 20秒、60℃ 20秒、72℃ 30秒」×42サイクル(G3PDHの場合は28サイクル)、次いで72℃ 3分の条件でPCRをおこなった。PCR反応液は1.5%Seakem GTGアガロース(TaKaRa社)で電気泳動を行った。
その結果、「Tespec PRO−1」及び「Tespec PRO−2」の両者とも精巣で高い発現が確認された(図6)。興味深いことに、この遺伝子はマウス心臓cDNAプラスミドライブラリーよりクローニングしたにもかかわらず、心臓での発現はほとんどないことが判明した。また、精巣以外の組織においても、目的とする大きさのバンドが非常に弱いながらも観察された。
さらに、「Tespec PRO−1」のコーディング領域の一部(Box 1−IIを完全に含む領域、110〜401核酸残基)、及び「Tespec PRO−2」のexon2−VI付近(340〜723核酸残基)(「Tespec PRO−2」には多くのスプライシングアイソフォームが存在し、このプローブはそれらの共通領域であるので「Tespec PRO−2」特異的なプローブではなく、「Tespec PRO−2」及びそのスプライシングアイソフォームを認識するものである)をプローブとしてmouse MTN blot(CLONTECH社)による組織分布を解析した。
成体マウス精巣のcDNAをテンプレートとし、No9−AとNo9−Bのプライマーで増幅したRT−PCR生成物をMegaprime DNA labelling system(Amersherm社)を使用し[α−32P]dCTPでラベリングし、未反応の[α−32P]dCTPを除去したものを「Tespec PRO−1」プローブとした。同様にNo9−GとNo9−Jのプライマーで増幅した後、[α−32P]dCTPでラベリングしたものを[Tespec PRO−2」プローブとした。Mouse Multiple Tissue Northern(MTN)blotおよびMouse Embryo Multiple Tissue Northern(MTN)blot(CLONTECH社)を用い、ExpressHyb Hybridization Solution(CLONTECH社)中で、添付マニュアルの方法に従い、68℃でハイブリダイゼーションを行った。
「Tespec PRO−1」のプローブを用いたところ、精巣にのみ約1.2Kbのバンドが観察できた(図7)。また、精巣以外の組織や胎児期にはこのバンドは観察できなかった。「Tespec PRO−2」のプローブを用いたところ、「Tespec PRO−1」と同様に精巣にのみ約1.2Kbのバンドが観察でき(図7)、精巣以外の組織や胎児期ではバンドは観察できなかった。
以上の結果より「Tespec PRO−1」及び「Tespec PRO−2」の両者は精巣特異的な発現をしていることが判明した。
[実施例6]「Tespec PRO−1」及び「Tespec PRO−2」遺伝子の精巣での発現時期
マウスにおいて原始生殖細胞は受精後7日目の胎児において出現し、生殖巣への移動(受精後11日目)後、前精原細胞へと分化をする(受精後13日目)。この前精原細胞はそれ以降停止期に入るが、出生後生殖幹細胞である精原細胞として自己増殖と精子への分化を開始する。精原細胞から精母細胞、精子細胞を経て熟成した精子へと分化するのに約34日かかる(実際には精原細胞にも分化段階があるためそれを含めると約42日である)。そのため出生後のマウスの精巣を経日的に採取し、そこでの「Tespec PRO−1」及び「Tespec PRO−2」遺伝子の発現を確認することで、これらの遺伝子がどの分化段階の精子で発現しているか、あるいは精巣内の支持細胞(セルトリ細胞やラディッヒ細胞)で発現しているかが判明する。
一方、突然変異体のマウスとして第5染色体異常に起因するW(Witespotting)がある(P.Besmerら(1993)Dev.Suppl.,125−137)。これは精原細胞及び精母細胞に発現する受容体型チロシンキナーゼであるc−ki先に異常のある変異体で、これにより精巣内のセルトリ細胞やラディヒ細胞などの支持細胞は正常であるにもかかわらず、生殖細胞が欠損したり(完全変異型)、精原細胞以降の分化が不全となったり(不完全変異型)する。そこでこの変異体マウスW/Wvの精巣での「Tespec PRO−1」及び「Tespec PRO−2」の発現も確認した。
出生後4日、8日、12日、18日、42日のマウス精巣より単離した全RNA、及び生後56日目の異なる3匹のW/Wvマウス精巣より単離した全RNAを用いて作成したcDNAをテンプレートとしてRT−PCRをおこなった。このとき同時に成体マウスの精巣、肝臓由来のcDNAを用いたRT−PCRも実施した。プライマーは上記実施例5の「Tespec PRO−1」特異的プライマー、「Tespec PRO−2」特異的プライマーを使用し、40サイクル(G3PDHは29サイクル)のPCRを実施例5と同様に行った。
RT−PCRの結果、「Tespec PRO−1及び「Tespec PRO−2」は生後18日目以降の精巣で発現の上昇が見られたが、両遺伝子とも生後12日目以前及びW/Wv変異体マウスの精巣では発現が全く認められなかった(図8)。またネガティブコントロールとしておこなった肝臓においても、発現は確認できなかった。以上の結果は、「Tespec PRO−1」及び「Tespec PRO−2」の両者の発現が、セルトリ細胞やラディッヒ細胞のような支持細胞ではなく、生殖細胞が分化した精母細胞あるいは減数分裂後の精子細胞あたりから上昇していることを示唆する。
[実施例7]ヒト「Tespec PRO−2」全長cDNAのクローニング
マウス「Tespec PRO−2」の塩基配列を基にしてヒト「Tespec PRO−2」のクローニングをおこなった。ヒト精巣poly A+RNA(CLONTECH社)をSuperScript II(GIBCO社)を逆転写酵素として用い、(dT)30VNプライマーでcDNA合成をしRT−PCRのテンプレートとし、マウス「Tespec PRO−2」由来のNo9−GとNo9−QをプライマーとしてAmpliTaqGoldをポリメラーゼとして、95℃12分の後、「96℃ 20秒、55℃ 20秒、72℃ 30秒」×42サイクル、次いで72℃3分の低ストリンジェンシーの条件でPCRをおこなった。
その結果得られたRT−PCR産物について、直接塩基配列を決定した。その結果、このPCR産物はマウス「Tespec PRO−2」の塩基配列と約80%の相同性を持つ、ヒト「Tespec PRO−2」の遺伝子断片であることが判明した。この塩基配列を基に5’RACE用プライマーとしてh−B(配列番号:31/5’AGA GGT CAC TGT CGA GCT GGG3’)、h−D(配列番号:32/5’TGT GAA TAA TGA CCT TCT GCA C3’)を、3’RACE用プライマーとしてh−A(配列番号:33/5’TTC AGC AAC ATC CAC TCG GAG A 3’)、h−C(配列番号:34/5’AAG CAA GTG CAG AAG GTC ATT A 3’)を作成し、humantesitis Marathon ready cDNA(CLONTECH社)をテンプレートとして、添付マニュアルの方法に従いネスティド(nested)3’及び5’RACEを実施した。その結果、ヒト「Tespec PRO−2」の全長cDNAをクローニングすることに成功した。その塩基配列を配列番号:5に、アミノ酸配列を配列番号:6に示す。
ヒト「Tespec PRO−2」のcDNAは1035塩基で、265アミノ酸をコードしていると予想される(図9)。ヒト及びマウス「Tespec PRO−2」では、核酸及びアミノ酸レベルで互いにそれぞれ74.2%、69.8%の相同性を持つが、マウス「Tespec PRO−2」に比較してアミノ酸配列のC末端が54残基短く、それに伴い核酸配列の3’非コード領域が長くなっている(図10,11)。また、N末端にはシグナルペプチドと思われる領域が存在し、C末端領域も疎水性アミノ酸に富んでいる。ヒト「Tespec PRO−2」の予想されるアミノ酸配列には、トリプシンファミリーセリンプロテアーゼモチーフである「Trypsin−His」を持つ。更に「Trypsin−Ser」については12アミノ酸よりなるモチーフ([DNSTAGC]−[GSTAPIMVQH]−X−X−G−[DE]−S−G−[GS]−[SAPHV]−[LIVMFYWH]−[LIVMFYSTANQH])中、1アミノ酸(GIFKGDSGAPLV)がこのコンセンサスから外れている(マウス「Tespec PRO−2」では12アミノ酸モチーフ中2アミノ酸がコンセンサスから外れている)。
データベースサーチの結果、取得したヒト[Tespec PRO−2」は、核酸およびアミノ酸レベルで高い相同性を示す既知の遺伝子、タンパク質は存在せず、新規なトリプシンファミリーセリンプロテアーゼであることが判明した。
[実施例8]ヒト「Tespec PRO−2」の染色体マッピング
ヒト染色体パネル(CORRIELL CELL REPOSITORIES社製)をテンプレートとし、h−Aとh−F(配列番号:35/5’CAT TGG TCG TTA CCC ACT GTG C 3’)のプライマーで、Advantage cDNA polymerase(CLONTECH社)をポリメラーゼとして、95℃ 1分の後、「96℃ 15秒、60℃ 15秒、68℃ 30秒」×37サイクル、次いで68℃ 3分の条件でPCRをおこなった。PCR反応液は1.5%Seakem GTGアガロース(TaKaRa)で電気泳動を行った。
電気泳動の結果を基に染色体マッピングを行った結果、ヒト「Tespec PRO−2」は第8染色体上に存在することが判明した(図12)。
[実施例9]ヒト「Tespec PRO−3」遺伝子の全長cDNAクローニング
ヒト精巣poly A+RNA(CLONTECH社)をSuperScript II(GIBCO社)を逆転写酵素として用い、(dT)30VNプライマーでcDNA合成をしRT−PCRのテンプレートとし、マウス「Tespec PRO−1」由来の塩基配列より合成したPRO1−E(配列番号:36/5’ATT CTC AAT GAG TGG TGG GTT CT 3’)とPRO1−D(配列番号:37/5’CCA GCACAC AGC ATA TTC TTG G 3’)をプライマーとして用い、AmpliTaqGoldをポリメラーゼとして、95℃ 12分の後、「96℃ 20秒、50℃ 20秒、72℃ 45秒」×5サイクル、次いで「96℃ 20秒、60℃ 20秒、72℃ 45秒」×35サイクル、次いで72℃ 3分の低ストリンジェンシーの条件でPCRをおこなった。
その結果得られたRT−PCR産物をゲルろ過後、塩基配列を決定したところ、トリプシンファミリーセリンプロテアーゼをコードする遺伝子断片であることが判明した。この遺伝子断片をアミノ酸に翻訳するとそのアミノ酸配列には「Trypsin−His」のモチーフが含まれていた。この遺伝子断片の塩基配列のデータベースサーチをおこなったところ、ヒト EST(AA781356、aj25c04.s1 Soares−testis−NHT Homo sapiens cDNA clone 1391334 3’,mRNA sequence.)と一部重なり合うことが判明した。このESTをアミノ酸に翻訳すると「Trypsin−Ser」モチーフが存在した。そこで得られた遺伝子断片の塩基配列を基に、5’RACE用プライマーとしてhPRO3−B(配列番号:38/5’GGA AAC AGC TCC TCG GAA TAT AAG C 3’)およびhPRO3−D(配列番号:39/5’TGG ATG GGC TAG TTA AGT CGT TGG T 3’)を、3’RACE用プライマーとしてhPRO3−A(配列番号:40/5’TTC GAG GGA AGA ACT CGG TAT TC 3’)およびhPRO3−C(配列番号:41/5’TGT GAA AAC GGA TCT GAT GAA AGC G 3’)を作製し、human testis Marathon ready cDNA(CLONTECH社)をテンプレートとして、添付のマニュアルの方法に従いnested RACEを実施し、全長cDNAのクローニングをおこなった。RACE産物を直接またはpGEM T easy vectorにサブクローニングしてその塩基配列を決定した。その塩基配列を配列番号:9に、アミノ酸配列を配列番号:10に示す。
この新規ヒト遺伝子は、マウス「Tespec PRO−1」の塩基配列より合成したプライマーを用いて得られたにもかかわらず、マウス「Tespec PRO−1」よりもデータベース中のマウス精巣(mouse testis)EST(AA497965、AA497934、AA497919等)に、より相同性が高かった(図14)。そこで、この遺伝子をヒト「Tespec PRO−3」と名付けた。
ヒト「Tespec PRO−3」のcDNAは1123塩基で、352アミノ酸をコードしていると予想される(図13)。N末端にはシグナルペプチドと思われる配列が存在し、「Trypsin His」及び「Trypsin−Ser」モチーフを有していた。また分子内ジスルフィド結合をしていると思われるCys残基も他のセリンプロテアーゼと比較してよく保存されていた。
[実施例10]マウス「Tespec PRO−3」遺伝子の全長cDNAクローニング
上述したヒト「Tespec PRO−3」のマウスカウンターパートであるマウス「Tespec PRO−3」は、上述の数個のマウス精巣ESTの塩基配列を含む遺伝子であると思われる。この遺伝子のマウスESTは合計8つデータベースに登録されており、4つは精巣由来、1つは腎臓由来、残りの3つは組織不明のcDNA由来であった。そこでこれらのESTからプライマーを作成し、mouse testis Marathon ready cDNAをテンプレートとしたRACEをおこない、マウス「Tespec PRO−3」の全長cDNA配列のクローニングをおこなった。
マウスEST(AA497965,AA497934,AA497919,AA497949,AA271404,AA238183,AA240375,AA105229)の塩基配列を基に、5’RACE用プライマーとしてmPRO3−B(配列番号:42/5’CAC CTA CTG CCA GGA TCT GTG G 3’)及びmPRO3−D(配列番号:43/5’GGC TAT TTT CTC AAT CCA CAG GGT A 3’)を、3’RACE用プライマーとしてmPRO3−A(配列番号:44/5’ATA GAG TGG GAG GAA TGC TTA CAG A 3’)及びmPRO3−C(配列番号:45/5’GCT ACG ATG CTT GCC AGG GTG 3’)を作成し、mouse testis Marathon ready cDNA(CLONTECH)をテンプレートとして、添付マニュアルの方法に従いnested RACEを実施した。RACE産物を直接またはpGEM Teasy vectorにサブクローニングしてその塩基配列を決定した。その塩基配列を配列番号:7に、アミノ酸配列を配列番号:8に示す。
得られたマウス「Tespec PRO−3」のcDNAは1028塩基で、321アミノ酸をコードしていると思われる(図15)。予想されるアミノ酸配列は、「Trypsin−Ser」モチーフは持つが「Trypsin His」モチーフは6アミノ酸のコンセンサス[LIVM]−[ST]−A−[STAG]−H−Cから1アミノ酸異なる(LTVAHC)。しかしマウス「Tespec PRO−2」同様、既知のトリプシンファミリーセリンプロテアーゼにおいても、コンセンサス配列から数アミノ酸異なった配列を持つものも存在するため、得られたマウス「Tespec PRO−3」もプロテアーゼとして機能するものと考えられる。また、N末端にはシグナルペプチドと思われる疎水性領域が存在し、また分子内ジスルフィド結合をしていると思われるCys残基も他のセリンプロテアーゼと比較してよく保存されていた。
ヒト及びマウス「Tespec PRO−3」は、核酸及びアミノ酸レベルでそれぞれ70.2%、および59.6%の相同性を持つ(図16、17)。ヒト「Tespec PRO−3」に比べてマウス「Tespec PRO−3」は、核酸レベルにおいて5’側が約100塩基短く、またアミノ酸レベルにおいてもN末端側が約30アミノ酸短いことが判明した。
産業上の利用の可能性
本発明により、新規トリプシンファミリーセリンプロテアーゼおよびその遺伝子が提供された。本発明のタンパク質は、精子の分化・熟成または精子の機能(受精)に関与していることを示唆される。したがって、本発明のプロテアーゼやその遺伝子は、新しい不妊症の治療薬や不妊症診断薬の開発、あるいは新しい避妊薬の開発への利用が期待される。
【図面の簡単な説明】
図1は、マウス「Tespec PRO−1」のcDNA配列およびアミノ酸配列を示す図である。トリプシンファミリーセリンプロテアーゼ活性部位を下線で示した。また、ポリAシグナルを波線で示した。
図2は、マウス「Tespec PRO−2」のcDNA配列およびアミノ酸配列を示す図である。トリプシンファミリーセリンプロテアーゼ活性部位を下線で示した。また、ポリAシグナルを波線で示した。
図3は、マウス「Tespec PRO−1」、「Tespec PRO−2」および既知のプロテアーゼのアミノ酸配列のアラインメントを示す図である。全てで一致するアミノ酸は「*」で、類似するアミノ酸は「・」で表した。またトリプシンファミリーセリンプロテアーゼ活性部位を枠で囲んで示した。
図4は、マウス精巣のRT−PCRによる「Tespec PRO−1」、「Tespec PRO−2」cDNAの増幅結果を表す図である。上段に使用したプライマーの位置を、下段にRT−PCRによる増幅産物の電気泳動の図を示す。
図5は、マウス「Tespec PRO−1」、「Tespec PRO−2」およびそれらのスプライシングアイソフォームの構造を表す模式図である。長方形の下の数字は塩基数を示す。
図6は、RT−PCRによるマウス「Tespec PRO−1」、「Tespec PRO−2」の組織での発現を表す図である。上段に使用したプライマーの位置を、下段にRT−PCRによる増幅産物の電気泳動の図を示す。1;肝臓、2;脳、3;胸腺、4;心臓、5;肺、6;脾臓、7;精巣、8;卵巣、9;腎臓、10;10〜11日目胎児、11;蒸留水(対照)。
図7は、ノーザンブロットによるマウス「Tespec PRO−1」、「Tespec PRO−2」の組織での発現を表す図である。上段に使用したプローブの位置を、下段にノーザンブロットの結果を示す。1;7日胚、2;11日胚、3;15日胚、4;17日胚、5;心臓、6;脳、7;脾臓、8;肺、9;肝臓、10;骨格筋、11;腎臓、12;精巣。
図8は、RT−PCR解析によるマウス「Tespec PRO−1」、「Tespec PRO−2」の精巣での発現時期を示す図である。1;W/Wv No.1精巣、2;W/Wv No.2精巣、3;W/Wv No.3精巣、4;生後4日精巣、5;生後8日精巣、6;生後12日精巣、7;生後18日精巣、8;生後42日精巣、9;成体精巣、10;成体肝臓、11;蒸留水(対照)。
図9は、ヒト「Tespec PRO−2」のcDNA配列およびアミノ酸配列を示す図である。トリプシンファミリーセリンプロテアーゼ活性部位を下線で示した。また、ポリAシグナルを波線で示した。
図10は、マウスおよびヒト「Tespec PRO−2」の塩基配列の比較を示す図である。2つで一致する塩基は枠で囲んだ。
図11は、マウスおよびヒト「Tespec PRO−2」のアミノ酸配列の比較を示す図である。2つで一致するアミノ酸は「*」で、類似するアミノ酸は「・」で示した。また、トリプシンファミリーセリンプロテアーゼ活性部位を枠で囲んだ。
図12は、ヒト「Tespec PRO−2」の染色体マッピングのためのPCRの結果を示す図である。
図13は、ヒト「Tespec PRO−3」のcDNA配列およびアミノ酸配列を示す図である。トリプシンファミリーセリンプロテアーゼ活性部位を下線で示した。また、ポリAシグナルを波線で示した。
図14は、「Tespec PRO−1」および「Tespec PRO−3」の塩基配列の相同性の比較を表す図である。なお、塩基配列の相同性は、マウス「Tespec PRO−1」においては全長塩基配列、マウス「Tespec PRO−3」においては約400bPのEST領域、ヒト「Tespec PRO−3」においては実施例9に記載の低ストリンジェンシーRT−PCRで取得した約200bpの領域を比較した。
図15は、マウス「Tespec PRO−3」のcDNA配列およびアミノ酸配列を示す図である。トリプシンファミリーセリンプロテアーゼ活性部位を下線で示した。また、ポリAシグナルを波線で示した。
図16は、マウス「Tespec PRO−3」(m.Tespec PRO−3)およびヒト「Tespec PRO−3」(h.Tespec PRO−3)の塩基配列の比較を示す図である。2つで一致する塩基は枠で囲んだ。
図17は、マウス「Tespec PRO−3」(m.Tespec PRO−3)およびヒト「Tespec PRO−3」(h.Tespec PRO−3)のアミノ酸配列の比較を示す図である。2つで一致するアミノ酸残基は枠で囲んだ。
Claims (9)
- 配列番号:4または6に記載のアミノ酸配列からなるタンパク質。
- トリプシンファミリーセリンプロテアーゼ活性を有する、下記(a)または(b)に記載のタンパク質。
(a) 配列番号:4または6に記載のアミノ酸配列において1若しくは10個以下のアミノ酸が欠失、付加、挿入および/または他のアミノ酸による置換により修飾されたアミノ酸配列からなるタンパク質。
(b) 配列番号:3または5に記載の塩基配列からなるDNAとストリンジェントな条件下でハイブリダイズするDNAがコードするタンパク質。 - 請求項1または2に記載のタンパク質をコードするDNA。
- 請求項3に記載のDNAが挿入されたベクター。
- 請求項3に記載のDNAを発現可能に保持する形質転換体。
- 請求項5に記載の形質転換体を培養し、該形質転換体またはその培養上清から発現させたタンパク質を回収する工程を含む、請求項1または2に記載のタンパク質の製造方法。
- 請求項1または2に記載のタンパク質の基質をスクリーニングする方法であって、
(a)該タンパク質に被検試料を接触させる工程、
(b)該タンパク質の被検試料に対するプロテアーゼ活性を検出する工程、および
(c)該プロテアーゼ活性により分解または切断を受ける化合物を選択する工程、を含む方法。 - 請求項1または2に記載のタンパク質に結合する抗体。
- 請求項8に記載の抗体と、請求項1または2に記載のタンパク質が含まれると予想される試料とを接触させ、該抗体と該タンパク質との免疫複合体の生成を検出又は測定することを含んでなる、該タンパク質を検出又は測定する方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP31336698 | 1998-11-04 | ||
| PCT/JP1999/006111 WO2000026352A1 (fr) | 1998-11-04 | 1999-11-02 | Nouvelles serine proteases de la famille de la trypsine |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009205741A Division JP5058227B2 (ja) | 1998-11-04 | 2009-09-07 | 新規トリプシンファミリーセリンプロテアーゼ |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP4441121B2 true JP4441121B2 (ja) | 2010-03-31 |
Family
ID=18040401
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000579724A Expired - Fee Related JP4441121B2 (ja) | 1998-11-04 | 1999-11-02 | 新規トリプシンファミリーセリンプロテアーゼ |
| JP2009205741A Expired - Fee Related JP5058227B2 (ja) | 1998-11-04 | 2009-09-07 | 新規トリプシンファミリーセリンプロテアーゼ |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009205741A Expired - Fee Related JP5058227B2 (ja) | 1998-11-04 | 2009-09-07 | 新規トリプシンファミリーセリンプロテアーゼ |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20090035799A1 (ja) |
| EP (3) | EP1136548A4 (ja) |
| JP (2) | JP4441121B2 (ja) |
| AT (2) | ATE518950T1 (ja) |
| AU (1) | AU6369399A (ja) |
| WO (1) | WO2000026352A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2826022B1 (fr) * | 2001-06-13 | 2005-02-04 | Centre Nat Rech Scient | Procede de determination de l'existence de melanges d'especes d'origines animales ou vegetales dans des substrats organiques |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0239102A3 (en) | 1986-03-28 | 1989-07-12 | Tsuji, Kimiyoshi | Process for the formation of human-human hybridoma |
| WO1994025585A1 (en) | 1993-04-26 | 1994-11-10 | Genpharm International, Inc. | Transgenic non-human animals capable of producing heterologous antibodies |
| EP0814159B1 (en) | 1990-08-29 | 2005-07-27 | GenPharm International, Inc. | Transgenic mice capable of producing heterologous antibodies |
| WO1993002227A1 (en) | 1991-07-15 | 1993-02-04 | Eco-Tec Limited | Process and apparatus for treating fluoride containing acid solutions |
| EP0652950B1 (en) | 1992-07-24 | 2007-12-19 | Amgen Fremont Inc. | Generation of xenogeneic antibodies |
| JPH08205893A (ja) * | 1994-12-08 | 1996-08-13 | Sumitomo Metal Ind Ltd | Hcvプロテアーゼ活性測定法 |
| ATE390933T1 (de) | 1995-04-27 | 2008-04-15 | Amgen Fremont Inc | Aus immunisierten xenomäusen stammende menschliche antikörper gegen il-8 |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| WO1998036054A1 (en) * | 1997-02-13 | 1998-08-20 | Amrad Operations Pty. Ltd. | Novel molecules |
| JP2002505252A (ja) * | 1997-11-20 | 2002-02-19 | ノボ ノルディスク アクティーゼルスカブ | 哺乳類細胞のアポトーシスの調整又は予防のためへのヘパリン−結合タンパク質の使用 |
-
1999
- 1999-11-02 EP EP99951213A patent/EP1136548A4/en not_active Withdrawn
- 1999-11-02 EP EP07023493A patent/EP1895002B1/en not_active Expired - Lifetime
- 1999-11-02 EP EP07023492A patent/EP1895001B1/en not_active Expired - Lifetime
- 1999-11-02 WO PCT/JP1999/006111 patent/WO2000026352A1/ja active Application Filing
- 1999-11-02 AU AU63693/99A patent/AU6369399A/en not_active Abandoned
- 1999-11-02 AT AT07023493T patent/ATE518950T1/de not_active IP Right Cessation
- 1999-11-02 AT AT07023492T patent/ATE518949T1/de not_active IP Right Cessation
- 1999-11-02 JP JP2000579724A patent/JP4441121B2/ja not_active Expired - Fee Related
-
2008
- 2008-09-08 US US12/206,511 patent/US20090035799A1/en not_active Abandoned
-
2009
- 2009-09-07 JP JP2009205741A patent/JP5058227B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| EP1895001B1 (en) | 2011-08-03 |
| EP1136548A4 (en) | 2002-09-25 |
| EP1895002B1 (en) | 2011-08-03 |
| EP1136548A1 (en) | 2001-09-26 |
| EP1895002A1 (en) | 2008-03-05 |
| ATE518950T1 (de) | 2011-08-15 |
| AU6369399A (en) | 2000-05-22 |
| WO2000026352A1 (fr) | 2000-05-11 |
| JP5058227B2 (ja) | 2012-10-24 |
| JP2010011861A (ja) | 2010-01-21 |
| ATE518949T1 (de) | 2011-08-15 |
| US20090035799A1 (en) | 2009-02-05 |
| EP1895001A1 (en) | 2008-03-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2020036596A (ja) | 新規ヘモポエチン受容体蛋白質、nr10 | |
| WO2001023556A1 (fr) | Nouvelle proteine receptrice d'hemopoietine (nr12) | |
| WO2006073052A1 (ja) | 新規血管新生抑制因子 | |
| US7829083B2 (en) | Antibodies to brain specific membrane protein | |
| WO2001009345A1 (fr) | Nouveaux genes codant des proteines kinase et des proteines phosphatase | |
| JP4838961B2 (ja) | トランスポーター遺伝子oatp−b、c、d、およびe | |
| JP5058227B2 (ja) | 新規トリプシンファミリーセリンプロテアーゼ | |
| US20050164280A1 (en) | TSG-like gene | |
| WO2002020770A1 (fr) | Methode de criblage d'un agent antitumoral a l'aide d'une interaction entre une proteine arf et une proteine hk33 | |
| EP1120426A1 (en) | Novel g protein-coupled receptors | |
| JP4590107B2 (ja) | 新規胎児性遺伝子 | |
| US7794973B2 (en) | YS68 gene involved in primitive hematopoiesis | |
| JP2008099690A (ja) | 新規ヘモポエチン受容体蛋白質、nr12 | |
| US7067297B2 (en) | Mannosyltransferase polypeptides and polynucleotides encoding them and methods for making and using them | |
| JP4942904B2 (ja) | zincフィンガードメインを有する新規転写因子 | |
| WO2001014551A1 (fr) | NOUVEAU GENE DEC2 DE FACTEUR DE TRANSCRIPTION DE TYPE bHLH | |
| JP2002000279A (ja) | 初期造血に関わるys68遺伝子 | |
| JP2004267003A (ja) | ヒト白血球型抗原領域に存在する新規遺伝子 | |
| WO2000031255A1 (fr) | Nouvelle proteine semblable a l'ubiquitine | |
| WO2001083738A1 (fr) | Facteur de regulation de differenciation et de determination du sexe |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061026 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20061026 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090709 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090907 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091014 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091130 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20091221 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100108 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130115 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130115 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130115 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140115 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |