JP4201253B2 - 薬学的活性物質に潜在性を提供する方法 - Google Patents
薬学的活性物質に潜在性を提供する方法 Download PDFInfo
- Publication number
- JP4201253B2 JP4201253B2 JP2002555832A JP2002555832A JP4201253B2 JP 4201253 B2 JP4201253 B2 JP 4201253B2 JP 2002555832 A JP2002555832 A JP 2002555832A JP 2002555832 A JP2002555832 A JP 2002555832A JP 4201253 B2 JP4201253 B2 JP 4201253B2
- Authority
- JP
- Japan
- Prior art keywords
- lap
- nucleic acid
- fusion protein
- mmp
- protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1841—Transforming growth factor [TGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/495—Transforming growth factor [TGF]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/555—Interferons [IFN]
- C07K14/565—IFN-beta
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/50—Fusion polypeptide containing protease site
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/70—Fusion polypeptide containing domain for protein-protein interaction
- C07K2319/74—Fusion polypeptide containing domain for protein-protein interaction containing a fusion for binding to a cell surface receptor
- C07K2319/75—Fusion polypeptide containing domain for protein-protein interaction containing a fusion for binding to a cell surface receptor containing a fusion for activation of a cell surface receptor, e.g. thrombopoeitin, NPY and other peptide hormones
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Engineering & Computer Science (AREA)
- Toxicology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
方法
pcDNA3のEcoRI-NotI部位へのGS-MMP-GSリンカーのクローニング
GS-MMP-GSリンカーをEcoRI-NotI切断pCDNA3に挿入することによってベクターを構築した。pcDNAは、ヒトサイトメガロウイルス前初期プロモーターおよびエンハンサーを、転写を可能にするRNAプロセシングシグナルと共に含む発現ベクター(インビトロジェン(Invitrogen)社)である。
LAP(TGFβ)の次にGS-MMP-GSおよび成熟IFNβを含むベクターは以下のように構築した:
HindIIIおよびEcoRI末端を有する5'単位(シグナルペプチドを有する)としてのTGFβからのLAPを、プラスミドTGFβ-Babe neoからPCRによってクローニングした(Chernajovskyら、Gene Ther. 4、553〜559(1997))。以下のプライマーを用いた:
センスプライマー
アンチセンスプライマー
センスプライマー
アンチセンスプライマー
成熟mIFNβの後にGS-MMP-GSとLAP(TGFβ)とを続いて含むベクターを以下のように構築した:
シグナルペプチドを有し、停止コドンを有しないプレ-IFNβを以下のプライマーを用いて上記のようにPCRによって合成した:
センスプライマー
アンチセンスプライマー
センスプライマー
アンチセンスプライマー
プラスミドpPK14として、システインがセリン(223/225)に変異している変異ブタcDNA(Sandersonら、Proc. Natl. Acad. Sci. USA 92、2572〜2576(1995))は、メリーランド州ベセスダのNIHのP. J. Wirth氏から供与された。ブタLAPのクローニングは、以下のプライマーの組を用いてPCRによって行った:
シグナルペプチドで始まるセンスプライマーは
であった。このプライマーは、NcoI部位を作製するために開始ATG周辺で改変された配列を有する。
アンチセンスプライマー
構造に関する検討
二つのコンフォメーションのTGFβ融合蛋白質のLAPドメインを用いて潜在型サイトカインを開発するために、マウスIFNβのアミノ末端にLAPを含む潜在型サイトカイン(図1を参照のこと)と、COOH末端にLAPを含む潜在型サイトカイン(図2を参照のこと)とを構築した。
方法
DHFR欠損チャイニーズハムスター卵巣(CHO)細胞へのトランスフェクション
ジヒドロ葉酸レダクターゼ(DHFR)-欠損CHO細胞は、10%ウシ胎児血清(FBS)(ライフテクノロジーズ社)、ペニシリン/ストレプトマイシン、およびグルタミンを含むHAM-F12培地(ライフテクノロジーズ社、ペイスリー、イギリス)において維持した。
マウスIFNβ生物アッセイ法は、記述のように(Triantaphyllopoulosら、Gene Ther. 5、253〜263(1998))細胞上清の二倍希釈を用いて、マウスLTK-細胞におけるEMCウイルス(ロンドン、王立癌研究基金のI. Kerr氏の提供)感染症の細胞変性作用の阻害によって評価した。指示されている場合、血清不含CHO上清は、分子量カットオフ30,000 kDaのVivaspinフィルター(ザルトリウス(Sartorious)、ゲッチンゲン、ドイツ)を用いて遠心によって濃縮した。
永続的にトランスフェクトした細胞、または非トランスフェクトCHO細胞のコンフルエントプレートを、10%透析FBSを含み、チミジン、グルタミン、ペニシリン/ストレプトマイシンおよび150 μg/mlL-プロリンを添加したシステイン-メチオニン不含培地(ライフテクノロジーズ社)によって洗浄した。標識は、1 Ci/mmolの35S-メチオニン-システインミクス(アマシャム-ファルマシアバイオテック(Amersham-Pharmacia Biotech)、バックス、イギリス)の存在下で、培地5 mlにおいて250 mCi/プレートを用いて一晩または48時間のいずれかで行った。
代謝的に標識した細胞からの上清を、0.1%NP40(50%ビーズ/容積)(BDH、プール、イギリス)を含むPBS中で平衡にしたプロテイン-G-セファロース(アマシャム-ファルマシアバイオテック社)によって予めきれいにした。トリクロロ酢酸(TCA)(シグマ社)総沈殿蛋白質25×106 cpmを含む上清を用いた(細胞上清の約5〜7ml)。4℃で4時間十分に混合した後、プロテイン-G-セファロースを遠心(2000 rpm、5分)によって除去した。澄んだ上清をヤギ抗ヒト-LAP抗体(R&Dシステムズ、オキソン、イギリス、0.9 μg/ml)またはモノクローナルラット抗mIFNβ(7F-D3、AMS、アビンドン、イギリス;250倍希釈)のいずれかと共に4℃で3〜4時間インキュベートした。
組換え型プロMMP9(デトロイト、ウェイン大学のR. Fridman氏からの提供)または活性なMMP1およびMMP3(ロンドンのケネディリウマチインスチチュートのH. Nagase博士からの提供)を、CHO細胞からの免疫沈降した上清と共に、20 mMトリスHCl、pH 7.4、5 mM CaCl2、140 mM NaCl、および0.1%Brij35(全てシグマ社)50 μlにおいて1μg/mlで37℃で一晩インキュベートするか、または細胞上清に直接加えた(4μg/mlで)。特定の実験では、10μM酢酸アミノフェニル水銀(APMA)(シグマ社)を用いてプロ-MMP9を37℃で一晩活性化した(Ogataら、J. Biol. Chem.、270:18506〜18511(1995))。
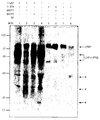
永続的にトランスフェクトされた細胞からの分泌蛋白質を、35S-メチオニンおよびシステインによって代謝的に標識した。LAP-mIFNβおよびmIFNβ-LAP標識蛋白質はいずれも、非還元状態において97 kDa以上の2個の主なバンドを示したが、これはCHO非トランスフェクト細胞からの上清では認められなかった(図6)。
免疫沈降複合体を単一のMMPまたはその組み合わせによって一晩処置した。図7に示すように、プロ-MMP9またはMMP1は、57 kDa組換え型産物をあまり効率的に切断しなかった。MMP1は、融合蛋白質のグリコシル化型を切断することができるが(図7、レーン3および4;図8A、レーン2)、MMP3は、それだけでグリコシル化型をいくつかの個別のバンドに消化することができた(図7、レーン5および6;図8Aおよび8B、レーン3および7)。
図8および表3は、リウマチ性関節炎患者からの滑液が潜在型サイトカインを活性化できることを示した。
LAP-mIFNβによって検出される潜在性が二量体ジスルフィド結合LAPによって結合された推定の閉鎖外皮状構造の形成を必要とするか否かを評価するために、223位および225位のシステインがセリンに変異しているブタLAPを用いて融合蛋白質を構築した。
構築物の調製
ブタLAPは、実施例1に説明したPCRによってクローニングした。用いたプライマーは、実施例において説明した通りであった(ブタLAPのクローニング)。クローニングしたブタLAPは、223位および225位のシステインがセリンに変異していた(Sandersonら、Proc. Natl. Acad. Science、92、2572〜2576(1995))。
プラスミドDNA、PorcLAP-mIFNβ、mIFNβ-LAPおよびLAP-mIFNβ対照20μgを、燐酸カルシウム共沈殿法によって上記のように9cmプレートに播種したCOS-7細胞0.5×106個に1試料あたり2個ずつトランスフェクトさせた。DNA共沈殿物は、4時間ではなくて一晩細胞上に残っていた。COS-7細胞は抗生物質および10%FBSを含むDMEMにおいて増殖させた。グリセロールショックの48時間後、上清をIFN抗ウイルスアッセイ法のために採取した。
変異構築物PorcLAP-mIFNβを、COS-7細胞への一過性のトランスフェクション後、インビトロでのその生物活性に関して他の構築物と比較した。表4は、以下を示すこのアッセイ法において、PorcLAP-mIFNβがmIFNβ-LAPと同程度に活性であることを示している。
結果は、223位と225位でのジスルフィド結合がLAP-mIFNβの潜在性にとって必要であることを示している。
ヒトIFNβ、IL-2、およびIL-10-LAP融合蛋白質のクローニングおよび発現
ヒトIFNβ-MMP-LAPおよびLAP-MMP-ヒトIFNβの構築は、CHO細胞株におけるこれらの構築物の発現の試験、ならびにインビトロおよびインビボでのいくつかのヒト細胞株による発現産物の活性のその後の試験を容易にするであろう。
方法
マウスIFNβ遺伝子(実施例1を参照のこと)の場合と同様に、以下のプライマーを用いて、ヒトIFN遺伝子をMMP部位(LAP後)のCOOH末端のNotI/XbaI部位でクローニングすると、分子OM52(LAP-huIFNβ)が得られた:
センスプライマー
アンチセンスプライマー
このデータは、LAP-MMPに融合したヒトIFNβが、LAP-MMPペプチドに融合したマウス蛋白質とは異なる挙動を示すことから、融合蛋白質の潜在性は予測できないことを示している。マウス配列の場合、LAP-MMP-IFNβコンフォメーションは潜在型であったが、ヒト(OM52)の場合この構築物は活性であり、その逆も同じであり、すなわちマウスIFN-LAPコンフォメーションは活性であるのに対し、ヒト(OM53)は不活性であった。
コラーゲン誘発関節炎(CIA)とDNA注射
DBA/1マウスを、Drejaら、Arthritis and Rheumatism、43、1698〜1708(2000)に記述されるようにII型コラーゲン(CII)によって免疫して、3週間後、フロイントの不完全アジュバントと共にCIIを追加免疫した。プラスミドDNAのPBS溶液100 μgを大腿4頭筋の3カ所に筋肉内注射して、関節炎が発症すると、2日ごとにマウスを臨床関節炎に関して採点して、後肢の腫脹を記述のようにノギスで測定した(Drejaら、Arthritis and Rheumatism、43、1698〜1708(2000))。
活性なサイトカイン分子は、TGFβの潜在性ドメインをそのNH2またはCOOH末端のいずれかに付加することによって、「潜在型」となるようにデザインすることができることが本明細書において示されている。サイトカインIFNβを実験モデルにおいて用いた。
Claims (23)
- 薬学的活性蛋白質への潜在性の提供に使用するための、TGFβ-1、2、3、4、または5の潜在性関連ペプチド(LAP)と異種のマトリクスメタロプロテイナーゼ(MMP)蛋白質分解切断部位とを含む融合蛋白質であって、該異種の MMP 蛋白質分解切断部位が LAP と薬学的活性蛋白質との間に人為的に供給されるものである、融合蛋白質。
- 潜在型薬学的活性蛋白質の部位特異的活性化の提供に使用するための、TGFβ-1、2、3、4、または5の潜在性関連ペプチド(LAP)と異種のマトリクスメタロプロテイナーゼ(MMP)蛋白質分解切断部位とを含む融合蛋白質であって、該異種の MMP 蛋白質分解切断部位が LAP と薬学的活性蛋白質との間に人為的に供給されるものである、融合蛋白質。
- MMP切断部位が、MMP1、MMP2、MMP3、MMP7、MMP8、MMP9、またはMMP10から選択されるマトリクスメタロプロテイナーゼによって開裂する、請求項1または2記載の融合蛋白質。
- 薬学的活性蛋白質が、増殖因子、分化因子、サイトカイン、ケモカイン、栄養因子、サイトカイン阻害剤、サイトカイン受容体、フリーラジカルスキャベンジャー酵素、プロドラッグ変換酵素、ペプチド模倣体、プロテアーゼ阻害剤、メタロプロテイナーゼ組織阻害剤、またはセリンプロテアーゼ阻害剤である、使用を目的とした請求項1〜3のいずれか一項記載の融合蛋白質。
- サイトカインがインターロイキンまたはインターフェロンである、使用を目的とした請求項4記載の融合蛋白質。
- 潜在型TGFβ結合蛋白質に会合している、使用を目的とした請求項1〜5のいずれか一項記載の融合蛋白質。
- マトリクスメタロプロテイナーゼ(MMP)蛋白質分解切断部位をコードする核酸配列が第一の核酸配列と第二の核酸配列との間に提供される、薬学的活性蛋白質をコードする第一の核酸配列とTGFβ-1、2、3、4、または5のLAPをコードする第二の核酸配列とを含む核酸構築物。
- MMP切断部位が、MMP1、MMP2、MMP3、MMP7、MMP8、MMP9、またはMMP10から選択されるマトリクスメタロプロテイナーゼによって開裂する、請求項7記載の核酸構築物。
- 薬学的活性蛋白質が、増殖因子、分化因子、サイトカイン、ケモカイン、栄養因子、サイトカイン阻害剤、サイトカイン受容体、フリーラジカルスキャベンジャー酵素、プロドラッグ変換酵素、ペプチド模倣体、プロテアーゼ阻害剤、メタロプロテイナーゼ組織阻害剤、またはセリンプロテアーゼ阻害剤である、請求項7または8記載の核酸構築物。
- サイトカインがインターロイキンまたはインターフェロンである、請求項9記載の核酸構築物。
- 第一の核酸配列が蛋白質IFNβをコードする、請求項7記載の核酸構築物。
- ベクターの形である、請求項7〜11のいずれか一項記載の核酸構築物。
- 請求項7〜12のいずれか一項記載の核酸構築物を含む細胞。
- 医学において用いるための請求項7〜12のいずれか一項記載の核酸構築物。
- 変形性関節炎、強皮症、腎疾患、リウマチ性関節炎、炎症性腸疾患、多発性硬化症、アテローム性動脈硬化症、炎症性疾患、または癌を治療するための医用薬剤の製造における請求項7〜12のいずれか一項記載の核酸構築物の使用。
- 薬学的に許容される担体と請求項7〜12のいずれか一項記載の核酸構築物とを含む薬学的組成物。
- TGFβ-1、2、3、4、または5のLAPと異種のマトリクスメタロプロテイナーゼ(MMP)蛋白質分解切断部位とを含む、薬学的活性蛋白質に会合している融合蛋白質であって、該異種の MMP 蛋白質分解切断部位が LAP と薬学的活性蛋白質との間に人為的に供給されるものである、融合蛋白質。
- 宿主細胞における発現による組換え的な融合蛋白質の産生、発現された融合蛋白質の精製、および化学的クロスリンクによる精製融合蛋白質に対する薬学的活性蛋白質の会合を含む、請求項17記載の融合蛋白質を調製するための方法。
- 医学において用いられる請求項17記載の融合蛋白質。
- 変形性関節炎、強皮症、腎疾患、リウマチ性関節炎、炎症性腸疾患、多発性硬化症、アテローム性動脈硬化症、炎症性疾患、または癌を治療するための医用薬剤の製造における請求項17記載の融合蛋白質の使用。
- 薬学的に許容される担体と請求項17記載の融合蛋白質とを含む薬学的組成物。
- TGFβ-1、2、3、4、または5の潜在性関連ペプチド(LAP)と異種のマトリクスメタロプロテイナーゼ(MMP)蛋白質分解切断部位とを含む融合蛋白質を薬学的活性蛋白質に会合させることを含む、薬学的活性蛋白質に潜在性を提供するインビトロでの方法であって、該異種の MMP 蛋白質分解切断部位が LAP と薬学的活性蛋白質との間に人為的に供給されるものである、方法。
- 請求項7〜12のいずれか一項記載の核酸構築物、または請求項17記載の融合蛋白質、および投与媒体を含む成分のキット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0100551.1A GB0100551D0 (en) | 2001-01-09 | 2001-01-09 | Protein |
| US09/756,283 US6942853B2 (en) | 2001-01-09 | 2001-01-09 | Latent fusion protein |
| PCT/GB2002/000068 WO2002055098A2 (en) | 2001-01-09 | 2002-01-09 | Latency associated peptide for providing latency to pharmaceutically active proteins |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2004520031A JP2004520031A (ja) | 2004-07-08 |
| JP2004520031A5 JP2004520031A5 (ja) | 2005-12-22 |
| JP4201253B2 true JP4201253B2 (ja) | 2008-12-24 |
Family
ID=26245544
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002555832A Expired - Fee Related JP4201253B2 (ja) | 2001-01-09 | 2002-01-09 | 薬学的活性物質に潜在性を提供する方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US6942853B2 (ja) |
| EP (1) | EP1349944B1 (ja) |
| JP (1) | JP4201253B2 (ja) |
| AT (1) | ATE293169T1 (ja) |
| AU (1) | AU2002219345B2 (ja) |
| DE (1) | DE60203692T2 (ja) |
| DK (1) | DK1349944T3 (ja) |
| ES (1) | ES2240740T3 (ja) |
| GB (1) | GB0100551D0 (ja) |
| WO (1) | WO2002055098A2 (ja) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7141392B2 (en) * | 2001-01-09 | 2006-11-28 | Queen Mary And Westfield College | Latent fusion protein |
| CA2475388A1 (en) * | 2002-02-14 | 2003-08-21 | William J. Rutter | Chimeric molecules for cleavage in a treated host |
| AU2006302587A1 (en) * | 2005-10-04 | 2007-04-19 | Greenville Hospital System | Latent procytotoxins and uses thereof |
| DE102006009324A1 (de) | 2006-03-01 | 2007-09-06 | Dr.Ing.H.C. F. Porsche Ag | Verfahren und Steuergerät zur Steuerung eines variablen Turbolader-Turbinenströmungsquerschnitts |
| WO2008130382A2 (en) | 2006-10-31 | 2008-10-30 | East Carolina University | Fusion proteins comprising an anti -inflammatory cytokine and an antigen for treatment of immune disorders |
| GB0724556D0 (en) * | 2007-12-17 | 2008-01-30 | Queen Mary & Westfield College | LAtency associated protein construct with aggrecanase sensitive cleavage site |
| FR2932190A1 (fr) | 2008-06-10 | 2009-12-11 | Commissariat Energie Atomique | Peptides cycliques fluorescents, procedes de preparation de ceux-ci et utilisation de ces peptides pour mesurer l'activite enzymatique d'une enzyme protease |
| AU2010234743A1 (en) | 2009-03-31 | 2011-10-20 | East Carolina University | Cytokines and neuroantigens for treatment of immune disorders |
| GB0911365D0 (en) | 2009-06-30 | 2009-08-12 | Bioceramic Therapeutics Ltd | Multicomponent glasses for use as coatings and in personal care products |
| US8734774B2 (en) | 2010-04-02 | 2014-05-27 | University Of Rochester | Protease activated cytokines |
| EP2878308B1 (en) * | 2013-12-02 | 2018-10-31 | Thomas Harder | Agents and methods for the suppression of T cell activation |
| GB201411506D0 (en) * | 2014-06-27 | 2014-08-13 | Univ London Queen Mary | Modified latency associated protein construct |
| JP6516235B2 (ja) * | 2014-10-31 | 2019-05-22 | 国立大学法人富山大学 | キメラタンパク質及びそれを用いたミクログリア活性阻害剤 |
| DK3794024T5 (da) | 2018-05-14 | 2024-08-19 | Werewolf Therapeutics Inc | Aktiverbare interleukin-2 polypeptider og fremgangsmåder til anvendelse heraf |
| EP3794023A1 (en) | 2018-05-14 | 2021-03-24 | Werewolf Therapeutics, Inc. | Activatable interleukin 12 polypeptides and methods of use thereof |
| WO2020023702A1 (en) | 2018-07-25 | 2020-01-30 | AskGene Pharma, Inc. | Novel il-21 prodrugs and methods of use thereof |
| US20220002370A1 (en) | 2018-09-27 | 2022-01-06 | Xilio Development, Inc. | Masked cytokine polypeptides |
| ES2780274A1 (es) * | 2019-02-15 | 2020-08-24 | Consejo Superior De Investig Científicas (Csic) | Cortistatina o un análogo de la misma como agente farmacéuticamente activo en forma latente |
| MX2021013766A (es) | 2019-05-14 | 2022-02-21 | Werewolf Therapeutics Inc | Restos de separacion y metodos de uso de los mismos. |
| WO2020252264A1 (en) | 2019-06-12 | 2020-12-17 | AskGene Pharma, Inc. | Novel il-15 prodrugs and methods of use thereof |
| AU2020384375A1 (en) * | 2019-11-14 | 2022-05-26 | Werewolf Therapeutics, Inc. | Activatable cytokine polypeptides and methods of use thereof |
| GB202004679D0 (en) | 2020-03-31 | 2020-05-13 | Stealthyx Therapeutics Ltd | Modified latercy associated protein construct |
| BR112022020440A2 (pt) * | 2020-04-10 | 2022-12-27 | Cytomx Therapeutics Inc | Construtos de citocinas ativáveis e composições e métodos relacionados |
| TW202235431A (zh) | 2020-11-25 | 2022-09-16 | 美商艾希利歐發展股份有限公司 | 腫瘤特異性可裂解連接子 |
| EP4308594A2 (en) | 2021-03-16 | 2024-01-24 | CytomX Therapeutics, Inc. | Masked activatable cytokine constructs and related compositions and methods |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5284763A (en) | 1985-03-22 | 1994-02-08 | Genentech, Inc. | Nucleic acid encoding TGF-β and its uses |
| CA2003886A1 (en) | 1988-12-16 | 1990-06-16 | Anthony F. Purchio | Cloning and expression of simian transforming growth factor-beta 1 |
| ATE131872T1 (de) | 1989-11-22 | 1996-01-15 | Genentech Inc | Latenz assoziierte peptide und deren verwendung |
| US5697901A (en) | 1989-12-14 | 1997-12-16 | Elof Eriksson | Gene delivery by microneedle injection |
| KR100227406B1 (ko) | 1993-05-12 | 1999-12-01 | 브루스 엠. 에이센 | Bmp-11 조성물 |
| CA2712304C (en) | 1994-06-10 | 2011-10-25 | United States Surgical Corporation | Recombinant chimeric proteins and methods of use thereof |
| US5800811A (en) * | 1995-06-06 | 1998-09-01 | Hall; Frederick L. | Artificial skin prepared from coclagen matrix containing transforming growth factor-β having a collagen binding site |
| JPH11513249A (ja) * | 1995-09-27 | 1999-11-16 | メディカル・リサーチ・カウンシル | プロテアーゼにより開裂可能なタンパク質を組込んだ組換えウイルス |
| DE19701141C1 (de) | 1997-01-16 | 1998-04-09 | Hoechst Ag | Genkonstrukte für durch Proteasen aktivierbare Wirksubstanzen |
| US6593132B1 (en) * | 1997-04-30 | 2003-07-15 | Twinstrand Therapeutics Inc. | Ricin-like toxin variants for treatment of cancer, viral or parasitic infections |
| GB2324960A (en) | 1997-05-09 | 1998-11-11 | Univ Manchester | Delivery of naked DNA for wound healing |
| EP1117805A2 (en) | 1998-10-07 | 2001-07-25 | STRYKER CORPORATION (a Michigan corporation) | Modified tgf-beta superfamily proteins |
| WO2002022883A1 (en) * | 2000-09-11 | 2002-03-21 | The Trustees Of Columbia University In The City Of New York | Combinatorial fluorescence energy transfer tags and uses thereof |
-
2001
- 2001-01-09 US US09/756,283 patent/US6942853B2/en not_active Expired - Lifetime
- 2001-01-09 GB GBGB0100551.1A patent/GB0100551D0/en not_active Ceased
-
2002
- 2002-01-09 WO PCT/GB2002/000068 patent/WO2002055098A2/en not_active Ceased
- 2002-01-09 DK DK02729440T patent/DK1349944T3/da active
- 2002-01-09 JP JP2002555832A patent/JP4201253B2/ja not_active Expired - Fee Related
- 2002-01-09 AT AT02729440T patent/ATE293169T1/de not_active IP Right Cessation
- 2002-01-09 ES ES02729440T patent/ES2240740T3/es not_active Expired - Lifetime
- 2002-01-09 EP EP02729440A patent/EP1349944B1/en not_active Expired - Lifetime
- 2002-01-09 DE DE60203692T patent/DE60203692T2/de not_active Expired - Lifetime
- 2002-01-09 AU AU2002219345A patent/AU2002219345B2/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| US20020151478A1 (en) | 2002-10-17 |
| EP1349944B1 (en) | 2005-04-13 |
| EP1349944A2 (en) | 2003-10-08 |
| DE60203692D1 (de) | 2005-05-19 |
| DK1349944T3 (da) | 2005-07-25 |
| DE60203692T2 (de) | 2006-03-02 |
| AU2002219345B2 (en) | 2006-03-16 |
| ES2240740T3 (es) | 2005-10-16 |
| US6942853B2 (en) | 2005-09-13 |
| ATE293169T1 (de) | 2005-04-15 |
| WO2002055098A3 (en) | 2002-11-21 |
| JP2004520031A (ja) | 2004-07-08 |
| GB0100551D0 (en) | 2001-02-21 |
| WO2002055098A2 (en) | 2002-07-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4201253B2 (ja) | 薬学的活性物質に潜在性を提供する方法 | |
| AU2002219345A1 (en) | Latency associated peptide for providing latency to pharmaceutically active proteins | |
| JP3681069B2 (ja) | Bmp−11組成物 | |
| US7122352B2 (en) | Polynucleotide encoding mammalian cytokine-like polypeptide-10 | |
| JPH05503003A (ja) | 潜在性関与ペプチドおよびその使用 | |
| US20200062814A1 (en) | Modified Latency Associated Protein Construct | |
| US20180009865A1 (en) | Bmp-2 peptides and methods of use | |
| KR20170026580A (ko) | 변형된 폰 빌레브란트 인자 | |
| WO1994009812A1 (en) | METHOD FOR PRODUCING LARGE LATENT TRANSFORMING GROWTH FACTOR-β COMPLEXES AND LARGE LATENCY ASSOCIATED PEPTIDE | |
| US8357515B2 (en) | Latency associated protein construct with aggrecanase sensitive cleavage site | |
| US7307147B2 (en) | Latent fusion protein | |
| SK8472003A3 (en) | Use of SARP-1 for the treatment and/or prevention of scleroderma | |
| ZA200305237B (en) | Latency associated peptide for providing latency to pharmaceutically active proteins | |
| US20030109439A1 (en) | KGF polypeptide compositions | |
| WO2021198324A1 (en) | Modified latency associated protein construct |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050105 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050105 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20050420 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080201 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080428 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080508 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080527 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080605 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080624 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080701 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080731 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080908 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081003 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4201253 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111017 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121017 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121017 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131017 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |