JP4185185B2 - 部分二重鎖dnaを利用したdnaの検出方法 - Google Patents
部分二重鎖dnaを利用したdnaの検出方法 Download PDFInfo
- Publication number
- JP4185185B2 JP4185185B2 JP12337198A JP12337198A JP4185185B2 JP 4185185 B2 JP4185185 B2 JP 4185185B2 JP 12337198 A JP12337198 A JP 12337198A JP 12337198 A JP12337198 A JP 12337198A JP 4185185 B2 JP4185185 B2 JP 4185185B2
- Authority
- JP
- Japan
- Prior art keywords
- dna
- oligonucleotide
- synthesized
- detected
- stranded
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 108020004414 DNA Proteins 0.000 title claims description 179
- 102000053602 DNA Human genes 0.000 title claims description 43
- 238000001514 detection method Methods 0.000 title claims description 19
- 238000000034 method Methods 0.000 claims description 49
- 230000003321 amplification Effects 0.000 claims description 48
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 48
- 108091034117 Oligonucleotide Proteins 0.000 claims description 42
- 238000005259 measurement Methods 0.000 claims description 38
- 230000000295 complement effect Effects 0.000 claims description 31
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 claims description 20
- 238000010438 heat treatment Methods 0.000 claims description 15
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 claims description 14
- 238000001816 cooling Methods 0.000 claims description 11
- 238000003752 polymerase chain reaction Methods 0.000 claims description 8
- 239000002299 complementary DNA Substances 0.000 claims description 7
- 238000002156 mixing Methods 0.000 claims description 7
- 108020004635 Complementary DNA Proteins 0.000 claims description 6
- 238000010804 cDNA synthesis Methods 0.000 claims description 6
- 238000006243 chemical reaction Methods 0.000 claims description 5
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 239000002773 nucleotide Substances 0.000 claims description 2
- 125000003729 nucleotide group Chemical group 0.000 claims description 2
- 210000004027 cell Anatomy 0.000 claims 1
- 230000002194 synthesizing effect Effects 0.000 claims 1
- 239000000047 product Substances 0.000 description 46
- 108090001008 Avidin Proteins 0.000 description 22
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 18
- 239000010408 film Substances 0.000 description 18
- 229910052751 metal Inorganic materials 0.000 description 18
- 239000002184 metal Substances 0.000 description 18
- 239000000523 sample Substances 0.000 description 14
- 238000007846 asymmetric PCR Methods 0.000 description 13
- 229960002685 biotin Drugs 0.000 description 11
- 239000011616 biotin Substances 0.000 description 11
- 235000020958 biotin Nutrition 0.000 description 10
- 239000011368 organic material Substances 0.000 description 10
- 241001333951 Escherichia coli O157 Species 0.000 description 9
- 239000012634 fragment Substances 0.000 description 9
- 230000001717 pathogenic effect Effects 0.000 description 9
- 239000000758 substrate Substances 0.000 description 9
- 238000010586 diagram Methods 0.000 description 8
- 108010017898 Shiga Toxins Proteins 0.000 description 7
- 239000006087 Silane Coupling Agent Substances 0.000 description 6
- -1 polyethylene terephthalate Polymers 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 5
- 229910052804 chromium Inorganic materials 0.000 description 5
- 239000011651 chromium Substances 0.000 description 5
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 5
- 229910052737 gold Inorganic materials 0.000 description 5
- 239000010931 gold Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 244000005700 microbiome Species 0.000 description 5
- 230000035945 sensitivity Effects 0.000 description 5
- 238000011282 treatment Methods 0.000 description 5
- 238000004925 denaturation Methods 0.000 description 4
- 230000036425 denaturation Effects 0.000 description 4
- 238000009396 hybridization Methods 0.000 description 4
- 238000004544 sputter deposition Methods 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 241000607142 Salmonella Species 0.000 description 3
- 108020004682 Single-Stranded DNA Proteins 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- RGKMQYRTDATEOH-UHFFFAOYSA-N 2,2,2-triaminoethanethiol Chemical compound NC(N)(N)CS RGKMQYRTDATEOH-UHFFFAOYSA-N 0.000 description 2
- PMNLUUOXGOOLSP-UHFFFAOYSA-N 2-mercaptopropanoic acid Chemical compound CC(S)C(O)=O PMNLUUOXGOOLSP-UHFFFAOYSA-N 0.000 description 2
- XLEURSGXFQRWFA-UHFFFAOYSA-N 3,3,3-triaminopropane-1-thiol Chemical compound NC(N)(N)CCS XLEURSGXFQRWFA-UHFFFAOYSA-N 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- 238000002105 Southern blotting Methods 0.000 description 2
- 238000000137 annealing Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000003100 immobilizing effect Effects 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 229910052709 silver Inorganic materials 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 239000003053 toxin Substances 0.000 description 2
- 231100000765 toxin Toxicity 0.000 description 2
- WYTZZXDRDKSJID-UHFFFAOYSA-N (3-aminopropyl)triethoxysilane Chemical compound CCO[Si](OCC)(OCC)CCCN WYTZZXDRDKSJID-UHFFFAOYSA-N 0.000 description 1
- GWOLZNVIRIHJHB-UHFFFAOYSA-N 11-mercaptoundecanoic acid Chemical compound OC(=O)CCCCCCCCCCS GWOLZNVIRIHJHB-UHFFFAOYSA-N 0.000 description 1
- 108020004465 16S ribosomal RNA Proteins 0.000 description 1
- 108020004463 18S ribosomal RNA Proteins 0.000 description 1
- JXCCWNSRNQAJGJ-UHFFFAOYSA-N 21-aminodocosanoic acid Chemical compound CC(N)CCCCCCCCCCCCCCCCCCCC(O)=O JXCCWNSRNQAJGJ-UHFFFAOYSA-N 0.000 description 1
- HXLAEGYMDGUSBD-UHFFFAOYSA-N 3-[diethoxy(methyl)silyl]propan-1-amine Chemical compound CCO[Si](C)(OCC)CCCN HXLAEGYMDGUSBD-UHFFFAOYSA-N 0.000 description 1
- IKYAJDOSWUATPI-UHFFFAOYSA-N 3-[dimethoxy(methyl)silyl]propane-1-thiol Chemical compound CO[Si](C)(OC)CCCS IKYAJDOSWUATPI-UHFFFAOYSA-N 0.000 description 1
- IYGAMTQMILRCCI-UHFFFAOYSA-N 3-aminopropane-1-thiol Chemical compound NCCCS IYGAMTQMILRCCI-UHFFFAOYSA-N 0.000 description 1
- RQPNXPWEGVCPCX-UHFFFAOYSA-N 3-sulfanylbutanoic acid Chemical compound CC(S)CC(O)=O RQPNXPWEGVCPCX-UHFFFAOYSA-N 0.000 description 1
- SJECZPVISLOESU-UHFFFAOYSA-N 3-trimethoxysilylpropan-1-amine Chemical compound CO[Si](OC)(OC)CCCN SJECZPVISLOESU-UHFFFAOYSA-N 0.000 description 1
- UUEWCQRISZBELL-UHFFFAOYSA-N 3-trimethoxysilylpropane-1-thiol Chemical compound CO[Si](OC)(OC)CCCS UUEWCQRISZBELL-UHFFFAOYSA-N 0.000 description 1
- RIRRYXTXJAZPMP-UHFFFAOYSA-N 4-aminobutane-1-thiol Chemical compound NCCCCS RIRRYXTXJAZPMP-UHFFFAOYSA-N 0.000 description 1
- NEAFWRKPYYJETG-UHFFFAOYSA-N 4-sulfanylpentanoic acid Chemical compound CC(S)CCC(O)=O NEAFWRKPYYJETG-UHFFFAOYSA-N 0.000 description 1
- 206010008631 Cholera Diseases 0.000 description 1
- 102000009016 Cholera Toxin Human genes 0.000 description 1
- 108010049048 Cholera Toxin Proteins 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 102000052510 DNA-Binding Proteins Human genes 0.000 description 1
- 108700020911 DNA-Binding Proteins Proteins 0.000 description 1
- 230000004568 DNA-binding Effects 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- RJQXTJLFIWVMTO-TYNCELHUSA-N Methicillin Chemical compound COC1=CC=CC(OC)=C1C(=O)N[C@@H]1C(=O)N2[C@@H](C(O)=O)C(C)(C)S[C@@H]21 RJQXTJLFIWVMTO-TYNCELHUSA-N 0.000 description 1
- REYJJPSVUYRZGE-UHFFFAOYSA-N Octadecylamine Chemical compound CCCCCCCCCCCCCCCCCCN REYJJPSVUYRZGE-UHFFFAOYSA-N 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 201000005702 Pertussis Diseases 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 108010090763 Shiga Toxin 2 Proteins 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 241000295644 Staphylococcaceae Species 0.000 description 1
- 241000607598 Vibrio Species 0.000 description 1
- 241000607272 Vibrio parahaemolyticus Species 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 230000027455 binding Effects 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- UFULAYFCSOUIOV-UHFFFAOYSA-N cysteamine Chemical compound NCCS UFULAYFCSOUIOV-UHFFFAOYSA-N 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 238000007772 electroless plating Methods 0.000 description 1
- 238000009713 electroplating Methods 0.000 description 1
- 239000005357 flat glass Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 238000007646 gravure printing Methods 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000007733 ion plating Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- ARYZCSRUUPFYMY-UHFFFAOYSA-N methoxysilane Chemical compound CO[SiH3] ARYZCSRUUPFYMY-UHFFFAOYSA-N 0.000 description 1
- 229960003085 meticillin Drugs 0.000 description 1
- DJNSXGBGUVWIDF-UHFFFAOYSA-N n-methylthiohydroxylamine Chemical compound CNS DJNSXGBGUVWIDF-UHFFFAOYSA-N 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6832—Enhancement of hybridisation reaction
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/686—Polymerase chain reaction [PCR]
Description
【発明の属する技術分野】
本発明は、部分二重鎖DNAを利用したDNAの検出方法、並びにその部分二重鎖DNA自体及びその作製方法に関する。
【0002】
【従来の技術】
あるDNAをそのDNAと相補的なDNA(以下、「相補鎖DNA」という)を用いて検出する方法は、従来から数多く知られている。例えば、特定のDNAを検出するサザンブロッテイング法はその代表的な例の一つである。また、DNAのクローニングの際に用いるプラークハイブリダイゼーションやコロニーハイブリダイゼーションもこのような検出方法の一種とみなすことができる。これらの方法は、いずれも検出しようとするDNAがその相補鎖DNAに特異的にハイブリダイズすることを利用するものなので、検出しようとするDNAを予め単鎖状態にしておかなくてはならない。しかし、サザンブロッテイング法のように膜に固定している場合を除き、単鎖状態のDNAは球状構造をとることが多く、そのような球状のDNAはもはや相補鎖DNAとハイブリダイズすることはできない。また、二重鎖DNAを単鎖DNAにするためには、加熱などの処理が必要であるが、このような処理は一般に検出しようとするDNAに好ましくない影響を与えることが多い。
【0003】
【発明が解決しようとする課題】
このように相補鎖DNAを利用したDNA検出方法には未だに数多くの問題がある。本発明の目的は、このような問題を解決し、相補鎖DNAを利用した新たなDNA検出方法を提供することにある。
【0004】
【課題を解決するための手段】
本発明者は、上記課題を解決するために鋭意検討を重ねた結果、検出しようとするDNAを部分二重鎖DNAに変換した後に、相補鎖DNAを用いて検出することにより、検出感度が著しく向上することを見出し、本発明を完成した。
即ち、本発明は、検出しようとするDNAをそのDNAと相補的なDNAを用いて検出する方法において、検出しようとするDNAを、その一部分において二重鎖構造をとり、他の部分において単鎖構造をとる部分二重鎖DNAに変換した後に、相補的なDNAを用いて検出することを特徴とするDNAの検出方法である。
【0005】
また、本発明は、下記の工程を含むことを特徴とする部分二重鎖DNAの作製方法である。
(1)作製しようとするDNAの一部と同一な塩基配列を有する1種類のオリゴヌクレオチドを合成する
(2)作製しようとするDNAの一部と相補的な塩基配列を有する2種類のオリゴヌクレオチドを合成する
(3)作製しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの一方をプライマーとして非対称ポリメラーゼ連鎖反応を行う
【0006】
(4)作製しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの他方をプライマーとして非対称ポリメラーゼ連鎖反応を行う
(5)工程(3)の増幅産物と工程(4)の増幅産物を混合した後、加熱、冷却し、部分二重鎖DNAを得る
さらに、本発明は、一部分において二重鎖構造をとり、他の部分において単鎖構造をとる部分二重鎖DNAであって、単鎖構造をとる部分が6塩基以上である部分二重鎖DNAである。
【0007】
【発明の実施の形態】
以下、本発明を詳細に説明する。
本発明のDNAの検出方法は、検出しようとするDNAを部分二重鎖DNAに変換した後に、相補鎖DNAを用いて検出することを特徴とする。
ここで「部分二重鎖DNA」とは、その一部分において二重鎖構造をとり、他の部分において単鎖構造をとるDNAのことをいう。但し、この「部分二重鎖DNA」を本発明の検出方法に利用するためには、単鎖部分は相補鎖DNAとハイブリダイズするのに十分な長さを持たなければならない。従って、通常、本発明において「部分二重鎖DNA」といった場合、前記定義のDNAのうち、単鎖部分の長さが6塩基以上であるものを意味する。また、「部分二重鎖DNAに変換する」とは、検出しようとするDNAを単純に加工して部分二重鎖DNAにする場合だけでなく、検出しようとするDNAをPCR法により増幅させて部分二重鎖DNAにする場合をも含む意である。
【0008】
検出しようとするDNAは、相補鎖DNAを調製できるものであればどのようなものでもよい。具体的には、病原性大腸菌のベロ毒素をコードするDNA、HIVの外殻タンパク質gp120 をコードするDNA、各種微生物の 16SrRNAの特異的塩基配列部分(cDNA)、メチシリン耐性ブドウ球菌(MRSA)の抗生物質結合タンパク質をコードするDNAなどの微生物由来のDNAのほか、ヒトの遺伝病に関係するDNAなども例示することができる。また、検出しようとするDNAは、夾雑物を含んだ状態にあってもよく、例えば、ベロ毒素をコードするDNAを検出する場合、病原性大腸菌の加熱処理物をそのまま検出試料とすることも可能である。
【0009】
部分二重鎖DNAに変換する方法としては、下記の工程を含む方法を例示できるが、これに限定されるわけではない。
(1)検出しようとするDNAの一部と同一な塩基配列を有する1種類のオリゴヌクレオチドを合成する
(2)検出しようとするDNAの一部と相補的な塩基配列を有する2種類のオリゴヌクレオチドを合成する
【0010】
(3)検出しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの一方をプライマーとして非対称PCRを行う
(4)検出しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの他方をプライマーとして非対称PCRを行う
(5)工程(3)の増幅産物と工程(4)の増幅産物を混合した後、加熱、冷却し、部分二重鎖DNAを得る
【0011】
工程(1)及び工程(2)で合成するオリゴヌクレオチドと検出しようとするDNAとの位置関係は図1に示す通りである。即ち、工程(1)のオリゴヌクレオチドは、工程(2)の2種類のオリゴヌクレオチドよりも、a又はa+bだけ5'末端側に位置する。このa及びbは、図1(A)に示すように、そのまま得られる部分二重鎖DNAの二重鎖部分の長さ及び単鎖部分の長さとなる。a及びbの長さは、検出に用いる相補的なDNAに応じて任意に決めることができるが、84塩基以下の場合はPCRによる副生成物が多いなどの問題点もあり、aの長さは、100 〜2000塩基とするのが好ましく、bの長さは、85〜1985塩基とするのが好ましい。
【0012】
工程(3)及び工程(4)では、工程(1)及び工程(2)で合成したオリゴヌクレオチドをプライマーとして非対称PCRを行う。非対称PCRとは、PCRの際に使用する2種類のプライマーのうち、一方を他方に対して過剰量添加して行うPCRをいう(Gyllensten,U.B. らProc.Natl.Acad.Sci.USA,85,7652-7656(1988) )。いずれのプライマーを過剰に添加するかは、図1(B)に示すように、長い増幅断片を得る場合は、工程(1)で作製したプライマーを過剰に添加し、短い増幅断片を得る場合は、工程(2)で作製したプライマーを過剰に添加する(図中の実線の矢印が過剰に添加するプライマーで破線の矢印が少量添加するプライマーである。)。プライマーの添加比は、過剰に添加するプライマーが、他方のプライマーの10〜100 倍とするのが好ましく、20倍とするのが更に好ましい。PCRにおける温度、時間、サイクル等は、増幅しようとするDNA断片に応じて決めればよく、特別な条件に限定されるものではない。以上のような条件で2種類のPCRを行うと、図1(B)に示すような増幅断片が得られる(図中の実線が多量に得られた増幅断片、破線が少量得られた増幅断片である)。
【0013】
工程(5)では、工程(3)及び工程(4)で得られた増幅産物を混合した後、加熱、冷却を行い、部分二重鎖DNAを得る。加熱処理は、90〜95℃で5〜10分行うのが好ましく、冷却処理は20〜30分かけて18〜30℃まで冷却するのが好ましい。この混合、加熱、冷却の一連の処理により、図1(C)に示すような(イ)、(ロ)、(ハ)、(ニ)の4種類のDNA断片が得られる。但し、得られるDNA断片の量は(イ)だけが多く、他の3種類のDNA断片はいずれも少量しか得られない。
【0014】
相補的なDNAを用いて検出する方法としては、標識した相補鎖DNAを用いる一般的なハイブリダイゼーション法を例示できるが、表面プラズモン共鳴バイオセンサーを用いる方法が好ましい。
以下、本発明のDNA検出方法に使用する表面プラズモン共鳴バイオセンサー及びそれに用いる測定チップについて説明する。
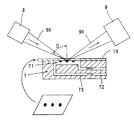
本発明に使用する表面プラズモン共鳴バイオセンサーの一例を図2に示す。この表面プラズモン共鳴バイオセンサーは、カートリッジブロック7と、光源8と、検出器9とを有し、カートリッジブロック7の上に相補鎖DNAを固定した測定チップ10を設置して使用する。カートリッジブロック7の上面には凹部が設けられており、この凹部と上記測定チップ10とで測定セル71が構成される。測定セル71は、流路72、73によりカートリッジブロック7の外部に連通しており、試料は流路72を通じて測定セル71中に流れ込み、測定に供された後流路73を通じて外部に排出される。
【0015】
光源8からは、測定チップ10の透明基板に向かって単色光が照射され(入射光80)、測定チップ10の裏面に設けられた金属膜で反射したその反射光90が、検出器9に入光する。検出器9では、反射光90の強度を検出することができる。
上記のような構造によって、ある入射角θに対して谷を形成する反射光強度曲線が得られる。反射光強度曲線における谷は、表面プラズモン共鳴によるものである。即ち、光が測定チップ10の透明基板と外との界面で全反射するときに、その界面にエバネッセント波といわれる表面波が生じ、一方、金属膜にも表面プラズモンといわれる表面波が生じる。この2つの表面波の波数が一致すると共鳴が起こり、光のエネルギーの一部が表面プラズモンを励起するために使用され、反射光の強度が低下する。ここで、表面プラズモンの波数は、金属膜表面のごく近くにある媒質の屈折率の影響を受けるため、検出しようとするDNAと相補鎖DNAとの相互作用により媒質の屈折率が変化すると、表面プラズモン共鳴が生じる入射角θが変化する。従って、反射光強度曲線の谷のずれによって、検出しようとするDNAの濃度の変化を検知することができる。入射角θの変化量は共鳴シグナルといわれ、10-4°の変化を1RUとして表す。
【0016】
測定チップ10は、表面プラズモン共鳴に必要な透明基板及び金属膜を有し、相補鎖DNAを金属膜上に固定できるものであればどのようなものでもよく、市販の測定チップ(例えば、ファルマシアバイオセンサー社製、BIAcore2000 用測定チップ )を使用することもできるが、図3に示すような構造を有する測定チップを使用することが好ましい。この測定チップは、透明基板1上に金属膜2、有機物質層3が形成されおり、その上にアビジン4が固定されており、このアビジンにビオチン5で標識された相補鎖DNA6が固定される。
【0017】
透明基板1としては、通常表面プラズモン共鳴バイオセンサー用の測定チップに使用されるものであればどのようなものでもよく、一般的にはガラス、ポリエチレンテレフタレート、ポリカーボネートなどのレーザー光に対して透明な材料からなるものが使用でき、偏光に対して異方性を示さずかつ加工性の優れた材料が望ましく、その厚さは0.1 〜20mm程度である。
金属膜2としては、表面プラズモン共鳴が生じ得るようなものであれば特に限定されない。この金属膜に使用することのできる金属の種類としては、金、銀、銅、アルミニウム、白金等が挙げられ、それらを単独で又は組み合わせて使用することができる。また、上記透明基板1への付着性を考慮して、透明基板1と金、銀等からなる層との間にクロム等からなる介在層を設けてもよい。
【0018】
金属膜2の膜厚は、100 〜2000Åであるのが好ましく、特に200 〜600 Åであるのが好ましい。3000Åを超えると、媒質の表面プラズモン現象を十分検出することができない。また、クロム等からなる介在層を設ける場合、その介在層の厚さは、5〜50Åであるのが好ましい。
金属膜2の形成は常法によって行えばよく、例えば、スパッタ法、蒸着法、イオンプレーティング法、電気めっき法、無電解めっき法等によって行うことができる。これらの方法の中でもスパッタ法を用いるのが好ましい。
【0019】
有機物質層3は、金属原子とアビジン分子の両者と結合することができる物質からなる層である。有機物質層3の厚さは、10〜200 Åであるのが好ましく、特に10〜50Åであるのが好ましい。また、アビジン−ビオチン結合を用いる以外にもエステル結合やアミド結合等の共有結合を利用してDNAを有機物質層3に固定化することも可能である。
有機物質層は、シランカップリング剤、メルカプト基と他の有機官能基を有する化合物(以下、単に「チオール化合物」という)用いて形成させることができ、また、LB(ラングミュア・ブロジェット)法によっても形成させることができる。LB法によって成膜した場合、シランカップリング剤やチオール化合物によって成膜した場合に比べ、金属膜との結合能が弱いという短所があるが、広範な物質に適用でき、また、凝集膜を形成できるので単位面積当たりに結合させる生理活性物質の数を増加させることができるという長所もある。
【0020】
有機物質層形成に使用できるシランカップリング剤としては、3−アミノプロピルトリエトキシシラン、3−アミノプロピルトリメトキシシラン、3−アミノプロピルジエトキシメチルシラン、3−(2−アミノエチルアミノプロピル)トリメトキシシラン、3−(2−アミノエチルアミノプロピル)ジメトキシメチルシラン、3−メルカプトプロピルトリメトキシシラン、ジメトキシ−3−メルカプトプロピルメチルシランなどが挙げられる。また、チオール化合物としては、メルカプトアミノメタン、2−メルカプト−1−アミノエタン、3−メルカプト−1−アミノプロパン、4−メルカプト−1−アミノブタン、1,1,1−トリアミノ−2−メルカプトエタン、メルカプト酢酸、2−メルカプトプロピオン酸、3−メルカプト酪酸、4−メルカプト吉草酸、1,1,1−トリアミノ−3−メルカプトプロパンなどが挙げられ、これらの中でも多官能物質であり、アビジンとの結合部位が多い1,1,1−トリアミノ−2−メルカプトエタン、1,1,1−トリアミノ−3−メルカプトプロパンなどを用いるのが好ましい。LB法に適用できる物質としては、21−アミノドコサン酸、ステアリルアミン、ポリリジンなどを例示することができる。
【0021】
シランカップリング剤を用いて有機物質層を形成する方法としては、シランカップリング剤の飽和蒸気中に金属膜を一定時間暴露する方法(飽和蒸気法)、シランカップリング剤を含む溶液中に金属膜を一定時間浸漬する方法(浸漬法)、スピンコータを用いる方法(スピンコーティング法)、グラビア印刷機を用いる方法(グラビア法)などを用いることができ、チオール化合物を用いて有機物質層3を形成する方法としては、飽和蒸気法、浸漬法、スピンコーティング法、グラビア法などを用いることができる。
【0022】
有機物質層3にアビジン4を固定することは、所定量のアビジン4を有機物質層3に所定時間接触させることにより形成させることができる。具体的な方法としては、フローセル型の表面プラズモン共鳴バイオセンサーに有機物質層3を形成させた透明基板1を設置して一定流量のアビジン4を所定時間(所定量)流す方法を例示できる。
【0023】
アビジン4に、ビオチンで標識した相補鎖DNA5に固定化する方法としては、インクジエット法、マクロディスペンサー法などを例示することができる。インクジェット法は、極めて狭い領域に精度よく相補鎖DNA5を含む液滴を発射できるので、固定化する相補鎖DNA5を有効利用できるという点で有利である。また、フローセル型の表面プラズモン共鳴バイオセンサーに測定チップを設置して一定流量の相補鎖DNA5を所定時間(所定量)流すことによっても固定化できる。この固定化方法によれば、アビジン4及び相補鎖DNA5の固定を一連の操作で行うことができるという点で有利である。相補鎖DNAをビオチンで標識する方法としては、ビオチンを結合させたプライマーを用いてPCRを行う方法を例示することができる。
【0024】
検出するDNAは1種類だけでなく、2種類以上であってもよい。2種類以上のDNAを検出するには、一つのチップに複数のDNAを固定するか、センサーに複数のチップを固定することにより行い得る。このように2種類以上のDNAを検出することにより、検出の精度を向上させることができる。例えば、ある微生物の持つ特異的なDNAと相補的なDNAを二つ以上チップに固定することにより、その微生物に由来するDNAが試料中に含まれているかどうかをより高い精度で判別することができる。また、固定化するDNAの中に目的のDNAとは結合しないDNA(陰性プローブ)を含ませておくことによっても精度を向上させることができる。さらに、固定化するDNAの選択を適切に行えば、例えば、試料中にベロ毒素が含まれるかどうかということだけでなく、そのベロ毒素がI型なのかII型なのかというようなことまで判別できる。
【0025】
2種類以上のDNAを固定する場合、使用する表面プラズモン共鳴バイオセンサーは、測定チップを水平方向に自由に移動可能なタイプのものが好ましい。このようなセンサーを使用すれば、光学系を固定したままチップ上の複数の試料のシグナルを測定できる。
【0026】
【実施例】
〔実施例1〕
市販の表面プラズモン共鳴バイオセンサー(ファルマシアバイオセンサー社製、BIAcore2000 )の測定セルに0.1 %アビジン溶液を流速5μl/分で10分間流し込み、測定チップにアビジンを固定した。一方、図4に示す2型ベロ毒素をコードするDNAの塩基配列の401 〜421 の塩基に相補的なオリゴヌクレオチドを合成し、その5'末端にビオチンを結合させた(以下、このオリゴヌクレオチドを「antiprobe VT2-2B」という)。antiprobe VT2-2Bを含む溶液を前記バイオセンサーの測定セルに流速1μl/分で50分間流し込み、測定チップ上にアビジンを介して固定した。
【0027】
次に、図4に示す塩基配列に基づき、下記のプライマーを合成した。
P-VT2Cは図4に示す塩基配列の301 〜321 塩基に対応し、asp-VT2-2aは381 〜401 塩基に対応し、asp-VT2-2bは433 〜433 に対応する。
【0028】
病原性大腸菌O−157から抽出したゲノムDNAを鋳型とし、P-VT2Cとasp-VT2-2bをプライマーとして非対称PCRを行った。P-VT2Cは、asp-VT2-2bの20倍量加えた。PCRは、初期変性(94℃3分)を行った後、変性(94℃1分)、アニーリング(59℃0.5 分)、伸長(72℃1分)のサイクルを10〜40に変化させて行った。
また、P-VT2Cとasp-VT2-2aをプライマーとして上記と同様に非対称PCRを行った。asp-VT2-2bは、P-VT2Cの20倍量加えた。
【0029】
上記で得られる2種類のPCR増幅産物を混合し、全量100 μl とした。95℃で10分加熱した後、30分かけて25℃まで冷却し、部分二重鎖DNAを作製した。この部分二重鎖DNAを含む混合増幅産物を、上記バイオセンサーの測定セルに流し込み、流量が10μl、20μl、30μl、及び40μlにおける共鳴シグナルを測定した。この結果を図5に示す。また、対照としてP-VT2Cとasp-VT2-2bをプライマーとしてPCR(対称PCR)を行い、その増幅産物を測定セルに流し込み、共鳴シグナルを測定した。この結果を図6に示す。図中の○が10サイクル、●が20サイクル、△が25サイクル、▲が30サイクル、□が40サイクルを示す。
図5及び図6に示すように、いずれの場合も30サイクル以上でハイブリダイゼーションによるシグナルを検出することができた。また、非対称PCR産物を部分二重鎖DNAにすることにより、検出感度が約2倍向上した。
【0030】
〔実施例2〕
病原性大腸菌O−157から抽出したゲノムDNAを鋳型とし、P-VT2Cとasp-VT2-2bをプライマーとして非対称PCRを行った(この増幅産物を「増幅産物A」という)。P-VT2Cはasp-VT2-2bの20倍量加えた。PCRは、初期変性(95℃3分)を行った後、変性(94℃1分)、アニーリング(61℃1分)、伸長(72℃1分)を40サイクル繰り返した。
病原性大腸菌O−157から抽出したゲノムDNAを鋳型とし、P-VT2Cとasp-VT2-2aをプライマーとして非対称PCRを行った(この増幅産物を「増幅産物B」という)。asp-VT2-2aはP-VT2Cの20倍量加えた。PCRの反応条件は、上記と同様にして行った。
【0031】
病原性大腸菌O−157から抽出したゲノムDNAを鋳型とし、P-VT2Cとasp-VT2-2bをプライマーとして対称PCRを行った(この増幅産物を「増幅産物C」という)。PCRの反応条件は、上記と同様にして行った。
病原性大腸菌O−157から抽出したゲノムDNAを鋳型とし、P-VT2Cとasp-VT2-2aをプライマーとして対称PCRを行った(この増幅産物を「増幅産物D」という)。PCRの反応条件は、上記と同様にして行った。
【0032】
増幅産物A〜Dを、▲1▼増幅産物C+増幅産物D、▲2▼増幅産物A+増幅産物B、▲3▼増幅産物A+増幅産物D、▲4▼増幅産物B+増幅産物Cの4通りの組み合わせで混合し、その混合増幅産物を95℃で10分加熱した後、30分かけて25℃まで冷却した。この4種類の混合増幅産物を、上記バイオセンサーの測定セルに流し込み、流量が10μl、20μl、30μl、及び40μlにおける共鳴シグナルを測定した。この結果を図7に示す。図中の○が混合増幅産物▲1▼、●が混合増幅産物▲2▼、△が混合増幅産物▲3▼、▲が混合増幅産物▲4▼を示す。
図7に示すように、非対称PCR増幅産物同士を混合した場合(混合増幅産物▲2▼)が最も検出感度が良好であった。
【0033】
〔実施例3〕
実施例2で調製した増幅産物Aと増幅産物Bとの混合増幅産物を95℃で10秒加熱した後、30分かけて25℃まで冷却し、部分二重鎖DNAを作製した。この部分二重鎖DNAを含む混合増幅産物を、上記バイオセンサーの測定セルに流し込み、流量が10μl、20μl、30μl、及び40μlにおける共鳴シグナルを測定した。また、対照1として増幅産物Aのみを加熱、冷却して調製したサンプル、対照2として増幅産物Aと増幅産物Bとの混合増幅産物を加熱、冷却せずに調製したサンプル、対照3として増幅産物Aのみを加熱、冷却せずに調製したサンプル、についても上記と同様に共鳴シグナルを測定した。この結果を図8に示す。図中の○が部分二重鎖DNAを含むサンプル、●が対照1のサンプル、△が対照2のサンプル、▲が対照3のサンプルを示す。
図8に示すように、増幅産物Aのみからなるサンプルでは十分なシグナルを検出できなかった。また、混合増幅産物からなるサンプルではいずれも一定のシグナルを検出することはできたが、加熱、冷却処理を施さない場合は明らかに感度が劣った。
【0034】
〔実施例4〕
13mm X 18mm 、厚さ0.3mm の青板ガラス(松浪硝子工業社製)上にスパッタリングによりクロムからなる層、次いで金からなる層を形成し、表面プラズモン共鳴バイオセンサー用の測定チップを作製した。スパッタリングは、クロムについては100W、30秒間、金については100W、150 秒間行った。得られたクロム層の厚さは32.2Åであり、金層の厚さは474 Åであった。この測定チップを11- メルカプトウンデカン酸の1mMエタノ−ル溶液に24時間浸漬し、金属層上に有機薄膜層を形成させた。次いで、50μl の5%アビジン溶液を同一チップ上の3箇所に滴下し、アビジン分子と有機薄膜層上の分子との間にアミド結合を形成させ、アビジン分子を固定化した。
【0035】
次に、5’末端にビオチンを結合させた下記の3種類のDNAを合成した(サワデー・テクノロジー社に合成を委託)。これらのDNAは、毒素産生菌Vibrio parahaemolyticus(腸炎ビブリオ)の毒性の要因となるtdh1 、tdh2 、trh2 の3種類の遺伝子の一部と相補的な配列を持つ。
【0036】
【0037】
上記DNAを含む溶液(10μl )をアビジン溶液を滴下した位置に30μl 滴下し、DNAをアビジン・ビオチン結合を介して測定チップ上に固定化した。
DNAを固定化した測定チップを表面プラズモン共鳴バイオセンサー(電気化学計器社製のSPR−20型のセンサーヘッド、給排液液を改造したもの)に設置した(図9)。このバイオセンサーでは、測定チップを水平方向に自由に移動させることができるので、光学系を固定したままチップ上に存在する複数の試料の共鳴シグナルを測定することが可能である。
【0038】
被検出物であるDNAは、実施例1と同様に非対称PCRを利用し、部分二重鎖DNA(二重鎖部分143bp, 単鎖部分101b)として増幅させた。増幅させた部分二重鎖DNAを含む溶液を、バイオセンサーの測定セルに流し込み、流量10μl における共鳴シグナルを測定した。結果を表1に示す。
【0039】
【表1】
【0040】
表1に示すよう配列1〜3のいずれも300RU(換算値)前後のシグナルを得ており、DNAの結合がない場合(陰性)のシグナルが10〜20RU(換算値)であることを考慮すると、固定した3種類のDNAに部分二重鎖が結合したもの(陽性)と考えられる。
【0041】
〔実施例5〕
実施例4と同様に青板ガラス上に金属層、有機薄膜層を形成させ、4枚の測定チップを作製した。次いで、50μl の5%アビジン溶液を4枚のチップ上の2箇所に滴下し(合計8箇所)、アビジン分子を固定化した。
次に、5’末端にビオチンを結合させた下記の8種類のDNAを合成した(サワデー・テクノロジー社に合成を委託)。配列1〜3は、Vibrio parahaemolyticusのtdh1、tdh2、trh2遺伝子のそれぞれの一部と相補的な配列を持つDNAであり、配列4はSalmonella enteritidis(サルモネラ)の18S rRNA、配列5はBorderella pertussis(百日咳菌)の百日咳毒素、配列6はVibrio chorera (コレラ)のコレラ毒素、配列7はEscherichia coli 0157 (病原性大腸菌O157)のベロ毒素1、配列8はEscherichia coli 0157 のベロ毒素2と相補的な配列を持つDNAである。
【0042】
【0043】
上記DNAを含む溶液(10μl )をアビジン溶液を滴下した位置に30μl 滴下し、DNAをアビジン・ビオチン結合を介して測定チップ上に固定化した。
DNAを固定化した測定チップを実施例4で使用した表面プラズモン共鳴バイオセンサーに設置した。被検出物であるDNAは、実施例4と同様に非対称PCRを利用し、部分二重鎖DNA(二重鎖部分143bp, 単鎖部分101b)として増幅させた。DNAは、大腸菌O157、腸炎ビブリオ、サルモネラのそれぞれから調製したDNAと、大腸菌O157から調製したDNAとサルモネラから調製したDNAの混合物の4種類使用した。増幅させた部分二重鎖DNAを含む溶液を、バイオセンサーの測定セルに流し込み、流量10μl における共鳴シグナルを測定した。結果を表2に示す。
【0044】
【表2】
【0045】
表2に示すように、各種微生物に対して陽性の場合300RU程度、陰性の場合30RU以下のシグナルが得られた。
【0046】
【発明の効果】
本発明は、DNAの新規な検出方法を提供する。この方法は、DNAを部分二重鎖の状態で検出するので、加熱等の処理が不要であり、また、単鎖DNAのように球状化することもないので、検出感度においても優れる。
【図面の簡単な説明】
【図1】非対称PCRを用いて本発明の部分二重鎖DNAを作製する方法の概要を示す図である。
【図2】本発明の検出方法に使用する表面プラズモン共鳴バイオセンサーの一実施例を示す図である。
【図3】本発明の検出方法に使用する表面プラズモン共鳴バイオセンサー用測定チップの一実施例を示す図である。
【図4】病原性大腸菌O−157の二型ベロ毒素をコードするDNAの塩基配列を示す図である。
【図5】部分二重鎖DNAを用いた場合のPCRサイクルと共鳴シグナルとの関係を示す図である。
【図6】部分二重鎖DNAを用いない場合のPCRサイクルと共鳴シグナルとの関係を示す図である。
【図7】検出しようとするDNAの構造と共鳴シグナルとの関係を示す図である。
【図8】増幅産物混合後の加熱の有無と共鳴シグナルとの関係を示す図である。
【図9】本発明の検出方法に使用する表面プラズモン共鳴バイオセンサーの一実施例を示す図である。
【符号の説明】
1…透明基板
2…金属膜
3…有機物質層
4…アビジン
5…ビオチン標識相補鎖DNA
6…部分二重鎖DNA
7…カートリッジブロック
71…測定セル
72,73…流路
8…光源
80…入射光
9…検出器
90…反射光
10…測定チップ
Claims (6)
- 検出しようとするDNAをそのDNAと相補的なDNAを用いて検出する方法において、検出しようとするDNAを、その一部分において二重鎖構造をとり、他の部分において単鎖構造をとる部分二重鎖DNAに変換した後に、相補的なDNAを用いて検出することを特徴とするDNAの検出方法であって、
部分二重鎖DNAに変換する方法が、下記の工程を含む変換方法であること特徴とする前記DNAの検出方法。
(1)検出しようとするDNAの一部と同一な塩基配列からなる1種類のオリゴヌクレオチドを合成する
(2)検出しようとするDNAの一部と相補的な塩基配列からなる2種類のオリゴヌクレオチドを合成する
(3)検出しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの一方をプライマーとして非対称ポリメラーゼ連鎖反応を行う
(4)検出しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの他方をプライマーとして非対称ポリメラーゼ連鎖反応を行う
(5)工程(3)の増幅産物と工程(4)の増幅産物を混合した後、加熱、冷却し、部分二重鎖DNAを得る - 前記相補的なDNAを表面プラズモン共鳴バイオセンサー用測定チップに固定し、該バイオセンサーによりDNAを検出することを特徴とする請求項1記載のDNAの検出方法。
- 二種類以上のDNAを検出することを特徴とする請求項2記載のDNAの検出方法。
- 下記の工程を含むことを特徴とする部分二重鎖DNAの作製方法。
(1)作製しようとするDNAの一部と同一な塩基配列からなる1種類のオリゴヌクレオチドを合成する
(2)作製しようとするDNAの一部と相補的な塩基配列からなる2種類のオリゴヌクレオチドを合成する
(3)作製しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの一方をプライマーとして非対称ポリメラーゼ連鎖反応を行う
(4)作製しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドの他方をプライマーとして非対称ポリメラーゼ連鎖反応を行う
(5)工程(3)の増幅産物と工程(4)の増幅産物を混合した後、加熱、冷却し、部分二重鎖DNAを得る(ただし、工程(3)の増幅産物と工程(4)の増幅産物をそれぞれ精製した後に、混合、加熱、冷却し、部分二重鎖DNAを得る場合を除く) - 作製される部分二重鎖DNAが、その単鎖構造をとる部分のDNAと相補的なDNAをフローセル型表面プラズモン共鳴バイオセンサー用測定チップに固定し、該バイオセンサーによりDNAを検出する方法に用いるためのものである、請求項4記載の方法。
- 工程(2)が、作製しようとするDNAの一部と相補的な塩基配列からなる、工程(1)で合成したオリゴヌクレオチドよりも a 又は a+b だけ 3 ’末端側に位置する2種類のオリゴヌクレオチドを合成する工程であり、
工程(3)が、作製しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌク レオチドと工程(2)で合成した2種類のオリゴヌクレオチドのうち、工程(1)で合成したオリゴヌクレオチドよりも a+b だけ 3 ’末端側に位置するオリゴヌクレオチドとをプライマーとして、工程(1)で合成したオリゴヌクレオチドを過剰に添加して非対称ポリメラーゼ連鎖反応を行う工程であり、
工程(4)が、作製しようとするDNAを鋳型とし、工程(1)で合成したオリゴヌクレオチドと工程(2)で合成した2種類のオリゴヌクレオチドのうち、工程(1)で合成したオリゴヌクレオチドよりも a だけ 3 ’末端側に位置するオリゴヌクレオチドとをプライマーとして、当該工程(2)で合成したオリゴヌクレオチドを過剰に添加して非対称ポリメラーゼ連鎖反応を行う工程である、
請求項4又は5に記載の方法。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP12337198A JP4185185B2 (ja) | 1997-05-08 | 1998-05-06 | 部分二重鎖dnaを利用したdnaの検出方法 |
| PCT/JP1998/002039 WO1998050581A1 (fr) | 1997-05-08 | 1998-05-08 | Procede de detection de sequences nucleotidiques cibles |
| DE69838538T DE69838538T2 (de) | 1997-05-08 | 1998-05-08 | Verfahren zur erkennung von zielnukleinsäuren |
| EP98919518A EP0915174B1 (en) | 1997-05-08 | 1998-05-08 | Method for detecting target nucleotide sequence |
| US09/147,251 US6391546B1 (en) | 1997-05-08 | 1998-05-08 | Method for detecting target nucleotide sequence |
| US10/103,798 US20030054378A1 (en) | 1997-05-08 | 2002-03-25 | Method for detecting target nucleotide sequence |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP11772597 | 1997-05-08 | ||
| JP9-117725 | 1998-03-23 | ||
| JP7444298 | 1998-03-23 | ||
| JP10-74442 | 1998-03-23 | ||
| JP12337198A JP4185185B2 (ja) | 1997-05-08 | 1998-05-06 | 部分二重鎖dnaを利用したdnaの検出方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPH11332566A JPH11332566A (ja) | 1999-12-07 |
| JP4185185B2 true JP4185185B2 (ja) | 2008-11-26 |
Family
ID=27301505
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP12337198A Expired - Lifetime JP4185185B2 (ja) | 1997-05-08 | 1998-05-06 | 部分二重鎖dnaを利用したdnaの検出方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US6391546B1 (ja) |
| EP (1) | EP0915174B1 (ja) |
| JP (1) | JP4185185B2 (ja) |
| DE (1) | DE69838538T2 (ja) |
| WO (1) | WO1998050581A1 (ja) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030165953A1 (en) * | 1997-07-09 | 2003-09-04 | Isao Karube | Method for detecting DNA with probe PNA |
| CA2409309A1 (en) * | 2000-05-19 | 2001-11-29 | Eragen Biosciences, Inc. | Materials and methods for detection of nucleic acids |
| JP2001337036A (ja) * | 2000-05-25 | 2001-12-07 | Masao Karube | 差動式sprセンサー及び該センサーを用いた測定法 |
| CA2425747C (en) | 2000-10-14 | 2012-01-24 | Eragen Biosciences, Inc. | Solid support assay systems and methods utilizing non-standard bases |
| AU2002247765B2 (en) | 2001-03-28 | 2007-04-26 | Clondiag Chip Technologies Gmbh | Device for referencing fluorescence signals |
| DE10132785A1 (de) * | 2001-07-06 | 2003-01-16 | Clondiag Chip Tech Gmbh | Verfahren zum Nachweis von in einer Polymerase-Kettenreaktion amplifizierten Nukleinsäuremolekülen |
| GB2393250A (en) * | 2002-09-17 | 2004-03-24 | Secr Defence | PCR assay |
| ATE417129T1 (de) | 2003-01-17 | 2008-12-15 | Eragen Biosciences Inc | Nukleinsäureamplifikation mit nichtstandardbasen |
| JP3923917B2 (ja) * | 2003-03-26 | 2007-06-06 | 株式会社東芝 | ターゲットの製造方法、標的配列検出方法、ターゲットおよび標的配列検出用アッセイキット |
| US7820808B2 (en) | 2003-04-01 | 2010-10-26 | Eragen Biosciences, Inc. | Polymerase inhibitor and method of using same |
| AU2004273783A1 (en) | 2003-07-12 | 2005-03-31 | Accelr8 Technology Corporation | Sensitive and rapid biodetection |
| US7341841B2 (en) * | 2003-07-12 | 2008-03-11 | Accelr8 Technology Corporation | Rapid microbial detection and antimicrobial susceptibility testing |
| US20120077206A1 (en) | 2003-07-12 | 2012-03-29 | Accelr8 Technology Corporation | Rapid Microbial Detection and Antimicrobial Susceptibility Testing |
| WO2006095550A1 (ja) * | 2005-03-04 | 2006-09-14 | Kyoto University | Pcrプライマー、それを利用したpcr法及びpcr増幅産物、並びにpcr増幅産物を利用するデバイス及びdna-タンパク複合体 |
| US7498136B2 (en) | 2005-03-18 | 2009-03-03 | Eragen Biosciences, Inc. | Methods for detecting multiple species and subspecies of Neisseria |
| EP1893777B1 (en) | 2005-06-07 | 2014-10-01 | Luminex Corporation | Methods for detection and typing of nucleic acids |
| CA2778449C (en) | 2009-10-23 | 2017-06-20 | Luminex Corporation | Amplification primers with non-standard bases for increased reaction specificity |
| ES2551922T3 (es) | 2011-03-07 | 2015-11-24 | Accelerate Diagnostics, Inc. | Sistemas rápidos de purificación celular |
| US10254204B2 (en) | 2011-03-07 | 2019-04-09 | Accelerate Diagnostics, Inc. | Membrane-assisted purification |
| US8883488B2 (en) * | 2011-11-15 | 2014-11-11 | Tuskegee University | Detection of food threat agents and food-borne pathogens |
| US9677109B2 (en) | 2013-03-15 | 2017-06-13 | Accelerate Diagnostics, Inc. | Rapid determination of microbial growth and antimicrobial susceptibility |
| EP3278115A2 (en) | 2015-03-30 | 2018-02-07 | Accelerate Diagnostics, Inc. | Instrument and system for rapid microorganism identification and antimicrobial agent susceptibility testing |
| US10253355B2 (en) | 2015-03-30 | 2019-04-09 | Accelerate Diagnostics, Inc. | Instrument and system for rapid microorganism identification and antimicrobial agent susceptibility testing |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5030557A (en) | 1987-11-24 | 1991-07-09 | Ml Technology Venture | Means and method for enhancing nucleic acid hybridization |
| CA2025179A1 (en) * | 1989-10-12 | 1991-04-13 | William G. Weisburg | Nucleic acid probes and methods for detecting cryptococcus neoformans |
| AU638568B2 (en) | 1990-02-26 | 1993-07-01 | United States of America, as represented by the Secretary, U.S. Department of Commerce, The | A method for the fluorescent detection of a dna sequence in real time |
| FR2663040B1 (fr) * | 1990-06-11 | 1995-09-15 | Bio Merieux | Procede de detection d'une sequence nucleotidique selon la technique d'hybridation sandwich. |
| US5695926A (en) | 1990-06-11 | 1997-12-09 | Bio Merieux | Sandwich hybridization assays using very short capture probes noncovalently bound to a hydrophobic support |
| JPH06502766A (ja) * | 1990-11-14 | 1994-03-31 | アクゾ・ノベル・ナムローゼ・フェンノートシャップ | ポリスチレン支持体ベース−サンドイッチハイブリダイゼーションアッセイ法を用いる核酸の非同位体検出およびそれに用いる組成物 |
| JP3514779B2 (ja) * | 1991-04-17 | 2004-03-31 | 株式会社アズウェル | アポリポプロテインe遺伝子タイプの検査方法及びその検査に好適なプライマー及びプローブ |
| DE69110032T2 (de) | 1991-06-08 | 1995-12-21 | Hewlett Packard Gmbh | Verfahren und Gerät zur Feststellung und/oder Konzentrationsbestimmung von Biomolekülen. |
| JP3408265B2 (ja) | 1992-03-13 | 2003-05-19 | 国際試薬株式会社 | Pcr増幅dnaの測定法 |
| JPH0630797A (ja) * | 1992-07-14 | 1994-02-08 | Hitachi Ltd | 遺伝子多型解析方法 |
| CA2119701A1 (en) * | 1993-04-16 | 1994-10-17 | Colleen M. Nycz | Nucleic acid assay procedure |
| US6007987A (en) * | 1993-08-23 | 1999-12-28 | The Trustees Of Boston University | Positional sequencing by hybridization |
| US5482845A (en) * | 1993-09-24 | 1996-01-09 | The Trustees Of Columbia University In The City Of New York | Method for construction of normalized cDNA libraries |
| DE69427876T2 (de) * | 1994-05-23 | 2002-04-11 | Biotronics Corp | Methode zur detektion einer gezielten nukleinsäure |
| US5485277A (en) * | 1994-07-26 | 1996-01-16 | Physical Optics Corporation | Surface plasmon resonance sensor and methods for the utilization thereof |
| US5753439A (en) * | 1995-05-19 | 1998-05-19 | Trustees Of Boston University | Nucleic acid detection methods |
-
1998
- 1998-05-06 JP JP12337198A patent/JP4185185B2/ja not_active Expired - Lifetime
- 1998-05-08 EP EP98919518A patent/EP0915174B1/en not_active Expired - Lifetime
- 1998-05-08 US US09/147,251 patent/US6391546B1/en not_active Expired - Lifetime
- 1998-05-08 DE DE69838538T patent/DE69838538T2/de not_active Expired - Fee Related
- 1998-05-08 WO PCT/JP1998/002039 patent/WO1998050581A1/ja active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| US6391546B1 (en) | 2002-05-21 |
| JPH11332566A (ja) | 1999-12-07 |
| EP0915174A1 (en) | 1999-05-12 |
| DE69838538T2 (de) | 2008-07-24 |
| EP0915174A4 (en) | 2002-06-12 |
| DE69838538D1 (de) | 2007-11-22 |
| WO1998050581A1 (fr) | 1998-11-12 |
| EP0915174B1 (en) | 2007-10-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4185185B2 (ja) | 部分二重鎖dnaを利用したdnaの検出方法 | |
| Zhai et al. | DNA based biosensors | |
| Peter et al. | Optical DNA-sensor chip for real-time detection of hybridization events | |
| US6060288A (en) | Method for performing amplification of nucleic acid on supports | |
| US8058005B2 (en) | Method for single nucleotide polymorphism and mutation detection using real time polymerase chain reaction microarray | |
| EP2468884B1 (en) | Multi-spot metal-deposited nucleic acid chip with nanostructure arrays for diagnosing corneal dystrophy | |
| JP4380631B2 (ja) | 選択結合性物質固定化担体 | |
| US6316608B1 (en) | Combined polynucleotide sequence as discrete assay endpoints | |
| JP3591653B2 (ja) | 核酸をプロセシングするための方法 | |
| US7964344B2 (en) | Stable hybrid | |
| WO1999002730A1 (fr) | Procede de detection d'adn au moyen d'une sonde de pna | |
| WO2001042512A2 (en) | Normalization controls and duplex probes for quantitative hybridization reactions | |
| EP2231876B1 (en) | A programmable oligonucleotide micro array | |
| US20030054378A1 (en) | Method for detecting target nucleotide sequence | |
| US20030165953A1 (en) | Method for detecting DNA with probe PNA | |
| Duman et al. | Detection of Mycobacterium tuberculosis complex using surface plasmon resonance based sensors carrying self-assembled nano-overlayers of probe oligonucleotide | |
| US7534566B2 (en) | Nucleic acid labeling method and liquid composition | |
| WO2009059447A1 (en) | A quantitative method for oligonucleotide microarray | |
| JP2004003913A (ja) | 核酸固定化担体 | |
| Watterson | Towards the development of a fiber-optic nucleic acid biosensor: An examination of factors affecting selectivity of detection of interfacial nucleic acid hybridization. | |
| Bill et al. | Immobilization-Mediated Reduction in Melting | |
| Piunno | Development of a fibre optic biosensor for determination of interfacial nucleic acid hybrid formation | |
| Vasantgadkar | A novel method for detecting DNA | |
| Niu | A label-free, fluorescence based assay for microarray | |
| Thiel | Detection of DNA hybridization to oligonucleotide arrays on gold surfaces using in situ surface plasmon resonance and fluorescence imaging techniques |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050425 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080507 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080707 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080902 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080905 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110912 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110912 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120912 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130912 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |