JP4170633B2 - 拡張型心筋症の原因となる新規点突然変異を有するデスミン遺伝子 - Google Patents
拡張型心筋症の原因となる新規点突然変異を有するデスミン遺伝子 Download PDFInfo
- Publication number
- JP4170633B2 JP4170633B2 JP2002034379A JP2002034379A JP4170633B2 JP 4170633 B2 JP4170633 B2 JP 4170633B2 JP 2002034379 A JP2002034379 A JP 2002034379A JP 2002034379 A JP2002034379 A JP 2002034379A JP 4170633 B2 JP4170633 B2 JP 4170633B2
- Authority
- JP
- Japan
- Prior art keywords
- desmin
- hamster
- cardiomyopathy
- gene
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/8509—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells for producing genetically modified animals, e.g. transgenic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4717—Plasma globulins, lactoglobulin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/05—Animals comprising random inserted nucleic acids (transgenic)
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
- A01K2267/0375—Animal model for cardiovascular diseases
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Pathology (AREA)
- Plant Pathology (AREA)
- Peptides Or Proteins (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
【発明の属する技術分野】
本発明は、遺伝性心筋症の原因となる遺伝子を解明したものである。本発明は、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置が点変異したデスミン遺伝子、変異した蛋白質、点変異部分を含むオリゴヌクレオチド、及びそれを用いた遺伝性心筋症を検出、同定する方法に関する。また、本発明は、変異したデスミン遺伝子のみを含有した疾患モデル動物に関する。
【0002】
【従来の技術】
心臓は全身に血液を送るための重要な臓器である。心臓のポンプとしての機能を担っているのが心筋である。心筋は不随意筋ではあるが、骨格筋と同じ横紋筋で構成されている。横紋筋は、筋原繊維におけるアクチンフィラメントとミオシンフィラメントからなる筋節(サルコメア)が暗帯(ミオシンフィラメント部分)と明帯(筋節の末端のZ線部分)との縞模様に観察されることから命名された筋肉組織である。筋細胞は、細長い繊維状の細胞であり、その細胞質(筋形質)には多数の筋原繊維やミトコンドリアが存在し、細胞質は筋鞘と呼ばれる細胞膜で包まれている。
筋形質に存在する筋原繊維は、アクチンフィラメントとミオシンフィラメントからなる筋節(サルコメア)からなり、各筋節の間には細い横線状のZ線がある。Z線部分には、筋形質膜表面に伝わった電気的興奮を深部の筋原線維に瞬時に伝搬する機能を有するT管が存在する。筋細胞に伝達された電気的興奮はT管を経由して筋節に伝達され、筋収縮が起こることになる。
【0003】
心筋はこのような筋細胞(心筋細胞)の網でできており、心臓をらせん状にとりまいており、自律的な収縮を繰り返して血液を全身に送っている。心臓の負荷が長期間継続すると、心筋は細胞分裂により心筋組織を大きくするのではなく、心筋細胞自体の長さや太さが増加する。これを心筋の肥大という。心筋が肥大しても、心筋細胞に酸素や栄養を供給する冠状動脈などがそれに見合って発達することは無く、心筋の肥大により心筋細胞に対する充分な血液の供給ができなくなる。一般に、心臓の重量が500gを越えるとこのような現象が起こることになる。
心筋症は、心筋の異常による疾患であり、生命維持に必須な心臓には自発再生能がなく、その進行性変性疾患である心筋症は極めて重篤である。心筋症は、拡張型心筋症(うっ血性心筋症)や肥大型心筋症のような原発性心筋症と感染性心筋症のような二次性心筋症に分類される。原発性心筋症には、心筋の肥大による肥大型心筋症と、他の要因による拡張型心筋症がある。
【0004】
遺伝性心筋症の代表的なモデル動物である心筋症ハムスターは1962年に発見され、これまでに病理学、薬理学、生理学など様々な見地から研究されてきた。プロトタイプである肥大型心筋症ハムスターBIO14.6(以下、Bと略す。)から肉眼的な心肥大を伴わない重症な亜系(TO−2、以下、Tと略す。)が分離されている。
図1にこれらの心筋症ハムスターの特徴を図面に代わる写真で示す。図1の左側のGは正常ゴールデンハムスターであり、中側のBは肥大型心筋症BIO14.6ハムスターであり、右側のTは拡張型心筋症TO−2ハムスターである。図1の上段の(A)は各ハムスターの左心室のヘマトキシリン&エオジン(hematoxylin & eosin)染色による光学顕微鏡像を示す。B及びT共に壊死、線維化、石灰化が見られる。(A)のバーは200μmを示す。図1の(B)は各ハムスターの左心室の水平断面像を示す。Bでは残存心筋の代償性肥大が顕著に見られるのに対し、Tの心室壁は極めて薄い。(B)のバーは2mmを示す。図1の下段の(C)は各ハムスターの心電図の胸部第一誘導を示す。ゴールデン(G)、BIO14.6(B)、TO−2(T)におけるQRSコンプレックス(complex)の電位はそれぞれ、0.55±0.06、0.98±0.06、0.22±0.06Vである。(C)の縦方向のバーは0.5Vを示し、横方向のバーは1秒を示す。
【0005】
これらの心筋症ハムスターに共通の遺伝子異常は、ジストロフィン(dystrophin)結合タンパク質の一つであるδ−サルコグリカン(δ−sarcoglycan)遺伝子の欠失であることを本発明者らが明らかにしてきた(Sakamoto A,et al. Proc. Natl. Acad. Sci. U.S.A. 1997,94(13873-13878);Sakamoto A, et al. FEBS Lett. 1999, 447,124-128.)。
しかし、Tのハムスターには心筋の肥大は観察されず、δ−サルコグリカン(δ−sarcoglycan)遺伝子の欠失のみでこれらのハムスターの心筋症の原因を論ずることはできず、Tのハムスターの心筋症の原因についてはさらなる解明が必要とされていた。
【0006】
【発明が解決しようとする課題】
本発明は、肥大型心筋症ハムスターBIO14.6(B)から分離された肉眼的な心肥大を伴わない重症な亜系(T)の心筋症の原因を解明し、拡張型心筋症の病因を明かにし、もってその予防・治療方法を確立することを目的としている。
また、本発明は、亜系Tのみの心筋症の原因となる遺伝子を含有する新規疾患モデル動物を提供すること、及びこれらの動物を用いた遺伝性心筋症に対する新たな治療法(医薬品、遺伝子治療、再生医療など)の開発あるいは評価方法を提供することを目的としている。
さらに本発明は、TO−2ハムスターあるいはその亜系動物を用いて、心筋における筋原線維と筋形質膜(T管を含む)との架橋構造の解明をするための手法を提供することを目的としている。
【0007】
【課題を解決するための手段】
本発明は、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置が点変異したデスミン遺伝子に関する。より詳細には、点変異が、GからAへの変異である点変異したデスミン遺伝子に関する。
本発明は、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置を含む5〜250塩基からなるオリゴヌクレオチド、又はその相補配列からなるオリゴヌクレオチドに関する。
【0008】
また、本発明は、遺伝性心筋症の原因となる遺伝子であるかどうかを判定するために、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置の点変異を検出、同定する方法に関する。より詳細には、検出、同定する方法が、PCRを用いて検出する方法、又は前記オリゴヌクレオチドを用いる方法である、点変異を検出、同定する方法に関する。
さらに、本発明は、このようなPCRのためのプライマーや、デスミンの各領域を増幅するためのプライマーに関する。
本発明は、前記したプライマーや、前記してきたオリゴヌクレオチドを用いて、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置の点変異を検出、同定するための測定キットに関する。
【0009】
また、本発明は、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置が点変異したデスミン遺伝子がコードしてなるデスミン、及びデスミンのヘッド領域、コイル−1領域、コイル−2領域、又はテイル領域からなるポリペプチド、これらのコイル−1領域に存在する191番目のアミノ酸であるアラニンがスレオニンに変異しているポリペプチド、並びにこれらのポリペプチドに対する抗体に関する。
さらに、本発明は、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置が点変異したデスミン遺伝子のみにより遺伝子異常が生じている疾患モデル動物、より詳細には、TO−2ハムスターを他のハムスター、例えば正常ハムスターとを交配させて得られる遺伝性心筋症の疾患モデル動物、及びこの疾患モデル動物を用いて、遺伝性心筋症に対する予防、治療法又は予防、治療剤をスクリーニングする方法に関する。
【0010】
遺伝性心筋症の代表的なモデル動物である心筋症ハムスターのプロトタイプである肥大型心筋症ハムスターBIO14.6(以下、Bと略す。)から肉眼的な心肥大を伴わない重症な亜系(TO−2、以下、Tと略す。)が分離されている。
本発明者らは、これらの心筋症ハムスターに共通の遺伝子異常は、ジストロフィン(dystrophin)結合タンパク質の一つであるδ−サルコグリカン(δ−sarcoglycan)遺伝子の欠失であることを明らかにしてきた(Sakamoto A,et al. Proc. Natl. Acad. Sci. U.S.A. 1997,94(13873-13878);Sakamoto A, et al. FEBS Lett. 1999, 447,124-128.)。しかし、Tのハムスターには心筋の肥大は観察されず、δ−サルコグリカン(δ−sarcoglycan)遺伝子の欠失のみでこれらのハムスターの心筋症の原因を論ずることはできず、Tのハムスターの心筋症の原因についてはさらなる解明が必要とされていた。
【0011】
心筋細胞は圧負荷や低酸素負荷に対して、細胞分裂はせずにその容積を増やすという特徴がある(代償性心肥大)。そこでまず、これに関連する遺伝子の発現量をRT−PCRで検討した。この結果を図2に図面に代わる写真で示す。図2の左側のGは正常ゴールデンハムスターであり、中側のBは肥大型心筋症BIO14.6ハムスターであり、右側のTは拡張型心筋症TO−2ハムスターである。図2の各段は上から、内部標準であるGAPDH(Glyceraldyde 3-Phosphate Dehydrogenase)、α−骨格筋型アクチン(α−Skeletal Muscle Actin)、β−ミオシン重鎖(β−Myosin heavy chain)、c−ミック(c-myc)、c−H−ラス(c-H-ras)、プレプロET−1(prepro-endothelin-1)、Brain Natriuretic Peptide(BNP)、及びGATA−4である。PCRのサイクルは、各々左から40、35、30、25で、バンドがより右側で検出できるほど発現量は多いことになる。測定に用いたゴールデン(G)、BIO14.6(B)、TO−2(T)のcDNAが等量であることは、内部標準であるGAPDH(Glyceraldyde 3-Phosphate Dehydrogenase)の増幅が同一であることから確認できる。
この結果、予想外なことにプレプロ−エンドセリン−1(prepro-endothelin-1)、C−ミック(c-myc)、β−ミオシン重鎖(β−myosin heavy chain)など心肥大に関連する遺伝子の発現はいずれもBよりTの方が亢進していた。
【0012】
次に病理学的な観点から、心筋細胞のアポトーシスとネクローシスについて検討した。まず、心臓正中断面でのTUNEL(TdT-mediated X-dUTP nick end labeling)陽性細胞数とゲノムDNAのラダーリングを検討した。結果を図3に図面に代わる写真で示す。図3の左側の(A)は心臓正中断面でのTUNEL陽性細胞数をG、B及びTのハムスターの6、12及び26週齢において検討した結果を示す。図3の右側の(B)は心筋から抽出したゲノムDNAの電気泳動をG、B及びTのハムスターの12及び26週齢において検討した結果を示す。
この結果、TUNEL陽性細胞数はB及びT共にやや多いが、両者の違いに有意差はなかった。また、ゲノムDNAのラダーリングについてもBIO14.6、TO−2いずれにおいても、アポトーシスに特異的な180塩基単位のラダーは検出されなかった。
【0013】
ネクローシスに関する検討ではいずれも26週齢のハムスターを用いてマッソントリクローム(Masson trichrome)染色とトルイジンブルー(Toluidine blue)染色を行った。結果を図4に図面に代わる写真で示す。図4の左側のGは正常ゴールデンハムスターであり、中側のBは肥大型心筋症BIO14.6ハムスターであり、右側のTは拡張型心筋症TO−2ハムスターである。図4の上段の(A)はマッソントリクローム(Masson trichrome)染色の場合を示し、図4の下段の(B)はトルイジンブルー(Toluidine blue)染色の場合を示す。
この結果、TO−2では、線維化(青く染色)が激しく(図4(A))、炎症細胞浸潤(arrow)が激しい(図4(B))ことが分かった。
このように、Tでは線維化と炎症細胞浸潤が強く(図4)、心筋変性の実体はアポトーシスではなくネクローシス(壊死)であることが分かった。
【0014】
さらに、透過型電子顕微鏡(TEM)及び超音波画像診断によりこれらのハムスターの病理を観察した。透過型電子顕微鏡の観察の結果を図5に図面に代わる写真で示し、超音波画像診断の観察の結果を図6に図面に代わる写真で示す。図5の左側のGは正常ゴールデンハムスターであり、中側のBは肥大型心筋症BIO14.6ハムスターであり、右側のTは拡張型心筋症TO−2ハムスターである。図6の左側のBは肥大型心筋症BIO14.6ハムスターであり、右側のTは拡張型心筋症TO−2ハムスターである。
この結果、TO−2のZ線(矢頭印)は細く、部分的に断裂し、間隔が不均一なところも見られる。また、TO−2ではT管(矢印)の数が少なく、Tの左心室筋には、(1)筋原線維の横紋に相当するZ線は細く、部分的に分断され、(2)T管の数が少なく、(3)Z線の間隔が不均一なところがある、という3つの形態異常を見出した(図5参照)。さらに、超音波画像診断により、BIO14.6の心室壁は同心円状に収縮するが、TO−2の心室壁は単に薄いのみでなく、心室全体としての動きに協調性がなく、心室の動きが空間的に無秩序であることも見出した(図6参照)。
【0015】
以上のことから、Tの心筋ではZ線が細く、部分的に分断されていることが観察され、TではZ線の構成タンパク質に異常が存在することが示された。生後6週の左心室筋から筋原線維を抽出し、さらに図7の左側に示される精製プロトコールに従ってミオシンとアクチンを段階的に除去し、Z線の構成タンパク質を濃縮した標品を調製した。そして、既知のZ線構成タンパク質であるα−アクチニンとデスミンの存否をイムノブロット(immunoblot)で追跡した。図7の右側はZ線の構成タンパク質を濃縮する工程における各段階での正常ゴールデンハムスター(G)とTO−2(T)におけるSDS−PAGEのCBB染色(上段)及びイムノブロット(下段)の結果を示す図面に代わる写真である。即ち、心筋のホモジネート段階をWとし、界面活性剤で可溶化した後の筋原繊維の分画をP1とし、他の分画をS1とし、P1の分画からミオシンを除去した分画をP2とし、さらにP2の分画からアクチンを除去した分画をP3とした。
α−アクチニンとデスミンは、生後6週のTの全ホモジネート(whole homogenate)、筋原線維画分、ミオシン除去の筋原線維画分ではGと変化はなかったが、アクチンの除去により共に激減した(図7参照)。Z線と結合するタンパク質であるアクチンの除去は、Z線を人為的に不安定化させることを意味する。従って、その結果としてα−アクチニンとデスミンが激減することは、TのZ線が構造的に脆いことを示唆し、TEMの所見と一致する。心筋は死ぬまで収縮を続けそれによる機械的ストレスは加齢と共に蓄積する。そこで次に、G、B、及びT(6、12、28、及び45週齢)の左心室の全ホモジネート(whole homogenate)におけるα−アクチニンとデスミンの加齢による変化を追跡した。結果を図8に図面に代わる写真で示す。図8の上段はSDS−PAGEのCBB染色の写真であり、下段はイムノブロットの写真である。その結果、Tでは加齢と共にデスミンは徐々に減少するがα−アクチニンの量に変化はなかった。以上から、TではZ線構成タンパク質、特にデスミンが極めて不安定であることが分かった。
【0016】
デスミンは骨格筋あるいは心筋のZ線に位置する中間系フィラメントタンパク質(intermediate filament protein)であり、その遺伝子異常は筋ジストロフィー症を合併する心筋症の原因となることが知られている(Goebel H.H.,et al.Muscle&Nerve,18:1306-1320,1995)。そのモデル動物としてはこれまでに、デスミン遺伝子を完全に破壊させたいわゆるノックアウトマウス(knock out mouse)が独立した2つのグループによって作成されている(Milner D.J.,et al.J Cell Biol.,134:1255-1270,1996:Li Z.,et al.Dev.Biol.,175:362-366,1996)。ところで、これまでに見出されたデスミン遺伝子の異常によるヒト心筋症には、デスミン遺伝子の完全欠失はなく、全て点突然変異である。この場合、デスミンタンパク質は小児期には存在するが、加齢と共に徐々にZ線から逸脱し、結果として心筋症が発症する。それに対してデスミンのノックアウトマウスでは、デスミンタンパク質は生下時にすでに完全に欠損し、筋原線維、ミトコンドリアなど心筋あるいは骨格筋細胞内の微細構造の破綻ならびに心筋症は速やかに起こる。そのため、デスミン遺伝子の異常による心筋細胞崩壊の経時的変化の追跡が難しく、また、発症前から予防的に行う心筋症の新規治療法の開発には不向きであるという問題点があった。
シリアンハムスターのデスミン遺伝子並びにcDNA自体はすでに単離され(Quax W.,et.al. Cell.1985;43(1):327-38.)、その遺伝子発現調節やタンパク質複合体形成に関する研究に用いられてきた。しかし、遺伝性心筋症ハムスターの原因及び発症機構における意義という観点で研究に用いられたことはない。
【0017】
すでに公表されたシリアンハムスターのデスミンのcDNAの塩基配列を基に、翻訳領域全体をRT−PCRで増幅するプライマーセットと反応条件を見出した(図9に示されるDes5F/Des5RとDes3F/Des3R)。そして、GとTのデスミンcDNAをクローニングし、塩基配列を決定した。Gのデスミン遺伝子の翻訳領域(open reading frame)は、1407塩基で、469残基のアミノ酸からなる分子量53,445のポリペプチドをコードすると考えられた。アミノ酸配列のコンピューター解析(Lupas,A.,Van Dyke,M.,and Stock,J.(1991)."Predicting Coled Coils from Protein Sequences" Science 252:1162-1164. http://www.ch.embnet.org/software/COILS_form.html)の結果、デスミンはコイルド−コイル(coiled-coil)構造をしたタンパク質であり、アミノ末端のヘッド(head)部分、中央の二つのコイル(coil)部分、そしてカルボキシル末端のテイル(tail)部分からなることが予測された(図14の(A)参照)。
【0018】
図9は、シリアンハムスターのデスミンのcDNAの塩基配列を示す。翻訳されるアミノ酸を対応コドンの上部に一文字表記で記した。塩基の番号は翻訳領域だけを対象とした。全翻訳領域をカバーするデスミンcDNAは、図9中のDes5F/Des5RとDes3F/Des3RによるRT−PCR産物を、ボックスで表記した制限酵素(Sal I)の認識部位で結合して得ることができる(図12参照)。デスミンの4つのドメイン(図14参照)を増幅するためのプライマーも矢印で明記した。
図12は、ゴールデンハムスターの左心室筋から合成したcDNAを鋳型とし、図9に示される2種類のプライマーセット(Des5F/Des5RとDes3F/Des3R)でPCRを行った結果を示す図面に代わる写真である。Mはマーカーである。この結果、Des5F/Des5RでPCRを行った場合には593bpのPCR産物が得られ、Des3F/Des3RでPCRを行った場合には973bpのPCR産物が得られることがわかる。
【0019】
そして、TのハムスターのデスミンのcDNAをクローニングし、塩基配列を決定した結果、Tでは、coil−1内に位置し、既知の全ての種で保存される191番目のアラニンをスレオニンに変える点変異(point mutation(G571A))が存在することがわかった。BIO14.6ハムスターはこの塩基変異はなく、TO−2における第二の遺伝子異常は、Z線を構成するデスミン遺伝子のミスセンス変異(missense mutation)であると考えられた。
図13は、拡張型心筋症ハムスターTO−2におけるゲノムの塩基変異とPCRによるその検出を示したものである。図13の(A)は、ゴールデンとTO−2ハムスターにおける、デスミン遺伝子の点突然変異(G571A)周辺のゲノムの塩基配列を示したものである。両者で共通のものはドット(・)で表示したある。大文字と小文字は、それぞれ第一エクソン、第一イントロン内の塩基配列であることを示す。番号は図9のcDNA配列に対応する。遺伝子診断に用いたプライマーの例を矢印で示した。図13の(B)は、プライマーセット(DesF/desGR)あるいは(DesF/DesTR)を用いたゲノムのPCRの結果を示す図面に代わる写真である。それぞれ、デスミンの571番目の塩基がGあるいはAに特異的なバンドを増幅することがわかる。ゴールデン、BIO14.6、TO−2におけるこのアレルは、(G/G)、(G/G)、(A/A)であることもわかった。
【0020】
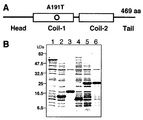
デスミンの分子構造と各ドメインの組み換えタンパク質の発現の結果を図14に図面に代わる写真で示す。図14の(A)は、デスミンの分子構造を模式的に示したものであり、TO−2におけるアミノ酸変異(図14(A)の○印)は、コイル−1(Coil−1)内に位置する。図14の(B)は、デスミンの全長及び各ドメインの組み換えタンパク質である。各ドメインのcDNAを図1のプライマーセットを用いて増幅し、発現ベクターpET33bに組み込み、大腸菌BL21(DE3)に発現させた結果を示す図面に代わる写真である。図は、各大腸菌の全溶出物(whole lysate)をSDS−PAGEにかけCBBで染色したものである。目的のタンパク質に対応するバンドには星印(*)を付した。レーン1は全長のものであり、レーン2はヘッド(head)部分のものであり、レーン3はコイル−2(Coli-2)のものであり、レーン4はテイル(Tail)部分のものであり、レーン5は正常なコイル−1(normal coil-1)(191A)のものであり、レーン6は変異コイル−1(mutant coil-1(191T))のものである。
【0021】
TO−2のデスミンには点突然変異(G571A)があり(図13参照)、そのため191番目のアミノ酸が正常のA(アラニン)からT(スレオニン)に変わったものである。この点変異したTO−2のデスミンの塩基配列を配列表の配列番号1に示し、その翻訳領域の対応するアミノ酸配列を配列番号2に示す。
【0022】
次に、デスミンの機能を調べるために、心筋の筋形質膜と筋原線維の架橋構造を検討した。
本発明者らは、正常ハムスター(G)の心筋ではジストロフィン(dystrophin)結合タンパク質であるα−ジストロブレビン(α−dystrobrevin)は、心筋のT管にも存在するが、45週のTではほとんど存在しないことを、単離心筋細胞の免疫染色により初めて見い出した。心筋の全ホモジネート(whole homogenate)を用いたイムノブロット(immunoblot)の結果を図10に図面に代わる写真で示す。α−ジストロブレビン(α−dystrobrevin)の消失は、心筋症ハムスターの共通原因遺伝子δ−サルコグリカン(δ−sarcoglycan)の欠失に依存せず、デスミンの消失した45週のTO−2に特異的であった。
これらの結果とTではT管がほとんど存在しないという透過型電顕の所見と考え合わせると、心筋の筋形質膜と筋原線維は、T管上のα−ジストロブレビン(α−dystrobrevin)とZ線上のデスミンとが直接あるいは間接的に結合することで架橋されていることが推測される。この構造を模式的にして図11に示す。図11はこれらの結果から予想される筋形質膜と筋原線維の架橋モデルを示しており、α−ジストロブレビン(α−dystrobrevin)とデスミンを介した心筋形質膜と筋原線維との架橋構造は、筋形質膜の電気的興奮を筋原線維に伝搬させる一方、筋原線維の張力を筋形質膜に伝達させる働きがあると考えられる。α−ジストロブレビン(α−dystrobrevin)とデスミンとの結合が、直接的なものか何らかの分子(docking molecule)を介した間接的なものかは、現時点では不明であるが、これらの分子が相互に作用するものであることが明らかにされた。
そして、Tでは、心筋細胞(透過型電顕像、図5)さらには心臓全体(超音波画像診断、図6)の収縮が空間的に不均一であるが、そのことは、デスミン遺伝子の異常によりT管の構造的異常が引き起こされ、筋形質膜から筋原線維への電気的興奮の伝搬が不均一になることで容易に理解できる。
【0023】
以上のように、本発明によりTO−2に存在する心筋症の第二原因遺伝子が解明された。さらに、T管と筋原線維との架橋の支持体としての、デスミンの機能的意義の発見は本発明が世界で初である。
【0024】
【発明の実施の形態】
本発明は、遺伝性心筋症の原因のひとつが心筋のT管に関連するデスミンの遺伝子の点変異であることを見出したものである。本発明の点変異の位置は、シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置であり、この位置がデスミンのcDNAの翻訳領域のどの位置になるかは動物によって異なることがあり、必ずしも571番目ということではない。例えば、ヒトのデスミンにおいてこの位置がデスミンのcDNAの翻訳領域の何番目に相当するかということは、アミノ酸配列の相同性やペプチドの立体配置などを考慮して決定されることである。したがって、本発明における「シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置」とは、デスミンのペプチドとしての機能における同様な機能を果たす位置に相当することを意味しており、動物の種類に応じてデスミンのアミノ酸配列の相同性やペプチドの立体配置などにより決定されるいる位置を意味している。
【0025】
シリアンハムスターにおいては、当該点変異はGからAへの変異であることを本発明は明らかにしてきたが、本発明はGからAへの変異に限定されるものではなく、本発明において重要なことはその位置の点変異により心筋症が発症してくるということであり、動物の種類による遺伝子の各種の変異を本発明は包含するものである。
シリアンハムスターにおける具体例においては、配列表の配列番号1に記載の塩基配列が示される。この配列表においては、翻訳開始の塩基が82番目であるから、点変異の位置は652番目に示されている。本来のデスミンは、652番目から654番目までの塩基配列が「gcc」でアラニンをコードするものであるが、本発明の遺伝子は「acc」に点変異してスレオニンをコードする配列となっている。
【0026】
本発明は、このようなデスミンの遺伝子の点変異により遺伝性心筋症が発症することを明らかにするものであり、「シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置」の点変異を検出、同定することにより、遺伝性心筋症の原因となる遺伝子であるかどうかを判定することができる。被検体としては、ヒト、ハムスター、ラットなどの動物のゲノムを使用することができる。
本発明の検出、同定する方法としては、通常の各種の遺伝子の検出、同定手段を使用することができる。例えば、点変異の前後の塩基配列を利用したPCR法などにより、点変異を含む部分の遺伝子を増幅させて、増幅の有無や増幅された遺伝子の解析により点変異の有無を検出、同定することができる。PCR法における好ましいプライマーとしては、配列番号9に記載の塩基配列を有するフォーワードプライマーと、配列番号10に記載の塩基配列を有するリバースプライマー、又は配列番号11に記載の塩基配列を有するリバースプライマー若しくは配列番号12に記載の塩基配列を有するリバースプライマーとの組み合わせが挙げられる。
また、点変異を含む部分のオリゴヌクレオチドを固定化させたDNAチップを用いて、ゲノムのSNPを検出、同定する方法と同様な手法により本発明の点変異を検出、同定することもできる。
【0027】
本発明は、「シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置」を含む5〜250塩基からなるオリゴヌクレオチド、又はその相補配列からなるオリゴヌクレオチドを提供するものである。本発明のオリゴヌクレオチドは、本発明の点変異を検出、同定などに使用することができる。本発明のオリゴヌクレオチドの長さとしては、検出、同定に必要な充分な長さがあればよく、例えば5〜250塩基、5〜150塩基、5〜50塩基、5〜30塩基、5〜20塩基、又は。7〜250塩基、7〜150塩基、7〜50塩基、7〜30塩基、7〜20塩基、さらには10〜250塩基、10〜150塩基、10〜50塩基、10〜30塩基、10〜20塩基程度の各種の長さでその目的に応じて使用することができる。
本発明のオリゴヌクレオチドは、プライマーやプローブとして使用することができ、プローブとしては標識化して使用することや、DNAチップのように担体に固定されて使用することができる。
【0028】
さらに、本発明は、「シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置」の点変異を検出、同定するための測定キットを提供するものである。このような測定キットとしては通常の遺伝子の検出、同定に使用されるキットを使用することができる。例えば、PCR法などによる増幅により検出、同定しようとする場合には、増幅のためのプライマーセット、増幅処理に必要な試薬類、増幅産物を検出、同定するための試薬類などから測定キットとなる。また、DNAチップなどの場合には、点変異を検出、同定するためのオリゴヌクレオチドが固定化されたDNAチップ、それを処理するための試薬類などからなる測定キットが挙げられる。
本発明の測定キットにより、遺伝性心筋症の原因となる遺伝子であるかどうかを判定することができる。
【0029】
本発明は、デスミン遺伝子の各領域を増幅するためのプライマーを提供する。デスミンは図14に示されるように、ヘッド領域、コイル−1領域、コイル−2領域、又はテイル領域からなるポリペプチドであり、この各領域の1つ又は連続した2個以上の領域を増幅するためのプライマーセットを提供するものである。より詳細には、図9に示されるように、ヘッド領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてHD−F(配列表の配列番号13)をリバースプライマーとしてHD−R(配列表の配列番号14)を使用することができ、コイル−1領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてCL1−F(配列表の配列番号15)をリバースプライマーとしてCL1−R(配列表の配列番号16)を使用することができ、コイル−2領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてCL2−F(配列表の配列番号17)をリバースプライマーとしてCL2−R(配列表の配列番号18)を使用することができ、又はテイル領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてTL−F(配列表の配列番号19)をリバースプライマーとしてTL−R(配列表の配列番号20)を使用することができる。また、これらのプライマーを適宜組み合わせることにより、2つ以上の連続した領域を同時に増幅することもできる。
【0030】
また、デスミンの5’端領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてDes5F(配列表の配列番号5)をリバースプライマーとしてDes5R(配列表の配列番号6)を使用することができ、デスミンの3’端領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてDes3F(配列表の配列番号7)をリバースプライマーとしてDes3R(配列表の配列番号8)を使用することができる。
さらに、点変異を含む領域を増幅すためのプライマーセットとしてはフォーワードプライマーとしてDesF(配列表の配列番号9)をリバースプライマーとしてDesGR(配列表の配列番号10)を使用することができ、点変異体を特異的に増幅させるためのプライマーセットとしてはフォーワードプライマーとしてDesF(配列表の配列番号9)をリバースプライマーとしてDesTR(配列表の配列番号12)又はより短いDesTR(配列表の配列番号11)を使用することができる。
本発明は、これらのプライマーセットを提供するものである。
【0031】
本発明は、「シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置」が点変異したデスミン遺伝子がコードしてなるデスミンを提供するものであり、本発明の点変異したデスミン遺伝子がコードしてなるデスミンとしては、ハムスター、ヒト、ラットなどの動物から得られるポリペプチドが挙げられる。本発明の点変異したデスミン遺伝子がコードしてなるデスミンは、心筋などの横紋筋における構造解析や機能解析に有用であるばかりでなく、T管における神経伝達機構の解明などにも有用なポリペプチドである。本発明の点変異したデスミン遺伝子がコードしてなるデスミンの具体例としては、配列表の配列番号2に記載されたアミノ酸配列を有するものが挙げられる。このアミノ酸配列は本発明のポリペプチドのひとつの例示であり、このアミノ酸配列のみに限定されるものではなく、同様な機能を有するものであれば一部のアミノ酸が欠失し、他のアミノ酸で置換され、又は他のアミノ酸がさらに付加されたものであってもよい。言い換えれば、本発明の点変異したデスミン遺伝子がコードしてなるデスミンとは、点変異を起こしたアミノ酸が存在するデスミンの機能を有するポリペプチドであるということもできる。
【0032】
また、本発明は、図14に示されるように、デスミンのヘッド領域、コイル−1領域、コイル−2領域、又はテイル領域からなるポリペプチドを提供するものである。デスミンのコイル−1領域は、本発明の点変異を含むものであり、本発明は、コイル−1領域のひとつのアラニンがスレオニンに変異しているデスミンのコイル−1領域からなるポリペプチドを提供するものである。
さらに、本発明は、これらの本発明のポリペプチドに対する抗体を提供するものである。本発明の抗体はポリクローナル抗体であってもよいし、モノクローナル抗体であってもよい。本発明の抗体は、本発明の前記したポリペプチドを用いて通常の抗体の製造方法、例えば免疫感作させたラットやウサギなどの動物の細胞を用いた細胞融合法などにより製造することができる。
【0033】
本発明は、デスミンの遺伝子の特定の位置の点変異が遺伝性の心筋症の原因であることを明らかにしたものであり、「シリアンハムスターのデスミンのcDNAの翻訳領域の塩基配列の571番目に相当する位置」が点変異したデスミン遺伝子を用いて遺伝子異常が生じている疾患モデル動物を製造することができる。本発明の疾患モデル動物としては、ヒトを除く動物であれば特に制限はないが、マウス、ハムスター、ラット、ニワトリ、ウサギ、イヌなどの各種の動物が挙げられる。本発明の疾患モデル動物は、本発明の点変異した遺伝子を用いてES細胞や受精卵により、ジーンターゲッティング法などの遺伝子操作法により製造することもできるが、疾患モデル動物が、ハムスターである場合には、TO−2ハムスターを他の正常ハムスターと交配させて製造することもできる。
【0034】
例えば、TO−2ハムスターとGoldenハムスターを交配させ、その子孫の耳介からゲノムDNAを抽出する。これらの子孫には、TO−2に由来するδ−サルコグリカン(δ−sarcoglycan)遺伝子の欠失とデスミン遺伝子の点突然変異がありうるが、前者は本発明者らがすでに開発した方法(Sakamoto A,et al.FEBS Lett.1999,447,124-128.)で、後者は本発明で開示した方法に従い遺伝子診断を行う。そして、δ−サルコグリカン(δ−sarcoglycan)遺伝子は正常ホモで、かつデスミン遺伝子は異常ホモであるオス、メスの個体を得、最終的にコンジェニックな系統を樹立する。
この新規遺伝性心筋症のモデル動物は発症が緩徐であることが予想され、デスミン遺伝子の異常によるヒト心筋症のよいモデル動物として期待できる。その具体的な応用例を以下にあげる。
(a)デスミン遺伝子の異常によるヒト心筋症に対し、その発症前から行う新しい治療法を開発するモデル動物として有用である。
(b)TO−2の心室筋では、心筋変性に適応するために様々な遺伝子の発現が変動している(図2参照)。従って、TO−2及び、上記方法で創出した動物の心筋サンプルは、ディファレンシャルディスプレー(differential display)法などにより、正常心筋と発現量が異なることを指標とし、新規の機能遺伝子の単離に有用である。
(c)デスミンタンパク質の脱落とT管の構造破綻との経時的相関関係の追跡に有用である。
【0035】
さらに、本発明は、このような疾患モデル動物を用いて、遺伝性心筋症に対する予防、治療法又は予防、治療剤をスクリーニングする方法を提供するものである。このような疾患モデル動物は、デスミンのみに異常が生じた動物であり、そしてデスミンは横紋筋に共通するポリペプチドであり、図10及び図11に示されるように、デスミンはα−ジストロブレビン(α−dystrobrevin)との結合を介し、T管の構造の支持に重要であることから、横紋筋の異常に関する筋ジストローフィーなどの原因の解明やその予防、治療方法の開発にも有用である。
【0036】
このように、本発明によれば、デスミンはα−ジストロブレビン(α−dystrobrevin)との結合を介しT管の構造の支持に重要であることが明らかにされ、本明細書で示した方法で得たデスミンの各ドメイン・タンパク質は、T管の構造支持を含め、デスミン分子の様々な機能解析に極めて有用である。特に未知の結合タンパク質の同定に威力を発揮することが期待される。
【0037】
【実施例】
以下、実施例により本発明をより具体的に説明するが、本発明はこれら実施例により何ら限定されるものではない。
【0038】
実施例1 (ハムスターのデスミンcDNAのRT−PCRによる増幅)
ゴールデン及びTO−2の各々の左心室筋より抽出した全RNA(total RNA)から、定法に従ってcDNAを合成した(Sakamoto A,et al. Proc Natl Acad
Sci USA.1997;94(25):13873-8.)。
PCRは以下の反応スケールで、ABI9700を用いて行った。
【0039】
デスミンの5’側の増幅に用いたプライマーセットは、
Des5F: TGC CTC CTC TGT GCG TCT GC
Des5R: CGA TCA AGT TGT CGC GCT CC
であり、反応条件は、94℃、2分;(94℃、20秒;60℃、30秒;72℃、1分)の38サイクルで、4℃であった。
【0040】
デスミンの3’側の増幅に用いたプライマーセットは、
Des3F: CCA GCG TGC CCG TGT CGA CG
Des3R: GGT GTG ACA TCC GAG AGT GG
であり、反応条件は、94℃、2分;(94℃、20秒;60℃、30秒;72℃、1分)の38サイクルで、4℃であった。
この結果、それぞれ、593bpと973bpの特異的な産物が増幅された(図12参照)。
【0041】
実施例2 (TO−2ハムスターにおけるデスミンの点突然変異のゲノムPCR
による検出)
ハムスターの組織(肝臓、耳介など)から定法に従いゲノムDNAを抽出し、以下の反応スケールでABI9700を用いてPCRを行った。
【0042】
正常アレル(571G)の検出に用いたプライマーセットは、
DesF : GAA AGT GCG CTT CTT GGA GC
DesGR: GTG CCC TCA CTT GGC
であり、反応条件は、94℃、2分;(94℃、20秒;67℃、30秒;72℃、1分)で35サイクルで、4℃であった。
【0043】
異常アレル(571A)の検出に用いたプライマーセットは、
DesF : GAA AGT GCG CTT CTT GGA GC
DesTR: CCG TGC CCT CAC TTG GT
であり、反応条件は、94℃、2分;(94℃、20秒;67℃、30秒;72℃、1分)で35サイクルで、4℃であった。
この結果、それぞれ、ゴールデンあるいはTO−2に特異的な産物が増幅された(図13参照)。
【0044】
実施例3 (デスミンの4つの構造的ドメインに対応するcDNAの増幅と発現)
実施例1で調製したゴールデンあるいはTO−2の全長デスミンcDNAを鋳型とし、以下の反応スケールでABI9700を用いてPCRを行った。
反応条件は、94℃、2分;(94℃、20秒;55℃、30秒;72℃、1分)で30サイクルで、4℃であった。
【0045】
各ドメインを増幅させるために用いたプライマーセットは以下の通りである。
ヘッド(Head)部分
HD−F: GGCATATGAGTCAGGCCTACTC
HD−R: CCGAATTCTAGAACTCCTGGTTCACCG
コイル−1部分(Coil-1)
CL1−F: GGCATATGCTGGCCACGCGCACCAAC
CL1−R: CCGAATTCTAGTCCATCTCCACCTGGAC
コイル−2部分(Coil-2)
CL2−F: GGCATATGTCCAAGCCAGACCTC
CL2−R: CCGAATTCTACTCCACATCCAAGGCCATC
テイル部分(Tail)
TL−F: GGCATATGATTGCCACCTACCGCAAG
TL−R: CCGAATTCTAGAGCACCTCGTGTTG
【0046】
下線部分は、ハムスターのデスミンのcDNAに特異的な配列である。それ以外はストップコドン(TAG)と大腸菌の発現ベクターpET33b(Novagen社)のNdeI(CATATG)とEcoRI(GAATTC)部位に挿入するための配列である。
各発現コンストラクトで形質転換させた大腸菌(BL21(DE3)株、OD600=0.8)の培養液に、IPTG(1mM)を添加し、25℃で1時間培養した。各全溶出物(whole lysate)をSDS−PAGEで展開した後にCBBで染色し、期待される分子量のタンパク質が誘導されることを確認した(図14参照)。
【0047】
【発明の効果】
本発明は、拡張型心筋症の発症原因が心筋を形成する横紋筋のT管に関連するポリペプチドであるデスミンの遺伝子の点変異であることを明らかにしたものである。これによる心筋症は緩慢に発症するが、発症後はデスミン及びこれに関連するポリペプチドの脱落により致命的な疾患となる。
本発明は、このような拡張型心筋症の原因となる遺伝子の検出、同定方法を提供するものであり、遺伝性心筋症の予防、治療に有用なものである。また、本発明はこのような遺伝子を有する疾患モデル動物を提供するものであり、遺伝性心筋症の予防、治療の開発のみならず、横紋筋の異常に関連する各種疾患の原因の解明や予防、治療方法の確立の有用なものである。
【0048】
【配列表】
【図面の簡単な説明】
【図1】図1は、正常ハムスターと心筋症ハムスターの特徴を示す図面に代わる写真である。図1のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。図1の(A)は各ハムスターの左心室のヘマトキシリンとエオジン染色による光学顕微鏡像を示し、(B)はその水平断面像を示し、(C)はこれらのハムスターの心電図の胸部第一誘導を示す。
【図2】図2は、正常ハムスターと心筋症ハムスターのRT−PCRによる心肥大関連遺伝子の定量の結果を示す図面に代わる写真である。図2のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。PCRのサイクルは、各々左から40、35、30、25である。内部標準としてGAPDH(Glyceraldyde 3-Phosphate Dehydrogenase)を用いた。
【図3】図3は、正常ハムスターと心筋症ハムスターのアポトーシスに関する検討を行った結果を示す図面に代わる写真である。図3のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。図3の(A)は心臓正中断面でのTUNEL陽性細胞数を示し、(B)は心筋から抽出したゲノムDNAの電気泳動を示す。
【図4】図4は、正常ハムスターと心筋症ハムスターのネクローシスに関する検討を行った結果を示す図面に代わる写真である。図4のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。図4の(A)はマッソントリクローム染色の場合を示し、(B)はトルイジンブルー染色の場合を示す。。TO−2における矢印は炎症細胞浸潤が激しい箇所を示す。検体はいずれも、生後26週である。
【図5】図5は、正常ハムスターと心筋症ハムスターの左心室の透過型電子顕微鏡像を示す図面に代わる写真である。図5のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。TO−2の矢頭印は細くなったZ線を示し、矢印はT管を示す。検体は全て、生後14週である。
【図6】図6は、心筋症ハムスターの心臓の超音波画像診断を示す図面に代わる写真である。図6のBは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。図6の上段は拡張期の映像であり、下段は収縮期の映像である。検体は全て、生後26週である。
【図7】図7は、正常ハムスターと拡張型心筋症TO−2ハムスターの心筋筋原線維の段階的精製工程とZ線タンパク質の挙動を検討した結果を示す図面に代わる写真である。図7のGは正常ゴールデンハムスター、Tは拡張型心筋症TO−2ハムスターを示す。図7の(A)は精製プロトコールを示し、各精製段階をW、S1、P1、P2、及びP3とした。(B)は各精製段階におけるSDS−PAGEのCBB染色(上段)とイムノブロット(下段)の結果を示す。サンプルは、生後6週である。
【図8】図8は、正常ハムスターと心筋症ハムスターの加齢によるZ線タンパク質の変動を検討した結果を示す図面に代わる写真である。図8のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。心筋の全ホモジネートを用いたSDS−PAGEのCBB染色(上段)とイムノブロット(下段)を示す。
【図9】図9は、正常シリアンハムスターのデスミンcDNAの塩基配列とTO−2における点突然変異を示す。翻訳されるアミノ酸を対応コドンの上部に一文字表記で記している。塩基の番号は翻訳領域だけを対象とした。全翻訳領域をカバーするデスミンcDNAは、Des5F/Des5RとDes3F/Des3RによるRT−PCR産物を、ボックスで表記した制限酵素(Sal I)認識部位で結合して得る(図12参照)。デスミンの4つのドメイン(図14参照)を増幅するプライマーも明記した。TO−2のデスミンには点突然変異(G571A)があり(図13参照)、そのため191番目のアミノ酸が正常のA(アラニン)からT(スレオニン)に変わる。
【図10】図10は、心筋症ハムスターTO−2におけるα−ジストロブレビンの特異的消失を検討した結果を示す図面に代わる写真である。図10のGは正常ゴールデンハムスター、Bは肥大型心筋症BIO14.6ハムスター、Tは拡張型心筋症TO−2ハムスターを示す。心筋の全ホモジネートを用いたイムノブロットの結果を示す。図10の上段は、δ−サルコグリカンを示し、下段はα−ジストロブレビンを示す。
【図11】図11は、T管部分における筋形質膜と筋原線維の架橋モデルを模式的に示したものである。α−ジストロブレビンとデスミンとの結合は直接的なものであるかもしれないが、図11に示されるように何らかのドッキング分子を介した間接的なものかもしれない。
【図12】図12は、正常ゴールデンハムスターの左心室筋から合成したcDNAを鋳型とし、2種類のプライマーセット(Des5F/Des5RとDes3F/Des3R)でPCRを行った結果を示す図面に代わる写真である。Mはマーカーを示す。
【図13】図13は、拡張型心筋症ハムスターTO−2におけるゲノムの塩基変異とPCRによるその検出を示す図面に代わる写真である。図13の(A)は正常ゴールデンハムスターと拡張型心筋症ハムスターTO−2における、デスミン遺伝子の点突然変異(G571A)周辺のゲノムの塩基配列を示す。両者で共通のものはドット(・)で表示した。大文字と小文字はそれぞれ第一エクソン、第一イントロン内の配列であることを示す。番号は図9のcDNA配列に対応する。遺伝子診断に用いたプライマーを矢印で示した。図13の(B)は矢印で示したプライマーセット(DesF/desGR)あるいは(DesF/DesTR)を用いたゲノムPCRの結果を示す図面に代わる写真である。この部位におけるアレルは、各々(G/G)、(G/G)、(A/A)である。
【図14】図14は、デスミンの分子構造と各ドメインの組み換えタンパク質の発現を示す図面に代わる写真である。図14の(A)はデスミンの4個の領域を模式図で示したものであり、TO−2におけるアミノ酸変異を丸印(○)で示した。図14の(B)はデスミンの全長及び各ドメインの組み換えタンパク質の発現を示す図面に代わる写真である。各ドメインのcDNAを図9に示すプライマーセットを用いて増幅し、発現ベクターpET33bに組み込み、大腸菌BL21(DE3)に発現させた。各大腸菌の全溶出物をSDS−PAGEにかけCBBで染色したものである。目的のタンパク質に対応するバンドには*を付した。レーン1は全長のものであり、レーン2はヘッド領域のものであり、レーン3はコイル−2領域のものであり、レーン4はテイル領域のものであり、レーン5は正常ハムスターのコイル−1領域(191A)のものであり、レーン6は変異したコイル−1領域(191T)のものである。
Claims (10)
- 拡張型心筋症ハムスター由来のデスミン遺伝子であって、配列表の配列番号1に記載のデスミンのcDNAの翻訳領域の塩基配列の571番目が、グアニン(G)からアデニン(A)に点変異したデスミン遺伝子。
- 心筋症モデルハムスターにおいて、配列表の配列番号1に記載のデスミンのcDNAの翻訳領域の塩基配列の571番目におけるグアニン(G)からアデニン(A)への点変異を検出、同定する方法であって、当該方法が、前記変異遺伝子が心筋症モデルハムスターの心筋症の原因遺伝子であるかどうかを判定するための方法である、点変異を検出、同定する方法。
- 検出、同定する方法が、PCRを用いて検出、同定する方法である請求項2に記載の方法。
- プライマーが、点変異の塩基を含むものである請求項3に記載の方法。
- プライマーが、配列番号9に記載の塩基配列からなるフォーワードプライマーと、配列番号10に記載の塩基配列からなるリバースプライマー、又は配列番号11に記載の塩基配列からなるリバースプライマー若しくは配列番号12に記載の塩基配列からなるリバースプライマーとの組み合わせからなる請求項3又は4に記載の方法。
- 心筋症モデルハムスターにおいて、請求項5に記載のプライマーを用いて、配列表の配列番号1に記載のデスミンのcDNAの翻訳領域の塩基配列の571番目におけるグアニン(G)からアデニン(A)への点変異を検出、同定するための測定キットであって、当該キットが、前記変異遺伝子が心筋症モデルハムスターの心筋症の原因遺伝子であるかどうかを判定するためのキットである、測定キット。
- 拡張型心筋症ハムスター由来のデスミンであって、配列表の配列番号1に記載のデスミンのcDNAの翻訳領域の塩基配列の571番目におけるグアニン(G)がアデニン(A)に点変異したデスミン遺伝子がコードしてなる配列表の配列番号2に記載されたアミノ酸配列からなるデスミン。
- 配列表の配列番号1に記載のデスミンのcDNAの翻訳領域の塩基配列の571番目におけるグアニン(G)がアデニン(A)に点変異したデスミン遺伝子のみにより遺伝子異常が生じている、拡張型心筋症モデルハムスター。
- TO−2ハムスターを他のハムスターと交配させて得られる請求項8に記載の拡張型心筋症モデルハムスター。
- 請求項8又は9に記載の拡張型心筋症モデルハムスターを用いて、遺伝性拡張型心筋症に対する予防、治療剤をスクリーニングする方法。
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002034379A JP4170633B2 (ja) | 2001-11-12 | 2002-02-12 | 拡張型心筋症の原因となる新規点突然変異を有するデスミン遺伝子 |
| EP02803090A EP1443111B1 (en) | 2001-11-12 | 2002-10-11 | Desmin gene having novel point mutation causative of dilated cardiomyopathy |
| HK04107030.3A HK1064408B (en) | 2001-11-12 | 2002-10-11 | Desmin gene having novel point mutation causative of dilated cardiomyopathy |
| DE60235393T DE60235393D1 (de) | 2001-11-12 | 2002-10-11 | Desmin-gen mit neuer punktmutation, die dilatationscardiomyopathie verursacht |
| US10/495,409 US7297487B2 (en) | 2001-11-12 | 2002-10-11 | Desmin gene having novel point mutation causative of dilated cardiomyopathy |
| PCT/JP2002/010569 WO2003042386A1 (en) | 2001-11-12 | 2002-10-11 | Desmin gene having novel point mutation causative of dilated cardiomyopathy |
| US11/975,760 US7825292B1 (en) | 2001-11-12 | 2007-10-22 | Desmin gene having novel point mutation causative of dilated cardiomyopathy |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001345491 | 2001-11-12 | ||
| JP2001-345491 | 2001-11-12 | ||
| JP2002034379A JP4170633B2 (ja) | 2001-11-12 | 2002-02-12 | 拡張型心筋症の原因となる新規点突然変異を有するデスミン遺伝子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2003204795A JP2003204795A (ja) | 2003-07-22 |
| JP4170633B2 true JP4170633B2 (ja) | 2008-10-22 |
Family
ID=26624460
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002034379A Expired - Fee Related JP4170633B2 (ja) | 2001-11-12 | 2002-02-12 | 拡張型心筋症の原因となる新規点突然変異を有するデスミン遺伝子 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US7297487B2 (ja) |
| EP (1) | EP1443111B1 (ja) |
| JP (1) | JP4170633B2 (ja) |
| DE (1) | DE60235393D1 (ja) |
| WO (1) | WO2003042386A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0428255D0 (en) * | 2004-12-23 | 2005-01-26 | Health Prot Agency | Detection of nucleic acid mutations |
| US7939537B2 (en) * | 2005-10-04 | 2011-05-10 | Istituto Di Ricerche Di Biologia Molecolare P. Angeletti S.P.A. | HIV integrase inhibitors |
| CN111004849B (zh) * | 2019-12-13 | 2022-08-26 | 南京艾迪康医学检验所有限公司 | 检测cdh1基因的多个位点突变的引物、方法和试剂盒 |
| CN112410418A (zh) * | 2020-11-23 | 2021-02-26 | 复旦大学附属中山医院 | 一种扩张型心肌病分子标志物 |
-
2002
- 2002-02-12 JP JP2002034379A patent/JP4170633B2/ja not_active Expired - Fee Related
- 2002-10-11 EP EP02803090A patent/EP1443111B1/en not_active Expired - Lifetime
- 2002-10-11 WO PCT/JP2002/010569 patent/WO2003042386A1/ja not_active Ceased
- 2002-10-11 US US10/495,409 patent/US7297487B2/en not_active Expired - Fee Related
- 2002-10-11 DE DE60235393T patent/DE60235393D1/de not_active Expired - Lifetime
-
2007
- 2007-10-22 US US11/975,760 patent/US7825292B1/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| EP1443111B1 (en) | 2010-02-17 |
| JP2003204795A (ja) | 2003-07-22 |
| WO2003042386A1 (en) | 2003-05-22 |
| US7297487B2 (en) | 2007-11-20 |
| DE60235393D1 (de) | 2010-04-01 |
| US20050155092A1 (en) | 2005-07-14 |
| EP1443111A4 (en) | 2005-06-22 |
| EP1443111A1 (en) | 2004-08-04 |
| HK1064408A1 (en) | 2005-01-28 |
| US7825292B1 (en) | 2010-11-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Brodehl et al. | Mutations in FLNC are associated with familial restrictive cardiomyopathy | |
| Al-Barghouthi et al. | Systems genetics in diversity outbred mice inform BMD GWAS and identify determinants of bone strength | |
| Olson et al. | Mutations that alter the surface charge of alpha-tropomyosin are associated with dilated cardiomyopathy | |
| Suzuki et al. | Identification of RALDH-3, a novel retinaldehyde dehydrogenase, expressed in the ventral region of the retina | |
| Szenker-Ravi et al. | Discovery of a genetic module essential for assigning left–right asymmetry in humans and ancestral vertebrates | |
| US20070028314A1 (en) | Bone and/or joint disease-associated genes | |
| Alastalo et al. | LMNA Mutation c. 917T> G (p. L306R) Leads to Deleterious Hyper‐Assembly of Lamin A/C and Associates with Severe Right Ventricular Cardiomyopathy and Premature Aging | |
| JP4170633B2 (ja) | 拡張型心筋症の原因となる新規点突然変異を有するデスミン遺伝子 | |
| JP5680407B2 (ja) | 新規x連鎖性筋疾患に関連するfhl1変異 | |
| US6368794B1 (en) | Detection of altered expression of genes regulating cell proliferation | |
| EP3305070B1 (en) | Dementia model transgenic mouse and screening method using thereof | |
| US6440666B1 (en) | Selection for dwarfism in poultry | |
| US8222383B2 (en) | DNA encoding polypeptide capable of modulating muscle-specific tyrosine kinase activity | |
| Al-Barghouthi et al. | Systems genetics analyses in Diversity Outbred mice inform human bone mineral density GWAS and identify Qsox1 as a novel determinant of bone strength | |
| US20100329987A1 (en) | Uses of Sperm Membrane Protein OBF | |
| CN116554297B (zh) | 一种α-肌球蛋白突变体及其应用 | |
| HK1064408B (en) | Desmin gene having novel point mutation causative of dilated cardiomyopathy | |
| Sano et al. | Characterization of teleost Mdga1 using a gene‐trap approach in medaka (Oryzias latipes) | |
| JP5187875B2 (ja) | 心肥大ならびに拡張型心筋症非ヒトモデル動物 | |
| Szenker-Ravi et al. | A functional operon delineates an extracellular pathway that controls body asymmetry only in animals with a ciliated left-right organizer | |
| Hewitt | Investigating the functions of LARGE: lessons from mutant mice | |
| JP2005333845A (ja) | ミトコンドリア局在型DsRed2及びECFP発現ベクター | |
| Alkhouli | The Role of MCTP2 in Health and Disease | |
| US20040241683A1 (en) | Hsst and angiogenesis | |
| KR20250116237A (ko) | Pde6b 유전자 변이를 갖는 망막 변성 동물 모델 및 이의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20031031 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20040129 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20041015 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20041111 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20041112 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20050119 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20050120 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070605 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070802 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20080205 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080404 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080404 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080516 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20080522 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080805 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080807 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110815 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110815 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120815 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120815 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130815 Year of fee payment: 5 |
|
| LAPS | Cancellation because of no payment of annual fees |