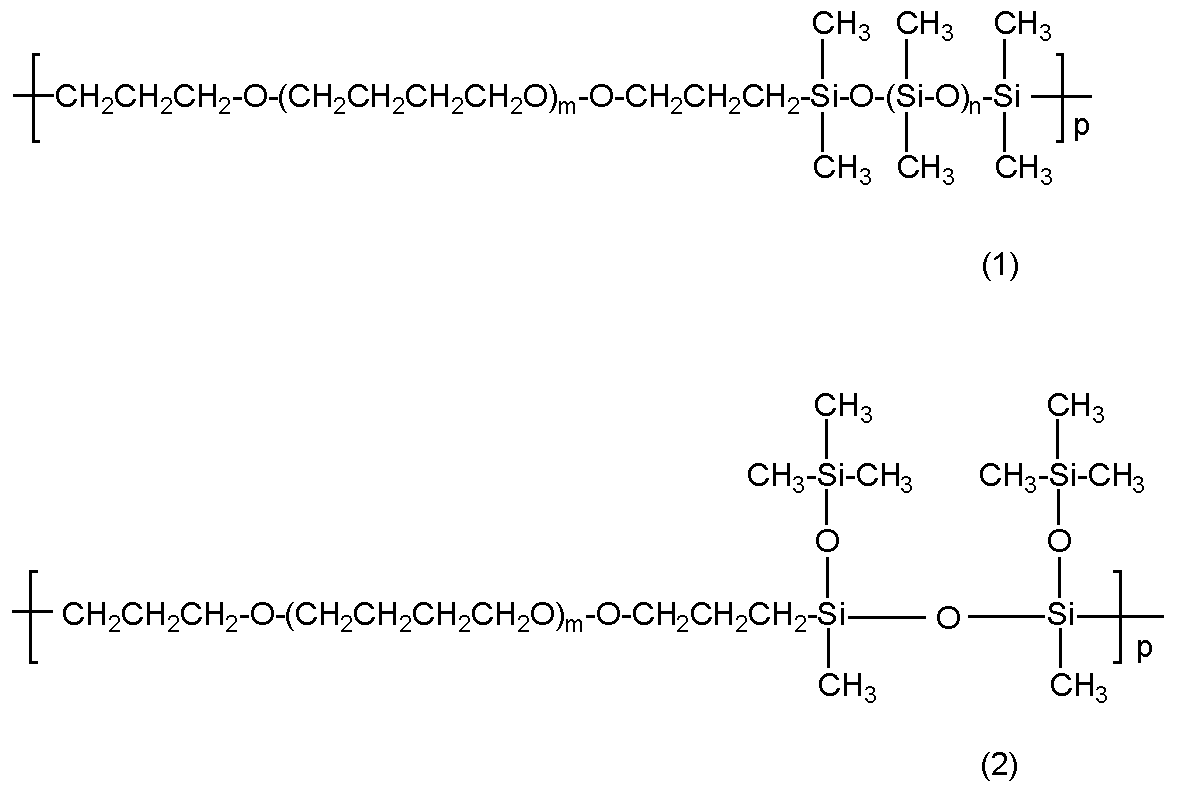JP3844065B2 - Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber - Google Patents
Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber Download PDFInfo
- Publication number
- JP3844065B2 JP3844065B2 JP2002116071A JP2002116071A JP3844065B2 JP 3844065 B2 JP3844065 B2 JP 3844065B2 JP 2002116071 A JP2002116071 A JP 2002116071A JP 2002116071 A JP2002116071 A JP 2002116071A JP 3844065 B2 JP3844065 B2 JP 3844065B2
- Authority
- JP
- Japan
- Prior art keywords
- meth
- acrylate
- optical fiber
- curable resin
- radiation curable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Description
【0001】
【発明の属する技術分野】
本発明は、シロキサン変性されたポリテトラメチレンエーテル骨格を有するウレタン(メタ)アクリレートオリゴマを含有し、低粘度で良好な低温保存性を有し、低ヤング率、耐熱性の良好な硬化物を与える液状放射線硬化型樹脂組成物、光ファイバ用被覆組成物、及び光ファイバに関する。
【0002】
【従来の技術及び発明が解決しようとする課題】
従来より、光通信用ファイバとして、石英系、多成分ガラス系、プラスチック系等、種々のものが知られているが、中でも、その軽量性、耐熱性、無誘導性が良好であること、更に低損失で大伝送容量の点から、石英系ファイバが広く用いられてきている。
【0003】
この石英系の光通信用ファイバは、上記特性を有するものの、極めて細くかつ脆く、外的要因により折れ易く、また外部応力により伝送損失の増加をきたすため、石英ガラスファイバを予め比較的軟らかいプライマリ、あるいはバッファコーティング材と称される液状硬化組成物により一次被覆、硬化した後、次いで、この上層にセカンダリ、あるいはトップコーティング材と称される液状硬化組成物により二次被覆し、硬化して一次被覆層を保護することが行われている。
【0004】
これらの一次被覆層のコーティング材には、
i.硬化後の各被覆層が、適切な機械物性(低ヤング率、高伸長、高強度)を有すること、
ii.硬化後の被覆層の硬さ(ヤング率)が、高温から低温までの広い温度範囲で変化が小さいこと、
iii.耐熱性、耐加水分解性、低吸水率、耐薬品性等が高信頼性であること、iv.生産性向上のために、速硬化性であることと同時に、低粘度であること
等が要求されている。
【0005】
従来から一次被覆用樹脂組成物として、ウレタンアクリレート系の紫外線硬化性樹脂組成物が提案されており、特公平1−19694号、第2784339号、第2811070号公報に記載されているように、ウレタンアクリレートオリゴマと、反応性モノマー、重合開始剤からなる紫外線液状硬化組成物が知られている。これらの紫外線硬化型の樹脂組成物において、主成分であるウレタンアクリレートオリゴマの前駆体である原料オリゴマは、低粘度、低ヤング率、温度特性(ヤング率の温度依存性)、耐久性(耐熱、耐水性)等から、ポリエチレンエーテルグリコール、ポリプロピレンエーテルグリコール、ポリブチレンエーテルグリコール、ポリテトラメチレンエーテルグリコール等のポリエーテルが検討され、特に性能、コストの面から、ポリプロピレンエーテルグリコール、ポリテトラメチレンエーテルグリコールが主に用いられている。
【0006】
これら両者を比較すると、ポリプロピレンエーテルグリコールは、低粘度、低ヤング率であるが、温度特性、耐久性が劣る。一方、ポリテトラメチレンエーテルグリコールは温度特性、耐久性は良好であるが、粘度、ヤング率が高く、また低温で組成物が結晶化し易く、作業性に劣る欠点があり、この欠点を解消することが要望されていた。
【0007】
本発明は、上記事情に鑑みてなされたものであり、ウレタンアクリレートオリゴマの主骨格であるポリテトラメチレンエーテルグリコールの上記欠点を解消した、低粘度、低温保存性、ヤング率、耐熱性が良好な硬化物を与える光ファイバ一次被覆に好適な液状放射線硬化型樹脂組成物、これからなる光ファイバ用被覆組成物、及びその硬化物で被覆した光ファイバを提供することを目的とする。
【0008】
【課題を解決するための手段及び発明の実施の形態】
本発明者は、上記目的を達成するために鋭意検討を重ねた結果、ウレタン(メタ)アクリレートオリゴマを含有する液状放射線硬化型樹脂組成物において、ウレタン(メタ)アクリレートオリゴマの主原料であるポリエーテルとしてシリコーン変性したポリテトラメチレンエーテルグリコールを用いることにより、その硬化物の粘度、ヤング率が低下し、またポリテトラメチレンエーテルグリコールの低温保存性、耐熱性を維持しつつ、更に低温での結晶化が抑制されることを知見し、本発明をなすに至った。
【0009】
従って、本発明は、
(A)分子中に下記一般式(1)及び/又は(2)で表される骨格を有するウレタン(メタ)アクリレートオリゴマ、
【化2】
(式中、m,n,pは、5≦m≦40、0≦n≦10、1≦p≦50を満足する整数である。)
(B)エチレン性不飽和化合物
を含有する液状放射線硬化型樹脂組成物、光ファイバ用被覆組成物、及び該光ファイバを提供する。
【0010】
以下、本発明につき更に詳しく説明する。
本発明の液状放射線硬化型樹脂組成物の(A)成分である分子中に上記一般式(1)及び/又は(2)で表される骨格を有するウレタン(メタ)アクリレートオリゴマは、(a)上記一般式(1)及び/又は(2)で表される骨格を有するジオール成分、あるいはこのジオールとポリテトラメチレンエーテルグリコールの混合物、(b)ポリイソシアネート及び(c)水酸基含有(メタ)アクリレート化合物のウレタン化反応により得ることができる。ウレタン(メタ)アクリレートオリゴマの重量平均分子量は、例えば、1000〜20000、好ましくは2000〜10000程度の範囲から選択できる。
【0011】
(a)上記一般式(1)及び/又は(2)で表される骨格を有するジオール成分上記一般式(1)及び/又は(2)で表される骨格を有するジオール成分は、下記一般式(3)、(4)で表されるシロキサン変性されたテトラメチレンエーテルグリコールが好ましい。
【0012】
【化3】
(式中、m,n,pは、5≦m≦40、0≦n≦10、1≦p≦50を満たす整数である。)
【0013】
上記一般式(1)〜(4)中、mは、5≦m≦40を満足する整数である。mが5未満だとシロキサン含有量が大きくなり、本発明の液状放射線硬化型樹脂組成物の屈折率、及び硬化物の物性(強度、伸び等)が低下する場合があり、40を超えると低粘度、低ヤング率、低温での結晶性抑制効果が達成されない場合がある。
nは、0≦n≦10を満たす整数である。nが10を超えるとシロキサン骨格とポリテトラメチレンエーテル骨格との相溶性がなくなり、濁りを生じる場合がある。
pは、1≦p≦50を満たす整数である。pが1未満だと、ヤング率が大きくなりすぎ、50を超えると、本発明の液状放射線硬化型樹脂組成物の低粘度及び適正な物性が達成されない場合がある。
【0014】
(a)成分のジオールは、下記に示す合成法で得ることができる。即ち、下記一般式(5)、(6)で示されるポリメチルハイドロジェンシロキサン、ポリテトラメチレンエーテルグリコールの末端アリルエーテル化されたポリテトラメチレンエーテル、及びアリルグリコールから、白金系触媒による公知の付加反応により合成される。
【0015】
【化4】
【0016】
【化5】
【0017】
(a)成分は、これらのジオール成分とポリテトラメチレンエーテルグリコールの混合物であってもよい。ポリテトラメチレンエーテルグリコールの分子量としては、500〜2000の範囲から選択できる。
【0018】
なお、これらのジオール成分とポリテトラメチレンエーテルグリコールとの混合比は、ポリテトラメチレンエーテルグリコールの重量割合として、60重量%以下、好ましくは50重量%以下である。60重量%を超えると、本発明の液状放射線硬化型樹脂組成物の低ヤング率、低粘度、低温下での結晶化抑制効果が達成されない可能性がある。
【0019】
(b)ポリイソシアネート
(b)成分のポリイソシアネートとしては、例えば、トリレンジイソシアネート、4,4’−ジフェニルメタンジイソシアネート、水添4,4’−ジフェニルメタンジイソシアネート、キシリレンジイソシアネート、水添キシリレンジイソシアネート、ヘキサメチレンジイソシアネート、イソホロンジイソシアネート、1,5−ナフタレンジイソシアネート、トリジンジイソシアネート、p−フェニレンジイソシアネート、トランスシクロヘキサン−1,4−ジイソシアネート、リジンジイソシアネート、テトラメチルキシレンジイソシアネート、リジンエステルトリイソシアネート、1,6,11−ウンデカントリイソシアネート、1,8−ジイソシアネート−4−イソシアネートメチルオクタン、1,3,6−ヘキサメチレントリイソシアネート、ビシクロヘプタントリイソシアネート、トリメチルヘキサメチレンジイソシアネート等が使用される。これらの中で、環状の構造を有するポリイソシアネートが、高ヤング率を有する硬化物が得られるので特に好ましい。
【0020】
(c)水酸基含有(メタ)アクリレート
(c)成分の水酸基含有(メタ)アクリレートとしては、例えば、ヒドロキシアルキル(メタ)アクリレート[例えば、2−ヒドロキシエチル(メタ)アクリレート、2−ヒドロキシプロピル(メタ)アクリレート、3−ヒドロキシプロピル(メタ)アクリレート、2−ヒドロキシブチル(メタ)アクリレート、4−ヒドロキシブチル(メタ)アクリレート、ペンタンジオールモノ(メタ)アクリレート、ヘキサンジオールモノ(メタ)アクリレート、ネオペンチルグリコールモノ(メタ)アクリレート等のヒドロキシ−C2 〜 10アルキル(メタ)アクリレート等]、2−ヒドロキシ−3−フェニルオキシプロピル(メタ)アクリレート、2−ヒドロキシアルキル(メタ)アクリロイルフォスフェート、4−ヒドロキシシクロヘキシル(メタ)アクリレート、シクロヘキサン−1,4−ジメタノールモノ(メタ)アクリレート、トリメチロールプロパンジ(メタ)アクリレート、ペンタエリスリトールトリ(メタ)アクリレート等が挙げられ、更にグリシジル基又はエポキシ基含有化合物(例えば、アルキルグリシジルエーテル、アリルグリシジルエーテル、グリシジル(メタ)アクリレート等)と(メタ)アクリル酸との付加反応により生成する化合物も挙げられる。これらの水酸基含有(メタ)アクリレートは、単独で又は2種以上組み合わせて使用できる。好ましい水酸基含有(メタ)アクリレートは、ヒドロキシC2 〜 4アルキル(メタ)アクリレート、特に2−ヒドロキシエチル(メタ)アクリレート、2−ヒドロキシプロピル(メタ)アクリレート等である。
【0021】
なお、ウレタン(メタ)アクリレートオリゴマは(a)〜(c)成分を反応させることにより調製することができ、ウレタン(メタ)アクリレートオリゴマを構成する各成分の割合は、例えば、(a)ジオール成分と、(b)ポリイソシアネート及び(c)水酸基含有(メタ)アクリレートの量は、イソシアネート基1モルに対して、ジオールの水酸基0.1〜0.8モル、好ましくは0.2〜0.7モル、(c)水酸基含有(メタ)アクリレート0.2〜0.9モル、好ましくは0.3〜0.8モルである。
【0022】
また、(a)〜(c)成分の反応方法は特に限定されず、各成分を一括混合して反応させてもよく、ポリイソシアネートと、ジオール成分及び水酸基含有(メタ)アクリレートのうちいずれか一方の成分とを反応させた後、他方の成分を反応させてもよい。
【0023】
これらウレタン化反応の触媒は、通常、スタナスオクトエート、ジブチルチンジアセテート、ジブチルチンジラウレート等の有機錫系ウレタン化触媒や、トリエチルアミン、トリエチレンジアミン、ジアザビシクロウンデセン等の第三級アミン系触媒が挙げられる。
触媒は、これらの1種単独又は2種以上を用いることができる。
【0024】
(B)エチレン性不飽和化合物
本発明に用いられる(B)成分のエチレン性不飽和化合物としては、例えば、N−ビニル化合物、アミノ基や水酸基を含む化合物に(メタ)アクリル酸がアミド化反応又はエステル化反応で結合した構造の化合物が挙げられ、例えば、下記の単官能性、2官能性、及び多官能性化合物を用いることができる。
【0025】
(単官能性化合物)
N−ビニル化合物としては、N−ビニルピロリドン、N−ビニルカプロラクタム、N−ビニルアセトアミド、N−ビニルホルムアミド等が挙げられ、またアミノ基や水酸基を含む化合物に(メタ)アクリル酸がアミド化反応又はエステル化反応で結合した構造の化合物として、メトキシエチレングリコール(メタ)アクリレート、メトキシポリエチレングリコール(メタ)アクリレート、ノニルフェノキシエチル(メタ)アクリレート、ノニルフェノキシポリエチレングリコール(メタ)アクリレート、ノニルフェノキシポリプロピレングリコール(メタ)アクリレート、3−クロロ−2−ヒドロキシプロピル(メタ)アクリレート、フェノキシエチル(メタ)アクリレート、フェノキシポリプロピレングリコール(メタ)アクリレート、ブトキシポリエチレングリコール(メタ)アクリレート、アルキル(メタ)アクリレート、シクロヘキシル(メタ)アクリレート、テトラヒドロフルフリル(メタ)アクリレート、イソボロニル(メタ)アクリレート、ベンジル(メタ)アクリレート、クミルフェノール(メタ)アクリレート、クミルフェノキシポリエチレングリコール(メタ)アクリレート、クミルフェノキシポリプロピレングリコール(メタ)アクリレート、2−ヒドロキシプロピル(メタ)アクリレート、2−エチルヘキシル(メタ)アクリレート、ジシクロペンタジエン(メタ)アクリレート、2−ヒドロキシ−3−フェノキシプロピル(メタ)アクリレート、2−(メタ)アクリロイルオキシエチル−2−ヒドロキシエチルフタル酸、3−アクリロイルオキシグリセリンモノ(メタ)アクリレート、2−ヒドロキシブチル(メタ)アクリレート、2−ヒドロキシ−1−(メタ)アクリロキシ−3−(メタ)アクリロキシプロパン、ポリプロピレングリコールモノ(メタ)アクリレート、ポリエチレングリコールモノ(メタ)アクリレート、ポリε−カプロラクトンモノ(メタ)アクリレート、ジアルキルアミノエチル(メタ)アクリレート、グリシジル(メタ)アクリレート、モノ[2−(メタ)アクリロイルオキシエチル]アシッドフォスフェート、トリクロロエチル(メタ)アクリレート、2,2,3,3−テトラフロロプロピル(メタ)アクリレート、2,2,3,4,4,4−ヘキサフロロブチル(メタ)アクリレート、パーフロロオクチルエチル(メタ)アクリレート、ジシクロペンテニル(メタ)アクリレート、ジシクロペンテニルオキシアルキル(メタ)アクリレート、トリシクロデカニル(メタ)アクリレート、トリシクロデカニルオキシエチル(メタ)アクリレート、イソボロニルオキシエチル(メタ)アクリレート、モルホリン(メタ)アクリレート等が挙げられる。
【0026】
(2官能性化合物)
2官能性化合物として、具体的には、2,2−ジメチル−3−ヒドロキシプロピル−2,2−ジメチル−3−ヒドロキシプロピオネートのジ(メタ)アクリレート、エチレングリコールジ(メタ)アクリレート、テトラエチレングリコールジ(メタ)アクリレート、ポリエチレングリコールジ(メタ)アクリレート、プロピレングリコールジ(メタ)アクリレート、ポリプロピレングリコールジ(メタ)アクリレート、1,4−ブタンジオールジ(メタ)アクリレート、1,6−ヘキサンジオールジ(メタ)アクリレート、グリコールジ(メタ)アクリレート、ネオペンチルグリセリンジ(メタ)アクリレート、ビスフェノールAのエチレンオキサイド付加物のジ(メタ)アクリレート、ビスフェノールAのプロピレンオキサイド付加物のジ(メタ)アクリレート、2,2’−ジ(ヒドロキシエトキシフェニル)プロパンのジ(メタ)アクリレート、トリシクロデカンジメチロールのジ(メタ)アクリレート、ジシクロペンタジエンジ(メタ)アクリレート、ペンタンジ(メタ)アクリレート、2,2−ビス(グリシジルオキシフェニル)プロパンのジ(メタ)アクリル酸付加物等が挙げられる。
【0027】
(多官能性化合物)
多官能性化合物としては、例えば、トリメチロールプロパントリ(メタ)アクリレート、トリメチロールプロパントリオキシエチル(メタ)アクリレート、ペンタエリスリトールテトラ(メタ)アクリレート、ジペンタエリスリトールヘキサ(メタ)アクリレート、トリス(アクリロキシメチル)イソシアヌレート、トリス(アクリロキシエチル)イソシアヌレート、トリス(アクリロキシプロピル)イソシアヌレート、トリアリルトリメリット酸、トリアリルイソシアヌレート等が挙げられる。
【0028】
本発明の液状放射線硬化型樹脂組成物は、特には低ヤング率の光ファイバ用一次被覆材(プライマリ材)として用いられるため、単官能性の化合物の使用が好ましい。
【0029】
(B)成分のエチレン性不飽和基を有する化合物の配合量は、(A)成分のウレタン(メタ)アクリレートオリゴマや(B)成分の化合物の種類、樹脂組成物の所望する粘度、あるいはその硬化物の物性に応じて、例えば、ウレタン(メタ)アクリレートオリゴマ100重量部に対して、5〜200重量部、好ましくは10〜150重量部、更に好ましくは20〜100重量部の範囲から選択できる。
【0030】
更に、必要であれば、重合開始剤を添加してもよい。
重合開始剤としては、公知のものを使用することができ、例えば、1−ヒドロキシシクロヘキシルフェニルケトン、2,2−ジメトキシ−2−フェニルアセトフェノン、フェニルアセトフェノンジエチルケタール、アルコキシアセトフェノン、ベンジルメチルケタール、ベンゾフェノン及び3,3−ジメチル−4−メトキシベンゾフェノン、4,4−ジメトキシベンゾフェノン、4,4−ジアミノベンゾフェノン等のベンゾフェノン誘導体、ベンゾイル安息香酸アルキル、ビス(4−ジアルキルアミノフェニル)ケトン、ベンジル及びベンジルメチルケタール等のベンジル誘導体、ベンゾイル及びベンゾインブチルメチルケタール等のベンゾイン誘導体、ベンゾインイソプロピルエーテル、2−ヒドロキシ−2−メチルプロピオフェノン、2,4−ジエチルチオキサントン及び2,4−ジクロロチオキサントン等のチオキサントン誘導体、フルオレン、2−メチル−1−[4−(メチルチオ)フェニル]2−モルホリノプロパン−1,2−ベンジル−2−ジメチルアミノ−1−(モルホリノフェニル)−ブタノン−1、2,4,6−トリメチルベンゾイルジフェニルホスフィンオキシド、ビス(2,6−ジメトキシベンゾイル)−2,4,4−トリメチルペンチルホスフィンオキシド等のホスフィンオキシド誘導体、過酸化ベンゾイル、t−ブチルペルオキシド、クメンハイドロペルオキシド等の有機過酸化物、アゾビスシアノ吉草酸、アゾビスブチロニトリル、アゾビス−(2,4−ジメチル)バレロニトリル、アゾビス−(2−アミノプロパン)ハイドロクロライドのような有機アゾ化合物等が挙げられる。
【0031】
これらは1種単独で使用してもよいし、2種以上使用してもよい。配合量は、本発明の被覆材の特性を満足すれば、特に限定はないが、通常、組成物全体の0.1〜10重量%、特に1〜5重量%が好ましい。
【0032】
本発明の液状放射線硬化型樹脂組成物には、上記成分の他に、例えば、酸化防止剤、紫外線吸収剤等の安定剤、有機溶剤、可塑剤、界面活性剤、シランカップリング剤、着色顔料、有機又は無機粒子等の添加剤を、本発明の目的を損なわない範囲で必要に応じて添加することができる。
【0033】
本発明の液状放射線硬化型樹脂組成物は、上記した所要の成分を配合し、撹拌混合して調製することができ、その粘度は、作業性の点で光ファイバ心線の製造条件との適合性から通常500〜10000mPa・s(25℃)、特に高速の製造条件では500〜4000mPa・s(25℃)の範囲が望ましい。
【0034】
本発明の液状放射線硬化型樹脂組成物を硬化する放射線として、赤外線、可視光線、紫外線、及び、X線、電子線、α線、β線、γ線等の電離放射線を用いることができる。
【0035】
本発明の液状放射線硬化型樹脂組成物は、特に光ファイバ用被覆組成物、とりわけ一次被覆材用として好適に用いられ、この組成物が硬化、被覆された光ファイバは、この組成物の硬化物の耐熱性が良好で、高い信頼性を与えるものである。
【0036】
なお、本発明の液状放射線硬化型樹脂組成物は、光ファイバ用被覆材だけではなく、防水ファイバケーブル、海底ケーブル光ファイバユニット等の緩衝材、充填材にも適応でき、更に種々の用途、例えば、離型性コーティング材、撥水性コーティング材、保護コーティング材、各種インキ、塗料等に応用することができる。
【0037】
【実施例】
以下、実施例及び比較例を示して本発明を具体的に説明するが、本発明は下記の実施例に制限されるものではない。なお、下記例中の部は重量部を示す。
【0038】
(A)ウレタン(メタ)アクリレートオリゴマの合成
[合成例1]
両末端アリル化ポリテトラメチレンエーテルの合成
ポリテトラメチレンエーテルグリコールPTMG650(OH価、178KOHmg/gr)629.2gr、第三ブトキシカリウム258.1gr、乾燥テトラヒドロフラン1000mlの混合溶液を、窒素下で4時間加熱還流した。この混合溶液を50℃の温度に冷却した後、臭化アリル292.2grと乾燥テトラヒドロフラン150mlの混合物を滴下した。次いで、6時間加熱還流した後、減圧下、80℃の温度でテトラヒドロフランを留去し、残液にヘキサン700mlを添加し、中性となるまで水洗した。ヘキサン層を無水硫酸ナトリウムで乾燥、ろ過し、減圧下、110℃の温度で低留分を留去し、両末端アリル化ポリテトラメチレンエーテル(A−PTMG650)を得た。この両末端アリル化ポリテトラメチレンエーテルの水酸基価を測定したところ、1.3mgKOH/grであった。(アリル化率99.3%)
【0039】
[合成例2]
シロキサン変性ポリテトラメチレンエーテルグリコールの合成
トルエン120gr、テトラメチル−1,3−ハイドロジェンジシロキサン(上記一般式(5)で示されるシロキサン化合物)60.45gr、塩化白金酸のオクチルアルコール変性溶液(白金含量2%)0.024grの混合溶液に、窒素下、合成例1で得られた両末端アリル化ポリテトラメチレンエーテル240grを滴下し、室温で1時間撹拌した後、110℃の温度で6時間加熱・撹拌した。次いで、30℃以下の温度に冷却した後、エチレングリコールモノアリルエーテル33.33gr、塩化白金酸のオクチルアルコール変性溶液(白金含量2%)0.024grを添加し、添加後80〜90℃の温度で5時間加熱した。次いで60℃以下の温度に冷却し、0.1%塩酸6gr、イソプロピルアルコール30grを添加し60℃の温度で2時間加熱した後、減圧下、110℃の温度で低留分を留去し、両末端に水酸基を含有した下記一般式(7)で示されるシロキサン変性ポリテトラメチレンエーテルグリコールAを得た。このグリコールの水酸基価を測定したところ、52mgKOH/grであった。
【0040】
【化6】
【0041】
[合成例3]
シロキサン変性ポリテトラメチレンエーテルグリコールの合成
合成例2と同様にテトラメチル−1,3−ハイドロジェンジシロキサンを1,2,3,4−オクタメチル−2,3−ハイドロジェンテトラシロキサン(上記一般式(6)で示されるシロキサン化合物)127.3grに代えた以外は同じ使用量、操作により両末端に水酸基を含有した下記一般式(8)で表されるシロキサン変性ポリテトラメチレンエーテルグリコールBを得た。このグリコールの水酸基価を測定したところ、51mgKOH/grであった。
【0042】
【化7】
【0043】
[合成例4]
ウレタンアクリレートオリゴマの合成
アロニックスM−113(東亜合成化学社製)28.07gr、重合禁止剤2,6−ジ−t−ブチルヒドロキシトルエン0.078gr、ジブチル錫ジラウレート0.066grを撹拌混合した。これに2,4−トルエンジイソシアネート26.1grを添加し、18〜20℃に冷却した。この混合溶液に乾燥空気雰囲気下2−ヒドロキシエチルアクリレート11.6grを反応温度25℃以下になるように滴下した。滴下終了後、常温で約1時間撹拌し、合成例(2)で得られたシロキサン変性ポリテトラメチレンエーテルグリコールA214.9grを反応温度40℃以下で滴下した。次いで、乾燥空気雰囲気下、65〜70℃の温度で7時間反応させ、赤外吸収スペクトルでイソシアネート基(NCO)に起因する吸収がないことを確認し、アロニックスM−113を10重量%含有する平均分子量約5,050のウレタンアクリレートオリゴマIを得た。
【0044】
[合成例5]
ウレタンアクリレートオリゴマの合成
合成例4と同様に、シロキサン変性ポリテトラメチレンエーテルグリコールAを合成例3で得られたシロキサン変性ポリテトラメチレンエーテルグリコールB219.6grに代えた以外は同じ使用量、操作により、アロニックスM−113を10重量%含有する平均分子量約5,150のウレタンアクリレートオリゴマIIを得た。
【0045】
[比較合成例1]
シロキサン変性ポリテトラメチレンエーテルグリコールAを、ポリテトラメチレンエーテルグリコールPTMG2000(三洋化成社製、水酸基価=55mgKOH/gr)202grに代えた以外は、合成例4と同様の使用量、操作により、アロニックスM−113を10重量%含有する平均分子量約4,790のウレタンアクリレートオリゴマIIIを得た。
【0046】
[比較合成例2]
シロキサン変性ポリテトラメチレンエーテルグリコールAをポリプロピレンエーテルグリコールPPG2000(三洋化成社製、水酸基価=53mgKOH/gr)210grに代えた以外は、合成例4と同様の使用量、操作により、アロニックスM−113を10重量%含有する平均分子量約4,950のウレタンアクリレートオリゴマIVを得た。
【0047】
[実施例1,2、比較例1,2]
上記で合成したウレタンアクリレートオリゴマI〜IVを使用し、表1で示したように、エチレン性不飽和基を含有する化合物、酸化防止剤を混合して実施例1,2、比較例1,2の液状放射線硬化型樹脂組成物を調製した。
得られた液状放射線硬化型樹脂組成物の物性を下記に示すようにして評価した。結果を表1に併記する。
【0048】
〈評価方法〉
(1)硬化フィルムの作成
ガラス板上に上記液状放射線硬化型樹脂組成物を50〜60μmの膜厚に塗布し、紫外線及び100kVで加速された電子線を、窒素下で30kGyの吸収線量で照射し、硬化フィルムを得た。
(2)ヤング率の測定
(1)で得られた硬化フィルムを、25℃、相対湿度50%で、24時間状態調整した後、標線間25mm、引っ張り速度1mm/minの条件で2.5%引っ張り弾性率を測定した。
(3)引っ張り強さ及び破断伸びの測定
25℃、相対湿度50%で硬化フィルムを24時間状態調整した後、標線間25mm、引っ張り速度50mm/minの条件で測定した。
(3)耐熱性の評価
(1)で得られた硬化フィルムを120℃で加熱し、(2)と同様に加熱後のヤング率を測定した。耐熱性は、下記式によりヤング率の保持率を求め、評価を行った。この保持率は100%に近いほど耐熱性がよい。
ヤング率の保持率(%)=(加熱後のヤング率/加熱前のヤング率)×100
(4)保存性の評価
実施例1,2、比較例1,2の液状放射線硬化型樹脂組成物50grをガラス瓶に入れ、10℃、24時間保存し状態(液状・固体)を観察した。
(5)ガラス転移温度の測定
実施例1,2、比較例1,2の液状放射線硬化型樹脂組成物に、光重合開始剤イルガキュア1700(チバスペシャリテイケミカルズ社製)を3重量%添加配合し、この配合物をガラス板上に200μmの膜厚に塗布し、500mJ/cm2(波長350nm)の紫外線を照射し、硬化フィルムを得た。
25℃、相対湿度50%で硬化フィルムを24時間状態調整した後、粘弾性挙動を測定する装置 Rheometrics Solids AnalyzerRSAII(レオメトリックス・サイエンテイフィックス・エフ・イ(株)製)を用いて、tanδの温度変化を測定し、その極大値をガラス転移温度とした。
【0049】
【表1】
*1:MB(住友化学工業社製)
*2:イルガノックス1035FF(酸化防止剤、チバガイギー社製)
【0050】
【発明の効果】
本発明のシロキサン変性ポリテトラメチレングリコール骨格を有するウレタンアクリレートオリゴマを含有する液状放射線硬化型樹脂組成物は、低粘度、高屈折、低温保存性の良好な液状組成物であり、また、低ヤング率で耐熱性の良好な硬化物を与える。[0001]
BACKGROUND OF THE INVENTION
The present invention contains a urethane (meth) acrylate oligomer having a siloxane-modified polytetramethylene ether skeleton, has a low viscosity, good low-temperature storage stability, and gives a cured product with low Young's modulus and good heat resistance. The present invention relates to a liquid radiation curable resin composition, an optical fiber coating composition, and an optical fiber.
[0002]
[Prior art and problems to be solved by the invention]
Conventionally, various optical communication fibers such as quartz, multicomponent glass, plastic, etc. are known. Among them, their lightness, heat resistance, non-inductivity are good, Silica-based fibers have been widely used in terms of low loss and large transmission capacity.
[0003]
Although this silica-based optical communication fiber has the above characteristics, it is extremely thin and fragile, easily broken by external factors, and increases transmission loss due to external stress. Alternatively, after primary coating and curing with a liquid curable composition called a buffer coating material, the upper layer is then secondarily coated with a liquid curable composition called a secondary or top coating material and cured to be a primary coating. Protecting the layer is done.
[0004]
For the coating material of these primary coating layers,
i. Each coating layer after curing has appropriate mechanical properties (low Young's modulus, high elongation, high strength),
ii. The hardness (Young's modulus) of the coating layer after curing is small in a wide temperature range from high temperature to low temperature.
iii. High reliability in heat resistance, hydrolysis resistance, low water absorption, chemical resistance, etc. iv. To improve productivity, it must be fast-curing and at the same time low viscosity
Etc. are required.
[0005]
Conventionally, as a resin composition for primary coating, a urethane acrylate-based ultraviolet curable resin composition has been proposed. As described in JP-B-1-19694, No. 2784339, No. 2811070, urethane is proposed. An ultraviolet liquid curable composition comprising an acrylate oligomer, a reactive monomer, and a polymerization initiator is known. In these ultraviolet curable resin compositions, the raw material oligomer which is a precursor of the main component urethane acrylate oligomer has low viscosity, low Young's modulus, temperature characteristics (temperature dependence of Young's modulus), durability (heat resistance, Polyether such as polyethylene ether glycol, polypropylene ether glycol, polybutylene ether glycol, and polytetramethylene ether glycol have been studied from the viewpoint of water resistance, etc., and in terms of performance and cost, polypropylene ether glycol and polytetramethylene ether glycol are particularly preferred. Mainly used.
[0006]
Comparing these two, polypropylene ether glycol has low viscosity and low Young's modulus, but is inferior in temperature characteristics and durability. Polytetramethylene ether glycol, on the other hand, has good temperature characteristics and durability, but has high viscosity and Young's modulus, and the composition tends to crystallize at low temperatures, resulting in poor workability. Was requested.
[0007]
The present invention has been made in view of the above circumstances, and has solved the above disadvantages of polytetramethylene ether glycol, which is the main skeleton of urethane acrylate oligomer, and has low viscosity, low temperature storage stability, Young's modulus, and heat resistance. It is an object of the present invention to provide a liquid radiation curable resin composition suitable for optical fiber primary coating to give a cured product, a coating composition for optical fiber comprising the same, and an optical fiber coated with the cured product.
[0008]
Means for Solving the Problem and Embodiment of the Invention
As a result of intensive studies to achieve the above object, the present inventor has obtained a polyether which is a main raw material of urethane (meth) acrylate oligomer in a liquid radiation curable resin composition containing urethane (meth) acrylate oligomer. By using polytetramethylene ether glycol modified with silicone, the viscosity and Young's modulus of the cured product are lowered, and the crystallization at a lower temperature is maintained while maintaining the low temperature storage stability and heat resistance of polytetramethylene ether glycol. Has been found to be suppressed, and has led to the present invention.
[0009]
Therefore, the present invention
(A) Urethane (meth) acrylate oligomer having a skeleton represented by the following general formula (1) and / or (2) in the molecule,
[Chemical 2]
(In the formula, m, n, and p are integers satisfying 5 ≦ m ≦ 40, 0 ≦ n ≦ 10, and 1 ≦ p ≦ 50.)
(B) Ethylenically unsaturated compound
A liquid radiation curable resin composition containing the above, a coating composition for optical fibers, and the optical fiber.
[0010]
Hereinafter, the present invention will be described in more detail.
The urethane (meth) acrylate oligomer having a skeleton represented by the above general formula (1) and / or (2) in the molecule which is the component (A) of the liquid radiation curable resin composition of the present invention is (a). A diol component having a skeleton represented by the above general formula (1) and / or (2), or a mixture of this diol and polytetramethylene ether glycol, (b) polyisocyanate and (c) hydroxyl group-containing (meth) acrylate compound Can be obtained by the urethanization reaction. The weight average molecular weight of the urethane (meth) acrylate oligomer can be selected from a range of, for example, about 1000 to 20000, preferably about 2000 to 10,000.
[0011]
(A) A diol component having a skeleton represented by the general formula (1) and / or (2)The diol component having a skeleton represented by the general formula (1) and / or (2) is preferably a siloxane-modified tetramethylene ether glycol represented by the following general formulas (3) and (4).
[0012]
[Chemical Formula 3]
(In the formula, m, n, and p are integers satisfying 5 ≦ m ≦ 40, 0 ≦ n ≦ 10, and 1 ≦ p ≦ 50.)
[0013]
In the general formulas (1) to (4), m is an integer satisfying 5 ≦ m ≦ 40. When m is less than 5, the siloxane content increases, and the refractive index of the liquid radiation curable resin composition of the present invention and the physical properties (strength, elongation, etc.) of the cured product may decrease. Viscosity, low Young's modulus, and low-temperature crystallinity suppression effects may not be achieved.
n is an integer satisfying 0 ≦ n ≦ 10. When n exceeds 10, compatibility between the siloxane skeleton and the polytetramethylene ether skeleton is lost, and turbidity may occur.
p is an integer satisfying 1 ≦ p ≦ 50. When p is less than 1, the Young's modulus becomes too large, and when it exceeds 50, the low viscosity and proper physical properties of the liquid radiation curable resin composition of the present invention may not be achieved.
[0014]
The diol of component (a) can be obtained by the synthesis method shown below. That is, a known addition by a platinum catalyst from polymethylhydrogensiloxane represented by the following general formulas (5) and (6), polytetramethylene ether terminally polyethermethylene ether of polytetramethylene ether glycol, and allyl glycol Synthesized by reaction.
[0015]
[Formula 4]
[0016]
[Chemical formula 5]
[0017]
The component (a) may be a mixture of these diol components and polytetramethylene ether glycol. The molecular weight of polytetramethylene ether glycol can be selected from a range of 500 to 2000.
[0018]
The mixing ratio of these diol components and polytetramethylene ether glycol is 60% by weight or less, preferably 50% by weight or less as the weight ratio of polytetramethylene ether glycol. If it exceeds 60% by weight, the liquid radiation curable resin composition of the present invention may not achieve the low Young's modulus, the low viscosity, and the effect of suppressing crystallization under low temperature.
[0019]
(B) Polyisocyanate
Examples of the polyisocyanate of component (b) include tolylene diisocyanate, 4,4′-diphenylmethane diisocyanate, hydrogenated 4,4′-diphenylmethane diisocyanate, xylylene diisocyanate, hydrogenated xylylene diisocyanate, hexamethylene diisocyanate, isophorone diisocyanate. 1,5-naphthalene diisocyanate, tolidine diisocyanate, p-phenylene diisocyanate, transcyclohexane-1,4-diisocyanate, lysine diisocyanate, tetramethylxylene diisocyanate, lysine ester triisocyanate, 1,6,11-undecane triisocyanate, 1, 8-diisocyanate-4-isocyanate methyloctane, 1,3,6-hexamethylene triisocy Sulfonates, bicycloheptane triisocyanate, trimethylhexamethylene diisocyanate and the like are used. Among these, a polyisocyanate having a cyclic structure is particularly preferable because a cured product having a high Young's modulus can be obtained.
[0020]
(C) Hydroxyl group-containing (meth) acrylate
Examples of the hydroxyl group-containing (meth) acrylate as the component (c) include hydroxyalkyl (meth) acrylate [for example, 2-hydroxyethyl (meth) acrylate, 2-hydroxypropyl (meth) acrylate, 3-hydroxypropyl (meth) Hydroxy-C such as acrylate, 2-hydroxybutyl (meth) acrylate, 4-hydroxybutyl (meth) acrylate, pentanediol mono (meth) acrylate, hexanediol mono (meth) acrylate, neopentyl glycol mono (meth) acrylate, etc.2 ~ TenAlkyl (meth) acrylate, etc.], 2-hydroxy-3-phenyloxypropyl (meth) acrylate, 2-hydroxyalkyl (meth) acryloyl phosphate, 4-hydroxycyclohexyl (meth) acrylate, cyclohexane-1,4-dimethanol Examples include mono (meth) acrylate, trimethylolpropane di (meth) acrylate, pentaerythritol tri (meth) acrylate, and glycidyl group or epoxy group-containing compounds (for example, alkyl glycidyl ether, allyl glycidyl ether, glycidyl (meth)). Examples thereof also include compounds formed by an addition reaction between acrylate and the like) and (meth) acrylic acid. These hydroxyl group-containing (meth) acrylates can be used alone or in combination of two or more. A preferred hydroxyl group-containing (meth) acrylate is hydroxy C2 ~ FourAlkyl (meth) acrylates, particularly 2-hydroxyethyl (meth) acrylate, 2-hydroxypropyl (meth) acrylate and the like.
[0021]
The urethane (meth) acrylate oligomer can be prepared by reacting the components (a) to (c), and the ratio of each component constituting the urethane (meth) acrylate oligomer is, for example, (a) diol component And (b) the amount of the polyisocyanate and (c) the hydroxyl group-containing (meth) acrylate is 0.1 to 0.8 mol, preferably 0.2 to 0.7 mol of the hydroxyl group of the diol with respect to 1 mol of the isocyanate group. Mol, (c) 0.2 to 0.9 mol of a hydroxyl group-containing (meth) acrylate, preferably 0.3 to 0.8 mol.
[0022]
Moreover, the reaction method of (a)-(c) component is not specifically limited, Each component may be mixed and made to react, either one among polyisocyanate, a diol component, and a hydroxyl-containing (meth) acrylate After reacting with one component, the other component may be reacted.
[0023]
These urethanization catalysts are usually organotin urethanation catalysts such as stannous octoate, dibutyltin diacetate and dibutyltin dilaurate, and tertiary amine catalysts such as triethylamine, triethylenediamine and diazabicycloundecene. Is mentioned.
These catalysts can be used alone or in combination of two or more.
[0024]
(B) Ethylenically unsaturated compound
Examples of the ethylenically unsaturated compound (B) used in the present invention include a structure in which (meth) acrylic acid is bonded to an N-vinyl compound, a compound containing an amino group or a hydroxyl group by an amidation reaction or an esterification reaction. For example, the following monofunctional, difunctional, and polyfunctional compounds can be used.
[0025]
(Monofunctional compound)
Examples of the N-vinyl compound include N-vinylpyrrolidone, N-vinylcaprolactam, N-vinylacetamide, N-vinylformamide and the like, and (meth) acrylic acid is amidated or reacted with a compound containing an amino group or a hydroxyl group. Compounds having a structure bonded by esterification reaction include methoxyethylene glycol (meth) acrylate, methoxypolyethylene glycol (meth) acrylate, nonylphenoxyethyl (meth) acrylate, nonylphenoxypolyethylene glycol (meth) acrylate, nonylphenoxypolypropylene glycol (meta ) Acrylate, 3-chloro-2-hydroxypropyl (meth) acrylate, phenoxyethyl (meth) acrylate, phenoxy polypropylene glycol (meth) acrylate, Xylethylene glycol (meth) acrylate, alkyl (meth) acrylate, cyclohexyl (meth) acrylate, tetrahydrofurfuryl (meth) acrylate, isobornyl (meth) acrylate, benzyl (meth) acrylate, cumylphenol (meth) acrylate, cumyl Phenoxypolyethylene glycol (meth) acrylate, cumylphenoxypolypropylene glycol (meth) acrylate, 2-hydroxypropyl (meth) acrylate, 2-ethylhexyl (meth) acrylate, dicyclopentadiene (meth) acrylate, 2-hydroxy-3-phenoxy Propyl (meth) acrylate, 2- (meth) acryloyloxyethyl-2-hydroxyethylphthalic acid, 3-acryloyloxyglyce Mono (meth) acrylate, 2-hydroxybutyl (meth) acrylate, 2-hydroxy-1- (meth) acryloxy-3- (meth) acryloxypropane, polypropylene glycol mono (meth) acrylate, polyethylene glycol mono (meth) acrylate , Poly ε-caprolactone mono (meth) acrylate, dialkylaminoethyl (meth) acrylate, glycidyl (meth) acrylate, mono [2- (meth) acryloyloxyethyl] acid phosphate, trichloroethyl (meth) acrylate, 2,2 , 3,3-tetrafluoropropyl (meth) acrylate, 2,2,3,4,4,4-hexafluorobutyl (meth) acrylate, perfluorooctylethyl (meth) acrylate, dicyclopentenyl (meta) Acrylate, dicyclopentenyloxyalkyl (meth) acrylate, tricyclodecanyl (meth) acrylate, tricyclodecanyloxyethyl (meth) acrylate, isobornyloxyethyl (meth) acrylate, morpholine (meth) acrylate, etc. It is done.
[0026]
(Bifunctional compound)
Specific examples of the bifunctional compound include 2,2-dimethyl-3-hydroxypropyl-2,2-dimethyl-3-hydroxypropionate di (meth) acrylate, ethylene glycol di (meth) acrylate, tetra Ethylene glycol di (meth) acrylate, polyethylene glycol di (meth) acrylate, propylene glycol di (meth) acrylate, polypropylene glycol di (meth) acrylate, 1,4-butanediol di (meth) acrylate, 1,6-hexanediol Di (meth) acrylate, glycol di (meth) acrylate, neopentylglycerin di (meth) acrylate, di (meth) acrylate of bisphenol A ethylene oxide adduct, dipropylene oxide adduct of bisphenol A (Meth) acrylate, di (meth) acrylate of 2,2′-di (hydroxyethoxyphenyl) propane, di (meth) acrylate of tricyclodecane dimethylol, dicyclopentadiene di (meth) acrylate, pentanedi (meth) acrylate, Examples include di (meth) acrylic acid adducts of 2,2-bis (glycidyloxyphenyl) propane.
[0027]
(Polyfunctional compound)
Examples of the polyfunctional compound include trimethylolpropane tri (meth) acrylate, trimethylolpropane trioxyethyl (meth) acrylate, pentaerythritol tetra (meth) acrylate, dipentaerythritol hexa (meth) acrylate, and tris (acryloxy). And methyl) isocyanurate, tris (acryloxyethyl) isocyanurate, tris (acryloxypropyl) isocyanurate, triallyl trimellitic acid, triallyl isocyanurate and the like.
[0028]
Since the liquid radiation curable resin composition of the present invention is used particularly as a primary coating material (primary material) for optical fibers having a low Young's modulus, it is preferable to use a monofunctional compound.
[0029]
The blending amount of the component (B) having an ethylenically unsaturated group is the urethane (meth) acrylate oligomer of the component (A), the type of the compound of the component (B), the desired viscosity of the resin composition, or its curing. Depending on the physical properties of the material, for example, it can be selected from the range of 5 to 200 parts by weight, preferably 10 to 150 parts by weight, and more preferably 20 to 100 parts by weight with respect to 100 parts by weight of the urethane (meth) acrylate oligomer.
[0030]
Furthermore, if necessary, a polymerization initiator may be added.
As the polymerization initiator, known ones can be used, such as 1-hydroxycyclohexyl phenyl ketone, 2,2-dimethoxy-2-phenylacetophenone, phenylacetophenone diethyl ketal, alkoxyacetophenone, benzylmethyl ketal, benzophenone and Benzophenone derivatives such as 3,3-dimethyl-4-methoxybenzophenone, 4,4-dimethoxybenzophenone, 4,4-diaminobenzophenone, alkyl benzoylbenzoate, bis (4-dialkylaminophenyl) ketone, benzyl and benzylmethyl ketal Benzyl derivatives, benzoin derivatives such as benzoyl and benzoin butylmethyl ketal, benzoin isopropyl ether, 2-hydroxy-2-methylpropiophenone, 2 Thioxanthone derivatives such as 4-diethylthioxanthone and 2,4-dichlorothioxanthone, fluorene, 2-methyl-1- [4- (methylthio) phenyl] 2-morpholinopropane-1,2-benzyl-2-dimethylamino-1- Phosphine oxide derivatives such as (morpholinophenyl) -butanone-1,2,4,6-trimethylbenzoyldiphenylphosphine oxide, bis (2,6-dimethoxybenzoyl) -2,4,4-trimethylpentylphosphine oxide, benzoyl peroxide , Organic peroxides such as t-butyl peroxide and cumene hydroperoxide, azobiscyanovaleric acid, azobisbutyronitrile, azobis- (2,4-dimethyl) valeronitrile, azobis- (2-aminopropane) hydrochloride Have Azo compounds, and the like.
[0031]
These may be used alone or in combination of two or more. The blending amount is not particularly limited as long as the characteristics of the coating material of the present invention are satisfied, but usually 0.1 to 10% by weight, particularly 1 to 5% by weight of the whole composition is preferable.
[0032]
In addition to the above components, the liquid radiation curable resin composition of the present invention includes, for example, stabilizers such as antioxidants and ultraviolet absorbers, organic solvents, plasticizers, surfactants, silane coupling agents, and coloring pigments. Additives such as organic or inorganic particles can be added as necessary within the range not impairing the object of the present invention.
[0033]
The liquid radiation curable resin composition of the present invention can be prepared by blending the above-mentioned required components and stirring and mixing, and the viscosity is compatible with the manufacturing conditions of the optical fiber core in terms of workability. In view of the properties, a range of 500 to 10000 mPa · s (25 ° C.) is desirable, particularly in high-speed production conditions.
[0034]
As radiation for curing the liquid radiation curable resin composition of the present invention, infrared rays, visible rays, ultraviolet rays, and ionizing radiation such as X-rays, electron beams, α rays, β rays, and γ rays can be used.
[0035]
The liquid radiation curable resin composition of the present invention is particularly suitably used as a coating composition for optical fibers, particularly as a primary coating material. An optical fiber cured and coated with this composition is a cured product of this composition. Has good heat resistance and gives high reliability.
[0036]
The liquid radiation curable resin composition of the present invention can be applied not only to a coating material for optical fibers but also to buffer materials and fillers such as waterproof fiber cables and submarine cable optical fiber units. It can be applied to releasable coating materials, water-repellent coating materials, protective coating materials, various inks and paints.
[0037]
【Example】
EXAMPLES Hereinafter, although an Example and a comparative example are shown and this invention is demonstrated concretely, this invention is not restrict | limited to the following Example. In addition, the part in the following example shows a weight part.
[0038]
(A) Synthesis of urethane (meth) acrylate oligomer
[Synthesis Example 1]
Synthesis of allylic polytetramethylene ethers at both ends
A mixed solution of polytetramethylene ether glycol PTMG650 (OH value, 178 KOH mg / gr) 629.2 gr, tert-butoxy potassium 258.1 gr, and dry tetrahydrofuran 1000 ml was heated to reflux under nitrogen for 4 hours. After cooling this mixed solution to a temperature of 50 ° C., a mixture of 292.2 g of allyl bromide and 150 ml of dry tetrahydrofuran was added dropwise. Subsequently, after refluxing for 6 hours, tetrahydrofuran was distilled off under reduced pressure at a temperature of 80 ° C., and 700 ml of hexane was added to the remaining liquid, followed by washing with water until neutrality. The hexane layer was dried over anhydrous sodium sulfate and filtered, and the low fraction was distilled off under reduced pressure at a temperature of 110 ° C. to obtain both terminal allylated polytetramethylene ether (A-PTMG650). It was 1.3 mgKOH / gr when the hydroxyl value of this all-terminal allylated polytetramethylene ether was measured. (Allylation rate 99.3%)
[0039]
[Synthesis Example 2]
Synthesis of siloxane-modified polytetramethylene ether glycol
Mixing of 120gr of toluene, 60.45gr of tetramethyl-1,3-hydrogendisiloxane (siloxane compound represented by the above general formula (5)), 0.024gr of octyl alcohol modified solution of chloroplatinic acid (platinum content 2%) Under nitrogen, 240 g of both end allylated polytetramethylene ether obtained in Synthesis Example 1 was added dropwise under nitrogen, and the mixture was stirred at room temperature for 1 hour, and then heated and stirred at a temperature of 110 ° C. for 6 hours. Subsequently, after cooling to a temperature of 30 ° C. or lower, 33.33 gr of ethylene glycol monoallyl ether and 0.024 gr of an octyl alcohol-modified solution of chloroplatinic acid (platinum content 2%) were added, and a temperature of 80 to 90 ° C. was added after the addition. For 5 hours. Next, the mixture was cooled to a temperature of 60 ° C. or lower, 0.1% hydrochloric acid 6 gr and isopropyl alcohol 30 gr were added and heated at 60 ° C. for 2 hours, and then the low fraction was distilled off at 110 ° C. under reduced pressure. A siloxane-modified polytetramethylene ether glycol A represented by the following general formula (7) containing hydroxyl groups at both ends was obtained. When the hydroxyl value of this glycol was measured, it was 52 mgKOH / gr.
[0040]
[Chemical 6]
[0041]
[Synthesis Example 3]
Synthesis of siloxane-modified polytetramethylene ether glycol
In the same manner as in Synthesis Example 2, tetramethyl-1,3-hydrogendisiloxane was changed to 1,2,3,4-octamethyl-2,3-hydrogentetrasiloxane (siloxane compound represented by the above general formula (6)) 127. A siloxane-modified polytetramethylene ether glycol B represented by the following general formula (8) containing hydroxyl groups at both ends was obtained by the same use amount and operation except that the amount was changed to 3 gr. When the hydroxyl value of this glycol was measured, it was 51 mgKOH / gr.
[0042]
[Chemical 7]
[0043]
[Synthesis Example 4]
Synthesis of urethane acrylate oligomers
Aronix M-113 (manufactured by Toagosei Co., Ltd.) 28.07 gr, polymerization inhibitor 2,6-di-t-butylhydroxytoluene 0.078 gr, dibutyltin dilaurate 0.066 gr were mixed with stirring. 2,4-Toluene diisocyanate 26.1gr was added to this, and it cooled at 18-20 degreeC. To this mixed solution, 11.6 gr of 2-hydroxyethyl acrylate was added dropwise under a dry air atmosphere so that the reaction temperature was 25 ° C. or lower. After completion of dropping, the mixture was stirred for about 1 hour at room temperature, and 214.9 gr of siloxane-modified polytetramethylene ether glycol A obtained in Synthesis Example (2) was added dropwise at a reaction temperature of 40 ° C. or lower. Next, the reaction is carried out at a temperature of 65 to 70 ° C. for 7 hours in a dry air atmosphere, and it is confirmed by infrared absorption spectrum that there is no absorption caused by isocyanate groups (NCO), and 10% by weight of Aronix M-113 is contained. A urethane acrylate oligomer I having an average molecular weight of about 5,050 was obtained.
[0044]
[Synthesis Example 5]
Synthesis of urethane acrylate oligomers
In the same manner as in Synthesis Example 4, except that siloxane-modified polytetramethylene ether glycol A was replaced with siloxane-modified polytetramethylene ether glycol B 219.6gr obtained in Synthesis Example 3, Aronix M-113 was prepared by the same amount and operation. A urethane acrylate oligomer II containing 10% by weight and having an average molecular weight of about 5,150 was obtained.
[0045]
[Comparative Synthesis Example 1]
By using the same amount and operation as in Synthesis Example 4 except that the siloxane-modified polytetramethylene ether glycol A was replaced with 202 g of polytetramethylene ether glycol PTMG2000 (manufactured by Sanyo Chemical Co., Ltd., hydroxyl value = 55 mgKOH / gr), Aronix M A urethane acrylate oligomer III containing 10% by weight of -113 and having an average molecular weight of about 4,790 was obtained.
[0046]
[Comparative Synthesis Example 2]
Except that siloxane-modified polytetramethylene ether glycol A was replaced with 210 gr of polypropylene ether glycol PPG2000 (manufactured by Sanyo Kasei Co., Ltd., hydroxyl value = 53 mg KOH / gr), the same amount and operation as in Synthesis Example 4 were used to prepare Aronix M-113. A urethane acrylate oligomer IV containing 10% by weight and having an average molecular weight of about 4,950 was obtained.
[0047]
[Examples 1 and 2, Comparative Examples 1 and 2]
Examples 1 and 2 and Comparative Examples 1 and 2 were prepared by mixing the urethane acrylate oligomers I to IV synthesized above and mixing an ethylenically unsaturated group-containing compound and an antioxidant as shown in Table 1. A liquid radiation curable resin composition was prepared.
The physical properties of the obtained liquid radiation curable resin composition were evaluated as shown below. The results are also shown in Table 1.
[0048]
<Evaluation methods>
(1) Creation of cured film
The liquid radiation curable resin composition was applied on a glass plate to a thickness of 50 to 60 μm, and an ultraviolet ray and an electron beam accelerated at 100 kV were irradiated with an absorbed dose of 30 kGy under nitrogen to obtain a cured film. .
(2) Measurement of Young's modulus
The cured film obtained in (1) was conditioned at 25 ° C. and 50% relative humidity for 24 hours, and then 2.5% tensile modulus was measured under the conditions of 25 mm between marked lines and 1 mm / min pulling speed. .
(3) Measurement of tensile strength and elongation at break
The cured film was conditioned for 24 hours at 25 ° C. and a relative humidity of 50%, and then measured under conditions of 25 mm between marked lines and a pulling speed of 50 mm / min.
(3) Evaluation of heat resistance
The cured film obtained in (1) was heated at 120 ° C., and the Young's modulus after heating was measured as in (2). The heat resistance was evaluated by obtaining the Young's modulus retention rate according to the following formula. As the retention rate is closer to 100%, the heat resistance is better.
Young's modulus retention (%) = (Young's modulus after heating / Young's modulus before heating) × 100
(4) Evaluation of storage stability
50 gr of the liquid radiation curable resin compositions of Examples 1 and 2 and Comparative Examples 1 and 2 were put in a glass bottle and stored at 10 ° C. for 24 hours, and the state (liquid / solid) was observed.
(5) Measurement of glass transition temperature
3% by weight of a photopolymerization initiator Irgacure 1700 (manufactured by Ciba Specialty Chemicals) was added to and blended with the liquid radiation curable resin compositions of Examples 1 and 2 and Comparative Examples 1 and 2, and this composition was added to a glass plate. Applied to a film thickness of 200 μm, 500 mJ / cm2Irradiated with ultraviolet rays having a wavelength of 350 nm, a cured film was obtained.
Using a device Rheometrics Solids Analyzer RSAII (manufactured by Rheometrics Scientific FFI Co., Ltd.) for measuring viscoelastic behavior after conditioning a cured film for 24 hours at 25 ° C. and 50% relative humidity, The temperature change was measured, and the maximum value was taken as the glass transition temperature.
[0049]
[Table 1]
* 1: MB (manufactured by Sumitomo Chemical Co., Ltd.)
* 2: Irganox 1035FF (Antioxidant, manufactured by Ciba Geigy)
[0050]
【The invention's effect】
The liquid radiation curable resin composition containing a urethane acrylate oligomer having a siloxane-modified polytetramethylene glycol skeleton of the present invention is a liquid composition having a low viscosity, a high refraction, and a low temperature storage stability, and also has a low Young's modulus. Gives a cured product with good heat resistance.
Claims (3)
(B)エチレン性不飽和化合物
を含有する液状放射線硬化型樹脂組成物。(A) Urethane (meth) acrylate oligomer having a skeleton represented by the following general formula (1) and / or (2) in the molecule,
(B) A liquid radiation curable resin composition containing an ethylenically unsaturated compound.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002116071A JP3844065B2 (en) | 2002-04-18 | 2002-04-18 | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002116071A JP3844065B2 (en) | 2002-04-18 | 2002-04-18 | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2003313256A JP2003313256A (en) | 2003-11-06 |
| JP3844065B2 true JP3844065B2 (en) | 2006-11-08 |
Family
ID=29533877
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002116071A Expired - Fee Related JP3844065B2 (en) | 2002-04-18 | 2002-04-18 | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3844065B2 (en) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5207530B2 (en) * | 2008-07-10 | 2013-06-12 | 大日精化工業株式会社 | Plastic paint |
| EP2230277B1 (en) * | 2009-03-12 | 2012-07-04 | Corning Incorporated | Composites and methods of making and using the composites |
-
2002
- 2002-04-18 JP JP2002116071A patent/JP3844065B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2003313256A (en) | 2003-11-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3746871B2 (en) | Liquid curable resin composition | |
| EP0860485B1 (en) | Liquid curable resin composition | |
| EP0892822B1 (en) | Liquid curable resin composition | |
| EP0785961A1 (en) | Optical glass fiber coating composition | |
| US5913004A (en) | Optical glass fiber coating composition | |
| JP4288453B2 (en) | Methylphenylpolysiloxane diol and method for producing the same, liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP2002243995A (en) | Coated optical fiber | |
| JP2001181359A (en) | Liquid curable resin composition and cured product | |
| JP2001261923A (en) | Radiation-curing type resin composition and coating agent for optical fiber | |
| JP2001131243A (en) | Liquid radiation-curable resin composition, coating material for optical fiber and optical fiber | |
| JP3844065B2 (en) | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP3900279B2 (en) | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP3871048B2 (en) | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP2000344844A (en) | Liquid radiation-curable resin composition, cladding composition for optical fiber, and optical fiber | |
| JP3748038B2 (en) | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP3741196B2 (en) | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP2002338641A (en) | Liquid radiation-curing resin composition, coating composition for optical fibre and optical fiber | |
| JP2883988B2 (en) | Liquid curable resin composition | |
| JP3738809B2 (en) | Liquid radiation curable resin composition, optical fiber coating composition, and optical fiber | |
| JP3796655B2 (en) | Optical fiber coating | |
| JP3772950B2 (en) | Optical fiber coating composition and optical fiber | |
| JP2002131594A (en) | Coated optical fiber | |
| JP2004043626A (en) | Liquid radiation-curable resin composition, coating composition for optical fiber, and optical fiber | |
| JP2003026738A (en) | Photocurable resin composition and optical fiber unit obtained using the same | |
| JP2003226558A (en) | Electron beam curing type resin composition for coating optical fiber and coated optical fiber |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040728 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20060721 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20060726 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20060808 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20090825 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120825 Year of fee payment: 6 |
|
| LAPS | Cancellation because of no payment of annual fees |