JP2022014150A - イオン制御バイオデバイスとその製造方法 - Google Patents
イオン制御バイオデバイスとその製造方法 Download PDFInfo
- Publication number
- JP2022014150A JP2022014150A JP2020116340A JP2020116340A JP2022014150A JP 2022014150 A JP2022014150 A JP 2022014150A JP 2020116340 A JP2020116340 A JP 2020116340A JP 2020116340 A JP2020116340 A JP 2020116340A JP 2022014150 A JP2022014150 A JP 2022014150A
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- acid molecule
- solid substrate
- lipid
- biological membrane
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Investigating Or Analyzing Materials By The Use Of Electric Means (AREA)
Abstract
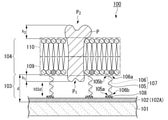
【解決手段】本発明のイオン制御バイオデバイス100は、固体基板101と、固体基板101の一方の主面に形成され、グラフェンからなる複数のマイクロ電極を配列させた電極アレイ102と、電極アレイ102と固体基板101の一方の主面の上に形成された界面層103と、界面層103の上に形成され、膜貫通タンパク質Pを貫通させて担持する生体膜104と、を有し、固体基板101側の膜貫通タンパク質Pの一端と、生体膜104との距離をh1とし、固体基板101と反対側の膜貫通タンパク質Pの他端と、生体膜104との距離をh2とし、固体基板101と生体膜104との距離をdとしたとき、下記(1)式の関係を満たす。
h1<d<h2 (1)
【選択図】図1
Description
図1は、本発明の第一実施形態に係るイオン制御バイオデバイス100の断面図である。イオン制御バイオデバイス100は、主に、固体基板101と、電極アレイ(マルチマイクロ電極)102と、界面層103と、生体膜(支持膜)104と、を有する。
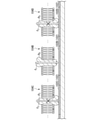
まず、プラスティック、ガラス、シリコン等の材料からなる固体基板101を準備し、その一方の主面101aに、化学気相成長法等の公知の成膜法を用いてグラフェン膜を形成(転写)する。このグラフェン膜に対し、フォトリソグラフィ法を用いて、図3(a)に示すように、所定のパターン・サイズを有する複数のマイクロ電極102Aによって構成される、電極アレイ102を形成する。
次に、スパッタリング法等の公知の成膜方法を用いて、図3(b)に示すように、マイクロ電極102Aの表面に、第一核酸分子105を固定するための接着分子108を付着させる。接着分子108としては、例えば、ピレンブタン酸などのピレンアルキルカルボン酸類を用いることができる。
次に、マイクロ電極102A上に、第一核酸分子105を含む溶液を導入し(流し)、図3(c)に示すように、マイクロ電極102Aに対し、接着分子108を介して第一核酸分子の一端105aを固定する。このとき、第一核酸分子の一端105aをアミノ基で修飾させておけば、ピレンブタジエン酸等の接着分子108との脱水縮合を通じて、マイクロ電極102Aに対し、第一核酸分子105をより強く吸着させることができるため、好ましい。
次に、第一核酸分子105と相補的な配列を有する第二核酸分子106が結合している複数の第一脂質分子109A、および第二核酸分子105が結合していない複数の第二脂質分子109Bの混合分散液と、第三脂質分子110Aの分散液を作製する。これらの分散液を用いて脂質二重膜を形成するプロセスとしては、例えば次の二通りのプロセス(ア)、(イ)が挙げられる。
また、分散液中における第二脂質分子109Bに対する第一脂質分子109Aのモル比は、1/1000以上1/10以下であることが好ましい。上記モル比であることにより、より安定した脂質二重膜を形成することができる。
第一脂質分子109A及び第二脂質分子109Bを分散させる溶媒としては、例えばクロロホルム等が挙げられる。
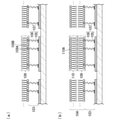
まず、気液界面に第一脂質分子109A及び第二脂質分子109Bを含む分散液を滴下し、溶媒を蒸発させて脂質単分子膜(第一脂質分子膜109)を形成させる。その後、更に脂質分子の相転移温度を上回る温度条件下で静置し、分子占有面積が細胞膜のそれと同程度になるまで脂質単分子膜を圧縮し、これを固体基板上に移す(図4(a))。この表面に第三脂質分子110Aのみを水に分散させた分散液を加えて、第一脂質分子109Aおよび第二脂質分子109Bからなる第一脂質分子膜109と、第三脂質分子110Aからなる第二脂質分子膜110と、で構成される安定な脂質二重膜を作製する(図4(b))。
酸化インジウムスズ(ITO)ガラス基板上に、第一脂質分子109A及び第二脂質分子109Bを含む分散液を滴下し、溶媒を蒸発させて完全に除去する。その後、交流電場下で水和させて脂質二重膜小胞を含む懸濁液を作製する。このとき、接着層上に固定化された第一の一本鎖核酸分子105は、第二の一本鎖核酸分子(第二核酸分子)106と、少なくとも一部に二本差構造を有する核酸分子107を形成すると同時に、脂質二重膜が互いに横方向に融合及び伸展していくことで、安定な脂質二重膜が界面層103直上に積層される(図4(b))。
本方法は、非特許文献9の開示内容に基づく方法である。具体的には、まず、水と有機溶媒(例えば、エタノールやイソプロパノール等)との1:1混合液中に、脂質分子を分散させ、これをグラフェン基板上に滴下する。ここに、所定の時間、少しずつ水を加え(例えば、30μL/min等)、水の体積分率を上昇させていくことで、脂質二重膜を自発的に形成させる。最後に十分な量の水で基板表面を洗浄し、不要な有機溶媒や過剰な脂質分子を除去し、目的の脂質二重膜を得る(図4(b))。
<1>気液界面に脂質混合液を滴下し、溶媒を蒸発させた後、分子占有面積が細胞膜と同程度になるまで膜を圧縮し、これを固体基板上に移す。この表面に脂質懸濁液を加えて安定な膜を作製する。
<2>ITOガラス基板上に脂質溶液を滴下し、溶媒を完全に除去したものを交流電場下で水和させて作製した脂質二分子膜小胞の懸濁液をグラフェン表面に滴下して安定な膜を作製する.
101・・・固体基板
101a・・・固体基板の一方の主面
102・・・電極アレイ
102A、102B、102C・・・マイクロ電極
103・・・界面層
104・・・生体膜
105・・・第一核酸分子
105a・・・第一核酸分子の一端
105b・・・第一核酸分子の他端
106・・・第二核酸分子
106a・・・第二核酸分子の一端
106b・・・第二核酸分子の他端
107・・・核酸分子
108・・・接着分子
109・・・下層側の脂質分子膜(第一脂質分子膜)
109A・・・第一脂質分子
109B・・・第二脂質分子
110・・・上層側の脂質分子膜(第二脂質分子膜)
110A・・・第三脂質分子
d・・・固体基板と生体膜との距離
h1・・・膜貫通タンパク質の一端と生体膜との距離
h2・・・膜貫通タンパク質の他端と生体膜との距離
P・・・膜貫通タンパク質
P1・・・膜貫通タンパク質の一端
P2・・・膜貫通タンパク質の他端
Claims (7)
- 固体基板と、
前記固体基板の一方の主面に形成され、グラフェンからなる複数のマイクロ電極を配列させた電極アレイと、
前記電極アレイとともに前記固体基板の一方の主面を覆うように形成された界面層と、
前記界面層の上に形成され、膜貫通タンパク質を厚み方向に貫通させた状態で担持する生体膜と、を有し、
前記固体基板側に位置する前記膜貫通タンパク質の一端と、前記生体膜との距離をh1とし、
前記固体基板と反対側に位置する前記膜貫通タンパク質の他端と、前記生体膜との距離をh2とし、
前記固体基板と前記生体膜との距離をdとしたとき、下記(1)式の関係を満たすことを特徴とするイオン制御バイオデバイス。
h1<d<h2 (1) - 前記マイクロ電極が、前記生体膜の厚み方向からの平面視において、前記生体膜のうち、膜貫通タンパク質が担持される領域と重ならない領域に形成されていることを特徴とする請求項1に記載のイオン制御バイオデバイス。
- 隣接する前記マイクロ電極の幅が、1μm以上100μm以下であることを特徴とする請求項1または2のいずれかに記載のイオン制御バイオデバイス。
- 前記界面層の厚みが5nm以上であることを特徴とする請求項1~3のいずれか一項に記載のイオン制御バイオデバイス。
- 前記界面層が、螺旋状の第一核酸分子、第二核酸分子からなる対の核酸分子を複数有し、前記第一核酸分子の一端が前記固体基板の一方の主面に固定され、前記第二核酸分子の一端が前記生体膜に固定されていることを特徴とする請求項1~4のいずれか一項に記載のイオン制御バイオデバイス。
- 前記生体膜が、複数の脂質分子膜が重なってなり、前記固体基板に最も近い側の前記脂質分子膜に、前記第二核酸分子の一端が固定されていることを特徴とする1~5のいずれか一項に記載のイオン制御バイオデバイス。
- 固体基板の一方の主面に、グラフェンからなる複数のマイクロ電極を配列させた電極アレイを形成する電極アレイ形成工程と、
前記マイクロ電極の表面に、前記第一核酸分子を固定するための接着分子を付着させる接着分子付着工程と、
前記マイクロ電極上に、前記接着分子を介して前記第一核酸分子の一端を固定する第一核酸分子固定工程と、
前記第一核酸分子と相補的な配列を有する第二核酸分子が結合している複数の第一脂質分子、および前記第二核酸分子が結合していない複数の第二脂質分子からなる第一脂質分子膜を形成する第一脂質分子膜形成工程と、
前記第一核酸分子と前記第二核酸分子とを反応させ、両核酸分子の対からなる界面層を形成する界面層形成工程と、
前記第二核酸分子が結合していない複数の第二脂質分子のみからなる第二脂質分子膜を、第一脂質分子膜上に形成する第二脂質分子膜形成工程と、を有し、
前記生体膜に、膜貫通タンパク質を厚み方向に貫通させた状態で担持させた際に、
前記固体基板側に位置する前記膜貫通タンパク質の一端と、前記生体膜との距離をh1とし、前記固体基板と反対側に位置する前記膜貫通タンパク質の他端と、前記生体膜との距離をh2とし、前記固体基板と前記生体膜との距離をdとしたとき、
下記(2)式の関係を満たすように、形成する前記界面層の厚みを調整することを特徴とするイオン制御バイオデバイスの製造方法。
h1<d<h2 (2)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020116340A JP2022014150A (ja) | 2020-07-06 | 2020-07-06 | イオン制御バイオデバイスとその製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020116340A JP2022014150A (ja) | 2020-07-06 | 2020-07-06 | イオン制御バイオデバイスとその製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2022014150A true JP2022014150A (ja) | 2022-01-19 |
Family
ID=80185272
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020116340A Pending JP2022014150A (ja) | 2020-07-06 | 2020-07-06 | イオン制御バイオデバイスとその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2022014150A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2024018237A (ja) * | 2022-07-29 | 2024-02-08 | 日本電信電話株式会社 | バイオセンサおよびバイオセンサの製造方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019216660A (ja) * | 2018-06-20 | 2019-12-26 | 日本電信電話株式会社 | 脂質二重膜基板におけるリンカー層の制御方法、並びに、脂質二重膜基板及びその製造方法 |
-
2020
- 2020-07-06 JP JP2020116340A patent/JP2022014150A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019216660A (ja) * | 2018-06-20 | 2019-12-26 | 日本電信電話株式会社 | 脂質二重膜基板におけるリンカー層の制御方法、並びに、脂質二重膜基板及びその製造方法 |
Non-Patent Citations (1)
| Title |
|---|
| BIOSENSORS & BIOELECTRONICS, vol. 14, JPN6023032381, 1999, pages 651 - 662, ISSN: 0005216337 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2024018237A (ja) * | 2022-07-29 | 2024-02-08 | 日本電信電話株式会社 | バイオセンサおよびバイオセンサの製造方法 |
| JP7828610B2 (ja) | 2022-07-29 | 2026-03-12 | Ntt株式会社 | バイオセンサおよびバイオセンサの製造方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Xing et al. | Highly shape-and size-tunable membrane nanopores made with DNA | |
| US20250369951A1 (en) | Membrane bound nucleic acid nanopores | |
| Rossi et al. | Biomimetic tethered lipid membranes designed for membrane-protein interaction studies | |
| Castellana et al. | Solid supported lipid bilayers: From biophysical studies to sensor design | |
| Chan et al. | Model membrane systems and their applications | |
| Prévost et al. | IRSp53 senses negative membrane curvature and phase separates along membrane tubules | |
| Loidl‐Stahlhofen et al. | Solid‐Supported Biomolecules on Modified Silica Surfaces—A Tool for Fast Physicochemical Characterization and High‐Throughput Screening | |
| Suzuki et al. | Microtechnologies for membrane protein studies | |
| Muller et al. | Strategies to prepare and characterize native membrane proteins and protein membranes by AFM | |
| CN113759105A (zh) | 混合纳米孔传感器 | |
| CN1902497A (zh) | 分析芯片以及所述分析芯片用于测定分子结构和功能的用途 | |
| Diamanti et al. | High resistivity lipid bilayers assembled on polyelectrolyte multilayer cushions: an impedance study | |
| Khan et al. | Electrophysiology of epithelial sodium channel (ENaC) embedded in supported lipid bilayer using a single nanopore chip | |
| Hirtz et al. | Self-limiting multiplexed assembly of lipid membranes on large-area graphene sensor arrays | |
| Della Pia et al. | A step closer to membrane protein multiplexed nanoarrays using biotin-doped polypyrrole | |
| Sek et al. | Molecular resolution imaging of an antibiotic peptide in a lipid matrix | |
| Reimhult et al. | Advances in nanopatterned and nanostructured supported lipid membranes and their applications | |
| JP6963284B2 (ja) | 脂質二重膜基板におけるリンカー層の制御方法、並びに、脂質二重膜基板及びその製造方法 | |
| JP2022014150A (ja) | イオン制御バイオデバイスとその製造方法 | |
| Hussein et al. | Silver nanoneedle probes enable sustained DC current, single-channel resistive pulse nanopore sensing | |
| US20240280530A1 (en) | Nanomechanically actuated nucleic acid nanopore | |
| JP7365022B2 (ja) | 生体分子の支持体とその製造方法 | |
| US8313956B2 (en) | Apparatus and associated methods | |
| Sacconi et al. | A comparative study of phosphatidylcholine versus phosphatidylserine-based solid supported membranes for the preparation of liposome-rich interfaces | |
| Guidelli et al. | Ion transport across biomembranes and model membranes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20200706 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220801 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230808 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231006 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20231212 |