JP2019517618A - 化合物 - Google Patents
化合物 Download PDFInfo
- Publication number
- JP2019517618A JP2019517618A JP2018563886A JP2018563886A JP2019517618A JP 2019517618 A JP2019517618 A JP 2019517618A JP 2018563886 A JP2018563886 A JP 2018563886A JP 2018563886 A JP2018563886 A JP 2018563886A JP 2019517618 A JP2019517618 A JP 2019517618A
- Authority
- JP
- Japan
- Prior art keywords
- group
- chemical formula
- compound
- formula
- substituent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/38—Polysiloxanes modified by chemical after-treatment
- C08G77/382—Polysiloxanes modified by chemical after-treatment containing atoms other than carbon, hydrogen, oxygen or silicon
- C08G77/388—Polysiloxanes modified by chemical after-treatment containing atoms other than carbon, hydrogen, oxygen or silicon containing nitrogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0834—Compounds having one or more O-Si linkage
- C07F7/0838—Compounds with one or more Si-O-Si sequences
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/0666—Polycondensates containing five-membered rings, condensed with other rings, with nitrogen atoms as the only ring hetero atoms
- C08G73/0672—Polycondensates containing five-membered rings, condensed with other rings, with nitrogen atoms as the only ring hetero atoms with only one nitrogen atom in the ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
- C08G73/1057—Polyimides containing other atoms than carbon, hydrogen, nitrogen or oxygen in the main chain
- C08G73/106—Polyimides containing other atoms than carbon, hydrogen, nitrogen or oxygen in the main chain containing silicon
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/22—Polysiloxanes containing silicon bound to organic groups containing atoms other than carbon, hydrogen and oxygen
- C08G77/26—Polysiloxanes containing silicon bound to organic groups containing atoms other than carbon, hydrogen and oxygen nitrogen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/80—Siloxanes having aromatic substituents, e.g. phenyl side groups
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- General Chemical & Material Sciences (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Silicon Polymers (AREA)
Abstract
Description
本出願は、2016年10月31日付けの韓国特許出願第10−2016−0143084号に基づく優先権の利益を主張し、当該韓国特許出願の文献に開示されたすべての内容は、本明細書の一部として含まれる。
R1 aR2 bSiO(4−a−b)/2
NMR分析は、Agilent社の500MHzのNMR装備を使用して製造社のマニュアルに沿って行った。NMRを測定するためのサンプルは、化合物をDMSO(dimethyl sulfoxide)−d6およびアセトン−d6に溶解させて製造した。
DSC分析は、TA instrument社のQ20システムを使用して35℃から400℃または450℃まで10℃/分の昇温速度で昇温しつつ、N2フロー雰囲気で行った。
TGA分析は、Mettler−Toledo社のTGA e850装備を使用して行った。
製造例で製造された化合物の場合、25℃から800℃まで10℃/分の昇温速度で昇温しつつ、N2フロー雰囲気で分析し、実施例または比較例で製造された組成物の場合は、375℃の温度でポスト硬化させた後、25℃から900℃まで10℃/分の昇温速度で昇温しつつ、N2フロー雰囲気で分析した。
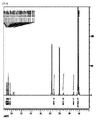
下記化学式Aの化合物(PN1)は、次の方式で合成した。下記化学式Bの化合物160gおよび200gのジメチルホルムアミド(Dimethyl Formamide、DMF)を三口丸底フラスコに投入し、常温で撹拌して溶解させた。次に、下記化学式Cの化合物52gを追加し、DMF200gを追加した後に撹拌して溶解させた。次に、炭酸カリウム62.2gおよびDMF100gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液に0.2N濃度の塩酸水溶液を注入した。前記混合溶液にクロロホルムを投入して生成物を抽出し、抽出した生成物を水洗した。真空蒸留にてクロロホルムと反応溶液であるDMFを除去した。水と残留溶媒を除去した後、重量平均分子量が1,350である下記化学式Aの化合物(PN1)を約87重量%の収率で収得した。化学式Aの化合物に対するNMR結果は、図1に示した。下記化学式Aの化合物(PN1)のNMR分析結果は、図1に示した。
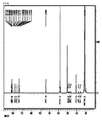
下記化学式Dの化合物(PN2)は、次の方式で合成した。下記化学式Eの化合物181gおよび200gのDMFを三口丸底フラスコに投入し、常温で撹拌して溶解させた。次に、前記化学式Cの化合物35gを追加し、DMF200gを追加した後、撹拌して溶解させた。次に、炭酸カリウム41.5gおよびDMF100gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液を0.2N濃度の塩酸水溶液に注入した。前記混合溶液にクロロホルムを投入して生成物を抽出し、抽出した生成物を水洗した。真空蒸留にてクロロホルムと反応溶液であるDMFを除去した。水と残留溶媒を除去した後、重量平均分子量が2,100である下記化学式Dの化合物(PN2)を約88重量%の収率で収得した。化学式Dの化合物に対するNMR結果は、図2に示した。
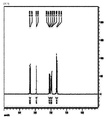
下記化学式Fの化合物(PN3)を次の方式で合成した。下記化学式Gの化合物54gおよび50gのDMFを三口丸底フラスコに投入し、常温で撹拌して溶解させた。次に、前記化学式Cの化合物7gを追加し、DMF50gを追加した後、撹拌して溶解させた。次に、炭酸カリウム8.3gおよびDMF30gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液に0.2N濃度の塩酸水溶液を注入した。前記混合溶液にクロロホルムを投入して生成物を抽出し、抽出した生成物を水洗した。次に、真空蒸留にてクロロホルムと反応溶液であるDMFを除去した。水と残留溶媒を除去した後、重量平均分子量が3,100である下記化学式Fの化合物(PN3)を約85重量%の収率で収得した。化学式Fの化合物に対するNMR結果は、図3に示した。
下記化学式Hの化合物(PN4)を次の方式で合成した。下記化学式Iの化合物56gおよび50gのDMFを三口丸底フラスコに投入し、常温で撹拌して溶解させた。次に、前記化学式Cの化合物4.5gを追加し、DMF50gを追加した後、撹拌して溶解させた。次に、炭酸カリウム5.4gおよびDMF30gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液に0.2N濃度の塩酸水溶液を注入した。前記混合溶液にクロロホルムを投入して生成物を抽出し、抽出した生成物を水洗した。次に、真空蒸留にてクロロホルムと反応溶液であるDMFを除去した。水と残留溶媒を除去した後、重量平均分子量が4,600である下記化学式Hの化合物(PN4)を約87重量%の収率で収得した。化学式Hの化合物に対するNMR結果は、図4に示した。
下記化学式Jの化合物(PN5)を次の方式で合成した。4、4’−ビス(ヒドロキシフェニル)メタン28.0gおよび150mlのDMFを三口丸底フラスコに投入し、常温で撹拌して溶解させた。前記混合物に4−ニトロフタロニトリル48.5gを添加し、DMF50gを添加した後、撹拌して溶かした。次に、炭酸カリウム58.1gおよびDMF50gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液を0.2N濃度の塩酸水溶液に注入して中和沈殿させ、フィルタリングした後に水洗した。その後、フィルタリングされた反応物を100℃の真空オーブンで一日間乾燥させ、水と残留溶媒を除去した後、下記化学式Jの化合物(PN5)を約83重量%の収率で収得した。化学式Jの化合物に対するNMR結果は、図5に示した。
下記化学式Kの化合物(PN6)を次の方式で合成した。前記化学式Lの化合物27.9gおよび100gのDMFを三口丸底フラスコに投入し、常温で撹拌して溶解させた。次に、前記化学式Cの化合物51.9gを追加し、DMF50gを追加した後、撹拌して溶解させた。次に、炭酸カリウム62.2gおよびDMF50gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液を0.2N濃度の塩酸水溶液に注入して中和沈殿させ、フィルタリングした後に水洗した。その後、フィルタリングされた反応物を100℃の真空オーブンで一日間乾燥させ、水と残留溶媒を除去した後、下記化学式Kの化合物を約83重量%の収率で収得した。前記化学式Kの化合物に対するNMR結果は、図6に示した。
下記化学式Mの化合物(PN7)を次のように合成した。下記化学式Nの化合物50.4gおよびDMF150gを三口丸底フラスコに投入し、常温で撹拌して溶解させた。その後、前記化学式Cの化合物51.9gを追加し、DMF50gを追加した後に撹拌して溶解させた。次に、炭酸カリウム62.2gおよびDMF50gを共に投入し、撹拌しながら温度を85℃まで昇温させた。前記状態で約5時間程度反応させた後に常温まで冷却させた。冷却された反応溶液を0.2N濃度の塩酸水溶液に注入して中和沈殿させ、フィルタリングした後に水洗した。その後、フィルタリングされた反応物を100℃の真空オーブンで一日間乾燥させ、水と残留溶媒を除去した後、下記化学式Mの化合物(PN8)を約87重量%の収率で収得した。前記化学式Mの化合物に対するNMR結果は、図7に示した。
下記化学式Oの化合物は、東京化成工業(TCI)社の市販製品を入手して、追加精製することなく使用した。
製造例5の化合物(PN5)および製造例2の化合物(PN2)の混合物(PN5とPN2の重量比(PN5:PN2)が80:20)に製造例8の硬化剤(CA1)を前記混合物1モル当たり約0.06モルが存在するように配合した。次に、DSC分析を通じて前記混合物の加工温度、硬化反応開始温度を確認し、これから組成物のプロセスウィンドウを計算した。
製造例6の化合物(PN6)および製造例2の化合物(PN2)の混合物(PN6とPN2の重量比(PN6:PN2)が80:20)に製造例8の硬化剤(CA1)を前記混合物1モル当たり約0.06モルが存在するように配合した。次に、DSC分析を通じて前記混合物の加工温度、硬化反応開始温度を確認し、これから組成物のプロセスウィンドウを計算した。
製造例7の化合物(PN7)および製造例2の化合物(PN2)の混合物(PN7とPN2の重量比(PN7:PN2)が80:20)に製造例8の硬化剤(CA1)を前記混合物1モル当たり約0.06モルが存在するように配合した。次に、DSC分析を通じて前記混合物の加工温度、硬化反応開始温度を確認し、これから組成物のプロセスウィンドウを計算した。
製造例5の化合物(PN5)に製造例8の硬化剤(CA1)を前記製造例5の化合物(PN5)1モル当たり0.06モルが存在するように配合した。次に、DSC分析を通じて前記混合物の加工温度、硬化反応開始温度を確認し、これから組成物のプロセスウィンドウを計算した。
製造例6の化合物(PN6)に製造例8の硬化剤(CA1)を前記製造例6の化合物(PN6)1モル当たり0.06モルが存在するように配合した。次に、DSC分析を通じて前記混合物の加工温度、硬化反応開始温度を確認し、これから組成物のプロセスウィンドウを計算した。
製造例7の化合物(PN7)に製造例8の硬化剤(CA1)を前記製造例7の化合物(PN7)1モル当たり0.06モルが存在するように配合した。次に、DSC分析を通じて前記混合物の加工温度、硬化反応開始温度を確認し、これから組成物のプロセスウィンドウを計算した。
Claims (11)
- 下記化学式1の平均単位式で表示され、重量平均分子量が700〜7,000の範囲内にある化合物:
[化学式1]
R1 aR2 bSiO(4−a−b)/2
化学式1でR1は、下記化学式2の置換基であり、R2は、水素原子、アルキル基、アルケニル基、アルコキシ基またはアリール基であり、aは、0.01〜0.4の範囲内の数であり、bは、0.5〜4の範囲内の数である:
- 融点が常温未満である、請求項1に記載の化合物。
- 下記化学式1の平均単位で表示される化合物由来の重合単位を含むフタロニトリル樹脂:
[化学式1]
R1 aR2 bSiO(4−a−b)/2
化学式1でR1は、下記化学式2の置換基であり、R2は、水素原子、アルキル基、アルケニル基、アルコキシ基またはアリール基であり、aは、0.01〜0.4の範囲内の数であり、bは、0.5〜4の範囲内の数である:
- 化学式1の平均単位で表示される化合物とは異なる構造を有するフタロニトリル化合物由来の重合単位をさらに含む、請求項4に記載のフタロニトリル樹脂。
- 芳香族アミン化合物の重合単位をさらに含む、請求項4に記載のフタロニトリル樹脂。
- 下記化学式1の平均単位を有する化合物と、硬化剤とを含む重合性組成物:
[化学式1]
R1 aR2 bSiO(4−a−b)/2
化学式1でR1は、下記化学式2の置換基であり、R2は、水素原子、アルキル基、アルケニル基、アルコキシ基またはアリール基であり、aは、0.01〜0.4の範囲内の数であり、bは、0.5〜4の範囲内の数である:
- 化学式1の平均単位で表示される化合物とは異なる構造を有するフタロニトリル化合物をさらに含む、請求項8に記載の重合性組成物。
- 硬化剤は、芳香族アミン化合物、フェノール化合物、無機酸、有機酸、金属または金属塩である、請求項8に記載の重合性組成物。
- 請求項4に記載のフタロニトリル樹脂と、充填剤とを含む複合体。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160143084A KR102089401B1 (ko) | 2016-10-31 | 2016-10-31 | 화합물 |
| KR10-2016-0143084 | 2016-10-31 | ||
| PCT/KR2017/011496 WO2018080088A1 (ko) | 2016-10-31 | 2017-10-18 | 화합물 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019517618A true JP2019517618A (ja) | 2019-06-24 |
| JP6710782B2 JP6710782B2 (ja) | 2020-06-17 |
Family
ID=62025192
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018563886A Active JP6710782B2 (ja) | 2016-10-31 | 2017-10-18 | 化合物 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US10913822B2 (ja) |
| EP (1) | EP3533799B1 (ja) |
| JP (1) | JP6710782B2 (ja) |
| KR (1) | KR102089401B1 (ja) |
| CN (1) | CN109415389B (ja) |
| WO (1) | WO2018080088A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019531391A (ja) * | 2016-11-25 | 2019-10-31 | エルジー・ケム・リミテッド | 化合物 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101959462B1 (ko) * | 2015-09-24 | 2019-03-18 | 주식회사 엘지화학 | 프탈로니트릴 화합물 |
| KR102071909B1 (ko) * | 2016-11-29 | 2020-01-31 | 주식회사 엘지화학 | 중합성 조성물 |
| KR102046576B1 (ko) | 2017-05-18 | 2019-11-21 | 주식회사 엘지화학 | 저마찰 중합성 조성물 |
| WO2018212533A1 (ko) * | 2017-05-18 | 2018-11-22 | 주식회사 엘지화학 | 저마찰 중합성 조성물 |
| KR102202060B1 (ko) | 2018-08-17 | 2021-01-12 | 주식회사 엘지화학 | 저마찰 수지 복합체 |
| CN112778525A (zh) * | 2020-12-31 | 2021-05-11 | 中硅艾德(厦门)新材料科技有限公司 | 一种常温下为液态的邻苯二甲腈单体及其合成方法 |
| CN116394600A (zh) * | 2023-03-28 | 2023-07-07 | 哈尔滨工业大学 | 一种硅氧烷改性邻苯二甲腈树脂基复合材料及其制备方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002519277A (ja) * | 1998-06-26 | 2002-07-02 | アメリカ合衆国 | フタロニトリル樹脂から誘導される炭素基質複合材 |
| US20030092907A1 (en) * | 2001-06-22 | 2003-05-15 | Snow Arthur W. | Phthalocyanines with peripheral siloxane substitution |
| US20160168326A1 (en) * | 2014-12-16 | 2016-06-16 | The Government Of The United States Of America, As Represented By The Secretary Of The Navy | Synthesis and polymerization of oligomeric aliphatic-aromatic based phthalonitriles |
| EP3211023A1 (en) * | 2014-10-24 | 2017-08-30 | Joint Stock Company Scientific and Production Association "Unichimtek" (JSC PSA "Unichimtek) | Phthalonitrile monomer modified with organosilicon fragments |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6001926A (en) | 1997-10-02 | 1999-12-14 | The United States Of America As Represented By The Secretary Of The Navy | Fiber-reinforced phthalonitrile composite cured with low-reactivity aromatic amine curing agent |
| AU6032199A (en) * | 1998-09-10 | 2000-04-03 | Spi Polyol, Inc. | Low temperature non-crystallizing liquid xylitol compositions and co-hydrogenation processes for making same |
| US9217064B2 (en) | 2013-01-24 | 2015-12-22 | The United States Of America, As Represented By The Secretary Of The Air Force | Thermosetting resins with enhanced cure characteristics containing organofunctional silane moieties |
| CN103387748B (zh) | 2013-07-22 | 2015-06-24 | 中国科学院化学研究所 | 有机无机杂化树脂与耐高温透波复合材料及其制备方法 |
-
2016
- 2016-10-31 KR KR1020160143084A patent/KR102089401B1/ko active Active
-
2017
- 2017-10-18 CN CN201780040126.3A patent/CN109415389B/zh active Active
- 2017-10-18 JP JP2018563886A patent/JP6710782B2/ja active Active
- 2017-10-18 EP EP17865878.7A patent/EP3533799B1/en active Active
- 2017-10-18 US US16/339,612 patent/US10913822B2/en active Active
- 2017-10-18 WO PCT/KR2017/011496 patent/WO2018080088A1/ko not_active Ceased
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002519277A (ja) * | 1998-06-26 | 2002-07-02 | アメリカ合衆国 | フタロニトリル樹脂から誘導される炭素基質複合材 |
| US20030092907A1 (en) * | 2001-06-22 | 2003-05-15 | Snow Arthur W. | Phthalocyanines with peripheral siloxane substitution |
| EP3211023A1 (en) * | 2014-10-24 | 2017-08-30 | Joint Stock Company Scientific and Production Association "Unichimtek" (JSC PSA "Unichimtek) | Phthalonitrile monomer modified with organosilicon fragments |
| US20160168326A1 (en) * | 2014-12-16 | 2016-06-16 | The Government Of The United States Of America, As Represented By The Secretary Of The Navy | Synthesis and polymerization of oligomeric aliphatic-aromatic based phthalonitriles |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019531391A (ja) * | 2016-11-25 | 2019-10-31 | エルジー・ケム・リミテッド | 化合物 |
| JP7080537B2 (ja) | 2016-11-25 | 2022-06-06 | エルジー・ケム・リミテッド | 化合物 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20190284338A1 (en) | 2019-09-19 |
| EP3533799B1 (en) | 2020-04-29 |
| JP6710782B2 (ja) | 2020-06-17 |
| KR20180047217A (ko) | 2018-05-10 |
| WO2018080088A1 (ko) | 2018-05-03 |
| CN109415389A (zh) | 2019-03-01 |
| EP3533799A4 (en) | 2019-10-16 |
| US10913822B2 (en) | 2021-02-09 |
| CN109415389B (zh) | 2021-08-24 |
| EP3533799A1 (en) | 2019-09-04 |
| KR102089401B1 (ko) | 2020-03-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6710782B2 (ja) | 化合物 | |
| JP6602394B2 (ja) | フタロニトリル化合物 | |
| JP6550153B2 (ja) | フタロニトリル樹脂 | |
| US10556859B2 (en) | Phthalonitrile compound | |
| JP6724144B2 (ja) | フタロニトリル樹脂 | |
| KR20170060897A (ko) | 프탈로니트릴 화합물 | |
| JP6630830B2 (ja) | フタロニトリル化合物 | |
| JP7080537B2 (ja) | 化合物 | |
| KR101985800B1 (ko) | 프탈로니트릴 화합물 | |
| KR20160137132A (ko) | 프탈로니트릴 화합물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181206 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20191017 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191028 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200120 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200511 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200527 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6710782 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |