JP2019072494A - 血圧推定装置及び方法並びにウェアラブル機器 - Google Patents
血圧推定装置及び方法並びにウェアラブル機器 Download PDFInfo
- Publication number
- JP2019072494A JP2019072494A JP2018196382A JP2018196382A JP2019072494A JP 2019072494 A JP2019072494 A JP 2019072494A JP 2018196382 A JP2018196382 A JP 2018196382A JP 2018196382 A JP2018196382 A JP 2018196382A JP 2019072494 A JP2019072494 A JP 2019072494A
- Authority
- JP
- Japan
- Prior art keywords
- blood pressure
- feature
- cardiovascular
- cardiovascular feature
- cardiac output
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 230000036772 blood pressure Effects 0.000 title claims abstract description 184
- 238000000034 method Methods 0.000 title claims abstract description 31
- 230000002526 effect on cardiovascular system Effects 0.000 claims abstract description 219
- 230000000747 cardiac effect Effects 0.000 claims description 128
- 230000035488 systolic blood pressure Effects 0.000 claims description 109
- 230000035487 diastolic blood pressure Effects 0.000 claims description 107
- 230000008859 change Effects 0.000 claims description 86
- 230000002792 vascular Effects 0.000 claims description 85
- 230000007423 decrease Effects 0.000 claims description 35
- 210000004204 blood vessel Anatomy 0.000 claims description 31
- 238000004891 communication Methods 0.000 claims description 28
- 239000000470 constituent Substances 0.000 claims description 14
- 238000002567 electromyography Methods 0.000 claims description 13
- 230000003247 decreasing effect Effects 0.000 claims description 4
- 238000000605 extraction Methods 0.000 description 22
- 239000000284 extract Substances 0.000 description 13
- 238000002565 electrocardiography Methods 0.000 description 9
- 230000007246 mechanism Effects 0.000 description 9
- 210000000707 wrist Anatomy 0.000 description 8
- 230000036541 health Effects 0.000 description 7
- 230000036581 peripheral resistance Effects 0.000 description 7
- 238000010586 diagram Methods 0.000 description 6
- 230000014509 gene expression Effects 0.000 description 6
- 230000003205 diastolic effect Effects 0.000 description 5
- 230000000875 corresponding effect Effects 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 230000035807 sensation Effects 0.000 description 4
- 238000003491 array Methods 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 230000000007 visual effect Effects 0.000 description 3
- 238000002091 elastography Methods 0.000 description 2
- 210000005240 left ventricle Anatomy 0.000 description 2
- 238000007726 management method Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 210000005245 right atrium Anatomy 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 101001135197 Rattus norvegicus Partitioning defective 3 homolog Proteins 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 125000003158 alcohol group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000009530 blood pressure measurement Methods 0.000 description 1
- 210000000748 cardiovascular system Anatomy 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 238000013500 data storage Methods 0.000 description 1
- 230000010339 dilation Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000013186 photoplethysmography Methods 0.000 description 1
- 238000007781 pre-processing Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/021—Measuring pressure in heart or blood vessels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/024—Detecting, measuring or recording pulse rate or heart rate
- A61B5/02416—Detecting, measuring or recording pulse rate or heart rate using photoplethysmograph signals, e.g. generated by infrared radiation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/103—Detecting, measuring or recording devices for testing the shape, pattern, colour, size or movement of the body or parts thereof, for diagnostic purposes
- A61B5/11—Measuring movement of the entire body or parts thereof, e.g. head or hand tremor, mobility of a limb
- A61B5/1102—Ballistocardiography
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/389—Electromyography [EMG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/72—Signal processing specially adapted for physiological signals or for diagnostic purposes
- A61B5/7235—Details of waveform analysis
Abstract
Description
前記センサーは、前記生体信号を獲得する複数のセンサーを含み得る。
前記血圧推定装置は、外部機器から生体信号を受信する通信部を更に含み得る。
前記第1心血管特徴は、心拍出量(cardiac output:CO)であり、前記第2心血管特徴は、総血管抵抗(total periphral resistance:TPR)であり得る。
前記プロセッサは、前記生体信号から心拍情報、前記生体信号の波形の形態、前記生体信号の最大点の時刻及び振幅、前記生体信号の最小点の時刻及び振幅、前記生体信号の波形の面積、並びに前記生体信号を構成する構成パルス波形の振幅及び時刻情報のうちの1つ以上を含む特徴点に基づいて、前記第1心血管特徴及び前記第2心血管特徴を抽出し得る。
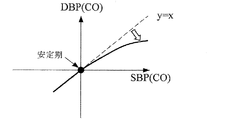
前記プロセッサは、前記第1変化傾向及び前記第2変化傾向に基づいて、収縮期血圧(SBP)及び拡張期血圧(DBP)を独立して推定し得る。
前記プロセッサは、前記第1心血管特徴を第3心血管特徴にスケーリングし、前記第2心血管特徴を第4心血管特徴にスケーリングし、前記第3心血管特徴に基づいて前記収縮期血圧を推定し、前記第4心血管特徴に基づいて前記拡張期血圧を推定し得る。
前記第1心血管特徴は、心拍出量であり、前記第2心血管特徴は、総血管抵抗であり得る。
前記プロセッサは、前記心拍出量を第1心拍出量及び第2心拍出量にスケーリングし、前記総血管抵抗を第1総血管抵抗及び第2総血管抵抗にスケーリングし、前記第1心拍出量及び前記第1総血管抵抗を線形結合して収縮期血圧を推定し、前記第2心拍出量及び前記第2総血管抵抗を線形結合して拡張期血圧を推定し得る。
前記プロセッサは、前記第1心拍出量及び前記第1総血管抵抗にそれぞれ第1心拍出量加重値及び第1総血管抵抗加重値を付与した後に線形結合し、前記第2心拍出量及び前記第2総血管抵抗にそれぞれ第2心拍出量加重値及び第2総血管抵抗加重値を付与した後に線形結合し得る。
前記プロセッサは、前記第1心拍出量及び前記第1総血管抵抗を線形結合した結果に所定の第1スケーリング要素を適用して収縮期血圧を推定し、前記第2心拍出量及び前記第2総血管抵抗を線形結合した結果に所定の第2スケーリング要素を適用して拡張期血圧を推定し得る。
前記プロセッサは、前記第1変化傾向及び前記第2変化傾向に基づいて、それぞれ前記第1心血管特徴及び前記第2心血管特徴のスケーリング程度を決定し得る。
前記プロセッサは、前記第1変化傾向が増加する場合、前記心拍出量の増加によって、前記第1心拍出量の増加率に対して前記第2心拍出量の増加率を同一にするか又は減少させ得る。
前記プロセッサは、前記第2変化傾向が減少する場合、前記総血管抵抗の減少によって、前記第1総血管抵抗の減少率に対して前記第2総血管抵抗の減少率を同一にするか又は増加させ得る。
前記血圧推定装置は、前記プロセッサの血圧推定結果を出力する出力部を更に含み得る。
前記第1心血管特徴は、心拍出量であり、前記第2心血管特徴は、総血管抵抗であり得る。
前記第1心血管特徴及び第2心血管特徴を抽出する段階は、前記生体信号から心拍情報、前記生体信号の波形の形態、前記生体信号の最大点の時刻及び振幅、前記生体信号の最小点の時刻及び振幅、前記生体信号の波形の面積、前記生体信号の時間経過、前記生体信号を構成する構成パルス波形の振幅及び時刻情報、並びに抽出された2つ以上の特徴点の間の内分点のうちの1つ以上を含む特徴点に基づいて、前記第1心血管特徴及び前記第2心血管特徴を抽出し得る。
前記血圧を推定する段階は、前記第1変化傾向及び前記第2変化傾向に基づいて、収縮期血圧(SBP)及び拡張期血圧(DBP)を独立して推定し得る。
前記血圧推定方法は、前記心拍出量を第1心拍出量及び第2心拍出量にスケーリングし、前記総血管抵抗を第1総血管抵抗及び第2総血管抵抗にスケーリングする段階を更に含み、前記血圧を推定する段階は、前記第1心拍出量及び前記第1総血管抵抗を線形結合して収縮期血圧を推定し、前記第2心拍出量及び前記第2総血管抵抗を線形結合して拡張期血圧を推定し得る。
前記心拍出量及び前記総血管抵抗をスケーリングする段階は、前記第1変化傾向及び前記第2変化傾向に基づいて、それぞれ前記第1心血管特徴及び前記第2心血管特徴のスケーリング程度を決定し得る。
前記スケーリングする段階は、前記第1変化傾向が増加する場合、前記心拍出量の増加によって、前記第1心拍出量の増加率に対して前記第2心拍出量の増加率を同一にするか又は減少させ得る。
前記スケーリングする段階は、前記第2変化傾向が減少する場合、前記総血管抵抗の減少によって、前記第1総血管抵抗の減少率に対して前記第2総血管抵抗の減少率を同一にするか又は増加させ得る。
前記血圧推定方法は、前記推定された血圧の結果を出力する段階を更に含み得る。
前記第1心血管特徴は、心拍出量であり、前記第2心血管特徴は、総血管抵抗であり得る。
前記プロセッサは、前記第1変化傾向及び前記第2変化傾向に基づいて、収縮期血圧(SBP)及び拡張期血圧(DBP)を独立して推定し得る。
前記プロセッサは、前記第1心血管特徴を第3心血管特徴にスケーリングし、前記第2心血管特徴を第4心血管特徴にスケーリングし、前記第3心血管特徴に基づいて前記収縮期血圧を推定し、前記第4心血管特徴に基づいて前記拡張期血圧を推定し得る。
前記ウェアラブル機器は、前記プロセッサの血圧推定結果を出力する表示部を更に含み得る。
前記ウェアラブル機器は、前記プロセッサの血圧推定結果を外部機器に伝送する通信部を更に含みうる。
前記プロセッサは、安定状態に比べて増加傾向を有する心拍出量に基づいて、前記拡張期血圧を推定するための心拍出量の第1スケーリング程度が前記収縮期血圧を推定するための心拍出量の第1スケーリング程度よりも更に小さくなるように決定し得る。
前記プロセッサは、安定状態に比べて減少傾向を有する総血管抵抗に基づいて、前記拡張期血圧を推定するための総血管抵抗の第2スケーリング程度が前記収縮期血圧を推定するための総血管抵抗の第2スケーリング程度よりも更に大きくなるように決定し得る。
110 獲得部
120、400、712 プロセッサ
210、713 通信部
220 出力部
230 保存部
250 外部機器
410 特徴点抽出部
420 特徴抽出部
430 スケーリング部
440 血圧推定部
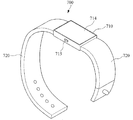
700 ウェアラブル機器
710 機器本体
711 脈波センサー
711a 光源
711b ディテクター
714 表示部
715 操作部
720 ストラップ
Claims (36)
- 被検体の生体信号を獲得するセンサーと、
前記生体信号に基づいて第1心血管特徴及び第2心血管特徴を抽出し、第1基準心血管特徴に比べて前記第1心血管特徴の第1変化傾向、及び第2基準心血管特徴に比べて前記第2心血管特徴の第2変化傾向に基づいて血圧を推定するプロセッサと、を備え、
前記第1変化傾向及び前記第2変化傾向は、互いに独立することを特徴とする血圧推定装置。 - 前記生体信号は、光電容積脈波(PPG)、心電図(ECG)、筋電図(EMG)、及び心臓弾動図(BCG)のうちの1つ以上を含むことを特徴とする請求項1に記載の血圧推定装置。
- 前記センサーは、前記生体信号を獲得する複数のセンサーを含むことを特徴とする請求項2に記載の血圧推定装置。
- 外部機器から生体信号を受信する通信部を更に含むことを特徴とする請求項1に記載の血圧推定装置。
- 前記プロセッサは、前記生体信号から心拍情報、前記生体信号の波形の形態、前記生体信号の最大点の時刻及び振幅、前記生体信号の最小点の時刻及び振幅、前記生体信号の波形の面積、並びに前記生体信号を構成する構成パルス波形の振幅及び時刻情報のうちの1つ以上を含む特徴点に基づいて、前記第1心血管特徴及び前記第2心血管特徴を抽出することを特徴とする請求項1に記載の血圧推定装置。
- 前記プロセッサは、前記第1変化傾向及び前記第2変化傾向に基づいて、収縮期血圧(SBP)及び拡張期血圧(DBP)を独立して推定することを特徴とする請求項1に記載の血圧推定装置。
- 前記プロセッサは、
前記第1心血管特徴を第3心血管特徴にスケーリングし、
前記第2心血管特徴を第4心血管特徴にスケーリングし、
前記第3心血管特徴に基づいて前記収縮期血圧を推定し、
前記第4心血管特徴に基づいて前記拡張期血圧を推定することを特徴とする請求項6に記載の血圧推定装置。 - 前記第1心血管特徴は、心拍出量であり、
前記第2心血管特徴は、総血管抵抗であることを特徴とする請求項1又は7に記載の血圧推定装置。 - 前記プロセッサは、
前記心拍出量を第1心拍出量及び第2心拍出量にスケーリングし、
前記総血管抵抗を第1総血管抵抗及び第2総血管抵抗にスケーリングし、
前記第1心拍出量及び前記第1総血管抵抗を線形結合して収縮期血圧を推定し、
前記第2心拍出量及び前記第2総血管抵抗を線形結合して拡張期血圧を推定することを特徴とする請求項8に記載の血圧推定装置。 - 前記プロセッサは、
前記第1心拍出量及び前記第1総血管抵抗にそれぞれ第1心拍出量加重値及び第1総血管抵抗加重値を付与した後に線形結合し、
前記第2心拍出量及び前記第2総血管抵抗にそれぞれ第2心拍出量加重値及び第2総血管抵抗加重値を付与した後に線形結合することを特徴とする請求項9に記載の血圧推定装置。 - 前記プロセッサは、
前記第1心拍出量及び前記第1総血管抵抗を線形結合した結果に所定の第1スケーリング要素を適用して収縮期血圧を推定し、
前記第2心拍出量及び前記第2総血管抵抗を線形結合した結果に所定の第2スケーリング要素を適用して拡張期血圧を推定することを特徴とする請求項9に記載の血圧推定装置。 - 前記プロセッサは、前記第1変化傾向及び前記第2変化傾向に基づいて、それぞれ前記第1心血管特徴及び前記第2心血管特徴のスケーリング程度を決定することを特徴とする請求項7に記載の血圧推定装置。
- 前記プロセッサは、前記第1変化傾向が増加する場合、前記心拍出量の増加によって、前記第1心拍出量の増加率に対して前記第2心拍出量の増加率を同一にするか又は減少させることを特徴とする請求項9に記載の血圧推定装置。
- 前記プロセッサは、前記第2変化傾向が減少する場合、前記総血管抵抗の減少によって、前記第1総血管抵抗の減少率に対して前記第2総血管抵抗の減少率を同一にするか又は増加させることを特徴とする請求項9に記載の血圧推定装置。
- 前記プロセッサの血圧推定結果を出力する出力部を更に含むことを特徴とする請求項1に記載の血圧推定装置。
- 被検体の生体信号を獲得する段階と、
前記生体信号に基づいて第1心血管特徴及び第2心血管特徴を抽出する段階と、
第1基準心血管特徴に比べて前記第1心血管特徴の第1変化傾向、及び第2基準心血管特徴に比べて前記第2心血管特徴の第2変化傾向に基づいて血圧を推定する段階と、を有し、
前記第1変化傾向及び前記第2変化傾向は、互いに独立することを特徴とする血圧推定方法。 - 前記生体信号は、光電容積脈波(PPG)、心電図(ECG)、筋電図(EMG)、及び心臓弾動図(BCG)のうちの1つ以上を含むことを特徴とする請求項16に記載の血圧推定方法。
- 前記第1心血管特徴は、心拍出量であり、
前記第2心血管特徴は、総血管抵抗であることを特徴とする請求項16に記載の血圧推定方法。 - 前記第1心血管特徴及び第2心血管特徴を抽出する段階は、前記生体信号から心拍情報、前記生体信号の波形の形態、前記生体信号の最大点の時刻及び振幅、前記生体信号の最小点の時刻及び振幅、前記生体信号の波形の面積、前記生体信号の時間経過、前記生体信号を構成する構成パルス波形の振幅及び時刻情報、並びに抽出された2つ以上の特徴点の間の内分点のうちの1つ以上を含む特徴点に基づいて、前記第1心血管特徴及び前記第2心血管特徴を抽出することを特徴とする請求項18に記載の血圧推定方法。
- 前記血圧を推定する段階は、前記第1変化傾向及び前記第2変化傾向に基づいて、収縮期血圧(SBP)及び拡張期血圧(DBP)を独立して推定することを特徴とする請求項18に記載の血圧推定方法。
- 前記心拍出量を第1心拍出量及び第2心拍出量にスケーリングし、前記総血管抵抗を第1総血管抵抗及び第2総血管抵抗にスケーリングする段階を更に含み、
前記血圧を推定する段階は、前記第1心拍出量及び前記第1総血管抵抗を線形結合して収縮期血圧を推定し、前記第2心拍出量及び前記第2総血管抵抗を線形結合して拡張期血圧を推定することを特徴とする請求項20に記載の血圧推定方法。 - 前記心拍出量及び前記総血管抵抗をスケーリングする段階は、前記第1変化傾向及び前記第2変化傾向に基づいて、それぞれ前記第1心血管特徴及び前記第2心血管特徴のスケーリング程度を決定することを特徴とする請求項21に記載の血圧推定方法。
- 前記スケーリングする段階は、前記第1変化傾向が増加する場合、前記心拍出量の増加によって、前記第1心拍出量の増加率に対して前記第2心拍出量の増加率を同一にするか又は減少させることを特徴とする請求項22に記載の血圧推定方法。
- 前記スケーリングする段階は、前記第2変化傾向が減少する場合、前記総血管抵抗の減少によって、前記第1総血管抵抗の減少率に対して前記第2総血管抵抗の減少率を同一にするか又は増加させることを特徴とする請求項22に記載の血圧推定方法。
- 前記推定された血圧の結果を出力する段階を更に含むことを特徴とする請求項16に記載の血圧推定方法。
- 被検体に着用される本体と、
前記本体の両端に連結され、被検体を取り囲んだ状態で本体を被検体に固定するストラップと、
前記本体に装着されて被検体から生体信号を獲得するセンサーと、
前記獲得された生体信号に基づいて第1心血管特徴及び第2心血管特徴を抽出し、第1基準心血管特徴に比べて前記第1心血管特徴の第1変化傾向、及び第2基準心血管特徴に比べて前記第2心血管特徴の第2変化傾向に基づいて血圧を推定するプロセッサと、を備え、
前記第1変化傾向及び前記第2変化傾向は、互いに独立することを特徴とするウェアラブル機器。 - 前記センサーは、光電容積脈波(PPG)センサー、心電図(ECG)センサー、筋電図(EMG)センサー、及び心臓弾動図(BCG)センサーのうちの1つ以上を含むことを特徴とする請求項26に記載のウェアラブル機器。
- 前記第1心血管特徴は、心拍出量であり、
前記第2心血管特徴は、総血管抵抗であることを特徴とする請求項26に記載のウェアラブル機器。 - 前記プロセッサは、前記第1変化傾向及び前記第2変化傾向に基づいて、収縮期血圧(SBP)及び拡張期血圧(DBP)を独立して推定することを特徴とする請求項26に記載のウェアラブル機器。
- 前記プロセッサは、
前記第1心血管特徴を第3心血管特徴にスケーリングし、
前記第2心血管特徴を第4心血管特徴にスケーリングし、
前記第3心血管特徴に基づいて前記収縮期血圧を推定し、
前記第4心血管特徴に基づいて前記拡張期血圧を推定することを特徴とする請求項29に記載のウェアラブル機器。 - 前記プロセッサの血圧推定結果を出力する表示部を更に含むことを特徴とする請求項26に記載のウェアラブル機器。
- 前記プロセッサの血圧推定結果を外部機器に伝送する通信部を更に含むことを特徴とする請求項26に記載のウェアラブル機器。
- 被検体に着用されて被検体から血圧を推定するウェアラブル機器であって、
被検体から生体信号を獲得するセンサーと、
前記生体信号に基づいて第1心血管特徴及び第2心血管特徴を抽出し、収縮期血圧を推定するための前記第1心血管特徴及び前記第2心血管特徴に対して互いに異なる第1スケーリング程度を決定し、拡張期血圧を推定するための前記第1心血管特徴及び前記第2心血管特徴に対して互いに異なる第2スケーリング程度を決定し、前記第1スケーリング程度が適用された第1心血管特徴の線形結合及び前記第2スケーリング程度が適用された第2心血管特徴の線形結合に基づいてそれぞれ収縮期血圧及び拡張期血圧を推定するプロセッサと、を備え、
前記収縮期血圧及び前記拡張期血圧を推定するための前記第1心血管特徴及び前記第2心血管特徴に対する前記第1スケーリング程度及び前記第2スケーリング程度は、それぞれ前記第1心血管特徴及び前記第2心血管特徴の変化傾向に基づいて独立して決定されることを特徴とするウェアラブル機器。 - 前記第1心血管特徴は、心拍出量であり、
前記第2心血管特徴は、総血管抵抗であることを特徴とする請求項33に記載のウェアラブル機器。 - 前記プロセッサは、安定状態に比べて増加傾向を有する心拍出量に基づいて、前記拡張期血圧を推定するための心拍出量の第1スケーリング程度が前記収縮期血圧を推定するための心拍出量の第1スケーリング程度よりも更に小さくなるように決定することを特徴とする請求項34に記載のウェアラブル機器。
- 前記プロセッサは、安定状態に比べて減少傾向を有する総血管抵抗に基づいて、前記拡張期血圧を推定するための総血管抵抗の第2スケーリング程度が前記収縮期血圧を推定するための総血管抵抗の第2スケーリング程度よりも更に大きくなるように決定することを特徴とする請求項34に記載のウェアラブル機器。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2017-0135399 | 2017-10-18 | ||
| KR20170135399 | 2017-10-18 | ||
| KR10-2018-0076434 | 2018-07-02 | ||
| KR1020180076434A KR102568904B1 (ko) | 2017-10-18 | 2018-07-02 | 혈압 추정 장치 및 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019072494A true JP2019072494A (ja) | 2019-05-16 |
| JP7317486B2 JP7317486B2 (ja) | 2023-07-31 |
Family
ID=66281436
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018196382A Active JP7317486B2 (ja) | 2017-10-18 | 2018-10-18 | 血圧推定装置及び方法並びにウェアラブル機器 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP7317486B2 (ja) |
| KR (1) | KR102568904B1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022121340A (ja) * | 2021-02-08 | 2022-08-19 | 阿部 真一 | 血圧計の測定結果から、血液の流動速度、血管の直径、血管の流動抵抗、心臓の負荷率などを算出して血圧計に表示する。 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102576126B1 (ko) * | 2019-09-19 | 2023-09-06 | 삼성전자주식회사 | 생체정보 추정 장치 및 방법 |
| KR102389499B1 (ko) * | 2019-11-25 | 2022-04-25 | 한국전자통신연구원 | 실시간 혈압 추정 장치 및 그 방법 |
| KR20220153790A (ko) * | 2021-05-12 | 2022-11-21 | (주)참케어 | 혈압 측정 시스템 및 이를 이용한 혈압 측정 방법 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10295657A (ja) * | 1997-04-24 | 1998-11-10 | Matsushita Electric Ind Co Ltd | 血圧測定装置 |
| JP2004154231A (ja) * | 2002-11-05 | 2004-06-03 | Seiko Instruments Inc | 血圧測定装置及び血圧測定方法 |
| JP2006192052A (ja) * | 2005-01-13 | 2006-07-27 | Yokogawa Electric Corp | 血圧測定装置 |
| JP2015054223A (ja) * | 2013-09-13 | 2015-03-23 | 旭化成株式会社 | 血圧情報出力装置、血圧情報出力プログラム、媒体、血圧情報出力方法 |
| WO2015098977A1 (ja) * | 2013-12-25 | 2015-07-02 | 旭化成株式会社 | 脈波測定装置、携帯機器、医療機器システム、及び生体情報コミュニケーションシステム |
| JP2018121829A (ja) * | 2017-01-31 | 2018-08-09 | 株式会社Arblet | 血圧情報測定システム、血圧情報測定方法、血圧情報測定プログラム、血圧情報測定装置、サーバ装置、演算方法及び演算プログラム |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20160047838A (ko) * | 2014-10-23 | 2016-05-03 | 삼성전자주식회사 | 생체 신호 처리 방법 및 그 장치 |
| KR20170048970A (ko) | 2015-10-27 | 2017-05-10 | 삼성전자주식회사 | 혈압 추정 방법 |
-
2018
- 2018-07-02 KR KR1020180076434A patent/KR102568904B1/ko active IP Right Grant
- 2018-10-18 JP JP2018196382A patent/JP7317486B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10295657A (ja) * | 1997-04-24 | 1998-11-10 | Matsushita Electric Ind Co Ltd | 血圧測定装置 |
| JP2004154231A (ja) * | 2002-11-05 | 2004-06-03 | Seiko Instruments Inc | 血圧測定装置及び血圧測定方法 |
| JP2006192052A (ja) * | 2005-01-13 | 2006-07-27 | Yokogawa Electric Corp | 血圧測定装置 |
| JP2015054223A (ja) * | 2013-09-13 | 2015-03-23 | 旭化成株式会社 | 血圧情報出力装置、血圧情報出力プログラム、媒体、血圧情報出力方法 |
| WO2015098977A1 (ja) * | 2013-12-25 | 2015-07-02 | 旭化成株式会社 | 脈波測定装置、携帯機器、医療機器システム、及び生体情報コミュニケーションシステム |
| JP2018121829A (ja) * | 2017-01-31 | 2018-08-09 | 株式会社Arblet | 血圧情報測定システム、血圧情報測定方法、血圧情報測定プログラム、血圧情報測定装置、サーバ装置、演算方法及び演算プログラム |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022121340A (ja) * | 2021-02-08 | 2022-08-19 | 阿部 真一 | 血圧計の測定結果から、血液の流動速度、血管の直径、血管の流動抵抗、心臓の負荷率などを算出して血圧計に表示する。 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102568904B1 (ko) | 2023-08-22 |
| KR20190043453A (ko) | 2019-04-26 |
| JP7317486B2 (ja) | 2023-07-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11123022B2 (en) | Blood pressure estimating apparatus and blood pressure estimating method | |
| KR102480197B1 (ko) | 생체정보 추정 장치 및 방법 | |
| JP7317486B2 (ja) | 血圧推定装置及び方法並びにウェアラブル機器 | |
| KR102626585B1 (ko) | 혈압 추정 장치 및 방법 | |
| EP3636146B1 (en) | Apparatus and method for estimating blood pressure | |
| US20230301526A1 (en) | Apparatus and method for estimating blood pressure | |
| EP3878352A1 (en) | Apparatus and method for estimating bio-information | |
| US11744526B2 (en) | Apparatus and method for estimating blood pressure | |
| KR20200078795A (ko) | 혈압 추정 장치 및 방법 | |
| KR102580268B1 (ko) | 생체정보 추정 모델의 캘리브레이션 장치 및 방법과, 생체정보 추정 장치 | |
| KR20210007368A (ko) | 생체정보 추정 장치 및 방법 | |
| KR20220107909A (ko) | 혈압 추정 장치 및 방법 | |
| KR102576126B1 (ko) | 생체정보 추정 장치 및 방법 | |
| KR20210072998A (ko) | 생체정보 추정 장치 및 방법 | |
| KR20200144688A (ko) | 생체정보 추정 모델의 캘리브레이션 장치 및 방법과, 생체정보 추정 장치 | |
| KR20200088700A (ko) | 생체정보 추정 장치 및 방법 | |
| US20230038983A1 (en) | Apparatus and method for estimating bio-information |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210412 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210419 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220228 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220405 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220705 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20221025 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230227 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20230227 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20230309 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20230314 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230530 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230602 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230620 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230719 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7317486 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |