JP2017514876A - 治療用胎盤組成物、その製造法及び使用法 - Google Patents
治療用胎盤組成物、その製造法及び使用法 Download PDFInfo
- Publication number
- JP2017514876A JP2017514876A JP2016566997A JP2016566997A JP2017514876A JP 2017514876 A JP2017514876 A JP 2017514876A JP 2016566997 A JP2016566997 A JP 2016566997A JP 2016566997 A JP2016566997 A JP 2016566997A JP 2017514876 A JP2017514876 A JP 2017514876A
- Authority
- JP
- Japan
- Prior art keywords
- composition
- placental
- tissue
- cells
- cryopreserved
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/48—Reproductive organs
- A61K35/50—Placenta; Placental stem cells; Amniotic fluid; Amnion; Amniotic stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/32—Bones; Osteocytes; Osteoblasts; Tendons; Tenocytes; Teeth; Odontoblasts; Cartilage; Chondrocytes; Synovial membrane
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/36—Skin; Hair; Nails; Sebaceous glands; Cerumen; Epidermis; Epithelial cells; Keratinocytes; Langerhans cells; Ectodermal cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/38—Albumins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P41/00—Drugs used in surgical methods, e.g. surgery adjuvants for preventing adhesion or for vitreum substitution
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
Description
本出願は、2014年、5月7日に、出願名「Immunocompatible Chorionic Membrane Products」及び「Immunocompatible Amniotic Membrane Products」と共出願されており、それらの全体を参照により本明細書に組み込む。
i)第一胎盤(例えば、羊膜または絨毛膜)組織を取得すること、
ii)その第一胎盤組織から、胎盤細胞を取得すること、
iii)第二胎盤(例えば、羊膜または絨毛膜)組織を取得すること、
iv)第二胎盤組織を破壊して、細胞外基質、治療因子、胎盤細胞及び組織断片を含む分散液を形成すること、及び
v)前記の胎盤細胞と分散液を組み合わせて、1つ以上の胎盤組成物及び/または産物を形成すること、
を含む平行プロセス法により生産される。
(i)胎盤(例えば、羊膜または絨毛膜)組織を取得すること、
(ii)その胎盤組織をコラゲナーゼに曝露すること、
(iii)その胎盤組織を、第一部分と第二部分に分けること、
(iv)第一胎盤部から胎盤細胞を単離すること、
(v)第二胎盤部を破壊して、治療因子、細胞外基質、胎盤細胞、及び組織断片部を含む分散液を形成すること、及び
(vi)前記の胎盤細胞と胎盤分散液を組み合わせて、当該胎盤組成物を形成すること、
のステップを含む。
(i)少なくとも1つの胎盤(例えば、羊膜または絨毛膜)組織を取得すること、
(ii)その胎盤組織を、胎盤細胞を放出するのに十分な時間で、少なくとも1つのコラゲナーゼに曝露すること、
(iii)そのコラゲナーゼに曝露された胎盤組織から、放出された胎盤細胞を単離すること、
(iv)そのコラゲナーゼに曝露された胎盤組織を破壊して、1つ以上の治療因子、細胞外基質、胎盤細胞、及び組織断片部を含む分散液を形成すること、及び
(v)前記の胎盤細胞と胎盤分散液を組み合わせて、少なくとも1つの胎盤組成物を形成すること、
のステップを含む。
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、
(iii)1つ以上の細胞外基質成分、及び
(iv)(i)、(ii)、(iii)またはそれらの組み合わせを含む組織断片部、
を有する、少なくとも1つの破壊された胎盤組織を含んで提供され、ここで、その冷凍保存された胎盤組織組成物のそれに続く解凍後に、その胎盤細胞の約40%を上回る細胞が生存しており、及びその組成物は、機能的免疫原性細胞(例えば、冷凍保存及びそれに続く解凍の前の、当該胎盤組織組成物と比較して)が枯渇している。
a.少なくとも1つの破壊された胎盤組織で、
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、
(iii)1つ以上の細胞外基質成分、及び
(iv)(i)、(ii)、(iii)またはそれらの組み合わせを含む組織断片部、
を含み、
b.1つ以上の冷凍保存剤、
を含んで提供され、ここで、その冷凍保存された胎盤組織組成物のそれに続く解凍後に、その胎盤細胞の約40%を上回る細胞が生存しており、そして、その組成物は、機能的免疫原性細胞が枯渇しており、そしてここで、1つ以上の胎盤細胞、治療因子、細胞外基質成分、またはそれらの組み合わせが、少なくとも1つの治療的な利点を与えるのに効果的な量で存在する。
a.胎盤細胞、治療因子、及び細胞外基質成分を有する胎盤組織を提供すること、
b.少なくとも1つの酵素でその胎盤組織を消化して、胎盤細胞及び胎盤組織断片部の懸濁液を形成すること、
c.その胎盤細胞及び胎盤組織断片部を単離すること、
d.その胎盤組織を破壊して、胎盤分散液を形成すること、
e.前記の胎盤細胞と胎盤分散液を組み合わせて、胎盤組織組成物を形成すること、及び
f.その胎盤組織組成物を冷凍保存すること、
のステップを含む胎盤組織組成物の調合に対する、少なくとも1つのプロセスを提供し、ここで、それに続くその凍結保存された胎盤組織組成物の解凍後に、その胎盤細胞の約40%を上回る細胞が生存しており、そしてここで、その組成物は、機能的免疫原性細胞が枯渇している。
a.破壊された胎盤組織で、
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、
(iii)1つ以上の細胞外基質成分、及び
(iv)(i)、(ii)、(iii)またはそれらの組み合わせを含む1つ以上の組織断片部、
を含み、及び
b.1つ以上の冷凍保存剤、
を含み、ここで、冷凍保存及びそれに続くその胎盤組織組成物の解凍後に、その胎盤細胞の約40%を上回る細胞が生存しており、そしてその組成物は、機能的免疫原性細胞が枯渇しており、そしてここで、1つ以上の胎盤細胞、治療因子、細胞外基質成分またはそれらの組み合わせが、
(i)炎症性サイトカインの量及び/または活性を低下させる、
(ii)抗炎症サイトカインの量及び/または活性を増加させる、
(iii)活性酸素種の量及び/または活性を低下させる、
(iv)抗酸化物質の量及び/または活性を増加させる、
(v)プロテアーゼの量及び/または活性を低下させる、
(vi)細胞増殖を増加させる、
(vii)血管新生を増加させる、及び/または
(viii)細胞移行を増加させる、
ことの1つ以上を実施するのに効果的な量で提供される。
a.ミンチ化された胎盤組織分散液で、
(i).1つ以上の胎盤細胞、
(ii).1つ以上の治療因子、及び
(iii).1つ以上の細胞外基質成分、
(iv).(i)、(ii)、(iii)またはそれらの組み合わせを含む1つ以上の組織断片部を含み、及び
b.少なくとも1つの冷凍保存剤、
を含む、1つ以上の冷凍保存された胎盤組織組成物を提供し、ここで、続くその凍結保存された胎盤組織組成物の解凍後に、その胎盤細胞の約40%を上回る細胞が生存しており、そしてここで、その組成物は、機能的免疫原性細胞が大幅に枯渇している。
概要
本発明技術の1つ以上の胎盤組成物が、機械的/物理的破壊または酵素による消化若しくは両者の組み合わせにより生産でき、全体または部分的な組織損傷若しくは組織欠損に対する投与に際し、実質的かつ優れた治療価値を持つ医薬品を生産できることが、意外にも発見されている。本発明技術の胎盤組成物はまた、予期せぬ複数の有利な性質を示した。
本発明技術の胎盤組成物は、作用圧力下で変形する能力などの流体の特定の特徴を共有し、そして粘度の尺度で定量化できる。したがって、そのような本発明の胎盤組成物は、適用されるものの表面上に広げることができる。例えば、胎盤組成物の1mLを、皮膚の約1cm2を超えて、約10cm2を超えて、約25cm2を超えて、約50cm2を超えて、または約100cm2を超えて、局所的に覆うように広げることができる。この流体(すなわち、流動性である)の性質は、シート状の産物(例えば、皮膚移植)では、治療が必要な様々な部分(例えば、トンネル傷、穿刺傷、大きな圧力傷、曲面など)への用途が限定されるという問題を解決する。それはまた、迅速な応用手段を提供する。拡散適用に加えて、当該胎盤組成物は、例えば、注射でまたは移植としての適用が可能である。本発明技術の本胎盤組成物の流動性は、トンネル傷、関節の咬合及び曲面への適用などの、新しい利用に対応した実践を可能にする。
理論に捉われずに記述すれば、本発明者らは、生存する胎盤細胞の存在が、それらが存在する場所で、内因性の細胞と多少類似した方法で、当該胎盤組成物に、生理学的刺激に応答する能力を与えていると考える。動的応答の証拠は、投与後の様々な時点での、刺激を受けた治療因子の放出またはその治療因子プロファイルにおける変化を含むことができる。
胎盤細胞は、任意の胎盤組織(例えば、絨毛膜または羊膜)から取得しても良い。胎盤細胞は、少なくとも1つの細胞型(例えば、MSCs)の細胞の生存を維持する任意の方法で、胎盤組織を加工することにより取得しても良い。例えば、胎盤細胞は、胎盤組織から単離または精製(例えば、絨毛膜のコラゲナーゼによる消化により)しても良く、または1つ以上の胎盤成分(例えば、細胞外基質)から、単離なしで取得しても良い。
胎盤分散液は、胎盤(例えば、絨毛膜)を破壊することにより、提供されても良い。この胎盤組織の破壊は、組織を破壊する任意の物理的/機械的方法(すなわち、「組織破壊体」または「破壊手段」の使用)により達成されても良い。例えば、破壊は、特に、均質化、浸軟、ブレンダーの使用、粉砕、またはミンチ化などを含んでも良い。破壊は、加えてまたは互換的に、せん断破壊、さいの目カット、またはみじん切りを含んでも良い。破壊は、加えてまたは互換的に、超音波処理を含んでも良い。
本発明技術の胎盤組成物は、その治療因子が、その胎盤分散液の成分またはその胎盤細胞またはそれらの組み合わせによりその胎盤組成物に放出された成分である、1つ以上の治療因子を含んでも良い。
本発明技術の胎盤組成物は、皮膚科学的に許容される医薬品として投与できる。任意で、医薬品有効成分または賦形剤若しくはそれらの組み合わせは、胎盤組成物との併用または添加若しくはそれらとの組み合わせで、加えることができる。
粘度は、治療が進行している兆候の関数として変動する、本発明技術において有用で望ましい値である。例えば、胎盤組成物の広い対象範囲(すなわち、皮膚の広い部分)またはより低い濃度が望ましい場合、低い粘度の処方物が有利である。低い粘度の処方物の例示としては、約1,000cPから約50,000cP、または約2,000cPから約25,000cP、若しくは約2,000cPから約10,000cP、または約5,000cPから約15,000cPのものである。そのような低い粘度の処方物は、適用される本発明技術の胎盤組成物の拡散を容易にすることができる。
概要
本発明技術の胎盤組成物は、本明細書に教示される技術的特徴を与える任意の適切な方法で、胎盤から製造されても良い。本発明技術に従う任意の胎盤組織は、有用である。本明細書に説明される、本発明技術のいくつかの実施形態は、その胎盤分散液が、栄養膜成分を枯渇しているかまたは欠いている絨毛膜の分散液である胎盤組成物を、特に受け入れることを意図している。別の選択肢もまた、想定内である。
(i)胎盤(例えば、絨毛膜または羊膜)組織を取得すること、
(ii)その胎盤組織を、1つ以上の基質分解酵素(例えば、コラゲナーゼ、任意でII型コラゲナーゼ)で消化すること、
(iii)その消化された胎盤組織から胎盤細胞を取得すること、
(iv)その消化された胎盤組織を、組織破壊体で破壊して、治療因子、細胞外基質、胎盤細胞、及び組織断片部を含む胎盤分散液を形成すること、及び
(v)前記の胎盤細胞と胎盤分散液を組み合わせて、当該胎盤組成物を形成すること、
を含むステップにより製造される。
(i)第一胎盤(例えば、絨毛膜または羊膜)組織を取得すること、
(ii)その第一胎盤組織を、1つ以上の基質分解酵素(例えば、コラゲナーゼ、任意でコラゲナーゼタイプII)で消化すること、
(iii)その消化された第一胎盤組織から胎盤細胞を取得すること、
(iv)第二胎盤組織を取得すること、
(v)その第二胎盤組織を、組織破壊体で破壊して、治療因子、細胞外基質、胎盤細胞、及び組織断片部を含む胎盤分散液を形成すること、及び
(vi)前記の胎盤細胞と胎盤分散液を組み合わせて、当該胎盤組成物を形成すること、
を含むステップにより製造される。
(i)胎盤組織を取得すること、
(ii)その組織を、おおまかに均一なサイズの断片部にミンチ化して、胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤分散液を形成すること、
を含むステップにより製造される。
a.胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤組織を与えること、
b.少なくともその胎盤組織の一部分を破壊して、胎盤組織断片部、胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤分散液を形成すること、及び
c.その胎盤分散液を冷凍保存して、胎盤組織組成物を形成し、ここで、その胎盤組織組成物の冷凍保存及びそれに続く解凍の後に、その胎盤細胞の40%を上回る細胞が生存しており、そしてここで、その組成物が、機能的な免疫原性細胞を枯渇していること、
のステップを含む。
a.胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤組織を与えること、
b.少なくともその胎盤組織を、少なくとも1つの酵素で消化して、胎盤細胞及び胎盤組織断片部の懸濁液を形成すること、及び
c.その胎盤細胞と胎盤組織断片部を分離すること、ならびに
d.その胎盤組織断片部を破壊して、分散液を形成すること、及び
e.その胎盤細胞とその分散液を組み合わせて、胎盤組織組成物を形成すること、ならびに
f.その胎盤組織組成物を冷凍保存し、ここで、その胎盤組織組成物の冷凍保存そしてそれに続く解凍の後に、その胎盤細胞の40%を上回る細胞が生存しており、そしてここでその組成物が、機能的免疫原性細胞を枯渇していること、
のステップを含む。
1つの実施形態において、当該胎盤組成物は、免疫的に互換性である。免疫互換性は、胎盤または胎盤由来組織(若しくはそれらの羊膜)からの免疫原性細胞または因子若しくは免疫原性を排除する、任意の選択的枯渇ステップにより達成できる。
少なくとも1つの実施形態において、栄養膜は、枯渇または実質的に除去されて、当該胎盤細胞または胎盤分散液若しくはその両方を誘導する当該胎盤組織が生産される。驚くことに、そのような胎盤組成物は、
a.実質的に非免疫原性であり、
b.顕著な治癒効果を提供し、及び
c.高められた治療効果を提供する、
ことの(特に)優れた性質の1つ以上を有する。
1つの実施形態において、機能性マクロファージは、当該胎盤組成物から枯渇させまたは除去する。意外なことに、そうような胎盤組成物は、
実質的に非免疫原性であり、
顕著な治癒効果を提供し、及び
高められた治療効果を提供する、
ことの優れた特徴の1つ以上を有する。
1つの実施形態において、母体血液細胞は、当該胎盤組成物から枯渇させまたは除去する。意外なことに、そのような胎盤組成物は、
実質的に非免疫原性であり、
顕著な治癒効果を提供し、及び
高められた治療効果を提供する、
ことの優れた特徴の1つ以上を有する。
本発明技術の胎盤組成物は、新鮮な状態で使用されても良く、または一定期間保存されても良い。
前述で考察のように、本明細書に記載の当該胎盤組成物及び特に冷凍保存された組成物(例えば、羊膜、絨毛膜、及び/または絨毛羊膜組成物)は、多数の有益な治療活性及び効果を促進するのに効果的な、一定量の生存細胞、治療因子、及び細胞外基質成分を提供する。本明細書に記載の方法において、当該組成物を適用しても良く、及び一定量の治療因子、生存細胞、及び細胞外基質成分を提供し、ならびに同様のまたは類似の治療有益性を提供する任意の数の治療因子を産生するために、内因性細胞を成長させる環境を提供する。
(i)炎症性サイトカインの量及び/または活性の低減、
(ii)抗炎症性サイトカインの量及び/または活性の増加、
(iii)活性酸素種の量及び/または活性の低減、
(iv)抗酸化物質の量及び/または活性の増加、
(v)プロアテーゼ量及び/または活性の低減、
(vi)細胞増殖の増加、
(vii)血管新生の増加、及び/または
(viii)細胞移行の増加、
を促進するのに効果的な、組織成分(例えば、細胞、治療因子、細胞外基質成分及びそれらの組み合わせ)の治療に必要な量を提供する。
(i)炎症性サイトカインの量及び/または活性を減らし、
(ii)抗炎症性サイトカインの量及び/または活性を増やし、
(iii)プロアテーゼ量及び/または活性を減らし、
(iv)血管新生を増やし、及び/または
(vi)細胞移行を増やす、
ことに効果的な量で、1つ以上の胎盤細胞、治療因子、細胞外基質成分またはそれらの組み合わせを提供する。
無傷胎盤を、インフォームドコンセントの後に、登録された組織バンクから取得した。この胎盤を、その母体表面(ザラザラの面)を下向きにして、滅菌トレイに乗せた。その羊−絨毛膜を切り取り、その胎盤から取り出した。次に、その絨毛膜を羊膜から分離し、そしてD−PBSで2回洗浄した。
絨毛膜(実施例1で取得した)を、II型コラゲナーゼ溶液(DMEM中に300U/mL)の200mLで、37℃で10分間の培養により、消化した。次に、残った未消化の絨毛膜を除去し(その組織断片部)、コラゲナーゼ及び胎盤細胞(その細胞断片部)を含む消化懸濁液を残した。
絨毛膜(18−84時間の抗生物質処理後、実施例1から取得した)を、37℃で10±2分間、200mLのII型コラゲナーゼ溶液(DMEM中に300U/mL)中で培養することにより、消化した。次に、未消化で残った絨毛膜を除去し(その組織断片部)、コラゲナーゼ及び胎盤細胞(その細胞断片部)を含む消化懸濁液を残した。
絨毛膜(抗生物質で18−84時間処置後、実施例1から取得した)を、冷蔵したガラス皿に移し、残った抗生物質溶液を除去するために洗浄し、そしてハーブミンチ器で6分間ミンチ化し、小さく、均等なサイズの断片部を得た。
[CM重量(g)×1.8(ml/g)−懸濁液の容積(mL)=添加する生理食塩水の容積(mL)]
絨毛膜(抗生物質で18−84時間処置後、実施例1から取得した)を、冷蔵したガラス皿に移し、そして6分間ミンチ化し、小さく、均等なサイズの断片部を得た。
限定的なII型コラゲナーゼによる消化が、生存細胞を含んだ懸濁液を得るために機能しているか、そして当該胎盤細胞の完全性を未だ保っている(例えば、治療因子を保持しそして生存細胞を残している)かどうかを、本発明において試験した。II型コラゲナーゼによる10分間の短い消化は、部分的に無傷組織を残し、そしてさらなる処理を可能にした。加えて、10分間のコラゲナーゼによる消化は、多数の生存細胞を生産できた。
複数の胎盤を加工し(D153、D154、D155、D156)、そして実施例6のように胎盤組成物を調合した。消化直後に、生存及び非生存細胞の細胞計数を実施した(図2)。冷凍及び解凍前後で、生存細胞の細胞計数を実施した(図3)。細胞を、血球計数器を使用して計数し、そして生存細胞を区別するために、トリパンブルー染色を利用した。細胞数のデータを集計し、そして平均値を求めた。
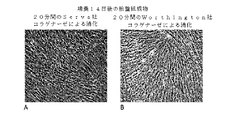
当該胎盤分散液中の生存細胞の優れた回収を行うための、製造法を検討した。特に、均質化前に、消化による細胞単離のステップの有無で製造される、胎盤組成物における生存細胞のレベルを決定する実験を行った。簡単に言えば、実施例1に記載の手順に従い、胎盤を準備した。次に、得られた絨毛膜を、半分に分割した。その半分の組織を、実施例2に記載のように加工した。その他の半分を、その均質化ステップに先立ち、II型コラゲナーゼでの消化により、細胞単離なしで、実施例2における組織断片部と同じ方法で加工した。細胞を、血球計数器を使用して数え、そして生存細胞を区別するために、トリパンブルー染色を利用した。そのデータを、図4に提供する。
異なるドナーからの胎盤で、実施例1及び実施例2に詳細に記された手順に従い、複数の胎盤組成物を調合し、そして治療因子を分析した。簡単に記述すると、各胎盤組成物からの1mLのホモジネートを、16,000rcfの速度のマイクロ遠心分離機で、10分間遠心分離した。
本発明技術の複数の胎盤組成物における、細胞表現型を決定するために、蛍光活性化細胞ソーティング法(FACS)を実施した。胎盤組成物を、実施例1及び実施例2に詳細に記される手順に従い調合した。当該組成物を解凍し、そしてそれに続いて細胞破片を取り除くために、100μmのフィルターを通してろ過した。次に、単一細胞懸濁液を、Beckman TJ−6を使用して、2000rpmの速度で10分間遠心分離し、そしてD−PBSで2回洗浄した。各洗浄の後、上清を捨て、そして細胞を、2mLのFACS染色緩衝液(D−PBS+0.09%NaN3+1%FBS)中に再懸濁した。
実施例1に詳細に記載の手順に従い、3つの胎盤(D138、D139、及びD140)を加工し、そして各絨毛膜を、半分に分割した。絨毛組織の各断片部を、実施例2に詳細に記載の手順に従い、
Plasma−LyteA(CTR溶液)中に、10%DMSO及び5%HSA、
Plasma−LyteA中に、5%DMSO及び5%HSA、
生理食塩水中に、5%DMSO、
生理食塩水中に、10%のグリセロール、
の冷凍保存剤の1つと共に加工した。
最終組成物の細胞生存率を、異なる冷凍保存溶液及び異なる絨毛組織の加工ステップ(ミンチ化対均質化)を使用して比較した。
・グループ1=コントロールグループ(均質化した組織断片部)、生理食塩水中の5%DMSO
・グループ2=試験グループ(ミンチ化した組織断片部)、生理食塩水中の5%DMSO
・グループ3=試験グループ(ミンチ化した組織断片部)、生理食塩水中の5%DMSO及び1%HSA
・グループ4=試験グループ(ミンチ化した組織断片部)、生理食塩水中の10%DMSO及び5%HSA
II型コラゲナーゼにおける絨毛膜などの、胎盤組織を消化するのに最適な時間を決定するために、3つの異なるドナーからの絨毛膜を分析した。実施例1の手順に従い、当該絨毛膜を加工した。次に、抗生物質溶液を除去するために、各絨毛膜組織を2回洗浄し、そして3分割した。初期重量を得るために(0分)、各組織片を計量し、次にII型コラゲナーゼ溶液(300U/mL)中で10分、20分、または30分間消化した。
実施例3の限定的な消化法を、当該胎盤組織が羊膜の場合に適用して、試験した。以下の手順を実施した。
1.胎盤の加工。
a.羊膜を取り出し、そしてD−PBSで2回洗浄する。
b.羊膜を、ほぐれた赤血球に浸す。
i.必要ならば、指で、組織から無い赤血球を取り除く。
c.羊膜組織を、抗生物質カクテル中で24時間培養する。
2.抗生物質カクテルから羊膜組織を取り出し、そしてD−PBSで2回洗浄する。
3.羊膜組織を、37℃で200mLのトリプシン溶液(0.25%)中で、30分間培養する。
4.トリプシン溶液から羊膜組織を取り出し、そしてD−PBSで2回洗浄する。
5.羊膜組織を、37℃で200mLのII型コラゲナーゼ溶液(DMEM中に300U/mL)中で、10分間培養する。
6.II型コラゲナーゼ溶液から羊膜組織を取り出し、そしてD−PBSで2回洗浄する。
7.II型コラゲナーゼ及びトリプシンでの生存細胞懸濁液の加工。
a.各懸濁液を、913rcfの速度で5分間、遠心分離する。
b.各上清を注ぎ出し、そして10mLのD−PBSに交換する。
i.細胞を、洗浄のためD−PBSに再懸濁する。
c.細胞懸濁液を、913rcfの速度で5分間、遠心分離する。
d.上清を注ぎ出し、そして細胞を、2mLの冷凍保存剤(生理食塩水中に5%DMSO)中で再懸濁する。
e.ペレットを組み合わせる。
8.羊膜組織の加工。
a.羊膜組織を、その羊膜重量(g)と等量の容積の冷凍保存剤(mL)と共に、均質化容器に収める。例えば、その羊膜の重量が、25gであれば、冷凍保存剤の25mLと共に、均質化容器に収める。
b.その羊膜組織及び冷凍保存剤を、氷上に少なくとも10分置く。
c.組織ホモジナイザーを使用して、5秒間の高速で2回均質化する。
9.単離した生存細胞をホモジネートと組み合わせ、そして十分に混合する(当該「胎盤組成物」)。
10.バイアル瓶に等分し、そして4℃で30−60分間静置する。
11.使用するまで、−80℃で冷凍する。
放出される相当数の生存胎盤細胞、
保存された内因性の治療因子、
保存された内因性の胎盤タンパク質(例えば、基質タンパク質)、及び
治療に効果的な成分、
という予期せぬ結果をもたらす、と結論づけられる。
本明細書に教示される製造ステップ(例えば、限定されたコラゲナーゼによる消化、胎盤組織の破壊前の胎盤細胞の取り出し、そして限定された破壊の方法)は、非常に効果的な治療組成物をもたらす。当該細胞断片部及び均質化された組織断片部由来の、最終胎盤組成物中の生存細胞数を評価した。
本発明技術の胎盤組成物は、創傷の治癒治療に対して望ましい、耐久性のある効果を発揮する。本技術に記載の当該絨毛膜由来の胎盤組成物内の、細胞外基質及び生存細胞の存在は、少なくとも14日間存在する、創傷治癒及び血管新生にとり、重要であるとして知られるタンパク質カクテルを可能にする。
実施例1及び実施例3に詳細に記載の手順に従って加工した胎盤組成物を、慢性創傷に見られる低酸素症状を模倣した、低酸素環境への応答に対して試験した。
実施例1及び実施例2に記載の手順に従って加工した、3ロットの胎盤組成物(D144、D145、D146)に対して、冷凍保存前後に、その血管新生増殖因子VEGF及びbFGFの含有量を測定した。
インターフェロン−2α(IFN−2α)及び形質転換増殖因子−β3(TGF−β3)は、瘢痕と拘縮形成の防止に重要な役割を果たすと文献に記述されている(Kwanら、Hand Clin,2009,25:511、Tredgetら、Surg Clin North Am 1997,77:701)。IFN−2αは、コラーゲン及びフィブロネクチン合成ならびに線維芽細胞を介した傷の拘縮を減らすとして知られている。臨床的には、IFN−2αが皮下投与され、そして瘢痕の質を改善したことが示されている(Nedelecら、Lab Clin Med 1995,126:474)。TGF−β3は、細胞外基質の沈着を調節し、そして齧歯動物の皮膚創傷モデルにおいて注射をした場合、瘢痕形成を減少させることが示されている。臨床的には、TGF−β3を創傷部に注射した場合、瘢痕の外観の改善が示されている(Occleston etら、J Biomater Sci Polym Ed 2008,19:1047)。
実施例1及び実施例2で記載のように調合した、複数ロットの胎盤組成物のTGF−β3含有量を測定した。4ロットの冷凍保存した胎盤組成物を解凍し、そしてマイクロ遠心分離機において、16,000rcfの速度で10分間遠心分離した。上清中のTGF−β3濃度を、ELISAで測定した。胎盤組成物におけるTGF−β3発現を示している結果を、図14に表す。
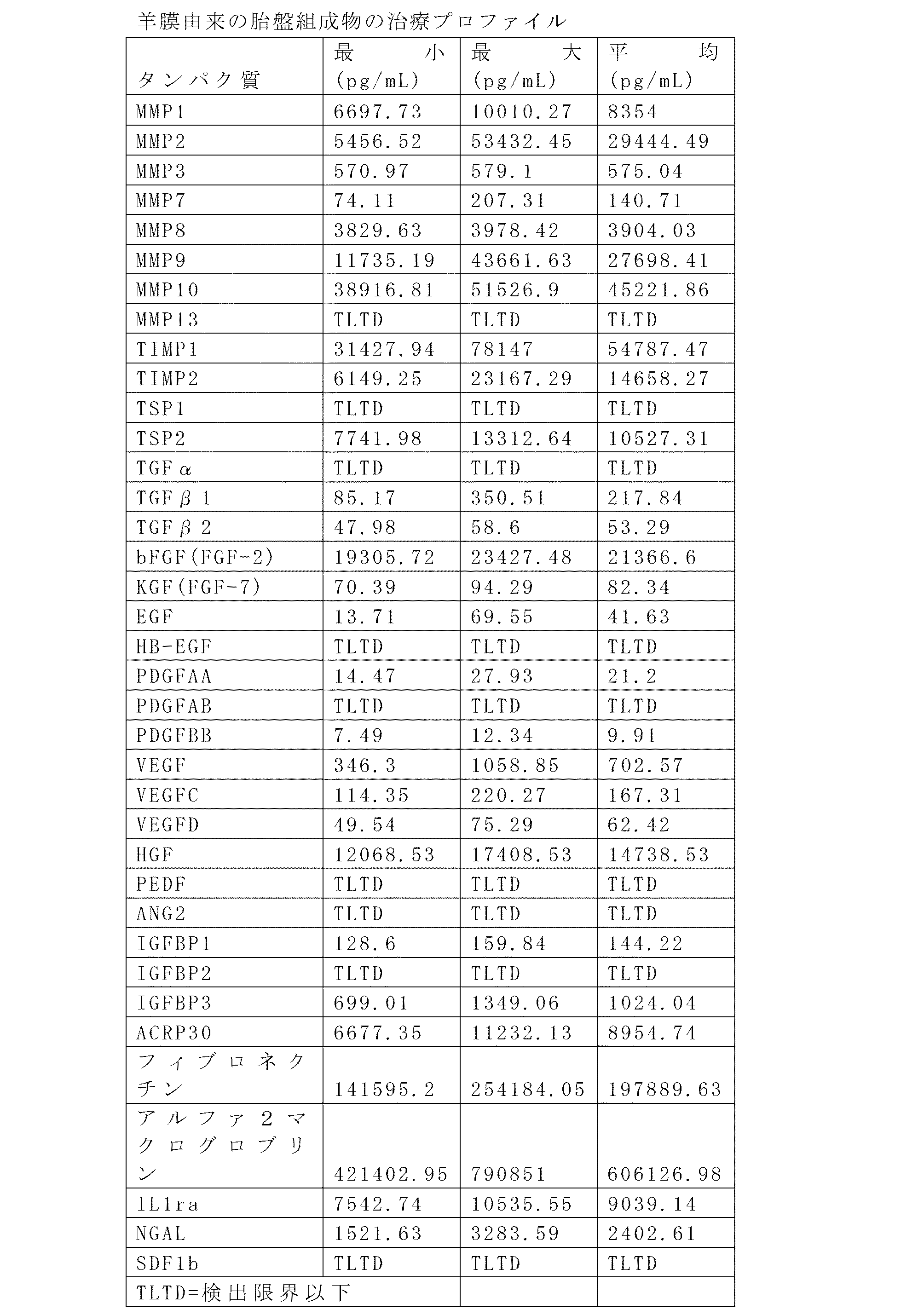
当該絨毛膜由来でそして実施例1及び実施例2で記載のように加工した胎盤組成物を、組織修復に重要であるタンパク質(例えば、治療因子または組織修復タンパク質)の存在に対して、分析した。
本発明の任意の実施形態において、胎盤細胞は、接着性であり、特にCD105などの細胞マーカーを発現し、そしてCD45などのその他のマーカーの発現を欠き、そして脂肪細胞、骨芽細胞、及び軟骨細胞への分化能力を示す。
実施例1及び実施例4で記載のように加工した、29ロットの胎盤組成物中の、生存細胞量を測定した。実施例4に記載のように作った胎盤組成物は、ミンチ化により生成した小組織片内に、当該胎盤細胞を含んでいる。これらの胎盤細胞を、血球計数器及びトリパンブルー排除を利用して定量化するためには、その細胞を最初に、コラゲナーゼ消化により、その組織断片部から分離せねばならない。
慢性創傷に見られる炎症状態を模倣した、炎症への応答に対して、胎盤組成物を試験した。当該胎盤組成物の免疫調節能力を決定するために、PBMCs(末梢血単核細胞)によるTNF−α産生の阻害を測定した。
慢性創傷はしばしば、再生段階への進展に際して、傷を防ぐMMPs(マトリックスメタロプロテアーゼ)及びエラスターゼなどのタンパク質分解酵素を、不釣り合いなほど高いレベルで有する。実施例1及び実施例4により加工した、ミンチ化した胎盤産物を、プロテアーゼ活性を媒介するその能力に対して、エラスターゼ阻害アッセイを試験した。
ミンチ化及び消化の胎盤組成物中の、血管新生増殖因子VEGFの量を、2ロットに対して決定した。
当該ミンチ化された組織断片部に埋め込まれている、ミンチ化及び消化の胎盤組成物のVEGFを捉えるために、胎盤組成物を、グアニジン塩酸中での溶解に供した。
当該ミンチ化の組織断片部に埋め込まれている、ミンチ化胎盤組成物のbFGFを捉えるために、胎盤組成物を、組織抽出緩衝液中で溶解に供した。前述の実験では、ELISAによるbFGFは、グアニジンHCl処理との互換性がないことを示したので、互換的な溶解緩衝液を検討した。
ミンチ化及び消化の胎盤組成物が、増殖因子の放出を、経時的に持続することを証明するために、その組成物を2週間培養し、そしてVEGF含有量を測定した。
ミンチ化胎盤組成物の細胞増殖能力を試験した。胎盤細胞を播種し、そして14日間培養した。
骨再生における、ミンチ化胎盤組成物の使用に対応する、異なるキャリアの互換性を試験した。
−80℃で24ヶ月の長期間における、産物劣化の可能性を評価するために、当該最終組成物の安定性を試験した。産物劣化の指標は、生存細胞数の減少及び細胞生存率の低下である。生存細胞及び細胞生存率の数値を、3ロットの胎盤組成物に対して、初期の冷凍温度の完全低下後及び冷凍24か月後で決定した。さらに、冷凍後12ヶ月及び24か月の無菌試験を実施した。
実施例1及び実施例4に記載の手順(ハーブミンチ器でのミンチ化)に従い調合した胎盤組成物の組織断片部のサイズを、実施例1及び実施例5に記載の手順(メッザルーナでのミンチ化)で調合した胎盤組成物と比較した。最終組成物を解凍し、及び10μLを血球計数器に移した。5μLのトリパンブルーを加え、そして丸いカバーガラスを、その細胞懸濁液の表面に置いた。ハーブミンチ器またはメッザルーナを使用して調合した最終組成物の組織断片部のサイズを比較した。ハーブミンチ器でミンチ化した絨毛膜の組織断片部の平均サイズは、0.421mm2(n=14)であり、そしてメッザルーナでミンチ化した絨毛膜に対しては、1.137mm2(n=14)であった。メッザルーナでミンチ化した絨毛膜の組織断片部は、ハーブミンチ器でミンチ化した絨毛膜の組織断片部に比べて、著しく大きかった(図26を参照)。
背景
34才の女性は、傷害の後、7.5ヶ月間も解消せずに残る、日常的な腰痛、臀部痛、及び彼女の右下肢の後方から両足側面に広がる知覚障害を持っていた。
身体検査で、1+の両側アキレス腱反射を伴う、2+の両側膝蓋反射、少ない右足背屈及びポジティブな真っ直ぐな右側の足上げが、明らかになった。X線及びCTで、右椎間孔の狭小化及び崩壊があること、ならびに脊椎症の証拠はないことが、明らかになった。
L5−S1 ヘルニア右椎間孔の狭小化と崩壊。
L5−S1の機械的不安定を伴う右L5及びS1の神経根障害。右の足首の弱さは、椎間板ヘルニア及び右下肢の脊髄神経根障害に一致。
傷害の約12か月後、右側のL5−S1の脚間窩を、マイクロ手術により解剖し、そして不具合物質を、脊椎関節突起切除術、椎間孔拡大術、及びマイクロ椎間板切除術により除去した。1mLの胎盤組成物と共に、15ccの脱灰骨基質(DBM)から成る、骨移植の準備を完了した。両移植物質は、移植において放射線透過性である。一旦減圧が完了したら、その端板を皮膚から剥がし、そして斜めの8mmのT−PALのPEEKスペーサーを、DBM+胎盤組成物の5ccと共に封入し、そして脊椎用に配置した。L5−S1の左背外側塊に沿って広範な剥皮術を、マイクロ手術の解剖を介して、完了した。DBM+胎盤組成物の残りの10ccを、アンレー融合のために、左背瘤に適用した。ロッド及びキャップアセンブリを完了した。
手術後6ヶ月での、冠状断面及び矢状断面CTは、左面関節を介した早期融合及び早期の椎体間骨梁形成の証拠を示している。椎体間骨移植およびハードウェアは、最適な位置にある。早期時点での、CTの薄層断面像は、非一体化を特定はできるが、しかし融合の特定に十分な感度ではない。早期の骨融合は、通常は、最短で6−12ヶ月で、CTで可視化できる(Williams A,Gornet M,Burkus K.CT Evaluation of Lumbar Interbody Fusion:Current Concepts.AJNR Am J Neuroradiol 2005;26:2057−2066)。
トンネル傷を伴っている患者を、少なくとも4から6週間の間、1mLの冷凍保存の胎盤組成物を週1回投与し、治療する。その傷の再上皮化及び閉鎖がある場合、治療を停止する。
本明細書に記載のように、当該羊膜及び絨毛膜に存在する胎生マクロファージは、組織免疫原性の主要な供給源である。理論に捉われずに記述すれば、本発明者らは、胎盤膜及び組成物からのCD14+胎生マクロファージの除去は、リンパ球の活性化を防止し、そして炎症性サイトカインのレベル及び組織の免疫原性を低下させる、と考える。胎生胎盤膜中のマクロファージは、TNF−αなどの炎症性の分泌により、細菌由来のLPSに対応する。したがって、各々の重要な生産段階で、胎盤膜の組織免疫原性を特徴づけるために、LPS応答に対するTNF−αの分泌を本明細書で使用する。各生産段階からのサンプルは、栄養膜(T)、絨毛栄養膜を伴う羊膜(ACT)、絨毛栄養膜(CT)、絨毛膜(CM)、及び羊膜(AM)を含んでいた。
Claims (110)
- 冷凍保存された胎盤組織組成物であって、
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、
(iii)1つ以上の細胞外基質成分、及び
(iv)(i)、(ii)、(iii)またはそれらの組み合わせ、
を含む破壊された胎盤組織を含み、ここで、前記冷凍保存された胎盤組織組成物の、それに続く解凍後に、その胎盤細胞の40%を上回る細胞が生存しており、且つその組成物が、機能性免疫原性細胞を枯渇している、前記冷凍保存された胎盤組織組成物。 - 前記胎盤組織組成物の冷凍保存及びそれに続く解凍後に、その生存細胞が、少なくとも1,000細胞/mLである、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織組成物の冷凍保存及びそれに続く解凍後に、その生存細胞が、少なくとも10,000細胞/mLである、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織組成物の冷凍保存及びそれに続く解凍後に、その生存細胞が、少なくとも20,000細胞/mLである、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織組成物の冷凍保存及びそれに続く解凍後に、その胎盤細胞の70%を上回る細胞が生存している、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織が、大幅に減らされた量の栄養膜細胞を有する絨毛膜胎盤組織である、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織が、羊膜組織である、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織組成物が、創傷治癒を促進する、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織組成物が、組織再生を促進する、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記組織組成物が、大幅に減らされた量の機能性CD14+マクロファージを有する、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記胎盤組織組成物が、冷凍保存剤をさらに含む、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記冷凍保存剤が、DMSO、グリセリン、グリセロール、糖、グリコール、プロピレングリコール、エチレングリコール、プロパンジオール、ポリエチレングリコール(PEG)、1,2−プロパンジオール(PROH)ポリビニルピロリドン、ヒドロキシエチル澱粉、多糖類、単糖類、アルギン酸、トレハロース、ラフィノース、デキストラン、ヒト血清アルブミン、フィコール、リポタンパク質、ポリビニルピロリドン、ヒドロキシエチルストラーチ(hydroxyethyl strarch)、自己血漿、及びそれらの混合物から成る群から選ばれる、請求項11に記載の冷凍保存された胎盤組織組成物。
- 前記冷凍保存剤が、前記組成物の最終容積の約3%から約100%から成る、請求項11に記載の冷凍保存された胎盤組織組成物。
- 前記冷凍保存剤が、前記組成物の最終容積の約3%から約50%から成る、請求項11に記載の冷凍保存された胎盤組織組成物。
- 前記冷凍保存剤が、前記組成物の最終容積の約3%から約10%から成る、請求項14に記載の冷凍保存された胎盤組織組成物。
- 前記組成物が、アルブミンをさらに含む、請求項11に記載の冷凍保存された胎盤組織組成物。
- 前記組成物が、薬学的に許容されるキャリアをさらに含む、請求項11に記載の冷凍保存された胎盤組織組成物。
- 前記組成物が、薬学的に許容される容器中に包装された、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記容器が、バイアル瓶、パウチ袋、袋、瓶、試験管、及びシリンジから選ばれる、請求項18に記載の冷凍保存された胎盤組織組成物。
- 前記枯渇した機能性免疫原性細胞が、母体血液細胞、新生児血液細胞、組織マクロファージ、栄養膜である、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記免疫原性細胞の枯渇した量が、免疫応答を産生するのに十分なレベル以下の量で、少なくとも1つの免疫原性因子を産生する、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記免疫原性細胞の枯渇した量が、検出限界を下回る量で、少なくとも1つの免疫原性因子を産生する、請求項21に記載の冷凍保存された胎盤組織組成物。
- 前記免疫原性細胞の枯渇した量が、350pg/cm2以下の量のTNF−αを産生する、請求項21に記載の冷凍保存された胎盤組織組成物。
- 前記免疫原性細胞の枯渇が、前記組成物を、約2℃から約8℃の温度に、約2分から約240分間静置することからもたらされる、請求項1に記載の冷凍保存された胎盤組織組成物。
- 前記組成物を、約2℃から約8℃の温度に、約10分から約60分間静置する、請求項24に記載の冷凍保存された胎盤組織組成物。
- 前記1つ以上の胎盤細胞が、上皮細胞、間充織幹細胞、線維芽細胞、またはそれらの組み合わせの1つ以上を含む、請求項1に記載の冷凍保存された胎盤組織組成物。
- 冷凍保存された胎盤組織組成物であって、
a.破壊された胎盤組織組成物で、
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、
(iii)1つ以上の細胞外基質成分、及び
(iv)(i)、(ii)、(iii)またはそれらの組み合わせ、
を含み、且つ
b.1つ以上の冷凍保存剤、
を含み、ここで、前記冷凍保存された胎盤組織組成物の、それに続く解凍後に、その胎盤細胞の40%を上回る細胞が生存しており、且つ、前記組成物が、機能性免疫原性細胞を枯渇しており、ここで、前記1つ以上の胎盤細胞、治療因子、細胞外基質成分、またはそれらの組み合わせが、治療の有効性を提供するのに効果的な量で存在する、前記冷凍保存された胎盤組織組成物。 - 冷凍保存された胎盤組織組成物であって、
a.破壊された胎盤組織組成物で、
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、
(iii)1つ以上の細胞外基質成分、及び
(iv)(i)、(ii)、(iii)またはそれらの組み合わせ、
を含み、且つ
b.1つ以上の冷凍保存剤、
を含み、ここで、前記胎盤組織組成物の、冷凍及びそれに続く解凍後に、その胎盤細胞の40%を上回る細胞が生存しており、及び前記組成物が、機能性免疫原性細胞を枯渇しており、ならびに前記1つ以上の胎盤細胞、治療因子、細胞外基質成分またはそれらの組み合わせが、
(i)炎症性サイトカインの量及び/または活性を低下させる、
(ii)抗炎症サイトカインの量及び/または活性を増加させる、
(iii)活性酸素種の量及び/または活性を低下させる、
(iv)抗酸化物質の量及び/または活性を増加させる、
(v)プロテアーゼの量及び/または活性を低下させる、
(vi)細胞増殖を増加させる、
(vii)血管新生を増加させる、及び/または
(viii)細胞移行を増加させる、
ことに有効な量で提供される、前記冷凍保存された胎盤組織組成物。 - 前記1つ以上の胎盤細胞、治療因子、細胞外基質成分またはそれらの組み合わせが、生体外の細胞において、
(i)炎症性サイトカインの量及び/または活性の低下、
(ii)抗炎症サイトカインの量及び/または活性の増加、
(iii)活性酸素種の量及び/または活性の低下、
(iv)抗酸化物質の量及び/または活性の増加、
(v)プロテアーゼの量の低下、
(vi)細胞増殖の増加、
(vii)血管新生の増加、及び/または
(viii)細胞移行の増加、
を促進するのに効果的な量で存在する、請求項28に記載の組成物。 - 前記1つ以上の胎盤細胞、治療因子、細胞外基質成分またはそれらの組み合わせが、生体内において、
(i)炎症性サイトカインの量及び/または活性の低下、
(ii)抗炎症サイトカインの量及び/または活性の増加、
(iii)活性酸素種の量及び/または活性の低下、
(iv)抗酸化物質の量及び/または活性の増加、
(v)プロテアーゼの量及び/または活性の低下、
(vi)細胞増殖の増加、
(vii)血管新生の増加、及び/または
(viii)細胞移行の増加、
を促進するのに効果的な量で存在する、請求項28に記載の組成物。 - 前記組成物が、治療の有効性が必要な対象者に適用され、ここで、前記1つ以上の胎盤細胞、治療因子、細胞外基質成分またはそれらの組み合わせが、
(i)炎症性サイトカインの量及び/または活性の低下、
(ii)抗炎症サイトカインの量及び/または活性の増加、
(iii)活性酸素種の量及び/または活性の低下、
(iv)抗酸化物質の量及び/または活性の増加、
(v)プロテアーゼの量及び/または活性の低下、
(vi)細胞増殖の増加、
(vii)血管新生の増加、及び/または
(viii)細胞移行の増加、
をすることに効果的な量で存在する、請求項1に記載の組成物。 - 前記組成物が、創傷または組織欠損の治療に使用される、請求項31に記載の冷凍保存された胎盤組織組成物。
- 前記創傷が、裂傷、擦り傷、火傷、切開、穿刺、発射に起因する傷、表皮の傷、皮膚の傷、慢性の傷、急性の傷、外部の傷、内部の傷、先天性の傷、潰瘍、褥瘡、糖尿病性潰瘍、トンネル傷、外科手術中またはそれに付随して生じた傷、静脈の潰瘍、脊髄損傷、眼の外傷または炎症、耳鼻科の傷害、及び虚血壊死から成る群から選ばれる、請求項32に記載の冷凍保存された胎盤組織組成物。
- 前記組成物が、組織移植手術、腱手術、靭帯手術、骨手術、脳神経外科、及び脊髄外科から成る群から選ばれる外科手術に使用される、請求項32に記載の冷凍保存された胎盤組織組成物。
- 前記組成物が、直接または間接的に組織再生を刺激する、請求項32に記載の冷凍保存された胎盤組織組成物。
- 前記組織が、ヒト組織である、請求項35に記載の冷凍保存された胎盤組織組成物。
- 前記ヒト組織が、軟骨、皮膚、靭帯、腱、または骨である、請求項36に記載の冷凍保存された胎盤組織組成物。
- 冷凍保存された胎盤組織組成物であって、
a.ミンチ化された胎盤組織分散液で、
(i)1つ以上の胎盤細胞、
(ii)1つ以上の治療因子、及び
(iii)1つ以上の細胞外基質成分、
(iv)(i)、(ii)、(iii)またはそれらの組み合わせ、
を含み、且つ
b.冷凍保存剤、
を含み、ここで、前記冷凍保存された胎盤組織組成物の、それに続く解凍後に、その胎盤細胞の40%を上回る細胞が生存しており、ここで、前記組成物が、機能性免疫原性細胞を大幅に枯渇している、前記冷凍保存された胎盤組織組成物。 - 前記冷凍保存された胎盤組成物が、室温で10分を下回る時間で解凍できる、請求項1から38のいずれか1項に記載の冷凍保存された胎盤組織組成物。
- 前記冷凍保存された胎盤組成物が、室温で3分を下回る時間で解凍できる、請求項39に記載の冷凍保存された胎盤組成物。
- 前記冷凍保存された胎盤組成物が、室温で1分を下回る時間で解凍できる、請求項40に記載の冷凍保存された胎盤組成物。
- 前記1つ以上の組織断片が、約0.01mm2から約5mm2のサイズである、請求項38に記載の冷凍保存された胎盤組織組成物。
- 前記組織断片が、約0.2mm2から約2mm2のサイズである、請求項42に記載の冷凍保存された胎盤組織組成物。
- 前記組織断片が、約100μmから約5μmの長さである、請求項38に記載の冷凍保存された胎盤組織組成物。
- 前記細胞の生存率が、冷凍貯蔵された際に、少なくとも24ヶ月間維持される、請求項1から44のいずれか1項に記載の冷凍保存された胎盤組織組成物。
- 前記冷凍保存された胎盤組織組成物が、解凍前に長期間貯蔵される、請求項1から44のいずれか1項に記載の冷凍保存された胎盤組織組成物。
- 前記長期間が、約6ヶ月から約36ヶ月である、請求項1から44のいずれか1項に記載の冷凍保存された胎盤組織組成物。
- 前記細胞の生存率が、解凍されても実質的に維持されている、請求項46または47のいずれかに記載の冷凍保存された胎盤組織組成物。
- 対象者のトンネル状態の傷の治療方法であって、請求項1または38のいずれかに記載の冷凍保存された胎盤組成物を、そのトンネル傷の部位に必要に応じて投与することを含む、前記治療方法。
- 対象者の創傷または組織欠損の治療方法であって、請求項1または38のいずれかに記載の冷凍保存された胎盤組成物を必要に応じて投与することを含む、前記治療方法。
- 前記投与が、その投与で炎症性サイトカインの量または活性を減らすのに効果的な量である、請求項50に記載の方法。
- 前記投与が、その投与で抗炎症性サイトカインの量または活性を増やすのに効果的な量である、請求項50に記載の方法。
- 前記投与が、その投与で炎症を抑えるのに効果的な量である、請求項50に記載の方法。
- 前記投与が、その投与で血管新生を促進するのに効果的な量である、請求項50に記載の方法。
- 前記量が、投与でVEGF発現または活性を増加させるのに効果的である、請求項54に記載の方法。
- 前記量が、投与でbFGF発現または活性を増加させるのに効果的である、請求項54に記載の方法。
- 前記量が、投与で抗酸化症状を提供するのに効果的である、請求項50に記載の方法。
- 前記創傷が、裂傷、擦り傷、火傷、切開、穿刺、発射に起因する傷、表皮の傷、皮膚の傷、慢性の傷、急性の傷、外部の傷、内部の傷、先天性の傷、潰瘍、褥瘡、糖尿病性潰瘍、トンネル傷、外科手術中またはそれに付随して生じた傷、静脈の潰瘍、脊髄損傷、眼の外傷、及び虚血壊死から成る群から選ばれる、請求項50から57のいずれか1項に記載の方法。
- 前記創傷または組織欠損が、トンネル傷である、請求項50から57のいずれか1項に記載の方法。
- 前記創傷または組織欠損が、外科手術によりまたはその間にできた、請求項50から57のいずれか1項に記載の方法。
- 前記外科手術が、骨修復手術である、請求項60に記載の前記方法。
- 創傷または組織欠損における、血管新生の促進方法であって、請求項1または38のいずれかに記載の冷凍保存された胎盤組成物を、血管新生を促進するのに効果的な量で投与するステップを含む、前記方法。
- 前記創傷または組織欠損が、トンネル傷である、請求項62に記載の前記方法。
- 前記冷凍保存された胎盤組成物が、VEGFの発現増加を促進するのに効果的な量で投与される、請求項62に記載の方法。
- 前記冷凍保存された胎盤組成物が、少なくとも投与後14日間でVEGFの発現増加を促進するのに効果的な量で投与される、請求項64に記載の方法。
- 前記冷凍保存された胎盤組成物が、bFGFの発現増加を促進するのに効果的な量で投与される、請求項64に記載の方法。
- 瘢痕形成の予防または低減方法であって、請求項1または38のいずれかに記載の冷凍保存された胎盤組成物を、瘢痕形成を予防または低減するのに効果的な量で、必要に応じてその部位に投与することを含む、前記瘢痕形成の予防または低減方法。
- 前記冷凍保存された胎盤組成物が、IFN−2αの発現を増加させるのに効果的な量で、瘢痕形成を低減するのに効果的な量で投与される、請求項67に記載の方法。
- 前記冷凍保存された胎盤組成物が、TGF−β3の発現を増加させるのに効果的な量で投与される、請求項67に記載の方法。
- 前記TGF−β3の発現を増加させる量が、瘢痕形成を低減するのに効果的である、請求項67に記載の方法。
- 創傷治癒の改善方法であった、請求項1または38のいずれかに記載の冷凍保存された胎盤組成物を必要に応じて投与することを含み、ここで前記冷凍保存された胎盤組成物が、1つ以上の治療因子の発現増加を促進させるのに効果的な量で与えられる、前記創傷治癒の改善方法。
- 組織再生の直接または間接的な刺激方法であって、請求項1または38のいずれかに記載の冷凍保存された胎盤組成物を必要に応じて投与することを含み、ここで前記冷凍保存された胎盤組成物が、1つ以上の治療因子の発現増加を促進させるのに効果的な量で与えられる、前記組織再生の直接または間接的な刺激方法。
- 創傷における炎症の抑制方法であって、請求項1または38のいずれかに記載の前記冷凍保存された胎盤組成物の、その創傷に効果的な量を投与することを含む、前記創傷における炎症の抑制方法。
- 前記冷凍保存された胎盤組成物が、投与でTNF−αの発現または活性を低下させるのに効果的な量で投与される、請求項73に記載の方法。
- 必要に応じた、部位でのプロテアーゼ活性の低減方法であって、その部位への投与で前記プロテアーゼ活性を減らすのに効果的な、請求項1または38のいずれかに記載の前記冷凍保存された胎盤組成物の量を投与することを含む、前記部位でのプロテアーゼ活性の低減方法。
- 前記部位が、創傷または組織欠損である、請求項75に記載の方法。
- 前記量が、少なくとも1つのマトリックスメタロプロテアーゼの活性または放出を阻害若しくは減らす、請求項75に記載の方法。
- 皮膚潰瘍の治療法であって、請求項1から48のいずれか1項に記載の前記組成物を、その皮膚潰瘍の治療に効果的な量で投与することを含む、前記皮膚潰瘍の治療法。
- 組成物であって、a)請求項1から44のいずれか1項に記載の、解凍された冷凍保存胎盤組織組成物、及びb)キャリアを含む、前記組成物。
- 前記キャリアが、生体適合性足場である、請求項79に記載の組成物。
- 前記生体適合性足場が、海綿、コラーゲン、自家移植、同種移植、異種移植、セラミック、サンゴ、複合材料、または脱灰骨基質である、請求項80に記載の組成物。
- 前記組成物が、外科手術に使用される、請求項79に記載の組成物。
- 創傷治療のキットであって、
a.薬学的に許容される容器に収められた、請求項1から48のいずれか1項における胎盤組織組成物、及び
b.前記創傷治療のための、前記胎盤組織組成物の投与説明書、
を含む、前記キット。 - 前記胎盤組織組成物がさらに添加物を含む、請求項83に記載のキット。
- 前記添加物が、抗生物質、皮膚軟化剤、角質溶解剤、保湿剤、抗酸化物質、防腐剤、治療薬、救急絆創膏、注射器、カテーテル、医療用具、ハサミ、メス、洗面器、接着剤、及びそれらの組み合わせから選ばれる、請求項84に記載のキット。
- 前記薬学的に許容される容器が、バイアル瓶、パウチ袋、瓶、袋、試験管及びシリンジである、請求項84に記載のキット。
- 胎盤組織組成物の調合プロセスであって、
a.胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤組織を提供すること、
b.前記胎盤組織の少なくとも一部分を破壊して、胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤懸濁液を形成すること、
c.前記胎盤懸濁液を冷凍保存して、冷凍保存された胎盤組織組成物を形成すること、
のステップを含み、ここで、前記冷凍保存された胎盤組織組成物の冷凍及びそれに続く解凍後に、その胎盤細胞の約40%を上回る細胞が生存しており、ここで、前記組成物は、機能的免疫原性細胞が枯渇している、前記プロセス。 - 前記破壊ステップに先立ち、さらに
a1.前記胎盤組織を少なくとも1つの酵素で消化して、胎盤細胞及び胎盤組織断片の懸濁液を形成すること、及び
a2.前記胎盤細胞及び胎盤組織断片を分離すること、
のステップをさらに含み、ここでステップ(b)において、その破壊ステップが、ステップ(a2)において分離された前記胎盤組織断片を破壊することを含み、次に、ステップ(b)の後のステップ(c)において、ステップ(a2)で分離された前記胎盤細胞と破壊された組織断片を組み合わせて、前記胎盤分散液を形成して成る、請求項87に記載のプロセス。 - 胎盤組織組成物の調合プロセスであって、
a.胎盤細胞、治療因子、及び細胞外基質成分を含む胎盤組織を提供すること、
b.前記胎盤組織を少なくとも1つの酵素で消化して、胎盤細胞及び細胎盤組織断片の懸濁液を形成すること、
c.前記胎盤細胞及び前記胎盤組織断片を分離すること、
d.前記胎盤組織断片を破壊して、胎盤分散液を形成すること、
e.前記胎盤細胞と前記胎盤分散液を組み合わせて、胎盤組織組成物を形成すること、及び
f.その胎盤組織組成物を冷凍保存すること、
のステップを含み、ここで前記冷凍保存された胎盤組織組成物のそれに続く解凍後に、その胎盤細胞の40%を上回る細胞が生存しており、ここで、前記組成物が、機能的免疫原性細胞を枯渇している、前記プロセス。 - 前記冷凍保存のステップが、冷凍保存剤の添加を含む、請求項87から89のいずれか1項に記載のプロセス。
- 前記冷凍保存剤が、当該最終組成物の容積に対して、約3%から約100%の量である、請求項90に記載のプロセス。
- 前記冷凍保存剤が、当該最終組成物の容積に対して、約3%から約50%の量である、請求項90に記載のプロセス。
- 前記冷凍保存剤が、当該最終組成物の容積に対して、約5%から約10%の量である、請求項90に記載のプロセス。
- 前記組成物が、a.冷凍保存剤の容積で約5%から約20%、b.血清アルブミンの容積で約5%から約15%、及びc.任意で、薬学的に許容されるキャリアを含む、請求項90に記載のプロセス。
- 前記冷凍保存のステップが、a.前記胎盤組成物に、冷凍保存剤を添加し、b.前記胎盤組成物を、約2℃から約8℃の温度で、約2分から約240分間静置し、及びc.前記胎盤組成物を、約−20℃から約−196℃の温度で冷凍することを含む、請求項87から94のいずれか1項に記載のプロセス。
- ステップが、前記胎盤組成物に血清アルブミンを添加することをさらに含む、請求項90に記載のプロセス。
- 前記機能性免疫原性細胞が、母体血液細胞、新生児血液細胞、マクロファージ、栄養膜から選択される、請求項87から96のいずれか1項に記載のプロセス。
- 前記免疫原性細胞の枯渇量が、免疫応答を産生するのに十分な量を下回って、少なくとも1つの免疫原性因子を産生する、請求項87から96のいずれか1項に記載のプロセス。
- 前記少なくとも1つの免疫原性因子が、検出限界を下回った量で産生される、請求項98に記載のプロセス。
- 前記少なくとも1つの免疫原性因子が、350pg/cm2以下の量のTNF−αである、請求項98に記載のプロセス。
- 前記胎盤組織が、ミンチ化により破壊される、請求項87に記載のプロセス。
- ミンチ化が、ハーブミンチ器またはメッザルーナによる、請求項100に記載のプロセス。
- 前記胎盤組織が、均質化により破壊される、請求項87に記載のプロセス。
- 前記胎盤組織が、栄養膜が枯渇した絨毛膜である、請求項87に記載のプロセス。
- 前記胎盤組織が、シリンジを通り抜けるのに十分に小さい組織断片部にミンチ化される、請求項101に記載のプロセス。
- 前記組成物中の生存細胞量が、少なくとも1,000/mLである、請求項87から105のいずれか1項に記載のプロセス。
- 前記組成物中の生存細胞量が、少なくとも10,000/mLである、請求項87から106のいずれか1項に記載のプロセス。
- 前記胎盤組織組成物の冷凍保存及びそれに続く解凍後に、その胎盤細胞の50%を上回る細胞が生存している、請求項87から107のいずれか1項に記載のプロセス。
- 前記胎盤組織組成物の冷凍保存及びそれに続く解凍後に、その胎盤細胞の70%を上回る細胞が生存している、請求項87から107のいずれか1項に記載のプロセス。
- 先行請求項87から109のいずれか1項に記載の前記プロセスによりつくられる産物。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/US2014/037201 WO2015171142A1 (en) | 2014-05-07 | 2014-05-07 | Therapeutic placental compositions, methods of making and methods of use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017514876A true JP2017514876A (ja) | 2017-06-08 |
Family
ID=54392804
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016566997A Pending JP2017514876A (ja) | 2014-05-07 | 2014-05-07 | 治療用胎盤組成物、その製造法及び使用法 |
Country Status (7)
| Country | Link |
|---|---|
| EP (1) | EP3139935A4 (ja) |
| JP (1) | JP2017514876A (ja) |
| KR (1) | KR20160147058A (ja) |
| AU (1) | AU2014393402A1 (ja) |
| CA (1) | CA2948126A1 (ja) |
| SG (1) | SG11201609254YA (ja) |
| WO (1) | WO2015171142A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11510947B2 (en) | 2010-02-18 | 2022-11-29 | Osiris Therapeutics, Inc. | Methods of manufacture of immunocompatible amniotic membrane products |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7011135B2 (ja) * | 2016-02-19 | 2022-02-10 | 佳秀工業株式会社 | 血管内皮増殖因子産生促進剤の製造方法及び発毛剤の製造方法、並びに血管内皮増殖因子産生促進剤及び発毛剤 |
| EP4008400A1 (en) * | 2016-03-14 | 2022-06-08 | Plakous Therapeutics, Inc. | Acellular placental preparations |
| US10960027B2 (en) | 2016-03-23 | 2021-03-30 | Mimedx Group, Inc. | Compositions and methods of treatment with amniotic fluid |
| US10271942B2 (en) | 2016-08-24 | 2019-04-30 | Arthrex, Inc. | Tissue use for repair of injury |
| WO2018144694A1 (en) | 2017-02-01 | 2018-08-09 | Plakous Therapeutics, Inc. | Placental tissue compositions |
| US11511017B2 (en) | 2019-03-12 | 2022-11-29 | Arthrex, Inc. | Ligament reconstruction |
| WO2021003257A1 (en) * | 2019-07-01 | 2021-01-07 | Auxocell Laboratories, Inc. | Methods and compositions for collecting and using placental tissue cells and placental blood cells |
| AU2020386363A1 (en) * | 2019-11-21 | 2022-05-19 | Bioventus, Llc . | Placental tissue particulate compositions and methods of use |
| WO2021123320A1 (en) * | 2019-12-20 | 2021-06-24 | Dr. Kalali Prof. Mostafazadeh Dipl. Ing. Miedl (Kmm) Gesellschaft Bürgerlichen Rechts | A composition and its use for a universal therapy against tumor cells |
| KR102116954B1 (ko) * | 2019-12-26 | 2020-05-29 | 주식회사 엠케이바이오텍 | 태아 유래 줄기세포의 동결 보존 및 동결 건조용 배지 조성물 |
| WO2022074523A1 (en) * | 2020-10-06 | 2022-04-14 | Osiris Therapeutics, Inc. | Primed placental tissue and uses in regenerative medicine |
| WO2022183100A1 (en) * | 2021-02-26 | 2022-09-01 | Crown Scientific, L.L.C. | Villi stromal cells compositions and uses thereof |
| WO2023192484A2 (en) * | 2022-04-01 | 2023-10-05 | Bright Cell, Inc. | A mesenchymal stem cells formulation for cosmetic use |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007528703A (ja) * | 2003-06-27 | 2007-10-18 | エチコン、インコーポレイテッド | 分娩後由来細胞を使用する眼組織の修復および再生 |
| US20110206776A1 (en) * | 2010-02-18 | 2011-08-25 | Samson Tom | Methods of manufacture of immunocompatible amniotic membrane products |
| US20140106447A1 (en) * | 2012-10-12 | 2014-04-17 | Mimedx Group, Inc. | Compositions and methods for recruiting stem cells |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5101778B2 (ja) * | 2000-02-11 | 2012-12-19 | ザ ジェネラル ホスピタル コーポレイション | 光化学作用による組織接着 |
| US20030187515A1 (en) * | 2002-03-26 | 2003-10-02 | Hariri Robert J. | Collagen biofabric and methods of preparing and using the collagen biofabric |
| EP2271209B1 (en) * | 2008-03-27 | 2016-07-13 | Biolife Solutions, Inc. | Materials and methods for hypothermic collection of whole blood |
| US8632512B2 (en) * | 2010-04-09 | 2014-01-21 | Kci Licensing, Inc. | Apparatuses, methods, and compositions for the treatment and prophylaxis of chronic wounds |
-
2014
- 2014-05-07 KR KR1020167034174A patent/KR20160147058A/ko not_active Application Discontinuation
- 2014-05-07 WO PCT/US2014/037201 patent/WO2015171142A1/en active Application Filing
- 2014-05-07 CA CA2948126A patent/CA2948126A1/en not_active Abandoned
- 2014-05-07 AU AU2014393402A patent/AU2014393402A1/en not_active Abandoned
- 2014-05-07 EP EP14891336.1A patent/EP3139935A4/en not_active Withdrawn
- 2014-05-07 JP JP2016566997A patent/JP2017514876A/ja active Pending
- 2014-05-07 SG SG11201609254YA patent/SG11201609254YA/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007528703A (ja) * | 2003-06-27 | 2007-10-18 | エチコン、インコーポレイテッド | 分娩後由来細胞を使用する眼組織の修復および再生 |
| US20110206776A1 (en) * | 2010-02-18 | 2011-08-25 | Samson Tom | Methods of manufacture of immunocompatible amniotic membrane products |
| US20140037598A1 (en) * | 2010-02-18 | 2014-02-06 | Osiris Therapeutics, Inc. | Therapeutic products comprising vitalized placental dispersions |
| US20140106447A1 (en) * | 2012-10-12 | 2014-04-17 | Mimedx Group, Inc. | Compositions and methods for recruiting stem cells |
Non-Patent Citations (1)
| Title |
|---|
| MELLER, D. ET AL., DTSCH ARTEBL INT, vol. 108, no. 14, JPN6018042804, 2011, pages 243 - 8, ISSN: 0004045474 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11510947B2 (en) | 2010-02-18 | 2022-11-29 | Osiris Therapeutics, Inc. | Methods of manufacture of immunocompatible amniotic membrane products |
| US11590172B2 (en) | 2010-02-18 | 2023-02-28 | Osiris Therapeutics, Inc. | Immunocompatible chorionic membrane products |
| US11590173B2 (en) | 2010-02-18 | 2023-02-28 | Osiris Therapeutics, Inc. | Methods of manufacture of therapeutic products comprising vitalized placental dispersions |
| US11638725B2 (en) | 2010-02-18 | 2023-05-02 | Osiris Therapeutics, Inc. | Methods of manufacture of immunocompatible chorionic membrane products |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2014393402A1 (en) | 2016-11-24 |
| WO2015171142A1 (en) | 2015-11-12 |
| EP3139935A1 (en) | 2017-03-15 |
| KR20160147058A (ko) | 2016-12-21 |
| CA2948126A1 (en) | 2015-11-12 |
| EP3139935A4 (en) | 2017-11-15 |
| SG11201609254YA (en) | 2016-12-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11510947B2 (en) | Methods of manufacture of immunocompatible amniotic membrane products | |
| JP2017514876A (ja) | 治療用胎盤組成物、その製造法及び使用法 | |
| US20150010506A1 (en) | Therapeutic placental compositions, methods of making and methods of use | |
| US20150010610A1 (en) | Immunocompatible amniotic membrane products | |
| US20150010609A1 (en) | Immunocompatible chorionic membrane products | |
| KR20160149292A (ko) | 면역적합성 융모막 생성물 | |
| KR20170002572A (ko) | 면역적합성 양막 생성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170508 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180227 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180528 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20181106 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20190604 |