JP2017161447A - 分析方法 - Google Patents
分析方法 Download PDFInfo
- Publication number
- JP2017161447A JP2017161447A JP2016048290A JP2016048290A JP2017161447A JP 2017161447 A JP2017161447 A JP 2017161447A JP 2016048290 A JP2016048290 A JP 2016048290A JP 2016048290 A JP2016048290 A JP 2016048290A JP 2017161447 A JP2017161447 A JP 2017161447A
- Authority
- JP
- Japan
- Prior art keywords
- protein
- ions
- analysis method
- ion
- mass spectrometer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Other Investigation Or Analysis Of Materials By Electrical Means (AREA)
Abstract
Description
まず、分析対象となる試料が準備される。分析対象となる試料はタンパク質を含むものであれば特に限定されない。分析対象試料としては、血液、血清、血漿、組織抽出液、細胞抽出液、尿、脳脊髄液等の生体試料が挙げられる。生体試料中には、様々なタンパク質が含まれている。また、タンパク質以外にも多種多様な夾雑物が含まれている。
LCシステム:高速液体クロマトグラフ Nexera X2
分析カラム: Shim-pack ODS-III
流速: 0.4ml/分
移動相: A液 0.1%ギ酸水溶液、B液 0.1%ギ酸アセトニトリル溶液
グラジエントプログラム:以下の表1に示す通り
<MS条件>
イオン化モード: ESI(+)
<試料のSPE処理>
96ウェルの陰イオン交換SPEプレートにメタノール(500μl)を加えて遠心し、次いで超純水(500μl)を加えて遠心した。所定量のヒトインスリンの標品を添加して遠心した後、5%アンモニア水(500μl)を加えて遠心し、次いで10%アセトニトリル(500μl)を加えて遠心し、溶出液を回収した。SPE処理後の試料に40%酢酸(200μl)を添加して、分析用試料とした。
(プリカーサスキャン)
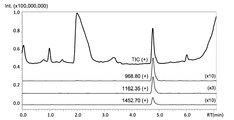
ヒトインスリン標品のプリカーサスキャンのMSクロマトグラムを図2、マススペクトルを図3に示す。図2および図3に示すように、LC溶出時間4.8分に、m/z 969、1162、1452のピークが確認された。これらのピークは、それぞれインスリンの6価、5価、4価のイオンと同定された。
インスリンの4価イオン、5価イオンおよび6価イオンをプリカーサイオンとして選択し、プロダクトスイオンスキャンを行い、表2に示すプリカーサイオンとプロダクトイオンのm/zの組合せ、および各プロダクトイオンの最適コリジョンエネルギー(CE)を得た。
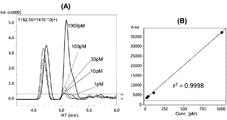
SPEプレートにロードするインスリンの量を変化させて、MRM分析を行った。結果を図4に示す。図4(A)は、MRMクロマトグラムであり、インスリンのロード量が2fmolの試料でも、プロダクトイオンが検出されていることが分かる。インスリンのロード量を横軸、プロダクトイオン量(ピーク面積)の対数を縦軸としてプロットしたところ、インスリンの両とピーク面積の対数との間に線形関係がみられ、図4(B)に示す検量線が得られた。
<試料の前処理>
血漿(500μl)を、容量2mlのチューブに採取し、50%酢酸を(5μl)を添加し、次いで5%アンモニア水(500μl)を添加した。この試料に、所定濃度(1pM、10pM、30pM、100pM)となるようにインスリン標品を添加した後、SPEプレートにロードし、実施例1と同様にして分析用試料を調製した。
上記実施例1と同様の条件でMRM分析を実施した結果を図5に示す。図5(A)はMRMクロマトグラムであり、インスリンのスパイク濃度が1pMの試料でも、プロダクトイオンが検出されていることが分かる。インスリンのロード量を横軸、プロダクトイオン量(ピーク面積)の対数を縦軸としてプロットしたところ、インスリンの両とピーク面積の対数との間に線形関係がみられ、図5(B)に示す検量線が得られた。
2人の健常人から採取した血漿を試料として、実施例2と同様に前処理を行った後、インスリンをスパイクせずにMRM分析を実施した。結果を図6(A)および図(B)に示す。
Claims (9)
- 質量分析計を用いたタンパク質の分析方法であって、
質量分析計は、試料をイオン化するイオン化部;特定のm/zを有するイオンをプリカーサイオンとして選別する第一質量分離部;第一質量分離部で選別されたプリカーサイオンから複数種のプロダクトイオンを生成する開裂部;前記プロダクトイオンをm/zに基づいて選別する第二質量分離部;および前記第二質量分離部で選別された特定のm/zを有するプロダクトイオンを検出する検出部を備え、
分析対象のタンパク質をインタクトなタンパク質として含む試料が質量分析計のイオン化部に導入され
前記第一質量分離部において、前記タンパク質の多価イオンが前記プリカーサイオンとして選別される、分析方法。 - 前記イオン化部において、エレクトロスプレーイオン化法により前記タンパク質のイオン化が行われる、請求項1に記載の分析方法。
- 前記質量分析計がトリプル四重極質量分析計である、請求項1または2のいずれか1項に記載の分析方法。
- 前記プリカーサイオンのm/zが500〜2000である、請求項1〜3のいずれか1項に記載の分析方法。
- 前記プロダクトイオンのm/zが500以上である、請求項1〜4のいずれか1項に記載の分析方法。
- 分析対象のタンパク質がジスルフィド結合を有する、請求項1〜5のいずれか1項に記載の分析方法。
- 分析対象のタンパク質の分子量が、2000〜10000Daである、請求項1〜6のいずれか1項に記載の分析方法。
- 分析対象のタンパク質がインスリンである、請求項1〜7のいずれか1項に記載の分析方法。
- 前記プリカーサイオンが4価〜6価のイオンである、請求項8に記載の分析方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016048290A JP2017161447A (ja) | 2016-03-11 | 2016-03-11 | 分析方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016048290A JP2017161447A (ja) | 2016-03-11 | 2016-03-11 | 分析方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017161447A true JP2017161447A (ja) | 2017-09-14 |
Family
ID=59856868
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016048290A Pending JP2017161447A (ja) | 2016-03-11 | 2016-03-11 | 分析方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2017161447A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20210302286A1 (en) * | 2018-09-18 | 2021-09-30 | Shimadzu Corporation | Method for pretreatment of biological sample |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004002950A1 (ja) * | 2002-06-28 | 2004-01-08 | Shimadzu Corporation | スルフェニル化合物、ラベル化試薬、及びペプチドの解析方法 |
| JP2005208037A (ja) * | 2003-12-22 | 2005-08-04 | Canon Inc | 検定試料およびその製造方法 |
| JP2014505869A (ja) * | 2010-12-28 | 2014-03-06 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によるインスリンの定量 |
-
2016
- 2016-03-11 JP JP2016048290A patent/JP2017161447A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004002950A1 (ja) * | 2002-06-28 | 2004-01-08 | Shimadzu Corporation | スルフェニル化合物、ラベル化試薬、及びペプチドの解析方法 |
| JP2005208037A (ja) * | 2003-12-22 | 2005-08-04 | Canon Inc | 検定試料およびその製造方法 |
| JP2014505869A (ja) * | 2010-12-28 | 2014-03-06 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によるインスリンの定量 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20210302286A1 (en) * | 2018-09-18 | 2021-09-30 | Shimadzu Corporation | Method for pretreatment of biological sample |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7498568B2 (en) | Real-time analysis of mass spectrometry data for identifying peptidic data of interest | |
| US8809062B2 (en) | Method and apparatus for fractionation-based chemical analyses | |
| US8165820B2 (en) | Methods and apparatus for performing retention-time matching | |
| US9018580B2 (en) | Method for detecting molecules through mass spectrometry | |
| US8592752B2 (en) | Techniques for performing retention-time matching of precursor and product ions and for constructing precursor and product ion spectra | |
| Niessen et al. | Introduction to mass spectrometry, a tutorial | |
| JP4959712B2 (ja) | 質量分析計 | |
| US20070231909A1 (en) | Methods for the development of a biomolecule assay | |
| JP5003274B2 (ja) | 質量分析システムおよび質量分析方法 | |
| JP5065543B1 (ja) | 翻訳後修飾ペプチドの検出および配列決定方法 | |
| JP2018535398A (ja) | マススペクトロメトリーによるアミロイドベータの検出 | |
| JP4959713B2 (ja) | 質量分析計 | |
| AU2018275881B2 (en) | Methods for absolute quantification of low-abundance polypeptides using mass spectrometry | |
| CN109459484A (zh) | 一种基于纳米材料的小分子样品的质谱分析方法 | |
| US9460903B2 (en) | Glycopeptide analyzer | |
| JP2017161447A (ja) | 分析方法 | |
| Nicolardi et al. | Identification of human serum peptides in fourier transform ion cyclotron resonance precision profiles | |
| Su et al. | Mass spectrometry instrumentation | |
| Nuccio | The effect of search accuracy on shotgun protemoics results using a validated protein database and high resolution fragment spectra |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180725 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20181225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190416 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20190417 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20191008 |