JP2017104097A - 上皮細胞の不死化および使用法 - Google Patents
上皮細胞の不死化および使用法 Download PDFInfo
- Publication number
- JP2017104097A JP2017104097A JP2016226280A JP2016226280A JP2017104097A JP 2017104097 A JP2017104097 A JP 2017104097A JP 2016226280 A JP2016226280 A JP 2016226280A JP 2016226280 A JP2016226280 A JP 2016226280A JP 2017104097 A JP2017104097 A JP 2017104097A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- nke
- cell
- epithelial cells
- epithelial
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0681—Cells of the genital tract; Non-germinal cells from gonads
- C12N5/0683—Cells of the male genital tract, e.g. prostate, epididymis; Non-germinal cells from testis, e.g. Leydig cells, Sertoli cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0625—Epidermal cells, skin cells; Cells of the oral mucosa
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0625—Epidermal cells, skin cells; Cells of the oral mucosa
- C12N5/0631—Mammary cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/067—Hepatocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0688—Cells from the lungs or the respiratory tract
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5091—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing the pathological state of an organism
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/05—Inorganic components
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/40—Nucleotides, nucleosides, bases
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/01—Modulators of cAMP or cGMP, e.g. non-hydrolysable analogs, phosphodiesterase inhibitors, cholera toxin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/11—Epidermal growth factor [EGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/30—Hormones
- C12N2501/33—Insulin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/30—Hormones
- C12N2501/38—Hormones with nuclear receptors
- C12N2501/39—Steroid hormones
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/70—Enzymes
- C12N2501/72—Transferases (EC 2.)
- C12N2501/727—Kinases (EC 2.7.)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/13—Coculture with; Conditioned medium produced by connective tissue cells; generic mesenchyme cells, e.g. so-called "embryonic fibroblasts"
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/13—Coculture with; Conditioned medium produced by connective tissue cells; generic mesenchyme cells, e.g. so-called "embryonic fibroblasts"
- C12N2502/1323—Adult fibroblasts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2503/00—Use of cells in diagnostics
- C12N2503/02—Drug screening
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
- C12N2510/04—Immortalised cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/106—Pharmacogenomics, i.e. genetic variability in individual responses to drugs and drug metabolism
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Cell Biology (AREA)
- Dermatology (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Reproductive Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pulmonology (AREA)
- Physics & Mathematics (AREA)
- Hematology (AREA)
- Pathology (AREA)
- Urology & Nephrology (AREA)
- Gastroenterology & Hepatology (AREA)
- Physiology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Biophysics (AREA)
- Food Science & Technology (AREA)
Abstract
【課題】非ケラチノサイト上皮細胞を培養する方法、及び不死化された非ケラチノサイト上皮細胞を使用する方法の提供。【解決手段】非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、を含む非ケラチノサイト上皮細胞を連続的に培養する方法。【選択図】なし
Description
関連出願の相互参照
本出願は、2010年11月12日出願の米国仮出願第61/413,291号、および2011年4月13日出願の同第61/474,901号に対する優先権を主張するものであり、これら両方は、参照により組み込まれる。
本出願は、2010年11月12日出願の米国仮出願第61/413,291号、および2011年4月13日出願の同第61/474,901号に対する優先権を主張するものであり、これら両方は、参照により組み込まれる。
連邦支援の研究または開発に関する声明
本発明の開発中に行われた作業の一部は、米国国立衛生研究所(National Institutes of Health)の助成金交付番号R01CA106400およびR01−CA053371のもとで米国政府の資金を利用した。米国政府は、本発明においてある特定の権利を有する。
本発明の開発中に行われた作業の一部は、米国国立衛生研究所(National Institutes of Health)の助成金交付番号R01CA106400およびR01−CA053371のもとで米国政府の資金を利用した。米国政府は、本発明においてある特定の権利を有する。
発明の背景
本発明は、非ケラチノサイト上皮細胞を培養する方法を対象とし、方法は、培養中に、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。本発明は、これらの不死化された非ケラチノサイト上皮細胞を使用する方法も対象とする。
本発明は、非ケラチノサイト上皮細胞を培養する方法を対象とし、方法は、培養中に、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。本発明は、これらの不死化された非ケラチノサイト上皮細胞を使用する方法も対象とする。
肺、腎臓、肝臓、膵臓、および皮膚等の生命維持に必要な器官は、とりわけ、器官特異的な分化上皮細胞の存在を特徴とする。分化上皮細胞は、言うまでもなく、それぞれのそのような器官の特定の機能に関連している。特定の機能は、例えば、肺でのガス交換、腎臓での濾過、肝臓での解毒および抱合、膵島細胞でのインスリン産生、または皮膚による危険な環境に対する保護と様々であり得る。そのような器官の疾患もしくは変性は、変性したか、または失われた器官構造が、多くの場合、十分に置換されず、かつ1つの器官の特殊化した細胞が、別の器官の機能を引き継ぐことができないため、多くの場合、生命にかかわる。
腎臓上皮細胞、膵臓のランゲルハンス島中のインスリン産生細胞、ならびに真皮の腺細胞および/または毛包細胞等の分化細胞は、可能であったとしても、回復困難であり、体内環境から取り出されると、維持するのがより困難である。実際、分化上皮細胞は、培養下で極めて限られた寿命を有する。一般的に言えば、動物から採取されるケラチノサイト以外の上皮細胞を、恐らく、1継代または2継代のみ培養下で増殖させることができる。
生体外の非ケラチノサイト上皮(NKE)細胞を研究するために、ウイルス性または細胞性癌遺伝子の挿入等の一種の遺伝子操作は、細胞が数継代以上生存することを可能にするために必要とされている。しかしながら、これらの遺伝子操作は、細胞が正常な上皮細胞に類似しないか、または正常な上皮細胞のように機能しなくてもよいように、細胞の遺伝的背景、ならびに生理機能を変化させる。さらに、これらの遺伝子改変された細胞は、無傷の動物への移植の候補ではない。
細胞を遺伝子改変することなく、器官から採取されるNKE細胞を長期間培養する方法が、当技術分野で必要とされている。本発明は、遺伝子操作を必要とすることなく、NKE細胞を長期間培養することに関連する問題を解決する。
本発明は、非ケラチノサイト上皮細胞を培養する方法を対象とし、方法は、培養中に、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。
本発明は、条件的に不死化された非ケラチノサイト上皮細胞を産生する方法も対象とし、方法は、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるROCKの活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。非ケラチノサイト上皮細胞をそのような条件下で培養して、条件的に不死化された非ケラチノサイト上皮細胞を産生する。
本発明は、少なくとも部分的に分化した非ケラチノサイト上皮細胞を産生する方法も対象とし、方法は、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるROCKの活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下である一定期間培養して、条件的に不死化された非ケラチノサイト上皮細胞を産生することを含む。条件的に不死化された非ケラチノサイト上皮細胞をこれらの条件下で培養した後、条件的に不死化された非ケラチノサイト上皮細胞は、条件的に不死化された非ケラチノサイト上皮細胞の分化を促進する条件下に設置される。
本発明は、非ケラチノサイト上皮細胞の増殖を刺激する方法も対象とし、方法は、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるROCKの活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。そのような条件下での非ケラチノサイト上皮細胞の培養が、非ケラチノサイト上皮細胞を刺激して増殖させるが、他の方法では、細胞は増殖することができない。
本発明は、非ケラチノサイト上皮細胞を培養する方法を対象とし、方法は、培養中に、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。
本明細書で使用される「上皮」または「上皮細胞」という用語は、管腔器官を一列に並べる細胞(単数もしくは複数)、ならびに体の腺および外表面を構成する細胞(単数または複数)を指す。概して、4種類の上皮細胞、すなわち、扁平上皮細胞、円柱上皮細胞、腺腫上皮細胞、および移行上皮細胞が存在すると考えられ得る。器官および位置に応じて、上皮細胞を単層または多層に設置することができる。ケラチノサイトは、皮膚、食道、および頸部等の解剖学的部位に見られる扁平上皮を構成する細胞である。ケラチノサイトは、防護壁を形成することによって環境および感染からの保護を助ける平坦な高度に角化した非生存細胞に最終分化する。本発明は、任意の種類の非ケラチノサイト上皮細胞(「NKE細胞」)を対象とする。NKE細胞は、乳房、前立腺、肝臓、および消化管等に見られる体の腺上皮を形成する。NKE細胞は、吸収および/または分泌のいずれかにおいて機能することができる機能的な生存細胞に分化し、これらの細胞は、扁平上皮細胞の特徴を示す高度に角化した構造を形成しない。「非ケラチノサイト上皮細胞」という語句は、当技術分野において十分に理解されており、当業者であれば、その用語の共通の一般的な意味を容易に理解するであろう。本発明の方法において使用されるNKE細胞は、任意の種類または起源組織であってもよい。
本明細書で使用される用語によって包含されるNKE細胞の例には、前立腺細胞、乳房細胞、肝細胞、β細胞を含む膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸および小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、子宮頸部上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、下垂体細胞が挙げられるが、これらに限定されない。
細胞は、マウス、ラット、イヌ、ネコ、ウシ、ウマ、ブタ、非ヒトおよびヒト霊長類等の
任意の哺乳動物を含むが、これらに限定されない任意の動物由来であってもよい。本培地での培養に特に好適な哺乳類細胞には、乳房、前立腺、肝臓、膵臓、腎臓、気管支、および気管等であるが、これらに限定されない組織に由来する初代細胞であり得るヒト起源の上皮細胞が含まれる。加えて、形質転換細胞または樹立細胞株、例えば、HeLa子宮頸部上皮細胞株を使用することができる。本発明で使用される細胞は、罹患していないか、または遺伝子改変されていない正常な健常細胞であってもよく、あるいは細胞は、罹患しているか、または遺伝子改変されていてもよい。したがって、「罹患した上皮細胞」は、本明細書において、NKE細胞の一部である。「罹患した細胞」とは、細胞が、動物の血液循環、すなわち、循環腫瘍細胞(CTC)から単離された罹患した細胞を含むが、これらに限定されない、新生物形成、過形成、または悪性腫瘍もしくは良性腫瘍等に由来する異常な組織に由来することを意味する。CHO細胞、COS細胞、VERO細胞、BHK細胞(BHK−21細胞を含む)およびそれらの誘導体またはサブクローン等であるが、これらに限定されない他の哺乳類細胞も、本発明の方法に好適である。一実施形態において、細胞は、正常な組織または異常な組織の試料由来の初代または二次ヒトNKE細胞である。別の実施形態では、細胞は、樹立細胞株、形質転換細胞、以前に凍結させた回収物由来の解凍細胞等由来の細胞等の初代細胞ではない。本発明による培養用の動物細胞を、例えば、ATCC(Rockville,Md.)、Cell Systems,Inc.(Kirkland,Wash.)、Clonetics Corporation(San Diego,Calif.)、BioWhittaker(Walkersville,Md.)、またはCascade Biologicals(Portland,Oreg.)から商業的に入手することができる。
任意の哺乳動物を含むが、これらに限定されない任意の動物由来であってもよい。本培地での培養に特に好適な哺乳類細胞には、乳房、前立腺、肝臓、膵臓、腎臓、気管支、および気管等であるが、これらに限定されない組織に由来する初代細胞であり得るヒト起源の上皮細胞が含まれる。加えて、形質転換細胞または樹立細胞株、例えば、HeLa子宮頸部上皮細胞株を使用することができる。本発明で使用される細胞は、罹患していないか、または遺伝子改変されていない正常な健常細胞であってもよく、あるいは細胞は、罹患しているか、または遺伝子改変されていてもよい。したがって、「罹患した上皮細胞」は、本明細書において、NKE細胞の一部である。「罹患した細胞」とは、細胞が、動物の血液循環、すなわち、循環腫瘍細胞(CTC)から単離された罹患した細胞を含むが、これらに限定されない、新生物形成、過形成、または悪性腫瘍もしくは良性腫瘍等に由来する異常な組織に由来することを意味する。CHO細胞、COS細胞、VERO細胞、BHK細胞(BHK−21細胞を含む)およびそれらの誘導体またはサブクローン等であるが、これらに限定されない他の哺乳類細胞も、本発明の方法に好適である。一実施形態において、細胞は、正常な組織または異常な組織の試料由来の初代または二次ヒトNKE細胞である。別の実施形態では、細胞は、樹立細胞株、形質転換細胞、以前に凍結させた回収物由来の解凍細胞等由来の細胞等の初代細胞ではない。本発明による培養用の動物細胞を、例えば、ATCC(Rockville,Md.)、Cell Systems,Inc.(Kirkland,Wash.)、Clonetics Corporation(San Diego,Calif.)、BioWhittaker(Walkersville,Md.)、またはCascade Biologicals(Portland,Oreg.)から商業的に入手することができる。
本明細書で使用されるとき、初代細胞は、生検等の生体組織から直接採取されたか、または血液循環から単離され、継代されていないか、または1代のみ継代された細胞である。したがって、初代細胞は、多くの場合、組織消化を介して新たに単離され、プレーティングされたものである。細胞が1代以下継代された場合、初代細胞は、凍結されてもされなくてもよく、その後、しばらく経ってから解凍されてもよい。加えて、初代細胞が単離される組織は、処理の直前に他のある様式で凍結または保存されてもされなくてもよい。
本発明で使用するNKE細胞は、未分化な胚幹細胞ではない。したがって、本明細書で使用される非ケラチノサイト上皮細胞という語句は、未分化胚幹細胞を自動的に排除する。本明細書および当技術分野で使用されるとき、胚幹細胞は、永久に再生または自己再生する能力を有する未分化細胞である。本明細書の方法で使用されるNKE細胞は、成人幹細胞であってもなくてもよい。本明細書で使用されるとき、成人幹細胞は、動物組織から単離され、完全に分化した細胞よりも分化の程度が低いが、胚幹細胞よりも分化の程度は高い。一実施形態において、本発明の方法に従って培養されるNKE細胞は、成人幹細胞である。本発明の別の実施形態では、本発明の方法に従って培養されるNKE細胞は、成人幹細胞ではない。本発明で使用されるNKE細胞は、通常、永久に自己再生する能力を有しない。さらに、NKE細胞は、NKE細胞が未分化幹細胞に典型的に関連しない細胞表面マーカーを有するか、または逆に、NKE細胞が未分化幹細胞に典型的に関連した細胞表面マーカーを有しないという点で、最初の単離およびプレーティング時は完全に未分化した細胞ではない。
初代細胞を単離するとき、組織は、理想的には、標準の滅菌技術および層流安全キャビネットを用いて取り扱われるべきである。一実施形態において、単一針生検は、本発明の細胞培養方法を開始するのに十分な数の初代細胞を単離するのに十分である。組織生検の場合、組織を、滅菌器具を用いて小片に切断することができる。別の実施形態では、対象の血液循環から単離された単一細胞は、本発明の細胞培養方法を開始するのに十分な材料である。その後、小片を、滅菌食塩水、または抗生物質もしくは他の成分が補充されてもされなくてもよいPBS等の他の緩衝液で数回洗浄することができる。洗浄後、小片は、組
織基質からの細胞の解離を促進するために、多くの場合、コラゲナーゼ、ディスパーゼ、またはトリプシン等であるが、これらに限定されない酵素液で処理されるが、必須ではない。
織基質からの細胞の解離を促進するために、多くの場合、コラゲナーゼ、ディスパーゼ、またはトリプシン等であるが、これらに限定されない酵素液で処理されるが、必須ではない。
ディスパーゼは、多くの場合、上皮を下層組織から解離するために使用される。その後、この無傷の上皮を、トリプシンまたはコラゲナーゼで処理してもよい。これらの消化ステップは、多くの場合、解離細胞および組織基質を含有するスラリーをもたらす。その後、スラリーの残りから細胞を分離するのに十分な力でスラリーを遠心分離してもよい。その後、細胞ペレットを除去し、緩衝液および/または生理食塩水および/または細胞培養培地で洗浄してもよい。遠心分離および洗浄を、何度でも繰り返してもよい。最終洗浄後、細胞を、任意の好適な細胞培養培地で洗浄してもよい。言うまでもなく、単離時に細胞が下層組織から十分に分離されない場合、例えば、針生検の場合、または血液循環から単離される場合、消化および洗浄ステップを行う必要はない。例えば、腫瘍細胞等の細胞を、特定の種類の腫瘍細胞に特異的な細胞マーカーを発現する細胞を単離する現在利用可能な技術を用いて、生物の血液循環から単離してもよい。参照により組み込まれる、Lu.J.,et al.,Int’l.J.Cancer,126(3):669−683(2010)およびYu,M.,et al.,J.Cell Biol.,192(3):373−382(2011)を参照されたい。コールターカウンター等の電子細胞カウンターを使用して細胞を計数してもしなくてもよく、または血球計を使用して細胞を手動で計数してもよい。言うまでもなく、細胞を計数する必要は全くない。
本発明の目的のために、細胞は、1代以上継代された後、初代細胞であるとは見なされない。加えて、1代以上継代され、かつ継代直後に凍結された細胞も、解凍されると初代細胞とは見なされない。本発明の選択実施形態において、NKE細胞は、最初は初代細胞であり、本発明の方法を用いることにより、継代後に非初代細胞になる。
「細胞培養」または「培養」とは、人工的な生体外環境での細胞の維持を意味する。「細胞培養」という用語は、個々の細胞および組織の培養も包含する
初代であるか否かにかかわらず、本発明に従って培養される細胞は、必要に応じて、実験条件に従って技術者によって培養およびプレーティングされてもよい。本明細書における例は、本明細書に記載の方法と併せて用いることができる少なくとも1つの機能な一連の培養条件を示す。所与の動物細胞型のプレーティングおよび培養条件が知られていない場合、日常的な実験のみを用いて、当業者が決定することができる。細胞を、付着因子を用いて培養容器の表面にプレーティングしてもしなくてもよい。付着因子が使用される場合、培養容器を、コラーゲン、フィブロネクチン、およびそれらの天然または合成断片等であるが、これらに限定されない天然組換えもしくは合成付着因子(単数もしくは複数)またはそのペプチド断片で予め被覆してもよい。
それぞれの実験条件の細胞播種密度を、必要とされる特定の培養条件のために操作することができる。プラスチック製の培養容器内での日常的な培養について、1cm2当たり約1×104細胞から約1〜10×105細胞の初期播種密度が極めて典型的であり、例えば、1×106細胞は、多くの場合、75cm2の培養フラスコ中で培養される。しかしながら、本発明の方法を用いて、単一の細胞さえも最初にプレーティングすることができる。したがって、最初の細胞播種に1、2、3、4、5、6、7、8、9、10、20、30、40、50、60、70、80、90、100個、またはそれ以上の数の細胞を用いて、本発明の方法を行うことができる。言うまでもなく、1×103、1×104、1×105等であるが、これらに限定されないより多い細胞播種数を使用することができる。細胞密度を任意の継代で必要に応じて変更してもよい。
哺乳類細胞は、典型的には、細胞インキュベータ(標準大気圧で約37℃)内で培養される。インキュベータ内の大気は、通常、加湿され、多くの場合、空中に約3〜10%の二酸化炭素を含有する。温度、圧力、およびCO2濃度を必要に応じて変更してもよいが、但し、細胞が依然として生存していることを条件とする。培養培地のpHは、約7.1〜約7.6、具体的には、約7.1〜約7.4、より具体的には、約7.1〜約7.3の範囲内であり得る。
細胞培養培地は、通常、1〜2日毎に、または特定の細胞型が必要とするより高い頻度もしくは低い頻度で取り換えられる。NKE細胞が培養容器内でコンフルエンスに近づくと、それらは、通常、継代される。本明細書で使用される細胞継代は、当技術分野で使用されるように使用され、細胞を分割または分裂し、その細胞の一部を新たな培養容器または培養環境に移すことを意味する。本発明の方法で使用されるNKE細胞は、細胞培養表面に付着している可能性が高く、剥離する必要がある。付着細胞を培養容器の表面から剥離する方法は周知であり、一般的に採用されており、トリプシン等の酵素の使用を含んでもよい。
単一継代は、技術者が細胞を1回分割または手動で分裂し、より少ない数の細胞を新たな容器または環境に移すときを指す。継代するとき、細胞が付着および増殖することを可能にする任意の比率に細胞を分割してもよい。したがって、単一継代時、細胞を、1:2、1:3、1:4、1:5等の比率に分割してもよい。したがって、細胞の継代は、集団倍加と同等ではない。本明細書で使用される集団倍加は、培養下の細胞の数が約2倍になるように、細胞が培養下で1回分裂するときである。細胞を計数して、細胞集団が他のある要因によって2倍になるか、3倍になるか、または累加されるかを決定する必要がある。言い換えると、さらに生体外で培養するために、細胞を継代してそれらを1:3の比率で分割することが、細胞集団が3倍になるということと同等であると見なされるべきではない。
本発明の一実施形態において、NKE細胞は、生体外で連続的に培養される。本明細書で使用される「連続的に培養する」とは、細胞が健康状態を維持するために継代および新たな培地を必要とするように、細胞が細胞培養容器内で連続的に分裂して、コンフルエンスに達するか、またはそれに近づくという観念である。したがって、「連続的に培養する」という概念は、NKE細胞が不死化されるという概念に類似している。一実施形態において、本発明の方法および条件を用いて培養されるとき、正常なNKE細胞は、少なくとも5、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、250、もしくは300代継代、またはそれ以上増殖および分裂し続けることができる。
本発明は、NKE細胞、具体的には、正常なNKE細胞の増殖を生体外で刺激する方法も対象とし、方法は、フィーダー細胞、NKE細胞、またはこれら両方におけるROCKの活性を阻害しながら、NKE細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。そのような条件下でのNKE細胞培養が、NKE細胞を刺激して増殖または増殖させるが、他の方法では、細胞は増殖することができない。特定の一実施形態において、細胞は、堅固なクラスター状に増殖し、すなわち、細胞は、堅固に付着するようになる。一実施形態において、培養されたNKE細胞は、e−カドヘリン、非筋ミオシン、およびp120カテニンを含む接合部を形成する。これらの種類の接合部を、参照により組み込まれるLi,D.et al.,J.Cell Biol.,191(3):631−644(2010)に従ってアッセイすることができる。
本明細書で使用され、かつ本明細書を通じて使用される「細胞増殖」は、1つの「母細胞」が2つの「娘細胞」に分裂するような細胞分裂を指す。本明細書で使用される「細胞増
殖」は、細胞の実寸法の増加を指さない。細胞集団を時間経過とともにプロットすることによって、細胞増殖の刺激をアッセイすることができる。より急な増殖曲線を有する細胞集団は、さほど急ではない曲線を有する細胞集団よりも早く増殖していると見なすことができる。増殖曲線を、同一の細胞型間の様々な治療のために比較することができるか、または増殖曲線を、同一の状態を有する異なる細胞型のために比較することができる。
殖」は、細胞の実寸法の増加を指さない。細胞集団を時間経過とともにプロットすることによって、細胞増殖の刺激をアッセイすることができる。より急な増殖曲線を有する細胞集団は、さほど急ではない曲線を有する細胞集団よりも早く増殖していると見なすことができる。増殖曲線を、同一の細胞型間の様々な治療のために比較することができるか、または増殖曲線を、同一の状態を有する異なる細胞型のために比較することができる。
後期継代NKE細胞、具体的には、本発明の正常な後期継代NKE細胞は、それらのテロメア長を特徴としてもしなくてもよい。一般に起こるように、テロメア長は、概して、細胞が分裂するときに短くなる。細胞は、通常、テロメアの平均長が臨界長、例えば、4kbまで減少したときに分裂を停止する。本発明において、後期継代細胞のテロメアの平均長は、最短で2kbの長さまで減少し、増殖し続けることができる。テロメアの平均長は、当技術分野において日常的な方法および技術を用いて容易に決定される。したがって、一実施形態において、本発明は、本発明の培養条件下で分裂することができるNKE細胞、具体的には、正常なNKE細胞を提供し、NKE細胞のテロメアの平均長は、異なる培養条件または従来の日常的な培養条件下に設置されるときに通常分裂しないであろうNKE細胞のテロメアの平均長よりも短い。例えば、老化したヒト前立腺上皮細胞(HPEC)のテロメアの平均長は約4kbであり、したがって、HPECのテロメアの平均長が約4kbまで減少すると、細胞は、通常、現在当技術分野において前立腺細胞の培養を許容できるか、またはさらにはそれに最適であると見なされる培養条件下に設置されるとき、分裂しない。しかしながら、本発明の培養条件を用いて、HPECのテロメアの平均長を、最短で2kb、またはさらにはそれ以下の長さに減少させることができ、依然として、分裂および増殖することができる。したがって、本発明の方法は、条件的に不死化されたNKE細胞、具体的には、条件的に不死化された正常なNKE細胞を生成することができ、それによって、細胞は、通常分裂することができるNKE細胞のテロメアの平均長よりも短いテロメアの平均長を有し、それによって、条件的に不死化されたNKE細胞は、テロメア長が減少したにもかかわらず、依然として分裂することができる。明確にするために、NKE細胞、具体的には、正常なNKE細胞は、現在当技術分野において前立腺細胞の培養を許容できるか、またはさらにはそれに最適であると見なされる培養条件下に設置される場合であっても、通常、テロメアの平均長がある特定の長さまで減少されるとき、分裂を停止する。テロメアの平均長は、細胞型によって異なり得る。
そのような現在許容できるか、または最適な上皮細胞の培養条件は、概して、明確に定義されたか、または合成の血清を含まない培地での細胞の培養を含む。例えば、前立腺細胞の培養は、通常、血清の添加を伴わない前立腺細胞特異的培地での培養を含む。加えて、前立腺細胞、およびすべての他のNKE細胞は、概して、フィーダー細胞の不在下で培養される。したがって、「現在許容できる」または「現在最適な」培養条件は、培地が血清または血清代替物を含まず、フィーダー細胞の使用を含まない培養条件である。「現在許容できる」または「現在最適な」培養条件は、明確に定義されたか、または合成の培地、例えば、前立腺細胞に対して前立腺特異的な細胞培地の使用も含み得る。したがって、本発明の方法は、NKE細胞、具体的には、正常なNKE細胞を培養および継代することができるという予期せぬ結果を提供し、現在許容できる条件または現在最適な条件を用いてそのように培養および継代することができたであろう頃からずいぶん経っている。
本明細書で使用される「条件的に不死化された」という用語は、NKE細胞が、正常な老化したNKEのテロメアの平均長にわたって減少したテロメアの平均長を有するが、依然として、無限に増殖することができることを示すが、但し、条件的に不死化された正常なNKE細胞を含むが、これに限定されない条件的に不死化されたNKE細胞が、本発明の培養条件下で維持されることを条件とする。細胞が条件的に不死化されるかを決定するとき、条件的に不死化された細胞のテロメアの平均長を、通常生体外で老化した非条件的に不死化されたNKE細胞のテロメアの平均長と比較することを必要とし得る。「通常老化
した」という語句は、本明細書に概説される条件がなくても、分裂能力を生体外でさらに低下させ、したがって、これ以上継代される必要のない細胞集団を指すために使用される。したがって、本発明は、NKE細胞、具体的には、正常なNKE細胞を条件的に不死化する方法を提供し、方法は、培養中に、フィーダー細胞、NKE細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害しながら、NKE細胞、具体的には、正常なNKE細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。本明細書で使用される「条件的に不死化された細胞」は、誘導された多能性幹細胞(IPS細胞)ではない。誘導された多能性幹細胞は、多能性幹細胞に類似し、かつ多能性幹細胞のように機能するように再プログラミングされた細胞であり、したがって、IPS細胞は、複数の異なる組織を生成することができる。対照的に、本発明の条件的に不死化されたNKE細胞は、最終分化NKE細胞よりも分化の程度は低くなり得るが、本明細書に概説される条件下で増殖することができる。本明細書で定義されるとき、本発明の条件的に不死化されたNKE細胞は、複数の組織型に分化する能力を獲得しない。本発明の一実施形態において、本明細書に記載の方法によって生成された条件的に不死化された細胞は、初代細胞が単離された組織に戻し分化するか、またはそれを形成する能力を保持する。別の実施形態では、本明細書に記載の方法によって生成された条件的に不死化されたNKE細胞は、初代細胞が単離された組織に完全に戻し分化するか、またはそれを形成する能力を保持しない。
した」という語句は、本明細書に概説される条件がなくても、分裂能力を生体外でさらに低下させ、したがって、これ以上継代される必要のない細胞集団を指すために使用される。したがって、本発明は、NKE細胞、具体的には、正常なNKE細胞を条件的に不死化する方法を提供し、方法は、培養中に、フィーダー細胞、NKE細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害しながら、NKE細胞、具体的には、正常なNKE細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。本明細書で使用される「条件的に不死化された細胞」は、誘導された多能性幹細胞(IPS細胞)ではない。誘導された多能性幹細胞は、多能性幹細胞に類似し、かつ多能性幹細胞のように機能するように再プログラミングされた細胞であり、したがって、IPS細胞は、複数の異なる組織を生成することができる。対照的に、本発明の条件的に不死化されたNKE細胞は、最終分化NKE細胞よりも分化の程度は低くなり得るが、本明細書に概説される条件下で増殖することができる。本明細書で定義されるとき、本発明の条件的に不死化されたNKE細胞は、複数の組織型に分化する能力を獲得しない。本発明の一実施形態において、本明細書に記載の方法によって生成された条件的に不死化された細胞は、初代細胞が単離された組織に戻し分化するか、またはそれを形成する能力を保持する。別の実施形態では、本明細書に記載の方法によって生成された条件的に不死化されたNKE細胞は、初代細胞が単離された組織に完全に戻し分化するか、またはそれを形成する能力を保持しない。
NKE細胞は、生体外で増殖し、連続的な培養を必要とするようになり、かつ/またはあらゆる代に継代した後に細胞の核型を明らかに変化させることなく条件的に不死化され得る。したがって、本発明の方法は、NKE細胞、具体的には、正常なNKE細胞を連続的に培養することを含み、それによって、初代細胞または初期継代細胞の同一の種類の核型と比較して、任意の継代の細胞の核型は、変化しないか、または実質的には変化しない。細胞の核型の変化には、染色体もしくはその一部分の重複または欠失、および/または1つの染色体の一部分から別の染色体の一部分への転座が含まれるが、これらに限定されない。核型の同定およびその変化は、当技術分野において一般的な技術である。したがって、本発明の一実施形態は、後期継代NKE細胞、具体的には、正常な後期継代NKE細胞を対象とし、後期継代NKE細胞は、(a)同一の起源の初代NKE細胞の核型と比較して、変化していない核型、または(b)同一の起源の最初に解凍したNKE細胞の核型と比較して、変化していない核型を有する。本明細書で使用される後期継代NKE細胞は、少なくとも5、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、250、もしくは300代継代、またはそれ以上の継代を経験したNKE細胞と定義される。
本発明は、条件的に不死化されたNKE細胞、具体的には、条件的に不死化された正常なNKE細胞も対象とする。選択実施形態において、条件的に不死化されたNKE細胞、具体的には、条件的に不死化された正常なNKE細胞は、(a)同一の起源の初代NKE細胞の核型と比較して、変化していない核型、または(b)同一の起源の最初に解凍したNKE細胞の核型と比較して、変化していない核型を有する。
本発明の方法は、フィーダー細胞の使用を含む。「フィーダー細胞」という用語は、当技術分野で使用されるように本明細書で使用される。すなわち、フィーダー細胞は、本発明のNKE細胞とともに培養される細胞である。本明細書で使用される「NKE細胞とともに培養する」とは、フィーダー細胞が同一の培地および同一の容器をNKE細胞と共有して培養されることを意味する。したがって、それら両方の組の細胞が、同一の培地を共有する同一の容器内に存在するが、フィーダー細胞は、NKE細胞と直接接触しなくてもよく、例えば、NKE細胞から、例えば、多孔質フィルタを用いて、物理的に分離されてもよい。一実施形態において、フィーダー細胞は、非増殖性フィーダー細胞である。本発明
の一実施形態において、引き続きそれらを存続させ、かつ代謝的に活性にしながら、フィーダーの増殖を阻害するようにフィーダー細胞を処理することができる。例えば、フィーダー細胞を、ガンマ線照射で照射し、かつ/またはマイトマイシンCで処理することができ、これは、細胞分裂を停止するが、細胞を代謝的に活性な状態で維持する。細胞分裂を停止するが、代謝的に活性な状態を維持するように細胞を処理する方法は、当技術分野で周知である。別の実施形態では、フィーダー細胞は、増殖を阻害するように処理されていない。例えば、フィーダーの増殖を阻害するようにフィーダー細胞を処理することを必要とすることなく、NKE細胞との物理的接触を阻止する多孔質フィルタ上に設置されるフィーダー細胞を、NKE細胞とともに培養することができる。
の一実施形態において、引き続きそれらを存続させ、かつ代謝的に活性にしながら、フィーダーの増殖を阻害するようにフィーダー細胞を処理することができる。例えば、フィーダー細胞を、ガンマ線照射で照射し、かつ/またはマイトマイシンCで処理することができ、これは、細胞分裂を停止するが、細胞を代謝的に活性な状態で維持する。細胞分裂を停止するが、代謝的に活性な状態を維持するように細胞を処理する方法は、当技術分野で周知である。別の実施形態では、フィーダー細胞は、増殖を阻害するように処理されていない。例えば、フィーダーの増殖を阻害するようにフィーダー細胞を処理することを必要とすることなく、NKE細胞との物理的接触を阻止する多孔質フィルタ上に設置されるフィーダー細胞を、NKE細胞とともに培養することができる。
フィーダー細胞は、任意の哺乳動物由来であってもよく、フィーダー細胞の動物源は、培養されるNKE細胞と同一の動物源である必要はない。例えば、フィーダー細胞は、マウス、ラット、イヌ、ネコ、ウシ、ウマ、ブタ、非ヒト、およびヒト霊長類フィーダー細胞であってもよいが、これらに限定されない。使用されるフィーダー細胞の種類は、典型的には、脾臓細胞、マクロファージ、胸腺細胞、および/または線維芽細胞である。一実施形態において、脾臓細胞、マクロファージ、胸腺細胞、および/または線維芽細胞は、それらが非増殖性であるように処理されている。本発明の方法で使用することができるフィーダー細胞の一例には、J2細胞集団がある。J2細胞は、樹立されたスイス3T3細胞株に由来するマウス線維芽細胞のサブクローンである。一実施形態において、J2細胞は、ガンマ線照射される。別の実施形態では、J2細胞は、マイトマイシンCで処理される。
別の実施形態では、フィーダー細胞で馴化された培地が、フィーダー細胞のNKE細胞との培養の代わりに使用される。馴化培地の調製は、当技術分野では日常的である。概して、馴化培地の調製は、培地、例えば、本明細書で定義されるF培地中で細胞を数日間培養することと、この培地を回収することとを含む。馴化培地は、多くの場合、希釈された様式で新たな培地と合わせられるが、必須ではない。「新たな培地」に対する馴化培地の最適な希釈比率を見出すことは日常的であるが、比率は、約1:99〜約99:1の「馴化培地」:「新たな培地」であってもよい。本明細書で使用される「馴化培地」は、培地のすべてまたはある割合の培地が培養中で使用された任意の培地である。
さらに別の実施形態では、フィーダー細胞抽出物を、フィーダー細胞自体の代わりに培地に添加することができる。フィーダー細胞抽出物の調製方法は一般的であり、Graham,J.and Sandall J.,Biochem.J.,182:157−164(1979)、Graham,J.,Biochem.J.,130:1113−1124(1972)、およびDickson,R.,et al.,Proc.Nat’l
Acad.Sci.,U.S.A.,80:5335−5339(1983)に記載されており、これらはすべて、参照により本明細書に組み込まれる。培地に対するフィーダー細胞抽出物の最適な希釈比率を見出すことは日常的であるが、比率は、約1:99〜約99:1の抽出:培地であってもよい。
Acad.Sci.,U.S.A.,80:5335−5339(1983)に記載されており、これらはすべて、参照により本明細書に組み込まれる。培地に対するフィーダー細胞抽出物の最適な希釈比率を見出すことは日常的であるが、比率は、約1:99〜約99:1の抽出:培地であってもよい。
本発明の細胞培養培地は、任意の水ベースの培地であってもよく、DMEM(ダルベッコ修飾必須培地)、ハムF12培地、ハムF10培地、RPMI1640、イーグル基礎培地(EBM)、イーグル最小必須培地(MEM)、HEPES、培地199等であるが、これらに限定されない任意の「古典的な」培地を含み得る。培養培地は、DMEMおよびF12培地の組み合わせ等であるが、これらに限定されない古典的な培地のうちのいずれかの組み合わせであってもよい。
さらなる成分を、本発明の方法で使用される培養培地に添加することができる。そのようなさらなる成分には、アミノ酸、ビタミン、無機塩、アデニン、エタノールアミン、D−
グルコース、ヘパリン、N−[2−ヒドロキシエチル]ピペラジン−N’−[2−エタンスルホン酸](HEPES)、ヒドロコルチゾン、インスリン、リポ酸、フェノールレッド、リン酸エタノールアミン、プトレッシン、ピルビン酸ナトリウム、トリヨードチロニン(T3)、チミジン、およびトランスフェリンが含まれるが、これらに限定されない。あるいは、インスリンおよびトランスフェリンを、クエン酸第二鉄または硫酸第一鉄キレートに置き換えてもよい。これらのさらなる成分はそれぞれ市販されている。
グルコース、ヘパリン、N−[2−ヒドロキシエチル]ピペラジン−N’−[2−エタンスルホン酸](HEPES)、ヒドロコルチゾン、インスリン、リポ酸、フェノールレッド、リン酸エタノールアミン、プトレッシン、ピルビン酸ナトリウム、トリヨードチロニン(T3)、チミジン、およびトランスフェリンが含まれるが、これらに限定されない。あるいは、インスリンおよびトランスフェリンを、クエン酸第二鉄または硫酸第一鉄キレートに置き換えてもよい。これらのさらなる成分はそれぞれ市販されている。
本発明の培地に含んでもよいアミノ酸成分には、L−アラニン、L−アルギニン、L−アスパラギン、L−アスパラギン酸、L−システイン、L−グルタミン酸、L−グルタミン、グリシン、L−ヒスチジン、L−イソロイシン、L−ロイシン、L−リジン、L−メチオニン、L−フェニルアラニン、L−プロリン、L−セリン、L−トレオニン、L−トリプトファン、L−チロシン、およびL−バリンが含まれるが、これらに限定されない。
添加してもよいビタミンには、ビオチン、塩化コリン、D−Ca+2−パントテン酸塩、葉酸、i−イノシトール、ナイアシンアミド、ピリドキシン、リボフラビン、チアミン、およびビタミンB12が含まれるが、これらに限定されない。
添加してもよい無機塩成分には、カルシウム塩(例えば、CaCl2)、CuSO4、FeSO4、KCl、マグネシウム塩、例えば、MgCl2、マンガン塩、例えば、MnCl2、酢酸ナトリウム、NaCl、NaHCO3、Na2HPO4、Na2SO4、ならびに微量元素セレン、シリコン、モリブデン、バナジウム、ニッケル、錫、および亜鉛のイオンが含まれるが、これらに限定されない。これらの微量元素を、様々な形態、好ましくは、Na2SeO3、Na2 SiO3、(NH4)6Mo7 O24、NH4 VO3、NiSO4、SnCl、およびZnSO等の塩形態で提供することができる。
さらなる成分には、ヘパリン、上皮増殖因子(EGF)、細胞内環状アデノシン一リン酸(cAMP)レベルを増加させる少なくとも1つの作用物質、および少なくとも1つの線維芽細胞増殖因子(FGF)が含まれるが、これらに限定されない。ヘパリン、EGF、cAMP増加作用物質(複数を含む)およびFGF(複数を含む)を、基礎培地に添加することができるか、またはそれらを、例えば、ダルベッコリン酸緩衝生理食塩水(DPBS)の溶液中に混合し、基礎培地に添加して本発明の方法で使用する培地を作成するまで凍結状態で保管してもよい。
ヘパリンを商業的に入手することができる。ヘパリンは、主に増殖因子成分、例えば、FGFの活性を安定化させるために、本培地に添加される。ヘパリンが使用される場合、それを約1〜500USP単位/リットルの濃度で基礎培地に添加してもよい。EGFは、市販されている。EGFが使用される場合、それを約0.00001〜10mg/Lの濃度で基礎培地に添加してもよい。
細胞内cAMPレベルを増加させる様々な作用物質を、本発明の培地を作成する際に使用することができる。細胞内cAMPレベルの直接増加を誘導する作用物質(例えば、ジブチリルcAMP)、細胞Gタンパク質との相互作用によって細胞内cAMPレベルの増加を引き起こす作用物質(例えば、コレラ毒素およびホルスコリン)、βアドレナリン受容体の作動薬として作用することによって細胞内cAMPレベルの増加を引き起こす作用物質(例えば、イソプロテレノール)、ならびにcAMPホスホジエステラーゼの活性を阻害することによって細胞内cAMPレベルの増加を引き起こす作用物質(例えば、イソブチルメチルキサンチン(IBMX)およびテオフィリン)が含まれる。これらのcAMPを増加させる作用物質は市販されている。
本発明の方法で使用される培養培地は、カルシウム源を含む。一実施形態において、カル
シウム源は、血清または血清代替物である。別の実施形態では、カルシウム源は、培地に添加されるカルシウム含有塩である。血清がカルシウム源として使用される場合、血清は、約1%〜約35%の濃度(v/v)であり得る。選択実施形態において、血清は、約1%〜約20%、または約1%〜約15%、または約1%〜約10%、または約1%〜約5%の濃度である。血清代用物または血清代替物がカルシウム源として使用される場合、これらを製造業者が推奨するプロトコルに従って培地に添加することができる。血清代用物の例には、Pall CorporationのUltroser(商標)等の市販の代用物、脱脂粉乳濾過物等であるが、これに限定されない乳汁または乳汁画分が挙げられるが、これらに限定されない。
シウム源は、血清または血清代替物である。別の実施形態では、カルシウム源は、培地に添加されるカルシウム含有塩である。血清がカルシウム源として使用される場合、血清は、約1%〜約35%の濃度(v/v)であり得る。選択実施形態において、血清は、約1%〜約20%、または約1%〜約15%、または約1%〜約10%、または約1%〜約5%の濃度である。血清代用物または血清代替物がカルシウム源として使用される場合、これらを製造業者が推奨するプロトコルに従って培地に添加することができる。血清代用物の例には、Pall CorporationのUltroser(商標)等の市販の代用物、脱脂粉乳濾過物等であるが、これに限定されない乳汁または乳汁画分が挙げられるが、これらに限定されない。
本発明の実施形態で使用されるCa+2濃度の範囲は、細胞型によって異なり得る。一実施形態において、本発明の方法で使用される培地中のCa+2の濃度は、0.1mM〜10.0mMである。より具体的な実施形態では、本発明の方法で使用される培地中のCa+2の濃度は、約0.2mM〜約8mM、約0.4mM〜約7mM、約0.5mM〜約5mM、約0.8mM〜約4mM、約1.0mM〜約3mM、約1.2mM〜約2.8mM、約1.4mM〜約2.6mM、および約1.5mM〜約2.5mMであり得る。
本発明の方法は、培養物中でのRho関連コイルドコイルタンパク質キナーゼ(ROCK)の阻害を含む。Rhoキナーゼは、Rho、Rac1、およびCdc42キナーゼを含むRho GTPaseタンパク質ファミリーに属する。Rhoの最もよく特徴付けられたエフェクタ分子のうちの1つは、ROCKであり、これは、RhoのGTP結合形態に結合するセリン/トレオニンキナーゼである。セリン/トレオニンキナーゼの特徴を示している保存モチーフを含むROCKの触媒キナーゼドメインがN末端に見られる。ROCKタンパク質は、Rho結合ドメイン(RBD)を含む中央コイルドコイルドメインも有する。C末端は、内部高システインドメインを有するプレクストリン相同(PH)ドメインで構成されている。コイルドコイルドメインは、他のαヘリックスタンパク質と相互作用すると考えられている。コイルドコイルドメイン内に位置するRBDは、RhoA、RhoB、およびRhoCを含む活性化したRho GTPasesのみと相互作用する。pHドメインは、アラキドン酸およびスフィンゴシルホスフォリルコリン等の脂質メディエータと相互作用すると考えられており、タンパク質局在化に関与し得る。pHドメインおよびRBDのキナーゼドメインとの相互作用は、自己阻害ループをもたらす。加えて、キナーゼドメインは、ROCK活性の負の調節因子であるRhoEへの結合に関与する。
ROCKファミリーは、現在、2つのメンバー、ROCK1(別名、ROKβまたはp160ROCK)およびROCK2(別名、ROKα)からなる。ROCK1は、約1354アミノ酸長であり、ROCK2は、約1388アミノ酸長である。ヒトROCK1およびヒトROCK2のアミノ酸配列は周知である。例えば、ROCK1およびROCK2のアミノ酸配列を、それぞれ、UniProt Knowledgebase(UniProtKB)受入番号Q13464およびO75116で見出すことができる。ヒトROCK1およびROCK2のヌクレオチド配列を、それぞれ、GenBank受入番号NM_005406.2およびNM_004850で見出すことができる。様々な動物由来のROCK1およびROCK2タンパク質のヌクレオチドおよびアミノ酸配列は周知であり、UniProtおよびGenBankデータベースの両方で見出すことができる。
両方のROCKアイソフォームが組織内で遍在的に発現するが、それらは、いくつかの組織において異なる強度を呈する。例えば、ROCK2が、脳および骨格筋により蔓延している一方で、ROCK1は、肝臓、精巣、および腎臓でより豊富である。両方のアイソフォームが、血管平滑筋および心臓内で発現する。休止状態にあるとき、ROCK1およびROCK2のいずれも主として細胞質であるが、Rhoを活性化するときに膜に転位置する。ROCK活性は、いくつかの異なる機構によって調節され、したがって、Rho依存
性ROCK活性化は、収縮性の変化、細胞透過性、移行、および増殖からアポトーシスに至るまで、高度に細胞型依存的である。少なくとも20個のROCK基質が同定されている。Hu and Lee,Expert Opin.Ther.Targets 9:715−736(2005)、Loirand et al,Cir.Res.98:322−334(2006)、およびRiento and Ridley,Nat.Rev.MoI.Cell Biol.4:446−456(2003)を参照されたく、これらはすべて、参照により組み込まれる。
性ROCK活性化は、収縮性の変化、細胞透過性、移行、および増殖からアポトーシスに至るまで、高度に細胞型依存的である。少なくとも20個のROCK基質が同定されている。Hu and Lee,Expert Opin.Ther.Targets 9:715−736(2005)、Loirand et al,Cir.Res.98:322−334(2006)、およびRiento and Ridley,Nat.Rev.MoI.Cell Biol.4:446−456(2003)を参照されたく、これらはすべて、参照により組み込まれる。
アポトーシスシグナル伝達の調節におけるROCKの役割は、高度に細胞型依存的かつ刺激依存的である。その一方で、ROCKは、生体外および生体内細胞生存シグナルの媒介に関連している。ROCK媒介性生存促進性効果は、上皮細胞、癌細胞、および内皮細胞、ならびに他の細胞型において報告されている。気道上皮細胞において、Y−27632またはHA1077(別名、ファスジル)での阻害は、膜の波打ち現象、アクチンストレスファイバーの喪失、およびアポトーシスを誘導する(Moore et al.,Am.J.Respir.Cell MoI.Biol.30:379−387,2004)。
Rho/ROCK活性化は、酸化的ストレス誘導性腸上皮細胞傷害中に生存促進の役割も果たし得る(Song et al.,Am.J.Physiol.Cell Physiol.290:C1469−1476,2006)。ROCKは、甲状腺癌細胞(Zhong et al.,Endocrinology 144:3852−3859,2003)、グリオーマ細胞(Rattan et al,J.Neurosci.Res.83:243−255,2006)、ヒト臍静脈内皮細胞(Li et al.,J.Biol.Chem.277:15309−15316,2002)、肝星細胞(Ikeda et al.,Am.J.Physiol.Gastrointest.Liver Physiol.285:G880−886,2003)、およびヒト神経芽腫細胞(De Sarno et al.,Brain Res.1041:112−115,2005)における生存促進事象にも関連している。ROCKが生存促進の役割を果たすという証拠も、例えば、管平滑筋細胞(Shibata et al,Circulation 103:284−289,2001)および脊髄運動ニューロン(Kobayashi et al,J.Neurosci.24:3480−3488,2004)において生体内で報告されている。
本明細書で使用されるとき、ROCKの阻害とは、ROCK1またはROCK2のうちの少なくとも1つの活性、機能、もしくは発現の低下を意味し得る。活性、機能、もしくは発現を完全に抑圧することができ、すなわち、活性、機能、もしくは発現が存在しないか、または活性、機能、もしくは発現は、処理されていない細胞と比較して処理された細胞において単に低い場合がある。概して、ROCKは、GTP結合Rhoの結合を介して活性化された後に、LIMキナーゼおよびミオシン軽鎖(MLC)ホスファターゼをリン酸化する。したがって、本発明の一実施形態は、ROCK1および/もしくはROCK2が活性化されないか、またはその活性が処理されていない細胞よりも低くなるように、ROCK1および/もしくはROCK2、例えば、GTP結合Rhoの上流経路の遮断を含む。他の上流エフェクタには、インテグリン;TGF−βおよびEGFRを含むが、これらに限定されない増殖因子受容体;カドヘリン;Gタンパク質共役受容体等が含まれるが、これらに限定されない。したがって、本発明の別の実施形態は、ROCK1および/またはROCK2が任意のシグナルを伝播することができないか、または処理されていない細胞と比較して低下したシグナルのみを伝播することができるように、活性化されたROCK1および/またはROCK2の下流エフェクタ分子の活性、機能、もしくは発現の遮断を含む。下流エフェクタには、ミオシンホスファターゼ標的タンパク質(MYPT)、ビメンチン、LIMK、ミオシン軽鎖キナーゼ、NHE1、コフィリン、ミオシンII等が
含まれるが、これらに限定されない。例えば、Rhoの活性を阻害するROCK上流阻害剤であるC3トランスフェラーゼ、およびミオシンIIの活性を阻害するROCK下流阻害剤であるブレビスタチンのいずれも、ROCK阻害剤の代わりに本明細書に記載の培養条件下で使用されるとき、細胞が分化を回避することを可能にし、かつ生体外増殖を可能にするような様式で細胞に影響を及ぼした(図23)。直接ROCK阻害の代わりに、かつ本明細書に記載および要求される他の培養条件と併せて、ROCKの上流または下流阻害は、条件的に不死化されたNKE細胞を生成する場合もしない場合もある。
含まれるが、これらに限定されない。例えば、Rhoの活性を阻害するROCK上流阻害剤であるC3トランスフェラーゼ、およびミオシンIIの活性を阻害するROCK下流阻害剤であるブレビスタチンのいずれも、ROCK阻害剤の代わりに本明細書に記載の培養条件下で使用されるとき、細胞が分化を回避することを可能にし、かつ生体外増殖を可能にするような様式で細胞に影響を及ぼした(図23)。直接ROCK阻害の代わりに、かつ本明細書に記載および要求される他の培養条件と併せて、ROCKの上流または下流阻害は、条件的に不死化されたNKE細胞を生成する場合もしない場合もある。
本発明の方法は、NKE細胞、具体的には、正常なNKE細胞を培養しながら、ROCKを阻害することを含む。一実施形態において、ROCKの阻害は、ROCK阻害剤を培養培地に添加することによって達成される。ROCK阻害剤が培養培地に添加されるこの実施形態において、ROCK阻害剤がNKE細胞に加えてフィーダー細胞にも影響を及ぼし得る可能性がある。
ROCK阻害剤の例には、Y−27632、HA1100、HA1077、チアゾビビン、およびGSK429286が挙げられるが、これらに限定されず、これらの構造は、図11に示される。これらの化合物は周知であり、市販されている。さらなる小分子Rhoキナーゼ阻害剤には、PCT公開第WO03/059913号、同第WO03/064397号、同第WO05/003101号、同第WO04/112719号、同第WO03/062225号、および同第WO03/062227号に記載されている阻害剤、ならびに米国特許第7,217,722号および同第7,199,147号、ならびに米国特許出願公開第2003/0220357号、同第2006/0241127号、同第2005/0182040号、および同第2005/0197328号に記載されている阻害剤が含まれるが、これらに限定されず、これらのすべての内容は、参照により組み込まれる。
ROCKキナーゼを阻害する別の方法は、RNA干渉(RNAi)を用いることである。RNAi技術は周知であり、dsRNAの一方の鎖がROCK1をコードするmRNAのコード鎖に対応し、もう一方の鎖が第1の鎖に補完的である二本鎖RNA(dsRNA)に依存する。所与のヌクレオチド配列に最適なRNAi種の要件は周知であるか、または最高水準を考慮して容易に解明することができる。例えば、最適なdsRNAは、約20〜25ntの長さであることが知られており、dsRNAのそれぞれの鎖の3’末端に2塩基オーバーハンドを有し、多くの場合、低分子干渉RNA(siRNA)と称される。言うまでもなく、低分子ヘアピンRNA(shRNA)等の他の周知の形状も功を奏し得る。shRNAは、分子が少なくとも一部分において二本鎖であるように一部分が自己相補的な1つの連続したRNA鎖である。細胞がshRNAをsiRNAに処理したと考えられる。本明細書で使用されるRNAi分子という用語は、dsRNAの一方の鎖がサイレンシングされる標的遺伝子をコードするmRNAのコード鎖に対応し、もう一方の鎖が第1の鎖に補完的である任意の二本鎖RNA(dsRNA)である。
したがって、本発明の一実施形態は、ROCKの活性を阻害するために、少なくとも1つのRNAi分子および/または少なくとも1つのアンチセンス分子の使用を含む。特定の一実施形態において、RNAi分子および/またはアンチセンス分子は、ROCK1に特異的である。別の実施形態では、RNAi分子またはアンチセンス分子は、ROCK2に特異的である。さらに別の実施形態では、RNAi分子および/またはアンチセンス分子は、ROCK1およびROCK2の両方に特異的である。さらに別の実施形態では、少なくとも2つのRNAi分子および/またはアンチセンス分子が使用され、一方はROCK1に特異的であり、もう一方はROCK2に特異的である。
RNAi分子および/またはアンチセンス分子は、参照により組み込まれるClemen
s,J.C.,et al.,PNAS,97(12):6499−6503(2000)において報告されているように、ネイキッドRNAi分子および/またはアンチセンス分子を有する細胞を単に浸漬することによる細胞培養物の一部であり得る。RNAi分子および/またはアンチセンス分子は、RNAi分子またはアンチセンス/分子を細胞に挿入するために使用され得るリポソーム複合体等の複合体の一部であり得る。
s,J.C.,et al.,PNAS,97(12):6499−6503(2000)において報告されているように、ネイキッドRNAi分子および/またはアンチセンス分子を有する細胞を単に浸漬することによる細胞培養物の一部であり得る。RNAi分子および/またはアンチセンス分子は、RNAi分子またはアンチセンス/分子を細胞に挿入するために使用され得るリポソーム複合体等の複合体の一部であり得る。
リポソームは、2つの広範なクラスに分類される。カチオン性リポソームは、安定した複合体を形成するために負に荷電したdsRNA分子と相互作用する正に荷電したリポソームである。正に荷電したdsRNA/リポソーム複合体は、負に荷電した細胞表面に結合し、エンドソームに内部移行される。エンドソーム内の酸性pHにより、リポソームは破裂され、それらの内容物を細胞質に放出する(Wang et at.,Biochem.Biophys.Res.Commun.,1987,147,980−985)。
pH感受性であるか、または負に荷電したリポソームは、それを有する複合体ではなくdsRNAを捕捉する。dsRNAおよび脂質のいずれも同様に荷電されるため、複合体形成ではなく反発が生じる。したがって、dsRNAは、これらのリポソームの水性内部に捕捉される。pH感受性リポソームは、例えば、チミジンキナーゼ遺伝子をコードするdsRNAを培養下の細胞単層に送達するために使用されている(Zhou et al.,Journal of Controlled Release,1992,19,269−274)。リポソーム組成物の主な種類の1つに、天然由来のホスファチジルコリン以外のリン脂質がある。天然リポソーム組成物を、例えば、ジミリストイルホスファチジルコリン(DMPC)またはジパルミトイルホスファチジルコリン(DPPC)から形成することができる。アニオン性リポソーム組成物が、概して、ジミリストイルホスファチジルグリセロールから形成される一方で、アニオン性融合性リポソームは、主に、ジオレオイルホスファチジルエタノールアミン(DOPE)から形成される。リポソーム組成物の別の種類は、例えば、大豆PC、および卵PC等のホスファチジルコリン(PC)から形成される。別の種類は、リン脂質および/またはホスファチジルコリンおよび/またはコレステロールの混合物から形成される。核酸を含むリポソームは、例えば、国際公開第WO96/40062号、米国特許第5,264,221号、米国特許第5,665,710号、およびLoveらの国際公開第WO97/04787号に記載されており、これらすべて、参照により組み込まれる。
リポソームの別の種類であるトランスファーソームは、薬物送達ビヒクルにとって魅力的な高度に変形可能な脂質凝集体である(Cevc et al.,1998,Biochim Biophys Acta.1368(2):201−15)。トランスファーソームは、高度に変形可能であるため、それらが脂質滴よりも小さい孔を貫通することができる脂質滴と称されてもよい。トランスファーソームは、それらが使用される環境に適応可能であり、例えば、それらは、形状に適応でき、自己修復性であり、高い頻度で、断片化することなくそれらの標的に達し、多くの場合、自動装填式である。例えば、表面エッジ活性剤、通常、界面活性剤を、標準のリポソーム組成物に添加することによって、トランスファーソームを作製することができる。
ROCK1および/またはROCK2 RNAiが細胞にアクセスすることができる本発明の方法における別の方法は、RNAi分子および/またはアンチセンス分子をコードするDNA発現ベクターの使用である。ある特定の実施形態は、例えば、RNAi分子がshRNAであるとき、または対抗するプロモーターがRNAi分子のコード配列のいずれかの端に配置されるとき、1つのみのベクターを利用する。したがって、「ROCKの活性の阻害」は、転写されるときにROCKの活性、機能、または産生を遮断することができるDNAの使用を含む。上述のリポソーム送達系は、RNAiおよび/またはアンチセンスをコードするDNAが細胞に進入することができる1つの手段である。
あるいは、RNAiおよび/またはアンチセンスをコードするDNAを、細胞に進入する能力を有するウイルスベクター系において調製することができる。これらは当技術分野で周知であり、Madzak et al.,J.Gen.Virol.,73:1533−36(1992)(パポバウイルスSV40)、Berkner et al.,Curr.Top.Microbiol.Immunol.,158:39−61(1992)(アデノウイルス)、Moss et al.,Curr.Top.Microbiol.Immunol.,158:25−38(1992)(ワクシニアウイルス)、Muzyczka,Curr.Top.Microbiol.Immunol.,158:97−123(1992)(アデノ随伴ウイルス)、Margulskee,Curr.Top.Microbiol.Immunol.,158:67−93(1992)(単純ヘルペスウイルス(ISV)およびエプスタイン・バーウイルス(HBV))、Miller,Curr.Top.Microbiol.Immunol.,158:1−24(1992)(レトロウイルス)、Brandyopadhyay et al.,Mol.Cell.Biol.,4:749−754(1984)(レトロウイルス)、Miller et al.,Nature,357:455−450(1992)(レトロウイルス)、Anderson,Science,256:808−813(1992)(レトロウイルス)、C.Hofmann et al.,Proc.Natl.Acad.Sci.USA,1995;92,pp.10099−10103(バキュロウイルス)を含む。
別の実施形態では、ROCK1および/もしくはROCK2は、ノックアウト構築物またはドミナントネガティブ構築物のいずれかを含むトランスジェニック技術等であるが、これに限定されない遺伝子操作技術を用いて阻害される。そのような構築物は、参照により本明細書に組み込まれるKhyrul,W.,et al.,J.Biol.Chem.,279(52):54131−54139(2004)に記載されている。
上述のように、ROCKを遮断する一実施形態は、小分子阻害剤、RNAi技術、アンチセンス技術、および/または遺伝子操作等であるが、これらに限定されない本明細書に記載の方法のうちのいずれかを用いて、ROCKの上流もしくは下流エフェクタ分子を個別または集合的に遮断または阻害することである。したがって、阻害することができる任意の上流エフェクタには、インテグリン;TGF−βおよびEGFRを含むが、これらに限定されない増殖因子受容体;カドヘリン;Gタンパク質共役受容体等が含まれるが、これらに限定されない。加えて、阻害することができる任意の下流エフェクタには、ビメンチン、LIMK、ミオシン軽鎖キナーゼ、NHE1、コフィリン等が含まれるが、これらに限定されない。
本発明の条件下で培養された後、細胞をこれらの条件から除去し、フィーダー細胞を欠き、カルシウム源を欠き、かつ/またはROCK阻害剤を欠く細胞培養環境下に設置される。フィーダー細胞、カルシウム源、およびROCK阻害剤の1つ、2つ、または3つの任意の組み合わせが、その後の環境に不在であってもよい。本明細書で使用される「その後の環境」とは、胞培養環境に関連して使用されるとき、フィーダー細胞、カルシウム源、およびROCK阻害剤のうちの少なくとも1つを欠く細胞培養環境である。一実施形態において、ROCK阻害剤、カルシウム源、またはフィーダー細胞が、その後の環境に不在である。別の実施形態では、フィーダー細胞およびROCK阻害剤が、その後の環境に不在である。別の実施形態では、フィーダー細胞およびカルシウム源が、その後の環境に不在である。別の実施形態では、カルシウム源およびROCK阻害剤が、その後の環境に不在である。別の実施形態では、フィーダー細胞、ROCK阻害剤、およびカルシウム源が、その後の環境に不在である。
一実施形態において、NKE細胞、後期継代NKE細胞、および/もしくは条件的に不死化されたNKE細胞に対するその後の環境は、分化を促進することができ、かつ/またはNKE細胞、後期継代NKE細胞、および/もしくは条件的に不死化されたNKE細胞の永久増殖を可能にしない環境である。その後の環境は、細胞が元来由来した器官、すなわち、自家性移植片と同様または同一の生体内環境であり得る。例えば、本発明の方法に従って培養された肝細胞を、その細胞が最初に生検または単離された対象の肝臓に再導入することができる。図20は、条件的に不死化された前立腺癌細胞株を作成するために、採取して本明細書に記載の培養条件に供したヒト前立腺腫瘍細胞を示す。条件的に不死化された前立腺癌細胞は、SCIDマウス、すなわち、その後の生体内環境下に設置され、これらの条件的に不死化された前立腺癌細胞は、マウスにおいて新たな腫瘍を生成することができた。
その後の環境は、このその後の環境下に設置された時点で細胞が元来由来した器官の生化学的性質または生理学的性質により密接に類似した生体外環境であってもよい。その後の環境は、生体外での分化を促進することで知られている因子が細胞培養に添加されるような「合成環境」であってもよい。例えば、後期継代肝上皮細胞は、細胞の分化を促進するように設計されたその後の環境下に設置されると、クラスターの形成および/または成熟肝上皮細胞に類似したタンパク質の発現を開始し得る。
一実施形態において、NKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞は、細胞が元来由来した器官の細胞への細胞の分化の刺激に特異的なその後の環境下に設置される。例えば、条件的に不死化された前立腺上皮細胞を本発明の条件から除去し、前立腺細胞の分化を促進するように設計された培養条件下に設置することができる。上皮細胞を培養するための様々な環境は、参照により組み込まれる、Culture of Epithelial Cells(Ian Freshney and
Mary G.Freshney,Eds.Wiley−Liss,Inc.)(第2版、2002年)に詳述されている。
Mary G.Freshney,Eds.Wiley−Liss,Inc.)(第2版、2002年)に詳述されている。
あるいは、細胞を、その後の環境下で、天然もしくは合成三次元細胞培養表面の中に、またはその上に播種することができる。三次元表面の1つの非限定的な例は、Matrigel(登録商標)でコーティングされた培養表面である。他の三次元培養環境は、ヒドロゲル等であるが、これに限定されない任意の形状のコラーゲンゲルおよび/または合成生体高分子材料を含む表面を含む。言うまでもなく、様々な三次元培養表面を本発明の方法と同時に用いることができる。三次元培養環境が使用される場合、フィーダー細胞も同様に使用してもしなくてもよい。これらの三次元細胞培養表面環境は、分化を促進する場合もしない場合もある。
一実施形態において、NKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞を、目的とするタンパク質を発現するように遺伝子改変することができる。細胞の遺伝子改変は、ウイルスタンパク質の挿入等の細胞を不死化させるように設計された改変ではない。むしろ、細胞の遺伝子改変は、例えば、タンパク質をコードする導入遺伝子を挿入するように設計される。例えば、肝細胞を、本発明の細胞培養方法を用いて単離および拡大することができる。続いて、これらの細胞を操作してもよく、細胞が第VIII因子を産生することができるように、第VIII因子をコードする導入遺伝子を細胞のゲノムに挿入することができる。その後、これらの細胞をその後の環境下に設置すること、例えば、自家性移植片を対象に設置することによって、細胞は、第VIII因子を産生することができる。別の例として、肺上皮細胞を、嚢胞性線維症に罹患する対象から単離してもよい。その後、これらの細胞を、本発明の細胞培養方法を用いて拡大してもよく、嚢胞性線維症膜コンダクタンス制御因子をコードする導入遺伝子をこれらの細胞に生体外で挿入してもよい。その後、遺伝子改変されたNKE細胞を、裸にされた気管支上
皮上に再構成して、正常機能を回復させることができる。正常機能を回復させるために上皮表面の10%のみが取り換えられる必要があると推定される。偽重層円柱上皮の繊毛細胞での形成が、正常な組織の再形成を示す。参照により組み込まれる、Fulcher M.L.et al.,Well−Differentiated Human Airway Epithelial Cell Cultures.Methods in Molecular Medicine,107:Human Cell Culture Protocols,pp183−206,Second Edition Edited by:J.Picot.Humana Press Inc.,Totowa,NJを参照されたい。
皮上に再構成して、正常機能を回復させることができる。正常機能を回復させるために上皮表面の10%のみが取り換えられる必要があると推定される。偽重層円柱上皮の繊毛細胞での形成が、正常な組織の再形成を示す。参照により組み込まれる、Fulcher M.L.et al.,Well−Differentiated Human Airway Epithelial Cell Cultures.Methods in Molecular Medicine,107:Human Cell Culture Protocols,pp183−206,Second Edition Edited by:J.Picot.Humana Press Inc.,Totowa,NJを参照されたい。
導入遺伝子が細胞に導入される方法は、DNAの哺乳類細胞への生体外移動についての文献から既知の標準の方法、例えば、参照により組み込まれる国際公開第WO93/07283号に記載の電気穿孔法、リン酸カルシウム沈殿、または受容体媒介エンドサイトーシスに基づく方法等である。目的とする遺伝子を細胞に挿入するための他の方法および物質は、参照により組み込まれるSambrook et al.,Molecular Cloning:A Laboratory Manual,Cold Springs Harbor Laboratory Press,Third Edition(2001)に開示されている。
多種多様の目的とする遺伝子を、NKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞内で発現させることができる。これらの目的とする遺伝子は、毒素、凝固因子、酵素、プロドラッグ変換酵素、免疫応答を刺激する抗原、腫瘍壊死因子、サイトカイン、ならびに治療用途を有する様々なタンパク質(例えば、増殖ホルモンおよび調節因子)をコードする配列を含むが、これらに限定されない。
本発明のNKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞をトランスフェクトした後、うまくトランスフェクトされたこれらの細胞を、当技術分野で周知のマーカーを用いて選択することができる。うまくトランスフェクトされた細胞を選択した後、本発明の遺伝子改変されたNKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞を、本発明の細胞培養技術を用いて培養して、遺伝子改変されたNKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞の集団を産生することができる。続いて、これらの細胞を回収し、対象に戻して設置することを含むが、これに限定されない上述のその後の環境下、すなわち、自家性移植片に設置することができる。
本発明は、治療を必要とする対象のために候補治療を同定する方法も対象とし、対象は、異常なNKE細胞または罹患したNKE細胞の存在を特徴とする状態を有する。異常なNKE細胞または罹患したNKE細胞の存在を特徴とするそのような状態には、新生物形成、過形成、または悪性腫瘍もしくは良性腫瘍が含まれるが、これらに限定されない。方法は、本発明の培養方法のいずれかに従って、異常なNKE細胞の試料を対象から得ることと、異常なNKE細胞を培養して、生体外の異常なNKE細胞集団を産生することとを含む。例えば、循環腫瘍細胞(CTC)を生物の血液循環から単離することができ、本発明の方法を利用して、さらなる分析での使用に十分な数の細胞を得ることができ、これらの細胞は、表現型的または遺伝的に特徴付けられた細胞等であるが、これらに限定されない。CTCを単離する1つの方法が本明細書に開示されているが、本発明は、CTCが単離される任意の方法に限定されない。これまで、CTCは単離されたが、研究および分析を可能にするのに有意な期間さえも培養下で保つことができなかった。しかしながら、本発明は、最小数のCTC、さらには単一の細胞が単離およびプレーティングされることを可能にすることによりこの問題を解決する。その後、プレーティングされたCTC(複数を含む)は、その後の遺伝分析、機能分析、および/または表現型分析を可能にするのに十
分な数の細胞を達成および維持するために、本発明の発明的方法に供される。実際、十分な数の異常なNKE細胞または罹患したNKE細胞が得られると、それらの源にかかわらず、これらの細胞をアッセイして、対象の候補治療を同定するために用いることができる応答プロファイルを決定することもできる。
分な数の細胞を達成および維持するために、本発明の発明的方法に供される。実際、十分な数の異常なNKE細胞または罹患したNKE細胞が得られると、それらの源にかかわらず、これらの細胞をアッセイして、対象の候補治療を同定するために用いることができる応答プロファイルを決定することもできる。
本明細書で使用される応答プロファイルは、異常なNKE細胞が生体内設定にある場合、例えば、臨床医に、特定の治療がそれらの異常なNKE細胞における所望の応答を産生する可能性を示す1つ以上のデータ点の収集である。応答プロファイルに関連して使用される「応答」は、任意の手段による細胞死(壊死、毒性、アポトーシス等)または異常な細胞の増殖速度の低下のいずれかであってもなくてもよい。応答プロファイルは、100%の精度で応答を予測する必要はない。応答プロファイルは、単一のデータ点であっても、データの収集であってもよい。
任意の方法を用いて、所与の異常なNKE細胞集団の応答プロファイルを同定または決定することができる。例えば、異常な細胞から単離されるDNAまたはRNAの少なくとも一部を配列決定することにより、応答プロファイルを評価することができる。これは、ウイルス、例えば、ヒトパピローマウイルス(HPV)、ヒト免疫不全ウイルス(HIV)が異常な状態を引き起こしている可能性を疑うときに特に有用であり得る。少なくとも1つのデータ点を応答プロファイルに提供するために、DNA/RNAのすべてが配列決定される必要はない。例えば、ポリメラーゼ連鎖反応(PCR)を含む周知の技術を用いて、生成物が作成されるかを決定するために、PCR反応において、例えば、HPVまたはHIVが存在する疑いのあるDNA/RNAに特異的な配列を有するPCRプライマーを用いることは、現在、簡単な手順の問題である。検出可能な生成物が特定のプライマーを用いたPCR反応後に生成されない場合、PCRプライマーが特異的なウイルスの一部が存在しないかもしれないという結論を下すことが可能であり得る。同様に、特定のDNA/RNA配列の不在の決定も、応答プロファイルにおけるデータ点であり得る。この様式で、細胞から単離されたDNA/RNAの全配列の正確な配列は決定されないが、DNAまたはRNAは、本発明の目的のために「配列決定される」。したがって、本明細書で使用される「配列決定」は、単離したDNA/RNAの全ヌクレオチド配列の生成をもたらす場合も、もたらさない場合もある。サザンブロット、ノーザンブロット、RT−PCR、自動配列決定等であるが、これらに限定されない他の方法を用いて、単離したDNA/RNAの配列を決定することもできる。DNA/RNAを配列決定する方法は、当技術分野で周知であり、本明細書で繰り返す必要はない。
同様に、生体外の異常なNKE細胞中に産生され得る1つのmRNAの少なくとも一部の存在または不在を同定することによって、応答プロファイルを評価することができる。上のDNA/RNAの配列を決定するように、mRNAの正確な配列を、細胞から単離される全mRNAにおいて決定する必要はない。単離したmRNAの配列の存在または不在を決定するために用いることができる方法には、ノーザンブロット、RT−PCR、自動配列決定等が含まれるが、これらに限定されない。少なくとも1つのmRNAの存在または不在を同定する方法は、当技術分野で周知であり、本明細書で繰り返す必要はない。
同様に、生体外の異常なNKE細胞中に産生され得る1つのタンパク質の少なくとも一部の存在または不在を同定することによって、応答プロファイルを評価することができる。上のDNA/RNAの配列を決定するように、存在するか、または不在のタンパク質の正確なアミノ酸配列を、全タンパク質において決定する必要はない。単離したタンパク質の配列の存在または不在を決定するために用いることができる方法には、ウエスタンブロット、免疫組織化学的方法、ELISA法等が含まれるが、これらに限定されない。少なくとも1つのタンパク質の存在または不在を同定する方法は、当技術分野で周知であり、本明細書で繰り返す必要はない。タンパク質、例えば、受容体の存在または不在は、細胞が
、例えば、細胞死をもたらし得る特定の治療の影響を受けやすいことを示し得る。
、例えば、細胞死をもたらし得る特定の治療の影響を受けやすいことを示し得る。
生体外の異常なNKE細胞を化学療法剤に供し、化学療法剤に対する細胞の応答を決定することによって、応答プロファイルを評価することができる。本明細書で使用される化学療法剤は、従来の癌治療に限定されないが、化学物質を用いた任意の種類の治療療法を示すために使用される。一実施形態において、細胞に対する治療薬の治療指数を決定することによって、治療薬への応答を評価することができる。治療指数の決定は、当技術分野で一般的であり、単にLD50/EC50の比率であり、LD50は、細胞上での治療薬の平均致死量を表し、EC50は、その半最大用量を表す。治療薬への応答を評価する他の方法には、容量応答曲線の決定、細胞生存曲線の決定等が含まれるが、これらに限定されない。一実施形態において、治療薬への異常なNKE細胞の応答を決定するために使用される治療薬は、後に対象に投与される治療薬と同一または異なる治療薬であってもよい。
本発明は、対象における異常な非ケラチノサイト上皮(NKE)細胞を同定する方法も対象とする。これらの方法は、本発明の細胞培養方法に従って、対象から単離された少なくとも1つの異常な候補NKE細胞を培養することを含む。NKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞が拡大された時点で、細胞の組織起源プロファイルを決定して、異常な候補NKE細胞の可能性のある起源組織を決定することができる。NKE細胞、後期継代NKE細胞、および/または条件的に不死化されたNKE細胞の少なくとも1つの特性を、異常な候補NKE細胞の決定された組織起源プロファイルの組織と同一の組織から得られる正常なNKE細胞の同一の特性と比較することができる。細胞増殖特性、例えば、細胞表面、Matrigel(商標)、または他の三次元表面上でのコロニー形成を含むが、これらに限定されない、異常な細胞または罹患した細胞と正常な細胞との間の任意の差異を用いることができる。疾患した細胞と正常な細胞との間の差異を決定する他の手段は、細胞のプロテオミクスプロファイルの評価、細胞の代謝学的プロファイルの評価、ゲノムプロファイルの評価、および/または疾患した細胞もしくは異常な細胞と正常な細胞との間の差異を強調する他の生物学的アッセイの使用を含むが、これらに限定されない。異常な候補NKE細胞と正常なNKE細胞との間の検出された差異は、異常な候補NKE細胞が、正常なNKE細胞と比較して、異常であることを示す。
応答プロファイルを評価するために使用される同一の方法を用いて、組織起源プロファイルを評価することができる。例えば、異常な候補細胞をmRNA転写産生、タンパク質発現についてアッセイすることができ、組織起源も組織学的評価を介して視覚的に評価することができる。組織起源プロファイルを評価する方法は、免疫組織化学的染色も含む。異常な候補細胞の可能性のある起源組織が樹立された時点で、細胞を同一の組織由来の正常な細胞の少なくとも1つの特性についてアッセイすることができる。例えば、異常な候補細胞が乳房組織に由来すると同定された場合、これらの細胞を、BRCA1および/またはBRCA2変異、HER−2/Neu増殖因子受容体の過剰発現等についてアッセイすることができる。異常な候補細胞がBRCA1変異を有する場合、細胞が異常な乳房細胞であると確定することができる。本発明は、起源組織を同定するために使用されるアッセイの種類にも、正常な細胞と異常である可能性のある細胞の間の差異を決定するために使用されるアッセイの種類にも限定されない。本発明の細胞培養方法は、単離した細胞を拡大するための方法を提供することにより、これらの細胞の同定を可能にする。
本発明は、対象における疾患の進行または疾患の治療を監視する方法も対象とする。本明細書で使用される「進行を監視する」という語句は、NKE細胞および/またはそれらの細胞内容物を、進行もしくは退行の様々なマーカーについてアッセイすることによって、個人における異常な状態が、進行(悪化)しているか、退行(改善)しているか、または停滞したままである(検出可能な変化なし)かを決定するために、対象における異常な状
態が定期的にチェックされることを示すために使用される。これらの治療の有効性を監視するために、監視方法を、異常な状態の他の監視方法または治療レジメンと併せて用いてもよい。したがって、「進行を監視する」ことは、NKE細胞および/またはそれらの細胞内容物を、進行もしくは退行の様々なマーカーについて定期的にアッセイし、かつ対象における経時的な任意の差異を、異常な状態の進行、退行、または停滞と相関させることによって、治療レジメンの有効性を評価することも示すよう意図されている。例えば、本発明の方法を用いて、乳房切除術中または乳房切除術後の対象を監視することができる。具体的には、本方法を用いて、乳房切除術が成功した患者を監視することができ、したがって、本方法を用いて、CTCを単離し、患者のCTCにおいて様々な分析を行うのに十分な数のCTCを生体外で培養および生成し、例えば、フォローアップマンモグラムまたはボディースキャンが必要であるかを決定することができる。監視方法を用いて、最初の治療後に好適なフォローアップ治療レジメンを決定することもできる。例えば、最初の治療後、NKE細胞を生検または単離することができ、培養方法を用いて、十分な数の細胞を生体外で生成し、残りの異常な細胞の遺伝子構造または表現型が新たな治療を保証するのに十分に異なるかを決定することができる。したがって、一実施形態において、本発明は、治療レジメンを個別化する方法を提供する。監視することは、試料が採取される2つの時点でNKE細胞における特定のマーカーのレベルを評価することも含んでもよく、またはそれは、より多くの時点を含んでもよく、所与の対象由来の1つの特定の時点でのマーカーのレベルのうちのいずれかを、それぞれ、1つ以上の他の時点で、同一の対象におけるバイオマーカーのレベルと比較することができる。
態が定期的にチェックされることを示すために使用される。これらの治療の有効性を監視するために、監視方法を、異常な状態の他の監視方法または治療レジメンと併せて用いてもよい。したがって、「進行を監視する」ことは、NKE細胞および/またはそれらの細胞内容物を、進行もしくは退行の様々なマーカーについて定期的にアッセイし、かつ対象における経時的な任意の差異を、異常な状態の進行、退行、または停滞と相関させることによって、治療レジメンの有効性を評価することも示すよう意図されている。例えば、本発明の方法を用いて、乳房切除術中または乳房切除術後の対象を監視することができる。具体的には、本方法を用いて、乳房切除術が成功した患者を監視することができ、したがって、本方法を用いて、CTCを単離し、患者のCTCにおいて様々な分析を行うのに十分な数のCTCを生体外で培養および生成し、例えば、フォローアップマンモグラムまたはボディースキャンが必要であるかを決定することができる。監視方法を用いて、最初の治療後に好適なフォローアップ治療レジメンを決定することもできる。例えば、最初の治療後、NKE細胞を生検または単離することができ、培養方法を用いて、十分な数の細胞を生体外で生成し、残りの異常な細胞の遺伝子構造または表現型が新たな治療を保証するのに十分に異なるかを決定することができる。したがって、一実施形態において、本発明は、治療レジメンを個別化する方法を提供する。監視することは、試料が採取される2つの時点でNKE細胞における特定のマーカーのレベルを評価することも含んでもよく、またはそれは、より多くの時点を含んでもよく、所与の対象由来の1つの特定の時点でのマーカーのレベルのうちのいずれかを、それぞれ、1つ以上の他の時点で、同一の対象におけるバイオマーカーのレベルと比較することができる。
方法は、異常なNKE細胞の試料を対象から得ることと、本発明の培養方法のうちのいずれかに従って異常なNKE細胞を培養して、生体外で異常なNKE細胞集団を産生することとを含む。
「進行を監視する」という語句は、本発明の方法を用いた対象におけるAIB1−△4ペプチドのレベルである。
本発明は、NKE細胞を培養し、かつ/または条件的に不死化されたNKE細胞を生成するためのキットも提供する。キットは、培養容器、湿式形態もしくは乾式形態の培養培地、および/または血清もしくはいくつかの他のカルシウム源等の個々の培地成分を含んでもよい。キットは、凍結フィーダー細胞、細胞を継代するためのトリプシン等の他の化学物質等を含んでも含まなくてもよい。
実施例1−初代ヒト前立腺細胞(HPEC)の採取および培養
十分に説明した上で患者または親の同意を得て、正常なヒト前立腺組織を回収した。トリプシンを用いた確立した手順に従って、初代前立腺細胞懸濁液を調製した。簡潔に、前立腺組織を採取し、トリプシンで消化した。その後、細胞を、(トリプシンを中和するために)10%の血清を含有するDMEM中に懸濁し、即座に遠心分離して、ペレット状の細胞を単離した。そのような前立腺上皮細胞の日常的な単離および培養方法は、参照により組み込まれるCulture of Epithelial Cells(Ian Freshney and Mary G.Freshney,Eds.Wiley−Liss,Inc.)(第2版、2002年)で見出される。
回転させた後、ペレットを除去し、分配し、「F培地」にプレーティングした。F培地を、5%のウシ胎児血清を有する3:1(v/v)比率のF−12およびDMEM(Gibco)、0.4μg/mLのヒドロコルチゾン、5μg/mLのインスリン、8.4ng/mLのコレラ毒素、10ng/mLの上皮増殖因子(EGF)、24μg/mLのアデ
ニン、100U/mLのペニシリン、および100μg/mLのストレプトマイシンを混合することによって調製する。ROCK阻害剤であるY027632を、約10μMの濃度でF培地に添加した。
ニン、100U/mLのペニシリン、および100μg/mLのストレプトマイシンを混合することによって調製する。ROCK阻害剤であるY027632を、約10μMの濃度でF培地に添加した。
細胞を非増殖性フィーダー細胞の存在下でプレーティングした。この具体的な場合において、フィーダー細胞は、ガンマ線照射されたスイス3T3細胞のサブクローンである周知のマウス線維芽細胞フィーダーJ2細胞である。ガンマ線照射またはマイトマイシンCでの処理は、これらの細胞を増殖不能にする。
正常細胞培養条件下(37℃で5%のCO2および標準大気圧)で、細胞を標準の細胞培養容器中で培養した。培地を、増殖速度に応じて2〜3日毎に取り換えた。
細胞がコンフルエンスに達した後、細胞を、参照により組み込まれるChapman,S.et al.,J.Clin.Invest.,120(7):2619−2626(2010)に記載の標準の細胞培養技術を用いて採取および継代した。
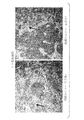
図3Aに示されるように、初期継代HPECは単層に増殖することができ、これらの細胞は増殖し続けた。
実施例2−初代ヒト乳房上皮細胞(HMEC)の採取および培養
十分に説明した上で患者または親の同意を得て、正常なヒト乳房組織を回収した。初代乳房細胞懸濁液を、当技術分野で確立した手順に従って調製した。簡潔に、乳房組織を採取し、ディスパーゼおよびコラゲナーゼ1Aの混合物での消化に供し、続いて、トリプシンで消化した。そのような乳房上皮細胞の日常的な単離および培養方法は、参照により組み込まれるCulture of Epithelial Cells(Ian Freshney and Mary G.Freshney,Eds.Wiley−Liss,Inc.)(第2版、2002年)で見出される。
回転させた後、ペレットを除去し、分配し、「F培地」にプレーティングした。F培地を、5%のウシ胎児血清を有する3:1(v/v)比率のF−12(Gibco)、0.4μg/mLのヒドロコルチゾン、5μg/mLのインスリン、8.4ng/mLのコレラ毒素、10ng/mLの上皮増殖因子(EGF)、24μg/mLのアデニン、100U/mLのペニシリン、および100μg/mLのストレプトマイシンを混合することによって調製する。ROCK阻害剤であるY027632を、約10μMの濃度でF培地に添加した。細胞をガンマ線照射された非増殖性J2細胞の存在下でプレーティングした。
正常細胞培養条件下(37℃で5%のCO2および標準大気圧)で、細胞を標準の細胞培養容器中で培養した。培地を、2〜3日毎に取り換えた。
細胞がコンフルエンスに達した後、細胞を、参照により組み込まれるChapman,S.et al.,J.Clin.Invest.,120(7):2619−2626(2010)に記載の標準の細胞培養技術を用いて採取および継代した。
図3Bに示されるように、初期継代HMECは単層に増殖することができ、これらの細胞は増殖し続けた。
実施例3−様々な条件下におけるHMECおよびHPECの増殖曲線の比較
初代HMECおよびHPECを、図2に記述される4つの異なる条件下で増殖させた。図
2を参照して、PrEGM(Lifeline Cell Technology)は、血清を含有しない前立腺上皮細胞を培養するために特別に設計された合成培地(「Postalife上皮細胞培養培地」)であり、その中で、補助剤が合成であり、明確に定義される。MEGM(Lifeline Cell Technology)は、血清を含有しない乳房上皮細胞を培養するために特別に設計された合成培地(「Brochialife上皮細胞培養培地」)であり、その中で、補助剤が合成であり、明確に定義される。フィーダーは、ガンマ線照射されたJ2マウス線維芽細胞であった。ROCK阻害剤は、最初のプレーティング時およびその後に細胞に適用された10μMの濃度のY27632であった。Y軸は集団倍加であり、X軸は日数である。すべての群の培地を、2〜3日毎に取り換えた。
2を参照して、PrEGM(Lifeline Cell Technology)は、血清を含有しない前立腺上皮細胞を培養するために特別に設計された合成培地(「Postalife上皮細胞培養培地」)であり、その中で、補助剤が合成であり、明確に定義される。MEGM(Lifeline Cell Technology)は、血清を含有しない乳房上皮細胞を培養するために特別に設計された合成培地(「Brochialife上皮細胞培養培地」)であり、その中で、補助剤が合成であり、明確に定義される。フィーダーは、ガンマ線照射されたJ2マウス線維芽細胞であった。ROCK阻害剤は、最初のプレーティング時およびその後に細胞に適用された10μMの濃度のY27632であった。Y軸は集団倍加であり、X軸は日数である。すべての群の培地を、2〜3日毎に取り換えた。
図2は、PrEGM中で増殖した初代前立腺細胞の増殖が約25日後に止まり、MEGM中で増殖した初代乳房細胞の増殖が約50〜60日後に止まったことを示す。ROCK阻害剤を合成培地に添加しても、増殖には影響を及ぼさなかった。ROCK阻害剤を有しないF培地中のフィーダー細胞の存在下で増殖した細胞は、ほぼ同一の増殖速度を有し、すなわち、線の勾配はほぼ同一であったが、フィーダー細胞の存在下で増殖した細胞の増殖は、最終的に止まった。F培地中のフィーダー細胞の存在下で増殖し、かつROCK阻害剤が補充された初代細胞は、増殖し続けた。
実施例4−後期継代HMECおよびHPECの細胞表面マーカー染色
継代29のHPECおよび継代32のHMECを滅菌ガラス製カバースリップ上で増殖させ、4%(重量/体積)のパラホルムアルデヒド中に固定し、製造業者のプロトコルに従って、初代抗体(マウス抗p63、Santa Cruz、sc−863)および二次抗体(Alexa Fluor488ロバ抗マウスIgG)で標識した。細胞中のDNAを、室温で3分間、PBS中の0.5μg/mLのHoescht(33342)で染色し、PBSで3回洗浄した。カバースリップをProLong退色防止封入剤(Invitrogen)を用いて室温で1時間ガラススライド上に載置し、4℃で保管した。63倍対物レンズおよびHammamutsu電荷結合素子カメラを装備したZeiss Axioskop顕微鏡(Carl Zeiss,Inc.,Thornwood,NY)を用いて細胞を撮像した。画像をOpenlab3.0.7ソフトウェアを用いて処理した。図4は、後期継代HMECおよびHPECのいずれも基底細胞マーカーp63を発現した一方で、陰性対照細胞(LnCAP)は発現しなかったことを示す。
実施例5−条件的に不死化されたHMECおよびHPECの形態学的構造
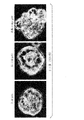
条件的に不死化されたHPEC(継代32)、HMEC(継代36)、および遺伝的に不死化されたHMEC(MycT58A)(継代39)を、Matrigel(登録商標)ベースの三次元培養に移した。
三次元培養の5日目までに、条件的に不死化された正常なHMECおよびHPECが、組織化された多房状の球体構造を形成した一方で、遺伝的に不死化されたmyc変異体乳房細胞は、ランダムな組織化されていない塊を形成した。
三次元培養下で5日後のHMECの代表的なクラスターを、標準の技術を用いてβカテニン染色した。βカテニンは、正常な上皮細胞層を維持するのに必要な接着結合の形成に関与するタンパク質である。HMECは、正にβカテニン染色し、組織化された多房状の球体構造を示した。
実施例6−同一の患者由来の正常な前立腺細胞および前立腺腫瘍細胞の培養および拡大
先に採取および凍結された正常な前立腺細胞および前立腺腫瘍細胞を別個に解凍し、上の実施例1に記載の条件を用いてプレーティングした。図6に示されるように、両方の組の細胞が、解凍後6日目までに、増殖し、拡大し、細胞培養表面上に単層を作成した。
2代継代した後、正常な細胞および腫瘍細胞を、上の実施例5のように三次元細胞培養上にプレーティングした。実施例5の後期継代HPECと同一でないにしても、その後期継代HPECと同様に、解凍した正常なHPECは、組織化された多房状の球体構造を形成し、腫瘍細胞は、ランダムな組織化されていない塊を形成した。
実施例7−条件的に不死化された細胞のテロメラーゼ活性およびテロメア長
全細胞RNAを、TRIzol試薬(Invitrogen)を用いて単離し、製造業者の指示に従ってDNAを含まないキット(Ambion)で処理した。第1鎖cDNAを、RT−PCRのSuperscript第1鎖合成システム(Invitrogen)の指示に従って、2μgの全細胞RNAを用いていくらか改変して合成した。TaqmanリアルタイムQRT−PCRを、hTERT mRNAの定量化のために、参照により組み込まれるFu et al.,Cancer Research 63,7815-
7824,(2003)で以前に報告されたように、プライマーおよびプローブセンスプライマー5’−TGACACCTCACCTCACCCAC−3’、アンチセンスプライマー5’−CACTGTCTTCCGCAAGTTCAC−3’、およびTaqmanプローブ5’−ACCCTGGTCCGAGGTGTCCCTGAG−3’を用いて、Bio−Rad iCycler MyiQ上で行った。ゲノムDNAを、Qiagen DNeasy血液および組織キット(カタログ番号69506)を用いて細胞から抽出した。テロメアの平均長を、参照により組み込まれるCawthon R.,Nucleic
Acids Res.37(3):e21(2009)およびCawthon R.,Nucleic Acids Res.,30(10):e47(2002)に以前に記載されたリアルタイムPCRベースのテロメアアッセイの修正法を用いて評価した。
7824,(2003)で以前に報告されたように、プライマーおよびプローブセンスプライマー5’−TGACACCTCACCTCACCCAC−3’、アンチセンスプライマー5’−CACTGTCTTCCGCAAGTTCAC−3’、およびTaqmanプローブ5’−ACCCTGGTCCGAGGTGTCCCTGAG−3’を用いて、Bio−Rad iCycler MyiQ上で行った。ゲノムDNAを、Qiagen DNeasy血液および組織キット(カタログ番号69506)を用いて細胞から抽出した。テロメアの平均長を、参照により組み込まれるCawthon R.,Nucleic
Acids Res.37(3):e21(2009)およびCawthon R.,Nucleic Acids Res.,30(10):e47(2002)に以前に記載されたリアルタイムPCRベースのテロメアアッセイの修正法を用いて評価した。
簡潔に、テロメア反復コピー数対一遺伝子コピー数(T/S)の比率を、96ウェル形式のBio−Rad IQ5サーモサイクラーを用いて決定した。5ナノグラムのゲノムDNAを、Rio−Rad SYBR Green Super混合物とのPCR反応に供した。テロメア長およびHBG1(単一コピー遺伝子)のプライマーは、Tel−1:5’CGGTTTGTTTGGGTTTGGGTTTGGGTTTGGGTTTGGGTT−3、およびTel−2:5’−GGCTTGCCTTACCCTTACCCTTACCCTTACCCTTACCCT−3’、HBG1 5’−TGTGCTGGCCCATCACTTTG、およびHBG2 5’−ACCAGCCACCACTTTCTGATAGG−3’であった。1サイクルの反応は95℃で5分間進み、続いて、41サイクルの反応は95℃で15秒間、60℃で45秒間進んだ。テロメア反応およびグロビン反応の両方の試料すべてを三重に行った。これらの試料に加えて、それぞれの96ウェルプレートは、Roche TeloキットのゲノムDNA(テロメア長10.4kb)を用いた0、0.2、1、5、25、125ngの6点標準曲線を含有した。平均HBG Ct値を平均テロメアCt値から正規化することによって、それぞれの試料におけるT/S比(dCt)を計算した。
実施例8−非ケラチノサイト上皮細胞の他の種類の培養
肝組織(図8)または乳房組織(図9)を異なる遺伝的背景を有するマウスから回収した。異なる細胞型を説明するために、初代細胞懸濁液を実施例1の方法に従って調製し、当技術分野で確立した手順に従って必要に応じて改変した。簡潔に、組織を採取し、ディス
パーゼおよびコラゲナーゼ1Aの混合物での消化に供し、続いて、トリプシンで消化した。
パーゼおよびコラゲナーゼ1Aの混合物での消化に供し、続いて、トリプシンで消化した。
回転させた後、ペレットを除去し、分配し、「F培地」にプレーティングした。F培地を、5%のウシ胎児血清を有する3:1(v/v)比率のF−12およびDMEM、0.4μg/mLのヒドロコルチゾン、5μg/mLのインスリン、8.4ng/mLのコレラ毒素、10ng/mLの上皮増殖因子(EGF)、24μg/mLのアデニン、100U/mLのペニシリン、および100μg/mLのストレプトマイシンを混合することによって調製する。ROCK阻害剤であるY027632を、約10μMの濃度でF培地に添加した。細胞をJ2フィーダー細胞の存在下でプレーティングした。
正常細胞培養条件下(37℃で5%のCO2および標準大気圧)で、細胞を標準の細胞培養容器中で培養した。培地を、2〜3日毎に取り換えた。
細胞がコンフルエンスに達した後、細胞を、標準の細胞培養技術を用いて採取および継代した。
実施例9−気管支由来のヒト上皮細胞の培養
凍結細胞をLifeline Cell Technologiesから購入し、上記の本明細書で使用されるF培地中で解凍した。ROCK阻害剤であるY027632を、約10μMの濃度でF培地に添加した。細胞をガンマ線照射された非増殖性J2細胞の存在下でプレーティングした。
正常細胞培養条件下(37℃で5%のCO2および標準大気圧)で、細胞を標準の細胞培養容器中で培養した。培地を、2〜3日毎に取り換えた。
実施例10−条件的に不死化されたHPECと正常なHPECとの間の増殖速度の比較
HPECを採取し、実施例1の方法に従って培養する。並行して、別の組のHPECを採取し、フィーダー細胞を用いず、前立腺上皮細胞用に設計された合成細胞培養培地を用いて培養する。この第2の組の条件下で培養される細胞は、「正常なHPEC」と称される。簡潔に、正常なHPECを、明確に定義されたPrEGM血清を含まない培地または25μg/mLのウシ下垂体抽出物および0.2ng/mLの組換え上皮増殖因子が補充されたケラチノサイト血清を含まない(KSF)培地中に存在するフィーダー細胞を用いることなく増殖させる。
組織の消化後、それぞれの群由来の細胞を計数し、75cm2の培養フラスコ中に約1×105でプレーティングする。正常細胞培養条件下(37℃で5%のCO2および標準大気圧)で、細胞を標準の細胞培養容器中で培養する。それぞれの群の培地を、増殖速度に応じて2〜3日毎に取り換える。
数日後、細胞を採取し、標準の細胞培養技術を用いて計数する。PrEGM培地またはKSF培地のいずれかにおいて、条件的に不死化された細胞が正常な細胞よりも多く生成され、この培養条件が現在標準の条件よりもHPECの増殖を刺激することを示す。
実施例11−条件的に不死化されたHMECと正常なHMECとの間の増殖速度の比較
HMECを採取し、実施例2の方法に従って培養する。並行して、別の組のHMECを採取し、フィーダー細胞を用いず、前立腺上皮細胞用に設計された合成細胞培養培地を用い
て培養する。この第2の組の条件下で培養される細胞は、「正常なHMEC」と称される。簡潔に、正常なHMECを、明確に定義されたMEGM血清を含まない培地または25μg/mLのウシ下垂体抽出物および0.2ng/mLの組換え上皮増殖因子が補充されたケラチノサイト血清を含まない(KSF)培地中に存在するフィーダー細胞を用いることなく増殖させる。
て培養する。この第2の組の条件下で培養される細胞は、「正常なHMEC」と称される。簡潔に、正常なHMECを、明確に定義されたMEGM血清を含まない培地または25μg/mLのウシ下垂体抽出物および0.2ng/mLの組換え上皮増殖因子が補充されたケラチノサイト血清を含まない(KSF)培地中に存在するフィーダー細胞を用いることなく増殖させる。
組織の消化後、それぞれの群由来の細胞を計数し、75cm2の培養フラスコ中に約1×105でプレーティングする。細胞を1ウェル当たり合計約10,000個の細胞でプレーティングする。正常細胞培養条件下(37℃で5%のCO2および標準大気圧)で、細胞を標準の細胞培養容器中で培養する。それぞれの群の培地を、2〜3日毎に取り換える。
数日後、細胞を採取し、標準の細胞培養技術を用いて計数する。MEGM培地またはKSF培地のいずれかにおいて、条件的に不死化された細胞が正常な細胞よりも多く生成され、この培養条件が現在標準の条件よりもHMECの増殖を刺激することを示す。
肝細胞、膵臓細胞等であるが、これらに限定されない任意の種類のNKEにおいて、実施例10および実施例11を繰り返すことができる。
実施例12−個人の候補治療薬の同定
再発性喉頭乳頭腫症に16年間罹患する22歳の男性患者をこの研究に選んだ。疾患は、徐々に喉頭を巻き込んだだけでなく、上気道(気管および気管支)、近年では、肺実質にも転移した。患者は、350回以上の手術を受けた。手術以外では、インターフェロン治療(1996〜2010)、メトトレキサート(2001〜03)、病巣内シドフォビル(2007〜2010)、および病巣内アバスチン(2010)を含む複数の治療が失敗に終わった。2008年のCTスキャンは、複数の肺結節が存在したことを示した。2010年の10月までには、検査したそれぞれの肺病巣の大きさが増大していた。最後の外科的介入期間中、転移性腫瘍を除去するために右肺上葉の楔状切除術を行った。切除された標本の病理学的分析は、匙型細胞様異型を有する扁平上皮乳頭腫の存在を示した(図12)。そのような腫瘍の細胞空胞化は、腫瘍が感染性HPVを産生していることを示す。しかしながら、介入時、この腫瘍に関与するHPVの種類は同定されなかった。腫瘍がいくつもの異なる治療モダリティに応答しなかったため、手術後に患者をどのように治療すべきかも不明であった。
手術時に肺腫瘍(および正常な肺組織)の生検を少量得て、組織を処理して細胞株を生成した(図13)。本明細書に記載の細胞培養方法を用いて、正常な組織および腫瘍組織の両方から細胞株を生成し、その後、これらを用いて、どの種類のHPVがこの腫瘍の病原体であるかを決定した。図14に示されるように、DNAを腫瘍細胞から抽出し、特定のプライマーおよびPCRを、危険性の低いHPV(HPV−6、HPV−11)または危険性の高いHPV(HPV−16またはHPV−18)が存在するかについて評価した。危険性の低いHPV−11のDNAのみが検出された。
HPV−11のDNAの一部を配列決定して、ゲノムの初期領域および後期領域のいずれも無傷であるかを決定した。L1後期遺伝子(ウイルスカプシドタンパク質)と同様に、E6初期形質転換遺伝子およびE7初期形質転換遺伝子の両方が存在したことは明らかであった。「プライマー歩行法」を利用して、全L1遺伝子が存在するかについても評価した。L1遺伝子の存在または不在は、抗L1ワクチンをこの患者の治療において使用することができるかを決定するのに有用である。図15のデータは、全L1遺伝子(bp5775〜7001由来)が異常なNKE細胞において無傷であったことを示す。最終的に、
これらの初期遺伝子および後期遺伝子がmRNAに転写されたことが立証された。図16は、初期E6およびE7形質転換遺伝子が転写されたが、L1遺伝子は転写されなかったことを示す。L1タンパク質が産生されなかったため、HPVワクチンの使用(L1タンパク質に基づく)がこの患者に有効ではないという理由から、これは重大な所見であった。したがって、この遺伝分析に基づいて、この腫瘍を治療する代替方法を用いるべきであると決定された。
これらの初期遺伝子および後期遺伝子がmRNAに転写されたことが立証された。図16は、初期E6およびE7形質転換遺伝子が転写されたが、L1遺伝子は転写されなかったことを示す。L1タンパク質が産生されなかったため、HPVワクチンの使用(L1タンパク質に基づく)がこの患者に有効ではないという理由から、これは重大な所見であった。したがって、この遺伝分析に基づいて、この腫瘍を治療する代替方法を用いるべきであると決定された。
DNeasy血液および組織キット(Qiagen)を用いて、全DNAを患者の培養細胞または組織から単離した。Illustra TempliPhi RCAキット(GE Healthcare)を用いて、DNAを増幅した。生成物をBamHIで消化し、pUC19ベクターにクローニングした。プライマー歩行サービス(Primer Walking Services)(Genewiz)を用いてウイルスゲノムを二方向から配列決定した。
Bio−Rad iCycler MyiQ上でTaqMan(商標)キットを用いて、HPV11 L2(センスプライマー5’−TGACACCTCACCTCACCCAC−3’、抗センスプライマー5−CACTGTCTTCCGCAAGTTCAC−3’、およびTaqManプローブ5’−ACCCTGGTCCGAGGTGTCCCTGAG−3’)の定量化のためにプライマーおよびプローブを用いて、リアルタイム定量PCRを行った。それぞれの反応において、ヒトβグロビン遺伝子を内因性の参照として使用した。すべての試料において、リアルタイムPCR反応を三重で行った。製造業者(Bio−Rad)のガイドラインに従って、正規化発現({Delta}{Delta}CT)法を有するiQ5ソフトウェアを用いてHPV DNAのレベルを分析した。
ほとんどのRRP症例はHPV6またはHPV11によって引き起こされる。いくつかの研究は、HPV11が、通常、より攻撃的なウイルスであると考えられており、かつ肺病変を有するRRPの大部分がHPV11によって引き起こされたことを示している。一般的なHPV検出プライマーおよびHPV型特異的プライマーをHPV分類アッセイに用いた。HPV11感染を確認するために、ローリングサークル増幅法(RCA)を用いてエピソームHPV DNAを増幅した。驚いたことに、制限消化は、典型的なHPV11のパターンと一致しなかった。原型HPV11が1つのBamHI部位を有したのに対し、原型HPV11が肺腫瘍細胞から単離されたウイルスゲノムは、2つのBamHI部位を有した。さらに重要なことに、ウイルスゲノムの大きさは、10kb以上であると推定された。ほとんどのHPVが約8kbの大きさのゲノムを有し、原型HPV11の大きさは、7931個の塩基対である。さらなる制限酵素消化は、BamHI以外に、L1−LCR−E6−E7−E1の領域中の酵素AatII、AgeI、FspI、XcmI、およびpPuMIがすべて、ウイルスゲノムを1回のみではなく2回切断することを明らかにした。HPV11のすべての他の単一消化酵素部位がウイルスゲノム上に保持され、ウイルスDNAがL1−LCR−E6−E7−E1の重複を有し得ることを示唆する。重複の詳細を決定するために、全ウイルスゲノムをベクターpUC19にクローニングし、ウイルスゲノムを二方向から配列決定した。配列決定データが立証され、GenBank(受入番号JN644141)に提出された。肺腫瘍細胞中のHPV11は、10,424塩基対長のエピソームゲノムを有した。2493塩基対長の確認された重複配列は、部分L1−LCR−E6−E7−部分E1配列を含んだ。これらの重複配列を、L1(B)、LCR(B)、E6(B)、E7(B)、およびE1(B)と注釈を付けた。患者が変異ウイルスに感染したか、または変異が患者において疾患進行中に起こったかを解明するために、患者の喉頭組織由来のウイルスゲノムを単離した。喉頭由来のウイルスゲノムもクローニングし、配列決定した(GenBank受入番号JN644142)。最初の感染部位のウイルスゲノムは、7933個の塩基対であり、かつ重複を有しないという点において、原型HPV11に非常に類似しており、ウイルスゲノム変異が再発性呼吸乳頭腫の腫
瘍進行を併発したことを示唆する。定量リアルタイムPCRを用いてウイルス力価を測定し、肺腫瘍細胞は、喉頭病巣よりも7倍多くのHPVゲノムを含有した。肺における1細胞当たり約40.16コピーのウイルスDNA、および喉頭における1細胞当たり約5.74コピーのウイルスDNAで、ウイルスゲノムを計算した。
瘍進行を併発したことを示唆する。定量リアルタイムPCRを用いてウイルス力価を測定し、肺腫瘍細胞は、喉頭病巣よりも7倍多くのHPVゲノムを含有した。肺における1細胞当たり約40.16コピーのウイルスDNA、および喉頭における1細胞当たり約5.74コピーのウイルスDNAで、ウイルスゲノムを計算した。
以前の研究は、アルテミシニン誘導体(DHAおよびアーテスネート)ならびにHDAC阻害剤(SAHA)が危険性の高いHPVを発現する子宮頸癌細胞を効率的に死滅させることができることを示した。しかしながら、HPV−6またはHPV−11を含有する樹立された細胞株が存在しないため、これらの阻害剤の危険性の低いHPVを含有する細胞への効果を分析するデータは文献内には存在しない。細胞培養方法は、HPV−11を発現する細胞株の樹立を可能にした。さらに重要なことに、上の阻害剤に対する感受性を評価し、これを同一の患者から単離された正常な肺細胞の感受性と比較するために、この細胞株を使用した(図17)。
患者由来のHPV−11含有腫瘍細胞のDHAおよびSAHAに対する感受性が、正常な肺細胞よりも約100倍高いことは明らかである。例えば、SAHAのEC50は2μMであり、LD50は約200μMである。治療指数は、LD50/EC50と定義され、この場合、それは100である。この値は、優れた治療指数を表し、SAHAが治療用の実行可能な薬剤に相当し得ることを示唆する。DHAの治療指数は100ではないが、DHAにおいても同一のことが言える。シドフォビルは、RRPの治療に使用される最も一般的な薬物である。興味深いことに、シドフォビル(図17A)は、非常に高い濃度(50〜200μM)でも生体外では全く無効であった。
生体外の感受性データに基づいて、患者は、2011年1月にボリノスタット治療を受けた。ボリノスタット治療は、400mg/日の4週間サイクル(3週間継続、1週間中断)から成った。その後のCTスキャンは、新たな病巣が同定されず、比較的小さい病巣が縮小し、かついくつかの比較的大きい病巣も小さくなったという非常に有望な結果を示した。より最近のCTスキャンは、すべての病巣が安定化し、かつ主な副作用が観察されなかったことを示した。したがって、本発明の細胞培養方法の使用は、異常な細胞の応答プロファイルの決定に重要であり、これは、この患者の腫瘍を治療するのに有用であり得る少なくとも2つの化学療法剤の同定を可能にした。本発明の細胞培養方法を用いて、遺伝分析および治療指数を含む応答プロファイルは、生検の1週間以内に作成された。
実施例13−単一針生検由来の細胞株の樹立
別個の実験において、ラット乳房腫瘍由来の針生検標本を本発明の細胞培養方法で使用した。ラット乳房腫瘍細胞は順調に増殖し、細胞株は樹立され、これを生体外研究で使用することができた(図18)。したがって、細胞株を生成するのに十分な数の腫瘍細胞を単一針生検で得た。これは、非常に小さい臨床試料上での遺伝学的研究、生化学的研究、および分子的研究を行う可能性を大いに拡大した。例えば、乳房腫瘍の場合において、針生検の評価は、現在に至るまで、これらの細胞を拡大および培養するいかなる方法も存在しなかったため、現在、試料のH&EおよびIHC染色に限定されている。
本明細書に開示の実施形態の例は、例示目的であり、いかなる様式でも本発明の範囲を限定することを意図していない。
実施例14−冷凍および解凍後の細胞株の樹立
縮小乳房形成患者由来の新たなヒト乳房組織を、最大1〜3mmの大きさで小片または薄片に細分化した。その後、組織片を、−80℃の90%のウシ胎児血清/10%のDMS
O(v/v)/5μMのY−27632中、または液体窒素中で凍結させた。凍結させた組織を37℃で解凍し、ペレット状にし、F培地中に懸濁して、ディスパーゼ/コラゲナーゼで短時間消化した。細胞懸濁液を上述のように培養系に供した。細胞培養の写真(図19)をプレーティングの5日後(上のパネル)および8日後(下のパネル)に撮影した。
O(v/v)/5μMのY−27632中、または液体窒素中で凍結させた。凍結させた組織を37℃で解凍し、ペレット状にし、F培地中に懸濁して、ディスパーゼ/コラゲナーゼで短時間消化した。細胞懸濁液を上述のように培養系に供した。細胞培養の写真(図19)をプレーティングの5日後(上のパネル)および8日後(下のパネル)に撮影した。
実施例15−循環腫瘍細胞(CTC)由来の細胞株の樹立
7mLのヒト血液試料を健常なドナーから取り出し、CPT管(BD Vacutainer(登録商標)CPT(商標)ヘパリンナトリウムNを有する細胞調製管)に注入した。血液試料を回収後した後、LnCAP(前立腺癌細胞株)細胞(総細胞数50〜1000個)をスパイクした。試料を、水平ローター遠心分離機内で、1500〜1800RCF(相対遠心力)で最低15分間、室温で遠心分離した。遠心分離した後、単核細胞および血小板は血漿層真下の白っぽい層内に位置した(CPT管を参照のこと)。細胞層を乱さないように注意して、血漿のおよそ半分を吸引した。その後、細胞層をパスツールピペットで回収し、蓋を有する15mLの「U」底円錐形遠心分離管に移した。ヒト系統細胞枯渇カクテル(LineageCell Depletion Cocktail)(カタログ番号:51−9005225)を管に添加し、混合し、室温で約15分間静置させた。静置させた後、約12mLの1倍PBSを管に添加し、管を約1000rmpで回転させた。上清を吸引した。IMagストレプトアビジン粒子プラスDM(Becton,Dickinson:カタログ番号:51−9003746)をボルテックスし、細胞ペレットを75μLのIMag粒子と完全に混合した。混合物を室温で約30分間インキュベートさせた。インキュベートさせた後、1mLの1倍PBSを管に添加し、混合し、管をBD IMagnet上に6分間設置した。上清を新たな管に移した。BD IMagnetに付着した管内の残り部分を1mLのPBSと再度混合した。この第2の上清を別の新たな管に移した。これらの2つの管を沈降させ、ペレットを3mLのF培地(+Y−27632)に再懸濁し、フィーダー細胞を有する6ウェルプレートに設置した。図22は、スパイクされた腫瘍細胞が血液から回収され、本明細書に記載の培養条件に供した後に、これらの細胞がコロニーを形成し始めたことを示す。
配列番号1:センスプライマー
配列番号2:アンチセンスプライマー
配列番号3:TaqManプローブ
配列番号4:プライマー
配列番号5:プライマー
配列番号6:プライマー
配列番号7:プライマー
配列番号8:センスプライマー
配列番号9:アンチセンスプライマー
配列番号10:TaqManプローブ
配列番号2:アンチセンスプライマー
配列番号3:TaqManプローブ
配列番号4:プライマー
配列番号5:プライマー
配列番号6:プライマー
配列番号7:プライマー
配列番号8:センスプライマー
配列番号9:アンチセンスプライマー
配列番号10:TaqManプローブ
本発明は、非ケラチノサイト上皮細胞の増殖を刺激する方法も対象とし、方法は、フィーダー細胞、非ケラチノサイト上皮細胞、またはこれら両方におけるROCKの活性を阻害しながら、非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養することを含む。そのような条件下での非ケラチノサイト上皮細胞の培養が、非ケラチノサイト上皮細胞を刺激して増殖させるが、他の方法では、細胞は増殖することができない。
項1.
非ケラチノサイト上皮細胞を連続的に培養する方法であって、
a)前記非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び
b)培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、
を含む、前記方法。
項2.
前記非ケラチノサイト上皮細胞は、初代細胞である、上記項1に記載の方法。
項3.
前記非ケラチノサイト上皮細胞は、初代細胞ではない、上記項1に記載の方法。
項4.
前記非ケラチノサイト上皮細胞は、腫瘍細胞である、上記項1に記載の方法。
項5.
前記非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される、上記項2、3、または4に記載の方法。
項6.
前記非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される、上記項5に記載の方法。
項7.
前記カルシウム含有培地は、血清または血清代替物を含む、上記項6に記載の方法。
項8.
前記フィーダー細胞は、増殖性線維芽細胞または非増殖性線維芽細胞である、上記項7に記載の方法。
項9.
前記非増殖性線維芽細胞は、マウス線維芽細胞またはヒト線維芽細胞である、上記項8に記載の方法。
項10.
前記ROCKは、Rhoキナーゼ阻害剤1(ROCK1)、Rhoキナーゼ阻害剤2(ROCK2)、またはこれら両方である、上記項8に記載の方法。
項11.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞を小分子ROCK阻害剤の存在下で培養することを含む、上記項10に記載の方法。
項12.
前記小分子ROCK阻害剤は、Y−27632、HA1100塩酸塩、HA1077、およびGSK429286からなる群から選択される、上記項11に記載の方法。
項13.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞をROCK1、ROCK2、またはこれら両方に特異的なRNA干渉(RNAi)分子の存在下で培養することを含む、上記項10に記載の方法。
項14.
c)ROCKを阻害した後に、前記非ケラチノサイト上皮細胞を継代すること、及び
d)前記継代細胞をROCKが阻害されていない細胞培養環境下に設置すること、
をさらに含む、上記項1に記載の方法。
項15.
前記ROCKが阻害されていない環境は、三次元細胞培養環境である、上記項14に記載の方法。
項16.
前記ROCKが阻害されていない環境は、前記非ケラチノサイトの分化を通常誘導しない環境である、上記項14に記載の方法。
項17.
前記ROCKが阻害されていない環境は、前記非ケラチノサイトの分化を誘導する環境である、上記項14に記載の方法。
項18.
条件的に不死化された非ケラチノサイト上皮細胞集団。
項19.
前記条件的に不死化された非ケラチノサイト上皮細胞は、正常な細胞に由来する、上記項18に記載の細胞集団。
項20.
前記条件的に不死化された非ケラチノサイト上皮細胞は、腫瘍に由来する、上記項18に記載の細胞集団。
項21.
前記条件的に不死化された非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される細胞に由来する、上記項19または20に記載の細胞集団。
項22.
前記条件的に不死化された非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される細胞への分化を促進するその後の環境下に設置された後にそれらに分化することができる、上記項21に記載の細胞集団。
項23.
非ケラチノサイト上皮細胞の増殖を刺激する方法であって、
a)前記非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び
b)培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、を含み、
それによって、前記Rhoキナーゼの活性を阻害しながら前記非ケラチノサイト上皮細胞を培養することが、非ケラチノサイト上皮細胞の増殖を刺激する、
前記方法。
項24.
前記非ケラチノサイト上皮細胞は、初代細胞である、上記項23に記載の方法。
項25.
前記非ケラチノサイト上皮細胞は、初代細胞ではない、上記項23に記載の方法。
項26.
前記非ケラチノサイト上皮細胞は、腫瘍細胞である、上記項23に記載の方法。
項27.
前記非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される上記項24、25、または26に記載の方法。
項28.
前記非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される、上記項27に記載の方法。
項29.
前記カルシウム含有培地は、血清または血清代替物を含む、上記項28に記載の方法。
項30.
前記フィーダー細胞は、非増殖性線維芽細胞である、上記項29に記載の方法。
項31.
前記非増殖性線維芽細胞は、マウス線維芽細胞またはヒト線維芽細胞である、上記項30に記載の方法。
項32.
前記ROCKは、Rhoキナーゼ阻害剤1(ROCK1)、Rhoキナーゼ阻害剤2(ROCK2)、またはこれら両方である、上記項30に記載の方法。
項33.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞を小分子ROCK阻害剤の存在下で培養することを含む、上記項32に記載の方法。
項34.
前記小分子ROCK阻害剤は、Y−27632、HA1100塩酸塩、HA1077、およびGSK429286からなる群から選択される、上記項33に記載の方法。
項35.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞をROCK1、ROCK2、またはこれら両方に特異的なRNA干渉(RNAi)分子の存在下で培養することを含む、
上記項32に記載の方法。
項36.
前記腫瘍細胞は、対象の血液循環から単離された、上記項26に記載の方法。
項37.
前記腫瘍細胞は、対象由来の異常な組織から単離された、上記項26に記載の方法。
項38.
異常な非ケラチノサイト上皮(NKE)細胞の存在を特徴とする状態の治療を必要とする対象の候補治療を同定する方法であって、
a)前記異常なNKE細胞試料を前記対象から得ること、
b)前記異常なNKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外で異常なNKE細胞集団を産生すること、
c)生体外で、前記異常なNKE細胞の少なくとも一部の応答プロファイルを決定すること、及び
d)前記決定された応答プロファイルに基づいて、前記対象の候補治療を同定すること、
を含む、前記方法。
項39.
前記応答プロファイルは、生体外で、前記異常なNKE細胞から抽出されるDNAの少なくとも一部の配列を同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項40.
前記応答プロファイルは、生体外で、前記異常なNKE細胞中に産生される少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項41.
前記応答プロファイルは、生体外で、前記異常なNKE細胞中に産生されない少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項42.
前記応答プロファイルは、生体外で、前記異常なNKE細胞が発現する1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項43.
前記応答プロファイルは、生体外で、前記異常なNKE細胞が発現しない1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項44.
前記応答プロファイルは、生体外で、前記異常なNKE細胞を化学療法剤に供し、かつ、生体外で、前記異常なNKE細胞に対する前記化学療法剤の治療指数を決定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項45.
前記対象由来の前記異常なNKE細胞は、前記対象の血液循環から得られる、上記項38に記載の方法。
項46.
対象における異常な非ケラチノサイト上皮(NKE)細胞を同定する方法であって、
a)前記対象から単離された少なくとも1つの異常な候補NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外で異常な候補NKE細胞集団を産生すること、
b)生体外で、前記異常な候補NKE細胞集団の少なくとも一部の組織起源プロファイルを決定すること、及び
c)前記異常な候補NKE細胞の少なくとも1つの特性を、前記異常な候補NKE細胞の前記決定された組織起源プロファイルの組織と同一の組織から得られる正常なNKE細胞の同一の特性と比較して、前記異常な候補NKE細胞と前記正常なNKE細胞との間に差異があるかを決定すること、を含み、
差異は、前記異常な候補NKE細胞が正常なNKE細胞と比較して異常であることを示す、
前記方法。
項47.
前記異常な候補NKE細胞は、前記対象の血液循環から得られる、上記項46に記載の方法。
項48.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞中に産生される少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項49.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞中に産生されない少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項50.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞が発現する1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項51.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞が発現しない1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項52.
前記組織起源プロファイルは、組織学的に少なくとも部分的に決定される、上記項46に記載の方法。
項53.
自家性標的非ケラチノサイト上皮(NKE)細胞を、さらなる標的NKE細胞を必要とする対象に投与する方法であって、
a)標的NKE細胞の試料を前記対象から得ること、
b)前記標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の自家性標的NKE細胞集団を産生すること、
c)前記生体外の自家性標的NKE細胞集団を回収すること、及び
d)前記自家性標的NKE細胞の回収物を、自家性NKE細胞を必要とする前記対象に投与すること、
を含む、前記方法。
項54.
前記自家性標的NKE細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸および小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、子宮頸部上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、ならびに下垂体細胞からなる群から選択される、上記項53に記載の方法。
項55.
遺伝子改変された自家性標的非ケラチノサイト上皮(NKE)細胞を、さらなる標的NKE細胞を必要とする対象に投与する方法であって、
a)標的NKE細胞の試料を前記対象から得ること、
b)前記標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つ
のRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の標的NKE細胞集団を産生すること、
c)生体外で前記標的NKE細胞集団の少なくとも一部を遺伝子改変すること、
d)遺伝子改変された前記標的NKE細胞を選択すること、
e)前記選択された遺伝子改変された標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の遺伝子改変された自家性標的NKE細胞集団を産生すること、
f)生体外で遺伝子改変された前記自家性標的NKE細胞集団を回収すること、及び
g)前記遺伝子改変された自家性標的NKE細胞の回収物を、さらなる標的NKE細胞を必要とする前記対象に投与すること、
を含む、前記方法。
項56.
前記対象から得られる前記標的NKE細胞は、肝細胞、肺上皮細胞、および膵島細胞からなる群から選択される、上記項55に記載の方法。
項57.
前記対象から得られる前記標的肝細胞は、第VIII因子のコーディング領域を含む導入遺伝子を挿入することによって遺伝子改変される、上記項55に記載の方法。
項58.
前記対象から得られる前記標的肺上皮細胞は、嚢胞性線維症膜コンダクタンス制御因子(CFTR)のコーディング領域を含む導入遺伝子を挿入することによって遺伝子改変される、上記項55に記載の方法。
項1.
非ケラチノサイト上皮細胞を連続的に培養する方法であって、
a)前記非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び
b)培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、
を含む、前記方法。
項2.
前記非ケラチノサイト上皮細胞は、初代細胞である、上記項1に記載の方法。
項3.
前記非ケラチノサイト上皮細胞は、初代細胞ではない、上記項1に記載の方法。
項4.
前記非ケラチノサイト上皮細胞は、腫瘍細胞である、上記項1に記載の方法。
項5.
前記非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される、上記項2、3、または4に記載の方法。
項6.
前記非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される、上記項5に記載の方法。
項7.
前記カルシウム含有培地は、血清または血清代替物を含む、上記項6に記載の方法。
項8.
前記フィーダー細胞は、増殖性線維芽細胞または非増殖性線維芽細胞である、上記項7に記載の方法。
項9.
前記非増殖性線維芽細胞は、マウス線維芽細胞またはヒト線維芽細胞である、上記項8に記載の方法。
項10.
前記ROCKは、Rhoキナーゼ阻害剤1(ROCK1)、Rhoキナーゼ阻害剤2(ROCK2)、またはこれら両方である、上記項8に記載の方法。
項11.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞を小分子ROCK阻害剤の存在下で培養することを含む、上記項10に記載の方法。
項12.
前記小分子ROCK阻害剤は、Y−27632、HA1100塩酸塩、HA1077、およびGSK429286からなる群から選択される、上記項11に記載の方法。
項13.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞をROCK1、ROCK2、またはこれら両方に特異的なRNA干渉(RNAi)分子の存在下で培養することを含む、上記項10に記載の方法。
項14.
c)ROCKを阻害した後に、前記非ケラチノサイト上皮細胞を継代すること、及び
d)前記継代細胞をROCKが阻害されていない細胞培養環境下に設置すること、
をさらに含む、上記項1に記載の方法。
項15.
前記ROCKが阻害されていない環境は、三次元細胞培養環境である、上記項14に記載の方法。
項16.
前記ROCKが阻害されていない環境は、前記非ケラチノサイトの分化を通常誘導しない環境である、上記項14に記載の方法。
項17.
前記ROCKが阻害されていない環境は、前記非ケラチノサイトの分化を誘導する環境である、上記項14に記載の方法。
項18.
条件的に不死化された非ケラチノサイト上皮細胞集団。
項19.
前記条件的に不死化された非ケラチノサイト上皮細胞は、正常な細胞に由来する、上記項18に記載の細胞集団。
項20.
前記条件的に不死化された非ケラチノサイト上皮細胞は、腫瘍に由来する、上記項18に記載の細胞集団。
項21.
前記条件的に不死化された非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される細胞に由来する、上記項19または20に記載の細胞集団。
項22.
前記条件的に不死化された非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される細胞への分化を促進するその後の環境下に設置された後にそれらに分化することができる、上記項21に記載の細胞集団。
項23.
非ケラチノサイト上皮細胞の増殖を刺激する方法であって、
a)前記非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び
b)培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、を含み、
それによって、前記Rhoキナーゼの活性を阻害しながら前記非ケラチノサイト上皮細胞を培養することが、非ケラチノサイト上皮細胞の増殖を刺激する、
前記方法。
項24.
前記非ケラチノサイト上皮細胞は、初代細胞である、上記項23に記載の方法。
項25.
前記非ケラチノサイト上皮細胞は、初代細胞ではない、上記項23に記載の方法。
項26.
前記非ケラチノサイト上皮細胞は、腫瘍細胞である、上記項23に記載の方法。
項27.
前記非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される上記項24、25、または26に記載の方法。
項28.
前記非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される、上記項27に記載の方法。
項29.
前記カルシウム含有培地は、血清または血清代替物を含む、上記項28に記載の方法。
項30.
前記フィーダー細胞は、非増殖性線維芽細胞である、上記項29に記載の方法。
項31.
前記非増殖性線維芽細胞は、マウス線維芽細胞またはヒト線維芽細胞である、上記項30に記載の方法。
項32.
前記ROCKは、Rhoキナーゼ阻害剤1(ROCK1)、Rhoキナーゼ阻害剤2(ROCK2)、またはこれら両方である、上記項30に記載の方法。
項33.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞を小分子ROCK阻害剤の存在下で培養することを含む、上記項32に記載の方法。
項34.
前記小分子ROCK阻害剤は、Y−27632、HA1100塩酸塩、HA1077、およびGSK429286からなる群から選択される、上記項33に記載の方法。
項35.
ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞をROCK1、ROCK2、またはこれら両方に特異的なRNA干渉(RNAi)分子の存在下で培養することを含む、
上記項32に記載の方法。
項36.
前記腫瘍細胞は、対象の血液循環から単離された、上記項26に記載の方法。
項37.
前記腫瘍細胞は、対象由来の異常な組織から単離された、上記項26に記載の方法。
項38.
異常な非ケラチノサイト上皮(NKE)細胞の存在を特徴とする状態の治療を必要とする対象の候補治療を同定する方法であって、
a)前記異常なNKE細胞試料を前記対象から得ること、
b)前記異常なNKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外で異常なNKE細胞集団を産生すること、
c)生体外で、前記異常なNKE細胞の少なくとも一部の応答プロファイルを決定すること、及び
d)前記決定された応答プロファイルに基づいて、前記対象の候補治療を同定すること、
を含む、前記方法。
項39.
前記応答プロファイルは、生体外で、前記異常なNKE細胞から抽出されるDNAの少なくとも一部の配列を同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項40.
前記応答プロファイルは、生体外で、前記異常なNKE細胞中に産生される少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項41.
前記応答プロファイルは、生体外で、前記異常なNKE細胞中に産生されない少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項42.
前記応答プロファイルは、生体外で、前記異常なNKE細胞が発現する1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項43.
前記応答プロファイルは、生体外で、前記異常なNKE細胞が発現しない1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項44.
前記応答プロファイルは、生体外で、前記異常なNKE細胞を化学療法剤に供し、かつ、生体外で、前記異常なNKE細胞に対する前記化学療法剤の治療指数を決定することによって少なくとも部分的に決定される、上記項38に記載の方法。
項45.
前記対象由来の前記異常なNKE細胞は、前記対象の血液循環から得られる、上記項38に記載の方法。
項46.
対象における異常な非ケラチノサイト上皮(NKE)細胞を同定する方法であって、
a)前記対象から単離された少なくとも1つの異常な候補NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外で異常な候補NKE細胞集団を産生すること、
b)生体外で、前記異常な候補NKE細胞集団の少なくとも一部の組織起源プロファイルを決定すること、及び
c)前記異常な候補NKE細胞の少なくとも1つの特性を、前記異常な候補NKE細胞の前記決定された組織起源プロファイルの組織と同一の組織から得られる正常なNKE細胞の同一の特性と比較して、前記異常な候補NKE細胞と前記正常なNKE細胞との間に差異があるかを決定すること、を含み、
差異は、前記異常な候補NKE細胞が正常なNKE細胞と比較して異常であることを示す、
前記方法。
項47.
前記異常な候補NKE細胞は、前記対象の血液循環から得られる、上記項46に記載の方法。
項48.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞中に産生される少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項49.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞中に産生されない少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項50.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞が発現する1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項51.
前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞が発現しない1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、上記項46に記載の方法。
項52.
前記組織起源プロファイルは、組織学的に少なくとも部分的に決定される、上記項46に記載の方法。
項53.
自家性標的非ケラチノサイト上皮(NKE)細胞を、さらなる標的NKE細胞を必要とする対象に投与する方法であって、
a)標的NKE細胞の試料を前記対象から得ること、
b)前記標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の自家性標的NKE細胞集団を産生すること、
c)前記生体外の自家性標的NKE細胞集団を回収すること、及び
d)前記自家性標的NKE細胞の回収物を、自家性NKE細胞を必要とする前記対象に投与すること、
を含む、前記方法。
項54.
前記自家性標的NKE細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸および小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、子宮頸部上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、ならびに下垂体細胞からなる群から選択される、上記項53に記載の方法。
項55.
遺伝子改変された自家性標的非ケラチノサイト上皮(NKE)細胞を、さらなる標的NKE細胞を必要とする対象に投与する方法であって、
a)標的NKE細胞の試料を前記対象から得ること、
b)前記標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つ
のRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の標的NKE細胞集団を産生すること、
c)生体外で前記標的NKE細胞集団の少なくとも一部を遺伝子改変すること、
d)遺伝子改変された前記標的NKE細胞を選択すること、
e)前記選択された遺伝子改変された標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の遺伝子改変された自家性標的NKE細胞集団を産生すること、
f)生体外で遺伝子改変された前記自家性標的NKE細胞集団を回収すること、及び
g)前記遺伝子改変された自家性標的NKE細胞の回収物を、さらなる標的NKE細胞を必要とする前記対象に投与すること、
を含む、前記方法。
項56.
前記対象から得られる前記標的NKE細胞は、肝細胞、肺上皮細胞、および膵島細胞からなる群から選択される、上記項55に記載の方法。
項57.
前記対象から得られる前記標的肝細胞は、第VIII因子のコーディング領域を含む導入遺伝子を挿入することによって遺伝子改変される、上記項55に記載の方法。
項58.
前記対象から得られる前記標的肺上皮細胞は、嚢胞性線維症膜コンダクタンス制御因子(CFTR)のコーディング領域を含む導入遺伝子を挿入することによって遺伝子改変される、上記項55に記載の方法。
Claims (58)
- 非ケラチノサイト上皮細胞を連続的に培養する方法であって、
a)前記非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び
b)培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、
を含む、前記方法。 - 前記非ケラチノサイト上皮細胞は、初代細胞である、請求項1に記載の方法。
- 前記非ケラチノサイト上皮細胞は、初代細胞ではない、請求項1に記載の方法。
- 前記非ケラチノサイト上皮細胞は、腫瘍細胞である、請求項1に記載の方法。
- 前記非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される、請求項2、3、または4に記載の方法。
- 前記非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される、請求項5に記載の方法。
- 前記カルシウム含有培地は、血清または血清代替物を含む、請求項6に記載の方法。
- 前記フィーダー細胞は、増殖性線維芽細胞または非増殖性線維芽細胞である、請求項7に記載の方法。
- 前記非増殖性線維芽細胞は、マウス線維芽細胞またはヒト線維芽細胞である、請求項8に記載の方法。
- 前記ROCKは、Rhoキナーゼ阻害剤1(ROCK1)、Rhoキナーゼ阻害剤2(ROCK2)、またはこれら両方である、請求項8に記載の方法。
- ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞を小分子ROCK阻害剤の存在下で培養することを含む、請求項10に記載の方法。
- 前記小分子ROCK阻害剤は、Y−27632、HA1100塩酸塩、HA1077、およびGSK429286からなる群から選択される、請求項11に記載の方法。
- ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞をROCK1、ROCK2、またはこれら両方に特異的なRNA干渉(RNAi)分子の存在下で培養することを含む、請求項10に記載の方法。
- c)ROCKを阻害した後に、前記非ケラチノサイト上皮細胞を継代すること、及び
d)前記継代細胞をROCKが阻害されていない細胞培養環境下に設置すること、
をさらに含む、請求項1に記載の方法。 - 前記ROCKが阻害されていない環境は、三次元細胞培養環境である、請求項14に記載の方法。
- 前記ROCKが阻害されていない環境は、前記非ケラチノサイトの分化を通常誘導しない環境である、請求項14に記載の方法。
- 前記ROCKが阻害されていない環境は、前記非ケラチノサイトの分化を誘導する環境である、請求項14に記載の方法。
- 条件的に不死化された非ケラチノサイト上皮細胞集団。
- 前記条件的に不死化された非ケラチノサイト上皮細胞は、正常な細胞に由来する、請求項18に記載の細胞集団。
- 前記条件的に不死化された非ケラチノサイト上皮細胞は、腫瘍に由来する、請求項18に記載の細胞集団。
- 前記条件的に不死化された非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される細胞に由来する、請求項19または20に記載の細胞集団。
- 前記条件的に不死化された非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される細胞への分化を促進するその後の環境下に設置された後にそれらに分化することができる、請求項21に記載の細胞集団。
- 非ケラチノサイト上皮細胞の増殖を刺激する方法であって、
a)前記非ケラチノサイト上皮細胞をフィーダー細胞およびカルシウム含有培地の存在下で培養すること、及び
b)培養中に、前記フィーダー細胞、前記非ケラチノサイト上皮細胞、またはこれら両方におけるRhoキナーゼ(ROCK)の活性を阻害すること、を含み、
それによって、前記Rhoキナーゼの活性を阻害しながら前記非ケラチノサイト上皮細胞を培養することが、非ケラチノサイト上皮細胞の増殖を刺激する、
前記方法。 - 前記非ケラチノサイト上皮細胞は、初代細胞である、請求項23に記載の方法。
- 前記非ケラチノサイト上皮細胞は、初代細胞ではない、請求項23に記載の方法。
- 前記非ケラチノサイト上皮細胞は、腫瘍細胞である、請求項23に記載の方法。
- 前記非ケラチノサイト上皮細胞は、扁平上皮細胞、円柱細胞、腺腫細胞、および移行上皮細胞からなる群から選択される請求項24、25、または26に記載の方法。
- 前記非ケラチノサイト上皮細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸上皮細胞、小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、および下垂体細胞からなる群から選択される、請求項27に記載の方法。
- 前記カルシウム含有培地は、血清または血清代替物を含む、請求項28に記載の方法。
- 前記フィーダー細胞は、非増殖性線維芽細胞である、請求項29に記載の方法。
- 前記非増殖性線維芽細胞は、マウス線維芽細胞またはヒト線維芽細胞である、請求項30に記載の方法。
- 前記ROCKは、Rhoキナーゼ阻害剤1(ROCK1)、Rhoキナーゼ阻害剤2(ROCK2)、またはこれら両方である、請求項30に記載の方法。
- ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞を小分子ROCK阻害剤の存在下で培養することを含む、請求項32に記載の方法。
- 前記小分子ROCK阻害剤は、Y−27632、HA1100塩酸塩、HA1077、およびGSK429286からなる群から選択される、請求項33に記載の方法。
- ROCKの活性の阻害は、前記非ケラチノサイト上皮細胞をROCK1、ROCK2、またはこれら両方に特異的なRNA干渉(RNAi)分子の存在下で培養することを含む、請求項32に記載の方法。
- 前記腫瘍細胞は、対象の血液循環から単離された、請求項26に記載の方法。
- 前記腫瘍細胞は、対象由来の異常な組織から単離された、請求項26に記載の方法。
- 異常な非ケラチノサイト上皮(NKE)細胞の存在を特徴とする状態の治療を必要とする対象の候補治療を同定する方法であって、
a)前記異常なNKE細胞試料を前記対象から得ること、
b)前記異常なNKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外で異常なNKE細胞集団を産生すること、
c)生体外で、前記異常なNKE細胞の少なくとも一部の応答プロファイルを決定すること、及び
d)前記決定された応答プロファイルに基づいて、前記対象の候補治療を同定すること、を含む、前記方法。 - 前記応答プロファイルは、生体外で、前記異常なNKE細胞から抽出されるDNAの少なくとも一部の配列を同定することによって少なくとも部分的に決定される、請求項38に記載の方法。
- 前記応答プロファイルは、生体外で、前記異常なNKE細胞中に産生される少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、請求項38に記載の方法。
- 前記応答プロファイルは、生体外で、前記異常なNKE細胞中に産生されない少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、請求項38に記載の方法。
- 前記応答プロファイルは、生体外で、前記異常なNKE細胞が発現する1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、請求項38に記載の方法。
- 前記応答プロファイルは、生体外で、前記異常なNKE細胞が発現しない1つ以上のタン
パク質を同定することによって少なくとも部分的に決定される、請求項38に記載の方法。 - 前記応答プロファイルは、生体外で、前記異常なNKE細胞を化学療法剤に供し、かつ、生体外で、前記異常なNKE細胞に対する前記化学療法剤の治療指数を決定することによって少なくとも部分的に決定される、請求項38に記載の方法。
- 前記対象由来の前記異常なNKE細胞は、前記対象の血液循環から得られる、請求項38に記載の方法。
- 対象における異常な非ケラチノサイト上皮(NKE)細胞を同定する方法であって、
a)前記対象から単離された少なくとも1つの異常な候補NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外で異常な候補NKE細胞集団を産生すること、
b)生体外で、前記異常な候補NKE細胞集団の少なくとも一部の組織起源プロファイルを決定すること、及び
c)前記異常な候補NKE細胞の少なくとも1つの特性を、前記異常な候補NKE細胞の前記決定された組織起源プロファイルの組織と同一の組織から得られる正常なNKE細胞の同一の特性と比較して、前記異常な候補NKE細胞と前記正常なNKE細胞との間に差異があるかを決定すること、を含み、
差異は、前記異常な候補NKE細胞が正常なNKE細胞と比較して異常であることを示す、
前記方法。 - 前記異常な候補NKE細胞は、前記対象の血液循環から得られる、請求項46に記載の方法。
- 前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞中に産生される少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、請求項46に記載の方法。
- 前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞中に産生されない少なくとも1つのmRNAを同定することによって少なくとも部分的に決定される、請求項46に記載の方法。
- 前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞が発現する1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、請求項46に記載の方法。
- 前記組織起源プロファイルは、生体外で、前記異常な候補NKE細胞が発現しない1つ以上のタンパク質を同定することによって少なくとも部分的に決定される、請求項46に記載の方法。
- 前記組織起源プロファイルは、組織学的に少なくとも部分的に決定される、請求項46に記載の方法。
- 自家性標的非ケラチノサイト上皮(NKE)細胞を、さらなる標的NKE細胞を必要とする対象に投与する方法であって、
a)標的NKE細胞の試料を前記対象から得ること、
b)前記標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つ
のRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の自家性標的NKE細胞集団を産生すること、
c)前記生体外の自家性標的NKE細胞集団を回収すること、及び
d)前記自家性標的NKE細胞の回収物を、自家性NKE細胞を必要とする前記対象に投与すること、
を含む、前記方法。 - 前記自家性標的NKE細胞は、前立腺細胞、乳房細胞、肝細胞、膵島細胞、肺上皮細胞、腎細胞、膀胱細胞、胃上皮細胞、大腸および小腸上皮細胞、尿道上皮細胞、精巣上皮細胞、卵巣上皮細胞、子宮頸部上皮細胞、甲状腺細胞、副甲状腺細胞、副腎細胞、胸腺細胞、胆嚢細胞、ならびに下垂体細胞からなる群から選択される、請求項53に記載の方法。
- 遺伝子改変された自家性標的非ケラチノサイト上皮(NKE)細胞を、さらなる標的NKE細胞を必要とする対象に投与する方法であって、
a)標的NKE細胞の試料を前記対象から得ること、
b)前記標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の標的NKE細胞集団を産生すること、
c)生体外で前記標的NKE細胞集団の少なくとも一部を遺伝子改変すること、
d)遺伝子改変された前記標的NKE細胞を選択すること、
e)前記選択された遺伝子改変された標的NKE細胞をフィーダー細胞、カルシウム含有培地、および少なくとも1つのRhoキナーゼ(ROCK)阻害剤の存在下で培養して、生体外の遺伝子改変された自家性標的NKE細胞集団を産生すること、
f)生体外で遺伝子改変された前記自家性標的NKE細胞集団を回収すること、及び
g)前記遺伝子改変された自家性標的NKE細胞の回収物を、さらなる標的NKE細胞を必要とする前記対象に投与すること、
を含む、前記方法。 - 前記対象から得られる前記標的NKE細胞は、肝細胞、肺上皮細胞、および膵島細胞からなる群から選択される、請求項55に記載の方法。
- 前記対象から得られる前記標的肝細胞は、第VIII因子のコーディング領域を含む導入遺伝子を挿入することによって遺伝子改変される、請求項55に記載の方法。
- 前記対象から得られる前記標的肺上皮細胞は、嚢胞性線維症膜コンダクタンス制御因子(CFTR)のコーディング領域を含む導入遺伝子を挿入することによって遺伝子改変される、請求項55に記載の方法。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US41329110P | 2010-11-12 | 2010-11-12 | |
| US61/413,291 | 2010-11-12 | ||
| US201161474901P | 2011-04-13 | 2011-04-13 | |
| US61/474,901 | 2011-04-13 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013538933A Division JP6076258B2 (ja) | 2010-11-12 | 2011-11-11 | 上皮細胞の不死化および使用法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017104097A true JP2017104097A (ja) | 2017-06-15 |
Family
ID=46051584
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013538933A Active JP6076258B2 (ja) | 2010-11-12 | 2011-11-11 | 上皮細胞の不死化および使用法 |
| JP2016226280A Pending JP2017104097A (ja) | 2010-11-12 | 2016-11-21 | 上皮細胞の不死化および使用法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013538933A Active JP6076258B2 (ja) | 2010-11-12 | 2011-11-11 | 上皮細胞の不死化および使用法 |
Country Status (6)
| Country | Link |
|---|---|
| US (5) | US9279106B2 (ja) |
| EP (2) | EP2638149B1 (ja) |
| JP (2) | JP6076258B2 (ja) |
| CA (1) | CA2817712C (ja) |
| DK (1) | DK2638149T3 (ja) |
| WO (1) | WO2012065067A2 (ja) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2817712C (en) * | 2010-11-12 | 2020-03-24 | Georgetown University | Immortalization of epithelial cells and methods of use |
| WO2014082096A1 (en) | 2012-11-26 | 2014-05-30 | The Trustees Of Columbia University In The City Of New York | Method for culture of human and mouse prostate organoids and uses thereof |
| GB2516196B (en) * | 2013-01-25 | 2015-09-09 | Xcell Biosciences Inc | Methods, compositions, kits, and systems for selective enrichment of target cells |
| WO2014172340A1 (en) * | 2013-04-15 | 2014-10-23 | Georgetown University | Immortalization of circulating tumor cells and methods of use |
| WO2015192035A1 (en) * | 2014-06-13 | 2015-12-17 | Georgetown University | Compositions and methods for immortalization of epithelial cells |
| SG11201610857TA (en) | 2014-06-27 | 2017-01-27 | Univ California | Cultured mammalian limbal stem cells, methods for generating the same, and uses thereof |
| KR102276424B1 (ko) | 2014-10-06 | 2021-07-12 | 삼성전자주식회사 | 로-키나제 저해제를 포함하는 세포의 노화를 감소시키기 위한 조성물 및 그의 용도 |
| MX2017012206A (es) | 2015-04-03 | 2018-01-24 | Propagenix Inc | Proliferacion ex vivo de celulas epiteliales. |
| US10100285B2 (en) | 2015-04-03 | 2018-10-16 | Propagenix Inc. | Ex vivo proliferation of epithelial cells |
| CA2998372A1 (en) | 2015-09-11 | 2017-03-16 | Chengkang ZHANG | Ex vivo proliferation of epithelial cells |
| US11753626B2 (en) | 2016-03-09 | 2023-09-12 | Beijing Percans Oncology Co., Ltd. | Tumor cell suspension cultures and related methods |
| US20190151371A1 (en) * | 2016-06-09 | 2019-05-23 | Georgetown University | Process for continuous cell culture of islet cells |
| CN107267446A (zh) * | 2017-07-27 | 2017-10-20 | 广州齐志生物工程设备有限公司 | 一种应用于条件性重编程技术的饲养细胞的处理方法 |
| CN110093310B (zh) * | 2018-01-29 | 2021-07-02 | 中国科学院动物研究所 | 一种将成纤维细胞转化为永生化细胞的方法及其应用 |
| CN110093309B (zh) * | 2018-01-29 | 2021-07-02 | 中国科学院动物研究所 | 一种诱导成纤维细胞转分化为脂肪细胞的方法 |
| CN111344392B (zh) * | 2018-01-29 | 2021-07-30 | 中国科学院动物研究所 | 一种细胞诱导的方法 |
| WO2019199881A1 (en) * | 2018-04-09 | 2019-10-17 | Cedars-Sinai Medical Center | Methods for in vitro expansion of adult tissue stem cells |
| EP3775170A4 (en) * | 2018-04-13 | 2022-01-26 | Shanghai Lide Biotech Co., Ltd. | METHOD OF OBTAINING AN ANIMAL MODEL FROM CONDITIONALLY REPROGRAMMED CELLS AND USE OF THE ANIMAL MODEL FOR THE SCREENING OF ANTITUMORS AGENTS |
| CN112126627B (zh) * | 2020-09-30 | 2022-08-19 | 扬州大学 | 一种犬角膜上皮细胞永生化细胞系的构建方法和应用 |
| WO2023085423A1 (ja) * | 2021-11-12 | 2023-05-19 | Ism株式会社 | 大腸上皮細胞の長期間培養 |
| CN117025503A (zh) * | 2022-05-10 | 2023-11-10 | 上海赛立维生物科技有限公司 | 肝内胆管前体样细胞、细胞制剂及制备方法和应用 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5665710A (en) | 1990-04-30 | 1997-09-09 | Georgetown University | Method of making liposomal oligodeoxynucleotide compositions |
| JP3220180B2 (ja) | 1991-05-23 | 2001-10-22 | 三菱化学株式会社 | 薬剤含有タンパク質結合リポソーム |
| NZ244306A (en) | 1991-09-30 | 1995-07-26 | Boehringer Ingelheim Int | Composition for introducing nucleic acid complexes into eucaryotic cells, complex containing nucleic acid and endosomolytic agent, peptide with endosomolytic domain and nucleic acid binding domain and preparation |
| US5756122A (en) | 1995-06-07 | 1998-05-26 | Georgetown University | Liposomally encapsulated nucleic acids having high entrapment efficiencies, method of manufacturer and use thereof for transfection of targeted cells |
| EP0843555B1 (en) | 1995-08-01 | 2003-08-27 | Isis Pharmaceuticals, Inc. | Liposomal oligonucleotide compositions |
| US7217722B2 (en) | 2000-02-01 | 2007-05-15 | Kirin Beer Kabushiki Kaisha | Nitrogen-containing compounds having kinase inhibitory activity and drugs containing the same |
| JPWO2002100833A1 (ja) | 2001-06-12 | 2004-09-24 | 住友製薬株式会社 | Rhoキナーゼ阻害剤 |
| AU2003202263A1 (en) | 2002-01-10 | 2003-07-30 | Bayer Healthcare Ag | Roh-kinase inhibitors |
| JP4469179B2 (ja) | 2002-01-23 | 2010-05-26 | バイエル ファーマセチカル コーポレーション | Rhoキナーゼ阻害剤としてのピリミジン誘導体 |
| US6943172B2 (en) | 2002-01-23 | 2005-09-13 | Bayer Pharmaceuticals Corporation | Rho-kinase inhibitors |
| TW200306819A (en) | 2002-01-25 | 2003-12-01 | Vertex Pharma | Indazole compounds useful as protein kinase inhibitors |
| GB0206860D0 (en) | 2002-03-22 | 2002-05-01 | Glaxo Group Ltd | Compounds |
| US7645878B2 (en) | 2002-03-22 | 2010-01-12 | Bayer Healthcare Llc | Process for preparing quinazoline Rho-kinase inhibitors and intermediates thereof |
| AU2003220935A1 (en) | 2002-04-03 | 2003-10-13 | Sumitomo Pharmaceuticals Company, Limited. | Benzamide derivatives |
| DE50304983D1 (de) | 2002-10-28 | 2006-10-19 | Bayer Healthcare Ag | Heteroaryloxy-substituierte phenylaminopyrimidine als rho-kinaseinhibitoren |
| ES2374272T3 (es) | 2003-06-19 | 2012-02-15 | Glaxosmithkline Llc | Derivados de 5-(acilamino)indazol como inhibidores de quinasas. |
| CA2530389A1 (en) | 2003-07-02 | 2005-01-13 | Biofocus Discovery Limited | Pyrazine and pyridine derivatives as rho kinase inhibitors |
| US20100016329A1 (en) * | 2008-07-21 | 2010-01-21 | Kaohsiung Medical University | Xanthine-based cyclic gmp-enhancing rho-kinase inhibitor inhibits physiological activities of lung epithelial cell line |
| US8008075B2 (en) * | 2008-11-04 | 2011-08-30 | Viacyte, Inc. | Stem cell aggregate suspension compositions and methods of differentiation thereof |
| ES2743204T3 (es) | 2008-11-04 | 2020-02-18 | Viacyte Inc | Composiciones de suspensión de agregados de células madre y métodos para su diferenciación |
| KR101837080B1 (ko) | 2008-11-20 | 2018-03-09 | 얀센 바이오테크 인코포레이티드 | 마이크로-캐리어 상의 만능 줄기 세포 배양 |
| WO2010065907A2 (en) * | 2008-12-05 | 2010-06-10 | The United States Of America As Represented By The Secretary, Department Of Health And Human Services | Use of a rock inhibitor to sustain primary human keratinocytes in a proliferative state |
| DK2421957T3 (da) * | 2009-04-22 | 2021-01-25 | Viacyte Inc | Cellesammensætninger afledt af dedifferentierede omprogrammerede celler |
| WO2011137485A1 (en) * | 2010-05-05 | 2011-11-10 | Sydney Ivf Limited | Media and methods for cell culture |
| CA2817712C (en) * | 2010-11-12 | 2020-03-24 | Georgetown University | Immortalization of epithelial cells and methods of use |
-
2011
- 2011-11-11 CA CA2817712A patent/CA2817712C/en active Active
- 2011-11-11 EP EP11839723.1A patent/EP2638149B1/en active Active
- 2011-11-11 WO PCT/US2011/060378 patent/WO2012065067A2/en active Application Filing
- 2011-11-11 JP JP2013538933A patent/JP6076258B2/ja active Active
- 2011-11-11 EP EP19174241.0A patent/EP3553168A1/en active Pending
- 2011-11-11 US US13/885,078 patent/US9279106B2/en active Active
- 2011-11-11 DK DK11839723.1T patent/DK2638149T3/da active
-
2014
- 2014-09-26 US US14/498,089 patent/US9657272B2/en active Active
-
2016
- 2016-02-10 US US15/040,770 patent/US10041048B2/en active Active
- 2016-02-10 US US15/040,783 patent/US9951315B2/en active Active
- 2016-11-21 JP JP2016226280A patent/JP2017104097A/ja active Pending
-
2018
- 2018-04-04 US US15/945,718 patent/US11001808B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2012065067A3 (en) | 2013-09-19 |
| EP2638149B1 (en) | 2019-05-15 |
| DK2638149T3 (da) | 2019-08-12 |
| JP6076258B2 (ja) | 2017-02-08 |
| EP2638149A2 (en) | 2013-09-18 |
| EP2638149A4 (en) | 2014-09-17 |
| US20160289643A1 (en) | 2016-10-06 |
| WO2012065067A2 (en) | 2012-05-18 |
| JP2014502151A (ja) | 2014-01-30 |
| US20130309681A1 (en) | 2013-11-21 |
| US20190233798A1 (en) | 2019-08-01 |
| US9951315B2 (en) | 2018-04-24 |
| US9657272B2 (en) | 2017-05-23 |
| US10041048B2 (en) | 2018-08-07 |
| CA2817712A1 (en) | 2012-05-18 |
| US11001808B2 (en) | 2021-05-11 |
| EP3553168A1 (en) | 2019-10-16 |
| US20150099267A1 (en) | 2015-04-09 |
| US9279106B2 (en) | 2016-03-08 |
| US20160289644A1 (en) | 2016-10-06 |
| CA2817712C (en) | 2020-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11001808B2 (en) | Immortalization of epithelial cells and methods of use | |
| US11530385B2 (en) | Hormone responsive tissue culture system and uses thereof | |
| Mou et al. | Dual SMAD signaling inhibition enables long-term expansion of diverse epithelial basal cells | |
| Liu et al. | ROCK inhibitor and feeder cells induce the conditional reprogramming of epithelial cells | |
| US8936939B2 (en) | Hormone responsive tissue culture system and uses thereof | |
| JP2002520594A (ja) | 不死化ヒトケラチノサイト細胞系統 | |
| JP2014508540A (ja) | 正常ヒト管状卵巣上皮およびヒト管状卵巣腫瘍由来の細胞を培養するための組成物および方法 | |
| JP2010500878A (ja) | ポリマー膜を用いた幹細胞とフィーダー細胞の共培養方法 | |
| WO2019006132A1 (en) | ORGANOIDS DERIVED FROM A SINGLE PULMONARY CELL | |
| WO2014172340A1 (en) | Immortalization of circulating tumor cells and methods of use | |
| Liu et al. | Conditionally immortalized brown preadipocytes can switch between proliferative and differentiated states | |
| WO2014185692A1 (ko) | 3차원 콜라겐 겔 환경에서 라이실-tRNA 합성효소가 발현하거나 발현하지 않도록 조절된 세포 또는 회전타원체로 덩어리진 세포 배양을 이용한 암 전이 억제제의 스크리닝 방법 | |
| CA2237391A1 (en) | Novel method of culturing human epithelial cells for the identification of cancer therapeutics and diagnostics | |
| US20190161737A1 (en) | Process for continuous cell culture of cancer cells and cancer stem cells | |
| US20190151371A1 (en) | Process for continuous cell culture of islet cells | |
| WO2015192035A1 (en) | Compositions and methods for immortalization of epithelial cells | |
| US20230167414A1 (en) | Methods for isolating and culturing tumor cells | |
| US20200283726A1 (en) | Process for continuous cell culture of gpscs | |
| Gemenetzidis | The role of FOXM1 in oral squamous cell carcinoma | |
| KR20150133314A (ko) | 상피성 종양세포의 세포간 결합을 조절하는 물질의 모니터링 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170905 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20171204 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180327 |