JP2016190855A - ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 - Google Patents
ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 Download PDFInfo
- Publication number
- JP2016190855A JP2016190855A JP2016108936A JP2016108936A JP2016190855A JP 2016190855 A JP2016190855 A JP 2016190855A JP 2016108936 A JP2016108936 A JP 2016108936A JP 2016108936 A JP2016108936 A JP 2016108936A JP 2016190855 A JP2016190855 A JP 2016190855A
- Authority
- JP
- Japan
- Prior art keywords
- leptin
- pharmaceutical composition
- composition according
- adipose tissue
- tissue atrophy
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/2264—Obesity-gene products, e.g. leptin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/155—Amidines (), e.g. guanidine (H2N—C(=NH)—NH2), isourea (N=C(OH)—NH2), isothiourea (—N=C(SH)—NH2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/74—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving hormones or other non-cytokine intercellular protein regulatory factors such as growth factors, including receptors to hormones and growth factors
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Hematology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Urology & Nephrology (AREA)
- Obesity (AREA)
- Biomedical Technology (AREA)
- Endocrinology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pathology (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Microbiology (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Biotechnology (AREA)
- Gastroenterology & Hepatology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Emergency Medicine (AREA)
- Virology (AREA)
- Vascular Medicine (AREA)
Abstract
Description
本発明は、一部をNIHからの財源によって支援された。政府は本発明にて一部の権利を有する。
(関連した出願の相互参照)
本出願実用特許は、2001年10月22日出願の米国仮出願番号60/336394(Depaoli et al.)に対して優先権を主張し、その開示内容は引用により本明細書に包含される。
(発明の属する技術分野)
本発明は、ヒト脂肪組織萎縮症の処置のためのレプチン、レプチン類似体、およびレプチン誘導体の治療的使用の分野に関連する。
以下の実施例は、HIV関連脂肪組織萎縮症症候群(HIV−LS)の進行が、体脂肪の蓄積、欠損または再分配に寄与する血清中の低下レプチンによって影響を受け得ることを示す。
ヒトにおける脂肪組織萎縮症を処置するためにレプチンを用いることの効果を決定するため、様々な形態の脂肪組織萎縮症と診断された9人の女性患者に対し、レプチン置換治療も行った。本研究の患者は、米国およびヨーロッパにて多数の内科医によって調査された。適格性として、患者には、脂肪組織萎縮症に関連する低レベル(男性にて3.0ng/ml未満、女性にて4.0ng/ml未満の血清レプチン濃度として定義する)を有すること、および以下の少なくとも1つの代謝異常を伴うことを要求した。:それは、(1)米国糖尿病連合協会による糖尿病の存在(Peters et al. 1998参照。);(2)空腹時血清トリグリセリド濃度が200mg/dLより高い;および/または(3)空腹時血清インスリン濃度が300μU/mlより高い、である。脂肪組織萎縮症の診断は、当業者によって周知の臨床上の観点に基づいて行われた。
本研究は、糖尿病、消化および腎臓疾患(NIDDK)の国立研究所の糖尿病部門、およびダラスのテキサス大学南西(UT Southwestern)医療センターにて、予期される非盲検研究として設計された。Amgen Inc.(Thousand Oaks, CA)は、試みとして組換えメチオニルヒトレプチン(組換えレプチン)を提供した。各々の患者の応答を、各自の基準状態と比較した。脂肪組織萎縮症症候群の希少性および臨床特性の変動性のため、無作為化された偽薬処置した対照群を含むことは実現不可能であった。NIDDKおよびテキサス大学南西医療センターの施設内倫理委員会は、本研究を承認した。書面による同意書は、患者または法定後見人から得られた。
血清グルコースおよびトリグリセリドレベルは、自動日立機器(Boehringer Mannheim, Indianapolis, IN)およびベックマン機器(Beckman, CA)を使用し、標準の方法によって決定した。ヘモグロビンAicは、イオン交換高圧液体クロマトグラフィー(バイオ・ラッド・ラボラトリーズ社、ヘラクレス、CA)によって決定した。血清遊離脂肪酸(FFA)レベルは、業務用キット(Wako,Richmond, VA)にて決定した。血清インスリンレベルは、Abbott Imx機器 (Abbott Park, IL)および業務用キット(Linco Research, Inc. , St. Charles, MO)によって提供された試薬を用いた免疫分析によって決定した。血清レプチンレベルは、業務用キット(Linco Research, Inc. St. Charles, MO)を用いた免疫分析によって決定した。
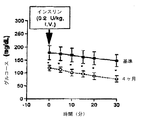
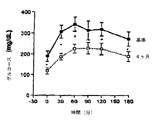
安静時エネルギー消費は、Deltatrac設備(Sensormedics, Yorba Linda, CA)を用いて測定した。試験は、午前6時および8時の間に起きた安静時の患者にて8時間以上の一晩の断食後に行った。経口グルコース耐性試験は、75gのブドウ糖を用いた一晩の断食後に行った。血清グルコースは、グルコース負荷の−10、0、30、60、90、120および180分に測定した。
測定値は平均±SEMとして示す。様々な研究期間にて研究変数を比較するため、反復手段分散分析を用いた。トリグリセリド濃度および測定したK定数のような非対称データは、対数変換した。対応のあるt検定は、適用可能な限り様々な時間ポイントと基準データを比較するために用いた。経口グルコース耐性試験期間中の血漿グルコース濃度は、繰り返された因子としてモデル化されたテスト期間での研究期間および時間の2−因子分散分析を用いて比較した。平均間の相違の95パーセントの信頼区間は、分散分析および平均間の相違に由来した(Hanh et al.,1991)。変換は、p<0.05で統計的に有意であると考えられた。同時比較のための調節は、特別な優先仮説の統計分析のために行われなかった。
基準患者の特性
本研究にて9人中8人は糖尿病であり、全員が高脂血症であった(表1)。すべての糖尿病患者は、本研究前に薬物療法を受け(表1、2)、4人の患者は、脂肪管理のための薬物療法を受けていた(表1)。糖尿病患者の平均HbAicは、9.1±0.5%(通常:<5.6%)であった。平均トリグリセリドレベルは、1405mg/dLに上がっていた(範囲:322〜7420mg/dL;通常範囲:35〜155mg/dL)[16mmol/L、範囲:3.6〜8.7mmol/L]。遊離脂肪酸(FFA)レベルは、通常の上限のおよそ3倍に増加していた(1540±407μmol/L;通常:350〜550μmol/L)。7人のNIH患者のうち6人は、超音波での脂肪肝および物理的試験での肥大肝臓を有していた。患者のうち3人は肝臓生検を経験し、3人のうち2人は、組織病理学の基準に基づいた非アルコール性脂肪性肝炎と診断された。(Manton et al. , 2000; Berasain et al. , 2000; Luyckx, et al., 2000)。
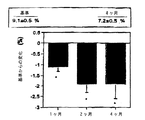
本研究にて処置した最初の患者(NIH−1)は最も重度に罹患しており、彼女の経過は、他のすべての可能性のある治療が中止された後でさえこの集団におけるレプチン置換の劇的な効果を示すことにて示唆的である。この患者は、健康に生まれたが10および12歳の間に脂肪欠損を経験した。彼女は13歳で重度高トリグリセリド血症および14歳で糖尿病を発現した。彼女は、トリグリセリドレベルが一貫して10000mg/dLより高く(113nmol/Lより高く)、9.5%のHbAicを備えた糖尿病に罹患した15歳の時にNIH臨床センターに来院した。彼女は、散在性の有痛性発疹性皮膚黄色腫を身体および骨盤の縁まで及ぶ巨大肝腫の全体に持っていた。週間血漿交換治療およびオーリスタット(Orlistat)を、高トリグリセリド血症を軽減するために加えた(図1A)(Bolan et al)。他の顕著な臨床特徴は、大変な食欲(彼女は3200kcal/日を越えて食べることを報告した)および予測値の180%である2010kcal/日の非常に高い安静時代謝率を含んでいた。4か月以上の組換えレプチンは、血漿交換および糖尿病薬物を中止したための高トリグリセリド血症および高血糖症における著しい進歩的な改良を起こした(図1A)。代謝パラメーターにおける改善には、皮膚黄色腫の消失が伴った。さらに、彼女の肝臓容量は、(図1Bにて示される基準の4213mLから、4か月後の2644mLまで)40%減少した。
レプチン治療の開始に先立って、8人の糖尿病性脂肪組織萎縮症患者は弱い代謝制御を有していた。4か月のレプチン置換治療で、HbAicは、平均1.9パーセンテージポイント(95%CI、1.1〜2.7%、p=0.0012)減少した(図2)。患者の個々の反応は、表3に示す。減少または中止の基準抗糖尿病治療にもかかわらず血糖制御が改善したことは特記できる(表2)。
基準平均肝臓容量は、3097±391mLであった(年齢および性別一致の正常体重の個人の比較にて約4倍上昇した)。レプチンは、基準から平均28%(CI、20〜36%)肝臓容量を減少させた。肝臓容量の平均減少は、987mL(CI、546〜1428mL、p=0.0024)であった。肝臓サイズにおける改善は、肝機能検査法における改善に関連していた。基準アラニンアミノ基転移酵素濃度は、4か月の終端にて66±16U/Lから24±4U/Lに減少した(p=0.023)。同様に、血清アスパラギン酸アミノ基転移酵素濃度は、4か月の終端にて基準および21±2U/Lで53±12U/Lであった(p=0.03)。
自己報告された日々の摂取カロリーは、2680±250kcal/日の基準から1600±150kcal/日に非常に減少した(p=0.005、n=7)。正確な安静時代謝率1920±150 kcal/日から1580±80kcal/日に並列の減少があった(p=0.003、n=9)。
注入部位での皮膚反応は、報告または観察されなかった。所定の生化学的または血液パラメーターでの副作用効果の傾向はなかった。患者NIH−1は、第1投与量後に吐き気および嘔吐の発作を有していた。患者NIH−6は、洗浄に関連する第2投与量後に高血圧症の悪化を有していた。
本研究では、レプチン置換が、リポジストロフィおよびレプチン欠損に罹患した患者の1群にて明瞭および劇的な代謝上の利益を与えた。本研究期間にて、組換えレプチンとの置換が、HbAicを1.9パーセンテージポイント改善させ、これは糖尿病人口(英国PDS、1998年)の〜22%に網膜症を発現する関係リスクを減少させると推定される。さらに、トリグリセリドレベルは60%に減少し、これは母集団全体中の心臓血管事象のための相対的な危険を35〜65%に減少させると推定される(Kreisberg、1998年;Garg、2000年)。
脂肪組織萎縮性糖尿病におけるカロリー摂取の制限は、グルコースおよび脂質異常を改善すると認識されている(Trygstad et al.,1977)。しかしながら、患者は自らの食欲のために食事制限に従うことが困難である。レプチンは、明白にこれらの患者における食物摂取を減少させた。代謝パラメーター上の減少した食物摂取の貢献を決定するため、制限した研究を患者NIH−1に行った。病院では、彼女は、9日間レプチンを使用中止し、カロリー摂取を使用中止前のレベルに固定した。安定したダイエット中にもかかわらず、彼女の空腹時インスリン、トリグリセリドおよびグルコース濃度は48時間以内に増加した。これらの観察は、レプチンが食物摂取に対する効果と無関係に、インスリン感受性およびトリグリセリド代謝に対して効果を有することを示す。レプチン投与ありの場合またはなしの場合の脂肪組織萎縮症マウスにおけるペア摂食実験(pair-feeding)を用いた同様のデータが報告されている(Shimomura et al., 1999;Ebihara et al., 2001)。
脂肪組織萎縮症の様々なマウスモデルは、脂肪組織の不存在がこの症候群におけるインスリン抵抗性の原因であることを示唆した(Burant et al., 1997; Moitra et al., 1998; Shimomura et al., 2000)。脂肪組織萎縮症マウスにて脂肪組織の移植が劇的にインスリン抵抗性を改善し、代謝制御を改善するという証明は、本仮説を強く支持する(Gavrilova et al., 2000)。しかしながら、なぜ全身インスリン感受性を維持するために脂肪組織が必要なのかは、不明なままであった。上述のシモムラ(Shimomura)らと共に、前記考察した観察および結果は、全身インスリン感受性における脂肪組織の調節作用の大部分がレプチンを介して作用することを示唆する。
Zuckerラットにおけるレプチン投与が、脂質蓄積部位として機能する様々な器官にて脂肪症の補正を導くことが報告された;それは、肝臓または心臓細胞の島細胞のような部位にてである(Unger, 1995; Unger et al., 1999)。脂肪細胞の外側の脂質蓄積は、トリグリセリドを貯蔵する最大容積に達した脂肪細胞に起因する現象に波及するかもしれない。リポジストロフィでは、これらの器官が脂質を貯蔵できるただ一つの部位である。リポジストロフィを備えたマウスにおけるレプチン処置は、肝臓トリグリセリド貯蔵に劇的な低下を引き起こす。並行して、リポジストロフィに罹患したヒトにおけるレプチン治療が、肝臓容積の著しく、極めて大きな減少を引き起こす。
脂肪組織が内分泌器官であるという概念は、レプチンの発見によって強く支持された。レプチンは、脳、肝臓、筋肉、脂肪および膵臓を含む代謝の主要な器官にて直接および/または間接的両方の効果がある。レプチンは確かに、唯一の循環型脂肪細胞シグナルではない。例えば、他の脂肪細胞ホルモンとしては、筋肉および肝臓にて脂肪酸化を引き起こすことにおいて重要に見える脂肪細胞特異的組成物関連タンパク質(ACRP)30/アディポネクチン/AdipoQがある(Yamauchi et al., 2001;Fruebis et al., 2001; Berg et al., 2001)。脂肪細胞の欠損が、既知および未だ発見されていないすべての脂肪誘導シグナルの欠損に帰着するのであれば、従って脂肪の欠失によって特徴づけられた症候群で見られた異常の多くに寄与する。本研究は、脂肪欠損の状態における脂肪誘導ホルモンを置換する代謝効果から判断する最初のヒト研究である。脂肪組織萎縮症に関連して見られた代謝異常に対して(それだけではないが)レプチン欠損が主に貢献することが明らかとなった。そのため、本研究は、ヒトにおけるレプチン置換治療を考慮する重要な理由を強調する;それは、すなわち重度のリポジストロフィである。
成熟組換えメチオニルヒトレプチンのためのアミノ酸配列は、配列番号1として本明細書に示し、ここでマチュアなタンパク質の第1のアミノ酸がバリン(1位)で、メチオニル残基が−1位(本明細書にてrHu−レプチン1−146、配列番号1と定義する)に位置する。
米国特許番号 US5,521,283;US 5,525,705;US 5,532,336;US 5,552,522;US 5,552,523;US 5,552,524;US 5,554,727;US 5,559,208;US 5,563,243;US 5,563,244;US 5,563,245;US 5,567,678;US 5,567,803;US 5,569,743;US 5,569,744;US 5,574,133;US 5,580,954;US 5,594,101;US 5,594,104;US 5,605,886;US 5,614,379;US 5,691,309;US 5,719,266(Eli Lilly and Company);
PCT WO96/23513;WO96/23514;WO96/23515;WO96/23516;WO96/23517;WO96/23518;WO96/23519;WO96/34111;WO 96 37517;WO96/27385;WP 97/00886;EP 725078;EP 725079;EP 744408;EP 745610;EP 835879 (Eli Lilly and Company);
PCT WO96/22308 (Zymogenetics);
PCT WO96/31526 (Amylin Pharmaceuticals, Inc.)
PCTWO96/34885;WO 97/46585 (SmithKline Beecham, PLC);
PCT WO 96/35787 (Chiron Corporation);
PCT WO97/16550 (Bristol-Myers Squibb);
PCT WO 97/20933 (Schering Corporation)
EP 736599 (Takeda) ;
EP 741187 (F. Hoffman La Roche)がある。
標準酵素結合免疫吸着検定法(ELISA)は、本発明の1つの実施例による脂肪組織萎縮症患者の血清中のレプチンレベルを決定するために用いることができる。ELISA法は、血清からのレプチンを捕らえるために精製ラットモノクローナル抗−rmetHu−レプチン抗体を用いることができる。ホースラディッシュペルオキシダーゼ結合親和性精製ラビット抗−rmetHu−レプチンポリクローナル抗体も捕獲したレプチンを検知するために用いられることができる。これらの抗体を用いた該分析の検知の限界は、0.5−0.8ng/mlの範囲にあるかもしれない。ある抗体が使用されたかもしれないが、好ましい抗体は天然のヒトレプチンと特異的に反応し、5ng/ml血清以下のレプチン量を検知するために感度がよい。
Claims (28)
- チアゾリジンジオン、フィブラート、スタチンおよびメトホルミンからなる群から選択される少なくとも1つの化合物を含むプロテアーゼ阻害物質、および配列表番号1および2からなる群から選択されるレプチンタンパク質の組合せを含む、脂肪組織萎縮症を処置するための医薬組成物。
- 脂肪組織萎縮症に関連する代謝異常を処置するための請求項1記載の医薬組成物。
- 脂肪組織萎縮症が後天性型の疾患である、請求項1記載の医薬組成物。
- 脂肪組織萎縮症がHIV陽性患者における、請求項1記載の医薬組成物。
- 後天性型の脂肪組織萎縮症が、HIV陽性患者における高活性抗レトロウイルス剤療法(HAART)に関連する、請求項3記載の医薬組成物。
- レプチン、レプチン類似体またはレプチン誘導体を有効成分とする、脂肪組織萎縮症を処置するための医薬組成物。
- さらに医薬的に許容される担体を含む、請求項6記載の医薬組成物。
- さらに医薬的に許容される希釈剤を含む、請求項6記載の医薬組成物。
- 4ng/ml以下のレプチンレベルを有する患者に投与するための、請求項6記載の医薬組成物。
- 2ng/ml以下のレプチンレベルを有する患者に投与するための、請求項9記載の医薬組成物。
- 脂肪組織萎縮症が後天性型である、請求項6記載の医薬組成物。
- HIV陽性患者に投与するための、請求項11記載の医薬組成物。
- 後天性型の脂肪組織萎縮症が、HIV陽性患者における高活性抗レトロウイルス剤療法(HAART)に関連する、請求項12記載の医薬組成物。
- 脂肪組織萎縮症が遺伝型である、請求項6記載の医薬組成物。
- 脂肪組織萎縮症の遺伝型が先天性全身脂肪組織萎縮症である、請求項14記載の医薬組成物。
- 脂肪組織萎縮症が代謝異常を含む、請求項6記載の医薬組成物。
- 代謝異常が高血糖症、異常脂質血症、高脂血症、高コレステロール血症、高トリグリセリド血症、アテローム性動脈硬化症、血管再狭窄およびインスリン抵抗性からなる群から選択される、請求項16記載の医薬組成物。
- 代謝異常が糖尿病である、請求項16記載の医薬組成物。
- 代謝異常がインスリン抵抗性である、請求項17記載の医薬組成物。
- 代謝異常が高トリグリセリド血症である、請求項17記載の医薬組成物。
- 脂肪組織萎縮症が脂肪肝である、請求項6記載の医薬組成物。
- 脂肪組織萎縮症が脂肪組織の分配の異常である、請求項6記載の医薬組成物。
- 皮下投与用である、請求項6記載の医薬組成物。
- レプチンが配列表番号1および2の組換えヒトレプチンからなる群から選択される、請求項23記載の医薬組成物。
- さらに医薬的に許容される担体を含む、請求項24記載の医薬組成物。
- さらに医薬的に許容される希釈剤を含む、請求項24記載の医薬組成物。
- レプチンが組換えヒトレプチンである、請求項6記載の医薬組成物。
- 組換えヒトレプチンが配列表番号1である、請求項27記載の医薬組成物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US33639401P | 2001-10-22 | 2001-10-22 | |
| US60/336,394 | 2001-10-22 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010137501A Division JP2010209114A (ja) | 2001-10-22 | 2010-06-16 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018141461A Division JP6764906B2 (ja) | 2001-10-22 | 2018-07-27 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2016190855A true JP2016190855A (ja) | 2016-11-10 |
Family
ID=23315890
Family Applications (7)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003537565A Pending JP2005506994A (ja) | 2001-10-22 | 2002-10-22 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2010137501A Pending JP2010209114A (ja) | 2001-10-22 | 2010-06-16 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2014160718A Pending JP2014224142A (ja) | 2001-10-22 | 2014-08-06 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2016108936A Withdrawn JP2016190855A (ja) | 2001-10-22 | 2016-05-31 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2016153889A Pending JP2016190872A (ja) | 2001-10-22 | 2016-08-04 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2018141461A Expired - Lifetime JP6764906B2 (ja) | 2001-10-22 | 2018-07-27 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2019232609A Withdrawn JP2020055868A (ja) | 2001-10-22 | 2019-12-24 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Family Applications Before (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003537565A Pending JP2005506994A (ja) | 2001-10-22 | 2002-10-22 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2010137501A Pending JP2010209114A (ja) | 2001-10-22 | 2010-06-16 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2014160718A Pending JP2014224142A (ja) | 2001-10-22 | 2014-08-06 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Family Applications After (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016153889A Pending JP2016190872A (ja) | 2001-10-22 | 2016-08-04 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2018141461A Expired - Lifetime JP6764906B2 (ja) | 2001-10-22 | 2018-07-27 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| JP2019232609A Withdrawn JP2020055868A (ja) | 2001-10-22 | 2019-12-24 | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Country Status (14)
| Country | Link |
|---|---|
| US (7) | US7183254B2 (ja) |
| EP (2) | EP1444516B1 (ja) |
| JP (7) | JP2005506994A (ja) |
| AT (1) | ATE475094T1 (ja) |
| AU (1) | AU2002359288B2 (ja) |
| CA (1) | CA2464277C (ja) |
| DE (1) | DE60237100D1 (ja) |
| DK (2) | DK1444516T3 (ja) |
| ES (2) | ES2418954T3 (ja) |
| MX (1) | MXPA04003773A (ja) |
| PL (1) | PL214862B1 (ja) |
| PT (1) | PT2219031E (ja) |
| SI (1) | SI2219031T1 (ja) |
| WO (1) | WO2003034996A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016190872A (ja) * | 2001-10-22 | 2016-11-10 | アムジェン インコーポレイテッド | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| US11535659B2 (en) | 2010-09-28 | 2022-12-27 | Amryt Pharmaceuticals Inc. | Engineered polypeptides having enhanced duration of action |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2286837A3 (en) | 2004-11-01 | 2013-09-04 | Amylin Pharmaceuticals, LLC | Treatment of obesity and obesity related diseases |
| US8227408B2 (en) * | 2005-09-07 | 2012-07-24 | Neurotez, Inc. | Leptin as an anti-amyloidogenic biologic and methods for delaying the onset and reducing Alzheimer's disease-like pathology |
| US20070066512A1 (en) * | 2005-09-12 | 2007-03-22 | Dominique Verhelle | Methods and compositions using immunomodulatory compounds for the treatment of disorders associated with low plasma leptin levels |
| WO2008048691A2 (en) * | 2006-10-18 | 2008-04-24 | Amylin Pharmaceuticals, Inc. | Use of leptin for treating post-lipectomy ectopic fat deposition and other post-lipectomy associated disorders |
| AU2009248914A1 (en) | 2008-05-21 | 2009-11-26 | Neurotez, Inc. | Methods for Treating Neurodegenerative Disorders Related to Neurofibrillary Tangles |
| WO2009149379A2 (en) * | 2008-06-05 | 2009-12-10 | Regents Of The University Of Michigan | Use of leptin for the treatment of fatty liver diseases and conditions |
| CN102300581B (zh) | 2008-11-04 | 2016-12-21 | 尼古拉斯·泰萨普塞蒂斯 | 用于治疗因神经原纤维缠结和β淀粉状蛋白的积聚引起的进行性认知功能障碍的瘦蛋白组合物和方法 |
| US20110218141A1 (en) * | 2010-03-03 | 2011-09-08 | Hamrick Mark W | Leptin therapy to increase muscle mass and to treat muscle wasting conditions |
| JP6040464B2 (ja) | 2011-07-08 | 2016-12-07 | アエゲリオン・ファーマシューティカルズ・インコーポレイテッドAegerion Pharmaceuticals, Inc. | 作用持続期間が増大し、免疫原性が減少した操作されたポリペプチド |
| RU2650646C2 (ru) | 2012-09-27 | 2018-04-16 | Дзе Чилдрен'З Медикал Сентер Корпорейшн | Соединения, предназначенные для лечения ожирения, и способы их применения |
| EP3010529B1 (en) | 2013-06-21 | 2020-05-06 | Millendo Therapeutics SAS | Use of unacylated ghrelin, fragments and analogs thereof as antioxidant |
| PT3074033T (pt) | 2013-11-26 | 2019-02-08 | Childrens Medical Ct Corp | Compostos para o tratamento de obesidade e métodos de utilização dos mesmos |
| WO2015153933A1 (en) | 2014-04-03 | 2015-10-08 | The Children's Medical Center Corporation | Hsp90 inhibitors for the treatment of obesity and methods of use thereof |
| JP2015205846A (ja) * | 2014-04-22 | 2015-11-19 | 出光興産株式会社 | レプチン分泌促進剤 |
| TWI580690B (zh) * | 2014-08-25 | 2017-05-01 | The use of multidipins for the manufacture of pharmaceutical compositions for in vivo multipurpose effects | |
| TWI752920B (zh) | 2015-10-12 | 2022-01-21 | 美商再生元醫藥公司 | 活化瘦素受體的抗原結合蛋白 |
| EP3509624B1 (en) | 2016-09-12 | 2023-08-09 | Amryt Pharmaceuticals Inc. | Methods of detecting anti-leptin neutralizing antibodies |
| AU2019249273B2 (en) | 2018-04-06 | 2026-02-05 | Regeneron Pharmaceuticals, Inc. | Methods of treatment using a leptin receptor agonist antibody |
| GB202100311D0 (en) * | 2021-01-11 | 2021-02-24 | Univ Court Of The Univ Of Aberdeen | Treatment for Lipodystrophy |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996040912A1 (en) * | 1995-06-07 | 1996-12-19 | Amgen Inc. | Ob protein compositions and method |
| JPH09506264A (ja) * | 1994-08-17 | 1997-06-24 | ザ ロックフェラー ユニバーシティ | 体重のモジュレーター、対応する核酸およびタンパク質、ならびにそれらの診断および治療用途 |
| JP2001199887A (ja) * | 1999-11-10 | 2001-07-24 | Takeda Chem Ind Ltd | 体重増加抑制剤 |
| JP2010209114A (ja) * | 2001-10-22 | 2010-09-24 | Amgen Inc | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Family Cites Families (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5827734A (en) | 1995-01-20 | 1998-10-27 | University Of Washington | Materials and methods for determining ob protein in a biological sample |
| US5552523A (en) | 1995-01-31 | 1996-09-03 | Eli Lilly And Company | Anti-obesity proteins |
| US5563244A (en) | 1995-01-31 | 1996-10-08 | Eli Lilly And Company | Anti-obesity proteins |
| US5563245A (en) | 1995-01-31 | 1996-10-08 | Eli Lilly And Company | Anti-obesity proteins |
| US5567678A (en) | 1995-01-31 | 1996-10-22 | Eli Lilly And Company | Anti-obesity proteins |
| US5605886A (en) | 1995-01-31 | 1997-02-25 | Eli Lilly And Company | Anti-obesity proteins |
| US5567803A (en) | 1995-01-31 | 1996-10-22 | Eli Lilly And Company | Anti-obesity proteins |
| US5580954A (en) | 1995-01-31 | 1996-12-03 | Eli Lilly And Company | Anti-obesity proteins |
| US5563243A (en) | 1995-01-31 | 1996-10-08 | Eli Lilly And Company | Anti-obesity proteins |
| US5594104A (en) | 1995-01-31 | 1997-01-14 | Eli Lilly And Company | Anti-obesity proteins |
| US5559208A (en) | 1995-01-31 | 1996-09-24 | Eli Lilly And Company | Anti-obesity proteins |
| US5569744A (en) | 1995-01-31 | 1996-10-29 | Eli Lilly And Company | Anti-obesity proteins |
| US5569743A (en) | 1995-01-31 | 1996-10-29 | Eli Lilly And Company | Anti-obesity proteins |
| CA2211664A1 (en) | 1995-01-31 | 1996-08-08 | Eli Lilly And Company | Anti-obesity proteins |
| US5574133A (en) | 1995-01-31 | 1996-11-12 | Eli Lilly And Company | Anti-obesity proteins |
| US5691309A (en) | 1995-01-31 | 1997-11-25 | Eli Lilly And Company | Anti-obesity proteins |
| US5521283A (en) | 1995-01-31 | 1996-05-28 | Eli Lilly And Company | Anti-obesity proteins |
| US5554727A (en) | 1995-01-31 | 1996-09-10 | Eli Lilly And Company | Anti-obesity proteins |
| US5525705A (en) | 1995-01-31 | 1996-06-11 | Eli Lilly And Company | Anti-obesity proteins |
| US5532336A (en) | 1995-01-31 | 1996-07-02 | Eli Lilly And Company | Anti-obesity proteins |
| US5552522A (en) | 1995-01-31 | 1996-09-03 | Eli Lilly And Company | Anti-obesity proteins |
| CA2211656A1 (en) | 1995-01-31 | 1996-08-08 | Margret B. Basinski | Anti-obesity proteins |
| US5552524A (en) | 1995-01-31 | 1996-09-03 | Eli Lilly And Company | Anti-obesity proteins |
| US5594101A (en) | 1995-03-03 | 1997-01-14 | Eli Lilly And Company | Anti-obesity proteins |
| US5719266A (en) | 1995-03-17 | 1998-02-17 | Eli Lilly And Company | Anti-obesity proteins |
| EP0736599A3 (en) | 1995-04-03 | 1996-12-11 | Takeda Chemical Industries Ltd | The rat obesity gene, its gene product and its production |
| AU5539596A (en) | 1995-04-06 | 1996-10-23 | Amylin Pharmaceuticals, Inc. | Anti-obesity agents |
| US5614379A (en) | 1995-04-26 | 1997-03-25 | Eli Lilly And Company | Process for preparing anti-obesity protein |
| EP0741187A2 (en) | 1995-05-05 | 1996-11-06 | F. Hoffmann-La Roche Ag | Recombinant obese (Ob) proteins |
| GB9509164D0 (en) | 1995-05-05 | 1995-06-28 | Smithkline Beecham Plc | Novel compounds |
| CA2218529A1 (en) | 1995-05-08 | 1996-11-14 | Chiron Corporation | Nucleic acids for treating obesity |
| JP2001501906A (ja) | 1995-05-26 | 2001-02-13 | イーライ・リリー・アンド・カンパニー | Rhesus obタンパク質およびdna |
| WO1997000886A1 (en) | 1995-06-22 | 1997-01-09 | Eli Lilly And Company | Obesity protein intermediates and their preparation and use |
| CN1195293A (zh) * | 1995-06-30 | 1998-10-07 | 伊莱利利公司 | 治疗糖尿病的方法 |
| DE69631605T2 (de) | 1995-08-17 | 2005-01-05 | Amgen Inc., Thousand Oaks | Verfahren zur verringerung und zur erhaltung von verringerten blutspiegeln von lipiden mittels zubereitungen von ob-proteinen |
| WO1997016550A1 (en) | 1995-11-02 | 1997-05-09 | Bristol-Myers Squibb Company | Polypeptide fragments derived from the obese gene product |
| DK0866720T3 (da) | 1995-11-22 | 2004-06-14 | Amgen Inc | OB-protein til forögelse af mager kropsmasse |
| AU1406497A (en) | 1995-12-06 | 1997-06-27 | Schering Corporation | Mutational variants of mammalian ob gene proteins |
| WO1997038014A1 (en) | 1996-04-04 | 1997-10-16 | Amgen Inc. | Fibulin pharmaceutical compositions and related methods |
| EP0912609A2 (en) | 1996-06-06 | 1999-05-06 | Smithkline Beecham Plc | Fragments of leptin (ob protein) |
| US5922678A (en) * | 1996-06-28 | 1999-07-13 | Eli Lilly And Company | Methods for treating diabetes |
| JP2001501177A (ja) | 1996-08-30 | 2001-01-30 | アムジエン・インコーポレーテツド | Obタンパク質受容体をアップレギュレートすることによりobタンパク質に対する個体の感受性を増加させる方法 |
| AU4582597A (en) | 1996-10-11 | 1998-05-11 | Eli Lilly And Company | Therapeutic proteins |
| JP4175668B2 (ja) | 1996-12-20 | 2008-11-05 | アムジエン・インコーポレーテツド | Ob融合タンパク質組成物および方法 |
| EP1118001A1 (en) | 1998-10-02 | 2001-07-25 | Amgen Inc. | Method to determine a predisposition to leptin treatment |
| CA2359840C (en) * | 1999-02-12 | 2012-10-23 | Amgen Inc. | Glycosylated leptin compositions and related methods |
| US6258932B1 (en) * | 1999-08-09 | 2001-07-10 | Tripep Ab | Peptides that block viral infectivity and methods of use thereof |
| US6899892B2 (en) * | 2001-12-19 | 2005-05-31 | Regents Of The University Of Minnesota | Methods to reduce body fat |
-
2002
- 2002-10-22 EP EP02793811A patent/EP1444516B1/en not_active Expired - Lifetime
- 2002-10-22 DK DK02793811.7T patent/DK1444516T3/da active
- 2002-10-22 JP JP2003537565A patent/JP2005506994A/ja active Pending
- 2002-10-22 ES ES10165256T patent/ES2418954T3/es not_active Expired - Lifetime
- 2002-10-22 MX MXPA04003773A patent/MXPA04003773A/es active IP Right Grant
- 2002-10-22 CA CA2464277A patent/CA2464277C/en not_active Expired - Lifetime
- 2002-10-22 AU AU2002359288A patent/AU2002359288B2/en not_active Expired
- 2002-10-22 AT AT02793811T patent/ATE475094T1/de not_active IP Right Cessation
- 2002-10-22 PL PL374301A patent/PL214862B1/pl unknown
- 2002-10-22 PT PT101652568T patent/PT2219031E/pt unknown
- 2002-10-22 WO PCT/US2002/033875 patent/WO2003034996A2/en not_active Ceased
- 2002-10-22 DE DE60237100T patent/DE60237100D1/de not_active Expired - Lifetime
- 2002-10-22 ES ES02793811T patent/ES2350924T3/es not_active Expired - Lifetime
- 2002-10-22 EP EP10165256.8A patent/EP2219031B1/en not_active Expired - Lifetime
- 2002-10-22 SI SI200231031T patent/SI2219031T1/sl unknown
- 2002-10-22 DK DK10165256.8T patent/DK2219031T3/da active
-
2003
- 2003-07-18 US US10/623,189 patent/US7183254B2/en active Active
-
2006
- 2006-11-29 US US11/606,805 patent/US20070099836A1/en not_active Abandoned
-
2010
- 2010-06-16 JP JP2010137501A patent/JP2010209114A/ja active Pending
-
2011
- 2011-05-09 US US13/103,294 patent/US8318666B2/en not_active Expired - Fee Related
-
2012
- 2012-11-05 US US13/669,324 patent/US20130190225A1/en not_active Abandoned
-
2014
- 2014-08-06 JP JP2014160718A patent/JP2014224142A/ja active Pending
-
2016
- 2016-05-13 US US15/154,749 patent/US20170095535A1/en not_active Abandoned
- 2016-05-31 JP JP2016108936A patent/JP2016190855A/ja not_active Withdrawn
- 2016-08-04 JP JP2016153889A patent/JP2016190872A/ja active Pending
-
2018
- 2018-07-27 JP JP2018141461A patent/JP6764906B2/ja not_active Expired - Lifetime
- 2018-11-19 US US16/195,661 patent/US20190321447A1/en not_active Abandoned
-
2019
- 2019-12-24 JP JP2019232609A patent/JP2020055868A/ja not_active Withdrawn
-
2020
- 2020-02-05 US US16/782,773 patent/US20200268853A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09506264A (ja) * | 1994-08-17 | 1997-06-24 | ザ ロックフェラー ユニバーシティ | 体重のモジュレーター、対応する核酸およびタンパク質、ならびにそれらの診断および治療用途 |
| WO1996040912A1 (en) * | 1995-06-07 | 1996-12-19 | Amgen Inc. | Ob protein compositions and method |
| JP2001199887A (ja) * | 1999-11-10 | 2001-07-24 | Takeda Chem Ind Ltd | 体重増加抑制剤 |
| JP2010209114A (ja) * | 2001-10-22 | 2010-09-24 | Amgen Inc | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
Non-Patent Citations (2)
| Title |
|---|
| BERG, J.P. ET AL., EUROPEAN JOURNAL OF ENDOCRINOLOGY, vol. 142, JPN6008063676, 2000, pages 114 - 116, ISSN: 0003531505 * |
| SHIMOMURA, I. ET AL., NATURE, vol. 401, JPN6008063678, 1999, pages 73 - 76, ISSN: 0003531506 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016190872A (ja) * | 2001-10-22 | 2016-11-10 | アムジェン インコーポレイテッド | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 |
| US11535659B2 (en) | 2010-09-28 | 2022-12-27 | Amryt Pharmaceuticals Inc. | Engineered polypeptides having enhanced duration of action |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6764906B2 (ja) | ヒト脂肪組織萎縮症を処置するためのレプチンの使用および該処置のための素因決定方法 | |
| AU2002359288A1 (en) | Use of leptin for treating human lipoatrophy and method of determining predisposition to said treatment | |
| Gorden et al. | The clinical uses of leptin | |
| JP2004331674A (ja) | 胃腸の運動性を調節する方法 | |
| JP2010540519A (ja) | 肥満症治療における肥満細胞安定化薬 | |
| Triplitt et al. | Pioglitazone and alogliptin combination therapy in type 2 diabetes: a pathophysiologically sound treatment | |
| Barnett et al. | Rosiglitazone in Type 2 diabetes mellitus: an evaluation in British Indo‐Asian patients | |
| Zinman | PPARγ agonists in type 2 diabetes: how far have we come in ‘preventing the inevitable’? A review of the metabolic effects of rosiglitazone. | |
| Scarpace et al. | Leptin antagonist reveals an uncoupling between leptin receptor signal transducer and activator of transcription 3 signaling and metabolic responses with central leptin resistance | |
| Desouza et al. | Management of the insulin resistance syndrome | |
| Del Prato et al. | Rosiglitazone plus metformin: combination therapy for Type 2 diabetes | |
| Agent | PrACH-Pioglitazone | |
| Tablets et al. | Pr ACT PIOGLITAZONE | |
| Agent | Pr PRO-PIOGLITAZONE | |
| Agent | PrRAN™-PIOGLITAZONE | |
| KR20220110506A (ko) | 비만 치료를 위한 글루카곤 및 glp-1 공동-작용제를 사용하는 조합 치료법 | |
| Tablets et al. | Pr MINT-PIOGLITAZONE | |
| Tablets et al. | RAN-Pioglitazone | |
| Agent | PrJamp-Pioglitazone | |
| Agent | PrVAN-Pioglitazone | |
| Agent | PrSANDOZ PIOGLITAZONE | |
| Agent | Pr AURO-PIOGLITAZONE |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160629 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160629 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170404 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170626 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170901 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180327 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180727 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20180904 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20181026 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20191129 |