JP2012502005A - イソqc阻害剤の使用 - Google Patents
イソqc阻害剤の使用 Download PDFInfo
- Publication number
- JP2012502005A JP2012502005A JP2011525553A JP2011525553A JP2012502005A JP 2012502005 A JP2012502005 A JP 2012502005A JP 2011525553 A JP2011525553 A JP 2011525553A JP 2011525553 A JP2011525553 A JP 2011525553A JP 2012502005 A JP2012502005 A JP 2012502005A
- Authority
- JP
- Japan
- Prior art keywords
- isoqc
- alkyl
- imidazol
- inhibitor
- dione
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 *C(*)(C(N(*)C1=*)=*)N1c(cc1)cc2c1[n]cn2 Chemical compound *C(*)(C(N(*)C1=*)=*)N1c(cc1)cc2c1[n]cn2 0.000 description 10
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4178—1,3-Diazoles not condensed 1,3-diazoles and containing further heterocyclic rings, e.g. pilocarpine, nitrofurantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/433—Thidiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Physical Education & Sports Medicine (AREA)
- Rheumatology (AREA)
- Immunology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Virology (AREA)
- Pain & Pain Management (AREA)
- Communicable Diseases (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Molecular Biology (AREA)
- Transplantation (AREA)
- Endocrinology (AREA)
- Reproductive Health (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
【選択図】なし
Description
さらに、本発明は、該阻害剤の使用に基づいた診断キット及び方法に関する。
その上、「イソQC」又は「QPCTL」と呼ばれるQCのイソ酵素が存在することが、最近WO 2008/034891に示された。
これらの目的は、本発明によって解決される。
本発明は、イソグルタミニルペプチドシクロトランスフェラーゼ(イソQC)の阻害剤、並びに下記から選択される炎症性疾患からなる群から選択される疾患又は障害の治療及び/又は予防のための該阻害剤の使用に関する
a.慢性及び急性炎症、例えば関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症の結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症。
(酵素阻害剤)
可逆的酵素阻害剤は、競合的阻害剤、非競合的可逆的阻害剤、ゆっくりと結合し又は密に結合する阻害剤、遷移状態類似体、及び多基質類似体を含む。
i)活性部位以外の部位(アロステリックな結合部位)に結合する
ii)酵素の高次構造上の変化を生じさせて、触媒活性を低下又は停止させる。
i)阻害剤と酵素の間の平衡にゆっくりと到達する競合的阻害剤であり、
ii)(kオンが、緩徐である)おそらく酵素、又は阻害剤において生じなければならない高次構造上の変化に起因して
a)たいてい遷移状態類似体であり
b)酵素濃度と同様の濃度において有効であり(nM以下のKD値)
c)kオフ値が非常に低いため、この種の阻害剤は、「ほぼ」不可逆的である。
2つ以上の基質を含む反応については、2つ以上の基質に似ている構造的特徴を含む競合的阻害剤又は遷移状態類似体を設計することができる。
活性部位に配向した不可逆的阻害剤(競合的不可逆的阻害剤)は、酵素(可逆的な特異的結合)によって、続いて共有結合形成によって認識され、かつ、
i)基質、遷移状態、又は産物に構造的に類似し、薬物と標的酵素の間で特異的に相互作用することができ、
ii)反応性官能基(例えば、求核試薬、-COCH2Br)を含み、共有結合を形成することができる。
競合的酵素阻害剤が、本発明では最も好ましい。
遊離化合物とこれらの塩又は溶媒和物の形態の化合物の間の緊密な関係からみて、化合物又は阻害剤が、それぞれ、この状況において引用されるときはいつでも、対応する塩又は溶媒和物も意図されるが、ただし、このようなものが本状況下で可能であり、又は適切であることを条件とする。
溶媒和物の例には、水和物を含む。
更にまた、阻害剤の結晶形のいくつかは、多形として存在してもよく、それ自体、本発明に含まれることが意図される。加えて、化合物のいくつかは、水との溶媒和物(すなわち、水和物)、又は普遍的な有機溶媒との溶媒和物を形成するであろうし、このような溶媒和物も、また本発明の範囲内に包含されることが意図される。これらの塩を含む阻害剤はまた、それらの水和物の形態で得ることもでき、又はこれらの結晶化のために使用されるその他の溶媒を含む。
本発明は、その範囲内に本発明の阻害剤のプロドラッグを更に含む。一般に、このようなプロドラッグは、インビボで所望の治療活性のある阻害剤に容易に変換できる阻害剤の機能的誘導体であるだろう。従って、これらの場合、本発明の治療の方法において、「投与すること」という用語には、項目に挙げた阻害剤のうちの1つ以上に関するプロドラッグバージョンだが、対象への投与後にインビボで上記の指定した阻害剤に変換するプロドラッグバージョンを用いての、記載した種々の障害の治療を包含するであろう。例えば、適切なプロドラッグ誘導体の選択、及び製造のための従来の手順は、例えばH. Bundgaardの文献(「プロドラッグの設計("Design of Prodrugs")」, Elsevier, 1985)、及び特許出願DE 198 28 113、DE 198 28 114、WO99/67228、及びWO99/67279に説明されており、これらは、引用により本明細書中に完全に組み込まれている。
本発明の阻害剤の製造のための方法のいずれの間にも、関係する分子のいずれかに対して感応基若しくは反応基を保護することが必要であり及び/又は望ましいかもしれない。これは、引用により本明細書中に完全に組み込まれているJ.F.W. McOmieの文献(「有機化学における保護基(Protective Groups in Organic Chemistry)」, Plenum Press, 1973);並びにT.W. Greene及びP.G.M. Wutsの文献(「有機合成における保護基(Protective Groups in Organic Synthesis)」, John Wiley & Sons, 1991)において説明した保護基などの、従来の保護基によって達成してもよい。保護基は、当該技術分野において公知の方法を使用して、都合の良いその後の段階で除去してもよい。
本明細書及び特許請求の範囲を通じて、表現「アルキル」は、特に限定しない限りは、C1-12アルキル基、適切にはC1-6アルキル基、例えばC1-6アルキル基、例えばC1-4アルキル基を意味する。アルキル基は、直鎖又は分岐鎖であってよい。適切なアルキル基には、例えばメチル、エチル、プロピル(例えばn-プロピル及びイソプロピル)、ブチル(例えばn-ブチル、iso-ブチル、sec-ブチル及びtert-ブチル)、ペンチル(例えばn-ペンチル)、ヘキシル(例えばn-ヘキシル)、ヘプチル(例えばn-ヘプチル)及びオクチル(例えばn-オクチル)を含む。例えば、「アルコキシ」、「ハロアルキル」及び「チオアルキル」の表現において、表現「アルキ(alk)」は、「アルキル」の定義に従い解釈されるべきである。典型的なアルコキシ基には、メトキシ、エトキシ、プロポキシ(例えばn-プロポキシ)、ブトキシ(例えばn-ブトキシ)、ペントキシ(例えばn-ペントキシ)、ヘキソキシ(例えばn-ヘキソキシ)、ヘプトキシ(例えばn-ヘプトキシ)及びオクトキシ(例えばn-オクトキシ)を含む。典型的なチオアルキル基には、メチルチオ-を含む。典型的なハロアルキル基には、フルオロアルキル、例えばCF3を含む。
表現「アルキレン」は、式-(CH2)n-の鎖を意味し、式中nは、特に限定しない限りは、整数であり、例えば2〜5である。
表現「-アルキルヘテロアリール」は、特に限定しない限りは、アルキレン部分、例えばC1-4アルキレン部分を介して結合されているヘテロアリール残基を示す。
用語「アミノ」は、-NH2基を指す。
用語「フェニルによって置換されたフェニル」はビフェニルを指す。
ベンズイミダゾリルが、下記式:
このことは、すべての同様の状況に準用して適用する。
例えば懸濁液、エリキシル剤、及び溶液などの液体経口製剤については、適切な担体、及び添加物には、水、グリコール、油、アルコール、調味料、保存料、着色料等を都合よく含んでいてもよく;例えば散剤、カプセル剤、ジェルキャップ剤、及び錠剤などの固体経口製剤については、適切な担体及び添加物には、デンプン、糖、希釈剤、造粒剤、潤滑剤、結合剤、崩壊剤等を含む。
崩壊剤には、デンプン、メチルセルロース、寒天、ベントナイト、キサンタンゴム等を含むが、これらに限定されるわけではない。
本明細書で使用される用語「アンタゴニスト」は、QPCTLに結合した場合に、QPCTLの生物学的又は免疫学的活性の効果の量又は時間を低下させる阻害剤分子、例えば、該ぺプチダーゼの酵素活性を低下させて、QPCTL基質のN末端におけるGlu残基又はGln残基を環化させる阻害剤分子を指す。アンタゴニストには、タンパク質、核酸、炭水化物、抗体、又はQPCTLの効果を低下させるその他の分子を含んでもよく;例えば、該アンタゴニストには、QPCTLに結合し、かつ競合的又は非競合的な種類の機序によってQPCTLを失活させる低分子及び有機化合物を含んでもよい。QPCTLの低分子阻害剤が好ましい。QPCTLの競合的低分子阻害剤が最も好ましい。
本明細書で使用される用語「QC」は、グルタミニル-ペプチドシクロトランスフェラーゼ(QPCT)と同義のグルタミニルシクラーゼ(QC)を含み;その一方で、イソQCはQC様酵素を指し、グルタミニル-ペプチドシクロトランスフェラーゼ様タンパク質(QPCTL)と同義である。QC及びQC様酵素は、「QC活性」又は「イソQC活性」としてさらに定義される類似の酵素活性を有する。しかしながら、QC様酵素は基本的に、その分子構造がQCとは異なり得る。
「QC活性」は、グルタミニルシクラーゼ(QC、QPCT)及びQC様酵素(QPCTL)の触媒活性として定義される。これらの酵素は、腎臓、肝臓、腸、脳、及び脳脊髄液等の体液を含む哺乳類の身体の種々の組織において見つかっており、該酵素は、生物学的に活性のあるペプチドのN末端でグルタミン又はグルタミン酸を高い特異性で環化させる。
本明細書で使用される用語「EC」は、EC(グルタミン酸シクラーゼ)活性としてさらに定義される、ECとしてのグルタミニルシクラーゼ(QC、QPCT)及びQC様酵素(QPCTL)の活性を含む。
本明細書で使用される用語「EC活性」は、グルタミニルシクラーゼ(QC、QPCT)及びQC様酵素(QPCTL)によるN末端グルタミン酸残基のピログルタミン酸(pGlu*)への分子内環化として定義される。その点においてはスキーム3を参照されたい。
用語「(イソ)QC阻害剤」又は「(イソ)グルタミニルシクラーゼ阻害剤」は一般的に、当業者に公知であり、好ましくは阻害剤と個々の酵素との直接的な相互作用によって、グルタミニルシクラーゼ(QPCT)の若しくはイソグルタミニルシクラーゼ酵素(QPCTL)の触媒活性を、又はそれらのグルタミルシクラーゼ(EC)活性を阻害する酵素阻害剤を意味する。
本明細書で定義される用語「選択的イソQC阻害剤」は、イソグルタミニルシクラーゼ(イソQC、QPCTL)の触媒活性を阻害するが、グルタミニルシクラーゼ(QC、QPCT)の触媒活性を阻害する能力を有さないか又は該能力のより低い酵素阻害剤を意味する。グルタミニルシクラーゼ(QC)の阻害についてKi値よりも10%低いKi値を有するイソグルタミニルシクラーゼ(イソQC)を阻害する選択的イソQC阻害剤が好ましい。より好ましくは、イソグルタミニルシクラーゼ(イソQC、QPCTL)の阻害についての選択的イソQC阻害剤のKi値は、グルタミニルシクラーゼ(QC)の阻害についての選択的イソQC阻害剤のKi値よりも50%低い。グルタミニルシクラーゼ(QC)の阻害についての選択的イソQC阻害剤のKi値よりも1オーダーの程度ほど低い選択的イソQC阻害剤がさらにより好ましい。より好ましくは、イソグルタミニルシクラーゼ(イソQC、QPCTL)の阻害についての該選択的イソQC阻害剤のKi値は、グルタミニルシクラーゼ(QC)の阻害についての該選択的イソQC阻害剤のKi値よりも2オーダーの程度ほど低い。イソグルタミニルシクラーゼ(イソQC、QPCTL)の阻害についての選択的イソQC阻害剤のKi値がグルタミニルシクラーゼ(QC)の阻害についての選択的イソQC阻害剤のKi値よりも3オーダーの程度ほど低い選択的イソQC阻害剤がさらにより好ましい。グルタミニルシクラーゼ(QC)を阻害しない選択的イソQC阻害剤が最も好ましい。
イソQC阻害との相関の点で、好ましい実施態様において、対象となる方法及び医薬的用途は、イソQC阻害についてのKi が10μM以下の、より好ましくは0.01μM以下の、又は最も好ましくは0.001μM以下である阻害剤を利用する。実際、より低いμMの、好ましくはnMの、さらにより好ましくはpMのKi値を有する阻害剤が熟慮される。このように、活性薬が簡便のため「イソQC阻害剤」として本明細書に記載されているが、このような名称が、本発明の対象を特定の作用機序に限定するよう意図しているものではないことは理解されるであろう。
一般に、対象の方法又は医学的用途に関するイソQC阻害剤は、例えば分子量が1000g/mol以下、500g/mol以下、好ましくは400g/mol以下、及びさらにより好ましくは350g/mol以下、及びさらには300g/mol以下の分子量を有する小分子であろう。
本明細書で使用される用語「対象(subject)」は、治療、観察、又は実験の対象(object)であった動物、好ましくは哺乳類、最も好ましくはヒトである。
本明細書で使用される用語「治療的有効量」は、研究者、獣医、医師、又は他の臨床医によって調べられている組織の系、動物、又はヒトにおける、治療されている疾患又は障害の症状の軽減を含む生物学的又は医学的応答を惹起する活性化合物又は医薬剤の量を意味する。
本明細書で使用されるように、用語「医薬として許容し得る」は、ヒトでの用途及び獣医学的な用途の両方を包含する:例えば、用語「医薬として許容し得る」は、獣医学的に許容し得る化合物、又はヒトの医学及び保健医療において許容し得る化合物を包含する。
特に、本発明は以下の項目に関する:
1.a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防するためのイソQC阻害剤。
2.a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防するためのイソQC阻害剤の使用。
3.a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防する薬剤の製造のためのイソQC阻害剤の使用。
4.a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防する方法であって、治療的有効量のイソQC阻害剤を該治療及び/又は予防を必要とする対象に投与する、該方法。
5.前記炎症性疾患が、関節リウマチ、粥状硬化、再狭窄、膵炎、及び骨粗鬆症から選択される慢性及び急性炎症である、項目1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
6.前記炎症性疾患が、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症から選択される、項目1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
7.前記炎症性疾患が神経炎症である、項目1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
8.前記炎症性疾患が、神経炎症から結果として生じ得る神経変性疾患である、項目1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
9.前記神経変性疾患が、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症から選択される、項目8記載のイソQC阻害剤、使用、又は方法。
10.前記イソQC阻害剤が、抗炎症薬、向知性薬、神経保護薬、抗パーキンソン病薬、アミロイドタンパク質沈着阻害剤、βアミロイド合成阻害剤、抗うつ薬、抗不安薬、抗精神病薬、及び抗多発性硬化症薬、アンギオテンシン変換酵素(ACE)の阻害剤、アンギオテンシンII受容体遮断薬、利尿薬、カルシウムチャネル遮断薬(CCB)、β遮断薬、血小板凝集阻害剤、コレステロール吸収モジュレーター、HMG-Co-A還元酵素阻害剤、高密度リポタンパク質(HDL)を増加させる化合物、レニン阻害剤、IL-6阻害剤、抗炎症性コルチコステロイド、抗増殖薬、一酸化窒素ドナー、細胞外マトリックス合成の阻害剤、増殖因子又はサイトカインシグナル伝達阻害剤、MCP-1アンタゴニスト、及びチロシンキナーゼ阻害剤からなる群から選択されるさらなる薬剤と組み合わせて投与される、項目1〜9のいずれか一項記載のイソQC阻害剤、使用、又は方法。
11.前記疾患及び/又は容態がヒトを苦しめる、項目1〜10のいずれか一項記載のイソQC阻害剤、使用、又は方法。
12.項目1〜9のいずれか一項記載のイソQC阻害剤又は項目10記載の組み合わせを含む医薬組成物。
13.前記イソQC阻害剤が式(I)の化合物、又はそのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体
R1は、-C3-8カルボシクリル-ヘテロアリール、-C2-6アルケニルヘテロアリール、-C1-6アルキルヘテロアリール、又は(CH2)aCR5R6(CH2)bヘテロアリールを表し、式中、a及びbは独立して、0〜5の整数を表し、但し、a+b=0〜5であり、かつR5及びR6が、それらの結合する炭素と共にC3-C5シクロアルキル基又は二環式ヘテロアリール基を形成するアルキレンであり;
ここで、上記のヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R2は、C1-8アルキル、アリール、ヘテロアリール、カルボシクリル、ヘテロシクリル、-C1-4アルキルアリール、-C1-4アルキルヘテロアリール、-C1-4アルキルカルボシクリル、又はC1-4アルキルヘテロシクリルを表し;
ここで、上記のアリール基及びヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いはR2は、フェニルによって置換されたフェニル、単環式ヘテロアリール基によって置換されたフェニル、ベンジルオキシによって置換されたフェニル、カルボシクリルに縮合したフェニル、ヘテロシクリルに縮合したフェニル、-C1-4アルキル(フェニルによって置換されたフェニル)、-C1-4アルキル(単環式ヘテロアリール基によって置換されたフェニル)、-C1-4アルキル(ベンジルオキシによって置換されたフェニル)、-C1-4アルキル(任意に置換されたカルボシクリルに縮合した任意に置換されたフェニル)、又はC1-4アルキル(任意に置換されたヘテロシクリルに縮合した任意に置換されたフェニル)を表し;
ここで、上記のフェニル基、ベンジルオキシ基、及びヘテロアリール基のいずれも、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく、かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R3は、H、-C1-4アルキル、又はアリールを表し;
ここで、上記のアリールは、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、1つ以上のC1-2アルキル基によって任意に置換されたカルボシクリル環を形成するよう結合し;
或いは、R2及びR3は、フェニルに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はフェニルは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、単環式ヘテロアリールに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はヘテロアリールは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R4は、H、-C1-8アルキル、-C(O)C1-6アルキル、又はNH2を表し;
Xは、O又はSを表し;かつ
Yは、O又はSを表す、項目1〜12のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
14.R1が、二環式ヘテロアリール基を表す、項目13記載のイソQC阻害剤、使用、方法、又は医薬組成物。
15.R1が、1個又は2個の窒素原子を含む5員環に縮合したベンゼン環又はピリジン環を表す、項目14記載のイソQC阻害剤、使用、方法、又は医薬組成物。
16.結合点が、ベンゼン環又はピリジン環を介している、項目15記載のイソQC阻害剤、使用、方法、又は医薬組成物。
17.R1が、
18.R1が、
19.R1が-C1-6アルキルヘテロアリールを表す、項目18記載のイソQC阻害剤、使用、方法、又は医薬組成物。
20.R1のヘテロアリール基が、C1-4アルキル、C1-4アルコキシ-、及びハロゲンから選択される1つ以上の置換基によって任意に置換された1〜3個の窒素原子を含む5員環である、項目19記載のイソQC阻害剤、使用、方法、又は医薬組成物。
21.前記ヘテロアリール基が、
22.R1が、
式中、Aが、非分岐の若しくは分岐したC1-6アルキレン鎖を表し、又はAが、分岐したC1-6アルキレン鎖を表し、又はAが(CH2)aCR5R6(CH2)bを表し、
かつR11、R12、及びR13が独立して、H若しくはC1-2アルキルを表す、項目13記載のイソQC阻害剤、使用、方法、又は医薬組成物。
23.R1が、
式中、Bが、結合、-CH2-、-CH2-CH2-、-CH(Me)-、-CH(Me)-CH2-、又は-CH2-CH(Me)-を表し、かつ
R14及びR15が独立して、H又はC1-2アルキルを表す、項目14又は項目19記載のイソQC阻害剤、使用、方法、又は医薬組成物。
24.下記式:
25.R2が、アリール、ヘテロアリール、フェニルによって置換されたフェニル、ヘテロシクリルに縮合したフェニルを表し、又はR2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成し;上記のアリール、ヘテロアリール、フェニル、ヘテロシクリル、及びカルボシクリルが任意に置換されている、項目13〜24のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
26.R2が、フェニルによって置換されたフェニルを表し、上記のフェニル基が、同じでも又は異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1つ以上の置換基によって任意に置換されている、項目25記載のイソQC阻害剤、使用、方法、又は医薬組成物。
27.R2が-ビフェニル-4-イルである、項目26記載のイソQC阻害剤、使用、方法、又は医薬組成物。
28.R2が、同じでも又は異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1、2、又は3個の置換基によって任意に置換されたフェニルを表す、項目25記載のイソQC阻害剤、使用、方法、又は医薬組成物。
29.R2が、n-プロピルオキシによって置換されたフェニルである、項目28記載のイソQC阻害剤、使用、方法、又は医薬組成物。
30.R3がHを表す、項目13〜29のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
31.R2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成する、項目13〜25のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
32.R4がHを表す、項目13〜31のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
33.XがOを表す、項目13〜32のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
34.YがOを表す、項目13〜33のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
35.式(I)の化合物が
36.式(I)の化合物が、
5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-5-メチルフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-フルオロ-5-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ブロモ-5-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-フルオロ-4(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-3-メトキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-ブロモ-4-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-[3-(1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
5-(2-ブロモ-5-フルオロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-[3-(5-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-フェニルフェニル)イミダゾリジン-2,4-ジオン;
5-(3-クロロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-[3-(4-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン;
5-(3-クロロフェニル)-1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
3-(1H-ベンズイミダゾール-5-イル)-1',3'-ジヒドロ-2H,5H-スピロ[イミダゾリジン-4,2'-インデン]-2,5-ジオン;
5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-4-チオキソイミダゾリジン-2-オン;
3-(1H-ベンズイミダゾール-5-イル)-5-チオキソ-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-6-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-3-メチル-5-フェニルイミダゾリジン(phenylimida4zolidine)-2,4-ジオン;
1-(H-イミダゾ[1,2-a]ピリジン-7-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
又はそのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体から選択される、項目13〜35のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
37.前記イソQC阻害剤が、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオンの化合物であり、下記構造:
38.イソQC阻害剤を含む診断アッセイ。
39.前記イソQC阻害剤が、項目13〜37のいずれか一項において定義したようなその医薬として許容し得る塩、溶媒和物、及び立体異性体を含む化合物である、項目38記載の診断アッセイ。
40.前記イソQC阻害剤が、(1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオンである、項目38又は39のいずれか一項記載の診断アッセイ。
41.項目1〜9のいずれか一項において定義したような疾患及び/又は容態のいずれか1つを診断する方法であって、
-該疾患及び/又は容態で苦しめられていることが疑われる対象から試料を収集する工程、
-該試料をイソQC阻害剤と接触させる工程、及び
-該対象が該疾患及び/又は容態によって苦しめられているか否かを決定する工程、
を含む、該方法。
42.前記対象がヒトである、項目41記載の方法。
43.前記イソQC阻害剤が、項目13〜31のいずれか一項において定義したようなその医薬として許容し得る塩、溶媒和物、及び立体異性体を含む化合物である、項目41又は42記載の方法。
44.前記イソQC阻害剤が、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオンである、項目41〜43のいずれか一項記載の方法。
45.前記試料が、血液試料、血清試料、脳脊髄液の試料、又は尿試料である、項目41〜44のいずれか一項記載の方法。
46.検出手段として項目38〜40のいずれか一項記載の診断アッセイと決定手段とを含む、項目41〜45のいずれか一項記載の方法を実施するための診断キット。
47.前記イソQC阻害剤が、配列番号11、12、13、14、15、16、17、18、57、58、59、若しくは60のいずれかの配列を含むポリペプチド又は配列番号2、3、4、5、6、7、8、9、53、54、55、若しくは56のいずれかの配列を含む核酸によってコードされるポリペプチドの群から選択されるポリペプチドのいずれか1つを阻害する、上記の項目のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
48.前記イソQC阻害剤が、配列番号11若しくは12のいずれかの配列を含むポリペプチド又は配列番号2若しくは3のいずれかの配列を含む核酸によってコードされるポリペプチドの群から選択されるポリペプチドのいずれか1つを阻害する、上記の項目のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
49.前記イソQC阻害剤が、配列番号11の配列を含むポリペプチド又は配列番号2の配列を含む核酸によってコードされるポリペプチドを阻害する、上記の項目のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
50.前記イソQC阻害剤が、配列番号12の配列を含むポリペプチド又は配列番号3の配列を含む核酸によってコードされるポリペプチドを阻害する、上記の項目のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
(b)他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
(c)神経炎症、並びに
(d)神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
から選択される慢性又は急性の炎症を治療するためのイソQC阻害剤の効果は、本発明の実施例12、15、及び17において説明されるインビボアッセイを使用して試験することができる。
粥状硬化又は多発性硬化症を治療する方法におけるイソQC阻害剤の使用が、本発明に従ってさらに好ましい。
QPCTL酵素活性阻害剤の具体的な例を以下に説明する。阻害剤は例えば、QPCTLシクラーゼ活性の阻害剤、又はそれに替わるものとして、QPCTLが相互作用するタンパク質へのQPCTLの結合活性の阻害剤であり得る。このような阻害剤の具体的な例には、例えば、所望の細胞種に導入することができる培地中に処方される抗QPCTL抗体、ペプチド、タンパク質断片、又は低分子ペプチジルプロテアーゼ阻害剤、又は低分子非ペプチド有機分子阻害剤を含むことができる。或いは、このような阻害剤は、細胞仲介性エンドサイトーシス及び他の受容体仲介性事象による導入のための標的リガンドに結合することができる。このような方法は以下にさらに説明され、本明細書に記載されたQPCTLヌクレオチド及びアミノ酸の配列を与えられた当業者によって実施することができる。
R1が-C2-6アルケニルヘテロアリールを表す場合、C2-6アルケニルの例には、C2-4アルケニル、特にプロペニルを含む。典型的な-アルケニルヘテロアリール基は、3-イミダゾール-1-イル-プロパ-2-エニル-である。
最も適切には、該アルキル基は、-CH2-、-(CH2)2、又は-(CH2)3-であり、-(CH2)3-が特に適切である。特に適切な-アルキルヘテロアリール基は、3-イミダゾール-1-イル-プロピル-である。
R11、R12、及びR13は独立して、H又はC1-2アルキルを表す。
R14及びR15は独立して、H又はC1-2アルキルを表す。
R16及びR17は独立して、H又はC1-2アルキルを表す。
R18及びR19は独立して、H又はC1-2アルキルを表す。
一実施態様において、R14はHを表し、かつR15はHを表す。別の実施態様において、R14はHを表し、かつR15はC1-2アルキルを表す。第三の実施態様において、R14はC1-2アルキルを表し、かつR15はHを表す。
R11は適切にはHを表し、
R12は適切にはH又はメチルを表す。
R13は適切にはH又はメチルを表す。
本発明の一実施態様において、R12はHを表し、かつR13はメチルを表す。別の実施態様において、R12はメチルを表し、かつR13はHを表す。第三の実施態様において、R12はHを表し、かつR13はHを表す。
或いは、Aは分岐C2-5アルキレン鎖を表す。
Aが、同じ位置で2個のアルキレン置換基によって置換されたC2-5アルキレン鎖を表す場合(ここで、2個のアルキレン置換基は互いに結合して、C3-5スピロ-シクロアルキル基を形成する。)、該スピロ-シクロアルキル基は適切には、C3スピロ-シクロアルキルである。
一実施態様において、R16はHを表し、かつR17はHを表す。別の実施態様において、R16はHを表し、かつR17はC1-2アルキルを表す。第三の実施態様において、R16はC1-2アルキルを表し、かつR17はHを表す。
適切には、Cは、結合、-CH2-、又は-CH2CH2-を表す。一実施態様において、Cは結合を表す。別の実施態様において、Cは-CH2-を表す。第三の実施態様において、Cは-CH2CH2-を表す。
一実施態様において、R18はHを表し、かつR19はHを表す。別の実施態様において、R18はHを表し、かつR19はC1-2アルキルを表す。第三の実施態様において、R18はC1-2アルキルを表し、かつR19はHを表す。
適切には、Dは、結合、-CH2-、又は-CH2CH2-を表す。一実施態様において、Dは結合を表す。別の実施態様において、Dは-CH2-を表す。第三の実施態様において、Dは-CH2CH2-を表す。
最も適切には、R1は、下記式を表す
特に適切な実施態様において、式(I)の化合物は、下記式によって表される
最も適切には、式(I)の化合物は、下記式によって表される
R2が、フェニルによって置換されたフェニルを表し、ここで、上記のフェニル基のいずれも任意に置換してもよい場合、例には-ビフェニル-4-イルを含む。
R2が、任意に置換されたヘテロシクリルに縮合した任意に置換されたフェニルを表す場合、例には、ベンゾ[1,3]ジオキソ-4-イル-及び2,3-ジヒドロ-ベンゾ[1,4]ジオキシン-4-イル-を含む。
R2が、-C1-4アルキル(単環式ヘテロアリール基によって置換されたフェニル)を表す場合、例には、4-(オキサゾール-5-イル)フェニル-メチル-を含む。
特に適切なR2基は、n-プロピルオキシによって置換されたフェニル、特に4-n-プロポキシフェニルである。
R3が、任意に置換されたアリールを表す場合、アリールは典型的には、フェニルを表し得る。典型的な置換フェニル基には、2,4-ジクロロフェニル-、2,4-ジフルオロロフェニル(difluororophenyl)-、2,4-ジメトキシフェニル-、2,4-ジメチルフェニル-、2,4-ビス(トリフルオロメチル)フェニル-、2,4,6-トリフルオロフェニル-、2,4,6-トリメチルフェニル-、2,6-ジクロロフェニル-、2,6-ジフルオロフェニル-、2,6-ジメトキシフェニル-、2-イソプロピル-6-メチルフェニル-、3-(シクロペンチルオキシ)-4-メトキシフェニル-、3,4,5-トリメトキシフェニル-、3,4-ジメトキシフェニル-、3,4-ジクロロフェニル-、3,4-ジメチルフェニル-、3,4,5-トリフルオロフェニル-、3,5-ビス(トリフルオロロメチル(trifluororophenyl))フェニル-、3,5-ジメトキシフェニル-、3-メトキシフェニル-、4-(トリフルオロメチル)フェニル-、4-ブロモ-2-(トリフルオロメチル)フェニル-、4-ブロモフェニル-、4-クロロ-3-(トリフルオロメチル)フェニル-、4-クロロフェニル-、4-シアノフェニル-、4-エトキシフェニル-、4-エチルフェニル-、4-フルオロフェニル-、4-イソプロピルフェニル-、4-メトキシフェニル-を含む。或いは、R3は、非置換フェニル-を表してもよい。さらなる典型的な置換フェニル基には、2-ブロモ-4-フルオロフェニル-、2-ブロモ-5-フルオロフェニル-、2-クロロフェニル-、2-フルオロ-5-(トリフルオロメチル)フェニル-、2-ヒドロキシ-3-メトキシフェニル-、2-ヒドロキシ-5-メチルフェニル-、3-クロロフェニル-、3-フルオロ-4-(トリフルオロメチル)フェニル-、3-ヒドロキシ-4-メトキシフェニル-、4-クロロ-3-(トリフルオロメチル)フェニル-、4-クロロフェニル-、4-フルオロフェニル-、及び4-プロポキシフェニル-を含む。
R2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成する場合;例には、インダニル(例えば、インダン-2-イル)及びテトラリニルを含む。
適切には、R3はHを表すか又は、R2及びR3は結合して、フェニルに縮合したカルボシクリル環を形成する。最も適切にはR3はHを表す。
R4が-C(O)C1-6アルキルを表す場合;例には、-C(O)メチル、-C(O)エチル、-C(O)プロピル、及び-C(O)ブチルなどの-C(O)C1-4アルキルを含む。
適切には、R4は、H、-C1-8アルキル、又は-C(O)C1-6アルキルを表す。より適切には、R4はH又は-C1-8アルキル、例えばH又はメチルを表す。最も適切には、R4はHを表す。
一実施態様において、YはOを表す。代替的な実施態様において、YはSを表す。
一実施態様において、XはOを表しかつYはSを表す。代替的な実施態様において、XはSを表しかつYはOを表す。適切には、X及びYは両方ともOを表す。
最も適切には、式(I)の化合物は下記式によって表される
1. 5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン
2. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニルイミダゾリジン-2,4-ジオン
3. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-5-メチルフェニル)イミダゾリジン-2,4-ジオン
4. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-フルオロ-5-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
5. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ブロモ-5-フルオロフェニル)イミダゾリジン-2,4-ジオン
6. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン
7. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
8. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
9. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)イミダゾリジン-2,4-ジオン
10. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-3-メトキシフェニル)イミダゾリジン-2,4-ジオン
11. 1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2,4-ジオン
12. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン
13. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)イミダゾリジン-2,4-ジオン
14. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン
15. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-フルオロフェニル)イミダゾリジン-2,4-ジオン
16. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イル)イミダゾリジン-2,4-ジオン
17. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン
18. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-ブロモ-4-フルオロフェニル)イミダゾリジン-2,4-ジオン
19. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン
20. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
21. 1-[3-(1H-イミダゾール-1-イル)プロピル-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン
22. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン
23. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン
24. 1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン
25. 5-(2-ブロモ-5-フルオロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン
26. 1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン
27. 1-[3-(5-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-フェニルフェニル)イミダゾリジン-2,4-ジオン
28. 5-(3-クロロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン
29. 1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン
30. 1-[3-(4-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン
31. 5-(3-クロロフェニル)-1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン
32. 3-(1H-ベンズイミダゾール-5-イル)-1',3'-ジヒドロ-2H,5H-スピロ[イミダゾリジン-4,2'-インデン]-2,5-ジオン
33. 5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)-2-チオキソイミダゾリジン-4-オン
34. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-2-チオキソイミダゾリジン-4-オン
35. 1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-2-チオキソイミダゾリジン-4-オン
36. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)-2-チオキソイミダゾリジン-4-オン
37. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-4-チオキソイミダゾリジン-2-オン
38. 1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-4-チオキソイミダゾリジン-2-オン
39. 3-(1H-ベンズイミダゾール-5-イル)-5-チオキソ-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン
40. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-チオキソイミダゾリジン-2-オン
41. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-チオキソイミダゾリジン-2-オン
42. 1-(1H-ベンゾ[d]イミダゾール-6-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-チオキソイミダゾリジン-2-オン
43. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-チオキソイミダゾリジン-2-オン
44. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-チオキソイミダゾリジン-2-オン
45. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-3-メチル-5-フェニルイミダゾリジン-2,4-ジオン
46. 1-(H-イミダゾ[1,2-a]ピリジン-7-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
又はそのすべての互変異性体及び立体異性体を含むそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体。
哺乳類におけるイソQC(QPCTL)の生理的基質は、例えば、アミロイドβ-ペプチド(3-40)(配列番号91)、(3-42)(配列番号92)、(11-40)(配列番号93)、及び(11-42)(配列番号94)、ABri(配列番号95)、ADan(配列番号96)、ガストリン(配列番号97)、ニューロテンシン(配列番号98)、FPP(配列番号99)、CCL2(配列番号100)、CCL7(配列番号101)、CCL8(配列番号102)、CCL13(配列番号103)、CCL16(配列番号104)、CCL18(配列番号105)、フラクタルキン(配列番号106)、オレキシンA(配列番号107)、[Gln5]-サブスタンスP(5-11)(配列番号108)、及びペプチドQYNAD(配列番号109)である。本発明記載のイソQC阻害剤及び/又は組み合わせ並びに、少なくとも1種のイソQC阻害剤を含む医薬組成物は、QC活性の調節により治療することができる容態の治療に有用である。
3、11、及び/又は22位にピログルタミン酸残基を伴うβ-アミロイドペプチドは、アミロイドβ-ペプチド1-40(42/43)よりも、より細胞傷害性があり、かつより疎水性であることが説明されている(Saido T.C.の文献(2000 Medical Hypotheses 54(3): 427-429))。
a.慢性及び急性の炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症。
多発性硬化症の治療のためのイソQC阻害剤の使用がさらに好ましい。
神経炎症の治療のためのイソQC阻害剤の使用がもっとも好ましい。
(方法1(実施例1〜32))
生成物の遊離塩基を水に懸濁し、1当量のNaOH(水溶液)を添加した。溶液を凍結させ、凍結乾燥に供した。
1当量の対応する4-メチルイミノ-イムダゾルジン-2-オンを1.25MのHCl含有メタノール(無水、0.25mmolの出発材料につき1mL)に溶解し、1当量の1.5当量の硫化ナトリウム含有溶液を密封したマイクロ波容器に加える。反応混合物をマイクロ波において140℃で20分間加熱する。
a)生成物を無水CHCl3に取り、EtO(CO)Cl及びトリエチルアミンを添加した。混合物を還流下で12時間維持した。その後、溶媒を除去し、残余の油を無水EtOHに溶解し、NaOEtを添加した。還流下で溶液を10時間維持し;又は
b)生成物をトルエンに溶解し、カルボニルジイミダゾール及びトリエチルアミンを添加した。溶液を還流下で18時間維持し、又は
c)生成物をホルムアミドに取り、200℃で2時間維持した。
本システムは、Luna(登録商標)100-7 C18半分取用カラム(Phenomenex.長さ:250mm、直径:21mm)を装備したMerck-Hitachi社の装置(モデルLaChrom)から構成された。本化合物は、勾配を用いて流速6mL/分で精製し;これにより、溶離剤(A)はアセトニトリルであり、溶離剤(B)は水であり、両方とも0.1%(v/v)トリフルオロ酢酸を含有し、下記勾配を適用した:0分〜40分。40〜95%の(A)。
(実施例1:5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン)
方法1において説明したとおり、5-アミノベンズイミダゾール5.32g(40mmol)、ベンゾ[c][1,2,5]チアジアゾール-6-イル-カルボアルデヒド6.56g(40mmol)、n-ブチルイソニトリル4.24mL(40mmol)、及びKOCN 3.28g(40mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール1.331g(10mmol)、ベンズアルデヒド1.02mL(10mmol)、ベンジルイソニトリル1.22mL(10mmol)、及びKOCN 0.84g(10mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.4g(3.0mmol)、2-ヒドロキシ-5-メチルフェニルカルボアルデヒド0.409g(3.0mmol)、n-ブチルイソニトリル0.316mL(3.0mmol)、及びKOCN 0.244g(0.2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、2-フルオロ-5-(トリフルオロメチル)フェニルカルボアルデヒド0.362mL(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、2-ブロモ-5-フルオロフェニルカルボアルデヒド0.325(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、4-プロポキシフェニルカルボアルデヒド0.253mL(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、4-クロロ-3-(トリフルオロメチル)フェニルカルボアルデヒド0.23mL(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.133g(1mmol)、3-フルオロ-4-(トリフルオロメチル)フェニルカルボアルデヒド0.192g(1mmol)、n-ブチルイソニトリル0.083g(1mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.081g(1mmol)から出発して、本化合物を合成した。
収量:0.151g(40%);MS m/z 379.2 (M+H)+
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、3-ヒドロキシ-4-メトキシフェニルカルボアルデヒド0.244g(1.6mmol)、n-ブチルイソニトリルn-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.133g(1mmol)、2-ヒドロキシ-3-メトキシフェニルカルボアルデヒド0.153g(1mmol)、n-ブチルイソニトリル0.106mL(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.133g(1mmol)、1,1'-ビフェニル-4-イルカルボアルデヒド0.183(1mmol)、n-ブチルイソニトリルn-ブチルイソニトリル0.106mL(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール2.13g(16mmol)、3-クロロベンズアルデヒド2.24g(16mmol)、n-ブチルイソニトリル1.69mL(16mmol)、KOCN 1.3g(16mmol)、及び塩化ピリジニウム1.85g(16mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、4-クロロベンズアルデヒド0.224g(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.130g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、2-クロロベンズアルデヒド0.225mg(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.130g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.134g(1mmol)、4-フルオロベンズアルデヒド0.125g(1mmol)、n-ブチルイソニトリル0.106mL(1mmol)、塩化ピリジニウム0.116g(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.134g(1mmol)、2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イルカルボアルデヒド0.165g(1mmol)、n-ブチルイソニトリル0.106mL(1mmol)、塩化ピリジニウム0.116g(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン1.0g(7.98mmol)、ベンズアルデヒド0.807mL(7.98mmol)、ベンジルイソニトリル0.972mL(7.98mmol)、塩化ピリジニウム0.920、及びKOCN 0.648g(7.98mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、2-ブロモ4-フルオロベンズアルデヒド0.610g(3mmol)、ベンジルイソニトリル0.365mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、4-プロポキシフェニルカルボアルデヒド0.492g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、3-フルオロ-4-(トリフルオロメチル)フェニルカルボアルデヒド0.576g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、4-フェニルベンズアルデヒド0.546g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、3-クロロフェニルカルボアルデヒド0.42g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イ(y))プロピルアミン0.358mL(3mmol)、2-クロロベンズアルデヒド0.420g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、ベンズアルデヒド0.202mL(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、2-ブロモ-5-フルオロフェニルカルボアルデヒド0.406g(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、4-プロポキシフェニルカルボアルデヒド0.316mL(2mmol)、ベンジルイソニトリル0.245mL(2mmol)、塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、4-フェニルベンズアルデヒド0.364g(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、3-クロロフェニルカルボアルデヒド0.226mL(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(4-メチル-1H-イミダゾール-1-イル)プロピルアミン0.250g(1.8mmol)、ベンズアルデヒド0.182mL(1.8mmol)、ベンジルイソニトリル0.220mL(1.8mmol)塩化ピリジニウム0.210g(1.8mmol)、及びKOCN 0.150g(1.8mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(4-メチル-1H-イミダゾール-1-イル)プロピルアミン0.250g(1.8mmol)、4-フェニル-ベンズアルデヒド0.220g(1.8mmol)、ベンジルイソニトリル0.220mL(1.8mmol)、塩化ピリジニウム0.210g(1.8mmol)、及びKOCN 0.150g(1.8mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(4-メチル-1H-イミダゾール-1-イル)プロピルアミン0.250g(1.8mmol)、3-クロロフェニルカルボアルデヒド0.204mL(1.8mmol)、ベンジルイソニトリル0.220mL(1.8mmol)塩化ピリジニウム0.210g(1.8mmol)、及びKOCN 0.150g(1.8mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.4g(3mmol)、インダン-2-オン0.4g(3mmol)、n-ブチルイソニトリル0.316mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.244g(3mmol)から出発して、本化合物を合成した。
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)、ベンゾ[c][1,2,5]チアジアゾール-6-イルカルボアルデヒド0.016g(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.0045g(12%);MS m/z 367.2 (M+H)+;HPLC(λ=220nm, [B]):室温1.91分(94%)。
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)ベンズアルデヒド0.01mL(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.0069g(22%);MS m/z 309.3 (M+H)+;HPLC(λ=220nm, [B]):室温1.52分(96%)
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)、4-フェニルベンズアルデヒド0.018g(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.00346g(8.9%);MS m/z 385.5 (M+H)+;HPLC(λ=220nm, [B]):室温2.93分(96%)。
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)、3-ヒドロキシ-4-メトキシフェニルカルボアルデヒド0.015g(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.00162g(3.5%);MS m/z 355.3 (M+H)+;HPLC(λ=220nm, [B]):室温0.81分(92%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-4-(メチルイミノ)-5-フェニルイミダゾリジン-2-オン0.076g(0.25mmol)、及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.0092g(12%);MS m/z 309.5 (M+H)+;HPLC(λ=220nm, [B]):室温2.61分(64%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-4-(メチルイミノ)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2-オン0.095g(0.25mmol)Na2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00036g(0.37%);MS m/z 385.4 (M+H)+;HPLC(λ=220nm, [B]):室温3.02分(97%)。
方法3において説明したとおり、3-(1H-ベンズイミダゾール-5-イル)-4-(メチルイミノ)-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン0.082g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.0016g(1.9%);MS m/z 335.2 (M+H)+;HPLC(λ=220nm, [D]):室温2.81分(84%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.084g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00088g(1.0%);MS m/z 343.8 (M+H)+;HPLC(λ=220nm, [D]);室温2.73分(99%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.090g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00613g(6.7%);MS m/z 363.2 (M+H)+;HPLC(λ=220nm, [D]):室温2.02分(97%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.100g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00071g(0.6%);MS m/z 406.2 (M+H)+;HPLC(λ=220nm, [D]):室温2.94分(90%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.088g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.0055g(6.1%);MS m/z 359.2 (M+H)+;HPLC(λ=220nm, [D]):室温3.12分(97%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.088g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00221g(2.4%);MS m/z 357.2 (M+H)+;HPLC(λ=220nm, [D]):室温3.21分(80%)。
方法4に従って、5-アミノベンズイミダゾール0.266g(2mmol)、ジ-(1H-イミダゾール-1-イル)メタノン0.324g(2mmol)、塩酸メチルアミン0.135g(2mmol)TEA 0.255mL(2mmol)、及びフェニルグリオキサル水和物0.102g(0.67mmol)から出発して、本化合物を合成した。
方法4に従って、1-(H-イミダゾ[1,2-a]ピリジン-7-イル)尿素0.03g(0.170mmol)及びフェニルグリオキサル水和物0.028g(0.20mmol)から出発して、本化合物を合成した。
同時投与には、少なくとも1つのイソQC阻害剤とその他の薬剤のうちの少なくとも1つとを含む製剤の投与、又は各薬剤の個別の製剤の本質的に同時の投与を含む。
−粥状硬化の治療及び/又は予防のための、イソQC阻害剤、特にイソQC-Iと、アトルバスタチンとの併用
−再狭窄の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、免疫抑制薬、好ましくはラパマイシンとの併用
−再狭窄の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、免疫抑制薬、好ましくはパクリタキセルとの併用
−多発性硬化症の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、インターフェロン、好ましくはアロネックス(Aronex)との併用
−多発性硬化症の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、インターフェロン、好ましくはベタフェロンとの併用
−多発性硬化症の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、インターフェロン、好ましくはレビフとの併用
−多発性硬化症の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、コパクソンとの併用
−再狭窄の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、デキサメタゾンとの併用
−粥状硬化の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、デキサメタゾンとの併用
−関節リウマチの予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、デキサメタゾンとの併用
−再狭窄の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、HMG-CoA-レダクターゼ阻害剤との併用、ここでHMG-CoA-レダクターゼ阻害薬は、アトルバスタチン、セリバスタチン、フラバスタチン、ロバスタチン、ピタバスタチン、プラバスタチン、ロスバスタチン及びシンバスタチンから選択される
−粥状硬化の予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、HMG-CoA-レダクターゼ阻害剤との併用、ここでHMG-CoA-レダクターゼ阻害薬は、アトルバスタチン、セリバスタチン、フラバスタチン、ロバスタチン、ピタバスタチン、プラバスタチン、ロスバスタチン及びシンバスタチンから選択される
−関節リウマチの予防及び/又は治療のための、イソQC阻害剤、特にイソQC-Iと、HMG-CoA-レダクターゼ阻害剤との併用、ここでHMG-CoA-レダクターゼ阻害薬は、アトルバスタチン、セリバスタチン、フラバスタチン、ロバスタチン、ピタバスタチン、プラバスタチン、ロスバスタチン及びシンバスタチンから選択される
−軽度認知障害の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、アミロイド-β抗体との併用、ここでアミロイド-β抗体はAcl-24である、
−アルツハイマー病の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、アミロイド-β抗体との併用、ここでアミロイド-β抗体はAcl-24である、
−ダウン症候群における神経変性の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、アミロイド-β抗体との併用、ここでアミロイド-β抗体はAcl-24である、
−軽度認知障害の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、βセクレターゼ阻害剤との併用、ここでβセクレターゼ阻害剤は、WY-25105、GW-840736X及びCTS-21166から選択される、
−アルツハイマー病の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、βセクレターゼ阻害剤との併用、ここでβセクレターゼ阻害剤は、WY-25105、GW-840736X及びCTS-21166から選択される、
−ダウン症候群における神経変性の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、βセクレターゼ阻害剤との併用、ここでβセクレターゼ阻害剤は、WY-25105、GW-840736X及びCTS-21166から選択される、
−軽度認知障害の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、γ-セクレターゼ阻害剤との併用、ここでγ-セクレターゼ阻害剤は、LY-450139、LY-411575及びAN-37124から選択される、
−アルツハイマー病の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、γ-セクレターゼ阻害剤との併用、ここでγ-セクレターゼ阻害剤は、LY-450139、LY-411575及びAN-37124から選択される、
−ダウン症候群における神経変性の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、γ-セクレターゼ阻害剤との併用、ここでγ-セクレターゼ阻害剤は、LY-450139、LY-411575及びAN-37124から選択される、
−軽度認知障害の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、アセチルコリンエステラーゼ阻害剤との併用、ここでアセチルコリンエステラーゼ阻害剤は、ドネゼピル(donezepil)及びジメボンから選択される、
−アルツハイマー病の予防及び/又は治療のための、イソQC阻害剤、好ましくはイソQC-Iと、アセチルコリンエステラーゼ阻害剤との併用、ここでアセチルコリンエステラーゼ阻害剤は、ドネゼピル(donezepil)及びジメボンから選択される、
−ダウン症候群における神経変性の予防及び/又は治療のための、、イソQC阻害剤、好ましくはイソQC-Iと、アセチルコリンエステラーゼ阻害剤との併用、ここでアセチルコリンエステラーゼ阻害剤は、ドネゼピル(donezepil)及びジメボンから選択される。
(細胞株及び培地)
アフリカミドリザル腎臓細胞株COS-7、ヒト神経芽細胞腫細胞株SH-SY5Y、ヒトアサトロサイトーマ(asatrocytoma)細胞株LN405、ヒト角質細胞腫(keratinocytoma)細胞株HaCaT、及びヒト肝細胞癌細胞株Hep-G2を、37℃で、5%CO2(HaCaT、Hep-G2、COS-7)又は10%CO2(SH-SY5Y、LN405)の高湿大気下で、適切な細胞培地(Cos-7、SH-SY5Y、LN405、HaCaTについてはDMEM、10%FBS)(Hep-G2についてはRPMI1640、10%FBS)において培養した。
RNeasy Mini Kit(Qiagen)を使用してSH-SY5Y、LN405、HaCaT、及びHep-G2細胞から全RNAを単離し、SuperScript II(Invitrogen)によって逆転写した。その後、プライマーイソQCh-1(センス、配列番号19)及びイソQCh-2(アンチセンス、配列番号20)を使用して、生じたcDNA産物を、Herculase Enhanced DNA Polymerase(Stratagene)を有する25μLの反応液に1:12.5で希釈したものにおいて、ヒトイソQCを増幅した。Strataprep PCR Purification Kit(Stratagene)を利用して、Hep-G2のPCR産物を精製し、配列決定によって確認した。
(RT-PCRを用いたヒトイソQC発現の分析)
ヒトイソQCの転写産物は、細胞株SH-SY5Y(図2、レーン1)、LN405(図2、レーン2)、HaCaT(図2、レーン3)、及びHep-G2(図2、レーン4)において存在することがわかった。Hep-G2のPCR産物を配列決定により確認した。
ヒトイソQCの全長cDNAを、RT-PCRを用いてHep-G2細胞から単離した。簡潔には、Hep-G2細胞の全RNAをSuperScript II(Invitrogen)によって逆転写した。その後、プライマーイソQChu-1(センス、配列番号21)及びイソQChu-2(アンチセンス、配列番号22)を使用して、生じたcDNA産物を、Herculase Enhanced DNA Polymerase(Stratagene)を有する25μLの反応液に1:12.5で希釈したものにおいて、ヒトイソQCを増幅した。
(ヒトイソQC-EGFP融合タンパク質をコードするプラスミドベクターの分子クローニング)
すべてのクローニング手順は、標準的な分子生物学の技術を適用して実施した。ヒト細胞におけるヒトイソQC-EGFP融合タンパク質の発現のために、ベクターpEGFP-N3(Invitrogen)を使用した。メチオニンI又はメチオニンIIのいずれかで始まる天然のヒトイソQC cDNAを、高感度緑色蛍光タンパク質(EGFP)をコードしたプラスミドと、フレームにおいてN末端で融合した。プライマーイソQC EGFP-1 Met I(配列番号23)及びイソQC EGFP-3(配列番号25)を、メチオニンIで開始するヒトイソQCの増幅に使用し、プライマーイソQC EGFP-2 Met II(配列番号24)及びイソQC EGFP-3(配列番号25)を、メチオニンIIで開始するヒトイソQCの増幅に使用した。EcoRI及びSalIの制限部位を採用するベクターpEGFP-N3(Invitrogen)に断片を挿入し、正確な挿入を配列決定によって確認した。その後、細胞培養目的のために、EndoFree Maxi Kit(Qiagen)を使用してベクターを単離した。
加えて、増幅のために、EGFP-1(センス)(配列番号48)及びEGFP-2(アンチセンス)(配列番号49)を使用して、ベクターpEGFP-N3(Invitrogen)のEGFP配列をベクターpcDNA 3.1(Invitrogen)に導入した。断片をpcDNA 3.1のXhoI部位へと導入した。メチオニンIで開始するhイソQCのN末端断片についてはイソQC EGFP-1 Met I(センス、配列番号23)及び(アンチセンス)としてhイソQC SS EGFP pcDNA(配列番号50)を、並びにメチオニンIIで開始するhイソQCのN末端断片についてはイソQC EGFP-2 Met II(センス、配列番号24)及び(アンチセンス)としてのhイソQC SS EGFP pcDNA(配列番号50)を使用して、メチオニンI及びIIで開始し、セリン53で各々終止するhイソQCのN末端配列を、C末端でベクターpcDNA 3.1におけるEGFPと融合させた。断片をベクターpcDNA 3.1のEcoRI及びNotI制限部位へと挿入した。その後、細胞培養目的のために、EndoFree Maxi Kit(Qiagen)を使用してベクターを単離した。
hQCについてはプライマーhQC-1(センス)(配列番号45)及びhQC-2(アンチセンス)(配列番号46)を、メチオニンIで開始するhイソQCについてはイソQC EGFP-1 Met I(センス)(配列番号23)及び(アンチセンス)としてのhイソQC pcDNA(配列番号47)を、並びにメチオニンIIで開始するhイソQCについてはイソQC EGFP-2 Met II(センス)(配列番号24)及び(アンチセンス)としてのhイソQC pcDNA(配列番号47)を利用した増幅後に、天然のhQCをベクターpcDNA 3.1 (+)(Invitrogen)のHindIII及びNotI制限部位に挿入し、天然のhイソQCをEcoRI及びNotI制限部位に挿入した。
プライマーhQC-1(センス)(配列番号45)及び(アンチセンス)としてのhQC C-FLAG pcDNA(配列番号51)を適用した増幅後に、ヒトQCをC末端FLAGタグとともにベクターpcDNA 3.1のHindIII及びNotI制限部位にクローニングした。メチオニンIで開始するhイソQCについては、プライマーイソQC EGFP-1 MetI(センス)(配列番号23)及び(アンチセンス)としてのhイソQC C-FLAG pcDNA(配列番号52)を、メチオニン2で開始するhイソQCについては、プライマーイソQC EGFP-2 Met II(センス)(配列番号24)及び(アンチセンス)としてのhイソQC C-FLAG pcDNA(配列番号52)を使用する増幅後に、ヒトイソQCをC末端FLAGタグとともにpcDNA 3.1に挿入した。
(COS-7及びLN405のトランスフェクション及び組織化学的染色)
メチオニンI又はメチオニンIIのいずれかで開始するヒトイソQC-EGFP融合タンパク質の発現のために、カバーガラスを含む6ウェルのディッシュでCOS-7及びLN405を培養した。80%培養密度まで細胞を増殖させ、製造元のマニュアルに従ってLipofectamin2000(Invitrogen)を用いてトランスフェクトし、トランスフェクション溶液において5時間インキュベートした。その後、溶液を適切な増殖培地と交換し、細胞を一晩増殖させた。
(1.LN405のトランスフェクション及び組織化学的染色)
細胞株LN405におけるメチオニンI及びメチオニンIIで開始するヒトイソQC-EGFP融合タンパク質の発現(緑色蛍光)は、結果として生じるタンパク質の区画化を結果的に生じる。マンノシダーゼII抗体を用いたLN405のゴルジ領域の対比染色(赤色蛍光)及びマンノシダーゼIIによるヒトイソQC-EGFPのその後の重ね合わせは、ゴルジ区画内でのヒトイソQC-EGFP融合タンパク質の局在性を示唆している。これにより、メチオニンIIで開始するヒトイソQCが、ヒトイソQC融合タンパク質のゴルジ局在を生じるのに十分であることが明白である。
細胞株LN405におけるメチオニンI及びメチオニンIIで開始するヒトイソQC-EGFP融合タンパク質の発現に類似して、COS-7におけるメチオニンI及びメチオニンIIで開始するヒトイソQC-EGFP融合タンパク質の発現は、結果として生じるタンパク質の区画化(緑色蛍光)を結果的に生じる。マンノシダーゼII抗体を用いたCOS-7細胞のゴルジ領域の対比染色(赤色蛍光)及びマンノシダーゼIIを用いたヒトイソQC-EGFPのその後の重ね合わせは、COS-7のゴルジ区画内でのヒトイソQC-EGFP融合タンパク質の局在性を示唆している。また、COS-7細胞において、メチオニンIIで開始するヒトイソQC-EGFP融合タンパク質の発現は、ゴルジ局在を生じるのに十分である。
(宿主の系及び培地)
プラスミドの増殖のために大腸菌株DH5αを用い、ヒトイソQCの発現のために大腸菌株BL21を用いた。製造元の説明書(Qiagen(DH5α),Stratagene(B21))に従って、大腸菌株を増殖させ、形質転換し、分析した。大腸菌に必要な培地、すなわち、ルリア・ベルターニ(LB)培地を、製造元の推奨に従って製造した。
標準的な分子生物学の技術を適用して、すべてのクローニング手順を実施した。大腸菌BL21における発現のために、ベクターpET41a(Novagen)を用いた。コドン30(メチオニンIIから計数)で開始する成熟ヒトイソQCのcDNAを、GST-タグをコードしたプラスミドとフレームにおいて融合させた。プライマーhイソQC pET41a-1(配列番号26)及びhイソQC pET41a-2(配列番号27)を利用した増幅(表5)の後に、エンテロキナーゼ及びC末端(His)6-タグについてはN末端プロテーゼ切断部位を導入した。サブクローニング後、SpeI及びEcoR Iの制限部位を採用する発現ベクターに、断片を挿入した。
ヒトイソQCをコードするコンストラクトを、BL21細胞へと形質転換し(Stratagene)、37℃で選択的LBアガープレート上で増殖させた。1%グルコースを含むLB培地において、タンパク質の発現を37℃で実施した。およそ0.8のOD600に到達した後、20μM IPTGを用いてイソQC発現を37℃で4時間誘導した。細胞を遠心分離(4000×g、20分)によって培地から分離し、PBS(140mM NaCl、2.7mM KCl、10mM Na2HPO4、1.8mM KH2PO4、pH7,3)に再懸濁し、1周期の凍結及び融解後に1周期のフレンチプレスによって溶解した。リン酸含有緩衝液(50mM Na2HPO4、500mM NaCl、pH7.3)を用いて、細胞溶解液を1.5Lの最終容積に希釈し、13.400×g、4℃で1時間遠心分離した。遠心分離後、Bradfordの方法を用いて、結果として生じる上清のタンパク質濃度を決定した。必要な場合、溶液を再度希釈して、0.6mg/mLの総タンパク質終濃度を得た。4工程プロトコールを利用して、GST-イソQC融合タンパク質を精製した(表6)。精製を図5のSDS-PAGE分析によって示す。
(蛍光アッセイ)
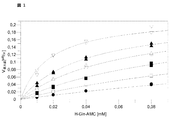
すべての測定は、マイクロプレート用NovoStar読み取り装置(BMG Labtechnologies)により30℃で行った。QC活性は、H-Gln-βNAを用い、蛍光定量により評価した。試料は、最終容積250μl中における、0.2mM蛍光発生基質20mM 、0.25Uピログルタミルアミノぺプチダーゼ(Qiagen, Hilden, Germany)含有0.05Mトリス/HCl(pH8.0)、及び適宜希釈した一定分量のイソQCからなった。励起/発光波長は、320/410nmであった。該アッセイ反応は、グルタミニルシクラーゼの添加により開始した。イソQC活性は、アッセイ条件下でのβ-ナフチルアミンの標準曲線から決定した。1単位は、記載した条件下で、1分間にH-Gln-βNAから1μmolのpGlu-βNAの形成を触媒するイソQC量と定義されている。
このアッセイを用いて、ほとんどのイソQC基質の動力学的パラメータを決定した。イソQC活性は、補助的な酵素としてグルタミン酸デヒドロゲナーゼを利用す不連続アッセイ(Schilling, S. らの文献(2003 Biol Chem 384, 1583-1592))を用い、分光光度的に分析した。試料は、最終容積250μl中における、各イソQC基質、0.3mM NADH、14mMα-ケトグルタル酸、及び30U/mLグルタミン酸デヒドロゲナーゼからなった。反応は、イソQCの添加により出発し、吸光度の低下を340nmで8〜15分間モニタリングすることにより追跡した。初速度を評価し、酵素活性を、アッセイ条件下でのアンモニアの標準曲線から決定した。すべての試料は、マイクロプレート用Sunrise読み取り装置を用い、30℃で測定した。動力学的データは、GraFitソフトウェアを用いて評価した。
阻害剤の試験に関して、試料組成物は、推定阻害化合物を添加したこと以外は、先に記載したものと同じであった。イソQC-阻害に関する迅速試験について、試料は、4mMの各阻害剤及び1KMの基質濃度を含んでいた。阻害の詳細な研究及びKi-値の決定については、補助的な酵素に及ぼす阻害剤の影響を最初に調べた。あらゆる場合において、検出されたいずれの酵素についても影響はなく、従ってイソQC阻害の信頼できる決定が可能であった。阻害定数は、GraFitソフトウェアを用い、反応進行曲線のセットを、競合的阻害に関する一般式にあてはめることにより評価した。
種々の異なる基質をヒトイソQCによる変換に関して評価した(表4)。分析した基質はすべてイソQCによって変換され、ヒトQCと類似した、全体的に比較的緩んだ特異性を示した(Schilling, S.らの文献(2003 Biol Chem. 384, 1583-1592))。N末端グルタミニル残基に隣接した大きな疎水性アミノ酸を有する基質、例えばGln-AMCについて、最大の特異性定数(kcat/KM)を観察した。対照的に、ヒトイソQCにおける負に帯電した残基は、Gln-Gluについて観察されたように、特異性において激烈な低下をもたらし、イソQCの負に帯電した活性部位を示した。ヒトQCと比較して、両方の組換えイソQCはより低い酵素活性を発揮した(図7)。その差は、最大1オーダーの程度であった。イソQCの特異性によると、酵素がインビボで異なる基質の変換を生じる、すなわち、イソQCが、多くの異なる生理学的基質の発生に関与していると仮定することは妥当である。
その上、ヒトイソQC活性を式(I)の実施例化合物によって阻害した(表7A)。
(宿主株及び培地)
プラスミドの増殖のために大腸菌株DH5αを用い、酵母におけるヒトイソQCの発現のためにピキア・パストリス株X-33を用いた。製造元の説明書(Qiagen(DH5α)、Invitrogen(X-33))に従って、大腸菌及びピキア・パストリスを増殖させ、形質転換し、及び分析した。大腸菌に必要な培地、すなわち、ルリア・ベルターニ(LB)培地を製造元の推奨に従って製造した。ピキア・パストリスに必要な培地、すなわち、BMMY、BMGY、YPD、YPDS、及び抗生物質の濃縮物、すなわちZeocinを、ピキアマニュアル(invitrogen、カタログ番号K1740-01)に説明されているとおり製造した。また、該マニュアルには酵母の取り扱いについての関連するすべての説明を含む。
標準的な分子生物学の技術を適用して、すべてのクローニング手順を実施した。ピキア・パストリスX-33における発現のために、pPiCZαA(invitrogen)を用いた。コドン30(メチオニンIIから計数)で開始する成熟ヒトイソQCのcDNAを、タンパク質を分泌経路へと配向させるα因子をコードするプラスミドとフレームにおいて融合させた。プライマーhイソQC HIS C-Term pPICZAA-1(配列番号28)又はhイソQC HIS N-Term pPICZAA-1(配列番号29)をセンスプライマーとして、かつhイソQC HIS N-Term pPICZAA-2(配列番号30)及びhイソQC HIS C-Term pPICZAA-2(配列番号32)(表5)をアンチセンスプライマーとして利用した増幅の後、NotI及びEcoR Iの制限部位を採用する発現ベクターに断片を挿入した。コンストラクトに応じて、突然変異をコドン55(Ile)及び351(Cys)に導入した。標準的なPCR技術に次いで、DpnIを用いる親DNAの消化(quik-change II 位置指定突然変異誘発キット、Stratagene、カタログ番号200524)に従って、突然変異誘発を実施した。生じたコンストラクトを図3において模式的に説明する。
製造元の説明書(BioRad)に従った電気穿孔によるピキア・パストリアコンピテント細胞の形質転換のために、1〜2μgのプラスミドDNAを適用した。100μg/mLのZeocinを含むプレートにおいて選択を実施した。イソQC発現に関して組換え酵母クローンを試験するために、2mLのBMGYを含む10mLのコニカルチューブにおいて組換え体を24時間増殖させた。その後、酵母を遠心分離し、0.5%メタノールを含む2mLのBMMYにおいて再懸濁した。メタノールを24時間ごとに約72時間添加することによって、この濃度を維持した。その後、上清におけるイソQCの活性を決定した。最大活性を呈するクローンをさらなる実験及び発酵のために選択した。発現したコンストラクトに応じて、培地におけるイソQC活性は異なった(図4)。
ピキア・パストリスにおけるイソQCの大規模発現のために、小規模発現において説明した条件を維持したが、総容積は8Lであった。振蘯フラスコにおいて発現を実施した。発現後、遠心分離によって細胞を培地から分離し(1500×g、20分)、ペレットを廃棄した。上清のpH値を中性に調整し、再度遠心分離し、第一の精製工程に適用した。3工程プロトコールを利用して、イソQCタンパク質を精製した(表8)。精製を図5におけるSDS-PAGE分析によって説明する。
メチロトローフ酵母であるピキア・パストリスにおいてヒトイソQCをうまく発現させた。酵母における最良の発現条件を選択するために、いくつかの異なるコンストラクトを生じた(図3)。図4において示すように、発現している細胞の培地において発現及び存在するイソQCの活性は、発現したコンストラクトに応じて変動する。コンストラクトYSShイソQCN55IC351A C-His及びYSShイソQCN55I C-Hisから観察できるように、グリコシル化部位の導入は結果的に、適切な分泌を生じた。培地における最大活性により、コンストラクトYSShイソQCN55IC351A C-Hisを大規模に発現して精製した。表8に説明したとおり精製を実施し、精製の収率は59%であった。より低い分子量への泳動におけるシフトによって証明されるように、見かけの均質なタンパク質をグリコシル化した(図5)。グリコシル化は、酵素の触媒活性に影響を及ぼさなかった。
H-Gln-βNAを用いた蛍光定量アッセイ(実施例5において説明)を適用して、触媒特異性のpH依存性を研究した。7μMの基質濃度で、すなわち、[S]≪KMで反応を実施した。それゆえ、観察した特異性定数は、基質変換の推移曲線(progress curve)の初速度から直接推定することができた。これらの研究において、反応緩衝液は、0.075M酢酸、0.075M MES、及び0.15Mトリスからなり、HCl又はNaOHを用いて所望のpHに調整した。緩衝液は、非常に広範なpH範囲にわたって、一定のイオン強度を保証した。下記の等式:
kcat/KM(pH)=kcat/KM(限界値)×1/(1+[H+]/KHS+KE1/[H+]+KE1/[H+]×KE2/[H+])
(式中、kcat/KM(pH)は、pH依存性の(観察された)動力学的パラメータを示す。)
を用いて、獲得した酵素動力学的データの評価を実施した。kcat/KM(限界値)は、pH依存性の(「限界の」)値を示す。KHS、KE1、及びKE2は、酸性pH範囲における解離群の解離定数、及び酵素の2つの解離群をそれぞれ示した。GraFitソフトウェア(バージョン5.0.4、ウィンドウズ用、ERITHACUS SOFTWARE Ltd., Horley, UK)を用いて、すべての動力学的データの評価を実施した。
hイソQCは、pH7〜8における特異性に関する至適pHを示す。このように、触媒の至適pHは、ヒトQCと非常に類似している。3つの解離群に基づいたモデルに従ったデータの適合によって結果的に、hイソQC及びhQCのpH依存性の良好な解釈がもたらされた(図8)。このように、両酵素反応の触媒作用は、類似の解離群によって影響されており、類似の触媒機序を一般に示唆している。
ヒトQCについて、該酵素がN末端グルタミン酸のピログルタミン酸への環化を触媒することが説明されている。それゆえ、QCは、pGlu修飾されたアミロイドペプチドの作製に関与している。
(細胞株及び培地)
ヒト神経芽細胞腫細胞株SH-SY5Y、ヒト胚腎臓細胞株HEK293、及びヒト単球細胞株THP-1を適切な細胞培地(DMEM、SH-SY5Y、及びHEK293のための10%のFBS)(RPMI1640、THP-1のための10%のFBS)において、5%CO2(HEK293、THP-1)又は10%CO2(SH-SY5Y)の加湿された大気下で、37℃で培養した。
ヒトMCP-1の全長cDNAは、RT-PCRを使用してSH-SY5Y細胞から単離した。SH-SY5Y細胞の全RNAをSuperScript II(Invitrogen)によって逆転写して、その後にヒトMCP-1を、プライマーhMCP-1-1(センス)、及びhMCP-1-2(アンチセンス)(表9)を使用して、Pfu-DNA-Polymerase(Promega)で、25μl反応において産生したcDNA産物の1:12.5希釈で増幅させた。生じるPCR産物は、HindIII及びNotI制限部位を使用してベクターpcDNA 3.1へとクローニングし、配列をDNA配列決定によって確認した。
成熟ヒトMCP-1の第1の(ΔQ1)並びに第1及び第2の(ΔQ1P2)アミノ酸の欠失は、ΔQ1(表9)のためにプライマーΔQ1-1、及びΔQ1-2、並びにΔQ1P2(表9)のためにプライマーΔQ1P2-1及びΔQ1P2-2を使用して、位置指定突然変異誘発によって作製した。親DNAは、Dpn Iで消化した。成熟ヒトMCP-1の欠失ΔQ1及びΔQ1P2をもつpcDNA 3.1プラスミドを、大腸菌JM109に形質転換した。アンピシリン耐性クローンを配列決定によって確認して、その後EndoFree Maxi Kit(Qiagen)を使用して細胞培養目的のために単離した。
ヒトMCP-1のN末端変異体の発現のためには、HEK293細胞をコラーゲンIコーティングした6ウェルディッシュにおいて培養して、80%の培養密度まで培養し、製造元のマニュアルに従ってLipofectamin2000(Invitrogen)を使用してトランスフェクトし、トランスフェクション溶液において5時間インキュベートした。その後、細胞を通常の増殖培地で一晩回復させた。その翌日、細胞を増殖培地において更に24時間インキュベートした。QC阻害の有効性の解析のために、細胞を特異的阻害剤の不在下又は存在下で24時間インキュベートした。24時間後、ヒトMCP-1変異体を含む培地を収集して、走化性能について遊走アッセイで調査した。更にまた、細胞培養上清の一定分量を、ヒトMCP-1-ELISA(Pierce)を使用するヒトMCP-1濃度の定量化のために、−80℃にて貯蔵した。
走化性アッセイは、5μmの孔径をもつ24ウェルTransWellプレート(Corning)を使用して行った。HEK293に発現したヒトMCP-1変異体を含む培地を化学誘引物質として使用した。これを助けるために、600μlのN末端ヒトMCP-1変異体の培地をRPMI1640における無希釈、又は1:3、1:10、及び1:30希釈で、TransWellプレートの下部チャンバーに適用した。更にまた、ベクター対照をトランスフェクトしたHEK293細胞の無希釈培地を、ネガティブ対照として下部チャンバーに適用した。THP-1細胞を収集して、1×106個/100μlの濃度でRPMI1640中に再懸濁して、100μlの一定分量で上部チャンバーに適用した。細胞を37℃で2時間化学誘引物質の方へ遊走させた。その後に、上部チャンバーの細胞を廃棄して、下部チャンバーを50μlの70mM EDTA含有PBSと混合して、37℃で15分間インキュベートして、メンブレンに付着した細胞を遊離させた。その後、下部チャンバーに遊走した細胞を、細胞計数システム(Scharfe System)を使用して計数した。走化性指数は、刺激に遊走した細胞をネガティブ対照に遊走した細胞で除することによって算出した。
(A.クローニング手順)
EGFPをタグ付けしたラット及びマウスのイソQCに関するクローニングのために、ベクターpEGFP-N3(Invitrogen)のEGFP配列をベクターpcDNA 3.1(Invitrogen)に、プライマー1(センス)(配列番号61)及び2(アンチセンス)(配列番号62)(以下の表10参照)を増幅のために用いて導入した。断片をpcDNA 3.1のXhoI部位に導入した。生じたベクターをpcDNA-EGFPと命名した。MetI(配列番号53)又はMetII(配列番号54)のいずれかで開始する天然マウス-イソQC、及びMetI(配列番号55)又はMetII(配列番号56)のいずれかで開始するラット-イソQCのcDNAを、ベクターpcDNA-EGFPにおけるEGFPとフレームにおいてC末端で融合させた。プライマー3(センス)(配列番号63)及び4(アンチセンス)(配列番号64)(表10)を、MetIで開始するマウス-イソQC(配列番号53)の増幅のために用い、プライマー5(センス)(配列番号65)及び4(アンチセンス)(配列番号64)(表10)を、MetIIで開始するマウス-イソQC(配列番号54)の増幅のために用いた。プライマー6(センス)(配列番号66)、7(アンチセンス)(配列番号67)、並びに5(センス)(配列番号65)、及び7(アンチセンス)(配列番号67)(表10)をそれぞれ、MetI(配列番号55)並びにMetII(配列番号56)で開始するラット-イソQCの増幅のために用いた。EcoRI及びNotIの制限部位を採用するベクターpcDNA-EGFPに断片を挿入し、断片の正確な挿入を配列決定によって確認した。また、MetI及びMetIIで各々開始し、セリン55(MetIから計数)で終止するマウス-イソQC(両方に関して配列番号57及び58)並びにMetI及びMetIIで各々開始し、セリン55(MetIから計数)で終止するラット-イソQC(両方に関して配列番号59及び60)を、プライマー3(センス)(配列番号63)及びプライマー8(アンチセンス)(配列番号68)(表10)をMetIで開始するマウス-イソQCのN末端断片について、並びにプライマー5(センス)(配列番号65)及びプライマー8(アンチセンス)(配列番号68)(表10)をMetIIで開始する断片について用いて、ベクターpcDNA-EGFPにおけるEGFPとC末端で融合させた。ラット-イソQCのN末端断片を、プライマー6(センス)(配列番号66)及びプライマー9(アンチセンス)(配列番号69)(表10)をMetIで開始するものについて、並びにプライマー5(センス)(配列番号65)及びプライマー9(アンチセンス)(配列番号69)(表10)をMetIIで開始するものについて用いて増幅させた。その後、すべてのベクターを細胞培養目的のために、EndFree Maxi Kit(Qiagen)を用いて単離した。
ヒトアストロサイトーマ細胞株LN405及びヒト神経芽細胞種細胞株SH-SY5Yを、適切な細胞培養液(ダルベッコ変法イーグル培地、10%ウシ胎仔血清)において、10%CO2の加湿した大気下で、37℃で培養した。トランスフェクションのために、LN405細胞及びSH-SY5Y細胞を2ウェルチャンバースライド(BD Falcon)において培養し、80%培養密度まで増殖させ、製造元のマニュアルに従って、Lipofectamin2000(Invitrogen)及び(工程Aにおいて先に得られた)個々のプラスミドを含む溶液におけるインキュベーションによってトランスフェクトした。5時間後に溶液を適切な増殖培地と交換し、細胞を一晩増殖させた。
組織化学的分析のために、トランスフェクションの1日後に、LN405細胞及びSH-SY5Y細胞をD-PBS(Invitrogen )で2回洗浄し、氷冷メタノールを用いて−20℃で10分間固定した後、D-PBSの室温で5分間の3回の洗浄工程を実施した。ゴルジ複合体の染色のために、LN405細胞及びSH-SY5Y細胞を、抗体をD-PBSに1:100に希釈した抗マンノシダーゼIIポリクローナル抗体(Chemicon)とともに室温で3時間インキュベートした。その後、細胞をD-PBSで5分間、3回洗浄した。細胞を、Cy3を結合したヤギ抗ウサギIgG二次抗体とともに暗所で室温で45分間インキュベートした。その後、試料をD-PBSで5分間、3回洗浄し、核の染色のために1μg/mLの4',6-ジアミジン-2'-フェニルインドール-(DAPI)溶液(Roche)とともにインキュベートし、D-PBSで1回洗浄した。カバーガラスを顕微鏡スライドの上にCitifluor(Citiflour Ltd., Leicester, UK)とともに載せた。細胞を共焦点レーザー走査顕微鏡(Carl-Zeiss)で観察した。
哺乳類細胞におけるマウス-イソQC及びラット-イソQCの細胞内局在並びに推定上の開始メチオニンの関連性を研究するために、メチオニンI(MetI)又はメチオニンII(MetII)のいずれかで開始するマウス-イソQC-EGFP融合体及びラット-イソQC-EGFP融合体を作製した。ヒトLN405細胞及びSH-SY5Y細胞を一過性にトランスフェクトし、共焦点レーザー走査顕微鏡を用いて細胞内分布を検討した。マウス-イソQC(MetI)-EGFP及びラット-イソQC-(MetI)-EGFP融合タンパク質の発現は結果的に、導入遺伝子を発現する事実上すべての細胞の核の近くに明瞭な染色を生じた(図9a、10a、11a、及び12a)。細胞性マンノシダーゼIIの対比染色によって、LN405及びSH-SY5Yにおけるゴルジ複合体内に、マウス-イソQC(MetI)-EGFP及びラット-イソQC(MetI)-EGFPの存在が明らかとなった。マウス-イソQC(MetII)-EGFP及びラット-イソQC(MetII)-EGFP融合タンパク質の発現は結果的に、非常に類似した蛍光染色を生じ、このことは、マンノシダーゼIIの局在性と十分に一致した(図9a、10a、11a、及び12a)。このように、マウス-イソQC及びラットイソQCの細胞内分布は、N末端メチオニンとは無関係である。
(A.RAW264.7細胞の特徴づけ)
マウス単球/マクロファージ細胞株RAW264.7(以下:RAW)をCLS(Eppelheim, Germany)から得た。NucleoSpin RNA IIキット(Macherey Nagel)を用いて、製造元の説明書に従って、RNAを単離した。1000ng定量のRNAを、ランダムプライマー(Roche)及びSuperscript II(Invitrogen)を用いてcDNAに逆転写した。QuantiTect SYBR Green RT-PCRキット(Qiagen)を用いてRotorgene3000(Corbett Research)において定量的リアルタイムPCRを実施した。適用したプライマーを表11A及び11Bに示す。
THP1(ヒト急性単球性白血病)細胞をCLS(Eppelheim, Germany)から得た。RNAの単離、cDNAの合成、及びPCRを、RAW細胞について説明したとおり実施した。ヒトQPCT及びヒトQPCTLの定量のために用いたプライマーを表12に示す。
マウスQPCT(mQPCT)のエクソン1内の産物を増幅しているプライマー対を用いて、PCR産物を得ることができた(図13(a)、プライマー対F5/F6(配列番号70及び73)、F5/R14(配列番号70及び74)、F5/R16(配列番号70及び75);表11A参照)。対照的に、エクソン2からエクソン7までの領域に結合するプライマー対は、RAW細胞から単離したcDNAを用いた産物を検出しなかった(図13(a)、プライマー対F5/R12(配列番号70及び76)、F5/R20(配列番号70及び77)、F3/R4(配列番号71及び78)、F3/R20(配列番号70及び77)、F3/R2(配列番号70及び79)、F11/R22(配列番号72及び80)、表11A、Qiagenから得たプライマー)。すべてのプライマー対は、B16マウスメラノーマ細胞から及びマウス脳組織から単離したcDNAを用いて産物を増幅した。結果的に、RAW細胞は、全長のmQPCT mRNAを発現しなかった。RAW細胞、B16細胞、及びマウス脳組織は、マウスQPCTL(mQPCTL)を発現した(表11B、図13(a))。RAW細胞は、全長のmQPCT RNAを発現しなかったが、mQPCTLを発現した;それゆえ、この細胞株は、mQPCTL活性の阻害剤をインビトロで試験するための有用なツールである。
(RAW264.7におけるpGlu-MCP-1形成の阻害)
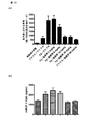
マウス単球/マクロファージ細胞株RAW264.7を用いて、LPS刺激後の細胞によって分泌されるMCP-1のN末端ピログルタミン酸(pGlu)の形成に及ぼすグルタミニルシクラーゼ(QC)阻害剤及びイソグルタミニルシクラーゼ(QPCTL)阻害剤の効果を調べた。96ウェルマイクロプレートにおいて1ウェルあたり40.000個/100μLを蒔種し、10%FBS及びゲンタマイシン(Invitrogen)を含むDMEM(Invitrogen)において増殖させた。24時間後、培地を、適切な濃度の阻害剤又は対照物(DMSO)を含む150μLのDMEM/10%FBS/ゲンタマイシンに交換した。阻害剤スクリーニング実験のために、試験化合物を10μMの終濃度で用いた。各化合物につき、4回の複製を実施した。30分後、阻害剤適用細胞を、LPS(10ng/mL、大腸菌株055:B5由来、Sigma)の添加によって刺激した。LPS刺激の24時間後、上清を回収し、MCP-1の分析まで−20℃で保存した。特異的ELISAによって、総MCP-1及びpGlu1-MCP-1(mMCP-1 N1pE)を決定した。
総mMCP-1及びmMCP-1 N1pEの決定のために、特異的ELISAを展開した。簡潔には、コーティング緩衝液(PBS、pH7.4)において96ウェルプレートの1ウェルあたり、25ngの捕捉抗体ウサギ抗mJE(Peprotech)をコーティングした。プレートを室温で一晩インキュベートした。その後、各ウェルを200μLのブロッキング緩衝液(タンパク質非含有(TBS)ブロッキング緩衝液(Perbio))の添加によって2時間ブロッキングした後、300μLの洗浄緩衝液(タンパク質非含有T20(TBS)ブロッキング緩衝液(Perbio))を用いて3回洗浄した。希釈緩衝液(タンパク質非含有T20(TBS)ブロッキング緩衝液)を用いて、標準ペプチド(Peprotech)及び試料を希釈し、100μLを試験プレートに適用した。試験試料及び標準ペプチドのインキュベーションを室温で2時間実施した後、洗浄緩衝液を用いてプレートを3回洗浄した。mMCP-1 N1pEの検出のために、抗pE1-MCP-1特異的モノクローナル抗体クローン4B8(Probiodrugによって製造、0.65mg/mL)を0.25μg/mLの濃度で、1:2000の希釈における抗マウスHRP接合体(KPL)との組み合わせで適用した。総MCP-1の検出のために、ラット抗マウスMCP-1(R&D Systems、1mg/mL)を0.25μg/mLの濃度で、1:2000の希釈における抗ラットHRP接合体(Sigma)との組み合わせで適用した。抗体を希釈緩衝液において希釈し、各ウェルに100μLの容積で適用し、室温で2時間インキュベートした。その後、ウェルを300μLの洗浄緩衝液で5回洗浄した後、各ウェルに100μLの容積で色素原SureBlue(KPL)を適用した。暗所で30分間インキュベートした後、50μLの停止溶液(1.2N H2SO4)を用いて該反応を抑止し、450nmで吸光度を決定した。550nmの基準波長を、450nmにおける試料吸光度から減算した。
RAW264.7細胞におけるmMCP-1 N1pEアッセイを用いて、マウスQC陰性かつマウスイソQC陽性の細胞株RAW264.7によるpGlu1-MCP-1の形成を抑制するQC阻害剤の有効性を示すことができた。ヒトイソQCについての阻害剤定数とpGlu-MCP-1形成の阻害との相関が認められた。イソQCの強い阻害を示す化合物(Ki<100nM)のみがpGlu-MCP-1の形成を効率よく阻害できるのに対し、強いQC阻害剤であるが弱いイソQC阻害剤は、RAW264.7細胞におけるpGlu-MCP-1形成における弱い細胞性効力しか示さない。
このように、RAW細胞は、QCによる基質変換の影響を潜在的に妨害することとは無関係にイソQCの阻害を研究するための優れた系を提供する。
(A.宿主株及び培地)
大腸菌株DH5αをプラスミドの増殖のために用い、ピキア・パストリス株X-33を酵母におけるヒトイソQCの発現のために用いた。大腸菌株及びピキア・パストリス株を製造元の説明書(Qiagen(DH5α)、Invitrogen(X-33))に従って増殖させ、形質転換し、及び分析した。大腸菌に必要な培地、すなわち、ルリア・ベルターニ(LB)培地を製造元の推奨に従って製造した。ピキア・パストリスに必要な培地、すなわち、BMMY、BMGY、YPD、YPDS、及び抗生物質の濃縮物、すなわちZeocinを、ピキアマニュアル(Invitrogen、カタログ番号K1740-01)において説明されているとおり製造した。また、該マニュアルには、酵母の取り扱いについてのすべての関連する説明も含む。
標準的な分子生物学の技術を適用して、すべてのクローニング手順を実施した。ピキア・パストリスX-33における発現のために、pPiCZαAベクター(Invitrogen)を用いた。オープンリーディングフレームのコドン43(Glu43)で開始する成熟マウスイソQCのcDNA(メチオニンIIから計数、すなわち、図15において示されるように、膜貫通配列は取り除かれ、酵母発現ベクターには挿入されていない。)を、分泌経路にタンパク質を配向させるpPiCZαA-プラスミドでコードしたα因子分泌シグナルとフレームにおいて融合させた。プライマー10(センス)(配列番号83)及びプライマー11(アンチセンス)(配列番号84)(表13)を利用するマウスイソQCの増幅後、断片を、NotI及びEcoR Iの制限部位を採用する発現ベクターへと挿入した。グリコシル化部位の挿入のために、プライマー12(センス)(配列番号85)及びプライマー13(アンチセンス)(配列番号86)(表13)によって、イソQCのオープンリーディングフレームのコドン56に突然変異を導入した(Ile56Asn)(メチオニンIIが該タンパク質の最初のアミノ酸であると再度仮定)。標準的なPCR技術に従って突然変異誘発を実施した後、DpnIを用いて親DNAを消化した(quik-change II位置指定突然変異誘発キット、Stratagene、カタログ番号200524)。
製造元の説明書(BioRad)に従って、電気穿孔によるピキア・パストリスコンピテント細胞の形質転換のために、1〜2μgのプラスミドDNAを適用した。100μg/mLのZeocinを含むプレートにおいて選択を実施した。マウスイソQC発現のための組換え酵母クローンを試験するために、2mLのBMGYを含む10mLのコニカルチューブにおいて細胞を24時間増殖させた。その後、酵母を遠心分離し、0.5%メタノールを含む2mLのBMMYにおいて再懸濁した。この濃度を、メタノールを24時間ごとに約72時間添加することによって維持した。その後、上清におけるQC活性を決定した。最大活性を示すクローンをさらなる実験及び発酵のために選択した。
ピキア・パストリスにおけるイソQCの大規模発現を、5L反応器において実施した(Biostad B;Braun Biotech, Melsungen, Germany)。簡潔には、微量の塩を追加したpH5.5の基礎塩培地において発酵を実施した。まず、バイオマスを1回分及び流加相において、唯一の炭素源としてのグリセロールを用いて約28時間蓄積した。Invitrogenによって推奨される3工程特性に従ったメタノール供給によって、イソQCの発現をおよそ65時間の完全発酵のために開始した。発現後、細胞を遠心分離(8000×g、20分)によって培地から分離し、ペレットを廃棄した。アンモニアを上清に0.8Mの終濃度まで添加し、その後再度遠心分離し、結果として生じる上清を、第一の精製工程のためにさらに用いた。4工程プロトコールを利用して、イソQCタンパク質を精製した(表14)。精製したタンパク質をQC活性の決定及び金属含有量の分析のために用いた。精製を図16において示す。
これらのアッセイを、実施例5において説明したとおり実施した。
(F.ピキア・パストリスにおけるラット-イソQCの発現及び精製)
(ラットイソQCをコードするプラスミドベクターの分子クローニング)
標準的な分子生物学の技術を適用して、すべてのクローニング手順を実施した。ピキア・パストリスX-33における発現のために、pPiCZαAベクター(Invitrogen)を用いた。オープンリーディングフレームのコドン43(Glu43)で開始する成熟ラットイソQCのcDNA(メチオニンIIから計数、図15)を、分泌経路にタンパク質を配向させるα因子をコードしたプラスミドとフレームにおいて融合させた。プライマー14(配列番号87)をセンスとして、かつプライマー15(配列番号88)をアンチセンスとして利用する増幅(表15)の後、断片を、NotI及びEcoRIの制限部位を採用する発現ベクターへと挿入した。プライマー16(センス)(配列番号89)及びプライマー17(アンチセンス)(配列番号90)を用いて、突然変異をコドン56において導入した(Ile56Asn)。標準的なPCR技術に続いてDpnIを用いた親DNAの消化に従って、突然変異誘発を実施した(quik-change II位置指定突然変異誘発キット、Stratagene、カタログ番号200524)。
ピキア・パストリスにおけるイソQCの大規模発現を、5L反応器において実施した(Biostad B;Braun Biotech, Melsungen, Germany)。簡潔には、微量の塩を追加したpH5.5の基礎塩培地において発酵を実施した。まず、バイオマスを1回分及び流加相において、唯一の炭素源としてのグリセロールを用いて約28時間蓄積した。Invitrogenによって推奨される3工程特性に従ったメタノール供給によって、イソQCの発現をおよそ65時間の完全発酵時間のために開始した。発現後、細胞を遠心分離(8000×g、20分)によって培地から分離し、ペレットを廃棄した。上清のpH値を中性に調整し、再度遠心分離し、第一の精製工程のために適用した。3工程プロトコールを利用して、イソQCタンパク質を精製した(表16)。精製を図17におけるSDS-PAGE分析によって示す。
精製した組換えタンパク質ヒトイソQC及びラットイソQCタンパク質をアジュバントとともに用いて、ウサギを免疫した。5回の注射の後、ウサギを屠殺し、抗体をレクチンアフィニティカラムクロマトグラフィーによって精製した。2個体のウサギを、ヒトイソQC(h-イソQC)を用いて免疫し、さらに2個体は、ラットイソQC(r-イソQC)の注射を受けた。
((1)マウスイソQCの発現及び精製)
メチロトローフ酵母であるピキア・パストリスにおいてマウスイソQCをうまく発現させた。位置56におけるグリコシル化部位を含むグルタミン酸43で開始するタンパク質を5Lの生物反応器における発酵によって、大規模で発現させた。表14において説明したように精製を実施した。精製手順は結果的に、均質な組換えタンパク質の単離を生じた(図16)。
メチロトローフ酵母であるピキア・パストリスにおいてラットイソQCをうまく発現させた。(ピキア・パストリスにおけるh-イソQCの発現に従った)位置56におけるグリコシル化部位を含むグルタミン酸43で開始するタンパク質は、発酵によって大規模に発現させることができた。表16において説明したように精製を実施した。精製手順は結果的に、均質な組換えタンパク質の単離を生じた(図17)。
いくつかの異なるペプチド基質を分析した(表17)。すべての基質がマウスイソQC及びラットイソQCによって変換され、ヒトイソQCと類似の広範な基質特異性を示唆した。最大特異性定数(kcat/KM)を、N末端グルタミニル残基に隣接した大きな疎水性アミノ酸を有する基質、すなわちGln-Phe-Ala(QFA)について観察した。対照的に、該位置で負に帯電した残基は、Gln-Glu(QE)について観察されるように特異性における顕著な低下をもたらし、マウスイソQCの負に帯電した活性部位を示した。ヒトイソQCと比較して、マウスイソQCは、2〜3倍高い酵素活性を発揮した(図18)。広範な特異性は、本発明において説明したすべてのイソQCによる多くの異なる生理学的基質の変換を支持している。
(先のG.において作製した)ポリクローナルイソQC抗体の特異性を調べるために、HEK293細胞にヒトイソQC、ラットイソQC、ヒトQC、及びラットQCをトランスフェクトし、ウェスタンブロットを用いて発現を分析した(図19)。ヒトイソQC抗体pAb 8695の適用によって、ヒトイソQC、ヒトQC、ラットイソQC、及びラットQCをトランスフェクトした細胞における37kDaにおけるバンドが検出された。最も高強度のシグナルは、ヒトイソQCをトランスフェクトしたHEK293細胞において観察された(図16a)。イソQCは、ゴルジ複合体に局在する酵素である。従って、ヒトイソQCをトランスフェクトした細胞由来のシグナルが期待された。シグナル強度における差は、基本的に発現したヒトイソQCの検出を示した。Restore(商標)Western Blot Stripping Buffer(Thermo Scientific)を用いたウェスタンブロットメンブレンを洗浄して、ヒトQC抗体pAb 8695とともにインキュベートした後、hQCをトランスフェクトした細胞の培地におけるシグナルが現れた(図19b)。このように、作製したポリクローナルh-イソQC抗体は、イソQCとQCの間に交差反応を示さない。
(A.マトリックス支援レーザー脱離/イオン化飛行時間型質量分析)
マトリックス支援レーザー脱離/イオン化質量分析を、線形時間の飛行分析装置を備えたVoyager De-Pro(Applied Biosystems, Darmstadt)を用いて実施した。機器には337nmの窒素レーザー、電位加速源、及び1.4mの飛行チューブが装備されていた。検出器の操作は、正イオンモードであった。試料(5μL)を等容積のマトリックス溶液と混合した。マトリックス溶液としてシナピニン酸を用い、20mgのシナピニン酸(Sigma-Aldrich)を1mLのアセトニトリル/0.1%TFA含有水(1:1(v/v))に溶解することによって製造した。少量(およそ1μL)のマトリックス-分析物混合物をプローブチップに転移した。
別個の実験において、N末端グルタミンで開始する全長の組換えケモカインCCL21(Q)-76(MCP-1)、CCL71(Q)-76(MCP-3)、CCL81(Q)-76(MCP-2)、及びCCL131(Q)-75(MCP-4)の各1つを25mMトリス/HCl pH7.6に、CCL2については20μg/mL、並びにCCL7、8、及び13については10μg/mLの濃度で個別に溶解した。個々のCCLを組換えヒトイソQCとともに37℃で2時間プレインキュベートした後、組換えヒトDP4(Probiodrug)とともに37℃でインキュベートし、又は前もってイソQCを適用せずにDP4とともにインキュベートするかのいずれかであった。結果として生じるDP4切断産物を、示された時点において最長4時間まで分析した。切断産物を、Maldi-TOF質量分析を用いて分析した。
ヒトDP4のヒトMCPへの適用は、ヒト組換えMCPのN末端配列(Gln-Pro)がDP4切断部位に似ているので、最初の2つのアミノ酸のN末端分解をもたらす(図21a、22a、23a、24a)。対照的に、MCP-1、MCP-2、MCP-3、及びMCP-4と組換えヒトイソQCとのプレインキュベーションは、ヒトMCPをヒトDP4によるさらなる切断から保護するN末端のpGlu残基の形成をもたらす(図21b、22b、23b、24b)。それゆえ、すべてのヒトMCPであるMCP-1(CCL2)、MCP-2(CCL8)、MCP-3(CCL7)、及びMCP-4(CCL13)は、インビトロでのヒトイソQCの基質である。
(A.実験手順)
C57/B16JマウスをCharles River Laboratories(Kisslegg, Germany)から購入した。各実験につき、マウスを齢及び性別で符合させた。25mL/体重kgの滅菌8%(w/v)チオグリコール酸(Sigma-Aldrich)の腹腔内注射を用いて、腹膜炎を誘発させた。チオグリコール酸刺激の30分前に、動物に、異なる用量のイソQC阻害剤イソQC-Iを注射した。腹膜の洗浄のために、動物を、2%イソフルランを用いて麻酔した。チオグリコール酸注射の4時間後に8mLの滅菌PBSを用いて腹膜を洗浄することによって、腹膜滲出液を回収した。1mLの洗浄液の細胞を遠心分離(300g、10分)によって回収し、BD Trucountチューブのための製造元の説明書に従って染色した(BD Trucountチューブ;カタログ番号340334;BD Biosciences, Heidelberg, Germany)。細胞をCD16/32(Caltag)で4℃で15分間ブロッキングし、7/4-FITC(Serotec, Dusseldorf, Germany)/Ly6G-PE(Miltenyi, Bergisch Gladbach, Germany)及びIgG1-PE(BD)/IgG2a-FITC(Miltenyi)をアイソタイプ対照として用いて、室温で15分間染色した。染色後、赤血球をBD FACSLyse(BD)で暗所で室温で15分間溶解した。PBSによる洗浄後、フローサイトメトリー分析を、基準標準物質としての1試料あたり5000個のビーズに基づいたBD FACSCalibur(BD)において実施した。
C57/B16Jマウスの腹膜へのチオグリコール酸の注射後、この区画への単球の浸潤を、FACS分析を用いて検出した。このモデルにおけるQC/イソQC特異的阻害剤であるイソQC-Iの適用は、浸潤している単球の用量依存的減少を引き起こす。現象はすでに、6mg/kgのイソQC-Iを用いて観察することができた。18mg/kgは、基線値まで単球の浸潤を減少させ、塩類溶液単独を注射した場合にこのことは検出された(図25a)。同様に、個々の洗浄液におけるpGlu-MCP-1の決定は、pGlu含有量の減少を示し、標的酵素における阻害剤の作用に応じた治療効果を示唆している(図25b)。
QPCTLノックアウトマウスをゲノム突然変異誘発アプローチにおいて作出した。
QPCTLノックアウト動物におけるチオグリコール酸の適用は、腹膜への単球の浸潤を刺激しない。しかしながら、QPCTL野生型同腹仔において、イソQCの活性が存在しており、結果的にMCPの適切な成熟を生じているので、単球の浸潤が検出された(図26a)。顆粒球の浸潤は、イソQC(QPCTL)ノックアウトによって影響されなかった(図26b)。単球の低い浸潤は、QPCTLノックアウトマウスにおける低濃度のpGlu-MCP-1と相関していたのに対し、総MCP-1レベルは正常のままであった(図27)。それゆえ、マウスイソQCノックアウトは、pGlu-MCP-1形成の影響を有し、pGlu-MCP-1の減少は、この動物モデルの腹膜への単球の動員に及ぼす影響を有する。加えて、原理の遺伝子的立証は、チオグリコール酸誘発性腹膜炎におけるイソQC阻害剤の適用の特異性を実証している。該実験によって、イソQCの阻害がpGlu-MCPの非活性化を結果的に生じ、それゆえ、炎症性疾患のための新規の治療戦略であることが立証されている。
(A.血漿及びPBMCの単離)
末梢血単核細胞(PBMC)の単離のために、QPCTLノックアウト動物及び野生型同腹仔を、2%イソフルランを用いて麻酔し、ヘパリン処理した血液を心穿刺により回収した。その後、血液を、同じ遺伝的背景を有する動物からプールし(それぞれ、イソQCホモ接合性ノックアウト動物及び野生型動物)、ヘパリン処理した血液を1000×gで10分間遠心分離して得た血漿を回収した。血漿を一定分量で分注し、−80℃で保存した。沈降した血液細胞を細胞培養液(RPMI1640、10%FBS、100μg/mLゲンタマイシン)において再懸濁した。
QPCTLノックアウトマウス及び野生型同腹仔から単離したPBMCの刺激は、培養上清における高い総MCP-1濃度をもたらす。刺激していないPBMCは、少量の総MCP-1しか分泌しない(図28a)。野生型動物由来の細胞の培地において検出された総MCP-1レベルは、ノックアウト動物由来の個々の細胞と比較して高い。野生型PBMCから分泌されるMCP-1は、pGlu修飾したN末端を有しており、等量の総MCP-1及びpGlu-MCP-1によって示されている(図28a、28b)。対照的に、QPCTLノックアウトマウス由来の細胞は、ELISAによって検出される少量のpGlu-MCP-1(図28a)及び野生型同腹仔における90%超と比較したおよそ10%の低い比のpGlu-MCP-1対総MCP-1(図28b)によって示されるように、N末端でpGlu修飾された微量のMCP-1しか生じない。
(A.TXRF測定)
マウスイソQCの精製後に、10mMトリス-HCl、pH7.6においてあらかじめ平衡化しておいたSephadex G-25迅速脱塩カラム(1.0×10cm)を用いるサイズ排除クロマトグラフィーによって酵素を脱塩した。タンパク質を3mg/mLに濃縮した。全反射X線蛍光(TXRF)を用いて元素分析を実施した。溶出緩衝液を背景対照として用いた。5μLの希釈していない試料溶液又は対照緩衝液をTXRFクォーツガラス試料支持体に適用し、赤外線照射の下で乾燥させた。その後、5μLの希釈したSe標準水溶液(内部標準物質、Aldrich;Taufkirchen, Germany)を各試料に添加し、再度乾燥させた。X線蛍光信号を100秒間回収した。すべての決定について、Link QX 2000検出器/分析装置(Oxford Instruments, High Wycombe, UK)に接続したモリブデン及びタングステン主要X線源を含むExtra II TXRFモジュール(Seifert, Ahrensburg, Germany)を用いた。X線源は、50kV及び38mAで操作した。
マウスイソQC及びマウスQCを、5mMの1,10-フェナントロリン、5mM EDTA、500mM NaCl含有50mMビストリス(pH6.8)を含む1.0Lの緩衝液に対する4℃における一晩の透析によって、マウスイソQC及びマウスQCを失活させた。1Lの、50g/LのChelex-100(Bio-RAD, Munich)を含む50mMビストリス(pH6.8)、500mM NaCl、又は50g/LのChelex-100を含む10mM NaH2PO4(pH6.8)に対する4℃での透析によって、キレート剤をアポ酵素から分離した。透析の2時間後及び4時間後に、緩衝液を2回交換した。最終的な透析は5時間実施した。すべての緩衝液を金属非含有ポリスチレン容器において製造した。その後、アポ酵素を4℃、20.000×gで1時間遠心分離し、タンパク質濃度をUV吸光度によって決定した。
分光分析のために、タンパク質を10mM NaH2PO4において調製した。マウスQC及びマウスイソQCのCDスペクトルを、1mm経路長のクォーツキュベットを用いるJasco J-715スペクトル偏光計で獲得した。190〜260nmの10回走査の平均を算出し、緩衝液スペクトルの減算によってスペクトルを補正した。二次構造要素の%を、Yangの方法に基づいたJasco二次構造概算プログラムを用いて算出した。アポ酵素及び酵素の再活性化を、分光分析後のQC活性測定によって確認した。
マウスQCについて、1mol亜鉛/酵素molの金属含有量を先に決定した。また、QCの亜鉛結合モチーフは、イソQCの配列において保存されている。それゆえ、マウスイソQCの金属含有量を、TXRFを用いて分析した。3つの独立した酵素試料の測定によって、亜鉛0.99±0.38mol/酵素molの亜鉛含有量を決定した。このように、イソQCタンパク質は、本発明において初めて示されるように、単一の亜鉛メタロ酵素を表す。
Claims (50)
- a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防するためのイソQC阻害剤。 - a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防するためのイソQC阻害剤の使用。 - a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防する薬剤の製造のためのイソQC阻害剤の使用。 - a.慢性及び急性炎症、例えば、関節リウマチ、粥状硬化、再狭窄、膵炎、骨粗鬆症、
b.他の炎症性疾患、例えば、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症、
c.神経炎症、並びに
d.神経炎症から結果として生じ得る神経変性疾患、例えば、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症
からなる群から選択される炎症性の疾患又は容態を治療及び/又は予防する方法であって、治療的有効量のイソQC阻害剤が該治療及び/又は予防を必要とする対象に投与する、前記方法。 - 前記炎症性疾患が、関節リウマチ、粥状硬化、再狭窄、膵炎、及び骨粗鬆症から選択される慢性及び急性炎症である、請求項1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
- 前記炎症性疾患が、神経因性疼痛、移植片拒絶反応/移植片不能/移植性脈管障害、HIV感染/エイズ、妊娠中毒症、結節性硬化症、ギラン・バレー症候群、慢性炎症性脱髄性多発性神経根症、及び多発性硬化症から選択される、請求項1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
- 前記炎症性疾患が神経炎症である、請求項1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
- 前記炎症性疾患が、神経炎症から結果として生じ得る神経変性疾患である、請求項1〜4のいずれか一項記載のイソQC阻害剤、使用、又は方法。
- 前記神経変性疾患が、軽度認知障害(MCI)、アルツハイマー病、ダウン症候群における神経変性、家族性英国型認知症、及び家族性デンマーク型認知症から選択される、請求項8記載のイソQC阻害剤、使用、又は方法。
- 前記イソQC阻害剤が、抗炎症薬、向知性薬、神経保護薬、抗パーキンソン病薬、アミロイドタンパク質沈着阻害剤、βアミロイド合成阻害剤、抗うつ薬、抗不安薬、抗精神病薬、及び抗多発性硬化症薬、アンギオテンシン変換酵素(ACE)の阻害剤、アンギオテンシンII受容体遮断薬、利尿薬、カルシウムチャネル遮断薬(CCB)、β遮断薬、血小板凝集阻害剤、コレステロール吸収モジュレーター、HMG-Co-A還元酵素阻害剤、高密度リポタンパク質(HDL)を増加させる化合物、レニン阻害剤、IL-6阻害剤、抗炎症性コルチコステロイド、抗増殖薬、一酸化窒素ドナー、細胞外マトリックス合成の阻害剤、増殖因子又はサイトカインシグナル伝達阻害剤、MCP-1アンタゴニスト、及びチロシンキナーゼ阻害剤からなる群から選択されるさらなる薬剤と組み合わせて投与される、請求項1〜9のいずれか一項記載のイソQC阻害剤、使用、又は方法。
- 前記疾患及び/又は容態がヒトを苦しめる、請求項1〜10のいずれか一項記載のイソQC阻害剤、使用、又は方法。
- 請求項1〜9のいずれか一項記載のイソQC阻害剤又は請求項10記載の組み合わせを含む医薬組成物。
- 前記イソQC阻害剤が式(I)の化合物、又はそのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体
R1は、-C3-8カルボシクリル-ヘテロアリール、-C2-6アルケニルヘテロアリール、-C1-6アルキルヘテロアリール、又は(CH2)aCR5R6(CH2)bヘテロアリールを表し、式中、a及びbは独立して、0〜5の整数を表し、但し、a+b=0〜5であり、かつR5及びR6が、それらの結合する炭素と共にC3-C5シクロアルキル基又は二環式ヘテロアリール基を形成するアルキレンであり;
ここで、上記のヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R2は、C1-8アルキル、アリール、ヘテロアリール、カルボシクリル、ヘテロシクリル、-C1-4アルキルアリール、-C1-4アルキルヘテロアリール、-C1-4アルキルカルボシクリル、又はC1-4アルキルヘテロシクリルを表し;
ここで、上記のアリール基及びヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いはR2は、フェニルによって置換されたフェニル、単環式ヘテロアリール基によって置換されたフェニル、ベンジルオキシによって置換されたフェニル、カルボシクリルに縮合したフェニル、ヘテロシクリルに縮合したフェニル、-C1-4アルキル(フェニルによって置換されたフェニル)、-C1-4アルキル(単環式ヘテロアリール基によって置換されたフェニル)、-C1-4アルキル(ベンジルオキシによって置換されたフェニル)、-C1-4アルキル(任意に置換されたカルボシクリルに縮合した任意に置換されたフェニル)、又はC1-4アルキル(任意に置換されたヘテロシクリルに縮合した任意に置換されたフェニル)を表し;
ここで、上記のフェニル基、ベンジルオキシ基、及びヘテロアリール基のいずれも、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく、かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R3は、H、-C1-4アルキル、又はアリールを表し;
ここで、上記のアリールは、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、1つ以上のC1-2アルキル基によって任意に置換されたカルボシクリル環を形成するよう結合し;
或いは、R2及びR3は、フェニルに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はフェニルは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、単環式ヘテロアリールに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はヘテロアリールは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R4は、H、-C1-8アルキル、-C(O)C1-6アルキル、又は-NH2を表し;
Xは、O又はSを表し;かつ
Yは、O又はSを表す、請求項1〜12のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。 - R1が、二環式ヘテロアリール基を表す、請求項13記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R1が、1個又は2個の窒素原子を含む5員環に縮合したベンゼン環又はピリジン環を表す、請求項14記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- 結合点が、ベンゼン環又はピリジン環を介している、請求項15記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R1が-C1-6アルキルヘテロアリールを表す、請求項18記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R1のヘテロアリール基が、C1-4アルキル、C1-4アルコキシ-、及びハロゲンから選択される1つ以上の置換基によって任意に置換された1〜3個の窒素原子を含む5員環である、請求項19記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R2が、アリール、ヘテロアリール、フェニルによって置換されたフェニル、ヘテロシクリルに縮合したフェニルを表し、又はR2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成し;上記のアリール、ヘテロアリール、フェニル、ヘテロシクリル、及びカルボシクリルが任意に置換されている、請求項13〜24のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R2が、フェニルによって置換されたフェニルを表し、上記のフェニル基が、同じでも又は異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1つ以上の置換基によって任意に置換されている、請求項25記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R2が-ビフェニル-4-イルである、請求項26記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R2が、同じでも又は異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1、2、又は3個の置換基によって任意に置換されたフェニルを表す、請求項25記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R2が、n-プロピルオキシによって置換されたフェニルである、請求項28記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R3がHを表す、請求項13〜29のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成する、請求項13〜25のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- R4がHを表す、請求項13〜31のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- XがOを表す、請求項13〜32のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- YがOを表す、請求項13〜33のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。
- 式(I)の化合物が、
5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-5-メチルフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-フルオロ-5-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ブロモ-5-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-フルオロ-4(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-3-メトキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-ブロモ-4-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-[3-(1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
5-(2-ブロモ-5-フルオロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-[3-(5-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-フェニルフェニル)イミダゾリジン-2,4-ジオン;
5-(3-クロロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-[3-(4-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン;
5-(3-クロロフェニル)-1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
3-(1H-ベンズイミダゾール-5-イル)-1',3'-ジヒドロ-2H,5H-スピロ[イミダゾリジン-4,2'-インデン]-2,5-ジオン;
5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-4-チオキソイミダゾリジン-2-オン;
3-(1H-ベンズイミダゾール-5-イル)-5-チオキソ-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-6-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-3-メチル-5-フェニルイミダゾリジン-2,4-ジオン;
1-(H-イミダゾ[1,2-a]ピリジン-7-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
又はそのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体から選択される、請求項13〜35のいずれか一項記載のイソQC阻害剤、使用、方法、又は医薬組成物。 - イソQC阻害剤を含む診断アッセイ。
- 前記イソQC阻害剤が、請求項13〜37のいずれか一項において定義したようなその医薬として許容し得る塩、溶媒和物、及び立体異性体を含む化合物である、請求項38記載の診断アッセイ。
- 前記イソQC阻害剤が、(1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオンである、請求項38又は39のいずれか一項記載の診断アッセイ。
- 請求項1〜9のいずれか一項において定義したような疾患及び/又は容態のいずれか1つを診断する方法であって、
-該疾患及び/又は容態で苦しめられていることが疑われる対象から試料を収集する工程、
-該試料をイソQC阻害剤と接触させる工程、及び
-該対象が該疾患及び/又は容態によって苦しめられているか否かを決定する工程、
を含む、前記方法。 - 前記対象がヒトである、請求項41記載の方法。
- 前記イソQC阻害剤が、請求項13〜31のいずれか一項において定義したようなその医薬として許容し得る塩、溶媒和物、及び立体異性体を含む化合物である、請求項41又は42記載の方法。
- 前記イソQC阻害剤が、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオンである、請求項41〜43のいずれか一項記載の方法。
- 前記試料が、血液試料、血清試料、脳脊髄液の試料、又は尿試料である、請求項41〜44のいずれか一項記載の方法。
- 検出手段として請求項38〜40のいずれか一項記載の診断アッセイと決定手段とを含む、請求項41〜45のいずれか一項記載の方法を実施するための診断キット。
- 前記イソQC阻害剤が、配列番号11、12、13、14、15、16、17、18、57、58、59、若しくは60のいずれかの配列を含むポリペプチド又は配列番号2、3、4、5、6、7、8、9、53、54、55、若しくは56のいずれかの配列を含む核酸によってコードされるポリペプチドの群から選択されるポリペプチドのいずれか1つを阻害する、上記の請求項のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
- 前記イソQC阻害剤が、配列番号11若しくは12のいずれかの配列を含むポリペプチド又は配列番号2若しくは3のいずれかの配列を含む核酸によってコードされるポリペプチドの群から選択されるポリペプチドのいずれか1つを阻害する、上記の請求項のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
- 前記イソQC阻害剤が、配列番号11の配列を含むポリペプチド又は配列番号2の配列を含む核酸によってコードされるポリペプチドを阻害する、上記の請求項のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
- 前記イソQC阻害剤が、配列番号12の配列を含むポリペプチド又は配列番号3の配列を含む核酸によってコードされるポリペプチドを阻害する、上記の請求項のいずれか一項記載のイソQC阻害剤、使用、方法、キット、又は医薬組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US9411808P | 2008-09-04 | 2008-09-04 | |
| US61/094,118 | 2008-09-04 | ||
| US17942409P | 2009-05-19 | 2009-05-19 | |
| US61/179,424 | 2009-05-19 | ||
| PCT/EP2009/061440 WO2010026209A1 (en) | 2008-09-04 | 2009-09-04 | Use of isoQC inhibitors |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012502005A true JP2012502005A (ja) | 2012-01-26 |
| JP2012502005A5 JP2012502005A5 (ja) | 2013-03-21 |
| JP5788320B2 JP5788320B2 (ja) | 2015-09-30 |
Family
ID=41226647
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011525553A Active JP5788320B2 (ja) | 2008-09-04 | 2009-09-04 | イソqc阻害剤の使用 |
Country Status (3)
| Country | Link |
|---|---|
| EP (1) | EP2344158B1 (ja) |
| JP (1) | JP5788320B2 (ja) |
| WO (1) | WO2010026209A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012502006A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | 新規の阻害剤 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2762404A1 (en) * | 2009-05-19 | 2010-11-25 | Probiodrug Ag | Mouse models carrying a knock-out mutation of the qpctl-gene |
| EP2606129B1 (en) | 2010-08-19 | 2015-03-25 | Probiodrug AG | Crystal structure of glutaminyl cyclase |
| JP2013541938A (ja) | 2010-09-02 | 2013-11-21 | プロビオドルグ エージー | アイソqc関連障害の治療のためのインビボスクリーニングモデル |
| JP6026425B2 (ja) | 2010-11-02 | 2016-11-16 | プロビオドルグ エージー | イソグルタミニルシクラーゼの結晶構造 |
| CN114874186B (zh) * | 2022-05-16 | 2023-07-11 | 深圳大学 | 一种谷氨酰胺酰基环化酶同工酶抑制剂及其制备方法与应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008034891A2 (en) * | 2006-09-21 | 2008-03-27 | Probiodrug Ag | Novel genes related to glutaminyl cyclase |
| WO2008055947A1 (en) * | 2006-11-09 | 2008-05-15 | Probiodrug Ag | Novel inhibitors of glutaminyl cyclase |
| JP2012502006A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | 新規の阻害剤 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD293584A5 (de) * | 1990-03-23 | 1991-09-05 | Adw,Zi Fuer Organische Chemie,De | Verfahren zur herstellung von neuen 3,5,5-trisubstituierten 1-(benzimidazol-2-yl)-imidazolidin-2,4-dionen bzw. -4-on-2-thionen |
| US20040006011A1 (en) * | 1996-07-12 | 2004-01-08 | Gour Barbara J. | Peptidomimetic modulators of cell adhesion |
| JP4806628B2 (ja) * | 2003-05-05 | 2011-11-02 | プロビオドルグ エージー | グルタミニルシクラーゼ阻害剤 |
-
2009
- 2009-09-04 WO PCT/EP2009/061440 patent/WO2010026209A1/en active Application Filing
- 2009-09-04 JP JP2011525553A patent/JP5788320B2/ja active Active
- 2009-09-04 EP EP09782596.2A patent/EP2344158B1/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008034891A2 (en) * | 2006-09-21 | 2008-03-27 | Probiodrug Ag | Novel genes related to glutaminyl cyclase |
| WO2008055947A1 (en) * | 2006-11-09 | 2008-05-15 | Probiodrug Ag | Novel inhibitors of glutaminyl cyclase |
| JP2012502006A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | 新規の阻害剤 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012502006A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | 新規の阻害剤 |
| US8962860B2 (en) | 2008-09-04 | 2015-02-24 | Probiodrug Ag | Inhibitors of glutaminyl cyclase |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2344158A1 (en) | 2011-07-20 |
| JP5788320B2 (ja) | 2015-09-30 |
| WO2010026209A1 (en) | 2010-03-11 |
| EP2344158B1 (en) | 2017-12-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101432848B1 (ko) | 글루타미닐 사이클라제에 관련된 신규한 유전자 | |
| TWI353985B (en) | Novel compounds | |
| JP5788320B2 (ja) | イソqc阻害剤の使用 | |
| KR102638253B1 (ko) | C5a 억제제로서의 6-5 융합 고리 | |
| RU2567544C2 (ru) | Bir домен iap связывающие соединения | |
| JP5930573B2 (ja) | グルタミニルシクラーゼ阻害剤の新規使用 | |
| CN109475593A (zh) | 用于治疗心血管疾病的组合物和方法 | |
| KR20030022412A (ko) | TAFIa 억제제인 치환된 이미다졸 | |
| US9000183B2 (en) | Cyclohexane-1,2′-indene-1′,2″-imidazol compounds and their use as BACE inhibitors | |
| JP2006500351A (ja) | マトリックスメタロプロテアーゼ−13阻害剤としてのピリミジン−2,4−ジオン誘導体 | |
| US20230374143A1 (en) | A sortilin antagonist for use in the prevention or treatment of hearing loss | |
| US6455532B1 (en) | Pyrazinone thrombin inhibitors | |
| Tokuhara et al. | Discovery of benzimidazole derivatives as orally active renin inhibitors: Optimization of 3, 5-disubstituted piperidine to improve pharmacokinetic profile | |
| US6521625B2 (en) | Pyrazinone thrombin inhibitors | |
| US8889709B2 (en) | Use of isoQC inhibitors in the treatment and prevention of inflammatory diseases or conditions | |
| US7026324B2 (en) | Thrombin inhibitors | |
| JP2014148508A (ja) | グルタミニルシクラーゼ阻害剤の新規使用 | |
| US20240092801A1 (en) | Allosteric akt inhibitors for use in the treatment of hereditary hemorrhagic telangiectasia | |
| AU2012241108B2 (en) | Novel genes related to glutaminyl cyclase |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120903 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120903 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130131 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140107 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140401 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140408 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140702 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141209 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150306 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150605 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150707 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150729 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5788320 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |