JP2012193207A - インターフェロンを用いる肺疾患の処置方法 - Google Patents
インターフェロンを用いる肺疾患の処置方法 Download PDFInfo
- Publication number
- JP2012193207A JP2012193207A JP2012157469A JP2012157469A JP2012193207A JP 2012193207 A JP2012193207 A JP 2012193207A JP 2012157469 A JP2012157469 A JP 2012157469A JP 2012157469 A JP2012157469 A JP 2012157469A JP 2012193207 A JP2012193207 A JP 2012193207A
- Authority
- JP
- Japan
- Prior art keywords
- patients
- interferon
- treatment
- ifn
- lung
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Abstract
【解決手段】例えば特発性肺線維症(IPF)及び喘息等の肺疾患を処置する方法であって、インターフェロンα、インターフェロンβ、又はインターフェロンγ等のエアロゾル化インターフェロンを治療有効量投与することを含む方法が、本明細書で提供される。又、1つ以上のエアロゾル化インターフェロンの薬学的組成物も提供される。一態様において、本発明は、肺疾患に罹患した患者の肺疾患を処置する方法であって、エアロゾル化インターフェロンを治療有効量で投与することを含む、方法を特徴とする。多くの実施形態において、肺疾患は閉塞性肺疾患である。幾つかの実施形態において、肺疾患は喘息又は特発性肺線維症である。
【選択図】なし
Description
本発明に導いたいくつかの研究は、部分的に、研究用NIHグラントR01 HL55791、K07 HL03030、およびM01 RR00096によって支援された。政府は、本発明において一定の権利を有する。
本発明は、エアロゾルインターフェロンを使用して肺疾患を処置する方法、エアロゾル送達のための1つ以上のインターフェロンの製剤、及びエアロゾル沈着を測定する方法に関する。
現行のNAEPP/NIHのガイドラインによる喘息処置の主流は、依然として抗炎症薬であり、中でもコルチコステロイドが最も有効である。しかし、コルチコステロイドの長期投与は、全身性の副作用を伴う。更に、喘息患者の中には、コルチコステロイドに対して耐性を示す者もいる。従って、アレルギー性気道疾患の炎症反応を対象とした新たな薬剤が必要とされている。
13(1):54−59)。
1996 Feb; 153(2):535−9)。Kipsは、免疫処置時にIL−12を投与し、特異的IgEの産生、気道の好酸球増加症、及び気道過敏性を防止することによって、この説をin vivoで確認した。予め感作したマウスのエアロゾル誘発時にIL−12を投与することで、気道の好酸球増加症及び気道過敏性が防止されたが、特異的IgEの産生は減少せず、従って、IL−12がナイーブTh細胞のTh1細胞への分化を刺激し、Th2細胞の発現を抑制する可能性があることが示唆されている。IL−12による抗原誘発性の気道好酸球増加症の阻害は、最初の感作時にはIFN−γに依存するが、第二の誘発時にはIFN−γに依存しなくなる(Brusselle, et
al., Am J Respir Cell Mol Biol 1997 Dec; 17(6):767−71)。更に、エアロアレルゲンの誘発より前に感作したマウスに、ワクシニアウイルスベクターで肺におけるIL−12遺伝子の粘膜遺伝子導入を行ったところ、IFN−γに依存してIL−4、IL−5、気道過敏性及び気道の好酸球増加症が抑制されることが実証されている(Hogan, et al., − Eur J lmmunol 1998 Feb.; 28(2):413−23)。
(1997) J lnterferon Cytokine Res 17(8):
481−7)。喘息患者のBAL液におけるサイトカイン濃度によって、IFN−γの濃度が低いことが判明している(Kang, et al., (1997) J Interferon Cytokine Res 17(8): 481−7)。
21(3): 239−47; Weening, et al., (1995) Eur J Pediatr 154(4): 295−8)。Boguniewiczは、エアロゾル化rIFN−γを、用量を漸増しながら(最大用量500mcg、全試験用量2,400mcg)、5名の軽度アトピー型喘息患者に20日間吸入させる処置を行った(非特許文献1)。全ての患者は、噴霧されたrIFN−γに対して耐性を示したが、最大流量を含む評価エンドポイントにおける顕著な変化は見られなかった。
Pulmonary Multiple Drug Resistant Tuberculosis (MDR−TB) Who have Failed an Appropriate Three Month Treatment”と題したMDR−TB臨床試験では、数箇所(ケープタウン、ポートエリザベス、ダーバン、メキシコ)のMDR−TB患者80名が登録され、二次療法に加えてエアロゾルrIFN−γ(500μg
MWF)又はプラセボを少なくとも6ヶ月間投与するために、患者を無作為化した。しかし、この臨床試験は、喀痰塗抹、M tb培養、又は胸部X線の変化に対する有効性に欠けることから、早期に中断された。
一態様において、本発明は、肺疾患に罹患した患者の肺疾患を処置する方法であって、エアロゾル化インターフェロンを治療有効量で投与することを含む、方法を特徴とする。多くの実施形態において、肺疾患は閉塞性肺疾患である。幾つかの実施形態において、肺疾患は喘息又は特発性肺線維症である。一実施形態において、肺疾患の症状の改善は、予測努力性肺活量(FVC)の値が処置前に比べて、少なくとも約10%の増加、好ましくは少なくとも約20%、又は少なくとも約25%、更には33%の増加によって測定される場合がある。インターフェロンは、インターフェロンα、インターフェロンβ、又はインターフェロンγである場合がある。
例えば、本願発明は以下の項目を提供する。
(項目1)
肺疾患に罹患する対象において肺疾患を処置する方法であって、エアロゾル化インターフェロンを治療有効量投与することを含む、方法。
(項目2)
前記肺疾患が閉塞性肺疾患である、項目1に記載の方法。
(項目3)
前記肺疾患が特発性肺線維症である、項目1に記載の方法。
(項目4)
前記肺疾患が喘息である、項目1に記載の方法。
(項目5)
処置が行われる前の値に比べて、少なくとも10%の予測FVCの増加よりも前記疾患が改善される、項目1に記載の方法。
(項目6)
前記肺疾患に罹患する前記対象が、コルチコステロイド、シクロホスファミド、及びアザチオプリンの1つ以上を使用した処置に対して効果を示さない、項目1に記載の方法。
(項目7)
エアロゾル化インターフェロンが週3回、約250〜750μgの範囲の用量で投与される、項目1に記載の方法。
(項目8)
エアロゾル化インターフェロンが週3回、約500μgの用量で投与される、項目1に記載の方法。
(項目9)
エアロゾル化インターフェロンの前記投与量が計算及び最適化されたものである、項目1に記載の方法。
(項目10)
前記投与が、肺疾患を有する患者の肺におけるインターフェロンの沈着をもたらす、項目1に記載の方法。
(項目11)
前記投与が肺機能検査の結果の改善をもたらす、項目1に記載の方法。
(項目12)
前記インターフェロンがインターフェロンαである、項目1に記載の方法。
(項目13)
前記インターフェロンがインターフェロンβである、項目1に記載の方法。
(項目14)
前記インターフェロンがインターフェロンγである、項目1に記載の方法。
(項目15)
肺疾患を有する患者を処置する方法であって、免疫抑制薬又は抗炎症薬の治療有効量と共に、エアロゾル化インターフェロンの治療有効量を送達することを含む、方法。
(項目16)
前記免疫抑制薬又は抗炎症薬が、コルチコステロイド、アザチオプリン、及びシクロホスファミドからなる群から選択される、項目15に記載の方法。
(項目17)
前記肺疾患が閉塞性肺疾患である、項目15に記載の方法。
(項目18)
前記肺疾患が特発性肺線維症である、項目15に記載の方法。
(項目19)
前記肺疾患が喘息である、項目15に記載の方法。
(項目20)
処置が行われる前の値に比べて、少なくとも10%の予測FVCの増加よりも前記疾患が改善される、項目15に記載の方法。
(項目21)
前記肺疾患に罹患する前記患者が、コルチコステロイド、シクロホスファミド、及びアザチオプリンの1つ以上を使用した処置に対して効果を示さない、項目15に記載の方法。
(項目22)
エアロゾル化インターフェロンが週3回、約250〜750μgの範囲の用量で投与される、項目15に記載の方法。
(項目23)
エアロゾル化インターフェロンが週3回、約500μgの用量で投与される、項目15に記載の方法。
(項目24)
エアロゾル化インターフェロンの前記投与量が計算及び最適化されたものである、項目15に記載の方法。
(項目25)
前記投与が、肺疾患を有する患者の肺におけるインターフェロンの沈着をもたらす、項目15に記載の方法。
(項目26)
前記投与が、肺機能検査の結果の改善をもたらす、項目15に記載の方法。
(項目27)
前記インターフェロンがインターフェロンαである、項目15に記載の方法。
(項目28)
前記インターフェロンがインターフェロンβである、項目15に記載の方法。
(項目29)
前記インターフェロンがインターフェロンγである、項目15に記載の方法。
(項目30)
肺疾患を有する患者を処置するための、エアロゾル化インターフェロンを治療有効量含む、薬学的組成物。
(項目31)
免疫抑制薬又は抗炎症薬も更に含む、項目30に記載の薬学的組成物。
(項目32)
前記免疫抑制薬又は抗炎症薬が、コルチコステロイド、アザチオプリン、及びシクロホスファミドからなる群から選択される、項目30に記載の薬学的組成物。
(項目33)
前記肺疾患が閉塞性肺疾患である、項目30に記載の薬学的組成物。
(項目34)
前記肺疾患が特発性肺線維症である、項目30に記載の薬学的組成物。
(項目35)
前記肺疾患が喘息である、項目30に記載の薬学的組成物。
(項目36)
前記肺疾患に罹患する患者が、コルチコステロイド、シクロホスファミド、及びアザチオプリンの1つ以上を使用した処置に対して効果を示さない、項目30に記載の薬学的組成物。
(項目37)
前記インターフェロンがインターフェロンαである、項目30に記載の薬学的組成物。
(項目38)
前記インターフェロンがインターフェロンβである、項目30に記載の薬学的組成物。
(項目39)
前記インターフェロンがインターフェロンγである、項目30に記載の薬学的組成物。
本発明の方法及び処置法の説明に入る前に、本発明は特定の方法及び記載の実験条件に制限されることはなく、方法及び条件は変更される場合があることが理解されるものとする。又、本発明の適用範囲は添付の特許請求の範囲によってのみ限定されることから、本明細書で使用される用語が単に特定の実施形態の説明を目的としたものであり、限定を目的としたものではないことも理解されるものとする。
具体的な実施形態において、「症状の改善」という用語は、処置前の値に比べて少なくとも10%の予測FVCの改善として評価される。
近年、IFN−γに対する一時的な調節経路を再現した培養細胞で、シグナル伝達経路が研究された(Vilcek, et al., (1994) Int Arch Allergy Immunol 104(4): 311−6; Young, et al., (1995) J Leukoc Biol 58(4): 373−81)。添加したIFN−γが細胞外の受容体領域に結合すると、最初の事象が生じ、細胞内の受容体領域において、既存のシグナル伝達物質及び転写1(STAT−1)のアクチベーターのチロシンリン酸化を生じる。チロシンリン酸化されたSTAT−1のみが活性化され、これはホモダイマー(又はヘテロダイマー)を形成して特異的なDNA配列に結合する。
802−7)。しかし、IRF−1のリン酸化がin vivoで制御されるという明白な証拠は示されていない。STAT−1活性はチロシンリン酸化に依存しており、セリンリン酸化の程度に影響される。しかし、多数の潜在的STAT−1も調節される。IFN−γで一晩処理された細胞は、チロシンリン酸化及びDNA結合活性が刺激されていない細胞より僅かに多いだけであるものの、STAT−1タンパク質の濃度増加が見られる(Pine, et al., (1994) Embo J 13(1): 158−67)。
近年、IPFに罹患した患者の小規模無作為試験が、インターフェロン−γ(IFN−γ)の皮下処理により行われた(Ziesche, et al., (1999) N. Engl. J. Med. 341: 1264−1269)。IFN−γによる処置前及び処置の6ヶ月後における経気管支の生検標本解析では、増殖因子−β(TGF−β)を形質転換する線維化促進サイトカインの異常増加を処理前に示し、結合組織増殖因子(CTGF)はIFN−γによる処置後に顕著な減少を示した。(Ziesche,
et al. (1999) supra)。プレドニゾロンのみで処置された患者は、TGF−β及びCTGFの濃度変化が見られなかった。
エアロゾル送達
発明の広範な態様において、肺疾患に罹患した患者の喘息及び特発性肺線維症(IPF)等の肺疾患を処置する方法は、インターフェロン−γ等のエアロゾル化インターフェロンを肺疾患の症状が改善する治療有効量で投与することを含む。症状の改善とは、処置前の値と比較した予測FVCの少なくとも10%以上の増加である場合がある。好ましい実施形態において、エアロゾル化IFN−γは、コルチコステロイド、シクロホスファミド、及びアザチオプリンの1つ以上による処置に効果を示さない、喘息又はIPFに罹患した患者の治療に使用される場合がある。更に、肺線維症患者においてIFN−γ等のエアロゾル化インターフェロンの投与が計算及び最適化される。このような投与によって、患者の肺機能検査における改善が見込まれる。
of Symposium on Respiratory Drug Delivery II, Keystone, Colorado, March, 1990;及びPlatz, et al.,米国特許第5,284,656号)。治療用製品を肺へ送達するよう設計された広範な機械装置(ネブライザー、定量吸入器、及び粉末吸入器を含むがこれに限定されず、全て当業者に周知である)が、本発明の実施における使用において検討されている。
タンパク質の鼻部送達も考えられる。鼻部送達は、肺における薬品沈着を必要とすることなく、鼻部への治療薬の投与後にタンパク質を直接血流へ輸送することを可能にする。鼻部送達用の製剤は、デキストラン又はシクロデキストランを含有する製剤を含む。
更なる試験の実施の際に、種々の患者における種々の病態の処置に好適な、投与量に関する情報が明らかになることが理解されており、当業者は、投与患者の治療上の背景、年齢、及び健康状態を考慮して適切な投薬を決定することができる。一般的に、注射又は注入におけるインターフェロン−γの投与量は、生理活性タンパク質250μg(化学修飾を含まないタンパク質のみの質量で計算)〜750μg(同様に基づく)の間で週1〜5回の投与が予測される。更に好ましくは、約500μgで週3回の投与が行われる場合がある。一般的に、注射又は注入におけるインターフェロン−αの投与量は、通常250〜750μgで週1〜5回の投与、好ましくは約500μgで週3回の投与である。インターフェロン−βの場合において、投与量は、通常0.10〜1mgで週1〜3回の投与、好ましくは週に約0.25mgで3回の投与である。投薬スケジュールは、タンパク質の循環半減期、及び使用される製剤により異なる場合がある。
肺疾患の処置に使用される1つ以上の薬学的組成物と併用してインターフェロンを投与する場合があることは、本発明の更なる態様である。又、例えばシクロホスファミド、アザチオプリン、又はコルチコステロイドといった抗炎症薬又は免疫抑制薬が同時に投与される場合もある。投与は同時行われる場合もあれば、連続して行われる場合もある。
患者集団
試験対象は、American Thoracic Societyの基準A又はB(下記)によって診断された特発性肺線維症(IPF)に罹患した患者であった。患者集団は、コルチコステロイド、シクロホスファミド、及び/又はアザチオプリンによる従来の治療に対して効果を示さなかった、又は適応しなかった。患者集団は、エアロゾル化IFN−γを12週間使用することにより処置された。
I. 上記の基準3つが全て満たされる。
II. 経気管支肺生検(TBBx)又は気管支肺胞洗浄(BAL)が、他の診断を支持する特徴を示さない。
III. 以下4つの小基準の内の3つに合致する。
1. 年齢50歳超
2. 未解明の運動時呼吸困難の潜伏性発症
3. 罹患期間3ヶ月超
4. 両肺基底部の吸気性クラックル
以下の改善が示される。
(1)ステロイド治療前に得られるFVCと比べた、処置前の値から10%の予測FVCの増加。
(2)患者のFVCが処置前の値から10%を超えて増加を示し、その後治療に関係なく処置前の値まで戻る場合。
総ビリルビン量:正常値上限の1.5倍超
アラニンアミノトランスフェラーゼ:正常値上限の3倍超
アルカリホスファターゼ:正常値上限の3倍超
アルブミン:スクリーニング時に3.0未満
(b)指定の限度値を外れたCBC。
ヘマトクリット:30未満又は59超
血小板:100,000/mm3未満
(c)クレアチニン:スクリーニング時に正常値上限の1.5倍超;
(10)6週間前以内にコルチコステロイド、シクロホスファミド、及び/又はアザチオプリンを除外した肺線維症治療の薬剤。
最初に、エアロゾル化インターフェロン−γによる非盲検の予備実験に登録されるIPF登録所から10名の患者が召集される。10名の患者は、参加及び除外基準に適合すると見込まれる。収集されたデータには、身長、体重、及びバイタルサイン(全ての投薬における個人歴、及び徹底した職業的及び喫煙経歴、身体検査、EKG、CBC、電解質パネル、肝臓酵素及び凝固プロフィール、CXR、胸部CT、PFT、ABG、出産年齢の女性における妊娠試験)等、過去の病歴が含まれる。
臨床上の有用性
慢性アレルギーの既往歴を有する38歳のハイチ人女性は、次第に増加する息切れ及び運動性呼吸困難の1年半の既往歴があった。患者のPFTは、主に拡散能の低い限定的なパターンを示し、間質性肺疾患の疑いがあった。彼女は他の胸部CTスキャンを受け、前記のPFT結果が確証され、主に肺底部で胸膜下線維形成及び蜂巣状の変化が明らかになった。開胸肺生検は、UIP/IPFと一致したパターンを示した。
BAL液は、タンパク質の測定のために使用され、送達される薬剤量を測定するためウイルス抑制試験によってIFN−γを評価する。濃縮したBAL液及び24時間の細胞培養上清は、ELISA(R&D[米国ミネソタ州ミネアポリス])によってサイトカインIL−1β、IL−4、IL−6、IL−8、及びTNF−αについて評価される。無細胞のBAL上清は、ELISA及びルシフェラーゼレポーター検定によってTGF−β活性の測定に使用される。経気管支生検(TBBX)標本は、半定量的なRT−PCRによってTGF−β遺伝子の転写の測定に使用される。線維芽細胞はTBBX標本から得られ、コラーゲンI、III、及びフィブロネクチンRNAの量がRT−PCRによって測定される。RNA(10μg)はTBBX又はTBBXの培養細胞から得られ、ノーザンブロット解析が行われる。ヒドロキシプロリン含有タンパク質の含有量は、BAL液、BAL上清、及びTBBX標本を使用した分光光度法によって測定される。処置前後の両治療試料のBAL液細胞数は、各患者において計算される。保存のため、血液試料が各患者から採取される。
各患者は、携帯型ネブライザーによるIFN−γ投与の沈着試験への参加を依頼された(別の同意の下)。この沈着試験は以下に記載する通り、エアロゾル化IFN−γを試験するように計画された。薬剤は99mTcで標識され、エアロゾルネブライザーによって投与された。「減衰技法」を使用して、肺の種々の部分に送達されたIFN−γの投与量が計算された。IFN−γの初期投与量500μgの安全性が以前に示されたため、この投与量が使用された。投与量は、個々の患者の沈着試験によって調節される。後に続く気管支鏡検査は、治療終了後に上記のプロトコールを使用して実施された。BALは肺沈着図に従って誘導されたため、薬剤沈着が最も多い部分が分析され、最も薬剤送達の少ない部分及びエアロゾルIFN−γ処置前試料と比較された。このように、肺の各部位に対する全投与量は、計算及び定量が可能である。臨床反応及びBALデータに従って、投与量は最適な臨床及び沈着パラメータを反映するために調整することができる。可能な場合は、試料の同様の部分に対する試みが処置前及び処置後に行われる。各患者は、治療の1ヶ月後に経過観察が評価される。全ての手順、検査評価、放射線試験、及び肺の生理学的評価の結果は、患者の医療記録で詳細に記録される。全試験の評価は、NYU医療センターのGCRCで実施される。
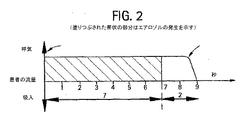
雲の発生(換気なし): カスケードインパクターは、ピストンポンプ(ポンプは回路から接続分離される)によって起こる換気を行わずに、1Lpmにおいて管から直接粒子試料を採取した。AeroEclipseからの粒子の発生により、呼吸作動弁はサンプリング期間中に手動で圧縮された。
換気中: Harvardポンプはシステムで正弦曲線の流量を発生するために使用され、患者の呼吸に類似であった。750mLの1呼吸容量では、20/mの呼吸数及び0.5の負荷サイクルが利用された。
全患者のIFN−γ沈着は、AeroEclipseネブライザーを使用して行われた。キセノン画像診断及び減衰試験(下記参照)が実施された。
患者は、後部に配置されたガンマ線カメラ(Picker Dinaカメラ;米国コネティカット州ノースフォード)の前に着席した。99mテクネチウム(99mTc)に対する室内バックグラウンド画像を撮影した後、カメラは133Xeに対して設定された。患者は機能的残気量(FRC)で安静呼吸を行い、計数率が15秒にわたり土10%に安定するまで、5〜10mCiの133Xeを吸入した。1.0分のガンマ線カメラ画像(133Xe平衡画像)が得られ、解析のためコンピュータで保存された(Nuclear
Mac v1.2/94; Scientific Imaging Inc.[米国コロラド州リトルトン])。この画像は肺の外縁を示すのに使用された。
133Xe画像診断の後、カメラは99mTcに切り替えられた。そこで、患者は放射標識したエアロゾル化IFN−γをネブライザーから吸入した。各装置に、呼気フィルターが吐き出された粒子を捕捉するために設置された。ネブライザーは乾燥するまで運転された。最終吸入の後、患者は口部から胃までの物質を洗うために、コップ1杯の水を飲んだ。胃活性測定により上気道の沈着を評価した。
肺の減衰係数を計算するために、肺血流スキャンが行われた。沈着画像診断の後に続いて、5mCiの99mTc−粗大凝集アルブミンが直ちに末梢静脈を経て注入された。全ての粗大凝集体が心臓の右面を横断し、局所血流に比例して肺で分散したことが想定された。1分の画像が得られた。血流は、測定された活性から前(沈着)画像で測定された活性を減算して計算された。肺の減衰係数は、注入された活性量でカメラが測定した活性量を除算することによって測定した(肺減衰係数=測定した活性/注入した活性)。
患者には既知量の99mTcを添加したパンが与えられ、摂取後に胃のガンマ線カメラ画像が撮影された。胃減衰は、ガンマ線カメラで測定した活性で経口摂取した活性を除算することによって計算された(胃減衰係数=測定した活性/経口摂取した活性)。
肺の輪郭を明示して肺気量を網羅するために、コンピュータを使用して関心領域が保存平衡133Xe平衡スキャンに関して視覚的に示された。二次元の肺領域内部の3分の1の輪郭を表した肺中央部分がその時に示された。キセノン部分が示された後、同部分は沈着画像の上に配置され、胃の活性が確認された。この時「胃部分」は、胃の輪郭が視覚的に示された。胃部分と左肺のキセノン平衡部分との重複があった場合、重複する部分は「肺上の胃」又はSOLとして定義された。肺の全沈着を測定するため、胃及び肺部分上の胃からの放射活性は除外された。
肺活性の特定の中枢対末梢比は、キセノン平衡画像でエアロゾル画像を除算することによって定められた。この比は、部位的肺ガス量に対して正規化したエアロゾル沈着の分布を表す。
エアロゾルがガスとして完全に機能して133Xe分布に追従する場合、sC/P比は1.0となる。粒子が気道中央に優先的に沈着した場合、2.0又はそれ以上のsC/P比が得られる。
肺気量に関して正規化する場合、肺の末梢より中心において比較的多くの粒子が存在する(sC/P比=1.618、上気道の沈着は殆どなし)。
エアロゾルIFN−γの作用
副作用
エアロゾル化IFN−γで15名の個人(健常志願者と肺結核患者)を処置した。エアロゾルの投与は、時折の咳又は筋肉痛を訴える患者が数名いたが、耐性は良好であった。投与の最長期間は、副作用が増幅しない3ヶ月であった。更に、Jaffeは、通常の患者に与えられるエアロゾル化IFN−γが非経口で送達されたrIFN−γとは対照的に、全身性の副作用がなく安全であること、及び肺胞マクロファージとPBMC以外を活性化することができ、その作用は末梢血のみで示される可能性があることを発見した(Jaffe, et al., (1991) J Clin Invest 88(1):
297−302)。
IFN−γのエアロゾル沈着特性を調査した。沈着画像は、放射活性(エアロゾル)が肺の正常な部位全てに沈着されることを示し、明らかにする。疾患及び空洞性部位は沈着されない。血流スキャンは、同様に空洞性部位に血流が殆ど無いことを示す。沈着の予備測定において、質量平衡技法及びキセノン(図)を使用することにより肺に送達されたエアロゾルが投与量の10〜20%の範囲であることを明らかにする。肺に対する薬剤の標的への送達が、正常な肺実質において薬剤沈着を示すことが結論付けられた(Condos,, et al., (1998) Am J Respir Crit Care
Med 157(3): A187)。
以前に、IFN−γで処置された、重症の多種薬剤耐性の結核患者群における臨床状態の改善を示した。患者は、処置の前後にX線撮影で病変した部位のBALを使用して気管支鏡検査を受けた。24時間の細胞培養上清及びBAL由来の液体はELISAによって評価され、TNF−a(平均172〜117pg/mL)、IL1−b(平均25〜8pg/mL)の濃度が時間の経過と共に減少し、IFN−γ(平均3.3〜2.5pg/mL)の濃度があまり検出されないことが示された。IFN−γの投与が、疾患部で局所的に産生されるTNF−aの減少に関係していることが結論付けられた。これにより、進行したMDR−TBにおけるIFN−γの有益な効果を部分的に説明することができる(Condos, et al., (1998) Am J Respir Crit Care Med 157(3): A187)。
特発性肺線維症の効果的な処置
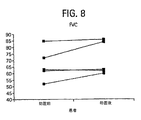
IPFに罹患する5名の患者に対するエアロゾルrIFN−γの試験において、耐性が良好な処置を発見した。副作用には、疲労、咳、及び微熱(n=1)が含まれた。試験期間中の定期的な検査評価は、異常を示さなかった。患者全員が息切れの自覚的な改善を報告した。3ヶ月の治療の終了時までに、試験での患者の全肺気容量において統計的に有意な増加が示された。図7は、処置を受けた5名の患者の内の3名が、処置後に予測された全肺気容量の増加率が認められたことを示す。被験患者5名の内の2名の努力性肺活量においても、200ccを超える(それぞれ200及び500cc)の改善が見られた。図8は、処置された5名の患者の内の3名における、処置後の予測努力性肺活量の増加率を示す。これらの生理学的変化は、これらの患者の気管支肺胞洗浄(BAL)液(肺内部の内壁から洗出される液体)から回収された活性化TGF−β濃度の減少を伴った。図9は、処置された5名の患者において、総タンパク質のTGF−βの減少した部分を示す。TGF−βは、肺の線維症の重要な介在物質の1つである。その活性化は、コラーゲン産生を誘導する。その濃度の減少により、肺のコラーゲン沈着の減少及び線維形成の減少が誘導されるはずである。更に、エアロゾル療法の前後に患者のBAL液でインターフェロン−γの濃度を測定し、薬剤のエアロゾル投与に関連した増加が示された。図10は、結核患者と特発性肺線維症に罹患する患者の肺において、インターフェロン−γによるエアロゾル処置の前後両方で測定されたインターフェロン−γの量を示す。
サイトカイン遺伝子調節
この試験において、転写制御因子の存在量、リン酸化、及びDNA結合活性の調査により、エアゾールIFN−γ処置が潜在的なSTAT−1を活性化し、IRF−1の新規合成を誘導するため、細胞シグナル伝達経路に影響を与えるという仮説が試験される。肺結核患者のIFN−γによる処置前後の肺の、非疾患及び疾患部位から得たBAL細胞において、これらの実験を実施した(Condos, et al., (1999) Am
J Respir Crit Care Med (in press))。IRF−1の精製及びクローニングは、Laboratory of Molecular Cell Biology at Rockefeller University with James E. Darnell, Jr.においてRichard Pine, Ph.Dにより行われた最初の作業の主要な部分であった(Pine, et al., (1990) Mol Cell Biol 10(6): 2448−57)。本プロジェクトの「目的3」に対して提唱された免疫ブロット法及び電気泳動移動度シフト試験の同法又は類似の方法が、ここに言及された作業で使用された。
喘息処置の有効性
標準処置に対してIFN−γエアロゾル処置を受ける30名の軽度から中等度の喘息患者を召集する。本試験は、症状抑制のためコルチコステロイドの吸入による中等度の投与量を必要とする軽度から中等度の持続性喘息に罹患する患者における、無作為化、プラセボ対照、クロスオーバー、二重盲検rIFN−γエアロゾル送達試験として行われる。
1)全病歴及び現症、並びに定期的な実験作業、
2)肺機能測定(FEV1、FVC、及び最大呼気速度)、
3)静脈刺入によって採血された50mLのヘパリン添加血、
4)血液試料は、全IgE、特定のアレルゲンに対する特異的IgEと好酸球算定のために採取される、
5)細胞数/差、及び24時間の培養上清におけるIFN−γ、IL−4、IL−5、GM−CSF、IL−10、IL−12、及びIL−13の濃度のELISAによる解析を伴った、BALによる光ファイバーの気管支鏡検査。
1)徴候及び症状についての簡単なアンケート。
2)毎日の日誌カード及びb−アゴニスト使用のモニターのレビュー。
3)エアロゾル療法の前後にモニターしている最大流量。
4)簡略された既往歴及び毎週の身体検査。
5)患者は、エアロゾル化IFN−γ治療の前中後に、毎日の日誌で症状の特徴を示す。患者は、咳、喘鳴及び息切れの症状の程度を評価する。患者は、毎日の最大流量測定も記録する。
1)全病歴及び現症、並びに定期的な検査作業、
2)肺機能測定(FEV1、FVC、及び最大呼気速度)、
3)静脈刺入によって採血された50mLのヘパリン添加血、
4)血液試料は、全IgE、特定のアレルゲンに対する特異的IgEと好酸球算定のために採取される、
5)BALによる光ファイバーの気管支鏡検査が、最後のIFN−γ治療後又は治療のない日に行われる。細胞数/差、及び24時間の培養上清におけるIFN−γ、IL−4、IL−5、GM−CSF、IL−10、IL−12、及びIL−13の濃度がELISAによって解析される。
6)全ての患者は喘息の病院で以下を継続する。
b)定期的な実験
c)肺活量測定及び最大流量測定
種々の理由のために低用量の吸入ステロイドを常用する、軽度から中等度の持続性の喘息に罹患する試験患者を選択した。第一に、軽度の断続的な症状のみの患者が含まれた場合、このような集団において感受性の生理学的変化か、症状的変化か、免疫的変化の判別が不可能になる恐れがある。第二に、この治験の治療を中断するため吸入ステロイドを要求する患者は認められない。更に本試験の目的は、エアロゾル化IFN−γがすでに指定された治療法の補助として利用することができるかを判定することである。コルチコステロイドがサイトカイン濃度に影響する可能性があるため、吸入ステロイドの使用が本試験との混同を招く恐れがあると理解される。「洗浄」は全患者が同基準で開始するための期間であることが含まれる。
喘息患者の肺機能における効果
肺機能測定におけるエアロゾル化rIFN−γの効果を測定するため、エアロゾル治療前の各患者に対する全肺気容量(TLC)及び機能的残気量(FRC)を含む1秒努力呼気肺活量(FEV1)、努力性肺活量(FVC)、最大呼気流量、及び肺容量における肺活量測定値を得る。この測定は、Bellevue Hospital Pulmonary Function Laboratoryで行われる。
BAL検体の効果
BAL検体は30名の喘息患者から得られる。IFN−γがサイトカイン産生を調節するかを評価するため、15名のこれらの患者にエアロゾルIFN−γを8週間投与する。これらの患者は、処置の前後にBAL及び採血が行われる。
患者は、医学的な病歴と現症、肺活量測定、酸素測定、気管支過敏性の評価、凝固試験(PT、PTT、血小板)、及びCBCを使用して事前にスクリーニングを行い、化学スクリーニングを行う。処置の間、患者は心拍数及びO2飽和度の継続的なモニタリング、患者の症状及び投薬量の記録、適所での静脈カテーテル、吸入b−アゴニストによる前投薬、アトロピン皮下投与(0.4mg)、及び鎮静剤の使用(ミダゾラム、静脈注入)、及び酸素補給が行われる。光ファイバー気管支鏡は、少量の前投薬と、鼻部及び上気道の表面麻酔の後に導入される。気管支鏡の先端は、右中葉又は小舌の区域又は亜区域気管支に挿入される。37℃の標準生理食塩水100mLが、20mLの分割量で気管支に注入される。加温した生理食塩水により、喘息患者の熱による気管支痙攣の誘発が回避されるはずである。流出液を回収するために、穏やかな断続的吸入が行われる。軽度の喘息患者において60〜80%の液体回収が予測される。回収率は、中等度から重度の疾患患者において50%まで減少する[Jarjour, 1998#62]。パルス酸素濃度計及び患者の状態における臨床評価は、処置後にも継続される。退院指導は、追跡治療のための週内の受診、及び電話連絡を含む。
細胞は標準的な技法によって行われた気管支肺胞洗浄(BAL)によって採取され、培養に対して以下の通りに調製される。液体は粘液のかたまりを除去するため、一層の滅菌ガーゼを通して濾過された。総細胞数は血球計で計測され、合計500の計測された細胞が改変ライト−ギムザ染色で染色され、その細胞遠心分離標本において細胞差が計測された。細胞生存率はトリパンブルー除外法によって測定され、全症例において、実験に使用される回収された細胞の生存率は90%以上になる。20の細胞遠心分離標本は、BALの各葉から調製され、一度10%のホルマリンで固定され、−70℃にて凍結される。BAL細胞は洗浄され、10%の熱失活したウシ胎児血清(FCS)及び100u/mLのペニシリン及び100mcg/mLのストレプトマイシンを加えたRPMI(GIBCO)により、106細胞/mLの濃度で24時間培養される(37℃)。
IFN−γ処置の終了前後に、一日のうち一定の時間に静脈刺入によって採血が行われる。PBMCは、Ficoll−Hypaque密度勾配遠心法によってヘパリン処置された静脈血から単離される。ヘパリン処置された静脈血はFicoll−Hypaqueの上に重層させて、2500rpmで20分間遠心分離される。PBMCの低密度層は吸引され、リン酸緩衝生理食塩水(PBS)で洗浄され、10%の熱失活したFCS、100U/mLのペニシリン、及び100mcg/mLのストレプトマイシンを加えたRPMI−1640(GIBCO)により106細胞/mLの濃度で再懸濁される。その時細胞培養は、37℃の5%CO2で24時間インキュベートされる。その時細胞上清は回収され、サイトカインについてELISAによって評価される。
24時間にわたって回収されたBAL細胞上清106細胞/mLを、IFN−γ、IL−4、IL−5、IL−10、IL−12、IL−13、及びGM−CSFについてELISA(Endogen)で評価する。各サイトカインに対して三つ組で検体を測定することができるように、106細胞/mLのチューブを5本採取する。肺区域につき平均で30〜40×106のBAL細胞になるため、各患者のBAL細胞上清を評価することが予期できる。BAL後の検体中のIFN−γを回収することができるため、及びBAL細胞の自発的なサイトカインの放出に重点が置かれているため、BAL液中のサイトカインの測定は行われない。
IFN−γ処置によって起こる遺伝子調節の機序
臨床処置プロトコールにより、IFN−γに反応して遺伝子発現を制御する転写因子の存在量において明確な効果及び活性が示され、サイトカインの特性とこれらのデータの相関は、喘息の免疫応答を評価できる基準を拡張する。更に、得られたデータにより、サイトカイン産生の解析及びサイトカインと他の遺伝子の発現による結果の機構の説明が可能になる。
処置プロトコールの前後にこれらの転写因子の総量を定量化することが有益である主な理由が2つある。これらのデータは、IFN−γ治療に対する制御された反応の全体的な解釈のために重要である。これにより、得られたタンパク質がリン酸化反応を受ける程度とDNA結合活性がある総タンパク質量の割合について結論が導かれる。更に、タンパク質の存在量は、因子をコードする遺伝子の制御された発現の最終測定により示され、従って、更に誘起された免疫応答の機能及び調節態様を集積する今後の研究のための根拠を提示する。免疫ブロット法検出は、ここで使用される主要な技法である。細胞質又は核抽出物から最大で5×106の細胞が各解析に使用される。上述の細胞は、各患者から10検体を得ることにより調達される。1名の患者から得たPBMC及びBAL細胞の抽出物全ては一回の試験に使用され、これにより検体のセット内での相対定量が容易になる。培養された細胞株から調製される対照の細胞質及び核抽出物も又、各試験に使用される。前の試験に基づき、これらの検体は、標的タンパク質を含むことが分かっており、免疫ブロット法の検出で陽性対照を提示することができる。更に、その検体は得られたデータが定量的であるか、又は定量的検出の範囲を明らかにする検証に使用することができる。
転写因子のリン酸化の変化は、因子の存在と因子の機能の関連性を示すことが多い。このことは、DNA結合活性がリン酸化の変化によって直接変化しなくても当てはまる(David, et al., (1995) Science 269(5231): 1721−3; Wen, Z, et al., (1995) Ceil 82(2): 241−50; Pine, et al., (1994) Embo J 13(1): 158−67; Cho, et al., (1996) J Immuno1 157(11): 4781−9; David, et a1., (1996) J Bio1 Chem 271(27): 15862−5; Gupta, et a1., (1995) Science 267(5196): 389−93; Hibi, et al., (1993) Genes Dev 7(11): 2135−48; Parker, et al., (1996) Mol Ce11
Bio1 16(2): 694−703; Schindler, et a1.,
(1992) Science 257(5071): 809−13; Shuai, et a1., (1992) Science 258(5089): 1808−12)。上述の通り、STAT−1のチロシン及びセリンのリン酸化は調節され、その活性を制御する。IRF−1はリンタンパク質であるが、リン酸化の自然発生的な変化については文献が存在せず、CIITAのリン酸化についても殆ど研究されていない。本明細書に記載する実験では、主に細胞培養系で以前に実証されたリン酸化反応についてPBMC及びBAL細胞からの抽出物を検査することにより、in vivoにおけるSTAT−1の調節に関するデータを得る。IRF−1及びCIITAについて得られるデータは、以前に測定されたものを上回る。
DNA結合活性の測定によって、処置プロトコールへの分子反応の調節を評価するために必要となる最終データが得られる。実験試料の電気泳動移動度シフト検定によるSTATファミリー及びIRF−1転写因子の検出及び定量化は、確立された手順によって達成される。培養細胞から調製される抽出物は、陽性対照としてこれらの検定で使用される。当該因子の特異性及び同定のための対照は、競合オリゴヌクレオチド又は抗血清を使用した反応を行うことによって提供される。オリゴヌクレオチド又は抗血清は、非特異的及び特異的の両方のものが使用される。
GITC及び超遠心分離を使用することにより、10×106のBAL細胞からmRNAを抽出する。RT−PCRはこのような僅かな細胞量で行うことができることから、全RNAが抽出され、−70℃にて保存され、IRF−1の遺伝子発現について検定される。PCRプライマーは、公開された配列に基づいており、サイトカイン遺伝子において記載したRT−PCRを行い、対照としてb−アクチン又はGAPDHと転写強度を比較する。IRF−1は基礎量発現することから、RT−PCRの定量的な手法が必要となる。BAL細胞由来の全RNAは、標準の方法に従い、オリゴd(T)及びPCRを使用して逆転写される。1回目のPCRは、以下のオリゴヌクレオチド(フォワードプライマー:5’−GTCAGGGACTTGGACAGGAG−3’、及びリバースプライマー:5’−AGCTCGGGGGAAATGTTAGT−3’)を使用したcDNAの20%を使用して行われる。IRF−1の発現は、GAPDHの発現に対して正規化される。
BAL由来の細胞は、上述の通り、血清を加えていないRPMI培地に移して処理された後、計数して、組織培養プレートへ移される。37℃にて2時間静置した後、非接着細胞は培地で除去され、再度計数される。接着細胞の量は、2つの細胞数の差から得られる。PBMCは、上述の通り、血清を加えていないRPMI培地に移して処理された後、計数される。残りの手順は全て、0〜4℃にて実施される。懸濁液中の細胞は、遠心分離され(200×g、10分)、上清が吸引された後、ペレットがリン酸緩衝食塩水(PBS)に再懸濁される。この手順が繰り返され、細胞が再度遠心分離された後、最終的なPBS上清が吸引される。付着した細胞単層は、そこで吸引用のPBSを加えることによって洗浄される。再度PBSが加えられ、単層が擦り落とされる。細胞及びPBSは遠心管へ移されて遠心分離が行われた後、PBSが吸引除去される。洗浄した細胞ペレットは、溶解緩衝剤(20mM Hepes・Na、pH 7.9、0.1mM EDTA・Na、0.1M NaCl、0.5% NP−40、10%グリセロール、1mM DTT、0.4mM PMSF、3μg/mLアプロチニン、2μg/mLロイペプチン、1μg/mLペプスタチン、100μM Na3VO4、10mM Na2P2O7、5mM NaF)(3μL/細胞105)で懸濁し、5分間インキュベートすることにより溶解される。核は遠心分離によって回収される(500×g、10分)。上清は除去された後、遠心分離によって浄化される(13,000×g、10分)。得られた上清は細胞質抽出物として回収され、砕いたドライアイス又は液体窒素で冷凍された後、−80℃にて保存される。核ペレットは洗浄緩衝剤(NP−40を除く溶解緩衝剤)で再懸濁された後、遠心分離によって回収される。上清が吸引された後、ペレットは抽出緩衝剤(洗浄緩衝剤、0.1M NaClの代わりに0.3MのNaClを除く)で懸濁され(3μL/細胞105)、30分間混合される。抽出した核は、遠心分離によってペレット化し、核抽出物として上清が回収され、上述の通り冷凍保存される。同量の異なる抽出物が実験で使用できるように、タンパク質濃度が計量される。単一系列又は異なる試料の核又は細胞質抽出物においては、通常、細胞数に対する抽出緩衝剤の量の比率を固定することで均一のタンパク質濃度が得られることから、これにおいては通常、各抽出物で同じ量を使用する必要がある。
免疫ブロットは、以下の通りに行われる。抽出物及びタンパク質サイズの標準物質が、SDS−PAGE用に濃縮したLaemmli試料添加緩衝剤と混合され、標準のプロトコールに従って8%の分離用ゲルと4%の濃縮用ゲルで調製された不連続なトリスグリシンゲルシステムに適用された。このゲルの比率は、対象のタンパク質を全て分離する。マーカー色素がゲルの最下部に到達するまで、電気泳動は一定の電圧で行われる。ゲルは転写用緩衝剤(トリスグリシン+15%のメタノール)で平衡化された後、タンパク質はセミドライ式装置(BioRad Transblot SD)を使用し、同じ緩衝剤によってニトロセルロースメンブレンに転写される。メンブレンは、標準的な手順によって展開される。簡潔に言えば、トリス緩衝食塩水+Tween 20界面活性剤に加えた脱脂粉ミルクとインキュベーションすることによりブロッキングを行い、特異的な一次抗体とインキュベートし、ブロッキング溶液で数回洗浄し、酵素結合の二次抗体とインキュベートし、ブロッキング剤を含まない緩衝剤で洗浄し、酵素基質でインキュベートする必要がある。化学発光基質の場合は、X線写真でシグナルが検出される。或いは、化学蛍光基質のシグナル検出には、PHRIのMolecular Dynamics Storm 860装置が使用可能である。実験計画に基づき、STAT−1及びIRF−1の転写に最適な条件が、(既にほぼ同じであることが判明しているが(Pine, et al., (1994) Embo J 13(1): 158−67; Pine, et al., (1990) Mol Cell Biol 10(6): 2448−57; Pine unpublished))、本プロジェクトでも、これらの各タンパク質に最適な以前の展開条件を同じように使用される。CIITAの場合、最適な検出条件は、ブロッキング剤の選択、界面活性剤の濃度、各手順のインキュベーション時間、及び検出方法を含め、培養細胞から調製した対照抽出物により経験的に決定される。STAT−1及びIRF−1の免疫沈降は、僅かに改変されているものの、既述の通りに行われる。具体的には、抗IRF−1抗体に結合するIRF−1の回収にS. aureus細胞を使用するところを、タンパク質−Aアガロースを使用することに置き換えている。
指定されたSTATファミリーのそれぞれ及びIRF−1に対し、最適な検定が行われた(Pine and Gilmour, supra)。反応において、非特異的及び特異的競合物質又は非特異的及び特異的抗体が使用される。各反応において、抽出タンパク質を通常は2〜3μLであるが、5μgを使用して行われる。競合物質との反応のため抽出物と混合する場合、オリゴヌクレオチドは放射識別されたプローブと共に使用される。抗体との反応のためタンパク質−DNA結合反応は通常通り行われ、それから抗血清が加えられ、インキュベーションが続行される。インキュベーションが完了した時、反応物質は未変性のポリアクリルアミドゲルに加えられ、4℃にて電気泳動される。ゲルが乾燥した後、結果はオートラジオグラフィにより、又はMolecular Dynamic
PhosphoImagerを使用して得られる。
喘息の個人400名において医学的評価が行われる。30名の軽度から中等度の持続性アレルギー性喘息患者は、IFN−γエアロゾル(n=15)又はこれに対する標準処置(n=15)を受けるために無作為化される。患者は、肺機能及び気管支誘発測定を行われなければならない。ファイバー気管支鏡検査に対する禁忌があってはならない。大部分の試験集団は、Bellevue Hospital Primary Care Asthma Clinicから召集される。患者集団の人口統計的特性は以下の通りである。90%は少数民族(主にヒスパニック系及びアフリカ系アメリカ人)で、年齢18〜79才(中央値=39)、男女比は1:2である。
一般的に、インターフェロン−γ(IFN−γ)に対する副作用のリスク及び重症度は、与えられる投薬量に関連する。この試験で使用される投与量(50mcg/m2)で、最もよく起こりうる副作用は、熱、頭痛、及び倦怠感等である。高用量で時折の嘔気と嘔吐が報告された。エアロゾル状散布においては副作用との関連がなかったが、頭痛、咳及び熱が予測される場合がある。症状が重症である場合、投薬は中断される。喘息に関連のないIFN−γにおける未知の副作用のリスクが、以前より存在する。一つに考えられるのはIFN−γのタンパク質部分に対するアレルギー反応を呈することであり、その場合、投薬は中止される。
あらゆるリスクを最小化するため、気管支肺胞洗浄は心臓病又はアンギナの既往歴を有する個人を除外する医学的評価の後に行われる。胸部X線と出血性パラメータを含む血液検査が行われる。気管支肺胞洗浄は、医師の監督下で肺疾患の人によって行われる。この手順に続いて、試験対象は3時間絶食を続け、バイタルサインは30分毎に3時間記録される。処置の間、全患者の心臓がモニターされ、低酸素血を防ぐため処置中と処置後に2時間鼻部への02を受ける。全ての患者のデータは、肺疾患調査室に施錠して保管される。対象に副作用が起こった場合のために、気管内チューブ、注射用のリドカイン及びエピネフリン等と一緒に光ファイバー気管支鏡を揃えた「緊急用カート」が備えられ、全手順は病棟医とCPRチームが待機している病院で行われる。気管支肺胞洗浄処置の全ては、副作用の発生増加を全て確認し、原因を特定するため、定期的にチェックされる。
インターフェロン−γのエアロゾル投与を受けた全患者は、改善可能な気道疾患を評価するため肺活量測定で検査された。殆どの患者は、改善可能性の徴候がない閉塞性気道疾患を有した。各エアロゾル療法で、患者は各処置の前後に最大流量が観察された。全患者に関するデータは、図11で示される。最大流量測定の変化率の要約データは、図12で示される。平均最大流量は、エアロゾルインターフェロン−γの処理後で増加し、一部の患者では顕著な増加を示した。これらのデータは、エアロゾルインターフェロン−γが、気道疾患患者において安全且つ耐性が良好であることを示す。
Claims (1)
- 本願明細書に記載された発明。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012157469A JP2012193207A (ja) | 2012-07-13 | 2012-07-13 | インターフェロンを用いる肺疾患の処置方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012157469A JP2012193207A (ja) | 2012-07-13 | 2012-07-13 | インターフェロンを用いる肺疾患の処置方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008532198A Division JP5175198B2 (ja) | 2005-09-20 | 2005-09-20 | インターフェロンを用いる肺疾患の処置方法 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014258344A Division JP2015057446A (ja) | 2014-12-22 | 2014-12-22 | インターフェロンを用いる肺疾患の処置方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012193207A true JP2012193207A (ja) | 2012-10-11 |
| JP2012193207A5 JP2012193207A5 (ja) | 2013-01-10 |
Family
ID=47085448
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012157469A Withdrawn JP2012193207A (ja) | 2012-07-13 | 2012-07-13 | インターフェロンを用いる肺疾患の処置方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2012193207A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116251174A (zh) * | 2022-12-23 | 2023-06-13 | 北京三元基因药业股份有限公司 | 一种包含人干扰素α1b吸入溶液的药物组件 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003519169A (ja) * | 1999-12-30 | 2003-06-17 | インターミューン インコーポレイテッド | γ−IFN液滴エアロゾルおよび方法 |
| WO2004004656A2 (en) * | 2002-07-03 | 2004-01-15 | The Kenneth S. Warren Institute, Inc. | Tissue protective cytokines for the protection, restoration, and enhancement of responsive cells, tissues and organs |
| JP2004529122A (ja) * | 2001-03-19 | 2004-09-24 | モナシュ ユニバーシティ | 呼吸器系病態の治療法 |
-
2012
- 2012-07-13 JP JP2012157469A patent/JP2012193207A/ja not_active Withdrawn
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003519169A (ja) * | 1999-12-30 | 2003-06-17 | インターミューン インコーポレイテッド | γ−IFN液滴エアロゾルおよび方法 |
| JP2004529122A (ja) * | 2001-03-19 | 2004-09-24 | モナシュ ユニバーシティ | 呼吸器系病態の治療法 |
| WO2004004656A2 (en) * | 2002-07-03 | 2004-01-15 | The Kenneth S. Warren Institute, Inc. | Tissue protective cytokines for the protection, restoration, and enhancement of responsive cells, tissues and organs |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116251174A (zh) * | 2022-12-23 | 2023-06-13 | 北京三元基因药业股份有限公司 | 一种包含人干扰素α1b吸入溶液的药物组件 |
| CN116251174B (zh) * | 2022-12-23 | 2023-09-29 | 北京三元基因药业股份有限公司 | 一种包含人干扰素α1b吸入溶液的药物组件 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20120148532A1 (en) | Method of treating pulmonary disease with interferons | |
| Keatings et al. | Effects of inhaled and oral glucocorticoids on inflammatory indices in asthma and COPD. | |
| Borish et al. | Efficacy of soluble IL-4 receptor for the treatment of adults with asthma | |
| Tanaka et al. | IL-18 might reflect disease activity in mild and moderate asthma exacerbation | |
| Wylam et al. | Aerosol granulocyte-macrophage colony-stimulating factor for pulmonary alveolar proteinosis | |
| Watanabe et al. | Increased levels of HMGB-1 and endogenous secretory RAGE in induced sputum from asthmatic patients | |
| Panina-Bordignon et al. | The CC chemokine receptors CCR4 and CCR8 identify airway T cells of allergen-challenged atopic asthmatics | |
| Stirling et al. | Interleukin-5 induces CD34+ eosinophil progenitor mobilization and eosinophil CCR3 expression in asthma | |
| Krug et al. | Cytokine profile of bronchoalveolar lavage–derived CD4+, CD8+, and γδ T cells in people with asthma after segmental allergen challenge | |
| US20050220763A1 (en) | Method of treating idiopathic pulmonary fibrosis with aerosolized IFN-gamma | |
| EP2627673B1 (en) | Therapies for improving pulmonary function | |
| Mashikian et al. | Identification of IL-16 as the lymphocyte chemotactic activity in the bronchoalveolar lavage fluid of histamine-challenged asthmatic patients | |
| D'Armiento et al. | Eosinophil and T cell markers predict functional decline in COPD patients | |
| Ikeda et al. | Resolution of airway inflammation following ovalbumin inhalation: comparison of ISS DNA and corticosteroids | |
| Tenero et al. | Effect of montelukast on markers of airway remodeling in children with asthma. | |
| EP1922081B1 (en) | Interferon lambda therapy for treatment of respiratory diseases | |
| Taube et al. | Inhibition of early airway neutrophilia does not affect development of airway hyperresponsiveness | |
| Sano et al. | Effects of suplatast tosilate on allergic eosinophilic airway inflammation in patients with mild asthma | |
| JP5175198B2 (ja) | インターフェロンを用いる肺疾患の処置方法 | |
| JP2012193207A (ja) | インターフェロンを用いる肺疾患の処置方法 | |
| US8486383B2 (en) | Method of treating pulmonary disease with interferons | |
| JP2015057446A (ja) | インターフェロンを用いる肺疾患の処置方法 | |
| Julius et al. | Safety of segmental allergen challenge in human allergic asthma | |
| KR20080093016A (ko) | 인터페론을 사용하여 폐질환을 치료하는 방법 | |
| Xue et al. | Up-regulation of CD44 expression by interleukin-13 in a murine model of asthma |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120713 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121120 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140122 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20140418 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140821 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141222 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150204 |
|
| A911 | Transfer of reconsideration by examiner before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20150227 |
|
| A912 | Removal of reconsideration by examiner before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20150410 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160310 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160408 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160509 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20160523 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20161221 |