JP2011504092A - 血管内皮増殖因子(vegf)の血管新生誘発性アイソフォームに特異的な抗体 - Google Patents
血管内皮増殖因子(vegf)の血管新生誘発性アイソフォームに特異的な抗体 Download PDFInfo
- Publication number
- JP2011504092A JP2011504092A JP2010530629A JP2010530629A JP2011504092A JP 2011504092 A JP2011504092 A JP 2011504092A JP 2010530629 A JP2010530629 A JP 2010530629A JP 2010530629 A JP2010530629 A JP 2010530629A JP 2011504092 A JP2011504092 A JP 2011504092A
- Authority
- JP
- Japan
- Prior art keywords
- vegf
- antibody
- angiogenic
- antibodies
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Urology & Nephrology (AREA)
- Genetics & Genomics (AREA)
- Rheumatology (AREA)
- Biophysics (AREA)
- Dermatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Cardiology (AREA)
- Pain & Pain Management (AREA)
- Ophthalmology & Optometry (AREA)
- Heart & Thoracic Surgery (AREA)
- Pulmonology (AREA)
- Vascular Medicine (AREA)
- Physical Education & Sports Medicine (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
本発明は、血管新生を伴う疾患、例えば、腫瘍および網膜障害の処置に有用な治療用および診断用抗体に関する。特に、本発明は、VEGFの血管新生誘発性アイソフォームに特異的な抗体を提供する。
血管新生
血管新生は、血管内皮細胞が増殖し、余分なものを取り除き、再編成して、既存の血管網から新たな血管を形成する重要な細胞性事象である。血管分布の発達は、正常な増殖性プロセスおよび病理学的増殖性プロセスに不可欠であるという説得力のある証拠がある(非特許文献1)。酸素および栄養分の送達、ならびに異化生成物の除去は、多細胞生物体において起こる増殖プロセスの大部分において律速段階である。したがって、血管区画は、胚発生中の器官の発生と分化だけでなく、成体の創傷治癒および生殖機能にも必要である。
血管内皮細胞増殖因子(VEGF)は、正常な血管新生と異常な血管新生の両方の枢要な調節因子であると報告されており、その最も一般的な形態は、VEGF−Aすなわち血管透過性因子(VPF)である(非特許文献5)。血管の形成プロセスに寄与している他の増殖因子と比べ、VEGFは、血管系内の内皮細胞に対する特異性が高い点で特殊である。VEGFは、胚の脈管形成および血管新生に不可欠である(非特許文献6;非特許文献7)。さらに、VEGFは、雌の生殖器系における周期的血管増殖ならびに骨の成長および軟骨形成に必要である(非特許文献8;非特許文献9)。ヒトVEGFは、血管拡張、血管透過性の増大および内皮細胞の有糸分裂誘発を媒介する32〜42kDaの二量体糖タンパク質である。
VEGFスプライスバリアント(本明細書においてVEGFxxxbとも表示する)のファミリーの一例は、VEGFの抗血管新生性アイソフォームのものであり、限定されないが、VEGF165b VEGF145b VEGF189b、VEGF206b(特許文献1に開示)およびVEGF121bが含まれ、BatesおよびHarperによって同定された。このバリアントは、識別的にスプライシングされたものであり、エキソン6と8a(以前はエキソン8と称されていた)が欠失しており、アミノ酸配列Ser−Leu−Thr−Arg−Lys−Asp(SLTRKD、配列番号:2)をコードするこれまで未知であったエキソン8b(以前はエキソン9と称されていた)を含む。VEGF165b、および他のアゴニストVEGF種(本明細書においてVEGFxxxbとも表示する)は、従来からのVEGFポリペプチドのアンタゴニストであり、BatesおよびHarperによって、抗血管新生活性、抗血管拡張活性、抗透過活性および抗増殖活性を有することが示された(非特許文献11および非特許文献12)。HarperおよびBatesの最近の刊行物(非特許文献13)において、著者らは、VEGF165bは結腸直腸腫瘍の増殖を阻害すると結論づけている。さらに、VEGF165bは、腫瘍の増殖に対するベバシズマブ(AVASTIN(登録商標))の効果を低下させる。
抗VEGF抗体「ベバシズマブ(BV)」は、「rhuMAb VEGF」または「AVASTIN(登録商標)」としても知られており、非特許文献15に従って生成される組換えヒト化抗VEGFモノクローナル抗体である。AVASTIN(登録商標)は、治療用途に承認されており、種々の癌の処置について、さらに臨床的に研究されている。
本発明は、VEGFに対する現在利用可能な抗体は、VEGFのアゴニスト形態を中和するだけでなく、VEGFのアンタゴニスト(抗血管新生性)形態も中和し、したがって、組織中に存在するVEGFアイソフォームのバランスに応じて臨床応答を伴って混合型アンタゴニスト−アゴニストとして作用するという概念に基づくものである。したがって、本発明は、血管新生誘発性バリアントと抗血管新生性バリアントとを識別することができ、前者のアイソフォームのみを中和することができる、血管新生誘発性VEGFに特異的な抗体を初めて提供するものである。また、本発明は、かかる抗体を得るための方法、その作製方法、ならびにその治療的および診断的使用を提供する。
i.試料を、VEGFのアゴニストアイソフォームに特異的な抗体または少なくとも抗原結合部分を含むその抗体断片とともにインキュベートする工程;
ii.検出可能なプローブを用いて、結合されたアゴニストVEGFを検出する工程;
iii.(ii)の量を、既知量の血管新生誘発性VEGFを含む参照試料で得られた標準曲線と比較する工程;および
iv.体液試料中の該血管新生誘発性抗体の量を、該標準曲線から計算する工程
を含む、血管新生誘発性のVEGFの形態の存在を検出または定量するための方法が提供される(is provides)。
i.生物学的試料を、VEGFのアゴニストアイソフォームに特異的な抗体または少なくとも抗原結合部分を含むその抗体断片とともにインキュベートする工程;
ii.検出可能なプローブを用いて、結合されたアゴニストVEGFを検出する工程;
iii.(ii)の量を、既知量の血管新生誘発性VEGFを含む参照試料で得られた標準曲線と比較する工程;
iv.体液試料中の該血管新生誘発性抗体の量を、該標準曲線から計算する工程;および
v.(iv)の量を、通常量の血管新生誘発性VEGF量と比較する工程
を含む、血管新生誘発性のVEGFの形態と関連している疾患または障害の診断方法が提供される。
本発明は、VEGFの有害な形態に特異的であるが、該タンパク質の有益なアンタゴニスト形態は中和することができない抗体を初めて提供するものである。これは、VEGFの抗血管新生性/アンタゴニスト形態と血管新生誘発性/アゴニスト形態の構造の違いにより可能となった。例えば、天然のVEGFである抗血管新生性/アンタゴニストVEGF165bは、エキソン8aにコードされた配列が欠損しているが、該配列は、ほとんどのVEGFの血管新生誘発性形態には存在している。
用語「VEGF」は、(限定されないが)121−、145−、165−、189−、および206−アミノ酸の血管内皮細胞増殖因子(Leungら Science,1989,246,1306,およびHouckら Mol.Endocrin.,1991,5,1806に記載)ならびにその天然に存在する対立遺伝子形態およびプロセッシングされた形態をいうために用いる。用語「VEGF」は、あらゆる形態のVEGF−A、例えば、VEGFファミリーである165−アミノ酸ヒト血管内皮細胞増殖因子のアミノ酸8〜109または1〜109を含むポリペプチドの切断型形態、ならびに抗血管新生性形態VEGF165b、VEGF121bおよび一連の全VEGFxxxbをいうために用いる。
本発明ではまた、本明細書において種々に記載の病状の処置または予防のための治療用組成物の製造のための、VEGFのアゴニストアイソフォームに特異的な少なくとも1種類の抗体を活性薬剤として含む、ヒトに対する医療的使用のための医薬用製剤が想定される。
抗体を調製およびキャラクタライズするための手段は、当該技術分野でよく知られている。以下に、本発明による抗VEGFxxx抗体の作製のための手法に関する例示を記載する。抗体の作製に使用されるVEGF抗原は、VEGFのアゴニスト形態に存在するがアンタゴニスト形態には存在しないVEGFxxxの任意のペプチド配列である。
ポリクローナル抗体は、好ましくは、動物において、該当する抗原とアジュバントの反復皮下(sc)または腹腔内(ip)注射によって生成させたものである。これは、該当する抗原を、免疫処置対象の種において免疫原性であるタンパク質(例えば、スカシガイヘモシニアン(KLH)、血清アルブミン、ウシサイログロブリン、またはダイズトリプシンインヒビター)に、二官能性薬剤または誘導体化剤(例えば、マレイミドベンゾイルスルホスクシニミドエステル(システイン残基によるコンジュゲーション)、N−ヒドロキシスクシニミド(リシン残基による)、グルタルアルデヒド、無水コハク酸、SOCl2、またはR1N=C=NR(式中、RおよびR1は異なるアルキル基である)を用いてコンジュゲートさせるのに有用であり得る。
血管新生誘発性アイソフォームVEGF165に結合して阻害するが、抗血管新生性形態VEGF165bにはそうでないポリクローナル抗体を設計した。VEGF165の7つのC末端アミノ酸残基を含むペプチドRCDKPRRをKLHに、アミノヘキサン酸スペーサーによってカップリングさせ、ウサギの免疫処置に使用した。ポリクローナル抗体を含有する血清を、免疫処置したウサギから収集した。
ペプチドのチオール基は、合成後に減少する傾向を有するため、KLHまたは樹脂いずれかへのカップリング前にペプチドのチオール基を確認した。
1.100mgのスカシガイヘモシニアン(KLH)を2mlの水に溶解させ、超音波処理し、ボルテックスし、4℃で約4時間、回転装置上に置いた。
1.NHS活性化Sepharose(登録商標)4 Fast Flowは、予備活性化アガアロースマトリックスである。NHS(N−ヒドロキシスクシニミド)カップリングにより、第1級アミノ基を含むリガンドとの化学的に安定なアミド結合が形成される。NHS活性化Sepharose(登録商標)4 Fast Flowによりスペーサーアームが提供され、したがって、低分子タンパク質およびペプチドリガンドの固定化に特に好適である。高い安定性とスペーサーアームが、樹脂の高い流動性と安定性という特性と組み合わされることにより、医薬としての使用に魅力的となる。
10%脱脂粉乳/PBS/0.05%tween中で一晩ブロッキング;
一次抗体−2.5%ブロック溶液中で2時間、1:50に希釈したウサギ全血清;
二次抗体−2.5%ブロック溶液中で1:8000に希釈し、x線に20秒間曝露したヤギ抗ウサギ
図2に示されるように、アフィニティ精製したポリクローナル抗体画分(エキソン8aのRCDKPRRのエピトープに対して生成)は、VEGF165を検出するがVEGF165bは検出せず(左パネル)、一方、VEGF165bに特異的な抗体(エキソン8bのエピトープSLTRKDに対して生成)は、VEGF165bを認識するがVEGF165は認識しない(右パネル)。
ELISA(Perrinら,diabetologia 2005,48,2422;Vareyら,British J.Cancer 2008,1;
遊走アッセイ(Batesら,Cancer Research 2002,62,4123に記載);
眼血管新生(Konopatskayaら,Molecular Vision 200626,626に記載);
インビボ腫瘍試験(Rennelら,Eur.J.Cancer 2008,44,1883に記載);
免疫組織化学検査(Pritchard−Jonesら,Br.J.Cancer 2007,Br J.Cancer,97,223に記載)
によってさらに評価される。
遊走の阻害を、Batesら,Cancer Research 2002,62,4123−4131に記載のようにして試験した。アッセイは、コラーゲンコートポリカーボネート製のフィルター挿入体(8m孔径;Millipore)を含む変形型24ウェルBoydenチャンバにて行なった。フィルターを、0.5ml/ウェルのVEGFアイソフォームを4〜80ng/mlの精製抗体画分とともに、またはなしで入れた24ウェルプレート内に配置した。ヒト臍静脈内皮細胞(HUVEC)を無血清培地中に懸濁させ、25,000個の細胞を各ウェルの上側のチャンバに添加した。プレートを6時間インキュベートして遊走させ、培地を除去し、両方のチャンバをPBSで2回洗浄した。次いで、0.2mg/mlのチアゾリルブルー(MTT)を両方のチャンバの培地に添加し、37℃で3時間インキュベートした。培地を除去し、チャンバをPBSで2回洗浄した。上側のチャンバ内の非遊走細胞の結晶(青色に染色)を綿棒で取り出し、これを1mlのDMSOに入れ、MTT生成物を溶解させた。また、遊走細胞結晶(該挿入体の裏面上)もMTTに溶解させた。試料を一晩放置し、生成物の完全な溶解に可能にさせた。分光測光器を使用し、570nmの波長で可溶性MTTの吸光度を測定した。次いで、遊走割合を、下側のウェルの強度から両ウェルの全強度に対する割合として計算した。
モノクローナル抗体は、例えば、ハイブリドーマ法(最初にKohlerら,Nature,1975,256:495によって記載)を用いて作製され得るか、または組換えDNA法(米国特許第4,816,567号)によって作製され得る。
VEGF165の6アミノ酸および9アミノ酸C末端配列(CDKPRR配列番号:1、TCRCDKPRR配列番号:5)の合成ペプチド断片を、スカシガイヘモシアニン(KLH)(担体分子としての機能を果たす)にカップリングさせ(Department of Biochemistry,University of Bristol,UK)、次いで、6〜8週齢の雌Balb/cマウスの免疫処置に使用した。
1.VEGF165遊離ペプチド:10mg/ml(ストック濃度)、作業濃度10μg/ml。
4.VEGF165b 6アミノ酸−BSA、ストック濃度、2.5mg/ml;作業濃度、1ug/ml(1:2,500希釈)
5.ペプチド−myc(骨髄球腫症ウイルス癌遺伝子ホモログ):(陰性対照)myc−BSA、ストック濃度、1.4mg/ml;作業濃度、炭酸塩コート溶液中1ug/ml(1:1,400)。
75μl(24ウェルプレート由来のもの)、または75μlの希釈試料(96ウェルプレート由来のもの)をPBS/Tween内で添加する(ペプチドは清浄であり、BSAでのブロックは必要でない)。
HRP−コンジュゲートヤギ抗マウス免疫グロブリン(Sigma A 0412)の1:2,500希釈物を、低バックグラウンドでのペプチド検出のために使用した)。振とうしながら37℃で15分間のインキュベーション。
基質の添加:
クエン酸リン酸バッファー(pH5.0)を室温まで昇温させた。
停止溶液:100ul/ウェルの1MのHCl(40mlの濃HClを、424mlのdH2Oを入れた瓶に添加)を添加した。
解析:
492nmにおける吸光度を、プレート読取装置を用いて測定した。
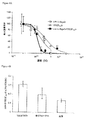
VEGFの血管新生誘発性形態に対するモノクローナル抗体の効力を測定するため、ECV304内皮細胞を用いた遊走阻害アッセイを使用した。このアッセイは、抗体が、VEGF165および/またはVEGF165bによる刺激に応答したECV304内皮細胞の遊走を阻害する能力を測定するものであり、以下のようにして行なわれる。
条件(1nMは40ng/ml VEGF165である):
1.陽性対照(5%FCS、すなわち通常の完全培地)
2.陰性対照(0.1%FCS、すなわち低血清)
3.0nMの抗体+1nMのVEGF165
4.10nMの抗体+1nMのVEGF165
5.20nMの抗体+1nMのVEGF165
6.40nMの抗体+1nMのVEGF165
7.60nMの抗体+1nMのVEGF165
8.80nMの抗体+1nMのVEGF165
溶液は、滅菌されたもの、または滅菌濾過したものであるのがよい。
[(細胞計数/挿入体/0.0028637)/1×l05]*100
0.0028637=Falconの5mm直径のMillipore挿入体の場合での視野によって占有される挿入体の面積であり、この値は0.00477である。
血管新生誘発性VEGFアイソフォーム(VEGFxxx)に対する抗体を単独およびVEGF165bとの組み合わせで試験する。動物およびヒトにおけるVEGFxxx特異的抗体の安全性プロフィールは、VEGFスカベンジャーおよびVEGFR遮断薬で見られるものよりも良好であると予測される。
VEGFの血管新生誘発性形態に対する抗体の心血管安全性プロフィールは、抗VEGFxxxまたはVEGF165bまたはVEGF165またはVEGFRチロシンキナーゼインヒビター(TKI)で処置した動物の血圧の測定によって特性評価する。現在利用可能な治療アプローチでは血圧が上昇するが、血管新生誘発性VEGFアイソフォームに特異的な抗体は、動物およびヒトにおいて、より良好な安全性心血管プロフィールを有すると予測される。
VEGFインヒビターは、毛細血管の退縮および内皮細胞死を引き起こすことが示された。VEGF165bは、培養状態の内皮細胞に対して細胞傷害性ではなく、対照的に細胞保護的であるが、VEGF165b抗体は細胞傷害性を増大させる。細胞の生存に対するVEGFの血管新生誘発性形態に特異的な抗体の効果は、VEGF165b、VEGF165、VEGFスカベンジャーおよびVEGFR遮断薬の比較によって特性評価する。
細胞保護因子であるVEGF165bは、潜在的な網膜用眼科治療薬である。VEGF165bが網膜色素上皮細胞に対して毒性であるか保護的であるかを調べるため、RPE細胞を血清飢餓状態にし、VEGF165bまたはVEGF165bに対する抗体で処理し、細胞細胞傷害性をLDHアッセイによって測定した。結果は、VEGF165bがRPE細胞の内在性生存因子であることを明白に示す。VEGFの血管新生誘発性形態に特異的な抗体は、血清枯渇によって誘発される網膜色素上皮細胞死の阻害に関して試験される。
VEGF165bは、他の細胞型に対しても細胞保護的である。新生仔ラット由来の海馬ニューロンは、グルタミン酸化合物による興奮毒性中、VEGF165によって細胞死から救済されることが以前に示された。CA1またはCA3ニューロンをVEGF165bで処理すると、グルタミン酸化合物誘発性細胞傷害性が低減された。VEGF165bに再生効果があるかどうかを調べるため、成体ラット由来の後根神経節を、培養状態で解離させた後にVEGF165bに供し、軸索長を測定した。VEGF165b処理により軸索長が長くなることが示され、これは、VEGF165bが、インビトロで細胞保護特性およびニューロン再生特性を有することを示す。
ヒト化抗体は、典型的には、非ヒトCDRがグラフティングされたヒトフレームワークを有する。したがって、ヒト化抗体には、非ヒト供給源由来の1つ以上のアミノ酸配列が内部に導入されている。このような非ヒトアミノ酸残基は、しばしば「輸入(import)」残基と称され、これは、典型的には「輸入」可変ドメインから採用される。ヒト化は、本質的に、Winterおよび共同研究者の方法(Jonesら,Nature,321:522−525(1986);Riechmannら,Nature,332:323−327(1988);Verhoeyenら,Science,239:1534−1536(1988))に従い、齧歯類のCDRまたはCDR配列を、対応するヒト抗体の配列の代わりに使用することにより行なわれ得る。したがって、かかる「ヒト化」抗体は、実質的にあまりインタクトでないヒト可変ドメインが、対応する非ヒト種由来配列で置換されたキメラ抗体である(米国特許第4,816,567号)。実際、ヒト化抗体は、典型的には、一部のCDR残基および場合によっては一部のFR残基が、齧歯類抗体の相似部位由来の残基で置換されたヒト抗体である。
抗体断片の作製のための種々の手法が開発されている。従来より、このような断片は、インタクトな抗体のタンパク質分解性消化によって誘導されるものであった(例えば、Morimotoら,Journal of Biochemical and Biophysical Methods 24:107−117(1992)およびBrennanら,Science,229:81(1985)参照)。しかしながら、このような断片は、現在、組換え宿主細胞によって直接産生させることができる。例えば、抗体断片は、上記の抗体ファージライブラリーから単離することができる。あるいはまた、Fab’−SH断片を大腸菌から直接回収し、化学的にカップリングさせてF(ab’)2断片を形成することができる(Carterら,Bio/Technology 10:163−167(1992))。別のアプローチによれば、F(ab’)2断片を組換え宿主細胞培養物から直接に単離することができる。抗体断片の作製のための他の手法は当業者に自明であろう。他の実施形態において、一般的に好まれる抗体は単鎖Fv断片(scFv)である。
本発明は、VEGFの血管新生誘発性のアイソフォームに特異的であるが、VEGFの抗血管新生性形態に対しては寛容である抗体を提供する。有意な蛋白尿は、VEGFスカベンジャーおよびVEGFR遮断薬での処置と関連している。
VEGF165は、血管透過性を増大させることがわかっており、VEGF165発現によって水に対する腎臓の高い透過性が維持され、他の組織における透過性が増大すると考えられるのは、この機構のためである。経上皮電気抵抗アッセイを使用すると、VEGF165bは、糸球体内皮細胞内でVEGF165によって誘導される透過性を阻害することが示された(図10)。ヒト条件的不死化糸球体内皮細胞を2時間血清飢餓状態にし、次いで、何もなし(対照)、1nMのVEGF165、1nMのVEGF165bまたは1nMのVEGF165&1nMのVEGF165bの組合せのいずれかに応答した、培養単層状態の糸球体内経内皮電気抵抗を測定した。結果は、対照(すなわち、時間点0分、SEM)に対する平均増加倍数である。n=5、プリズムによるデータ解析:p±<0.0001、一元配置ANOVA、反復測定、ボンフェローニポストテストによる。対照対VEGF165 p<0.001、対照対VEGF165b p,0.01、対照対両者p>0.05、VEGF165対VEGF165bと両者 p<0.001、VEGF165b対両者 p<0.01。SSPSを用いたデータ解析、全般的なp値>0.0005 一元配置ANOVA、反復測定、ポストホックボンフェローニ 対照対VEGF 0.001、対他のNSVEGF対他の3つの群 すべて有意 165対両者 0.037。VEGFの血管新生誘発性形態に特異的な抗体が、糸球体内皮細胞内でVEGF165によって誘導される透過性も阻害することは、好都合である。
VEGF165は、インビボで、蛋白尿を誘発し、糸球体の透過性を増大させることが示された。VEGFアンタゴニストもまた、インビボで蛋白尿および糸球体の透過性を増大させる。しかしながら、有足突起特異的ネフリンプロモーターの制御下でVEGF165bを18ヶ月発現させているマウスでは、水に対する糸球体の透過性(透水率)の有意な低下がみとめられる(図11)。インビボでの糸球体におけるVEGFの血管新生誘発性形態に特異的な抗体での連続的処置の効果を調べるため、VEGF165bを18ヶ月発現しているトランスジェニックマウスから単離した糸球体の透過性を測定した。糸球体は、18ヶ月齢の野生型でヘテロ接合型またはホモ接合型のpod−VEGF165bマウスから単離したものであり、透水率は、単位容積あたりの単位面積あたりで測定されたものである(LpA/Vi)。ホモ接合型マウスは、ヘテロ接合体と比べて低い透過性を有し、これは遺伝子量効果を示す。VEGFの血管新生誘発性形態に特異的な抗体での処置の効果は、腎臓安全性プロフィールに対する効果を特性評価するために他のVEGFスカベンジャーおよびVEGFR TKIとの比較において同様に試験される。
Claims (32)
- 血管新生誘発性VEGFアイソフォームに結合し得るが、抗血管新生性VEGFアイソフォームに結合し得ない、VEGFに特異的な抗体または少なくともその抗原結合部分を含む断片。
- エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する、請求項1に記載の抗体。
- CDKPRR(配列番号:1)、RCDKPRR(配列番号:3)、CRCDKPRR(配列番号:4)およびTCRCDKPRR(配列番号:5)からなる群より選択される抗原決定基を認識するものである、請求項2に記載の抗体。
- 抗原決定基がDRARQEK(配列番号:7)を含まない、請求項2に記載の抗体。
- エピトープSLTRKD(配列番号:2)を含むVEGFアイソフォームを中和することができない、請求項2に記載の抗体。
- 前記VEGFアイソフォームがVEGF165bおよびVEGF121bからなる群より選択される、請求項5に記載の抗体。
- 前記抗体がモノクローナル抗体である、請求項1に記載の抗体。
- European Collection of Cell Cultures(ECACC)に寄託されたMR93 A26クローン13−8−8受託番号08101401;MR93 A26クローン13−8−10受託番号08101402;MR93 A26クローン13−8−3受託番号08101403からなる群より選択されるハイブリドーマ細胞株によって産生される、請求項7に記載の抗体。
- European Collection of Cell Cultures(ECACC)に寄託されたMR93 A26クローン13−8−8受託番号08101401;MR93 A26クローン13−8−10受託番号08101402;MR93 A26クローン13−8−3受託番号08101403からなる群より選択されるハイブリドーマ細胞株によって産生されるモノクローナル抗体。
- 前記抗体がヒト化抗体である、請求項7に記載の抗体。
- 前記抗体がヒト抗体である、請求項7に記載の抗体。
- 前記抗体がキメラ抗体である、請求項7に記載の抗体。
- 前記抗体がポリクローナル抗体である、請求項1に記載の抗体。
- Fab、Fab’、F(ab’)2、Fd、Fd’、Fv、dAb、単離されたCDR領域および単鎖抗体からなる群より選択される請求項1に記載の抗体断片。
- 請求項1に記載の抗体またはその抗体断片をコードする単離されたポリヌクレオチド。
- 活性成分として、VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片;および薬学的に許容され得る担体を含む医薬組成物。
- 処置を必要としている被検体に、VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片を投与することを含み、それにより、VEGFの過剰発現と関連している障害または疾患に罹患している被検体が処置される、VEGFの過剰発現と関連している障害または疾患に罹患している被検体の処置方法。
- 前記障害または疾患が、細胞増殖性疾患または障害、過剰透過性疾患または障害、および血管新生に関連している疾患または障害からなる群より選択される、請求項17に記載の方法。
- 前記障害または疾患が、血管新生、ネフローゼ症候群、急性呼吸窮迫症候群、癌、増殖性眼疾患、網膜障害、関節リウマチ、および乾癬からなる群より選択される、請求項17に記載の方法。
- 請求項1に記載の抗体を、VEGFの抗血管新生性アイソフォームとともに投与することを含む、処置を必要としている被検体の処置方法。
- 前記VEGFの抗血管新生性アイソフォームがVEGF165bである、請求項20に記載の方法。
- 前記VEGFの抗血管新生性アイソフォームが、VEGF121b、VEGF145b、VEGF189bおよびVEGF206bからなる群より選択される、請求項20に記載の方法。
- VEGFと関連している障害または疾患の処置のための医薬の調製のための、VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片の使用。
- VEGFと関連している障害または疾患の処置のための、VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片の使用。
- 血管新生誘発性形態のVEGFと抗血管新生性形態のVEGFの比を測定するための、VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片の使用。
- VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片を使用することを含む、試料中の血管新生誘発性VEGFアイソフォームの存在を検出または定量するための方法。
- i.試料を、VEGFに特異的であり、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片とともにインキュベートする工程;
ii.検出可能なプローブを用いて、結合されたアゴニストVEGFを検出する工程;
iii.(ii)の量を、既知量の血管新生誘発性VEGFアイソフォームを含む参照試料で得られた標準曲線と比較する工程;および
iv.体液試料中の該血管新生誘発性抗体の量を、該標準曲線から計算する工程
を含む、請求項26に記載の方法。 - VEGFに対する抗体であって、エピトープCDKPRR(配列番号:1)を含む抗原決定基を認識する抗体または少なくとも抗原結合部分を含むその抗体断片を使用することを含む、血管新生誘発性VEGFアイソフォームが関連している疾患または障害を診断するための方法。
- i.生物学的試料を、VEGFのアゴニストアイソフォームに特異的な抗体または少なくとも抗原結合部分を含むその抗体断片とともにインキュベートする工程;
ii.検出可能なプローブを用いて、結合されたアゴニストVEGFを検出する工程;
iii.(ii)の量を、既知量の血管新生誘発性VEGFを含む参照試料で得られた標準曲線と比較する工程;
iv.体液試料中の該血管新生誘発性抗体の量を、該標準曲線から計算する工程;および
v.(iv)の量を、通常量の血管新生誘発性VEGF量と比較する工程
を含む、請求項28に記載の方法。 - 処置を必要としている被検体に、VEGFの抗血管新生性アイソフォームを投与することを含む、腎障害の処置方法。
- 前記VEGFの抗血管新生性アイソフォームがVEGF165bである、請求項30に記載の方法。
- 前記VEGFの抗血管新生性アイソフォームが、VEGF121b、VEGF145b、VEGF189bおよびVEGF206bからなる群より選択される、請求項30に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US98243807P | 2007-10-25 | 2007-10-25 | |
| PCT/IL2008/001410 WO2009053987A1 (en) | 2007-10-25 | 2008-10-26 | Antibodies specific to pro-angiogenic isoforms of vascular endothelial growth factor (vegf) |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011504092A true JP2011504092A (ja) | 2011-02-03 |
| JP2011504092A5 JP2011504092A5 (ja) | 2012-11-15 |
Family
ID=40385456
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010530629A Pending JP2011504092A (ja) | 2007-10-25 | 2008-10-26 | 血管内皮増殖因子(vegf)の血管新生誘発性アイソフォームに特異的な抗体 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8592563B2 (ja) |
| EP (1) | EP2203480A1 (ja) |
| JP (1) | JP2011504092A (ja) |
| CN (1) | CN101970486A (ja) |
| AU (1) | AU2008315414A1 (ja) |
| CA (1) | CA2703154A1 (ja) |
| WO (1) | WO2009053987A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014528693A (ja) * | 2011-06-15 | 2014-10-30 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 抗ヒトepo受容体抗体及び使用方法 |
| WO2016194708A1 (ja) * | 2015-05-29 | 2016-12-08 | 国立大学法人名古屋大学 | 尿中VEGF-A165bを指標とした腎機能の検査方法及び検査装置、腎機能の検査装置として機能させるためのプログラム及び記録媒体 |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PT2066694E (pt) | 2006-09-29 | 2016-01-27 | Oncomed Pharm Inc | Composições e métodos de diagnóstico e tratamento do cancro |
| CN102459346B (zh) | 2009-04-27 | 2016-10-26 | 昂考梅德药品有限公司 | 制造异源多聚体分子的方法 |
| DK2488204T3 (en) | 2009-10-16 | 2016-06-06 | Oncomed Pharm Inc | Therapeutic combination and use of DLL4 antagonist antibodies and blood pressure lowering agents |
| EP2517014B1 (en) * | 2009-12-21 | 2014-11-19 | Mayo Foundation For Medical Education And Research | Early marker of proteinuria in patients treated with an anti-vegf treatment |
| US8551479B2 (en) | 2010-09-10 | 2013-10-08 | Oncomed Pharmaceuticals, Inc. | Methods for treating melanoma |
| HRP20230078T1 (hr) | 2011-09-23 | 2023-05-12 | Mereo Biopharma 5, Inc. | Sredstva za vezivanje vegf/dll4 i njihova uporaba |
| US9599620B2 (en) | 2012-10-31 | 2017-03-21 | Oncomed Pharmaceuticals, Inc. | Methods and monitoring of treatment with a DLL4 antagonist |
| WO2014117053A1 (en) * | 2013-01-27 | 2014-07-31 | The Cleveland Clinic Foundation | Anti-angiogenic vegf-ax isoform |
| ES2808153T3 (es) | 2014-10-31 | 2021-02-25 | Mereo Biopharma 5 Inc | Terapia de combinación para tratamiento de enfermedad |
| WO2017053705A1 (en) | 2015-09-23 | 2017-03-30 | Oncomed Pharmaceuticals, Inc. | Methods and compositions for treatment of cancer |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001513111A (ja) * | 1997-03-03 | 2001-08-28 | ベス・イスラエル・デイーコネス・メデイカル・センター | 腫瘍付随血管(tumor−associated blood vessels)上の血管透過因子の複数のエピトープに結合する同時インビボイムノコンジュゲート |
| JP2005502333A (ja) * | 2001-08-01 | 2005-01-27 | ユニバーシティ オブ ブリストル | 増殖因子イソ型 |
| WO2005007198A2 (en) * | 2003-07-08 | 2005-01-27 | Attogen, Inc. | Design of disease specific agents for diagnostics and therapeutics based on the protein isoform of vegf, her-2, psa |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5530101A (en) * | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US7667004B2 (en) | 2001-04-17 | 2010-02-23 | Abmaxis, Inc. | Humanized antibodies against vascular endothelial growth factor |
| JP2008538927A (ja) * | 2005-04-29 | 2008-11-13 | (オーエスアイ)アイテツク・インコーポレーテツド | Vegf変種 |
| US20080031815A1 (en) * | 2006-07-27 | 2008-02-07 | Xiaoyuan Chen | Pet imaging of vascular endothelial growth factor receptor (VEGFR), compositions for VEGF cancer imaging, and methods of VEGF cancer imaging |
| GB0704678D0 (en) | 2007-03-09 | 2007-04-18 | Univ Bristol | Pro- and anti-angiogenic treatments |
-
2008
- 2008-10-26 JP JP2010530629A patent/JP2011504092A/ja active Pending
- 2008-10-26 CN CN2008801226493A patent/CN101970486A/zh active Pending
- 2008-10-26 WO PCT/IL2008/001410 patent/WO2009053987A1/en active Application Filing
- 2008-10-26 CA CA2703154A patent/CA2703154A1/en not_active Abandoned
- 2008-10-26 EP EP08842953A patent/EP2203480A1/en not_active Withdrawn
- 2008-10-26 AU AU2008315414A patent/AU2008315414A1/en not_active Abandoned
- 2008-10-26 US US12/739,619 patent/US8592563B2/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001513111A (ja) * | 1997-03-03 | 2001-08-28 | ベス・イスラエル・デイーコネス・メデイカル・センター | 腫瘍付随血管(tumor−associated blood vessels)上の血管透過因子の複数のエピトープに結合する同時インビボイムノコンジュゲート |
| JP2005502333A (ja) * | 2001-08-01 | 2005-01-27 | ユニバーシティ オブ ブリストル | 増殖因子イソ型 |
| WO2005007198A2 (en) * | 2003-07-08 | 2005-01-27 | Attogen, Inc. | Design of disease specific agents for diagnostics and therapeutics based on the protein isoform of vegf, her-2, psa |
Non-Patent Citations (4)
| Title |
|---|
| JPN6013037826; Cancer Res., 2004, 64(21), pp.7822-7835 * |
| JPN6013037827; Diabetologia, 2005, 48(11), pp.2422-2427 * |
| JPN6013037828; Br. J. Cancer, 2007, 97(2), pp.223-230 (Epub 2007 Jun 26) * |
| JPN6013037829; Mol. Vis., 2006, 12, pp.626-632 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014528693A (ja) * | 2011-06-15 | 2014-10-30 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 抗ヒトepo受容体抗体及び使用方法 |
| WO2016194708A1 (ja) * | 2015-05-29 | 2016-12-08 | 国立大学法人名古屋大学 | 尿中VEGF-A165bを指標とした腎機能の検査方法及び検査装置、腎機能の検査装置として機能させるためのプログラム及び記録媒体 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2703154A1 (en) | 2009-04-30 |
| EP2203480A1 (en) | 2010-07-07 |
| US20100272733A1 (en) | 2010-10-28 |
| AU2008315414A1 (en) | 2009-04-30 |
| US8592563B2 (en) | 2013-11-26 |
| WO2009053987A1 (en) | 2009-04-30 |
| CN101970486A (zh) | 2011-02-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2011504092A (ja) | 血管内皮増殖因子(vegf)の血管新生誘発性アイソフォームに特異的な抗体 | |
| JP6591428B2 (ja) | 癌治療のためのpd−1拮抗薬およびvegfr阻害剤の組み合わせ | |
| JP6000427B2 (ja) | 抗エンドグリン抗体及び抗vegf剤を用いる癌の併用療法 | |
| JP6385277B2 (ja) | 癌治療のための抗ceacam1組換え型抗体 | |
| KR101320198B1 (ko) | 신생물의 치료를 위한 조성물 및 방법 | |
| KR20200034817A (ko) | 항-vegf 항체를 사용한 치료 | |
| MX2012009554A (es) | Terapia anti-angiogenesis para el tratamiento del cancer ovarico. | |
| KR20120096401A (ko) | 아주반트 암 요법 | |
| JP7408559B2 (ja) | プラチナベースの薬剤と抗組織因子抗体-薬物コンジュゲートの組み合わせを用いるがんの治療方法 | |
| US11081235B2 (en) | Extracellular matrix metalloproteinase inducer (EMMPRIN) peptides and binding antibodies | |
| JP2016117718A (ja) | 以前に治療された乳癌の治療のための抗血管新生療法 | |
| JP2022545959A (ja) | Amhrii結合性 抗体薬物コンジュゲート、及び癌の処置におけるそれらの使用 | |
| KR20210066837A (ko) | 암 치료를 위한 pd-1 안타고니스트, atr 억제제 및 백금화제의 조합 | |
| WO2011119656A1 (en) | Anti-angiogenesis therapy for treating abdominal aortic aneurysm | |
| JP2019531337A (ja) | 増殖因子を標的とする二機能性分子を使用したがんの治療方法 | |
| KR102207221B1 (ko) | 도펠-타겟팅 분자를 이용한 병리학적 신생혈관 생성을 억제하는 방법 | |
| AU2022402850A1 (en) | Anti-folate receptor conjugate cancer therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110930 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110930 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120919 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130731 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20131227 |