JP2010538252A - 器官損傷の同定方法 - Google Patents
器官損傷の同定方法 Download PDFInfo
- Publication number
- JP2010538252A JP2010538252A JP2010522447A JP2010522447A JP2010538252A JP 2010538252 A JP2010538252 A JP 2010538252A JP 2010522447 A JP2010522447 A JP 2010522447A JP 2010522447 A JP2010522447 A JP 2010522447A JP 2010538252 A JP2010538252 A JP 2010538252A
- Authority
- JP
- Japan
- Prior art keywords
- sample
- protein
- identification method
- patient
- induced
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/90—Enzymes; Proenzymes
- G01N2333/91—Transferases (2.)
- G01N2333/912—Transferases (2.) transferring phosphorus containing groups, e.g. kinases (2.7)
- G01N2333/91205—Phosphotransferases in general
- G01N2333/9121—Phosphotransferases in general with an alcohol group as acceptor (2.7.1), e.g. general tyrosine, serine or threonine kinases
- G01N2333/91215—Phosphotransferases in general with an alcohol group as acceptor (2.7.1), e.g. general tyrosine, serine or threonine kinases with a definite EC number (2.7.1.-)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/90—Enzymes; Proenzymes
- G01N2333/99—Isomerases (5.)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/08—Hepato-biliairy disorders other than hepatitis
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Analytical Chemistry (AREA)
- Biotechnology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
(化学物質)
全ての化学物質は、特記されない限りはSigma(Poole,UK)から得られる。
健康な、男性のボランティア(24〜40才、(MREC倫理承認番号06/MRE00/67))は、エジンバラ大学のQueen's Medical Research Instituteからリクルートされた。
健康な個人から12ml(4×3クエン酸チューブ)の人の血液が集められた。血液を4000×gにて20分間遠心して、細胞から血漿を分離した。遠心された血漿の上層の500μlを夫々のチューブから抽出し、10000rpmにて4℃で一時間遠心された(Optima(TM) TLX Ultracentrifuge, Beckman Coulter, Inc., USA)。上清は200μlの食塩水にて洗い流され、ペレットは1mlの食塩水(Braun)にて2回洗浄された。ペレットは200μlの食塩水に再懸濁され、フローサイトメトリー分析に処されるまで4℃にて保存された(図1A参照)。
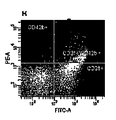
フルオレッセンイソチオシアネート(FITC)ラベルされた抗ヒトCD3及びPhycoerythrin(PE)ラベルされた抗ヒトCD42b抗体マーカー(BD Biosciences, San Jose, USA) (20 μl 抗体/ 100μl MP 試料)がMPパレットに添加され、室温にて、通常の振盪にて30分間培養された。フルオレッセンス活性化細胞選別(FACS)分析は、エジンバラ大学のFlow cytometry core facility, QMRIにおいてDiVaオプションを有するFACS VANTAGE(BD, San Jose, USA)により行われた。事象は、前方散乱強度及び後方散乱強度によりドットにて示されるように同定され、MPsとしてゲート制御され、1色又は2色の蛍光ヒストグラムとしてプロットされる。EMPsはCD31+CD42b-として定義され、PMPsはCD31+CD42b+として定義される。
6名のボランティア(23〜40才、(MREC倫理承認番号06/MRE00/67))は、尿試料を滅菌された50mlのプラスチック容器に提供した。夫々の試料に対しプロテアーゼインヒビターが添加された(1mMレオペプチン50:1)。パラセタモール過剰投与後4及び24時間後の患者からの尿試料が分析された。患者6名中3名において顕著な肝臓損傷が認定された24時間後に血清アラニン・トランスアミナーゼ(ALT)が上昇していた。試料は15000gにて15分間4℃で遠心され、尿沈渣をペレット化した。「15000gの上清」は、10000rpmにて1時間4℃で遠心され、低濃度のエキソソームペレットが得られた。10000rpmの上清はデキャントされ、付加的な「15000gの上清」と置き換えられ、再度、超遠心に供された。超遠心のステップは4〜6回繰返され、15000gの上清18〜24mlからエキソソームペレットが回収される。ペレットは、50μlの単離溶液(10 mM トリエタノールアミン/ 250 mM スクロース (pH 7.6))に再懸濁される。パラセタモールを過剰投与した患者からの尿が3mlのみであることから、15000g上清を10000rpmにて1時間超遠心して、得られる尿エキソソームを最大とするようにプロトコールを変更した(図1b参照)。
尿及びMPsのタンパク質の量は、BCA(登録商標)タンパク質アッセイキット(Pierce, USA)用いて、その説明書に従い決定された。20μgの通常の尿エキソソーム試料がウェル毎にロードされる。パラセタモール過剰投与試料の各ローディング量は、尿の濃度に違いによった尿のクレアチンにより標準化される。0.2MのDTT(Bio-Rad)を有するLaemmli Sample Bufferの均等量はタンパク質試料に添加され、かかる試料は95℃にて5分間加熱される。タンパク質試料は、12 % Tris-HClゲル(Bio-Rad)内を1D SDS/ポリアクリルアミドゲル電気泳動により、移動バッファー (25 mM Tris (Fisher Scientific), 192 mM グリシン及び0.1 % SDS)内にてゲル毎に25 mAで1時間、分子量マーカー(Bio-Rad)とともに流され、分離された。
タンパク質の体積(20μg)はゲルのウェル毎にロードされることから、ゲルは100μgのタンパク質を含み、前述したように流された。次いで、ゲルは、7%の氷酢酸及び40%のメタノールにより、1時間固定される。ゲルはコロイド状のクマシーブルーにより1時間染色され、10%氷酢酸及び25%のメタノールにより30秒間脱色されられる。ゲルは同一の溶液により脱色される前に、25%メタノールによりリンスされる。ゲルは(図6に示すように)スライスされ、また、更に小さな部分へとスライスされ、タンパク抽出のステップまで-80℃にて保存される。
APAPを過剰投与したRoyal Infirmary of Edinburghの患者から約50mlの尿が集められた。尿は集められ、CyPAレベルを測定する前に、−80℃にて保存される。
(フローサイトメトリー分析)
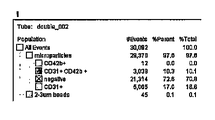
図2は、FACSを使用して選別された試料の側方散乱/前方散乱ドットプロットヒストグラムを示す。強調された2.5μmキャリブレーションビーズは、MPsの寸法を示し、MPsの全ての集団は、過去のMPs研究に基づき2.5μm寸法未満であった。EMPsは、図2(B及びF)に示すように、PMPsよりもわずかに寸法が小さく、図2(C及びD)に示すように、PMP集団の下方に位置している。単一染色したMPsは、集団の位置を同定するコントロールとして、CD31又はCD43bにより染色され、そして、両細胞表面マーカーの存在しない試料は、ネガティブコントロールとなり、非内皮細胞の血小板由来のMPsを提供する。大多数のMPsはCD31及びCD42bに対し陰性であり、これらは異なる起源及び細胞種に由来するものである。MPsの陰性のグループは、異なる集団を形成し、72.6%の試料を作り出した。EMPs及びPMPsはともに異なる寸法を有する粒子の異なる集団として同定される。パネルD及びHは、EMPs及びPMPsを選別するために二重染色した試料を示す。17%まで至る単一の陽性のCD43bMPs及びCD41+EMPsはないが、CD31+CD42bPMPsは全量の10.3%に至る。FITCラベルされたMPs量が少ないと、MPsは内皮細胞性をより起源とするものであり、CD31が多いとMPsはよりCD42+であり、血小板をより起源とするものである。
転写因子GATA-2が微粒子中に存在するか否かをウェスタンブロットにより調査した。EMP及びPMP集団が選別された後、試料はMPsをペレット化するために超遠心に供された。超遠心した後のペレット及び上清の両方は保持され、GATA-2の存在を検出するためのウェスタンブロットが行われた。図4はGATA-2が上清に存在しており、一つの上清のみにおいてGATA-2が存在していたことを示しているウェスタンブロットの結果である。個人1からのEMP及びPMP試料(夫々レーン1及び4)は、その他のMP試料に比べGATA-2のレベルが大きかった。このことは、個人(夫々5516089及び380548;図3の試料4)から単離されたEMPs及びPMPsと整合している。
パラセタモールを過剰投与し、器官損傷した、又はしていない患者の尿中のエキソソームタンパク質の濃度は、通常の尿と比較された。6名の通常の尿エキソソーム試料では、平均が3.54±1.22μgタンパク質/ml尿であった。パラセタモールの過剰投与4時間後に、器官損傷を示さなかった3名の患者からプールされた試料は、通常の健康な個人に比べ、約7倍のタンパク質量の増大が見られた。また、パラセタモールの過剰投与4時間後に、器官損傷を示した3名の患者からプールされた試料は、プールされた試料中のエキソソームタンパク質は37倍までの増大が見られた。過剰投与の24時間後には、器官損傷を有する患者及び有さない患者の双方において、プールされた尿試料内のエキソソームタンパク質量が同様のレベルまで減少していた(通常のレベルに対し1.5〜2.0倍)。
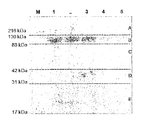
通常の尿試料のパイロットプロテオミクスを行うために、〜100μgの通常のエキソソームがゲルにロードされ、コロイド状のクマシーブルーにより染色され、タンパク質の存在を調べた。図6は、染色されたゲルを示し、エキソソーム試料中に異なる寸法のタンパク質が存在することの証拠を提供するものである。また、最も豊富なタンパク質のバンドはゲルの部分Bであり、THPであると推定されるものである。ドット線は、LC-MS/MSによるプロテオミクス分析に供される異なる試料を準備するためのゲルが切られた位置を示す。
この実験は、血液中のMPs及び尿中のエキソソームがバイオマーカーとしての候補源として使用し得るかを調査するためのものである。主たる成果は、EMPs(内皮性微粒子)がフローサイトメトリーにより単離されるが、(図3Aに示すように)単離された微粒子数は個人間差が大きく、標準的なタンパク質分析では検出することが難しいレベルのタンパク質量しか得られない。MPsの分離は、時間を要するものであり、臨床試験には効果的な方法ではない。In vitroの実験系を用いて、内皮細胞を培養して、かかる培養細胞からMPsを単離することが有効な解決策となり得るものである。これは他のグループにより成功している(Combes et al., 1999)。候補タンパク質は、そのレベルにより決定される。可能性のある候補タンパク質がin vitro研究により見つかったら、器官が機能不となっている患者において、そのタンパク質の発現レベルが変化しているかを確認する。
GATA-2は、GATA-2転写因子ファミリーに属する。GATA-2は、造血現象において重要な役割を果たす。原始的造血細胞は高レベルでGATA-2を発現するが、血液細胞の異なるタイプへの細胞の成熟の過程で、そのレベルは減少する(Tsai et al, 1994)。大人の造血細胞では、GATA-2が発現し、内皮特異的な遺伝子の転写調節に重要である(Zhang et al., 1995)。GATA-2には複数の燐酸化された形態があり(Towatari et al., 1995)、図4は、EMPsとPMPsの双方に複数の形態のGATA-2があることを示している。しかし、これらの結果は、in vitroにてヒト臍の静脈内皮細胞(HUVECS)を使用して、GATA-2の同じ形が検出されることができるかどうか調べて立証される。MPs中のGATA-2をGATA-2の転写因子であるとして観察することは興味深く、このことは転写因子をin vivoでの遺伝子発現のバイオマーカーとして使用し得る可能性を示唆するものである。
図5Aは、パラセタモールの過剰投与が、過剰投与4時間後に、エキソソームタンパク尿症を増大させることを示すものである。タンパク尿症は、器官損傷を有する患者において特に多い(〜37回、通常比較された)。過剰投与した患者の超遠心した上清は、同一の分析にて同様の尿試料を用いた場合にも、多様性を示した(データ不図示)。このことは、尿内におけるパラセタモール(アセトアミノフェン)代謝産物の存在によるものであり、かかる代謝産物はこの実験系にて使用されるBSA分析等のタンパク質分析に干渉するものである(Marshall and Williams, 1991)。かかるタンパク尿症が発症する正確な理由は解明されていない。エキソソームが腎臓から放出され、循環MPsが糸球体を経て尿に入り込んでいるかどうかも知られていない。また、薬が腎臓または血管に対する効果を有するかどうか、は決定されないままである。薬の過剰投与24時間後にはタンパク質レベルが通常に対し1.5倍まで落ちることは興味深いことであるが、このことは、肝損傷の減少又は血液のパラセタモール濃度の減少させるための臨床介入によって説明することができる。
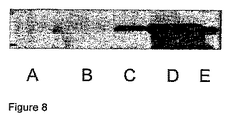
APAP誘導器官損傷を有する患者の尿において、CyPA濃度が増大していた。図8は、健康な対象(A)、僅かな肝臓損傷(B)、中程度の肝臓損傷(C)、重症な肝臓損傷(D)及び重症な肝臓及び腎臓損傷(E)を有する患者からの尿ウェスタンブロットを示す。
パラセタモールの過剰投与は、イギリス及び米国(Larson et al., 2005)では急性の肝機能不全の主たる原因となっている。パラセタモール代謝と肝臓損傷とをリンクさせる経路は未だ完全に明らかとなっていない。パラセタモールの過剰投与初期には、サイトカイン及びケモカインは、その損傷(Ishida et al., 2002)及び回復(Hogaboam et al., 1999)に関係するものである。
疾患の研究におけるプロテオミクスは、有用なツールであり、疾患を有する又は有さない個人の試料内のタンパク質を同定するために使用することができる。しかし、プロテオミクスに問題が無いわけではない。この研究では、LC-MS/MS分析に供されたゲルスライス試料の5つのうちの3つにおいて、コロイド状のクマシーブルーを多く含み過ぎているために、検出することができなかった。また、プロテオミクスにて使用される装置は、感度が極めて高く、過剰な染色により損傷をうける場合がある。分析できた2つの資料では、よくあることではあるが、何らペプチド断片が得られなかった。これらの問題は、修正され、プロトコールを僅かに変えながら実験は繰り返された。プロテオミクスの主たる問題は、非常に大量のタンパク質(例えば血漿のアルブミン及び尿のTHP)が、プロテオミクス分析に供される前に試料から取り除かれない限りは、より少ないタンパク質の検出の妨げることにある。THPは、試料に還元剤を処理することにより、そして、試料を再度超遠心することにより、取り除くことができる。THPは上清に残り、少ない量のタンパク質についてペレットを分析に供することができる(Pisitkun et al., 2004)。アルブミンは、SwellGel Albumin Removal kit from Pierce, Rockford, USAなどの商業的に利用可能なキットを用いて取り除くことができる。或いは、血清アルブミンを取り除くために、トリクロロ酢酸及びアセトンを使用することができる(Chen et al., 2005)。試料のプロテオミクス分析の前に、これら大量のタンパク質を取り除くことにより、体の健康状態及び一部の疾患の病因について有益な情報を与えるかもしれない低い濃度のタンパク質を同定し得る機会が増える。MPs及びエキソソームについて有効なタンパク質の同定が報告された。Smalleyら(2007)は、血小板MPs内ではなく、血漿MPs内にて21種のタンパク質を同定することに成功し、Zhouら(2006)は、急性の腎臓損傷に対するバイオマーカー候補を同定した。
Amabile, N., Guerin, A.P., Leroyer, A., Mallat, Z., Nguyen, C, Boddaert, J., London, G.M., Tedgui, A. and Boulanger, CM. (2005). Circulating endothelial microparticles are associated with vascular dysfunction in patients with end-stage renal failure. J Am Soc Nephrol 16: 3381-88.
Anderson, N.L. and Anderson, N.G. (2002). The human plasma proteome: history, character, and disagnostic prospects. MoI Cell Proteomics 1: 845-67.
Banfi, C, Brioschi, M., Wait, R., Begum, S., Gianazza, E., Pirillo, A., Mussoni, L. and Tremoli, E. (2005). Proteome of endothelial cell-derived procoagulant microparticles. Proteomics 5: 4443-4455.
Bateman DN. Poisoning: focus on paracetamol. Royal College of Physiciansof Edinburgh CME 2007; http://www.rcpe.ac.uk/fellows/CME/clin-pharmacol/bateman/bateman-2.html
Bohmann, D., Bos, T.J., Admon, A., Nishimura, T., Vogt, P.K. and Tjian, R. (1987). Human proto-oncogene c-Jun encodes a DNA binding protein with structural and functional properties of transcription factor API. Science 238: 1386-1392.
Brodsky, S. V., Zhang F., Nasjletti A. and Goligorsky M.S.(2004). Endothelium- derived microparticles impair endothelial function in vitro. Am J Physiol Heart Circ Physiol 286: 1910-15.
Chen, Y. Y. , Lin, S., Yeh, Y., Hsiao, H., Wu, C, Chen,S. and Wang, A.H. (2005). A modified protein precipitation procedure for efficient removal of albumin from serum. Electrophoresis 26: 2117-27.
Combes, V., Simon, A.C., Grau, G.E., Arnoux, D., Camoin, L., Sabatier, F., Mutin, M., Sanmarco, M., Sampol, J. and Dignat-George, F. (1999). In vitro generation of endothelial microparticles and possible prothrombotic activity in patients with lupus anticoagulant. J Clin Invest 104: 93-102.
George, J.N., Thoi, L.L., McManus, L.M. and Reimann, T.A. (1982). Isolation of human platelet microparticles from plasma and serum. Blood 60: 834-840.
Henderson, N.C., Pollock, K., Frew, J., Mackinnon, A.C., Flavell, R.A., Davis, RJ., Sethi, T. and Simpson, K. J. (2006). Critical role of c-jun (NH2) terminal kinase in paracetamol-induced acute liver failure. Gut (E-pub ahead of print).
Hewitt, S.M., Dear, J. W., Star, R.A. (2004). Discovery of protein biomarkers for renal diseases. JAm Soc Nephrol 15: 1677-89.
Hogaboam, CM., Simpson, K.J., Chensue, S.W., Steinhauser, MX., Lukacs, N. W., Gauldie, J., Strieter, R.M. and Kunkel, S.L. (1999). Macrophage inflammatory protein-2 gene therapy attenuates adenovirus-and paracetamol-mediated hepatic injury. Gene Ther 6: 573-584.
Ishida, Y., Kondo, T., Ohshima, T., Fujiwara, H., Iwakura, Y. and Mukaida, N. (2002). A pivotal involvement of IFN-gamma in the pathogenesis of paracetamol- induced acute liver injury. FASEB J 16:1227-1236.
Johnstone, R.M., Adam, M., Hammond, J.R., Orr, L. and Turbide, C. (1987). Vesicle formation during reticulocyte maturation. Association of plasma membrane activities with released vesicles (exosomes). J Biol Chem 262: 9412-20.
Larson, A.M., Poison, J., Fontana, R.J., Davern, T.J., Lalani, E., Hynan, L.S., Reisch, J.S., Schiodt, F. V., Ostapowicz, G., Shakil, A.O. and Lee, W.M. (2005). Acetaminophen-induced acute liver failure: results of a United Statesmulticenter, prospective study. Hepatology 42 (6): 1364-72.
Liu, H., Lo, CR. and Czaja, M.J. (2002). NF-kappa B inhibition sensitizes hepatocytes to TNF-induced apoptosis through a sustained activation of JNK and c-Jun. Hepatology 35:772-778.
Marshall, T. and Williams, K.M. (1991). Drug interference in the Bradford and 2,2'- bicinchoninic acid protein assays. Anal Biochem 198: 352-4. Pisitkun, T., Shen, R.F. and Knepper, M. A. (2004). Identification and proteomic profiling of exosomes in human urine. Proc Natl Acad Sci USA 101: 13368-73.
Preston, R.A., Jy, W., Jimenez, J.J., Mauro, L.M., Horstman, L.L., Valle, M., Aime, G. and Ahn, Y. (2003). Effects of severe hypertension on endothelial and platelet microparticles. Hypertension 41: 211-217.
Reilly TP, Bourdi M, Brady JN, Pise-Masison CA, Radonovich MF, George JW, et al. Expression profiling of acetaminophen liver toxicity in mice using microarray technology. Biochem Biophys Res Commun 2001;282(l):321-8
Smalley, D.M., Root, K.E., Cho, H., Ross, M.M. and Ley, K. (2007). Proteomic discovery of 21 proteins expressed in human plasma-derived but not platelet-derived microparticles. Thromb Haemost 97: 67-80.
Towatari, M., May, G.E., Marais, R., Perkins, G.R., Marshall, CJ., Cowley, S. and Enver, T (1995). Regulation of GATA-2 Phosphorylation by Mitogen-activated Protein Kinase and Interleukin-3. J Biol Chem 270: 4101-4107.
Tsai, F. Y., Keller, G., Kuo, F.C., Weiss, M., Chen, J., Rosenblatt, M., Alt, F.W. and Orkin, S.H. (1994). An early haematopoietic defect in mice lacking the transcription factor GAT A-2. Nature 371: 221-226.
Wolf, P. (1967). The nature and significance of platelet products in human plasma. Br J Haematol 3: 269-88.
Zhang, R., Min, W. and Sessa, W.C. (1995). Functional analysis of the human endothelial nitric oxide synthase promoter: SpI and GATA factors are necessary for basal transcription in endothelial cells. J Biol Chem. 270: 15320-15326.
Zhou, H., Yuen, P.S.T., Pisitkun, T., Gonzales, P.A., Yasuda, H., Dear, J. W., Gross, P., Knepper, M. A. and Star, R.A. (2006). Collection, storage, preservation and normalisation of human urinary exosomes for biomarker discovery. Kidney International 69: 1471-76.
Zhou, H., Pisitkun, T., Aponte, A., Yuen, P.S,T., Hoffert, J.D., Yasuda, H., Hu, X., Chawla, L., Shen, R.F., Knepper, M.A. and Star, R.A. (2006). Exosomal Fetuin-A identified by proteomics: A novel urinary biomarker for detecting acute kidney injury. Kidney International 70: 1847-1857.
1. Waring WS, Stephen AF, Robinson OD, Dow MA, Pettie JM. Lower incidence of anaphylactoid reactions to N-acetylcysteine in patients with high acetaminophen concentrations after overdose. Clinical Toxicology 2008; 46(6):496 - 500.
2. Colgan J, Asmal M, Yu B, Luban J. Cyclophilin A-Deficient Mice Are Resistant to Immunosuppression by Cyclosporine. J Immunol 2005; 174(10):6030-6038.
3. Takahashi N, Hayano T, Suzuki M. Peptidyl-prolyl cis-trans isomerase is the cyclosporin A-binding protein cyclophilin. Nature 1989; 337(6206):473-5.
4. Luban J, Bossolt KL, Franke EK, Kalpana GV, Goff SP. Human immunodeficiency virus type 1 Gag protein binds to cyclophilins A and B. Cell 1993 ;73(6): 1067-78.
5. Arora K, Gwinn WM, Bower MA, Watson A, Okwumabua I, MacDonald HR, et al. Extracellular cyclophilins contribute to the regulation of inflammatory responses. J Immunol 2005; 175(l):517-22.
6. Yurchenko V, Constant S, Bukrinsky M. Dealing with the family: CD 147 interactions with cyclophilins. Immunology 2006; 117(3):301-9.
7. Dear JW, Leelahavanichkul A, Aponte A, Hu X, Constant SL, Hewitt SM, et al. Liver proteomics for therapeutic drug discovery: Inhibition of the cyclophilin receptor CD 147 attenuates sepsis-induced acute renal failure*. CrH Care Pled 2007; 35(10):2319-2329.
8. Holly MK, Dear JW, Hu X, Schechter AN, Gladwin MT, Hewitt SM, et al. Biomarker and drug-target discovery using proteomics in a new rat model of sepsis- induced acute renal failure. Kidney Int 2006; 70(3):496-506.
9. Gwinn WM, Damsker JM, Falahati R, Okwumabua I, Kelly- Welch A, Keegan AD, et al. Novel approach to inhibit asthma-mediated lung inflammation using anti-CD 147 intervention. J Immunol 2006; 177(7):4870-9.
10. Billich A, Winkler G, Aschauer H, Rot A, Peichl P. Presence of Cyclophilin A in Synovial Fluids of Patients with Rheumatoid Arthritis. J. Exp. Med. 1997; 185(5):975- 980.
11. Tegeder I, Schumacher A, John S, Geiger H, Geisslinger G, Bang H, et al. Elevated serum cyclophilin levels in patients with severe sepsis. J Clin Immunol 1997;17(5):380-6.
Claims (16)
- 患者が、開発薬により誘導された器官損傷を有する或いはそのリスクを有するか否かを同定する方法であって、該方法は、
(c)患者から試料を準備するステップと、
(d)該試料中のタンパク質レベルを同定するステップと、を含み、
タンパク質レベルの増大は、患者が開発薬により誘導された器官損傷を有する或いはそのリスクを有することを示すことを特徴とする同定方法。 - 前記器官損傷は、1種以上の抗生物質及び/又は抗炎症、解熱薬、鎮痛剤或いは/並びに化学療法剤により誘導される、請求項1に記載の同定方法。
- 前記器官損傷は、パラセタモール(N(4-ヒドロキシフェニル)エタンアミド)によって誘導される、請求項1又は2に記載の同定方法。
- 損傷を受けた器官が肝臓である、請求項1から3のいずれか一項に記載の同定方法。
- 前記試料は、組織試料、生検材料及び/又は全血液から選択される体液、細胞質、血清、リンパ、尿、汗、唾液及び組織或いは/並びに腺分泌物である、請求項1〜4のいずれか一項に記載の同定方法。
- 前記試料は尿である、請求項1から5のいずれか一項に記載の同定方法。
- 前記試料は、微粒子及び/又はそれ由来のエキソソームを単離し得るプロトコールに処される、請求項1から6のいずれか一項に記載の同定方法。
- 同定されたタンパク質のレベルを、コントロール又は基準試料にて同定されたタンパク質のレベルと比較するステップを更に具える、請求項1から7のいずれか一項に記載の同定方法。
- 前記基準又はコントロール試料は、微粒子/エキソソーム単離プロトコールに処される、請求項8に記載の同定方法。
- 前記試料内のタンパク質レベルを同定するステップにおいて、準備された試料中の核酸レベルを同定する、請求項1から9のいずれか一項に記載の同定方法。
- 前記試料内のタンパク質レベルを同定するステップにおいて、免疫学的手法を用いる、請求項1から9のいずれか一項に記載の同定方法。
- 前記試料内のタンパク質は、転写因子及び/又は細胞内タンパク質である、請求項1から11のいずれか一項に記載の同定方法。
- 前記転写因子はc-Jun N末端キナーゼ(JNK)であり、細胞内タンパク質はサイクロフィリンA(CyPA)である、請求項12に記載の同定方法。
- 前記核酸は、転写因子c-Jun及び/又はCyPAをコードする、請求項10に記載の同定方法。
- 患者が、開発薬により誘導された器官損傷を有する或いはそのリスクを有するか否かを同定する方法であって、該方法は、
(a)患者から試料を準備するステップと、
(b)該試料中のタンパク質レベルを同定するステップと、を含み、
タンパク質レベルの増大は、患者がパラセタモールにより誘導された肝臓損傷を有する或いはその発症リスクを有することを示すことを特徴とする同定方法。 - 前記タンパク質は、c-Jun N末端キナーゼ(JNK)及び/又はサイクロフィリンA(CyPA)である、請求項15に記載の同定方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0716804.0A GB0716804D0 (en) | 2007-08-29 | 2007-08-29 | Identifying organ damage |
| PCT/GB2008/002947 WO2009027703A2 (en) | 2007-08-29 | 2008-08-29 | Identifying organ damage |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010538252A true JP2010538252A (ja) | 2010-12-09 |
| JP2010538252A5 JP2010538252A5 (ja) | 2011-10-13 |
Family
ID=38616940
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010522447A Pending JP2010538252A (ja) | 2007-08-29 | 2008-08-29 | 器官損傷の同定方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US8110371B2 (ja) |
| EP (1) | EP2183601A2 (ja) |
| JP (1) | JP2010538252A (ja) |
| GB (1) | GB0716804D0 (ja) |
| WO (1) | WO2009027703A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019215342A (ja) * | 2018-06-07 | 2019-12-19 | 株式会社Lsiメディエンス | ヒト尿からのマイクロベシクルの分離方法及び分析方法 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2463401B (en) | 2008-11-12 | 2014-01-29 | Caris Life Sciences Luxembourg Holdings S A R L | Characterizing prostate disorders by analysis of microvesicles |
| JP2012531605A (ja) * | 2009-07-01 | 2012-12-10 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 心血管死亡率リスクを予測するための方法 |
| CA2791905A1 (en) | 2010-03-01 | 2011-09-09 | Caris Life Sciences Luxembourg Holdings, S.A.R.L. | Biomarkers for theranostics |
| AU2011237669B2 (en) | 2010-04-06 | 2016-09-08 | Caris Life Sciences Switzerland Holdings Gmbh | Circulating biomarkers for disease |
| ITNA20110012A1 (it) * | 2011-03-14 | 2012-09-15 | Amal Raj Delfin Albert | Procedura di isolamento e di purificazione degli esosomi urinari per la ricerca di biomarcatori proteici |
| CN105606811A (zh) * | 2016-02-01 | 2016-05-25 | 中南大学 | 一种鼻咽癌诊断试剂盒 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10507184A (ja) * | 1994-10-12 | 1998-07-14 | ペーアーツェト アルツナイミッテル−エントヴィックルングスゲゼルシャフト ミット ベシュレンクテル ハフツング | ヒトにおけるショック状態の診断評価法及び経過コントロール法及び治療用薬剤 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6719969B1 (en) * | 1999-08-09 | 2004-04-13 | The Regents Of The University Of Michigan | Treatment of liver disease and injury with CXC chemokines |
| AU2002216273A1 (en) * | 2000-12-29 | 2002-07-16 | Oxford Glycosciences (Uk) Limited | Proteins, genes and their use for diagnosis and treatment of kidney response |
| US7469185B2 (en) * | 2002-02-04 | 2008-12-23 | Ocimum Biosolutions, Inc. | Primary rat hepatocyte toxicity modeling |
| US8758991B2 (en) * | 2006-04-26 | 2014-06-24 | University Of Louisville Research Foundation, Inc. | Isolation of membrane vesicles from biological fluids and methods of using same |
-
2007
- 2007-08-29 GB GBGB0716804.0A patent/GB0716804D0/en not_active Ceased
-
2008
- 2008-08-29 JP JP2010522447A patent/JP2010538252A/ja active Pending
- 2008-08-29 EP EP08788492A patent/EP2183601A2/en not_active Withdrawn
- 2008-08-29 WO PCT/GB2008/002947 patent/WO2009027703A2/en active Application Filing
- 2008-08-29 US US12/675,479 patent/US8110371B2/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10507184A (ja) * | 1994-10-12 | 1998-07-14 | ペーアーツェト アルツナイミッテル−エントヴィックルングスゲゼルシャフト ミット ベシュレンクテル ハフツング | ヒトにおけるショック状態の診断評価法及び経過コントロール法及び治療用薬剤 |
Non-Patent Citations (1)
| Title |
|---|
| JPN6012037899; Gut Vol.56, 2006, p982-990 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019215342A (ja) * | 2018-06-07 | 2019-12-19 | 株式会社Lsiメディエンス | ヒト尿からのマイクロベシクルの分離方法及び分析方法 |
| JP7444386B2 (ja) | 2018-06-07 | 2024-03-06 | 株式会社Lsiメディエンス | ヒト尿からのマイクロベシクルの分離方法及び分析方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009027703A2 (en) | 2009-03-05 |
| EP2183601A2 (en) | 2010-05-12 |
| US20110039276A1 (en) | 2011-02-17 |
| US8110371B2 (en) | 2012-02-07 |
| GB0716804D0 (en) | 2007-10-10 |
| WO2009027703A3 (en) | 2009-06-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8741580B2 (en) | Markers of renal transplant rejection and renal damage | |
| EP2281203B1 (en) | A marker for graft failure and mortality | |
| Jung et al. | Quantification of ATP7B protein in dried blood spots by peptide immuno-SRM as a potential screen for Wilson’s disease | |
| US8110371B2 (en) | Identifying organ damage | |
| JP6841765B2 (ja) | 慢性腎疾患の発症のリスクを予測するための方法 | |
| Kongtasai | Renal biomarkers in cats: A review of the current status in chronic kidney disease | |
| JP2012524883A (ja) | 腎臓障害生物マーカとしてのwnt1 | |
| US20210116462A1 (en) | Methods and Compositions for the Diagnosis and Treatment of Kawasaki Disease | |
| Tomar et al. | New biomarkers in brain trauma | |
| JPWO2008056480A1 (ja) | 脂肪性肝疾患の診断方法、診断装置、診断プログラム、診断薬及び脂肪性肝疾患用治療薬のスクリーニング方法 | |
| US20140370531A1 (en) | Method of diagnosing mild traumatic brain injury | |
| Khan et al. | Proteomics in idiopathic pulmonary fibrosis: the quest for biomarkers | |
| Brown et al. | Protein and microRNA biomarkers from lavage, urine, and serum in military personnel evaluated for dyspnea | |
| Sigdel et al. | Assessment of circulating protein signatures for kidney transplantation in pediatric recipients | |
| US20160244835A1 (en) | Urinary neuropilin-1 (nrp-1) as a prognostic marker for nephritis and lupus nephritis | |
| WO2017126514A1 (ja) | 非アルコール性脂肪肝炎検出方法 | |
| JP7271442B2 (ja) | 腎機能を診断またはモニターする方法、または腎機能障害を診断することを補助する方法 | |
| US8969015B2 (en) | Methods and kits for diagnosing Sjögren's syndrome | |
| US20200064344A1 (en) | Use of serum 2-cysteine peroxiredoxins (2-cys-prdx) as biomarkers of chronic kidney diseases | |
| JP2009513960A (ja) | 神経変性疾患を診断するためのinvitro方法 | |
| US20170030929A1 (en) | Diagnosis of chronic kidney disease by quantitative analysis of post-translational modifications of plasma proteins | |
| JP5010220B2 (ja) | 造血幹細胞移植療法の施行患者の病態把握方法 | |
| Donia et al. | Study for the relationship between lupus nephritis and Anti-C1q antibodies | |
| WO2021245413A1 (en) | Methods of determining cancer | |
| US20150064715A1 (en) | Urinary biomarkers of renal and mitochondrial dysfunction |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7426 Effective date: 20101228 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20101228 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110202 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20110202 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110826 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110826 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120718 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120724 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20121024 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20121031 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20121126 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20121203 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130312 |