JP2010523676A - ヒト免疫不全ウイルスに対する中和抗体を誘導する方法 - Google Patents
ヒト免疫不全ウイルスに対する中和抗体を誘導する方法 Download PDFInfo
- Publication number
- JP2010523676A JP2010523676A JP2010503070A JP2010503070A JP2010523676A JP 2010523676 A JP2010523676 A JP 2010523676A JP 2010503070 A JP2010503070 A JP 2010503070A JP 2010503070 A JP2010503070 A JP 2010503070A JP 2010523676 A JP2010523676 A JP 2010523676A
- Authority
- JP
- Japan
- Prior art keywords
- peptide
- hiv
- mab
- liposome
- mper
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 241000725303 Human immunodeficiency virus Species 0.000 title claims abstract description 42
- 238000000034 method Methods 0.000 title claims abstract description 29
- 230000001939 inductive effect Effects 0.000 title claims abstract description 10
- 230000003472 neutralizing effect Effects 0.000 title abstract description 38
- 239000002502 liposome Substances 0.000 claims description 91
- 230000027455 binding Effects 0.000 claims description 80
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 74
- 241000713772 Human immunodeficiency virus 1 Species 0.000 claims description 53
- 101800001690 Transmembrane protein gp41 Proteins 0.000 claims description 37
- 239000000562 conjugate Substances 0.000 claims description 34
- 150000002632 lipids Chemical class 0.000 claims description 30
- 230000002163 immunogen Effects 0.000 claims description 19
- 239000012528 membrane Substances 0.000 claims description 15
- TZCPCKNHXULUIY-RGULYWFUSA-N 1,2-distearoyl-sn-glycero-3-phosphoserine Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(=O)OC[C@H](N)C(O)=O)OC(=O)CCCCCCCCCCCCCCCCC TZCPCKNHXULUIY-RGULYWFUSA-N 0.000 claims description 12
- ZWZWYGMENQVNFU-UHFFFAOYSA-N Glycerophosphorylserin Natural products OC(=O)C(N)COP(O)(=O)OCC(O)CO ZWZWYGMENQVNFU-UHFFFAOYSA-N 0.000 claims description 12
- GZQKNULLWNGMCW-PWQABINMSA-N lipid A (E. coli) Chemical compound O1[C@H](CO)[C@@H](OP(O)(O)=O)[C@H](OC(=O)C[C@@H](CCCCCCCCCCC)OC(=O)CCCCCCCCCCCCC)[C@@H](NC(=O)C[C@@H](CCCCCCCCCCC)OC(=O)CCCCCCCCCCC)[C@@H]1OC[C@@H]1[C@@H](O)[C@H](OC(=O)C[C@H](O)CCCCCCCCCCC)[C@@H](NC(=O)C[C@H](O)CCCCCCCCCCC)[C@@H](OP(O)(O)=O)O1 GZQKNULLWNGMCW-PWQABINMSA-N 0.000 claims description 11
- 239000012634 fragment Substances 0.000 claims description 9
- 230000006698 induction Effects 0.000 claims description 8
- 238000004519 manufacturing process Methods 0.000 claims description 6
- 238000011282 treatment Methods 0.000 claims description 6
- 239000000863 peptide conjugate Substances 0.000 claims description 5
- 102100030802 Beta-2-glycoprotein 1 Human genes 0.000 claims description 4
- 101710180007 Beta-2-glycoprotein 1 Proteins 0.000 claims description 4
- 230000000694 effects Effects 0.000 claims description 4
- 230000028993 immune response Effects 0.000 claims description 4
- 230000001363 autoimmune Effects 0.000 claims description 3
- 230000036436 anti-hiv Effects 0.000 claims description 2
- 201000010099 disease Diseases 0.000 claims 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 26
- 150000001875 compounds Chemical class 0.000 abstract description 3
- 210000004027 cell Anatomy 0.000 description 45
- ZGSPNIOCEDOHGS-UHFFFAOYSA-L disodium [3-[2,3-di(octadeca-9,12-dienoyloxy)propoxy-oxidophosphoryl]oxy-2-hydroxypropyl] 2,3-di(octadeca-9,12-dienoyloxy)propyl phosphate Chemical compound [Na+].[Na+].CCCCCC=CCC=CCCCCCCCC(=O)OCC(OC(=O)CCCCCCCC=CCC=CCCCCC)COP([O-])(=O)OCC(O)COP([O-])(=O)OCC(OC(=O)CCCCCCCC=CCC=CCCCCC)COC(=O)CCCCCCCC=CCC=CCCCCC ZGSPNIOCEDOHGS-UHFFFAOYSA-L 0.000 description 36
- 208000030507 AIDS Diseases 0.000 description 28
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 27
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 26
- 238000003556 assay Methods 0.000 description 26
- 150000003904 phospholipids Chemical class 0.000 description 24
- 230000009257 reactivity Effects 0.000 description 24
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 21
- 241000700605 Viruses Species 0.000 description 19
- FHQVHHIBKUMWTI-OTMQOFQLSA-N {1-hexadecanoyl-2-[(Z)-octadec-9-enoyl]-sn-glycero-3-phospho}ethanolamine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(=O)OCCN)OC(=O)CCCCCCC\C=C/CCCCCCCC FHQVHHIBKUMWTI-OTMQOFQLSA-N 0.000 description 19
- 239000002671 adjuvant Substances 0.000 description 16
- 210000003719 b-lymphocyte Anatomy 0.000 description 15
- 238000006386 neutralization reaction Methods 0.000 description 15
- 238000002965 ELISA Methods 0.000 description 13
- 238000012360 testing method Methods 0.000 description 13
- 239000000427 antigen Substances 0.000 description 12
- 102000004196 processed proteins & peptides Human genes 0.000 description 12
- 208000023275 Autoimmune disease Diseases 0.000 description 11
- 108020004414 DNA Proteins 0.000 description 11
- 102000002689 Toll-like receptor Human genes 0.000 description 11
- 108020000411 Toll-like receptor Proteins 0.000 description 11
- 210000002966 serum Anatomy 0.000 description 11
- JZNWSCPGTDBMEW-UHFFFAOYSA-N Glycerophosphorylethanolamin Natural products NCCOP(O)(=O)OCC(O)CO JZNWSCPGTDBMEW-UHFFFAOYSA-N 0.000 description 10
- 235000012000 cholesterol Nutrition 0.000 description 10
- PSGAAPLEWMOORI-PEINSRQWSA-N medroxyprogesterone acetate Chemical compound C([C@@]12C)CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2CC[C@]2(C)[C@@](OC(C)=O)(C(C)=O)CC[C@H]21 PSGAAPLEWMOORI-PEINSRQWSA-N 0.000 description 10
- 150000008104 phosphatidylethanolamines Chemical class 0.000 description 10
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 10
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 230000003429 anti-cardiolipin effect Effects 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 108091007433 antigens Proteins 0.000 description 8
- 102000036639 antigens Human genes 0.000 description 8
- 210000002230 centromere Anatomy 0.000 description 8
- 239000003153 chemical reaction reagent Substances 0.000 description 8
- 238000013461 design Methods 0.000 description 8
- MWRBNPKJOOWZPW-CLFAGFIQSA-N dioleoyl phosphatidylethanolamine Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(COP(O)(=O)OCCN)OC(=O)CCCCCCC\C=C/CCCCCCCC MWRBNPKJOOWZPW-CLFAGFIQSA-N 0.000 description 8
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 8
- 239000001963 growth medium Substances 0.000 description 8
- 230000002209 hydrophobic effect Effects 0.000 description 8
- 150000001413 amino acids Chemical class 0.000 description 7
- 230000003053 immunization Effects 0.000 description 7
- 238000002649 immunization Methods 0.000 description 7
- 208000015181 infectious disease Diseases 0.000 description 7
- 239000002953 phosphate buffered saline Substances 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 238000012546 transfer Methods 0.000 description 7
- 108010033040 Histones Proteins 0.000 description 6
- 102000004389 Ribonucleoproteins Human genes 0.000 description 6
- 108010081734 Ribonucleoproteins Proteins 0.000 description 6
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 239000003446 ligand Substances 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 241001430294 unidentified retrovirus Species 0.000 description 6
- 102000053602 DNA Human genes 0.000 description 5
- 208000031886 HIV Infections Diseases 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 5
- 241000219061 Rheum Species 0.000 description 5
- 230000036755 cellular response Effects 0.000 description 5
- 230000000120 cytopathologic effect Effects 0.000 description 5
- 230000001086 cytosolic effect Effects 0.000 description 5
- 238000001514 detection method Methods 0.000 description 5
- 230000005764 inhibitory process Effects 0.000 description 5
- 229910052757 nitrogen Inorganic materials 0.000 description 5
- 241000282412 Homo Species 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- -1 anionic phospholipid Chemical class 0.000 description 4
- 239000013553 cell monolayer Substances 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 230000004927 fusion Effects 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 206010025135 lupus erythematosus Diseases 0.000 description 4
- 229920001184 polypeptide Polymers 0.000 description 4
- 238000000159 protein binding assay Methods 0.000 description 4
- 238000000527 sonication Methods 0.000 description 4
- 230000003612 virological effect Effects 0.000 description 4
- 238000003260 vortexing Methods 0.000 description 4
- 208000003343 Antiphospholipid Syndrome Diseases 0.000 description 3
- 241000700198 Cavia Species 0.000 description 3
- 241000700199 Cavia porcellus Species 0.000 description 3
- 102100037473 Glutathione S-transferase A1 Human genes 0.000 description 3
- 229940033332 HIV-1 vaccine Drugs 0.000 description 3
- 101001026125 Homo sapiens Glutathione S-transferase A1 Proteins 0.000 description 3
- 102100022742 Lupus La protein Human genes 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 108010094028 Prothrombin Proteins 0.000 description 3
- 102100027378 Prothrombin Human genes 0.000 description 3
- 241001112090 Pseudovirus Species 0.000 description 3
- 102000004142 Trypsin Human genes 0.000 description 3
- 108090000631 Trypsin Proteins 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 230000005875 antibody response Effects 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 230000021615 conjugation Effects 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- 239000012091 fetal bovine serum Substances 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 230000036039 immunity Effects 0.000 description 3
- 239000012678 infectious agent Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 230000003278 mimic effect Effects 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 230000001717 pathogenic effect Effects 0.000 description 3
- 229940039716 prothrombin Drugs 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 239000013638 trimer Substances 0.000 description 3
- 239000012588 trypsin Substances 0.000 description 3
- 210000002845 virion Anatomy 0.000 description 3
- WTJKGGKOPKCXLL-VYOBOKEXSA-N 1-hexadecanoyl-2-(9Z-octadecenoyl)-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCC\C=C/CCCCCCCC WTJKGGKOPKCXLL-VYOBOKEXSA-N 0.000 description 2
- BFSVOASYOCHEOV-UHFFFAOYSA-N 2-diethylaminoethanol Chemical compound CCN(CC)CCO BFSVOASYOCHEOV-UHFFFAOYSA-N 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 208000035473 Communicable disease Diseases 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 102000006947 Histones Human genes 0.000 description 2
- 101000972485 Homo sapiens Lupus La protein Proteins 0.000 description 2
- 108010048209 Human Immunodeficiency Virus Proteins Proteins 0.000 description 2
- 208000004554 Leishmaniasis Diseases 0.000 description 2
- 206010024229 Leprosy Diseases 0.000 description 2
- 239000000232 Lipid Bilayer Substances 0.000 description 2
- 210000001744 T-lymphocyte Anatomy 0.000 description 2
- 238000011053 TCID50 method Methods 0.000 description 2
- 108010060818 Toll-Like Receptor 9 Proteins 0.000 description 2
- 102100033117 Toll-like receptor 9 Human genes 0.000 description 2
- 230000001154 acute effect Effects 0.000 description 2
- 239000010441 alabaster Substances 0.000 description 2
- 230000003302 anti-idiotype Effects 0.000 description 2
- 239000007900 aqueous suspension Substances 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- WORJEOGGNQDSOE-UHFFFAOYSA-N chloroform;methanol Chemical compound OC.ClC(Cl)Cl WORJEOGGNQDSOE-UHFFFAOYSA-N 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 210000002919 epithelial cell Anatomy 0.000 description 2
- 238000001125 extrusion Methods 0.000 description 2
- 239000003517 fume Substances 0.000 description 2
- 125000002966 glycerophosphoglycerophosphoglycerol group Chemical group 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 229940030980 inova Drugs 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 238000002794 lymphocyte assay Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 2
- BZQFBWGGLXLEPQ-REOHCLBHSA-N phosphoserine Chemical compound OC(=O)[C@@H](N)COP(O)(O)=O BZQFBWGGLXLEPQ-REOHCLBHSA-N 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 230000007928 solubilization Effects 0.000 description 2
- 238000005063 solubilization Methods 0.000 description 2
- 230000009870 specific binding Effects 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 208000006379 syphilis Diseases 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- PGOHTUIFYSHAQG-LJSDBVFPSA-N (2S)-6-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-4-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-1-[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2R)-2-[[(2S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-amino-4-methylsulfanylbutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]propanoyl]pyrrolidine-2-carbonyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-methylpentanoyl]amino]acetyl]amino]-3-hydroxypropanoyl]amino]-4-methylpentanoyl]amino]-3-sulfanylpropanoyl]amino]-4-methylsulfanylbutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-hydroxybutanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-3-hydroxypropanoyl]amino]-3-hydroxypropanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]amino]-4-methylpentanoyl]amino]-3-hydroxybutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]-5-oxopentanoyl]amino]-3-hydroxybutanoyl]amino]-3-hydroxypropanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]-5-oxopentanoyl]amino]-3-phenylpropanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-oxobutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-4-carboxybutanoyl]amino]-5-oxopentanoyl]amino]hexanoic acid Chemical compound CSCC[C@H](N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](Cc1cnc[nH]1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(O)=O PGOHTUIFYSHAQG-LJSDBVFPSA-N 0.000 description 1
- CITHEXJVPOWHKC-UUWRZZSWSA-N 1,2-di-O-myristoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCCCCCCC CITHEXJVPOWHKC-UUWRZZSWSA-N 0.000 description 1
- FHQVHHIBKUMWTI-ZCXUNETKSA-N 1-palmitoyl-2-oleoyl phosphatidylethanolamine Chemical compound CCCCCCCCCCCCCCCC(=O)OCC(COP(O)(=O)OCCN)OC(=O)CCCCCCC\C=C/CCCCCCCC FHQVHHIBKUMWTI-ZCXUNETKSA-N 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 102100035875 C-C chemokine receptor type 5 Human genes 0.000 description 1
- 101710149870 C-C chemokine receptor type 5 Proteins 0.000 description 1
- 241000282836 Camelus dromedarius Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 241000251730 Chondrichthyes Species 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- 102000003915 DNA Topoisomerases Human genes 0.000 description 1
- 108090000323 DNA Topoisomerases Proteins 0.000 description 1
- GZDFHIJNHHMENY-UHFFFAOYSA-N Dimethyl dicarbonate Chemical compound COC(=O)OC(=O)OC GZDFHIJNHHMENY-UHFFFAOYSA-N 0.000 description 1
- 238000012286 ELISA Assay Methods 0.000 description 1
- 101710091045 Envelope protein Proteins 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 229940033330 HIV vaccine Drugs 0.000 description 1
- 101000669447 Homo sapiens Toll-like receptor 4 Proteins 0.000 description 1
- 101000669402 Homo sapiens Toll-like receptor 7 Proteins 0.000 description 1
- 101001057752 Human cytomegalovirus (strain AD169) Uncharacterized protein IRL4 Proteins 0.000 description 1
- 101001057744 Human cytomegalovirus (strain AD169) Uncharacterized protein IRL9 Proteins 0.000 description 1
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 1
- 108700005091 Immunoglobulin Genes Proteins 0.000 description 1
- 102100034349 Integrase Human genes 0.000 description 1
- 102100034353 Integrase Human genes 0.000 description 1
- 229920000057 Mannan Polymers 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 201000002481 Myositis Diseases 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 108010076504 Protein Sorting Signals Proteins 0.000 description 1
- 101710188315 Protein X Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 241001068263 Replication competent viruses Species 0.000 description 1
- 241000220317 Rosa Species 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 201000009594 Systemic Scleroderma Diseases 0.000 description 1
- 206010042953 Systemic sclerosis Diseases 0.000 description 1
- 108010000499 Thromboplastin Proteins 0.000 description 1
- 102000002262 Thromboplastin Human genes 0.000 description 1
- 102100039360 Toll-like receptor 4 Human genes 0.000 description 1
- 102100039390 Toll-like receptor 7 Human genes 0.000 description 1
- 241000700618 Vaccinia virus Species 0.000 description 1
- 230000010530 Virus Neutralization Effects 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 229940037003 alum Drugs 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 230000010100 anticoagulation Effects 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000003114 blood coagulation factor Substances 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 210000004970 cd4 cell Anatomy 0.000 description 1
- 230000034303 cell budding Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 230000006037 cell lysis Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 239000000645 desinfectant Substances 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- BPHQZTVXXXJVHI-UHFFFAOYSA-N dimyristoyl phosphatidylglycerol Chemical compound CCCCCCCCCCCCCC(=O)OCC(COP(O)(=O)OCC(O)CO)OC(=O)CCCCCCCCCCCCC BPHQZTVXXXJVHI-UHFFFAOYSA-N 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000012202 endocytosis Effects 0.000 description 1
- 108010078428 env Gene Products Proteins 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 239000013029 homogenous suspension Substances 0.000 description 1
- 230000005745 host immune response Effects 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 210000004408 hybridoma Anatomy 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- CBVCZFGXHXORBI-PXQQMZJSSA-N indinavir Chemical compound C([C@H](N(CC1)C[C@@H](O)C[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H]2C3=CC=CC=C3C[C@H]2O)C(=O)NC(C)(C)C)N1CC1=CC=CN=C1 CBVCZFGXHXORBI-PXQQMZJSSA-N 0.000 description 1
- 229960001936 indinavir Drugs 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000002054 inoculum Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 238000000464 low-speed centrifugation Methods 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 210000001806 memory b lymphocyte Anatomy 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 229940035032 monophosphoryl lipid a Drugs 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 230000014508 negative regulation of coagulation Effects 0.000 description 1
- 238000004848 nephelometry Methods 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- 239000007764 o/w emulsion Substances 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 238000002823 phage display Methods 0.000 description 1
- 150000003907 phosphatidylinositol monophosphates Chemical class 0.000 description 1
- 150000003905 phosphatidylinositols Chemical class 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 230000002064 post-exposure prophylaxis Effects 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 230000037452 priming Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000003331 prothrombotic effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 238000010079 rubber tapping Methods 0.000 description 1
- 238000013515 script Methods 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- JZNWSCPGTDBMEW-YFKPBYRVSA-N sn-glycero-3-phosphoethanolamine Chemical compound NCCO[P@@](O)(=O)OC[C@@H](O)CO JZNWSCPGTDBMEW-YFKPBYRVSA-N 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- QLNOOKSBAYIHQI-SKZICHJRSA-M sodium;2,3-dihydroxypropyl [(2r)-2,3-di(tetradecanoyloxy)propyl] phosphate Chemical compound [Na+].CCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC(O)CO)OC(=O)CCCCCCCCCCCCC QLNOOKSBAYIHQI-SKZICHJRSA-M 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 230000017960 syncytium formation Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 230000002885 thrombogenetic effect Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 229940044616 toll-like receptor 7 agonist Drugs 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 238000005829 trimerization reaction Methods 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- 238000002255 vaccination Methods 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 239000002821 viper venom Substances 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/21—Retroviridae, e.g. equine infectious anemia virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/385—Haptens or antigens, bound to carriers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6905—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion
- A61K47/6911—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion the form being a liposome
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
- C07K16/1036—Retroviridae, e.g. leukemia viruses
- C07K16/1045—Lentiviridae, e.g. HIV, FIV, SIV
- C07K16/1063—Lentiviridae, e.g. HIV, FIV, SIV env, e.g. gp41, gp110/120, gp160, V3, PND, CD4 binding site
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55555—Liposomes; Vesicles, e.g. nanoparticles; Spheres, e.g. nanospheres; Polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55561—CpG containing adjuvants; Oligonucleotide containing adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55566—Emulsions, e.g. Freund's adjuvant, MF59
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55572—Lipopolysaccharides; Lipid A; Monophosphoryl lipid A
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/575—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 humoral response
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6018—Lipids, e.g. in lipopeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
- A61K2039/625—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier binding through the biotin-streptavidin system or similar
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
- A61K2039/627—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier characterised by the linker
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/64—Medicinal preparations containing antigens or antibodies characterised by the architecture of the carrier-antigen complex, e.g. repetition of carrier-antigen units
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/15011—Lentivirus, not HIV, e.g. FIV, SIV
- C12N2740/15022—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16111—Human Immunodeficiency Virus, HIV concerning HIV env
- C12N2740/16122—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16111—Human Immunodeficiency Virus, HIV concerning HIV env
- C12N2740/16134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
Abstract
Description
技術分野
本発明は、一般的に、ヒト免疫不全ウイルス(HIV)に、そして特に、HIVに対する中和抗体を誘導する方法に、そしてこうした方法で使用するのに適した化合物および組成物に関する。
自己抗原またはその断片を、例えば、プライム・ブースト措置において用いてもよく、こうした措置は、当業者によって容易に最適化可能である(こうした措置のタンパク質性構成要素をコードするDNA配列を、タンパク質性構成要素がin vivoで産生される条件下で投与してもよい)。例えば、交差反応性自己抗原を、第一のワクチン・プライムとして用いて、天然自己抗体(例えば抗カルジオリピン4E10および2F5様抗体)をブーストしてもよい。自己抗原(例えばカルジオリピン(またはその断片))、または交差反応性エピトープ(単数または複数)、例えば2F5および/または4E10エピトープ(このエピトープには、それぞれ、少なくとも配列ELDKWAおよびNWFDITが含まれてもよい)を含むHIVエンベロープタンパク質/ポリペプチド/ペプチドは、いずれも、ブーストとして使用可能である。(PCT/US04/30397に開示される配列を参照されたい。)(HIVエンベロープは自己抗原でないことが理解されるであろう。)
自己抗原および/またはHIVタンパク質/ポリペプチド/ペプチド、またはコード配列の投与様式は、免疫原、患者および求める効果によって多様であり、投与用量も同様である。最適投薬措置は、当業者によって容易に決定可能である。典型的には、投与は皮下、筋内、静脈内、鼻内または経口である。
上述のリポソームを、β2糖タンパク質1の組換えドメインVと混合して、このドメインに対する抗体を誘発してもよい。
本発明のペプチド−リポソーム免疫原を、頑強な抗体応答を促進する脂質A、oCpG、TRL4アゴニストまたはTLR7アゴニストなどのアジュバントとともに配合してもよいし、そして/または投与してもよい(Raoら, Immunobiol. Cell Biol. 82(5):523(2004))。使用可能な他のアジュバントにはミョウバンおよびQ521(存在するB細胞寛容を中断しないもの)が含まれる。好ましい配合物は、B細胞寛容の型を中断するように設計されたアジュバント、例えばEmulsigen(水中油エマルジョン)などの油エマルジョン中のoCpGを含む(Tranら, Clin. Immunol. 109(3):278−287(2003))。さらなる適切なアジュバントには、2005年12月14日出願の11/302,505に記載されるものが含まれ、該出願に開示されるTRLアゴニストが含まれる。
広範反応性中和抗体を誘導可能なHIV−1免疫原の設計は、HIV−1ワクチン開発の大きな目的である。HIV−1を広範に中和する稀なヒトmabが存在する一方、HIV−1エンベロープ免疫原は、これらの抗体特異性を誘導しない。この研究において、2つの最も広範に反応性であるHIV−1エンベロープgp41ヒトmab、2F5および4E10は、カルジオリピンと反応性である多重特異性自己抗体であることが立証された。したがって、gp41膜近位エピトープが自己抗原を模倣しているため、現在のHIV−1ワクチンは、膜近位gp41エピトープに対する抗体を誘導しない可能性もある。
モノクローナル抗体。Mab 2F5、2G12、および4E10を、記載されるように産生した(Steiglerら, AID Res. Human Retroviruses 17:1757(2001)、Purtscherら, AIDS 10:587(1996)、Trkolaら, J. Virol. 70:1100(1996))。IgG1b12(Burtonら, Science 266:1024−1027(1994))は、Dennis Burton、Scripps Institute、カリフォルニア州ラホヤの寛大な贈り物であった。Mab 447−52D(Zolla−Paznerら, AIDS Res. Human Retrovirol. 20:1254(2004))を、AIDS試薬貯蔵所、NIAID、NIHから得た。表1中のmabの残りは、HIV−1感染被験体から産生され、そしてこれらを、記載されるように用いた(Robinsonら, AIDS Res. Human Retrovirol. 6:567(1990)、Binleyら, J. Virol. 78:13232(2004))。
mab 2F5および4E10、2つのさらなる稀な広範反応性中和mab(2G12およびIgG1b12)、および31の一般的な抗HIV−1 Envヒトmabsと、カルジオリピン(Robinsonら, AIDS Res. Human Retrovirol. 6:567(1990))との反応性を決定した(表1)。2F5および4E10はどちらもカルジオリピンと反応したが、33の他のmabはすべて陰性であった。Mab 2F5はまた、SS−A/Ro、ヒストンおよびセントロメアB自己抗原とも反応し、一方、mab 4E10は、全身性エリテマトーデス(SLE)自己抗原、SS−A/Roと反応した。2F5および4E10はどちらも、散在性の細胞質および核パターンで、Hep−2ヒト上皮細胞と反応した(Robinsonら, AIDS Res. Human Retrovirol. 6:567(1990))(図2)。したがって、2F5および4E10はどちらも、多重特異性自己反応性によって特徴付けられる。
自己抗原として、カルジオリピン(層状および六方晶相)、1−パルミトイル−2−オレオイル−sn−グリセロ−3−[ホスホ−L−セリン](POPS)(層状および六方晶相)、1−パルミトイル−2−オレオイル−ホスファチジルエタノールアミン(POPE)(層状相)、およびジオレオイルホスファチジルエタノールアミン(DOPE)(六方晶相)を用いて、本発明の自己抗原が、中和抗体の産生を誘導する能力を研究した。モルモット(群あたり4匹)を、10;gのoCpG中のリン脂質(カルジオリピン層状相、カルジオリピン六方晶相、POPS層状相、POPS六方晶相、POPE層状相またはDOPE六方晶相)で、各免疫を2週間ずつ離して、4回免疫した。4回のリン脂質免疫後、10:gのoCpGと100:gのM群コンセンサスEnv、CON−S gp140CFIオリゴマー(すなわち図4Aに示すタンパク質のCFI型)を用いて、IPで最終免疫を行った。
細胞培養
TZM−blは、接着細胞株であり、そしてこれをT−75培養フラスコ中で維持する。完全増殖培地(GM)は、10%ウシ胎児血清(FBS、熱不活化)およびゲンタマイシン(50μg/ml)を補ったD−MEMからなる。トリプシン/EDTAでの処理によって、細胞単層を破壊し、そして除去する:
TZM−bl細胞単層を破壊するためのトリプシン−EDTA処理:集密(confluency)状態で、ルーチン維持のために細胞を分割する際、そしてアッセイ用に細胞を調製する際、トリプシン/EDTAでの処理によって、T−75培養フラスコ中に維持した細胞単層を破壊しそして除去する。
2. 細胞単層を覆うように、2.5mlの0.25%トリプシン−EDTA溶液をゆっくりと添加する。室温で30〜45秒間インキュベーションする。トリプシン溶液をデカントし、そして37℃で4分間インキュベーションする。細胞が剥離するのを待つ間、フラスコを叩いたりまた振盪したりすることによって細胞を攪拌してはならない。
4. 15mlのGM中、新しいT−75培養フラスコにおよそ106細胞を植え付ける。培養を、5%CO2/95%空気環境において、37℃でインキュベーションする。細胞はおよそ3日ごとに分割しなければならない。
クローニングされていないウイルスのストックを、PBMCまたはT細胞株いずれかで産生してもよい。293T細胞などの適切な細胞種にトランスフェクションすることによって、偽ウイルスを産生してもよい。すべてのウイルスストックは、低速遠心分離およびろ過(0.45ミクロン)によって細胞不含にして、そして20%FBSを含有するGM中、−80℃で保存すべきである。
中和アッセイを行う前に、TZM−bl細胞中、単細胞感染アッセイ(2日インキュベーション)において、各ウイルスストックのTCID50を測定する必要がある。TCID50アッセイにおいて、陽性感染を定量化する際には、2.5倍バックグラウンドRLUのカットオフ値を用いる。
注1:別に明記しない限り、加湿37℃、5%CO2インキュベーター中ですべてのインキュベーションを行った。
1. 96ウェル平底培養プレートの形式を用いて、第1列のすべてのウェルにGM 150μlを入れる(細胞対照)。第2〜11列のすべてのウェルに100μlを入れる(第2列はウイルス対照になるであろう)。第3〜12列、第H行のすべてのウェルにさらに40μlを入れる(試験試料を受け取るため)。
4. 第2〜12列、第A〜H行のすべてのウェルに、細胞不含ウイルス50μl(200 TCID50)を分注する。各トランスファー後にピペット操作によって混合する。各トランスファー間で、40ml滅菌PBSを含有する試薬貯蔵所中でピペットチップをリンスして、キャリー・オーバーを回避する。
6. DEAEデキストラン(37.5μg/ml)を含有するGM中、1x105細胞/mlの密度で、TZM−bl細胞の懸濁物を調製する(使用およそ10〜15分前にトリプシン処理する)。100μlの細胞懸濁物(ウェルあたり10,000細胞)を第1〜12列、第A〜H行中の各ウェルに分注する。各トランスファー間で、滅菌PBSが充填された試薬貯蔵所中でピペットチップをリンスして、キャリー・オーバーを回避する。DEAEデキストランの最終濃度は15μg/mlである。
8. 各ウェルから培地150μlを除去し、およそ100μlを残す。100μlのBright GloTM試薬を各ウェルに分注する。室温で2分間インキュベーションして、完全な細胞溶解を可能にする。ピペット操作(少なくとも2回の動作)によって混合し、そして対応する96ウェル黒プレートに150μlをトランスファーする。ルミノメーター中でプレートを直ちに読み取る。
実施例3
免疫原設計
疎水性リンカー(GTH1)に連結されたmAb 2F5および4E10の名目上のエピトープそれぞれを含むペプチド配列を合成し、そして合成リポソーム内に包埋した(図6)。脂質二重層の遠位端に2F5および4E10エピトープ配列を持つ第一世代の免疫原を設計した(図6A)。これらの構築物は、それぞれのエピトープに対するmAbの拘束されないアクセスを提供した。2F5および4E10 mAbエピトープ配列が疎水性リンカーの近位に連結された、MPER領域の天然配向を模倣する、第二世代構築物が設計されている(図6A、6B)。
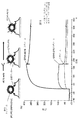
免疫戦略は、寛容の一時的な中断を可能にする措置を取り込んだ。プロトコルは、マウスにおける抗dsDNA抗体の産生のため、寛容を中断するために用いられてきているTLR9リガンドであるoCpGの使用を伴う(Tranら, Clin. Immunol. 109(3):278−287(2003))。ペプチド−リポソーム・コンジュゲートを、EmulsigenにoCpGを加えたアジュバントと混合した(1:1)。375μLのEmulsigen、250μLのoCpGおよび625μLの生理食塩水を混合することによって、Emulsigen混合アジュバント(2x)を調製した。各モルモットを、21日間隔で、250μgのペプチドのみまたは等量のペプチドを含むペプチド−リポソーム・コンジュゲートのいずれかで免疫した。初回免疫、そして続く免疫各々の前に、血清試料を前採血として採取した。ペプチドエピトープに対する結合に関してELISAアッセイ(図12)によって、そしてウイルス中和アッセイ(表2)のため、血清試料を分析した。図12中のデータは、GTH1−4E10リポソームで免疫した2匹のモルモット由来の血清の4E10ペプチドに対する強い反応性を示し、一方、4E10ペプチド免疫動物由来の血清においては、低レベルの反応性しか観察されなかった。陽性血清はまた、どちらも、HIV−1 MN株も中和した(表2)。
上述のペプチド−リポソーム・コンジュゲートは、MPER特異的B細胞応答の検出用の試薬として利用されてきている。脂質組成物中にフルオレセイン−POPEを取り込むことによって、ペプチド−リポソーム構築物(2F5および4E10)をフルオレセインとコンジュゲート化した。フルオレセイン−POPEを45:55の比で非コンジュゲート化POPEと混合し、そして次いで、上述のようなモル比で、残りの脂質と混合した。BIAcore結合アッセイにおいて、フルオレセインとコンジュゲート化された2F5および4E10−ペプチド−リポソームはどちらも、それぞれのmAbに対する結合特異性を保持した(図11)。
ペプチド−脂質コンジュゲートの生成。クロロホルム中に溶解されたリン脂質、POPC(1−パルミトイル−2−オレオイル−sn−グリセロ−3−ホスファチジルコリン)、POPE(1−パルミトイル−2−オレオイル−sn−グリセロ−3−ホスホエタノールアミン)、DOPE(1,2−ジオレオイル−sn−グリセロ−3−ホスファチジル・エタノールアミン);DMPA(1,2−ジミリストイル−sn−グリセロ−3−ホスフェート)、およびコレステロールをAvanti Polar Lipids(アラバマ州アラバスター)より購入した。クロロホルム耐性試験管中で、適切なモル量のリン脂質を分注することによって、リン脂質リポソームを調製した。モル比45:25:20:10(POPC:POPE:DMPA:コレステロール)で、脂質のクロロホルム溶液をペプチド溶液に添加した。HIV−1膜近位ペプチドを70%クロロホルム、30%メタノール中に溶解した。各ペプチドを1:420のペプチド:総リン脂質のモル比まで添加した。穏やかにボルテックスすることによってリン脂質を混合し、そして穏やかな窒素流のもとに、ドラフト中で混合物を乾燥させた。高圧下で脂質を保存する(15時間)ことによって、クロロホルムのいかなる残渣も除去した。PBSまたはTBS緩衝液、pH7.4を添加し、そしてTmより高い温度で10〜30分間維持しつつ、断続的に勢いよくボルテックスしてリン脂質を再懸濁することによって、リン脂質の水性懸濁物を調製し、その後、超音波処理装置槽(Misonix Sonicator 3000、Misonix Inc.、ニューヨーク州ファーミングデール)で超音波処理した。超音波処理装置は、周期あたり総超音波処理45秒間の3連続周期を実行するようにプログラミングされた。各周期には、5秒間の超音波パルス(70ワット出力)、その後の12秒間のパルスオフ期が含まれた。超音波終了時、層状リポソームの懸濁物を4℃で保存し、そしてBIAcoreセンサーチップ上で捕捉する前に、上述のように再び超音波処理した。
i)POPC:POPE:DMPA:コレステロール
ii)POPC:POPS
iii)POPC:POPS:リゾPC
iv)POPC:POPE:スフィンゴミエリン:コレステロール
を含む多様な組成の合成リポソーム内に取り込まれるであろう。
実施例5
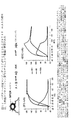
ストレプトアビジンをコーティングしたBIAcoreセンサーチップ(SA)上にビオチン化2F5名目上エピトープペプチド(SP62)を係留し、そして2F5 mabまたは2F5 Fabのいずれかをペプチド表面上に注入した。HR−1ペプチド対照表面上の非特異的シグナルを減じた後、2F5 mAb(46.6〜1800nM)または2F5 Fab(120〜2000nM)の特異的結合を得た。BIAevaluationソフトフェアを用いて、単純ラングミュア等式に対する全体的曲線適合後、Kdを計算した。図13に示すデータは、ペプチドエピトープに対するMPER mAb結合が、単純なモデル(ラングミュア等式)に適合することを示す。
抗リン脂質症候群の患者由来のヒト・モノクローナル抗体(CL1、IS4およびIS6と称される)が研究されてきている(表4を参照されたい)(Gilesら, J. Immunol. 177:1729−1736(2006)、Zhuら, Brit. Jour. Haematol. 105:102−109(1999)、Chukwuochaら, Mol. Immunol. 39:299−311(2002)、Zhuら, Brit. Jour. Haematol. 135:214−219(2006)、Pierangeliら, Thromb. Haemost. 84:388−395(2000)、Linら, Arth Rheum 56:1638(2007)、Alamら, J. Immunol. 178:4424−4435(2007)、Zhaoら, Arth. Rheum. 42:2132−2138(1999)、Luら, Arth. Rheum. 52:4018−4027(2005))。IS4およびIS6は病原性抗脂質抗体であり、一方、CL1は非病原性抗脂質自己抗体である(表4)。これらの抗体はいずれも、ビリオン−細胞融合によって初期感染を反映する偽ウイルス阻害アッセイにおいて、HIV偽ウイルスを中和しなかった(Liら, J. Virol. 79:10108−25(2005))(表5)が、これらの抗体3つすべては、HIVのエンドサイトーシスに依存し、そしてin vivoのCD4細胞のHIV感染性を反映するPBMC HIV中和アッセイにおいて、HIV−1を中和した(表6)。CL1がHIVを中和することは:a)ヒトはHIVを中和する非病原性抗脂質抗体を作製可能であり、そしてb)CL1は、HIV感染被験体の治療のために、あるいはHIVまたはHIV感染物質への針、性的または他の曝露後、被験体の曝露後予防の状況において、療法Mabとして安全に使用可能な抗体であるという事実を証明する。
図18に示すToll様受容体リガンドをgp41 MPERペプチド免疫原を含むリポソーム型に配合した。
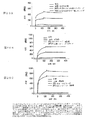
ペプチド−リポソーム構築物中のエピトープに対する2F5 mAbの結合に関するBiacoreアッセイによって、TLRアジュバントの取り込みまたはコンジュゲート化が、HIV中和抗体2F5の結合に影響を及ぼさないことを明らかにした。mAb 2F5および4E10両方の強い結合が観察された(図20を参照されたい)。
膜貫通ドメインに先行するHIV−1 gp41膜近位外部領域が、広範中和性抗体2F5および4E10のターゲットである。MPERペプチドが、膜界面、ならびに抗体2F5および4E10の脂質反応性に分割されるという事実が、広範中和性gp41 MPER抗体の誘導のための候補免疫原として、MPERペプチド−リポソーム・コンジュゲートの設計につながった。ここで用いたペプチド−リポソーム・コンジュゲート化戦略は、2F5および4E10 mAb両方のエピトープを含有し、そしてHIV−1 gp41の膜貫通ドメイン(gp160の残基656〜707)を取り込んでいるMPERに対応する合成ペプチド、MPER656−TMD(図21)の設計を伴った。
Claims (12)
- 患者において、抗HIV抗体の産生を誘導する方法であって、こうした方法が必要な患者に、前記誘導を達成するのに十分な量で、少なくとも1つのリポソーム−ペプチド・コンジュゲートの量を投与する工程を含み、前記ペプチドが膜外部近位領域(MPER)エピトープを含み、そして前記リポソームがリゾホスホリルコリンまたはホスファチジルセリンを含む、前記方法。
- 前記ペプチドが、配列ELDKWASまたはWFNITNWを含む、請求項1記載の方法。
- 前記リポソーム−ペプチド・コンジュゲートがさらに脂質Aを含む、請求項1記載の方法。
- 前記リポソーム−ペプチド・コンジュゲートをβ2糖タンパク質1の組換えドメインVと混合する、請求項1記載の方法。
- リポソーム中に包埋されたMPERエピトープを含む免疫原であって、前記リポソームがリゾホスホリルコリンまたはホスファチジルセリンを含む、前記免疫原。
- 前記免疫原がさらに脂質Aを含む、請求項5記載の免疫原。
- 前記免疫原がさらに、β2糖タンパク質1の組換えドメインVを含む、請求項5記載の免疫原。
- HIVを治療する方法であって、こうした方法が必要な患者に、HIV表面上またはHIV感染細胞表面上の脂質に結合し、そしてそれによってHIV−1を中和する、正常被験体からまたは自己免疫疾患被験体から誘導可能な抗体を投与する工程を含み、前記抗体がCL1、またはその結合特異性を有する抗体、またはその結合性断片であり、そして前記治療を達成するのに十分な量で投与される、前記方法。
- HIV−1 gp41およびMPERペプチドの膜貫通ドメインを含む免疫原性コンジュゲートであって、前記MPERペプチドが前記膜貫通ドメインを介してリポソーム中に係留される、前記コンジュゲート。
- 前記リポソームが合成脂質を含む、請求項9記載の免疫原性コンジュゲート。
- 前記MPERペプチドが2F5または4E10モノクローナル抗体のエピトープを含む、請求項9記載の免疫原性コンジュゲート。
- 患者において免疫応答を誘導する方法であって、前記患者に、前記誘導を達成するのに十分な量の請求項9記載の前記免疫原性コンジュゲートを投与する工程を含む、前記方法。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/785,077 US9402893B2 (en) | 2005-04-12 | 2007-04-13 | Liposome-peptide conjugate and method of using same to induce production of anti-HIV antibodies |
| US11/812,992 US20080057075A1 (en) | 2005-04-12 | 2007-06-22 | Method of inducing neutralizing antibodies to human immunodeficiency virus |
| US96041307P | 2007-09-28 | 2007-09-28 | |
| PCT/US2008/004709 WO2008127651A1 (en) | 2007-04-13 | 2008-04-11 | Method of inducing neutralizing antibodies to human immunodeficiency virus |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010523676A true JP2010523676A (ja) | 2010-07-15 |
| JP2010523676A5 JP2010523676A5 (ja) | 2010-11-18 |
Family
ID=39864256
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010503070A Pending JP2010523676A (ja) | 2007-04-13 | 2008-04-11 | ヒト免疫不全ウイルスに対する中和抗体を誘導する方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US8956627B2 (ja) |
| EP (1) | EP2139516A4 (ja) |
| JP (1) | JP2010523676A (ja) |
| AU (1) | AU2008239628B2 (ja) |
| CA (1) | CA2683752A1 (ja) |
| WO (1) | WO2008127651A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2006235507B2 (en) | 2005-04-12 | 2012-08-30 | Duke University | Method of inducing neutralizing antibodies to human immunodeficiency virus |
| EP2139516A4 (en) | 2007-04-13 | 2011-06-29 | Univ Duke | METHOD FOR INDUCING NEUTRALIZING ANTIBODIES AGAINST THE HUMAN IMMUNODEFICIENCY VIRUS |
| US20120070488A1 (en) * | 2007-09-28 | 2012-03-22 | Duke University | Method of inducing neutralizing antibodies to human immunodeficiency virus |
| WO2010027502A2 (en) * | 2008-09-05 | 2010-03-11 | Duke University | Method of inducing an anti-viral immune response |
| JP2013505201A (ja) * | 2009-04-03 | 2013-02-14 | デューク ユニバーシティー | 広域反応性中和抗hiv抗体を誘導するための配合物 |
| WO2011046623A2 (en) * | 2009-10-16 | 2011-04-21 | Duke University | Hiv-1 antibodies |
| JP2013520498A (ja) * | 2010-02-25 | 2013-06-06 | デューク ユニバーシティー | 防御的抗hiv−1抗体の産生を誘導する方法 |
| WO2013134293A1 (en) * | 2012-03-05 | 2013-09-12 | Duke University | Vaccine formulation |
| WO2015048635A1 (en) | 2013-09-27 | 2015-04-02 | Duke University | Mper-liposome conjugates and uses thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996033219A1 (en) * | 1995-04-19 | 1996-10-24 | Polymun Scientific Immunbiologische Forschung Gmbh | Monoclonal antibodies against hiv-1 and vaccines made thereof |
| JPH09501169A (ja) * | 1993-08-06 | 1997-02-04 | オパーバス ホールディング ビー ヴィ | 小胞に生体高分子物質を高度に充填する方法 |
| WO2006110831A2 (en) * | 2005-04-12 | 2006-10-19 | Duke University | Method of inducing neutralizing antibodies to human immunodeficiency virus |
Family Cites Families (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5916588A (en) * | 1984-04-12 | 1999-06-29 | The Liposome Company, Inc. | Peptide-containing liposomes, immunogenic liposomes and methods of preparation and use |
| US5831034A (en) | 1987-11-13 | 1998-11-03 | Hermann Katinger | Human monoclonal anti-HIV-I-antibodies |
| US4994440A (en) | 1989-02-13 | 1991-02-19 | Creaven Patrick J | Method for the treatment of renal cell carcinoma |
| DE69311764T2 (de) | 1992-05-14 | 1998-02-05 | Polymun Scient Immunbio Forsch | Peptide, die Antikörper induzieren, die genetisch divergierende HIV-1 Isolationen neutralisieren |
| CA2157900A1 (en) | 1993-03-11 | 1994-09-15 | Angeline Douvas | Therapeutic strategies for immunoinfective cluster virus infections |
| ATE246513T1 (de) | 1993-05-27 | 2003-08-15 | Entremed Inc | Zubereitungen und verfahren für die behandlung von krebs und hyperproliferierenden krankheiten |
| BR9407531A (pt) | 1993-09-11 | 1997-08-26 | Polymun Scient Immunbio Forsch | Peptideos que provocam a formação de anticorpos neutralizadores contra cepas de HIV-1 geneticamente divergentes |
| CA2185129A1 (en) | 1994-03-14 | 1995-09-21 | Angeline Douvas | Methods to diagnose and treat hiv-1 infection |
| US6156337A (en) * | 1994-07-08 | 2000-12-05 | Opperbas Holding B.V. | Method for high loading of vesicles with biopolymeric substances |
| US6207646B1 (en) | 1994-07-15 | 2001-03-27 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules |
| WO1996040243A1 (en) * | 1995-06-07 | 1996-12-19 | U.S. Department Of The Army | Liposomes containing human immunodeficiency virus glycoprotein and methods for use thereof |
| US5910306A (en) | 1996-11-14 | 1999-06-08 | The United States Of America As Represented By The Secretary Of The Army | Transdermal delivery system for antigen |
| US5901306A (en) * | 1997-06-23 | 1999-05-04 | Sun Microsystems, Inc. | Method and apparatus for reducing a computational result to the range boundaries of a signed 8-bit integer in case of overflow |
| US6761888B1 (en) | 2000-05-26 | 2004-07-13 | Neuralab Limited | Passive immunization treatment of Alzheimer's disease |
| US6300308B1 (en) | 1997-12-31 | 2001-10-09 | Board Of Regents, The University Of Texas System | Methods and compositions for inducing autoimmunity in the treatment of cancers |
| AU2002340880B2 (en) | 2001-09-07 | 2007-08-23 | Polymun Scientific Immunbiologische Forschung Gmbh | Peptides mimicking a cryptic epitope of GP41 HIV-1 and antibodies directed against them |
| US7195768B2 (en) | 2001-11-07 | 2007-03-27 | Duke University | Polyvalent immunogen |
| ATE444310T1 (de) | 2002-01-17 | 2009-10-15 | Polymun Scient Immunbio Forsch | Antiidiotypische antikörper die hiv-1 neutralisierende antikörper induzieren |
| US7790159B2 (en) | 2002-07-15 | 2010-09-07 | Board Of Regents, The University Of Texas System | Methods, combinations and kits for treating viral infections using immunoconjugates and antibodies to aminophospholipids |
| US20040131622A1 (en) | 2002-07-15 | 2004-07-08 | Board Of Regents | Combinations and kits for treating viral infections using immunoconjugates to aminophospholipids |
| US7678386B2 (en) | 2002-07-15 | 2010-03-16 | Board Of Regents The University Of Texas | Liposomes coated with selected antibodies that bind to aminophospholipids |
| CN104001181B (zh) | 2002-07-15 | 2017-05-10 | 得克萨斯大学体系董事会 | 与阴离子磷脂和氨基磷脂结合的选定抗体及其治疗和诊断用途 |
| US7611704B2 (en) | 2002-07-15 | 2009-11-03 | Board Of Regents, The University Of Texas System | Compositions and methods for treating viral infections using antibodies and immunoconjugates to aminophospholipids |
| US7455833B2 (en) | 2002-07-15 | 2008-11-25 | Board Of Regents, The University Of Texas System | Methods and compositions for treating viral infections using antibodies and immunoconjugates to aminophospholipids |
| US7906115B2 (en) | 2002-07-15 | 2011-03-15 | Thorpe Philip E | Combinations kits and methods for treating viral infections using antibodies and immunoconjugates to aminophospholipids |
| US7384909B2 (en) | 2002-07-15 | 2008-06-10 | Board Of Regents, The University Of Texas System | Anti-viral treatment methods using phosphatidylethanolamine-binding peptides linked to anti-viral agents |
| JP2007524603A (ja) | 2003-03-27 | 2007-08-30 | ザ ユニバーシティー オブ テキサス | Hiv/エイズの受動免疫治療用ループス抗体 |
| WO2005111079A2 (en) | 2004-05-14 | 2005-11-24 | The United States Of America As Represented By The Secretary Department Of Health And Human Services | Hiv vaccine immunogens and immunization strategies to elicit broadly-neutralizing anti-hiv-1 antibodies against the membrane proximal domain of hiv gp41 |
| US20080057075A1 (en) | 2005-04-12 | 2008-03-06 | Haynes Barton F | Method of inducing neutralizing antibodies to human immunodeficiency virus |
| EP2139516A4 (en) | 2007-04-13 | 2011-06-29 | Univ Duke | METHOD FOR INDUCING NEUTRALIZING ANTIBODIES AGAINST THE HUMAN IMMUNODEFICIENCY VIRUS |
| WO2008142133A1 (en) | 2007-05-24 | 2008-11-27 | Glaxosmithkline Biologicals S.A | Lyophilised antigen composition |
| US20120070488A1 (en) | 2007-09-28 | 2012-03-22 | Duke University | Method of inducing neutralizing antibodies to human immunodeficiency virus |
| WO2009111304A2 (en) | 2008-02-29 | 2009-09-11 | President And Fellows Of Harvard College | A fusion-intermediate state of hiv-1 gp41 targeted by broadly neutralizing antibodies |
| SI2340038T1 (en) | 2008-10-10 | 2018-05-31 | Children's Medical Center Corporation | A biochemically stabilized HIV-1 ENV TRIMER vaccine |
| JP2013505201A (ja) | 2009-04-03 | 2013-02-14 | デューク ユニバーシティー | 広域反応性中和抗hiv抗体を誘導するための配合物 |
| US20120177721A1 (en) | 2009-04-03 | 2012-07-12 | Alam S Munir | Formulation |
-
2008
- 2008-04-11 EP EP08742782A patent/EP2139516A4/en not_active Withdrawn
- 2008-04-11 AU AU2008239628A patent/AU2008239628B2/en not_active Ceased
- 2008-04-11 JP JP2010503070A patent/JP2010523676A/ja active Pending
- 2008-04-11 CA CA002683752A patent/CA2683752A1/en not_active Abandoned
- 2008-04-11 US US12/450,779 patent/US8956627B2/en not_active Expired - Fee Related
- 2008-04-11 WO PCT/US2008/004709 patent/WO2008127651A1/en active Application Filing
-
2015
- 2015-02-03 US US14/612,665 patent/US20150147387A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09501169A (ja) * | 1993-08-06 | 1997-02-04 | オパーバス ホールディング ビー ヴィ | 小胞に生体高分子物質を高度に充填する方法 |
| WO1996033219A1 (en) * | 1995-04-19 | 1996-10-24 | Polymun Scientific Immunbiologische Forschung Gmbh | Monoclonal antibodies against hiv-1 and vaccines made thereof |
| WO2006110831A2 (en) * | 2005-04-12 | 2006-10-19 | Duke University | Method of inducing neutralizing antibodies to human immunodeficiency virus |
Non-Patent Citations (3)
| Title |
|---|
| JPN6012057486; British Journal of Haematology Vol.105, No.1, 1999, p.102-109 * |
| JPN6012057487; Journal of Virology Vol.79, No.2, 2005, p.1252-1261 * |
| JPN6012057488; Methods in Enzymology Vol.373, 2003, p.51-73 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20150147387A1 (en) | 2015-05-28 |
| US20100047331A1 (en) | 2010-02-25 |
| CA2683752A1 (en) | 2008-10-23 |
| WO2008127651A1 (en) | 2008-10-23 |
| EP2139516A4 (en) | 2011-06-29 |
| EP2139516A1 (en) | 2010-01-06 |
| AU2008239628B2 (en) | 2014-01-30 |
| US8956627B2 (en) | 2015-02-17 |
| AU2008239628A1 (en) | 2008-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10588960B2 (en) | Liposome-peptide conjugate and method of using same to induce production of anti-HIV antibodies | |
| Montero et al. | The membrane-proximal external region of the human immunodeficiency virus type 1 envelope: dominant site of antibody neutralization and target for vaccine design | |
| US20150147387A1 (en) | Method of inducing antibodies to human immunodeficiency virus involving the administration of mper peptide-liposome conjugates | |
| Dennison et al. | Induction of antibodies in rhesus macaques that recognize a fusion-intermediate conformation of HIV-1 gp41 | |
| Zwick | The membrane-proximal external region of HIV-1 gp41: a vaccine target worth exploring | |
| Matyas et al. | Neutralizing antibodies induced by liposomal HIV-1 glycoprotein 41 peptide simultaneously bind to both the 2F5 or 4E10 epitope and lipid epitopes | |
| Liu et al. | The development of HIV vaccines targeting gp41 membrane-proximal external region (MPER): challenges and prospects | |
| Kim et al. | Comparison of HIV Type 1 ADA gp120 monomers versus gp140 trimers as immunogens for the induction of neutralizing antibodies | |
| US20080057075A1 (en) | Method of inducing neutralizing antibodies to human immunodeficiency virus | |
| US20120128758A1 (en) | Formulation for inducing broadly reactive neutralizing anti-hiv antibodies | |
| Venditto et al. | Rational design of membrane proximal external region lipopeptides containing chemical modifications for HIV-1 vaccination | |
| US20120070488A1 (en) | Method of inducing neutralizing antibodies to human immunodeficiency virus | |
| Huarte et al. | Recognition of membrane-bound fusion-peptide/MPER complexes by the HIV-1 neutralizing 2F5 antibody: implications for anti-2F5 immunogenicity | |
| US20140322262A1 (en) | Method of inducing neutralizing antibodies to human immunodeficiency virus | |
| US20110159037A1 (en) | Methods of treating and protecting against human immunodeficiency virus | |
| CN101588813A (zh) | 诱导人类免疫缺陷病毒的中和抗体的方法 | |
| AU2014202366A1 (en) | Method of Inducing Neutralizing Antibodies to Human Immunodeficiency Virus | |
| Scott et al. | The Membrane-Proximal External Region of | |
| Huarte et al. | Recognition of Membrane-Bound Fusion-Peptide | |
| Huarte Arrayago et al. | Recognition of Membrane-Bound Fusion-Peptide/MPER Complexes by the HIV-1 Neutralizing 2F5 Antibody: Implications for Anti-2F5 Immunogenicity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100930 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100930 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121102 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130201 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130208 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130304 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130311 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130402 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130409 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130502 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131101 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140131 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140207 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140228 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140307 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140401 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140408 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140701 |