JP2009528060A - 集団hlaタイピングとその使用 - Google Patents
集団hlaタイピングとその使用 Download PDFInfo
- Publication number
- JP2009528060A JP2009528060A JP2008557340A JP2008557340A JP2009528060A JP 2009528060 A JP2009528060 A JP 2009528060A JP 2008557340 A JP2008557340 A JP 2008557340A JP 2008557340 A JP2008557340 A JP 2008557340A JP 2009528060 A JP2009528060 A JP 2009528060A
- Authority
- JP
- Japan
- Prior art keywords
- hla
- primer
- probe
- exon
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6834—Enzymatic or biochemical coupling of nucleic acids to a solid phase
- C12Q1/6837—Enzymatic or biochemical coupling of nucleic acids to a solid phase using probe arrays or probe chips
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
- C07H21/04—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids with deoxyribosyl as saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6881—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for tissue or cell typing, e.g. human leukocyte antigen [HLA] probes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Cell Biology (AREA)
- Biomedical Technology (AREA)
- Crystallography & Structural Chemistry (AREA)
- Plant Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
Description
Charron, D. (1997) Genetic Diversity of HLA: Functional and Medical Implications. EDK, Paris, France Marsh, et al. (2000) HLA FactsBook. Academic Press, London, UK Trowsdale and Campbell (1992) Eur J Immunogenet. 19, 45-55 Little, A. M. and Parhams P. (1999) Rev Immunogenet. 1999, 105-123 Trachtenberg, et al. (2003) Nat Med., 9, 928-935 Kruskall, et al. (1992) J Exp Med. 175, 495-502 McCloskey, et al. (1993) Handbook of HLA typing techniques. Hui, K. M., Bidwell, J. L., Eds. Boca Raton, FL. CRC Press, Inc, 175-247 Wordswoth, P. (1991) Immunol Lett., 29, 37-39 Olerup and Setterquist (1993) Handbook of HLA typing techniques. Hui, K. M., Bidwell, J. L., Eds. Boca Raton, FL. CRC Press, Inc, 149-174 Teutsch, et al. (1996) Eur J Immunogenet., 23, 107-120 Hurley, C. K. (1997) Tissue Antigens, 49, 323-328 Dinauer, et al. (2000) Tissue Antigens, 55, 364-368 Schena, et al. (1995) Science 270, 467-70 Saiki, et al. (1989) Proc Natl Acad Sci USA 86 6230-6234 Guo, et al. (2001) Genome Res., 12, 447-457 Wang, et al. (2003) The Eighth Annual Structural Biology Symposium of Sealy Center for Structural Biology, p 157, Galveston, Texas Belosludtsev, et al. (2001) Anal. Biochem. 292, 250-256 Robinson, et al. (2003) Nuc. Acids Res. 31, 311-314 Fofanov, et al. (2002) The 2002 Bioinformatics Symposium, Keck/GCC Bioinformatics Consortium, p 14 Fofanov, et al. (2002) The Seventh Structural Biology Symposium of Sealy Center for Structural Biology, p 51, Galveston, Texas Hayney, et al. (1995) Mayo Clin Proc. 70, 951-954 Mitra, et al. (2003) Analytica Chemica Acta, 469, 141-148 Lemeshko, et al. (2001) Nuc. Acids Res. 29, 3051-3058
本発明はさらに、フィールド環境における即時集団HLA対立遺伝子型決定のための方法も目的とする。その方法は、集団の一人以上のメンバーからのDNA採取、分析のためのDNA精製、及びDNAを構成する、対象とするHLA遺伝子からの、前記遺伝子特異的プライマーを使った標的アンプリコンの生成を含む。前記マイクロアレイを構成するハイブリダイゼーションプローブを標的に接触させ、接触後形成される各HLA対立遺伝子型に特有なハイブリダイゼーションパターンを画像化する。本発明は、決定された対立遺伝子型に基づく各個人の生物剤や兵器による感染リスクの評価のための関連方法も目的とする。本発明は、各個人の生物剤や兵器に対する特定のワクチン応答の評価のための別の関連方法も目的とする。
本発明のさらに別の実施の形態では、集団の一人以上の構成員からDNAを採取し、前記DNAを分析用に精製し、遺伝子特異的プライマーを用いて、前記DNAに含まれる、対象とするHLA遺伝子から標的アンプリコンを生成し、上記マイクロアレイを構成するハイブリダイゼーションプローブを前記標的と接触させ、前記接触後に形成される、ハイブリダイゼーションパターンを画像化し、ここで、各HLA対立遺伝子型はそれに関連するパターンを有する、各工程を有してなる、フィールド環境における即時集団HLA対立遺伝子タイピングの方法を提供する。
クラスI及びII HLA遺伝子座の増幅のためのプライマー
SNP特異的プライマーの設計アルゴリズムの検証
フォワードプライマー、5’GCTCCCACTCCATGAGGTAT3’(配列番号1)、及び、リバースプライマー、5’ATACCTCATGGAGTGGGAGC3’(配列番号2)は、クラスI HLA-B型エクソン2のPCR産物を増幅し、456塩基対の特異的生成物を産生するために使用された(非特許文献文献15)。ここに提示したアルゴリズムは、これらのプライマーが特異的で、クラスI HLA-B座エクソン2のみをプライムするかどうかを確認するために使用された。フォワードプライマーは、クロモソーム6中の11の他の位置に結合し、またクロモソームx中の1箇所にも結合すると決定された。クラスI HLA-B座エクソン2用リバースプライマーは、クロモソーム6中の5つの他の位置に結合し、かつクロモソーム4及び13中の1箇所にも結合することが見出された。クラスI HLA-Bエクソン3増幅用の別のプライマー、5’ACCCGGTTTACCCGGTTTCATTTG3’(配列番号 6)は、クロモソーム6中イントロン2、164−184位以外に8箇所、及びその他数クロモソームに結合することが見出された(表1)。表1は、下線で示したプライマーまたはプライマーの部分配列が、正しい場所以外で見出された回数を示す。アルゴリズム(19-20)は、プライマーのデザインが高分解度HLAタイピングを実行するために非常に重要であることを明白に示す。問題は、ヒト体液中に存在する他の細菌やウイルス由来の夾雑物の可能性によってさらに複雑になる。
各HLA遺伝子の対象とする領域全域にわたる単純な500塩基対長のアンプリコン、及び一対の約250塩基対長の産物が作成された。これは、HLA-A、BまたはDRB1の単純PCRアッセイに適している。しかし、全HLA遺伝子群は、この方法によって設計された14または28対のプライマーを必要とするであろう。
クラスI及びII HLA遺伝子座の一次及び二次増幅
HLA-A及びB座及びエクソン2及び3
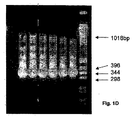
一次PCR反応では、HLA-A座用プライマー対A-LOC-FP1/A-LOC-RP1及びHLA-B座用プライマー対B-LOC-FP1/B-LOC-RP1は、種々のUCLA標準品、陽性対照及び陰性対照の増幅産物を生成するのに用いられた。PCRのプロトコルは、96穴プレート中で50μlの体積用である:94℃で4分間の前PCR変性1サイクル、98℃で1分、71℃で1分、72℃で1分のPCR35サイクル、72℃で7分の保持サイクル(ポリメラーゼ:ロシュ社製ファストスタートTaq)。増幅産物(10μlのサンプル)を、150Vで35分間、2%アガロースゲル上を泳動させる(レーン1:C1-034、レーン2:C1-035、レーン3:C1-036 、レーン4:CCR1)、陽性対照(レーン5:ロッシュ社製DNA)、及び陰性対照(レーン6:H2O );最終レーンは質量標準である。ゲルはHLA-Aの980塩基対産物(図1A)及びHLA-Bの1007塩基対産物(図1B)を示す。
一次PCR反応において、HLA-A座用プライマー対DRB-LOC-FP1a/DRB-LOC-RP1及びHLA-B座用プライマーB-LOC-FP1/B-LOC-RP1は、増幅産物を生成するのに用いられる。PCRプロトコルは、96ウェルプレート中で25μlの体積用である: 94℃で4分間の前PCR変性1サイクル、98℃で1分間、及び55.2℃、56.5℃、58.3℃、60.7℃、63.3℃、66.0℃、68.6℃、71.0℃、73.0℃、74.4℃、または75.2℃のうち一つで30秒間のPCR35サイクル、72℃7分間の保持サイクル(ポリメラーゼ:ロッシュ社製ファストスタートTaq)。増幅産物(10μlのサンプル)を、150Vで35分間、2%アガロースゲル上を泳動させる(レーン1:DRB1陰性対照、レーン2: 55.2℃、レーン3: 56.5℃、レーン4: 58.3℃、レーン5: 60.7℃、レーン6: 63.3℃、レーン7: 66.0℃、レーン8: 68.6℃、レーン9: 71.0℃、レーン10: 73.0℃、レーン11:74.4℃、レーン12: 75.2℃;図1G)。
マイクロアレイ用プローブの設計
適切に設計されたマイクロアレイは、所定のミスマッチに対して全ての可能な最も近い類似体のハイブリダイゼーションパターンをテストするのに使用された。これは、どんな一塩基多型の競合も考慮する。3塩基の配列には64の組み合わせがあり、それらは、最も近い類似体中の中央塩基の対形成及び非形成によって研究された。これらの全ての組み合わせから得られた結果は、どのHLAサブタイプに対する一塩基多型の結合特性の予測も可能にする。これは、熱融解特性によるよりもはるかに優れた推定である。
表3−6は、各々HLA-A及びHLA-B遺伝子座エクソン2及び3用プローブの配列を特定する。オリゴ-Tフランキングセグメントは、フランキングセグメントがアレイ表面には吸着するが、溶液状態の標的核酸に対してほとんど、または全く親和性を持たないように、各プローブの3‘及び5’末端に導入される。プローブ認識サイズは約9−15塩基であり、オリゴ-Tセグメントは、全てのマイクロアレイプローブが最終全長30塩基長となるよう3‘及び5’末端の両方に付加された。
マイクロアレイの製造
マイクロアレイは、Belosludtsevらの方法を使用して製造される(非特許文献17)。手短に言うと、使用される基材は、界面活性剤を用い超音波槽中で洗浄(2分)後、蒸留水及びメタノールで洗浄し、乾燥(30分、40℃)したシリカスライドである。洗浄したスライドをラックに集め、(63.5cm)の25インチ水銀柱、70−80℃の真空オーブン中で終夜、50%シラン/p-キシレン溶液と平衡状態にある気相中で、3-アミノプロピルトリメトキシシランまたは3-グリシドキシプロピルトリメトキシシランを用いてシラン化処理する。
サンプル採取及び抽出の検証
「口腔洗浄」法(非特許文献21)は、サンプルの採取に使用できる。このサンプル採取の技法は、大規模集団研究用の口腔由来DNAの採取、及び、地理的に分散した大規模集団研究からのサンプル収集に理想的である。「口腔洗浄」法は医学的指導を全く必要としない。この技法は、種々の温度条件にさらされても、サンプルを新鮮なDNAと比べて一週間無傷に保つことが示されている(図2A−2B)。
画像分析とパターン認識
マイクロアレイのデジタル画像は、イメージアナライザー(ImageAnalyzer)なるソフトウェア中のアルゴリズムを用いて分析される。簡単に述べると、エッジ検出法は、画像からバックグラウンドを差し引き(図4A)、バックグラウンドよりも高い、予め定義された閾値において明確なパターンを作成する(図4B)ために使用される。HLA型決定のためのパターン認識と2次元バーコードの作成は、ハイブリダイゼーションスポットのパターンと、それらの各HLA型との位置的な相関関係に基づく。HLA型の各対立遺伝子は、決まったスポットパターンを有し、それはバーコードとして使用される。
K-rasモデル:吸着マイクロアレイ上における遺伝子タイピング及びSNPの検出
アンプリコンの生成とオリゴヌクレオチドプローブ
HLAタイピングに用いられるマイクロアレイは、K-ras遺伝子座の、一塩基多型によって野生型と異なる遺伝子型を成功裡に特定し決定するのに使用されてきた。152塩基対のK-rasアンプリコンは、ポリメラーゼ連鎖反応によって生成された。野生型アンプリコン(K-ras 1)は、市販のゲノムDNA原料(シグマ社製)の増幅によって得た。K-ras 2及びK-ras 7変異体は、各々、A549 及びSW480細胞株由来のヒトゲノムDNAの増幅によって得た。PCRの手順は以下の通りである: 94℃で12分間、60℃で1分間及び72℃で1分間の前PCRサイクル1回、95℃で1分間、57℃で1分間、72℃で1分間のPCR35サイクル、72℃で7分間、4℃で保持からなる保持サイクル。K-rasアンプリコン用PCRプライマーは、5’末端がジゴキシゲニンで標識されており、以下の配列を有する:
5’-DIG-ACTGAATATAAACTTGTGGTAGTTGGACCT-3’(配列番号292)、及び
5’-DIG-TCAAAGAATGGTCCTGCACC-3’(配列番号293)。K-rasアンプリコンは、コドン12に異なる点突然変異をもつ。特異的オリゴヌクレオチドは、マイクロアレイ捕獲プローブとして機能するよう表8に示すように設計した。下線を付したヌクレオチドは、点突然変異を示す。
ナトリウムイオン濃度として150mMのコハク酸ナトリウムを含む前ハイブリダイゼーション溶液、Denhardtの5倍溶液、pH8.0は、10分以上アレイに適用された。この溶液を減圧除去し、ハイブリダーゼーション液(1nMアンプリコン、0.1mMシャペロン、ナトリウム濃度として150mMのコハク酸ナトリウム、Denhardtの5倍溶液、pH8.0)をアレイに適用した。これらの研究において、捕獲プローブK-ras 1、K-ras 2、及びK-ras 7に相補的なアンプリコンのみが使用された。2時間のハイブリダイゼーション後、アレイを、ナトリウム濃度で100mMのコハク酸ナトリウムで10分間ずつ2回洗浄した後、13SSC中で軽くすすいだ。ジゴキシゲニン標識されたアンプリコンは、ELF-97mRNA in situハイブリダイゼーションキット(ベーリンガー・マンハイム社製)のブロッキング緩衝剤中1:1000に希釈したアルカリフォスファターゼに結合した抗ジゴキシゲニン抗体の後、同キットの緩衝剤Aによる洗浄、及びアルカリフォスファターゼ基質であるELFのキット記載の通り適用して検出した。アルカリフォスファターゼによる切断後、ELF分子は沈殿し、UV励起により蛍光を発する。蛍光強度はアルファイメージャー2000装置で検出し、シグマプロット3.0ソフトウェアで処理した(図5A−5D)。
実施例8
HLA-B中のSNP検出
HLA-B検証モデル
UCLAは、HLA型既知の特性がよく明らかにされた75のDNAサンプルからなるライブラリーを収集し、世界中で参照標準品として使用される。この参照セットを入手し、参照セット中の配列バリエーションのより高分解度の理解のために、HLA-B超可変領域の配列を再分析した。図6A−6Bに示す通り、UCLA由来のデータは極めて正確で、配列の片側再分析に関し4−5の不一致しかない。
HLA-B標的の調製
HLA-Bエクソン2由来の500塩基対フラグメントは、試験的に精製したヒトゲノムDNAサンプルから上記のようにデザインされたプライマーを用いてポリメラーゼ連鎖反応(PCR)によって得られる。以下のPCR手順が、増幅500塩基対フラグメントの作成に使用される: 94℃で12分間、60℃で1分間、及び72℃で1分間の前PCRサイクル1回、95℃で1分間、57℃で1分間、72℃で1分間のPCR35サイクル、72℃で7分間、4℃で保持の保持サイクル。HLA-Bアンプリコン用のPCRプライマーは、T7ポリメラーゼ認識配列5’ ATGTAATACGACTCACTATAG 3’(配列番号317)を含むように修飾される。
ナトリウムイオン濃度として150mMのコハク酸ナトリウム、5倍濃縮のDenhardtの溶液、pH8.0を含む前ハイブリダイゼーション溶液は、最低10分間アレイに適用される。前ハイブリダイゼーション溶液を減圧除去し、ナトリウムとして150mMのコハク酸ナトリウム、5倍濃縮のDenhardtの溶液、pH8.0中の標識付一本鎖cRNA標的を含むハイブリダイゼーション溶液が、HLAマイクロアレイとハイブリダイゼーションするようアレイに加えられた。2時間のハイブリダイゼーション後、アレイを、ナトリウムとして100mMのコハク酸ナトリウムで10分間ずつ2回洗浄した後、1倍SSC中で軽くすすいだ。 ストレプトアビジンと結合したフィコエリスリンが、cRNA標的上のビオチンに結合する(非特許文献22)。蛍光強度は、CCDを具えたマイクロアレイ画像化装置(Array Worx、API社製(米国ワシントン州イサクア所在))で検出する。
図7A−7Fは、HLA-Bコドン9のハイブリダイゼーションデータを示す。このアレイにおいて、オリゴT フランキング配列を持たない9−12塩基長のプローブは右上に、対応するオリゴT含有30塩基誘導体はマイクロアレイの左にある。ハイブリダイゼーションは、UCLAのHLA参照DNAライブラリーから得られた既知配列バリエーション(サンプル72、21、27、57)の、Cy-3標識した281塩基対のネステッドPCR産物を用いて実施された。また、図7F−G には、ボランティア(MH、BI)から得た281塩基対産物に対するマイクロアレイハイブリダイゼーションのデータを示す。プローブ認識配列を一定に保つなら、オリゴTの付加は短鎖プローブ同族体に比べてハイブリダーゼーションシグナルが10倍向上する。
自動マイクロアレイシグナル分析
生画像(図7Aのような)から強度を抽出する前に、適切な格子作成技術の選択を行う必要がある(図8)。格子の構造情報はスポットの概算の位置を配置するために使用される。マイクロアレイスポットは中心の周りに対称であるから、最適化処理は、スポット近傍で最適なスポットの中心を探すように実行されることができる。生マイクロアレイ画像から始まり、格子作成過程は、生格子概算、局所的スポット中心調整、及び構造的スポット中心調整を含む。格子作成が完了した後、何ピクセルがスポットの一部とみなせるかを決定する必要がある。半径R(ピクセル単位で測定)なら、スポットを囲む2R+1の大きさの四角形が容易に構築できる。ピクセルがスポットの内側かどうかを決めるには、図7A−7Fに例示したように、あるピクセルと四角形の中心ピクセルとの距離Dを計算し、それが半径Rよりも小さいか同じであるかを見る。各ピクセルの情報を保存するのに効率的なデータ構造を利用することにより、上記の方法はあまり大きくないメモリーと計算時間で何千ものスポットを含むマイクロアレイ画像を取り扱うことができる。
科学的興味のあるHLA対立遺伝子決定のための知識に基づいた文献スクリーニングツール
10,000以上のHLA対立遺伝子が知られているが、最も臨床上優位なHLAチップを開発するには、全対立遺伝子のうち科学的関心が最も蓄積した部分に集中することが重要である。その様な対立遺伝子を決定するための知識に基づく文献スクリーニングツールは、PubMedデータベース内の引用によって定義される様に本発明において開発された。一次知識ベーススクリーニングに基づき、約210の対立遺伝子が最も潜在的関心が高いものとして特定された。有意性の測定は、対立遺伝子名を検索語句としてPubMed検索を実施した時のヒット数である。Entrez PubMedは、一般的なウェッブ質問インターフェイスの外のEntrezデータにアクセスを許可するため、eUtilsとして知られる7つのサーバー側プログラムを提供する。EsearchはeUtilの一つで、主ID及び用語翻訳を検索・回収し、ユーザーの環境において将来使用するために結果を保持しておくことも出来る。それは、相対日時、日時範囲、回収モード、ソート順位等の異なるオプションに基づいてIDを回収する。各検索語句用にeUtilのURLをNCBIに通知するスクリプトが、HLA対立遺伝子を検索するために書かれた。それは、PubMed収載のタイトル、要旨、及び全文内に検索語句を探す。スクリプトは、XMLフォーマットの結果を回収する。XMLファイルの「カウント」タグに含まれている各検索語句に対するヒット数は、ファイルを構成要素に分析する事によって得られる。その様な検索は、21のHLA遺伝子由来の対立遺伝子に対して実施した。表10は、21対立遺伝子引用の自動PubMed検索の結果を列挙する。
HLAチップ用候補プローブの選択
IMGT/HLAデータベースは、各HLA遺伝子座の複数の整列を提供する。整列した配列は、SNPが明白に印付けられるようなフォーマットである。SNPは、ある対立遺伝子を他とは異ならせるものである。SNPの組合せは、対立遺伝子を特異的に示すことができる。簡単な計算から、HLA-Bエクソン2中には125、エクソン3には93のSNPがあり、各々553及び562の対立遺伝子をコードしていることが知られている。SNPが起こる各位置において、SNPの周囲の短いn量体(13−15ヌクレオチド長)は、候補プローブ配列のテンプレートから除かれる。単純テンプレートと複合テンプレートの2種類のテンプレートがある。単純テンプレートは、ただ一つのSNPを含む。例えば、エクソン3中36位にSNPがあり、両側6ヌクレオチド以内に他のSNPはない。中央のSNPとその両側の6ヌクレオチドから成る13残基のテンプレートが、このSNP用に作製された。テンプレートは、5’-TGCGACXTGGGGC(配列番号318)であり、ここでXはSNPを示す。対立遺伝子B*7301では、この場所は「A」である。対立遺伝子B*0712及び他の126対立遺伝子においては、「C」である。参照対立遺伝子を含む残りのHLA-B対立遺伝子においては、「G」である。従って、A-、C-、G-多型をもつ 3種のプローブ候補がこのテンプレートから作製された。この場合、対立遺伝子B*0712及びSNP位に「C」をもつ他の全対立遺伝子は、C-多型をもつプローブ候補により特定されるといわれる。同時に、対立遺伝子B*7301は、A-多型をもつプローブ候補によって特定される。
対象とする遺伝子座を増幅するための最適PCR数
表9は、10の対象とする遺伝子座を増幅するのに要する、一次及び、いくつかの例については二次PCR反応のおよその数を示す。一次及び二次(ネステッド)PCRの両方とも、A、B、Cに必要であろう。3つの一次PCRは多重進行により一つの反応にでき、その後、ネステッドステップの第2の多重反応が続く。 従って、クラスI遺伝子の全セットに、2つのPCR反応だけが必要である。
Claims (36)
- HLA遺伝子を増幅するためのプライマー。
- 前記HLA遺伝子がHLA A、B、またはDRB1、またはそれらのエクソンであることを特徴とする請求項1記載のプライマー。
- 前記HLA-Aプライマーが配列番号14−15に示す配列を有し、前記HLA-Aエクソン2プライマーが配列番号20−21に示す配列を有し、前記HLA-Aエクソン3プライマーが配列番号22−26に示す配列を有することを特徴とする請求項2記載のプライマー。
- 前記HLA-Bプライマーが配列番号16−19に示す配列を有し、前記HLA-Bエクソン2プライマーが配列番号27−28に示す配列を有し、HLA-Bエクソン3プライマーが配列29−31に示す配列を有することを特徴とする請求項2記載のプライマー。
- 前記HLA-DRB1プライマーが配列番号32−37に示す配列を有し、前記HLA-Bエクソン2プライマーが配列番号38−47に示す配列を有することを特徴とする請求項2記載のプライマー。
- HLA遺伝子内の一塩基多型(SNP)を検出するためのハイブリダイゼーションプローブであって、
前記SNPを含む領域に相補的な約9−15残基のオリゴヌクレオチドと、
5’末端及び3’末端側のフランキング配列と、
を含むことを特徴とするプローブ。 - 前記フランキング配列がオリゴチミジンまたはオリゴチミジン様ポリアニオン系ポリマーであることを特徴とする請求項6記載のハイブリダイゼーションプローブ。
- 前記SNPがHLA-Aエクソン2またはエクソン3、HLA-Bエクソン2またはエクソン3、またはHLA-DRB1エクソン2内に位置することを特徴とする請求項6記載のハイブリダイゼーションプローブ。
- 前記HLA-Aエクソン2プローブが配列番号48−49に示す配列を有し、前記HLA-Aエクソン3プローブが配列番号100−153に示す配列を有することを特徴とする請求項8記載のハイブリダイゼーションプローブ。
- 前記HLA-Bエクソン2プローブが配列番号154−237に示す配列を有し、前記HLA-Bエクソン3プローブが配列番号238−239に示す配列を有することを特徴とする請求項8記載のハイブリダイゼーションプローブ。
- 陽イオン性表面を有する基材と、
吸着された、1つ以上の請求項6記載のハイブリダイゼーションプローブを含む、単分子層と、
を有してなる、
HLA遺伝子の対立遺伝子タイピング用のマイクロアレイ装置。 - 前記陽イオン性表面が、アミノシラン、グアニジニウム、酸化スズ、酸化アルミニウム、または酸化ジルコニウム、あるいは、他の同等の荷電部分を含むことを特徴とする請求項11記載のマイクロアレイ装置。
- 前記基材がガラス、プラスティック、または金属であることを特徴とする請求項11記載のマイクロアレイ装置。
- 前記ハイブリダイゼーションプローブとともに共吸着されたオリゴチミジンをさらに含むことを特徴とする請求項11記載のマイクロアレイ装置。
- 前記オリゴチミジンが約20から約40のチミジンを有することを特徴とする請求項14記載のマイクロアレイ装置。
- オリゴチミジンに結合した蛍光色素をさらに含むことを特徴とする請求項14記載のマイクロアレイ装置。
- キャップ剤をさらに含むことを特徴とする請求項11記載のマイクロアレイ装置。
- HLA遺伝子を増幅するための遺伝子特異的プライマーと、
請求項11記載のマイクロアレイ装置と、
を含む、
集団HLA遺伝子タイピング用のキット。 - 前記プライマーが配列番号14−47に示す配列を有することを特徴とする請求項18記載のキット。
- PCR反応用緩衝剤及びポリメラーゼ、または蛍光色素、またはこれらの組合せをさらに含むことを特徴とする請求項18記載のキット。
- フィールド環境における即時ハイスループット集団HLA対立遺伝子タイピング用のシステムであって、
請求項11記載のマイクロアレイ装置と、
集団を構成する個人からDNAサンプルを採取及び精製する手段と、
採取したDNAから1つ以上の対象とするHLA遺伝子のcRNA標的アンプリコンをPCRによって生成する手段と、
対象とする各個人のHLA遺伝子にHLA対立遺伝子型を割り当てる手段と、
を有してなり、
前記システムを構成する個々の手段及び装置が、携帯可能であって、フィールド環境で即時操作可能であることを特徴とする、
システム。 - 前記HLA遺伝子がHLA-A、HLA-BまたはHLA-DRB1であることを特徴とする請求項21記載のシステム。
- 前記DNAサンプルを採取するための手段が、
個人から採取した口腔洗浄サンプル、口腔綿サンプル、または血液サンプルを収容するのに適した容器
を含むことを特徴とする請求項21記載のシステム。 - 前記標的アンプリコンを生成するための手段が、対象とする前記HLA遺伝子を増幅するためのHLA遺伝子特異的プライマーを含むことを特徴とする請求項21記載のシステム。
- 前記遺伝子特異的プライマーが配列番号14−47に示す配列を有することを特徴とする請求項24記載のシステム。
- 前記各個人にHLA対立遺伝子型を割り当てるための手段が、
マイクロアレイ装置上に吸着されたハイブリダイゼーションプローブに標的をハイブリダイゼーションした後に、該マイクロアレイ装置上に形成されるハイブリダイゼーションパターンを検出するのに適合した画像化装置と、
画像化されたハイブリダイゼーションパターンをHLA対立遺伝子型として認識するのに適合したアルゴリズム集を含むパターン認識ソフトウェアと、
を含むことを特徴とする請求項21記載のシステム。 - 前記ハイブリダイゼーションプローブが配列番号48−289に示す配列を有することを特徴とする請求項26記載のシステム。
- 即時ハイスループット遺伝子タイピングが、一時間一稼動システムあたり約200から約300のHLA対立遺伝子型であることを特徴とする請求項21記載のシステム。
- フィールド環境における即時集団HLA対立遺伝子タイピングの方法であって、
前記集団の一人以上の構成員からDNAを採取し、
前記DNAを分析用に精製し、
遺伝子特異的プライマーを用いて、前記DNAに含まれる対象とするHLA遺伝子から標的アンプリコンを生成し、
請求項11記載のマイクロアレイを構成するハイブリダイゼーションプローブを前記標的と接触させ、
前記接触後に形成される、ハイブリダイゼーションパターンを画像化し、ここで、各HLA対立遺伝子型はそれに関連するパターンを有する、
各工程を有してなる、
方法。 - 前記採取したDNAを保存する工程をさらに含むことを特徴とする請求項29記載の方法。
- 前記DNAが、血液から、口腔綿を用いて、または口腔洗浄により採取されることを特徴とする請求項29記載の方法。
- 前記遺伝子特異的プライマーが配列番号14−47に示す配列を有することを特徴とする請求項29記載の方法。
- 前記ハイブリダイゼーションプローブが配列番号48−289に示す配列を有することを特徴とする請求項29記載の方法。
- 決定された対立遺伝子型に基づいて、各個人の生物剤または兵器による感染リスクを評価する工程をさらに含むことを特徴とする請求項29記載の方法。
- 各個人の生物剤または兵器に対する特定のワクチンに対する応答を評価する工程をさらに含むことを特徴とする請求項29記載の方法。
- 前記集団の各個人に割り当てられた対立遺伝子型が、それらの決定手段を含むことを特徴とする請求項29記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US77707806P | 2006-02-27 | 2006-02-27 | |
| PCT/US2007/005121 WO2008048355A2 (en) | 2006-02-27 | 2007-02-27 | Population scale hla-typing and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009528060A true JP2009528060A (ja) | 2009-08-06 |
| JP2009528060A5 JP2009528060A5 (ja) | 2010-04-15 |
Family
ID=39314565
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008557340A Pending JP2009528060A (ja) | 2006-02-27 | 2007-02-27 | 集団hlaタイピングとその使用 |
Country Status (9)
| Country | Link |
|---|---|
| US (4) | US7667026B2 (ja) |
| EP (1) | EP1991558B1 (ja) |
| JP (1) | JP2009528060A (ja) |
| KR (1) | KR20080100461A (ja) |
| AU (1) | AU2007313472B2 (ja) |
| CA (1) | CA2643771A1 (ja) |
| NZ (2) | NZ571513A (ja) |
| SG (1) | SG172644A1 (ja) |
| WO (1) | WO2008048355A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013100139A1 (ja) * | 2011-12-28 | 2013-07-04 | 凸版印刷株式会社 | Hla-a*24グループの判定方法 |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1536021A1 (en) * | 2003-11-27 | 2005-06-01 | Consortium National de Recherche en Genomique (CNRG) | Method for HLA typing |
| NZ571513A (en) * | 2006-02-27 | 2012-02-24 | Genomics Usa | Population scale HLA-typing and uses thereof |
| DE102009035286A1 (de) * | 2009-07-30 | 2011-02-10 | Siemens Aktiengesellschaft | Verfahren und Vorrichtung zur Darstellung computertomographischer Untersuchungsdaten eines Untersuchungsobjektes |
| US8771951B2 (en) | 2009-11-16 | 2014-07-08 | Genomics Usa, Inc. | Methods for PCR and HLA typing using raw blood |
| US8969254B2 (en) | 2010-12-16 | 2015-03-03 | Dana-Farber Cancer Institute, Inc. | Oligonucleotide array for tissue typing |
| HUP1200622A2 (en) * | 2012-10-30 | 2014-05-28 | Budapesti Mueszaki Es Gazdasagtudomanyi Egyetem | Method and computer program product for genotype classification |
| WO2014160046A1 (en) * | 2013-03-14 | 2014-10-02 | The Trustees Of The University Of Pennsylvania | A method for detecting mutations in single cells or single molecules |
| US9751069B2 (en) | 2013-05-14 | 2017-09-05 | Genomics Usa, Inc. | Compositions and methods for entrapping protein on a surface |
| WO2017093353A1 (en) * | 2015-12-01 | 2017-06-08 | Fundación Centro Nacional De Investigaciones Cardiovasculares Carlos Iii (Cnic) | Method for diagnosing cardiomyopathies |
| US10612075B2 (en) * | 2015-12-28 | 2020-04-07 | PathogenDX Inc | Microarray based multiplex pathogen analysis and uses thereof |
| US11542498B2 (en) * | 2015-12-28 | 2023-01-03 | Pathogendx, Inc. | Microarray based multiplex pathogen analysis and uses thereof |
| KR102511161B1 (ko) * | 2021-11-01 | 2023-03-20 | 대한민국 | 한국인 특이적 snp 정보 및 최적화된 파이프라인을 이용한 hla-a 유전자형 분석 방법 |
| KR102511162B1 (ko) * | 2021-11-01 | 2023-03-20 | 대한민국 | 한국인 특이적 snp 정보 및 최적화된 파이프라인을 이용한 hla-drb1 유전자형 분석 방법 |
| KR102543976B1 (ko) * | 2021-11-01 | 2023-06-15 | 대한민국 | 한국인 특이적 snp 정보 및 최적화된 파이프라인을 이용한 hla-b 유전자형 분석 방법 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000061795A2 (en) * | 1999-04-09 | 2000-10-19 | Innogenetics N.V. | Method for the amplification of hla class i alleles |
| WO2000079006A1 (en) * | 1999-06-17 | 2000-12-28 | Fred Hutchinson Cancer Research Center | Oligonucleotide arrays for high resolution hla typing |
| WO2005042764A2 (en) * | 2003-10-28 | 2005-05-12 | Dynal Biotech Llc | Primers, methods and kits for amplifying or detecting human leukocyte antigen alleles |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4582788A (en) * | 1982-01-22 | 1986-04-15 | Cetus Corporation | HLA typing method and cDNA probes used therein |
| US5567809A (en) * | 1986-03-13 | 1996-10-22 | Hoffmann-La Roche Inc. | Methods and reagents for HLA DRbeta DNA typing |
| AU6657996A (en) * | 1995-07-18 | 1997-02-18 | Guido Krupp | Ribozymes for the selective inhibition of expression by mhc llele genes, and drugs containing such ribozymes |
| WO2000031295A1 (fr) * | 1998-11-26 | 2000-06-02 | Shionogi & Co., Ltd. | Procede permettant de distinguer les alleles hla de classe i |
| WO2001006011A2 (en) * | 1999-07-14 | 2001-01-25 | Genometrix Genomics, Inc. | Arrays comprising non-covalently associated nucleic acid probes and methods for making and using them |
| US6670124B1 (en) * | 1999-12-20 | 2003-12-30 | Stemcyte, Inc. | High throughput methods of HLA typing |
| CA2566860A1 (en) | 2004-05-20 | 2005-12-01 | Bioarray Solutions Ltd. | Genotyping of multiple loci with pcr for different loci amplification at different temperatures |
| NZ571513A (en) * | 2006-02-27 | 2012-02-24 | Genomics Usa | Population scale HLA-typing and uses thereof |
-
2007
- 2007-02-27 NZ NZ571513A patent/NZ571513A/en not_active IP Right Cessation
- 2007-02-27 AU AU2007313472A patent/AU2007313472B2/en not_active Ceased
- 2007-02-27 KR KR1020087023410A patent/KR20080100461A/ko not_active Application Discontinuation
- 2007-02-27 US US11/711,561 patent/US7667026B2/en not_active Expired - Fee Related
- 2007-02-27 WO PCT/US2007/005121 patent/WO2008048355A2/en active Application Filing
- 2007-02-27 SG SG2011038734A patent/SG172644A1/en unknown
- 2007-02-27 CA CA002643771A patent/CA2643771A1/en not_active Abandoned
- 2007-02-27 EP EP07861253.8A patent/EP1991558B1/en not_active Not-in-force
- 2007-02-27 JP JP2008557340A patent/JP2009528060A/ja active Pending
-
2010
- 2010-02-18 US US12/660,002 patent/US8183360B2/en not_active Expired - Fee Related
-
2011
- 2011-12-19 NZ NZ597200A patent/NZ597200A/xx not_active IP Right Cessation
-
2012
- 2012-05-21 US US13/476,774 patent/US8575325B2/en not_active Expired - Fee Related
-
2013
- 2013-11-04 US US14/070,819 patent/US20140135231A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000061795A2 (en) * | 1999-04-09 | 2000-10-19 | Innogenetics N.V. | Method for the amplification of hla class i alleles |
| WO2000079006A1 (en) * | 1999-06-17 | 2000-12-28 | Fred Hutchinson Cancer Research Center | Oligonucleotide arrays for high resolution hla typing |
| WO2005042764A2 (en) * | 2003-10-28 | 2005-05-12 | Dynal Biotech Llc | Primers, methods and kits for amplifying or detecting human leukocyte antigen alleles |
Non-Patent Citations (2)
| Title |
|---|
| JPN6012022389; Hum.Immunol.,Vol.62(2001)p.850-857 * |
| JPN6012022390; J.Microbiol.Methods,Vol.42(2000)p.203-207 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013100139A1 (ja) * | 2011-12-28 | 2013-07-04 | 凸版印刷株式会社 | Hla-a*24グループの判定方法 |
| CN104024410A (zh) * | 2011-12-28 | 2014-09-03 | 凸版印刷株式会社 | Hla-a*24组的判定方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20070298425A1 (en) | 2007-12-27 |
| WO2008048355A2 (en) | 2008-04-24 |
| US8575325B2 (en) | 2013-11-05 |
| NZ571513A (en) | 2012-02-24 |
| US7667026B2 (en) | 2010-02-23 |
| EP1991558B1 (en) | 2015-11-18 |
| US20120302457A1 (en) | 2012-11-29 |
| SG172644A1 (en) | 2011-07-28 |
| CA2643771A1 (en) | 2008-04-24 |
| WO2008048355A3 (en) | 2008-11-13 |
| EP1991558A4 (en) | 2009-11-04 |
| KR20080100461A (ko) | 2008-11-18 |
| NZ597200A (en) | 2013-06-28 |
| US8183360B2 (en) | 2012-05-22 |
| US20100279889A1 (en) | 2010-11-04 |
| US20140135231A1 (en) | 2014-05-15 |
| AU2007313472A1 (en) | 2008-04-24 |
| EP1991558A2 (en) | 2008-11-19 |
| AU2007313472B2 (en) | 2014-01-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2007313472B2 (en) | Population scale HLA-typing and uses thereof | |
| US20220106586A1 (en) | Compositions and methods for library sequencing | |
| US7972791B2 (en) | Methods for haplotyping genomic DNA | |
| AU783278B2 (en) | Genomic profiling: a rapid method for testing a complex biological sample for the presence of many types of organisms | |
| US6376191B1 (en) | Microarray-based analysis of polynucleotide sequence variations | |
| JP5968879B2 (ja) | Dna分子タグ技術及びdna不完全断片化技術に基づいたpcrシークエンシング法及びそれを用いたhla遺伝子タイピング法 | |
| US7732138B2 (en) | Rapid genotyping analysis and the device thereof | |
| EP2563939B1 (en) | Rapid genotyping analysis for human papillomavirus and the device thereof | |
| JP2014507164A (ja) | ハプロタイプ決定のための方法およびシステム | |
| JP2009528060A5 (ja) | ||
| EP3350351A1 (en) | Virome capture sequencing platform, methods of designing and constructing and methods of using | |
| US20090143245A1 (en) | Microarrays for genotyping and methods of use | |
| AU2013273684A1 (en) | Population scale hla-typing and uses thereof | |
| JP2010515452A (ja) | スタフィロコッカス・アウレウス検出用dnaチップ | |
| JP2004113196A (ja) | 特異的繰り返し遺伝子配列が多数含まれる結核菌特異的遺伝子群を用いたタイピング用dnaチップおよびその利用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100226 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100226 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100902 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120501 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120801 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120808 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130108 |