JP2008538700A - 免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 - Google Patents
免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 Download PDFInfo
- Publication number
- JP2008538700A JP2008538700A JP2008508001A JP2008508001A JP2008538700A JP 2008538700 A JP2008538700 A JP 2008538700A JP 2008508001 A JP2008508001 A JP 2008508001A JP 2008508001 A JP2008508001 A JP 2008508001A JP 2008538700 A JP2008538700 A JP 2008538700A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- endosialin
- cells
- cell
- antibodies
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39583—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials not provided for elsewhere, e.g. haptens, coenzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6817—Toxins
- A61K47/6819—Plant toxins
- A61K47/6825—Ribosomal inhibitory proteins, i.e. RIP-I or RIP-II, e.g. Pap, gelonin or dianthin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6891—Pre-targeting systems involving an antibody for targeting specific cells
- A61K47/6897—Pre-targeting systems with two or three steps using antibody conjugates; Ligand-antiligand therapies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2851—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the lectin superfamily, e.g. CD23, CD72
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Molecular Biology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Biophysics (AREA)
- Epidemiology (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nanotechnology (AREA)
- Toxicology (AREA)
- Biochemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Botany (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Medical Informatics (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
【選択図】 図3
Description
本発明の抗体は、ヒト−マウスキメラ抗体を含む(これに限定されるものではないが)キメラ抗体であっても良い。本発明の抗体はヒト化されていても良い。本発明の抗体は完全にヒト化されていても良い。本発明において、本発明の抗体を発現したハイブリドーマ細胞、本発明の抗体をコードしたポリヌクレオチド、前記本発明の抗体をコードしたポリヌクレオチドを有するベクター、およびトランスフェクトーマと呼ばれる、本発明のポリヌクレオチドを有する発現細胞もまた提供される。
「予防する」という用語は、微生物が感染するか、異形成または新生血管疾患などの異常な状態を発生させる可能性を低下させることを指す。
抗体由来分子は、抗原結合特異性を保持し、例えば、少なくとも1つの可変領域(重鎖または軽鎖可変領域)を有する完全な抗体の一部を有する。抗体由来分子には、例えば、Fabフラグメント、Fab’フラグメント、F(ab’)2フラグメント、Fdフラグメント、F(v)フラグメント、Fabcフラグメント、Fdフラグメント、Fabcフラグメント、Sc抗体(単鎖抗体)、ダイアボディ、個々の抗体軽鎖、個々の抗体重鎖、抗体鎖と他の分子とのキメラ融合、重鎖単量体または二量体、軽鎖単量体または二量体、重鎖1つと軽鎖1つから成る二量体などの分子を含む。すべてのクラスの免疫グロブリン(例えば、IgA、IgD、IgE、IgG、およびIgM)とそのサブクラスが含まれる。
本発明の抗体は特異的に、例えば立体構造エピトープなどのエンドシアリンのエピトープに結合し、インアウト活性(つまり、選択的に免疫エフェクター活性を誘導し、エンドシアリン陽性細胞に内部移行する能力)を示す。本発明の抗体が結合するエンドシアリンは好ましくは哺乳類であり、さらに好ましくはヒトである。ヒトエンドシアリンは配列ID番号1でコードされ、配列ID番号2のアミノ酸配列を有する。
本発明の抗体には、タイプIgA、IgG、IgE、IgD、IgM(およびそのサブタイプ)を含む、すべてのアイソタイプの完全な免疫グロブリンを含むことができる。前記免疫グロブリンの軽鎖はκまたはλである。
本発明の抗体とその誘導体は、解離定数(Kd)が1×10−2未満である結合親和性を有する。一部の実施形態によると、前記Kdは1×10−3未満である。他の実施形態によると、前記Kdは1×10−4未満である。一部の実施形態によると、前記Kdは1×10−5未満である。さらに他の実施形態によると、前記Kdは1×10−6未満である。他の実施形態によると、前記Kdは1×10−7未満である。他の実施形態によると、前記Kdは1×10−8未満である。他の実施形態によると、前記Kdは1×10−9未満である。他の実施形態によると、前記Kdは1×10−10未満である。さらに他の実施形態によると、前記Kdは1×10−11未満である。一部の実施形態によると、前記Kdは1×10−12未満である。他の実施形態によると、前記Kdは1×10−13未満である。他の実施形態によると、前記Kdは1×10−14未満である。さらに他の実施形態によると、前記Kdは1×10−15未満である。
本発明には、本発明の抗FRA抗体の重鎖および/または軽鎖をコードする核酸も含まれる。本明細書において用いられる「核酸」または「核酸分子」は、一本鎖または二本鎖のすべてのDNAまたはRNA分子を指し、一本鎖の場合は直鎖または環状型の相補的配列の分子を指す。核酸分子について考察する場合、5’から3’方向の配列を提供する通常の慣習に従い、特定の核酸分子の配列または構造について本明細書に説明することがある。本発明の一部の実施形態では、核酸分子は「単離」されている。この用語は、核酸分子に用いられる場合、由来する生物体の天然型ゲノムに隣接する配列から分離された核酸分子を指す。例えば、「単離核酸」は、プラスミドまたはウイルスベクターなどのベクターに挿入されるか、原核または真核細胞または宿主微生物のゲノムDNAに組み込まれたDNA分子を有する。RNAに用いる場合、前記「単離核酸」という用語は、主に、上記に定義した単離DNA分子によってコードされるRNA分子を指す。あるいは、前記用語は、天然の状態(つまり、細胞または組織中)で関連すると考えられる他の核酸から十分分離されたRNA分子を指す。単離核酸(DNAまたはRNA)は、さらに生物学的方法または合成法によって直接作製されたか、その作製中に存在する他の成分から分離された分子を示す。
免疫化動物
本発明では、エンドシアリンに特異的に結合するインアウトモノクローナル抗体を作製する方法も提供する。エンドシアリンは、タンパク質を単離および精製するための様々な既知の技術を利用し、細胞または組み換え系から精製することができる。例えば、これに限定されるものではないが、FRAは前記タンパク質の見かけ上の分子量に基づき、前記タンパク質をSDS−PAGEゲルに流し、前記タンパク質を膜にブロットすることで単離することができる。その後、エンドシアリンに対応する適切なサイズのバンドを膜から切り取り、直接動物で免疫原として利用するか、まず前記タンパク質を前記膜から抽出または溶出してから利用することができる。代わりの例として、前記タンパク質はサイズ排除クロマトグラフィーのみ、または他の単離および精製法との併用で単離することができる。他の精製法は、Zola,MONOCLONAL ANTIBODIES:PREPARATION AND USE OF MONOCLONAL ANTIBODIES AND ENGINEERED ANTIBODY DERIVATIVES (BASICS: FROM BACKGROUND TO BENCH) Springer−Verlag Ltd.,New York,2000;BASIC METHODS IN ANTIBODY PRODUCTION AND CHARACTERIZATION,Chapter 11,"Antibody Purification Methods,"Howard and Bethell,Eds.,CRC Press,2000;ANTIBODY ENGINEERING(SPRINGER LAB MANUAL.),Kontermann and Dubel,Eds.,Springer−Verlag,2001などの標準的な参考書籍で参照可能である。
エンドシアリンに特異的に結合するインアウト抗体のスクリーニングは、酵素免疫吸着測定法(ELISA)を利用し、免疫エフェクター活性を持つ抗体をスクリーニングする、および/または内部移行をアッセイすることで達成することができる。免疫エフェクター活性を示す抗体は、抗体依存性細胞傷害作用(ADCC)または補体依存性細胞傷害作用(CDC)をモニターする標準的な免疫エフェクター法を利用することで同定することができる。内部移行可能な抗体は、前記抗体を蛍光色素またはプロドラッグなどの検出可能な標識と結合させ、可視化した内部移行能力または毒性をモニターすることで、同定可能である。1若しくはそれ以上のこれらのアッセイ(ELISA、免疫エフェクター法、および内部移行法)は、本発明のインアウト抗体を同定する任意の順序で実行することができる。
本発明の別の観点では、本発明の抗エンドシアリン抗体の薬学的組成物を特徴としている。前記薬学的組成物を使用し、患者のエンドシアリン陽性細胞の成長を抑制または軽減することができる。特定の実施形態では、前記薬学的組成物が製剤化され、注射または注入により投与される。
本発明のさらに別の観点では、インビトロまたはインビボでエンドシアリン陽性細胞の成長を阻害または抑制するキットが提供される。また、インビトロまたはインビボでエンドシアリン陽性細胞の有無を確認するキットも提供される。
本発明の方法には、卵巣癌、膵癌、前立腺癌、または肺癌細胞を含む(これに限定されるものではないが)、表面にエンドシアリンを提示する、異型細胞または新生血管細胞などの細胞を検出する方法を含む。前記方法は、生物サンプルに対してインビトロで、またはインビボで実行することができる。本発明のエンドシアリン陽性細胞の検出方法は、本発明の抗エンドシアリン抗体を生物サンプルと接触させる工程または本発明の抗エンドシアリン抗体を患者に投与する工程(前記抗体は例えば放射性、蛍光性、または発色試薬(例えば、111In−DOTA)などの(これに限定されるものではないが)検出可能な標識で標識される)、および前記抗体の細胞への結合を決定する工程を有する。前記検出可能な標識は酵素とすることもある。
本発明のインアウト抗エンドシアリン抗体は、インビトロまたはインビボにおいてエンドシアリン陽性細胞の成長を抑制するための使用に適している。本発明の方法は、エンドシアリンを発現する細胞を含む組織、好ましくは増強されたエンドシアリンの発現を示す細胞に関連した腫瘍疾患または血管新生疾患を有すると同定された非ヒト動物での使用に適している。本発明の利益を受ける非ヒト動物には、ペット、外来性(例えば、動物園の動物)および国産家畜を含む。好ましくは、前記非ヒト動物は哺乳類である。
モノクローナル抗体ES−1はエンドシアリンに特異的なヒト化抗体である、前記抗体はエンドシアリンタンパク質、エンドシアリンを発現した癌細胞、ヒト胚内皮細胞、および白血球に対する特異的な結合を示す。エンドシアリンに特異的な結合性を立証するために、当業者によって用いられる方法に従って、96型ウェル中、エンドシアリン発現細胞を用いて全細胞ELISAを行った。ELISAによって反応が見出された抗体はさらに、製造プロトコールに従って、FACS分析を用いたエンドシアリン結合分析を行った。インアウト抗体は、免疫組織化学(immunohistochemistry:IHC)を用いてスクリーニングすることにより同定した。IHCを用いることによって、エンドシアリンを発現している内皮細胞(endothelial cells:ECs)の免疫組織化学による前記細胞表面上で発現したエンドシアリンに結合可能な抗体が検出された。前記抗エンドシアリンまたは正常IgG抗体は、ECs濃度(0.5ug/mLおよび2.5μg/mL)に対して適用された。Phosphate−リン酸緩衝食塩水[PBS(0.15M NaCl,pH7.2)]+1%ウシ血清アルブミンを第1抗体に対する希釈液として使用した。Cells細胞はスライドに播種して培養し、Tissue−Tek(商標)OCT培地中で固定した。スライドを−70℃以下で染色するまで保存した。染色直前、スライドを10%中性緩衝ホルマリン中に10秒間固定した。
免疫エフェクター活性は、エンドシアリン発現Lu細胞株にて標準的な抗体依存性細胞傷害(antibody−dependent cellular cytotoxicity:ADCC)分析により評価した。簡潔に述べると、OVCAR−3標的細胞を完全成長培地(10% FBS、2mM L−グルタミン含有RPMI−1640)中、平底96ウェルマイクロプレートに播種した。翌日、前記完全培地を100ulのCHO−CD無血清培地(Sigma)と交換し、抗体含有ならし培地50ulを標的細胞に追加し、37℃で20分間インキュベートした。その後、2×105のエフェクター細胞を含む100ulの無血清培地を加え、5%CO2、37℃で5〜6時間インキュベートした。エフェクター細胞はヒト末梢血単核球(peripheral blood mononuclear cells:PBMCs)から誘導し、健常ドナーから単離した(Interstate Blood Bankより購入)。ADCCにて使用する前に、PBMCsを約10ng/mlのヒト組み換え型インターロイキン2(R&D Systems)を含む完全RPMI中に2.5×106/mlで播種し、37℃、5% CO2にて3日間、PBMCsを活性化した。次に、活性化PBMCsをエフェクター細胞:標的細胞比を5:1としてOVCAR−3細胞に追加し、この培地を37℃、5%CO2にて5〜6時間インキュベートした。各ウェルから上清を回収し、ELISAプレートに移し、以下のとおりADCCを分析行った。ADCCは乳酸脱水素酵素(lactase dehydrogenase:LDH)、標準分析においてADCCの測定に使用される内因性酵素の放出によってモニターした。LDHは、100μlのLDH基質(Roche)を上清に添加し、周囲温度で10分間インキュベートすることによってモニターし、LDHによって変換された化学物質は分光光度法でOD490にて検出可能であった。LDH活性は、溶解標的細胞から放出される前記LDH酵素の量と比例する。490nmの吸光度(OD490)は分光光度法で得られる。2%トリトンXを「最大値(max)」の陽性対照としてエフェクター細胞単独に追加し、抗体は加えてないがPBMCを伴った標的細胞は「自然値(spontaneous)」としての陰性対照とした。LDH値を取得し、以下の式により細胞傷害性の割合を決定した。(サンプル値−自然値)/(最大値−自然値)×100%(式中、「自然値」=エフェクター細胞不在下での標的細胞の溶解、「最大値」=2%トリトン混在下での標的細胞の溶解)。100ng/mlの正常ヒトIgG1抗体を用い、非特異的細胞傷害性をモニターする。前記%細胞傷害性を各ウェル/クローンの抗体濃度で割って得られた比(つまり、比=50(%)/100(ng/ml)=0.5)を、エフェクター機能が高いと考えられるリードクローンを選択する基準として設定する。
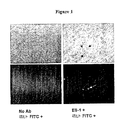
ES−1はエンドシアリン発現細胞に結合すると内部移行する。この所見は、Hum−ZAP分析を用いた図3に示した。第2の免疫毒素は、2次抗体とリボソーム不活化タンパク質サポリンの複合体である。試験している1次抗体が内部移行すると、前記サポリンは前記2次抗体と結合して前記細胞に運ばれる内部移行したサポリンがそのIgG複合体から一旦分離すると、タンパク質合成が阻害され、最終的に細胞死が引き起こされる。Hum−ZAP(Advanced Targeting Systems、cat# IT−22)は、ヒトモノクローナル抗体を認識するアフィニティー精製したヤギ抗ヒトIgG(分子量210kDa)の2次化学的複合体である。対照分子のヤギIgG−SAP(Advanced Targeting Systems cat#IT−19)は、正常なヤギIgGとサポリンの複合体である。簡潔に述べると、10%FCS、2.0mMグルタミン、1.0mMピルビン酸ナトリウム、および0.1mM MEM非必須アミノ酸を含む80ulのRPMI 1640中の平底96ウェル組織培養プレートに、2500/ウェルで細胞を播種した。24時間後、10μlの1次抗体ES−1またはMORAb−A92を10μlのHum−ZAPまたはヤギIgG−SAPとともに添加し、総量を100ulにした。実験では抗体の滴定を行い、1次抗体および2次抗体を対照として含ませた。4日後、分光光度法により生存細胞数を読み取るPromega CellTiter(登録商標)細胞傷害性アッセイ(cat#G3581)を用いて、細胞の生存率を評価した。すべての検査は3回ずつ行った。データは処理および未処理ウェルを比較することにより評価し、結果は対照のパーセントとして表した。図3に示したように、サポリンに結合したES−1はエンドシアリンを過剰発現したLu細胞を死滅させたが、ES−1抗体単独と比較して(図示せず)、アイソタイプ対照抗体MORAb−A92は複合体毒素形態において細胞を死滅させたかった(四角)。対照としてエンドシアリンを発現しない細胞を使用し、ES−1は複合または非複合形態において毒性効果を有していないことが示された(図示せず)。これらのデータは、ES−1がエンドシアリン提示細胞に内部移行するという知見を支持するものである。
Claims (48)
- (a)エンドシアリンに特異的に結合し、さらに(b)選択的に免疫エフェクター活性を誘発するか、或いはエンドシアリン提示細胞に内部移行する抗体。
- 請求項1記載の抗体において、前記抗体は少なくとも約1×10−7Mの親和性でエンドシアリンに結合する。
- 請求項1記載の抗体において、前記抗体は少なくとも約1×10−8Mの親和性でエンドシアリンに結合する。
- 請求項1記載の抗体において、前記抗体は少なくとも約1×10−9Mの親和性でエンドシアリンに結合する。
- 請求項1記載の抗体において、前記抗体は少なくとも約1×10−10Mの親和性でエンドシアリンに結合する。
- 請求項1記載の抗体において、前記抗体はキメラ抗体である。
- 請求項6記載の抗体において、前記キメラ抗体はヒト−マウスキメラ抗体である。
- 請求項1記載の抗体において、前記抗体はヒト化抗体である。
- 請求項1記載の抗体において、前記抗体は完全ヒト抗体である。
- 請求項1記載の抗体において、抗体は化学治療物質に結合するものである。
- 請求項10記載の抗体において、前記化学治療物質は放射性核種である。
- 請求項1記載の抗体において、エンドシアリンは配列ID番号2のアミノ酸配列を有するものである。
- 請求項1記載の抗体において、エンドシアリンは配列ID番号1のヌクレオチド配列によってコードされるものである。
- 請求項1記載の抗体において、前記免疫エフェクター活性は抗体依存性細胞傷害作用である。
- 請求項1記載の抗体の重鎖をコードするポリヌクレオチド。
- 請求項1記載の抗体の軽鎖をコードするポリヌクレオチド。
- 請求項1記載の抗体の重鎖および軽鎖をコードするポリヌクレオチド。
- 請求項1記載の抗体を有する薬学的組成物。
- 請求項18記載の薬学的組成物において、前記抗体は化学治療物質に結合するものである。
- 請求項19記載の薬学的組成物において、前記化学治療物質は放射性核種である。
- 請求項1記載の抗体の重鎖をコードするポリヌクレオチドを有するベクター。
- 請求項1記載の抗体の軽鎖をコードするポリヌクレオチドを有するベクター。
- 請求項1記載の抗体の重鎖と請求項1記載の抗体の軽鎖とをコードするポリヌクレオチドを有するベクター。
- 請求項1記載の抗体の重鎖をコードするポリヌクレオチドと、請求項1記載の抗体の軽鎖をコードするポリヌクレオチドとを有する発現細胞。
- 請求項23記載のベクターを有する発現細胞。
- 請求項25記載の発現細胞において、前記細胞は哺乳類細胞である。
- 請求項24記載の発現細胞において、前記細胞は哺乳類細胞である。
- 請求項1記載の抗体を産生する細胞。
- 請求項28記載の細胞において、前記細胞はハイブリドーマである。
- エンドシアリンに特異的に結合するインアウト抗体を作製する方法であって、
請求項28記載の細胞を培養する工程と、
成長培地から前記抗体を回収する工程と
を有する方法。 - エンドシアリン陽性細胞の成長を阻害する方法であって、
前記細胞を有する対象にインアウト抗エンドシアリン抗体を投与する工程を有する、方法。 - 請求項31記載の方法において、前記インアウト抗FRA抗体は生体分子に結合されるものである。
- 請求項31記載の方法において、前記エンドシアリン陽性細胞は異型細胞である。
- 請求項31記載の方法において、エンドシアニリン陽性細胞は血管神経細胞である。
- 請求項31記載の方法において、前記対象はヒトである。
- 請求項31記載の方法において、前記抗体は化学治療物質と結合されるものである。
- 請求項36記載の方法において、前記化学治療物質は放射性核種である。
- 請求項31記載の方法において、この方法は、さらに、
細胞傷害性物質を前記対象に投与する工程を有するものである。 - 請求項31記載の方法において、この方法は、さらに、
細胞増殖抑制物質を前記対象に投与する工程を有するものである。 - 請求項31記載の方法において、この方法は、さらに、
化学治療物質を前記対象に投与する工程を有するものである。 - 請求項31記載の方法において、前記抗体は非複合型抗体として投与されるものである。
- 請求項31記載の方法において、前記抗体は非複合型抗体と化学治療物質に結合した抗体との混合物として投与されるものである。
- キットであって、インアウト抗エンドシアリン抗体と、対象においてエンドシアリン陽性細胞の増殖を阻害する方法において前記キットを使用するための使用説明書とを有する、キット。
- 請求項43記載のキットであって、このキットは、さらに、
少なくとも1つの化学治療物質を有するものである。 - 請求項43記載のキットにおいて、このキットは、さらに、
少なくとも1つの診断薬を有するものである。 - 請求項43記載のキットにおいて、このキットは、さらに、
前記抗体を前記対象に投与する方法と使用説明書を有するものである。 - キットであって、インアウトエンドシアリン抗体と、インビトロまたはインビボでエンドシアリン提示細胞の有無を特定する方法において、前記キットを使用するための使用説明書とを有するキット。
- 請求項47のキットにおいて、このキットは、さらに、
少なくとも1つの診断薬を有するものである。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US67434405P | 2005-04-22 | 2005-04-22 | |
| PCT/US2006/015724 WO2006116451A2 (en) | 2005-04-22 | 2006-04-24 | Antibodies with immune effector activity and that internalize in endosialin-positive cells |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011290448A Division JP2012100676A (ja) | 2005-04-22 | 2011-12-29 | 免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008538700A true JP2008538700A (ja) | 2008-11-06 |
| JP2008538700A5 JP2008538700A5 (ja) | 2009-07-02 |
Family
ID=37215438
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008508001A Pending JP2008538700A (ja) | 2005-04-22 | 2006-04-24 | 免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 |
| JP2011290448A Pending JP2012100676A (ja) | 2005-04-22 | 2011-12-29 | 免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011290448A Pending JP2012100676A (ja) | 2005-04-22 | 2011-12-29 | 免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 |
Country Status (6)
| Country | Link |
|---|---|
| US (3) | US7615372B2 (ja) |
| EP (1) | EP1871809A2 (ja) |
| JP (2) | JP2008538700A (ja) |
| AU (1) | AU2006241235B2 (ja) |
| CA (1) | CA2607455A1 (ja) |
| WO (1) | WO2006116451A2 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2534077A1 (en) * | 2003-07-29 | 2005-02-10 | Morphotek Inc. | Antibodies and methods for generating genetically altered antibodies with enhanced effector function |
| AU2005311660B2 (en) * | 2004-12-03 | 2011-07-07 | Morphotek, Inc. | Use of endosialin binding proteins to isolate endosialin positive cells |
| AU2006241235B2 (en) | 2005-04-22 | 2012-04-05 | Eisai, Inc. | Antibodies with immune effector activity and that internalize in endosialin-positive cells |
| SI2137217T1 (sl) | 2007-04-05 | 2014-07-31 | Morphotek, Inc. | Postopki za inhibiranje vezave endosialina na ligande |
| US9290556B2 (en) * | 2008-09-29 | 2016-03-22 | The Trustees Of The University Of Pennsylvania | Tumor vascular marker-targeted vaccines |
| US20100260769A1 (en) * | 2009-04-09 | 2010-10-14 | Morphotek, Inc. | Endosialin binding molecules |
| JP2013543379A (ja) | 2010-09-29 | 2013-12-05 | モルフォテック, インコーポレイテッド | 操作されたヒトエンドシアリン発現齧歯動物 |
| NL2007179C2 (en) | 2011-07-26 | 2013-01-29 | Stichting Katholieke Universiteit | Chitosan-based hydrogels containing enzyme alkaline phosphatase. |
| US20160015750A1 (en) | 2013-03-09 | 2016-01-21 | Baylor College Of Medicine | Vascular-targeted t-cell therapy |
| GB201702926D0 (en) * | 2017-02-23 | 2017-04-12 | Univ Birmingham | Modulators |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004078942A2 (en) * | 2003-03-04 | 2004-09-16 | Kirin Beer Kabushiki Kaisha | Endothelial cell specific antibodies and uses thereof |
Family Cites Families (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| IL162181A (en) | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| US5530101A (en) * | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5789650A (en) * | 1990-08-29 | 1998-08-04 | Genpharm International, Inc. | Transgenic non-human animals for producing heterologous antibodies |
| US5965132A (en) | 1992-03-05 | 1999-10-12 | Board Of Regents, The University Of Texas System | Methods and compositions for targeting the vasculature of solid tumors |
| US5342757A (en) | 1992-11-13 | 1994-08-30 | Ludwig Institute For Cancer Research | Monoclonal antibodies which specifically binds to endosialin, a 165 Kd glycoprotein found on tumor vascular endothelium, and uses thereof |
| ATE244888T1 (de) * | 1993-02-05 | 2003-07-15 | Epigen Inc | Humanes carcinoma-antigen (hca), hca antikörper, hca immunoassays, aufzeichnungsmethoden und therapy |
| DE4335025A1 (de) * | 1993-10-14 | 1995-04-20 | Boehringer Ingelheim Int | Endosomolytisch wirksame Partikel |
| WO1995024483A1 (en) | 1994-03-08 | 1995-09-14 | Scotgen Biopharmaceuticals, Inc. | Recombinant humanized anti-fb5 antibodies |
| DE19541844C1 (de) * | 1995-11-09 | 1997-07-24 | Gsf Forschungszentrum Umwelt | Verfahren zur Herstellung von menschlichen Antikörpern und deren Verwendung |
| US6146894A (en) * | 1998-04-14 | 2000-11-14 | The Johns Hopkins University | Method for generating hypermutable organisms |
| CA2355337A1 (en) | 1998-09-09 | 2000-03-16 | U.S. Army Institute Of Surgical Research | Method for monitoring arterial oxygen saturation |
| EP1268855A2 (en) | 2000-03-15 | 2003-01-02 | Epigenomics AG | Diagnosis of diseases associated with tumor suppressor genes and oncogenes |
| AU2001283062A1 (en) | 2000-08-02 | 2002-02-13 | The Johns Hopkins University | Endothelial cell expression patterns |
| JP5036119B2 (ja) | 2001-01-15 | 2012-09-26 | モーフオテク・インコーポレーテツド | ミスマッチ修復の化学阻害剤 |
| US20040043928A1 (en) | 2001-08-02 | 2004-03-04 | Ramesh Kekuda | Therapeutic polypeptides, nucleic acids encoding same, and methods of use |
| US20030124579A1 (en) | 2001-09-05 | 2003-07-03 | Eos Biotechnology, Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| US20040014058A1 (en) | 2001-10-05 | 2004-01-22 | Alsobrook John P. | Novel human proteins, polynucleotides encoding them and methods of using the same |
| EP1576131A4 (en) | 2002-08-15 | 2008-08-13 | Genzyme Corp | EXPRESSION PATTERN IN BRAIN DENTHELIC CELLS |
| AU2003298786A1 (en) | 2002-11-26 | 2004-06-18 | Protein Design Labs, Inc. | Methods of detecting soft tissue sarcoma, compositions and methods of screening for soft tissue sarcoma modulators |
| US6905082B1 (en) * | 2003-12-05 | 2005-06-14 | Sheng Li Wu | Sprayer device having buffering structure |
| WO2005086713A2 (en) | 2004-03-04 | 2005-09-22 | Kirin Brewery Co., Ltd. | Role of human endothelial precursor cells and vascular pericytes tumor in angiogenesis |
| WO2006017759A2 (en) * | 2004-08-05 | 2006-02-16 | Kirin Brewery Co., Ltd. | Tumor endothelial marker-1 (tem1) binding antibodies and uses thereof |
| WO2006029045A2 (en) | 2004-09-03 | 2006-03-16 | Kirin Brewery Co., Ltd. | Endothelial cell specific antibodies and uses thereof |
| DE602005025659D1 (ja) | 2004-09-23 | 2011-02-10 | Guerbet Sa | |
| AU2005311660B2 (en) * | 2004-12-03 | 2011-07-07 | Morphotek, Inc. | Use of endosialin binding proteins to isolate endosialin positive cells |
| US7998695B2 (en) | 2005-02-10 | 2011-08-16 | Oncotherapy Science, Inc. | Method of diagnosing bladder cancer |
| AU2006241235B2 (en) | 2005-04-22 | 2012-04-05 | Eisai, Inc. | Antibodies with immune effector activity and that internalize in endosialin-positive cells |
| DE102005050933A1 (de) | 2005-10-21 | 2007-04-26 | Justus-Liebig-Universität Giessen | Erfindung betreffend Expressionsprofile zur Vorhersage von septischen Zuständen |
| US7908090B2 (en) | 2005-11-30 | 2011-03-15 | The Board Of Trustees Of The Leland Stanford Junior University | Signatures for human aging |
| WO2007111733A2 (en) | 2005-12-16 | 2007-10-04 | Genentech, Inc. | Method for diagnosing, prognosing and treating glioma |
| WO2008084331A2 (en) | 2006-06-21 | 2008-07-17 | Hopitaux Universitaires De Geneve | Biomarkers for renal disorders |
| US20090239223A1 (en) | 2006-07-13 | 2009-09-24 | Siemens Healthcare Diagnostics Inc. | Prediction of Breast Cancer Response to Taxane-Based Chemotherapy |
| EP2049713A4 (en) | 2006-07-21 | 2010-06-16 | Univ Alberta | TISSUE REJECTION |
| WO2008021288A2 (en) | 2006-08-11 | 2008-02-21 | Johns Hopkins University | Consensus coding sequences of human breast and colorectal cancers |
| US20080300170A1 (en) | 2006-09-01 | 2008-12-04 | Cohava Gelber | Compositions and methods for diagnosis and treatment for type 2 diabetes |
| WO2008063479A2 (en) | 2006-11-17 | 2008-05-29 | Fred Hutchinson Cancer Research Center | Pancreatic cancer biomarkers |
| US20110119776A1 (en) | 2007-02-05 | 2011-05-19 | Wong Kwok-Kin | Methods of diagnosing and prognosing lung cancer |
| WO2008101118A2 (en) | 2007-02-14 | 2008-08-21 | The Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services | A gene expression signature identifying pro-angiogenic genes in ovarian tumor endothelial cell isolates |
| SI2137217T1 (sl) | 2007-04-05 | 2014-07-31 | Morphotek, Inc. | Postopki za inhibiranje vezave endosialina na ligande |
| EP1986010A1 (en) | 2007-04-05 | 2008-10-29 | Vereniging voor christelijk hoger onderwijs, wetenschappelijk onderzoek en patiëntenzorg | Methods and tools for discriminating colorectal adenomas and adenocarcinomas |
| EP2696203A3 (en) | 2007-08-16 | 2014-05-28 | The Royal Institution for the Advancement of Learning/McGill University | Tumor cell-derived microvesicles |
| ES2936256T3 (es) | 2008-02-01 | 2023-03-15 | Massachusetts Gen Hospital | Uso de microvesículas en el diagnóstico, y pronóstico de enfermedades y afecciones médicas |
| CA2715774A1 (en) | 2008-02-19 | 2009-08-27 | Oncomethylome Sciences Sa | Detection and prognosis of lung cancer |
| WO2009120877A2 (en) | 2008-03-26 | 2009-10-01 | The Johns Hopkins University | Microrna-based diagnostic testing and therapies for inflammatory bowel disease and related diseases |
| US20100092470A1 (en) | 2008-09-22 | 2010-04-15 | Icb International, Inc. | Antibodies, analogs and uses thereof |
| US20100136584A1 (en) | 2008-09-22 | 2010-06-03 | Icb International, Inc. | Methods for using antibodies and analogs thereof |
| US20110256560A1 (en) | 2008-10-20 | 2011-10-20 | University Health Network | Methods and compositions for the detection of ovarian cancer |
| NZ606687A (en) | 2009-01-14 | 2014-08-29 | Us Health | Ratio based biomarkers and methods of use thereof |
| US20100260769A1 (en) | 2009-04-09 | 2010-10-14 | Morphotek, Inc. | Endosialin binding molecules |
-
2006
- 2006-04-24 AU AU2006241235A patent/AU2006241235B2/en active Active
- 2006-04-24 US US11/410,472 patent/US7615372B2/en active Active
- 2006-04-24 CA CA002607455A patent/CA2607455A1/en not_active Abandoned
- 2006-04-24 WO PCT/US2006/015724 patent/WO2006116451A2/en active Application Filing
- 2006-04-24 EP EP06769889A patent/EP1871809A2/en not_active Withdrawn
- 2006-04-24 JP JP2008508001A patent/JP2008538700A/ja active Pending
-
2009
- 2009-09-30 US US12/570,334 patent/US8389691B2/en active Active
-
2011
- 2011-12-29 JP JP2011290448A patent/JP2012100676A/ja active Pending
-
2012
- 2012-11-26 US US13/685,231 patent/US8524237B2/en active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004078942A2 (en) * | 2003-03-04 | 2004-09-16 | Kirin Beer Kabushiki Kaisha | Endothelial cell specific antibodies and uses thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2006116451A2 (en) | 2006-11-02 |
| JP2012100676A (ja) | 2012-05-31 |
| AU2006241235B2 (en) | 2012-04-05 |
| US8524237B2 (en) | 2013-09-03 |
| AU2006241235A1 (en) | 2006-11-02 |
| US20060239911A1 (en) | 2006-10-26 |
| WO2006116451A3 (en) | 2007-04-12 |
| EP1871809A2 (en) | 2008-01-02 |
| US7615372B2 (en) | 2009-11-10 |
| US8389691B2 (en) | 2013-03-05 |
| CA2607455A1 (en) | 2006-11-02 |
| US20130078242A1 (en) | 2013-03-28 |
| US20100021454A1 (en) | 2010-01-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5788443B2 (ja) | 抗メソテリン抗体 | |
| US10253106B2 (en) | Antibodies with immune effector activity and that internalize in folate receptor alpha-positive cells | |
| JP2012100676A (ja) | 免疫エフェクター活性を有するエンドシアリン細胞に内部移行する抗体 | |
| AU2012254877B2 (en) | Anti-mesothelin antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090423 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090423 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20090609 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20110520 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110830 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111128 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111205 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111229 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120404 |