JP2008522632A - 骨再構築のプロセスに関与するポリヌクレオチド及びポリペプチド配列 - Google Patents
骨再構築のプロセスに関与するポリヌクレオチド及びポリペプチド配列 Download PDFInfo
- Publication number
- JP2008522632A JP2008522632A JP2007545800A JP2007545800A JP2008522632A JP 2008522632 A JP2008522632 A JP 2008522632A JP 2007545800 A JP2007545800 A JP 2007545800A JP 2007545800 A JP2007545800 A JP 2007545800A JP 2008522632 A JP2008522632 A JP 2008522632A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- polypeptide
- polynucleotide
- sequence
- nos
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6887—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids from muscle, cartilage or connective tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/12—Drugs for disorders of the metabolism for electrolyte homeostasis
- A61P3/14—Drugs for disorders of the metabolism for electrolyte homeostasis for calcium homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/14—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4
- A61P5/16—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4 for decreasing, blocking or antagonising the activity of the thyroid hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/18—Drugs for disorders of the endocrine system of the parathyroid hormones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/51—Bone morphogenetic factor; Osteogenins; Osteogenic factor; Bone-inducing factor
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
Abstract
Description
a)転写プロモーター;
b)(オープンリーディングフレームを含み得る)ポリヌクレオチドセグメント;及び
c)転写ターミネーター;
を含んで良い。
本発明によって得られるポリヌクレオチドを使用して、発現産物、例えばNSEQ由来のまたはNSEQと相同的なmRNA、相補的DNA(cDNA)、及びタンパク質を検出及び単離できる。一実施態様では、本発明のNSEQと相同的なmRNAの発現を、例えばハイブリダイゼーション分析、逆転写、及びin vitro核酸増幅法によって検出できる。このような方法によって、種々の組織型または異なる発生段階におけるmRNAを検出できる。前記組織特異的または発生段階に特異的な形式で発現される対象の核酸は、組織特異的マーカーとして、あるいは特定の病状を定義し得る細胞または組織のサンプルの発生段階を定義するのに有用である。当業者は、前記NSEQをこれらの目的に容易に適合させ得る。
生物学的な活性があるポリペプチドを発現させるために、NSEQまたはその誘導体を発現ベクター、すなわち特定の宿主中の挿入されたコード配列の転写及び翻訳制御用のエレメントを含むベクター中に挿入して良い。これらのエレメントには、エンハンサー、構成的及び誘導性プロモーター等の制御配列、並びに5'及び3'非翻訳領域等が含まれる。当業者に公知の方法を使用して、このような発現ベクターを構築できる。これらの方法には、in vitro組換えDNA技術、合成技術、及びin vivoでの遺伝的組換えが含まれる。
a)本明細書に記載するポリペプチドの作用を阻害するその能力を測定しようと試みる、濃度が増大する少なくとも1つの化合物を含む培養培地中で試験細胞を培養する工程であって、前記試験細胞は、本明細書に記載のポリヌクレオチド配列を、野生型ポリヌクレオチドと比較して改善されたトランス活性化転写活性を有し、且つレポーター遺伝子と作用上連結した応答エレメントを含む形態で含み得る工程;及びその後、
b)前記培養培地中の可能性のあるアンタゴニスト化合物の濃度の関数として、前記レポーター遺伝子の産物の発現レベルを細胞において調べ、それによって本明細書に記載のポリヌクレオチド配列によってコードされるポリペプチドの活性を阻害する、可能性のあるアンタゴニスト化合物の能力を示す工程;
を含んで良い。
a)本明細書に記載のポリヌクレオチド配列によってコードされるポリペプチドの作用を促進するその能力を測定しようと試みる、濃度が増大する少なくとも1つの化合物を含む培養培地中で試験細胞を培養する工程であって、前記試験細胞は、本明細書に記載のポリヌクレオチド配列を、野生型ポリヌクレオチドと比較して改善されたトランス活性化転写活性を有し、且つレポーター遺伝子と作用上連結した応答エレメントを含む形態で含み得る工程;及びその後、
b)前記培養培地中の可能性のあるアゴニスト化合物の濃度の関数として、前記レポーター遺伝子の産物の発現レベルを細胞において調べ、それによって本明細書に記載のポリヌクレオチド配列によってコードされるポリペプチドの活性を促進する、可能性のあるアゴニスト化合物の能力を示す工程;
を含んで良い。
当業者は、NSEQを診断目的で使用して、当該遺伝子の非存在、存在、または変化した発現(すなわち、正常と比較して増大または低下した発現)を測定することができることを容易に理解するはずである。当該ポリヌクレオチドは少なくとも10ヌクレオチド長または少なくとも12ヌクレオチド長、あるいは少なくとも15ヌクレオチド長、任意の所望の長さまでであって良く、相補的RNA及びDNA分子、分枝した核酸、及び/またはペプチド核酸(PNA)を含んで良い。ある代替型において、前記ポリヌクレオチドを使用して、NSEQの発現が疾患と関係あるサンプル中の遺伝子発現を検出及び定量化できる。他の代替型において、NSEQを使用して、疾患と関係ある遺伝的多型を検出できる。これらの多型は転写産物cDNAにおいて検出できる。
当業者は、前述の発現系及びアッセイを使用して、動物試験、臨床試験における特定の療法治療措置の有効性を評価すること、または個々の被験者の治療をモニターすることができることを容易に理解するはずである。疾患の存在が確定次第、治療プロトコールが開始され、ハイブリダイゼーションまたは増幅アッセイが通常の原則に基づいて繰り返され、患者中の発現のレベルが、健康な被験者中で観察されるレベルに近づき始めているかどうか測定することができる。連続アッセイから得た結果を使用して、数日から数年に及ぶ期間の治療の有効性を示すことができる。
a)適量の所望のポリペプチドまたはそのポリペプチド断片で哺乳動物(例えば、マウス、ヒトIgを産生し得るトランスジェニック哺乳動物等)を免疫化する工程;
b)前記哺乳動物から血清を回収する工程;及び
c)前記哺乳動物の血清から前記ポリペプチド特異的抗体を単離する工程;
を含んで良い。
a)適量の所望のポリペプチド、そのポリペプチド断片または類似体で哺乳動物(例えば、マウス、ヒトIgを産生し得るトランスジェニック哺乳動物等)を免疫化する工程;
b)(a)から得た前記免疫化された動物からリンパ様細胞を得る工程;
c)前記リンパ様細胞と不死化細胞を融合させてハイブリッド細胞を作製する工程;及び
d)前記ポリペプチド、そのポリペプチド断片または類似体と特異的に結合する抗体を産生するハイブリッド細胞を選択する工程;
を含んで良い。
a)ファージまたはリボソーム上で抗体のライブラリーを合成する工程;
b)本明細書に記載のポリペプチドまたはポリペプチド断片を含む組成物と前記ファージまたはリボソームを接触させることによって、サンプルに対してライブラリーを選別する工程;
c)前記ポリペプチドまたはポリペプチド断片と結合するファージを単離する工程;及び
d)前記ファージまたはリボソームから抗体を得る工程;
を含んで良い。
a)宿主哺乳動物から抗体の産生を担う細胞を抽出する工程;
b)(a)の細胞からRNAを単離する工程;
c)mRNAを逆転写してcDNAを産生する工程;、
d)(抗体特異的)プライマーを使用することによってcDNAを増幅させる工程;及び
e)抗体がファージまたはリボソーム上で発現されるように、ファージディスプレイベクターまたはリボソームディスプレイカセット中に(d)のcDNAを挿入する工程;
によって調製され得るライブラリー(例えば、バクテリオファージライブラリー)から得られて良い。
a)本明細書に記載の1つ以上の抗体;及び
b)レポーター基を含み得る検出用試薬;
を含んで良い。
本発明は最終的に、研究上、生物学的、臨床上、及び療法目的で、NSEQ、それらのオープンリーディングフレーム、あるいはNSEQのポリヌクレオチドまたはそのオープンリーディングフレームによってコードされるポリペプチド、またはその一部分、それらのバリアント、類似体、及び誘導体を利用する生成物、組成物、プロセス、及び方法を提供する。例えば、スプライスバリアント、突然変異体、及び多型を同定するために。
a)分化破骨細胞及び未分化破骨前駆体細胞由来の全メッセンジャーRNAを別々に提供する工程であって、前記全メッセンジャーRNAは、例えば、少なくとも1つの内在的に差異的に発現する配列を含んでよい工程;
b)分化破骨細胞の各メッセンジャーRNA由来の一本鎖cDNA(の例えば1つのコピー)を作製し、且つ前記一本鎖cDNAの3'末端を、RNAポリメラーゼプロモーター配列及び第一の配列タグで(例えば無作為に)タグ化する工程;
c)未分化破骨前駆体細胞の各メッセンジャーRNA由来の一本鎖cDNA(の例えば1つのコピー)を作製し、且つ前記一本鎖cDNAの3'末端を、RNAポリメラーゼプロモーター配列及び第二の配列タグで(例えば無作為に)タグ化する工程;
d)b)及びc)のそれぞれに由来する部分的または完全な二本鎖5'-タグ-DNAを別々に作製する工程であって、前記二本鎖5'-タグ-DNAは、従って、二本鎖RNAポリメラーゼプロモーター、第一または第二の配列タグ及び内在的に発現される配列を5'-3'方向に含んで良い工程;
e)d)のそれぞれに由来する第一及び第二のタグ化センスRNAを、(タグ化に使用する前記プロモーターに基づいて選択されて良い)RNAポリメラーゼ酵素を用いて別々に線形的に増幅させる工程;
f)e)の1つに由来する一本鎖の相補的な第一または第二のタグ化DNAを作製する工程;
g)f)の一本鎖の相補的な第一または第二のタグ化DNAを、e)の他の線形的に増幅させたセンスRNAとハイブリダイズさせる工程;
h)前記第一または第二の配列タグの助力により(例えば、PCRまたはハイブリダイゼーションによって)ハイブリダイズされていないRNAを回収する工程;並びに
i)ハイブリダイズされていないRNAのヌクレオチド配列を同定(決定)する工程;
を含んで良い。
a)配列番号1−56、配列番号83、配列番号84、または配列番号87のいずれか1つ;
b)配列番号1−56、配列番号83、配列番号84、または配列番号87のいずれか1つのオープンリーディングフレーム;
c)a)またはb)と実質的に同一である配列を含み得るポリヌクレオチド;及び
d)a)からc)のいずれか1つの断片;
にある、またはこれを含み得るポリヌクレオチドからなる群から選択されて良い。
a)配列番号1−56、配列番号83、配列番号86、または配列番号87のいずれか1つを含み得るポリヌクレオチド;
b)配列番号1−56、配列番号83、配列番号86、または配列番号87のいずれか1つのオープンリーディングフレームを含み得るポリヌクレオチド;
c)a)またはb)と実質的に同一である(例えば、全配列または配列の一部分が約50-100%、または約60-100%、または約70-100%、または約80-100%、または約85、90、95-100%同一である)配列を含み得るポリヌクレオチド;
d)a)またはb)と実質的に相補的である(例えば、全配列または配列の一部分が約50-100%、または約60-100%、または約70-100%、または約80-100%、または約85、90、95-100%相補的である)配列を含み得るポリヌクレオチド;
e)a)からd)のいずれか1つの断片;
f)上記にあるポリヌクレオチド;
からなる群から選択される1種を含んで良い。
a)配列番号1−56または83−89のいずれか1つを含むポリヌクレオチド;
b)配列番号1−56または83−89のいずれか1つのオープンリーディングフレームを含むポリヌクレオチド;及び
c)a)またはb)と実質的に同一であるポリヌクレオチド;
からなる群から選択されて良い。
a)配列番号1−5、8−56、または83−89のいずれか1つ;
b)配列番号1−5、8−56、または83−89のいずれか1つのオープンリーディングフレーム;及び
c)配列番号6または配列番号7のいずれか1つの核酸配列と相補的であって良い少なくとも10核酸の配列;
を含み得るポリヌクレオチドからなる群から選択されて良い。
a)配列番号6または配列番号7のいずれか1つ;
b)配列番号6または配列番号7のいずれか1つのオープンリーディングフレーム;及び
c)配列番号1−5、8−57、または83−89のいずれか1つの核酸配列と相補的である少なくとも10核酸の配列;
を含み得るポリヌクレオチドからなる群から選択されて良い。
a)配列番号1−57及び83−89のいずれか1つを含み得るポリヌクレオチド;
b)配列番号1−57及び83−89のいずれか1つのオープンリーディングフレームを含み得るポリヌクレオチド;
c)a)またはb)と実質的に同一である(例えば、全配列または配列の一部分が約50-100%、または約60-100%、または約70-100%、または約80-100%、または約85、90、95-100%同一である)配列を含み得るポリヌクレオチド;
d)a)またはb)と実質的に相補的である(例えば、全配列または配列の一部分が約50-100%、または約60-100%または約70-100%または約80-100%または約85、90、95-100%相補的である)配列を含み得るポリヌクレオチド;及び
e)a)〜d)のいずれか1つの断片;
からなる群から選択される少なくとも1種を含んで良い。
a)(例えば、破骨細胞の分化を阻害し得る)本明細書で定義した単離ポリヌクレオチド;及び
b)製薬上許容し得る担体;
を含んで良い。
a)(例えば、破骨細胞の分化を促進し得る)単離ポリヌクレオチド;及び
b)製薬上許容し得る担体;
を含んで良い。
a)配列番号1−57及び83−89のいずれか1つを含むポリヌクレオチド;
b)配列番号1−57及び83−89のいずれか1つのオープンリーディングフレームを含むポリヌクレオチド;
c)a)またはb)と実質的に同一である(例えば、全配列または配列の一部分が約50-100%、または約60-100%、または約70-100%、または約80-00%、または約85、90、95-100%同一である)配列を含むポリヌクレオチド;、
d)a)またはb)と実質的に相補的である(例えば、全配列または配列の一部分が約50-100%、または約60-100%、または約70-100%、または約80-100%、または約85、90、95-100%相補的である)配列を含むポリヌクレオチド;
e)a)からd)のいずれか1つの断片;及び
f)a)からd)のいずれか1つを含むライブラリー;
からなる群から選択されて良い少なくとも1つのポリヌクレオチドの使用に関する。
a)配列番号93−97または101−155のいずれか1つ;
b)a)のいずれか1つの生物学的な活性がある断片;及び
c)a)のいずれか1つの生物学的な活性がある類似体;
からなる群から選択される配列を含んで良い(またはそれにあって良い)。
a)配列番号98及び配列番号99のいずれか1つを含み得る、またはそれにあり得る配列;
b)a)のいずれか1つの生物学的な活性がある断片;
c)a)のいずれか1つの生物学的な活性がある類似体;
からなる群から選択される配列を含んで良い。
a)請求項40に記載の抗体;及び
b)製薬上許容し得る担体;
を含み得る組成物(例えば、医薬組成物)に関する。
(1)疎水性:ノルロイシン、メチオニン(Met)、アラニン(Ala)、バリン(Val)、ロイシン(Leu)、イソロイシン(Ile);
(2)中性親水性:システイン(Cys)、セリン(Ser)、スレオニン(Thr);
(3)酸性:アスパラギン酸(Asp)、グルタミン酸(Glu);
(4)塩基性:アスパラギン(Asn)、グルタミン(Gln)、ヒスチジン(His)、リシン(Lys)、アルギニン(Arg);
(5)鎖の配向に影響を与える残基:グリシン(Gly)、プロリン(Pro);及び
芳香族:トリプトファン(Trp)、チロシン(Tyr)、フェニルアラニン(Phe);
に分けられる。
本開示において言及された商業的に入手可能な試薬は、別に指示しない限り、供給元の使用説明書に従って使用された。本開示を通して、いくつかの開始材料を以下のように調製した。
RAW264.7(RAW)破骨細胞前駆体細胞株及びヒトCD34+前駆体は、破骨細胞形成のマウス及びヒトモデルとして当該技術分野で公知である。従って、これらのマウス及びヒト破骨細胞は、破骨細胞の機能に特定化された遺伝子を単離し、且つ特徴づけするための優れた材料源である。
破骨細胞に特有の差異的に発現する配列を発見する鍵は、本出願者が特許取得したSTAR技術(Subtractive Transcription-based Amplification of mRNA;米国特許第5,712,127号、Malek et al, January 27, 1998)の使用である。この方法では、完全に分化した破骨細胞から単離されたmRNAを用いて「テスターRNA」を調製し、これを、破骨細胞前駆体mRNAから調製した相補的一本鎖「ドライバーDNA」にハイブリダイズさせ、ハイブリダイズしなかった「テスターRNA」のみを回収し、「サブトラクションライブラリー(subtracted libraries)」と称されるクローン化cDNAライブラリーを作製するために使用する。従って、より優れた診断方法及び治療ストラテジーの開発のために重要な遺伝子標的の中に入ることが予想され、マイクロアレイハイブリダイゼーション分析によって見逃されることの多い、稀少且つ新規のmRNAを含む差異的に発現する配列が、前記「サブトラクションライブラリー」に多く含まれている。
RAW前駆体細胞及び対応する完全に分化した(5日目)破骨細胞を、前述のように調製した。標準的な方法(Quiagen社、Mississauga、ON)を用いることによって、細胞RNAの単離、次いで各々からのmRNAの精製を行った。Malekら(米国特許第5,712,127号)の教示に従い、各サンプルからの2μgのポリA+mRNAを用いて、テスター及びドライバー材料の調製に必要な非常に代表的な(>2×106CFU)cDNAライブラリーを、特殊化プラスミドベクター中に調製した。各々の場合において、3'ロッキングヌクレオチド(例えば、A、G、またはC)を有し、Not I認識部位を含むオリゴdT11プライマーを用いて、第一鎖cDNAを合成した。次に二本鎖cDNA合成のための製造元の方法に従って第二鎖cDNA合成を行い(Invitrogen社、Burlington、ON)、得られた二本鎖cDNAをAsc I認識部位を含むリンカー(New England Biolabs社、Pickering、ON)に結合させた。次いで、Asc I及びNot I制限酵素(New England Biolabs社、Pickering、ON)で前記二本鎖cDNAを消化し、Invitrogen社(Burlington、ON)製のcDNA分画化カラムを、製造元により指定されたように用いることによって、過剰リンカーから精製し、各々を、テスター及びドライバー材料それぞれの調製に用いられる特殊化プラスミドベクターp14(配列番号58)及びp17+(配列番号59)内に結合させる。その後、前記結合させたcDNAを、大腸菌DH10B内に形質転換し、所望のcDNAライブラリー(RAW264.7-前駆体-p14、RAW264.7-前駆体-p17+、RAW264.7-破骨細胞-p14、及びRAW264.7-破骨細胞-p17+)を得た。各cDNAライブラリーに対するプラスミドDNAプールを精製し、各々の2μg一定分量をNot I制限酵素によって線形化する。次いで、T7 RNAポリメラーゼ及びsp6 RNAポリメラーゼそれぞれで、Not Iで消化されたp14及びp17+プラスミドライブラリーのin vitro転写を実施した(Ambion社、Austin、TX)。
物を、RNase A及びRNase Hで処理して、RNAを除去し、フェノール抽出し、脱塩して使用した。
テスター1 −p14において、RAW264.7-破骨細胞-3';
テスター2 −p14において、RAW264.7-前駆体-3';
ドライバー1−p17において、RAW264.7-前駆体-3';
ドライバー2−p17において、RAW264.7-破骨細胞-3';
を調製した。
T04-22−pCATRMANにおいて、テスター1(破骨細胞)−ドライバー1(前駆体)(1ラウンド);
SL22−pCATRMANにおいて、テスター1(破骨細胞)−ドライバー1(前駆体)(2ラウンド);
SL22−p20において、テスター1(破骨細胞)−ドライバー1(前駆体)(2ラウンド);
SL27−pCATRMANにおいて、テスター2(前駆体)−ドライバー2(破骨細胞)(2ラウンド);
SL27-p20において、テスター2(前駆体)−ドライバー2(破骨細胞)(2ラウンド);
を調製した。
AO1:テスター1 RNA+ドライバー1 DNA+RNアーゼH(1ラウンド);
AO2:テスター1 RNA+ドライバー1 DNA+RNアーゼH(2ラウンド);
AP1:テスター2 RNA+ドライバー2 DNA+RNアーゼH(1ラウンド);
AP2:テスター2 RNA+ドライバー2 DNA+RNアーゼH(2ラウンド);
BO1:テスター1 RNA+ドライバー1 DNA−RNアーゼH(1ラウンド);
BO2:テスター1 RNA+ドライバー1 DNA−RNアーゼH(2ラウンド);
BP1:テスター2 RNA+ドライバー2 DNA−RNアーゼH(1ラウンド);
BP2:テスター2 RNA+ドライバー2 DNA−RNアーゼH(2ラウンド);
CO1:テスター1 RNA−ドライバー1 DNA+RNアーゼH(1ラウンド);
CO2:テスター1 RNA−ドライバー1 DNA+RNアーゼH(2ラウンド);
CP1:テスター2 RNA−ドライバー2 DNA+RNアーゼH(1ラウンド);
CP2:テスター2 RNA−ドライバー2 DNA+RNアーゼH(2ラウンド);
DP:テスター2 RNA
DO:テスター1 RNA
を含む。
GAPDH(前記参照)は、2ラウンド後に最も効率的にサブトラクションされたため(SL-22)、このライブラリーは差異的に発現する破骨細胞関連配列に対して最も濃縮されるであろうことが予想された。従って、TO4-22(576クローン)と比較して、より徹底的なDNA配列分析が、SL22に含まれるクローン(1536クローン)について実施された。
前記TO4-22及びSL22ライブラリーから注釈された配列を表すPCR単位複製配列を用いて、DNAマイクイロアレイを調製した。前節において調製した70μL中に含まれた精製PCR単位複製配列を凍結乾燥し、それぞれを、3×SSC及び0.1%サルコシル(sarkosyl)を含む20μLのスポッティング溶液中で再構成した。次いで、各単位複製配列の三重のDNAマイクロアレイを、CMT-GAP2スライド(Corning社、Corning、NY)及びGMS 417スポッター(Affymetrix社、Santa Clara、CA)を用いて調製した。
SL22及びTO4-22双方のライブラリーに関してF節で同定した差異的に発現する配列を、ナイロン膜ベースのマクロアレイに対するハイブリダイゼーションによって、破骨細胞特異性に関して試験した。前記マクロアレイは、5つの独立した実験のマウス前駆体及び破骨細胞からのRAMP増幅RNAを用いることによって調製し、種々の正常なマウス組織(肝臓、脳、胸腺、心臓、肺、精巣、卵巣、腎臓、及び胎仔)は商業的に購入した(Ambion社、Austin、TX)。これらのサンプルの多くに対して利用できるmRNAの量が限られていたため、RAMP方法論を用いることによってまずmRNAを増幅する必要があった。増幅した各RNAサンプルを、96ウェルのマイクロタイタープレートにおいて、3×SSC及び0.1%サルコシル中で最終濃度250ng/μLに再構成し、特殊化MULTI-PRINT(登録商標)装置(VP Scientific社、San Diego、CA)を用いてHybond N+ナイロン膜上に1μLをスポットし、風乾させ、UV交差結合させた。供給元(Amersham Bioscience社、Piscataway、NJ)により推奨されたランダムプライミング法を用いることによって、SL22及びTO4-22から選択された合計556の異なる配列をα-32P-dCTPで個々に放射標識し、プローブとして前記マクロアレイ上で用いた。当業者に公知の標準的操作に従って、ハイブリダイゼーション及び洗浄工程を実施した。
配列番号1によってコードされる候補タンパク質は、精巣特異的プロテアーゼまたはTsp50という名称を有する以前に同定された遺伝子である。当該マウスのポリヌクレオチドは、1317bpのオープンリーディングフレームを含み、439アミノ酸のポリペプチドをコードする。当該ヒトのポリヌクレオチドは、1155bpのオープンリーディングフレームを含み、385アミノ酸のポリペプチドをコードする。それは本来、ヒト乳癌細胞におけるゲノムDNAの低メチル化領域において発現するために記載され、クローン化された(Yuan et al., 1999)。一次アミノ酸配列の分析により、当該タンパク質を細胞膜に標的化すると推定されるアミノ末端シグナルペプチド、当該タンパク質を細胞膜に固定するカルボキシ末端膜貫通ドメイン、及びセリンプロテアーゼに相同性の予想される触媒ドメイン(Shan et al., 2002;Netzel-Arnett et al., 2003)の存在が示唆される。Tsp50の予想される触媒活性の性質及び正確な細胞局在は、まだ結論的に確立されていない。出願者は、Tsp50が主題となっている米国特許第6,617,434号(Duffy、2003年9月9日)及び米国特許第6,451,555号(Duffy、2002年9月17日)に注意を向けるよう読者に指示する。前記の全ての知見に関わらず、破骨細胞または骨再構築障害との機能的関連は、本開示前には記載されていない。
配列番号2によってコードされる候補タンパク質は、液胞(V-)ATPaseマルチサブユニット複合体のd2サブユニットをコードする以前同定された遺伝子である。前記d2サブユニットは膜を貫通していないが、膜貫通複合体の一部であり、膜貫通特性を含むより大型のサブユニットと直接相互作用する(Nishi and Forgac, 2002)。マウスのV-ATPase d2タンパク質をコードするcDNAが最近記載されたが、骨生理学におけるその機能はまだ確立されていない(Nishi et al., 2003)。破骨細胞または骨再構築障害との機能的関連は、本開示前には記載されていない。
配列番号3によってコードされる候補タンパク質は、軟骨関連タンパク質、Crtapをコードする以前同定された遺伝子である(Morello et al., 1999;Tonachini et al., 1999)。前記遺伝子は、本来ニワトリ胎仔からクローン化され、軟骨組織に局在している(Morello et al., 1999)。破骨細胞または骨再構築障害との機能的関連は、本開示前には記載されていない。
配列番号4によってコードされる候補タンパク質は、現在のデータベースに見られ、RIKEN Genome Exploration Research Groupの一部としてクローン化された(Kawai et al., 2001)。当該mRNAは予想されるオープンリーディングフレームを含むが、本開示前に、この配列に帰属された機能はない。
配列番号5によってコードされる候補タンパク質は、現在のデータベースに見られ、RIKEN Genome Exploration Research Groupの一部としてクローン化された(Strausberg et al., 2002)。当該mRNAは予想されるオープンリーディングフレームを含むが、本開示前に、この配列に帰属された機能はない。
配列番号6によってコードされる候補タンパク質は、現在のデータベースに見られ、RIKEN Genome Exploration Research Groupの一部としてクローン化された(Strausberg et al., 2002)。当該mRNAは予想されるオープンリーディングフレームを含むが、本開示前に、この配列に帰属された機能はない。
配列番号7によってコードされる候補タンパク質は、B細胞の活性化に対するリンカーをコードする以前同定された遺伝子である。当該遺伝子は胸腺細胞においてある役割を担うと報告されている(Janssen et al., 2003)。破骨細胞または骨再構築障害との機能的関連は、本開示前には記載されていない。
配列番号57によってコードされる候補タンパク質は、jun二量体化タンパク質2をコードする以前同定された遺伝子である。この遺伝子は、アンチセンス技術を用いることによって、破骨細胞形成に関与していることが示されている(Kawaida et al., 2003)。この例は、破骨細胞特異的遺伝子の同定における出願者のアプローチについての構想のさらなる証明として役立つ。
当該発現タンパク質の機能的試験を実施するために、完全長cDNA配列を得ることが必要であった。スプライスバリアントが組織特異的機能に関与していることが次第に示唆されているので、試験中の系のcDNAクローンを用いた研究が極めて必要となる。出願者はまた、スプライスバリアントが必ずしも関与していない可能性があると認識している。従って、バリアント及び特異性に関するそれらの可能性のある役割を同定するために、出願者のアプローチは、関連する完全長cDNA配列を破骨細胞から直接単離することである。
RNA干渉は、分解のためのmRNAを標的とすることにより、配列特異的な遺伝子発現の低下をともなう最近発見された遺伝子制御機構であり、本来は、植物において記載されたものであるが、原生動物及び無脊椎動物からより高等な真核生物まで、多くの動物界にわたって発見されている(Agrawal et al., 2003)。生理学的設定において、RNA干渉の機構は、細胞内で活性なダイサーと称されるRNase III様タンパク質によって切断される二本鎖RNA分子の存在によって誘発され、21〜23bpのsiRNAを放出する。前記siRNAは、相同性により生じる様式で、mRNAの存在下でRISC(RNA誘導サイレンシング複合体)と称されるRNA-タンパク質結合体へと複合体を形成し、mRNA発現の低下をもたらす分解を引き起こす(Agrawal et al., 2003)。
各ヌクレオチド配列の特徴づけに利用される個々のsiRNA発現カセット及び方法の設計及びサブクローニングを下記に記載する。ポリヌクレオチドの選択は、破骨細胞におけるそれらのRANKリガンド依存性上方制御、及び他の組織と比較した破骨細胞におけるそれらの発現の選択的性質に基づいて選択された(前記、F節及びG節を参照)。siRNA配列の設計は、当業者が自由に利用可能なウェブベースのソフトウェア(例えば、Qiagen社)を用いることによって実施された。これらの選択された配列、通常19量体は、ショートヘアピンRNA、すなわち、19ntのセンス配列、9ntのリンカー領域(ループ)、19ntのアンチセンス配列、次いでRNAポリメラーゼIIIの終止用5-6ポリT領域のための鋳型を形成する2つの相補的オリゴヌクレオチド中に含まれる。これらのオリゴヌクレオチドの末端に適切な制限部位を挿入して、転写開始点がhU6プロモーターの下流の正確な位置にくるように、当該挿入体の適切な位置とりを促進した。選択された各配列に対して、少なくとも2種の異なるsiRNA発現ベクターを構築し、RNA干渉の観察機会を増加させた。
<配列番号1>
RNA干渉に用いた配列は、ポリヌクレオチド配列番号1から得られたものであり、配列番号64、65、及び66を有する(もちろん、他の配列を用いても良い)。3種のsiRNA、pd2-hU6/0440.1、pd2-hU6/0440.2、及びpd2-hU6/0440.3をコードするプラスミドをトランスフェクトしたRAW細胞から得られた細胞株は、その後、それぞれRAW-0440.1、(配列番号64)、RAW-0440.2(配列番号65)、及びRAW-0440.3(配列番号66)と称され、集合的にRAW-0440と称される。さらに、正常な破骨細胞形成に対するポジティブコントロールとして、RAW細胞にsiRNAを含まない空ベクター(pd2-hU6)をトランスフェクトした。全細胞系の表現型分析を、図4Aに示す。図4Aのパネルaは、多核化破骨細胞の存在が観察されず、且つ未分化RAW細胞がTRAP染色されないRANKリガンド非存在下における、コントロール細胞株RAW-hU6を示している。RANKリガンドで処理した場合、大型の多核化したTRAP陽性の破骨細胞が正常な分化を示していることが観察される(パネルb)。RAW細胞中の配列番号1に特異的なsiRNAの存在により、これらの細胞がRANKリガンドの存在下で大型の成熟した破骨細胞を形成する能力が大きく低下した(パネルc-e)。1ウェル当りの破骨細胞数の減少に加えて、前記RAW-0440細胞は、より小型であり、多くはTRAP染色のわずかな減少を示した。より詳細な検査により、これらのより小型の破骨細胞が多核化しており、RAW-0440前駆体の正常な細胞融合を示唆していることを明らかになった。等量の3種全てのsiRNA発現ベクターをトランスフェクトした他のRAW細胞株RAW-0440混合体の分析により、先の表現型の観察結果が立証された。前と同様に、空ベクターをトランスフェクトしたコントロール細胞株は、TRAPに染色される大型の多核化破骨細胞を形成した(図4、パネルb)。パネルcに示されるように、RAW-0440混合体破骨細胞は多核化していたが、小型で、且つ数がより少なかった。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号2から得られたものであり、配列番号67、68、及び69を有する。3種のsiRNA、pd2-hU6/0179.1、pd2-hU6/0179.2、及びpd2-hU6/0179.3をコードするプラスミドをトランスフェクトしたRAW細胞から得られた細胞株は、本明細書で、それぞれ、RAW-0179.1(配列番号67)、RAW-0179.2(配列番号68)、及びRAW-0179.3(配列番号69)と称される。さらに、正常な破骨細胞形成に対するポジティブコントロールとして、RAW細胞に、任意のsiRNAを含まない空ベクター(pd2-hU6)をトランスフェクトした。全細胞系の表現型分析を、図6に示す。図6のパネルaは、多核化破骨細胞の存在が観察されず、且つ未分化RAW細胞がTRAP染色されないRANKリガンド非存在下における、コントロール細胞株RAW-hU6を示している。RANKリガンドで処理した場合、大型の多核化したTRAP陽性の破骨細胞が正常な分化を示していることが観察される(パネルb)。前記siRNAの2つ、すなわちRAW-0179.1及びRAW-0179.2によってコードされるものにより、RANKリガンドの存在下で大型の成熟した破骨細胞を形成するこれらの細胞の能力が著しく低下した(パネルc、d)。第三のsiRNA配列、RAW-0179.3は有効でなかった(図6、パネルeを参照)。1ウェル当りの破骨細胞数の減少に加えて、前記RAW-0179.1細胞及びRAW-0179.2細胞は、一般により小型であり、含有する核は少なかった。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号3から得られたものであり、配列番号70、71、及び72を有する。配列番号1及び2に対して本発明に記載のRNA干渉の使用を、配列番号3に適用した。得られた結果は同様であり、この遺伝子もRAW破骨細胞の適切な分化にとって必要であることを示している。この結果の一例を、図8に示す。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号4から得られたものであり、配列番号73及び74を有する。配列番号1及び2に対して本発明に記載のRNA干渉の使用を、配列番号4に適用した。得られた結果は同様であり、この遺伝子もRAW破骨細胞の適切な分化にとって必要であることを示している。この結果の一例を、図9に示す。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号5から得られたものであり、配列番号75及び76を有する。配列番号1及び2に対して本発明に記載のRNA干渉の使用を、配列番号5に適用した。得られた結果は同様であり、この遺伝子もRAW破骨細胞の適切な分化にとって必要であることを示している。この結果の一例を、図10に示す。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号6から得られたものであり、配列番号77及び78を有する。この配列に対して、以下の修正をしてRNA干渉に対する同じアプローチを適用した。siRNA発現プラスミド、pd2-hU6/1200.1及びpd2-hU6/1200.2を、等量用いた混合物としてトランスフェクトした。配列番号1に対して観察されたように、siRNA発現プラスミドをプールすることによって、個々のプラスミドトランスフェクション体から得られたものと同様の結果が生じる。従って、このトランスフェクションから得られた細胞株を、RAW-1200混合体と称した(図11を参照)。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号7から得られたものであり、配列番号79及び80を有する。配列番号1及び2に対して本発明に記載のRNA干渉の使用を、配列番号7に適用した。得られた結果(データは示していない)は、配列番号6の結果と同様であり、この遺伝子のノックダウンが破骨細胞分化の増加をもたらすことを示し、配列番号7がRAW細胞におけるこのプロセスの負の調節因子であることを示唆している。
RNA干渉に用いた配列は、ポリヌクレオチド配列番号57から得られたものであり、配列番号81及び82を有する。配列番号1及び2に対して本発明に記載のRNA干渉の使用を、配列番号57に適用した。得られた結果は同様であり、この遺伝子がRAW破骨細胞の適切な分化にとって必要であることを示している。この結果の一例を、図13に示す。
同定した破骨細胞特異的配列の機能性を、Osteologic(登録商標)(BD Bioscience社、Mississauga、ON)ディスク上に当該細胞を播種することによって探索し、それらの骨吸収活性を測定した。Osteologic(登録商標)ディスクは商業的に入手可能であり、合成リン酸カルシウム基質を含有し、骨分解のモデルとして当業者に公知である。
RAW-0440細胞株の機能が、配列番号1のノックダウンによって影響を受けたかどうかを判定するために、当該細胞を、Osteologic(登録商標)ディスク上で培養し、分化させた。各ディスク上に等しい数のRAW細胞を播種し、4日間、RANKリガンドで処理してから、固定し、リン酸カルシウム基質を染色する製造元の修正フォンコッサ法によって染色した。前記ディスク上の白色領域が破骨細胞の吸収を示す。図14Aに示されるように、コントロール細胞株のRAW-hU6は、当該ディスク上の吸収面積に大きな増加を生じなかった(パネルa)が、破骨細胞形成を誘導するRANKリガンドの処理によって、かなりの量の基質が破骨細胞により分解される結果となった(パネルb)。全ての3種のRAW-0440細胞株は、当該基質を分解する能力を減少させ、当該ディスクは広い面積の未吸収リン酸カルシウム基質を有した(パネルc-e)。これらの結果を図14Bに示す。RAW-0440.1、RAW-0440.2、及びRAW-0440.3細胞株からの破骨細胞に対する総吸収面積の値(ブラック画素%)は、それぞれ8.7%、45.9%、及び22.2%であった。これらの結果は、破骨細胞中の配列番号1遺伝子を標的とすることは、骨基質を吸収するそれらの能力を低下させる効果を有することを示している。
配列番号1に用いたアプローチを使用して、RAW-0179細胞株を分析した。図15に示されるように、当該破骨細胞は、基質を吸収する能力の低下を示した(図15)。当該ディスク上の残留物質の定量分析により、全吸収面積は、RAW-0179.1、RAW-0179.2、及びRAW-0179.3細胞株に対して、それぞれ36.1%、29.4%、及び51.2%であることが示された(図15B)。これらの結果は、破骨細胞中の配列番号2の遺伝子を標的とすることは、骨基質を吸収するそれらの能力を低下させる効果を有することを示している。
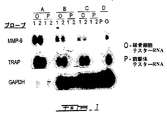
いくつかのマウス破骨細胞特異的遺伝子に対するヒトオルソログは、RT-PCR増幅用の遺伝子特異的プライマー、及びヒト破骨細胞のmRNAからの対応する二本鎖cDNAのクローニングを用いることによって単離され、それらの差異的発現パターンは、ヒトCD34+前駆体及び破骨細胞からのRNAを用いて測定された。また、それらの組織特異性は、Ambion社(Austin、TX)から購入された30種のヒト組織(副腎、乳房、空腸、気管、肝臓、胎盤、大動脈、脳、肺、副腎皮質、食道、大腸、卵巣、腎臓、前立腺、胸腺、骨格筋、大静脈、胃、小腸、心臓、輸卵管、脾臓、膀胱、頚部、膵臓、回腸、十二指腸、甲状腺、及び精巣)のRNAを用いて測定された。全てのRNAサンプルはRAMPを用いて増幅され、マクロ配列はG節に記載したようにに調製した。各ヒトオルソログcDNAを、供給元(Amersham社、Piscataway、NJ)により指定されたランダムプライミング法を用いてα-32P-dCTPで放射標識し、マクロアレイに存在するRNAに対するプローブとして使用した。ハイブリダイゼーション及び洗浄工程は、当該技術分野で公知の標準的方法に従って実施した。図16Aは、マクロアレイ上に表される種々の組織及び破骨細胞サンプル中の配列番号2及び配列番号4に対するヒトオルソログの差異的発現の例を示している。しかし、配列番号1の場合、当該マクロアレイ上のハイブリダイゼーションシグナルは、この配列の相対的に低い存在量のため検出できなかった。このように、ヒトTSP50に対する遺伝子特異的プライマーを用いた標準的RT-PCRを、その発現を測定するために、ヒト前駆体及び破骨細胞のサンプルについて実施した(図16B)。1.3kbのTSP50 PCRの単位複製配列は、ドナー1及びドナー4(図16B、それぞれレーン2及び4)の両方に対して、ヒト破骨細胞サンプル中に検出されたが、対応する前駆体サンプル(図16B、それぞれレーン1及び3)中には検出されなかった。1.3kbのPCRの単位複製配列は、TSP50として配列分析により確認された。これらの結果から、いくつかのマウスの選択された破骨細胞特異的配列のヒトオルソログは、ヒトCD34+由来破骨細胞において同様に上方制御され、また非常に特異的であることが明白である。従って、これらの結果は、ヒト破骨細胞形成に関与する破骨細胞特異的遺伝子を同定するための前記マウスRAW264.7モデルの使用が、有効なストラテジーであることを示唆している。
配列番号1(配列番号88)に対するヒトオルソログの生物学的重要性を検証するために、配列番号1に対してマウス破骨細胞モデルに見られる機能が、ヒト破骨細胞に保存されていることを示すことは重要であった。破骨細胞の分化に細胞株を使用し得るマウスモデルとは異なり、相当するモデルがヒトには存在しない。従って、検証試験は、別に記載されない限り、製造元(Invitrogen社、Burlington、ON)により記載された市販のレンチウイルスのショートヘアピン(sh)RNA送達システムを用いて、ヒト一次骨髄細胞において実施した。siRNA配列、5'-CTGCCTGATCTGGCGTGAT-3'(配列番号90)が、配列番号88を特異的に標的にするために使用され、当該コード配列は、組織内のヒト破骨細胞cDNAライブラリーからクローン化されたものである。
対応する内因性マウスタンパク質を欠失しているRAW264.7細胞からのマウス破骨細胞の分化における、配列番号88の機能を試験するための相補性アッセイを開発した。成熟破骨細胞に分化する能力を大きく低下させることを示した配列番号1に対するマウス特異的shRNA(RAW-AB0440si)を含むRAW264.7細胞株に、Ip200-hAB0440と称される配列番号88に対して完全コード配列を含む真核生物発現ベクターをトランスフェクトした。このIp200発現ベクター(配列番号91)は、市販のベクターのpd2-EGFP-N1(Clontech社、Mountain View、CA)から修飾し、NEO-KAN抗生物質カセットを、哺乳動物細胞における選択のためにハイグロマイシン耐性遺伝子に、且つ原核生物における増殖のためにアンピシリン耐性遺伝子で置換した。挿入されたヒト遺伝子配列の発現は、Ip200における強力なCMVプロモーターの制御下にある。およそ2.5×105RAW-0440si細胞/ウェルを6ウェルプレートに接種し、Fugene 6(Roche社、Laval、QC)を用いて1μgのIp200またはIp200-hAB0440のいずれかをトランスフェクトし、安定なトランスフェクション体を50μg/mLのハイグロマイシンの存在下で5日間選択した。2種のRAW264.7-044siの安定な細胞株を選択し、1種は配列番号88(Ip200-hAB0440)を発現し、もう一方の種はベクター(Ip200)のみを含有した。これら2種の細胞株の増殖後、各々4000細胞/ウェルを96プレートに接種し、処理しない、または100ng/mLのRANKリガンドで4日間処理した。当該細胞を固定し、成熟破骨細胞を可視化するためにTRAP発現に対して染色した。
配列番号88は、Tsp50と称される膜結合または分泌プロテアーゼをコードし得ることが文献に考慮されている。配列番号88に対するポリペプチドが実際に膜結合するか、または分泌されるかどうかを判定するために、配列番号88に対する全コード配列を含むプラスミド(pCMX-HA-hAB0440)を構築した。発現ベクターのpCMX-HA(配列番号92)は、HAエピトープ及びcDNA挿入物の発現のために強力なCMVプロモーターを含む。およそ2.5×105Cos-7細胞/ウェルを6ウェルプレートに接種し、Fugene 6(Roche社、Laval、QC)を用いて、1μgのpCMX-HA-hAB0440発現プラスミドを一過性にトランスフェクトする。いくつかのウェル中の細胞は処理しなかった(−)が、他の細胞は2μg/mLのツニカマイシン(T)で24時間、または0.5単位/mLのホスホイノシトールホスホリパーゼC(P)で1時間処理した。ツニカマイシンは、糖タンパク質合成の第一工程でUDP-GlcNAc及びDol-Pの反応を阻害し、それによって全てのN-結合糖タンパク質の合成を阻害する。ホスホイノシトールホスホリパーゼCは、グリコシル−ホスホイノシトール(GPI)結合を特異的に切断し、GPIアンカータンパク質を周囲の培地中に放出する。配列番号88に対する発現したHA融合ポリペプチドを、抗HA抗体(Sigma社、St. Louis、MO)によるウェスタンブロット解析により検出した。pCMX-HA-hAB0440-Cos-7細胞を溶解後、可溶性画分を調製し、SDS-ポリアクリルアミドゲル上で分離し、PVDF膜に転写した。次いで、当該タンパク質ブロットを、抗HA抗体とともに1時間インキュベートし、バンドをRoche社(Laval、QC)製のECLキットを用いて可視化した。同じウェスタンブロットを剥離し、タンパク質サンプルを等しく充填するよう調節するために、抗アクチン抗体と反応させた。
配列番号88(配列番号153に示された)に対するポリペプチドは、破骨細胞の分化にとって必須であり(例Nを参照)、当該ペプチドは細胞表面に局在化している(例Pを参照)ことを示す当該結果を考慮すると、このタンパク質は、骨粗しょう症の症状を治療するための抗体療法ストラテジーの開発にとって良好な候補物となる。マウスTsp50に対するモノクローナル抗体(R&D Systems社、Minneapolis、MN)を購入し、配列番号1(配列番号93に示された)に対するポリペプチドに対する特異的抗体が、RAW 264.7モデルにおいて破骨細胞の分化を阻害するか否かを試験するために使用した。およそ4000個のRAW264.7細胞/ウェルを96ウェルプレートに接種し、Tsp50に対するマウスモノクローナル抗体またはコントロール抗HA抗体(Sigma社、St. Louis、MO)のいずれかの増加濃度存在下で100ng/mLのRANKリガンドで処理した。3日後、当該細胞を固定し、TRAP発現に対して染色し、多核化細胞をカウントした。
配列番号2(AB0179)は、いくつかのサブユニットを含む大きなタンパク質複合体である破骨細胞特異的液胞(v)-ATPaseに属する。v-ATPaseのaサブユニットは、V0ドメインを構成する4種のイソ体(a1-a4)を含む。細胞膜を通って、成熟破骨細胞の波状膜と骨表面との間に作られるポケットへのプロトンの分泌に必要なエネルギーを提供するために、このドメインはATPの加水分解にとって重要である。破骨細胞において、a3サブユニットは、ATPase複合体の構造完全性にとって重要であるdサブユニットと相互作用する(Nishi and Forgac, 2002)。ヒトでは2種のサブユニットであるd1及びd2があり、後者はもっぱら破骨細胞に見られ、ポリヌクレオチドの配列番号89(配列番号154をコードする)に対応する配列番号2のヒトオルソログによりコードされる。配列番号2に対するsiRNAの存在下で、成熟破骨細胞の骨吸収活性が著しく低下した、RAW264.7モデルを用いた検証試験により、破骨細胞の機能におけるd2の重要性は明確に立証された(K節−RNA干渉試験の結果)。さらに、a3イソ体は、一般に破骨細胞及び骨中のv-ATPaseのaサブユニットの主要形態であることが十分に文書化されている(Smith et al., 2005)。従って、破骨細胞中のv-ATPaseの機能を阻害し得る分子を同定するために、d2サブユニットとa3サブユニットとの間の特異的相互作用を利用する。
配列番号1−7、及び57は、破骨細胞に存在し、特異的siRNAによる阻害後、破骨細胞形成に影響を及ぼすことが立証された差異的に発現する配列を示す。配列番号8−56は、骨再構築において役割を有することが推定される破骨細胞に存在する差異的に発現する配列を示す。配列番号58−82は、本明細書で実施された実験に用いられたプラスミド、オリゴヌクレオチドプライマー、及びsiRNAのヌクレオチド配列を示す。
Claims (55)
- 未分化破骨前駆体細胞と比較して分化破骨細胞において差異的に発現する単離ポリヌクレオチドであって、:
a)配列番号1−56、配列番号83、配列番号86、または配列番号87のいずれか1つを含むポリヌクレオチド;
b)配列番号1−56、配列番号83、配列番号86、または配列番号87のいずれか1つのオープンリーディングフレームを含むポリヌクレオチド;
c)a)またはb)と実質的に同一である配列を含むポリヌクレオチド;
d)a)またはb)と実質的に相補的である配列を含むポリヌクレオチド;及び
e)a)からd)のいずれか1つの断片;
からなる群から選択される1種を含む単離ポリヌクレオチド。 - 前記実質的に同一であるポリヌクレオチドが配列番号84、配列番号85、配列番号88、配列番号89、及び配列番号84、配列番号85、配列番号88、または配列番号89のいずれか1つのオープンリーディングフレームからなる群から選択される、請求項1に記載の単離ポリヌクレオチド。
- 前記断片が、配列番号1−56または配列番号83−89のいずれか1つの核酸配列と実質的に相補的である少なくとも10核酸の配列を含む、請求項1または2に記載のポリヌクレオチド。
- 前記断片が配列番号64−80または90のいずれか1つからなる群から選択される、請求項3に記載のポリヌクレオチド。
- 破骨細胞の分化に関与する単離ポリヌクレオチドであって、:
a)配列番号1−56または83−89のいずれか1つを含むポリヌクレオチド;
b)配列番号1−56または83−89のいずれか1つのオープンリーディングフレームを含むポリヌクレオチド;及び
c)a)またはb)と実質的に同一であるポリヌクレオチド;
からなる群から選択される単離ポリヌクレオチド。 - 破骨細胞の分化を促進し得る単離ポリヌクレオチドであって、:
a)配列番号1−5、8−56、または83−89のいずれか1つ;
b)配列番号1−5、8−56、または83−89のいずれか1つのオープンリーディングフレーム;及び
c)配列番号6または配列番号7のいずれか1つの核酸配列と相補的である少なくとも10核酸の配列;
を含むポリヌクレオチドからなる群から選択される単離ポリヌクレオチド。 - 破骨細胞の分化を阻害し得る単離ポリヌクレオチドであって、前記配列が:
a)配列番号6または配列番号7のいずれか1つ;
b)配列番号6または配列番号7のいずれか1つのオープンリーディングフレーム;及び
c)配列番号1−5、8−57、または83−89のいずれか1つの核酸配列と相補的である少なくとも10核酸の配列;
を含むポリヌクレオチドからなる群から選択される単離ポリヌクレオチド。 - 配列が配列番号64−82及び90からなる群から選択される、請求項7に記載の単離ポリヌクレオチド配列。
- 前記破骨細胞の分化を誘導する、請求項6または7のいずれか一項に記載の単離ポリヌクレオチド配列。
- 前記ポリヌクレオチドがRNA分子である、請求項1から9のいずれか一項に記載の単離ポリヌクレオチド。
- 前記ポリヌクレオチドがDNA分子である、請求項1から9のいずれか一項に記載の単離ポリヌクレオチド。
- 請求項10または11のいずれか一項に記載のDNAまたはRNA分子を含むベクター。
- 前記ベクターが発現ベクターである、請求項12に記載のベクター。
- 未分化破骨前駆体細胞と比較して分化破骨細胞において差異的に発現するポリヌクレオチド配列のライブラリーであって、:
a)配列番号1−57及び83−89のいずれか1つを含むポリヌクレオチド;
b)配列番号1−57及び83−89のいずれか1つのオープンリーディングフレームを含むポリヌクレオチド;
c)a)またはb)と実質的に同一である配列を含むポリヌクレオチド;
d)a)またはb)と実質的に相補的である配列を含むポリヌクレオチド;及び
e)a)からd)のいずれか1つの断片;
からなる群から選択される少なくとも1種を含むライブラリー。 - 請求項14に記載の、ポリヌクレオチドのライブラリーを含み、前記ポリヌクレオチドのそれぞれが発現ベクター内に含まれる発現ライブラリー。
- 請求項14に記載の、ポリヌクレオチド配列のライブラリーを含むアレイ。
- 骨吸収を阻害するための医薬組成物であって、:
a)請求項7に記載の単離ポリヌクレオチド;及び
b)製薬上許容し得る担体;
を含む医薬組成物。 - それを必要とする哺乳動物における骨吸収を阻害するための方法であって、前記方法は請求項7に記載の単離ポリヌクレオチドまたは請求項17に記載の医薬組成物を前記哺乳動物に投与する工程を含む方法。
- 前記哺乳動物が、骨粗しょう症、骨減少症、骨軟化症、副甲状腺機能亢進症、甲状腺機能亢進症、性腺機能低下症、甲状腺中毒症、全身性肥満細胞症、成人型低ホスファターゼ症、副腎皮質機能亢進症、骨形成不全症、パジェット病、クッシング病/症候群、チューマー症候群、ゴーシェ病、エーラース-ダンロス症候群、マルファン症候群、メンケス症候群、ファンコニー症候群、多発性骨髄腫、高カルシウム血症、低カルシウム血症、関節炎症、歯周病、くる病、線維形成不全症骨、ピクノディスオストーシス等の骨硬化症障害、及びマクロファージ媒介性炎症プロセスによって引き起こされる障害からなる群から選択される状態に罹患している、請求項18記載の方法。
- 骨吸収疾患の治療のための医薬品を調製するための、請求項7に記載の単離ポリヌクレオチドの使用。
- それを必要とする哺乳動物における破骨細胞の分化を促進するための医薬組成物であって、:
a)請求項6に記載の単離ポリヌクレオチド;及び
b)製薬上許容し得る担体;
を含む医薬組成物。 - それを必要とする哺乳動物における破骨細胞の分化を促進するための方法であって、請求項6に記載の単離ポリヌクレオチドまたは請求項21に記載の医薬組成物を前記哺乳動物に投与する工程を含む方法。
- 不十分な骨吸収に関連する疾患の治療のための医薬品を調製するための、請求項6に記載の単離ポリヌクレオチドの使用。
- 骨再構築に関連する状態を診断する際の、:
a)配列番号1−57及び83−89のいずれか1つを含むポリヌクレオチド;
b)配列番号1−57及び83−89のいずれか1つのオープンリーディングフレームを含むポリヌクレオチド;
c)a)またはb)と実質的に同一である配列を含むポリヌクレオチド;
d)a)またはb)と実質的に相補的である配列を含むポリヌクレオチド;
e)a)からd)のいずれか1つの断片;及び
f)a)からd)のいずれか1つを含むライブラリー;
からなる群から選択される少なくとも1つのポリヌクレオチドの使用。 - 骨再構築に関連する状態を診断するためのキットであって、配列番号1−57または83−89のいずれか1つと実質的に相補的である少なくとも1つの配列、配列番号1−57または83−89のいずれか1つのオープンリーディングフレーム、及びその断片を含むキット。
- 破骨細胞の分化を促進し得る単離ポリペプチド配列であって、前記ポリペプチドが:
a)配列番号93−97または101−105のいずれか1つ;
b)a)のいずれか1つの生物学的な活性がある断片;
c)a)のいずれか1つの生物学的な活性がある類似体;
からなる群から選択される配列を含む、単離ポリペプチド配列。 - 前記生物学的な活性がある類似体が、前記配列中に少なくとも1つの保存的アミノ酸置換を含む、請求項26に記載の単離ポリペプチド。
- 破骨細胞の分化を促進するための医薬組成物であって、請求項26または27のいずれか一項に記載のポリペプチド及び製薬上許容し得る担体を含む医薬組成物。
- それを必要とする哺乳動物における破骨細胞の分化を促進するための方法であって、請求項26または27に記載の単離ポリペプチドまたは請求項28に記載の医薬組成物を前記哺乳動物に投与する工程を含む方法。
- 不十分な骨吸収に関連する疾患の治療のための医薬品を調製するための、請求項26または27に記載の単離ポリペプチドの使用。
- 破骨細胞の分化を阻害し得る単離ポリペプチド配列であって、前記ポリペプチドが:
a)配列番号98及び配列番号99のいずれか1つの配列;
b)a)のいずれか1つの生物学的な活性がある断片;
c)a)のいずれか1つの生物学的な活性がある類似体;
からなる群から選択される配列を含む、単離ポリペプチド配列。 - 前記生物学的な活性がある類似体が、前記配列中に少なくとも1つの保存的アミノ酸置換を含む、請求項31に記載の単離ポリペプチド。
- 請求項31または32に記載の単離ポリペプチドを含む医薬組成物。
- それを必要とする個体における骨吸収を改善するための方法であって、請求項31または32に記載の単離ポリペプチドまたは請求項33に記載の医薬組成物を投与する工程を含む方法。
- それを必要とする個体における骨吸収を改善するための方法であって、配列番号93−97及び101−155からなる群から選択されるポリペプチドの活性または発現を阻害し得る化合物を投与する工程を含む方法。
- 前記哺乳動物が、骨粗しょう症、骨減少症、骨軟化症、副甲状腺機能亢進症、甲状腺機能亢進症、性腺機能低下症、甲状腺中毒症、全身性肥満細胞症、成人型低ホスファターゼ症、副腎皮質機能亢進症、骨形成不全症、パジェット病、クッシング病/症候群、チューマー症候群、ゴーシェ病、エーラース-ダンロス症候群、マルファン症候群、メンケス症候群、ファンコニー症候群、多発性骨髄腫、高カルシウム血症、低カルシウム血症、関節炎症、歯周病、くる病、線維形成不全症骨、ピクノディスオストーシス等の骨硬化症障害、及びマクロファージ媒介性炎症プロセスによって引き起こされる障害からなる群から選択される状態に罹患している、請求項34または35に記載の方法。
- それを必要とする個体における骨吸収疾患の治療のための医薬品を調製する際の、請求項31または32に記載のポリペプチドの使用。
- それを必要とする個体における骨吸収疾患の治療のための医薬品を調製するための、配列番号93−97及び101−155からなる群から選択されるポリペプチドの活性または発現を阻害し得る化合物の使用。
- 配列番号93−97及び101−155からなる群から選択されるポリペプチドのいずれかと結合し得る、抗体及びその抗原結合断片。
- 前記抗体が破骨細胞の分化を阻害し得る、請求項39に記載の抗体。
- a)請求項40に記載の抗体;及び
b)製薬上許容し得る担体;
を含む医薬組成物。 - 破骨細胞の分化を阻害する方法であって、それを必要とする哺乳動物に請求項40に記載の抗体または請求項41に記載の医薬組成物を投与する工程を含む方法。
- それを必要とする個体における骨吸収疾患の治療のための医薬品を調製するための、請求項40に記載の抗体の使用。
- 配列番号93−155からなる群から選択されるポリペプチド、その類似体または断片、あるいは(a)配列番号1−56及び83−89、(b)配列番号1−56及び83−89のオープンリーディングフレームを含むポリヌクレオチド、並びに(c)(a)または(b)のいずれか1つと実質的に同一である配列からなる群から選択される核酸、あるいはそれらの免疫学的な活性があるポリペプチドをコードし得る(a)、(b)、または(c)のいずれか1つの断片を含む免疫性組成物。
- それを必要とする個体における骨吸収障害または疾患に関連する状態の診断方法であって、前記個体由来のサンプル中の(a)配列番号1−56及び83−89、(b)配列番号1−56及び83−89のオープンリーディングフレームを含むポリヌクレオチド、及び(c)(a)または(b)のいずれか1つと実質的に同一である配列からなる群から選択される核酸配列、あるいは93−155からなる群から選択されるポリペプチド配列を、標準または正常値と比較して定量化する工程を含む方法。
- 配列番号93−97及び100−155からなる群から選択されるポリペプチドの機能または発現を害し得る阻害化合物を同定するための方法であって、前記ポリペプチドまたは前記ポリペプチドを発現する細胞を候補化合物と接触させる工程、及び前記ポリペプチドの機能または発現を測定する工程を含み、前記ポリペプチドの機能または活性の低下によって適切な阻害化合物を明確に同定する方法。
- 前記害された機能または活性が、破骨細胞の分化を促進する前記ポリペプチドの能力の低下と関連する、請求項46に記載の方法。
- 前記破骨細胞の分化を誘導する、請求項47に記載の方法。
- 前記細胞が前記ポリペプチドを本来発現せず、あるいは本来発現されるポリペプチド類似体の発現が抑制される、請求項46または47に記載の方法。
- 前記ポリペプチドが配列番号153であり、配列番号93の発現が抑制され、且つ前記細胞がマウス破骨細胞である、請求項49に記載の方法。
- 前記害された機能または活性が、既知のパートナーと相互作用する前記ポリペプチドの能力の低下と関連する、請求項46に記載の方法。
- 前記ポリペプチドが配列番号154であり、且つ前記化合物が前記ポリペプチドとv-ATPase-a3サブユニットの相互作用を害し得る、請求項51に記載の方法。
- 配列番号98及び配列番号99からなる群から選択されるポリペプチドの機能または発現を害し得る阻害化合物を同定するための方法であって、前記ポリペプチドまたは前記ポリペプチドを発現する細胞を候補化合物と接触させる工程、及び前記ポリペプチドの機能または発現を測定する工程を含み、前記ポリペプチドの機能または活性の低下によって適切な阻害化合物を明確に同定する方法。
- 前記害された機能または活性が、破骨細胞の分化を阻害する前記ポリペプチドの能力の低下と関連する、請求項53に記載の方法。
- 前記細胞が前記ポリペプチドを本来発現せず、あるいは本来発現されるポリペプチド類似体の発現が抑制される、請求項53または54に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US63498104P | 2004-12-13 | 2004-12-13 | |
| PCT/CA2005/001917 WO2006063462A1 (en) | 2004-12-13 | 2005-12-13 | Polynucleotides and polypeptide sequences involved in the process of bone remodeling |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008522632A true JP2008522632A (ja) | 2008-07-03 |
| JP2008522632A5 JP2008522632A5 (ja) | 2008-11-27 |
Family
ID=36587499
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007545800A Pending JP2008522632A (ja) | 2004-12-13 | 2005-12-13 | 骨再構築のプロセスに関与するポリヌクレオチド及びポリペプチド配列 |
Country Status (6)
| Country | Link |
|---|---|
| US (3) | US7947436B2 (ja) |
| EP (2) | EP2275547B1 (ja) |
| JP (1) | JP2008522632A (ja) |
| AU (1) | AU2005316169B2 (ja) |
| CA (1) | CA2590751A1 (ja) |
| WO (1) | WO2006063462A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014230493A (ja) * | 2013-05-28 | 2014-12-11 | 三菱レイヨン株式会社 | 間葉系幹細胞からの分化状態を識別する遺伝子群及び分化状態の評価方法 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8168181B2 (en) | 2006-02-13 | 2012-05-01 | Alethia Biotherapeutics, Inc. | Methods of impairing osteoclast differentiation using antibodies that bind siglec-15 |
| US7989160B2 (en) | 2006-02-13 | 2011-08-02 | Alethia Biotherapeutics Inc. | Polynucleotides and polypeptide sequences involved in the process of bone remodeling |
| WO2008114709A1 (ja) * | 2007-03-15 | 2008-09-25 | Reverse Proteomics Research Institute Co., Ltd. | 血球系に特異的あるいは破骨細胞分化に特異的なバイオマーカー |
| CA2928851A1 (en) | 2012-07-19 | 2014-01-23 | Alethia Biotherapeutics Inc. | Anti-siglec-15 antibodies |
| KR101463325B1 (ko) * | 2013-01-14 | 2014-11-20 | 가톨릭대학교 산학협력단 | HtrA2 단백질을 유효성분으로 포함하는 자가면역질환의 예방 또는 치료용 조성물 |
| US20210052695A1 (en) * | 2018-01-26 | 2021-02-25 | Cambridge Enterprise Limited | Peptide exchange protein |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002027502A1 (fr) * | 2000-09-26 | 2002-04-04 | Kabushiki Kaisha Toshiba | Support d'enregistrement portant un programme d'envoi et de réception de courrier électronique |
| JP2003334094A (ja) * | 2002-03-15 | 2003-11-25 | Sankyo Co Ltd | 骨代謝異常の治療または予防剤の試験方法 |
| WO2004076639A2 (en) * | 2003-02-26 | 2004-09-10 | Wyeth | Use of gene expression profiling in the diagnosis and treatment of lupus nephritis and systemic lupus erythematosus |
Family Cites Families (116)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100202640B1 (ko) * | 1995-12-07 | 1999-06-15 | 구본준 | 씨알티의 잔류자속 제거방법 |
| US5712127A (en) | 1996-04-29 | 1998-01-27 | Genescape Inc. | Subtractive amplification |
| US5871917A (en) * | 1996-05-31 | 1999-02-16 | North Shore University Hospital Research Corp. | Identification of differentially methylated and mutated nucleic acids |
| US6617434B1 (en) * | 1996-05-31 | 2003-09-09 | North Shore Long Island Jewish Research Institute | Identificiaton of differentially methylated and mutated nucleic acids |
| US5968782A (en) | 1996-12-04 | 1999-10-19 | Brigham And Womens's Hospital, Inc. | Mast cell protease that cleaves fibrinogen |
| US6479274B1 (en) * | 1997-02-13 | 2002-11-12 | Amrad Operations Pty., Ltd. | DNA molecules encoding human HELA2 or testisin serine proteinases |
| US7368531B2 (en) | 1997-03-07 | 2008-05-06 | Human Genome Sciences, Inc. | Human secreted proteins |
| US7193048B2 (en) | 1997-03-31 | 2007-03-20 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US5981830A (en) * | 1997-05-30 | 1999-11-09 | Schering Aktiengesellschaft | Knockout mice and their progeny with a disrupted hepsin gene |
| US20020192659A1 (en) * | 1997-09-17 | 2002-12-19 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US20030082540A1 (en) * | 1997-09-17 | 2003-05-01 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| CA2303834A1 (en) | 1997-09-17 | 1999-03-25 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US6203979B1 (en) * | 1998-01-16 | 2001-03-20 | Incyte Pharmaceuticals, Inc. | Human protease molecules |
| US7022821B1 (en) | 1998-02-20 | 2006-04-04 | O'brien Timothy J | Antibody kit for the detection of TADG-15 protein |
| WO1999057144A2 (en) | 1998-05-05 | 1999-11-11 | Incyte Pharmaceuticals, Inc. | Human transcriptional regulator molecules |
| US6998260B1 (en) | 1998-05-15 | 2006-02-14 | Promega Corporation | Recombinant proteolytic tryptases, active site mutants thereof, and methods of making same |
| WO2000029448A2 (en) | 1998-11-17 | 2000-05-25 | Sagami Chemical Research Center | Human proteins having hydrophobic domains and dnas encoding these proteins |
| US20050053983A1 (en) * | 1998-11-20 | 2005-03-10 | Fuso Pharmaceutical Industries, Ltd. | Novel serine protease BSSP4 |
| CA2348971C (en) | 1998-11-20 | 2012-02-07 | Fuso Pharmaceutical Industries, Ltd. | Novel serine proteases bssp4 |
| KR20010102960A (ko) | 1998-12-22 | 2001-11-17 | 제넨테크, 인크. | 종양 치료용 조성물 및 방법 |
| EP1161266A4 (en) | 1999-03-12 | 2007-09-19 | Univ Georgetown | MATRIPTASE, SERINE PROTEASE, AND USE THEREOF |
| US20070048818A1 (en) | 1999-03-12 | 2007-03-01 | Human Genome Sciences, Inc. | Human secreted proteins |
| US7368527B2 (en) | 1999-03-12 | 2008-05-06 | Human Genome Sciences, Inc. | HADDE71 polypeptides |
| US6485957B1 (en) | 1999-04-30 | 2002-11-26 | Ortho-Mcneil Pharmaceutical, Inc. | DNA encoding the human serine protease EOS |
| US6420157B1 (en) * | 1999-04-30 | 2002-07-16 | Ortho-Mcneil Pharmaceutical, Inc. | Zymogen activation system |
| US20030207348A1 (en) * | 1999-07-20 | 2003-11-06 | Shimkets Richard A. | Polypeptides and polynucleotides encoding same |
| WO2001005971A2 (en) * | 1999-07-20 | 2001-01-25 | Curagen Corporation | Secreted polypeptides and corresponding polynucleotides |
| US6514741B1 (en) * | 1999-08-18 | 2003-02-04 | Zymogenetics, Inc. | Tryptase-like polypeptide ztryp1 |
| AU6637700A (en) | 1999-08-18 | 2001-03-13 | Zymogenetics Inc. | Tryptase-like polypeptide ztryp1 |
| US6426199B1 (en) * | 1999-08-31 | 2002-07-30 | Ortho-Mcneil Pharmaceutical, Inc. | Dna |
| US6458564B1 (en) * | 1999-08-31 | 2002-10-01 | Ortho-Mcneil Pharmaceutical, Inc. | DNA encoding the human serine protease T |
| EP1087230A1 (en) * | 1999-09-24 | 2001-03-28 | Boehringer Ingelheim International GmbH | Method for identifying compounds useful in the therapy of bone disorders |
| JP2003510074A (ja) | 1999-09-27 | 2003-03-18 | ヒューマン ジノーム サイエンシーズ, インコーポレイテッド | 26個のヒト分泌タンパク質 |
| US20060084054A1 (en) | 1999-09-27 | 2006-04-20 | John Alsobrook | Novel proteins and nucleic acids encoding same |
| US7030231B1 (en) | 1999-09-30 | 2006-04-18 | Catalyst Biosciences, Inc. | Membrane type serine protease 1 (MT-SP1) and uses thereof |
| AU1205901A (en) * | 1999-10-14 | 2001-04-23 | Board Of Trustees Of The University Of Arkansas, The | Tumor antigen derived gene-16 (tadg-16): a novel extracellular serine protease and uses thereof |
| WO2001036645A2 (en) | 1999-11-17 | 2001-05-25 | Curagen Corporation | Serine/threonine kinase and serine protease polypeptides and nucleic acids encoding same |
| EP1235838A4 (en) | 1999-11-19 | 2003-09-10 | Human Genome Sciences Inc | 23 HUMAN SECRETED PROTEINS |
| CA2394789A1 (en) | 1999-12-23 | 2001-06-28 | Incyte Genomics, Inc. | Proteases |
| US20020042096A1 (en) | 2000-01-31 | 2002-04-11 | Rosen Craig A. | Nucleic acids, proteins, and antibodies |
| US20030050231A1 (en) | 2000-01-31 | 2003-03-13 | Rosen Craig A. | Nucleic acids, proteins, and antibodies |
| US7700341B2 (en) | 2000-02-03 | 2010-04-20 | Dendreon Corporation | Nucleic acid molecules encoding transmembrane serine proteases, the encoded proteins and methods based thereon |
| US20040043930A1 (en) * | 2000-02-08 | 2004-03-04 | Anderson David W. | Novel proteins and nucleic acids encoding same |
| AU2001238303A1 (en) | 2000-02-15 | 2001-08-27 | Curagen Corporation | Polypeptides and nucleic acids encoding same |
| EP1261712B1 (en) | 2000-03-03 | 2006-12-13 | Curagen Corporation | Proteins named fctrx and nucleic acids encoding same |
| US20030065140A1 (en) | 2000-04-03 | 2003-04-03 | Vernet Corine A.M. | Novel proteins and nucleic acids encoding same |
| AU2001274888A1 (en) | 2000-05-19 | 2001-12-03 | Human Genome Sciences, Inc. | Nucleic acids, proteins, and antibodies |
| WO2001098503A2 (en) | 2000-06-21 | 2001-12-27 | Bayer Aktiengesellschaft | Regulation of human eosinophil serine protease 1-like enzyme |
| WO2001098467A2 (en) | 2000-06-23 | 2001-12-27 | Bayer Aktiengesellschaft | Regulation of human prostasin-like serine protease |
| WO2001098466A2 (en) * | 2000-06-23 | 2001-12-27 | Bayer Aktiengesellschaft | Regulation of human prostasin-like serine protease |
| JP2004501637A (ja) * | 2000-06-26 | 2004-01-22 | スージェン・インコーポレーテッド | 新規プロテアーゼ |
| US20030077647A1 (en) * | 2001-10-09 | 2003-04-24 | Millennium Pharmaceuticals, Inc. | 14081, a human trypsin-like serine protease family member and uses therefor |
| US20020045230A1 (en) | 2000-08-14 | 2002-04-18 | Rosen Craig A. | Nucleic acids, proteins, and antibodies |
| WO2002046408A2 (en) | 2000-10-24 | 2002-06-13 | Curagen Corporation | Human proteins, polynucleotides encoding them and methods of using the same |
| AU2002246808A1 (en) | 2000-12-19 | 2002-08-06 | Curagen Corporation | Human nucleic acids and polypeptides and methods of use thereof |
| US7122345B2 (en) | 2001-01-09 | 2006-10-17 | Curagen Corporation | Nucleic acid encoding a NOVX13 polypeptide |
| WO2002068647A2 (en) | 2001-01-16 | 2002-09-06 | Curagen Corporation | Proteins, polynucleotides encoding them and methods of using the same |
| WO2002098917A2 (en) | 2001-02-12 | 2002-12-12 | Curagen Corporation | Human proteins and nucleic acids encoding same |
| US20030049645A1 (en) * | 2001-02-14 | 2003-03-13 | David Mu | Amplified cancer gene hepsin |
| US6482630B2 (en) * | 2001-03-29 | 2002-11-19 | Applera Corporation | Isolated human protease proteins, nucleic acid molecules encoding human protease proteins, and uses thereof |
| JP2004535169A (ja) | 2001-04-06 | 2004-11-25 | ランコート,デリック,イー. | 着床セリンプロテアーゼ |
| US20060188903A1 (en) * | 2001-04-06 | 2006-08-24 | Rancourt Derrick E | Implantation serine proteinases |
| KR20040004642A (ko) | 2001-05-23 | 2004-01-13 | 덴드레온 샌 디에고 엘엘씨 | 세포 표면 프로테아제에 의해 활성화되는 접합체 및 이의치료학적 용도 |
| WO2003000012A2 (en) | 2001-06-21 | 2003-01-03 | Millennium Pharmaceuticals, Inc. | Compositions, kits, and methods for identification, assessment, prevention, and therapy of breast and ovarian cancer |
| US20030108963A1 (en) | 2001-07-25 | 2003-06-12 | Millennium Pharmaceuticals, Inc. | Novel genes, compositions, kit, and methods for identification, assessment, prevention and therapy of prostate cancer |
| AU2002324700A1 (en) | 2001-08-14 | 2003-03-03 | Bayer Ag | Nucleic acid and amino acid sequences involved in pain |
| WO2003063688A2 (en) | 2002-01-25 | 2003-08-07 | Incyte Corporation | Protein modification and maintenance molecules |
| US20040126777A1 (en) * | 2002-01-28 | 2004-07-01 | Bhatt Ramesh Rajani | Lp mammalian proteins; related reagents |
| WO2003065871A2 (en) | 2002-02-04 | 2003-08-14 | Millennium Pharmaceuticals Inc. | Methods and compositions for treating hematological disorders |
| US7160994B2 (en) * | 2002-03-28 | 2007-01-09 | Trustees Of The University Of Pennsylvania | Osteoclast-specific genes and proteins and uses thereof |
| EP1792912A3 (en) | 2002-04-02 | 2007-08-29 | Curagen Corporation | Novel proteins and nucleic acids encoding same |
| US20040001801A1 (en) * | 2002-05-23 | 2004-01-01 | Corvas International, Inc. | Conjugates activated by cell surface proteases and therapeutic uses thereof |
| US20030124706A1 (en) * | 2002-06-21 | 2003-07-03 | Junming Yang | Proteases |
| WO2004009803A2 (en) | 2002-07-23 | 2004-01-29 | Bayer Healthcare Ag | Regulation of human hepsin |
| US6977170B2 (en) * | 2002-09-06 | 2005-12-20 | Applera Corporation | Isolated human hepsin/46 proteins, nucleic acid molecules encoding human hepsin/46 proteins, and uses thereof |
| AU2003289716A1 (en) | 2002-09-12 | 2004-04-30 | Incyte Corporation | Molecules for diagnostics and therapeutics |
| EP1585482A4 (en) * | 2002-09-25 | 2009-09-09 | Genentech Inc | NEW COMPOSITIONS AND METHODS FOR TREATING PSORIASIS |
| WO2004030615A2 (en) * | 2002-10-02 | 2004-04-15 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| WO2004033630A2 (en) | 2002-10-04 | 2004-04-22 | Schering Aktiengesellschaft | Modified hepsin molecules having a substitute activation sequence and uses thereof |
| AU2003279829A1 (en) | 2002-10-04 | 2004-05-04 | Incyte Corp | Protein modification and maintenance molecules |
| AU2002951912A0 (en) | 2002-10-08 | 2002-10-24 | Unisearch Limited | Tryptase polypeptide and uses thereof |
| WO2004044178A2 (en) | 2002-11-13 | 2004-05-27 | Genentech, Inc. | Methods and compositions for diagnosing dysplasia |
| AU2003298786A1 (en) | 2002-11-26 | 2004-06-18 | Protein Design Labs, Inc. | Methods of detecting soft tissue sarcoma, compositions and methods of screening for soft tissue sarcoma modulators |
| AU2003300815A1 (en) | 2002-12-05 | 2004-06-30 | Incyte Corporation | Protein modification and maintenance molecules |
| CA2886504C (en) * | 2002-12-20 | 2019-01-08 | Celera Corporation | Wdr12 polymorphisms associated with myocardial infarction, methods of detection and uses thereof |
| US20050181375A1 (en) | 2003-01-10 | 2005-08-18 | Natasha Aziz | Novel methods of diagnosis of metastatic cancer, compositions and methods of screening for modulators of metastatic cancer |
| WO2004086035A1 (en) | 2003-03-28 | 2004-10-07 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with hepsin (hpn) |
| US20050255114A1 (en) * | 2003-04-07 | 2005-11-17 | Nuvelo, Inc. | Methods and diagnosis for the treatment of preeclampsia |
| WO2004093804A2 (en) | 2003-04-18 | 2004-11-04 | Five Prime Therapeutics, Inc. | Human polypeptides encoded by polynucleotides and methods of their use |
| US8207311B2 (en) | 2003-05-16 | 2012-06-26 | Diadexus, Inc. | Ovr115 antibody compositions and methods of use |
| WO2004106536A2 (en) | 2003-05-28 | 2004-12-09 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with serine protease 8 (prss8) |
| WO2005046573A2 (en) | 2003-06-27 | 2005-05-26 | Diadexus, Inc. | Pro104 ANTIBODY COMPOSITIONS AND METHODS OF USE |
| WO2005005647A2 (en) | 2003-06-30 | 2005-01-20 | Diadexus, Inc. | Compositions, splice variants and methods relating to ovarian specific genes and proteins |
| US20040137623A1 (en) * | 2003-09-17 | 2004-07-15 | Isis Pharmaceuticals, Inc. | Delivery of oligonucleotide compounds into osteoclasts and modulation of osteoclast differentiation |
| US20050176030A1 (en) * | 2003-10-28 | 2005-08-11 | Li Gan | Regulated nucleic acids in pathogenesis of Alzheimer's Disease |
| CA3050151C (en) * | 2003-11-26 | 2023-03-07 | Celera Corporation | Single nucleotide polymorphisms associated with cardiovascular disorders and statin response, methods of detection and uses thereof |
| US20050153333A1 (en) | 2003-12-02 | 2005-07-14 | Sooknanan Roy R. | Selective terminal tagging of nucleic acids |
| US7569662B2 (en) | 2004-01-27 | 2009-08-04 | Compugen Ltd | Nucleotide and amino acid sequences, and assays and methods of use thereof for diagnosis of lung cancer |
| WO2006131783A2 (en) | 2004-01-27 | 2006-12-14 | Compugen Usa, Inc. | Polynucleotides, polypeptides, and diagnosing lung cancer |
| EP1713929A2 (en) | 2004-02-03 | 2006-10-25 | Bayer HealthCare AG | Diagnostics and therapeutics for diseases associated with plasma kallikrein (klkb1) |
| US20060084066A1 (en) | 2004-02-20 | 2006-04-20 | Sah Dinah W Y | Surrogate markers of neuropathic pain |
| WO2005119262A2 (en) | 2004-05-27 | 2005-12-15 | Galapagos N.V. | Methods, compositions and compound assays for inhibiting amyloid-beta protein production |
| NZ551908A (en) | 2004-07-26 | 2009-10-30 | Genentech Inc | Methods and compositions for modulating hepatocyte growth factor HGF activation |
| WO2006013016A2 (en) | 2004-08-04 | 2006-02-09 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with eosinophil serine protease 1 (prss21) |
| WO2006013015A2 (en) | 2004-08-04 | 2006-02-09 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with marapsin (mpn) |
| US7622265B2 (en) | 2005-02-22 | 2009-11-24 | Genentech, Inc. | Methods and compositions for modulating prostasin |
| US20070099251A1 (en) | 2005-10-17 | 2007-05-03 | Institute For Systems Biology | Tissue-and serum-derived glycoproteins and methods of their use |
| AU2006304804B2 (en) * | 2005-10-21 | 2011-06-02 | Vertex Pharmaceuticals Incorporated | Modified proteases that inhibit complement activation |
| US7510850B2 (en) | 2005-11-10 | 2009-03-31 | Carnegie Institution Of Washington | Isolation of the mitotic spindle matrix and its methods of use |
| CA2634146A1 (en) | 2005-12-19 | 2007-06-28 | Genizon Biosciences Inc. | Genemap of the human genes associated with crohn's disease |
| WO2007140907A1 (en) | 2006-06-07 | 2007-12-13 | Bayer Healthcare Ag | Use of serine endopeptidases 22 (prss22) as a therapeutic or diagnostic target |
| CA2655986A1 (en) | 2006-06-22 | 2007-12-27 | Genentech, Inc. | Methods and compositions for modulating hepsin activation of urokinase-type plasminogen activator |
| CN101490088B (zh) | 2006-06-22 | 2015-04-08 | 健泰科生物技术公司 | 用于靶向hepsin的方法和组合物 |
| WO2008016356A2 (en) * | 2006-08-02 | 2008-02-07 | Genizon Biosciences | Genemap of the human genes associated with psoriasis |
| US8586006B2 (en) | 2006-08-09 | 2013-11-19 | Institute For Systems Biology | Organ-specific proteins and methods of their use |
| CA2670107A1 (en) * | 2006-11-22 | 2008-06-05 | The Board Of Trustees Of The University Of Arkansas | Multi-epitope peptide-loaded dendritic cell immunotherapy for cancer |
-
2005
- 2005-12-13 JP JP2007545800A patent/JP2008522632A/ja active Pending
- 2005-12-13 CA CA002590751A patent/CA2590751A1/en not_active Abandoned
- 2005-12-13 EP EP10011409.9A patent/EP2275547B1/en not_active Not-in-force
- 2005-12-13 WO PCT/CA2005/001917 patent/WO2006063462A1/en active Application Filing
- 2005-12-13 EP EP05820749A patent/EP1831370A4/en not_active Withdrawn
- 2005-12-13 US US11/792,932 patent/US7947436B2/en not_active Expired - Fee Related
- 2005-12-13 AU AU2005316169A patent/AU2005316169B2/en not_active Ceased
-
2011
- 2011-04-07 US US13/082,107 patent/US20110293604A1/en not_active Abandoned
-
2012
- 2012-05-23 US US13/478,556 patent/US8444975B2/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002027502A1 (fr) * | 2000-09-26 | 2002-04-04 | Kabushiki Kaisha Toshiba | Support d'enregistrement portant un programme d'envoi et de réception de courrier électronique |
| JP2003334094A (ja) * | 2002-03-15 | 2003-11-25 | Sankyo Co Ltd | 骨代謝異常の治療または予防剤の試験方法 |
| WO2004076639A2 (en) * | 2003-02-26 | 2004-09-10 | Wyeth | Use of gene expression profiling in the diagnosis and treatment of lupus nephritis and systemic lupus erythematosus |
Non-Patent Citations (5)
| Title |
|---|
| JPN6011027297; J Bone Mineral Res., 19[Sup1] (2004 Oct) p.S415 * |
| JPN6011027300; J Biol Chem., 279 (2004 Apr) p.13984-13992. * |
| JPN6011027303; Gene Cell., 3 (1998) p.459-475. * |
| JPN6011027305; 実験医学, 13[4] (1995) p.46-52. * |
| JPN6012025231; Cancer Res., 59[13] (1999) p.3215-21. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014230493A (ja) * | 2013-05-28 | 2014-12-11 | 三菱レイヨン株式会社 | 間葉系幹細胞からの分化状態を識別する遺伝子群及び分化状態の評価方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US8444975B2 (en) | 2013-05-21 |
| WO2006063462A1 (en) | 2006-06-22 |
| EP2275547A3 (en) | 2011-05-04 |
| EP1831370A1 (en) | 2007-09-12 |
| US7947436B2 (en) | 2011-05-24 |
| WO2006063462A9 (en) | 2007-07-26 |
| US20090004206A1 (en) | 2009-01-01 |
| US20120308561A1 (en) | 2012-12-06 |
| AU2005316169A1 (en) | 2006-06-22 |
| US20110293604A1 (en) | 2011-12-01 |
| AU2005316169B2 (en) | 2011-11-17 |
| EP2275547B1 (en) | 2014-03-05 |
| CA2590751A1 (en) | 2006-06-22 |
| EP2275547A2 (en) | 2011-01-19 |
| EP1831370A4 (en) | 2009-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| USRE47672E1 (en) | Methods of impairing osteoclast differentiation using antibodies that bind siglec-15 | |
| JP6224182B2 (ja) | 骨リモデリングのプロセスと関係があるポリヌクレオチドおよびポリペプチド配列 | |
| DK2081586T3 (en) | RSPONDINES AS MODULATORS OF ANGIOGENESE AND VASCULOGENESES | |
| US8444975B2 (en) | Method for inhibiting bone resorption | |
| JP2003334088A (ja) | ヒト由来の新規Klotho様タンパク質及びその遺伝子 | |
| AU2014200123B2 (en) | Polynucleotides and polypeptide sequences involved in the process of bone remodeling | |
| JP2002355063A (ja) | 新規疾患関連遺伝子およびその用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081002 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081002 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110531 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110811 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110818 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111122 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120522 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120731 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120807 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130312 |