JP2007209651A - 治療子経路表示装置 - Google Patents
治療子経路表示装置 Download PDFInfo
- Publication number
- JP2007209651A JP2007209651A JP2006034911A JP2006034911A JP2007209651A JP 2007209651 A JP2007209651 A JP 2007209651A JP 2006034911 A JP2006034911 A JP 2006034911A JP 2006034911 A JP2006034911 A JP 2006034911A JP 2007209651 A JP2007209651 A JP 2007209651A
- Authority
- JP
- Japan
- Prior art keywords
- plane
- tomographic
- point
- subject
- pixel value
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 230000001225 therapeutic effect Effects 0.000 title claims abstract description 28
- 238000003780 insertion Methods 0.000 claims description 15
- 230000037431 insertion Effects 0.000 claims description 15
- 238000003384 imaging method Methods 0.000 claims description 11
- 238000004364 calculation method Methods 0.000 claims description 8
- 238000003860 storage Methods 0.000 claims description 5
- 238000013170 computed tomography imaging Methods 0.000 claims description 4
- 230000008014 freezing Effects 0.000 abstract description 56
- 238000007710 freezing Methods 0.000 abstract description 56
- 230000003902 lesion Effects 0.000 abstract description 37
- 230000017074 necrotic cell death Effects 0.000 abstract description 6
- 230000035515 penetration Effects 0.000 abstract description 4
- 238000012544 monitoring process Methods 0.000 description 35
- 238000000034 method Methods 0.000 description 30
- 239000007789 gas Substances 0.000 description 26
- 238000010257 thawing Methods 0.000 description 19
- 238000012545 processing Methods 0.000 description 15
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 10
- 230000008859 change Effects 0.000 description 10
- 238000010586 diagram Methods 0.000 description 9
- 210000004204 blood vessel Anatomy 0.000 description 7
- 206010028980 Neoplasm Diseases 0.000 description 6
- 201000011510 cancer Diseases 0.000 description 6
- 238000000315 cryotherapy Methods 0.000 description 6
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 5
- 206010028851 Necrosis Diseases 0.000 description 5
- 229910052786 argon Inorganic materials 0.000 description 5
- 239000001307 helium Substances 0.000 description 5
- 229910052734 helium Inorganic materials 0.000 description 5
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 5
- 201000005202 lung cancer Diseases 0.000 description 5
- 208000020816 lung neoplasm Diseases 0.000 description 5
- 238000005259 measurement Methods 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 238000009826 distribution Methods 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 230000033001 locomotion Effects 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 230000009471 action Effects 0.000 description 2
- 230000036760 body temperature Effects 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000002594 fluoroscopy Methods 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000013307 optical fiber Substances 0.000 description 2
- 238000004088 simulation Methods 0.000 description 2
- 230000002123 temporal effect Effects 0.000 description 2
- 238000003325 tomography Methods 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 230000006837 decompression Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 230000020169 heat generation Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
Images
Landscapes
- Thermotherapy And Cooling Therapy Devices (AREA)
- Apparatus For Radiation Diagnosis (AREA)
Abstract
【課題】凍結端子を有する治療子は体内に侵入させて病巣部位の壊死をはかる。かかる治療子の侵入点及び病巣部位たる到達点、そしてそのルートや侵入角度の決定を確実・正確に行いたい。
【解決手段】本発明では、侵入点P1、到達点P2を設定した後で、このP1、P2点を通る互いに所定の角度(例えば90°)を有する2つの平面Q1、Q2を選ぶ。2つの平面Q1、Q2での画素値を、実際、被検体のCT断層像データから近似値に求める。この2つの平面Q1、Q2の近似値に求めた画素値からなる算出断層像を表示部に表示させて、P1、P2点が正しく設定されたか否かをチェックする。
【選択図】図4
【解決手段】本発明では、侵入点P1、到達点P2を設定した後で、このP1、P2点を通る互いに所定の角度(例えば90°)を有する2つの平面Q1、Q2を選ぶ。2つの平面Q1、Q2での画素値を、実際、被検体のCT断層像データから近似値に求める。この2つの平面Q1、Q2の近似値に求めた画素値からなる算出断層像を表示部に表示させて、P1、P2点が正しく設定されたか否かをチェックする。
【選択図】図4
Description
本発明は、被検体内の穿刺して治療等を行う治療子の経路表示装置に関する。
医療装置の中には、被検体の体内に侵入具(治療子)を侵入(穿刺を含む)させる装置がある。例えば胃カメラ、監視用光ファイバー、組織を切り取って採取する採取具、特定の部位に薬剤を注入する注入具、病巣部位に熱や電磁波などのエネルギーを照射して治療を行う治療具などがある。
こうした侵入具の侵入監視用に透視像をリアルタイムで得て表示して侵入を監視する透視監視法、X線CT断層像をリアルタイムで得て二次元又は三次元表示させて侵入を監視するCT監視法がある。
こうした透視監視法、CT監視法は、術者が画面を見ながら監視し、この監視画像から術者が位置やルートを決定確認しながら、医療を施すやり方をとる。
CT監視法とは、侵入経路及び患部をCT撮影しながらリアルタイムでCT画像及び又はその三次元化した画像を表示させ、この表示画面を術者が監視しながら侵入具の進行及び治療を行う治療法を指す。CT監視法は、複雑な部位や身体の深化した部位(肺や心臓、前立腺や膵臓等)での監視に向いている。このCT監視法を使用した最新例として、肺癌組織の壊死をはかる凍結治療法がある。この凍結療法とは、肺癌部位細胞を凍結させ、その後で融解させ、その融解の過程で塩濃度の差の発生等により細胞内を破壊し、細胞死に至らしめるという原理による。凍結と融解には、2つの高圧ガスを使う。高圧のガスは急激に体積を膨張させると、分子の種類により急激に温度を上げるものと、急激に温度を下げるものとがあり、これは物理現学の1つであるJoule-Thompson効果と呼ばれる。そこで、温度を揚げる方に高圧アルゴンガスを、温度を下げる方にヘリウムガスを使用する。治療には、侵入具として中空の金属性の治療子(治療具と同義。ガイドニードルとも呼ばれる)を用いる。CT監視下で、この治療子を患部まで誘導し、上記2つのガスを交互に中空内から又は中空部の先端から外部へ放出し、熱交換作用を利用して患部への凍結療法を行う。
こうした侵入具の侵入監視用に透視像をリアルタイムで得て表示して侵入を監視する透視監視法、X線CT断層像をリアルタイムで得て二次元又は三次元表示させて侵入を監視するCT監視法がある。
こうした透視監視法、CT監視法は、術者が画面を見ながら監視し、この監視画像から術者が位置やルートを決定確認しながら、医療を施すやり方をとる。
CT監視法とは、侵入経路及び患部をCT撮影しながらリアルタイムでCT画像及び又はその三次元化した画像を表示させ、この表示画面を術者が監視しながら侵入具の進行及び治療を行う治療法を指す。CT監視法は、複雑な部位や身体の深化した部位(肺や心臓、前立腺や膵臓等)での監視に向いている。このCT監視法を使用した最新例として、肺癌組織の壊死をはかる凍結治療法がある。この凍結療法とは、肺癌部位細胞を凍結させ、その後で融解させ、その融解の過程で塩濃度の差の発生等により細胞内を破壊し、細胞死に至らしめるという原理による。凍結と融解には、2つの高圧ガスを使う。高圧のガスは急激に体積を膨張させると、分子の種類により急激に温度を上げるものと、急激に温度を下げるものとがあり、これは物理現学の1つであるJoule-Thompson効果と呼ばれる。そこで、温度を揚げる方に高圧アルゴンガスを、温度を下げる方にヘリウムガスを使用する。治療には、侵入具として中空の金属性の治療子(治療具と同義。ガイドニードルとも呼ばれる)を用いる。CT監視下で、この治療子を患部まで誘導し、上記2つのガスを交互に中空内から又は中空部の先端から外部へ放出し、熱交換作用を利用して患部への凍結療法を行う。
こうした一般的な凍結療法の文献として、非特許文献1がある。更に、凍結療法に用いる治療子を含む機械系、及びその治療のやり方と実際事例とを解説した文献として、非特許文献2がある。
雑誌「医学のあゆみ」(Vol.206No.3,2003.7.19)。川村他著「肺癌の凍結融解壊死療法」(P229〜P231)。 雑誌「低温医学」(30巻、2004)。中塚、川村他著「CT透視を用いた肺悪性腫瘍に対する経皮的凍結療法の実際」(P9〜P15)。
雑誌「医学のあゆみ」(Vol.206No.3,2003.7.19)。川村他著「肺癌の凍結融解壊死療法」(P229〜P231)。 雑誌「低温医学」(30巻、2004)。中塚、川村他著「CT透視を用いた肺悪性腫瘍に対する経皮的凍結療法の実際」(P9〜P15)。
文献2は、治療子の穿刺状態を、リアルタイムでX線CT装置で撮影してこれをリアルタイムで断層画像として再構成して表示させ、手技を行うとしたものである。X線CT装置は、マルチスライス撮影であり、一回で多数の断層像を得て表示させる。治療子の進行を監視でき、患部位置への追跡、手技に沿ってほぼリアルタイムで画像としてみることができる。
一方、治療子は、先端が刃物状に突起するステンレス製の二重管(コアキシャルニードル)を使う。治療に当っては、この二重管を体表面にあてがった状態で、二重管の中心軸に沿って長く細い誘導針を挿入し、その誘導針を患部まで穿刺する。次にその誘導針に沿って二重管を患部まで進行させ、更に二重管を進めて腫瘍を貫通させる。
この後で上記誘導針を抜いて、代りに凍結端子本体を二重管内の中空の軸に沿って挿通装填する。この際凍結端子本体の凍結・解凍部位となる端子先端は、二重管の先端のまるみを帯びた内面に当接又は近接した位置とする。凍結端子本体は高圧アルゴンガス注入口と高圧ヘリウムガス注入口へと切替バルブを介してつながる。充填確認後に切替バルブを切替えて高圧ヘリウムガスを注入し、次いで高圧アルゴンガスを注入し、凍結と解凍とを短時間で実行する。このサイクルを複数回繰返すこともある。これらの一連の動作はリアルタイムでのCT画像を表示させてのCT監視下で、観察確認しながら行う。
凍結端子を含む治療子は事前に定めたルート(経路)に従って行ったり、患部を開いて観察できる状態にしたりして、穿刺を行う。
経路は、侵入点と目標病巣位置(到達点)とを定めた上で決定する。しかし、経路状に血管や他の臓器や骨などの障害物がないことを確認するのは容易ではない。この確認をCT画像や透視像をもとにして行う例もある。
侵入点と到達点とを結ぶ経路を画像上で正確に確認できれば、治療効率につながり、操作者の負担も軽くなる。
経路は、侵入点と目標病巣位置(到達点)とを定めた上で決定する。しかし、経路状に血管や他の臓器や骨などの障害物がないことを確認するのは容易ではない。この確認をCT画像や透視像をもとにして行う例もある。
侵入点と到達点とを結ぶ経路を画像上で正確に確認できれば、治療効率につながり、操作者の負担も軽くなる。
本発明の目的は、侵入点と到達点とを結ぶ経路を断層画像上に正確に表示可能な表示装置を提供するものである。
更に本発明の目的は、そのために計測で求めたものでない、経路の判断しやすい新たな断層面と断層像を算出し表示可能とする表示装置を提供するものである。
本発明は、被検体の撮影で得た断層像を断層平面と直交する方向に重ねて得られる三次元画像データを格納する格納手段と、
上記三次元画像における被検体侵入具の侵入点と被検体内到達点とを設定する手段と、
この侵入点と到達点を通る第1平面、及びこの侵入点と到達点とを通り上記第1平面に所定角度をなす第2平面を設定する手段と、
第1平面と上記三次元画像データの各断層面との交点の画素値、又は交点近傍の画素値から近似した画素値を、第1平面の交点の画素値として決定し、かくして第1平面の断層画像データを算出する第1の算出手段と、
第2平面と上記三次元画像データの各断層面との交点の画素値、又は交点近傍の画素値から近似した新画素値を、第2平面の交点の画素値として決定し、かくして第2平面の断層画像データを算出する第2の算出手段と、
上記算出した第1平面の断層像、第2平面の断層像を表示する表示手段と、
を備える治療子経路表示装置を開示する。
上記三次元画像における被検体侵入具の侵入点と被検体内到達点とを設定する手段と、
この侵入点と到達点を通る第1平面、及びこの侵入点と到達点とを通り上記第1平面に所定角度をなす第2平面を設定する手段と、
第1平面と上記三次元画像データの各断層面との交点の画素値、又は交点近傍の画素値から近似した画素値を、第1平面の交点の画素値として決定し、かくして第1平面の断層画像データを算出する第1の算出手段と、
第2平面と上記三次元画像データの各断層面との交点の画素値、又は交点近傍の画素値から近似した新画素値を、第2平面の交点の画素値として決定し、かくして第2平面の断層画像データを算出する第2の算出手段と、
上記算出した第1平面の断層像、第2平面の断層像を表示する表示手段と、
を備える治療子経路表示装置を開示する。
更に本発明は、前記所定角度は90°とする治療子経路表示装置を開示する。
更に本発明は、前記格納手段は、侵入具の進行時の先端位置をCT撮影・再構成して得た先端位置近傍の複数の断層像を含むものとした治療子経路表示装置を開示する。
更に本発明は、被検体の撮影で得られた断層像を断層像平面と直交する方向に重ねて得られる3次元画像データを求め、被検体侵入具の侵入点と到達点とを同一平面内に持つ様に定めた画像表示装置を開示する。
更に本発明は、被検体の撮影で得られた断層像を断層像平面と直交する方向に重ねて得られる3次元画像データを求め、被検体侵入具の侵入点と到達点とを同一平面内に持つように定めた画像と侵入具の侵入点と到達点とを結ぷ直線を軸として回転して得られる他の画像の2つ以上を表示することの出来る画像表示装置を開示する。
更に本発明は、被検体の撮影で得られた断層像を断層平面と直交する方向に重ねて得られる3次元画像データを求め被検体侵入具侵入点と到達点とを結んで得られる直線の3次元画像データとの角度を持った侵入具挿入装置を開示する。
本発明の表示装置によれば、侵入点と到達点とを結ぶ2つの経路平面の断層像を観察でき、経路の確認や治療子の侵入の様子がわかるようになった。
本発明を治療子の穿刺経路表示装置の例で説明する。治療子とは、患者の体内に穿刺して病巣部位の治療を行う素子である。例えば肺癌の除去手段として凍結端子本体を内部に有する金属管から成る治療子を使う例がある。かかる治療子は、肺癌病巣部位まで凍結端子を穿刺して、病巣部位に到達後に、凍結端子本体の先端からその周囲に対して凍結と解凍とを繰返して病巣部位を壊死させるものである。
かかる凍結端子、及び凍結端子を含む広義の治療子を使う治療装置に関して、本件出願人は既に特許出願を行っている(特願2005−364654、特願2005−364659)。
かかる凍結端子、及び凍結端子を含む広義の治療子を使う治療装置に関して、本件出願人は既に特許出願を行っている(特願2005−364654、特願2005−364659)。
凍結端子を含む治療子の穿刺を行うためには、侵入点としての体内への穿刺入口位置と到達点としての病巣部位到達位置とを特定した上でその両者を結ぶ穿刺経路を決定し、この経路に沿うような挿入角度を与えて、その経路に沿うように治療子の穿刺を行う。
入口位置から病巣部位位置までの治療子の進行は、CT監視下で行う。CT監視とは、治療子の存在位置を含むCT断層像をリアルタイムで計測・再構成を行って表示させるものであり、治療子の侵入位置に併せて次々に断層像を得て表示させ、治療子が事前に決定した経路を進んでいるかを監視するものである。
入口位置から病巣部位位置までの治療子の進行は、CT監視下で行う。CT監視とは、治療子の存在位置を含むCT断層像をリアルタイムで計測・再構成を行って表示させるものであり、治療子の侵入位置に併せて次々に断層像を得て表示させ、治療子が事前に決定した経路を進んでいるかを監視するものである。
本発明は、かかるCT監視を行うに際して、通常のCT断層像を表示させると共に、侵入点P1と病巣目標位置即ち到達点P2とを含む新たな2つの平面Q1、Q2を設定し、この2つの平面Q1、Q2上の全画素値を、上記通常の断層像の画素値から算出する。かくして、断層面Q1、Q2での断層画像データR1、R2を得る。これを画面に表示する。画面上にはP1、P2点が明示的に表示する。平面Q1、Q2とは例えば平面間の角度βが90°(直交)である。従って、平面Q1の断層像によってQ1平面上で、治療子がP1→P2への経路をたどっているかを監視できると共に、それに直交する平面Q2上で、P1→P2への経路をたどっているかを監視できることになる。
これによって、1つの平面Q1だけではその平面上での動きだけの監視のみであるのに対し、本発明では、互いに直交する平面Q1とQ2とで立体的に動きを監視することができる。
これによって、1つの平面Q1だけではその平面上での動きだけの監視のみであるのに対し、本発明では、互いに直交する平面Q1とQ2とで立体的に動きを監視することができる。
以下、図面を利用して具体的に説明する。
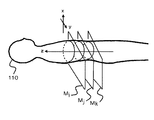
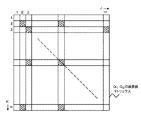
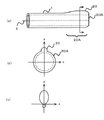
図1は、被検体110と断層面と座標系X−Y−Zとの関係を示す図である。断層面は体軸方向に複数個有し、図では模式的に、i、j、kの3断層面を示している。断層面そのものはX−Y座標系とし、体軸方向をZ座標系として、被検体の任意の点は、(X,Y,Z)の座標系で定義できる。断層面の体軸方向でのピッチは、1mm以下、例えば100分の1mmとかである。断層面の画像はCT計測で得たCT画像であり、またピッチを細かくするために補間によって新断層面のCT画像を得る例もある。
図1は、被検体110と断層面と座標系X−Y−Zとの関係を示す図である。断層面は体軸方向に複数個有し、図では模式的に、i、j、kの3断層面を示している。断層面そのものはX−Y座標系とし、体軸方向をZ座標系として、被検体の任意の点は、(X,Y,Z)の座標系で定義できる。断層面の体軸方向でのピッチは、1mm以下、例えば100分の1mmとかである。断層面の画像はCT計測で得たCT画像であり、またピッチを細かくするために補間によって新断層面のCT画像を得る例もある。
図2(a)は、治療子の挿入点P1、及び目標点(到達点)P2を示した図である。新断層面MkのP1点を挿入点、断層面MiのP2点を到達点と指定した例を示す。図2(b)が断層面Mkの断層画像上の挿入点P1、図2(c)が断層面Miの断層画像上の到達点P2であり、P1点は被検体の外皮位置、P2点は被検体の内部病巣位置に設定した。
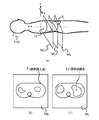
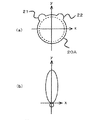
図3(a)は、点P1,P2を新断層面Q1の設定例を示す。当然の事ながら、新断層面Q1は本来のCT断層面(…Mi、…Mj、…Mk、…)と非平行である。図3(b)は、新断層面Q1上での算出画素値から成る新断層像例を示す。ここで、算出画素値とは、新平面Q1でのものであることから、計測したCT断層面(…Mi、…Mj、…Mk、…)の画素値から算出して得たものである。この算出の意味については後述する。
図3(a)は、点P1,P2を新断層面Q1の設定例を示す。当然の事ながら、新断層面Q1は本来のCT断層面(…Mi、…Mj、…Mk、…)と非平行である。図3(b)は、新断層面Q1上での算出画素値から成る新断層像例を示す。ここで、算出画素値とは、新平面Q1でのものであることから、計測したCT断層面(…Mi、…Mj、…Mk、…)の画素値から算出して得たものである。この算出の意味については後述する。
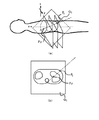
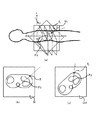
図4(a)は、新平面Q1と所定の角度βをなす新平面Q2の設定例を示す。新平面Q2は平面Q1と同じく点P1とP2とを通る平面であり、角度βは、例えば90°(直交)である。図4(b)は、平面Q1の新断層像、図4(c)は平面Q2の新断層像であり、いずれも算出された画素値より成る。
かかるP1とP2とを通る互いに角度βをなす2つの新平面Q1とQ2との新断層像を表示することで、P1とP2との経路がどんなものであるか、その途中に障害物があるかがわかることになり、P1、P2の評価が可能となる。また、治療子の挿入角度θの設定及び評価が可能となる。そして、もし、更に別のP1、P2、θの設定が良いと判断されれば、別個にP1、P2、θを設定し直し、同様の表示を行って評価をすればよい。
かかるP1とP2とを通る互いに角度βをなす2つの新平面Q1とQ2との新断層像を表示することで、P1とP2との経路がどんなものであるか、その途中に障害物があるかがわかることになり、P1、P2の評価が可能となる。また、治療子の挿入角度θの設定及び評価が可能となる。そして、もし、更に別のP1、P2、θの設定が良いと判断されれば、別個にP1、P2、θを設定し直し、同様の表示を行って評価をすればよい。
次に、平面Q1とQ2との設定を説明する。
Q1とQ2とが互いに直交する平面であるとすると、平面Q1を定めると、平面Q2は1つしかなく一義的に定まる。然るに平面Q1はP1とP2とを含む平面であり無数に存在する。そこで、事前に、穿刺経路上にあって侵入の障害物(例えば血管とか骨とか)がなく、経路監視のしやすい平面Q1候補がいくつか存在する。一方、これらの各平面Q1候補についてそれぞれに直交する平面Q2候補が定まる。平面Q2候補にあっても障害物が経路上にないことが必要である。こうしたQ1とQ2の各候補の中で、障害物がなく、監視しやすい経路を有する平面をQ1、Q2として決定する。これらの決定法は、術者によって画面を見ながら行うが、ソフトウェアによって行うやり方もある。
Q1とQ2とが互いに直交する平面であるとすると、平面Q1を定めると、平面Q2は1つしかなく一義的に定まる。然るに平面Q1はP1とP2とを含む平面であり無数に存在する。そこで、事前に、穿刺経路上にあって侵入の障害物(例えば血管とか骨とか)がなく、経路監視のしやすい平面Q1候補がいくつか存在する。一方、これらの各平面Q1候補についてそれぞれに直交する平面Q2候補が定まる。平面Q2候補にあっても障害物が経路上にないことが必要である。こうしたQ1とQ2の各候補の中で、障害物がなく、監視しやすい経路を有する平面をQ1、Q2として決定する。これらの決定法は、術者によって画面を見ながら行うが、ソフトウェアによって行うやり方もある。
平面Q1とQ2とは直交させない例もある。例えば適切な直交平面Q2が見いだせなかった場合には、直交平面以外の平面Q2を選ぶ必要がある。また、直交平面以外の角度の平面Q2が経路監視に適した例もある。こうした場合も、平面Q1に対応する所定の回転角度β(≠90°)の関係にある平面Q2を事前に決定しておく。例えばβ=60°の事例では、Q1に対して4個の60°平面Q2があり、どれかに特定する。
平面Q1とQ2上での新画素値の算出を図5で説明する。平面Q1はm×nの画素数のマトリックス構成である。この画素値算出は、ソフトウェアによって自動的に行う。平面Q1とCT断層面との角度は90°以外の角度αである。穿刺入口P1が皮膚表面であって病巣位置P2が内部である故にP1とP2とを結ぶ平面Q1は、CT平面に対して90°以外の角度になるからである。
平面Q1上の画素位置を(J,K)とし、CT断層平面の画素位置を(X,Y)とし、CT断層面の体軸方向の座標をZとする。CT断層面を手前からM1、M2、…Mnとする。こうしたCT断層面M1、M2、…Mnが並んであり、これに角度αで平面Q1がCT断層面M1、M2、…Mnを切断(角度αでの交叉)するような関係である。
そこで、その全交叉位置での、Q1平面の座標(J,K)とそれに交叉するCT断層面M1、M2、…Mnの座標(X,Y)に、図5の斜線画素位置の如き、画素値があれば、それをQ1平面の対応座標の画素値とする。座標(X,Y)に、図5の非斜線画素位置の如き、画素値がない場合が多く、この場合には座標(X,Y)の周囲2点とか4点とかの画素値から近似算出した近似画素値を座標(J,K)の画素値とする。この算出は、平均値とするとか、距離差を考慮した比例配分値とするとかである。算出しないで、最も違い位置の画素値をそのまま利用する例もある。
平面Q2についても同様である。
平面Q1上の画素位置を(J,K)とし、CT断層平面の画素位置を(X,Y)とし、CT断層面の体軸方向の座標をZとする。CT断層面を手前からM1、M2、…Mnとする。こうしたCT断層面M1、M2、…Mnが並んであり、これに角度αで平面Q1がCT断層面M1、M2、…Mnを切断(角度αでの交叉)するような関係である。
そこで、その全交叉位置での、Q1平面の座標(J,K)とそれに交叉するCT断層面M1、M2、…Mnの座標(X,Y)に、図5の斜線画素位置の如き、画素値があれば、それをQ1平面の対応座標の画素値とする。座標(X,Y)に、図5の非斜線画素位置の如き、画素値がない場合が多く、この場合には座標(X,Y)の周囲2点とか4点とかの画素値から近似算出した近似画素値を座標(J,K)の画素値とする。この算出は、平均値とするとか、距離差を考慮した比例配分値とするとかである。算出しないで、最も違い位置の画素値をそのまま利用する例もある。
平面Q2についても同様である。
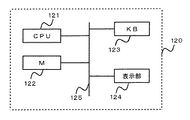
図6は、本発明の表示装置のシステム図である。表示装置120は、共通パス125にCPU121、メモリ(M)122、キーボード123、表示部124をつなげた構成であり、メモリ122には、図1に示した如き複数断層面の断層像が格納され、これをキーボード123の指示によりCPU121の働きで読み出し、表示部124に書く断層像順に表示する。そこから、操作者が表示画面を見て、P1,P2点を指示する。書く断層像の順次表示で手間がかかる故に、全断層像を三次元的に表示させて、そこからP1,P2点を指示するやり方もある。
更に、図6では、P1,P2点を通る平面Q1、Q2を手動又は自動にて指定する。例えばキーボード123で指示する。CPU121は、この指示を受けて、平面Q1、Q2の新断層像データR1、R2を算出する。
図7は、図6での処理フローを示す、ステップS20でCT画像を取得してメモリ122に格納する。ステップS21は、必要な断層面のCT画像を順次表示させて、その中から挿入点となる断層面Mk、到達点となる断層面Miを選択し指示する。ステップS22は、その断層面Mk、Mi上で点P1,P2を指定する。ステップS23では点P1,P2を通る第1平面Q1、第2平面Q2を指定し、ステップS24でその画素値を算出し、ステップS24で表示を行う。表示を見て適切な経路か否か判断し、不適切であればステップS21に戻り、適切であれば、Mj、Mk、P1、P2 、Q1、Q2並びに挿入角度θとして決定する。
病巣部位が複数個点在している例がある。これは、X、Y、Z軸でみると、P2の座標X、Y、Zがそれぞれ異なりP21(X、Y、Z)、P22(X、Y、Z)、P23(X3、Y3、Z3)、…であったりすることであり、基本的にはどれか1点を到達点として定め、他点はCT監視下で治療子を移動させるやり方をとる。この場合、事前にP1とP21、P1とP22、P1とP23の如き組合せで経路のチェックを、前述の如き新平面、新断層像を造り表示させて行い、全点に関しての障害等チェックを行うことが好ましい。
次に、リアルタイムでのCT画像の形成法について説明する。
CT断層面M1、M2、…Mnのすべてについて治療子の位置いかんを問わず、その都度、計測し再構成する必要はない。治療子の現在位置を中心とするその近辺のみの断層面のCT画像を計測・再構成し、それ以外の断層面のCT画像はそれ迄に得た過去の画像を利用する。例えばある時点での治療子の先端位置をZiとしたとき、Zi近傍のi=i±γの幅内断層面(γは近傍値であり、数個の断層数〜数10個の断層数となる値である)で計測を行い、断層像を得る。かくして、リアルタイム性を維持してCT計測・再構成が可能となる。
この場合、Q1平面、Q2平面についてのCT断層面の中でi=i±γの断層面がリアルタイム性を維持したCT画素値を提供し、その他の断層面はその時点以前に計測・再構成したCT画素値である。
CT断層面M1、M2、…Mnのすべてについて治療子の位置いかんを問わず、その都度、計測し再構成する必要はない。治療子の現在位置を中心とするその近辺のみの断層面のCT画像を計測・再構成し、それ以外の断層面のCT画像はそれ迄に得た過去の画像を利用する。例えばある時点での治療子の先端位置をZiとしたとき、Zi近傍のi=i±γの幅内断層面(γは近傍値であり、数個の断層数〜数10個の断層数となる値である)で計測を行い、断層像を得る。かくして、リアルタイム性を維持してCT計測・再構成が可能となる。
この場合、Q1平面、Q2平面についてのCT断層面の中でi=i±γの断層面がリアルタイム性を維持したCT画素値を提供し、その他の断層面はその時点以前に計測・再構成したCT画素値である。
本発明の治療装置の実施例を説明する。
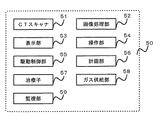
図8は、治療装置50の全体構成例図である。治療装置50は、CTスキャナ51、画像処理部52、表示部53、操作部54、駆動制御部55、計画部56、治療子57、ガス供給部58、監視部59、を具える。
図8は、治療装置50の全体構成例図である。治療装置50は、CTスキャナ51、画像処理部52、表示部53、操作部54、駆動制御部55、計画部56、治療子57、ガス供給部58、監視部59、を具える。
CTスキャナ51と画像処理部52と、表示部53と操作部54とは、本来のCT装置である。このCT装置を利用して事前に複数の断層像を取得し、三次元画像を形成しておく。複数の断層像から、更にその隙間を埋め合わせるための補間画像を三次元画像として利用する例もある。
CT装置51は、穿刺動作時のリアルタイムCT画像を得るのにも利用する。そしてこのリアルタイム画像は、監視部59での治療子57の穿刺動作をも併せて重ねて得ており、穿刺の追跡監視・治療監視に利用する。
計画部56は、画像処理部52と共同して、事前に得たデータに基づいて、又はこれと治療子57の形状(及び又は構造)データとに基づいて穿刺開始位置(挿入点)、治療部位(到達点)、その治療子の進行ルートの決定をデータ処理にて行い計画データを作成する。また熱持性や病巣部位物性値(生理値を含む)に基づくガス供給制御法を決定する。
計画部56は、画像処理部52と共同して、事前に得たデータに基づいて、又はこれと治療子57の形状(及び又は構造)データとに基づいて穿刺開始位置(挿入点)、治療部位(到達点)、その治療子の進行ルートの決定をデータ処理にて行い計画データを作成する。また熱持性や病巣部位物性値(生理値を含む)に基づくガス供給制御法を決定する。
駆動制御部55は、計画部56の計画データに基づいて治療子57の移動等の駆動制御並びにガス供給部58の供給制御を行い、凍結と解凍との交互動作を行う。
監視部59は、駆動制御の監視を行う。監視には、CT画像による監視と制御の仕組みの監視とがある。監視部59は、表示部53が兼務してもよい。
ここで、画像処理部52及び計画部56の一部が前記経路表示装置に相当する。
。この治療装置50は、治療子として凍結端子を用いた例であり、凍結端子及びその治療装置については先に示した先願がある。
監視部59は、駆動制御の監視を行う。監視には、CT画像による監視と制御の仕組みの監視とがある。監視部59は、表示部53が兼務してもよい。
ここで、画像処理部52及び計画部56の一部が前記経路表示装置に相当する。
。この治療装置50は、治療子として凍結端子を用いた例であり、凍結端子及びその治療装置については先に示した先願がある。
本発明の治療装置50は、以下の処理及び動作を行う。
(1)凍結端子の穿刺入口位置P1と病巣位置P2とを決定する。この決定は、体軸方向に撮影・再構成した複数のCT断層像から選び、例えば断層面Ziの座標位置(Xa,Ya)をP1、断層面Zjの座標位置(Xb,Yb)をP2とする。選択の仕方は、例えばCT断層像を次々に体軸方向に沿って表示させ、操作者がZi、Zjの断層面、及びその面上の座標としての点P1、P2を指定するやり方、又は上記先願と同じく、体軸上に沿う三次元画像の三次元輪郭画像をみて決定する。
(2)点P1、P2とを通る平面Q1及びそれに直交する平面Q2、又は所定の角度をなす平面Q2を決定する。
これは画像処理部52と計画部56と用いてソフトウェアによる処理を利用する。
(3)駆動制御部56の働きにより穿刺動作を開始する。その監視は、監視部59で行う。穿刺動作の監視のために、X線CT装置によって、例えばマルチスライス計測(1回で複数断面の撮影を可能にする構造)によりCT撮影・再構成を行いCT断層像を得る。撮影範囲は、凍結端子の先端部近傍であり、凍結端子の穿刺の進行に併せて先端位置が進行し、その進行に応じて先端部近傍を次々にCT撮影・再構成を行いCT断層像を得る。
(4)CT監視下で得た最新断層像は、監視部59によって、メモリに記憶させた上で次々に表示部53に表示して進行の監視に利用する。これと併せて、画像処理部52と計画部56とで、本願発明の特徴の1つである上記(2)で決定したQ1、Q2平面上でのCT画素値を算出し、Q1、Q2平面上の画素位置(座標位置)対応に埋め込み断層像R1、R2を得、これを表示装置に表示する。
この断層像R1、R2を得るに際して、凍結端子の先端近傍に含まれる複数の断層面は、リアルタイムで得た断層画像を持つものであり、それ以外の断層面はそれ以前に得られた断層画像を持つものである。ここで、以前の断層像とは、穿刺動作に入る前に撮影して得た断層像又は先端位置の進行時にその先端位置よりも手前側で撮影して得た直前の断層像を含む。
(5)かくして、凍結端子の穿刺の経路を、最新のCT断層像及びQ1、Q2平面上での断層像が表示されることで、リアルタイムで監視できる。もし、経路をずれる様子があれば最新の断層像及びQ1、Q2平面上の断層像をみて凍結端子の方向の修正が可能となる。例えばQ1平面上で距離にして2mmずれとかQ2平面上で距離にして3mmずれとかの判断が可能となり、それを正しい経路に戻す操作を、凍結端子に行う。凍結端子がアクチュエーターで自動的に動くのであれば、その修正動作指令を与えたり、操作者の手動で行っているのであれば、手動操作で正規経路に戻す。
(1)凍結端子の穿刺入口位置P1と病巣位置P2とを決定する。この決定は、体軸方向に撮影・再構成した複数のCT断層像から選び、例えば断層面Ziの座標位置(Xa,Ya)をP1、断層面Zjの座標位置(Xb,Yb)をP2とする。選択の仕方は、例えばCT断層像を次々に体軸方向に沿って表示させ、操作者がZi、Zjの断層面、及びその面上の座標としての点P1、P2を指定するやり方、又は上記先願と同じく、体軸上に沿う三次元画像の三次元輪郭画像をみて決定する。
(2)点P1、P2とを通る平面Q1及びそれに直交する平面Q2、又は所定の角度をなす平面Q2を決定する。
これは画像処理部52と計画部56と用いてソフトウェアによる処理を利用する。
(3)駆動制御部56の働きにより穿刺動作を開始する。その監視は、監視部59で行う。穿刺動作の監視のために、X線CT装置によって、例えばマルチスライス計測(1回で複数断面の撮影を可能にする構造)によりCT撮影・再構成を行いCT断層像を得る。撮影範囲は、凍結端子の先端部近傍であり、凍結端子の穿刺の進行に併せて先端位置が進行し、その進行に応じて先端部近傍を次々にCT撮影・再構成を行いCT断層像を得る。
(4)CT監視下で得た最新断層像は、監視部59によって、メモリに記憶させた上で次々に表示部53に表示して進行の監視に利用する。これと併せて、画像処理部52と計画部56とで、本願発明の特徴の1つである上記(2)で決定したQ1、Q2平面上でのCT画素値を算出し、Q1、Q2平面上の画素位置(座標位置)対応に埋め込み断層像R1、R2を得、これを表示装置に表示する。
この断層像R1、R2を得るに際して、凍結端子の先端近傍に含まれる複数の断層面は、リアルタイムで得た断層画像を持つものであり、それ以外の断層面はそれ以前に得られた断層画像を持つものである。ここで、以前の断層像とは、穿刺動作に入る前に撮影して得た断層像又は先端位置の進行時にその先端位置よりも手前側で撮影して得た直前の断層像を含む。
(5)かくして、凍結端子の穿刺の経路を、最新のCT断層像及びQ1、Q2平面上での断層像が表示されることで、リアルタイムで監視できる。もし、経路をずれる様子があれば最新の断層像及びQ1、Q2平面上の断層像をみて凍結端子の方向の修正が可能となる。例えばQ1平面上で距離にして2mmずれとかQ2平面上で距離にして3mmずれとかの判断が可能となり、それを正しい経路に戻す操作を、凍結端子に行う。凍結端子がアクチュエーターで自動的に動くのであれば、その修正動作指令を与えたり、操作者の手動で行っているのであれば、手動操作で正規経路に戻す。
本発明は、穿刺経路計画の作成や確認用にも使用できるので、以下説明する。
経路計画の作成や確認用では、リアルタイム性は不要であるので、すべて作成や確認のために事前に撮影・再構成した断層像を使う。こうした断層像を記憶装置に格納させた上で、P1、P2とを通る2つの平面Q1、Q2の断層像を作成(算出)し表示させて、P1、P2との確定を行う。ここで、P2は病巣部位であるため固定であり、従ってP1をどこに設定するかがポイントである。かかる適切なP1を売るために平面Q1、Q2の断層像を作成表示させ、探索し確定する。以上は作成用であるが、別法により作成したP1とP2との経路確認時にも、同様の表示を行って適切な設定であるか否かを確認できる。
以上の実施例では、凍結端子の事例としたが、それ以外の治療子、例えば患部をはぎとってくる、検査や治療のための素子、患部の監視のために侵入する素子(超小型カメラや光ファイバー端子)、超音波は電磁波などのエネルギーを患部に照射する素子、等種々のものに適用できる。
経路計画の作成や確認用では、リアルタイム性は不要であるので、すべて作成や確認のために事前に撮影・再構成した断層像を使う。こうした断層像を記憶装置に格納させた上で、P1、P2とを通る2つの平面Q1、Q2の断層像を作成(算出)し表示させて、P1、P2との確定を行う。ここで、P2は病巣部位であるため固定であり、従ってP1をどこに設定するかがポイントである。かかる適切なP1を売るために平面Q1、Q2の断層像を作成表示させ、探索し確定する。以上は作成用であるが、別法により作成したP1とP2との経路確認時にも、同様の表示を行って適切な設定であるか否かを確認できる。
以上の実施例では、凍結端子の事例としたが、それ以外の治療子、例えば患部をはぎとってくる、検査や治療のための素子、患部の監視のために侵入する素子(超小型カメラや光ファイバー端子)、超音波は電磁波などのエネルギーを患部に照射する素子、等種々のものに適用できる。
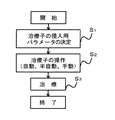
図9は、凍結端子を治療子とする治療装置の処理フローを示す。ステップS1では、CT画像データを体軸方向に沿って複数枚(数10枚以上)取得する。これはCT装置による。また事前にCT装置で取得してメモリに格納した被検体のメモリへの格納画像を用いることもある。
ステップS2は、侵入用パラメータである挿入点、治療対象である病巣部位の目標点、挿入角度より成る治療子パラメータを決定する。このステップS2では、本願発明の穿刺経路表示装置を利用する。
ステップS3は、そのパラメータを用いての実際の穿刺及び治療の動作を行う。治療に際しては、病巣目標点に到達したならば凍結と解凍とを凍結端子の先端部で繰返させて病巣の壊死を行う。この動作は、自動、半自動、手動のいずれでもよい。
ステップS2は、侵入用パラメータである挿入点、治療対象である病巣部位の目標点、挿入角度より成る治療子パラメータを決定する。このステップS2では、本願発明の穿刺経路表示装置を利用する。
ステップS3は、そのパラメータを用いての実際の穿刺及び治療の動作を行う。治療に際しては、病巣目標点に到達したならば凍結と解凍とを凍結端子の先端部で繰返させて病巣の壊死を行う。この動作は、自動、半自動、手動のいずれでもよい。
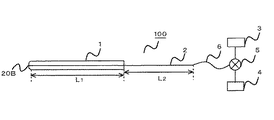
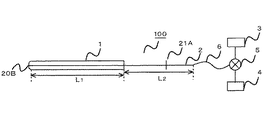
図10は、凍結端子である治療子100の概略図である。治療子100は、二重管(一重管の例もある。以下同じ。)1と凍結端子本体2、及びそれにつながる管路6、切替バルブ5、高圧ヘリウムガス供給源3、高圧アルゴンガス供給源4、より成る。管1の長さL1、凍結端子本体2の外部露出部の長さL2とすると、この治療子100は略(L1+L2)の長さの直線成分と考えてよく、かかる直線成分を刃物状の最先端20Bから挿入点P1から病巣部位の一点である目標点P2にまで侵入させてゆくことを想定して、その時の挿入角度θ,P1,P2,P1→P2(ルート)を算出できる。
凍結端子100の二重管の先端部に方向によって熱持性を異ならしめた例を図11、図12に示す。管の先端は、凍結と解凍との2つの動作部位であり、いわゆる熱交換機能を果たす。癌病巣である病巣部位も種々の形状を有し、どのような方向から穿刺するのが効率的凍結法であるかも重要な検討事項である。更に病巣に近接する正常組織を凍結・解凍(特に凍結)から保護する必要もある。そこで方向性のある熱の指向特性に大小を持たせて病巣部位に応じた集中的に熱エネルギー付与のための熱分布特性を与える。これが図12に示す管の実施例図である。
図11(a)は、二重金属管1の最先端20Bの直前の先端部20Aの周囲の一部を突起させて突起部20を設けた例である。その矢印断面は、図11(b)に示すように外方に向かって丸みを帯びた形状であり、その熱指向特性は図11(c)となる。先端部20Aの最先端20Bは穿刺の先端で刃物状であり、穿刺しやすく、且つ深部方向に熱指向特性を持たせるようにする例もある。
図12(a)は、先端部20Aに、2つの突起部21,22を持たせて熱指向特性を細長くさせた例である。これによって、図12(b)に示すようにy方向の(+)方向に鋭い熱指向特性を持たせた。
先端部20A及び20Bは、凍結・解凍に関与する部位である。
先端部20A及び20Bは、凍結・解凍に関与する部位である。
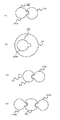
図13に、この先端形状に特徴を持つ治療子の使用例を示す。図13(a)は、球形状の癌病巣23の側面に治療子100を穿刺させて癌病巣23をその指向特性に基づいて熱エネルギーを与えて壊死させる例を示す。この癌病巣23は、組織的にしっかりした例であり、病巣23に直接穿刺させるよりは囲りから壊死させるに適したものである。
図13(b)は癌病巣24の内部左側に穿刺し、右側への方向性を持つ治療子100で治療させた例である。これも、病巣全体の壊死に役立つ。
図13(c)は、血管24が近くにあり、この血管24から遠ざけて病巣23を治療を行なうときの事例である。血管24の反対側(右側)に治療子100を穿刺した。これは、血管を傷つけないことの他に、血管の温度の治療への影響を少なくしたいこと、の目的を持つ。図13(d)は、2つ以上の治療子100A,100Bを用いて、病巣23の両側に穿刺して同時治療を行なった例である。図13(d)は、病巣サイズが大きい事例に効果を持つ。
図13(b)は癌病巣24の内部左側に穿刺し、右側への方向性を持つ治療子100で治療させた例である。これも、病巣全体の壊死に役立つ。
図13(c)は、血管24が近くにあり、この血管24から遠ざけて病巣23を治療を行なうときの事例である。血管24の反対側(右側)に治療子100を穿刺した。これは、血管を傷つけないことの他に、血管の温度の治療への影響を少なくしたいこと、の目的を持つ。図13(d)は、2つ以上の治療子100A,100Bを用いて、病巣23の両側に穿刺して同時治療を行なった例である。図13(d)は、病巣サイズが大きい事例に効果を持つ。
以上の各実施例で、突起形状の種類や態様は、どのような指向特性を持たせるかで定まる。突起形状の代わりに内側方向に凹部を持たせるやり方もある。指向特性を実現する突起形状(凹部を含む)は、計算機によって求めることができる。種々の突起形状の管を用意しておき、病巣や治療の目的に沿って使い分けるやり方もある。
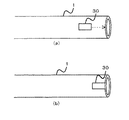
図14(a)は、二重管の他の実施例図である。図11では、固定突起形状化したが、図14では可動翼30を二重管1の外部側面に沿って設けておき、この可動翼30を、管の先端部まで図14(b)の如く移動させ、図11の如き突起状形状化させる。可動翼30は例えばスプリングで移動させる。これは、例えば凍結端子の進行に応じてスプリングを凍結端子に連動させるやり方をとる。この場合、可動翼30が人体を傷つけないように周囲に丸みを作っておく。
使い方は、人体挿入時には、図14(a)の如くしておき、患部到達時に図15(b)の如く移動させて使う。
使い方は、人体挿入時には、図14(a)の如くしておき、患部到達時に図15(b)の如く移動させて使う。
図15は、凍結端子本体2の途中に操作に便となる操作(タッチ)部21Aを設けた実施例を示す。タッチ部21Aは手で握れる程度の大きさがあればよく、例えば端子本体2の直交方向に若干延びたバー形状体である。タッチ部21Aによって、凍結端子本体2の進行、端子自体の回転(Φ)を確実に行える利点がある。このタッチ部にアクチュエーターをつけておくことで、自動化、半自動化の操作が可能となる。
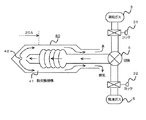
図16は凍結端子の具体例図である。40が凍結端子本体であり、熱伝導性の低い素材、例えば金属より成り、その内部には、熱交換機構41を持つ。切替バルブ5を介して高圧ガスが流入し、その先端開放部42から本体40の内側に放出し外部へ排気を行う。尚、31、32は各ガス毎のコックである。
温度特性(温度変化)について説明する。
その具体例を図17に示す。図17(a)は、凍結ピーク温度と解凍ピーク温度とを同一絶対値T1(実際には凍結時−T1、解凍時+T1)とした1サイクル例である。両者で熱エネルギーが相殺されることが好ましいため、凍結時と解凍時との(温度)×(時間)で定まる面積は同一面積(S1)とする。図17(b)は、凍結ピーク温度と解凍ピーク温度との絶対値をT1、T2(T1>T2)とした例である。T1>T2の故に、同一面積S1の達成のために、解凍期間を凍結期間よりも大きくとる。尚、17(a)、(b)の変形例として、凍結1回、解凍2回で1サイクルの如き例もありうる。
図17(c)は凍結と解凍との2サイクル供与例である。3サイクル以上の例もある。
尚、面積を凍結と解凍とで同一としたが、病巣の壊死という目的達成が得られるのであれば、厳密な同一性は必要ない。人間の治療部位には38℃とかの体温がある故に、かかる体温を考慮して、実際の温度特性を定めることが多い。
かかる種々の温度特性(温度変化)を実現するためには、治療子100へのヘリウムとアルゴンとの両者のガス供給を、量と時間とをパラメータとして制御すればよい。
その具体例を図17に示す。図17(a)は、凍結ピーク温度と解凍ピーク温度とを同一絶対値T1(実際には凍結時−T1、解凍時+T1)とした1サイクル例である。両者で熱エネルギーが相殺されることが好ましいため、凍結時と解凍時との(温度)×(時間)で定まる面積は同一面積(S1)とする。図17(b)は、凍結ピーク温度と解凍ピーク温度との絶対値をT1、T2(T1>T2)とした例である。T1>T2の故に、同一面積S1の達成のために、解凍期間を凍結期間よりも大きくとる。尚、17(a)、(b)の変形例として、凍結1回、解凍2回で1サイクルの如き例もありうる。
図17(c)は凍結と解凍との2サイクル供与例である。3サイクル以上の例もある。
尚、面積を凍結と解凍とで同一としたが、病巣の壊死という目的達成が得られるのであれば、厳密な同一性は必要ない。人間の治療部位には38℃とかの体温がある故に、かかる体温を考慮して、実際の温度特性を定めることが多い。
かかる種々の温度特性(温度変化)を実現するためには、治療子100へのヘリウムとアルゴンとの両者のガス供給を、量と時間とをパラメータとして制御すればよい。
温度特性(温度変化)の実現化及びガス供給制御法の決定について説明する。
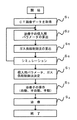
i.被検体病巣部位の比熱、導伝率などの熱的定数及び体積重量を取り入れた病巣部位の形状などの物理的定数を考慮して、その物体の温度の時間変化を決定する。
ii.被検体の熱的定数、物理定数を考慮した侵入具到達点周辺の時間に対する温度変化を計算し、設定温度に対する動的変化又は動的変化に至る設定時間を決定し得る如く定める。
iii.この定めた到達点近傍の熱的時間変化について設定目的の温度変化となる様に侵入具の回転角を決定する。
iv.書く熱持性の異なる複数の侵入具の挿入に対する、到達点部位及びその近傍周辺の部位の熱的温度の時間変化を決定する。
v.この複数の熱的方向性を有した侵入具が上記決定された幾可学的定数のもとで侵入具が到達点及びその近傍において熱的温度の時間変化を繰り返し、試験操作を行いその結果から被検体への侵入開始位置、侵入具の輪郭上の到達点、侵入方向、侵入具の角度及び回転角、開始位置から到達点までの進行ルート、の少なくともいずれか1つを求め決定しかつ周辺物体の温度分布及び時間変化を決定する。
vi.上記侵入具の先端に装備された熱交換器の発熱、吸熱を切換えるガス流入路のガス切換えスイッチを到達点近傍の定められた温度変化になるようなガス量と供給シーケンス(タイミング)とのガス供給制御法を求める。治療時には、侵入用パラメータに従って穿刺を行い、治療部位到達後には上記ガス供給制御法によってガス供給を行う。
i.被検体病巣部位の比熱、導伝率などの熱的定数及び体積重量を取り入れた病巣部位の形状などの物理的定数を考慮して、その物体の温度の時間変化を決定する。
ii.被検体の熱的定数、物理定数を考慮した侵入具到達点周辺の時間に対する温度変化を計算し、設定温度に対する動的変化又は動的変化に至る設定時間を決定し得る如く定める。
iii.この定めた到達点近傍の熱的時間変化について設定目的の温度変化となる様に侵入具の回転角を決定する。
iv.書く熱持性の異なる複数の侵入具の挿入に対する、到達点部位及びその近傍周辺の部位の熱的温度の時間変化を決定する。
v.この複数の熱的方向性を有した侵入具が上記決定された幾可学的定数のもとで侵入具が到達点及びその近傍において熱的温度の時間変化を繰り返し、試験操作を行いその結果から被検体への侵入開始位置、侵入具の輪郭上の到達点、侵入方向、侵入具の角度及び回転角、開始位置から到達点までの進行ルート、の少なくともいずれか1つを求め決定しかつ周辺物体の温度分布及び時間変化を決定する。
vi.上記侵入具の先端に装備された熱交換器の発熱、吸熱を切換えるガス流入路のガス切換えスイッチを到達点近傍の定められた温度変化になるようなガス量と供給シーケンス(タイミング)とのガス供給制御法を求める。治療時には、侵入用パラメータに従って穿刺を行い、治療部位到達後には上記ガス供給制御法によってガス供給を行う。
図18は、温度特性を考慮した処理フローを示す。図9に比べて、ステップS2とS3との間に新たなステップS5、S6、S7を付加した。ステップS5では、前述の温度特性の決定、及びそれに基づくガス供給制御法の算出を行う。ステップS6はステップS2、S58で算出したパラメータ、温度特性、並びにガス供給制御法に基づく治療シミュレーションを行う。シミュレーションの結果、治療効果がないとの判定であればステップS2へ戻る。治療効果があるとの判定であればステップS7へ進み、最終決定を行う。
1 1重又は2重の金属管
2 凍結端子本体
100 治療子
110 被検体
2 凍結端子本体
100 治療子
110 被検体
Claims (6)
- 被検体の撮影で得た断層像を断層平面と直交する方向に重ねて得られる三次元画像データを格納する格納手段と、
上記三次元画像における被検体侵入具の侵入点と被検体内到達点とを設定する手段と、
この侵入点と到達点を通る第1平面、及びこの侵入点と到達点とを通り上記第1平面に所定角度をなす第2平面を設定する手段と、
第1平面と上記三次元画像データの各断層面との交点の画素値、又は交点近傍の画素値から近似した画素値を、第1平面の交点の画素値として決定し、かくして第1平面の断層画像データを算出する第1の算出手段と、
第2平面と上記三次元画像データの各断層面との交点の画素値、又は交点近傍の画素値から近似した新画素値を、第2平面の交点の画素値として決定し、かくして第2平面の断層画像データを算出する第2の算出手段と、
上記算出した第1平面の断層像、第2平面の断層像を表示する表示手段と、
を備える治療子経路表示装置。 - 上記所定角度は90°とする請求項1の治療子経路表示装置。
- 上記格納手段は、侵入具の進行時の先端位置をCT撮影・再構成して得た先端位置近傍の複数の断層像を含むものとした請求項1の治療子経路表示装置。
- 被検体の撮影で得られた断層像を断層像平面と直交する方向に重ねて得られる3次元画像データを求め、被検体侵入具の侵入点と到達点とを同一平面内に持つ様に定めた画像表示装置。
- 被検体の撮影で得られた断層像を断層像平面と直交する方向に重ねて得られる3次元画像データを求め、被検体侵入具の侵入点と到達点とを同一平面内に持つように定めた画像と侵入具の侵入点と到達点とを結ぷ直線を軸として回転して得られる他の画像の2つ以上を表示することの出来る画像表示装置。
- 被検体の撮影で得られた断層像を断層平面と直交する方向に重ねて得られる3次元画像データを求め被検体侵入具侵入点と到達点とを結んで得られる直線の3次元画像データとの角度を持った侵入具挿入装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006034911A JP2007209651A (ja) | 2006-02-13 | 2006-02-13 | 治療子経路表示装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006034911A JP2007209651A (ja) | 2006-02-13 | 2006-02-13 | 治療子経路表示装置 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007209651A true JP2007209651A (ja) | 2007-08-23 |
Family
ID=38488556
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006034911A Withdrawn JP2007209651A (ja) | 2006-02-13 | 2006-02-13 | 治療子経路表示装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2007209651A (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012147652A1 (ja) * | 2011-04-27 | 2012-11-01 | 株式会社デージーエス・コンピュータ | 穿刺治療支援方法および穿刺治療支援装置ならびに穿刺治療支援装置用プログラム |
| EP2526869A2 (en) | 2011-05-23 | 2012-11-28 | Fujifilm Corporation | Image processing device, radiographic image capture system, image processing method and image processing program storage medium |
| JP2013154161A (ja) * | 2012-06-14 | 2013-08-15 | Toshiba Corp | X線ct装置 |
| JP2017051649A (ja) * | 2016-11-16 | 2017-03-16 | 東芝メディカルシステムズ株式会社 | X線ct装置、x線ctシステム |
| JP2018505010A (ja) * | 2015-02-23 | 2018-02-22 | クール セラピューティクス, インコーポレイテッド | 凍結された粒子の気管内送達のためのシステムおよび方法 |
-
2006
- 2006-02-13 JP JP2006034911A patent/JP2007209651A/ja not_active Withdrawn
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012147652A1 (ja) * | 2011-04-27 | 2012-11-01 | 株式会社デージーエス・コンピュータ | 穿刺治療支援方法および穿刺治療支援装置ならびに穿刺治療支援装置用プログラム |
| EP2526869A2 (en) | 2011-05-23 | 2012-11-28 | Fujifilm Corporation | Image processing device, radiographic image capture system, image processing method and image processing program storage medium |
| JP2012239745A (ja) * | 2011-05-23 | 2012-12-10 | Fujifilm Corp | 画像処理装置、放射線画像撮影システム、画像処理プログラム、及び画像処理方法 |
| JP2013154161A (ja) * | 2012-06-14 | 2013-08-15 | Toshiba Corp | X線ct装置 |
| JP2018505010A (ja) * | 2015-02-23 | 2018-02-22 | クール セラピューティクス, インコーポレイテッド | 凍結された粒子の気管内送達のためのシステムおよび方法 |
| JP2017051649A (ja) * | 2016-11-16 | 2017-03-16 | 東芝メディカルシステムズ株式会社 | X線ct装置、x線ctシステム |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7871406B2 (en) | Methods for planning and performing thermal ablation | |
| JP5214120B2 (ja) | 心房細動を治療するための案内された手技 | |
| US20100185087A1 (en) | Methods and apparatuses for performing and monitoring thermal ablation | |
| JP6695882B2 (ja) | Copdおよび肺気腫を処置するためのシステムおよび方法 | |
| CN111248998B (zh) | 用于超声图像引导的消融天线放置的系统和方法 | |
| US20090196480A1 (en) | Methods And Apparatuses For Planning, Performing, Monitoring And Assessing Thermal Ablation | |
| JP5095149B2 (ja) | 侵襲的手技のシミュレーション | |
| US20080033417A1 (en) | Apparatus for planning and performing thermal ablation | |
| US20080033419A1 (en) | Method for planning, performing and monitoring thermal ablation | |
| US12178514B2 (en) | Volumetric imaging | |
| JP4448818B2 (ja) | 医療装置 | |
| JP7538214B2 (ja) | 切除術を監視するシステムおよび方法 | |
| WO2012147652A1 (ja) | 穿刺治療支援方法および穿刺治療支援装置ならびに穿刺治療支援装置用プログラム | |
| WO2008112005A1 (en) | Methods and systems for planning, performing and monitoring thermal ablation | |
| JP2007054622A (ja) | 心房細動のカテーテルベースの治療の標準化 | |
| JP2013135738A (ja) | 手術支援システム | |
| US10687774B2 (en) | Method and apparatus for visualizing a blood vessel | |
| JP5731267B2 (ja) | 治療支援システム及び医用画像処理装置 | |
| CN105007815A (zh) | 使用光相干层析探头的器官映射系统 | |
| EP1463437A2 (en) | Planning and facilitation systems and methods for cryosurgery | |
| JP2000237205A (ja) | 超音波治療装置 | |
| US20250127573A1 (en) | Volumetric imaging | |
| US20080033418A1 (en) | Methods for monitoring thermal ablation | |
| JP2007209651A (ja) | 治療子経路表示装置 | |
| JP4807830B2 (ja) | 画像診断装置及び治療支援システム |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A300 | Application deemed to be withdrawn because no request for examination was validly filed |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20090512 |