JP2006506643A - 蛍光ポリマーと消光剤−連結鎖−リガンド・バイオコンジュゲートとを使用するバイオセンシング法 - Google Patents
蛍光ポリマーと消光剤−連結鎖−リガンド・バイオコンジュゲートとを使用するバイオセンシング法 Download PDFInfo
- Publication number
- JP2006506643A JP2006506643A JP2004553594A JP2004553594A JP2006506643A JP 2006506643 A JP2006506643 A JP 2006506643A JP 2004553594 A JP2004553594 A JP 2004553594A JP 2004553594 A JP2004553594 A JP 2004553594A JP 2006506643 A JP2006506643 A JP 2006506643A
- Authority
- JP
- Japan
- Prior art keywords
- bioconjugate
- biotinylated
- nucleic acid
- quencher
- sensor
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 0 C*(c1ccccc1)c(cc1)cc(O2)c1C(c1c(**(CC3)CCC3C=O)cccc1)=C(C=C1)C2=CC1=*(*)c1ccccc1 Chemical compound C*(c1ccccc1)c(cc1)cc(O2)c1C(c1c(**(CC3)CCC3C=O)cccc1)=C(C=C1)C2=CC1=*(*)c1ccccc1 0.000 description 1
- YWBXDOUUNWNZEM-DZKIICNBSA-N COCCOCCOCCNC(CCCC[C@@H]([C@H]1N2)SC[C@@H]1NC2=O)=O Chemical compound COCCOCCOCCNC(CCCC[C@@H]([C@H]1N2)SC[C@@H]1NC2=O)=O YWBXDOUUNWNZEM-DZKIICNBSA-N 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/52—Use of compounds or compositions for colorimetric, spectrophotometric or fluorometric investigation, e.g. use of reagent paper and including single- and multilayer analytical elements
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82B—NANOSTRUCTURES FORMED BY MANIPULATION OF INDIVIDUAL ATOMS, MOLECULES, OR LIMITED COLLECTIONS OF ATOMS OR MOLECULES AS DISCRETE UNITS; MANUFACTURE OR TREATMENT THEREOF
- B82B1/00—Nanostructures formed by manipulation of individual atoms or molecules, or limited collections of atoms or molecules as discrete units
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/531—Production of immunochemical test materials
- G01N33/532—Production of labelled immunochemicals
- G01N33/533—Production of labelled immunochemicals with fluorescent label
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y15/00—Nanotechnology for interacting, sensing or actuating, e.g. quantum dots as markers in protein assays or molecular motors
Abstract
ビオチン化蛍光ポリマーとビオチン結合タンパク質との複合体および該蛍光ポリマー複合体でコートされた固体支持体が述べられる。この複合体は生物学的認識事象(たとえば、核酸ハイブリダイゼーション反応または酵素誘導ポリペプチド開裂)の検出センサとして使用することができる。この複合体の作製方法ならびに試料中の標的検体の存在および/または量を検出するためのこの複合体の使用方法も述べられる。標的検体は酵素(たとえば、β−セクレターゼ)または核酸(たとえば、1本鎖または2本鎖核酸)であってよい。
Description
本出願は本引証によりその全開示内容を本願明細書に引用したものとする2002年11月14日出願の米国特許出願第60/426,034号[U.S.Patent Application Serial No.60/426,034]に対する優先権を主張する。
本出願は2001年5月8日出願の米国特許出願第09/850,074号[U.S.Patent Application Serial No.09/850,074]および2003年7月18日出願の米国特許出願第10/621,311号[U.S.Patent Application Serial No.10/621,311]に関連している。これらの出願はそれぞれ本引証によりその全開示内容を本願明細書に引用したものとする。
合衆国政府は本発明に関して支払済み実施権を有するとともに、限定された事情のもとで、特許権者に対し国防省高度先進プロジェクト庁(DARPA)承認の契約No.MDA972−00−C−006の条項に定める適正な条件で他者に特許使用許諾を与えるよう求める権利を有する。
本発明は一般に分子センサおよび分子間相互作用を検出するための方法に関する。特に、本発明は蛍光ポリマー複合体および該複合体のバイオセンシング用途への使用法に関する。
固相酵素免疫測定法(つまり、ELISA)は広範囲に及ぶタンパク質、抗体、細胞、ウイルス等の存在と生理活性とを検出するために最も広く使用され、受け入れられている技術である。ELISAとは最初に検体の生体分子が表面固着抗体に結合させられる多段階「サンドイッチ法」である。次いで2次抗体が当該生体分子に結合する。ある場合には、2次抗体に触媒酵素が付着させられ、該触媒酵素は続いて増幅反応を「発現」する。他の場合には、この2次抗体はビオチン化されて第3のタンパク質(たとえばアビジンまたはストレプトアビジン)と結合する。このタンパク質には増幅された比色変化を招来する化学カスケードをつくり出す酵素が付着させられるか、または蛍光標識用の蛍光団が付着させられる。
広範に使用されているにもかかわらず、ELISAには多くの短所が存在する。たとえば、多段階手順には試薬と発現時間とのいずれについても正確なコントロールが必要とされるため、時間がかかると共に「偽陽性」を生じがちである。さらにまた、吸着された非特異的な試薬を除去するために慎重な洗浄が必要である。
蛍光共鳴エネルギ移動(つまりFRET)法はポリメラーゼ連鎖反応ベースの(PCT)遺伝子配列分析およびイムノアッセイのいずれにも使用されてきている。FRETは均質に結合された検体生体分子を使用して、オフ状態で消光される染料の蛍光を活性化する。FRET法の代表例において、蛍光染料は抗体に連結され(F−Ab)、この2連子が消光剤と連結された抗原と結合される(Ag−Q)。結合されたこの複合体(F−Ab:Ag−Q)はエネルギ移動によって消光(つまり非蛍光)される。Qと連結されていない同一の検体抗原(Ag)が存在する場合には、Ag−Q2連子は、相対濃度[Ag−Q]/[Ag]によって決定される平衡結合確率によって決定されるように、定量的に置換さ
れる。これによってFRET法は抗原がすでに十分に特徴付けられた定量アッセイに制限され、抗原をQに連結する化学技法が新たな事例ごとに案出されなければならない。
れる。これによってFRET法は抗原がすでに十分に特徴付けられた定量アッセイに制限され、抗原をQに連結する化学技法が新たな事例ごとに案出されなければならない。
その他のFRET基質およびアッセイは米国特許第6,291,201号[U.S.Patent No.6,291,201]ならびに以下の論文に開示されている: Anne, et al.,「ボツリヌスB型神経毒プロテアーゼ活性を測定するためのハイスループット蛍光発生アッセイ[High Throughput Fluorogenic Assay for Determination of Botulinum Type B Neurotoxin Protease Activity]」、Analytical Biochemistry, 291, 253〜261(2001); Cummings, et al.,「炭疸菌致死因子プロテアーゼのペプチドベース蛍光共鳴エネルギ移動アッセイ[A Peptide Based Fluorescence Resonance Energy Transfer Assay for Bacillus Anthracis Lethal Factor Protease]」、Proc.Natl.Acad.Scie.99、6603〜6606(2002);およびMock,et al.,「炭疸菌致死活性因子急速スクリーニングの進歩[Progress in Rapid Screening of Bacillus Anthracis Lethal Activity Factor]」、Proc.Natl.Acad.Scie.99、6527〜6529(2002)。
分子内消光蛍光体を採用するその他のアッセイは以下の論文に開示されている: Zhong,et al.,「大腸菌・リーダーペプチダーゼに関する分子内消光蛍光体の開発[Development of Internally Quenched Fluorescent Substrate for Escherichia Coli Leader Peptidase]」、Analytical Biochemistry 255、66〜73(1998); Rosse,et al.,「組合わせペプチドライブラリを使用した新規プロテアーゼ基質の急速識別[Rapid Identification of Substrates for Novel Protease Using a Combinatorial Peptide Library]」、J.Comb.Chem.、2、461〜466(2000);ならびにThompson,et al.,「カルパインおよびその他のプロテアーゼの活性を測定するためのBODIPY蛍光マイクロプレートアッセイ[A BODIPY Fluorecent Microplate Assay for Measuring Activity of Calpains and Other Proteases]」、Analytical Biochemistry、279、170〜178(2000)。蛍光偏光の変化が測定されて、検体量の定量に使用されるアッセイも開発されてきた。以下参照。たとえば、Levine,et al.,「蛍光偏光を使用するプロテアーゼ比活性の測定[Measurement of Specific Protease Activity Utilizing Fluorescence Polarization]」、Analytical Biochemistry 247、83〜88(1997)。以下も参照のこと。Schade,et al.,「蛍光偏光を使用するプロテアーゼアッセイのためのBODIPY−α−カゼイン、pH非依存タンパク基質[BODIPY−α−Casein, a pH−Independent Protein Substrate for Protease Assasys Using Fluorescence Polarization]」、Analytical Biochemistry 243、1〜7(1996)。
しかしながら、生物学的関連分子を急速かつ正確に検出し、高感度で定量する必要性は
なお存在している。
なお存在している。
本発明の第1の局面により、生物学的認識事象を検出するためのセンサ作製方法が提供される。この方法はビオチン化蛍光ポリマーとビオチン結合タンパク質とを水溶液中で結合させて、フリーのビオチン結合部位を有する複合体を形成するステップを含む。ビオチン化蛍光タンパク質(たとえばフィコエリトリンまたはフィコビリゾーム)がビオチン化蛍光ポリマーおよびビオチン結合タンパク質に結合させられてよい。この複合体は固体支持体(たとえば微小球、ナノ粒子またはビーズ)の表面に配置されてよい。この固体支持体はシリカまたはラテックス微小球であってよい。この固体支持体の表面はアンモニウム官能基を含んでいてよい。ビオチン結合タンパク質はアビジン、ストレプトアビジンおよびノイトラビジンからなる群から選択されてよい。
前記の方法はさらに、ポリヌクレオチド配列、ペプチド核酸配列またはポリペプチド配列を含むビオチン化バイオコンジュゲートを前記溶液に添加するステップを含んでいてよく、この場合、ビオチン化バイオコンジュゲートは前記複合体のフリーのビオチン結合部位に結合する。1実施形態において、前記のビオチン化バイオコンジュゲートはポリヌクレオチドまたはペプチド核酸配列を含み、生物学的認識事象は標的検体に対するビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列の核酸ハイブリダイゼーションである。この実施形態による方法は消光剤とポリヌクレオチドまたはペプチド核酸配列とを含む第2のバイオコンジュゲートを前記溶液に添加するプロセスも含むことができ、この場合、消光剤は蛍光ポリマーの増幅超消光を行なうことができ、第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことができる。第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列と相補的であってよい。
代替の実施形態において、ビオチン化バイオコンジュゲートはポリペプチド配列と蛍光ポリマーの増幅超消光を行なうことのできる消光剤とを含み、生物学的認識事象はポリペプチド配列の酵素誘導開裂である。
本発明の第2の局面により、ビオチン化蛍光ポリマーとビオチン結合タンパク質との複合体からなり、該複合体はフリーのビオチン結合部位を有する、生物学的認識事象を検出するためのセンサが提供される。この複合体は固体支持体(たとえば微小球、ナノ粒子またはビーズ)の表面に配置されていてよい。この固体支持体はシリカまたはラテックス微小球であってよい。ポリヌクレオチド配列、ペプチド核酸配列またはポリペプチド配列を含むビオチン化バイオコンジュゲートが前記複合体に結合させられてよい。たとえば、ビオチン化バイオコンジュゲートはポリヌクレオチドまたはペプチド核酸配列を含み、生物学的認識事象は標的検体に対するビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列の核酸ハイブリダイゼーションであってよい。あるいは、ビオチン化バイオコンジュゲートはポリペプチド配列と消光剤とを含み、消光剤は蛍光ポリマーの増幅超消光を行なうことができ、生物学的認識事象はポリペプチド配列の酵素誘導開裂であってよい。ビオチン結合タンパク質はアビジン、ストレプトアビジンまたはノイトラビジンであってよい。固体支持体の表面はアンモニウム官能基からなっていてよい。センサはまた、ビオチン化蛍光ポリマーおよびビオチン結合タンパク質との複合体を形成するビオチン化蛍光タンパク質(たとえばフィコエリトリンまたはフィコビリゾーム)を含んでいてよい。
また、固体支持体表面に配置された、ビオチン化蛍光ポリマー、ビオチン結合タンパク
質およびビオチン化バイオコンジュゲートの複合体からなり、ビオチン化バイオコンジュゲートはポリヌクレオチドまたはペプチド核酸配列を含むと共にさらに蛍光ポリマーの増幅超消光を行なうことのできる消光剤を含んでいるセンサも提供される。この実施形態において、ポリヌクレオチド配列はビオチン化バイオコンジュゲート上で消光剤とビオチンとの間に配置される。試料を(たとえば溶液中で)センサと結合させるステップを含む、前記センサを使用して試料中の標的検体の存在および/または量を検出する方法も提供される。この実施形態において、標的検体はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことのできるポリヌクレオチド配列を含み、標的検体とビオチン化バイオコンジュゲートとのハイブリダイゼーションは固体支持体表面からの消光剤分離の増加とそれに伴う蛍光の増強とを生ずる。
質およびビオチン化バイオコンジュゲートの複合体からなり、ビオチン化バイオコンジュゲートはポリヌクレオチドまたはペプチド核酸配列を含むと共にさらに蛍光ポリマーの増幅超消光を行なうことのできる消光剤を含んでいるセンサも提供される。この実施形態において、ポリヌクレオチド配列はビオチン化バイオコンジュゲート上で消光剤とビオチンとの間に配置される。試料を(たとえば溶液中で)センサと結合させるステップを含む、前記センサを使用して試料中の標的検体の存在および/または量を検出する方法も提供される。この実施形態において、標的検体はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことのできるポリヌクレオチド配列を含み、標的検体とビオチン化バイオコンジュゲートとのハイブリダイゼーションは固体支持体表面からの消光剤分離の増加とそれに伴う蛍光の増強とを生ずる。
更なる実施形態において、固体支持体表面に配置された蛍光ポリマー複合体からなる上述したセンサはさらに連結鎖の第1と第2の位置に結合されたリガンドおよびビオチン成分からなるビオチン化バイオコンジュゲートを含むことができ、この場合、リガンドは蛍光ポリマーの増幅超消光を行なうことのできる消光剤成分からなると共に生物学的認識事象に関与することができる。この実施形態において、第1と第2の位置の間の連結鎖部は生物学的認識事象の発生が固体支持体表面からの消光剤の分離とそれに伴う蛍光の増強とを生ずるような長さと柔軟性とを有している。リガンドはポリペプチド配列からなっていてよい。第1と第2の位置の間の連結鎖部は化学式
(式中、nは正の整数である)によって表される繰返し単位を含んでいてよい。上述したセンサを使用して試料中の標的検体の存在および/または量を検出する方法も提供される。標的検体は芽胞、細胞、細菌またはウイルスであってよい。また、上述したセンサとその表面に配置された多数の標的成分を有する第2の固体支持体とを含む、生物学的認識事象を検出するためのセンシングシステムも提供され、この場合、リガンドは標的成分と相互作用して消光剤を蛍光体から分離し、これによって蛍光ポリマーの蛍光が増大する。この第2の固体支持体は微小球(たとえばシリカまたはラテックス微小球)、ナノ粒子またはビーズであってよい。さらにまた、センシングシステムを試料と結合させるステップを含み、標的検体がリガンドを認識してそれと相互作用し、標的検体とリガンドとの相互作用が蛍光の減少を生ずる、試料中の標的検体の存在および/または量を検出する方法も提供される。リガンドはポリペプチドを含み、生物学的認識事象はリガンドのポリペプチドとポリペプチドを含む標的検体との相互作用であってよい。
本発明の第3の局面により、試料をヌクレオチド配列、ペプチド核酸配列またはポリペプチド配列を含むビオチン化バイオコンジュゲートおよび上述した蛍光ポリマー複合体からなるセンサと結合させるステップを含む、試料中の標的検体の存在および/または量を検出する方法が提供される。ビオチン化バイオコンジュゲートがポリヌクレオチドまたはペプチド核酸配列を含む場合には、この方法はさらに試料を消光剤とポリヌクレオチドまたはペプチド核酸配列とを含む第2のバイオコンジュゲートと結合させるプロセスを含むことができ、この場合、消光剤は蛍光ポリマーの増幅超消光を行なうことができ、第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行
なうことができる。この実施形態において、標的検体はビオチン化バイオコンジュゲートかまたは第2のバイオコンジュゲートのいずれかのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことのできるポリヌクレオチド配列を含む。たとえば、第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列と相補的であってよい。更なる実施形態において、センサとビオチン化バイオコンジュゲートとはビオチン化バイオコンジュゲートがセンサと複合するようにして結合され、試料は続いてセンサ/ビオチン化バイオコンジュゲート・複合体と共にインキュベーションされ、続いて第2のバイオコンジュゲートがインキュベーションされた試料に加えられる。代替の実施形態において、標的検体のヌクレオチド配列は2本鎖核酸を含んでいてよい。この代替の実施形態において、方法はさらに、インキュベーションされた試料を第2のバイオコンジュゲートの存在下で試料中の2本鎖核酸が融解するのに十分な温度にまで加熱するステップと、2重鎖生成が可能となるまで試料を冷却するステップとを含む。試料中に存在する標的検体と第2のバイオコンジュゲートとの間の2重鎖生成は蛍光の増強を生ずる。あるいは、ビオチン化バイオコンジュゲートはポリペプチド配列と消光剤とを含み、標的検体はポリペプチド配列を開裂させることのできる酵素(たとえば、β−セクレターゼ)であってよい。
なうことができる。この実施形態において、標的検体はビオチン化バイオコンジュゲートかまたは第2のバイオコンジュゲートのいずれかのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことのできるポリヌクレオチド配列を含む。たとえば、第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列と相補的であってよい。更なる実施形態において、センサとビオチン化バイオコンジュゲートとはビオチン化バイオコンジュゲートがセンサと複合するようにして結合され、試料は続いてセンサ/ビオチン化バイオコンジュゲート・複合体と共にインキュベーションされ、続いて第2のバイオコンジュゲートがインキュベーションされた試料に加えられる。代替の実施形態において、標的検体のヌクレオチド配列は2本鎖核酸を含んでいてよい。この代替の実施形態において、方法はさらに、インキュベーションされた試料を第2のバイオコンジュゲートの存在下で試料中の2本鎖核酸が融解するのに十分な温度にまで加熱するステップと、2重鎖生成が可能となるまで試料を冷却するステップとを含む。試料中に存在する標的検体と第2のバイオコンジュゲートとの間の2重鎖生成は蛍光の増強を生ずる。あるいは、ビオチン化バイオコンジュゲートはポリペプチド配列と消光剤とを含み、標的検体はポリペプチド配列を開裂させることのできる酵素(たとえば、β−セクレターゼ)であってよい。
本発明の第4の局面により、表面のレセプターに対する多数のリガンドを有する細菌芽胞またはウイルスと、細菌芽胞またはウイルスの表面に配置された蛍光ポリマーまたは蛍光ポリマー複合体と、リガンドに対するレセプターに結合された消光剤を含む多数のバイオコンジュゲートとを含み、レセプターとリガンドとは相互作用し、レセプターとリガンドの相互作用が蛍光ポリマーの蛍光の増幅超消光を生ずる、標的生物学的種を検出するためのセンサが提供される。また、試料を上述したセンサと共にインキュベーションし、標的検体はレセプターを認識してそれと相互作用し、標的検体とレセプターとの相互作用が蛍光の増強を生ずる、試料中の標的検体の存在および/または量を検出する方法も提供される。標的検体は表面のレセプターに対する多数のリガンドを有する細菌芽胞またはウイルスであってよい。
本発明は添付図面を参照してよりよく理解することができる。
詳細な説明
蛍光ポリマー(P)と会合してそれを消光する消光剤(Q)と連結(T)した、標的生物学的分子のリガンド(L)からなるバイオコンジュゲートは米国特許出願第09/850,074号[U.S.Patent Application No.09/850,074]に開示されており、同出願は本引証によりその全開示内容を本願明細書に引用したものとする。これらのバイオコンジュゲート(「QTLバイオコンジュゲート」と称される)はたとえば電子移動またはエネルギ移動消光による蛍光高分子電解質の超消光を利用する。蛍光ポリマー(P)はQTLバイオコンジュゲートとの間で、通例、蛍光ポリマーのそれとは反対の電荷を有した会合複合体を形成することができる。このQTLバイオコンジュゲートは特定の生体分子に対して特異的なリガンド(L)と共有連結鎖によって連結された消光剤(Q)を含んでいる。QTLバイオコンジュゲートのリガンドと生体分子との会合は蛍光ポリマーからQTLバイオコンジュゲートを分離させるかまたはその消光を容易に検出し得るようにして変化させ、こうして、蛍光の変化によって生体分子のセンシングを可能とする。このようにして生体分子は非常に低い濃度で検出可能である。
蛍光ポリマー(P)と会合してそれを消光する消光剤(Q)と連結(T)した、標的生物学的分子のリガンド(L)からなるバイオコンジュゲートは米国特許出願第09/850,074号[U.S.Patent Application No.09/850,074]に開示されており、同出願は本引証によりその全開示内容を本願明細書に引用したものとする。これらのバイオコンジュゲート(「QTLバイオコンジュゲート」と称される)はたとえば電子移動またはエネルギ移動消光による蛍光高分子電解質の超消光を利用する。蛍光ポリマー(P)はQTLバイオコンジュゲートとの間で、通例、蛍光ポリマーのそれとは反対の電荷を有した会合複合体を形成することができる。このQTLバイオコンジュゲートは特定の生体分子に対して特異的なリガンド(L)と共有連結鎖によって連結された消光剤(Q)を含んでいる。QTLバイオコンジュゲートのリガンドと生体分子との会合は蛍光ポリマーからQTLバイオコンジュゲートを分離させるかまたはその消光を容易に検出し得るようにして変化させ、こうして、蛍光の変化によって生体分子のセンシングを可能とする。このようにして生体分子は非常に低い濃度で検出可能である。
また、支持体たとえばラテックスまたはシリカビーズまたはナノ粒子に蛍光ポリマーをコートすることにより超消光の増強と、マクロ分子たとえばタンパク質または核酸との非特異的な相互作用による付随的な蛍光減少変化とがもたらされることも明らかにされてい
る。結果として、蛍光ポリマーと同一粒子に同配置されたレセプターとを使用し、QTLと蛍光ポリマーとの相互作用がQTLコンジュゲートのL部と特異レセプターとの会合によって媒介されるようにするアッセイが考案されている。このタイプのアッセイは2002年3月8日に提出された米国特許出願第10/098,387号[U.S.Patent Application Serial No.10/098,387]に開示されており、同出願は本引証によりその全開示内容を本願明細書に引用したものとする。これらのアッセイは典型的には、検体が表面会合されたレセプターによって認識される配列Lのみからなるかまたはそれを含んでいる競合法である。したがって、Lとレセプターとの結合はポリマーまたはポリマー集合からの蛍光の変化をほとんど生じないかまたはまったく生じない。他方、レセプターとの会合によるQTLの結合は蛍光の消光を結果として生じる。
1.溶液中および支持フォーマットでのセンシング用のプレフォームされたポリマー−タンパク質・複合体
前述したように、QTL−ポリマー超消光アッセイは支持体たとえばラテックスまたはシリカビーズまたはナノ粒子上に同配置される蛍光ポリマーたとえば高分子アニオンポリフェニレンエチニレン(1)
る。結果として、蛍光ポリマーと同一粒子に同配置されたレセプターとを使用し、QTLと蛍光ポリマーとの相互作用がQTLコンジュゲートのL部と特異レセプターとの会合によって媒介されるようにするアッセイが考案されている。このタイプのアッセイは2002年3月8日に提出された米国特許出願第10/098,387号[U.S.Patent Application Serial No.10/098,387]に開示されており、同出願は本引証によりその全開示内容を本願明細書に引用したものとする。これらのアッセイは典型的には、検体が表面会合されたレセプターによって認識される配列Lのみからなるかまたはそれを含んでいる競合法である。したがって、Lとレセプターとの結合はポリマーまたはポリマー集合からの蛍光の変化をほとんど生じないかまたはまったく生じない。他方、レセプターとの会合によるQTLの結合は蛍光の消光を結果として生じる。
1.溶液中および支持フォーマットでのセンシング用のプレフォームされたポリマー−タンパク質・複合体
前述したように、QTL−ポリマー超消光アッセイは支持体たとえばラテックスまたはシリカビーズまたはナノ粒子上に同配置される蛍光ポリマーたとえば高分子アニオンポリフェニレンエチニレン(1)
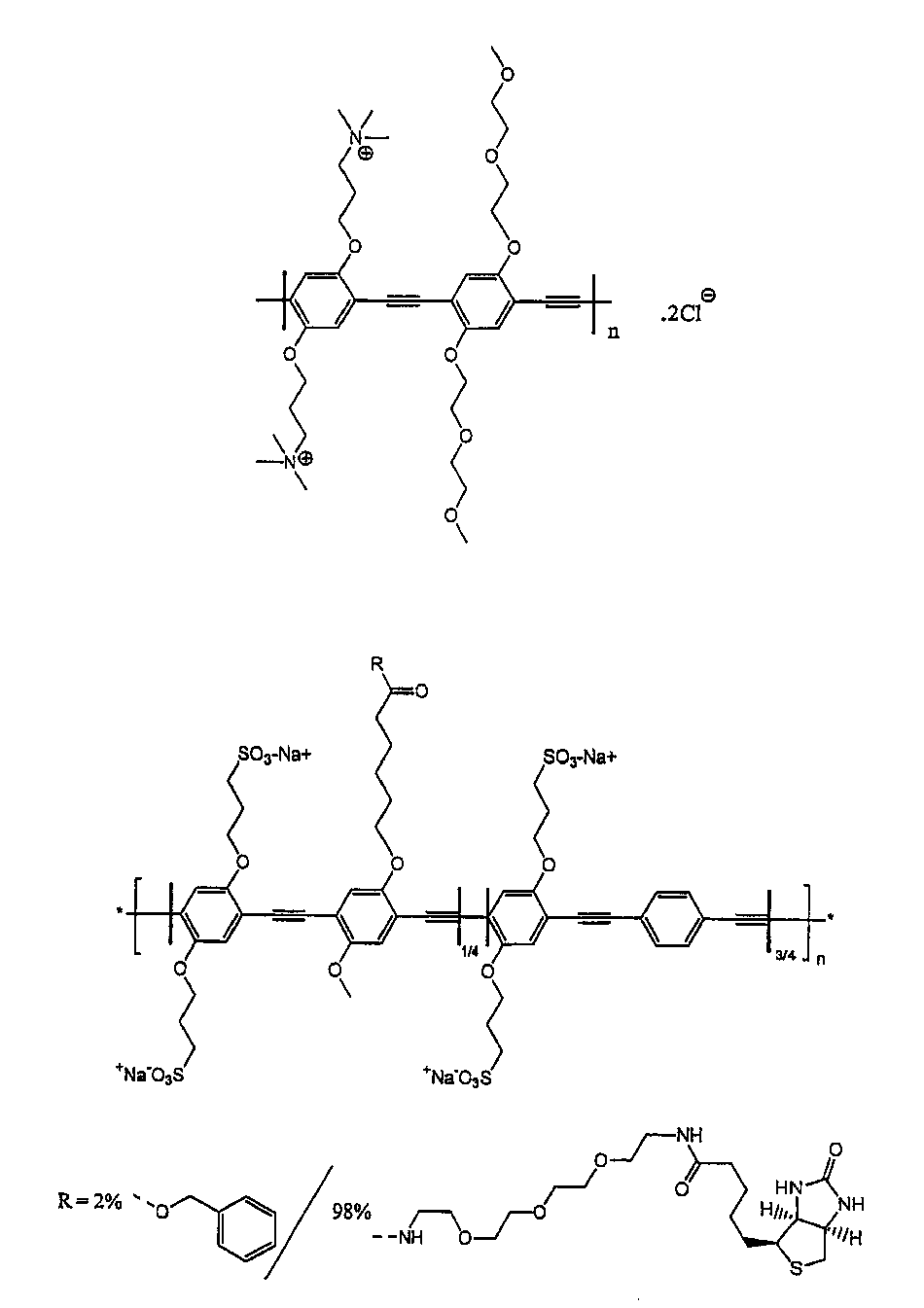
またはビオチン化ポリフェニレンエチニレン(2)
とレセプターとによって構成されている。一般にレセプターは抗体、タンパク質、オリゴヌクレオチドまたはその他のリガンドであってよい。レセプターおよび/またはポリマーはビオチン−アビジン会合によって支持体に固着させることができる。ビオチン結合タンパク質(アビジン、ノイトラビジンまたはストレプトアビジン)の1つはポリマーまたはレセプターの付加前に支持体に共有結合させることができる。
本発明により、ビオチン化蛍光ポリマー(たとえば、ポリマー2)とビオチン結合タンパク質との溶液中における当初複合化からなる、同配置される蛍光ポリマーとアクセプタとに代わる手段が提供される。ポリマー2はいくつかの有効なビオチンを含むが、これらのタンパク質の各々の4つのビオチン結合部位の1つもしくはせいぜい2つとしか結合し得ない。これは一部、PPEポリマーの大きなセグメントの「剛性ロッド」性に帰着される。
ただし、水溶液中におけるビオチン結合タンパク質たとえばノイトラビジンへのビオチン化蛍光ポリマーたとえばポリマー2の付加はタンパク質によるポリマーの架橋を生ずる。ポリマー2については、この架橋はポリマー蛍光の適度な増強と、光の散乱によって示されるように集合規模の有意な増大とを伴う。こうして生じたビオチン化蛍光ポリマーとビオチン結合タンパク質との集合は、ビオチン結合タンパク質とポリマーとの比ならびに付加の正確な配列に応じ、特異なビオチン化レセプターたとえば抗体、タンパク質、オリゴヌクレオチドまたはペプチドを固定するのに使用し得る適度な数のフリーのビオチン結合部位を含むことができる。ビオチン機能化レセプターが(レセプターの一部またはレセプターQTL・複合体として)消光剤を含んでいれば、ポリマー蛍光の効果的な消光が生ずる。
ビオチン結合タンパク質/ビオチン化蛍光ポリマー・集合は固体支持体にコートすることができる。たとえば、ノイトラビジン/ポリマー2・集合(つまり、1ノイトラビジン:15ポリマー反復単位)は第4アンモニウム基で機能化されたラテックス微小球にコートされた。こうして生じた微小球は高度蛍光性を生じた。この蛍光は特にビオチン−消光剤・コンジュゲートの付加によって消光することができた。対照的に、ビオチンを包含しない消光剤の付加は微弱な非特異的な消光を生じた。消光は、同じ組成物溶液相ノイトラビジン:ポリマー2集合について観察されたものよりもわずかに増強された。
かくてプレフォームされたポリマー−ビオチン結合タンパク質・複合体は溶液中または支持フォーマットにおけるセンシング用途の基礎を提供する。いずれの「プラットフォーム」においても複合体は一定の利点を供する。第1に、レセプターとポリマーとの近接性が保証される。第2に、この集合体は試薬たとえばタンパク質、小さな有機分子および無機イオンとの非特異的な相互作用を生じにくい。これに加えてさらに、アッセイの広範なチューニングも可能である。たとえば、1つまたは複数の以下のパラメータを変更することが可能である:ビオチン結合タンパク質とビオチン化ポリマーとの比、ポリマー上のビオチン密度、付加の配列または、使用される特異的なビオチン結合タンパク質。こうしてアッセイを特定の用途向けに適応させることが可能である。さらに、複合体の総電荷をポリマー上の帯電側基の変更またはビオチン結合タンパク質の変更によって調整することもできる。こうして複合体を選択して、他のタンパク質との非特異的結合、他の生体分子(たとえばDNAまたはPNA)との非特異的結合または、帯電または中性表面との非特異的結合を高めまたは除去することができる。
2.蛍光ポリマー超消光をベースとした1本鎖および2重鎖DNAのアッセイ
蛍光高分子電解質を使用したセンシングはオリゴヌクレオチド−オリゴヌクレオチド認識に適用することができる。たとえば、最近、QTLをベースとした1本鎖DNAのセンシングが報告されている[Kushon,et al.,ラングミューア[Langmuir]、18、7245〜7249(2002)]。この最も単純なケースにおいて、1
本鎖「標的」DNA配列を相補「捕獲」1本鎖と会合させ、ポリマーまたはポリマー集合の蛍光を変化させる(消光または増強させる)ことができる。1つのアプローチは「標的」配列と相補的な、DNAのビオチン化捕獲鎖の使用を含んでいる。未知量の標的検体の存在下で既知量の消光剤標識された標的(DNA−QTL)を使用する競合法が開発された。これらのアッセイにおいて、ビオチン化捕獲鎖は蛍光高分子電解質とビオチン結合タンパク質たとえばアビジン、ストレプトアビジンまたはノイトラビジンとからなるビーズ支持体と会合させられた。ビオチン化捕獲鎖とビーズとの(ビオチン−アビジン会合による)会合はポリマー蛍光の変化をほとんど生じないかまたはまったく生じなかった。同様に、ビオチン化捕獲鎖標的検体2重鎖とビーズとの会合も蛍光をほとんど変化させないかまたはまったく変化させなかった。ただし、ビオチン化捕獲鎖DNA−QTL2重鎖とビーズまたは前もって結合されたビオチン化捕獲鎖を有したDNA−QTLとの会合はポリマー蛍光の強度の消光を生じた。
2.蛍光ポリマー超消光をベースとした1本鎖および2重鎖DNAのアッセイ
蛍光高分子電解質を使用したセンシングはオリゴヌクレオチド−オリゴヌクレオチド認識に適用することができる。たとえば、最近、QTLをベースとした1本鎖DNAのセンシングが報告されている[Kushon,et al.,ラングミューア[Langmuir]、18、7245〜7249(2002)]。この最も単純なケースにおいて、1
本鎖「標的」DNA配列を相補「捕獲」1本鎖と会合させ、ポリマーまたはポリマー集合の蛍光を変化させる(消光または増強させる)ことができる。1つのアプローチは「標的」配列と相補的な、DNAのビオチン化捕獲鎖の使用を含んでいる。未知量の標的検体の存在下で既知量の消光剤標識された標的(DNA−QTL)を使用する競合法が開発された。これらのアッセイにおいて、ビオチン化捕獲鎖は蛍光高分子電解質とビオチン結合タンパク質たとえばアビジン、ストレプトアビジンまたはノイトラビジンとからなるビーズ支持体と会合させられた。ビオチン化捕獲鎖とビーズとの(ビオチン−アビジン会合による)会合はポリマー蛍光の変化をほとんど生じないかまたはまったく生じなかった。同様に、ビオチン化捕獲鎖標的検体2重鎖とビーズとの会合も蛍光をほとんど変化させないかまたはまったく変化させなかった。ただし、ビオチン化捕獲鎖DNA−QTL2重鎖とビーズまたは前もって結合されたビオチン化捕獲鎖を有したDNA−QTLとの会合はポリマー蛍光の強度の消光を生じた。
ビーズと予備会合されたビオチン化捕獲鎖をめぐるDNA−QTLと標的検体との間の直接の競合は、DNA−QTLと捕獲鎖との会合が(非標識化検体と比較して)より急速(速度論的)であることから、アッセイ感度を低下させた。ただし、DNA−QTLの付加を伴う、検体とビーズ結合捕獲鎖との段階的な会合は感度の良い、ただし単純な定量アッセイをもたらした。感度の良い類似のアッセイは、ビオチン化捕獲鎖、DNA−QTLおよび検体1本鎖DNAを予備インキュベーションし、次いでこの混合物を蛍光ポリマーコートされたビーズに曝露させることによっても得られた。後に挙げたアッセイのいずれについても、蛍光レベルは1本鎖検体DNAの濃度の高まりと共に上昇する。
上記の一連のアッセイは1本鎖DNAを使用し、標的検体と同じ塩基配列を含むDNA−QTLの使用を含んでいる。図1は代替のアッセイフォーマットを示したものである。このアッセイフォーマットは標的検体と相補的な塩基配列を有するDNA−QTLの使用を必要とする。
図1に示したように、エネルギ移動または電子移動消光剤はDNA−QTLをつくり出すために鎖の一端に共有結合させることができる。さらにまた図1に示したように、標的検体と同じ配列を有するビオチン化鎖とこの鎖の一端のビオチンとを捕獲鎖として使用することができる。ビオチン化捕獲鎖と蛍光ポリマーコートされたビーズとの会合はポリマーから生ずる蛍光のレベルをほとんど変化させないかまたはまったく変化させない。ただし、DNA−QTLとビーズ結合捕獲鎖との間の2重鎖形成はポリマーとDNA−QTL上の消光剤との間の密な会合によってポリマー蛍光の消光を生ずる。
1本鎖検体DNA用のアッセイを実現するため、検体(未知レベル)とDNA−QTLとをビオチン化標的を含むビーズの懸濁液と混合することができる。標的検体とDNA−QTLとの間の2重鎖形成は「遊離」DNA−QTLを除去し、これによって、標的の欠如下で発生すると考えられるポリマーの消光を妨げる。こうして、1本鎖検体用の単純かつ均一な定量アッセイを提供することができる。
上述したアッセイ材料は2重鎖として存在する標的検体のセンシング用の単純かつ均一なフォーマットも提供することができる。たとえば、検体と、検体と相補的な塩基配列を有する2重鎖DNA−QTLとを含む試料が、同配置された蛍光ポリマーとビオチン化捕獲試薬とからなる固体支持体(たとえば、ビーズの懸濁液)に加えられ、続いて、2重鎖の「融解」を生ずるのに十分な温度に加熱され得る。これは、混合物を周囲温度に戻した後、DNA−QTLと1本鎖検体とのペアリングと、試料中の標的鎖のレベルに比例した蛍光消光の減衰とを生ずる。
先に報告され、以上に説明したものと類似のアッセイはペプチド核酸のビオチン化捕獲
鎖(つまり、ビオチン化PNA)を使用して構成することができる。ビオチン化PNAは標的検体DNAの相補鎖またはDNA−QTLとのペアリングにおいて類似の選択性を示すが、より強い2重鎖をもたらし、こうして1本鎖標的検体用のアッセイにおいてより高い感度さえも供することができる。捕獲鎖としてのビオチン化PNAの利点は、より強力なDNA−PNA会合が鎖の侵襲によって2重鎖化された標的用の周囲温度均一アッセイの基礎を供することである。
鎖(つまり、ビオチン化PNA)を使用して構成することができる。ビオチン化PNAは標的検体DNAの相補鎖またはDNA−QTLとのペアリングにおいて類似の選択性を示すが、より強い2重鎖をもたらし、こうして1本鎖標的検体用のアッセイにおいてより高い感度さえも供することができる。捕獲鎖としてのビオチン化PNAの利点は、より強力なDNA−PNA会合が鎖の侵襲によって2重鎖化された標的用の周囲温度均一アッセイの基礎を供することである。
更に代替のDNA検出方法はビオチン化DNA−QTLの使用を含んでいる。ビオチンとコンジュゲート中の消光剤とは両側末端に配置される。ビオチン結合タンパク質を担持するポリマーコートされた微小球に曝露されると、ビオチン−DNA−QTLはビオチンを通じて表面に付着する。さらに、使用される消光剤の一般的な疎水性により、消光剤標識された末端は表面に向かって折り返され、消光剤が表面上のポリマーを消光することが可能になる。ただし、標的鎖が存在する場合には、ビオチン−DNA−QTLはDNA2重鎖中にハイブリダイゼーションされる。DNA2重鎖は1本鎖DNAに比較して相対的に剛的であることが知られている。したがって、2重鎖の形成は、ビオチン−DNA−QTLが標的に対してハイブリダイゼーションされたDNAで表面に向かって容易に折り返されることができないため、消光剤と表面との間の間隔の増大を生じ得る。結果として、消光レベルは減少させられ得る。
3.長い柔軟な連結鎖(たとえば、親水性高分子連結鎖)の使用をベースとしたセンシングフォーマット
上述したように、蛍光ポリマーまたはポリマー集合の消光/非消光をベースとしたバイオセンシングに使用されるQTLコンジュゲートは一般に3つの成分:消光剤(Q);連結鎖(T);およびリガンドまたはレセプター(L)からなっている。エネルギ移動によるものであろうと電子移動によるものであろうと超消光の程度は蛍光ポリマーまたはポリマー集合に対する消光剤の近接性に依存している。検出される生物学的認識事象の感知程度は一般に、認識事象と、消光剤とポリマー集合とを隔てる間隔の変化との組合わせに依存している。
3.長い柔軟な連結鎖(たとえば、親水性高分子連結鎖)の使用をベースとしたセンシングフォーマット
上述したように、蛍光ポリマーまたはポリマー集合の消光/非消光をベースとしたバイオセンシングに使用されるQTLコンジュゲートは一般に3つの成分:消光剤(Q);連結鎖(T);およびリガンドまたはレセプター(L)からなっている。エネルギ移動によるものであろうと電子移動によるものであろうと超消光の程度は蛍光ポリマーまたはポリマー集合に対する消光剤の近接性に依存している。検出される生物学的認識事象の感知程度は一般に、認識事象と、消光剤とポリマー集合とを隔てる間隔の変化との組合わせに依存している。
ポリマー/QTL超消光相互作用をベースとしたバイオセンシングへの当初アプローチにおいて、(溶液中においてかまたは支持体たとえば微小球またはナノ粒子に固定された)ポリマーは非特異的相互作用(一般にクーロン引力と疎水性相互作用との組合わせ)によってQTLと会合する。蛍光「消光」アッセイにおいて、生物学的認識事象中に生ずるQTLとポリマーとの会合は蛍光の消光を生ずる。代わって、QTLと特異的レセプターとの会合は予備会合されたポリマーとQTLとの分離を生じ、蛍光「発光」センシングをもたらす。このアッセイプラットフォームは、標的検体と合成QTLとに応じ、直接アッセイならびに競合アッセイのいずれにも使用することができる。
代替のセンシングプラットフォームにおいて、蛍光ポリマーとレセプター(つまり、QTLバイオコンジュゲートのリガンド「L」に対するレセプター)との双方は固体支持体たとえばミクロンサイズまたはサブミクロンサイズのラテックスビーズ、シリカ微小球、ナノ粒子または表面に同配置される。このケースにおいて、QTLとレセプターとの特異的な会合は蛍光の消光に至り、他方、QTLの解放は蛍光の発光に至る。前述したセンシングアプローチのいずれにおいても、QTLコンジュゲートは一般に、QTLがポリマーまたはポリマー集合と会合させられる場合に、蛍光ポリマーと、QTLの消光剤およびリガンド部の双方との至近性が実現されるように最小の長さの連結鎖を使用する。
代替のアプローチは長い柔軟な連結鎖を有するQTLコンジュゲートを使用する。図2A〜2Cに示したように、消光剤を担持する認識分子からビオチン「コネクタ」を切離す「柔軟な」連結鎖の構築はビオチン結合タンパク質と蛍光ポリマーとからなるビーズ「プラットフォーム」と会合し得るQTLをもたらす。
図2A〜2Cに示したように、蛍光ポリマーでコートされ、有効なアビジンまたはストレプトアビジンレセプター部位を有する固体支持体(ビーズで示されている)は長い柔軟な連結鎖を有するビオチン化消光剤と複合することができる。結果として、蛍光は消光される(図2B)。ただし、認識分子を結合する検体の存在は消光剤を蛍光支持体から引き離すことができ、これによって蛍光の増強が生ずる(図2C)。
柔軟な連結鎖はさまざまな構造をとっていてよい。好適な1実施形態において、柔軟な連結鎖は、図2Aに示したように、ポリ(エチレングリコール)(つまり、PEG)直鎖からなっている。一例において、ビオチンは約75反復単位を有するPEG連結鎖によってレセプターから切離されている。もしこの鎖が完全に延びた形をとれば、ビオチンコネクタとレセプターとの間の間隔は約278オングストロームとなろう。
水性溶媒中でPEG鎖はある程度折り畳まれることとなり、折り畳まれたまたはコイル化された状態で、消光剤標識されたレセプターはビーズに固定された蛍光ポリマーと相対的に密に接近させられることとなる。これはQTLのビオチンが会合させられるビオチン結合タンパク質部位から(ビーズの表面で)相対的に引き離されていてよいポリマー域からの蛍光の消光を生ずる。鎖の末端の消光剤レセプターと表面上の蛍光ポリマーとの間の相互作用の程度は、表面と消光剤レセプターとの電荷の変化、消光剤レセプターの疎水性の変化または懸濁液に付加される試薬によって調整することができる。
柔軟な鎖は、それが表面から完全に延ばされると消光剤標識されたレセプターがポリマーから離れすぎて有意な消光を生じなくなる程度の長さを有しているのが好適である。レセプター消光剤とビーズ表面の蛍光ポリマーとの間の会合は弱いので、大きな検体の付加はレセプター消光剤の引き離しとポリマーの消光範囲外へのPEGの延伸を生じ得る。大きな多価検体については、多数のレセプター消光剤が同一または多数のビーズから引き離されることによりセンシングが増幅されることとなる。したがって、このアッセイフォーマットは相対的に大きな検体たとえば芽胞、細胞、細菌またはウイルスに特に適当している。
4.QTLバイオセンシングの基礎としての多価抗原ビーズ
本発明の更なる1実施形態において、同じビーズと、上述した長い柔軟な連結鎖を有し、さらに、標的タンパク質検体が存在する場合に異なった相互作用を展開する2つの成分を含むコンジュゲートとを使用して、アッセイを構成することができる。この場合のアッセイは、前記のセクション3に述べた反応を誘起せず、ただしレセプター消光剤集合と、蛍光ポリマーからのそれらの引き離しを生ずることなく、結合することのできる小さなタンパク質検体に特に適している。この場合、成分の1つはビオチン結合タンパク質と上記のセクション3に述べたビオチン−柔軟な連結鎖−レセプター消光剤「QTL成分」とを含む、蛍光ポリマーコートされたビーズである。第2の成分は、レセプターを認識する標的抗原の多数のコピーで表面が「装飾」されたポリマービーズまたは微小球(つまり、「多価抗原ビーズ」またはMVAB)であってよい。図3は1つのMVABを示したものである。
4.QTLバイオセンシングの基礎としての多価抗原ビーズ
本発明の更なる1実施形態において、同じビーズと、上述した長い柔軟な連結鎖を有し、さらに、標的タンパク質検体が存在する場合に異なった相互作用を展開する2つの成分を含むコンジュゲートとを使用して、アッセイを構成することができる。この場合のアッセイは、前記のセクション3に述べた反応を誘起せず、ただしレセプター消光剤集合と、蛍光ポリマーからのそれらの引き離しを生ずることなく、結合することのできる小さなタンパク質検体に特に適している。この場合、成分の1つはビオチン結合タンパク質と上記のセクション3に述べたビオチン−柔軟な連結鎖−レセプター消光剤「QTL成分」とを含む、蛍光ポリマーコートされたビーズである。第2の成分は、レセプターを認識する標的抗原の多数のコピーで表面が「装飾」されたポリマービーズまたは微小球(つまり、「多価抗原ビーズ」またはMVAB)であってよい。図3は1つのMVABを示したものである。
図3に示したように、ビオチン化抗原はビオチン結合タンパク質で機能化されたポリマービーズと複合されて、本発明による多価抗原ビーズを形成することができる。
多価抗原ビーズをビオチン−柔軟な連結鎖−レセプター消光剤を含むビーズの懸濁液に加えるとビーズ表面からの消光剤−レセプターの引き離しによってポリマーからの蛍光の発光が生ずる。続いて標的検体を加えると、レセプターをめぐる競合とMVABの置換によって蛍光の消光が生ずる。このアッセイは既知量のMVABと未知量の標的タンパク質検体とが蛍光ポリマーからなるビーズの懸濁液に同時に付加される直接競合モードで実施
することができる。蛍光消光のレベルによって検体濃度を直接に測定することが可能である。このアッセイはまた、蛍光ポリマー−レセプター・コートされたビーズを標的検体で、その後にMVABで順次処理するかまたはその逆の処理による置換競合アッセイとして実施することもできる。
5.蛍光ポリマーまたはポリマー集合標識された標的によるQTLセンシング
抗原反応部位と化学反応部位との双方からなる反復パターンを表面に有する大きくかつ頑丈な生物学的種たとえば細菌芽胞およびウイルスは代替のポリマー超消光アッセイを供する。図4に概略的に示したように、このタイプの不活化された標的は蛍光ポリマーまたは蛍光ポリマー集合の表面に反応によって共有結合させるかまたはその他の方法で付着させることができる。
することができる。蛍光消光のレベルによって検体濃度を直接に測定することが可能である。このアッセイはまた、蛍光ポリマー−レセプター・コートされたビーズを標的検体で、その後にMVABで順次処理するかまたはその逆の処理による置換競合アッセイとして実施することもできる。
5.蛍光ポリマーまたはポリマー集合標識された標的によるQTLセンシング
抗原反応部位と化学反応部位との双方からなる反復パターンを表面に有する大きくかつ頑丈な生物学的種たとえば細菌芽胞およびウイルスは代替のポリマー超消光アッセイを供する。図4に概略的に示したように、このタイプの不活化された標的は蛍光ポリマーまたは蛍光ポリマー集合の表面に反応によって共有結合させるかまたはその他の方法で付着させることができる。
図4に示したように、蛍光ポリマーは不活化標的(たとえば、細菌芽胞)と共有結合して、機能化された不活化標的を形成することができる。図4には蛍光芽胞を示してある。付着レベルをコントロールして、標的に対するレセプターの結合部位をアクセスし得るようにしておくことが可能である。
図4に示したように、機能化された不活化標的(つまり、蛍光芽胞)は高度蛍光性を有している。レセプター消光剤・QTLバイオコンジュゲート(たとえばここでレセプターは抗体、抗体フラグメントまたはその他の結合試薬たとえばペプチドまたはその他の小分子結合剤であってよい)の付加は蛍光標的との結合を生じ、その蛍光の消光をもたらす。図4に示したように、標識された各々の標的はレセプター消光剤・コンジュゲートのいくつかの分子を収容することができる。さらにまた図4に示したように、非標識標的の付加はレセプター結合部位の「希釈」と、蛍光標識された標的からのレセプター消光剤・コンジュゲートの引き離しとを生ずる。結果として、蛍光の増強が観察されることとなる。
上述したアッセイの感度は、標的への蛍光ポリマーのコーティング程度の調節、コンジュゲートの構造と標識化/非標識化標的へのその親和力のチューニングによって調整することが可能である。前述したいくつかのQTLポリマー超消光アッセイで示されたように、実際の競合は、消光剤−結合剤・QTLと共に標識化標的を予備インキュベーションすることから、QTL、標的および標識化標的の直接の混合までに及ぶいくつかの異なったモードで実施することができる。
(溶液中および支持フォーマットでのセンシング用のプレフォームされたポリマー−タンパク質・複合体)
(溶液中でのセンシング用のポリマー−タンパク質・複合体の作製)
QTL溶液センサ(「センサSS」)は、56.5nmolのアビジン(ビオチン結合タンパク質、BBP)と848nmolのビオチン化PPEポリマー(1)とを混合して総容量11.3mLとし、CRTで24時間にわたってインキュベーションして作製された。ポリマーとBBPとはビオチン−アビジン相互作用を通じて互いに結合し、安定した要素を形成する。こうして作製された溶液センサはそれぞれの実験の開始時に緩衝液で適宜希釈された。ポリマー(1)の構造は以下の通りである。
QTL溶液センサ(「センサSS」)は、56.5nmolのアビジン(ビオチン結合タンパク質、BBP)と848nmolのビオチン化PPEポリマー(1)とを混合して総容量11.3mLとし、CRTで24時間にわたってインキュベーションして作製された。ポリマーとBBPとはビオチン−アビジン相互作用を通じて互いに結合し、安定した要素を形成する。こうして作製された溶液センサはそれぞれの実験の開始時に緩衝液で適宜希釈された。ポリマー(1)の構造は以下の通りである。
(固体−溶液・境界面でのセンシングへのプレフォームされたタンパク質−ポリマー・複合体の適応)
この実施例において、ポリマー−タンパク質・集合は第4アンモニウム基で機能化された、直径0.55ミクロンのポリスチレン微小球(MS)(Interfacial Dynamics Corporation製)に2段階手順でコートされた。第1段階において、前もって定められた量のポリマー(1)の溶液がノイトラビジン(もう1つのBBP)の溶液に付加されて、ポリマー反復単位(PRUs)とBBPとの最終的な比が5:1とされる。この溶液は周囲条件下で30分間にわたってインキュベーションされる。第2段階において、ポリマー/タンパク質・混合物はポリスチレン微小球に付加され、pH=7で2時間にわたってインキュベーションされ、次いでダイアフィルトレーションされ、リン酸緩衝生理食塩水に交換される。ポリマーとタンパク質のコーティング密度を定量するため示差蛍光分光分析法が使用された。
この実施例において、ポリマー−タンパク質・集合は第4アンモニウム基で機能化された、直径0.55ミクロンのポリスチレン微小球(MS)(Interfacial Dynamics Corporation製)に2段階手順でコートされた。第1段階において、前もって定められた量のポリマー(1)の溶液がノイトラビジン(もう1つのBBP)の溶液に付加されて、ポリマー反復単位(PRUs)とBBPとの最終的な比が5:1とされる。この溶液は周囲条件下で30分間にわたってインキュベーションされる。第2段階において、ポリマー/タンパク質・混合物はポリスチレン微小球に付加され、pH=7で2時間にわたってインキュベーションされ、次いでダイアフィルトレーションされ、リン酸緩衝生理食塩水に交換される。ポリマーとタンパク質のコーティング密度を定量するため示差蛍光分光分析法が使用された。
PPE−Bにつき、測定されたポリマーコーティング密度は4.75×106PRU/MS、測定されたタンパク質コーティング密度は9.5×105ノイトラビジン/MSである。微小球表面へのポリマー/タンパク質・混合物のコート完了後、蛍光標識されたビオチン誘導体を使用した結合実験から判明したように、球は球当たり約1.3×105ビオチン結合部位を有することが確認された。
図5は、ノイトラビジンと蛍光ポリマーの混合物が複合化され、こうして生じた複合物が固体支持体にコートされる上述したセンサ製造の反応スキームを示したものである。上述したように、ポリマー反復単位とノイトラビジンとの比は5:1である。図5に示したように、この複合体は静電相互作用により、アンモニウム基で機能化された微小球の表面
に固着され得る。
に固着され得る。
(実施例1で作製されたQTL溶液センサ(「センサSS」)を使用する酵素活性センシング)
384ウェル・プレートのBSEC−1(構造は以下に示す通りである)の400nMアッセイ緩衝液溶液5μLに、5μLのアッセイ緩衝液に溶解されたβ−セクレターゼ酵素30ngが加えられた。BSEC−1は以下のペプチド構造を有している:
(QSY7)−T−E−E−I−S−E−V−N−L−D−A−E−F−(K−ビオチン)−OH 配列番号1
(前記配列中、「QSY7」と「ビオチン」とは以下の式によって表される。
384ウェル・プレートのBSEC−1(構造は以下に示す通りである)の400nMアッセイ緩衝液溶液5μLに、5μLのアッセイ緩衝液に溶解されたβ−セクレターゼ酵素30ngが加えられた。BSEC−1は以下のペプチド構造を有している:
(QSY7)−T−E−E−I−S−E−V−N−L−D−A−E−F−(K−ビオチン)−OH 配列番号1
(前記配列中、「QSY7」と「ビオチン」とは以下の式によって表される。
この混合物は3連作製され、30分間にわたってCRTでインキュベーションされた。対照ウェルはペプチドしか含まず、酵素は含まなかった。インキュベーションの後、上記溶液センサの100倍の希釈液が各々のウェルに20μLずつ加えられた。プレートはマイクロプレート・リーダ内部でシェイクされ、ウェルは、440nmでポリマーを励起し、475nmカットオフ・フィルタを使用した530nmでの発光強度の測定によって検査された。対照ウェルの平均RFU値は5,400±200、酵素を含む試料ウェルの平均RFU値は8,350±200であった。この蛍光の差が酵素活性の測度であった。
以上にあってはBSEC−1を開示したが、その他のポリペプチドもβ−セクレターゼ酵素活性のアッセイに使用することが可能である。たとえば、本発明の代替の実施形態において、BSEC−3をβ−セクレターゼ酵素活性のアッセイに使用することができる。BSEC−3は以下に述べるポリペプチド構造を有している。
(AZO)−T−E−E−I−S−E−V−N−L−D−A−E−F−(K−ビオチン)−OH 配列番号2
上記のペプチド構造において、「QSY7」と「ビオチン」とは上述したように定義され、「AZO」は以下の式によって表される構造を有している。
(AZO)−T−E−E−I−S−E−V−N−L−D−A−E−F−(K−ビオチン)−OH 配列番号2
上記のペプチド構造において、「QSY7」と「ビオチン」とは上述したように定義され、「AZO」は以下の式によって表される構造を有している。
(BBP上の付加的なビオチン結合部位を使用し、ポリマー−タンパク質・複合体と複合し得るビオチン−R−フィコエリトリンを使用するアッセイ)
実施例3のアッセイ性能は上記の実施例1に述べたQTL溶液センサに少量のビオチン−R−フィコエリトリン(BRPE)をドープすることによって改善された。このようにして得られる溶液センサ(「センサYY」)は各々の実験の開始時に、「センサSS」のマスタストックをBRPEで、混合物40μL中に250 fmolのBRPEが含まれるような比で200倍に希釈した液をインキュベーションすることによって作製された。BSEC−3の300nMアッセイ緩衝液溶液5μLに、5μLのアッセイ緩衝液に溶解されたβ−セクレターゼ酵素30ngが加えられた。BSEC−3は上述したポリペプチド構造を有している。対照混合物と試料混合物を30分間にわたってCRTでインキュベーションした後、ドープされた溶液センサ(センサYY)40μLが各々のウェルに加えられた。プレートはプレート・リーダ内部で60秒間にわたってシェイクされ、ウェルの蛍光強度が、440nmでポリマーを励起し、576nmでの発光強度を475nmカットオフ・フィルタを使用して測定することによって検査された。対照ウェルの平均RFU値は5,200±200、酵素を含む試料ウェルのRFU値は14,500±200であった。観察されたこの差が酵素活性の測度であった。
実施例3のアッセイ性能は上記の実施例1に述べたQTL溶液センサに少量のビオチン−R−フィコエリトリン(BRPE)をドープすることによって改善された。このようにして得られる溶液センサ(「センサYY」)は各々の実験の開始時に、「センサSS」のマスタストックをBRPEで、混合物40μL中に250 fmolのBRPEが含まれるような比で200倍に希釈した液をインキュベーションすることによって作製された。BSEC−3の300nMアッセイ緩衝液溶液5μLに、5μLのアッセイ緩衝液に溶解されたβ−セクレターゼ酵素30ngが加えられた。BSEC−3は上述したポリペプチド構造を有している。対照混合物と試料混合物を30分間にわたってCRTでインキュベーションした後、ドープされた溶液センサ(センサYY)40μLが各々のウェルに加えられた。プレートはプレート・リーダ内部で60秒間にわたってシェイクされ、ウェルの蛍光強度が、440nmでポリマーを励起し、576nmでの発光強度を475nmカットオフ・フィルタを使用して測定することによって検査された。対照ウェルの平均RFU値は5,200±200、酵素を含む試料ウェルのRFU値は14,500±200であった。観察されたこの差が酵素活性の測度であった。
(蛍光ポリマー超消光をベースとした1本鎖および2本鎖DNAのアッセイ)
以下のデータはDNA検出に関するQTLアッセイの特異性を証明している。ここで使用されたアプローチはセンシング微小球の表面での相補捕獲鎖をめぐる標的と消光剤標識された標的との競合を含んでいる。
以下のデータはDNA検出に関するQTLアッセイの特異性を証明している。ここで使用されたアプローチはセンシング微小球の表面での相補捕獲鎖をめぐる標的と消光剤標識された標的との競合を含んでいる。
図7はさまざまなオリゴヌクレオチドとオリゴヌクレオチド混合物によるPPE蛍光の消光を示すグラフである。図7から看取されるように、DNA−QTLと微小球表面との非特異的な相互作用に帰着される最少消光が観察される。対照的に、DNA−QTL・コンジュゲートと捕獲鎖との特異的な相互作用は非特異的な消光のそれを上回る有意の消光を生じた。使用された捕獲鎖(つまり、ALF−捕獲。構造は以下に示す)は炭疽菌致死因子(ALF)のコード配列領域に対して相補的な配列を担持するビオチン化DNA捕獲鎖であった。
図7は17マーと20マーのDNA−QTLを使用した結果を示したものである。図7に示したすべての実験は96ウェル・プレート(ウェル当たり200mL Vt)で25℃にて実施された。各々の場合に、20pmolのオリゴヌクレオチドまたはオリゴヌクレオチド混合物が加えられた。
図7に挙げられたポリペプチドは以下のように定義される。
ALF−捕獲:
5’−ビオチン−TAA ATA CCA TTA AAA ATG CA−3’ 配列番号3
ALF−標的:
5’−TGC ATT TTT AAT GGT ATT TA−3’
配列番号4
DNA−QTL(20マー):
5’−TGC ATT TTT AAT GGT ATT TA−QSY7−3’ 配列番号5
DNA−QTL(17マー):
5’−ATT TTT AAT GGT ATT TA−QSY7−3’ 配列番号6
(前記配列中、「ビオチン」と「QSY7」とは上記に定義された通りである)。非相補的なDNAオリゴヌクレオチドは図7において「NC」と表記されている。
ALF−捕獲:
5’−ビオチン−TAA ATA CCA TTA AAA ATG CA−3’ 配列番号3
ALF−標的:
5’−TGC ATT TTT AAT GGT ATT TA−3’
配列番号4
DNA−QTL(20マー):
5’−TGC ATT TTT AAT GGT ATT TA−QSY7−3’ 配列番号5
DNA−QTL(17マー):
5’−ATT TTT AAT GGT ATT TA−QSY7−3’ 配列番号6
(前記配列中、「ビオチン」と「QSY7」とは上記に定義された通りである)。非相補的なDNAオリゴヌクレオチドは図7において「NC」と表記されている。
図7から看取されるように、ALF−捕獲鎖とDNA−QTLとの双方の存在は有意な消光増強を生じた。消光の増強はDNA−QTLとALF−捕獲鎖とのハイブリダイゼーションの結果である。さらに、ビオチン化されたALF−捕獲鎖は微小球の表面で蛍光ポリマーおよびビオチン結合タンパク質と複合体を形成する。それゆえ、DNA−QTLとALF−捕獲鎖とのハイブリダイゼーションは消光剤を蛍光ポリマーに近接させ、増幅された超消光を生ずる。
(単一ヌクレオチドDNA不整合を検出するための支持ポリマー−タンパク質・複合体の使用)
以下の例はセンサ(たとえば実施例2で説明したセンサ)がたとえ単一ヌクレオチドDNA不整合であっても存在を検出するために使用できることを証明している。この実験で使用されたアプローチはセンシング微小球の表面での相補捕獲鎖をめぐる標的と消光剤標識された標的との競合を含んでいる。
以下の例はセンサ(たとえば実施例2で説明したセンサ)がたとえ単一ヌクレオチドDNA不整合であっても存在を検出するために使用できることを証明している。この実験で使用されたアプローチはセンシング微小球の表面での相補捕獲鎖をめぐる標的と消光剤標識された標的との競合を含んでいる。
図8は以下に示す構造を有するPNAベースの捕獲鎖(「PNA−Cap」と称される)で負荷された微小球センサによる不整合分析を示すグラフである。実験は総ウェル容積200μLで40℃にて実施された。
上記の実験で使用された、図8に挙げたポリペプチドは以下のように定義される。
ALF標的:
5’−TGC ATT TTT AAT GGT ATT TA−3’
配列番号7
G−T不整合:
5’−TGC ATT TTT GAT GGT ATT TA−3’
配列番号8
T−T不整合:
5’−TGC ATT TTT TAT GGT ATT TA−3’
配列番号9
C−T 不整合:
5’−TGC ATT TTT CAT GGT ATT TA−3’
配列番号10
ダブル不整合:
5’−TGC ATA TTT AAT GGA ATT TA−3’
配列番号11
DNA−QTL:
5’−ATT TTT AAT GGT ATT TA−QSY7−3’ 配列番号12
PNA−捕獲:
ビオチン−TAA ATA CCA TTA AAA−Lys−NH2 配列番号13
前記配列中、「ビオチン」および「QSY7」は上記に定義した通りである。
ALF標的:
5’−TGC ATT TTT AAT GGT ATT TA−3’
配列番号7
G−T不整合:
5’−TGC ATT TTT GAT GGT ATT TA−3’
配列番号8
T−T不整合:
5’−TGC ATT TTT TAT GGT ATT TA−3’
配列番号9
C−T 不整合:
5’−TGC ATT TTT CAT GGT ATT TA−3’
配列番号10
ダブル不整合:
5’−TGC ATA TTT AAT GGA ATT TA−3’
配列番号11
DNA−QTL:
5’−ATT TTT AAT GGT ATT TA−QSY7−3’ 配列番号12
PNA−捕獲:
ビオチン−TAA ATA CCA TTA AAA−Lys−NH2 配列番号13
前記配列中、「ビオチン」および「QSY7」は上記に定義した通りである。
図8から判明するように、AAダブル不整合標的を除き、すべての標的につき標的量の増加と共に相対蛍光の増強が観察された。ただし、標的量の増加と共に観察された増強蛍光量は完全補体標的については遥かに高いものであった。
固体支持体はバイオアッセイへの使用に適したどんな材料からも作製することができる。この固体支持体はどんなサイズ、形状および形態であってもよい。固体支持体が作製される材料および固体支持体のサイズ、形状および形態は実施されるアッセイの要件に応じて変化させられてよい。典型的な固体支持体は微小球、ナノ粒子およびビーズであるが、ただしそれに制限されるものではない。たとえば、シリカまたはラテックス微小球を固体支持体として使用することが可能である。
固体支持体の表面は官能基からなっていてよい。固体支持体は官能基を含む材料から作製することができ、あるいはまた、そうした基を含まない固体支持体の表面は認知された技法を用いてそうした基を含むように機能化されてもよい。上述したように、固体支持体の表面はアンモニウム官能基からなっていてよい(たとえば、固体支持体の表面はアンモニウム官能基を含むように機能化されてよい)。固体支持体の表面は、ただしこれらに制限されるものではないが、帯電反応基、中性反応基およびカルボキシレート反応基を含むその他の官能基からなっているかまたはそれらの官能基からなるように機能化されてよい。
複合体に使用される蛍光ポリマーは、中性であるか、正または負に帯電しているか、または双性イオンである複合ポリマーであってよい。蛍光ポリマーはまた、J型凝集挙動を示すペンダント蛍光染料を有する非複合骨格からなる側鎖ポリマーであってもよい。典型的な蛍光ポリマーの構造は以下に示す通りである。
蛍光を消光するために励起された蛍光ポリマーからの放射エネルギを吸収し得るどんな成分も消光剤として使用することができる。典型的な消光剤は以下の種、つまり中性種、正または負に帯電しているかまたは双性イオン種、非蛍光または蛍光種、有機種、無機種、有機金属種、生物学的種または高分子種、あるいはエネルギもしくは電子移動種であるが、ただしこれらに制限されるものではない。本発明の1実施形態において、消光剤は非蛍光小分子染料たとえば前述したようなQSY−7またはAzo染料である。1実施形態において、消光剤は蛍光ポリマーの増幅消光(つまり、超消光)を行なうことができる。更なる1実施形態において、消光剤は蛍光体から吸収した放射エネルギを蛍光として再放出することができる。
蛍光ポリマー複合体はさらにビオチン化蛍光タンパク質を含んでいてよい。ビオチン化蛍光タンパク質はビオチン結合タンパク質のフリーのビオチン結合部位に結合することができる。典型的な蛍光タンパク質はフィコエリトリンおよびフィコビリゾームであるが、ただしこれらに制限されるものではない。たとえば、ビオチン化蛍光タンパク質はビオチン化R−フィコエリトリン(BRPE)であってよい。蛍光タンパク質が存在する場合に
は、励起された蛍光ポリマーの発色団はそのエネルギを複合体中の蛍光タンパク質分子に移動させることができる。すると、蛍光タンパク質分子はそのエネルギをより効率的に再放出することができる。たとえば、BPREを含む蛍光ポリマー複合体の使用は鮮明な、赤にシフトされた蛍光信号を生ずる。この場合、複合体からの蛍光放出は、消光剤を含むバイオコンジュゲートが複合体と会合すると(たとえば、消光剤を含むビオチン化バイオコンジュゲートが複合体に結合するかあるいはポリヌクレオチドまたはペプチド核酸配列と消光剤とを含む第2のバイオコンジュゲートが複合体と会合した捕獲鎖に対してハイブリッド形成すると)、消光され得る。
は、励起された蛍光ポリマーの発色団はそのエネルギを複合体中の蛍光タンパク質分子に移動させることができる。すると、蛍光タンパク質分子はそのエネルギをより効率的に再放出することができる。たとえば、BPREを含む蛍光ポリマー複合体の使用は鮮明な、赤にシフトされた蛍光信号を生ずる。この場合、複合体からの蛍光放出は、消光剤を含むバイオコンジュゲートが複合体と会合すると(たとえば、消光剤を含むビオチン化バイオコンジュゲートが複合体に結合するかあるいはポリヌクレオチドまたはペプチド核酸配列と消光剤とを含む第2のバイオコンジュゲートが複合体と会合した捕獲鎖に対してハイブリッド形成すると)、消光され得る。
上記明細書は説明を目的とした一連の実施例により本発明の原理を教示するものであるが、他方、本開示を一読することにより当業者には本発明の趣旨を逸脱することなく形態および詳細につき様々な変化を行なうことが可能である旨理解されよう。
Claims (57)
- ビオチン化蛍光ポリマーとビオチン結合タンパク質とを水溶液中で結合させて複合体を形成するステップを含み、該複合体はフリーのビオチン結合部位を有するように構成した、生物学的認識事象を検出するためのセンサの作製方法。
- さらに、ビオチン化蛍光タンパク質をビオチン化蛍光ポリマーおよびビオチン結合タンパク質と結合させるステップを含む、請求項1に記載の方法。
- 蛍光タンパク質はフィコエリトリンまたはフィコビリゾームである、請求項2に記載の方法。
- さらに、複合体を固体支持体の表面に配置するステップを含む、請求項1に記載の方法。
- 固体支持体は微小球、ナノ粒子またはビーズを含む、請求項4に記載の方法。
- 固体支持体の表面はアンモニウム官能基、カルボキシレート官能基、帯電反応基および中性反応基のみからなる群から選択された官能基を含む、請求項4に記載の方法。
- ビオチン結合タンパク質はアビジン、ストレプトアビジンおよびノイトラビジンからなる群から選択される、請求項1に記載の方法。
- さらに、ヌクレオチド配列、ペプチド核酸配列またはポリペプチド配列を含むビオチン化バイオコンジュゲートが水溶液に添加されるステップを含み、該ビオチン化バイオコンジュゲートは複合体に結合する、請求項1に記載の方法。
- ビオチン化バイオコンジュゲートはポリヌクレオチドまたはペプチド核酸配列を含み、生物学的認識事象は標的検体に対する該ビオチン化バイオコンジュゲートのポリヌクレオチド配列またはペプチド核酸の核酸ハイブリダイゼーションである、請求項9に記載の方法。
- ビオチン化バイオコンジュゲートはポリペプチド配列と消光剤とを含み、該消光剤は蛍光ポリマーの増幅超消光を行なうことができ、生物学的認識事象はポリペプチド配列の酵素誘導開裂である、請求項9に記載の方法。
- さらに、消光剤とポリヌクレオチドまたはペプチド核酸配列とを含む第2のバイオコンジュゲートが水溶液に添加されるステップを含み、該消光剤は蛍光ポリマーの増幅超消光を行なうことができ、第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことができる、請求項10に記載の方法。
- 第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列と相補的である、請求項12に記載の方法。
- ビオチン化蛍光ポリマーとビオチン結合タンパク質との複合体を含み、該複合体はフリーのビオチン結合部位を有する、生物学的認識事象を検出するためのセンサ。
- さらに、固体支持体を含み、複合体は該固体支持体の表面に配置されている、請求項16に記載のセンサ。
- さらに、ポリヌクレオチド配列、ペプチド核酸配列またはポリペプチド配列を含むビオチン化バイオコンジュゲートを含み、該ビオチン化バイオコンジュゲートは複合体に結合させられている、請求項16に記載のセンサ。
- ビオチン化バイオコンジュゲートはポリヌクレオチド配列を含み、生物学的認識事象は標的検体に対するビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列の核酸ハイブリダイゼーションである、請求項18に記載のセンサ。
- ビオチン化バイオコンジュゲートはポリペプチド配列と消光剤とを含み、該消光剤は蛍
光ポリマーの増幅超消光を行なうことができ、生物学的認識事象はポリペプチド配列の酵素誘導開裂である、請求項18に記載のセンサ。 - ビオチン結合タンパク質はアビジン、ストレプトアビジンおよびノイトラビジンからなる群から選択される、請求項16に記載のセンサ。
- 固体支持体は微小球、ナノ粒子またはビーズを含む、請求項17に記載のセンサ。
- 固体支持体の表面はアンモニウム官能基、カルボキシレート官能基、帯電反応基および中性反応基からなる群から選択されたいずれかの官能基からなる、請求項17に記載のセンサ。
- 請求項17に記載のセンサであって、前記複合体はさらに、
連結鎖の第1と第2の位置に結合されたリガンドおよびビオチン成分を含むビオチン化バイオコンジュゲートを含み;
前記リガンドは消光剤成分を含み;
前記消光剤成分は蛍光ポリマーの増幅超消光を行なうことができ;
前記リガンドは生物学的認識事象に関与することができ;そして
前記の第1と第2の位置の間の連結鎖部は生物学的認識事象の発生が固体支持体表面からの前記消光剤の分離とそれに伴う蛍光の増強とを生ずるような長さと柔軟性とを有している
センサ。 - リガンドはポリペプチド配列を含む、請求項25に記載のセンサ。
- nは70以上80以下の整数である、請求項27に記載のセンサ。
- nは75である、請求項27に記載のセンサ。
- 連結鎖は完全に延びた状態において少なくとも250Åの長さを有する、請求項25に記載のセンサ。
- さらに、ビオチン化蛍光タンパク質を含み、該ビオチン化蛍光タンパク質はビオチン化蛍光ポリマーおよびビオチン結合タンパク質と複合体を形成している、請求項16に記載のセンサ。
- 蛍光タンパク質はフィコエリトリンまたはフィコビリゾームである、請求項31に記載のセンサ。
- 試料を、
ポリヌクレオチド配列、ペプチド核酸配列またはポリペプチド配列を含むビオチン化バイオコンジュゲート;および
請求項16に記載のセンサ
と結合させるステップを含む、試料中の標的検体の存在および/または量を検出する方法。 - 請求項33に記載の方法であって、ビオチン化バイオコンジュゲートがポリヌクレオチドまたはペプチド核酸配列を含む場合、該方法はさらに:
試料を消光剤とポリヌクレオチドまたはペプチド核酸配列とを含む第2のバイオコンジュゲートと結合させるステップを含み;
該消光剤は蛍光ポリマーの増幅超消光を行なうことができ;
第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことができ;そして
標的検体はビオチン化バイオコンジュゲートかまたは第2のバイオコンジュゲートのいずれかのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行なうことのできるポリヌクレオチド配列を含む
方法。 - 第2のバイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列と相補的である、請求項34に記載の方法。
- ビオチン化バイオコンジュゲートはポリペプチド配列を含むと共にさらに消光剤を含み
、ビオチン化バイオコンジュゲートと複合体との結合は蛍光ポリマーの蛍光を消光し、標的検体はポリペプチド配列を開裂させることのできる酵素である、請求項33に記載の方法。 - 試料を請求項25に記載のセンサと結合させるステップを含む、試料中の標的検体の存在および/または量を検出する方法。
- リガンドはポリペプチド配列を含む、請求項37に記載の方法。
- 標的検体は、芽胞、細胞、細菌またはウイルスからなる群から選択される、請求項37に記載の方法。
- 請求項25に記載のセンサと、その表面に配置された多数の標的成分を有する第2の固体支持体を含み、ビオチン化バイオコンジュゲートのリガンドは標的成分と相互作用して消光剤を蛍光体から分離し、これによって蛍光ポリマーの蛍光が増大する、生物学的認識事象を検出するためのセンシングシステム。
- リガンドはポリペプチド配列を含む、請求項40に記載のセンシングシステム。
- 第2の固体支持体は微小球、ナノ粒子またはビーズである、請求項40に記載のセンシングシステム。
- 請求項40に記載のセンシングシステムを試料と結合させるステップを含み、標的検体はリガンドを認識してそれと相互作用し、標的検体とリガンドとの相互作用は蛍光の減少を生ずる、試料中の標的検体の存在および/または量を検出する方法。
- リガンドはポリペプチドを含み、生物学的認識事象はリガンドのポリペプチドとポリペプチドを含む標的検体との相互作用を包含する、請求項43に記載の方法。
- 試料をビオチン化バイオコンジュゲートおよび第2のバイオコンジュゲートと共にインキュベーションし、インキュベーションされた試料にセンサを加えるステップを含む、請求項34に記載の方法。
- センサとビオチン化バイオコンジュゲートとはビオチン化バイオコンジュゲートがセンサと複合するようにして結合され、続いて試料がセンサ/ビオチン化バイオコンジュゲート・複合体と共にインキュベーションされ、続いて第2のバイオコンジュゲートがインキュベーションされた試料に加えられる、請求項34に記載の方法。
- 請求項46に記載の方法であって、標的検体のヌクレオチド配列が2本鎖核酸を含む場合、該方法は以下のステップ;
インキュベーションされた試料を第2のバイオコンジュゲートの存在下で試料中の2本鎖核酸が融解するのに十分な温度にまで加熱するステップ;および
2重鎖生成が可能となるまで試料を冷却するステップ
を包含し、試料中に存在する標的検体と第2のバイオコンジュゲートとの間の2重鎖生成は蛍光の増強を生ずる方法。 - ビオチン化バイオコンジュゲートはペプチド核酸配列を含む、請求項46に記載の方法。
- 表面のレセプタに対する多数のリガンドを有する細菌芽胞またはウイルスと、細菌芽胞
またはウイルスの表面に配置された蛍光ポリマーまたは蛍光ポリマー複合体と、リガンドに対するレセプタに結合された消光剤を含む多数のバイオコンジュゲートを含み、レセプタとリガンドとは相互作用し、レセプタとリガンドの相互作用は蛍光ポリマーの蛍光の増幅超消光を生ずる、標的生物学的種を検出するためのセンサ。 - 試料を請求項49に記載のセンサと共にインキュベーションするステップを含み、試料中の標的検体はレセプタを認識してそれと相互作用し、試料中の標的検体とレセプタとの相互作用は蛍光の増強を生ずる、試料中の標的検体の存在および/または量を検出する方法。
- 標的検体は表面のレセプタに対する多数のリガンドを有する細菌芽胞またはウイルスを含む、請求項50に記載の方法。
- ビオチン化バイオコンジュゲートはポリヌクレオチドまたはペプチド核酸配列を含むと共にさらに蛍光ポリマーの増幅超消光を行なうことのできる消光剤を含み、ポリヌクレオチド配列はビオチン化バイオコンジュゲートの消光剤とビオチンとの間に位置している、請求項17に記載のセンサ。
- 試料を請求項52に記載のセンサと結合させるステップを含み、標的検体はビオチン化バイオコンジュゲートのポリヌクレオチドまたはペプチド核酸配列に対するハイブリッド形成を行うことのできるポリヌクレオチド配列を含み、該ハイブリダイゼーションは固体支持体の表面からの消光剤分離の増加とそれに伴う蛍光の増強とを生ずる、試料中の標的検体の存在および/または量を検出する方法。
- 固体支持体はシリカまたはラテックス微小球を含む、請求項6に記載の方法。
- 固体支持体はシリカまたはラテックス微小球を含む、請求項23に記載のセンサ。
- 第2の固体支持体の表面はアンモニウム官能基、カルボキシレート官能基、帯電反応基および中性反応基からなる群から選択されたいずれかの官能基を含む、請求項40に記載のセンシングシステム。
- 第2の固体支持体はシリカまたはラテックス微小球を含む、請求項42に記載のセンシングシステム。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US42603402P | 2002-11-14 | 2002-11-14 | |
| PCT/US2003/036153 WO2004046687A2 (en) | 2002-11-14 | 2003-11-14 | Methods of biosensing using fluorescent polymers and quencher-tether-ligand bioconjugates |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2006506643A true JP2006506643A (ja) | 2006-02-23 |
Family
ID=32326307
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004553594A Withdrawn JP2006506643A (ja) | 2002-11-14 | 2003-11-14 | 蛍光ポリマーと消光剤−連結鎖−リガンド・バイオコンジュゲートとを使用するバイオセンシング法 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20040175768A1 (ja) |
| EP (1) | EP1579215A4 (ja) |
| JP (1) | JP2006506643A (ja) |
| KR (1) | KR20050086658A (ja) |
| CN (1) | CN1742201A (ja) |
| AU (1) | AU2003295485A1 (ja) |
| CA (1) | CA2505907A1 (ja) |
| WO (1) | WO2004046687A2 (ja) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050147534A1 (en) * | 1998-05-05 | 2005-07-07 | Massachusetts Institute Of Technology | Emissive sensors and devices incorporating these sensors |
| US8198096B2 (en) | 1998-05-05 | 2012-06-12 | Massachusetts Institute Of Technology | Emissive polymers and devices incorporating these polymers |
| WO1999057222A1 (en) | 1998-05-05 | 1999-11-11 | Massachusetts Institute Of Technology | Emissive polymers and devices incorporating these polymers |
| US6706474B1 (en) | 2000-06-27 | 2004-03-16 | Board Of Trustees Of The University Of Illinois | Nucleic acid enzyme biosensors for ions |
| US7462325B2 (en) * | 2001-11-30 | 2008-12-09 | Nomadics, Inc. | Luminescent polymer particles |
| US6890719B2 (en) | 2002-05-10 | 2005-05-10 | The Board Of Trustess Of The University Of Illinois | Fluorescence based biosensor |
| US20050014160A1 (en) * | 2003-07-18 | 2005-01-20 | Sriram Kumaraswamy | Assays for protease enzyme activity |
| US8617819B2 (en) | 2004-09-17 | 2013-12-31 | Massachusetts Institute Of Technology | Polymers for analyte detection |
| US20070026388A1 (en) * | 2005-07-28 | 2007-02-01 | Doorn Stephen K | Analyte detection using carbon nanotubes |
| US7892734B2 (en) | 2005-08-11 | 2011-02-22 | The Board Of Trustees Of The University Of Illinois | Aptamer based colorimetric sensor systems |
| US7799554B2 (en) | 2006-03-16 | 2010-09-21 | The Board Of Trustees Of The University Of Illinois | Lateral flow devices |
| US8158437B2 (en) * | 2006-08-04 | 2012-04-17 | Massachusetts Institute Of Technology | Luminescent detection of hydrazine and hydrazine derivatives |
| WO2008042289A2 (en) | 2006-09-29 | 2008-04-10 | Massachusetts Institute Of Technology | Polymer synthetic technique |
| US8802447B2 (en) | 2006-10-05 | 2014-08-12 | Massachusetts Institute Of Technology | Emissive compositions with internal standard and related techniques |
| US20090215189A1 (en) * | 2006-10-27 | 2009-08-27 | Massachusetts Institute Of Technology | Sensor of species including toxins and chemical warfare agents |
| US8058415B2 (en) | 2007-04-24 | 2011-11-15 | The Board Of Trustees Of The University Of Illinois | Aptamer- and nucleic acid enzyme-based systems for simultaneous detection of multiple analytes |
| SG192445A1 (en) * | 2008-06-02 | 2013-08-30 | Brookhaven Science Ass Llc | Controllable assembly and disassembly of nanoparticle systems via protein and dna agents |
| JP5476376B2 (ja) * | 2008-07-16 | 2014-04-23 | ラジオメーター・メディカル・アー・ペー・エス | 高性能固相 |
| CN102516836B (zh) * | 2011-12-03 | 2014-04-16 | 东南大学 | 噻吩-共-噁二唑作为氧猝灭物质的应用 |
| GB2502306A (en) * | 2012-05-22 | 2013-11-27 | Univ Singapore | Microparticle sensor |
| WO2014038744A1 (ko) * | 2012-09-07 | 2014-03-13 | 제노마인 | 신장암 혈액 바이오마커의 검출 방법 및 키트 |
| EP3172569A1 (en) | 2014-07-25 | 2017-05-31 | Selux Diagnostics Inc. | Assay methods involving dissociable nanoparticles |
| CN107430107B (zh) * | 2015-03-11 | 2019-08-30 | 双孔人公司 | 通过竞争分析的小分子的纳米孔隙检测 |
| AU2016256391B2 (en) * | 2015-04-29 | 2019-07-11 | Dots Technology Corp. | Compositions and methods for allergen detection |
| WO2019191482A1 (en) | 2018-03-30 | 2019-10-03 | Becton, Dickinson And Company | Water-soluble polymeric dyes having pendant chromophores |
| EP3814748A4 (en) | 2018-06-28 | 2022-03-30 | Becton, Dickinson and Company | LIGHT DETECTION SYSTEMS WITH INTEGRATED PREAMPLIFIER AND METHODS OF USE THEREOF |
| CN111850103B (zh) * | 2020-08-20 | 2022-12-02 | 清华大学深圳国际研究生院 | 一种基于阳离子共轭聚合物和核酸酶辅助循环扩增的检测目的核酸的方法 |
| CN113358612B (zh) * | 2021-05-24 | 2022-11-08 | 宁波大学 | 一种藻类检测微纳光学传感器及其制作与检测方法 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4859582A (en) * | 1981-10-06 | 1989-08-22 | The Board Of Trustees Of The Leland Stanford Jr. University | Fluorescent conjugates for analysis of molecules and cells |
| US5055556A (en) * | 1981-10-06 | 1991-10-08 | The Board Of Trustees Of The Leland Stanford Jr. Univ. | Fluorescent conjugates for analysis of molecules and cells |
| US4542104A (en) * | 1983-04-06 | 1985-09-17 | The Board Of Trustees Of The Leland Stanford Jr. Univ. | Phycobiliprotein fluorescent conjugates |
| FR2638462B1 (fr) * | 1988-10-28 | 1992-05-22 | Oris Ind | Complexes tridimensionnels a base de streptavidine (ou avidine) et de composes luminescents polybiotinyles |
| US5708154A (en) * | 1989-02-24 | 1998-01-13 | City Of Hope | RNA-DNA hybrid molecules of nucleic acid |
| US5260004A (en) * | 1991-12-02 | 1993-11-09 | The United States Of America As Represented By The Secretary Of The Army | Process of making Langmuir-Blodgett films having photo-electronic properties |
| US5736410A (en) * | 1992-09-14 | 1998-04-07 | Sri International | Up-converting reporters for biological and other assays using laser excitation techniques |
| US5536820A (en) * | 1993-02-26 | 1996-07-16 | E. I. Du Pont De Nemours And Company | Avidin-binding azo reagents |
| US6342389B1 (en) * | 1995-04-10 | 2002-01-29 | Roger S. Cubicciotti | Modified phycobilisomes and uses therefore |
| US6133429A (en) * | 1997-10-03 | 2000-10-17 | Becton Dickinson And Company | Chromophores useful for the preparation of novel tandem conjugates |
| US20010008766A1 (en) * | 1998-03-17 | 2001-07-19 | Sylvia Daunert | Quantitative binding assays using green fluorescent protein as a label |
| FR2778918B1 (fr) * | 1998-05-25 | 2000-07-21 | Commissariat Energie Atomique | Baton moleculaire et ses applications |
| US6303325B1 (en) * | 1998-05-29 | 2001-10-16 | Dade Behring Inc. | Method for detecting analytes |
| IL153943A0 (en) * | 2000-07-19 | 2003-07-31 | Upjohn Co | SUBSTRATES AND ASSAYS FOR beta-SECRETASE ACTIVITY |
| US20020160363A1 (en) * | 2001-01-31 | 2002-10-31 | Mcdevitt John T. | Magnetic-based placement and retention of sensor elements in a sensor array |
| KR20040010610A (ko) * | 2001-03-16 | 2004-01-31 | 큐티엘 바이오시스템즈 엘엘씨 | 형광 폴리머 수퍼퀀칭-기초로 한 생물학적 어세이 |
| CA2458405A1 (en) * | 2001-08-23 | 2003-03-06 | Qtl Biosystems, Llc | Bio-sensing platforms for detection and quantitation of biological molecules |
| EP1437594B1 (en) * | 2001-09-19 | 2011-01-12 | Sekisui Medical Co., Ltd. | Luminescent polymer and use thereof in bioassay |
-
2003
- 2003-11-14 EP EP03786675A patent/EP1579215A4/en not_active Withdrawn
- 2003-11-14 WO PCT/US2003/036153 patent/WO2004046687A2/en not_active Application Discontinuation
- 2003-11-14 KR KR1020057008718A patent/KR20050086658A/ko not_active Application Discontinuation
- 2003-11-14 CN CNA2003801087483A patent/CN1742201A/zh active Pending
- 2003-11-14 US US10/712,004 patent/US20040175768A1/en not_active Abandoned
- 2003-11-14 CA CA002505907A patent/CA2505907A1/en not_active Abandoned
- 2003-11-14 AU AU2003295485A patent/AU2003295485A1/en not_active Abandoned
- 2003-11-14 JP JP2004553594A patent/JP2006506643A/ja not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| CA2505907A1 (en) | 2004-06-03 |
| US20040175768A1 (en) | 2004-09-09 |
| WO2004046687A3 (en) | 2005-07-21 |
| WO2004046687A2 (en) | 2004-06-03 |
| AU2003295485A1 (en) | 2004-06-15 |
| EP1579215A2 (en) | 2005-09-28 |
| EP1579215A4 (en) | 2007-01-17 |
| CN1742201A (zh) | 2006-03-01 |
| KR20050086658A (ko) | 2005-08-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2006506643A (ja) | 蛍光ポリマーと消光剤−連結鎖−リガンド・バイオコンジュゲートとを使用するバイオセンシング法 | |
| US6974669B2 (en) | Bio-barcodes based on oligonucleotide-modified nanoparticles | |
| EP1379693B1 (en) | Bio-barcodes based on oligonucleotide-modified particles | |
| US20030054413A1 (en) | Bio-sensing platforms for detection and quantitation of biological molecules | |
| AU2003237180B2 (en) | Nanoparticle probes with raman spectroscopic fingerprints for analyte detection | |
| EP1766085B1 (en) | Aptamer-nanoparticle conjugates and method of use for target analyte detection | |
| EP1747295B1 (en) | Bio-barcode based detection of target analytes | |
| US20090111094A1 (en) | Methods for preparing hybrid substrates comprising DNA and antibodies and uses thereof | |
| JP2003525429A (ja) | 固体物に付着されたマークを識別する方法 | |
| Noel et al. | DNA for non-nucleic acid sensing | |
| US20050239078A1 (en) | Sequence tag microarray and method for detection of multiple proteins through DNA methods | |
| AU2002329805A1 (en) | Bio-sensing platforms for detection and quantitation of biological molecules | |
| US20040121401A1 (en) | Integrated light source for diagnostic arrays |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061114 |
|
| A072 | Dismissal of procedure [no reply to invitation to correct request for examination] |
Free format text: JAPANESE INTERMEDIATE CODE: A073 Effective date: 20070424 |
|
| A300 | Application deemed to be withdrawn because no request for examination was validly filed |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20070501 |