JP2005291909A - 内面処理された検体用容器およびその処理方法 - Google Patents
内面処理された検体用容器およびその処理方法 Download PDFInfo
- Publication number
- JP2005291909A JP2005291909A JP2004106929A JP2004106929A JP2005291909A JP 2005291909 A JP2005291909 A JP 2005291909A JP 2004106929 A JP2004106929 A JP 2004106929A JP 2004106929 A JP2004106929 A JP 2004106929A JP 2005291909 A JP2005291909 A JP 2005291909A
- Authority
- JP
- Japan
- Prior art keywords
- container
- group
- colloidal silica
- specimen
- groups
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims description 61
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims abstract description 115
- 239000008119 colloidal silica Substances 0.000 claims abstract description 107
- 125000003277 amino group Chemical group 0.000 claims abstract description 105
- 239000000427 antigen Substances 0.000 claims abstract description 64
- 102000036639 antigens Human genes 0.000 claims abstract description 62
- 108091007433 antigens Proteins 0.000 claims abstract description 62
- 239000003550 marker Substances 0.000 claims abstract description 61
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims abstract description 54
- 230000027455 binding Effects 0.000 claims abstract description 23
- 238000002372 labelling Methods 0.000 claims abstract description 14
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims abstract description 10
- 125000003396 thiol group Chemical group [H]S* 0.000 claims abstract description 10
- 238000003018 immunoassay Methods 0.000 claims abstract description 9
- 125000000524 functional group Chemical group 0.000 claims description 37
- 239000002245 particle Substances 0.000 claims description 31
- 238000004381 surface treatment Methods 0.000 claims description 18
- -1 amine compound Chemical class 0.000 claims description 16
- 239000002904 solvent Substances 0.000 claims description 13
- 125000005641 methacryl group Chemical group 0.000 claims description 11
- 125000001841 imino group Chemical group [H]N=* 0.000 claims description 8
- 229920000083 poly(allylamine) Polymers 0.000 claims description 6
- 239000003513 alkali Substances 0.000 claims description 5
- 230000007062 hydrolysis Effects 0.000 claims description 5
- 238000006460 hydrolysis reaction Methods 0.000 claims description 5
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 claims description 4
- 229920000768 polyamine Polymers 0.000 claims description 4
- 238000006482 condensation reaction Methods 0.000 claims description 3
- 150000004985 diamines Chemical class 0.000 claims description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 2
- 210000000987 immune system Anatomy 0.000 abstract description 15
- 238000004458 analytical method Methods 0.000 abstract description 3
- 125000005395 methacrylic acid group Chemical group 0.000 abstract description 2
- 239000007790 solid phase Substances 0.000 abstract description 2
- 239000007787 solid Substances 0.000 abstract 1
- 238000005259 measurement Methods 0.000 description 29
- 238000002474 experimental method Methods 0.000 description 20
- 239000000243 solution Substances 0.000 description 15
- 239000000126 substance Substances 0.000 description 13
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 12
- 108090001008 Avidin Proteins 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 102000004169 proteins and genes Human genes 0.000 description 11
- 108090000623 proteins and genes Proteins 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 10
- 230000008569 process Effects 0.000 description 9
- 239000011521 glass Substances 0.000 description 8
- 229920003023 plastic Polymers 0.000 description 8
- 239000004033 plastic Substances 0.000 description 8
- 230000000903 blocking effect Effects 0.000 description 7
- 238000003672 processing method Methods 0.000 description 7
- 241000238366 Cephalopoda Species 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 6
- 229960002685 biotin Drugs 0.000 description 6
- 235000020958 biotin Nutrition 0.000 description 6
- 239000011616 biotin Substances 0.000 description 6
- 239000010419 fine particle Substances 0.000 description 6
- 238000001179 sorption measurement Methods 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- 229910000859 α-Fe Inorganic materials 0.000 description 6
- 239000004925 Acrylic resin Substances 0.000 description 5
- 229920000178 Acrylic resin Polymers 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 5
- 230000035945 sensitivity Effects 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 4
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 239000007853 buffer solution Substances 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 4
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 4
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 4
- 239000006228 supernatant Substances 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 238000004364 calculation method Methods 0.000 description 3
- 230000008878 coupling Effects 0.000 description 3
- 238000010168 coupling process Methods 0.000 description 3
- 238000005859 coupling reaction Methods 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 230000002209 hydrophobic effect Effects 0.000 description 3
- 230000003100 immobilizing effect Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000008055 phosphate buffer solution Substances 0.000 description 3
- 238000000087 superconducting quantum interference device magnetometry Methods 0.000 description 3
- 238000010998 test method Methods 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 2
- BTJIUGUIPKRLHP-UHFFFAOYSA-N 4-nitrophenol Chemical compound OC1=CC=C([N+]([O-])=O)C=C1 BTJIUGUIPKRLHP-UHFFFAOYSA-N 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- 229910004298 SiO 2 Inorganic materials 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- OHDRQQURAXLVGJ-HLVWOLMTSA-N azane;(2e)-3-ethyl-2-[(e)-(3-ethyl-6-sulfo-1,3-benzothiazol-2-ylidene)hydrazinylidene]-1,3-benzothiazole-6-sulfonic acid Chemical compound [NH4+].[NH4+].S/1C2=CC(S([O-])(=O)=O)=CC=C2N(CC)C\1=N/N=C1/SC2=CC(S([O-])(=O)=O)=CC=C2N1CC OHDRQQURAXLVGJ-HLVWOLMTSA-N 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000003431 cross linking reagent Substances 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 230000009881 electrostatic interaction Effects 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 238000012856 packing Methods 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 238000007781 pre-processing Methods 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 229910000077 silane Inorganic materials 0.000 description 2
- 230000009870 specific binding Effects 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- VLEHUIOENHDIKW-YFKPBYRVSA-N (2s)-2-(prop-2-enoylamino)pentanedioic acid Chemical compound OC(=O)CC[C@@H](C(O)=O)NC(=O)C=C VLEHUIOENHDIKW-YFKPBYRVSA-N 0.000 description 1
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 1
- HKAVADYDPYUPRD-UHFFFAOYSA-N 1h-pyrazine-2-thione Chemical compound SC1=CN=CC=N1 HKAVADYDPYUPRD-UHFFFAOYSA-N 0.000 description 1
- XYPTZZQGMHILPQ-UHFFFAOYSA-N 2-methyl-6-trimethoxysilylhex-1-en-3-one Chemical compound CO[Si](OC)(OC)CCCC(=O)C(C)=C XYPTZZQGMHILPQ-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 235000011330 Armoracia rusticana Nutrition 0.000 description 1
- 240000003291 Armoracia rusticana Species 0.000 description 1
- 229920001342 Bakelite® Polymers 0.000 description 1
- 101100191768 Caenorhabditis elegans pbs-4 gene Proteins 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical compound NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 102000004890 Interleukin-8 Human genes 0.000 description 1
- 108090001007 Interleukin-8 Proteins 0.000 description 1
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 1
- 238000006845 Michael addition reaction Methods 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000006087 Silane Coupling Agent Substances 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000005904 alkaline hydrolysis reaction Methods 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000004637 bakelite Substances 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000029918 bioluminescence Effects 0.000 description 1
- 238000005415 bioluminescence Methods 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 238000011088 calibration curve Methods 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 238000002296 dynamic light scattering Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000001917 fluorescence detection Methods 0.000 description 1
- BHEPBYXIRTUNPN-UHFFFAOYSA-N hydridophosphorus(.) (triplet) Chemical compound [PH] BHEPBYXIRTUNPN-UHFFFAOYSA-N 0.000 description 1
- 125000005462 imide group Chemical group 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- XKTZWUACRZHVAN-VADRZIEHSA-N interleukin-8 Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](NC(C)=O)CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N1[C@H](CCC1)C(=O)N1[C@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC(O)=CC=1)C(=O)N[C@H](CO)C(=O)N1[C@H](CCC1)C(N)=O)C1=CC=CC=C1 XKTZWUACRZHVAN-VADRZIEHSA-N 0.000 description 1
- 229940096397 interleukin-8 Drugs 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000005389 magnetism Effects 0.000 description 1
- 230000005415 magnetization Effects 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-N picric acid Chemical compound OC1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-N 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000012827 research and development Methods 0.000 description 1
- 238000003118 sandwich ELISA Methods 0.000 description 1
- 239000011163 secondary particle Substances 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
Images
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
Abstract
【解決手段】固相化された一次抗体に抗原を捕捉させ、更に標識マーカーによって標識化された二次抗体を該抗原に捕捉させることで該抗原を定量化する各種免疫測定法に使用される検体用容器において、多数のアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基が付加されたコロイダルシリカが、容器内面の所要領域を覆うように結合させた。
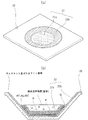
【選択図】図1
Description
シンプル免疫学 南江堂
NUNC catalogue 2002−2003
固相化された一次抗体に抗原を捕捉させ、更に標識マーカーによって標識化された二次抗体を該抗原に捕捉させることで該抗原を定量化する各種免疫測定法に使用される検体用容器において、
多数のアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基が付加されたコロイダルシリカが、容器内面の所要領域を覆うように結合されており、
前記標識マーカーによって標識化された二次抗体は、一次抗体および抗原を介して、前記コロイダルシリカのアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基だけに結合されるよう構成したことを特徴とする。
固相化された一次抗体に抗原を捕捉させ、更に標識マーカーによって標識化された二次抗体を該抗原に捕捉させることで該抗原を定量化する各種免疫測定法に使用される検体用容器の内面処理方法にあって、
検体用容器の容器内面に前処理を実施して所要の官能基を付与し、
別工程でアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基を付加した所要粒径のコロイダルシリカを、前記前処理で付与させた官能基に結合させて、前記容器内面の所要領域を被覆させ、
前記標識マーカーによって標識化された二次抗体を、一次抗体および抗原を介して、前記コロイダルシリカのアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基だけに結合させるようにしたことを特徴とする。
SUMITOMO BAKELITE Co.JP ホームページ資料「SUMILON」2002
前述の実施例においては標識化された二次抗体ab2として、抗原agに対して特異性を有する二次抗体ab2と標識マーカーMとを単に結合した形態の例を挙げているが(図4参照)、本発明はこれに限定されるのではなく、必要に応じて二次抗体ab2と標識マーカーMとを、別の特異性を有する抗体同士の結合を介して結合させるようにしてもよい。例えば標識マーカーMとして使用される磁気マーカーは、現在においてはその経時変化による安定性が6ヶ月程度であり、長期保存にあまり向いていないことが確認されている。その一方で抗原agの迅速な測定を考える場合、磁気マーカーは予め二次抗体ab2と結合した状態として保存しておくことが望ましい。しかし磁気マーカーは前述の如く、その長期に亘る安定性が低いため、二次抗体ab2と結合させた状態で長期に亘って保存をすると、磁気マーカーの構造が崩壊し、これに伴って該磁気マーカーに結合された二次抗体ab2までもが崩壊、すなわち抗原に捕捉されなくなってしまう。
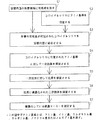
以下に本発明に係る検体用容器の処理方法の一例と、該処理方法によって得られる検体用容器の一次抗体の捕捉量(度合い)、すなわち標識化された二次抗体の捕捉量についての実験例を示す。なお、本発明に係る内面処理された検体用容器およびその処理方法は、この実験例に限定されるものではない。
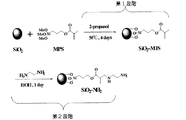
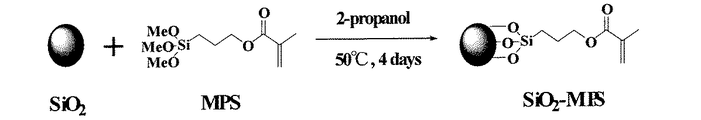
前処理工程S1:図1に示した形状のアクリル樹脂製の検体用容器を、メタノールで充分に脱脂した後、温度50℃、時間15分間の条件で1規定NaOH水溶液に浸漬し表面処理を行ない、その後にカルボキシル基を結合させた。このとき結合されたカルボキシル基を定量したところ、8〜12nmol/cm2(50〜70個/nm2)であった。なお測定方法は以下の通りである。
検体用容器をN,N'−ジシクロヘキシルカルボジイミド(DCC)の1%シクロヘキサン溶液中で2時間撹拌し、その後、P−ニトロフェノールを加えて8時間撹拌し、更に4%アンモニア水を加えて8時間撹拌した後、上澄み中の反応したP−ニトロフェノールの400nmにおける吸光度を測定する。なお測定値は、予め作成した検量線によって算出した。
Langmuir2000,16,9031−9034
検体用容器を0.1molのピクリン酸エタノール溶液に入れて測定すべきアミノ基を反応させ、超音波照射後、検体用容器を乾燥させてジイソプロピルエチルアミン(DIEA)の5%ターシャルブタノール液を加えて遠心分離を行ない、上澄み液の吸光度を測定する、所謂Gizin法によって定量した。
pH7.0のリン酸緩衝溶液5mlに対して、WSC10mgと磁気マーカー10mgとを加え、超音波照射後、アビジン15mggを添加し、氷冷下で1時間撹拌し、更に室温下で6時間撹拌し、その後リン酸緩衝溶液を使用した超音波洗浄・遠心洗浄を3回繰り返して磁気マーカーのカルボキシル基と、アビジンのアミノ基とを反応させた該磁気マーカーへのアビジンの固定化を行なった。なお遠心分離後の上澄み液中の未反応物質のUV測定により、磁気マーカーへのアビジンの固定化量を測定したところ、10mg/gであった。
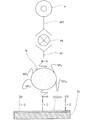
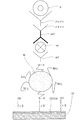
図12に示す如く、メタノール10mlに、マイクロモノマーとしてのポリビニルピロリドン(0.004〜0.04mg範囲内の一定量)にフェライト(Fe2O3)微粒子0.05gを加え、超音波照射し、更に攪拌ほ実施した後に遠心分離を行なうことによってポリビニルピロリドンを吸着したフェライト微粒子を作製し、次いでテトラヒドロフラン(THF)5mlに、N−アクロイル−L−グルタミン酸0.20g(フェライト微粒子に吸着したポリビニルピロリドンのビニル基量の100倍量)と、0〜100倍量の架橋剤トリ(アクロイルオキシ)アミン塩酸塩とを溶解させて準備溶液とし、これに粒子1g当たりに0.2gのポリビニルピロリドンを吸着したフェライト微粒子0.018gと、2,2'−アゾビス(イソブチロニトリル)(AIBN)0.01gとを加え、温度35℃、時間10時間の条件で攪拌し、更に遠心分離(5回繰り返し)を実施して磁気マーカーを得る。なおこの方法で得られたフェライト微粒子のポリマー量は、架橋剤の増加に伴って増大し、最大値はフェライト微粒子1g当たり947mgであった。また磁気マーカーの粒径は、29〜30nmであることが分散溶液の動的光散乱法から測定された。粒子間凝集は起こっておらず、水溶液中で4週間以上分散状態の保持が確認された。更に磁気マーカーの表面に結合したカルボキシル基は、最大97μmol/gであった。
本発明に係る内面処理(実験1における[0035]、[0037]および[0038])を実施した検体用容器(実施例1)と、全く何の処理も実施しない検体用容器(比較例1)とにおける一次抗体(抗原)の捕捉量(度合い)、すなわちアミノ基の付加量についての実験を行なった。なお実験方法については、免疫反応の簡便な評価法として用いられるサンドイッチELISA法を採用した。
実験2−1から得られる結果を下記の表1に記する。この表1に記載の結果から、本発明に係る内面処理を施した検体用容器は、なにも処理を施さない検体用容器と比較して平均で8倍程度の高い抗原捕捉量を発現することが確認された。
実験2−1で作製した検体用容器(実施例1)と、コロイダルシリカに対してアミノ基を付加させ、このコロイダルシリカを容器内面に結合させる代わりに、アミノ基を直接的に容器内面に結合させた検体用容器(比較例2)とにおける抗原の捕捉量(度合い)、すなわちアミノ基の付加量についての実験を行なった。
実験2−2から得られる結果を下記の表2に記する。この表2に記載の結果から、カルボキシル基の結合量が略同一であっても、コロイダルシリカを用いる場合(実施例1)と、そうでない場合(比較例2)との間では10倍以上の差がついていた。すなわちコロイダルシリカを用いる本発明に係る内面処理方法は、一次抗体を捕捉するためのアミノ基の結合方法として優れていることが確認された。
前述の実験2−1および実験2−2(実施例1、比較例1および比較例2)の結果を、一次抗体(抗原)の捕捉量(度合い)を指標とすると共に、比較例1を1に設定して比較すると、下記の表3のように纏めることができた。すなわち本発明の内面処理方法によって処理された検体用容器の検体の捕捉量、言い換えれば一次抗体の固相化量は、従来の検体捕捉に使用される各種処理方法に比較して大きく増大(比較例1に較べて約8倍、比較例2に較べて10〜15倍)していると確認された。これは検体量をこれまでの1/8程度しか含有しない被測定溶液についても、これまでと同様に測定し得ることを意味する。
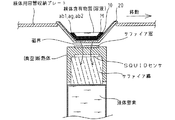
22 容器内面
ab1 一次抗体
ab2 二次抗体
ag 抗原
M 標識マーカー
Claims (18)
- 固相化された一次抗体(ab1)に抗原(ag)を捕捉させ、更に標識マーカー(M)によって標識化された二次抗体(ab2)を該抗原(ag)に捕捉させることで該抗原(ag)を定量化する各種免疫測定法に使用される検体用容器において、
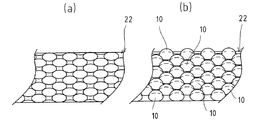
多数のアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基が付加されたコロイダルシリカ(10)が、容器内面(22)の所要領域を覆うように結合されており、
前記標識マーカー(M)によって標識化された二次抗体(ab2)は、一次抗体(ab1)および抗原(ag)を介して、前記コロイダルシリカ(10)のアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基だけに結合されるよう構成した
ことを特徴とする内面処理された検体用容器。 - 前記コロイダルシリカ(10)の粒径は、50〜500nmの範囲に設定される請求項1記載の内面処理された検体用容器。
- 前記コロイダルシリカ(10)の粒径の多分散度は、0.1以下に設定される請求項1または2記載の内面処理された検体用容器。
- 前記コロイダルシリカ(10)に付加され、前記一次抗体(ab1)と結合するアミノ基の量は、少なくとも5nmol/cm2以上とされる請求項1〜3の何れかに記載の内面処理された検体用容器。
- 前記アミノ基の付加は、エチレンジアミン等のジアミン類、ビス−2−アミノエチルエーテル等のエーテルジアミン類またはポリアリルアミンの如きポリアミン類から選択されたアミン化合物の使用によってなされる請求項1〜4の何れかに記載の内面処理された検体用容器。
- 前記容器内面(22)には、アミノ基を付加する前処理としてアルカリ加水分解により5〜15nmol/cm2のアミノ基の結合を許容する官能基が付与されている請求項1〜5の何れかに記載の内面処理された検体用容器。
- 前記アミノ基の結合を許容する官能基は、カルボキシル基である請求項6記載の内面処理された検体用容器。
- 前記コロイダルシリカ(10)に付加され、前記一次抗体(ab1)と結合するカルボキシル基の量は、少なくとも5nmol/cm2以上とされる請求項1〜3の何れかに記載の内面処理された検体用容器。
- 前記容器内面(22)には、カルボキシル基の付加する前処理としてアルカリ加水分解と、それに続くポリアリルアミンとの縮合反応とを実施することで5〜15nmol/cm2のカルボキシル基の結合を許容する官能基が付与されている請求項1〜3または8記載の内面処理された検体用容器。
- 前記カルボキシル基の結合を許容する官能基は、アミノ基である請求項9記載の内面処理された検体用容器。
- 固相化された一次抗体(ab1)に抗原(ag)を捕捉させ、更に標識マーカー(M)によって標識化された二次抗体(ab2)を該抗原(ag)に捕捉させることで該抗原(ag)を定量化する各種免疫測定法に使用される検体用容器の内面処理方法にあって、
検体用容器(20)の容器内面(22)に前処理を実施して所要の官能基を付与し、
別工程でアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基を付加した所要粒径のコロイダルシリカ(10)を、前記前処理で付与させた官能基に結合させて、前記容器内面(22)の所要領域を被覆させ、
前記標識マーカー(M)によって標識化された二次抗体(ab2)を、一次抗体(ab1)および抗原(ag)を介して、前記コロイダルシリカ(10)のアミノ基、イミノ基、カルボキシル基、カルボニル基、メタクリル基またはメルカプト基だけに結合させるようにした
ことを特徴とする検体用容器の内面処理方法。 - 前記コロイダルシリカ(10)として、その粒径が50〜500nmの範囲に設定されたものが使用される請求項11記載の検体用容器の内面処理方法。
- 前記コロイダルシリカ(10)として、その粒径の多分散度が0.1以下に設定されたものが使用される請求項11または12記載の検体用容器の内面処理方法。
- 前記コロイダルシリカ(10)は、所要の溶媒に分散させられた状態で容器内面(22)に供給される請求項11〜13の何れかに記載の検体用容器の内面処理方法。
- 前記前処理で付与される官能基として、カルボキシル基が使用される請求項11〜14の何れかに記載の検体用容器の内面処理方法。
- 前記前処理としてアルカリ加水分解が実施され、前記容器内面(22)に5〜15nmol/cm2のカルボキシル基を付与するようにした請求項13記載の検体用容器の内面処理方法。
- 前記前処理で付与される官能基として、アミノ基が使用される請求項11〜14の何れかに記載の検体用容器の内面処理方法。
- 前記前処理としてアルカリ加水分解と、それに続くポリアリルアミンとの縮合反応とが実施され、前記容器内面(22)に5〜15nmol/cm2のアミノ基を付与するようにした請求項17記載の検体用容器の内面処理方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004106929A JP2005291909A (ja) | 2004-03-31 | 2004-03-31 | 内面処理された検体用容器およびその処理方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004106929A JP2005291909A (ja) | 2004-03-31 | 2004-03-31 | 内面処理された検体用容器およびその処理方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005291909A true JP2005291909A (ja) | 2005-10-20 |
Family
ID=35324997
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004106929A Pending JP2005291909A (ja) | 2004-03-31 | 2004-03-31 | 内面処理された検体用容器およびその処理方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005291909A (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008190946A (ja) * | 2007-02-02 | 2008-08-21 | Kyushu Institute Of Technology | タンパク質吸着阻害剤を用いた免疫測定法と免疫測定用の基板及びキット |
| JP2011169886A (ja) * | 2010-01-21 | 2011-09-01 | Sysmex Corp | 試料調製装置 |
| JPWO2011158759A1 (ja) * | 2010-06-16 | 2013-08-19 | ウシオ電機株式会社 | 生産装置、生産方法、抗体チップ、プログラム及び記録媒体 |
-
2004
- 2004-03-31 JP JP2004106929A patent/JP2005291909A/ja active Pending
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008190946A (ja) * | 2007-02-02 | 2008-08-21 | Kyushu Institute Of Technology | タンパク質吸着阻害剤を用いた免疫測定法と免疫測定用の基板及びキット |
| JP2011169886A (ja) * | 2010-01-21 | 2011-09-01 | Sysmex Corp | 試料調製装置 |
| JPWO2011158759A1 (ja) * | 2010-06-16 | 2013-08-19 | ウシオ電機株式会社 | 生産装置、生産方法、抗体チップ、プログラム及び記録媒体 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA1336393C (en) | Test method and reagent kit therefor | |
| CN104316697A (zh) | 固定有抗原的免疫荧光载片的制备方法和由该方法制备的免疫荧光载片 | |
| JPS6315551B2 (ja) | ||
| AU648625B2 (en) | Test method and reagent kit therefor | |
| JP6118761B2 (ja) | 被検物質測定キット及び被検物質の測定方法 | |
| CN1258091C (zh) | 免疫测定 | |
| JP2015072249A (ja) | 被検物質の測定方法、被検物質測定キット及び被検物質測定試薬 | |
| JP2005291909A (ja) | 内面処理された検体用容器およびその処理方法 | |
| EP0682255A1 (en) | Immunoassays using a carbon sol label | |
| JP2010181155A (ja) | 物質固定基板の製造方法 | |
| CN114252613B (zh) | 一种用于检测HBsAg抗原蛋白的组合物及其使用方法 | |
| Guo et al. | Development of a low density colorimetric protein array for cardiac troponin I detection | |
| US20080248591A1 (en) | Gas bubble biosensor | |
| CN1114423A (zh) | 使用碳溶胶标记物的免疫测定法 | |
| JP2010164513A (ja) | 抗体固定基板、並びに該抗体固定基板の製造方法及び利用 | |
| CA2414704A1 (en) | Tertiary amine compounds for use in immunoassays | |
| JP2000304749A (ja) | 特異結合免疫分析容器 | |
| EP0525178B1 (en) | Elements and methods employing polymeric surface amplification agents | |
| CN102834713A (zh) | 感应化学品的方法 | |
| Hahn et al. | Current advances in antibody immobilization on different surfaces and beads | |
| JPH11174057A (ja) | 免疫測定用基材 | |
| HK1001235B (en) | Test method and reagent kit therefor | |
| HK1001235A (en) | Test method and reagent kit therefor | |
| HK1001234B (en) | Test method and reagent kit therefor | |
| HK1001234A (en) | Test method and reagent kit therefor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A625 | Written request for application examination (by other person) |
Free format text: JAPANESE INTERMEDIATE CODE: A625 Effective date: 20061221 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20080214 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20080305 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20080305 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20080214 |
|
| A977 | Report on retrieval |
Effective date: 20081009 Free format text: JAPANESE INTERMEDIATE CODE: A971007 |
|
| A131 | Notification of reasons for refusal |
Effective date: 20081021 Free format text: JAPANESE INTERMEDIATE CODE: A131 |
|
| A02 | Decision of refusal |
Effective date: 20090303 Free format text: JAPANESE INTERMEDIATE CODE: A02 |