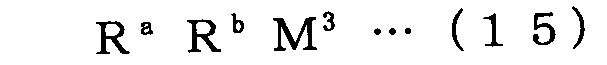JP2005200445A - Fuel oil composition - Google Patents
Fuel oil composition Download PDFInfo
- Publication number
- JP2005200445A JP2005200445A JP2004005113A JP2004005113A JP2005200445A JP 2005200445 A JP2005200445 A JP 2005200445A JP 2004005113 A JP2004005113 A JP 2004005113A JP 2004005113 A JP2004005113 A JP 2004005113A JP 2005200445 A JP2005200445 A JP 2005200445A
- Authority
- JP
- Japan
- Prior art keywords
- cyclopentadienyl
- group
- fuel oil
- hydrocarbon group
- olefin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 C*(*)(C1CCCC1)C1C2C(*)=C(*)C(*)=C(*)C2C2C(*)=*C(*)=C(*)C12 Chemical compound C*(*)(C1CCCC1)C1C2C(*)=C(*)C(*)=C(*)C2C2C(*)=*C(*)=C(*)C12 0.000 description 2
Abstract
Description
本発明は、燃料油組成物に関し、詳しくは、中留分燃料油と、特定のα−オレフィン(共)重合体からなる燃料油流動性改良剤を含む、低温流動性に優れた燃料油組成物に関するものである。 The present invention relates to a fuel oil composition, and more specifically, a fuel oil composition having excellent low-temperature fluidity, comprising a middle distillate fuel oil and a fuel oil fluidity improver comprising a specific α-olefin (co) polymer. It is about things.
軽油、重油などの中留分燃料油は低温下で使用または保存すると、油中に含まれるワックスの結晶が成長し、このようなワックスが成長した油を用いると、配管を閉塞したり、油全体の粘度が極端に上昇して流動性を失うという問題点があり、このような問題点を解消するためエチレン・α−オレフィン共重合体などの流動性向上剤を中留分燃料に添加することが知られている。 When middle distillate fuel oil such as light oil and heavy oil is used or stored at low temperature, wax crystals contained in the oil grow, and when such wax-grown oil is used, piping is blocked or oil There is a problem that the overall viscosity is extremely increased and the fluidity is lost. In order to solve such a problem, a fluidity improver such as ethylene / α-olefin copolymer is added to the middle distillate fuel. It is known.
また、低温濾過器目詰まり点(CFPP)を低下させるために1,2−結合が70%以上の水酸基末端ポリブタジエンまたはその水素添加物などを中留分燃料油に添加することも知られている。 It is also known to add a hydroxyl-terminated polybutadiene having 1,2-bonds of 70% or more or a hydrogenated product thereof to the middle distillate fuel oil in order to reduce the low temperature filter clogging point (CFPP). .
しかし、これらの添加剤を用いても、燃料油の低温流動性およびCFPPの改善は充分とは言えず、更なる改善が要望されている However, even if these additives are used, the low temperature fluidity and CFPP of the fuel oil cannot be improved sufficiently, and further improvements are desired.
本発明が解決しようとする課題は、低濃度の流動性改良剤の添加により低温濾過器目詰まり点(CFPP)および流動点を大幅に低減した燃料油組成物を提供することにある。 The problem to be solved by the present invention is to provide a fuel oil composition in which the low temperature filter clogging point (CFPP) and the pour point are greatly reduced by the addition of a low concentration flowability improver.
上記課題を解決すべく鋭意検討を行った結果、特定の炭素原子数のα−オレフィンを(共)重合することにより得られるα−オレフィン(共)重合物が燃料油の流動性改良剤として優れたCFPP降下能、流動点降下能を有していることを見出し、本発明を完成するに到った。 As a result of intensive studies to solve the above problems, an α-olefin (co) polymer obtained by (co) polymerizing an α-olefin having a specific number of carbon atoms is excellent as a fluidity improver for fuel oil. The present inventors have found that they have CFPP lowering ability and pour point lowering ability and have completed the present invention.
即ち、本発明は
(A)沸点が150℃〜400℃にある中留分燃料油と、
(B)メタロセン触媒を主触媒として重合された(i)(a)炭素原子数8〜20のα−オレフィンから選ばれる少なくとも1種類の単量体から導かれる構成単位を20〜100モル%の範囲で含有し、(b)エチレンから導かれる構成単位を0〜80モル%の範囲の量で含有し、
(ii)135℃でデカリン中で測定した極限粘度[η]が0.1〜1.0dl/gの範囲にあることを特徴とするα−オレフィン(共)重合体からなる燃料油流動性改良剤と
を含むことを特徴とする燃料油組成物である。
That is, the present invention provides (A) a middle distillate fuel oil having a boiling point of 150 ° C to 400 ° C,
(B) 20-100 mol% of structural units derived from at least one monomer selected from (i) (a) an α-olefin having 8-20 carbon atoms, polymerized using a metallocene catalyst as the main catalyst (B) containing structural units derived from ethylene in an amount ranging from 0 to 80 mol%,
(Ii) Fuel oil fluidity improvement comprising an α-olefin (co) polymer, wherein the intrinsic viscosity [η] measured in decalin at 135 ° C. is in the range of 0.1 to 1.0 dl / g. It is a fuel oil composition characterized by including an agent.
本発明の燃料油組成物は、ワックスの結晶成長や粘度上昇がなく、低温濾過器目詰まり点および流動点が低く、さらに低温流動性に優れている。 The fuel oil composition of the present invention does not have wax crystal growth or viscosity increase, has a low temperature filter clogging point and a pour point, and is excellent in low temperature fluidity.
以下、本発明について詳細に説明する。 Hereinafter, the present invention will be described in detail.
本発明で用いられる中留分燃料油は、沸点が150℃〜400℃にあり、その典型的な
ものは軽油、A重油などであり、90%留出温度と初留点との差が110℃以上、例えば200℃以下、好ましくは115℃〜190℃であって、低温濾過器目詰まり点が−10℃〜+10℃の範囲にあるものが特に好ましい。
The middle distillate fuel oil used in the present invention has a boiling point of 150 ° C. to 400 ° C., and typical ones thereof are light oil, A heavy oil, etc. It is particularly preferable that the temperature is not less than 200 ° C., for example, 200 ° C. or less, preferably 115 ° C. to 190 ° C., and the clogging point of the low temperature filter is in the range of −10 ° C. to + 10 ° C.
これらの中留分燃料油は1種または2種以上の混合物であってもよい。 These middle distillate fuel oils may be one or a mixture of two or more.
本発明において用いられる(B)α−オレフィン(共)重合体を構成する(a)炭素原子数8〜20のα−オレフィンとしては、1−オクテン、1−ノネン、1−デセン、1−ウンデセン、1−ドデセン、1−トリセン、1−トリデセン、1−テトラデセン、1−ペンタデセン、1−ヘキサデセン、1−ヘプタデセン、1−オクタデセン、1−ノナデセン、1−エイコセンの直鎖状α―オレフィンや8-メチルー1−ノネン、7-メチル−1−デセン、6−メチル−1−ウンデセン、6,8−ジメチル−1−デセンなどの分岐を有するα―オレフィンを挙げることができるが、好ましくは炭素原子数10〜20の直鎖状α―オレフィンである。 The (a) α-olefin having 8 to 20 carbon atoms constituting the (B) α-olefin (co) polymer used in the present invention includes 1-octene, 1-nonene, 1-decene, 1-undecene. 1-dodecene, 1-tricene, 1-tridecene, 1-tetradecene, 1-pentadecene, 1-hexadecene, 1-heptadecene, 1-octadecene, 1-nonadecene, 1-eicosene linear α-olefin and 8- Examples include α-olefins having a branch such as methyl-1-nonene, 7-methyl-1-decene, 6-methyl-1-undecene, and 6,8-dimethyl-1-decene. 10 to 20 linear α-olefins.
本発明で用いられる(B)α−オレフィン(共)重合体は、少なくとも1種以上の上記(a)炭素原子数8〜20のα−オレフィンからなる単量体の単独重合体または、(b)エチレンとの共重合体である。更に、必要に応じて炭素原子数3〜6のα−オレフィンを共重合成分として含有させることもできる。この様な炭素原子数3〜6のα−オレフィンとしてはプロピレン,1−ブテン、1−ペンテン、1−ヘキセンなどの直鎖状α−オレフィンや4−メチル−1−ペンテンなどの分岐を有するα−オレフィンを挙げることができる。これらのα−オレフィンは単独でまたは2種以上組合わせて用いることができる。 The (B) α-olefin (co) polymer used in the present invention is a homopolymer of a monomer comprising at least one or more of the above (a) α-olefin having 8 to 20 carbon atoms, or (b ) Copolymer with ethylene. Furthermore, a C3-C6 alpha olefin can also be included as a copolymerization component as needed. Examples of the α-olefin having 3 to 6 carbon atoms include linear α-olefins such as propylene, 1-butene, 1-pentene, and 1-hexene, and branched α-olefins such as 4-methyl-1-pentene. Mention may be made of olefins. These α-olefins can be used alone or in combination of two or more.
本発明で用いられる(B)α−オレフィン(共)重合体を構成する(a)炭素原子数8〜20のα−オレフィンから導かれる構成単位の含有率は20〜100モル%の範囲であり、好ましくは30〜100モル%、更に好ましくは50〜100モル%である。 The content of the structural unit derived from (a) the α-olefin having 8 to 20 carbon atoms constituting the (B) α-olefin (co) polymer used in the present invention is in the range of 20 to 100 mol%. , Preferably 30 to 100 mol%, more preferably 50 to 100 mol%.
また、本発明で用いられる(B)α−オレフィン(共)重合体を構成する(b)エチレンから導かれる構成単位の含有率は0〜80モル%の範囲であり、好ましくは0〜70モル%、更に好ましくは0〜50モル%である。 The content of the structural unit derived from (b) ethylene constituting the (B) α-olefin (co) polymer used in the present invention is in the range of 0 to 80 mol%, preferably 0 to 70 mol. %, More preferably 0 to 50 mol%.
更に必要に応じて加えられる炭素原子数3〜6のα−オレフィンから導かれる構成単位の含有率は0〜30モル%の範囲であることが好ましい。 Furthermore, it is preferable that the content rate of the structural unit guide | induced from the C3-C6 alpha-olefin added as needed is the range of 0-30 mol%.
本発明で用いられる(B)α−オレフィン(共)重合体の135℃でのデカリン中で測定した極限粘度[η]は0.1〜1.0dl/gの範囲にあり、好ましくは0.15〜0.8dl/gの範囲にあり、更に好ましくは0.2〜0.5dl/gの範囲にある。 The intrinsic viscosity [η] measured in decalin at 135 ° C. of the (B) α-olefin (co) polymer used in the present invention is in the range of 0.1 to 1.0 dl / g, preferably 0.8. It exists in the range of 15-0.8 dl / g, More preferably, it exists in the range of 0.2-0.5 dl / g.
本発明で用いられる(B)α−オレフィン(共)重合体の数平均分子量(Mn)は5,000〜100,000の範囲であり、好ましくは7,000〜80,000、更に好ましくは10,000〜50,000の範囲である。 The number average molecular weight (Mn) of the (B) α-olefin (co) polymer used in the present invention is in the range of 5,000 to 100,000, preferably 7,000 to 80,000, more preferably 10 , 50,000 to 50,000.
数平均分子量は分子量既知の標準物質(単分散ポリスチレン)を用いて較正されたゲルパーミエイションクロマトグラフィー(GPC)によって測定することができる。 The number average molecular weight can be measured by gel permeation chromatography (GPC) calibrated using a standard substance (monodisperse polystyrene) having a known molecular weight.
また、本発明で用いられる(B)α−オレフィン(共)重合体のゲルパーミエーションクロマトグラフィーによって測定した分子量分布(Mw/Mn)は3以下であり、好ましくは2.8以下、更に好ましくは2以下である。 The molecular weight distribution (Mw / Mn) of the (B) α-olefin (co) polymer used in the present invention measured by gel permeation chromatography is 3 or less, preferably 2.8 or less, more preferably. 2 or less.
更に本発明のα−オレフィン(共)重合体はα−オレフィン連鎖部分が高い立体規則性
を有していることが好ましい。特に、(B)α−オレフィン(共)重合体を構成する(a)炭素原子数8〜20のα−オレフィンから導かれる構成単位の含有率が50〜100モル%である場合には、α−オレフィン連鎖部分がシンジオタクティック構造を有する。
Further, the α-olefin (co) polymer of the present invention preferably has a high stereoregularity in the α-olefin chain portion. In particular, when the content of the structural unit derived from the (a) α-olefin having 8 to 20 carbon atoms constituting the (B) α-olefin (co) polymer is 50 to 100 mol%, α The olefin chain moiety has a syndiotactic structure.
シンジオタクティック構造とは、側鎖の立体構造が規則的に制御されているもののうち、炭素−炭素結合から形成される主鎖に対して側鎖が交互に反対方向に位置する立体構造を有するものである。規則性の程度を表す指標としてはタクティシティーが用いられ、シンジオタクティック構造の程度を表す指標としてはシンジオタクティシティ−が用いられる。 The syndiotactic structure has a three-dimensional structure in which the side chains are alternately positioned in opposite directions with respect to the main chain formed from carbon-carbon bonds among the structures in which the three-dimensional structure of the side chains is regularly controlled. Is. Tacticity is used as an index representing the degree of regularity, and syndiotacticity is used as an index representing the degree of syndiotactic structure.
シンジオタクティシティーは13C−NMR(同位体炭素による核磁気共鳴法スペクトル)を用いて公知の文献[Macromolecules 24,2334(1991);Polymer,30,1350(1989)]等に記載の方法により求めることができる。 Syndiotacticity is determined by a method described in known literature [Macromolecules 24, 2334 (1991); Polymer, 30, 1350 (1989)] using 13 C-NMR (isotope carbon nuclear magnetic resonance spectrum). Can be sought.
13C−NMRにより定量されるタクティシティーは連続する複数個の構成単位の存在割合(すなわち、連続する構成単位の相対的立体配座関係の存在割合)、例えば2個の場合はダイアッド、3個の場合はトリアッドによって示すことができる。本発明におけるタクティシティーはトリアッドで50%以上のシンジオタクティシティーを有するものであり、好ましくは70%以上である。 The tacticity determined by 13 C-NMR is the abundance ratio of a plurality of consecutive constitutional units (ie, the abundance ratio of the relative conformation of consecutive constitutional units). Can be indicated by a triad. The tacticity in the present invention is a triad having a syndiotacticity of 50% or more, and preferably 70% or more.
ここで、トリアッド連鎖でみたシンジオタクティシティー(以下、トリアッドシンジオタクティシティー、rr分率とも称する)について説明する。 Here, syndiotacticity (hereinafter also referred to as triad syndiotacticity, rr fraction) as seen in the triad chain will be described.
このα−オレフィン(共)重合体のrr分率は、α−オレフィン(共)重合体の13C−NMRスペクトルおよび下記式(7)により、頭−尾結合したα−オレフィン単位3連鎖部の第2単位目の側鎖第一メチレン基(化学式(8)中の[C3])の強度(面積)比として求められる。 The rr fraction of the α-olefin (co) polymer is determined by the 13 C-NMR spectrum of the α-olefin (co) polymer and the following formula (7), and the α-olefin unit 3 chain portion bonded head-to-tail. It is calculated | required as intensity | strength (area) ratio of the side chain 1st methylene group ([C3] in Chemical formula (8)) of the 2nd unit.
rr分率(%)=PPP(rr)/{PPP(mm)+PPP(mr)+PPP(rr)} …(7)
(式中、PPP(mm)、PPP(mr)、PPP(rr)は、それぞれ13C-NMRスペクトルで観察される頭−尾結合したα−オレフィン単位3連鎖部の2単位目の側鎖第一メチレン基[C3]の面積である。)
rr fraction (%) = PPP (rr) / {PPP (mm) + PPP (mr) + PPP (rr)} (7)
(Wherein, PPP (mm), PPP (mr), and PPP (rr) represent the first side chain of the second unit of the 3-chain unit of α-olefin units bonded head-to-tail, respectively, as observed in the 13 C-NMR spectrum. This is the area of the methylene group [C3].)
(式中、R1、R2,R3=CnH2n+1、0≦n≦17であり、それぞれ同一であっても異なっていても良い) (Wherein R1, R2, R3 = C n H 2n + 1 , 0 ≦ n ≦ 17, which may be the same or different)
このようなPPP(mm)、PPP(mr)、PPP(rr)は、それぞれ下記構造の頭−尾結合したα−オレフィンの3単位連鎖を示す。 Such PPP (mm), PPP (mr), and PPP (rr) each represent a three-unit chain of α-olefin having a head-to-tail bond having the following structure.
(式中、R1、R2,R3=CnH2n+1、0≦n≦17であり、それぞれ同一であっても異なっていても良い) (Wherein R1, R2, R3 = C n H 2n + 1 , 0 ≦ n ≦ 17, which may be the same or different)
α−オレフィン(共)重合体の製造
上記のα−オレフィン(共)重合体の製造の際に使用されるメタロセン触媒としては、特開平2-41303号公報、特開平41305号公報、特開平2-274703号公報、特開平2-274704号公報、特開平3-179005号公報、公報、特開平3-179006号公報、特開平4-69394号公報、特開平5-17589号公報、特開平8−120127号公報、あるいはJ.A.Ewenらの文献「J.Am.Chem.Soc.,1988,110,6255-6256」に記載されているような触媒系を用いることができ、例えば、互いに非対称な配位子を有する架橋型遷移金属化合物と有機アルミニウム等の助触媒とからなる触媒系が挙げられる。
Production of α-olefin (co) polymer As the metallocene catalyst used in the production of the above α-olefin (co) polymer, JP-A-2-41303, JP-A-41305, JP-A-2 -274703, JP-A-2-274704, JP-A-3-179005, JP-A-3-179006, JP-A-4-69394, JP-A-5-17589, JP-A-8 Catalyst system as described in JP-A No. 1202015 or J. A. Ewen et al., “J. Am. Chem. Soc., 1988, 110, 6255-6256” can be used. Examples thereof include a catalyst system comprising a bridged transition metal compound having an asymmetric ligand and a promoter such as organoaluminum.
本発明におけるα−オレフィン(共)重合体を製造するメタロセン触媒成分としては遷移金属化合物が下記一般式(12)、(13)、(14)で表される第4族遷移金属化合物を例示することができる。
まず、一般式(12)で表される第4族遷移金属化合物について説明する。
Examples of the metallocene catalyst component for producing the α-olefin (co) polymer in the present invention include group 4 transition metal compounds represented by the following general formulas (12), (13), and (14) as transition metal compounds. be able to.
First, the Group 4 transition metal compound represented by the general formula (12) will be described.
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R9およびR10は、水素原子、炭化水素基およびケイ素含有炭化水素基から選ばれ、互いに同一でも異なっていてもよく、R1ないしR8およびR9ないしR10で示される基のうち隣接した基は互いに結合して環を形成してもよく、Yは炭素原子またはケイ素原子であり、nは2〜4の整数、Mは周期表第4族から選ばれた金属を示し、jは1〜4の整数であり、Qはハロゲン原子、炭化水素基、アニオン配位子および孤立電子対で配位可能な中性配位子から選ばれ、jが2以上のときはQは互いに同一でも異なっていてもよい。)
上記一般式(12)において、炭化水素基としては、好ましくは炭素数1〜20のアルキル基、炭素数7〜20のアリールアルキル基、炭素数6〜20のアリール基、または炭素数7〜20のアルキルアリール基であり、1つ以上の環構造を含んでいてもよい。
Wherein R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 and R 10 are selected from a hydrogen atom, a hydrocarbon group and a silicon-containing hydrocarbon group. May be the same or different from each other, and among the groups represented by R 1 to R 8 and R 9 to R 10 , adjacent groups may be bonded to each other to form a ring, and Y represents a carbon atom or a silicon atom N represents an integer of 2 to 4, M represents a metal selected from Group 4 of the periodic table, j represents an integer of 1 to 4, Q represents a halogen atom, a hydrocarbon group, an anionic ligand, and (Selected from neutral ligands that can be coordinated by a lone pair, and when j is 2 or more, Qs may be the same or different from each other.)
In the general formula (12), the hydrocarbon group is preferably an alkyl group having 1 to 20 carbon atoms, an arylalkyl group having 7 to 20 carbon atoms, an aryl group having 6 to 20 carbon atoms, or 7 to 20 carbon atoms. And may contain one or more ring structures.
炭素および水素のみから構成されるアルキル、アルケニル、アルキニル、アリール基以外に、これらの炭素に直結した水素原子の一部がハロゲン原子、酸素含有基、窒素含有基、隣接する任意の二つの水素原子が同時に置換されて脂環族あるいは芳香族環を形成しているものも含む。 In addition to alkyl, alkenyl, alkynyl, and aryl groups composed only of carbon and hydrogen, some of the hydrogen atoms directly connected to these carbon atoms are halogen atoms, oxygen-containing groups, nitrogen-containing groups, and any two adjacent hydrogen atoms. Are substituted at the same time to form an alicyclic or aromatic ring.
その具体例としては、メチル基、エチル基、n-プロピル基、アリル(allyl)基、n-ブチル基、n-ペンチル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基、n-ノニル基、n-デカニル基などの直鎖状炭化水素基;イソプロピル基、イソブチル基、s-ブチル基、t-ブチル基、t-アミル基、ネオペンチル基、3-メチルペンチル基、1,1-ジエチルプロピル基、1,1-ジメチルブチル基、1-メチル-1-プロピルブチル基、1,1-プロピルブチル基、1,1-ジメチル-2-メチルプロピル基、1-メチル-1-イソプロピル-2-メチルプロピル基、シクロプロピルメチル基などの分岐状炭化水素基;シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、ノルボルニル基、アダマンチル基などの環状飽和炭化水素基;フェニル基、ナフチル基、ビフェニル基、フェナントリル基、アントラセニル基などの環状不飽和炭化水素基;ベンジル基、クミル基などのアリール基の置換した飽和炭化水素基、メトキシ基、エトキシ基、フェノキシ基などの酸素原子含有炭化水素基、N-メチルアミノ基、N,N-ジメチルアミノ基、N-フェニルアミノ基などの窒素原子含有炭化水素基、トリフルオロメチル基、トリブロモメチル基、ペンタフルオロエチル基、ペンタフルオロフェニル基などのハロゲン原子含有炭化水素基を挙げることができる。 Specific examples thereof include methyl group, ethyl group, n-propyl group, allyl group, n-butyl group, n-pentyl group, n-hexyl group, n-heptyl group, n-octyl group, n- Linear hydrocarbon groups such as nonyl and n-decanyl; isopropyl, isobutyl, s-butyl, t-butyl, t-amyl, neopentyl, 3-methylpentyl, 1,1- Diethylpropyl group, 1,1-dimethylbutyl group, 1-methyl-1-propylbutyl group, 1,1-propylbutyl group, 1,1-dimethyl-2-methylpropyl group, 1-methyl-1-isopropyl- Branched hydrocarbon groups such as 2-methylpropyl group and cyclopropylmethyl group; cyclic saturated hydrocarbons such as cyclopropyl group, cyclobutyl group, cyclopentyl group, cyclohexyl group, cycloheptyl group, cyclooctyl group, norbornyl group and adamantyl group Group: phenyl group, naphth Cyclic unsaturated hydrocarbon groups such as benzene, biphenyl, phenanthryl, and anthracenyl groups; saturated hydrocarbon groups substituted with aryl groups such as benzyl and cumyl, oxygen atoms such as methoxy, ethoxy, and phenoxy Hydrocarbon groups, N-methylamino groups, N, N-dimethylamino groups, nitrogen-containing hydrocarbon groups such as N-phenylamino groups, trifluoromethyl groups, tribromomethyl groups, pentafluoroethyl groups, pentafluorophenyl And a halogen atom-containing hydrocarbon group such as a group.
上記一般式(12)において、ケイ素含有炭化水素基としては、好ましくはケイ素数1〜4、炭素数3〜20のアルキルまたはアリールシリル基であり、例えば、シクロペンタジエニル基、インデニル基、フルオレニル基の環炭素がケイ素原子と直接共有結合している基のことを示し、その具体例としては、トリメチルシリル、tert-ブチルジメチルシリル、トリフェニルシリル等が挙げられる。 In the general formula (12), the silicon-containing hydrocarbon group is preferably an alkyl or arylsilyl group having 1 to 4 silicon atoms and 3 to 20 carbon atoms, such as a cyclopentadienyl group, an indenyl group, or a fluorenyl group. This indicates a group in which the ring carbon of the group is directly covalently bonded to the silicon atom, and specific examples thereof include trimethylsilyl, tert-butyldimethylsilyl, triphenylsilyl and the like.
本発明において、上記一般式(12)のR1からR10は水素、炭化水素基、ケイ素含有炭化水素基から選ばれ、それぞれ同一でも異なっていてもよい。好ましい炭化水素基、ケイ素含有炭化水素基の具体例としては、上記と同様のものを挙げることができる。 In the present invention, R 1 to R 10 in the general formula (12) are selected from hydrogen, a hydrocarbon group, and a silicon-containing hydrocarbon group, and may be the same or different. Specific examples of preferred hydrocarbon groups and silicon-containing hydrocarbon groups include the same as those described above.
上記一般式(12)のシクロペンタジエニル環上のR1からR8までの隣接した置換基は、互いに結合して環を形成してもよい。 The adjacent substituents from R 1 to R 8 on the cyclopentadienyl ring of the general formula (12) may be bonded to each other to form a ring.
一般式(12)のMは、周期律表第4族元素、すなわちジルコニウム、チタンまたはハフニウムであり、好ましくはジルコニウムである。 M in the general formula (12) is a group 4 element of the periodic table, that is, zirconium, titanium or hafnium, preferably zirconium.
Yは第14族原子であり、好ましくは炭素原子または珪素原子である。nは2〜4の整数であり、好ましくは2または3、特に好ましくは2である。 Y is a Group 14 atom, preferably a carbon atom or a silicon atom. n is an integer of 2 to 4, preferably 2 or 3, particularly preferably 2.
Qはハロゲン、炭化水素基、炭素数が10以下の中性、共役または非共役ジエン、アニオン配位子および孤立電子対で配位可能な中性配位子からなる群から同一または異なる組み合わせで選ばれる。Qが炭化水素基であるとき、より好ましくは炭素数が1〜10の炭化水素基である。 Q is the same or different combination from the group consisting of halogen, hydrocarbon group, neutral having 10 or less carbon atoms, conjugated or non-conjugated diene, anionic ligand and neutral ligand capable of coordinating with a lone electron pair. To be elected. When Q is a hydrocarbon group, it is more preferably a hydrocarbon group having 1 to 10 carbon atoms.
ハロゲンの具体例としては、フッ素、塩素、臭素、ヨウ素であり、炭化水素基の具体例としては、メチル、エチル、n-プロピル、イソプロピル、2-メチルプロピル、1,1-ジメチルプロピル、2,2-ジメチルプロピル、1,1-ジエチルプロピル、1-エチル-1-メチルプロピル、1,1,2,2-テトラメチルプロピル、sec-ブチル、tert-ブチル、1,1-ジメチルブチル、1,1,3-トリメチルブチル、ネオペンチル、シクロヘキシルメチル、シクロヘキシル、1-メチル-1-シクロヘキシル等が挙げられる。炭素数が10以下の中性、共役または非共役ジエンの具体例としては、s-シス-またはs-トランス-η4-1,3-ブタジエン、s-シス-またはs-トランス-η4-1,4-ジフェニル-1,3-ブタジエン、s-シス-またはs-トランス-η4-3-メチル-1,3-ペンタジエン、s-シス-またはs-トランス-η4-1,4-ジベンジル-1,3-ブタジエン、s-シス-またはs-トランス-η4-2,4-ヘキサジエン、s-シス-またはs-トランス-η4-1,3-ペンタジエン、s-シス-またはs-トランス-η4-1,4-ジトリル-1,3-ブタジエン、s-シス-またはs-トランス-η4-1,4-ビス(トリメチルシリル)-1,3-ブタジエン等が挙げられる。アニオン配位子の具体例としては、メトキシ、tert-ブトキシ、フェノキシ等のアルコキシ基、アセテート、ベンゾエート等のカルボキシレート基、メシレート、トシレート等のスルホネート基等が挙げられる。孤立電子対で配位可能な中性配位子の具体例としては、トリメチルホスフィン、トリエチルホスフィン、トリフェニルホスフィン、ジフェニルメチルホスフィンなどの有機リン化合物、またはテトラヒドロフラン、ジエチルエーテル、ジオキサン、1、2−ジメトキシエタン等のエーテル類が挙げられる。jが2以上の整数である場合は、複数のQは同一でも異なっていてもよい。 Specific examples of the halogen are fluorine, chlorine, bromine and iodine, and specific examples of the hydrocarbon group are methyl, ethyl, n-propyl, isopropyl, 2-methylpropyl, 1,1-dimethylpropyl, 2, 2-dimethylpropyl, 1,1-diethylpropyl, 1-ethyl-1-methylpropyl, 1,1,2,2-tetramethylpropyl, sec-butyl, tert-butyl, 1,1-dimethylbutyl, 1, Examples include 1,3-trimethylbutyl, neopentyl, cyclohexylmethyl, cyclohexyl, 1-methyl-1-cyclohexyl and the like. Neutral having 10 or less carbon atoms, and specific examples of the conjugated or non-conjugated dienes, s- cis - or s- trans eta 4-1,3-butadiene, s- cis - or s- trans eta 4 - 1,4-diphenyl-1,3-butadiene, s-cis- or s-trans-η 4 -3-methyl-1,3-pentadiene, s-cis- or s-trans-η 4 -1,4- Dibenzyl-1,3-butadiene, s-cis- or s-trans-η 4 -2,4-hexadiene, s-cis- or s-trans-η 4 -1,3-pentadiene, s-cis- or s -Trans-η 4 -1,4-ditolyl-1,3-butadiene, s-cis- or s-trans-η 4 -1,4-bis (trimethylsilyl) -1,3-butadiene and the like. Specific examples of the anionic ligand include alkoxy groups such as methoxy, tert-butoxy and phenoxy, carboxylate groups such as acetate and benzoate, and sulfonate groups such as mesylate and tosylate. Specific examples of the neutral ligand that can coordinate with a lone electron pair include organic phosphorus compounds such as trimethylphosphine, triethylphosphine, triphenylphosphine, and diphenylmethylphosphine, or tetrahydrofuran, diethyl ether, dioxane, 1,2- And ethers such as dimethoxyethane. When j is an integer greater than or equal to 2, several Q may be the same or different.
式(12)において、Yは2〜4の複数個存在するが、複数のYは相互に同一であっても異なっていてもよい。Yに結合する複数のR9及び複数のR10は、それぞれ相互に同一であっても異なっていてもよい。例えば同一のYに結合する複数のR9が相互に異なっていてもよいし、異なるYに結合する複数のR9が相互に同一であってもよい。また、R9もしくはR10同士が環を形成していてもよい。 In Formula (12), there are a plurality of Ys of 2 to 4, but the Ys may be the same or different from each other. The plurality of R 9 and the plurality of R 10 bonded to Y may be the same as or different from each other. For example, a plurality of R 9 bonded to the same Y may be different from each other, or a plurality of R 9 bonded to different Y may be the same. R 9 or R 10 may form a ring.
以下に、上記一般式(12)で表される第4族遷移金属化合物の具体例を示すが、特にこれによって本発明の範囲が限定されるものではない。
エチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、エチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、エチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリ
ド、エチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、プロピレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、プロピレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、プロピレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、プロピレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、テトラメチルエチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、テトラメチルエチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、テトラメチルエチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、テトラメチルエチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、テトラメチルジシリレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、テトラメチルジシリレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、テトラメチルジシリレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、テトラメチルジシリレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ジメチルエチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジメチルエチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジメチルエチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジメチルエチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、エチレン(シクロペンタジエニル)(フルオレニル)ハフニウムジクロリド、エチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ハフニウムジクロリド、エチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ハフニウムジクロリド、エチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ハフニウムジクロリド、プロピレン(シクロペンタジエニル)(フルオレニル)ハフニウムジクロリド、プロピレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ハフニウムジクロリド、プロピレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ハフニウムジクロリド、プロピレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ハフニウムジクロリド、エチレン(シクロペンタジエニル)(フルオレニル)チタニウムジクロリド、エチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)チタニウムジクロリド、エチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)チタニウムジクロリド、エチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)チタニウムジクロリド、プロピレン(シクロペンタジエニル)(フルオレニル)チタニウムジクロリド、プロピレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)チタニウムジクロリド、プロピレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)チタニウムジクロリド、プロピレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)チタニウムジクロリド、エチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジメチル、エチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジメチル、エチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジメチル、エチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジメチル、プロピレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジメチル、プロピレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジメチル、プロピレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジメチル、プロピレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジメチル、エチレン(シクロペンタジエニル)(フルオレニル)ハフニウムジメチル、エチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ハフニウムジメチル、エチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ハフニウムジメチル、エチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ハフニウムジメチル、プロピ
レン(シクロペンタジエニル)(フルオレニル)ハフニウムジメチル、プロピレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ハフニウムジメチル、プロピレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ハフニウムジメチル、プロピレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ハフニウムジメチル等を例示することができる。
次に、一般式(13)、(14)で表される第4族遷移金属化合物について説明する。
Specific examples of the Group 4 transition metal compound represented by the general formula (12) are shown below, but the scope of the present invention is not particularly limited by this.
Ethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, ethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, ethylene (cyclopentadienyl) (3,6-ditert -Butyl fluorenyl) zirconium dichloride, ethylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, propylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, propylene (cyclopentadienyl) ( 2,7-ditert-butylfluorenyl) zirconium dichloride, propylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, propylene (cyclopentadienyl) (octamethyloctahydro Dibenzofluorenyl) zirconium dichlor Tetramethylethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, tetramethylethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, tetramethylethylene (cyclopentadienyl) ) (3,6-ditert-butylfluorenyl) zirconium dichloride, tetramethylethylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, tetramethyldisylylene (cyclopentadienyl) ( Fluorenyl) zirconium dichloride, tetramethyldisilene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, tetramethyldisilene (cyclopentadienyl) (3,6-ditert-butyl Fluorenyl) zirconium dichloride, tetra Methyldisilene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, dimethylethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, dimethylethylene (cyclopentadienyl) (2,7-di tert-butylfluorenyl) zirconium dichloride, dimethylethylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, dimethylethylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorene) Nyl) zirconium dichloride, ethylene (cyclopentadienyl) (fluorenyl) hafnium dichloride, ethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, ethylene (cyclopentadienyl) (3 , 6-Ditert-butyl Oleenyl) hafnium dichloride, ethylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) hafnium dichloride, propylene (cyclopentadienyl) (fluorenyl) hafnium dichloride, propylene (cyclopentadienyl) (2,7- Di-tert-butylfluorenyl) hafnium dichloride, propylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) hafnium dichloride, propylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) ) Hafnium dichloride, ethylene (cyclopentadienyl) (fluorenyl) titanium dichloride, ethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) titanium dichloride, ethylene (cyclopentadienyl) (3, 6-ditert-butylfluorenyl) Titanium dichloride, ethylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) titanium dichloride, propylene (cyclopentadienyl) (fluorenyl) titanium dichloride, propylene (cyclopentadienyl) (2,7-di tert-butylfluorenyl) titanium dichloride, propylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) titanium dichloride, propylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) Titanium dichloride, ethylene (cyclopentadienyl) (fluorenyl) zirconium dimethyl, ethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dimethyl, ethylene (cyclopentadienyl) (3,6 -Di-tert-butylfluorenyl) zirconium Dimethyl, ethylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dimethyl, propylene (cyclopentadienyl) (fluorenyl) zirconium dimethyl, propylene (cyclopentadienyl) (2,7-ditert- Butylfluorenyl) zirconium dimethyl, propylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dimethyl, propylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dimethyl , Ethylene (cyclopentadienyl) (fluorenyl) hafnium dimethyl, ethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dimethyl, ethylene (cyclopentadienyl) (3,6-di tert-butylfluorenyl) hafnium dimethyl, ethyl (Cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) hafnium dimethyl, propylene (cyclopentadienyl) (fluorenyl) hafnium dimethyl, propylene (cyclopentadienyl) (2,7-ditert-butylfluorene Nyl) hafnium dimethyl, propylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) hafnium dimethyl, propylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) hafnium dimethyl, etc. can do.
Next, the Group 4 transition metal compound represented by the general formulas (13) and (14) will be described.
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R11およびR12は、水素原子、炭化水素基およびケイ素含有炭化水素基から選ばれ、互いに同一でも異なっていてもよく、R1ないしR8で示される基のうち隣接した基は互いに結合して環を形成してもよく、一般式(13)の場合はR1およびR8から選ばれる基とR11またはR12が互いに結合して環を形成してもよく、Aは不飽和結合および/または芳香族環を含んでいてもよい炭素原子数2〜20の2価の炭化水素基を示し、AはYと共に形成する環を含めて2つ以上の環構造を含んでいてもよく、Yは炭素原子またはケイ素原子であり、Mは周期表第4族から選ばれた金属を示し、jは1〜4の整数であり、Qはハロゲン原子、炭化水素基、アニオン配位子および孤立電子対で配位可能な中性配位子から選ばれ、jが2以上のときはQは互いに同一でも異なっていてもよい。)。 Wherein R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 11 and R 12 are selected from a hydrogen atom, a hydrocarbon group and a silicon-containing hydrocarbon group. May be the same or different from each other, and adjacent groups among the groups represented by R 1 to R 8 may be bonded to each other to form a ring. In the case of the general formula (13), R 1 and R 8 R 11 or R 12 may be bonded to each other to form a ring, and A is a divalent divalent having 2 to 20 carbon atoms and may contain an unsaturated bond and / or an aromatic ring. Represents a hydrocarbon group, A may include two or more ring structures including a ring formed with Y, Y is a carbon atom or a silicon atom, and M is selected from Group 4 of the periodic table. Represents a metal, j is an integer of 1 to 4, Q is a halogen atom, a hydrocarbon group, an anionic ligand, and a lone electron In it is selected from coordinating neutral ligands capable, when j is 2 or more Q may be the same or different.).
上記一般式(13)、(14)において、炭化水素基としては、好ましくは炭素数1〜20のアルキル基、炭素数7〜20のアリールアルキル基、炭素数6〜20のアリール基、または炭素数7〜20のアルキルアリール基であり、1つ以上の環構造を含んでいてもよい。 In the general formulas (13) and (14), the hydrocarbon group is preferably an alkyl group having 1 to 20 carbon atoms, an arylalkyl group having 7 to 20 carbon atoms, an aryl group having 6 to 20 carbon atoms, or carbon. These are alkylaryl groups of several 7 to 20, and may contain one or more ring structures.
炭素および水素のみから構成されるアルキル、アルケニル、アルキニル、アリール基以外に、これらの炭素に直結した水素原子の一部がハロゲン原子、酸素含有基、窒素含有基、隣接する任意の二つの水素原子が同時に置換されて脂環族あるいは芳香族環を形成しているものも含む。 In addition to alkyl, alkenyl, alkynyl, and aryl groups composed only of carbon and hydrogen, some of the hydrogen atoms directly connected to these carbon atoms are halogen atoms, oxygen-containing groups, nitrogen-containing groups, and any two adjacent hydrogen atoms. Are substituted at the same time to form an alicyclic or aromatic ring.
その具体例としては、メチル基、エチル基、n-プロピル基、アリル(allyl)基、n-ブチル基、n-ペンチル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基、n-ノニル基、n-デカニル基などの直鎖状炭化水素基;イソプロピル基、イソブチル基、s-ブチル基、t-ブチル基、t-アミル基、ネオペンチル基、3-メチルペンチル基、1,1-ジエチルプロピル基、1,1-ジメチルブチル基、1-メチル-1-プロピルブチル基、1,1-プロピルブチル基、1,1-ジメチル-2-メチルプロピル基、1-メチル-1-イソプロピル-2-メチルプロピル基、シクロプロピルメチル基などの分岐状炭化水素基;シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、ノルボルニル基、アダマンチル基などの環状飽和炭化水素基;フェニル基、ナフチル基、ビフェニル基、フェナントリル基、アントラセニル基などの環状不飽和炭化水素基;ベンジル基、クミル基などのアリール基の置換した飽和炭化水素基、メトキシ基、エトキシ基、フェノキシ基などの酸素原子含有炭化水素基、N-メチルアミノ基、N,N-ジメチルアミノ基、N-フェニルアミノ基などの窒素原子含有炭化水素基、トリフルオロメチル基、トリブロモメチル基、ペンタフルオロエチル基、ペンタフルオロフェニル基などのハロゲン原子含有炭化水素基を挙げることができる。 Specific examples thereof include methyl group, ethyl group, n-propyl group, allyl group, n-butyl group, n-pentyl group, n-hexyl group, n-heptyl group, n-octyl group, n- Linear hydrocarbon groups such as nonyl and n-decanyl; isopropyl, isobutyl, s-butyl, t-butyl, t-amyl, neopentyl, 3-methylpentyl, 1,1- Diethylpropyl group, 1,1-dimethylbutyl group, 1-methyl-1-propylbutyl group, 1,1-propylbutyl group, 1,1-dimethyl-2-methylpropyl group, 1-methyl-1-isopropyl- Branched hydrocarbon groups such as 2-methylpropyl group and cyclopropylmethyl group; cyclic saturated hydrocarbons such as cyclopropyl group, cyclobutyl group, cyclopentyl group, cyclohexyl group, cycloheptyl group, cyclooctyl group, norbornyl group and adamantyl group Group: phenyl group, naphth Cyclic unsaturated hydrocarbon groups such as benzene, biphenyl, phenanthryl, and anthracenyl groups; saturated hydrocarbon groups substituted with aryl groups such as benzyl and cumyl, oxygen atoms such as methoxy, ethoxy, and phenoxy Hydrocarbon groups, N-methylamino groups, N, N-dimethylamino groups, nitrogen-containing hydrocarbon groups such as N-phenylamino groups, trifluoromethyl groups, tribromomethyl groups, pentafluoroethyl groups, pentafluorophenyl And a halogen atom-containing hydrocarbon group such as a group.
上記一般式(13)、(14)において、ケイ素含有炭化水素基としては、好ましくはケイ素数1〜4、炭素数3〜20のアルキルまたはアリールシリル基であり、例えば、シクロペンタジエニル基、インデニル基、フルオレニル基の環炭素がケイ素原子と直接共有結合している基のことを示し、その具体例としては、トリメチルシリル、tert-ブチルジメチルシリル、トリフェニルシリル等が挙げられる。 In the general formulas (13) and (14), the silicon-containing hydrocarbon group is preferably an alkyl or arylsilyl group having 1 to 4 silicon atoms and 3 to 20 carbon atoms, such as a cyclopentadienyl group, Indenyl group and fluorenyl group represent a group in which the ring carbon is directly covalently bonded to a silicon atom, and specific examples thereof include trimethylsilyl, tert-butyldimethylsilyl, triphenylsilyl and the like.
本発明において、上記一般式(13)、(14)のR1からR10は水素、炭化水素基、ケイ素含有炭化水素基から選ばれ、それぞれ同一でも異なっていてもよい。好ましい炭化水素基、ケイ素含有炭化水素基の具体例としては、上記と同様のものを挙げることができる。 In the present invention, R 1 to R 10 in the general formulas (13) and (14) are selected from hydrogen, a hydrocarbon group, and a silicon-containing hydrocarbon group, and may be the same or different. Specific examples of preferred hydrocarbon groups and silicon-containing hydrocarbon groups include the same as those described above.
上記一般式(13)、(14)のシクロペンタジエニル環上のR1からR8までの隣接した置換基は、互いに結合して環を形成してもよい。 The adjacent substituents from R 1 to R 8 on the cyclopentadienyl ring of the general formulas (13) and (14) may be bonded to each other to form a ring.
上記一般式(13)、(14)のMは、周期律表第4族元素、すなわちジルコニウム、チタンまたはハフニウムであり、好ましくはジルコニウムである。 M in the general formulas (13) and (14) is a group 4 element of the periodic table, that is, zirconium, titanium, or hafnium, preferably zirconium.
Yは第14族原子であり、好ましくは炭素原子または珪素原子である。 Qはハロゲン、炭化水素基、炭素数が10以下の中性、共役または非共役ジエン、アニオン配位子および孤立電子対で配位可能な中性配位子からなる群から同一または異なる組み合わせで選ばれる。Qが炭化水素基であるとき、より好ましくは炭素数が1〜10の炭化水素基である。 Y is a Group 14 atom, preferably a carbon atom or a silicon atom. Q is the same or different combination from the group consisting of halogen, hydrocarbon group, neutral having 10 or less carbon atoms, conjugated or non-conjugated diene, anionic ligand and neutral ligand capable of coordinating with a lone electron pair. To be elected. When Q is a hydrocarbon group, it is more preferably a hydrocarbon group having 1 to 10 carbon atoms.
ハロゲンの具体例としては、フッ素、塩素、臭素、ヨウ素であり、炭化水素基の具体例としては、メチル、エチル、n-プロピル、イソプロピル、2-メチルプロピル、1,1-ジメチルプロピル、2,2-ジメチルプロピル、1,1-ジエチルプロピル、1-エチル-1-メチルプロピル、1,1,2,2-テトラメチルプロピル、sec-ブチル、tert-ブチル、1,1-ジメチルブチル、1,1,3-トリメチルブチル、ネオペンチル、シクロヘキシルメチル、シクロヘキシル、1-メ
チル-1-シクロヘキシル等が挙げられる。炭素数が10以下の中性、共役または非共役ジエンの具体例としては、s-シス-またはs-トランス-η4-1,3-ブタジエン、s-シス-またはs-トランス-η4-1,4-ジフェニル-1,3-ブタジエン、s-シス-またはs-トランス-η4-3-メチル-1,3-ペンタジエン、s-シス-またはs-トランス-η4-1,4-ジベンジル-1,3-ブタジエン、s-シス-またはs-トランス-η4-2,4-ヘキサジエン、s-シス-またはs-トランス-η4-1,3-ペンタジエン、s-シス-またはs-トランス-η4-1,4-ジトリル-1,3-ブタジエン、s-シス-またはs-トランス-η4-1,4-ビス(トリメチルシリル)-1,3-ブタジエン等が挙げられる。アニオン配位子の具体例としては、メトキシ、tert-ブトキシ、フェノキシ等のアルコキシ基、アセテート、ベンゾエート等のカルボキシレート基、メシレート、トシレート等のスルホネート基等が挙げられる。孤立電子対で配位可能な中性配位子の具体例としては、トリメチルホスフィン、トリエチルホスフィン、トリフェニルホスフィン、ジフェニルメチルホスフィンなどの有機リン化合物、またはテトラヒドロフラン、ジエチルエーテル、ジオキサン、1、2−ジメトキシエタン等のエーテル類が挙げられる。jが2以上の整数である場合は、複数のQは同一でも異なっていてもよい。
Specific examples of the halogen are fluorine, chlorine, bromine and iodine, and specific examples of the hydrocarbon group are methyl, ethyl, n-propyl, isopropyl, 2-methylpropyl, 1,1-dimethylpropyl, 2, 2-dimethylpropyl, 1,1-diethylpropyl, 1-ethyl-1-methylpropyl, 1,1,2,2-tetramethylpropyl, sec-butyl, tert-butyl, 1,1-dimethylbutyl, 1, Examples include 1,3-trimethylbutyl, neopentyl, cyclohexylmethyl, cyclohexyl, 1-methyl-1-cyclohexyl and the like. Neutral having 10 or less carbon atoms, and specific examples of the conjugated or non-conjugated dienes, s- cis - or s- trans eta 4-1,3-butadiene, s- cis - or s- trans eta 4 - 1,4-diphenyl-1,3-butadiene, s-cis- or s-trans-η 4 -3-methyl-1,3-pentadiene, s-cis- or s-trans-η 4 -1,4- Dibenzyl-1,3-butadiene, s-cis- or s-trans-η 4 -2,4-hexadiene, s-cis- or s-trans-η 4 -1,3-pentadiene, s-cis- or s -Trans-η 4 -1,4-ditolyl-1,3-butadiene, s-cis- or s-trans-η 4 -1,4-bis (trimethylsilyl) -1,3-butadiene and the like. Specific examples of the anionic ligand include alkoxy groups such as methoxy, tert-butoxy and phenoxy, carboxylate groups such as acetate and benzoate, and sulfonate groups such as mesylate and tosylate. Specific examples of the neutral ligand that can coordinate with a lone electron pair include organic phosphorus compounds such as trimethylphosphine, triethylphosphine, triphenylphosphine, and diphenylmethylphosphine, or tetrahydrofuran, diethyl ether, dioxane, 1,2- And ethers such as dimethoxyethane. When j is an integer greater than or equal to 2, several Q may be the same or different.
R11、R12は炭化水素基およびケイ素含有基から選ばれ、それぞれ同一でも異なっていてもよい。炭化水素基およびケイ素含有基としては前記と同一の基を挙げることができる。 R 11 and R 12 are selected from a hydrocarbon group and a silicon-containing group, and may be the same or different. Examples of the hydrocarbon group and the silicon-containing group include the same groups as described above.
R11およびR12が互いに結合して環を形成してもよい。
また、R11およびR12がフェニル基等のアリール基、またはアルキルアリール基である場合は、R1からR8が同時に水素ではないことが好ましい。具体的には、R2、R3、R4、R5、R6、R7の任意の二つ以上の置換基が水素ではないか、R2からR7の隣り合う基が互いに結合して環を形成していることが好ましい。
R 11 and R 12 may be bonded to each other to form a ring.
When R 11 and R 12 are an aryl group such as a phenyl group or an alkylaryl group, it is preferable that R 1 to R 8 are not simultaneously hydrogen. Specifically, any two or more substituents of R 2 , R 3 , R 4 , R 5 , R 6 , and R 7 are not hydrogen or adjacent groups of R 2 to R 7 are bonded to each other. To form a ring.
以下に、上記一般式(13)、(14)で表される第4族遷移金属化合物の具体例を示すが、特にこれによって本発明の範囲が限定されるものではない。 Specific examples of the Group 4 transition metal compounds represented by the above general formulas (13) and (14) are shown below, but the scope of the present invention is not particularly limited thereby.
シクロペンチリデン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、シクロペンチリデン(シクロペンタジエニル)(フルオレニル)ハフニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(フルオレニル) ハフニウムジクロリド、シクロペンチリデン(シクロペンタジエニル)(フルオレニル)チタニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(フルオレニル) チタニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(p- tert-ブチルフェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(p-n-ブチルフェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(m-トリル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、 (p-トリル)(フェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(p-イソプロピルフェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジメチル、(p-tert-ブチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、(p-n-エチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、(4-ビフェニル)(フェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジ(4-ビフェニル)メチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、ジメチルシリレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリドジフェニルシリレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリド、シクロペンチリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、シクロペンチリデン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(3,6−ジtert−ブチルフルオレニル)ジルコニウムジクロリド、シクロペンチリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)ハフニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) ハフニウムジクロリド、シクロペンチリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル)チタニウムジクロリド、シクロヘキシリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、アダマンチリデン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、モノフェニルモノメチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、ジメチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、ジフェニルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、ジ(p−トリル)メチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、ジエチルメチレン(シクロペンタジエニル)(2,7−ジtert−ブチルフルオレニル) チタニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-n-ブチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-n-ブチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、ジ(p-n-ブチルフェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(m-トリル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(m-トリル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、ジ(m-トリル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、 (p-トリル)(フェニル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ジ(p-イソプロピルフェニル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジメチル、(p-トリル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-イソプロピルフェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジメチル、(p-トリル)(フェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-イソプロピルフェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-tert-ブチルフェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(p-トリル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジメチル、(p-tert-ブチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、(p-tert-ブチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、(p-tert-ブチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、(p-n-エチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、(p-n-エチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、(p-n-エチルフェニル)(フェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、(4-ビフェニル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、(4-ビフェニル)(フェニル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、(4-ビフェニル)(フェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(4-ビフェニル)メチレン(シクロペンタジエニル)(2,7-ジtert-ブチルフルオレニル)ジルコニウムジクロリド、ジ(4-ビフェニル)メチレン(シクロペンタジエニル)(2,7-ジメチルフルオレニル)ジルコニウムジクロリド、ジ(4-ビフェニル)メチレン(シクロペンタジエニル)(3,6-ジtert-ブチルフルオレニル)ジルコニウムジクロ
リド、ビス(3,4-ジメチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ビス(3,4-ジメチルフェニル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ビス(3,5-ジメチルフェニル)メチレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ビス(3,5-ジメチルフェニル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ビス(4-シクロヘキシルフェニル)メチレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ビス(4-シクロヘキシルフェニル)メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ビス{3-(トリフルオロメチル)フェニル}メチレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ビス{3-(トリフルオロメチル)フェニル}メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ビス{3,5-ビス(トリフルオロメチル)フェニル}メチレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ビス{3,5-ビス(トリフルオロメチル)フェニル}メチレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ジメチルシリレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ジフェニルシリレン(シクロペンタジエニル)(2,7-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ジメチルシリレン(シクロペンタジエニル)(3,6-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ジフェニルシリレン(シクロペンタジエニル)(3,6-ジ-tert-ブチルフルオレニル)ジルコニウムジクロリド、ジメチルシリレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド、ジフェニルシリレン(シクロペンタジエニル)(オクタメチルオクタヒドロジベンゾフルオレニル)ジルコニウムジクロリド等を例示することができる。
Cyclopentylidene (cyclopentadienyl) (fluorenyl) zirconium dichloride, cyclohexylidene (cyclopentadienyl) (fluorenyl) zirconium dichloride, adamantylidene (cyclopentadienyl) (fluorenyl) zirconium dichloride, monophenyl monomethylmethylene ( Cyclopentadienyl) (fluorenyl) zirconium dichloride, dimethylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, diphenylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadi) (Enyl) (fluorenyl) zirconium dichloride, diethylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, cyclopentylidene (cyclopentadienyl) (phenyl) Olenyl) hafnium dichloride, cyclohexylidene (cyclopentadienyl) (fluorenyl) hafnium dichloride, adamantylidene (cyclopentadienyl) (fluorenyl) hafnium dichloride, monophenylmonomethylmethylene (cyclopentadienyl) (fluorenyl) hafnium dichloride Dimethylmethylene (cyclopentadienyl) (fluorenyl) hafnium dichloride, diphenylmethylene (cyclopentadienyl) (fluorenyl) hafnium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (fluorenyl) hafnium dichloride, diethylmethylene (Cyclopentadienyl) (fluorenyl) hafnium dichloride, cyclopentylidene (cyclopentadienyl) (fluorenyl) titanium dichloride, cyclohexylidene Lopentadienyl) (fluorenyl) titanium dichloride, adamantylidene (cyclopentadienyl) (fluorenyl) titanium dichloride, monophenylmonomethylmethylene (cyclopentadienyl) (fluorenyl) titanium dichloride, dimethylmethylene (cyclopentadienyl) (fluorenyl) Titanium dichloride, diphenylmethylene (cyclopentadienyl) (fluorenyl) titanium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (fluorenyl) titanium dichloride, diethylmethylene (cyclopentadienyl) (fluorenyl) titanium dichloride, Di (p-tolyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, di (p-tert-butylphenyl) methylene (cyclopentadienyl) (fluorenyl) di Conium dichloride, di (p-n-butylphenyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, di (m-tolyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, (p-tolyl) (Phenyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, di (p-isopropylphenyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, di (p-tert-butylphenyl) methylene (cyclopentadiene) (Enyl) (fluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dimethyl, (p-tert-butylphenyl) (phenyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride , (Pn-ethylphenyl) (phenyl) methylene (Si Lopentadienyl) (fluorenyl) zirconium dichloride, (4-biphenyl) (phenyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, di (4-biphenyl) methylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, dimethylsilylene (Cyclopentadienyl) (fluorenyl) zirconium dichloride diphenylsilylene (cyclopentadienyl) (fluorenyl) zirconium dichloride, cyclopentylidene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, Cyclohexylidene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, adamantylidene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, Monopheny Monomethylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, dimethylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, diphenylmethylene (Cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride Diethylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, cyclopentylidene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, Cyclohexylidene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, adamantyl Den (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, monophenylmonomethylmethylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, dimethyl Methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, diphenylmethylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (p -Tolyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, diethylmethylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, Cyclopentylidene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, cyclohexylide (Cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, adamantylidene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, monophenylmonomethyl Methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, dimethylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, diphenylmethylene ( Cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, Diethylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) hafnium dichloride, cyclopentylidene (cyclopent Tadienyl) (2,7-ditert-butylfluorenyl) titanium dichloride, cyclohexylidene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) titanium dichloride, adamantylidene (cyclopentadiene) Enyl) (2,7-ditert-butylfluorenyl) titanium dichloride, monophenylmonomethylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) titanium dichloride, dimethylmethylene (cyclopentadiyl) Enyl) (2,7-ditert-butylfluorenyl) titanium dichloride, diphenylmethylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) titanium dichloride, di (p-tolyl) methylene ( Cyclopentadienyl) (2,7-ditert-butylfluorenyl) titanium dichloride, diethylmethylene (cyclopentadienyl) (2, 7-ditert-butylfluorenyl) titanium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (p-tolyl) methylene ( Cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (p -tert-butylphenyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (p-tert-butylphenyl) methylene (cyclopentadienyl) (2,7- Dimethylfluorenyl) zirconium dichloride, di (p-tert-butylphenyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (p-n-butylphenyl) Tylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (p-n-butylphenyl) methylene (cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium Dichloride, di (p-n-butylphenyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (m-tolyl) methylene (cyclopentadienyl) (2, 7-ditert-butylfluorenyl) zirconium dichloride, di (m-tolyl) methylene (cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium dichloride, di (m-tolyl) methylene (cyclopentadi) Enyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium di Chloride, (p-tolyl) (phenyl) methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, di (p-isopropylphenyl) methylene (cyclopentadienyl) (octamethyloctahydrodibenzo Fluorenyl) zirconium dichloride, di (p-tert-butylphenyl) methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) ( Octamethyloctahydrodibenzofluorenyl) zirconium dimethyl, (p-tolyl) (phenyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (p-isopropylphenyl) Methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconi Um dichloride, di (p-tert-butylphenyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (2 , 7-Ditert-butylfluorenyl) zirconium dimethyl, (p-tolyl) (phenyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (p-isopropyl) Phenyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, di (p-tert-butylphenyl) methylene (cyclopentadienyl) (3,6-ditert-butyl Fluorenyl) zirconium dichloride, di (p-tolyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dimethyl, (p-tert-butylphenyl) (phenyl) methylene (cyclo Pentadienyl) (2,7- tert-butylfluorenyl) zirconium dichloride, (p-tert-butylphenyl) (phenyl) methylene (cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium dichloride, (p-tert-butylphenyl) ( Phenyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, (pn-ethylphenyl) (phenyl) methylene (cyclopentadienyl) (2,7-ditert-butyl Fluorenyl) zirconium dichloride, (pn-ethylphenyl) (phenyl) methylene (cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium dichloride, (pn-ethylphenyl) (phenyl) methylene (cyclopentadiene) Enyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, (4-biphenyl) (phenyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zyl Conium dichloride, (4-biphenyl) (phenyl) methylene (cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium dichloride, (4-biphenyl) (phenyl) methylene (cyclopentadienyl) (3, 6-ditert-butylfluorenyl) zirconium dichloride, di (4-biphenyl) methylene (cyclopentadienyl) (2,7-ditert-butylfluorenyl) zirconium dichloride, di (4-biphenyl) methylene ( Cyclopentadienyl) (2,7-dimethylfluorenyl) zirconium dichloride, di (4-biphenyl) methylene (cyclopentadienyl) (3,6-ditert-butylfluorenyl) zirconium dichloride, bis (3 , 4-Dimethylphenyl) methylene (cyclopentadienyl) (2,7-di-tert-butylfluorenyl) zirconium dichloride, bis (3,4-dimethylphenyl) methylene (cyclopentadiene) ) (Octamethyloctahydrodibenzofluorenyl) zirconium dichloride, bis (3,5-dimethylphenyl) methylene (cyclopentadienyl) (2,7-di-tert-butylfluorenyl) zirconium dichloride, bis ( 3,5-dimethylphenyl) methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, bis (4-cyclohexylphenyl) methylene (cyclopentadienyl) (2,7-di-tert- Butylfluorenyl) zirconium dichloride, bis (4-cyclohexylphenyl) methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, bis {3- (trifluoromethyl) phenyl} methylene (cyclopenta Dienyl) (2,7-di-tert-butylfluorenyl) zirconium dichloride, bis {3- (trif Oromethyl) phenyl} methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, bis {3,5-bis (trifluoromethyl) phenyl} methylene (cyclopentadienyl) (2,7- Di-tert-butylfluorenyl) zirconium dichloride, bis {3,5-bis (trifluoromethyl) phenyl} methylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, dimethylsilylene Pentadienyl) (2,7-di-tert-butylfluorenyl) zirconium dichloride, diphenylsilylene (cyclopentadienyl) (2,7-di-tert-butylfluorenyl) zirconium dichloride, dimethylsilylene Pentadienyl) (3,6-di-tert-butylfluorenyl) zirconium dichloride, diphenylsilylene ( Cyclopentadienyl) (3,6-di-tert-butylfluorenyl) zirconium dichloride, dimethylsilylene (cyclopentadienyl) (octamethyloctahydrodibenzofluorenyl) zirconium dichloride, diphenylsilylene (cyclopentadienyl) ) (Octamethyloctahydrodibenzofluorenyl) zirconium dichloride and the like.
また、助触媒成分としては以下の[1]〜[4]のうちから選ばれる少なくとも1種の化合物を用いることができる。 In addition, as the promoter component, at least one compound selected from the following [1] to [4] can be used.
[1]有機金属化合物
本発明のα−オレフィン(共)重合体を製造するために用いられる有機金属化合物として、具体的には下記のような有機金属化合物が用いられる。
[1] Organometallic compound As the organometallic compound used for producing the α-olefin (co) polymer of the present invention, the following organometallic compounds are specifically used.
(式中、Ra およびRb は、互いに同一でも異なっていてもよく、炭素原子数が1〜15、好ましくは1〜4の炭化水素基を示し、M3はMg、ZnまたはCdである。)で表される周期律表第2族または第12族金属のジアルキル化合物。 (In the formula, R a and R b may be the same or different from each other, and each represents a hydrocarbon group having 1 to 15 carbon atoms, preferably 1 to 4 carbon atoms, and M 3 is Mg, Zn or Cd. A dialkyl compound of a Group 2 or Group 12 metal represented by the following periodic table.
[2]有機アルミニウム化合物
オレフィン重合用触媒を形成する[2]有機アルミニウム化合物としては、例えば下記一般式(16)で表される有機アルミニウム化合物、下記一般式(17)で表されるI族金属とアルミニウムとの錯アルキル化物などを挙げることができる。
[2] Organoaluminum compound Forming the catalyst for olefin polymerization [2] As the organoaluminum compound, for example, an organoaluminum compound represented by the following general formula (16), a group I metal represented by the following general formula (17) And a complex alkylated product of aluminum and aluminum.
(式中、Ra およびRb は、互いに同一でも異なっていてもよく、炭素原子数が1〜15、好ましくは1〜4の炭化水素基を示し、Xはハロゲン原子を示し、mは0<m≦3、nは0≦n<3、pは0≦p<3、qは0≦q<3の数であり、かつm+n+p+q=3である。)で表される有機アルミニウム化合物。このような化合物の具体例として、トリメチルアルミニウム、トリエチルアルミニウム、トリイソブチルアルミニウム、ジイソブチルアルミニウムハイドライドを例示することができる。 (In the formula, R a and R b may be the same or different from each other, each represents a hydrocarbon group having 1 to 15 carbon atoms, preferably 1 to 4 carbon atoms, X represents a halogen atom, and m represents 0. <M ≦ 3, n is 0 ≦ n <3, p is a number of 0 ≦ p <3, q is a number of 0 ≦ q <3, and m + n + p + q = 3). Specific examples of such compounds include trimethylaluminum, triethylaluminum, triisobutylaluminum, and diisobutylaluminum hydride.
(式中、M2 はLi、NaまたはKを示し、Ra は炭素原子数が1〜15、好ましくは1〜4の炭化水素基を示す。)で表される周期律表第1族金属とアルミニウムとの錯アルキル化物。このような化合物としては、LiAl(C2H5)4、LiAl(C7H15)4 などを例示することができる。 (Wherein M 2 represents Li, Na or K, and R a represents a hydrocarbon group having 1 to 15 carbon atoms, preferably 1 to 4 carbon atoms). Alkylate complex of aluminum and aluminum. Examples of such compounds include LiAl (C 2 H 5 ) 4 and LiAl (C 7 H 15 ) 4 .
[3]有機アルミニウムオキシ化合物
本発明で用いられる[3] 有機アルミニウムオキシ化合物は、従来公知のアルミノキサンであってもよく、また特開平2−78687号公報に例示されているようなベンゼン不溶性の有機アルミニウムオキシ化合物であってもよい。
[3] Organoaluminum oxy compound [3] The organoaluminum oxy compound used in the present invention may be a conventionally known aluminoxane, or a benzene-insoluble organic compound as exemplified in JP-A-2-78687. An aluminum oxy compound may be used.
なお該アルミノキサンは、少量の有機金属成分を含有してもよい。また回収された上記のアルミノキサンの溶液から溶媒または未反応有機アルミニウム化合物を蒸留して除去した後、溶媒に再溶解またはアルミノキサンの貧溶媒に懸濁させてもよい。 The aluminoxane may contain a small amount of an organometallic component. Further, after removing the solvent or the unreacted organoaluminum compound from the recovered aluminoxane solution by distillation, it may be redissolved in a solvent or suspended in a poor aluminoxane solvent.
アルミノキサンを調製する際に用いられる有機アルミニウム化合物として具体的には、トリアルキルアルミニウム、トリシクロアルキルアルミニウムが好ましく、トリメチルアルミニウムが特に好ましい。 Specifically, as the organoaluminum compound used in preparing the aluminoxane, trialkylaluminum and tricycloalkylaluminum are preferable, and trimethylaluminum is particularly preferable.
上記のような有機アルミニウム化合物は、1種単独でまたは2種以上組み合せて用いられる。 The above organoaluminum compounds are used singly or in combination of two or more.
[4]遷移金属化合物と反応してイオン対を形成する化合物
遷移金属化合物と反応してイオン対を形成する化合物[4] (以下、「イオン化イオン性化合物」という。)としては、特開平1−501950号公報、特開平1−502036号公報、特開平3−179005号公報、特開平3−179006号公報、特開平3−207703号公報、特開平3−207704号公報、USP−5321106号公報などに記載されたルイス酸、イオン性化合物、ボラン化合物およびカルボラン化合物などを挙げることができる。
[4] Compound that forms an ion pair by reacting with a transition metal compound [4] (hereinafter referred to as “ionized ionic compound”) that forms an ion pair by reacting with a transition metal compound No. 501950, JP-A-1-502036, JP-A-3-179005, JP-A-3-179006, JP-A-3-207703, JP-A-3-207704, USP-5321106. And Lewis acids, ionic compounds, borane compounds and carborane compounds described in the above.
このようなイオン化イオン性化合物[4]は、1種単独でまたは2種以上組み合せて用いられる。 Such ionized ionic compounds [4] are used singly or in combination of two or more.
成分[1]は、成分[1]と、触媒として用いられる遷移金属化合物中の全遷移金属原子(M)とのモル比〔[1]/M〕が通常0.01〜5000、好ましくは0.05〜2000となるような量で用いられる。成分[2]は、成分[2]と、触媒として用いられる遷移金属化合物中の全遷移金属原子(M)とのモル比〔[2]/M〕が通常100〜25000、好ましくは500〜10000となるような量で用いられる。成分[3]は、成分[3]中のアルミニウム原子と、触媒として用いられる遷移金属化合物中の全遷移金属(M)とのモル比〔[3]/M〕が、通常10〜5000、好ましくは20〜2000となるような量で用いられる。成分[4]は、成分[4]と、触媒として用いられる遷移金属化合物中の遷移金属原子(M)とのモル比〔[4]/M〕が、通常1〜50、好ましくは1〜20となるような量で用いられる。 Component [1] has a molar ratio [[1] / M] of component [1] to all transition metal atoms (M) in the transition metal compound used as a catalyst of usually 0.01 to 5000, preferably 0. It is used in such an amount that it becomes 0.05 to 2000. Component [2] has a molar ratio [[2] / M] of component [2] to all transition metal atoms (M) in the transition metal compound used as a catalyst of usually 100 to 25000, preferably 500 to 10,000. Is used in such an amount that Component [3] has a molar ratio [[3] / M] of the aluminum atoms in component [3] and the total transition metals (M) in the transition metal compound used as a catalyst, usually 10 to 5000, preferably Is used in such an amount as to be 20-2000. Component [4] has a molar ratio [[4] / M] of component [4] and the transition metal atom (M) in the transition metal compound used as a catalyst, usually 1 to 50, preferably 1 to 20 Is used in such an amount that
本発明で用いられるα−オレフィン(共)重合体の製造方法としては、例えば上述したような触媒の存在下に、(a)炭素原子数8〜20のα−オレフィンおよび(b)エチレン、更に必要に応じて炭素原子数3〜6のα−オレフィンを通常液相で共重合させる。この際、重合溶媒として一般にヘキサン、トルエンの如き炭化水素溶媒が用いられるが、α−オレフィンを溶媒として用いてもよい。 Examples of the method for producing an α-olefin (co) polymer used in the present invention include (a) an α-olefin having 8 to 20 carbon atoms and (b) ethylene in the presence of the catalyst as described above. If necessary, an α-olefin having 3 to 6 carbon atoms is usually copolymerized in a liquid phase. At this time, a hydrocarbon solvent such as hexane or toluene is generally used as a polymerization solvent, but an α-olefin may be used as a solvent.
重合反応は、バッチ法あるいは連続法いずれの方法で行ってもよく、通常温度は−20℃〜+150℃、好ましくは0〜120℃、更に好ましくは0〜100℃であり、圧力が0を超えて7.8MPa(80kgf/cm2、ゲージ圧)以下、好ましくは0を越えて4.9MPa(50kgf/cm2、ゲージ圧)以下の条件下に行われる。 The polymerization reaction may be carried out by either a batch method or a continuous method, and the normal temperature is −20 ° C. to + 150 ° C., preferably 0 to 120 ° C., more preferably 0 to 100 ° C., and the pressure exceeds 0. And 7.8 MPa (80 kgf / cm 2 , gauge pressure) or less, preferably more than 0 and 4.9 MPa (50 kgf / cm 2 , gauge pressure) or less.
重合に際して、(a)炭素原子数8〜20のα−オレフィン、(b)エチレンおよび必要に応じて導入される炭素原子数3〜6のα−オレフィンは、特定組成のα−オレフィン(共)重合体が得られるような量割合で重合系内に供給される。また、重合の際には、水素などの分子量調節剤を添加することもできる。 In the polymerization, (a) an α-olefin having 8 to 20 carbon atoms, (b) ethylene and an α-olefin having 3 to 6 carbon atoms introduced as needed are α-olefins (co) having a specific composition. It is fed into the polymerization system in such an amount ratio that a polymer is obtained. In the polymerization, a molecular weight regulator such as hydrogen can be added.
本発明において流動性改良剤として用いられる(B)α−オレフィン(共)重合体は、50ppm〜5,000ppm、好ましくは100ppm〜2,000ppmの量で燃料油組成物に含まれる。 The (B) α-olefin (co) polymer used as a fluidity improver in the present invention is contained in the fuel oil composition in an amount of 50 ppm to 5,000 ppm, preferably 100 ppm to 2,000 ppm.
[実施例]
以下、実施例に基づいて本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。
[Example]
EXAMPLES Hereinafter, although this invention is demonstrated further more concretely based on an Example, this invention is not limited to these.
平均分子量・分子量分布
数平均分子量(Mn)および分子量分布(Mw/Mn)は、島津製作所製のGPC(クロマトパックC−R4A)を用い以下のようにして測定した。分離カラムとして、TSK
G6000H XL、G4000H XL、G3000H XL、G2000H XLを用い、カラム温度を40℃とし、移動相にはテトラヒドロフラン(和光純薬)を用い、展開速度を0.8ml/分とし、試料濃度を0.2重量%とし、試料注入量を200マイクロリットルとし、検出器として示差屈折計を用いた。標準ポリスチレンとしては、東ソー社製のものを用いた。
Average molecular weight / number distribution of molecular weight Average molecular weight (Mn) and molecular weight distribution (Mw / Mn) were measured as follows using GPC (Chromatopack C-R4A) manufactured by Shimadzu Corporation. TSK as a separation column
G6000H XL, G4000H XL, G3000H XL, G2000H XL are used, the column temperature is 40 ° C., the mobile phase is tetrahydrofuran (Wako Pure Chemical Industries), the development rate is 0.8 ml / min, and the sample concentration is 0.2. The amount of sample injection was 200 microliters, and a differential refractometer was used as a detector. As the standard polystyrene, those manufactured by Tosoh Corporation were used.
燃料油組成物の性能評価
市販の2号軽油(硫黄含量:0.1重量%)に、下記実施例の重合体を100ppm又は1,000ppmの割合で添加し、これらの燃料油組成物について低温濾過器目詰まり点(CFPP)および流動点を評価した。
低温濾過器目詰まり点はJIS K 2288に記載の方法に従って測定し、流動点はJIS K 2269に記載の方法に従って測定した。
Performance Evaluation of Fuel Oil Compositions Polymers of the following examples were added to commercially available No. 2 diesel oil (sulfur content: 0.1% by weight) at a ratio of 100 ppm or 1,000 ppm, and these fuel oil compositions were low in temperature. Filter clogging point (CFPP) and pour point were evaluated.
The clogging point of the low temperature filter was measured according to the method described in JIS K 2288, and the pour point was measured according to the method described in JIS K 2269.
内容量1000mlのガラス製オートクレーブに温度計、気体吹き込み管、ガラス製攪拌羽根を備え、充分に窒素置換した。その後、n-デカン450mlと1−デセン50mlを装入し、窒素を50リットル/時間で流通させながら温度を130℃にした。一方、充分に窒素置換した内容量30mlの枝付きフラスコにマグネチックスターラーチップを入れ、これに遷移金属化合物としてジフェニルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリドのトルエン溶液0.002mmol、およびメチルアルミノキサンのトルエン溶液(Al=1.53M)2mmolを加え、30分間攪拌した。ガラス製オートクレーブ中の窒素を止め、次にエチレンを20リットル/時間と水素を30リットル/時間の量で流通させてから、次いで上記溶液を加え、重合を開始した。重合中はエチレンを20リットル/時間と水素を30リットル/時間の量で連続的に供給し、常圧下、130℃で20分間重合を行った後、少量のイソプロパノールを添加し重合を停止した。これを、1Nの塩酸300ml中にポリマー溶液を加え、攪拌した。この溶液を分液ロートに移し、有機層を分取した後、有機層を水洗し、175℃、減圧下(1mmHg)で溶媒と未反応の1−デセンを留去した。得られた透明の液状ポリマーは46.52gであり、重合活性は69.8kg−polymer/mmol−Zr・hrであった。ポリマー分析の結果、エチレン含量は73モル%、[η]=0.46dl/gであり、Mw=101,910、Mn=65,330、Mw/Mn=1.56であった。 A glass autoclave with an internal volume of 1000 ml was equipped with a thermometer, a gas blowing tube, and a glass stirring blade, and sufficiently substituted with nitrogen. Thereafter, 450 ml of n-decane and 50 ml of 1-decene were charged, and the temperature was adjusted to 130 ° C. while nitrogen was circulated at 50 liters / hour. On the other hand, a magnetic stirrer chip was placed in a 30 ml branch flask with a sufficient internal volume substituted with nitrogen, and 0.002 mmol of a toluene solution of diphenylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride as a transition metal compound, and methyl 2 mmol of aluminoxane in toluene (Al = 1.53M) was added and stirred for 30 minutes. The nitrogen in the glass autoclave was stopped, then ethylene was passed in an amount of 20 liter / hour and hydrogen in an amount of 30 liter / hour, and then the above solution was added to initiate the polymerization. During the polymerization, ethylene was continuously supplied at a rate of 20 liters / hour and hydrogen at a rate of 30 liters / hour, and polymerization was carried out at 130 ° C. for 20 minutes under normal pressure, and then a small amount of isopropanol was added to terminate the polymerization. The polymer solution was added to 300 ml of 1N hydrochloric acid and stirred. This solution was transferred to a separatory funnel, and the organic layer was separated. The organic layer was washed with water, and the solvent and unreacted 1-decene were distilled off at 175 ° C. under reduced pressure (1 mmHg). The obtained transparent liquid polymer was 46.52 g, and the polymerization activity was 69.8 kg-polymer / mmol-Zr · hr. As a result of polymer analysis, the ethylene content was 73 mol%, [η] = 0.46 dl / g, Mw = 101,910, Mn = 65,330, and Mw / Mn = 1.56.
得られたポリマーを用いた燃料油組成物の性能評価結果を表1に示した。 The performance evaluation results of the fuel oil composition using the obtained polymer are shown in Table 1.
内容量1000mlのガラス製オートクレーブに温度計、気体吹き込み管、ガラス製攪拌羽根を備え、充分に窒素置換した。その後、n-デカン250mlと1−デセン250mlを装入し、窒素を50リットル/時間で流通させながら温度を110℃にした。一方、充分に窒素置換した内容量30mlの枝付きフラスコにマグネチックスターラーチップを入れ、これに遷移金属化合物としてジフェニルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリドのトルエン溶液0.002mmol、およびメチルアルミノキサンのトルエン溶液(Al=1.53M)2mmolを加え、30分間攪拌した。ガラス製オートクレーブ中の窒素を止め、次にエチレンを5リットル/時間と水素を40リットル/時間の量で流通させてから、次いで上記溶液を加え、重合を開始した。重合中はエチレンを5リットル/時間と水素を40リットル/時間の量で連続的に供給し、常圧下、110℃で20分間重合を行った後、少量のイソプロパノールを添加し重合を停止した。これを、1Nの塩酸300ml中にポリマー溶液を加え、攪拌した。この溶液を分液ロートに移し、有機層を分取した後、有機層を水洗し、175℃、減圧下(1mmHg)で溶媒と未反応の1−デセンを留去した。得られた透明の液状ポリマーは34.73gであり、重合活性は52.10kg−polymer/mmol−Zr・hrであった。ポリマー分析の結果、エチレン含量は15モル%、[η]=0.18dl/gであり、Mw=31,890、Mn=19,130、Mw/Mn=1.67であった。また、ポリマーのトリアッド連鎖でみたシンジオタクティシティーは65%であった。 A glass autoclave with an internal volume of 1000 ml was equipped with a thermometer, a gas blowing tube, and a glass stirring blade, and sufficiently substituted with nitrogen. Thereafter, 250 ml of n-decane and 250 ml of 1-decene were charged, and the temperature was set to 110 ° C. while nitrogen was circulated at 50 liters / hour. On the other hand, a magnetic stirrer chip was placed in a 30 ml branch flask with a sufficient internal volume substituted with nitrogen, and 0.002 mmol of a toluene solution of diphenylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride as a transition metal compound, and methyl 2 mmol of aluminoxane in toluene (Al = 1.53M) was added and stirred for 30 minutes. Nitrogen in the glass autoclave was stopped, then ethylene was passed in an amount of 5 liter / hour and hydrogen in an amount of 40 liter / hour, and then the above solution was added to initiate the polymerization. During the polymerization, ethylene was continuously supplied at a rate of 5 liters / hour and hydrogen at a rate of 40 liters / hour. Polymerization was carried out at 110 ° C. for 20 minutes under normal pressure, and then a small amount of isopropanol was added to terminate the polymerization. The polymer solution was added to 300 ml of 1N hydrochloric acid and stirred. This solution was transferred to a separatory funnel, and the organic layer was separated. The organic layer was washed with water, and the solvent and unreacted 1-decene were distilled off at 175 ° C. under reduced pressure (1 mmHg). The obtained transparent liquid polymer was 34.73 g, and the polymerization activity was 52.10 kg-polymer / mmol-Zr · hr. As a result of polymer analysis, the ethylene content was 15 mol%, [η] = 0.18 dl / g, Mw = 31,890, Mn = 19,130, and Mw / Mn = 1.67. Moreover, the syndiotacticity seen from the triad chain of the polymer was 65%.
得られたポリマーを用いた燃料油組成物の性能評価結果を表1に示した。 The performance evaluation results of the fuel oil composition using the obtained polymer are shown in Table 1.
内容量1000mlのガラス製オートクレーブに温度計、気体吹き込み管、ガラス製攪拌羽根を備え、充分に窒素置換した。その後、トルエン250mlと1−デセン250mlを装入し、窒素を50リットル/時間で流通させながら温度を50℃にした。一方、充分に窒素置換した内容量30mlの枝付きフラスコにマグネチックスターラーチップを入れ、これに遷移金属化合物としてジフェニルメチレン(シクロペンタジエニル)(フルオ
レニル)ジルコニウムジクロリドのトルエン溶液0.002mmol、およびメチルアルミノキサンのトルエン溶液(Al=1.53M)2mmolを加え、30分間攪拌した。ガラス製オートクレーブ中の窒素を止め、次にエチレンを5リットル/時間と水素を10リットル/時間の量で流通させてから、次いで上記溶液を加え、重合を開始した。重合中はエチレンを5リットル/時間と水素を10リットル/時間の量で連続的に供給し、常圧下、50℃で60分間重合を行った後、少量のイソプロパノールを添加し重合を停止した。これを、1Nの塩酸300ml中にポリマー溶液を加え、攪拌した。この溶液を分液ロートに移し、有機層を分取した後、有機層を水洗し、175℃、減圧下(1mmHg)で溶媒と未反応の1−デセンを留去した。得られた透明の液状ポリマーは51.90gであり、重合活性は25.95kg−polymer/mmol−Zr・hrであった。ポリマー分析の結果、エチレン含量は21モル%、[η]=0.48dl/gであり、Mw=117,550、Mn=71,020、Mw/Mn=1.66であった。また、ポリマーのトリアッド連鎖でみたシンジオタクティシティーは54%であった。
A glass autoclave with an internal volume of 1000 ml was equipped with a thermometer, a gas blowing tube, and a glass stirring blade, and sufficiently substituted with nitrogen. Thereafter, 250 ml of toluene and 250 ml of 1-decene were charged, and the temperature was set to 50 ° C. while flowing nitrogen at 50 liters / hour. On the other hand, a magnetic stirrer chip was placed in a 30 ml branch flask with a sufficient internal volume substituted with nitrogen, and 0.002 mmol of a toluene solution of diphenylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride as a transition metal compound, and methyl 2 mmol of aluminoxane in toluene (Al = 1.53M) was added and stirred for 30 minutes. Nitrogen in the glass autoclave was stopped, then ethylene was passed in an amount of 5 liters / hour and hydrogen in an amount of 10 liters / hour, and then the above solution was added to initiate polymerization. During the polymerization, ethylene was continuously supplied at a rate of 5 liters / hour and hydrogen at a rate of 10 liters / hour, polymerization was carried out at 50 ° C. for 60 minutes under normal pressure, and then a small amount of isopropanol was added to terminate the polymerization. The polymer solution was added to 300 ml of 1N hydrochloric acid and stirred. This solution was transferred to a separatory funnel, and the organic layer was separated. The organic layer was washed with water, and the solvent and unreacted 1-decene were distilled off at 175 ° C. under reduced pressure (1 mmHg). The obtained transparent liquid polymer was 51.90 g, and the polymerization activity was 25.95 kg-polymer / mmol-Zr · hr. As a result of polymer analysis, the ethylene content was 21 mol%, [η] = 0.48 dl / g, Mw = 117,550, Mn = 71,020, and Mw / Mn = 1.66. Further, the syndiotacticity as seen by the triad chain of the polymer was 54%.
得られたポリマーを用いた燃料油組成物の性能評価結果を表1に示した。 The performance evaluation results of the fuel oil composition using the obtained polymer are shown in Table 1.
内容量1000mlのガラス製オートクレーブに温度計、気体吹き込み管、ガラス製攪拌羽根を備え、充分に窒素置換した。その後、n−ヘプタン250mlと1−デセン250mlを装入し、窒素を50リットル/時間で流通させながら温度を80℃にした。一方、充分に窒素置換した内容量30mlの枝付きフラスコにマグネチックスターラーチップを入れ、これに遷移金属化合物としてジフェニルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリドのトルエン溶液0.002mmol、およびメチルアルミノキサンのトルエン溶液(Al=1.53M)2mmolを加え、30分間攪拌した。ガラス製オートクレーブ中の窒素を止め、次に水素を35リットル/時間の量で流通させてから、次いで上記溶液を加え、重合を開始した。重合中は水素を35リットル/時間の量で連続的に供給し、常圧下、80℃で60分間重合を行った後、少量のイソプロパノールを添加し重合を停止した。これを、1Nの塩酸300ml中にポリマー溶液を加え、攪拌した。この溶液を分液ロートに移し、有機層を分取した後、有機層を水洗し、175℃、減圧下(1mmHg)で溶媒と未反応の1−デセンを留去した。得られた透明の液状ポリマーは29.43gであり、重合活性は14.72kg−polymer/mmol−Zr・hrであった。ポリマー分析の結果、[η]=0.18dl/gであり、Mw=34,140、Mn=23,120、Mw/Mn=1.48であった。また、ポリマーのトリアッド連鎖でみたシンジオタクティシティーは81%であった。 A glass autoclave with an internal volume of 1000 ml was equipped with a thermometer, a gas blowing tube, and a glass stirring blade, and sufficiently substituted with nitrogen. Thereafter, 250 ml of n-heptane and 250 ml of 1-decene were charged, and the temperature was raised to 80 ° C. while flowing nitrogen at 50 liters / hour. On the other hand, a magnetic stirrer chip was placed in a 30 ml branch flask with a sufficient internal volume substituted with nitrogen, and 0.002 mmol of a toluene solution of diphenylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride as a transition metal compound, and methyl 2 mmol of aluminoxane in toluene (Al = 1.53M) was added and stirred for 30 minutes. Nitrogen in the glass autoclave was stopped, and then hydrogen was passed in an amount of 35 liters / hour, and then the above solution was added to initiate polymerization. During the polymerization, hydrogen was continuously supplied in an amount of 35 liters / hour, polymerization was performed at 80 ° C. for 60 minutes under normal pressure, and then a small amount of isopropanol was added to terminate the polymerization. The polymer solution was added to 300 ml of 1N hydrochloric acid and stirred. This solution was transferred to a separatory funnel, and the organic layer was separated. The organic layer was washed with water, and the solvent and unreacted 1-decene were distilled off at 175 ° C. under reduced pressure (1 mmHg). The obtained transparent liquid polymer was 29.43 g, and the polymerization activity was 14.72 kg-polymer / mmol-Zr · hr. As a result of polymer analysis, [η] = 0.18 dl / g, Mw = 34,140, Mn = 23,120, and Mw / Mn = 1.48. Moreover, the syndiotacticity seen from the triad chain of the polymer was 81%.
得られたポリマーを用いた燃料油組成物の性能評価結果を表1に示した。 The performance evaluation results of the fuel oil composition using the obtained polymer are shown in Table 1.
[比較例1]
内容量1000mlのガラス製オートクレーブに温度計、気体吹き込み管、ガラス製攪拌羽根を備え、充分に窒素置換した。その後、n−デカン250mlと1−デセン250mlを装入し、窒素を50リットル/時間で流通させながら温度を150℃にした。一方、充分に窒素置換した内容量30mlの枝付きフラスコにマグネチックスターラーチップを入れ、これに遷移金属化合物としてジフェニルメチレン(シクロペンタジエニル)(フルオレニル)ジルコニウムジクロリドのトルエン溶液0.002mmol、およびメチルアルミノキサンのトルエン溶液(Al=1.53M)2mmolを加え、30分間攪拌した。ガラス製オートクレーブ中の窒素を止め、次にエチレンを20リットル/時間と水素を20リットル/時間の量で流通させてから、次いで上記溶液を加え、重合を開始した。重合中はエチレンを20リットル/時間と水素を20リットル/時間の量で連続的に供給し、常圧下、150℃で60分間重合を行った後、少量のイソプロパノールを添加し重合を停止した。これを、1Nの塩酸300ml中にポリマー溶液を加え、攪拌した。この溶
液を分液ロートに移し、有機層を分取した後、有機層を水洗し、175℃、減圧下(1mmHg)で溶媒と未反応の1−デセンを留去した。得られた透明の液状ポリマーは16.82gであり、重合活性は8.41kg−polymer/mmol−Zr・hrであった。ポリマー分析の結果、エチレン含量は35モル%、[η]=0.09dl/gであり、Mw=15,790、Mn=10,520、Mw/Mn=1.50であった。また、ポリマーのトリアッド連鎖でみたシンジオタクチシティーは46%であった。
[Comparative Example 1]
A glass autoclave with an internal volume of 1000 ml was equipped with a thermometer, a gas blowing tube, and a glass stirring blade, and sufficiently substituted with nitrogen. Thereafter, 250 ml of n-decane and 250 ml of 1-decene were charged, and the temperature was adjusted to 150 ° C. while nitrogen was circulated at 50 liters / hour. On the other hand, a magnetic stirrer chip was placed in a 30 ml branch flask with a sufficient internal volume substituted with nitrogen, and 0.002 mmol of a toluene solution of diphenylmethylene (cyclopentadienyl) (fluorenyl) zirconium dichloride as a transition metal compound, and methyl 2 mmol of aluminoxane in toluene (Al = 1.53M) was added and stirred for 30 minutes. Nitrogen in the glass autoclave was stopped, then ethylene was passed in an amount of 20 liter / hour and hydrogen in an amount of 20 liter / hour, and then the above solution was added to initiate polymerization. During the polymerization, ethylene was continuously supplied at a rate of 20 liters / hour and hydrogen at a rate of 20 liters / hour, and polymerization was carried out at 150 ° C. for 60 minutes under normal pressure, and then a small amount of isopropanol was added to terminate the polymerization. The polymer solution was added to 300 ml of 1N hydrochloric acid and stirred. This solution was transferred to a separatory funnel, and the organic layer was separated. The organic layer was washed with water, and the solvent and unreacted 1-decene were distilled off at 175 ° C. under reduced pressure (1 mmHg). The obtained transparent liquid polymer was 16.82 g, and the polymerization activity was 8.41 kg-polymer / mmol-Zr · hr. As a result of polymer analysis, the ethylene content was 35 mol%, [η] = 0.09 dl / g, Mw = 15,790, Mn = 10,520, and Mw / Mn = 1.50. Further, the syndiotacticity as seen by the triad chain of the polymer was 46%.
得られたポリマーを用いた燃料油組成物の性能評価結果を表1に示した。 The performance evaluation results of the fuel oil composition using the obtained polymer are shown in Table 1.
[比較例2]
内容量1000mlのガラス製オートクレーブに温度計、気体吹き込み管、ガラス製攪拌羽根を備え、充分に窒素置換した。その後、トルエン500mlを装入し、窒素を50リットル/時間で流通させながら温度を60℃にした。一方、充分に窒素置換した内容量30mlの枝付きフラスコにマグネチックスターラーチップを入れ、これに遷移金属化合物としてビス(1,3−ジメチルシクロペンタジエニル)ジルコニウムジクロリドのトルエン溶液0.04mmol、およびメチルアルミノキサンのトルエン溶液(Al=1.53M)10mmolを加え、30分間攪拌した。ガラス製オートクレーブ中の窒素を止め、次にエチレンを25リットル/時間とプロピレンを25リットル/時間の量で流通させてから、次いで上記溶液を加え、重合を開始した。重合中はエチレンを25リットル/時間とプロピレンを25リットル/時間の量で連続的に供給し、常圧下、60℃で30分間重合を行った後、少量のイソプロパノールを添加し重合を停止した。これを、1Nの塩酸300ml中にポリマー溶液を加え、攪拌した。この溶液を分液ロートに移し、有機層を分取した後、有機層を水洗し、160℃、減圧下(1mmHg)で溶媒を留去した。得られた透明の液状ポリマーは18.85gであり、重合活性は0.94kg−polymer/mmol−Zr・hrであった。ポリマー分析の結果、エチレン含量は71モル%、[η]=0.20dl/gであり、Mw=13,340、Mn=6,770、Mw/Mn=1.57であった。
[Comparative Example 2]
A glass autoclave with an internal volume of 1000 ml was equipped with a thermometer, a gas blowing tube, and a glass stirring blade, and sufficiently substituted with nitrogen. Thereafter, 500 ml of toluene was charged, and the temperature was adjusted to 60 ° C. while flowing nitrogen at 50 liters / hour. On the other hand, a magnetic stirrer chip was placed in a 30 ml branch flask having a sufficient internal volume substituted with nitrogen, and 0.04 mmol of a toluene solution of bis (1,3-dimethylcyclopentadienyl) zirconium dichloride as a transition metal compound, and 10 mmol of a toluene solution of methylaluminoxane (Al = 1.53M) was added and stirred for 30 minutes. Nitrogen in the glass autoclave was stopped, then ethylene was passed in an amount of 25 liter / hour and propylene in an amount of 25 liter / hour, and then the above solution was added to initiate the polymerization. During the polymerization, ethylene was continuously supplied at a rate of 25 liters / hour and propylene at a rate of 25 liters / hour, and polymerization was performed at 60 ° C. for 30 minutes under normal pressure, and then a small amount of isopropanol was added to terminate the polymerization. The polymer solution was added to 300 ml of 1N hydrochloric acid and stirred. This solution was transferred to a separatory funnel, and the organic layer was separated. The organic layer was washed with water, and the solvent was distilled off at 160 ° C. under reduced pressure (1 mmHg). The obtained transparent liquid polymer was 18.85 g, and the polymerization activity was 0.94 kg-polymer / mmol-Zr · hr. As a result of polymer analysis, the ethylene content was 71 mol%, [η] = 0.20 dl / g, Mw = 13,340, Mn = 6,770, and Mw / Mn = 1.57.
得られたポリマーを用いた燃料油組成物の性能評価結果を表1に示した。 The performance evaluation results of the fuel oil composition using the obtained polymer are shown in Table 1.
[比較例3]
市販のポリデセン(Mw=27,450、Mn=10,850、Mw/Mn=2.53、アタクティックポリマー(シンジオタクティシティー<40%))を用いた燃料油組成物の性能評価結果を表1に示した。
[Comparative Example 3]
Results of performance evaluation of fuel oil composition using commercially available polydecene (Mw = 27,450, Mn = 10,850, Mw / Mn = 2.53, atactic polymer (syndiotacticity <40%)) are shown. It was shown in 1.
本発明の燃料油組成物は、ワックスの結晶成長や粘度上昇がなく、低温濾過器目詰まり点および流動点が低く、さらに低温流動性に優れているので、配管を閉塞したり、油全体の粘度が極端に上昇して流動性を失うというような従来の問題点を解消することができる。 The fuel oil composition of the present invention has no wax crystal growth or viscosity increase, has a low temperature filter clogging point and a low pour point, and is excellent in low temperature fluidity. The conventional problem that the viscosity is extremely increased and the fluidity is lost can be solved.
Claims (8)
(B)メタロセン触媒を主触媒として重合された(i)(a)炭素原子数8〜20のα−オレフィンから選ばれる少なくとも1種類の単量体から導かれる構成単位を20〜100モル%の範囲で含有し、(b)エチレンから導かれる構成単位を0〜80モル%の範囲の量で含有し、
(ii)135℃でデカリン中で測定した極限粘度[η]が0.1〜1.0dl/gの範囲にあるα−オレフィン(共)重合体からなる燃料油流動性改良剤と
を含むことを特徴とする燃料油組成物。 (A) a middle distillate fuel oil having a boiling point of 150 ° C to 400 ° C;
(B) 20-100 mol% of structural units derived from at least one monomer selected from (i) (a) an α-olefin having 8-20 carbon atoms, polymerized using a metallocene catalyst as the main catalyst (B) containing structural units derived from ethylene in an amount ranging from 0 to 80 mol%,
(Ii) a fuel oil fluidity improver comprising an α-olefin (co) polymer having an intrinsic viscosity [η] measured in decalin at 135 ° C. in the range of 0.1 to 1.0 dl / g. A fuel oil composition characterized by the above.
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R9およびR10は、水素原子、炭化水素基およびケイ素含有炭化水素基から選ばれ、互いに同一でも異なっていてもよく、R1ないしR8およびR9ないしR10で示される基のうち隣接した基は互いに結合して環を形成してもよく、Yは炭素原子またはケイ素原子であり、nは2〜4の整数、Mは周期表第4族から選ばれた金属を示し、jは1〜4の整数であり、Qはハロゲン原子、炭化水素基、アニオン配位子および孤立電子対で配位可能な中性配位子から選ばれ、jが2以上のときはQは互いに同一でも異なっていてもよい)。 The fuel oil composition according to claim 1, wherein the metallocene catalyst is a metallocene catalyst represented by the following general formula (1).
Wherein R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 and R 10 are selected from a hydrogen atom, a hydrocarbon group and a silicon-containing hydrocarbon group. May be the same or different from each other, and among the groups represented by R 1 to R 8 and R 9 to R 10 , adjacent groups may be bonded to each other to form a ring, and Y represents a carbon atom or a silicon atom N represents an integer of 2 to 4, M represents a metal selected from Group 4 of the periodic table, j represents an integer of 1 to 4, Q represents a halogen atom, a hydrocarbon group, an anionic ligand, and And selected from neutral ligands capable of coordinating with a lone pair, and when j is 2 or more, Qs may be the same or different from each other).
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R11およびR12は、水素原子、炭化水素基およびケイ素含有炭化水素基から選ばれ、互いに同一でも異なっていてもよく、R1ないしR8で示される基のうち隣接した基は互いに結合して環を形成してもよく、一般式(2)の場合はR1およびR8から選ばれる基とR11またはR12が互いに結合して環を形成してもよく、Aは不飽和結合および/または芳香族環を含んでいてもよい炭素原子数2〜20の2価の炭化水素基を示し、AはYと共に形成する環を含めて2つ以上の環構造を含んでいてもよく、Yは炭素原子またはケイ素原子であり、Mは周期表第4族から選ばれた金属を示し、jは1〜4の整数であり、Qはハロゲン原子、炭化水素基、アニオン配位子および孤立電子対で配位可能な中性配位子から選ばれ、jが2以上のときはQは互いに同一でも異なっていてもよい)。 The fuel oil composition according to claim 1, wherein the metallocene catalyst is a metallocene catalyst represented by the following general formula (2) or (3).
Wherein R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 11 and R 12 are selected from a hydrogen atom, a hydrocarbon group and a silicon-containing hydrocarbon group. May be the same or different from each other, and adjacent groups among the groups represented by R 1 to R 8 may be bonded to each other to form a ring. In the case of the general formula (2), R 1 and R 8 R 11 or R 12 may be bonded to each other to form a ring, and A is a divalent divalent having 2 to 20 carbon atoms and may contain an unsaturated bond and / or an aromatic ring. Represents a hydrocarbon group, A may include two or more ring structures including a ring formed with Y, Y is a carbon atom or a silicon atom, and M is selected from Group 4 of the periodic table. Represents a metal, j is an integer of 1 to 4, Q is a halogen atom, a hydrocarbon group, an anionic ligand and a lone pair Selected from coordinating neutral ligands capable, Q is may be the same or different when j is 2 or more).
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R9およびR10は、水素原子、炭化水素基およびケイ素含有炭化水素基から選ばれ、互いに同一でも異なっていてもよく、R1からR8は同時に水素ではなく、R1ないしR8およびR9ないしR10で示される基のうち隣接した基は互いに結合して環を形成してもよく、Yは炭素原子またはケイ素原子であり、nは2〜4の整数、Mは周期表第4族から選ばれた金属を示し、jは1〜4の整数であり、Qはハロゲン原子、炭化水素基、アニオン配位子および孤立電子対で配位可能な中性配位子から選ばれ、jが2以上のときはQは互いに同一でも異なっていてもよい)。 The fuel oil composition according to claim 1, wherein the metallocene catalyst is a metallocene catalyst represented by the following general formula (4).
Wherein R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 and R 10 are selected from a hydrogen atom, a hydrocarbon group and a silicon-containing hydrocarbon group. R 1 to R 8 may not be hydrogen at the same time, and adjacent groups among the groups represented by R 1 to R 8 and R 9 to R 10 are bonded to each other to form a ring. Y is a carbon atom or a silicon atom, n is an integer of 2 to 4, M is a metal selected from Group 4 of the periodic table, j is an integer of 1 to 4, and Q is a halogen atom. It is selected from an atom, a hydrocarbon group, an anionic ligand, and a neutral ligand capable of coordinating with a lone electron pair, and when j is 2 or more, Q may be the same or different.
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R11およびR12は、水素原子、炭化水素基およびケイ素含有炭化水素基から選ばれ、互いに同一でも異なっていてもよく、R1からR8は同時に水素ではなく、R1ないしR8で示される基のうち隣接した基は互いに結合して環を形成してもよく、一般式(5)の場合はR1からR8は同時に水素ではなく、R1およびR8から選ばれる基とR11またはR12が互いに結合して環を形成してもよく、Aは不飽和結合および/または芳香族環を含んでいてもよい炭素原子数2〜20の2価の炭化水素基を示し、AはYと共に形成する環を含めて2つ以上の環構造を含んでいてもよく、Yは炭素原子またはケイ素原子であり、Mは周期表第4族から選ばれた金属を示し、jは1〜4の整数であり、Qはハロゲン原子、炭化水素基、アニオン配位子および孤立電子対で配位可能な中性配位子から選ばれ、jが2以上のときはQは互いに同一でも異なっていてもよい)。 The fuel oil composition according to claim 1, wherein the metallocene catalyst is a metallocene catalyst represented by the following general formula (5) or (6).
Wherein R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 11 and R 12 are selected from a hydrogen atom, a hydrocarbon group and a silicon-containing hydrocarbon group. R 1 to R 8 may not be hydrogen at the same time, and adjacent groups among the groups represented by R 1 to R 8 may be bonded to each other to form a ring. In the case of (5), R 1 to R 8 are not simultaneously hydrogen, but a group selected from R 1 and R 8 and R 11 or R 12 may be bonded to each other to form a ring, and A is an unsaturated bond And / or a divalent hydrocarbon group having 2 to 20 carbon atoms which may contain an aromatic ring, and A may contain two or more ring structures including a ring formed with Y , Y is a carbon atom or a silicon atom, M represents a metal selected from Group 4 of the periodic table, and j is an integer of 1 to 4 Q is selected from a halogen atom, a hydrocarbon group, an anionic ligand and a neutral ligand capable of coordinating with a lone pair, and when j is 2 or more, Q may be the same or different from each other ).
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004005113A JP2005200445A (en) | 2004-01-13 | 2004-01-13 | Fuel oil composition |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004005113A JP2005200445A (en) | 2004-01-13 | 2004-01-13 | Fuel oil composition |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005200445A true JP2005200445A (en) | 2005-07-28 |
Family
ID=34819532
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004005113A Pending JP2005200445A (en) | 2004-01-13 | 2004-01-13 | Fuel oil composition |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005200445A (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101790346B1 (en) | 2010-04-22 | 2017-10-25 | 니치유 가부시키가이샤 | Flow improver for biodiesel fuels |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0561769U (en) * | 1992-01-23 | 1993-08-13 | 株式会社トミー | Learning toys |
| JPH0772961A (en) * | 1993-09-07 | 1995-03-17 | Canon Inc | Information processing system |
| JP2001194986A (en) * | 2000-01-12 | 2001-07-19 | Sente Creations:Kk | Intellectual education toy |
| JP2002278437A (en) * | 2001-03-21 | 2002-09-27 | Agatsuma:Kk | Intellectual toy |
| JP2004065516A (en) * | 2002-08-06 | 2004-03-04 | Tomy Co Ltd | Toy |
-
2004
- 2004-01-13 JP JP2004005113A patent/JP2005200445A/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0561769U (en) * | 1992-01-23 | 1993-08-13 | 株式会社トミー | Learning toys |
| JPH0772961A (en) * | 1993-09-07 | 1995-03-17 | Canon Inc | Information processing system |
| JP2001194986A (en) * | 2000-01-12 | 2001-07-19 | Sente Creations:Kk | Intellectual education toy |
| JP2002278437A (en) * | 2001-03-21 | 2002-09-27 | Agatsuma:Kk | Intellectual toy |
| JP2004065516A (en) * | 2002-08-06 | 2004-03-04 | Tomy Co Ltd | Toy |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101790346B1 (en) | 2010-04-22 | 2017-10-25 | 니치유 가부시키가이샤 | Flow improver for biodiesel fuels |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0611773B1 (en) | Catalyst component for use in the polymerization of alpha-olefins and process for producing alpha-olefin polymers using the same | |
| EP0611772B1 (en) | Catalyst component for use in the polymerization of alpha-olefins and process for producing alpha-olefin polymers using the same | |
| US5384299A (en) | Ionic metallocene catalyst compositions | |
| US5198401A (en) | Ionic metallocene catalyst compositions | |
| US7129306B2 (en) | Process for the oligomerization of α-olefins having low unsaturation | |
| US6617466B1 (en) | Monocylopentadienyl transition metal olefin polymerization catalysts | |
| US6423795B1 (en) | Tetramethylcyclopentadienyl titanium compounds for ethylene-α-olefin-copolymer production catalysts | |
| EP0671404A2 (en) | Monocyclopentadienyl transition metal olefin polymerization catalysts | |
| JP2000507959A (en) | Fused ring substituted indenyl metal complex and polymerization method | |
| EP0887355B1 (en) | Process for preparing olefin polymers | |
| JPH05331232A (en) | Production of ethylenic polymer composition | |
| JP5303264B2 (en) | 1-butene polymer and process for producing the same | |
| JP2005200450A (en) | METHOD FOR PRODUCING alpha-OLEFIN (CO)POLYMER | |
| JPH10259212A (en) | Production of olefin (co) polymer | |
| JP2012149188A (en) | Method for producing olefin polymer | |
| JP2005504853A (en) | Branched polymers based on alpha-olefins | |
| JPH05320248A (en) | Production of ethylenic polymer composition | |
| JP2005200453A (en) | METHOD FOR PRODUCING alpha-OLEFIN (CO)POLYMER | |
| US6562921B1 (en) | Catalyst precursor compound and olefin polymerization process using same | |
| JP2005200445A (en) | Fuel oil composition | |
| JPH06172433A (en) | Catalytic component for alpha-olefin polymerization and its use | |
| JPH06239917A (en) | Catalyst component for polymerizing alpha-olefin and production of alpha-olefinic polymer | |
| JP2005200452A (en) | METHOD FOR PRODUCING alpha-OLEFIN (CO)POLYMER | |
| JP3739701B2 (en) | Catalyst component for .ALPHA.-olefin polymerization. | |
| JP4245864B2 (en) | Olefin polymerization catalyst and polymerization method using the catalyst |