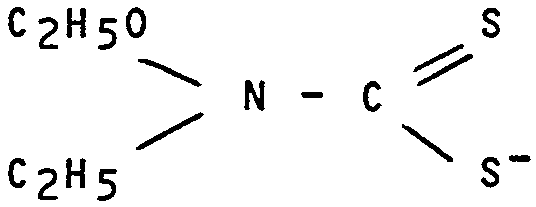FR2698272A1 - Procédé de marquage cellulaire au moyen de complexes nitruro-bis (dithiocarbamato)Tc-99m et trousse pour la mise en Óoeuvre de ce procédé. - Google Patents
Procédé de marquage cellulaire au moyen de complexes nitruro-bis (dithiocarbamato)Tc-99m et trousse pour la mise en Óoeuvre de ce procédé. Download PDFInfo
- Publication number
- FR2698272A1 FR2698272A1 FR9213963A FR9213963A FR2698272A1 FR 2698272 A1 FR2698272 A1 FR 2698272A1 FR 9213963 A FR9213963 A FR 9213963A FR 9213963 A FR9213963 A FR 9213963A FR 2698272 A1 FR2698272 A1 FR 2698272A1
- Authority
- FR
- France
- Prior art keywords
- sep
- cells
- formula
- suspension
- radiopharmaceutical
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 210000004027 cell Anatomy 0.000 title claims abstract description 55
- 239000003446 ligand Substances 0.000 title claims abstract description 18
- 210000003714 granulocyte Anatomy 0.000 title claims abstract description 17
- 238000000163 radioactive labelling Methods 0.000 title claims abstract description 9
- 229940056501 technetium 99m Drugs 0.000 title claims description 7
- -1 technetium-99m nitride Chemical class 0.000 title description 2
- GNVMUORYQLCPJZ-UHFFFAOYSA-M Thiocarbamate Chemical compound NC([S-])=O GNVMUORYQLCPJZ-UHFFFAOYSA-M 0.000 title 1
- 239000012217 radiopharmaceutical Substances 0.000 claims abstract description 39
- 238000000034 method Methods 0.000 claims abstract description 38
- 229940121896 radiopharmaceutical Drugs 0.000 claims abstract description 25
- 230000002799 radiopharmaceutical effect Effects 0.000 claims abstract description 25
- 239000000725 suspension Substances 0.000 claims abstract description 17
- DKVNPHBNOWQYFE-UHFFFAOYSA-N carbamodithioic acid Chemical compound NC(S)=S DKVNPHBNOWQYFE-UHFFFAOYSA-N 0.000 claims abstract description 10
- 239000012990 dithiocarbamate Substances 0.000 claims abstract description 10
- 229910052757 nitrogen Inorganic materials 0.000 claims description 33
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 24
- 210000004369 blood Anatomy 0.000 claims description 15
- 239000008280 blood Substances 0.000 claims description 15
- 239000003638 chemical reducing agent Substances 0.000 claims description 13
- 229910052799 carbon Inorganic materials 0.000 claims description 12
- 125000004432 carbon atom Chemical group C* 0.000 claims description 12
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 12
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 claims description 10
- 125000000962 organic group Chemical group 0.000 claims description 10
- 229910052751 metal Inorganic materials 0.000 claims description 9
- 239000002184 metal Substances 0.000 claims description 9
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 claims description 8
- 150000001875 compounds Chemical class 0.000 claims description 8
- FWPIDFUJEMBDLS-UHFFFAOYSA-L tin(II) chloride dihydrate Chemical group O.O.Cl[Sn]Cl FWPIDFUJEMBDLS-UHFFFAOYSA-L 0.000 claims description 8
- GKLVYJBZJHMRIY-OUBTZVSYSA-N Technetium-99 Chemical compound [99Tc] GKLVYJBZJHMRIY-OUBTZVSYSA-N 0.000 claims description 7
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 7
- 239000013067 intermediate product Substances 0.000 claims description 7
- 239000000203 mixture Substances 0.000 claims description 7
- 239000002253 acid Substances 0.000 claims description 6
- 229910052739 hydrogen Inorganic materials 0.000 claims description 5
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 claims description 4
- FCMYSEXCLRFWBP-UHFFFAOYSA-N [NH4+].[NH4+].[O-]S(=O)S([O-])=O Chemical compound [NH4+].[NH4+].[O-]S(=O)S([O-])=O FCMYSEXCLRFWBP-UHFFFAOYSA-N 0.000 claims description 4
- 125000001931 aliphatic group Chemical group 0.000 claims description 4
- 125000003118 aryl group Chemical group 0.000 claims description 4
- UAZDIGCOBKKMPU-UHFFFAOYSA-O azanium;azide Chemical compound [NH4+].[N-]=[N+]=[N-] UAZDIGCOBKKMPU-UHFFFAOYSA-O 0.000 claims description 4
- 239000006285 cell suspension Substances 0.000 claims description 4
- 229910021645 metal ion Inorganic materials 0.000 claims description 4
- 229910000073 phosphorus hydride Inorganic materials 0.000 claims description 4
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical group C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 claims description 4
- HCOMFAYPHBFMKU-UHFFFAOYSA-N butanedihydrazide Chemical compound NNC(=O)CCC(=O)NN HCOMFAYPHBFMKU-UHFFFAOYSA-N 0.000 claims description 3
- IUTCEZPPWBHGIX-UHFFFAOYSA-N tin(2+) Chemical compound [Sn+2] IUTCEZPPWBHGIX-UHFFFAOYSA-N 0.000 claims description 3
- 229910017464 nitrogen compound Inorganic materials 0.000 claims description 2
- 150000002830 nitrogen compounds Chemical class 0.000 claims description 2
- 239000001294 propane Substances 0.000 claims description 2
- TXUICONDJPYNPY-UHFFFAOYSA-N (1,10,13-trimethyl-3-oxo-4,5,6,7,8,9,11,12,14,15,16,17-dodecahydrocyclopenta[a]phenanthren-17-yl) heptanoate Chemical group C1CC2CC(=O)C=C(C)C2(C)C2C1C1CCC(OC(=O)CCCCCC)C1(C)CC2 TXUICONDJPYNPY-UHFFFAOYSA-N 0.000 claims 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 claims 1
- 229910021626 Tin(II) chloride Inorganic materials 0.000 claims 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims 1
- 235000011150 stannous chloride Nutrition 0.000 claims 1
- 239000001119 stannous chloride Substances 0.000 claims 1
- 238000002372 labelling Methods 0.000 abstract description 25
- 210000000601 blood cell Anatomy 0.000 abstract description 5
- 210000003743 erythrocyte Anatomy 0.000 abstract description 5
- 208000015181 infectious disease Diseases 0.000 abstract description 3
- 206010061218 Inflammation Diseases 0.000 abstract 1
- 230000004054 inflammatory process Effects 0.000 abstract 1
- 150000004767 nitrides Chemical class 0.000 abstract 1
- 230000000694 effects Effects 0.000 description 20
- 238000002360 preparation method Methods 0.000 description 20
- 239000000243 solution Substances 0.000 description 16
- 230000000052 comparative effect Effects 0.000 description 13
- 210000000265 leukocyte Anatomy 0.000 description 11
- 239000000047 product Substances 0.000 description 10
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 8
- 229910052708 sodium Inorganic materials 0.000 description 8
- 239000011734 sodium Substances 0.000 description 8
- 239000007864 aqueous solution Substances 0.000 description 7
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 241000282414 Homo sapiens Species 0.000 description 4
- 125000000066 S-methyl group Chemical group [H]C([H])([H])S* 0.000 description 4
- 230000007935 neutral effect Effects 0.000 description 4
- 229910052713 technetium Inorganic materials 0.000 description 4
- GKLVYJBZJHMRIY-UHFFFAOYSA-N technetium atom Chemical compound [Tc] GKLVYJBZJHMRIY-UHFFFAOYSA-N 0.000 description 4
- 230000035899 viability Effects 0.000 description 4
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 239000008188 pellet Substances 0.000 description 3
- 238000009825 accumulation Methods 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 230000035605 chemotaxis Effects 0.000 description 2
- 239000000084 colloidal system Substances 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000002405 diagnostic procedure Methods 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 230000002757 inflammatory effect Effects 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 230000000242 pagocytic effect Effects 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 239000000700 radioactive tracer Substances 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 150000003495 technetium Chemical class 0.000 description 2
- 125000004200 2-methoxyethyl group Chemical group [H]C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 1
- YEEGWNXDUZONAA-UHFFFAOYSA-K 5-hydroxy-2,8,9-trioxa-1-gallabicyclo[3.3.2]decane-3,7,10-trione Chemical compound [Ga+3].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O YEEGWNXDUZONAA-UHFFFAOYSA-K 0.000 description 1
- 206010056519 Abdominal infection Diseases 0.000 description 1
- 206010003011 Appendicitis Diseases 0.000 description 1
- 0 C1CC*CC1 Chemical compound C1CC*CC1 0.000 description 1
- YTRZHYVFLCVTGC-UHFFFAOYSA-N CN(C)CSCCSC Chemical compound CN(C)CSCCSC YTRZHYVFLCVTGC-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- YEEGWNXDUZONAA-RYDPDVNUSA-K Gallium Citrate (67 Ga) Chemical compound [67Ga+3].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O YEEGWNXDUZONAA-RYDPDVNUSA-K 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 238000001982 He+-excited Auger electron spectroscopy Methods 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- 239000012979 RPMI medium Substances 0.000 description 1
- IOEJYZSZYUROLN-UHFFFAOYSA-M Sodium diethyldithiocarbamate Chemical compound [Na+].CCN(CC)C([S-])=S IOEJYZSZYUROLN-UHFFFAOYSA-M 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- ZLRVWFDVJWKAIL-LXMACRGBSA-M [2,2-dimethyl-3-[(2r,3e)-3-oxidoiminobutan-2-yl]azanidylpropyl]-[(2r,3e)-3-hydroxyiminobutan-2-yl]azanide;oxotechnetium-99(3+) Chemical compound [99Tc+3]=O.O/N=C(\C)[C@@H](C)[N-]CC(C)(C)C[N-][C@H](C)C(\C)=N\[O-] ZLRVWFDVJWKAIL-LXMACRGBSA-M 0.000 description 1
- XVDFXDQCYAQYIK-UHFFFAOYSA-N [Tc+5] Chemical compound [Tc+5] XVDFXDQCYAQYIK-UHFFFAOYSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 1
- ZKLHYLQJFBULTC-UHFFFAOYSA-N amino(methyl)carbamodithioic acid Chemical compound CN(N)C(S)=S ZKLHYLQJFBULTC-UHFFFAOYSA-N 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000003788 cerebral perfusion Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- LMBWSYZSUOEYSN-UHFFFAOYSA-N diethyldithiocarbamic acid Chemical compound CCN(CC)C(S)=S LMBWSYZSUOEYSN-UHFFFAOYSA-N 0.000 description 1
- 150000004683 dihydrates Chemical class 0.000 description 1
- 229950004394 ditiocarb Drugs 0.000 description 1
- MSEQRUSCAMDFPD-UHFFFAOYSA-N ethoxycarbamodithioic acid Chemical compound CCONC(S)=S MSEQRUSCAMDFPD-UHFFFAOYSA-N 0.000 description 1
- 238000005188 flotation Methods 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 239000004922 lacquer Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- APGXDGZXGZROMN-UHFFFAOYSA-N n-piperidin-1-ium-1-ylcarbamodithioate Chemical compound SC(=S)NN1CCCCC1 APGXDGZXGZROMN-UHFFFAOYSA-N 0.000 description 1
- GQPLMRYTRLFLPF-UHFFFAOYSA-N nitrous oxide Inorganic materials [O-][N+]#N GQPLMRYTRLFLPF-UHFFFAOYSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- AOHJOMMDDJHIJH-UHFFFAOYSA-N propylenediamine Chemical compound CC(N)CN AOHJOMMDDJHIJH-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- YEENEYXBHNNNGV-XEHWZWQGSA-M sodium;3-acetamido-5-[acetyl(methyl)amino]-2,4,6-triiodobenzoate;(2r,3r,4s,5s,6r)-2-[(2r,3s,4s,5r)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound [Na+].CC(=O)N(C)C1=C(I)C(NC(C)=O)=C(I)C(C([O-])=O)=C1I.O[C@H]1[C@H](O)[C@@H](CO)O[C@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 YEENEYXBHNNNGV-XEHWZWQGSA-M 0.000 description 1
- GWQWBFBJCRDINE-UHFFFAOYSA-M sodium;carbamodithioate Chemical compound [Na+].NC([S-])=S GWQWBFBJCRDINE-UHFFFAOYSA-M 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
Classifications
-
- G—PHYSICS
- G21—NUCLEAR PHYSICS; NUCLEAR ENGINEERING
- G21H—OBTAINING ENERGY FROM RADIOACTIVE SOURCES; APPLICATIONS OF RADIATION FROM RADIOACTIVE SOURCES, NOT OTHERWISE PROVIDED FOR; UTILISING COSMIC RADIATION
- G21H5/00—Applications of radiation from radioactive sources or arrangements therefor, not otherwise provided for
- G21H5/02—Applications of radiation from radioactive sources or arrangements therefor, not otherwise provided for as tracers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/0474—Organic compounds complexes or complex-forming compounds, i.e. wherein a radioactive metal (e.g. 111In3+) is complexed or chelated by, e.g. a N2S2, N3S, NS3, N4 chelating group
- A61K51/0476—Organic compounds complexes or complex-forming compounds, i.e. wherein a radioactive metal (e.g. 111In3+) is complexed or chelated by, e.g. a N2S2, N3S, NS3, N4 chelating group complexes from monodendate ligands, e.g. sestamibi
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/12—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by a special physical form, e.g. emulsion, microcapsules, liposomes, characterized by a special physical form, e.g. emulsions, dispersions, microcapsules
- A61K51/1203—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by a special physical form, e.g. emulsion, microcapsules, liposomes, characterized by a special physical form, e.g. emulsions, dispersions, microcapsules in a form not provided for by groups A61K51/1206 - A61K51/1296, e.g. cells, cell fragments, viruses, virus capsides, ghosts, red blood cells, viral vectors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F13/00—Compounds containing elements of Groups 7 or 17 of the Periodic Table
- C07F13/005—Compounds without a metal-carbon linkage
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2123/00—Preparations for testing in vivo
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Physics & Mathematics (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Optics & Photonics (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- General Engineering & Computer Science (AREA)
- Engineering & Computer Science (AREA)
- High Energy & Nuclear Physics (AREA)
- Virology (AREA)
- Dispersion Chemistry (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
L'invention concerne un procédé de marquage cellulaire, en particulier des leucocytes, au moyen de complexes nitruro bis(dithiocarbamato)9 9 m Tc. Selon l'invention, on utilise un produit radiopharmaceutique comprenant un complexe nitruro bis(N,éthoxy-N,éthyldithiocarbamato) ou (N-diéthyldithiocarbamato)9 9 m Tc préparé de préférence par un procédé comprenant 1) la réaction d'un composé oxygéné de 9 9 m Tc avec un premier ligand azoté et un agent réducteur, puis 2) la réaction du produit intermédiaire ainsi obtenu avec au moins un composé de formule: (CF DESSIN DANS BOPI) dans laquelle R1 représente le groupe éthyle ou éthoxy, R2 est un ion de métal pharmaceutiquement acceptable de valence n, N+ ou NH4 + avec n=1. Par addition du produit radiopharmaceutique à une suspension de cellules telles que des leucocytes ou granulocytes, on obtient une suspension de cellules marquées avec un taux de marquage et une stabilité élevés, utilisable pour le diagnostic et la localisation des sites inflammatoires ou infectieux.
Description
Procédé de marquage celluLaire au doyen de complexes nitruro-bis (dithiocarbamato) Tc-99n et trousse pour La mise en oeuvre de ce procédé
La présente invention a pour objet un procédé de marquage cellulaire utilisant des complexes nitruro bis(dithiocarbamato) Tc-99m.
La présente invention a pour objet un procédé de marquage cellulaire utilisant des complexes nitruro bis(dithiocarbamato) Tc-99m.
De façon plus précise, elle concerne le marquage des cellules du sang telles que les leucocytes, plus particulièrement les granulocytes, en vue de la localisation anatomique des sites inflammatoires et des foyers infectieux.
La détection précoce et précise des complications infectieuses post-chirugicales, des infections dues à des blessures profondes après traumatisme et des appendicites, revêt une importance stratégique pour le clinicien, car elle permet de déclencher une thérapie précoce, clinique ou chirurgicale.
Les techniques radioisotopiques actuel le ment utilisées pour la détection des sites inflammatoires sont
- la scintigraphie avec le citrate de gallium (67Ga),
- le marquage des leucocytes par le 111Inoxinate ou le 11In-tropolonate,
- le marquage des leucocytes par le 99mTc via l'injection phagocytaire de colloïdes,
- le marquage des leucocytes par le 99mTc via l'accumulation d'un complexe neutre de technétium tel que le 99mTc-hexaméthylpropylèneamineoxime (Tc-HMPAO), et
- le marquage des leucocytes par des anticorps radiomarqués (antigranulocytes).
- la scintigraphie avec le citrate de gallium (67Ga),
- le marquage des leucocytes par le 111Inoxinate ou le 11In-tropolonate,
- le marquage des leucocytes par le 99mTc via l'injection phagocytaire de colloïdes,
- le marquage des leucocytes par le 99mTc via l'accumulation d'un complexe neutre de technétium tel que le 99mTc-hexaméthylpropylèneamineoxime (Tc-HMPAO), et
- le marquage des leucocytes par des anticorps radiomarqués (antigranulocytes).
La technique utilisant le citrate de gallium présente certains inconvénients. En effet, en raison de la lente accumulation du 67Ga, plus de 24h sont nécessaires entre l'injection et l'imagerie ; par ailleurs, la captation intestinale du citrate de 67Ga exclut son utilisation dans la recherche des infections abdominales.
Les techniques utilisant l'oxinate ou le tropolonate d'indium sont satisfaisantes mais ont l'inconvénient de délivrer une dose d'irradiation élevée aux patients et d'être très onéreuses en raison du coût élevé du radioisotope.
Les techniques utilisant le marquage des leucocytes via l'injection phagocytaire de colloides nécessitent une activation préliminaire des cellules qui conduit à une captation précoce du traceur dans les poumons.
Les techniques utilisant le marquage de cellules au moyen d'anticorps antigranulocytes se heurtent au problème de la nature murine des anticorps disponibles aujourd'hui qui peuvent induire chez l'homme une réaction immunitaire avec formation d'anticorps humains anti-souris (HAMA).
Les techniques utilisant des complexes neutres de technétium sont donc plus intéressantes, mais dans le cas du complexe 99mTc- HMPAO, connu comme traceur de perfusion cérébrale et comme marqueur des leucocytes par passage à travers la membrane cellulaire et fixation dans le cytoplasme, la préparation du complexe pose certains problèmes car La solution de 99mTc04- doit être exempte d'entraineur et le produit marqué n'est stable que 30min après sa préparation. La préparation de ce complexe et son utilisation pour le marquage de leucocytes sont décrits en particulier par Becker
W et al dans Nucl. Med. Comm., 9, 1988, p. 435447, par Danpure H.J. et al dans Nucl. Med. Comm., 9, 1988, p. 465-475, et par Kelbaek H et al dans
Eur. J. Nucl. Med., 14, 1988, p. 621-623.
W et al dans Nucl. Med. Comm., 9, 1988, p. 435447, par Danpure H.J. et al dans Nucl. Med. Comm., 9, 1988, p. 465-475, et par Kelbaek H et al dans
Eur. J. Nucl. Med., 14, 1988, p. 621-623.
Aussi, on a envisagé récemment d'utiliser d'autres complexes neutres de technétium du type nitruro bis(dithiocarbamato) technétium(V) comme il est décrit par Abram et Beyer dans Isotopenpraxis 26, 1990, 3, p.107-108.
Selon ces auteurs, les meilleurs résultats sont obtenus avec le complexe nitruro bis(N,N-di n-butyidithiocarbamato)99mTc. Ce complexe est obtenu par une réaction d'échange de ligands à partir de TcNCl4-, comme produit de départ, ce qui constitue un inconvénient car cette fabrication ne peut être effectuée facilement.
Le document W0 92/10214 décrit aussi l'utilisation de complexes de technétium comprenant des ligands dithiocarbamate pour le marquage radioactif de cellules sanguines. Selon ce document, le complexe est obtenu en ajoutant un pertechnétate de technétium 99m à un agent réducteur métallique, N un ligand ne contenant pas le motif N-Ns et un dithiocarbamate. Les complexes obtenus par cette technique ne sont donc pas des complexes nitruro de technétium.
La présente invention a précisément pour objet l'utilisation pour le marquage cellulaire de complexes spécifiques du type nitruro bis(dithiocarbamato) Tc-99m, qui peuvent être obtenus par un procédé simple et conduisent à un taux de marquage et à une stabilité élevés.
Aussi, l'invention a pour objet un procédé de marquage radioactif de cellules, qui consiste à ajouter à une suspension de ces cellules, un produit radiopharmaceutique comprenant un complexe de technétium 99m de formule
(Tc E N) L1 L2 (I) dans laquelle L1 et L2 qui peuvent être identiques ou différents, répondent à la formule ::
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy, à condition que l'un au moins des L1 et
L2 réponde à la formule
(Tc E N) L1 L2 (I) dans laquelle L1 et L2 qui peuvent être identiques ou différents, répondent à la formule ::
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy, à condition que l'un au moins des L1 et
L2 réponde à la formule
Dans ce procédé, l'utilisation d'un complexe comportant au moins un ligand N-éthyl,
N-éthoxydithiocarbamate, permet d'obtenir une efficacité de marquage élevée des cellules du sang telles que les leucocytes, en particulier les granulocytes, avec une bonne sélectivité vis-àvis d'autres cellules comme les hématies et une sélectivité encore plus élevée vis-à-vis des plaquettes.
N-éthoxydithiocarbamate, permet d'obtenir une efficacité de marquage élevée des cellules du sang telles que les leucocytes, en particulier les granulocytes, avec une bonne sélectivité vis-àvis d'autres cellules comme les hématies et une sélectivité encore plus élevée vis-à-vis des plaquettes.
Selon un mode préféré de réalisation de l'invention, le procédé de marquage radioactif de cellules consiste à ajouter à une suspension de ces cellules un produit radiopharmaceutique comprenant un complexe de technétium 99m de formule :
(Tc ~ N) L1 L2 (I) dans laquelle L1 et L2 qui peuvent être identiques ou différents, répondent à la formule ::
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy, ce produit radiopharmaceutique étant obtenu par un procédé comprenant 1) la réaction d'un composé oxygéné de 99mTc avec
a) un premier ligand azoté constitué
soit par un azoture d'ammonium ou
d'un métal pharmaceutiquement
acceptable, soit par un composé azoté
comportant un motif sN-Ns dans lequel
les N sont reliés à des atomes
d'hydrogène et/ou à des groupements
organiques monovalents par
l'intermédiaire d'un atome de carbone,
ou dans lequel l'un des N est relié
à l'atome de carbone d'un groupement
organique bivalent par l'intermédiaire
d'une double liaison et l'autre N
est relié à des atomes d'hydrogène
et/ou à des groupements organiques
monovalents par l'intermédiaire d'un
atome de carbone, et
b) un agent réducteur constitué, soit
par du dithionite d'ammonium ou d'un
métal pharmaceutiquement acceptable,
soit par de l'étain (II) présent sous
forme ionique dans la solution, soit
par une phosphine ou polyphosphine,
aliphatique ou aromatique, substituée
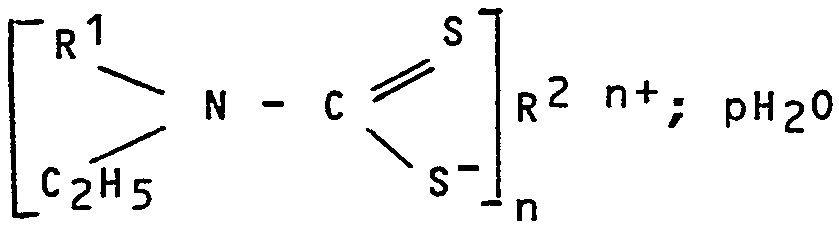
ou non substituée ; et 2) la réaction du produit intermédiaire obtenu dans la première étape avec au moins un composé de formule
dans laquelle R1 représente le groupe éthyle ou le groupe éthoxy, R2 est un ion de métal pharmaceuti quement acceptable de valence n, H avec n=1, ou
NH4+ avec n=1, et p est égal à O ou est un nombre alLant de 1 à 5.
(Tc ~ N) L1 L2 (I) dans laquelle L1 et L2 qui peuvent être identiques ou différents, répondent à la formule ::
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy, ce produit radiopharmaceutique étant obtenu par un procédé comprenant 1) la réaction d'un composé oxygéné de 99mTc avec
a) un premier ligand azoté constitué
soit par un azoture d'ammonium ou
d'un métal pharmaceutiquement
acceptable, soit par un composé azoté
comportant un motif sN-Ns dans lequel
les N sont reliés à des atomes
d'hydrogène et/ou à des groupements
organiques monovalents par
l'intermédiaire d'un atome de carbone,
ou dans lequel l'un des N est relié
à l'atome de carbone d'un groupement
organique bivalent par l'intermédiaire
d'une double liaison et l'autre N
est relié à des atomes d'hydrogène
et/ou à des groupements organiques
monovalents par l'intermédiaire d'un
atome de carbone, et
b) un agent réducteur constitué, soit
par du dithionite d'ammonium ou d'un
métal pharmaceutiquement acceptable,
soit par de l'étain (II) présent sous
forme ionique dans la solution, soit
par une phosphine ou polyphosphine,
aliphatique ou aromatique, substituée
ou non substituée ; et 2) la réaction du produit intermédiaire obtenu dans la première étape avec au moins un composé de formule
dans laquelle R1 représente le groupe éthyle ou le groupe éthoxy, R2 est un ion de métal pharmaceuti quement acceptable de valence n, H avec n=1, ou
NH4+ avec n=1, et p est égal à O ou est un nombre alLant de 1 à 5.
Généralement, R2 représente un ion de métal alcalin ou de métal alcalino-terreux, par exemple le sodium.
De préférence, dans la deuxième étape de re procédé, on utilise un composé de formules
dans lesquelles R2, n et p ont les significations données ci-dessus.
dans lesquelles R2, n et p ont les significations données ci-dessus.
Les ligands azotés, et les agents réducteurs utilisables pour la préparation de ce produit radiopharmaceutique sont ceux décrits en particulier dans les documents W0 90/08657, WO 90/ 06137 et
FR-A- 2 664 166.
FR-A- 2 664 166.
Selon l'invention, on peut utiliser par exemple un ligand azoté constitué par le S-méthyl,
N-méthyldithiocarbazate avec un agent réducteur constitué par la triphénylphosphine trisulfonée, un ligand azoté constitué par du S-méthyl, N-méthyl dithiocarbazate avec un agent réducteur constitué par du chlorure stanneux dihydraté introduit avec de l'acide propane-1,2-diamino-N,N,N',N'-tétracétique, ou encore un ligand azoté constitué par le succinyldihydrazide avec un agent réducteur constitué par du chlorure stanneux dihydraté introduit également avec de l'acide propane-1,2-diamino-N,N,N',N'tétracétique.
N-méthyldithiocarbazate avec un agent réducteur constitué par la triphénylphosphine trisulfonée, un ligand azoté constitué par du S-méthyl, N-méthyl dithiocarbazate avec un agent réducteur constitué par du chlorure stanneux dihydraté introduit avec de l'acide propane-1,2-diamino-N,N,N',N'-tétracétique, ou encore un ligand azoté constitué par le succinyldihydrazide avec un agent réducteur constitué par du chlorure stanneux dihydraté introduit également avec de l'acide propane-1,2-diamino-N,N,N',N'tétracétique.
Les modes de préparation des produits radiopharmaceutiques utilisés dans l'invention à partir de différents ligands azotés et de divers agents réducteurs sont décrits également dans les documents WO 90/08657, WO 90/06137 et FR-A-2 664 166.
Le procédé de l'invention peut être utilisé pour le marquage de nombreux types de cellules, et plus particulièrement pour le marquage des cellules du sang telles que Les leucocytes et plus particulièrement les granulocytes.
Dans ce cas, la suspension de cellules utilisée peut être constituée par un échantillon de sang total ou par des leucocytes ou granulocytes séparés du sang et remis en suspension dans un milieu approprié, par exemple le milieu de culture
RPMI ou un plasma pauvre en cellules. Dans ce dernier cas, la concentration en granulocytes ou leucocytes de la suspension est avantageusement de 2.107 à 108 cellules par 2 à 6ml de suspension.
RPMI ou un plasma pauvre en cellules. Dans ce dernier cas, la concentration en granulocytes ou leucocytes de la suspension est avantageusement de 2.107 à 108 cellules par 2 à 6ml de suspension.
Pour réaliser la séparation des leucocytes ou des granulocytes du sang, on utilise des techniques classiques, par exemple la méthode de sédimentation et flottation sur Ficoll.
Pour mettre en oeuvre le procédé de l'invention, on ajoute à la suspension de cellules, par exemple à la suspension de leucocytes (ou granulocytes) ou à l'échantillon de sang total, le produit radiopharmaceutique fraichement préparé qui contient le complexe neutre de nitruro bis (dithiocarbamato) technétium-99m, puis on laisse incuber pendant une durée appropriée, par exemple de 5 à 15min, en opérant sous agitation lente à la température ambiante.
De préférence, la quantité de produit radiopharmaceutique utilisée est telle que la radioactivité ajoutée soit de 50 à 300MBq pour 3.107 cellules. En effet, l'efficacité de marquage décroit lorsque l'activité est supérieure à 400MBq pour 3.107 cellules. Par ailleurs, la viabilité des cellules est conservée entre 50 et 300MBq alors qu'elle est réduite lorsque la radioactivité ajoutée dépasse 300MBq pour 3.107 cellules.
Le produit radiopharmaceutique ajouté a de préférence un pH ne dépassant pas 8,5 car au-delà de cette valeur, l'efficacité du marquage diminue.
Après incubation, on utilise la suspension pour effectuer des tests de diagnostic.
Aussi, l'invention a également pour objet une trousse pour le marquage radioactif de cellules, destinée à ces tests de diagnostic.
Selon l'invention, cette trousse de marquage comprend
- un premier flacon contenant un ligand azoté constitué soit par un azoture d'ammonium ou d'un métal pharmaceutiquement acceptable, soit par un composé azoté comportant un motif N-N dans lequel les N sont reliés à des atomes d'hydrogène et/ou à des groupements organiques monovalents par l'intermédiaire d'un atome de carbone, ou dans lequel l'un des N est relié à l'atome de carbone d'un groupement organique bivalent par l'intermediai- re d'une double liaison et l'autre N est relié à des atomes d'hydrogène et/ou à des groupements organiques monovalents par l'intermédiaire d'un atome de carbone ;;
- un deuxième flacon comprenant un agent réducteur constitué, soit du dithionite d'ammonium ou d'un métal pharmaceutiquement acceptable, soit par de l'étain (II) présent sous forme ionique, soit par une phosphine ou polyphosphine, aliphatique ou aromatique, substituée ou non substituée ; et
- un troisième flacon comprenant un dithiocarbamate de formule
dans laquelle R1 représente le groupe éthyle ou le groupe éthoxy, R2 est un ion de métal pharmaceutiquement acceptable de valence n ou H+ avec n=1, ou NH4+ avec n=1, et p est égal à 0 ou est un nombre allant de 1 à 5.
- un premier flacon contenant un ligand azoté constitué soit par un azoture d'ammonium ou d'un métal pharmaceutiquement acceptable, soit par un composé azoté comportant un motif N-N dans lequel les N sont reliés à des atomes d'hydrogène et/ou à des groupements organiques monovalents par l'intermédiaire d'un atome de carbone, ou dans lequel l'un des N est relié à l'atome de carbone d'un groupement organique bivalent par l'intermediai- re d'une double liaison et l'autre N est relié à des atomes d'hydrogène et/ou à des groupements organiques monovalents par l'intermédiaire d'un atome de carbone ;;
- un deuxième flacon comprenant un agent réducteur constitué, soit du dithionite d'ammonium ou d'un métal pharmaceutiquement acceptable, soit par de l'étain (II) présent sous forme ionique, soit par une phosphine ou polyphosphine, aliphatique ou aromatique, substituée ou non substituée ; et
- un troisième flacon comprenant un dithiocarbamate de formule
dans laquelle R1 représente le groupe éthyle ou le groupe éthoxy, R2 est un ion de métal pharmaceutiquement acceptable de valence n ou H+ avec n=1, ou NH4+ avec n=1, et p est égal à 0 ou est un nombre allant de 1 à 5.
L'invention a encore pour objet une composition radiopharmaceutique constituée par une suspension de cellules marquées par un complexe de 99m-Tc de formule :
De préférence, dans cette composition, les cellules sont des leucocytes.
L'invention concerne également une composition radiopharmaceutique constituée par une suspension de granulocytes marqués par un complexe de 99m-Tc de formule
(Tc = N) L1 L2 (I) dans laque île L1 et L2 qui peuvent être identiques ou différents, répondent à la formule
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy.
(Tc = N) L1 L2 (I) dans laque île L1 et L2 qui peuvent être identiques ou différents, répondent à la formule
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy.
D'autres caractéristiques et avantages de l'invention apparaîtront mieux à la lecture des exemples suivants donnés bien entendu à titre illustratif et non limitatif.
ExempLe 1: Préparation du complexe nitruro bis(Néthoxy N-éthyldithiocarbamato) technétium (99mTc) (TcN-NOET).
a) Préparation du produit intermédiaire.
Dans un flacon type pénicilline, on introduit 0,5ml d'une solution contenant 0,8-10-2mol/l (lmg/ml) de S-méthyl, N-méthyl dithiocarbazate dans l'eau, puis 0,5ml d'une solution à 2.10-2mol/l (10mg/ml) de triphényl phosphine tri sulfonée dans l'eau, et 0,1ml d'acide chlorhydrique 1N.
On ajoute ensuite 0,5 à 5ml d'une solution de pertechnétate de sodium (99mTc) ayant une activité de 37MBq à 3,7GBq (1 à 100mCi) et on effectue la réaction à 800C pendant 30min ou à 1000C pendant 15min.
b) Préparation du complexe final.
Au contenu du flacon obtenu dans l'étape a), on ajoute 0,lml d'une solution de NaOH 1N et 0,5ml d'une solution aqueuse contenant 0,1mol/l (22mg/ml) de (N-éthoxy, N-éthyl) dithiocarbamate de sodium.
Après 30min de réaction à la température ambiante, on obtient un produit radiopharmaceutique contenant le complexe 99mTcN-NOET.
Exemple 2 : Préparation du complexe 99 m ICN-NOET.
a) Préparation du produit intermédiaire.
Dans un flacon type pénicilline, on introduit 0,5ml d'une solution contenant 0,8.10-2mol/l (1mg/ml) de S-méthyl, N-méthyl dithiocarbazate dans l'eau, 0,5ml d'une solution contenant 3.10-2mol/l (îOmg/ml) d'acide propane 1,2-diamino
N,N,N',N' tétracétique dans l'eau, 0,1ml d'une solution contenant 2,2.10-3mol/l (0,5mg/ml) de chlorure stanneux dihydraté dans l'acide chlorhydrique 0,2 N et 1ml de tampon phosphate 0,2 M (pH7,8).
N,N,N',N' tétracétique dans l'eau, 0,1ml d'une solution contenant 2,2.10-3mol/l (0,5mg/ml) de chlorure stanneux dihydraté dans l'acide chlorhydrique 0,2 N et 1ml de tampon phosphate 0,2 M (pH7,8).
On ajoute ensuite 0,5 à 5ml d'une solution de pertechnétate de sodium (99mTc) ayant une activité de 37MBq à 3,7GBq (1 à 100mCi) et on effectue la réaction à 800C pendant 30min ou à 1000C pendant 15min.
b) Préparation du complexe final.
Au contenu du flacon obtenu dans l'étape a), on ajoute 0,5ml d'une solution aqueuse contenant 0,1mol/l (22mg/ml) de (N-éthoxy, N-éthyl) dithiocarbamate de sodium.
Après 30 minutes de réaction à la température ambiante, on obtient un produit radiopharmaceutique contenant 99mTcN-NOET.
Exemple 3 : Préparation du complexe 99mTcN-NOET.
a) Préparation du produit intermédiaire.
Dans un flacon type pénicilline, on introduit 0,5ml d'une solution contenant 0,14mol/l (20mg/ ml) de succinyl dihydrazide dans l'eau, 0,5ml d'une solution contenant 3.10-2mol/l (10mg/ml) d'acide propane 1,2-diamino N,N,N',N' tétracétique dans l'eau, 0,1ml d'une solution contenant 2,2.10~3mol/l (0,5mg/mU) de chlorure stanneux dihydraté dans l'acide chlorhydrique 0,2 N et 1ml de tampon phosphate 0,2 M (pH 7,8).
On ajoute ensuite 0,5 à 5ml d'une solution de pertechnétate de sodium (99mTc) ayant une activité de 37 MBq à 3,7 GBq (1 à 100mCi) et on effectue la réaction à la température ambiante pendant 15min.
b) Préparation du complexe final.
Au contenu du flacon obtenu dans l'étape a), on ajoute 0,5ml de solution aqueuse de (N-éthoxy,
N-éthyl) dithiocarbamate de sodium de formule
N-éthyl) dithiocarbamate de sodium de formule
Après 30 minutes de réaction à la température ambiante, on obtient un produit radiopharmaceutique contenant le complexe 99mTcN-NoET.
ExempLe 4 : Préparation du complexe nitruro bis(N,N diéthyldithiocarbamato) technétium (99mTcN-DEDC).
a) Préparation du produit intermédiaire.
On suit le même mode opératoire que dans l'exemple 1, 2 ou 3 pour préparer le produit intermédiaire en utilisant les mêmes réactifs et les mêmes conditions opératoires.
b) Préparation du complexe final.
Au contenu du flacon obtenu dans l'étape a), on ajoute 0,5ml d'une solution aqueuse contenant 0,1mol/l (22mg/ml) de diéthyldithiocarbamate de sodium tri hydraté de formule :
On effectue la réaction pendant 60min à la température ambiante et on obtient ainsi un produit radiopharmaceutique contenant le complexe
TcN-DEDC.
TcN-DEDC.
Exemple comparatif 1 : Préparation du complexe nitruro-bis (N-éthyl, N-(2-méthoxyéthyl) dithiocarbamato) 99mTc (TcN-EMEC).
On suit le même mode opératoire que dans l'exemple 4, sauf que l'on utilise dans la deuxième étape 0,5ml d'une solution aqueuse contenant 0,1mol/l (20mg/ml) de [N-éthyl, N-(2-methoxyéthyl)]dithiocarba- mate de sodium de formule
On obtient ainsi un produit radiopharmaceutique contenant le complexe TcN-EMEC.
Exemple coiparatif 2 : Préparation du complexe nitruro-bis(N,N,di-n-butYldithiocarbamate)99mTc (TcN-DBDC).
On suit le même mode opératoire que dans l'exemple 4, sauf que l'on utilise dans la dernière étape 0,5ml d'une solution aqueuse contenant 0,1mol/l (23mg/ml) de di(n-but-yl)dithiocarbamate de sodium.
On obtient ainsi un produit radiopharmaceutique contenant le complexe TcN-DBDC.
Exemple comparatif 3 : Préparation du complexe nitruro-bis(N-pipéridinodithiocarbamate)99mTc(TcN
PDC).
PDC).
On suit le même mode opératoire que dans l'exemple 4, sauf que l'on utilise dans la dernière étape 0,5ml d'une solution aqueuse contenant 0,1mol/l (18mg/ml) de 1-piperidine dithiocarbamate de sodium de formule :
On obtient ainsi un produit radiopharmaceutique contenant le complexe TcN-PDC.
ExempLe 5 : Marquage de granulocytes.
Dans cet exemple, on utilise le produit radiopharmaceutique de l'exemple 1 et le produit radiopharmaceutique de l'exemple 4 pour marquer des granulocytes après les avoir séparés d'un échantillon de sang humain d'un volontaire sain.
On prélève 50ml de sang sur de l'acide citrique dextrose (ACD) et on les laisse sédimenter par simple effet de la gravité après addition de 10 à 15ml HAES.
On dépose ensuite le surnageant, c'està-dire levplasma riche en cellules, sur du Lymphoprep et on le centrifuge à 2009 pendant 10min. On obtient ainsi environ 9.107 cellules.
On réalise le marquage sur 2.107 cellules en préparant une suspension de ces cellules dans 3 à 6ml de milieu RPMI et on y ajoute le produit radiopharmaceutique préparé dans l'exemple 1, puis on laisse 10 à 15min sous agitation lente à la température ambiante.
On sépare ensuite les cellules par centrifugation à 1509, on détermine leur activité puis on les lave 2h après avec une solution de RPMI et on détermine le pourcentage d'activité relarguée par les cellules.
On effectue des tests de viabilité (chimiotactisme et chimioluminescence) sur les cellules marquées.
Les résultats obtenus sont donnés dans le tableau 1 annexé.
Sur un autre lot de 2.107 cellules obtenues à partir du même échantillon de sang, on réalise un marquage avec le produit radiopharmaceutique de l'exemple 4, en utilisant également 2,2.107 cellules.
En fin d'opération, on détermine également le pourcentage d'activité incorporé dans les cellules, le pourcentage d'activité relarguée deux heures après le marquage ainsi que la viabilité.
Exemples 6 à 8 : Marquage de granulocytes.
Dans ces exemples, on suit le même mode opératoire que dans l'exemple 5 pour marquer à partir d'un même échantillon de sang humain des granulocytes, soit par le produit radiopharmaceutique de l'exemple 1, soit par les produits radiopharmaceutiques obtenus dans les exemples comparatifs 1, 2, et 3.
Les quantités de cellules utilisées dans chaque essai ainsi que les résultats obtenus sont donnés dans le tableau 1.
Dans ce tableau, on a indiqué également les résultats donnés dans les publications pour le produit radiopharmaceutique Tc-HMPAO de l'art antérieur.
Au vu du tableau 1, on remarque que les deux produits radiopharmaceutiques de l'invention donnent de très bons résultats puisque le pourcentage d'activité incorporée dans les cellules varie de 85 à 94% et que l'activité relarguée 2h après le marquage est très faible.
En revanche, lorsqu'on utilise les produits radiopharmaceutiques des exemples comparatifs 1 à 3, les résultats sont très inférieurs, notamment dans le cas de l'exemple comparatif 2 où le pourcentage d'activité incorporée n'est que de 17%, alors que selon la publication Isotopenpraxis 26 (1990), 3, p. 107-108, ce devrait être le meilleur complexe.
Les produits radiopharmaceutiques de l'invention donnent également de meilleurs résultats que le Tc-HMPAO. De plus, on peut noter que le marquage des cellules avec le complexe Tc-HMPAO nécessite une quantité 10 fois plus grande de cellules.
Exemple 9 : Marquage de leucocytes dans le sang total.
Dans cet exemple, on prélève 25 à 30ml de sang total et on y ajoute le produit
radiopharmaceutique obtenu dans l'exemple 2, en quantité telle qu'on ait une activité de 185 à
370MBq (5 à 10moi). Après lOmin d'incubation, on
centrifuge l'échantillon de sang pendant lOmin à 4009, puis on lave le culot cellulaire avec une
solution RPMI et on centrifuge à nouveau. On sépare ensuite les cellules sur Polymorphprep et on
détermine la radioactivité incorporée dans les
différentes fractions cellulaires correspondant
aux leucocytes et aux hématies.
radiopharmaceutique obtenu dans l'exemple 2, en quantité telle qu'on ait une activité de 185 à
370MBq (5 à 10moi). Après lOmin d'incubation, on
centrifuge l'échantillon de sang pendant lOmin à 4009, puis on lave le culot cellulaire avec une
solution RPMI et on centrifuge à nouveau. On sépare ensuite les cellules sur Polymorphprep et on
détermine la radioactivité incorporée dans les
différentes fractions cellulaires correspondant
aux leucocytes et aux hématies.
Les résultats sont reportés dans le tableau
2.
2.
Sur 4 à 5ml d'un échantillon de sang total de même origine que celui utilisé précédemment, on réalise le marquage au moyen du produit radiopharmaceutique de l'exemple 4 en utilisant la même activité et les mêmes durées d'incubation, puis on sépare les cellules comme précédemment et on
détermine le pourcentage d'activité incorporée
dans le culot cellulaire et le pourcentage d'activité
incorporée dans les leucocytes et les hématies.
détermine le pourcentage d'activité incorporée
dans le culot cellulaire et le pourcentage d'activité
incorporée dans les leucocytes et les hématies.
Les résultats sont également donnés dans
le tableau 2.
le tableau 2.
ExempLes 10 à 12 : Marquage des leucocytes dans
le sang total.
le sang total.
On suit le même mode opératoire que dans
l'exemple 9 pour réaliser un marquage du sang total
dans les mêmes conditions au moyen du produit radio
pharmaceutique obtenu dans l'exemple 2 et de l'un des produits radiopharmaceutiques obtenus dans les exemples comparatifs 1 à 3.
l'exemple 9 pour réaliser un marquage du sang total
dans les mêmes conditions au moyen du produit radio
pharmaceutique obtenu dans l'exemple 2 et de l'un des produits radiopharmaceutiques obtenus dans les exemples comparatifs 1 à 3.
Les résultats obtenus sont donnés dans le tableau 2.
Au vu de ces résultats, on remarque que les produits radiopharmaceutiques de l'invention manifestent des propriétés de marquage des leucocytes supérieures à celles des produits radiopharmaceutiques des exemples comparatifs 1 à 3 concernant des complexes analogues.
Ainsi, le choix conformément à l'invention des complexes TcN-NOET et TcN-DEDC permet d'atteindre de meilleurs résultats.
<SEP> Nombre <SEP> % <SEP> % <SEP> activité <SEP> Viabilité <SEP> Coloration
<tb> Ex. <SEP> Produit <SEP> de <SEP> activité <SEP> re-Larguée <SEP> chimiotactisme <SEP> bleu <SEP> tripan <SEP> cellules <SEP> incorporée <SEP> 2h <SEP> après <SEP> phagocytose <SEP> (%cellules
<tb> <SEP> dans <SEP> les <SEP> marquage <SEP> mortes)
<tb> <SEP> cellules
<tb> 5 <SEP> Ex <SEP> 1
<tb> <SEP> TcN-NOET <SEP> 2,2x107 <SEP> 85 <SEP> 6,2 <SEP> qui <SEP> < <SEP> 1
<tb> <SEP> Ex <SEP> 4 <SEP> 2,2x107 <SEP> 88 <SEP> 4,5 <SEP> qui <SEP> < <SEP> 1
<tb> <SEP> TcN-DEDT
<tb> 6 <SEP> Ex <SEP> 1 <SEP> 2,3x107 <SEP> 91 <SEP> 2,5 <SEP> qui <SEP> 2
<tb> <SEP> TcN-NOET
<tb> <SEP> Ex <SEP> comparatif <SEP> 1 <SEP> 2,3x107 <SEP> 45 <SEP> 35 <SEP> qui <SEP> 15
<tb> <SEP> TcN-EMEC
<tb> 7 <SEP> Ex1 <SEP> 2,2x107 <SEP> 94 <SEP> 5 <SEP> qui <SEP> < <SEP> 1
<tb> <SEP> TcN-NOET
<tb> <SEP> Ex <SEP> comparatif <SEP> 2 <SEP> 2,2x107 <SEP> 17 <SEP> 12 <SEP> qui <SEP> 1
<tb> <SEP> TcN-DBDC
<tb> 8 <SEP> Ex <SEP> comparatif <SEP> 3 <SEP> 3x107 <SEP> 53 <SEP> 26 <SEP> qui <SEP> 30
<tb> <SEP> TcN-PDC
<tb> <SEP> Ex <SEP> 1 <SEP> - <SEP> TcN-NOET <SEP> 3x107 <SEP> 93 <SEP> 3 <SEP> qui <SEP> 1
<tb> <SEP> Tc-HNPAO <SEP> 20x107 <SEP> 55#13 <SEP> 2) <SEP> 18 <SEP> 1)
<tb> <SEP> 44#13 <SEP> 1) <SEP> 10 <SEP> 2)
<tb> <SEP> 23x107 <SEP> 41-79 <SEP> 3) <SEP> 15 <SEP> 3)
<tb> 1) Becker W et al dans Nucl. Med. Comm. 9,435-447, 1988, 2) Danpure H.J. et al dans NuCl. Med. Comm. 9,465-475, 1988, 3) Kelbaek H. et al Eur. J. Nucl. Med. (1988). 14,621-623 TABLEAU 2
<tb> Ex. <SEP> Produit <SEP> de <SEP> activité <SEP> re-Larguée <SEP> chimiotactisme <SEP> bleu <SEP> tripan <SEP> cellules <SEP> incorporée <SEP> 2h <SEP> après <SEP> phagocytose <SEP> (%cellules
<tb> <SEP> dans <SEP> les <SEP> marquage <SEP> mortes)
<tb> <SEP> cellules
<tb> 5 <SEP> Ex <SEP> 1
<tb> <SEP> TcN-NOET <SEP> 2,2x107 <SEP> 85 <SEP> 6,2 <SEP> qui <SEP> < <SEP> 1
<tb> <SEP> Ex <SEP> 4 <SEP> 2,2x107 <SEP> 88 <SEP> 4,5 <SEP> qui <SEP> < <SEP> 1
<tb> <SEP> TcN-DEDT
<tb> 6 <SEP> Ex <SEP> 1 <SEP> 2,3x107 <SEP> 91 <SEP> 2,5 <SEP> qui <SEP> 2
<tb> <SEP> TcN-NOET
<tb> <SEP> Ex <SEP> comparatif <SEP> 1 <SEP> 2,3x107 <SEP> 45 <SEP> 35 <SEP> qui <SEP> 15
<tb> <SEP> TcN-EMEC
<tb> 7 <SEP> Ex1 <SEP> 2,2x107 <SEP> 94 <SEP> 5 <SEP> qui <SEP> < <SEP> 1
<tb> <SEP> TcN-NOET
<tb> <SEP> Ex <SEP> comparatif <SEP> 2 <SEP> 2,2x107 <SEP> 17 <SEP> 12 <SEP> qui <SEP> 1
<tb> <SEP> TcN-DBDC
<tb> 8 <SEP> Ex <SEP> comparatif <SEP> 3 <SEP> 3x107 <SEP> 53 <SEP> 26 <SEP> qui <SEP> 30
<tb> <SEP> TcN-PDC
<tb> <SEP> Ex <SEP> 1 <SEP> - <SEP> TcN-NOET <SEP> 3x107 <SEP> 93 <SEP> 3 <SEP> qui <SEP> 1
<tb> <SEP> Tc-HNPAO <SEP> 20x107 <SEP> 55#13 <SEP> 2) <SEP> 18 <SEP> 1)
<tb> <SEP> 44#13 <SEP> 1) <SEP> 10 <SEP> 2)
<tb> <SEP> 23x107 <SEP> 41-79 <SEP> 3) <SEP> 15 <SEP> 3)
<tb> 1) Becker W et al dans Nucl. Med. Comm. 9,435-447, 1988, 2) Danpure H.J. et al dans NuCl. Med. Comm. 9,465-475, 1988, 3) Kelbaek H. et al Eur. J. Nucl. Med. (1988). 14,621-623 TABLEAU 2
Ex. <SEP> Produit <SEP> % <SEP> activité <SEP> incorporée <SEP> % <SEP> activité <SEP> après
<tb> <SEP> dans <SEP> le <SEP> culot <SEP> séparation
<tb> <SEP> Cellulaire <SEP> G.B. <SEP> = <SEP> G.R. <SEP> =
<tb> <SEP> leucocytes <SEP> hématies
<tb> 9 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 49 <SEP> 70 <SEP> 20
<tb> <SEP> Ex <SEP> 4 <SEP> - <SEP> TcN <SEP> - <SEP> DEDC <SEP> 60 <SEP> 29 <SEP> 51
<tb> 10 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 30 <SEP> 42 <SEP> 33
<tb> <SEP> Ex <SEP> comparatif <SEP> 1 <SEP> 21 <SEP> 20 <SEP> 40
<tb> <SEP> TcN-EMEC
<tb> 11 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 30 <SEP> 43 <SEP> 31
<tb> <SEP> Ex <SEP> comparatif <SEP> 2 <SEP> 19 <SEP> 29 <SEP> 24
<tb> <SEP> TcN-DBDC
<tb> 12 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 26 <SEP> 40 <SEP> 36
<tb> <SEP> Ex <SEP> comparatif <SEP> 3 <SEP> 13 <SEP> 15 <SEP> 39
<tb> <SEP> EcN-PDC
<tb>
<tb> <SEP> dans <SEP> le <SEP> culot <SEP> séparation
<tb> <SEP> Cellulaire <SEP> G.B. <SEP> = <SEP> G.R. <SEP> =
<tb> <SEP> leucocytes <SEP> hématies
<tb> 9 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 49 <SEP> 70 <SEP> 20
<tb> <SEP> Ex <SEP> 4 <SEP> - <SEP> TcN <SEP> - <SEP> DEDC <SEP> 60 <SEP> 29 <SEP> 51
<tb> 10 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 30 <SEP> 42 <SEP> 33
<tb> <SEP> Ex <SEP> comparatif <SEP> 1 <SEP> 21 <SEP> 20 <SEP> 40
<tb> <SEP> TcN-EMEC
<tb> 11 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 30 <SEP> 43 <SEP> 31
<tb> <SEP> Ex <SEP> comparatif <SEP> 2 <SEP> 19 <SEP> 29 <SEP> 24
<tb> <SEP> TcN-DBDC
<tb> 12 <SEP> Ex <SEP> 2 <SEP> - <SEP> TcN-NOET <SEP> 26 <SEP> 40 <SEP> 36
<tb> <SEP> Ex <SEP> comparatif <SEP> 3 <SEP> 13 <SEP> 15 <SEP> 39
<tb> <SEP> EcN-PDC
<tb>
Claims (15)
1. Procédé de marquage radioactif de cellules, caractérisé en ce qu'il consiste à ajouter à une suspension de ces cellules un produit radiopharmaceutique comprenant un complexe de technétium 99m de formule :
CTc E N) L1 L2 (I) dans laquelle L1 et L2 qui peuvent être identiques ou différents, répondent à la formule
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy, à condition que l'un au moins des L1 et
L2 réponde à la formule :
2. Procédé selon la revendication 1, caractérisé en ce que L1 et L2 représentent
NH4+ avec n=1, et p est égal à O ou est un nombre allant de 1 à 5.
dans laquelle R1 représente le groupe éthyle ou le groupe éthoxy, R2 est un ion de métal pharmaceutiquement acceptable de valence n, H+ avec n=1, ou
et 2) la réaction du produit intermédiaire obtenu dans la première étape avec au moins un composé de formule :
que ou aromatique, substituée ou non substituée ;
soit par une phosphine ou polyphosphine, aliphati
(II) présent sous forme ionique dans la solution,
ceutiquement acceptable, soit par de l'étain
par du dithionite d'ammonium ou d'un métal pharma
b) un agent réducteur constitué, soit
l'intermédiaire d'un atome de carbone, et
des groupements organiques monovalents par
N est relié à des atomes d'hydrogène et/ou à
l'intermédiaire d'une double liaison et l'autre
d'un groupement organique bivalent par
lequel L'un- des N est relié à l'atome de carbone
l'intermédiaire d'un atome de carbone, ou dans
à des groupements organiques monovalents par
les N sont reliés à des atomes d'hydrogène et/ou
azoté comportant un motif N-N dans lequel
pharmaceutiquement acceptable, soit par un composé
soit par un azoture d'ammonium ou d'un métal
a) un premier ligand azoté constitué
dans laquelle R1 est le groupe éthyle ou le groupe éthoxy, le produit radiopharmaceutique étant obtenu par un procédé comprenant 1) la réaction d'un composé oxygéné de 99mTc avec
(Tc E N) L1 L2 (I) dans laquelle L1 et L2 qui peuvent être identiques ou différents, répondent à la formule ::
3.Procédé de marquage radioactif de cellules, caractérisé en ce qu'il consiste à ajouter à une suspension de ces cellules un produit radiopharmaceutique comprenant un complexe de technétium 99m de formule
4. Procédé selon la revendication 3, caractérisé en ce que le ligand azoté est le Sméthyl, N-méthyl dithiocarbazate, et l'agent réducteur est la triphénylphosphine trisulfonée.
5. Procédé selon la revendication 3, caractérisé en ce que le ligand azoté est le Sméthyl, N-méthyl dithiocarbazate, et l'agent réducteur est le chlorure stanneux dihydraté introduit avec de l'acide propane-1,2-diamino-N,N,N',N'tétracétique.
6. Procédé selon la revendication 3, caractérisé en ce que le ligand azoté est le succinyl dihydrazide, et l'agent réducteur est le chlorure stanneux du hydraté introduit avec de l'acide propane 1 ,2-di amino-N,N,N' ,N'-tét racéti que.
9. Procédé selon l'une quelconque des revendications 1 à 8, caractérisé en ce que la suspension de cellules est une suspension de leucocytes ou de granulocytes.
10. Procédé selon l'une quelconque des revendications 1 à 8, caractérisé en ce que la suspension de cellules est un échantillon de sang total.
12. Composition selon la revendication 11, caractérisée en ce que les cellules sont des leucocytes.
14. Trousse pour le marquage radioactif de cellules, caractérisée en ce qu'elle comprend
- un premier flacon contenant un ligand azoté constitué soit soit par un azoture d'ammonium ou d'un métal pharmaceutiquement acceptable, soit par un composé azoté comportant un motif N-N dans lequel les N sont reliés à des atomes d'hydrogè- ne et/ou à des groupements organiques monovalents par l'intermédiaire d'un atome de carbone, ou dans lequel l'un des N est relié à l'atome de carbone d'un groupement organique bivalent par l'intermédiaire d'une double liaison et l'autre N est relié à des atomes d'hydrogène et/ou à des groupements organiques monovalents par l'intermédiaire d'un atome de carbone ; ;
- un deuxième flacon comprenant un agent réducteur constitué, soit du dithionite d'ammonium ou d'un métal pharmaceutiquement acceptable, soit par de l'étain (II) présent sous forme ionique, soit par une phosphine ou polyphosphine, aliphatique ou aromatique, substituée ou non substituée ; et
- un troisième flacon comprenant un dithiocarbamate de formule
dans laquelle R1 représente le groupe éthyle ou le groupe éthoxy, R2 est un ion de métal pharmaceutiquement acceptable de valence n ou H+ avec n=1, ou NH4+ avec n=1, et p est égal à O ou est un nombre allant de 1 à 5.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9213963A FR2698272B1 (fr) | 1992-11-20 | 1992-11-20 | Procédé de marquage cellulaire au moyen de complexes nitruro-bis (dithiocarbamato)Tc-99m et trousse pour la mise en Óoeuvre de ce procédé. |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9213963A FR2698272B1 (fr) | 1992-11-20 | 1992-11-20 | Procédé de marquage cellulaire au moyen de complexes nitruro-bis (dithiocarbamato)Tc-99m et trousse pour la mise en Óoeuvre de ce procédé. |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2698272A1 true FR2698272A1 (fr) | 1994-05-27 |
| FR2698272B1 FR2698272B1 (fr) | 1994-12-30 |
Family
ID=9435742
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR9213963A Expired - Fee Related FR2698272B1 (fr) | 1992-11-20 | 1992-11-20 | Procédé de marquage cellulaire au moyen de complexes nitruro-bis (dithiocarbamato)Tc-99m et trousse pour la mise en Óoeuvre de ce procédé. |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2698272B1 (fr) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2736834A1 (fr) * | 1995-07-17 | 1997-01-24 | Cis Bio Int | Produits radiopharmaceutiques a tropisme cardiaque comportant un complexe nitruro d'un metal de transition et ayant une clairance myocardique rapide |
| WO1997025074A2 (fr) * | 1996-01-12 | 1997-07-17 | Redcell Canada, Inc. | Ancres de proteines seriques et cellulaires destinees a l'imagerie diagnostique |
| US5750088A (en) * | 1993-03-30 | 1998-05-12 | The Dupont Merck Pharmaceutical Company | Stable hydrazones linked to a peptide moiety as reagents for the preparation of radiopharmaceuticals |
| US6469146B1 (en) | 2000-05-23 | 2002-10-22 | Cis Bio International | Radiopharmaceutical products suitable for the selective labeling of lymphocytes, and their preparation |
| FR2832408A1 (fr) * | 2001-11-20 | 2003-05-23 | Schering Ag | Complexes de technetium ou de rhenium, produits radiopharmaceutiques les contenant et leur preparation |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1990006137A1 (fr) * | 1988-11-25 | 1990-06-14 | Cis Bio International | Produit radiopharmaceutique ayant notamment un tropisme cardiaque comportant un complexe nitruro d'un metal de transition, et son procede de preparation |
| WO1992010214A1 (fr) * | 1990-12-12 | 1992-06-25 | Mallinckrodt Medical, Inc. | Procede de marquage isotopique de cellules du sang et kit pour ce faire |
-
1992
- 1992-11-20 FR FR9213963A patent/FR2698272B1/fr not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1990006137A1 (fr) * | 1988-11-25 | 1990-06-14 | Cis Bio International | Produit radiopharmaceutique ayant notamment un tropisme cardiaque comportant un complexe nitruro d'un metal de transition, et son procede de preparation |
| WO1992010214A1 (fr) * | 1990-12-12 | 1992-06-25 | Mallinckrodt Medical, Inc. | Procede de marquage isotopique de cellules du sang et kit pour ce faire |
Non-Patent Citations (5)
| Title |
|---|
| CHEMICAL ABSTRACTS, vol. 106, no. 13 Columbus, Ohio, US; abstract no. 98660v, * |
| CHEMICAL ABSTRACTS, vol. 107, no. 11 Columbus, Ohio, US; abstract no. 92985d, * |
| CHEMICAL ABSTRACTS, vol. 109, no. 11 Columbus, Ohio, US; abstract no. 88903z, * |
| CHEMICAL ABSTRACTS, vol. 112, no. 25 Columbus, Ohio, US; abstract no. 231908z, * |
| CHEMICAL ABSTRACTS, vol. 114, no. 19 Columbus, Ohio, US; abstract no. 181436n, * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5750088A (en) * | 1993-03-30 | 1998-05-12 | The Dupont Merck Pharmaceutical Company | Stable hydrazones linked to a peptide moiety as reagents for the preparation of radiopharmaceuticals |
| FR2736834A1 (fr) * | 1995-07-17 | 1997-01-24 | Cis Bio Int | Produits radiopharmaceutiques a tropisme cardiaque comportant un complexe nitruro d'un metal de transition et ayant une clairance myocardique rapide |
| WO1997003705A1 (fr) * | 1995-07-17 | 1997-02-06 | Cis Bio International | Produits radiopharmaceutiques a tropisme cardiaque comportant un complexe nitruro d'un metal de transition et ayant une clairance myocardique rapide |
| WO1997025074A2 (fr) * | 1996-01-12 | 1997-07-17 | Redcell Canada, Inc. | Ancres de proteines seriques et cellulaires destinees a l'imagerie diagnostique |
| WO1997025074A3 (fr) * | 1996-01-12 | 1997-11-13 | Redcell Inc | Ancres de proteines seriques et cellulaires destinees a l'imagerie diagnostique |
| US6469146B1 (en) | 2000-05-23 | 2002-10-22 | Cis Bio International | Radiopharmaceutical products suitable for the selective labeling of lymphocytes, and their preparation |
| FR2832408A1 (fr) * | 2001-11-20 | 2003-05-23 | Schering Ag | Complexes de technetium ou de rhenium, produits radiopharmaceutiques les contenant et leur preparation |
| WO2003044031A1 (fr) * | 2001-11-20 | 2003-05-30 | Schering Aktiengesellschaft | Complexes de technetium ou de rhenium, produits radiopharmaceutiques les contenant |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2698272B1 (fr) | 1994-12-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0403524B1 (fr) | Preparation de complexes nitruro utilisables comme produits radiopharmaceutiques | |
| Linder et al. | TcO (PnAO-1-(2-nitroimidazole))[BMS-181321], a new technetium-containing nitroimidazole complex for imaging hypoxia: synthesis, characterization, and xanthine oxidase-catalyzed reduction | |
| FR2515046A1 (fr) | Anticorps monoclonaux marques par un radionucleide et leur application a la visualisation d'une tumeur | |
| EP0537242B1 (fr) | Procede de preparation de complexes nitruro de metaux de transition | |
| EP0445190B1 (fr) | Produit radiopharmaceutique ayant notamment un tropisme cardiaque comportant un complexe nitruro d'un metal de transition, et son procede de preparation | |
| FR2698272A1 (fr) | Procédé de marquage cellulaire au moyen de complexes nitruro-bis (dithiocarbamato)Tc-99m et trousse pour la mise en Óoeuvre de ce procédé. | |
| CH645190A5 (fr) | Procede et ensemble pour le marquage des globules rouges du sang avec du technetium-99. | |
| KR850001871B1 (ko) | 비-방사성 담체조성물 및 이를 사용한 방사성 진단제의 제조방법 | |
| CA1324317C (fr) | Produits radiodiagnostiques stables, mode de preparation | |
| FR2919189A1 (fr) | Nouvelles compositions a base de polyosides greffes par des composes polyamines ou polysoufres. | |
| JPH0445107B2 (fr) | ||
| Jellum et al. | Mercaptodextran, a metal-chelating and disulphide-reducing polythiol of high molecular weight | |
| EP2536438B1 (fr) | Composition pour le traitement du cancer du foie chez l'homme a base de rhenium-188 et procede de preparation d'une telle composition | |
| US4895960A (en) | Cyclo substituted propyleneamine oxime and its use as a brain imaging agent | |
| AU654663B2 (en) | Method for preparing a metal-radionuclide-labelled protein | |
| EP0839059B1 (fr) | Produits radiopharmaceutiques a tropisme cardiaque comportant un complexe nitruro d'un metal de transition et ayant une clairance myocardique rapide | |
| CA2066779A1 (fr) | Compositions a base de radionucleides therapeutiques stables, et leurs methodes de preparation | |
| FR2809401A1 (fr) | Produits radiopharmaceutiques utiles pour le marquage selectif des lymphocytes et leur preparation | |
| Srivastava et al. | Recent developments in blood cell labeling research | |
| JPH01186899A (ja) | 膜透過性を有するTc−99m単核錯体 | |
| Wu et al. | Stability of the four 2-(p-nitrobenzyl)-trans-CyDTPA 88Y complexes | |
| KR850001891B1 (ko) | 비방사성 담체 조성물 및 이를 사용한 혈액-뇌통과 방사성 진단제의 제조방법 | |
| Khaw et al. | Re: Concerning the Labeling of DTPA-Coupled Proteins with Tc-99m—Reply | |
| Srivastava et al. | Current state of the art of blood cell labeling | |
| BE853515A (fr) | Nouveaux agents radiodiagnostiques marques au technetium-99m pour l'exploration du foie et de la moelle osseuse et leur procede de preparation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ST | Notification of lapse |