FR2459800A2 - Enantiomeres du dihydro-4,5 phenyl-1 epoxy-1,4, 1h, 3 h-(1-4) oxazepino (4-3a) benzimidazole, leur procede de preparation et leur application en therapeutique - Google Patents
Enantiomeres du dihydro-4,5 phenyl-1 epoxy-1,4, 1h, 3 h-(1-4) oxazepino (4-3a) benzimidazole, leur procede de preparation et leur application en therapeutique Download PDFInfo
- Publication number
- FR2459800A2 FR2459800A2 FR7916050A FR7916050A FR2459800A2 FR 2459800 A2 FR2459800 A2 FR 2459800A2 FR 7916050 A FR7916050 A FR 7916050A FR 7916050 A FR7916050 A FR 7916050A FR 2459800 A2 FR2459800 A2 FR 2459800A2
- Authority
- FR
- France
- Prior art keywords
- sep
- formula
- enantiomers
- cpd
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- UHOVQNZJYSORNB-UHFFFAOYSA-N c1ccccc1 Chemical compound c1ccccc1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D498/18—Bridged systems
Abstract
A.ENANTIOMERES DU DIHYDRO-4,5 PHENYL-1 EPOXY-1,4 1H, 3H-1-4 OXAZEPINO 4-3A BENZIMIDAZOLE. B.CES ENANTIOMERES SONT RESPECTIVEMENT DE CONFIGURATION 1S-4R DEXTROGYRE ET 1R-4S LEVOGYRE. C.APPLICATION THERAPEUTIQUE.
Description
Le brevet principal n 73 35379 a notamment pour objet le composé de formule:
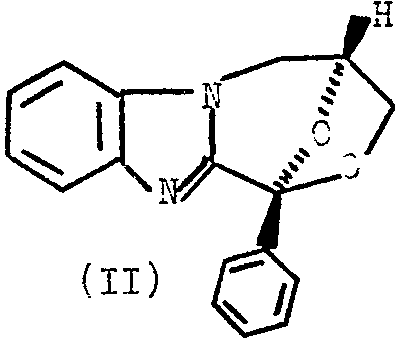
dans laquelle Y représente un noyau phényle, c'est-à-dire le dihydro -4,5 phényl-1 époxy-1,4, 1H, 311 L1-4] oxazépino [4-3a] benzimidazole connu pour ses propriétés analgésiques sous le nom d'OXAPADOL. Ce composé est en fait un mélange de deux énantiomères respectivement de formule (II) et
dans laquelle Y représente un noyau phényle, c'est-à-dire le dihydro -4,5 phényl-1 époxy-1,4, 1H, 311 L1-4] oxazépino [4-3a] benzimidazole connu pour ses propriétés analgésiques sous le nom d'OXAPADOL. Ce composé est en fait un mélange de deux énantiomères respectivement de formule (II) et
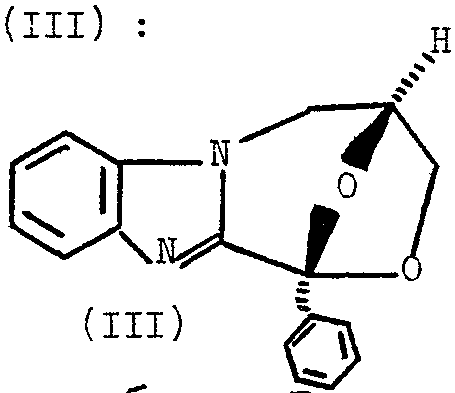
l'énantiomère de formule (II) étant de configuration L1s - 4R dextrogyre et lténan- tiomère de formule (III) étant de configuration [1R - 4S] lévogyre.
La présente demande de certificat d'addition a précisément pour objet ces deux énantiomères.
En effet, il a pour intéressant d'obtenir de manière specifique chacun de ces deux énantiomères et, l'étude pharmacologique de ces derniers chez l'animal de laboratoire a révélé que seul le composé de formule (III) et de configuration lévogyre [1R - 4S] présentait une activité analgésique vraiment importante. Cette activité a été mise en évidence par le test de la phénylbenzoquinone effectué selon le protocole de E. SIEGMUND modifié par TH. LINEE et C. GOURET et exposé dans J. Pharmacol. (Paris) 3, (4), 5 13, (1972). Les résultats ainsi obtenus avec les composés de formules (II) et (III) ainsi qu'avec l'OXA
PADOLE sont rassemblés dans le tableau ci-après.
PADOLE sont rassemblés dans le tableau ci-après.
<tb> Composé <SEP> testé <SEP> toxicité <SEP> ches <SEP> test <SEP> à <SEP> la <SEP> phénylbenzoquinone
<tb> <SEP> la <SEP> souris <SEP> Dose <SEP> administrée <SEP> Effet <SEP> à <SEP> Effet <SEP> à
<tb> <SEP> DL <SEP> 50 <SEP> 30 <SEP> minutes <SEP> 60 <SEP> minutes
<tb> <SEP> (mg/kg/p.o.) <SEP> (mg/kg/p.o.) <SEP> (%) <SEP> %
<tb> <SEP> (II) <SEP> 1800 <SEP> 100 <SEP> - <SEP> 23
<tb> <SEP> (III) <SEP> 1800 <SEP> 30 <SEP> 50
<tb> <SEP> 60 <SEP> - <SEP> 50
<tb> <SEP> OXAPADOLE <SEP> 1850 <SEP> 27 <SEP> 50
<tb> <SEP> 50 <SEP> - <SEP> 50
<tb>
Comme le montre le tableau ci-dessus, l'écart entre les doses toxiques et les doses actives permet en particulier utilisation du imposé de formule (III) en thérapeutique comme agent analgésique et notamment pour le traitement des douleurs in flaromatoires et d'origines diverses.
<tb> <SEP> la <SEP> souris <SEP> Dose <SEP> administrée <SEP> Effet <SEP> à <SEP> Effet <SEP> à
<tb> <SEP> DL <SEP> 50 <SEP> 30 <SEP> minutes <SEP> 60 <SEP> minutes
<tb> <SEP> (mg/kg/p.o.) <SEP> (mg/kg/p.o.) <SEP> (%) <SEP> %
<tb> <SEP> (II) <SEP> 1800 <SEP> 100 <SEP> - <SEP> 23
<tb> <SEP> (III) <SEP> 1800 <SEP> 30 <SEP> 50
<tb> <SEP> 60 <SEP> - <SEP> 50
<tb> <SEP> OXAPADOLE <SEP> 1850 <SEP> 27 <SEP> 50
<tb> <SEP> 50 <SEP> - <SEP> 50
<tb>
Comme le montre le tableau ci-dessus, l'écart entre les doses toxiques et les doses actives permet en particulier utilisation du imposé de formule (III) en thérapeutique comme agent analgésique et notamment pour le traitement des douleurs in flaromatoires et d'origines diverses.
La présente demande de certificat d'addition a donc également pour objet l'application thérapeutique de l'isomère de configuration [1R - 4s3 lévogyre de l'OXAPADOLE.
Il sera administré
- par voie orale sous forme de comprimes, dragées ou gélules contenant jusqu'à 250 mg de principe actif (1 à 6 par jour) ou sous forme de gouttes contenant jusqu'à 2 % de principe actif (20 à 60 gouttes, 1 à 4 fois par jour),
- par voie parentérale sous forme d'ampoules injectables contenant jusqu'à 100 mg de principe actif (1 à 3 par jour), ou
- par voie rectale sous forme de suppositoires contenant jusqu'à 250 mg de principe actif (1 à 3 par jour).
- par voie orale sous forme de comprimes, dragées ou gélules contenant jusqu'à 250 mg de principe actif (1 à 6 par jour) ou sous forme de gouttes contenant jusqu'à 2 % de principe actif (20 à 60 gouttes, 1 à 4 fois par jour),
- par voie parentérale sous forme d'ampoules injectables contenant jusqu'à 100 mg de principe actif (1 à 3 par jour), ou
- par voie rectale sous forme de suppositoires contenant jusqu'à 250 mg de principe actif (1 à 3 par jour).
Enfin, la présente demande concerne le procédé de préparation des deux énantiomères évoquées ci-dessus. Ce procédé consiste à ouvrir en milieu acide, le cycle dioxolannique du composé de formule (IV) et de configuration (R) su du composé de formule (V) et de configuration (S)
puis à cycliser les diols intermédiaires obtenus par l'aède paratoluène sulfonique en milieu solvant organique tel que le benzène.
puis à cycliser les diols intermédiaires obtenus par l'aède paratoluène sulfonique en milieu solvant organique tel que le benzène.
Les composés de formules (IV) et (V), nouveaux, sont quant à eux obtenus par condensation du benzoyl-2 benzimidazole de formule
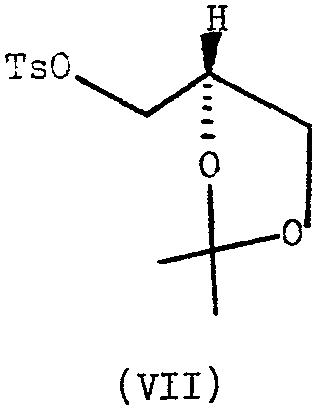
respectivement avec le tcsylate de formule (VII) et de configuration [2-S] dextro
décrits par WENDEL L. NELSON et coll. dans la revue J. Org. Chem. 42, (6), 1006, (1977).
respectivement avec le tcsylate de formule (VII) et de configuration [2-S] dextro
décrits par WENDEL L. NELSON et coll. dans la revue J. Org. Chem. 42, (6), 1006, (1977).
Les préparations suivantes sont données à titre d'exemple pour illustrer l'invention.
Préparation du dihydro-'4,5 phenyl-1 époxy-1,4, 1H, 3H, [1-4] oxazépino benzimidazole lévogyre [1R-4S]
Composé de formule (III)
1ère étape : [Diméthyl-2,2 dioxolanne [1-3] -yl méthyl-4] -1 benzoyl-2 benzimidazole
Composé de formule (V)
A une solution de 16,7 g de benzoyl-2 benzimidazole (VI) dans 100 ml de diméthyl formamide, on ajoute lentement 3,3 g d'hydrure de sodium à 55 %. On laisse en contact 20 mn, puis on porte la solution à 90 C et on ajoute en 15 mn une solution de 27,2 g de diméthyl-2,2 tosyloxy méthyl-4 dioxolanne-1,3 (VIII).On laisse en contact 80 heures à 950C, puis on dilue par de l'eau, sature avec du chlorure de sodium, extrait trois fois avec de l'acétate d'éthyle, lave la phase organique à l'eau, sèche sur sulfate de sodium, et évapore le solvant, on obtient 24 g de produit brut qui est utilisé tel quel dans le stade suivant.
Composé de formule (III)
1ère étape : [Diméthyl-2,2 dioxolanne [1-3] -yl méthyl-4] -1 benzoyl-2 benzimidazole
Composé de formule (V)
A une solution de 16,7 g de benzoyl-2 benzimidazole (VI) dans 100 ml de diméthyl formamide, on ajoute lentement 3,3 g d'hydrure de sodium à 55 %. On laisse en contact 20 mn, puis on porte la solution à 90 C et on ajoute en 15 mn une solution de 27,2 g de diméthyl-2,2 tosyloxy méthyl-4 dioxolanne-1,3 (VIII).On laisse en contact 80 heures à 950C, puis on dilue par de l'eau, sature avec du chlorure de sodium, extrait trois fois avec de l'acétate d'éthyle, lave la phase organique à l'eau, sèche sur sulfate de sodium, et évapore le solvant, on obtient 24 g de produit brut qui est utilisé tel quel dans le stade suivant.
Par le même procédé, mais par condensation des composés de formules (VI) et (VII), on obtient le composé de formule (IV) également utilisé brut dans la synthèse du composé de formule (II) correspondant.
2ème étape : Dihydro-4,5 phényl-1 époxy-1,4, 1H, 3H - [1-4] oxazépino [4-3a] benzimidazole lévogyre [1R-4S] (III)
On agite à température ambiante pendant 2 heures une solution de 21 g du composé de formule (V) obtenu g l'étape préeédente, dans 300 ml d'acide chlorhydrique 2 N, puis on neutralise par du carbonate de soude, extrait à l'acétate d'éthyle, lave la phase organique à l'eau, sèche sur sulfate de sodium et évapore le résidu.
On agite à température ambiante pendant 2 heures une solution de 21 g du composé de formule (V) obtenu g l'étape préeédente, dans 300 ml d'acide chlorhydrique 2 N, puis on neutralise par du carbonate de soude, extrait à l'acétate d'éthyle, lave la phase organique à l'eau, sèche sur sulfate de sodium et évapore le résidu.
Le résidu est dissous dans 300 ml de benzène, on ajoute 11,9 g d'acide paratoluène sulfonique et la solution est portée 3 heures au reflux en éliminant l'eau formée.
Puis la solution est concentrée, diluée par une solution aqueuse de carbonate de sodium, et on extrait à l'acétate d'éthyle. On lave la phase organique à l'eau, la sè che sur sulfate de sodium et évapore le solvant. On dissout le résidu dans 200 ml d'éther éthylique et ajoute 20 ml d'acide chlorhydrique éthanolique 5N. On filtre le précipité obtenu, le recristallise dans l'éthanol, le dissout dans de l'eau carbonatée, extrait à l'acétate d'éthyle, lave la phase organique à l'eau, sèche sur sulfate de sodium et évapore le solvant et cristallise le résidu dans l'éther éthylique. On obtient ainsi 7,2 g du produit attendu.
Rendement 41 %
Point de fusion # 100 C (avec décomposition) α]25 = - 3 59 (C = 5, éthanol)
D
Formule brute : C17 H14 N2 O2 . Poids moléculaire : 278,30 . Analyse élémentaire
Point de fusion # 100 C (avec décomposition) α]25 = - 3 59 (C = 5, éthanol)
D
Formule brute : C17 H14 N2 O2 . Poids moléculaire : 278,30 . Analyse élémentaire
<tb> <SEP> C <SEP> H <SEP> N
<tb> Calculé <SEP> (%) <SEP> 73,36 <SEP> 5,07 <SEP> 10,07
<tb> Trouvé <SEP> (%) <SEP> 73,57 <SEP> 4,86 <SEP> 10,17
<tb>
Par le meme procédé mais par mise en oeuvre du composé de formule (IV), on obtient le composé de formule (II) de configuration [1S - 4R] dextrogyre avec un rendement de 33 %.
<tb> Calculé <SEP> (%) <SEP> 73,36 <SEP> 5,07 <SEP> 10,07
<tb> Trouvé <SEP> (%) <SEP> 73,57 <SEP> 4,86 <SEP> 10,17
<tb>
Par le meme procédé mais par mise en oeuvre du composé de formule (IV), on obtient le composé de formule (II) de configuration [1S - 4R] dextrogyre avec un rendement de 33 %.
Point de fusion # 100 C (avec décomposition)
[α]25 = + 2096 (C = 5, éthanol)
Formule brute : C17 E14 N2 02
Poids moléculaire : 278,30
Analyse élémentaire
[α]25 = + 2096 (C = 5, éthanol)
Formule brute : C17 E14 N2 02
Poids moléculaire : 278,30
Analyse élémentaire
<tb> <SEP> C <SEP> H <SEP> N
<tb> Calculé <SEP> (%) <SEP> 73,36 <SEP> 5,07 <SEP> 10,07
<tb> Trouvé <SEP> (%) <SEP> 73,37 <SEP> 5,12 <SEP> 9,89
<tb>
<tb> Calculé <SEP> (%) <SEP> 73,36 <SEP> 5,07 <SEP> 10,07
<tb> Trouvé <SEP> (%) <SEP> 73,37 <SEP> 5,12 <SEP> 9,89
<tb>
Claims (7)
1. Enantiomères du composé de formule (I) selon la revendication 1 du brevet principal, formule (I) dans laquelle Y représente un noyau phényle.
4. A titre de médicement, l'enantiomère selon la revendication 3.
5. Procédé de préparation des composés selon les revendications 1,2 ou 3, caractérisé en ce qu'il consiste à ouvrir en milieu acide, le cycle dioxolannique du eomposé de formule (IV) et de configuration (R) ou du composé de formule (V)
puis à cycliser le diol intermédiaire obtenu par l'acide paratoluène sulfonique en milieu solvant organique tel que le benzène.
6. Procédé selon la revendication 5, caractérisé en ce que les composés de formules (IV) ou (V) sont obtenus par condensation du benzoyl-2 benzimidazole de formule
respectivement avec le tosylate de formule (VII) et de configuration -S) dextrogyre et le tosylate de formule (VIII) de configuration [2-R] lévogyre
7. A titre d'intermédiaires de synthèse mécessaires à la préparation des composés selon les revendications 1, 2 ou 3, les composés de formule (IV) et (V).
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR7916050A FR2459800A2 (fr) | 1979-06-22 | 1979-06-22 | Enantiomeres du dihydro-4,5 phenyl-1 epoxy-1,4, 1h, 3 h-(1-4) oxazepino (4-3a) benzimidazole, leur procede de preparation et leur application en therapeutique |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR7916050A FR2459800A2 (fr) | 1979-06-22 | 1979-06-22 | Enantiomeres du dihydro-4,5 phenyl-1 epoxy-1,4, 1h, 3 h-(1-4) oxazepino (4-3a) benzimidazole, leur procede de preparation et leur application en therapeutique |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| FR2459800A2 true FR2459800A2 (fr) | 1981-01-16 |
Family
ID=9226967
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR7916050A Pending FR2459800A2 (fr) | 1979-06-22 | 1979-06-22 | Enantiomeres du dihydro-4,5 phenyl-1 epoxy-1,4, 1h, 3 h-(1-4) oxazepino (4-3a) benzimidazole, leur procede de preparation et leur application en therapeutique |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2459800A2 (fr) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2257269A1 (fr) * | 1973-10-03 | 1975-08-08 | Delalande Sa |
-
1979
- 1979-06-22 FR FR7916050A patent/FR2459800A2/fr active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2257269A1 (fr) * | 1973-10-03 | 1975-08-08 | Delalande Sa |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2002081453A1 (fr) | Hiohydantoïnes et leur utilisation dans le traitement du diabete | |
| CH653021A5 (fr) | Derives piperidino, piperazino et homopiperazino, n-substitues par un groupe heterocyclique aromatique, leur procede de preparation et composition therapeutique les contenant. | |
| EP0103497A1 (fr) | Nouveaux dérivés de la xanthine, leur procédé de préparation et les compositions pharmaceutiques les renfermant | |
| FR2548666A1 (fr) | Nouveaux derives du nor-tropane et du granatane, leur procede de preparation et leur application en therapeutique | |
| EP0527081B1 (fr) | Nouvelles pipérazinylalcoyl-3 dihydro-2,3 4H-benzoxazine-1,3 ones-4 substituées, leur préparation et leur application en thérapeutique | |
| EP0306375A1 (fr) | Dérivés de[(pipéridinyl-4)méthyl]-2 tétrahydro-1,2,3,4 isoquinoléine, leur préparation et leur application en thérapeutique | |
| EP0351255B1 (fr) | Dérivés de [(pipéridinyl-4)méthyl]-2 tétrahydro-1,2,3,4 isoquinoléine, leur préparation et leur application en thérapeutique | |
| BE1009852A3 (fr) | Derives 1-[2(vinyl-substitues)]-3-4-dihydro-5h-2,3-benzodiazepine. | |
| FR2625678A1 (fr) | Agents anorexigenes a base de n-(quinuclidin-3-yl)-benzamides ou thiobenzamides | |
| EP0301936B1 (fr) | Dérivés de pipéridine, leur préparation et leur application en thérapeutique | |
| FR2528046A1 (fr) | Derives de l'oxazolidinone-2 n-arylee optiquement actifs, inhibiteurs specifiques et reversibles de la monoamine oxydase de type b et leur procede de preparation | |
| EP0178201B1 (fr) | Dérivés de furo [3,2-c]pyridines, leur préparation et leur application en thérapeutique | |
| EP0495709A1 (fr) | Nouveaux composés de structure aryltriazinique leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| CH616647A5 (fr) | ||
| EP0412899A2 (fr) | Dérivés d'oxazolo pyridines, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| EP0638568B1 (fr) | Pipérazines substituées, leur procédé de préparation et les compositions pharmaceutiques les contenant | |
| FR2637596A1 (fr) | Methyl-4 ((aryl-4 piperazinyl-1)-2 ethyl)-5 thiazole et ses derives, leur procede de preparation et les medicaments en contenant | |
| FR2512443A1 (fr) | Derives de phenoxy-3 propanol-2, leur preparation et leur application en therapeutique | |
| EP0099303A2 (fr) | Nouvelles benzothiopyranopyridinones et leurs sels, leur préparation, leur application comme médicaments et les compositions les renfermant | |
| CH634311A5 (fr) | Derives du benzo(d)thiazole, leur procede de preparation et leurs applications en therapeutique. | |
| FR2459800A2 (fr) | Enantiomeres du dihydro-4,5 phenyl-1 epoxy-1,4, 1h, 3 h-(1-4) oxazepino (4-3a) benzimidazole, leur procede de preparation et leur application en therapeutique | |
| FR2547822A1 (fr) | Acylpiperazinoquinazolines substituees utiles comme medicaments et procede pour leur preparation | |
| EP0105881B1 (fr) | Nouvelles cyanoguanidines, leur procede d'obtention et les compositions pharmaceutiques en renfermant | |
| EP0329563A2 (fr) | Nouveaux dérivés du benzocyclohexane et du benzocycloheptane ainsi que leurs sels, leurs procédé et intermédiaires de préparation, leur application comme médicaments et les compositions les renfermant | |
| EP0061379B1 (fr) | Dérivés de pyridine, leur préparation et leur application en thérapeutique |