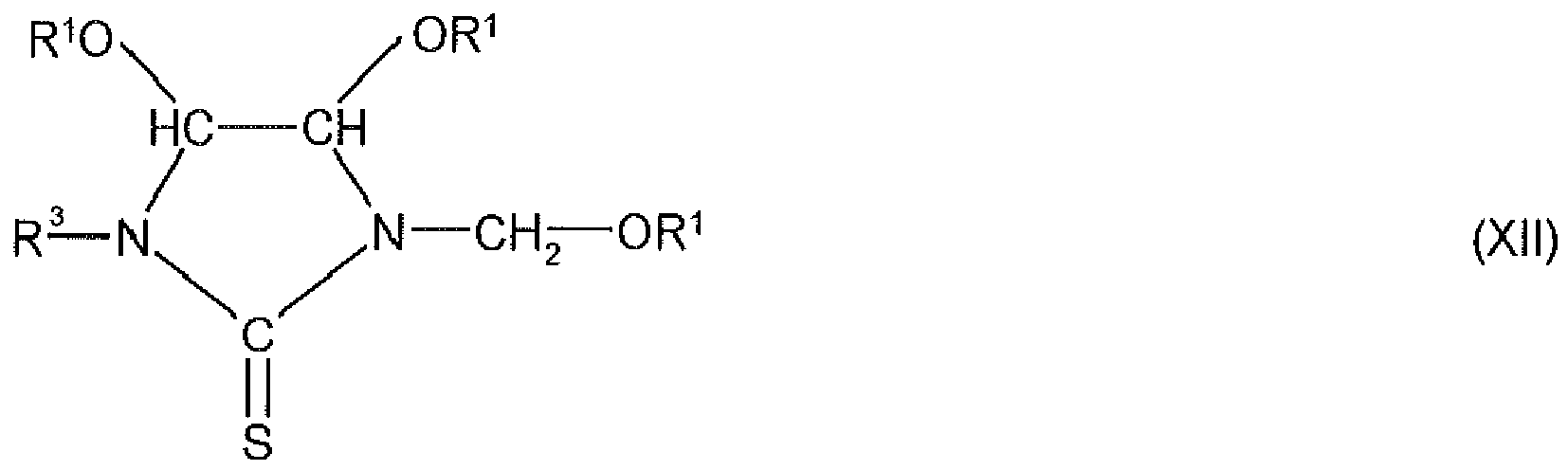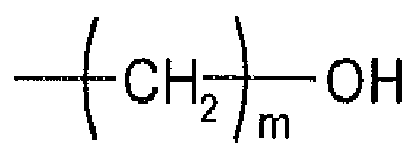EP2980308A1 - Compositions for the treatment of fibrous materials - Google Patents
Compositions for the treatment of fibrous materials Download PDFInfo
- Publication number
- EP2980308A1 EP2980308A1 EP14179257.2A EP14179257A EP2980308A1 EP 2980308 A1 EP2980308 A1 EP 2980308A1 EP 14179257 A EP14179257 A EP 14179257A EP 2980308 A1 EP2980308 A1 EP 2980308A1
- Authority
- EP
- European Patent Office
- Prior art keywords
- formula
- compound
- vii
- composition
- radical
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 95
- 239000002657 fibrous material Substances 0.000 title claims description 19
- 150000001875 compounds Chemical class 0.000 claims abstract description 84
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims abstract description 38
- 239000004753 textile Substances 0.000 claims abstract description 28
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 29
- 239000000047 product Substances 0.000 claims description 27
- 238000006266 etherification reaction Methods 0.000 claims description 22
- 238000006243 chemical reaction Methods 0.000 claims description 21
- 125000004432 carbon atom Chemical group C* 0.000 claims description 20
- 230000000694 effects Effects 0.000 claims description 17
- 150000001412 amines Chemical class 0.000 claims description 16
- 229920000742 Cotton Polymers 0.000 claims description 12
- 238000000034 method Methods 0.000 claims description 12
- 229920002678 cellulose Polymers 0.000 claims description 11
- 239000001913 cellulose Substances 0.000 claims description 11
- 229920000642 polymer Polymers 0.000 claims description 11
- 230000004888 barrier function Effects 0.000 claims description 9
- 239000007795 chemical reaction product Substances 0.000 claims description 8
- -1 dimethylsiloxy Chemical group 0.000 claims description 8
- 239000006096 absorbing agent Substances 0.000 claims description 6
- 239000002689 soil Substances 0.000 claims description 6
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 claims description 5
- 239000000835 fiber Substances 0.000 claims description 5
- 229910052717 sulfur Inorganic materials 0.000 claims description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 4
- 230000002292 Radical scavenging effect Effects 0.000 claims description 4
- 239000001257 hydrogen Substances 0.000 claims description 4
- 229910052739 hydrogen Inorganic materials 0.000 claims description 4
- 229910052757 nitrogen Inorganic materials 0.000 claims description 4
- 230000003287 optical effect Effects 0.000 claims description 4
- 229910052760 oxygen Inorganic materials 0.000 claims description 4
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical group C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 claims description 4
- 229920002994 synthetic fiber Polymers 0.000 claims description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 3
- 239000004952 Polyamide Substances 0.000 claims description 3
- 229920000297 Rayon Polymers 0.000 claims description 3
- 229910052799 carbon Inorganic materials 0.000 claims description 3
- 229920000058 polyacrylate Polymers 0.000 claims description 3
- 229920002239 polyacrylonitrile Polymers 0.000 claims description 3
- 229920002647 polyamide Polymers 0.000 claims description 3
- 229920000728 polyester Polymers 0.000 claims description 3
- 239000000126 substance Substances 0.000 claims description 3
- 239000012209 synthetic fiber Substances 0.000 claims description 3
- 210000002268 wool Anatomy 0.000 claims description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 2
- 239000004215 Carbon black (E152) Substances 0.000 claims description 2
- BRDWIEOJOWJCLU-LTGWCKQJSA-N GS-441524 Chemical compound C=1C=C2C(N)=NC=NN2C=1[C@]1(C#N)O[C@H](CO)[C@@H](O)[C@H]1O BRDWIEOJOWJCLU-LTGWCKQJSA-N 0.000 claims description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 2
- 229930195733 hydrocarbon Natural products 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims description 2
- 239000001301 oxygen Substances 0.000 claims description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 2
- 239000011593 sulfur Substances 0.000 claims description 2
- 125000003944 tolyl group Chemical group 0.000 claims description 2
- 239000004744 fabric Substances 0.000 abstract description 14
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 abstract description 11
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 abstract description 6
- 150000007974 melamines Chemical class 0.000 abstract description 5
- 239000004202 carbamide Substances 0.000 abstract description 4
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 78
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 75
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 40
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 32
- 239000000243 solution Substances 0.000 description 29
- 238000012360 testing method Methods 0.000 description 21
- LEQAOMBKQFMDFZ-UHFFFAOYSA-N glyoxal Chemical compound O=CC=O LEQAOMBKQFMDFZ-UHFFFAOYSA-N 0.000 description 16
- 239000007864 aqueous solution Substances 0.000 description 10
- 238000001816 cooling Methods 0.000 description 9
- 238000004821 distillation Methods 0.000 description 9
- 238000010998 test method Methods 0.000 description 9
- 229940015043 glyoxal Drugs 0.000 description 8
- 238000004132 cross linking Methods 0.000 description 7
- 239000004435 Oxo alcohol Substances 0.000 description 6
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 6
- QUBQYFYWUJJAAK-UHFFFAOYSA-N oxymethurea Chemical compound OCNC(=O)NCO QUBQYFYWUJJAAK-UHFFFAOYSA-N 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- JSPLKZUTYZBBKA-UHFFFAOYSA-N trioxidane Chemical compound OOO JSPLKZUTYZBBKA-UHFFFAOYSA-N 0.000 description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 235000011837 pasties Nutrition 0.000 description 5
- ZAEWYZIRRZVKGT-UHFFFAOYSA-N 1,3-dihydroxy-4,5-bis(hydroxymethyl)imidazolidin-2-one Chemical compound OCC1C(CO)N(O)C(=O)N1O ZAEWYZIRRZVKGT-UHFFFAOYSA-N 0.000 description 4
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- 235000019400 benzoyl peroxide Nutrition 0.000 description 4
- 239000003054 catalyst Substances 0.000 description 4
- 239000006185 dispersion Substances 0.000 description 4
- 229950005308 oxymethurea Drugs 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 239000004342 Benzoyl peroxide Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 239000004094 surface-active agent Substances 0.000 description 3
- 238000005690 transetherification reaction Methods 0.000 description 3
- 238000009736 wetting Methods 0.000 description 3
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- ZEYUSQVGRCPBPG-UHFFFAOYSA-N 4,5-dihydroxy-1,3-bis(hydroxymethyl)imidazolidin-2-one Chemical compound OCN1C(O)C(O)N(CO)C1=O ZEYUSQVGRCPBPG-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- LXEKPEMOWBOYRF-UHFFFAOYSA-N [2-[(1-azaniumyl-1-imino-2-methylpropan-2-yl)diazenyl]-2-methylpropanimidoyl]azanium;dichloride Chemical compound Cl.Cl.NC(=N)C(C)(C)N=NC(C)(C)C(N)=N LXEKPEMOWBOYRF-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 238000005576 amination reaction Methods 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- 230000009194 climbing Effects 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 238000004043 dyeing Methods 0.000 description 2
- 238000004945 emulsification Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000007730 finishing process Methods 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 150000003141 primary amines Chemical class 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 150000003672 ureas Chemical class 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- HCUSTBKCRHXROU-UHFFFAOYSA-N 1-[2,3-bis(2-phenylethenyl)phenoxy]-2,3-bis(2-phenylethenyl)benzene Chemical compound C=1C=CC(C=CC=2C=CC=CC=2)=C(C=CC=2C=CC=CC=2)C=1OC(C=1C=CC=2C=CC=CC=2)=CC=CC=1C=CC1=CC=CC=C1 HCUSTBKCRHXROU-UHFFFAOYSA-N 0.000 description 1
- WTFAGPBUAGFMQX-UHFFFAOYSA-N 1-[2-[2-(2-aminopropoxy)propoxy]propoxy]propan-2-amine Chemical compound CC(N)COCC(C)OCC(C)OCC(C)N WTFAGPBUAGFMQX-UHFFFAOYSA-N 0.000 description 1
- XUJLWPFSUCHPQL-UHFFFAOYSA-N 11-methyldodecan-1-ol Chemical compound CC(C)CCCCCCCCCCO XUJLWPFSUCHPQL-UHFFFAOYSA-N 0.000 description 1
- 229920003043 Cellulose fiber Polymers 0.000 description 1
- 239000004971 Cross linker Substances 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004115 Sodium Silicate Substances 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 238000005282 brightening Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000004737 colorimetric analysis Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000004064 cosurfactant Substances 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- MCPKSFINULVDNX-UHFFFAOYSA-N drometrizole Chemical compound CC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 MCPKSFINULVDNX-UHFFFAOYSA-N 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 229920001600 hydrophobic polymer Polymers 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 150000002605 large molecules Chemical class 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- DXGLGDHPHMLXJC-UHFFFAOYSA-N oxybenzone Chemical compound OC1=CC(OC)=CC=C1C(=O)C1=CC=CC=C1 DXGLGDHPHMLXJC-UHFFFAOYSA-N 0.000 description 1
- QVLMUEOXQBUPAH-UHFFFAOYSA-N p-hydroxystilbene Natural products C1=CC(O)=CC=C1C=CC1=CC=CC=C1 QVLMUEOXQBUPAH-UHFFFAOYSA-N 0.000 description 1
- 238000010979 pH adjustment Methods 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 239000000985 reactive dye Substances 0.000 description 1
- 238000007670 refining Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- NTHWMYGWWRZVTN-UHFFFAOYSA-N sodium silicate Chemical compound [Na+].[Na+].[O-][Si]([O-])=O NTHWMYGWWRZVTN-UHFFFAOYSA-N 0.000 description 1
- 229910052911 sodium silicate Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000004758 synthetic textile Substances 0.000 description 1
- 238000007669 thermal treatment Methods 0.000 description 1
- QVLMUEOXQBUPAH-VOTSOKGWSA-N trans-stilben-4-ol Chemical compound C1=CC(O)=CC=C1\C=C\C1=CC=CC=C1 QVLMUEOXQBUPAH-VOTSOKGWSA-N 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
Classifications
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/322—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing nitrogen
- D06M13/35—Heterocyclic compounds
- D06M13/352—Heterocyclic compounds having five-membered heterocyclic rings
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/10—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing oxygen
- D06M13/144—Alcohols; Metal alcoholates
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/10—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing oxygen
- D06M13/165—Ethers
- D06M13/17—Polyoxyalkyleneglycol ethers
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/10—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing oxygen
- D06M13/224—Esters of carboxylic acids; Esters of carbonic acid
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/322—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing nitrogen
- D06M13/372—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing nitrogen containing etherified or esterified hydroxy groups ; Polyethers of low molecular weight
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/322—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing nitrogen
- D06M13/402—Amides imides, sulfamic acids
- D06M13/432—Urea, thiourea or derivatives thereof, e.g. biurets; Urea-inclusion compounds; Dicyanamides; Carbodiimides; Guanidines, e.g. dicyandiamides
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M15/00—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment
- D06M15/19—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment with synthetic macromolecular compounds
- D06M15/37—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- D06M15/39—Aldehyde resins; Ketone resins; Polyacetals
- D06M15/423—Amino-aldehyde resins
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M15/00—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment
- D06M15/19—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment with synthetic macromolecular compounds
- D06M15/37—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- D06M15/39—Aldehyde resins; Ketone resins; Polyacetals
- D06M15/423—Amino-aldehyde resins
- D06M15/427—Amino-aldehyde resins modified by alkoxylated compounds or alkylene oxides
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M15/00—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment
- D06M15/19—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment with synthetic macromolecular compounds
- D06M15/37—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- D06M15/53—Polyethers
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M15/00—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment
- D06M15/19—Treating fibres, threads, yarns, fabrics, or fibrous goods made from such materials, with macromolecular compounds; Such treatment combined with mechanical treatment with synthetic macromolecular compounds
- D06M15/37—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- D06M15/643—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds containing silicon in the main chain
- D06M15/647—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds containing silicon in the main chain containing polyether sequences
Definitions
- the invention described below relates to compositions and their use for the treatment of fiber materials, in particular of cellulose.
- N-methylolated products of the formula used which can be prepared by reacting urea with glyoxal and with formaldehyde. Also methylolated melamine derivatives of the formula have already been used for this.
- the object of the present invention was to improve existing products so that the treated with them cellulose materials increased hydrophilicity while maintaining a pleasantly soft feel is mediated. This especially if the products are used in the context of a wet crosslinking. Another task was to find new, well-dispersible, reactive products that have the ability to trap radicals. Another task was to provide new reactive fluorosurfactants. Another object was to provide new reactive compounds with optically brightening properties.
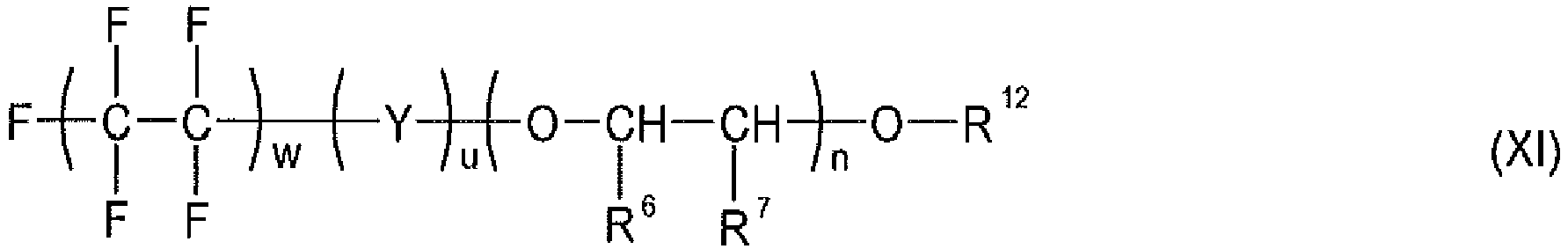
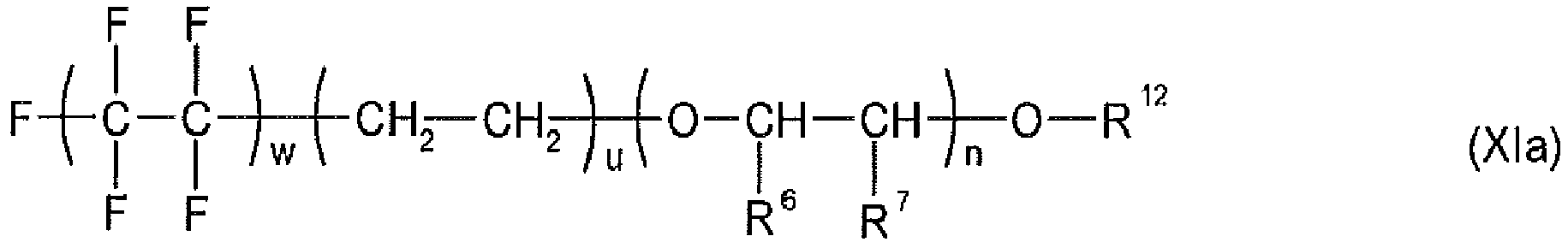
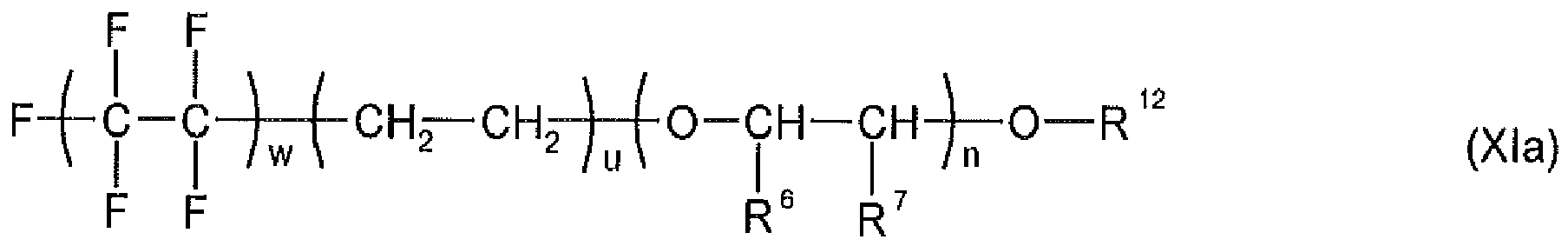
- composition which comprises at least one compound of the formula (II) or of the formula (III) or of the formula (IV) or of the formula (V) and wherein the composition comprises at least one compound of the formula (VII) or an amine of the formula (VIII) or (IX) or an oligo- or polyorganosiloxane which has polyoxyalkylene groups, of the general formula (X) or a compound of the formula (XI) , preferably of the formula (Xla), contains wherein the composition may additionally optionally contain an alcohol of the formula (VI), R 4 -OH (VI) where all radicals R 1 and R 2 independently of one another are H or a linear or branched alkyl radical having 1 to 5 carbon atoms, preferably CH 3 or C 2 H 5 or C 3 H 7 , or or for stand, wherein m is a number from 4 to 8 and t is 0 or 1 and p is a number from 8 to 20 and q is a number from 1 to 3, all radicals R 1 and R 2
- compositions of the present invention have less of a tendency to cleave present ether linkages, resulting in a lower tendency toward oligomerization, resulting in more stable products. They are good, therefore suitable for the treatment of fiber materials of natural fibers, preferably of cellulose or wool, but also of synthetic fibers, in particular polyester, polyamide, polyacrylonitrile, polyacrylate and viscose, as well as mixtures thereof, but in particular of fiber materials, which contain from 50 to 100% by weight made of cellulose. Especially cotton articles obtained by treatment with said compositions due to their surfactant character excellent properties.
- the fiber materials are here in particular in the form of tissues.
- compositions according to the invention or aqueous compositions containing such compositions is the wet crosslinking of articles made of cellulose fibers.
- compositions of this invention can be mixed with long-chain alkoxylated primary amines, including primary amines with a turf JEFFAMINE ® from Huntsman. This miscibility results in the resulting formulations being able to be used in processes where the finishing agent is used as a solution in supercritical carbon dioxide. Furnishing fiber articles using liquid supercritical carbon dioxide solutions offers several advantages over aqueous systems. Such processes are described, inter alia, in WO 94/18264 A1 . EP 1 126 072 A2 and EP 846 803 B1 ,
- the equipment with products according to the invention leads, if an etherification of the groups the melamine derivatives of the formula (III) or the urea derivatives of the formulas (II) or (V) is present, too low emissions of formaldehyde.
- the emissions of lower alcohols, in particular of methanol are reduced because the OH groups of the urea or melamine derivatives are not etherified exclusively with methanol.
- Cotton products equipped with compositions according to the invention or their aqueous compositions lead to a pleasantly soft feel of the end products.
- articles whose cotton content is 50 to 100% by weight obtain excellent properties.
- the articles are preferably fabric.
- compositions of the invention e.g. B. those containing compounds of formulas (II), (III), (IV) or (V) or their reaction products with alcohol of formula (VI) and compounds of formula (VII) can be analogous to the chemist Establish common methods. It is likewise possible to prepare compositions according to the invention which comprise an amine of the formula (VIII) or (IX) or an oligo- or polyorganosiloxane which has polyoxyalkylene groups, the general formula (X) or a compound of the formula (XI), preferably of the formula ( Xla), or contain their reaction products.
- R 4 -OH is a linear or optionally branched alkyl radical having 1 to 18, preferably having 1 to 4 carbon atoms, more preferably CH 3 or C 2 H 5 , R 4 -OH is preferably methanol.
- R 5 is a linear or branched alkyl radical or alkenyl radical having 4 to 18, preferably 8 to 18, carbon atoms preferred is the iso-tridecyl radical.
- one of R 6 and R 7 is hydrogen and the other is hydrogen or methyl.
- reaction described above can be carried out as follows: Aqueous glyoxal solution whose pH has been adjusted to about 5 is admixed with N, N'-dimetllyfolurea, then 37% aqueous formaldehyde and alcohol R 4 -OH and heated to 40 ° C. Subsequently, the pH is adjusted to about 7 by means of NaOH, then an excess of alcohol R 4 -OH and a compound of formula (VII) are added. Then add a little acid, for example hydrochloric acid added, with an increase in temperature takes place etherification. The etherification is then stopped by the addition of NaOH. An addition of an alkanolamine, eg triethanolamine, is then advantageous.
- an alkanolamine eg triethanolamine
- excess alcohol R 4 -OH is preferably distilled off. After pH adjustment to about 6 is distilled under reduced pressure at a temperature of 60 ° to 70 ° C, with excess alcohol R 4 -OH and water are removed.
- R 4 -OH is preferably methanol.
- the starting material used is a urea derivative of the formula (II), (IV) or (V) or a melamine derivative of the formula (III)
- the synthesis proceeds in an analogous manner by etherification with a mixture of alcohol R 4 -OH and compound of the formula (VII).
- an amine of the formula (VIII) or (IX) or a siloxane of the formula (X) or a compound of the formula (XI), preferably of the formula (Xla) may also be used instead of the compound of the formula (VII).
- compositions of the invention from known, in whose preparation, for example Dimethyloldihydroxyethylenharnstoff and methanol were used, is the fact that according to the invention in addition to a low molecular weight alcohol nor a relatively high molecular weight compound of formula (VII) or their ethers or an amine of formula (VIII) or (IX) or an oligo- or polyorganosiloxane of the general formula (X) or a compound of the formula (XI), preferably of the formula (Xla) is used.
- R 5 preferably represents a branched alkyl radical having 13 carbon atoms and I preferably a number from 2 to 20, particularly preferably from 2 to 8, in particular from 2 to 6.
- compositions according to the invention is expediently carried out by mixing and / or reacting at least one of the compounds of the formula (II), (III), (IV) or (V) with a mixture of at least one alcohol of the formula (VI) and at least one A compound of the formula (VII) or an amine of the formula (VIII) or (IX) or of an oligo- or polyorganosiloxane which has polyoxyalkylene groups, of the general formula (X) or of a compound of the formula (XI), preferably of the formula (Xla) , It is carried out at a temperature in the range of 30 to 130 ° C, preferably from 30 to 80 ° C, more preferably from 40 to 70 ° C, wherein the final distillation step also takes place in this temperature range.
- the etherification with alcohol of the formula (VI) is carried out at a pH of from 0.3 to 1, preferably from 0.45 to 0.75. This pH can be z. B. can be achieved by adding concentrated hydrochloric acid.
- This pH can be achieved by carrying out the etherification with alcohol of the formula (VI) z. B. by addition of sodium hydroxide and triethanolamine as a buffer stops.
- a particularly preferred embodiment of the invention is a composition containing a product obtained by reacting a compound of formula (II) or formula (III) or formula (IV) or formula (V) with a mixture of alcohols of Formula (VI) and compound of the formula (VII) or amine of the formula (VIII) or (IX) or oligo- or polyorganosiloxane which has polyoxyalkylene groups, of the general formula (X) or compound of the formula (XI), preferably of the formula ( XIa).
- this reaction is carried out at a temperature in the range of 40 to 70 ° C and at an acidic pH.
- compositions according to the invention can be used particularly advantageously in the form of aqueous compositions containing one or more of the above-described compositions, preferably with a water content of 20 to 60% by weight.
- compositions of the invention still NaCl, KCl or LiCl, preferably in amounts of 0.5 to 5 wt .-%, which may in particular enable better results in the cellulose crosslinking.
- compositions according to the invention are well suited for the treatment of fiber materials, both of natural fibers, preferably of cellulose or wool, and of synthetic fibers, in particular polyester, polyamide, polyacrylonitrile, polyacrylate and viscose, as well as of mixtures thereof, in particular those of the 50th consist of up to 100 wt .-% of cellulose.
- fiber materials both of natural fibers, preferably of cellulose or wool, and of synthetic fibers, in particular polyester, polyamide, polyacrylonitrile, polyacrylate and viscose, as well as of mixtures thereof, in particular those of the 50th consist of up to 100 wt .-% of cellulose.
- Particularly preferred materials are cotton articles in the form of fabrics for various applications, for example for shirt fabrics.
- Other materials are synthetic fabrics, for example, for the manufacture of awnings.
- compositions according to the invention or their aqueous compositions can be used very advantageously for the wet crosslinking of cotton materials. This wet crosslinking can be carried out by known methods. Compositions according to the invention may comprise further products known to the person skilled in the art which are customarily used for the achievement of various effects on textiles.
- compositions according to the invention also find application in that a composition comprising a proportion of at least one reacted compound of one of the formulas (VII) or (VIII) or (IX) or (X) or preferably (XI), in particular (XIa), in combination with Polymers which are suitable for generating barrier effects on textiles are used and the composition thus obtained is used for the treatment of fiber materials for achieving increased barrier effects.
- barrier effect one understands the characteristic of textiles, certain media, above all watery and oily liquids, but also dirt, dismiss, d. H. to prevent penetration of these into the fibers upon contact.
- Suitable for this are various polymers. These include polymers having perfluoroalkyl groups, e.g. As polyurethanes or poly (meth) acrylates and also their copolymers containing other monomers. Suitable for this purpose are z. As well as polyorganosiloxanes with certain functional groups.
- compositions according to the invention also find application in that a composition comprising a proportion of at least one reacted compound of one of the formulas (VII) or (VIII) or (IX) or (X) or (XI), preferably (Xla), in combination with polymers , which are suitable for generating barrier effects on textiles, and the composition thus obtained is used for the treatment of fiber materials for achieving or increasing soil release effects.
- inventive compositions and polymers which are suitable for generating barrier effects on textiles but which in themselves do not allow soil release effects to achieve a certain level of soil release properties on textiles.
- compositions according to the invention with polymers which are suitable for generating barrier effects on textiles and that already allow for soil release effects, these soil release effects can be further enhanced.
- compositions according to the invention can be used as surfactant or cosurfactant in the emulsification of the polymers, but they can also be added to the polymer emulsions after emulsification, where they then in the treatment of fiber materials as a carrier better introduction of the polymers in the Enable fiber materials.
- composition containing an optical brightener, especially based on a stilbene structure, or a UV absorber, preferably in reacted form, for introducing optical brighteners, in particular based on a stilbene structure, or of UV Absorbers on fiber materials is used.
- UV absorber is TINUVIN ® 1130 from BASF.
- Suitable UV absorbers are also the compounds 2- (2-hydroxy-5-methylphenyl) benzotriazole and 2-hydroxy-4-methoxybenzophenone and polyethylene glycol mono- (distyrylphenyl) ether.
- Another aspect of the invention is a compound of the formula (XII) wherein the radical R 3 is H or -CH 2 -OR 2 , all radicals R 1 and R 2 independently of one another are H or a linear or branched one Alkyl radical having 1 to 5 carbon atoms, preferably CH 3 or C 2 H 5 or C 3 H 7 , or for or for stand, where m is a number from 4 to 8 and q is a number from 1 to 3 and where the radical R 13 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably H or nC 4 H 9 , with the proviso that at least one of the radicals R 1 or R 2 present does not stand for H.
- the preparation of the compounds of the formula (XII) can be carried out by methods similar to those for the preparation of the already known compounds of the formula below, instead of urea, thiourea is chosen as the starting compound.
- the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree.
- the original became thin, clear and pale yellow.
- MARLIPAL O ® were 13/50 (C13 oxo alcohol with 5 moles of EO available from Sasol) was added and 265.9 g of methanol.
- the etherification was started by adding 5.0 g of concentrated hydrochloric acid (31-33% by weight). The exothermic reaction resulted in a temperature increase of about 8 ° C. After 7 minutes, the etherification was stopped by adding 2.0 g of a 50% sodium hydroxide solution and 0.3 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.9 with dilute sodium hydroxide solution or hydrochloric acid. This was followed for 6 hours at max. 70 ° C and under vacuum to an absolute pressure of 100 mbar distilling off 228 g of a methanol / water mixture.
- an aqueous finishing bath was prepared containing 220 g / l KNITTEX ® FA CONC (dimethyloldihydroxyethyleneurea, methanol-etherified, available from Huntsman), and 110 g / l KNITTEX CATALYST UMP (aqueous solution of several organic and inorganic acidic compounds obtainable from Huntsman) and 1 g / L of concentrated hydrochloric acid (31-33% by weight).
- Sections of a bleached, non-visually brightened 100% cotton shirt fabric having a basis weight of 110 g / m 2 were impregnated with aqueous liquors in the above-mentioned compositions on a laboratory tuft with a liquor pick-up of 66% by weight, then to a residual moisture content of 7%. dried and then stored for 20 hours at 30 ° C.
- the samples were washed for 10 minutes at 40 ° C with an aqueous solution of 10 g / l sodium carbonate, then once with warm water, then once with cold water, further with an aqueous solution of 0.5 g / l INVATEX ® AC ( aqueous solution of low-content citric acid, available from Huntsman), then rinsed with cold water and finally dried at 110 ° for 10 minutes.
- the fabric is then clamped with the chain and sometimes with the shot in the vertical direction.
- the composition according to Inventive Example No. 1 shows clearly better hydrophilic effects than the comparative test based on KNITTEX FA CONC, see Tables 1 and 2.
- Example 1 The distilling off of the methanol according to Example 1 can take place over different periods of time. With increasing distillation time, the degree of conversion of MARLIPAL O 13/50 with the Dimethyloldihydroxyethylenharnstoff (DMDHEH) increases. Accordingly, one can control the implementation so that products with different properties arise.
- DMDHEH Dimethyloldihydroxyethylenharnstoff
- Example 1 was repeated with different time periods for the distillation time, the corresponding values for which are given in Table 3 below.
- Table 3 Experiment No. 1 2 3 4 5 6 7 8th Distillation time (hours) 0 3.5 5.5 7.5 9.5 11.5 13.5 15.5
- an aqueous dispersion having a content of 200 g / l was prepared. These were shaken vigorously and then allowed to rest for 30 minutes. It can be seen from the aqueous dispersions that their ability to foam increases with increasing distillation time, see Figure 1.
- the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree.
- the original became thin, clear and pale yellow.
- the etherification was started by the addition of 3.6 g of concentrated hydrochloric acid (31-33 wt .-%). The exothermic reaction resulted in a temperature increase of about 8 ° C. After 7 minutes, the etherification was stopped by adding 1.4 g of a 50% sodium hydroxide solution and 0.2 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.9 with dilute sodium hydroxide solution or hydrochloric acid. It was then carried out for about 2 hours at max. 70 ° C and under vacuum to an absolute pressure of 100 mbar, distilling off 197 g of a methanol / water mixture.
- Example 1 The essential difference from Example 1 is therefore that oxo alcohol C13 was added with 5 moles of EO after distilling off methanol, that is, no etherification with oxoalcohol C13 with 5 moles of EO took place.
- an aqueous finishing liquor containing 220 g / l composition according to Example 2 100 g / l KNITTEX CATALYST UMP, 1 g / l concentrated hydrochloric acid (31-33 wt.%) And 50 g / TURPEX® ACN NEW (Aqueous dispersion of a wax, a common cotton fabric crosslinking formulation component available from Huntsman).
- an aqueous finishing bath was prepared containing 220 g / l KNITTEX ® FA CONC, 100 g / l KNITTEX CATALYST UMP, 1 g / l of concentrated hydrochloric acid (31-33 wt .-%) and 50 g / l TURPEX® ACN NEW , Sections of a colored, non-optically brightened 100% cotton poplin shirt fabric were impregnated with aqueous liquors in the above compositions on a laboratory tuft with a liquor pick-up of 66% by weight, then dried to a residual moisture of 7% and then at 30 ° for 20 hours C stored.
- the formaldehyde content on the fabric was also determined according to JIS L 1041: 2011, a Japanese standard (equivalent to ISO 14184-1: 1998).
- the composition according to inventive example no. 2 shows clearly better hydrophilic effects and lower formaldehyde content than the comparative test based on KNITTEX FA CONC, see Tables 4 and 5.
- the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree.
- the original became thin, clear and pale yellow.
- the etherification was started by adding 4.3 g of concentrated hydrochloric acid (31-33%). The exothermic reaction resulted in a temperature increase of about 9 ° C. After 8 minutes, the etherification was stopped by adding 1.7 g of a 50% sodium hydroxide solution and 0.2 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.9 with dilute sodium hydroxide solution or hydrochloric acid.
- the etherification is started by adding 19.5 g of concentrated hydrochloric acid (32%). The exothermic reaction resulted in a temperature increase of 9 ° C. After 9 minutes, the etherification was stopped by adding 7.5 g of a 50% sodium hydroxide solution.
- Mercerised cotton pieces were pad-batched with a dye solution containing 2.4 g / l NOVACRON® Blue CR (HUNTSMAN reactive dye), 15 ml / l sodium hydroxide 36 ° B, 70 ml / l sodium silicate 38-40 B, 2 g / l LYOPRINT® RG (dyeing auxiliaries from HUNTSMAN) and 1 g / l CIBAFLOW® PAD (dyeing auxiliaries from HUNTSMAN).
- the fabric pieces After padding, with a liquor pick-up of 70 wt .-%, the fabric pieces were stored for 16 hours at room temperature, then rinsed three times with water (cold, at boiling temperature, cold) and dried.
- BPO stands for benzoyl peroxide, more specifically dibenzoyl peroxide, which is used in dermatological preparations and, when applied to the skin, can damage the color of textiles due to its ability to easily form radicals.
- BPO stands for benzoyl peroxide, more specifically dibenzoyl peroxide, which is used in dermatological preparations and, when applied to the skin, can damage the color of textiles due to its ability to easily form radicals.
- 50 g of water, 0.1 g of Wako V50 (2,2'-azobis [2-methylpropionamidine] dihydrochloride, CAS NO 2997-92-4) 0.15 g of the inventive composition prepared as described above and 1 g dyed textile piece for 2 hours at 65 - 70 ° C stirred. The piece of fabric was then rinsed and dried. The textile piece was then slightly discolored.
- a dyed fabric piece was coated with 20 g / l of the inventive composition prepared as described above by the Pad-Dry-Thermofix method (described, for example, in U.S.P. DE 4133995 ) at a pH of 4 to 8 and a liquor uptake of 100 wt .-%, then dried for 1 minute at 110 ° C and heat-set at 170 ° C for 2 minutes.
- Pad-Dry-Thermofix method described, for example, in U.S.P. DE 4133995
- the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree.
- the original became thin, clear and pale yellow.
- MARLIPAL O 13/50 (oxoalcohol C 13 with 5 moles of EO) and 109.7 g of ZONYL® fluorosurfactant FS-300 (40% in water, an ethoxylated perfluoroalkylethyl alcohol, available from DuPont) and 203, 5 g of methanol added.
- the etherification was started by adding 7.8 g of concentrated hydrochloric acid (31-33% by weight). The exothermic reaction resulted in a temperature increase of about 9 ° C. After 9 minutes, the etherification was stopped by adding 4.8 g of a 50% sodium hydroxide solution and 0.2 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.8 with dilute sodium hydroxide solution or hydrochloric acid.
- the template was heated to 70 ° C.
Landscapes
- Engineering & Computer Science (AREA)
- Textile Engineering (AREA)
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Treatments For Attaching Organic Compounds To Fibrous Goods (AREA)
- Surface Treatment Of Glass Fibres Or Filaments (AREA)
Abstract
Es werden Zusammensetzungen beschrieben, welche sich für die Behandlung von textilen Flächengebilden eignen, denen hierdurch vorteilhafte Trageeigenschaften, insbesondere eine erhöhte Hydrophilie, verliehen werden. Die Zusammensetzungen enthalten Harnstoff-, Thioharnstoff- oder Melaminderivaie, Polyoxyalkylengruppen enthaltende Verbindungen und gegebenenfalls einen Alkohol, wobei diese Komponenten gegebenenfalls auch miteinander umgesetzt sein können.There are described compositions which are suitable for the treatment of textile fabrics, which thereby advantageous wearing properties, in particular an increased hydrophilicity, are awarded. The compositions contain urea, thiourea or melamine derivatives, polyoxyalkylene group-containing compounds and optionally an alcohol, these components also being able to be reacted with one another if appropriate.
Description
Die nachfolgend beschriebene Erfindung betrifft Zusammensetzungen und deren Verwendung zur Behandlung von Fasermaterialien, insbesondere aus Cellulose.The invention described below relates to compositions and their use for the treatment of fiber materials, in particular of cellulose.
Es ist bekannt, Textilmaterialien aus Cellulose mit sogenannten Cellulosevernetzern zu behandeln, um die Knitterneigung zu reduzieren. Bei diesen Veredlungsprozessen werden unter anderem N-methylolierte Produkte der Formel
Die genannten Produkte haben den Nachteil, dass bei thermischer Behandlung im Verlauf des Veredelungsprozesses Formaldehyd in die Umgebung abgegeben wird. Aus diesem Grund wurden Produkte entwickelt, in welchen eine oder mehrere der Hydroxygruppen verethert sind. Hierzu wird in erster Linie Methanol verwendet. Produkte der genannten Art und ihre Verwendung werden unter anderem in der
Aber auch die vollständig oder teilweise mit Methanol veretherten Produkte besitzen noch nicht optimale Eigenschaften. So sind beispielsweise die hydrophilen Eigenschaften von mit den Produkten ausgerüsteten Celluloseartikeln, insbesondere Artikeln aus Baumwolle, nicht immer auf dem gewünschten hohen Niveau, was sich in Benetzungstests bestätigt hat. Dies gilt unter anderem für Veredelungsverfahren, bei denen Baumwollartikel einer Feuchtvernetzung unterworfen werden.But also completely or partially etherified with methanol products do not have optimal properties. For example, the hydrophilic properties of cellulosic articles finished with the products, especially cotton articles, are not always at the desired high level, as has been confirmed in wetting tests. This applies inter alia to finishing processes in which cotton articles are subjected to wet crosslinking.
Die Aufgabe der vorliegenden Erfindung bestand darin, bestehende Produkte dahingehend zu verbessern, dass den mit ihnen behandelten Cellulosematerialien eine erhöhte Hydrophilie bei gleichzeitiger Beibehaltung eines angenehm weichen Griffs vermittelt wird. Dies insbesondere dann, wenn die Produkte im Rahmen einer Feuchtvernetzung eingesetzt werden. Eine weitere Aufgabe war es, neue, gut dispergierbare, reaktive Produkte zu finden, die die Fähigkeit haben, Radikale einzufangen. Eine weitere Aufgabe war es, neue reaktive Fluortenside zur Verfügung zu stellen. Eine weitere Aufgabe war es, neue reaktive Verbindungen mit optisch aufhellenden Eigenschaften zur Verfügung zu stellen.The object of the present invention was to improve existing products so that the treated with them cellulose materials increased hydrophilicity while maintaining a pleasantly soft feel is mediated. This especially if the products are used in the context of a wet crosslinking. Another task was to find new, well-dispersible, reactive products that have the ability to trap radicals. Another task was to provide new reactive fluorosurfactants. Another object was to provide new reactive compounds with optically brightening properties.
Die Aufgabe wurde gelöst durch eine Zusammensetzung, welche mindestens eine Verbindung der Formel (II) oder der Formel (III) oder der Formel (IV) oder der Formel (V)
wobei die Zusammensetzung zusätzlich gegebenenfalls einen Alkohol der Formel (VI) enthalten kann,
R4-OH (VI)
wobei alle Reste R1 und R2 unabhängig voneinander für H oder für einen linearen oder verzweigten Alkylrest mit 1 bis 5 Kohlenstoffatomen, vorzugsweise für CH3 oder C2H5 oder C3H7, oder für
wobei m eine Zahl von 4 bis 8 ist und t 0 oder 1 ist und p eine Zahl von 8 bis 20 und q eine Zahl von 1 bis 3 ist,
alle Reste R3 unabhängig voneinander für H oder für -CH2-O-R2 stehen,
wobei in Formel (V) mindestens ein Rest R3 für -CH2-O-R2 steht,
X für O oder S steht,
der Rest R4 für einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 18, bevorzugt mit 1 bis 4 Kohlenstoffatomen, besonders bevorzugt für CH3 oder C2H5 steht, R5 für einen linearen oder verzweigten Alkylrest oder Alkenylrest mit 4 bis 18, vorzugsweise mit 8 bis 18 Kohlenstoffatomen, besonders bevorzugt für einen verzweigten Alkylrest mit 13 Kohlenstoffatomen, steht oder für einen, gegebenenfalls durch einen oder mehrere Kohlenwasserstoffreste substituierten, aromatischen Rest, insbesondere für Phenyl, Tolyl oder Benzyl,
wobei k + y = 2 ist und k den Wert 1 oder 2 hat, einer der Reste R6 und R7 für H und der andere für H oder für CH3 steht, I für eine Zahl von 0 bis 20, vorzugsweise 2 bis 20, besonders bevorzugt von 2 bis 8, insbesondere für 2 bis 6, steht, wobei bei Anwesenheit einer Verbindung der Formel (VII) mit I = 0 auch eine Verbindung der Formel (VII) mit I >= 2 anwesend sein muss, n für eine Zahl von 2 bis 20, vorzugsweise von 2 bis 8, besonders bevorzugt von 2 bis 6, steht und R8 für H oder für
wobei r eine Zahl von 2 bis 15, s eine Zahl von 0 bis 20, v eine Zahl von 1 bis 18 ist und R11 für H oder CH3 steht und wobei im Siloxan der Formel (X) sowohl die Dimethylsiloxyeinheiten als auch die Methylsiloxyeinheiten mit Polyoxyalkylengruppen aufweisenden Resten beliebig über die Siloxankette verteilt sein können,
wobei der Rest R12 für H oder einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 4 Kohlenstoffatomen, bevorzugt für CH3 oder t-C4H9, besonders bevorzugt für H steht,
wobei der Rest R13 für H oder einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 4 Kohlenstoffatomen, bevorzugt für H oder n-C4H9 steht,
wobei w für eine Zahl von 2 bis 9, bevorzugt von 3 bis 8 steht, u 0 oder bevorzugt 1 ist, Y ein zweiwertiger Rest ist enthaltend Kohlenstoff und Wasserstoff und ggf. Schwefel und/oder Stickstoff und/oder Sauerstoff,
wobei die Zusammensetzung mindestens für den Fall, dass eine Verbindung der Formel (VII) mit I= 6 - 8 und t = 0 enthalten ist, ein Umsetzungsprodukt aus einer oder mehreren Verbindungen der Formeln (II) bis (V) mit einer oder mehreren Verbindungen der Formel (VII) und gegebenenfalls der Formel (VI) enthält,
und durch eine wässrige Zusammensetzung, welche eine solche Zusammensetzung enthält.The object has been achieved by a composition which comprises at least one compound of the formula (II) or of the formula (III) or of the formula (IV) or of the formula (V)
wherein the composition may additionally optionally contain an alcohol of the formula (VI),
R 4 -OH (VI)
where all radicals R 1 and R 2 independently of one another are H or a linear or branched alkyl radical having 1 to 5 carbon atoms, preferably CH 3 or C 2 H 5 or C 3 H 7 , or
wherein m is a number from 4 to 8 and t is 0 or 1 and p is a number from 8 to 20 and q is a number from 1 to 3,
all radicals R 3 independently of one another are H or -CH 2 -OR 2 ,
where in formula (V) at least one radical R 3 is -CH 2 -OR 2 ,
X stands for O or S,
the radical R 4 is a linear or optionally branched alkyl radical having 1 to 18, preferably having 1 to 4 carbon atoms, more preferably CH 3 or C 2 H 5 , R 5 is a linear or branched alkyl radical or alkenyl radical having 4 to 18, preferably having 8 to 18 carbon atoms, particularly preferably a branched alkyl radical having 13 carbon atoms, or represents an optionally substituted by one or more hydrocarbon radicals, aromatic radical, in particular phenyl, tolyl or benzyl,
where k + y = 2 and k has the value 1 or 2, one of the radicals R 6 and R 7 for H and the other is H or CH 3 , I is a number from 0 to 20, preferably 2 to 20, particularly preferably from 2 to 8, in particular from 2 to 6, wherein in the presence of a compound of formula (VII) with I = 0, a compound of formula (VII) with I> = 2 must be present, n is a number from 2 to 20, preferably from 2 to 8, particularly preferably from 2 to 6, and R 8 is H or for
wherein r is a number from 2 to 15, s is a number from 0 to 20, v is a number from 1 to 18 and R 11 is H or CH 3 and wherein in the siloxane of the formula (X) both the dimethylsiloxy and the methylsiloxy with radicals having polyoxyalkylene groups may be distributed as desired over the siloxane chain,
where the radical R 12 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably CH 3 or tC 4 H 9 , particularly preferably H,
where the radical R 13 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably H or nC 4 H 9 ,
where w is a number from 2 to 9, preferably from 3 to 8, u is 0 or preferably 1, Y is a bivalent radical containing carbon and hydrogen and optionally sulfur and / or nitrogen and / or oxygen,
wherein the composition is at least in the case that a compound of formula (VII) with I = 6-8 and t = 0 is included, a reaction product of one or more compounds of formulas (II) to (V) with one or more compounds of formula (VII) and optionally of formula (VI),
and by an aqueous composition containing such a composition.
Solche Zusammensetzungen haben nicht nur den Vorteil, den Celluloseartikeln erhöhte Hydrophilie zu vermitteln, sondern sie führen auch zu geringeren Emissionen an Alkohol R2-OH. Außerdem haben erfindungsgemäße Zusammensetzungen eine geringere Tendenz, vorliegende Etherbindungen zu spalten, woraus eine geringere Oligomerisierungsneigung resultiert, was zu stabileren Produkten führt. Sie sind daher vor allem gut geeignet zur Behandlung von Fasermaterialien aus Naturfasern, bevorzugt aus Cellulose oder Wolle, aber auch aus synthetischen Fasern, insbesondere Polyester, Polyamid, Polyacrylnitril, Polyacrylat und Viskose, sowie aus Mischungen davon, insbesondere aber von Fasermaterialien, welche zu 50 bis 100 Gew.-% aus Cellulose bestehen. Vor allem Baumwollartikel erhalten durch Behandlung mit den genannten Zusammensetzungen auf Grund deren tensidischen Charakters hervorragende Eigenschaften. Die Fasermaterialien liegen hierbei insbesondere in Form von Geweben vor.Not only do such compositions have the advantage of imparting increased hydrophilicity to the cellulosic articles, but they also result in lower emissions of alcohol R 2 -OH. In addition, compositions of the present invention have less of a tendency to cleave present ether linkages, resulting in a lower tendency toward oligomerization, resulting in more stable products. They are good, therefore suitable for the treatment of fiber materials of natural fibers, preferably of cellulose or wool, but also of synthetic fibers, in particular polyester, polyamide, polyacrylonitrile, polyacrylate and viscose, as well as mixtures thereof, but in particular of fiber materials, which contain from 50 to 100% by weight made of cellulose. Especially cotton articles obtained by treatment with said compositions due to their surfactant character excellent properties. The fiber materials are here in particular in the form of tissues.
Ein besonders gut geeignetes Anwendungsgebiet für erfindungsgemäße Zusammensetzungen bzw. wässrige Zusammensetzungen, die solche Zusammensetzungen enthalten, ist die Feuchtvernetzung von Artikeln aus Cellulosefasern.A particularly suitable field of application for compositions according to the invention or aqueous compositions containing such compositions is the wet crosslinking of articles made of cellulose fibers.
Eine Reihe von erfindungsgemäßen Zusammensetzungen ist mit längerkettigen alkoxilierten primären Aminen mischbar, unter anderem mit primären Aminen der Gamme JEFFAMINE® der Firma Huntsman. Diese Mischbarkeit führt dazu, dass die entstehenden Formulierungen in Prozessen eingesetzt werden können, bei denen das Ausrüstungsmittel als Lösung in superkritischem Kohlendioxid verwendet wird. Die Ausrüstung von Faserartikeln mittels Lösungen in flüssigem superkritischem Kohlendioxid bietet verschiedene Vorteile gegenüber Ausrüstung mittels wässriger Systeme. Solche Prozesse sind unter anderem beschrieben in
Die Ausrüstung mit erfindungsgemäßen Produkten führt, wenn eine Veretherung der Gruppen
Mit erfindungsgemäßen Zusammensetzungen bzw. deren wässrigen Zusammensetzungen ausgerüstete Baumwollprodukte führen zu einem angenehm weichen Griff der Endartikel. Insbesondere Artikel, deren Baumwollanteil 50 bis 100 Gew.-% beträgt, erhalten ausgezeichnete Eigenschaften. Die Artikel sind vorzugsweise Gewebe.Cotton products equipped with compositions according to the invention or their aqueous compositions lead to a pleasantly soft feel of the end products. In particular, articles whose cotton content is 50 to 100% by weight obtain excellent properties. The articles are preferably fabric.
Erfindungsgemäße Gemische lassen sich nach dem folgenden allgemeinen Verfahren herstellen:
- N,N'-Dimethylolharnstoff der Formel
- wird mit Glyoxal bei einem pH von etwa 5 in Gegenwart von Wasser zu Dimethyloldihydroxyethylenharnstoff der Formel (I)
- Durch Zugabe eines Überschusses an einem Alkohol R4-OH und gleichzeitiger Zugabe einer Verbindung der Formel (VII)
- N, N'-dimethylolurea of the formula
- is reacted with glyoxal at a pH of about 5 in the presence of water to form dimethyloldihydroxyethyleneurea of the formula (I)
- By addition of an excess of an alcohol R 4 -OH and simultaneous addition of a compound of formula (VII)
Andere erfindungsgemäße Zusammensetzungen, z. B. solche, die Verbindungen der Formeln (II), (III), (IV) oder (V) bzw. deren Umsetzungsprodukte mit Alkohol der Formel (VI) und Verbindungen der Formel (VII) enthalten, lassen sich nach analogen, dem Chemiker geläufigen Methoden herstellen. Ebenso lassen sich auch erfindungsgemäße Zusammensetzungen herstellen, die ein Amin der Formel (VIII) oder (IX) oder ein Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) oder eine Verbindung der Formel (XI), bevorzugt der Formel (Xla), bzw. deren Umsetzungsprodukte enthalten. Wenn eine Verbindung der Formel (VII) oder ein Siloxan der Formel (X) oder eine Verbindung der Formel (XI), bevorzugt der Formel (XIa), nicht nur zugesetzt, sondern auch chemisch umgesetzt werden, so ist es erforderlich, dass solche derartigen Verbindungen eingesetzt werden, in denen R12 = H.Other compositions of the invention, e.g. B. those containing compounds of formulas (II), (III), (IV) or (V) or their reaction products with alcohol of formula (VI) and compounds of formula (VII) can be analogous to the chemist Establish common methods. It is likewise possible to prepare compositions according to the invention which comprise an amine of the formula (VIII) or (IX) or an oligo- or polyorganosiloxane which has polyoxyalkylene groups, the general formula (X) or a compound of the formula (XI), preferably of the formula ( Xla), or contain their reaction products. When a compound of formula (VII) or a siloxane of formula (X) or a compound of formula (XI), preferably of formula (XIa), are not only added but also chemically reacted, it is necessary that such Compounds are used in which R 12 = H.
In dem Alkohol R4-OH steht R4 für einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 18, bevorzugt mit 1 bis 4 Kohlenstoffatomen, besonders bevorzugt für CH3 oder C2H5, R4-OH ist vorzugsweise Methanol.In the alcohol R 4 -OH R 4 is a linear or optionally branched alkyl radical having 1 to 18, preferably having 1 to 4 carbon atoms, more preferably CH 3 or C 2 H 5 , R 4 -OH is preferably methanol.
In der Verbindung der Formel (VII) steht R5 für einen linearen oder verzweigten Alkylrest oder Alkenylrest mit 4 bis 18, vorzugsweise mit 8 bis 18 Kohlenstoffatomen, besonders bevorzugt ist der iso-Tridecylrest. Ferner steht in Formel (VII) einer der Reste R6 und R7 für Wasserstoff und der andere für Wasserstoff oder die Methylgruppe. In Formel (VII) ist I eine Zahl von 0 bis 20, vorzugsweise von 2 bis 20, besonders bevorzugt von 2 bis 8, insbesondere von 2 bis 6, wobei bei Anwesenheit einer Verbindung der Formel (VII) mit I = 0 auch eine Verbindung der Formel (VII) mit >= 2 anwesend sein muss.In the compound of the formula (VII), R 5 is a linear or branched alkyl radical or alkenyl radical having 4 to 18, preferably 8 to 18, carbon atoms preferred is the iso-tridecyl radical. Further, in formula (VII), one of R 6 and R 7 is hydrogen and the other is hydrogen or methyl. In formula (VII), I is a number from 0 to 20, preferably from 2 to 20, more preferably from 2 to 8, in particular from 2 to 6, wherein in the presence of a compound of formula (VII) with I = 0 also a compound of formula (VII) with> = 2 must be present.
Die vorstehend beschriebene Umsetzung kann folgendermaßen durchgeführt werden: Man gibt zu wässriger Glyoxallösung, deren pH auf etwa 5 eingestellt wurde, N,N'-Dimetllyfolharnstoff, dann 37 %igen wässrigen Formaldehyd und Alkohol R4-OH und heizt auf 40°C. Anschließend wird mittels NaOH der pH auf etwa 7 eingestellt, dann ein Überschuss an Alkohol R4-OH und eine Verbindung der Formel (VII) hinzugefügt. Anschließend fügt man etwas Säure, z.B. Salzsäure hinzu, wobei unter Temperaturerhöhung eine Veretherung stattfindet. Die Veretherung wird dann durch Zugabe von NaOH abgebrochen. Vorteilhaft ist anschließend eine Zugabe eines Alkanolamins, z.B. Triethanolamin. Anschließend wird vorzugsweise überschüssiger Alkohol R4-OH abdestilliert. Nach pH-Einstellung auf etwa 6 wird unter vermindertem Druck bei einer Temperatur von 60° bis 70°C destilliert, wobei überschüssiger Alkohol R4-OH und Wasser entfernt werden. R4-OH ist vorzugsweise Methanol.The reaction described above can be carried out as follows: Aqueous glyoxal solution whose pH has been adjusted to about 5 is admixed with N, N'-dimetllyfolurea, then 37% aqueous formaldehyde and alcohol R 4 -OH and heated to 40 ° C. Subsequently, the pH is adjusted to about 7 by means of NaOH, then an excess of alcohol R 4 -OH and a compound of formula (VII) are added. Then add a little acid, for example hydrochloric acid added, with an increase in temperature takes place etherification. The etherification is then stopped by the addition of NaOH. An addition of an alkanolamine, eg triethanolamine, is then advantageous. Subsequently, excess alcohol R 4 -OH is preferably distilled off. After pH adjustment to about 6 is distilled under reduced pressure at a temperature of 60 ° to 70 ° C, with excess alcohol R 4 -OH and water are removed. R 4 -OH is preferably methanol.
Falls als Ausgangsprodukt ein Harnstoffderivat der Formel (II), (IV) oder (V) oder ein Melaminderivat der Formel (III) eingesetzt wird, verläuft die Synthese in analoger Weise durch Veretherung mit einem Gemisch aus Alkohol R4-OH und Verbindung der Formel (VII). An Stelle der Verbindung der Formel (VII) kann jedoch auch ein Amin der Formel (VIII) oder (IX) oder ein Siloxan der Formel (X) oder eine Verbindung der Formel (XI), bevorzugt der Formel (Xla), verwendet werden.If the starting material used is a urea derivative of the formula (II), (IV) or (V) or a melamine derivative of the formula (III), the synthesis proceeds in an analogous manner by etherification with a mixture of alcohol R 4 -OH and compound of the formula (VII). However, an amine of the formula (VIII) or (IX) or a siloxane of the formula (X) or a compound of the formula (XI), preferably of the formula (Xla), may also be used instead of the compound of the formula (VII).
Auf Grund der bekannten Tatsache, dass Veretherungen zu einem Gleichgewicht führen, sind auch bei der Herstellung erfindungsgemäßer Gemische im Normalfall nicht alle OH-Gruppen der Ausgangs- und der Endverbindungen verethert, sondern nur ein Teil. Ferner ist es möglich, dass bei den oben beschriebenen Synthesen anfangs keine Veretherung mit Verbindung der Formel (VII) stattfindet, sondern nur mit Alkohol R4-OH. Die teilweise Veretherung mit Verbindung der Formel (VII) findet in diesem Fall erst statt, während Alkohol R4-OH abdestilliert wird. Im erfindungsgemäßen Gemisch ist dann ein Teil der ursprünglichen OH-Gruppen mit Alkohol R4-OH verethert, ein anderer Teil mit Verbindung der Formel (VII) umgesetzt, in diesem Fall verethert. Gleiches gilt hier auch, wenn ein Amin der Formel (VIII) oder (IX) oder ein Siloxan derDue to the known fact that etherifications lead to an equilibrium, not all OH groups of the starting compounds and the end compounds are etherified in the normal case, but only a part in the preparation of mixtures according to the invention. Furthermore, it is possible that in the syntheses described above initially no etherification with compound of formula (VII) takes place, but only with alcohol R 4 -OH. The partial etherification with compound of the formula (VII) takes place in this case only while alcohol R 4 -OH is distilled off. In the mixture according to the invention, a part of the original OH groups is then etherified with alcohol R 4 -OH, another part is reacted with compound of the formula (VII), in this case etherified. The same applies here if an amine of the formula (VIII) or (IX) or a siloxane of the
Formel (X) oder eine Verbindung der Formel (XI), bevorzugt der Formel (Xla), eingesetzt wirdFormula (X) or a compound of formula (XI), preferably of the formula (Xla), is used
Analytische Untersuchungen haben ergeben, dass, wenn R4-OH Methanol ist und die Verbindung der Formel (VII) ein Alkohol der Formel (Vlla),
Was die erfindungsgemäßen Zusammensetzungen von bekannten unterscheidet, bei deren Herstellung beispielsweise Dimethyloldihydroxyethylenharnstoff und Methanol verwendet wurden, ist die Tatsache, dass erfindungsgemäß außer einem niedrigmolekularen Alkohol noch eine höhermolekulare Verbindung der Formel (VII) oder deren Ether bzw. ein Amin der Formel (VIII) oder (IX) oder ein Oligo- oder Polyorganosiloxan der allgemeinen Formel (X) oder eine Verbindung der Formel (XI), bevorzugt der Formel (Xla), verwendet wird.What distinguishes the compositions of the invention from known, in whose preparation, for example Dimethyloldihydroxyethylenharnstoff and methanol were used, is the fact that according to the invention in addition to a low molecular weight alcohol nor a relatively high molecular weight compound of formula (VII) or their ethers or an amine of formula (VIII) or (IX) or an oligo- or polyorganosiloxane of the general formula (X) or a compound of the formula (XI), preferably of the formula (Xla) is used.
In der Mischung von Alkohol der Formel R4-OH und Verbindung der Formel (VII) liegt im Normalfall ein Überschuss an Alkohol der Formel R4-OH vor.In the mixture of alcohol of the formula R 4 -OH and compound of the formula (VII), there is normally an excess of alcohol of the formula R 4 -OH.
Bevorzugt ist es, dass pro Mol an Alkohol R4-OH 0,01 bis 0,5 Mol an Verbindung der Formel (VII) oder Amin der Formel (VIII) oder (IX) oder Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) oder Verbindung der Formel (XI), bevorzugt der Formel (Xla), umgesetzt werden.It is preferred that per mole of alcohol R 4 -OH from 0.01 to 0.5 mol of compound of formula (VII) or amine of formula (VIII) or (IX) or oligo- or polyorganosiloxane having polyoxyalkylene groups, the general formula (X) or compound of formula (XI), preferably of formula (Xla).
In Formel (VII) steht R5 bevorzugt für einen verzweigten Alkylrest mit 13 Kohlenstoffatomen und I vorzugsweise für eine Zahl von 2 bis 20, besonders bevorzugt von 2 bis 8, insbesondere von 2 bis 6.In formula (VII), R 5 preferably represents a branched alkyl radical having 13 carbon atoms and I preferably a number from 2 to 20, particularly preferably from 2 to 8, in particular from 2 to 6.
Die Herstellung erfindungsgemäßer Zusammensetzungen erfolgt zweckmäßiger Weise durch Mischung und/oder Umsetzung mindestens einer der genannten Verbindungen der Formel (II), (III), (IV) oder (V) mit einem Gemisch aus mindestens einem Alkohol der Formel (VI) und mindestens einer Verbindung der Formel (VII) oder einem Amin der Formel (VIII) oder (IX) oder einem Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) oder einer Verbindung der Formel (XI), bevorzugt der Formel (Xla). Dabei arbeitet man bei einer Temperatur im Bereich von 30 bis 130° C, bevorzugt von 30 bis 80° C, besonders bevorzugt von 40 - 70°C, wobei der abschließende Destillationsschritt ebenfalls in diesem Temperaturbereich stattfindet. Bei der Destillation findet mit Entfernung von Alkohol der Formel (VI) eine Umetherung bzw. eine Aminierung statt. Dabei ist es von Vorteil, dass Temperatur, Druck und pH-Wert so gewählt werden, dass durch Abdestillieren von Alkohol der Formel (VI) das Reaktionsgleichgewicht zugunsten von Umsetzungsprodukten enthaltend einen größeren Anteil an mit einer Verbindung einer der Formeln (VII) bis (XIa) umgesetzten Verbindung einer der Formeln (II) bis (V) verschoben wird, wobei bevorzugt die Verbindung einer der Formeln (VII) bis (XIa) erst zur Reaktionsmasse zugegeben wird, nachdem ein Teil des überschüssigen Alkohols der Formel (VI) bereits abdestilliert wurde.The preparation of compositions according to the invention is expediently carried out by mixing and / or reacting at least one of the compounds of the formula (II), (III), (IV) or (V) with a mixture of at least one alcohol of the formula (VI) and at least one A compound of the formula (VII) or an amine of the formula (VIII) or (IX) or of an oligo- or polyorganosiloxane which has polyoxyalkylene groups, of the general formula (X) or of a compound of the formula (XI), preferably of the formula (Xla) , It is carried out at a temperature in the range of 30 to 130 ° C, preferably from 30 to 80 ° C, more preferably from 40 to 70 ° C, wherein the final distillation step also takes place in this temperature range. In the distillation takes place with removal of alcohol of formula (VI), a transetherification or an amination. It is advantageous that the temperature, pressure and pH are chosen so that by distilling off alcohol of formula (VI) the reaction equilibrium in favor of reaction products containing a greater proportion of with a compound of the formulas (VII) to (XIa ), wherein preferably the compound of one of the formulas (VII) to (XIa) is added first to the reaction mass after a part of the excess alcohol of the formula (VI) has already been distilled off ,
Die Veretherung mit Alkohol der Formel (VI) wird bei einem pH-Wert von 0,3 bis 1, vorzugsweise von 0,45 bis 0,75 durchgeführt. Dieser pH-Wert kann z. B. mittels Zugabe von konzentrierter Salzsäure erreicht werden. Die anschließende Umsetzung mit einer Verbindung der Formel (VII) mit R12 = H oder einem Amin der Formel (VIII) oder (IX) oder einem Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) mit R12 = H oder einer Verbindung der Formel (XI) mit R12 = H, bevorzugt der Formel (Xla), wird bei einem pH-Wert von 5 bis 7, bevorzugt von 5,6 bis 6,4, durchgeführt. Dieser pH-Wert kann erreicht werden, indem man die Veretherung mit Alkohol der Formel (VI) z. B. mittels Zugabe von Natronlauge und Triethanolamin als Puffer stoppt. Bei der Umsetzung mit einer Verbindung der Formel (VII) mit R12 = H oder einem Amin der Formel (VIII) oder (IX) oder einem Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) mit R12 = H oder einer Verbindung der Formel (XI) mit R12 = H, bevorzugt der Formel (XIa), arbeitet man zweckmäßiger Weise unter Vakuum, bei einem absoluten Druck von 50 bis 1000 mbar, bevorzugt von 50 bis 175 mbar. Bei dieser Umsetzung findet eine Umetherung statt, wenn eine Verbindung der Formel (VII) mit R12 = H oder ein Amin der Formel (IX) oder ein Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) mit R12 = H oder eine Verbindung der Formel (XI) mit R12 = H, bevorzugt der Formel (XIa), eingesetzt wird bzw. eine Aminierung, wenn ein Amin der Formel (VIII) eingesetzt wird.The etherification with alcohol of the formula (VI) is carried out at a pH of from 0.3 to 1, preferably from 0.45 to 0.75. This pH can be z. B. can be achieved by adding concentrated hydrochloric acid. The subsequent reaction with a compound of the formula (VII) where R 12 is H or an amine of the formula (VIII) or (IX) or an oligo- or polyorganosiloxane which has polyoxyalkylene groups of the general formula (X) where R 12 = H or a compound of the formula (XI) where R 12 = H, preferably of the formula (Xla), is carried out at a pH of from 5 to 7, preferably from 5.6 to 6.4. This pH can be achieved by carrying out the etherification with alcohol of the formula (VI) z. B. by addition of sodium hydroxide and triethanolamine as a buffer stops. In the reaction with a compound of formula (VII) with R 12 = H or an amine of formula (VIII) or (IX) or an oligo- or polyorganosiloxane having polyoxyalkylene groups of the general formula (X) where R 12 = H or a compound of the formula (XI) where R 12 = H, preferably of the formula (XIa), is advantageously carried out under reduced pressure, at an absolute pressure of from 50 to 1000 mbar, preferably from 50 to 175 mbar. In this reaction, a transetherification takes place when a compound of formula (VII) with R 12 = H or an amine of formula (IX) or an oligo- or polyorganosiloxane having polyoxyalkylene groups, the general Formula (X) with R 12 = H or a compound of formula (XI) with R 12 = H, preferably the formula (XIa) is used or an amination, when an amine of formula (VIII) is used.
Eine besonders bevorzugte Ausführungsform der Erfindung besteht in einer Zusammensetzung, welche ein Produkt enthält, das durch Umsetzung einer Verbindung der Formel (II) oder der Formel (III) oder der Formel (IV) oder der Formel (V) mit einem Gemisch aus Alkoholen der Formel (VI) und Verbindung der Formel (VII) oder Amin der Formel (VIII) oder (IX) oder Oligo- oder Polyorganosiloxan, das Polyoxyalkylengruppen aufweist, der allgemeinen Formel (X) oder Verbindung der Formel (XI), bevorzugt der Formel (XIa). Bevorzugt wird diese Umsetzung bei einer Temperatur im Bereich von 40 bis 70°C und bei einem sauren pH-Wert durchgeführt. Ferner ist es günstig, wenn nach der Umsetzung das erhaltene Produkt neutralisiert und anschließend überschüssiger Alkohol der Formel (VI) abdestilliert wird.A particularly preferred embodiment of the invention is a composition containing a product obtained by reacting a compound of formula (II) or formula (III) or formula (IV) or formula (V) with a mixture of alcohols of Formula (VI) and compound of the formula (VII) or amine of the formula (VIII) or (IX) or oligo- or polyorganosiloxane which has polyoxyalkylene groups, of the general formula (X) or compound of the formula (XI), preferably of the formula ( XIa). Preferably, this reaction is carried out at a temperature in the range of 40 to 70 ° C and at an acidic pH. Furthermore, it is advantageous if, after the reaction, the product obtained is neutralized and then excess alcohol of the formula (VI) is distilled off.
Die erfindungsgemäßen Zusammensetzungen lassen sich besonders vorteilhaft in Form wässriger Zusammensetzungen verwenden, die eine oder mehrere der oben beschriebenen Zusammensetzungen enthalten, vorzugsweise mit einem Gehalt an Wasser von 20 bis 60 Gew.-%.The compositions according to the invention can be used particularly advantageously in the form of aqueous compositions containing one or more of the above-described compositions, preferably with a water content of 20 to 60% by weight.
In einigen Fällen ist es von Vorteil, wenn die wässrigen Zusammensetzungen außer erfindungsgemäßen Zusammensetzungen noch NaCl, KCl oder LiCl, vorzugsweise in Mengen von 0,5 bis 5 Gew.-% enthalten, was insbesondere bessere Ergebnisse bei der Cellulosevernetzung ermöglichen kann.In some cases, it is advantageous if the aqueous compositions except compositions of the invention still NaCl, KCl or LiCl, preferably in amounts of 0.5 to 5 wt .-%, which may in particular enable better results in the cellulose crosslinking.
Erfindungsgemäße Zusammensetzungen sind gut geeignet für die Behandlung von Fasermaterialien, sowohl aus Naturfasern, bevorzugt aus Cellulose oder Wolle, als auch aus synthetischen Fasern, insbesondere Polyester, Polyamid, Polyacrylnitril, Polyacrylat und Viskose, sowie aus Mischungen davon, insbesondere von solchen, die zu 50 bis 100 Gew.-% aus Cellulose bestehen. Besonders bevorzugte Materialien sind Artikel aus Baumwolle in Form von Geweben für diverse Einsatzgebiete, beispielsweise für Hemdenstoffe. Andere Materialien sind synthetische Gewebe, beispielsweise für die Fertigung von Markisen.Compositions according to the invention are well suited for the treatment of fiber materials, both of natural fibers, preferably of cellulose or wool, and of synthetic fibers, in particular polyester, polyamide, polyacrylonitrile, polyacrylate and viscose, as well as of mixtures thereof, in particular those of the 50th consist of up to 100 wt .-% of cellulose. Particularly preferred materials are cotton articles in the form of fabrics for various applications, for example for shirt fabrics. Other materials are synthetic fabrics, for example, for the manufacture of awnings.
Erfindungsgemäße Zusammensetzungen bzw. deren wässrige Zusammensetzungen lassen sich sehr vorteilhaft für die Feuchtvernetzung von Baumwollmaterialien verwenden. Diese Feuchtvernetzung kann nach bekannten Verfahren erfolgen. Erfindungsgemäße Zusammensetzungen können weitere, dem Fachmann bekannte Produkte enthalten, die üblicherweise für die Erzielung von diversen Effekten auf Textilien eingesetzt werden.Compositions according to the invention or their aqueous compositions can be used very advantageously for the wet crosslinking of cotton materials. This wet crosslinking can be carried out by known methods. Compositions according to the invention may comprise further products known to the person skilled in the art which are customarily used for the achievement of various effects on textiles.
Bei Einsatz von erfindungsgemäßen Produkten auf Textilien zusammen mit hydrophoben Polymeren, beispielsweise mit Polyethylenwachsen oder nicht hydrophil funktionalisierten Polysiloxanen kann eine weitere Steigerung der hydrophilen Eigenschaften der Textilien erreicht werden. Eine Ursache dafür könnte die Inversion der Orientierung der tensidischen Verbindungen auf den so ausgerüsteten Fasermaterialien sein.When using products of the invention on textiles together with hydrophobic polymers, for example with polyethylene waxes or non-hydrophilic functionalized polysiloxanes, a further increase in the hydrophilic properties of the textiles can be achieved. One reason for this could be the inversion of the orientation of the surface-active compounds on the fiber materials thus treated.
Erfindungsgemäße Zusammensetzungen finden auch Anwendung darin, dass eine Zusammensetzung enthaltend einen Anteil an mindestens einer umgesetzten Verbindung einer der Formeln (VII) oder (VIII) oder (IX) oder (X) oder vorzugsweise (XI), insbesondere (XIa), in Kombination mit Polymeren, die geeignet sind, auf Textilien Barriereeffekte zu generieren, eingesetzt und die so erhaltene Zusammensetzung für die Behandlung von Fasermaterialien zur Erzielung von gesteigerten Barriereeffekten eingesetzt wird. Unter Barriereeffekt versteht man die Eigenschaft von Textilien, bestimmte Medien, vor allem wässrige und ölige Flüssigkeiten, aber auch Schmutz, abzuweisen, d. h. bei Kontakt ein Eindringen dieser in die Fasern zu verhindern. Geeignet dazu sind diverse Polymere. Hierunter fallen Polymere, die Perfluoralkylgruppen aufweisen, z. B. Polyurethane oder Poly(meth)acrylate sowie auch ihre Copolymere, die noch weitere Monomere enthalten. Geeignet dazu sind z. B. auch Polyorganosiloxane mit bestimmten funktionellen Gruppen.Compositions according to the invention also find application in that a composition comprising a proportion of at least one reacted compound of one of the formulas (VII) or (VIII) or (IX) or (X) or preferably (XI), in particular (XIa), in combination with Polymers which are suitable for generating barrier effects on textiles are used and the composition thus obtained is used for the treatment of fiber materials for achieving increased barrier effects. By barrier effect one understands the characteristic of textiles, certain media, above all watery and oily liquids, but also dirt, dismiss, d. H. to prevent penetration of these into the fibers upon contact. Suitable for this are various polymers. These include polymers having perfluoroalkyl groups, e.g. As polyurethanes or poly (meth) acrylates and also their copolymers containing other monomers. Suitable for this purpose are z. As well as polyorganosiloxanes with certain functional groups.
Erfindungsgemäße Zusammensetzungen finden auch Anwendung darin, dass eine Zusammensetzung enthaltend einen Anteil an mindestens einer umgesetzten Verbindung einer der Formeln (VII) oder (VIII) oder (IX) oder (X) oder (XI), vorzugsweise (Xla), in Kombination mit Polymeren, die geeignet sind, auf Textilien Barriereeffekte zu generieren, eingesetzt und die so erhaltene Zusammensetzung für die Behandlung von Fasermaterialien zur Erzielung oder Steigerung von Soil-Release-Effekten eingesetzt wird. So ist es möglich, unter Einsatz erfindungsgemäßer Zusammensetzungen und Polymeren, die geeignet sind, auf Textilien Barriereeffekte zu generieren, die aber an sich keine Soil-Release-Effekte ermöglichen, ein bestimmtes Niveau an Soil-Release-Eigenschaften auf Textilien zu erzielen. Bei Einsatz erfindungsgemäßer Zusammensetzungen mit Polymeren, die geeignet sind, auf Textilien Barriereeffekte zu generieren und die an sich bereits Soil-Release-Effekte ermöglichen, können diese Soil-Release-Effekte noch gesteigert werden.Compositions according to the invention also find application in that a composition comprising a proportion of at least one reacted compound of one of the formulas (VII) or (VIII) or (IX) or (X) or (XI), preferably (Xla), in combination with polymers , which are suitable for generating barrier effects on textiles, and the composition thus obtained is used for the treatment of fiber materials for achieving or increasing soil release effects. Thus, it is possible, using inventive compositions and polymers which are suitable for generating barrier effects on textiles, but which in themselves do not allow soil release effects to achieve a certain level of soil release properties on textiles. When using compositions according to the invention with polymers which are suitable for generating barrier effects on textiles and that already allow for soil release effects, these soil release effects can be further enhanced.
Bei den letzten beiden Anwendungen können die erfindungsgemäßen Zusammensetzungen als Tensid oder Cotensid bei der Emulgierung der Polymere zum Einsatz kommen, sie können aber auch nach Emulgierung den Polymeremulsionen zugesetzt werden, wo sie dann bei der Behandlung von Fasermaterialien als Carrier ein besseres Einbringen der Polymere in die Fasermaterialien ermöglichen.In the last two applications, the compositions according to the invention can be used as surfactant or cosurfactant in the emulsification of the polymers, but they can also be added to the polymer emulsions after emulsification, where they then in the treatment of fiber materials as a carrier better introduction of the polymers in the Enable fiber materials.
Eine weitere mögliche Anwendung ist die, dass eine erfindungsgemäße Zusammensetzung zum Einbringen von Radikale abfangenden Substanzen auf Fasermaterialien eingesetzt wird, insbesondere eine Zusammensetzung enthaltend einen Anteil an einer umgesetzten Verbindung der Formeln (II), (IV) oder (V) mit X = S, als Beispiele für Radikale abfangende Substanzen seien hier Vitamin C oder Vitamin E genannt, die eine antioxidative Wirkung aufweisen.A further possible application is that a composition according to the invention is used for introducing radical scavenging substances onto fiber materials, in particular a composition comprising a proportion of a reacted compound of the formulas (II), (IV) or (V) where X = S, as examples of radical scavenging substances are here called vitamin C or vitamin E, which have an antioxidant effect.
Eine weitere mögliche Anwendung ist die, dass eine Zusammensetzung, die einen optischen Aufheller, insbesondere auf einer Stilbenstruktur basierend, oder einen UV-Absorber, vorzugsweise in umgesetzter Form, enthält, zum Einbringen von optischen Aufhellern, insbesondere auf einer Stilbenstruktur basierend, oder von UV-Absorbern auf Fasermaterialien eingesetzt wird.Another possible application is that a composition containing an optical brightener, especially based on a stilbene structure, or a UV absorber, preferably in reacted form, for introducing optical brighteners, in particular based on a stilbene structure, or of UV Absorbers on fiber materials is used.
Ein Beispiel von einem geeigneten UV-Absorber ist TINUVIN® 1130 der Firma BASF. Geeignete UV-Absorber sind auch die Verbindungen 2-(2-Hydroxy-5-methylphenyl)-benzotriazol und 2-Hydroxy-4-methoxybenzophenon sowie Polyethylenglykolmono-(distyrylphenyl)ether.An example of a suitable UV absorber is TINUVIN ® 1130 from BASF. Suitable UV absorbers are also the compounds 2- (2-hydroxy-5-methylphenyl) benzotriazole and 2-hydroxy-4-methoxybenzophenone and polyethylene glycol mono- (distyrylphenyl) ether.
Ein weiterer Aspekt der Erfindung ist eine Verbindung der Formel (XII),
alle Reste R1 und R2 unabhängig voneinander für H oder für einen linearen oder verzweigten Alkylrest mit 1 bis 5 Kohlenstoffatomen, vorzugsweise für CH3 oder C2H5 oder C3H7, oder für
wobei m eine Zahl von 4 bis 8 und q eine Zahl von 1 bis 3 ist und
wobei der Rest R13 für H oder einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 4 Kohlenstoffatomen, bevorzugt für H oder n-C4H9 steht,
mit der Maßgabe, dass mindestens einer der anwesenden Reste R1 oder R2 nicht für H steht.Another aspect of the invention is a compound of the formula (XII)
all radicals R 1 and R 2 independently of one another are H or a linear or branched one Alkyl radical having 1 to 5 carbon atoms, preferably CH 3 or C 2 H 5 or C 3 H 7 , or for
where m is a number from 4 to 8 and q is a number from 1 to 3 and
where the radical R 13 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably H or nC 4 H 9 ,
with the proviso that at least one of the radicals R 1 or R 2 present does not stand for H.
Die Herstellung der Verbindungen der Formel (XII) kann nach ähnlichen Methoden wie für die Herstellung der bereits bekannten Verbindungen der untenstehenden Formel erfolgen,
Die Erfindung wird nachfolgend durch Beispiele veranschaulicht.The invention will now be illustrated by way of example.
207,3 g einer wässrigen 60%igen Glyoxallösung wurden bei Raumtemperatur vorgelegt und mit einer verdünnten Natriumhydroxidlösung auf pH 5,0 eingestellt.207.3 g of a 60% glyoxal aqueous solution was charged at room temperature and adjusted to pH 5.0 with a dilute sodium hydroxide solution.
Unter Rühren wurden anschließend 279,9 g Dimethylolharnstoff zugegeben. Es resultierte dabei eine weiße pastöse Masse. Danach wurden 21,8 g einer 37%igen Formalinlösung und 72,6 g Methanol zugegeben und auf 40°C aufgeheizt.While stirring, then 279.9 g of dimethylolurea were added. This resulted in a white pasty mass. Thereafter, 21.8 g of a 37% formalin solution and 72.6 g of methanol were added and heated to 40 ° C.
Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidiösung bzw. Salzsäure auf pH 7,0 eingestellt und auf 70°C geheizt. Dabei wurde die Vorlage dünnflüssig, klar und hellgelb.Subsequently, the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree. The original became thin, clear and pale yellow.
Nach einer Stunde bei 70°C erfolgte die Kühlung des Ansatzes auf 50°C.After one hour at 70 ° C, the cooling of the batch was carried out at 50 ° C.
Danach wurden 183,7 g MARLIPAL® O 13/50 (Oxoalkohol C13 mit 5 Mol EO, erhältlich von der Firma Sasol) und 265,9 g Methanol zugegeben.Thereafter, 183.7 g of MARLIPAL O ® were 13/50 (C13 oxo alcohol with 5 moles of EO available from Sasol) was added and 265.9 g of methanol.
Bei 50°C erfolgte der Start der Veretherung durch Zugabe von 5,0 g konzentrierter Salzsäure (31-33 Gew.-%). Durch die exotherme Reaktion resultierte ein Temperaturanstieg von ca. 8°C. Nach 7 Minuten erfolgte der Stop der Veretherung durch Zugabe von 2,0 g einer 50%igen Natriumhydroxidlösung und 0,3 g Triethanolamin (99%ig). Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 5,9 eingestellt. Danach erfolgte während 6 Stunden bei max. 70°C und unter Vakuum bis zu einem absoluten Druck von 100 mbar die Abdestillation von 228 g eines Methanol/Wasser-Gemisches.At 50 ° C., the etherification was started by adding 5.0 g of concentrated hydrochloric acid (31-33% by weight). The exothermic reaction resulted in a temperature increase of about 8 ° C. After 7 minutes, the etherification was stopped by adding 2.0 g of a 50% sodium hydroxide solution and 0.3 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.9 with dilute sodium hydroxide solution or hydrochloric acid. This was followed for 6 hours at max. 70 ° C and under vacuum to an absolute pressure of 100 mbar distilling off 228 g of a methanol / water mixture.
Nach Abkühlung auf Raumtemperatur resultierte ein relativ dünnflüssiges, klares und hellgelbes Produkt.After cooling to room temperature resulted in a relatively thin liquid, clear and pale yellow product.
Zur Prüfung der Eigenschaften der erfindungsgemäßen Zusammensetzung wurde eine wässrige Ausrüstungsflotte angesetzt enthaltend 220 g/l Zusammensetzung gemäß Beispiel 1, 110 g/l KNITTEX-KATALYSATOR UMP (erhältlich von der Firma Huntsman) und 1 g/l konzentrierte Salzsäure (31-33 Gew.-%). Zum Vergleich wurde eine wässrige Ausrüstungsflotte angesetzt enthaltend 220 g/l KNITTEX® FA CONC (Dimethyloldihydroxyethylenharnstoff, methanolverethert, erhältlich von der Firma Huntsman), 110 g/l KNITTEX-KATALYSATOR UMP (wässrige Lösung mehrerer organischer und anorganischer saurer Verbindungen, erhältlich von der Firma Huntsman) und 1 g/l konzentrierte Salzsäure (31-33 Gew.-%). Abschnitte eines gebleichten, nicht optisch aufgehellten Hemdstoffgewebes aus 100% Baumwolle mit einem Flächengewicht von 110 g/m2 wurden mit wässrigen Flotten in den o. a. Zusammensetzungen auf einem Laborfoulard mit einer Flottenaufnahme von 66 Gew.-% imprägniert, anschließend auf eine Restfeuchte von 7 % getrocknet und dann für 20 Stunden bei 30°C gelagert. Danach wurden die Muster 10 Minuten bei 40°C mit einer wässrigen Lösung von 10 g/l Natriumcarbonat gewaschen, anschließend einmal mit warmem Wasser, danach einmal mit kaltem Wasser, weiterhin mit einer wässrigen Lösung von 0,5 g/l INVATEX® AC (wässrige Lösung von Zitronensäure mit einem geringen Gehalt eines Polymers, erhältlich von der Firma Huntsman) neutralisiert, anschließend mit kaltem Wasser gespült und zuletzt für 10 Minuten bei 110° getrocknet. Anschließend erfolgte die Beurteilung der hydrophilen Eigenschaften der so ausgerüsteten Textilabschnitte bzw. auch jeweils eines nicht ausgerüsteten Textilabschnittes gemäß Water Drop Test AATCC Test Method 79, Absorbency of Textiles (Tropfentest) und der Wicking-Eigenschaften gemäß Wicking Test, AATCC Test Methode 197-2011 (Steighöhentest zur Beurteilung der Kapillarität von Textilien). Beim Tropfentest bedeuten niedere Sekunden-Werte bessere hydrophile Eigenschaften. Dabei wird ein Wassertropfen auf ein Gewebe aufgetragen und die Benetzung des Gewebes beobachtet. Der Sekunden-Wert beschreibt dabei den Zeitpunkt der kompletten Benetzung durch den Wassertropfen. Beim Wicking Test wird ein Textilmuster vertikal mit der Unterkante in Wasser eingetaucht und beobachtet, wie hoch die Flüssigkeit nach einer bestimmten Zeit im Gewebe gestiegen ist. Dabei wird das Gewebe mal mit der Kette und mal mit dem Schuss in vertikaler Richtung eingespannt. Die Zusammensetzung nach dem erfindungsgemäßen Beispiel Nr. 1 zeigt dabei eindeutig bessere hydrophile Effekte als der Vergleichsversuch auf Basis von KNITTEX FA CONC, siehe dazu Tabellen 1 und 2.
Die Abdestillation des Methanols gemäß Beispiel 1 kann über unterschiedliche Zeitspannen erfolgen. Mit steigender Destillationszeit steigt auch der Grad der Umsetzung von MARLIPAL O 13/50 mit dem Dimethyloldihydroxyethylenharnstoff (DMDHEH). Dementsprechend kann man die Umsetzung so steuern, dass Produkte mit unterschiedlichen Eigenschaften entstehen.The distilling off of the methanol according to Example 1 can take place over different periods of time. With increasing distillation time, the degree of conversion of MARLIPAL O 13/50 with the Dimethyloldihydroxyethylenharnstoff (DMDHEH) increases. Accordingly, one can control the implementation so that products with different properties arise.
Beispiel 1 wurde mit unterschiedlichen Zeitspannen für die Destillationszeit wiederholt, die entsprechenden Werte dafür finden sich in der untenstehenden Tabelle 3.
Von den erhaltenen Produkten wurde eine wässrige Dispersion mit einem Gehalt von 200 g/l hergestellt. Diese wurden kräftig geschüttelt und dann für 30 Minuten ruhen gelassen. An den wässrigen Dispersionen ist zu erkennen, dass mit steigender Destillationszeit auch deren Fähigkeit zur Schaumbildung steigt, siehe dazu Abbildung 1. Of the products obtained, an aqueous dispersion having a content of 200 g / l was prepared. These were shaken vigorously and then allowed to rest for 30 minutes. It can be seen from the aqueous dispersions that their ability to foam increases with increasing distillation time, see Figure 1.
Nach längerer Ruhezeit und Verschwinden des Schaums war erkennbar, dass mit steigender Destillationszeit bzw. mit steigendem Grad der Umetherung die entsprechenden wässrigen Dispersionen klarer bzw. durchsichtiger werden, siehe dazu Abbildung 2. Beide Auswertungen deuten darauf hin, dass steigende Destillationszeit und damit ein größerer Umsetzungsgrad von MARLIPAL O 13/50 Reaktionsprodukte mit erhöhten tensidischen Eigenschaften ergeben. Mit steigender Destillationszeit steigt auch die Viskosität des jeweils erhaltenen Produktes.After a longer period of rest and disappearance of the foam, it could be seen that with increasing distillation time or with increasing degree of transetherification, the corresponding aqueous dispersions become clearer or more transparent, see Figure 2. Both evaluations indicate that increasing distillation time and thus a greater degree of conversion of MARLIPAL O 13/50 results in reaction products with increased surfactant properties. As the distillation time increases, so does the viscosity of the product obtained.
150,0 g einer wässrigen 60%igen Glyoxallösung wurden bei Raumtemperatur vorgelegt und mit einer verdünnten Natriumhydroxidlösung auf pH 5,0 eingestellt.150.0 g of a 60% glyoxal aqueous solution was charged at room temperature and adjusted to pH 5.0 with a dilute sodium hydroxide solution.
Unter Rühren wurden anschließend 202,5 g Dimethylolharnstoff zugegeben. Es resultierte dabei eine weiße pastöse Masse. Danach wurden 15,8 g einer 37%igen Formalinlösung und 52,5 g Methanol zugegeben und auf 40°C aufgeheizt.With stirring, 202.5 g of dimethylolurea were then added. This resulted in a white pasty mass. Thereafter, 15.8 g of a 37% formalin solution and 52.5 g of methanol were added and heated to 40 ° C.
Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 7,0 eingestellt und auf 70°C geheizt. Dabei wurde die Vorlage dünnflüssig, klar und hellgelb.Subsequently, the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree. The original became thin, clear and pale yellow.
Nach einer Stunde bei 70°C erfolgte die Kühlung des Ansatzes auf 50°C.After one hour at 70 ° C, the cooling of the batch was carried out at 50 ° C.
Danach wurden 202,5 g Methanol zugegeben.Thereafter, 202.5 g of methanol were added.
Bei 50°C erfolgte der Start der Veretherung durch Zugabe von 3,6 g konzentrierter Salzsäure (31-33 Gew.-%). Durch die exotherme Reaktion resultierte ein Temperaturanstieg von ca. 8°C. Nach 7 Minuten erfolgte der Stop der Veretherung durch Zugabe von 1,4 g einer 50%igen Natriumhydroxidlösung und 0,2 g Triethanolamin (99%ig). Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 5,9 eingestellt. Danach erfolgte während ca. 2 Stunden bei max. 70°C und unter Vakuum bis zu einem absoluten Druck von 100 mbar, die Abdestillation von 197 g eines Methanol / Wasser-Gemisches.At 50 ° C, the etherification was started by the addition of 3.6 g of concentrated hydrochloric acid (31-33 wt .-%). The exothermic reaction resulted in a temperature increase of about 8 ° C. After 7 minutes, the etherification was stopped by adding 1.4 g of a 50% sodium hydroxide solution and 0.2 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.9 with dilute sodium hydroxide solution or hydrochloric acid. It was then carried out for about 2 hours at max. 70 ° C and under vacuum to an absolute pressure of 100 mbar, distilling off 197 g of a methanol / water mixture.
Nach Abkühlung auf Raumtemperatur wurden 132,9 g MARLIPAL O 13/50 eingerührt.After cooling to room temperature, 132.9 g of MARLIPAL O 13/50 were stirred in.
Der wesentliche Unterschied zu Beispiel 1 ist also der, dass Oxoalkohol C13 mit 5 Mol EO nach Abdestillation von Methanol zugegeben wurde, also keine Veretherung mit Oxoalkohol C13 mit 5 Mol EO stattfand.The essential difference from Example 1 is therefore that oxo alcohol C13 was added with 5 moles of EO after distilling off methanol, that is, no etherification with oxoalcohol C13 with 5 moles of EO took place.
Es resultierte ein relativ dünnflüssiges, klares und hellgelbes Produkt.This resulted in a relatively thin liquid, clear and pale yellow product.
Zur Prüfung der Eigenschaften der erfindungsgemäßen Zusammensetzung wurde eine wässrige Ausrüstungsflotte angesetzt enthaltend 220 g/l Zusammensetzung gemäß Beispiel 2, 100 g/l KNITTEX-KATALYSATOR UMP, 1 g/l konzentrierte Salzsäure (31-33 Gew.-%) und 50 g/l TURPEX® ACN NEU (wässrige Dispersion eines Wachses, eine übliche Rezepturkomponente für die Vernetzung von Baumwollgewebe, erhältlich von der Firma Huntsman). Zum Vergleich wurde eine wässrige Ausrüstungsflotte angesetzt enthaltend 220 g/l KNITTEX® FA CONC, 100 g/l KNITTEX-KATALYSATOR UMP, 1 g/l konzentrierte Salzsäure (31-33 Gew.-%) und 50 g/l TURPEX® ACN NEU. Abschnitte eines gefärbten, nicht optisch aufgehellten Hemdstoffgewebes aus 100% Baumwollpoplin wurden mit wässrigen Flotten in den o. a. Zusammensetzungen auf einem Laborfoulard mit einer Flottenaufnahme von 66 Gew.-% imprägniert, anschließend auf eine Restfeuchte von 7 % getrocknet und dann für 20 Stunden bei 30°C gelagert. Danach wurden die Muster 10 Minuten bei 40°C mit einer wässrigen Lösung von 10 g/l Natriumcarbonat gewaschen, anschließend einmal mit warmem Wasser, danach mit kaltem Wasser gewaschen, weiterhin mit einer wässrigen Lösung von 0,5 g/l INVATEX® AC neutralisiert, anschließend mit kaltem Wasser gespült und zuletzt für 10 Minuten bei 110° getrocknet. Anschließend erfolgte die Beurteilung der hydrophilen Eigenschaften der so ausgerüsteten Textilabschnitte bzw. auch jeweils eines nicht ausgerüsteten Textilabschnittes gemäß Water Drop Test AATCC Test Method 79, Absorbency of Textiles (Tropfentest) und der Wicking-Eigenschaften gemäß Wicking Test, AATCC Test Methode 197-2011 (Steighöhentest zur Beurteilung der Kapillarität von Textilien). Außerdem wurde auch der Formaldehydgehalt auf dem Gewebe nach JIS L 1041:2011, einem japanischen Standard (entspricht ISO 14184-1:1998), bestimmt. Die Zusammensetzung nach dem erfindungsgemäßen Beispiel Nr. 2 zeigt dabei eindeutig bessere hydrophile Effekte und niedrigeren Formaldehydgehalt als der Vergleichsversuch auf Basis von KNITTEX FA CONC, siehe dazu Tabellen 4 und 5.
177,5 g einer wässrigen 60%igen Glyoxallösung wurden bei Raumtemperatur vorgelegt und mit einer verdünnten Natriumhydroxidlösung auf pH 5,0 eingestellt.177.5 g of a 60% glyoxal aqueous solution was charged at room temperature and adjusted to pH 5.0 with a dilute sodium hydroxide solution.
Unter Rühren wurden anschließend 239,6 g Dimethylolharnstoff zugegeben. Es resultierte dabei eine weiße pastöse Masse. Danach wurden 18,7 g einer 37%igen Formalinlösung und 62,2 g Methanol zugegeben und auf 40°C aufgeheizt.With stirring, 239.6 g of dimethylolurea were then added. This resulted in a white pasty mass. Thereafter, 18.7 g of a 37% formalin solution and 62.2 g of methanol were added and heated to 40 ° C.
Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 7,0 eingestellt und auf 70°C geheizt. Dabei wurde die Vorlage dünnflüssig, klar und hellgelb.Subsequently, the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree. The original became thin, clear and pale yellow.
Nach einer Stunde bei 70°C erfolgte die Kühlung des Ansatzes auf 50°C.After one hour at 70 ° C, the cooling of the batch was carried out at 50 ° C.
Danach wurden 78,6 g MARLIPAL O 13/50 (Oxoalkohol C13 mit 5 Mol EO) und 227,6 g Methanol zugegeben.Thereafter, 78.6 g of MARLIPAL O 13/50 (oxoalcohol C 13 with 5 moles of EO) and 227.6 g of methanol were added.
Bei 50°C erfolgte der Start der Veretherung durch Zugabe von 4,3 g konzentrierter Salzsäure (31-33%). Durch die exotherme Reaktion resultierte ein Temperaturanstieg von ca. 9°C. Nach 8 Minuten erfolgte der Stop der Veretherung durch Zugabe von 1,7 g einer 50%igen Natriumhydroxidlösung und 0,2 g Triethanolamin (99%ig). Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 5,9 eingestellt.At 50 ° C, the etherification was started by adding 4.3 g of concentrated hydrochloric acid (31-33%). The exothermic reaction resulted in a temperature increase of about 9 ° C. After 8 minutes, the etherification was stopped by adding 1.7 g of a 50% sodium hydroxide solution and 0.2 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.9 with dilute sodium hydroxide solution or hydrochloric acid.
Danach erfolgte die Zugabe von 36,7 g trans-4-Hydroxystilben 98%. Während des anschließenden Aufheizens auf 70°C veränderte sich das Aussehen der Vorlage von trüb und orangefarben zu klar und hellgelb.This was followed by the addition of 36.7 g of trans-4-hydroxystilbene 98%. During the subsequent heating to 70 ° C, the appearance of the original changed from hazy and orange to clear and pale yellow.
Danach erfolgte während 6 Stunden bei max. 70°C und unter Vakuum bis zu einem absoluten Druck von 100 mbar die Abdestillation von 195,2 g eines Methanol/ WasserGemisches.This was followed for 6 hours at max. 70 ° C and under vacuum to an absolute pressure of 100 mbar distilling off 195.2 g of a methanol / water mixture.
Anschließend wurde der Ansatz gekühlt. Nach Erreichen von ca. 45°C erfolgte die Zugabe von 45 g entmineralisiertem Wasser.Subsequently, the batch was cooled. After reaching about 45 ° C, the addition of 45 g of demineralized water.
Danach wurde die Vorlage mit verdünnter Natriumhydroxidlösung von pH 5,2 auf pH 6,5 eingestellt.Thereafter, the original was adjusted to pH 6.5 with dilute sodium hydroxide solution of pH 5.2.
Nach Abkühlung auf Raumtemperatur resultierte ein pastöses, milchig trübes und cremefarbenes Produkt.After cooling to room temperature resulted in a pasty, milky cloudy and cream-colored product.
In einem Reaktor wurden bei Raumtemperatur 80,2 g Methanol, 243,2 g wässriger Formaldehyd mit 37 Gew.-% und 114,3 g Thioharnstoff vorgelegt. Der pH-Wert wurde auf 8,2 mit verdünnter Natriumhydroxidlösung eingestellt. Der Ansatz wurde 5 Stunden bei pH 8,2 auf 54°C geheizt.At room temperature, 80.2 g of methanol, 243.2 g of 37% by weight aqueous formaldehyde and 114.3 g of thiourea were placed in a reactor. The pH was adjusted to 8.2 with dilute sodium hydroxide solution. The batch was heated to 54 ° C for 5 hours at pH 8.2.
Danach wurden 137 g MARLIPAL O 13/50 (Oxoalkohol C13 mit 5 Mol EO) und 174,3 g Methanol zugegeben. Die Temperatur lag bei 47°C.Thereafter, 137 g of MARLIPAL O 13/50 (oxoalcohol C 13 with 5 moles of EO) and 174.3 g of methanol were added. The temperature was 47 ° C.
Der Start der Veretherung erfolgt durch Zugabe von 19,5 g konzentrierter Salzsäure (32%). Durch die exotherme Reaktion resultierte ein Temperaturanstieg von 9°C. Nach 9 Minuten erfolgte der Stopp der Veretherung durch Zugabe von 7,5 g einer 50%igen Natriumhydroxidlösung.The etherification is started by adding 19.5 g of concentrated hydrochloric acid (32%). The exothermic reaction resulted in a temperature increase of 9 ° C. After 9 minutes, the etherification was stopped by adding 7.5 g of a 50% sodium hydroxide solution.
Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 6,0 eingestellt. Danach erfolgte während 6,5 Stunden bei max. 70°C und unter Vakuum bis zu einem absoluten Druck von 90 mbar am Ende der Zeitspanne die Abdestillation von 445 ml eines Methanol/Wasser-Gemisches.Subsequently, the original was adjusted to pH 6.0 with dilute sodium hydroxide solution or hydrochloric acid. This was followed during 6.5 hours at max. 70 ° C and under vacuum to an absolute pressure of 90 mbar at the end of the period distilling off 445 ml of a methanol / water mixture.
Nach Abkühlung auf Raumtemperatur resultierte ein sehr dickes, trübes Produkt mit einem Trockengehalt von 98 Gew.-%.After cooling to room temperature resulted in a very thick, turbid product with a solids content of 98 wt .-%.
Mercerisierte Baumwollstücke wurden nach dem Pad-Batch Verfahren (mittels Foulard) mit einer Farbstofflösung enthaltend 2,4 g/l NOVACRON® Blue C-R (Reaktivfarbstoff von HUNTSMAN), 15 ml/l Natriumhydroxid 36°B, 70 ml/l Natriumsilikat 38-40°B, 2 g/l LYOPRINT® RG (Färbereihilfsmittel von HUNTSMAN) und 1 g/l CIBAFLOW® PAD (Färbereihilfsmittel von HUNTSMAN) gefärbt. Nach dem Foulardieren, mit einer Flottenaufnahme von 70 Gew.-%, wurden die Textilstücke 16 Stunden bei Raumtemperatur gelagert, dann dreimal mit Wasser gespült (kalt, bei Siedetemperatur, kalt) und getrocknet.Mercerised cotton pieces were pad-batched with a dye solution containing 2.4 g / l NOVACRON® Blue CR (HUNTSMAN reactive dye), 15 ml / l sodium hydroxide 36 ° B, 70 ml / l sodium silicate 38-40 B, 2 g / l LYOPRINT® RG (dyeing auxiliaries from HUNTSMAN) and 1 g / l CIBAFLOW® PAD (dyeing auxiliaries from HUNTSMAN). After padding, with a liquor pick-up of 70 wt .-%, the fabric pieces were stored for 16 hours at room temperature, then rinsed three times with water (cold, at boiling temperature, cold) and dried.
Die BPO-Echtheit wurde mittels "Wako Test", (interne Testmethode von HUNTSMAN) bestimmt. BPO steht hier für Benzoylperoxid, genauer gesagt Dibenzoylperoxid, das in dermatologischen Präparaten eingesetzt wird und nach Auftragung auf der Haut infolge seiner Eigenschaft, leicht Radikale zu bilden, die Farbe von Textilien schädigen kann. Dafür wurden 50 g Wasser, 0,1 g Wako V50 (2,2'-Azobis[2-methylpropionamidine] Dihydrochlorid, CAS NO. 2997-92-4), 0,15 g der wie oben beschrieben hergestellten erfindungsgemäßen Zusammensetzung und 1 g gefärbtes Textilstück 2 Stunden bei 65 - 70°C gerührt. Das Textilstück wurde dann gespült und getrocknet. Das Textilstück war danach leicht entfärbt.The BPO authenticity was determined by means of "Wako test", (internal test method of HUNTSMAN). BPO stands for benzoyl peroxide, more specifically dibenzoyl peroxide, which is used in dermatological preparations and, when applied to the skin, can damage the color of textiles due to its ability to easily form radicals. For this, 50 g of water, 0.1 g of Wako V50 (2,2'-azobis [2-methylpropionamidine] dihydrochloride, CAS NO 2997-92-4), 0.15 g of the inventive composition prepared as described above and 1 g dyed textile piece for 2 hours at 65 - 70 ° C stirred. The piece of fabric was then rinsed and dried. The textile piece was then slightly discolored.
Als Referenz wurden 50 g Wasser, 0,1 g Wako V50, und 1 g gefärbtes Textilstück 2 Stunden bei 65 - 70°C gerührt. Das Textilstück wurde dann gespült und getrocknet. Das Textilstück war danach sehr stark entfärbt.For reference, 50 g of water, 0.1 g of Wako V50, and 1 g of dyed fabric were stirred for 2 hours at 65-70 ° C. The piece of fabric was then rinsed and dried. The textile piece was then very much discolored.
Die Auswertung erfolgte via Farbmetrik.
Der Versuch zeigt, dass die wie oben beschrieben hergestellte erfindungsgemäße Zusammensetzung eindeutig radikalabfangende Eigenschaften hat.The experiment shows that the composition according to the invention prepared as described above clearly has radical scavenging properties.
Ein gefärbtes Textilstück wurde mit 20 g/l der wie oben beschrieben hergestellten erfindungsgemäßen Zusammensetzung nach dem Pad-Dry-Thermofix Verfahren (beschrieben z. B. in der
159,7 g einer wässrigen 60%igen Glyoxallösung wurden bei Raumtemperatur vorgelegt und mit einer verdünnten Natriumhydroxidlösung auf pH 5,0 eingestellt.159.7 g of a 60% glyoxal aqueous solution was charged at room temperature and adjusted to pH 5.0 with a dilute sodium hydroxide solution.
Unter Rühren wurden anschließend 215,8 g Dimethylolharnstoff zugegeben. Es resultierte dabei eine weiße pastöse Masse. Danach wurden 16,8 g einer 37%igen Formalinlösung und 56,0 g Methanol zugegeben und auf 40°C aufgeheizt.With stirring, 215.8 g of dimethylolurea were then added. This resulted in a white pasty mass. Thereafter, 16.8 g of a 37% formalin solution and 56.0 g of methanol were added and heated to 40 ° C.
Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 7,0 eingestellt und auf 70°C geheizt. Dabei wurde die Vorlage dünnflüssig, klar und hellgelb.Subsequently, the original was adjusted to pH 7.0 with dilute sodium hydroxide solution or hydrochloric acid and heated to 70.degree. The original became thin, clear and pale yellow.
Nach einer Stunde bei 70°C erfolgte die Kühlung des Ansatzes auf 50°C.After one hour at 70 ° C, the cooling of the batch was carried out at 50 ° C.
Danach wurden nacheinander 107,6 g MARLIPAL O 13/50 (Oxoalkohol C13 mit 5 Mol EO) und 109,7 g ZONYL® Fluorosurfactant FS-300 (40%ig in Wasser, ein ethoxylierter Perfluoralkylethylalkohol, erhältlich von DuPont) und 203,5 g Methanol zugegeben.Thereafter 107.6 g of MARLIPAL O 13/50 (oxoalcohol C 13 with 5 moles of EO) and 109.7 g of ZONYL® fluorosurfactant FS-300 (40% in water, an ethoxylated perfluoroalkylethyl alcohol, available from DuPont) and 203, 5 g of methanol added.
Bei 50°C erfolgte der Start der Veretherung durch Zugabe von 7,8 g konzentrierter Salzsäure (31-33 Gew.-%). Durch die exotherme Reaktion resultierte ein Temperaturanstieg von ca. 9°C. Nach 9 Minuten erfolgte der Stop der Veretherung durch Zugabe von 4,8 g einer 50%igen Natriumhydroxidlösung und 0,2 g Triethanolamin (99%ig). Anschließend wurde die Vorlage mit verdünnter Natriumhydroxidlösung bzw. Salzsäure auf pH 5,8 eingestellt.At 50 ° C., the etherification was started by adding 7.8 g of concentrated hydrochloric acid (31-33% by weight). The exothermic reaction resulted in a temperature increase of about 9 ° C. After 9 minutes, the etherification was stopped by adding 4.8 g of a 50% sodium hydroxide solution and 0.2 g of triethanolamine (99% pure). Subsequently, the template was adjusted to pH 5.8 with dilute sodium hydroxide solution or hydrochloric acid.
Danach wurde die Vorlage auf 70°C geheizt.Thereafter, the template was heated to 70 ° C.
Anschließend erfolgte während 6 Stunden bei max. 70°C und unter Vakuum bis zu einem absoluten Druck von 100 mbar die Abdestillation von 175,8 g eines Methanol / Wasser- Gemisches.This was followed for 6 hours at max. 70 ° C and under vacuum to an absolute pressure of 100 mbar distilling off 175.8 g of a methanol / water mixture.
Danach wurde der Ansatz gekühlt. Nach Erreichen von ca. 45°C erfolgte die Zugabe von 47 g entmineralisiertem Wasser.Thereafter, the batch was cooled. After reaching about 45 ° C, the addition was of 47 g of demineralized water.
Danach wurde die Vorlage mit verdünnter Natriumhydroxidlösung von pH 5,2 auf pH 6,5 eingestellt.Thereafter, the original was adjusted to pH 6.5 with dilute sodium hydroxide solution of pH 5.2.
Nach Abkühlung auf Raumtemperatur resultierte ein hellgelbes, klares Produkt.After cooling to room temperature resulted in a light yellow, clear product.
Claims (17)
wobei die Zusammensetzung zusätzlich gegebenenfalls einen Alkohol der Formel (VI) enthalten kann,
R4-OH (VI) wobei alle Reste R1 und R2 unabhängig voneinander für H oder für einen linearen oder verzweigten Alkylrest mit 1 bis 5 Kohlenstoffatomen, vorzugsweise für CH3 oder C2H5 oder C3H7, oder für
wobei m eine Zahl von 4 bis 8 ist und t 0 oder 1 ist und p eine Zahl von 8 bis 20 und q eine Zahl von 1 bis 3 ist,
alle Reste R3 unabhängig voneinander für H oder für -CH2-O-R2 stehen, wobei in Formel (V) mindestens ein Rest R3 für -CH2-O-R2 steht,
X für O oder S steht,
der Rest R4 für einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 18, bevorzugt mit 1 bis 4 Kohlenstoffatomen, besonders bevorzugt für CH3 oder C2H5 steht,
R5 für einen linearen oder verzweigten Alkylrest oder Alkenylrest mit 4 bis 18, vorzugsweise mit 8 bis 18 Kohlenstoffatomen, besonders bevorzugt für einen verzweigten Alkylrest mit 13 Kohlenstoffatomen, steht oder für einen, gegebenenfalls durch einen oder mehrere Kohlenwasserstoffreste substituierten, aromatischen Rest, insbesondere für Phenyl, Tolyl oder Benzyl,
wobei k + y = 2 ist und k den Wert 1 oder 2 hat, einer der Reste R6 und R7 für H und der andere für H oder für CH3 steht, I für eine Zahl von 0 bis 20, vorzugsweise von 2 bis 20, besonders bevorzugt von 2 bis 8, insbesondere für 2 bis 6, steht, wobei bei Anwesenheit einer Verbindung der Formel (VII) mit I = 0 auch eine Verbindung der Formel (VII) mit I >= 2 anwesend sein muss, n für eine Zahl von 2 bis 20, vorzugsweise 2 bis 8, besonders bevorzugt von 2 bis 6, steht und R8 für H oder für
wobei r eine Zahl von 2 bis 15, s eine Zahl von 0 bis 20, v eine Zahl von 1 bis 18 ist und R11 für H oder CH3 steht und wobei im Siloxan der Formel (X) sowohl die Dimethylsiloxyeinheiten als auch die Methylsiloxyeinheiten mit Polyoxyalkylengruppen aufweisenden Resten beliebig über die Siloxankette verteilt sein können,
wobei der Rest R12 für H oder einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 4 Kohlenstoffatomen, bevorzugt für CH3 oder t-C4H9, besonders bevorzugt für H steht,
wobei der Rest R13 für H oder einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 4 Kohlenstoffatomen, bevorzugt für H oder n-C4H9 steht,
wobei w für eine Zahl von 2 bis 9, bevorzugt von 3 bis 8 steht, u 0 oder bevorzugt 1 ist, Y ein zweiwertiger Rest ist enthaltend Kohlenstoff und Wasserstoff und ggf. Schwefel und/oder Stickstoff und/oder Sauerstoff,
wobei die Zusammensetzung mindestens für den Fall, dass eine Verbindung der Formel (VII) mit I = 6 - 8 und t = 0 enthalten ist, ein Umsetzungsprodukt aus einer oder mehreren Verbindungen der Formeln (II) bis (V) mit einer oder mehreren Verbindungen der Formel (VII) und gegebenenfalls der Formel (VI) enthält.Composition which comprises at least one compound of the formula (II) or of the formula (III) or of the formula (IV) or of the formula (V)
wherein the composition may additionally optionally contain an alcohol of the formula (VI),
R 4 -OH (VI) where all radicals R 1 and R 2 independently of one another are H or a linear or branched alkyl radical having 1 to 5 carbon atoms, preferably CH 3 or C 2 H 5 or C 3 H 7 , or
wherein m is a number from 4 to 8 and t is 0 or 1 and p is a number from 8 to 20 and q is a number from 1 to 3,
all radicals R 3 independently of one another are H or -CH 2 -OR 2 , where in formula (V) at least one radical R 3 is -CH 2 -OR 2 ,
X stands for O or S,
the radical R 4 is a linear or optionally branched alkyl radical having 1 to 18, preferably having 1 to 4, carbon atoms, particularly preferably CH 3 or C 2 H 5 ,
R 5 is a linear or branched alkyl radical or alkenyl radical having 4 to 18, preferably having 8 to 18 carbon atoms, particularly preferably a branched alkyl radical having 13 carbon atoms, or represents an optionally substituted by one or more hydrocarbon radicals, aromatic radical, in particular Phenyl, tolyl or benzyl,
where k + y = 2 and k is 1 or 2, one of R 6 and R 7 is H and the other is H or CH 3, I is a number from 0 to 20, preferably from 2 to 20, more preferably from 2 to 8, in particular from 2 to 6, wherein in the presence of a compound of formula (VII) with I = 0 and a compound of formula (VII) must be present with I> = 2, n for a number from 2 to 20, preferably 2 to 8, more preferably from 2 to 6, and R 8 is H or for
wherein r is a number from 2 to 15, s is a number from 0 to 20, v is a number from 1 to 18 and R 11 is H or CH 3 and wherein in the siloxane of the formula (X) both the dimethylsiloxy and the methylsiloxy with radicals having polyoxyalkylene groups may be distributed as desired over the siloxane chain,
wherein the radical R 12 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably CH 3 or tC 4 H 9 , especially preferably stands for H,
where the radical R 13 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably H or nC 4 H 9 ,
where w is a number from 2 to 9, preferably from 3 to 8, u is 0 or preferably 1, Y is a bivalent radical containing carbon and hydrogen and optionally sulfur and / or nitrogen and / or oxygen,
wherein the composition is at least in the case that a compound of formula (VII) with I = 6-8 and t = 0 is included, a reaction product of one or more compounds of formulas (II) to (V) with one or more compounds of formula (VII) and optionally of formula (VI).
alle Reste R1 und R2 unabhängig voneinander für H oder für einen linearen oder verzweigten Alkylrest mit 1 bis 5 Kohlenstoffatomen, vorzugsweise für CH3 oder C2H5 oder C3H7, oder für
wobei m eine Zahl von 4 bis 8 und q eine Zahl von 1 bis 3 ist und
wobei der Rest R13 für H oder einen linearen oder gegebenenfalls verzweigten Alkylrest mit 1 bis 4 Kohlenstoffatomen, bevorzugt für H oder n-C4H9 steht,
mit der Maßgabe, dass mindestens einer der anwesenden Reste R1 oder R2 nicht für H steht.Compound of the formula (XII),
all radicals R 1 and R 2 independently of one another are H or a linear or branched alkyl radical having 1 to 5 carbon atoms, preferably CH 3 or C 2 H 5 or C 3 H 7 , or
where m is a number from 4 to 8 and q is a number from 1 to 3 and
where the radical R 13 is H or a linear or optionally branched alkyl radical having 1 to 4 carbon atoms, preferably H or nC 4 H 9 ,
with the proviso that at least one of the radicals R 1 or R 2 present does not stand for H.
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14179257.2A EP2980308A1 (en) | 2014-07-31 | 2014-07-31 | Compositions for the treatment of fibrous materials |
| CN201580036196.2A CN106471182B (en) | 2014-07-31 | 2015-07-29 | For handling the composition of fibrous material |
| PCT/EP2015/067332 WO2016016282A2 (en) | 2014-07-31 | 2015-07-29 | Compositions for treatment of fiber materials |
| ES15744199T ES2949983T3 (en) | 2014-07-31 | 2015-07-29 | Compositions for the treatment of fiber materials |
| EP15744199.9A EP3175033B1 (en) | 2014-07-31 | 2015-07-29 | Compositions for treatment of fiber materials |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14179257.2A EP2980308A1 (en) | 2014-07-31 | 2014-07-31 | Compositions for the treatment of fibrous materials |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| EP2980308A1 true EP2980308A1 (en) | 2016-02-03 |
Family
ID=51257366
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP14179257.2A Withdrawn EP2980308A1 (en) | 2014-07-31 | 2014-07-31 | Compositions for the treatment of fibrous materials |
| EP15744199.9A Active EP3175033B1 (en) | 2014-07-31 | 2015-07-29 | Compositions for treatment of fiber materials |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP15744199.9A Active EP3175033B1 (en) | 2014-07-31 | 2015-07-29 | Compositions for treatment of fiber materials |
Country Status (4)
| Country | Link |
|---|---|
| EP (2) | EP2980308A1 (en) |
| CN (1) | CN106471182B (en) |
| ES (1) | ES2949983T3 (en) |
| WO (1) | WO2016016282A2 (en) |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4133995A1 (en) | 1990-10-17 | 1992-04-23 | Ciba Geigy Ag | Two=stage two bath dyeing of cellulose hydrophobic fibre mixt. - using reactive dyestuff then disperse dyestuff in bath contg. neutral salt to prevent sepn. |
| US5242463A (en) * | 1991-03-06 | 1993-09-07 | The United States Of America As Represented By The Secretary Of Agriculture | Anionically dyeable smooth-dry crosslinked cellulosic material created by treatment of cellulose with non-reactive glycol ether swelling agents and nitrogen based compounds |
| WO1994018264A1 (en) | 1993-02-11 | 1994-08-18 | Minnesota Mining And Manufacturing Company | Methods of polymer impregnation |
| US5358535A (en) * | 1992-05-07 | 1994-10-25 | Societe Francaise Hoechst | Use of polyalkyleneglycol diesters as formaldehyde collectors and finishing process for the textile industry |
| US5614591A (en) * | 1994-12-15 | 1997-03-25 | The Virkler Company | Process and composition for imparting durable press properties to textile fabrics |
| DE19633625A1 (en) | 1996-08-21 | 1998-02-26 | Basf Ag | Process for the preparation of aqueous concentrated solutions of N-methylol ethers suitable for the finishing of cellulose-containing textile materials |
| US6102973A (en) * | 1993-07-20 | 2000-08-15 | Morales; Rodolfo A. | Process for treating garments |
| US6123739A (en) | 1995-06-19 | 2000-09-26 | Westpoint Stevens Inc. | Method to impart wrinkle free properties to sheeting and other fabrics made from cotton |
| EP1126072A2 (en) | 2000-02-16 | 2001-08-22 | Stork Brabant B.V. | Method for dyeing textile materials in a supercritical fluid. |
| EP0846803B1 (en) | 1996-12-04 | 2003-05-28 | Amann & Söhne GmbH & Co. | Process for dyeing of textile materials |
| WO2004033170A1 (en) | 2002-10-04 | 2004-04-22 | Basf Aktiengesellschaft | Method for improving the durability, dimensional stability and surface hardness of a wooden body |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH1702468D (en) * | 1967-12-02 | |||
| US3620821A (en) * | 1968-09-18 | 1971-11-16 | Union Carbide Corp | Treatment of fibers with siloxane-polyoxyalkylene block copolymers containing methoxysiloxy groups |
| JPS62104986A (en) * | 1985-10-29 | 1987-05-15 | 東海染工株式会社 | Enhancement of dyeing fastness of cellulosic fiber-containing structure to chlorine treatment water |
| US5252233A (en) * | 1990-08-10 | 1993-10-12 | Union Carbide Chemicals & Plastics Technology Corporation | Silicone textile finishes |
| FI122239B (en) * | 2004-02-25 | 2011-10-31 | Kemira Oyj | Process for treating fibrous material and new composition |
| EP1947233A1 (en) * | 2007-01-19 | 2008-07-23 | Basf Se | Method for producing a coated textile |
| CN102767106B (en) * | 2012-05-29 | 2015-05-06 | 凯米罗总公司 | Method for treating fiber material and novel composition |
-
2014
- 2014-07-31 EP EP14179257.2A patent/EP2980308A1/en not_active Withdrawn
-
2015
- 2015-07-29 CN CN201580036196.2A patent/CN106471182B/en active Active
- 2015-07-29 ES ES15744199T patent/ES2949983T3/en active Active
- 2015-07-29 WO PCT/EP2015/067332 patent/WO2016016282A2/en active Application Filing
- 2015-07-29 EP EP15744199.9A patent/EP3175033B1/en active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4133995A1 (en) | 1990-10-17 | 1992-04-23 | Ciba Geigy Ag | Two=stage two bath dyeing of cellulose hydrophobic fibre mixt. - using reactive dyestuff then disperse dyestuff in bath contg. neutral salt to prevent sepn. |
| US5242463A (en) * | 1991-03-06 | 1993-09-07 | The United States Of America As Represented By The Secretary Of Agriculture | Anionically dyeable smooth-dry crosslinked cellulosic material created by treatment of cellulose with non-reactive glycol ether swelling agents and nitrogen based compounds |
| US5358535A (en) * | 1992-05-07 | 1994-10-25 | Societe Francaise Hoechst | Use of polyalkyleneglycol diesters as formaldehyde collectors and finishing process for the textile industry |
| WO1994018264A1 (en) | 1993-02-11 | 1994-08-18 | Minnesota Mining And Manufacturing Company | Methods of polymer impregnation |
| US6102973A (en) * | 1993-07-20 | 2000-08-15 | Morales; Rodolfo A. | Process for treating garments |
| US5614591A (en) * | 1994-12-15 | 1997-03-25 | The Virkler Company | Process and composition for imparting durable press properties to textile fabrics |
| US6123739A (en) | 1995-06-19 | 2000-09-26 | Westpoint Stevens Inc. | Method to impart wrinkle free properties to sheeting and other fabrics made from cotton |
| DE19633625A1 (en) | 1996-08-21 | 1998-02-26 | Basf Ag | Process for the preparation of aqueous concentrated solutions of N-methylol ethers suitable for the finishing of cellulose-containing textile materials |
| EP0846803B1 (en) | 1996-12-04 | 2003-05-28 | Amann & Söhne GmbH & Co. | Process for dyeing of textile materials |
| EP1126072A2 (en) | 2000-02-16 | 2001-08-22 | Stork Brabant B.V. | Method for dyeing textile materials in a supercritical fluid. |
| WO2004033170A1 (en) | 2002-10-04 | 2004-04-22 | Basf Aktiengesellschaft | Method for improving the durability, dimensional stability and surface hardness of a wooden body |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2016016282A2 (en) | 2016-02-04 |
| CN106471182A (en) | 2017-03-01 |
| ES2949983T3 (en) | 2023-10-04 |
| WO2016016282A3 (en) | 2016-06-02 |
| CN106471182B (en) | 2019-05-31 |
| EP3175033A2 (en) | 2017-06-07 |
| EP3175033B1 (en) | 2023-04-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1632521B1 (en) | Oil in water emulsions of aminosiloxanes | |
| EP1397548B1 (en) | Amidofunctional aminopolydiorganosiloxanes | |
| EP0313867B1 (en) | Organopolysiloxanes with bunte salt groups | |
| DE102010001350A1 (en) | Novel linear polydimethylsiloxane-polyether copolymers having amino and / or quaternary ammonium groups and their use | |
| DE102009029450A1 (en) | Novel polysiloxanes with quaternary ammonium groups and their use | |
| DE3011304A1 (en) | FOAM ABSORBERS AND THEIR USE IN SYNTHETIC RESIN, LACQUER AND COLOR DISPERSIONS | |
| EP1560972B1 (en) | Partially quaternised, amino-functional organopolysiloxanes and their use in aqueous systems | |
| EP1975193B1 (en) | Polysiloxane and textile aid containing a polysiloxane | |
| DE2645459C3 (en) | Textile fiber preparations | |
| EP0173231A2 (en) | Organopolysiloxanes with Si-bounded hydrogen and SiC-bounded epoxy groups, process for their fabrication and use of these organopolysiloxanes | |
| EP1914261B1 (en) | New phosphated organo-siloxanyl derivatives and their use for treating leather | |
| DE602004006552T2 (en) | Gemini glycidyl ether adducts of polyhydroxyalkylalkylenediamines | |
| DE2900396C2 (en) | Textile fiber preparation | |
| EP0536765B1 (en) | Aqueous compositions with polysiloxanes containing nitrogen | |
| DE10221521A1 (en) | Formulations of silicone softeners for textile finishing | |
| EP3929232A1 (en) | Use of surfactant formulations containing long-chain alcohols in aqueous polyurethane dispersions | |
| DE19652524A1 (en) | Emulsion for finishing textile substrates in aqueous baths and dye baths | |
| EP3303453A1 (en) | Polyurethane-organopolysiloxanes | |
| EP2980308A1 (en) | Compositions for the treatment of fibrous materials | |
| EP2885353B1 (en) | Method for producing silicone emulsions | |
| DE102005056864B4 (en) | Preparations based on ammonium- and polyether-modified organopolysiloxanes and their use for the finishing of textile substrates | |
| EP1171663A1 (en) | Treatment agents for textiles, method of producing same and their use | |
| DE60103296T2 (en) | POLYSILOXANE WITH QUARTARY NITROGEN GROUPS | |
| CH645659A5 (en) | METHOD FOR PRODUCING A HOMOGENEOUS AQUEOUS COMPOSITION CONTAINING A POLYDIMETHYLSILOXANE AND A PERMANENT PRESS RESIN. | |
| DE1231432B (en) | Water-soluble polymeric compounds as emulsifiers for emulsifying silicones in water |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): AL AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HR HU IE IS IT LI LT LU LV MC MK MT NL NO PL PT RO RS SE SI SK SM TR |
|
| AX | Request for extension of the european patent |
Extension state: BA ME |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION IS DEEMED TO BE WITHDRAWN |
|
| 18D | Application deemed to be withdrawn |
Effective date: 20160804 |