EP0742284A2 - Procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques et appareil et supports de mesure pour la mise en oeuvre de ce procédé - Google Patents
Procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques et appareil et supports de mesure pour la mise en oeuvre de ce procédé Download PDFInfo
- Publication number
- EP0742284A2 EP0742284A2 EP96440034A EP96440034A EP0742284A2 EP 0742284 A2 EP0742284 A2 EP 0742284A2 EP 96440034 A EP96440034 A EP 96440034A EP 96440034 A EP96440034 A EP 96440034A EP 0742284 A2 EP0742284 A2 EP 0742284A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- inoculum
- measurement
- support
- primary container
- supports
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M41/00—Means for regulation, monitoring, measurement or control, e.g. flow regulation
- C12M41/46—Means for regulation, monitoring, measurement or control, e.g. flow regulation of cellular or enzymatic activity or functionality, e.g. cell viability
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/02—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor using a plurality of sample containers moved by a conveyor system past one or more treatment or analysis stations
- G01N35/025—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor using a plurality of sample containers moved by a conveyor system past one or more treatment or analysis stations having a carousel or turntable for reaction cells or cuvettes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N2035/00465—Separating and mixing arrangements
- G01N2035/00495—Centrifuges
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/02—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor using a plurality of sample containers moved by a conveyor system past one or more treatment or analysis stations
- G01N35/04—Details of the conveyor system
- G01N2035/0401—Sample carriers, cuvettes or reaction vessels
- G01N2035/0429—Sample carriers adapted for special purposes
- G01N2035/0434—Sample carriers adapted for special purposes in the form of a syringe or pipette tip
Definitions
- the present invention relates to the field of microbiology and more particularly bacteriological analyzes, in particular the automatic identification of bacteria and the automatic determination of the resistance of bacteria to different antibiotics, or automatic antibiogram, and relates to a method of bacterial identification and determining the sensitivity of bacteria to antibiotics.
- These methods and devices generally consist in moving the measurement support (s) in front of a source of light radiation, and in measuring in one or more directions the light intensity of the beam after it has passed through the container (s) and their contents.
- FR-A-2 354 554 describes a tubular compartmentalized container allowing the automatic dispersion of a bacterial culture in different peripheral compartments. These peripheral compartments can each be provided, prior to their feeding in bacterial culture, with antibiotics placed at their bottom in the form of dehydrated reagent.
- the sampling of a given volume of bacterial colony and the transfers of the volumes of precalibrated inoculum into the measurement supports 104, 105 are carried out by means of a single sampling tool and transfer 101 'cooperating, for example by leak-proof fitting, with the primary container 101, the volumes of precalibrated inoculum to be transferred being determined from optical measurements of the bacterial concentration of said inoculum, carried out in the primary container 101, and calculated in depending on the amount of bacteria needed.
- the sample and the introduction into the primary container 101 of a given volume of bacterial colony are carried out by means of the sampling and transfer tool 101 ′ after its shaping in order to sample the desired volume (selection of one volume from two different volumes available) and the precalibrated inoculum transfers from the primary container 101 to the measurement supports 104, 105 are carried out by pipetting predetermined inoculum volumes.
- the measurement support 104, 105 comprises a rigid main body 126 delimiting, in the form of non-communicating compartments, a central chamber 127 and several peripheral cells 132, 145 associated, each with a collection niche 146.
- the transfer of the substance to be analyzed or identified, such as a bacterial inoculum, initially injected into the central chamber 127, towards the measurement cells 132, 145 situated on the periphery of said support 104, 105, can be carried out gradually and in a perfectly controlled manner as a function of the successive operations to be carried out.
- the latter has, for example, a composite structure comprising, for example, an outer layer of paper (serving as a printing medium), an intermediate layer of aluminum and an inner layer of hot-melt adhesive.
- the prechamber 143 projects into the annular concentric chamber 147 by a distance substantially equal to the length of the wall portions delimiting the collection niches 146 and has, at the level of the upper part of its wall parallel to the peripheral lateral wall 139 of the central chamber 127, a very fine capillary orifice 143 ′ forming an overflow evacuation passage during the equal distribution phase.
- the upper wall 128 may consist of an attached cover, fixed by fitting and gluing or welding at the level of the external peripheral wall of the main body 126 and comprising additional orifices 149 and radial surface grooves 149 ′ ensuring the return of air during the transfers of the substance to be analyzed injected into the central chamber 127 towards the periphery of said support 104, 105.
- the sampling tool is gripped by the handling means 121 (FIGS. 15A to 15C), and is raised relative to the primary container 101 into which a determined quantity of dilution liquid is injected.
- the selection of one, two or three bearing zones at the level of the membrane 135 is carried out by making a more or less significant downward movement of the pressing device 155.
- the concentration or density of the manually prepared inoculum has a value such that it is sufficient, that is to say that it exceeds a minimum value which can be easily verified by a person skilled in the art. In fact, the latter will produce an aqueous solution, the density of which he will verify by simply noting the appearance of said solution, experience enabling him to observe that the density or concentration is sufficient or not.
- Such an inoculum preparation is easily accessible to those skilled in the art and is intended for allow subsequent adjustment or calibration to a lower final value, by dilution.
- the transverse housing 12, and more particularly the raised part 12 ′ of the latter, is intended for the manual preparation of the inoculum in aqueous solution from a culture solution, said solution being deposited in the bottom of the housing 12, on the raised part 12 ′, by means of a sampling member serving simultaneously to make a first mixture of the culture solution with the added water.
- the conical upper part 16 of the primary container 1 is provided with at least one notch 17 of shallow depth and two notches 18 of greater depth and of different width, arranged in alignment with one another and at 90 ° relative to the axis passing through the shallow recess (s) 17, this shallow recess (s) 17 being aligned in the axis of the housing 12 at the bottom and the notches 18 of greater depth cooperating with lugs 19 of corresponding section provided on the sealing closure cover 15 which is provided, on the one hand, on its upper face, with a surface 20 extending in the axis of the lugs 19 and, on the other hand, with a conical wall 21 of corresponding shape to that of the conical upper part 16 of the container 1 and connecting the legs 19.
- the rotary support 4 for antibiogram shown in Figures 26 to 28 of the accompanying drawings, is advantageously in the form of an upper composite disc provided with peripheral cells 32 for receiving the inoculum and antibiotic preparations and is characterized in that '' it is provided with a concentric cylindrical body, of smaller diameter than the disc and linked to said disc, forming a central chamber 33, for receiving the inoculum for distribution by centrifugation, said chamber 33 being supplied through an orifice 23 of the upper face of the upper composite disc and being surrounded by a sleeve 35 for gripping and stiffening the assembly.
- the upper composite disc of the rotary support for antibiogram 4 is constituted, on the one hand, by a part of circular cover 22 provided in its center with an orifice 23 and, on the other hand, by a circular plate 31, the upper face of which faces the lower face of the cover portion 22 carries, in relief on its periphery, the receiving cells 32 inoculum and antibiotic preparations, this circular plate 31 being connected to the concentric chamber 33 closed by a bottom 34, the cover part 22 being provided with a flange 22 'extending concentrically over a circular wall 31 'of the circular plate 31, delimiting the raised cells 32 towards the outside, and fixed to said circular wall 31' by gluing or welding.
- the tight guide of the cup 28 by means of its wall 29 can be obtained by a slightly tight sliding assembly of said cup 28 and of its wall 29 in the concentric chamber 27.
- the movable cup 28 is intended for the preparation of the culture arranged on its bottom, this preparation being carried out in the form of an aqueous solution and then dried, the wall 29 ensuring the accommodation of the aqueous solution until complete drying.
- the upper composite disc of the rotary support for identification 5 is constituted, on the one hand, by a part of circular cover 43 and, on the other hand, by a lower part in the form of a circular plate 44 provided, on its upper face turned towards the lower face of the cover part 43, in relief on its periphery, cells 45 for receiving the inoculum and characterization reagents, the cover 43 being provided with a flange 43 'extending concentrically over the circular wall 44 'of the circular plate 44, delimiting the raised cells 45 towards the outside, and fixed to said circular wall 44' by gluing or welding.
- the raised cells 45 are delimited on their face facing the inside of the rotary support 5 by a concentric circular wall 45 'and are each provided, on the face of said concentric wall 45' opposite the cells 45, with vertical baffles 45 " determining the means of capturing the inoculum during centrifugation.
- the means for collecting the inoculum, during centrifugation, provided, seen in the radial direction, in front of each cell 32, 45, respectively of the supports 4 and 5, are each connected with the interior of a corresponding cell 32, 45 via a capillary 36, 49 and are open, moreover, on an interior space 30, 43 ", communicating with the concentric chamber 33 of the circular plate 31 forming the lower part of the body or with the reception space of the primary container 1 in the concentric sleeve 46 extending under the underside of the circular plate 44 forming the lower part of the composite disc, the raised cells 32, 45 being connected, moreover, each via a capillary radial 39, 50 to a circular capillary 40, 51 opening, via another capillary 41, 52, outside the circular cover plate 22 or the circular cover part 43, the pre-cell -incubatio n 37 provided on the measurement support 4 for antibiogram being connected directly, by a through hole corresponding to the circular capillary 40.
- the circular cover plate 22 and the circular cover 43 are further provided, above each cell 32, 45 and near its edge, with a measurement window 42, 53, a similar window 43, 54 being provided.
- a measurement window 42, 53 under the underside of the circular plate 31, 44 forming the lower part of the body or of the composite disc, opposite each measurement window 42, 53 and at least one reflecting indexing zone 42 ', 53', formed on the face external of the external peripheral wall of the supports 4, 5, being associated with each cell 32, 45 with a fixed angular offset relative to the latter.
- the passage of each cell in front of the measuring device is perfectly identified during the rotation of the rotary support 4 or 5 thanks to the reflective zones or indexing mirrors and the corresponding measurement can be carried out in perfectly synchronized manner .
- the automatic calibration device consists, on the one hand, of a lower unit 60 comprising in particular a means of reading the coded identification means attached to the transverse groove 20 of the cover 15 of the primary containers 1 and a means of measuring the optical density of the inoculum present in said containers 1 and, on the other hand, by an upper unit 61 essentially comprising a device for pipetting and injecting water and of air.
- This gripping member will also perform the injection of water during the automatic calibration phase as well as the detachment of the pipette 11 by tearing off or dislodging the bottom of the primary container 1, maintaining the pipette 11 in a retracted position with retention of the inoculum and introduction of said pipette into the rotary support 4 for antibiogram with injection of the inoculum.
- the upper unit 61 may also include a movable nozzle for the sealed connection of an overflow discharge pipe or a pipette connected to a continuous suction means and to a recovery tank, said movable nozzle or said pipette being able to engage on the free external end of the discharge pipe 10 of the overflow and / or of the leveling pipe 10 'integrated in the bottom of the primary container 1, when the latter is positioned at workplace level.
- Each primary container 1 can thus be brought individually and positioned vertically at the working location, by simply sliding the elongated profiled receptacle 60 ′.
- the storage magazine 67 is located in the upper part of the first module 2 and consists of a circular magazine which can be rotated and comprising a plurality of stacks of measurement supports 4, 5 fresh and used at its periphery.
- Each stack can be brought individually into the gripping area of the transporting member 7 ′, allowing the latter to lift the upper measurement support 4, 5 of a properly positioned stack, and to transfer it to the storage device.
- said conveyor member 7 ′ may also receive a used measurement support 4, 5, conveyed by the first conveyor member 7 to the place of exchange, and deposit it in a corresponding stack, previously positioned in the appropriate place. served by said second transporter 7 ′.
- the modules 3 and 6 are located in a confined enclosure and thermoregulated at a temperature favorable to incubation, while the storage magazine 67 for the supports 4, 5 is at ambient temperature or located in a space possibly cooled.
- the confined and thermoregulated enclosure may comprise, at the level of the exchange link between the first 7 and the second 7 'transporting members, a closable opening, possibly in a sealed manner, controlled by the computer means 8 of command and control.
- the apparatus for implementing the method according to the invention is therefore composed of a limited number of constituent parts, the movements of which, in particular at the level of the transfer means and of the automatic calibration device, are extremely simplified.
- the specific structure and internal arrangement of said device makes it possible to achieve minimum bulk for a given processing capacity.
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Cell Biology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Sustainable Development (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Physics & Mathematics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- General Physics & Mathematics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
Description
- La présente invention concerne le domaine de la microbiologie et plus particulièrement des analyses bactériologiques, notamment l'identification automatique de bactéries et la détermination automatique de la résistance de bactéries à différents antibiotiques, ou antibiogramme automatique, et a pour objet un procédé d'identification bactérienne et de détermination de la sensibilité des bactéries à des antibiotiques.
- La présente invention a pour but, en partant d'une colonie, notamment d'un inoculum ou suspension bactérienne, d'effectuer, d'une part, une identification de bactéries à partir d'un ensemble de caractères mesurés par photométrie, ainsi que, d'autre part, des essais de croissance en présence d'un nombre optimum d'antibiotiques pour constater par néphélémétrie leur action sur lesdites bactéries, en vue de l'obtention d'un antibiogramme.
- A cet effet, il est intéressant de réaliser, lors d'un même essai, un maximum de mesures avec des antibiotiques différents.
- L'inoculum est une suspension de bactéries associée à un échantillon et à un patient. Sa préparation s'effectue manuellement par transfert dans une solution aqueuse d'une ou de plusieurs colonies cultivées dans un milieu de culture sous forme d'un gel ou d'éléments préparés à partir d'urine ou d'une hémoculture. En effet, après détection de présence de bactéries par contrôle, par exemple de la variation du CO2 au-dessus d'une culture de l'échantillon à analyser, il est procédé à un repiquage de ce dernier dans une deuxième culture sous forme d'un gel, ce repiquage ayant pour effet un isolement d'un type spécifique de bactéries au détriment des autres et permettant l'obtention d'une souche monobactérienne. Cette souche est utilisée ensuite pour réaliser l'inoculum par mise en suspension dans une solution aqueuse.
- Généralement, les bactéries en suspension dans les inoculums présentent une virulence relativement réduite, due au traitement de préparation, ce qui entraîne des difficultés pour une expérimentation rapide, les différentes mises en culture avec les réactifs se développant relativement lentement.
- On connaît actuellement différents procédés et dispositifs permettant la réalisation d'un antibiogramme mettant en oeuvre en tant que support où s'effectuent les mesures, soit des récipients transparents individuels de réception de culture bactérienne (FR-A-2 091 133), soit des récipients transparents multiples disposés sous forme d'alvéoles sur des plaques planes (FR-A-2 449 891, EP-A-0 253 685, DE-A-25 21 025 et US-A-3 942 899).
- Ces procédés et dispositifs consistent généralement à déplacer le ou les supports de mesure devant une source de rayonnement lumineux, et à mesurer dans une ou plusieurs directions l'intensité lumineuse du faisceau après qu'il ait traversé le ou les récipients et leur contenu.
- L'alimentation du ou des récipients en solution bactérienne est effectuée de manière connue, soit au moyen de pipettes manuelles, soit au moyen d'un dispositif de pipetage automatique selon EP-A-0 522 602, les différents antibiotiques étant mis en place manuellement dans les différents récipients avant leur remplissage.
- Par ailleurs, FR-A-2 354 554 décrit un récipient compartimenté tubulaire permettant la dispersion automatique d'une culture bactérienne dans différents compartiments périphériques. Ces compartiments périphériques peuvent être munis chacun, préalablement à leur alimentation en culture bactérienne, d'antibiotiques disposés dans leur fond sous forme de réactif déshydraté.
- On connaît également, par FR-A-2 280 895, un dispositif de fractionnement adapté à une utilisation en néphélémétrie ou en photométrie, se présentant sous forme d'un disque muni sur sa périphérie d'alvéoles de réception d'un réactif, sous forme solide et d'une solution bactérienne, la solution bactérienne étant transférée à partir d'une chambre centrale vers les différentes alvéoles, par centrifugation.
- Ces différents procédés et dispositifs connus permettent, par séries de mesures distinctes, au moyen de contenants distincts, d'effectuer des mesures en photométrie et en néphélémétrie.
- Cependant, ces dispositifs et procédés connus ne permettent pas d'effectuer rapidement et successivement ces mesures sans intervention manuelle, ni avec une alimentation automatique des supports de mesure à partir d'un même contenant, tout en autorisant également la réalisation d'opérations simultanées d'identification et d'antibiogramme, même à partir d'un inoculum initial très peu concentré.
- La présente invention a pour but de pallier ces inconvénients en proposant un procédé et des moyens permettant des identifications et des déterminations automatiques sans intervention manuelle sur les milieux.
- A cet effet, elle a pour objet un procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques, sous forme d'antibiogramme, caractérisé en ce qu'il consiste à introduire manuellement, au moyen d'un outil de prélèvement et de transfert, un volume donné de colonie bactérienne dans un récipient primaire, à réaliser automatiquement la dispersion de cette colonie bactérienne au sein d'un liquide pour constituer un inoculum au moins précalibré dans ledit récipient primaire, à effectuer également automatiquement des transferts totaux ou partiels de cet inoculum précalibré entre ledit récipient primaire et un ou plusieurs supports de mesure destinés à réaliser, respectivement, soit l'identification, soit l'antibiogramme ou encore ces deux déterminations simultanément en une seule opération combinée, lesdits transferts étant réalisés sans que l'inoculum précalibré soit mis en contact avec un élément autre que, d'une part, un outil de prélèvement et de transfert et/ou le récipient primaire et, d'autre part, son ou ses supports finaux et de telle manière que les quantités de bactéries transférées correspondent aux quantités requises pour les analyses à réaliser, à effectuer automatiquement la répartition de l'inoculum précalibré, éventuellement après l'avoir convenablement dilué pour aboutir à une calibration définitive, dans une ou plusieurs alvéoles desdits supports de mesure contenant pour la plupart des réactifs appropriés, à réaliser, dans certains cas, notamment pour l'antibiogramme, à l'intérieur d'un support de mesure, une opération dite de pré-croissance destinée à mettre les bactéries en état de se multiplier rapidement avant de les soumettre à analyse et à faire des mesures sur le contenu desdites alvéoles pendant ou à la fin d'une ou plusieurs incubations subies par l'inoculum dans lesdits supports de mesure, les mesures relevées étant enregistrées par un moyen informatique et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- L'invention a également pour objet des appareils et des supports de mesure, sous forme de consommables, pour la mise en oeuvre de ce procédé et de variantes de réalisation de ce dernier, qui seront décrits en détail en regard des dessins énumérés ci-après.
- L'invention sera mieux comprise, grâce à la description ci-après, qui se rapporte à des modes de réalisation préférés, donnés à titre d'exemples non limitatifs, et expliqués avec référence aux dessins schématiques annexés, dans lesquels :
- la figure 1 est une vue de dessus de l'intérieur d'un appareil pour la mise en oeuvre du procédé conforme à l'invention, selon un premier mode de réalisation ;
- la figure 2 est une vue en élévation latérale et en coupe de l'appareil suivant la figure 1 ;
- la figure 3 est une vue en élévation latérale et en coupe d'un support de mesure selon l'invention ;
- la figure 4 est une vue en perspective et partiellement en coupe d'un support de mesure représenté à la figure 3 ;
- la figure 5 est une vue de détail à une échelle différente d'une partie du support de mesure représenté à la figure 4 ;
- la figure 6 est une vue simplifiée de dessus et par transparence d'un support de mesure selon l'invention ;
- les figures 6A et 6B sont des vues de détail et en perspective, à une échelle différente, de deux parties distinctes du support de mesure représenté à la figure 6 ;
- la figure 7 est une demi-vue en coupe transversale et en élévation latérale d'un support de mesure monté dans un poste de mesure et de centrifugation ;
- la figure 8 est une vue partielle en coupe et en perspective d'un support de mesure monté dans un poste de mesure et de centrifugation ;
- la figure 9 est une vue en perspective et partiellement en coupe d'un couvercle formant la paroi supérieure d'un support de mesure représenté à la figure 3 ;
- la figure 9A est une vue en détail, selon une autre perspective, d'une partie du couvercle représenté à la figure 9 ;
- la figure 10 est une vue simplifiée en perspective d'un corps principal faisant partie du support de mesure représenté à la figure 3 ;
- la figure 11 est une vue en élévation latérale et en coupe d'un ensemble récipient primaire / outil de prélèvement et de transfert ;
- la figure 12 est une vue en coupe d'un outil de prélèvement et de transfert ;
- les figures 13 et 14 sont des vues respectivement en élévation latérale et en perspective d'un outil de prélèvement et de transfert ;
- les figures 15A à 15J montrent différentes phases de manipulation successives de la préparation d'un inoculum précalibré dans le récipient primaire et de son transfert au moins partiel dans un support de mesure ;
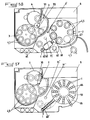
- la figure 16 est une vue en élévation et en coupe d'un appareil pour la mise en oeuvre d'une variante de réalisation du procédé conforme à l'invention ;
- la figure 17 est une vue en plan et en coupe, au niveau inférieur, de l'appareil suivant la figure 16 ;
- la figure 18 est une vue analogue à celle de la figure 17 de l'appareil au niveau supérieur ;
- la figure 19 est une vue en perspective éclatée d'un récipient primaire selon une variante de réalisation de l'invention, correspondant à l'appareil de la figure 16;
- la figure 20 est une vue en perspective par le dessous du récipient primaire de la figure 19 ;
- les figures 21 à 23 sont des vues schématiques en coupe représentant le récipient primaire de la figure 19 pendant les étapes successives de préparation de l'inoculum;
- la figure 24 est une vue en perspective éclatée, partiellement arrachée, d'un support de mesure pour l'identification destiné à être mis en oeuvre dans l'appareil des figures 16 à 18 ;
- la figure 25 est une vue en coupe du support de mesure de la figure 24 pour l'identification muni d'un récipient primaire associé ;
- la figure 26 est une vue analogue à celle de la figure 24 représentant un support de mesure pour antibiogramme destiné à être mis en oeuvre dans l'appareil des figures 16 à 18 ;
- la figure 27 est une vue en perspective partiellement arrachée du support suivant la figure 26 avant inoculation ;
- la figure 28 est une vue analogue à celle de la figure 25 représentant le support de mesure pour antibiogramme en position de répartition de l'inoculum dans les alvéoles, et
- la figure 29 est une vue en perspective et en coupe d'une variante de réalisation du récipient primaire de la figure 19 pour le traitement d'un matériel bactérien de faible volume, sans calibration automatique.
- Conformément à l'invention, le procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques, sous forme d'antibiogramme, consiste à introduire manuellement, au moyen d'un outil 101' de prélèvement et de transfert, un volume donné de colonie bactérienne dans un récipient primaire 1 ; 101 à réaliser automatiquement la dispersion de cette colonie bactérienne au sein d'un liquide pour constituer un inoculum au moins précalibré dans ledit récipient primaire 1 ; 101, à effectuer également automatiquement des transferts totaux ou partiels de cet inoculum précalibré entre ledit récipient primaire 1 ; 101 et un ou plusieurs supports de mesure 4, 5 ; 104, 105 destinés à réaliser, respectivement, soit l'identification, soit l'antibiogramme ou encore ces deux déterminations simultanément en une seule opération combinée, lesdits transferts étant réalisés sans que l'inoculum précalibré soit mis en contact avec un élément autre que, d'une part, un outil de prélèvement et de transfert 101'; 1, 101 et/ou le récipient primaire 1 ; 101 et, d'autre part, son ou ses supports de mesure finaux 4, 5 ; 104, 105 et de telle manière que les quantités de bactéries transférées correspondent aux quantités requises pour les analyses à réaliser, à effectuer automatiquement la répartition de l'inoculum précalibré, éventuellement après l'avoir convenablement dilué pour aboutir à une calibration définitive, dans une ou plusieurs alvéoles 32, 37, 45 ; 132, 137, 145 desdits supports de mesure 4, 5 ; 104, 105 contenant pour la plupart des réactifs appropriés, à réaliser, dans certains cas, notamment pour l'antibiogramme, à l'intérieur d'un support de mesure 4 ; 104 une opération dite de pré-croissance destinée à mettre les bactéries en état de se multiplier rapidement avant de les soumettre à analyse et à faire des mesures sur le contenu desdites alvéoles 32, 37, 45 ; 132, 137, 145 pendant ou à la fin d'une ou plusieurs incubations subies par l'inoculum dans lesdits supports de mesure 4, 5 ; 104, 105, les mesures relevées étant enregistrées par un moyen informatique 8 ; 108 et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- Selon un premier mode de réalisation de l'invention, le prélèvement d'un volume donné de colonie bactérienne et les transferts des volumes d'inoculum précalibré dans les supports de mesure 104, 105 sont effectués au moyen d'un outil unique de prélèvement et de transfert 101' coopérant, par exemple par emboîtement étanche, avec le récipient primaire 101, les volumes d'inoculum précalibré à transférer étant déterminés à partir de mesures optiques de la concentration bactérienne dudit inoculum, effectuées dans le récipient primaire 101, et calculés en fonction des quantités de bactéries nécessaires.
- Le prélèvement et l'introduction dans le récipient primaire 101 d'un volume donné de colonie bactérienne sont effectués au moyen de l'outil 101' de prélèvement et de transfert après sa mise en conformation en vue de prélever le volume souhaité (sélection d'un volume parmi deux volumes différents disponibles) et les transferts d'inoculum précalibré du récipient primaire 101 vers les supports de mesure 104, 105 sont réalisés par pipetage de volumes d'inoculum prédéterminés.
- Le transfert de l'inoculum à l'intérieur des supports de mesure 104, 105, notamment vers les alvéoles 132, 145, est contrôlé dynamiquement ou activement par commande de l'ouverture ou du blocage étanche de passages successifs conduisant progressivement vers lesdites alvéoles 132, 145.
- Dans le cadre de la mise en oeuvre de supports de mesure servant à la détermination des antibiogrammes ou à réaliser des déterminations combinées d'antibiogramme et d'identification, la pré-croissance de l'inoculum calibré est réalisée par une première incubation, dite pré-incubation, pendant laquelle les bactéries présentes dans l'inoculum sont incubées sans être mises en présence de réactifs et ce jusqu'à ce qu'un début de croissance bactérienne soit mesurable ou jusqu'à ce que la concentration bactérienne atteigne un niveau prédéfini, cette pré-croissance étant suivie de la mise en contact de l'inoculum avec les réactifs et d'une incubation finale pendant laquelle leurs interactions sont observées.
- Conformément à un mode de réalisation pratique avantageux de l'invention, la répartition de l'inoculum dans les alvéoles 32, 37, 45 ; 132, 137, 145 situées en périphérie des supports de mesure 4, 5 ; 104, 105 est réalisée par centrifugation, les mesures et les observations effectuées au niveau desdites alvéoles 32, 37, 45 ; 132, 137, 145 étant effectuées par mise en rotation des supports de mesure 4, 5 ; 104, 105 autour de l'axe central de centrifugation desdits supports.
- De plus, il peut être prévu, conformément à l'invention, que la mesure de la concentration de l'inoculum bactérien et la détermination du début de croissance, pendant la pré-croissance dans un support de mesure 4 ; 104 d'antibiogramme, sont réalisées par des mesures photométriques effectuées sur une partie aliquote de l'inoculum transférée à cet effet, par une première centrifugation, dans une alvéole périphérique spécifique 37 ; 137 dédiée à la caractérisation de la croissance pendant la pré-incubation et ne contenant pas de réactifs, le reste d'inoculum restant bloqué pendant la pré-incubation dans une chambre concentrique centrale 27 ; 127 dudit support 4 ; 104, avant d'être transféré, après achèvement de la pré-croissance dans les autres alvéoles périphériques 32 ; 132 par une deuxième centrifugation, précédée d'une action d'autorisation ou de déblocage appropriée ouvrant le passage pour le transfert du reste de l'inoculum vers lesdites autres alvéoles 32 ; 132 contenant des réactifs.
- En vue d'éviter toute contamination de l'inoculum calibré ou non présent dans le support de mesure d'antibiogramme 104, le passage de l'étape de pré-incubation à l'étape d'incubation est effectué sans rupture du confinement de l'intérieur du support rotatif de mesure concerné 104 par rapport à l'extérieur, ledit support restant clos et ledit passage étant réalisé par interruption d'une action sur un élément obturateur participant à la réalisation de ce confinement.
- Selon un mode de réalisation préférentiel de l'invention, les mesures photométriques sont réalisées par néphélémétrie pour les supports de mesure 4 ; 104 servant à l'antibiogramme et par détermination d'absorbance ou de densité optique pour les supports de mesure 5 ; 105 servant à l'identification ou aux déterminations combinées identification/antibiogramme. Il est également possible, par addition d'un marqueur fluorogène au réactif, de réaliser des mesures fluorimétriques.
- L'invention a également pour objet un support de mesure en forme de disque, pouvant notamment être avantageusement mis en oeuvre dans le cadre du procédé décrit ci-dessus, mais qui peut également trouver une application plus générale dans d'autres procédés d'analyse ou d'identification mettant en oeuvre des supports de mesure rotatifs et réalisant des transferts contrôlés des substances à analyser à l'intérieur desdits supports de mesure.
- Comme le montrent les figures 3 à 15 des dessins annexés, le support de mesure 104, 105 comprend un corps principal rigide 126 délimitant, sous forme de compartiments non communiquants, une chambre centrale 127 et plusieurs alvéoles périphériques 132, 145 associés, chacune, à une niche de captage 146.
- Conformément à l'invention, le corps principal 126 présente une paroi supérieure 128 pourvue de plusieurs ensembles d'orifices de transfert traversants 129, 130, 131, 133 débouchant respectivement dans la chambre centrale cylindrique 127, dans chaque niche de captage 146 affectée à chaque alvéole 132, 145 et dans chacune desdites alvéoles 132, 145 et recouverte, à l'exception d'une portion centrale entourant l'orifice de chargement 134 de ladite chambre centrale 127 et de la zone des fenêtres de mesure des alvéoles 132, 145, par une membrane flottante étanche affleurante 135 fixée localement et hermétiquement notamment à proximité de la périphérie externe du support de mesure et autour de l'orifice de chargement 134 de ladite paroi supérieure 128 et pouvant être pressée intimement contre la surface supérieure de ladite paroi 128 pour former des zones de contact temporaires étanches s'étendant entre ou recouvrant certains desdites ensembles d'orifices traversants 129, 130, 131, 133, notamment au cours de la rotation dudit support de mesure.
- On notera que, grâce à cette disposition, le transfert de la substance à analyser ou à identifier, telle qu'un inoculum bactérien, injectée initialement dans la chambre centrale 127, vers les alvéoles de mesure 132, 145 situées en périphérie dudit support 104, 105, peut être réalisé progressivement et de manière parfaitement contrôlée en fonction des opérations successives à effectuer.
- Selon un mode de réalisation préférentiel de l'invention, la paroi supérieure 128 comporte, au niveau de sa face supérieure, des rainures ou des renfoncements annulaires concentriques 140, 140' dans lesquel(le)s débouchent les orifices traversants 129, 130, 131, 133 disposés selon des cercles concentriques espacés, la rainure intérieure 140 comprenant une nervure 136 formant surface de contact annulaire et séparant les orifices de sortie 129 de la chambre centrale 127 et les orifices d'entrée 130 de la chambre concentrique annulaire 147 comprenant les niches radiales de captage 146, et les orifices de sortie 131 des niches de captage 146 débouchant au niveau de la face supérieure d'une nervure circulaire concentrique ou de structures proéminentes distinctes 138, par exemple sous forme de dômes, disposée(s) dans la rainure extérieure 140', les extrémités supérieures de la nervure 136 et des structures 138 étant situées dans un plan ou des plans s'étendant légèrement en retrait du plan de collage de la membrane étanche affleurante 135.
- La prévision de points ou de zones d'appui de la membrane 135, proéminent(e)s par rapport à la surface avoisinante des fonds de rainures annulaires 140, 140' ménagées dans la face supérieure de la paroi supérieure 128, mais s'arrêtant au moins légèrement en dessous du plan de collage de la membrane affleurante 135, et conformés avec une face supérieure restreinte et délimités par rapport à ladite surface avoisinante, permet d'obtenir une étanchéité reproductible et augmentée, de localiser précisément les zones de contact étanches et d'aboutir à une résistance accrue de ces dernières à la pression exercée par la substance ou l'inoculum lors de la rotation des supports de mesures 104, 105, lesdites zones de contact étant situées aux sommets d'élévation formant obstacles à la progression centripète de la substance ou de l'inoculum.
- En vue de faciliter les transferts et le vidage complet de la chambre centrale 127 et des niches de captage 146, il peut être prévu que la chambre centrale 127 comporte une paroi latérale périphérique 139 au moins légèrement inclinée vers l'extérieur en direction de la paroi supérieure 128, les orifices de sortie 129 de la chambre 127 centrale et les orifices de sortie 131 des niches de captage et d'équirépartition 146 étant situés sensiblement dans l'alignement des faces internes des parois latérales périphériques 139', 146' de ces dernières.
- Afin de diriger préférentiellement le flux de substance ou d'inoculum vers les orifices d'entrée au cours de la rotation des supports de mesure 104, 105, lesdits orifices d'entrée 130 de la chambre concentrique 147 comprenant les niches de captage et d'équirépartition 146 débouchent sur la face supérieure de la paroi supérieure 128 au pied d'un décrochement 141 délimitant latéralement et du côté externe le renfoncement annulaire 140 interne et les orifices d'entrée 133 des alvéoles de mesure 132, 145 débouchent et les orifices d'entrée 133 des alvéoles à la base ou dans un flanc incliné 141' d'un décrochement circulaire débouchant sur une surface proéminente extérieure 142 pouvant former une zone de contact ou de collage externe de la membrane flottante affleurante 135.
- Cette dernière présente, par exemple, une structure composite comprenant, par exemple, une couche externe en papier (servant de support d'impression), une couche intermédiaire en aluminium et une couche interne de colle thermofusible.
- La fixation de la membrane 135 au niveau de ses zones de solidarisation avec la paroi supérieure 128 peut alors être réalisée en appuyant intimement ladite membrane 135 sur ladite paroi 128 au niveau desdites zones et en induisant un courant de chauffage dans la couche en aluminium, qui aboutit à la fusion de la couche de colle interne.
- La nervure 136 et les structures saillantes ou proéminentes 138 présentent des hauteurs telles que leurs faces supérieures sont situées légèrement en dessous du plan de collage de la membrane 135, il en résulte que cette dernière n'adhérera pas à leur niveau lors de la fusion de la couche de colle thermofusible interne.
- Conformément à une autre caractéristique de l'invention, représentée notamment aux figures 3, 6, 6A et 10 des dessins annexés, le support de mesure 104, 105 peut comporter une alvéole de pré-incubation 137 identique aux autres alvéoles périphériques 132, 145, alignée circulairement avec ces dernières et communiquant avec une pré-chambre close 143 formée dans la chambre concentrique 147 renfermant les niches de captage et d'équirépartition 146 et alimentée en inoculum à partir d'une niche de captage interne 144 située au niveau d'une portion de la paroi latérale périphérique 139 de la chambre centrale 127, par l'intermédiaire d'un passage non obturable par les zones de contact étanches 136, 138, 142 pouvant être formées entre la membrane affleurante 135 et la paroi supérieure 128.
- De manière avantageuse, le passage d'alimentation de la pré-chambre 143, communiquant librement avec la chambre de pré-incubation 137 et formant également trop-plein pour les niches de captage 146, est constitué par un conduit 157, débutant dans la partie supérieure de la portion de paroi latérale périphérique 139 délimitant la niche de captage interne 144, formé par coopération d'une rainure ménagée dans la partie supérieure d'un prolongement saillant radial 158 de la paroi latérale périphérique 139 de la chambre centrale 127 et de la paroi supérieure 128 et débouchant dans ou à l'entrée d'une rainure 148 à extension radiale centripète, creusée dans la face supérieure de la paroi supérieure 128, formant un conduit étanche en coopération avec la membrane (135) contrecollée de part et d'autre de ladite rainure 148, dont l'extrémité distale se termine au niveau d'un orifice traversant 148' débouchant dans la préchambre 143.
- La préchambre 143 fait saillie dans la chambre concentrique annulaire 147 d'une distance sensiblement égale à la longueur des portions de paroi délimitant les niches de captage 146 et présente, au niveau de la partie supérieure de sa paroi parallèle à la paroi latérale périphérique 139 de la chambre centrale 127, un orifice capillaire très fin 143' formant passage d'évacuation du trop plein durant la phase d'équirépartition.
- Bien que les figures 6 et 10 notamment ne représentent qu'un nombre limité d'alvéoles 132, 145, il est bien évidemment entendu que ces dernières sont disposées sur toute la périphérie des supports de mesure 104 et 105 et sont, par exemple, au nombre d'environ cinquante.
- Conformément à un mode de réalisation préférentiel du support de mesure 104, 105, la paroi supérieure 128 peut consister en un couvercle rapporté, fixé par emboîtement et collage ou soudure au niveau de la paroi périphérique externe du corps principal 126 et comportant des orifices supplémentaires 149 et des rainures superficielles radiales 149' assurant le retour d'air au cours des transferts de la substance à analyser injectée dans la chambre centrale 127 vers la périphérie dudit support 104, 105.
- Une telle réalisation du support 104, 105 permet de fabriquer indépendamment ses trois composantes, à savoir le corps principal 126, le couvercle 128 et la membrane 135, puis de les assembler de manière adaptée, le corps principal et le couvercle 128 étant obtenus, par exemple, par moulage par injection d'un matériau thermoplastique, préférentiellement transparent.
- Dans le cas d'une mise en oeuvre de deux supports de mesure rotatifs 104, 105 de natures différentes, tels que des supports rotatifs 104 pour antibiogramme et des supports rotatifs 105 pour l'identification, ces derniers pourront présenter la même constitution et se différencier uniquement par la nature des réactifs disposés dans leurs alvéoles de mesure respectives 132, 145 et par les manipulations dont ils feront l'objet au cours de leur mise en oeuvre (prévision ou non d'une phase de préincubation).
- Une telle similarité de structure des supports de mesure 104, 105, destinés à des applications différentes, facilite sensiblement la standardisation de leur fabrication, aboutit à un prix de revient plus faible que pour des supports différenciés, facilite leur manipulation par l'appareil de traitement et d'analyse et permet de simplifier la constitution de ce dernier.
- Comme le montrent notamment les figures 3 et 4 des dessins annexés, l'orifice de chargement 134 de la chambre centrale 127 est situé dans un renfoncement 134' de la paroi supérieure 128 et est obturable au moyen d'un bouchon 150 dont la partie supérieure est sensiblement de niveau avec la face supérieure de la paroi supérieure 128.
- Ainsi aucune partie ne dépassera du plan contenant la face supérieure de la paroi supérieure 128.
- Le renfoncement 134' pourra être délimité latéralement par des parois formant une structure cylindrique tronconique dirigé vers l'orifice de chargement 134 (figures 3 et 4).
- En vue de la manipulation et du stockage par empilement des supports de mesure 104, 105, le fond de la chambre centrale 127 est entouré d'un manchon concentrique 151 de préhension et de rigidification, saillant au niveau de la face inférieure du support 104, 105. De plus, lesdits supports pourront également comporter des nervures de rigidification et de guidage au niveau de leurs alvéoles périphériques.
- En outre, afin de faciliter le réglage et le calage des dispositifs de mesures photométriques, les supports de mesures 104, 105 peuvent comporter, chacun, une ouverture traversante 152, ayant des dimensions identiques à celles d'une alvéole 132, 145, située en alignement circulaire avec ces dernières et qui est ménagée dans le corps principal 126 et dans la paroi supérieure 128, ladite ouverture 152 étant préférentiellement située adjacente à l'alvéole de pré-incubation 137, de manière à permettre un repérage aisé de cette dernière.
- Enfin, la paroi supérieure 128 est munie, au dessus de chaque alvéole 132, 137, 145 et près de son bord extérieur, d'une fenêtre de mesure, une fenêtre analogue étant prévue, dans chacune des portions de paroi du corps principal 126 constituant respectivement les fonds desdites alvéoles, en regard de chaque fenêtre de mesure précitée et au moins une zone réfléchissante d'indexation, formée sur la face externe de la paroi périphérique externe du corps principal 126, étant associée à chaque alvéole 132, 137, 145 avec un décalage angulaire fixe par rapport à cette dernière.
- Les zones réfléchissantes inclinées créent des repères optiques décalés pour les différentes alvéoles de mesure 132, 137, 145, et permettent un centrage guidé des dispositifs de mesures photométriques au niveau de chacune desdites alvéoles.
- Ainsi, les supports de mesure 104, 105 comprennent un corps fermé compartimenté (corps principal 126 + paroi supérieure 128) percé en des emplacements déterminés par des orifices 129, 130, 131, 133 de faible dimension et surmonté d'une membrane étanche souple affleurante 135, permettant par action contrôlée sur ladite membrane et dans le cadre du procédé décrit précédemment :
- soit de conserver la substance à analyser au centre du support de mesure considéré, pendant une phase d'homogénéisation et le cas échéant, de pré-incubation,
- soit de garder la substance à analyser dans la zone de la chambre concentrique annulaire 147 et des niches radiales de captage 146, en isolant celles-ci des alvéoles de mesure 132, 145, pendant la phase d'équirépartition de la substance à analyser par centrifugation, cette dernière pouvant être réalisée pendant la durée nécessaire à l'obtention d'une équirépartition parfaite de la substance à analyser dans lesdites niches, moyennant une fonction de trop-plein assurée par la préchambre 143 et l'alvéole de pré-incubation 137 par l'intermédiaire de l'orifice capillaire 143',
- soit d'ouvrir le passage entre les niches radiales de captage 146 et les alvéoles de mesure 132, 145, de manière à réaliser le transfert de la substance à analyser desdits niches vers lesdites alvéoles au cours d'une opération de centrifugation.
- L'invention a également pour objet un appareil pour la mise en oeuvre du procédé décrit ci-dessus, représenté aux figures 1 et 2 des dessins annexés, ledit appareil étant essentiellement constitué par un premier module 102 de support et de stockage de supports de mesure 104, 105 frais, tels que décrits précédemment, et de récipients primaires 101 coopérant chacun avec un outil de prélèvement et de transfert 101' correspondant, par un deuxième module 103 d'incubation des supports 104 et 105, après injection de l'inoculum bactérien, par un troisième module 106 de centrifugation et de mesures néphélémétriques et/ou photométriques et/ou fluorimétriques, par un ou plusieurs dispositifs 107, 107' de transfert desservant lesdits modules 102, 103 et 106 et par un moyen informatique 108 de contrôle et de commande des différentes étapes du procédé, et d'acquisition, d'enregistrement, de traitement, d'évaluation et/ou de restitution de données, les deuxième et troisième modules 103 et 106 étant disposés dans une enceinte de confinement.
- Conformément à l'invention, les récipients primaires 101 sont portés par un moyen support 109 en forme de couronne, s'étendant concentriquement autour et sous un moyen support 110 en forme de disque portant les supports de mesure 104, 105, les deux moyens supports 109, 110 étant montés avec faculté de rotation autour d'un même axe, chaque récipient primaire 101 pouvant être amené, par simple rotation dudit moyen support 109 en forme de couronne, au niveau d'un poste 111 de manipulation de l'outil 101' de prélèvement et de transfert associé et de mesure de densité optique du contenu dudit récipient primaire 101.
- Comme le montrent notamment les figures 11 à 14 des dessins annexés, chaque récipient primaire 101 de réception d'un volume donné de colonie bactérienne et de préparation d'un inoculum au moins précalibré se présente sous la forme d'un récipient cylindrique ouvert au niveau de sa partie supérieure, laquelle est munie d'un rebord radial 112 pour le maintien dudit récipient primaire 101 dans un des logements correspondants 109' ménagé(s) dans le support mobile 109 en forme de couronne.
- L'outil de prélèvement et de transfert 101' peut avantageusement consister en une seringue dont le corps 113 comporte une partie avant de prélèvement et d'éjection effilée 113' et une partie arrière 113" de stockage et de préhension sensiblement cylindrique, ladite partie arrière 113" présentant au moins un décrochement radial extérieur 114 au niveau de son extrémité contiguë à la paroi avant 113' en vue d'un emboîtement partiel avec blocage dudit corps 113 dans le récipient primaire 101, l'extrémité libre avant de la partie avant 113' étant alors située à faible distance du fond dudit récipient primaire 101.
- La partie arrière 113'' peut comporter des prolongements inférieurs 159 sous forme d'ailettes radiales, s'étendant depuis le décrochement 114 et pourvues chacune d'un chanfrein latéral inférieur 159', ces prolongements aidant au centrage de l'emboîtement de l'outil 101' dans le récipient primaire 101 et au blocage de son positionnement radial dans ce dernier.
- Selon une caractéristique de l'invention, représentée également sur les figures 11 à 14 des dessins annexés, la seringue 101' comporte, au niveau de son extrémité avant, des moyens 118, 118' pour prélever, en volume, une quantité réduite ou une quantité normale de colonie bactérienne, en fonction du positionnement de son piston 115.
- Le piston 115 de la seringue 101' est constitué par une tige d'actionnement effilée 116 dont la partie avant 116' coopère avec la partie avant 113' du corps 113 et peut dépasser de l'ouverture de prélèvement et d'éjection 113"' de ladite partie avant 113' du corps 113 par son extrémité libre, lorsque le piston 115 est totalement enfoncé dans le corps 113, ladite tige d'actionnement 116 présentant un décrochement radial 116" venant buter avec conjugaison de forme sur le fond 117 du volume interne de la partie arrière cylindrique 113" du corps 113, lorsque ledit piston 115 est entièrement enfoncé dans ledit corps 113.
- Le fond du récipient primaire 101 peut présenter, comme le montre la figure 11 des dessins annexés, un renfoncement central 160 pour la réception de l'extrémité libre avant de la tige d'actionnement 116 lorsqu'elle dépasse l'extrémité avant de la partie avant 113' du corps 113.
- Afin de pouvoir obtenir dans le récipient primaire 101 un inoculum au moins précalibré par une détermination au moins grossière de la quantité d'éléments de colonie bactérienne prélevée (prélèvement manuel ou micro-prélèvement), fonction notamment du type d'analyse envisagé, les extrémités libres des parties avant 113', 116' du corps 113 et de la tige d'actionnement 116 du piston 115 sont pourvus d'un décrochement ou d'un renfoncement 118, 118' formant des surfaces ou des volumes de prélèvement de quantités déterminées différentes de colonie bactérienne, l'extrémité libre de la partie avant 116' de la tige d'actionnement 116 étant opérationnelle pour le prélèvement lorsque le piston 115 est entièrement enfoncé et l'extrémité libre de la partie avant 113' du corps 113 étant opérationnelle lorsque le piston 115 est au moins légèrement rétracté dans ladite partie avant 113".
- L'inoculum précalibré est constitué par injection d'une quantité fixe de liquide de dilution, liquide injecté par un moyen 120.
- En vue de déterminer la concentration bactérienne de l'inoculum précalibré, chaque récipient primaire 101 comporte dans sa paroi latérale, à proximité de son fond, deux fenêtres de mesure 119, 119' en regard, adaptées pour la mesure de la densité optique du contenu dudit récipient primaire 101 au niveau du poste 111, ce dernier comportant également le moyen 120 d'injection de liquide de dilution dans ledit récipient primaire 101.
- A cela s'ajoute que la quantité d'inoculum prélevée dans le récipient primaire 101 et injectée dans les supports de mesure 104, 105 destinataires peut être aisément réglée, en calculant le volume à transférer compte tenu de la concentration bactérienne mesurée par densité optique, du fait de la mise en oeuvre d'un outil de prélèvement et de transfert 101' sous forme de seringue, manipulé automatiquement par un moyen adapté au niveau du poste 111 notamment.
- Ce moyen de manipulation 121 de la seringue 101' peut, par exemple, consister, comme le montrent les figures 15A à 15J des dessins annexés en deux ensembles de mâchoires 121' et 121" comprenant deux mâchoires externes 121' destinées à venir en prise rigide et bloquante avec un rebord radial 128 au niveau de l'ouverture de la partie arrière 113" du corps 113 et deux mâchoires internes 121", disposées concentriquement entre les deux mâchoires externes 121', destinées à venir en prise rigide et bloquante avec un renflement 122' de la tige d'actionnement 116, la fermeture des deux ensembles de mâchoires 121' et 121" étant réalisée séparément ou, de manière préférentielle, simultanément par coulissement d'un manchon 121"' autour et le long des mâchoires externes 121', les mâchoires internes 121" pouvant coulisser par rapport aux mâchoires externes 121', notamment en position de fermeture, et au manchon 121"' et ce dernier pouvant prendre appui sur le support mobile 109 en forme de couronne et sur le bord radial 112 de l'ouverture supérieure du récipient primaire 101 considéré, de manière à bloquer ce dernier en position dans son logement 109' lors du coulissement de l'un quelconque des deux ensembles de mâchoires 121', 121".
- La préparation d'un inoculum au moins précalibré dans un récipient primaire 101 et son transfert au moins partiel et en quantité contrôlée dans un support de mesure 104,105 va à présent être décrit plus en détail en se référant aux figures 15A et 15J des dessins annexés.
- Tout d'abord, l'opérateur prélève manuellement au moyen de l'outil 101' un volume déterminé de colonie bactérienne, ce volume étant défini par réglage dudit outil 101' en déplaçant le piston 115 dans une position correspondant à un enfoncement total (dépassement de l'extrémité avant de la partie avant 116' de la tige d'actionnement 116 au niveau de l'ouverture 113"' du corps 113) ou à une légère rétraction de ladite tige d'actionnement. En position rétractée du piston 115, l'outil 101' collecte une quantité de bactéries constituant un prélèvement dit normal, alors qu'en position enfoncée du piston, l'outil 101' collecte un prélèvement dit réduit ou micro-prélèvement (environ 1/100 du précédent).
- L'outil 101' portant une quantité déterminée de colonie bactérienne est ensuite emboîté dans un récipient primaire 101 et l'ensemble ainsi formé est disposé dans un logement 109' du moyen support 109.
- En début de préparation de l'inoculum, l'outil de prélèvement est saisi par le moyen de manipulation 121 (figures 15A à 15C), et est soulevé par rapport au récipient primaire 101 dans lequel on injecte une quantité déterminée de liquide de dilution.
- Puis, l'outil 101' est réemboîté dans le récipient primaire 101 et une homogénéisation de l'inoculum est réalisée dans le récipient primaire 101 par des opérations successives d'aspiration et d'éjection obtenus par coulissement alternatif de l'ensemble de mâchoires internes 121" (figures 15C, 15D et 15E). Après achèvement de cette opération, le récipient primaire 101 contient un inoculum précalibré.
- L'outil 101' est ensuite extrait du récipient primaire 101 et une mesure de densité optique est effectuée pour déterminer la concentration bactérienne de l'inoculum précalibré ce qui permet de déterminer, par calcul, le volume d'inoculum à transférer dans les supports de mesure 104, 105 pour y amener la quantité de bactéries nécessaire aux analyses prévues (figures 15F et 15G).
- Après une nouvelle phase éventuelle d'homogénéisation, il est procédé à un prélèvement de la quantité ainsi calculée d'inoculum précalibré dans le récipient primaire 101 au moyen de l'outil 101' (figure 15H), ce dernier étant ensuite déplacé par le dispositif de manipulation 121 jusqu'à être positionné au-dessus de ou partiellement dans l'orifice de chargement 134 d'un support de mesure 104, 105 dont le bouchon obturateur 150 a été préalablement enlevé, ledit support 104, 105 étant maintenu par un dispositif de manipulation et de transfert 107 correspondant, qui a extrait ledit support de mesure du moyen de support et de stockage 110.
- Le contenu de l'outil 101' est alors injecté dans la chambre centrale 127 du support de mesure 104, 105 considéré, par coulissement adapté de l'ensemble de mâchoires internes 121", aboutissant à un enfoncement total du piston 115 dans le corps 113 et donc à un vidage complet de ce dernier.
- Avant remise en place du bouchon obturateur 150, il est procédé à l'injection d'une quantité complémentaire déterminée de liquide de dilution, de manière à obtenir, dans la chambre centrale 127, un inoculum parfaitement calibré en fonction de l'application envisagée et ayant le volume requis.
- L'ensemble récipient primaire 101 / outil de prélèvement et de transfert 101' permet ainsi de réaliser les différentes opérations suivantes :
- prélèvement d'une partie de colonie bactérienne, selon une quantité relativement bien ajustée (deux volumes de prélèvement dans un rapport d'environ cent),
- dispersion et homogénéisation automatisée de cette colonie bactérienne dans un volume d'eau pour constituer un inoculum précalibré, dont la concentration bactérienne est supérieure à la concentration souhaitée pour l'inoculum calibré,
- mesure de la concentration de l'inoculum précalibré (nombre de bactéries par unité de volume),
- pipetage d'une partie de l'inoculum précalibré et transfert de cette dernière dans un support de mesure, l'inoculum transféré comprenant le nombre voulu de bactéries, le volume d'inoculum transféré étant complémenté par addition d'eau dans la chambre centrale 127 du support de mesure 104, 105 considéré, pour aboutir à un inoculum calibré.
- En vue de la manipulation des supports de mesure 104, 105 et, le cas échéant, de leur évacuation dans un contenant à déchets 160, ainsi que de celle des outils 101' et des récipients primaires 101, l'appareil selon l'invention comporte, d'une part, un premier dispositif de manipulation et de transfert 107, desservant les supports 109 et 110 et se présentant sous la forme d'un bras manipulateur monté avec faculté de rotation et de coulissement sur un premier axe vertical 123 et comprenant deux mâchoires de préhension pivotantes 124, 124' dont la première 124 est munie d'un moyen de prise 125 d'un récipient primaire 101 et dont la seconde 124' présente une forme courbée ou un crochet destiné à venir en prise en deux endroits distincts d'un support de mesure 104, 105, de manière à maintenir ce dernier par soutien inférieur et par pincement en coopération avec la première mâchoire de préhension 124 et, d'autre part, un second dispositif de manipulation et de transfert 107', desservant le module d'incubation 103 et le module 104 de centrifugation et de mesure se présentant sous la forme d'un bras support monté avec faculté de rotation et de coulissement sur un second axe vertical 123' et comportant à son extrémité libre un organe de réception 125' coopérant avec conjugaison de forme avec une partie au moins de la face inférieure des supports de mesure 104, 105, les deux dispositifs de manipulation et de transfert 107, 107' présentant une zone de chevauchement de leurs espaces ou zones de manoeuvre respectivement accessibles, au niveau de laquelle peut notamment s'effectuer le transfert des supports de mesure 104, 105 de l'un à l'autre.
- En vue de la préhension d'un récipient primaire 101 par le moyen de prise 125 de la première mâchoire 124, l'ensemble emboîté seringue 101' / récipient primaire 101 est d'abord soulevé par les ou une des paires de mâchoires 121, 121'.
- Les supports de mesure 104, 105 chargés en inoculum calibré au niveau de leur chambre centrale 127 sont amenés par le second dispositif de manipulation et de transfert 107' dans l'enceinte de confinement renfermant les deuxième et troisième modules 103 et 106, à travers une ouverture obturable 161.
- Durant les phases opératoires suivantes, les supports de mesure 104, 105 sont à plusieurs reprises transférés entre les modules 103 et 106 au moyen du dispositif 107', ce jusqu'à ce que les analyses soient achevées et les résultats enregistrés par l'unité informatique 108.
- Les supports de mesure 104, 105 peuvent ensuite, après exploitation, être évacués dans le contenant à déchets 160, en utilisant successivement les deux dispositifs de manipulation et de transfert 107 et 107'.
- Conformément à une caractéristique de l'invention, représentée partiellement sur les figures 7 et 8 des dessins annexés, le troisième module 106 comporte plusieurs postes de travail 153, notamment de mesure et de centrifugation, comprenant chacun, en plus des différents moyens de mesure par néphélémétrie, par photométrie et/ou par fluorimétrie, d'une part, une embase support 154 en forme de disque, portée par l'extrémité supérieure d'un arbre vertical 154' entraîné en rotation et pouvant s'engager avec enclenchement ou avec maintien par friction radiale dans le manchon concentrique 151 d'un support de mesure 104, 105 et, d'autre part, un dispositif presseur supérieur 155 de forme sensiblement discoïdale et entraîné en rotation autour de son axe de symétrie par friction sur le support 104, 105 disposé dans le poste de travail 153 considéré, chaque dispositif presseur 155 comprenant un ou plusieurs organes presseurs 156, 156', 156" de forme annulaire pouvant être déplacés, de manière réversible, d'une position haute dans laquelle lesdits organes presseurs ne sont pas en contact avec le support de mesure 104, 105 disposé sur l'embase support 154, vers plusieurs positions plus basses dans lesquelles les organes presseurs 156, 156', 156" sont mis successivement en appui sur la membrane flottante affleurante 135 selon un ordre prédéterminé 156", 156', 156, cette dernière prenant elle-même appui au niveau de zones de contact étanches, circulaires ou annulaires, concentriques, ou disposées selon des configurations circulaires ou annulaires concentriques, avec la paroi supérieure 128 du support de mesure 104, 105 considéré.
- En fonction du type de poste de travail 153 considéré, le dispositif presseur 155 associé pourra comporter un nombre variable d'organes presseurs 156, 156', 156".
- Ainsi dans les postes de mesure 153, l'organe presseur extérieur 156" sera absent du dispositif presseur 155 associé.
- La sélection d'une, de deux ou de trois zones d'appui au niveau de la membrane 135, est effectuée en réalisant un déplacement vers le bas plus ou moins important du dispositif presseur 155.
- En effet, les organes presseurs extérieurs 156' et 156" consistent en des structures annulaires concentriques et indépendantes du disque central formant l'organe presseur 156, tout en étant reliées à ce dernier par des moyens de liaisonnement élastiques qui entraînent lesdits organes presseurs 156' et 156" en appui contre la membrane 135 lorsque l'organe presseur 155 est moyennement descendu.
- Selon l'invention, une variante de réalisation du procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques, tel que décrit ci-dessus, peut consister à introduire manuellement au moyen d'un outil de prélèvement et de transfert (non représenté) un volume donné d'un inoculum bactérien initial dans un récipient primaire 1, à effectuer automatiquement une calibration définitive dudit inoculum dans ledit récipient primaire 1 en amenant sa concentration bactérienne et son volume à des valeurs imposées, à effectuer également automatiquement des transferts totaux ou partiels de cet inoculum calibré entre ledit récipient primaire 1 et un ou plusieurs supports de mesure 4, 5 destinés à réaliser, respectivement, soit l'identification, soit l'antibiogramme ou encore ces deux déterminations simultanément en une seule opération combinée, lesdits transferts étant réalisés sans que l'inoculum initial soit mis en contact avec un élément autre que son récipient initial et son ou ses récipients finaux et de manière à ce qu'à leur issue l'inoculum calibré reste confiné à l'intérieur desdits supports de mesure 4, 5 qui sont alors clos, à effectuer automatiquement la répartition de l'inoculum dans une ou plusieurs alvéoles 32, 45 desdits supports de mesure 4, 5 contenant pour la plupart des réactifs appropriés, à réaliser, dans certains cas, notamment pour l'antibiogramme, à l'intérieur d'un support de mesure 4, une opération dite de pré-croissance destinée à mettre les bactéries en état de se multiplier rapidement avant de les soumettre à analyse et à faire des mesures photométriques sur le contenu desdites alvéoles 32, 45 pendant ou à la fin d'une ou de plusieurs incubations subies par l'inoculum dans lesdits supports de mesure 4, 5, les mesures relevées étant enregistrées par un moyen informatique 8 et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- La concentration ou densité de l'inoculum préparé manuellement présente une valeur telle qu'elle soit suffisante, c'est-à-dire qu'elle dépasse une valeur minimale pouvant être facilement vérifiée par l'homme du métier. En effet, ce dernier réalisera une solution aqueuse dont il vérifiera la densité par simple constatation de l'aspect de ladite solution, l'expérience lui permettant de constater que la densité ou concentration est suffisante ou non. Une telle préparation de l'inoculum est facilement accessible à l'homme du métier et est destinée à permettre un ajustement ou une calibration ultérieur à une valeur finale inférieure, par dilution.
- Selon une première caractéristique de l'invention, la calibration automatique de l'inoculum dans le récipient primaire 1 consiste à réaliser, à partir d'un inoculum initial contenant une quantité de bactéries en excès par rapport aux besoins réactionnels, excès vérifié par observation visuelle de la turbidité de l'inoculum initial, une injection d'eau de dilution dans ledit récipient primaire 1, de manière à créer un volume augmenté d'inoculum plus dilué, puis à éliminer une partie de l'inoculum ainsi dilué par aspiration jusqu'à obtention du volume final d'inoculum calibré requis, ces opérations étant conduites et éventuellement répétées sur la base de mesures optiques faites au travers du récipient primaire 1 sur l'inoculum pour en déterminer la concentration, jusqu'à obtenir à la fois la concentration et le volume recherchés pour l'inoculum calibré.
- Conformément à un mode de réalisation préférentiel de l'invention, le transfert de l'inoculum calibré entre le récipient primaire 1 et le ou les supports de mesure 4, 5 est effectué par emboîtement de tout ou partie 11 du récipient primaire 1 contenant l'inoculum dans une cavité prévue à cet effet dans chaque support 4, 5, de manière à y transférer la quantité d'inoculum calibré voulue, contenue dans la partie emboîtée dudit récipient primaire, cet emboîtement assurant l'isolement nécessaire au confinement de l'inoculum dans l'ensemble formé par le support de mesure 4, 5 et le récipient primaire 1 ou la partie 11 du récipient primaire 1 emboîté dans ledit support 4, 5, ainsi que la fermeture de cet ensemble.
- En fonctionnement automatique et sans manipulation intermédiaire par un opérateur du récipient primaire 1 et des supports 4 et/ou 5, tous ces éléments sont introduits au départ par l'opérateur dans un premier module de stockage et de préparation 2, dans lequel les supports 4 et/ou 5 sont alimentés en inoculum, chacun par l'intermédiaire d'au moins une chambre de réception prévue dans lesdits supports, à partir du récipient primaire 1 ou directement au moyen de ce dernier.
- Après cette alimentation des supports 4 et/ou 5, il est effectué une équirépartition de l'inoculum dans les alvéoles de ces derniers par centrifugation, puis lesdits supports 4 rotatifs et/ou 5 sont transférés dans un deuxième module 3 d'incubation, dont ils sont périodiquement extraits pour être soumis dans le module 6 à des mesures néphélémétriques et/ou photométriques et/ou fluorimétriques en vue de l'identification et/ou de la réalisation d'antibiogrammes.
- Dans le cadre de la mise en oeuvre de cette variante de réalisation du procédé selon l'invention, les opérations de précroissance de l'inoculum, de répartition de l'inoculum dans les alvéoles de mesures, de détermination du début de la précroissance, de transfert de l'inoculum après achèvement de la précroissance et de mesures photométriques sur les supports de mesures, sont effectuées d'une manière analogue à celle décrite ci-dessus en regard de la première variante de réalisation, leur mise en oeuvre pratique et les moyens, dispositifs et appareil utilisés étant toutefois différentes, comme va le montrer la description qui suit.
- En vue d'éviter toute contamination de l'inoculum calibré ou non présent dans le support de mesure d'antibiogramme 4, le passage de l'étape de pré-incubation à l'étape d'incubation est effectué sans rupture du confinement de l'intérieur du support rotatif de mesure concerné 4 par rapport à l'extérieur, ledit support restant clos et ledit passage étant réalisé par une action, telle qu'une poussée, sur un élément obturateur participant à la réalisation de ce confinement.
- En outre, pour les cas où l'inoculum initial ne comporte pas suffisamment de matériel bactérien, il peut être prévu, selon une réalisation légèrement modifiée de la variante de réalisation du procédé décrite ci-dessus, d'omettre l'étape de calibration automatique.
- On introduit alors automatiquement un inoculum bactérien initial, mis en place manuellement, au moyen d'un outil de prélèvement et de transfert adapté, dans un récipient primaire 1', dans un support de mesure tel que mentionné ci-dessus et destiné à réaliser soit un antibiogramme, soit une analyse combinée simultanée d'identification et d'antibiogramme, ladite introduction automatique étant réalisée ou achevée de telle manière qu'à son issue le support de mesure soit fermé et isolé de l'extérieur.
- Le récipient primaire 1' présentera une conformation extérieure et un encombrement identiques au récipient primaire 1 et comportera un contenant de stockage et de manipulation de l'inoculum bactérien initial appelé macropipette 73 permettant le transfert de son contenu dudit récipient primaire 1' dans le support de mesure d'antibiogramme ou de détermination combinée destinataire.
- Après cette introduction de l'inoculum bactérien initial dans ledit support de mesure, le procédé consiste à répartir automatiquement, comme décrit précédemment, une partie aliquote de l'inoculum initial dans une ou plusieurs alvéoles 37, 45, ne contenant pas de réactifs, desdits supports de mesure 4, 5, puis à effectuer à l'intérieur du support de mesure 4, 5 une pré-croissance de cet inoculum initial, comme indiqué précédemment, consistant à mettre les bactéries de l'inoculum en état de se multiplier rapidement par une première incubation ou pré-incubation lors de laquelle des mesures photométriques, visant à mesurer la concentration de l'inoculum bactérien et à déterminer le début de croissance, sont réalisées au niveau de la ou des alvéoles 37, 45 contenant ladite première partie aliquote de l'inoculum, à répartir ensuite automatiquement par centrifugation le reste de l'inoculum dans les autres alvéoles 32, 45 contenant des réactifs, et à effectuer des mesures photométriques sur l'inoculum au niveau desdites alvéoles 32, 45, tel que décrit ci-dessus, pendant une nouvelle phase d'incubation subie par l'inoculum dans lesdits supports de mesure 4, 5, les mesures relevées étant enregistrées par un moyen informatique 8 et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- La variante de réalisation du procédé conforme à l'invention sera à présent décrite de manière détaillée à propos d'un exemple de mise en oeuvre pratique et en relation avec une description des matériels utilisés.
- Un appareil pour la mise en oeuvre de la variante de réalisation du procédé est représenté plus particulièrement sur les figures 16 à 18 des dessins annexés, et est essentiellement constitué par un premier module 2 de réception, de stockage et de préparation de supports rotatifs de mesure 4 et/ou 5 frais et usagés, par un deuxième module 3 d'incubation des supports rotatifs 4 et/ou 5, par un troisième module 6 de mesures néphélémétriques et/ou photométriques, par un dispositif 7, 7' de transfert desservant les modules 2, 3 et 6 et par un moyen informatique 8 de contrôle et de commande des différents étapes de procédé et d'acquisition, d'enregistrement, de traitement, d'évaluation et/ou de restitution de données.
- Conformément à l'invention, le premier module 2 de réception, de stockage et de préparation des supports rotatifs de mesure 4 et/ou 5 frais et usagés comporte, en outre, au moins un moyen 59 de réception et de stockage de récipients primaires 1 contenant de l'inoculum non calibré et un dispositif de calibration 60,61 de l'inoculum dans lesdits récipients primaires 1 et de préparation des supports rotatifs 4 et/ou 5.
- Selon une caractéristique de l'invention, chaque récipient primaire 1 de réception de l'inoculum se présente avantageusement (figures 19, 20) sous forme d'un récipient cylindrique muni sur son fond d'au moins un tube d'évent 9, d'une conduite d'évacuation de trop-plein 10 éventuellement d'une conduite 10' de mise à un niveau inférieur du volume d'inoculum, d'un moyen de prélèvement d'une quantité prédéterminée d'inoculum, monté de manière séparable, par arrachement ou par emboîtement, dans le fond du récipient 1 et excentré par rapport à l'axe dudit récipient 1, telle qu'une pipette 11, et d'un logement transversal 12 en forme d'auge s'étendant entre les parois du récipient 1 qui est pourvu à chaque extrémité dudit logement 12 d'une fenêtre de mesure 13, ce logement 12 étant muni, en outre, d'une partie surélevée 12' communiquant avec ledit logement 12, l'évent 9, la conduite de trop-plein 10, la conduite 10' de mise à un niveau inférieur et le moyen de prélèvement 11 étant fermés de manière étanche par un film arrachable 14, un couvercle de fermeture 15 coopérant par emboîtement conique étanche avec la partie supérieure conique 16 dudit récipient 1.
- Le logement transversal 12, et plus particulièrement la partie surélevée 12' de ce dernier, est destiné à la préparation manuelle de l'inoculum en solution aqueuse à partir d'une solution de culture, ladite solution étant déposée dans le fond du logement 12, sur la partie surélevée 12', au moyen d'un organe de prélèvement servant simultanément à réaliser un premier mélange de la solution de culture avec l'eau rajoutée.
- La partie supérieure conique 16 du récipient primaire 1 est pourvue d'au moins une encoche 17 de faible profondeur et de deux encoches 18 de profondeur plus importante et de largeur différente, disposées en alignement entre-elles et à 90° par rapport à l'axe passant par la ou les encoches 17 de faible profondeur, cette ou ces encoches de faible profondeur 17 étant alignées dans l'axe du logement 12 du fond et les encoches 18 de profondeur plus importante coopérant avec des pattes 19 de section correspondante prévues sur le couvercle de fermeture étanche 15 qui est pourvu, d'une part, sur sa face supérieure, d'une surface 20 s'étendant dans l'axe des pattes 19 et, d'autre part, d'une paroi conique 21 de forme correspondante à celle de la partie supérieure conique 16 du récipient 1 et reliant les pattes 19.
- La surface 20, légèrement en retrait et qui s'étend entre les pattes 19, et donc entre les encoches 18 lorsque le couvercle de fermeture 15 est monté sur le récipient primaire 1, est destinée à la réception d'un moyen d'identification codé 20', tel qu'une étiquette adhésive à code à barres.
- L'encoche 17 de faible profondeur permet de réaliser un positionnement précis du récipient primaire 1 dans le module 2, afin de permettre notamment la lecture du moyen d'identification. Cette encoche 17 est destinée, par ailleurs, à assurer une orientation correcte du récipient primaire 1 lors de la calibration automatique de l'inoculum, ainsi que pour l'inoculation du support rotatif 4 pour la réalisation d'antibiogrammes.
- La pipette 11 formant le moyen de prélèvement d'une quantité prédéterminée d'inoculum est montée de manière séparable par arrachement ou par emboîtement dans le fond du récipient 1 retourné de manière à présenter son couvercle 15 tourné vers le bas. Cette pipette 11 est pourvue, près de son extrémité dépassant sous le fond du récipient 1, d'une collerette ou d'un manchon 11', par laquelle elle est reliée avec le fond du récipient 1 au niveau de la traversée de ce fond, par exemple par une liaison étanche fragilisée ou par emboîtement. De manière connue, le fond et les parois latérales, ainsi que le couvercle 15, du récipient primaire 1 sont réalisés par moulage en un matériau synthétique. Ainsi, lors du remplissage du récipient 1 et pendant sa manipulation, l'étanchéité au niveau de la pipette 11 reste assurée, tandis que, après retournement du récipient 1 fermé par le couvercle, lors de la prise de la pipette 11 et par une légère poussée sur celle-ci, elle est désolidarisée du fond du récipient 1 et peut être transférée vers une utilisation après aspiration d'une quantité prédéterminée d'inoculum.
- Les figures 21 à 23 représentent schématiquement les étapes successives de préparation de l'inoculum et de vérification de sa densité minimale dans le récipient 1, puis la fermeture étanche de ce dernier par le couvercle 15, le film arrachable 14 fermant hermétiquement les orifices extérieurs du tube d'évent 9, de la conduite d'évacuation 10 et de la pipette 11. Lors de l'introduction du récipient primaire 1 dans le premier module 2 de réception et de stockage ainsi que de calibration de l'inoculum, le récipient 1 est retourné de manière à présenter son fond tourné vers le haut et le film 14 est arraché, afin de permettre la calibration de l'inoculum par ajustement éventuel de son volume et/ou par élimination du trop-plein, au moyen du dispositif 60, 61 de calibration de l'inoculum et de préparation des supports rotatifs 4 et/ou 5.
- Le support rotatif 4 pour antibiogramme, représenté aux figures 26 à 28 des dessins annexés, se présente avantageusement sous forme d'un disque composite supérieur muni d'alvéoles périphériques 32 de réception de l'inoculum et de préparations antibiotiques et est caractérisé en ce qu'il est muni d'un corps cylindrique concentrique, de plus petit diamètre que le disque et lié audit disque, formant une chambre centrale 33, de réception de l'inoculum pour la distribution par centrifugation, ladite chambre 33 étant alimentée à travers un orifice 23 de la face supérieure du disque composite supérieur et étant entourée par un manchon 35 de préhension et de rigidification de l'ensemble.
- Le disque composite supérieur du support rotatif pour antibiogramme 4 est constitué, d'une part, par une partie de couvercle circulaire 22 pourvue en son centre d'un orifice 23 et, d'autre part, par un plateau circulaire 31, dont la face supérieure tournée vers la face inférieure de la partie de couvercle 22 porte, en relief sur sa périphérie, les alvéoles 32 de réception de l'inoculum et de préparations antibiotiques, ce plateau circulaire 31 étant relié à la chambre concentrique 33 fermée par un fond 34, la partie de couvercle 22 étant pourvue d'un rebord 22' s'étendant concentriquement par-dessus une paroi circulaire 31' du plateau circulaire 31, délimitant les alvéoles en relief 32 vers l'extérieur, et fixé à ladite paroi circulaire 31' par collage ou soudage.
- Selon une caractéristique de l'invention, le plateau circulaire 31 de la partie inférieure de corps est pourvu, entre les alvéoles en relief 32, d'au moins une alvéole de pré-incubation 37 reliée, par l'intermédiaire d'un capillaire 38, à une chambre concentrique 27 ménagée sous le plateau circulaire 22 de la partie de couvercle, dans la chambre concentrique 33 du plateau circulaire 31 formant la partie inférieure du corps.
- L'orifice 23, prévu au centre de la partie de couvercle 22, est disposée dans un puits 25 s'étendant concentriquement à l'intérieur de la chambre concentrique 27 qui présente une coupelle mobile 28 pourvue d'un milieu de culture sec, ladite coupelle mobile 28 présentant une paroi de guidage étanche 29 délimitant avec ladite coupelle mobile 28 une cuvette, le puits 25 étant fermé par un film étanche 26 recouvrant la partie supérieure du plateau circulaire de couvercle et délimitant simultanément le capillaire 38.
- Le guidage étanche de la coupelle 28 au moyen de sa paroi 29 peut être obtenu par un montage glissant légèrement serré de ladite coupelle 28 et de sa paroi 29 dans la chambre concentrique 27. La coupelle mobile 28 est destinée à la préparation de la culture disposée sur son fond, cette préparation étant réalisée sous forme de solution aqueuse puis séchée, la paroi 29 assurant le logement de la solution aqueuse jusqu'à dessèchement complet.
- Les alvéoles en relief 32 sont délimitées sur leur face tournée vers l'intérieur du support rotatif 4 par une paroi circulaire concentrique 32' et sont pourvues chacune, sur la face de ladite paroi concentrique 32' opposée aux alvéoles 32, de chicanes verticales 32" déterminant des moyens de captage de l'inoculum lors de la centrifugation.
- Le support rotatif 5 pour l'identification, représenté aux figures 24 et 25 des dessins annexés, se présente également avantageusement sous forme d'un disque composite supérieur muni d'alvéoles périphériques 45 de réception de l'inoculum et de réactif de caractérisation et est caractérisé en ce qu'il est muni d'un corps cylindrique concentrique, de plus petit diamètre que le disque et lié audit disque, formant un manchon concentrique 46 de réception du récipient primaire 1 en position retournée, pour la distribution par centrifugation de l'inoculum, ledit manchon 46 étant entouré par un manchon concentrique 48 de préhension et de rigidification de l'ensemble.
- Le manchon concentrique 46 s'étend, au centre, sous la face inférieure du plateau circulaire 44, est relié à cette dernière et est muni à son extrémité libre d'une partie de paroi conique 47, s'étendant intérieurement audit manchon 46 et destinée à coopérer avec la paroi externe de la partie supérieure conique 16 du récipient primaire 1.
- Le disque composite supérieur du support rotatif pour l'identification 5 est constitué, d'une part, par une partie de couvercle circulaire 43 et, d'autre part, par une partie inférieure sous forme d'un plateau circulaire 44 pourvu, sur sa face supérieure tournée vers la face inférieure de la partie de couvercle 43, en relief sur sa périphérie, d'alvéoles 45 de réception de l'inoculum et de réactifs de caractérisation, le couvercle 43 étant pourvu d'un rebord 43' s'étendant concentriquement par-dessus la paroi circulaire 44' du plateau circulaire 44, délimitant les alvéoles en relief 45 vers l'extérieur, et fixé à ladite paroi circulaire 44' par collage ou soudage.
- Les alvéoles en relief 45 sont délimitées sur leur face tournée vers l'intérieur du support rotatif 5 par une paroi circulaire concentrique 45' et sont pourvues chacune, sur la face de ladite paroi concentrique 45' opposée aux alvéoles 45, de chicanes verticales 45" déterminant des moyens de captage de l'inoculum lors de la centrifugation.
- Les moyens de captage de l'inoculum, lors de la centrifugation, prévus, vus en sens radial, devant chaque alvéole 32, 45, respectivement des supports 4 et 5, sont reliés chacun avec l'intérieur d'une alvéole correspondante 32, 45 par l'intermédiaire d'un capillaire 36, 49 et sont ouverts, par ailleurs, sur un espace intérieur 30, 43", communiquant avec la chambre concentrique 33 du plateau circulaire 31 formant la partie inférieure de corps ou avec l'espace de réception du récipient primaire 1 dans le manchon concentrique 46 s'étendant sous la face inférieure du plateau circulaire 44 formant la partie inférieure du disque composite, les alvéoles en relief 32, 45 étant reliées, par ailleurs, chacune par l'intermédiaire d'un capillaire radial 39, 50 à un capillaire circulaire 40, 51 débouchant, par l'intermédiaire d'un autre capillaire 41, 52, à l'extérieur du plateau circulaire 22 de couvercle ou de la partie de couvercle circulaire 43, l'alvéole de pré-incubation 37 prévue sur le support de mesure 4 pour antibiogramme étant reliée directement, par un trou de passage correspondant, au capillaire circulaire 40. Ces différents capillaires sont délimités dans la partie supérieure du plateau circulaire 22 et du couvercle 43 par le film étanche 26 ou 52', les capillaires 41 et 52 communiquant en leur extrémité la plus proche de l'axe central des disques 31 et 44 avec les chambres intérieures 27 et 43" par des trous percés dans les plateaux circulaires 22 et 43.
- Un film étanche de scellement 26, 52 peut se présenter notamment, de manière connue, sous forme d'un film autocollant en deux matériaux, à savoir, par exemple, en aluminium et en polyéthylène. Ainsi, lors des remplissages successifs, par centrifugation, de l'alvéole de pré-incubation 37 et des alvéoles en relief 32, 45 au moyen des capillaires respectifs 38, 36 et 49, l'air contenu dans lesdites alvéoles peut s'échapper, en compensation du remplissage, à travers les capillaires 39, 50, 40, 51 et 52 vers les chambres 27 et 43".
- Le plateau circulaire de couvercle 22 et le couvercle circulaire 43 sont munis, en outre, au-dessus de chaque alvéole 32, 45 et près de son bord, d'une fenêtre de mesure 42, 53, une fenêtre analogue 43, 54 étant prévue sous la face inférieure du plateau circulaire 31, 44 formant la partie inférieure du corps ou du disque composite, en regard de chaque fenêtre de mesure 42, 53 et au moins une zone réfléchissante d'indexation 42', 53', formée sur la face externe de la paroi périphérique externe des supports 4, 5, étant associée à chaque alvéole 32, 45 avec un décalage angulaire fixe par rapport à cette dernière.
- Ainsi, lors des mesures, le passage de chaque alvéole devant le dispositif de mesure est parfaitement repéré au cours de la rotation du support rotatif 4 ou 5 grâce aux zones réfléchissantes ou miroirs d'indexation et la mesure correspondante peut être effectuée de manière parfaitement synchronisée.
- Le récipient primaire 1' utilisé pour l'introduction automatique d'un inoculum bactérien initial dans un support de mesure pour antibiogramme ou analyse combinée simultanée se présente avantageusement, comme le montre la figure 29 des dessins annexés, sous forme d'un réceptacle muni, d'une part, d'une pipette 11 identique à celle associée au récipient primaire 1 et, d'autre part, d'une macropipette 73 de transfert de la totalité du contenu du récipient 1', cette macropipette pouvant être détachée du récipient primaire 1', utilisée pour vider son contenu dans le support 4, puis replacée dans le récipient primaire 1', la pipette 11 étant ensuite détachée et utilisée pour obturer le support 4 en étant déposée dans le puits 25. Dans un tel cas, la solution est directement disposée dans la macropipette 73 et non dans le récipient 1', la pipette 11 servant uniquement de bouchon d'obturation pour un support 4 pour antibiogramme ou éventuellement pour un rajout d'eau.
- Comme il ressort des figures schématiques 21 à 23 des dessins annexés, l'inoculation d'un support rotatif 4 pour antibiogramme s'effectue par saisie, au moyen d'un organe préhenseur d'un dispositif 64 de pipetage et d'injection d'eau et de gaz de l'extrémité de la pipette 11 dépassant hors du fond du récipient 1, puis par introduction de ladite pipette 11, après perforation du film étanche 26, dans le puits 25 s'étendant concentriquement à l'intérieur de la chambre concentrique 27, de manière à dégager l'accès à cette dernière. L'inoculum peut alors être déversé dans la chambre concentrique 27 et un apport d'eau complémentaire peut être effectué. Dans la chambre 27, l'inoculum se mélange au milieu de culture sec destiné à alimenter sa croissance.
- La pipette 11 est alors enfoncée à travers l'orifice 23 et le puits 25 et guidée dans ces derniers au moyen de son manchon ou collerette 11' jusqu'à arriver en butée de la coupelle mobile 28 par son extrémité libre, de manière à réaliser une étanchéité par rapport à l'extérieur. Après une agitation favorisant l'homogénéisation du contenu de la coupelle 28, une première centrifugation est alors effectuée de manière à amener une partie dudit contenu dans l'alvéole de pré-incubation 37, à travers le capillaire 38.
- Dès que le début de croissance aura pu être observé par mesure néphélémétrique, le support rotatif pour antibiogramme 4 sera soumis à une nouvelle centrifugation, le fond mobile 28 de la chambre concentrique 27 étant préalablement poussé au moyen de la pipette 11 de manière à libérer entre sa paroi 29 et celle de ladite chambre 27 des passages permettant le déversement de l'inoculum dans la chambre concentrique 33. Le support rotatif 4 sera alors déplacé successivement dans le module de mesure 6 et dans le deuxième module 3 d'incubation en vue de la réalisation des mesures néphélémétriques et de l'incubation.
- L'inoculation du support rotatif 5 pour l'identification peut être effectuée immédiatement après l'inoculation du support 4, par transfert du récipient primaire 1 sous un support 5 et emboîtement étanche dans ledit support 1. A cet effet, la partie de paroi conique interne 47 du manchon concentrique 46 enserre la paroi extérieure de la partie supérieure conique 16 du récipient 1 et réalise l'étanchéité du montage.
- Une centrifugation du support rotatif 5 a alors pour effet d'amener l'inoculum contenu dans le récipient 1 vers l'espace délimité au-dessus de ce récipient 1 sous la partie de couvercle 43, à travers l'orifice réalisé par l'arrachage ou le retrait de la pipette 11 et de son manchon ou collerette 11' et, de là, vers les alvéoles 45, à travers les capillaires 49, l'air en excès étant évacué à travers les capillaires 50 à 52. Après incubation avec les réactifs de caractérisation, les mesures photométriques sont alors effectuées.
- Comme le montrent plus particulièrement les figures 16 à 18 des dessins annexés, le dispositif de calibration automatique est constitué, d'une part, par une unité inférieure 60 comportant notamment un moyen de lecture du moyen d'identification codé rapporté sur la rainure transversale 20 du couvercle 15 des récipients primaires 1 et un moyen de mesure de densité optique de l'inoculum présent dans lesdits récipients 1 et, d'autre part, par une unité supérieure 61 comportant essentiellement un dispositif de pipetage et d'injection d'eau et d'air.
- Ce dernier dispositif peut être, d'une part, muni d'un organe préhenseur mobile au moins dans une direction verticale et d'un dispositif d'évacuation du trop-plein et, d'autre part, relié à un moyen de pompage ou d'aspiration 62, à un ensemble 63 de vannes de commande des flux de liquides et d'air et à des récipients de liquides 64 et d'air.
- L'organe de préhension du dispositif de pipetage pourra venir en prise étanche, avec conjugaison de forme, sur l'extrémité extérieure libre de la pipette 11 d'un récipient 1, lorsque ce dernier est disposé à un emplacement adéquat, appelé emplacement de travail.
- Cet organe de préhension réalisera aussi l'injection d'eau lors de la phase de calibration automatique de même que le détachement de la pipette 11 par arrachage ou déboîtement du fond du récipient primaire 1, le maintien de la pipette 11 dans une position escamotée avec rétention de l'inoculum et l'introduction de ladite pipette dans le support rotatif 4 pour antibiogramme avec injection de l'inoculum.
- Ledit dispositif de pipetage pourra être relié alternativement à un moyen d'aspiration et à un moyen d'injection contrôlée d'une quantité de fluide, notamment d'eau ou d'air, extraite de réservoirs correspondants.
- L'unité supérieure 61 pourra également comporter un embout mobile pour le branchement étanche d'un tuyau d'évacuation de trop-plein ou d'une pipette relié à un moyen d'aspiration continue et à un réservoir de récupération, ledit embout mobile ou ladite pipette pouvant venir en prise sur l'extrémité libre extérieure de la conduite d'évacuation 10 du trop-plein et/ou de la conduite 10' de mise à niveau intégrée dans le fond du récipient primaire 1, lorsque ce dernier est positionné au niveau de l'emplacement de travail.
- Comme le montrent également les figures 16 à 18 des dessins annexés, le moyen de réception et de stockage 59 consiste en au moins un disque 65 pouvant être actionné en rotation de manière contrôlée et pourvu d'une pluralité de rainures de stockage 66 disposées suivants des rayons dudit disque 65 et pouvant contenir chacune, soit directement, soit au moyen d'un portoir intermédiaire, une rangée alignée de récipients primaires 1 en position inversée et indexés en position angulaire autour de leur axe de symétrie central, chacune desdites rainures 66 pouvant être amenée individuellement en regard de l'ouverture du dispositif de calibration automatique 60, 61, par simple rotation dudit disque 65 en vue de l'extraction de la rangée de récipients primaires 1 concernée.
- Les portoirs intermédiaires pourront avantageusement consister chacun en un réceptacle allongé profilé 60' pouvant contenir chacun simultanément une pluralité de récipients primaires 1, sous forme d'un alignement de récipients primaires 1 en positions inversées, dont chacun est indexé en position angulaire autour de son axe de symétrie central et peut être positionné individuellement à un emplacement de travail défini au niveau des unités supérieure 61 et inférieure 60 constituant le dispositif de calibration et de préparation automatique.
- Chaque récipient primaire 1 pourra ainsi être amené individuellement et positionné verticalement au niveau de l'emplacement de travail, par simple coulissement du réceptacle allongé profilé 60'.
- En outre, le guidage radial des réceptacles allongés profilés 60', formant portoirs pour des alignements de récipients primaires 1, dans les rainures de stockage 66 du moyen 59, permettra de réaliser une agitation des contenus de l'ensemble desdits récipients primaires 1, en soumettant successivement chacun desdits alignements, disposés chacun dans un desdits portoirs 60', à un mouvement alternatif en va-et-vient.
- Conformément à une autre caractéristique de l'invention, les dispositifs de transfert desservant les différents modules 2, 3 et 6 comprennent notamment, d'une part, un premier organe transporteur 7 assurant notamment le transfert des supports rotatifs 4 et 5 entre les modules d'incubation 3 et de mesure 6 et leur prise en charge en provenance du dispositif de calibration automatique 60, 61, d'autre part, un second organe transporteur 7' assurant la prise en charge et le dépôt d'un support rotatif 4 ou 5 au niveau d'un magasin de stockage 67 correspondant, son transfert et son maintien dans le dispositif de calibration automatique 60,61 et son acheminement à un emplacement déterminé permettant sa prise en charge par le premier organe transporteur 7.
- Les mouvements de transfert de supports rotatifs 4, 5 pouvant, bien évidemment, également être réalisés en sens inverse, en vue du rangement des supports 4, 5 usagés dont l'exploitation est achevée. Dans ce cas, chaque support 4, 5 usagé sera transmis par le premier organe transporteur 7 au second organe transporteur 7' qui l'acheminera vers le magasin de stockage 67 du premier module 2 où il sera déchargé et rangé à un ou plusieurs emplacements prévus à cet effet.
- Comme le montrent également les figures 16 à 18 des dessins annexés, le magasin de stockage 67 est situé dans la partie supérieure du premier module 2 et consiste en un magasin circulaire pouvant être animé d'un mouvement de rotation et comportant une pluralité de piles de supports de mesures 4, 5 frais et usagés au niveau de sa périphérie.
- Chaque pile peut être amenée individuellement dans la zone de préhension de l'organe transporteur 7', permettant à ce dernier de soulever le support de mesure 4, 5 supérieur d'une pile positionnée de manière adéquate, et de le transférer vers le dispositif de calibration automatique 60, 61.
- Bien entendu, ledit organe transporteur 7' pourra également recevoir un support de mesure 4, 5 usagé, acheminé par le premier organe transporteur 7 à l'endroit d'échange, et le déposer dans une pile correspondante, préalablement positionnée à l'endroit adéquat desservi par ledit second organe transporteur 7'.
- Selon un mode de réalisation préférentiel de l'invention, l'organe de manipulation du second organe transporteur 7' peut se présenter sous la forme d'une pince 68, ladite pince 68 pouvant notamment se positionner entre les unités inférieures 60 et supérieures 61 du dispositif de calibration automatique de telle manière que le support de mesure 4 ou 5 porté par cette dernière soit disposé au niveau de l'emplacement de travail dudit dispositif de calibration automatique.
- Le maintien des supports de mesure 4 et 5 par ladite pince 68 est réalisé par pincement au niveau de leur partie supérieure.
- Le positionnement des supports 4, 5 au niveau de l'emplacement de travail du dispositif de calibration automatique 60, 61 permettra soit l'introduction de la pipette 11 dans un support de mesure 4 pour antibiogramme, soit l'emboîtement d'un récipient primaire 1 dans un support de mesure 5 pour l'identification.
- Les premier et second organes transporteurs 7 et 7' peuvent consister avantageusement chacun en un bras support 70, respectivement 70', monté avec faculté de rotation et de translation verticale sur un axe 71, respectivement 71', solidaire du châssis de l'appareil.
- Les mouvements du premier organe transporteur 7, dont l'axe peut être fixé sur le module de mesure 6 et dont l'organe de manipulation peut consister en un plan support, permettent un chargement ou un déchargement d'un support de mesure 4 ou 5 à partir du ou vers le second organe transporteur 7', le module 3 d'incubation et le module 6 de mesure.
- Ce dernier peut comporter, au niveau de son ouverture d'accès, un mécanisme échangeur transférant les supports de mesure 4,5 entre un emplacement de chargement/déchargement accessible par l'organe transporteur 7 et un emplacement de mesure, en interchangeant deux supports de mesure 4, 5 entre ces deux emplacements.
- De manière préférentielle, et en vue d'augmenter l'efficience de l'appareil, la durée nécessaire pour le replacement d'un support 4 ou 5 après la phase de mesure et l'amenée d'un nouveau support 4 ou 5 au niveau du module 6 de mesure est environ identique à la durée de la phase de mesure.
- En outre, les supports de mesure 4, 5 peuvent être centrés et guidés en rotation au niveau de l'emplacement de mesure du module 6 de mesure, l'entraînement en rotation desdits supports de mesure 4, 5 étant réalisé par l'intermédiaire d'un organe escamotable supérieur.
- Afin de pouvoir effectuer une centrifugation à vitesse élevée en vue d'une répartition rapide de l'inoculum dans les alvéoles périphériques des supports de mesure 4, 5, le module 6 de mesure peut comprendre un dispositif 72 de centrifugation supplémentaire distinct pouvant être desservi par le premier organe transporteur 7.
- De manière avantageuse, les modules 3 et 6 sont situés dans une enceinte confinée et thermorégulée à une température favorable à l'incubation, alors que le magasin de stockage 67 des supports 4, 5 est à température ambiante ou situé dans un espace éventuellement refroidi.
- L'enceinte confinée et thermorégulée pourra comporter au niveau du lien d'échange entre le premier 7 et le second 7' organes transporteurs, une ouverture obturable, éventuellement de manière étanche, commandée par le moyen informatique 8 de commande et de contrôle.
- L'appareil pour la mise en oeuvre du procédé conforme à l'invention est par conséquent composé par un nombre limité de parties constitutives, dont les mouvements, notamment au niveau des moyens de transfert et du dispositif de calibration automatique, sont extrêmement simplifiés. En outre, la structure et l'agencement interne spécifique dudit appareil permet d'aboutir à un encombrement minimum pour une capacité de traitement donnée.
- Bien entendu, l'invention n'est pas limitée aux modes de réalisation décrits et représentés aux dessins annexés. Des modifications restent possibles, notamment du point de vue de la constitution des divers éléments ou par substitution d'équivalents techniques, sans sortir pour autant du domaine de protection de l'invention.
Claims (38)
- Procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques, sous forme d'antibiogramme, caractérisé en ce qu'il consiste à introduire manuellement, au moyen d'un outil de prélèvement, un volume donné de colonie bactérienne dans un récipient primaire (1 ; 101), à réaliser automatiquement la dispersion de cette colonie bactérienne au sein d'un liquide pour constituer un inoculum au moins précalibré dans ledit récipient primaire (1 ; 101), à effectuer également automatiquement des transferts totaux ou partiels de cet inoculum précalibré entre ledit récipient primaire (1 ; 101) et un ou plusieurs supports de mesure (4, 5 ; 104, 105) destinés à réaliser, respectivement, soit l'identification, soit l'antibiogramme ou encore ces deux déterminations simultanément en une seule opération combinée, lesdits transferts étant réalisés sans que l'inoculum précalibré soit mis en contact avec un élément autre que, d'une part, un outil de prélèvement et de transfert (101'; 1, 101) et/ou le récipient primaire (1 ; 101) et, d'autre part, son ou ses supports de mesure finaux (4,5 ; 104, 105) et de telle manière que les quantités de bactéries transférées correspondent aux quantités requises pour les analyses à réaliser, à effectuer automatiquement la répartition de l'inoculum précalibré, éventuellement après l'avoir convenablement dilué pour aboutir à une calibration définitive, dans une ou plusieurs alvéoles (32, 37, 45 ; 132, 137, 145) desdits supports de mesure (4, 5 ; 104, 105) contenant pour la plupart des réactifs appropriés, à réaliser, dans certains cas, notamment pour l'antibiogramme, à l'intérieur d'un support de mesure (4 ; 104), une opération dite de pré-croissance destinée à mettre les bactéries en état de se multiplier rapidement avant de les soumettre à analyse et à faire des mesures sur le contenu desdites alvéoles (32, 37, 45 ; 132, 137, 145) pendant ou à la fin d'une ou plusieurs incubations subies par l'inoculum dans lesdits supports de mesure (4, 5 ; 104, 105), les mesures relevées étant enregistrées par un moyen informatique (8 ; 108) et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- Procédé selon la revendication 1, caractérisé en ce que le prélèvement d'un volume donné de colonie bactérienne et les transferts des volumes d'inoculum précalibré dans les supports de mesure (104, 105) sont effectués au moyen d'un outil unique de prélèvement et de transfert (101') coopérant avec le récipient primaire (101), les volumes d'inoculum précalibré à transférer étant déterminés à partir de mesures optiques de la concentration bactérienne dudit inoculum, effectuées dans le récipient primaire (101), et calculés en fonction des quantités de bactéries nécessaires.
- Procédé selon l'une quelconque des revendications 1 et 2, caractérisé en ce que le prélèvement et l'introduction dans le récipient primaire (101) d'un volume donné de colonie bactérienne sont effectués au moyen de l'outil de prélèvement et de transfert (101') après sa mise en conformation en vue de prélever le volume souhaité et les transferts d'inoculum précalibré du récipient primaire (101) vers les supports de mesure (104, 105) sont réalisés par pipetage de volumes d'inoculum prédéterminés.
- Procédé selon l'une quelconque des revendications 1 à 3, caractérisé en ce que le transfert de l'inoculum à l'intérieur des supports de mesure (104, 105), notamment vers les alvéoles (132, 145), est contrôlé dynamiquement par commande de l'ouverture ou du blocage étanche de passages successifs conduisant progressivement vers lesdites alvéoles (132, 145).
- Procédé selon la revendication 1, caractérisé en ce qu'il consiste à introduire manuellement au moyen d'un outil de prélèvement et de transfert un volume donné d'inoculum bactérien initial dans un récipient primaire (1), à effectuer automatiquement une calibration définitive dudit inoculum dans ledit récipient primaire (1) en amenant sa concentration bactérienne et son volume à des valeurs imposées, à effectuer également automatiquement des transferts totaux ou partiels de cet inoculum calibré entre ledit récipient primaire (1) et un ou plusieurs supports de mesure (4, 5) destinés à réaliser, respectivement, soit l'identification, soit l'antibiogramme ou encore ces deux déterminations simultanément en une seule opération combinée, lesdits transferts étant réalisés sans que l'inoculum initial soit mis en contact avec un élément autre que son récipient initial et son ou ses récipients finaux et de manière à ce qu'à leur issue l'inoculum calibré reste confiné à l'intérieur desdits supports de mesure (4, 5) qui sont alors clos, à effectuer automatiquement la répartition de l'inoculum dans une ou plusieurs alvéoles (32, 45) desdits supports de mesure (4, 5) contenant pour la plupart des réactifs appropriés, à réaliser, dans certains cas, notamment pour l'antibiogramme, à l'intérieur d'un support de mesure (4), une opération dite de pré-croissance destinée à mettre les bactéries en état de se multiplier rapidement avant de les soumettre à analyse et à faire des mesures photométriques sur le contenu desdites alvéoles (32, 45) pendant ou à la fin d'une ou plusieurs incubations subies par l'inoculum dans lesdits supports de mesure (4, 5), les mesures relevées étant enregistrées par un moyen informatique (8) et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- Procédé, selon la revendication 5, caractérisé en ce que la calibration automatique de l'inoculum dans le récipient primaire (1) consiste à réaliser, à partir d'un inoculum initial contenant une quantité de bactéries en excès par rapport aux besoins réactionnels, excès vérifié par observation visuelle de la turbidité de l'inoculum initial, une injection d'eau de dilution dans ledit récipient primaire (1), de manière à créer un volume augmenté d'inoculum plus dilué, puis à éliminer une partie de l'inoculum ainsi dilué par aspiration jusqu'à obtention du volume final d'inoculum calibré requis, ces opérations étant conduites et éventuellement répétées sur la base de mesures optiques faites au travers du récipient primaire (1) sur l'inoculum pour en déterminer la concentration, jusqu'à obtenir à la fois la concentration et le volume recherchés pour l'inoculum calibré.
- Procédé, selon l'une quelconque des revendications 5 et 6, caractérisé en ce que le transfert de l'inoculum calibré entre le récipient primaire (1) et le ou les supports de mesure (4, 5) est effectué par emboîtement de tout ou partie (11) du récipient primaire (1) contenant l'inoculum dans une cavité prévue à cet effet dans chaque support (4, 5), de manière à y transférer la quantité d'inoculum calibré voulue, contenue dans la partie emboîtée dudit récipient primaire, cet emboîtement assurant l'isolement nécessaire au confinement de l'inoculum dans l'ensemble formé par le support de mesure (4, 5) et le récipient primaire (1) ou la partie (11) du récipient primaire (1) emboîté dans ledit support (4, 5), ainsi que la fermeture de cet ensemble.
- Procédé, selon l'une quelconque des revendications 1 et 5, caractérisé en ce que la pré-croissance de l'inoculum calibré est réalisée, dans les supports de mesure servant à la détermination des antibiogrammes ou dans certains supports de mesure servant à réaliser des déterminations combinées d'antibiogramme et d'identification, par une première incubation, dite pré-incubation, pendant laquelle les bactéries présentes dans l'inoculum sont incubées sans être mises en présence de réactifs et ce jusqu'à ce qu'un début de croissance bactérienne soit mesurable ou jusqu'à ce que la concentration bactérienne atteigne un niveau prédéfini, cette pré-croissance étant suivie de la mise en contact de l'inoculum avec les réactifs et d'une incubation finale pendant laquelle leurs interactions sont observées.
- Procédé, selon l'une quelconque des revendications 1 et 5, caractérisé en ce que la répartition de l'inoculum dans les alvéoles (32, 37, 45 ; 132, 137, 145) situées en périphérie des supports de mesure (4, 5 ; 104, 105) est réalisée par centrifugation, les mesures et les observations effectuées au niveau desdites alvéoles (32, 37, 45 ; 132, 137, 145) étant effectuées par mise en rotation des supports de mesure (4, 5 ; 104, 105) autour de l'axe central de centrifugation desdits supports.
- Procédé, selon l'une quelconque des revendications 1, 5, 8 et 9, caractérisé en ce que, pendant la pré-croissance dans un support de mesure (4 ; 104) d'antibiogramme, la mesure de la concentration de l'inoculum bactérien et la détermination du début de croissance sont réalisées par des mesures photométriques effectuées sur une partie aliquote de l'inoculum transférée à cet effet, par une première centrifugation, dans une alvéole périphérique spécifique (37 ; 137), dédiée à la caractérisation de la croissance pendant la pré-incubation et ne contenant pas de réactifs, le reste d'inoculum restant bloqué pendant la pré-incubation dans une chambre concentrique centrale (27 ; 127) dudit support (4 ; 104), avant d'être transféré, après achèvement de la pré-croissance, dans les autres alvéoles périphériques (32 ; 132) par une deuxième centrifugation, précédée d'une action d'autorisation ou de déblocage appropriée ouvrant le passage pour le transfert du reste de l'inoculum vers lesdites autres alvéoles (32 ; 132) contenant des réactifs.
- Procédé, selon l'une quelconque des revendications 1, 5, 9 et 10, caractérisé en ce que le passage de l'étape de pré-incubation à l'étape d'incubation est effectué sans rupture du confinement de l'intérieur du support rotatif de mesure concerné (4 ; 104) par rapport à l'extérieur, ledit support restant clos et ledit passage étant réalisé par une action, pour le support (4), ou une interruption d'action, pour le support (104), sur un élément obturateur participant à la réalisation de ce confinement.
- Procédé, selon l'une quelconque des revendications 1 à 11, caractérisé en ce que les mesures sont réalisées par néphélémétrie pour les supports de mesure (4 ; 104) servant à l'antibiogramme et par photométrie ou détermination d'absorbance ou de densité optique pour les supports de mesure (5 ; 105) servant à l'identification ou aux déterminations combinées identification/antibiogramme, ou encore par fluorimétrie, après addition préalable d'un marqueur fluorogène au réactif.
- Procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques, dans lequel on introduit automatiquement un inoculum bactérien initial dans un support de mesure selon l'une quelconque des revendications 5 et 8 à 12, destiné à réaliser soit un antibiogramme, soit une analyse combinée simultanée d'identification et d'antibiogrammes, ladite introduction étant réalisée ou achevée de telle manière qu'à son issue le support de mesure soit fermé et isolé de l'extérieur, caractérisé en ce qu'il consiste à répartir automatiquement une partie aliquote de l'inoculum initial dans une ou plusieurs alvéoles (37, 45), ne contenant pas de réactifs, desdits supports de mesure (4, 5), selon l'une quelconque des revendications 9 et 10, à effectuer à l'intérieur du support de mesure (4, 5) une pré-croissance de cet inoculum initial, selon l'une quelconque des revendications 8 et 10, consistant à mettre les bactéries de l'inoculum en état de se multiplier rapidement par une première incubation ou pré-incubation, lors de laquelle des mesures photométriques, selon l'une quelconque des revendications 10 et 12, sont réalisées au niveau de la ou des alvéoles (32, 45) contenant ladite première partie aliquote de l'inoculum, à répartir automatiquement le reste de l'inoculum dans les autres alvéoles (32, 45) contenant des réactifs, selon la revendication 9, et à effectuer des mesures photométriques sur l'inoculum au niveau desdites alvéoles (32, 45), selon la revendication 12 pendant une nouvelle phase d'incubation subie par l'inoculum dans lesdits supports de mesure (4, 5), les mesures relevées étant enregistrées par un moyen informatique (8) et traitées en vue de la caractérisation de la croissance des bactéries présentes dans l'inoculum, de leur identification et/ou de la détermination de leur sensibilité à différents antibiotiques.
- Support de mesure en forme de disque comprenant un corps principal rigide délimitant, sous forme de compartiments non communiquants, une chambre centrale et plusieurs alvéoles périphériques associées, chacune, à une niche de captage, caractérisé en ce que ledit corps principal (126) présente une paroi supérieure (128) pourvue de plusieurs ensembles d'orifices de transfert traversants (129, 130, 131, 133) débouchant respectivement dans la chambre centrale cylindrique (127), dans chaque niche de captage (146) affectée à chaque alvéole (132, 145) et dans chacune desdites alvéoles (132, 145) et recouverte, à l'exception d'une portion centrale entourant l'orifice de chargement (134) de ladite chambre centrale (127) et de la zone des fenêtres de mesure des alvéoles (132, 145), par une membrane flottante étanche affleurante (135) fixée localement et hermétiquement notamment à sa périphérie externe et autour de l'orifice de chargement (134) et pouvant être pressée intimement contre la surface supérieure de ladite paroi supérieure (128) pour former des zones de contact temporaires étanches (136, 138, 142) s'étendant entre ou recouvrant certains desdits ensembles d'orifices traversants (129, 130, 131, 133), notamment au cours de la rotation dudit support de mesure.
- Support de mesure selon la revendication 14, caractérisé en ce que la paroi supérieure (128) comporte, au niveau de sa face supérieure, des rainures ou des renfoncements annulaires concentriques (140, 140') dans lesquel(le)s débouchent les orifices traversants (129, 130, 131, 133) disposés selon des cercles concentriques espacés, la rainure intérieure (140) comprenant une nervure (136) formant surface de contact annulaire et séparant les orifices de sortie (129) de la chambre centrale (127) et les orifices d'entrée (130) de la chambre concentrique annulaire (147) comprenant les niches radiales de captage (146), et les orifices de sortie (131) des niches de captage (146) débouchant au niveau de la face supérieure d'une nervure circulaire concentrique ou de structures proéminentes distinctes (138), par exemple sous forme de dômes, disposée(s) dans la rainure extérieure (140'), les extrémités supérieures de la nervure (136) et des structures (138) étant situées dans un plan ou des plans s'étendant légèrement en retrait du plan de collage de la membrane étanche affleurante (135).
- Support de mesure selon l'une quelconque des revendications 14 et 15, caractérisé en ce qu'il comporte une alvéole de pré-incubation (137) identique aux autres alvéoles périphériques (132, 145), alignée circulairement avec ces dernières et communiquant avec une pré-chambre close (143) formée dans la chambre concentrique (147) renfermant les niches de captage et d'équirépartition (146) et alimentée en inoculum à partir d'une niche de captage interne (144) située au niveau d'une portion de la paroi latérale périphérique (139) de la chambre centrale (127), par l'intermédiaire d'un passage non obturable par les zones de contact étanches (136, 138, 142) pouvant être formées entre la membrane affleurante (135) et la paroi supérieure (128).
- Support de mesure selon la revendication 16, caractérisé en ce que le passage d'alimentation de la pré-chambre (143), communiquant librement avec l'alvéole de pré-incubation (137) et formant également trop-plein pour les niches de captage (146), est constitué par un conduit (157), débutant dans la partie supérieure de la portion de paroi latérale périphérique (139) délimitant la niche de captage interne (144), formé par coopération d'une rainure ménagée dans la partie supérieure d'un prolongement saillant radial (158) de la paroi latérale périphérique (139) de la chambre centrale (127) et de la paroi supérieure (128) et débouchant dans ou à l'entrée d'une rainure (148) à extension radiale centripète, creusée dans la face supérieure de la paroi supérieure (128), formant conduit étanche en coopération avec la membrane (135) contrecollée de part et d'autre de ladite rainure (148) et dont l'extrémité distale se termine au niveau d'un orifice traversant (148') débouchant dans la préchambre (143).
- Support de mesure selon l'une quelconque des revendications 14 à 17, caractérisé en ce que l'orifice de chargement (134) de la chambre centrale (127) est situé dans un renfoncement (134') de la paroi supérieure (128) et est obturable au moyen d'un bouchon (150) dont la partie supérieure est sensiblement de niveau avec la face supérieure de la paroi supérieure (128), en ce que le fond de la chambre centrale (127) est entouré d'un manchon concentrique (151) de préhension et de rigidification, saillant au niveau de la face inférieure du support (104, 105) et en ce qu'une ouverture traversante (152), ayant des dimensions identiques à celles d'une alvéole (132, 145) et située en alignement circulaire avec ces dernières, est ménagée dans le corps principal (126) et dans la paroi supérieure (128), ladite ouverture (152) étant préférentiellement située adjacente à l'alvéole de pré-incubation (137).
- Support de mesure selon l'une quelconque des revendications 14 à 18, caractérisé en ce que la paroi supérieure (128) est munie, au dessus de chaque alvéole (132, 137, 145) et près de son bord extérieur, d'une fenêtre de mesure, une fenêtre analogue étant prévue, dans chacune des portions de paroi du corps principal (126) constituant respectivement les fonds desdites alvéoles, en regard de chaque fenêtre de mesure précitée et au moins une zone réfléchissante d'indexation, formée sur la face externe de la paroi périphérique externe du corps principal (126), étant associée à chaque alvéole (132, 137, 145) avec un décalage angulaire fixe par rapport à cette dernière.
- Appareil pour la mise en oeuvre du procédé selon l'une quelconque des revendications 1 à 12, essentiellement constitué par un premier module (102) de support et de stockage de supports de mesure (104, 105) frais, selon l'une quelconque des revendications 14 à 19, et de récipients primaires (101) coopérant chacun avec un outil de prélèvement et de transfert (101') correspondant, par un deuxième module (103) d'incubation des supports (104 et 105), après injection de l'inoculum bactérien, par un troisième module (106) de centrifugation et de mesures néphélémétriques et/ou photométriques et/ou fluorimétriques, par un ou plusieurs dispositifs (107, 107') de transfert et de manipulation desservant lesdits modules (102, 103 et 106) et par un moyen informatique (108) de contrôle et de commande des différentes étapes du procédé, et d'acquisition, d'enregistrement, de traitement, d'évaluation et/ou de restitution de données, les deuxième et troisième modules (103) et (106) étant disposés dans une enceinte de confinement, appareil caractérisé en ce que les récipients primaires (101) sont portés par un moyen support (109) en forme de couronne, s'étendant concentriquement autour et sous un moyen support (110) en forme de disque portant les supports de mesure (104, 105), les deux moyens supports (109, 110) étant montés avec faculté de rotation autour d'un même axe et en ce que chaque récipient primaire (101) peut être amené, par simple rotation dudit moyen support (109) en forme de couronne, au niveau d'un poste (111) de manipulation de l'outil de prélèvement et de transfert (101') associé et de mesure de densité optique du contenu dudit récipient primaire (101).
- Appareil selon la revendication 20, caractérisé en ce que chaque récipient primaire (101) de réception d'un volume donnée de colonie bactérienne et de préparation d'un inoculum au moins précalibré se présente sous la forme d'un récipient cylindrique ouvert au niveau de sa partie supérieure, laquelle est munie d'un rebord radial (112) pour le maintien dudit récipient primaire (101) dans un des logements correspondants (109') ménagé(s) dans le support mobile (109) en forme de couronne et en ce que l'outil de prélèvement et de transfert (101') consiste en une seringue dont le corps (113) comporte une partie effilée avant de prélèvement et d'éjection (113') et une partie arrière (113") de stockage et de préhension sensiblement cylindrique, ladite partie arrière (113") présentant au moins un décrochement radial extérieur (114) au niveau de son extrémité contiguë à la paroi avant (113') en vue d'un emboîtement partiel avec blocage dudit corps (113) dans le récipient primaire (101), l'extrémité libre avant de la partie avant (113') étant alors située à faible distance du fond dudit récipient primaire (101).
- Appareil selon la revendication 21, caractérisé en ce que la seringue (101') comporte, au niveau de son extrémité avant, des moyens (118, 118') pour prélever, en volume, une quantité réduite ou une quantité normale de colonie bactérienne, en fonction du positionnement de son piston (115).
- Appareil selon l'une quelconque des revendications 20 à 22, caractérisé en ce que chaque récipient primaire (101) comporte dans sa paroi latérale, à proximité de son fond, deux fenêtres de mesure (119, 119') en regard, adaptées pour la mesure de la densité optique du contenu dudit récipient primaire (101) au niveau du poste (111).
- Appareil selon l'une quelconque des revendications 21 à 23, caractérisé en ce que le moyen de manipulation (121) de la seringue constituant l'outil de prélèvement (101'), au niveau du poste (111), consiste en deux ensembles de mâchoires (121' et 121") comprenant deux mâchoires externes (121') destinées à venir en prise rigide et bloquante avec un rebord radial (128) au niveau de l'ouverture de la partie arrière (113") du corps (113) et deux mâchoires internes (121"), disposées concentriquement entre les deux mâchoires externes (121'), destinées à venir en prise rigide et bloquante avec un renflement (122') de la tige d'actionnement (116), la fermeture des deux ensembles de mâchoires (121', 121") étant réalisée simultanément par coulissement d'un manchon (121"') autour et le long des mâchoires externes (121'), les mâchoires internes (121") pouvant coulisser par rapport aux mâchoires externes (121'), notamment en position de fermeture, et au manchon (121"') et ce dernier pouvant prendre appui sur le support mobile (109) en forme de couronne et sur le bord radial (112) de l'ouverture supérieure du récipient primaire (101) considéré, de manière à bloquer ce dernier en position dans son logement (109') lors du coulissement de l'un quelconque des deux ensembles de mâchoires (121', 121").
- Appareil selon l'une quelconque des revendications 20 à 24, caractérisé en ce qu'il comporte, d'une part, un premier dispositif de manipulation et de transfert (107), desservant les supports (109 et 110) et se présentant sous la forme d'un bras manipulateur monté avec faculté de rotation et de coulissement sur un premier axe vertical (123) et comprenant deux mâchoires de préhension (124, 124') dont la première (124) est munie d'un moyen de prise (125) d'un récipient primaire (101) et dont la seconde (124') présente une forme courbée ou un crochet destiné à venir en prise en deux endroits distincts d'un support de mesure (104, 105), de manière à maintenir ce dernier par soutien inférieur et par pincement en coopération avec la première mâchoire de préhension (124) et, d'autre part, un second dispositif de manipulation et de transfert (107'), desservant le module d'incubation (103) et le module (104) de centrifugation et de mesure, se présentant sous la forme d'un bras support monté avec faculté de rotation et de coulissement sur un second axe vertical (123') et comportant à son extrémité libre un organe de réception (125') coopérant avec conjugaison de forme avec une partie au moins de la face inférieure des supports de mesure (104, 105), les deux dispositifs de manipulation et de transfert (107, 107') présentant une zone de chevauchement de leurs espaces ou zones de manoeuvre respectivement accessibles, au niveau de laquelle peut notamment s'effectuer le transfert des supports de mesure (104, 105) de l'un à l'autre.
- Appareil selon l'une quelconque des revendications 20 à 25, caractérisé en ce que le troisième module (106) comporte plusieurs postes de travail (153), notamment de mesure et de centrifugation, comprenant chacun, en plus des différents moyens de mesure par néphélémétrie, par photométrie et/ou par fluorimétrie, d'une part, une embase support (154) en forme de disque, portée par l'extrémité supérieure d'un arbre vertical (154') entraîné en rotation et pouvant s'engager avec enclenchement ou avec maintien par friction radiale dans le manchon concentrique (151) d'un support de mesure (104, 105) et, d'autre part, un dispositif presseur supérieur (155) de forme sensiblement discoïdale et entraîné en rotation autour de son axe de symétrie par friction sur le support de mesure (104, 105), ledit dispositif presseur (155) comprenant un ou plusieurs organes presseurs (156, 156', 156") de forme annulaire et pouvant être déplacé, de manière réversible, d'une position haute dans laquelle lesdits organes presseurs ne sont pas en contact avec le support de mesure (104, 105) disposé sur l'embase support (154), vers plusieurs positions plus basses dans lesquelles ils sont successivement mis en appui sur la membrane flottante affleurante (135) selon un ordre prédéterminé (156", 156', 156), cette dernière prenant elle-même appui au niveau de zones de contact étanches, circulaires ou annulaires, concentriques, ou disposées selon des configurations circulaires ou annulaires concentriques, avec la paroi supérieure (128) du support de mesure (104, 105) considéré.
- Appareil pour la mise en oeuvre du procédé, selon l'une quelconque des revendications 5 à 12 et 13, essentiellement constitué par un premier module de réception et de stockage de supports de mesure (4 et/ou 5) frais et usagés, par un deuxième module (3) d'incubation des supports (4 et/ou 5), par un troisième module (6) de mesures néphélémétriques et/ou photométriques et/ou fluorimétriques, par un ou plusieurs dispositifs (7, 7') de transfert desservant les modules (2, 3 et 6) et par un moyen informatique (8) de contrôle et de commande des différents étapes de procédé, et d'acquisition, d'enregistrement, de traitement, d'évaluation et/ou de restitution de données, caractérisé en ce que le premier module (2) de réception et de stockage des supports de mesure (4 et/ou 5) frais et usagés comporte, en outre, au moins un moyen (59) de réception et de stockage de récipients primaires (1) contenant de l'inoculum bactérien initial et un dispositif de calibration (60, 61) de l'inoculum dans lesdits récipients primaires (1) et de préparation desdits supports de mesure (4 et/ou 5).
- Appareil, selon la revendication 27, caractérisé en ce que le récipient primaire (1) de réception de l'inoculum se présente sous forme d'un récipient cylindrique muni sur son fond d'au moins un tube d'évent (9), d'une conduite d'évacuation de trop-plein (10) éventuellement d'une conduite (10') de mise à un niveau inférieur du volume d'inoculum, d'un moyen de prélèvement d'une quantité prédéterminée d'inoculum, monté de manière séparable, par arrachement ou par emboîtement, dans le fond du récipient (1) et excentré par rapport à l'axe dudit récipient (1), telle qu'une pipette (11), et d'un logement transversal (12) en forme d'auge s'étendant entre les parois du récipient (1), qui est pourvu à chaque extrémité dudit logement (12) d'une fenêtre de mesure (13), ce logement (12) étant muni, en outre, d'une partie surélevée (12') communiquant avec ledit logement (12), l'évent (9), la conduite de trop-plein (10), la conduite (10') de mise à un niveau inférieur et le moyen de prélèvement (11) étant fermés de manière étanche par un film arrachable (14), un couvercle de fermeture (15) coopérant par emboîtement conique étanche avec la partie supérieure conique (16) dudit récipient (1).
- Appareil, selon la revendication 28, caractérisé en ce que la partie supérieure conique (16) du récipient primaire (1) est pourvue d'au moins une encoche (17) de faible profondeur et de deux encoches (18) de profondeur plus importante et de largeur différente, disposées en alignement entre-elles et à 90° par rapport à l'axe passant par la ou les encoches (17) de faible profondeur, cette ou ces encoches de faible profondeur (17) étant alignées dans l'axe du logement (12) du fond et les encoches (18) de profondeur plus importante coopérant avec des pattes (19) de section correspondante prévues sur le couvercle de fermeture étanche (15) qui est pourvu, d'une part, sur sa face supérieure, d'une surface (20) s'étendant dans l'axe des pattes (19) et, d'autre part, d'une paroi conique (21) de forme correspondante à celle de la partie supérieure conique (16) du récipient (1) et reliant les pattes (19).
- Appareil, selon la revendication 27, mettant en oeuvre un support rotatif (4) pour antibiogramme, qui se présente sous forme d'un disque composite supérieur muni d'alvéoles périphériques (32) de réception de l'inoculum et de préparations antibiotiques, caractérisé en ce que ledit support de mesure rotatif (4) est muni d'un corps cylindrique concentrique, de plus petit diamètre que le disque et lié audit disque, formant une chambre centrale (33), de réception de l'inoculum pour la distribution par centrifugation, ladite chambre (33) étant alimentée à travers un orifice (23) de la face supérieure du disque composite supérieur et étant entourée par un manchon (35) de préhension et de rigidification de l'ensemble.
- Appareil, selon l'une quelconque des revendications 27 et 30, caractérisé en ce que le disque composite supérieur du support rotatif pour antibiogramme (4) est constitué, d'une part, par une partie de couvercle circulaire (22) pourvue en son centre d'un orifice (23) et, d'autre part, par un plateau circulaire (31), dont la face supérieure tournée vers la face inférieure de la partie de couvercle (22) porte, en relief sur sa périphérie, les alvéoles (32) de réception de l'inoculum et de préparations antibiotiques, ce plateau circulaire (31) étant relié à la chambre concentrique (33) fermée par un fond (34), la partie de couvercle (22) étant pourvue d'un rebord (22') s'étendant concentriquement par-dessus une paroi circulaire (31') du plateau circulaire (31), délimitant les alvéoles en relief (32) vers l'extérieur, et fixé à ladite paroi circulaire (31') par collage ou soudage.
- Appareil, selon la revendication 31, caractérisé en ce que le plateau circulaire (31) de la partie inférieure de corps est pourvu, entre les alvéoles en relief (32), d'au moins une alvéole de pré-incubation (37) reliée, par l'intermédiaire d'un capillaire (38), à une chambre concentrique (27) ménagée sous le plateau circulaire (22) de la partie de couvercle, dans la chambre concentrique (33) du plateau circulaire (31) formant la partie inférieure du corps.
- Appareil, selon l'une quelconque des revendications 31 et 32, caractérisé en ce que l'orifice (23), prévu au centre de la partie de couvercle (22), est disposée dans un puits (25) s'étendant concentriquement à l'intérieur de la chambre concentrique (27) qui présente une coupelle mobile (28) pourvue d'un milieu de culture sec, ladite coupelle mobile (28) présentant une paroi de guidage étanche (29) délimitant avec ladite coupelle mobile (28) une cuvette, le puits (25) étant fermé par un film étanche (26) recouvrant la partie supérieure du plateau circulaire de couvercle et délimitant simultanément le capillaire (38).
- Appareil, selon la revendication 27, mettant en oeuvre un support rotatif (5) pour l'identification, se présentant sous forme d'un disque composite supérieur muni d'alvéoles périphériques (45) de réception de l'inoculum et de réactif de caractérisation, caractérisé en ce que ledit support rotatif (5) pour l'identification est muni d'un corps cylindrique concentrique, de plus petit diamètre que le disque et lié audit disque, formant un manchon concentrique (46) de réception du récipient primaire (1) en position retournée, pour la distribution par centrifugation de l'inoculum, ce manchon concentrique (46) s'étendant, au centre, sous la face inférieure du plateau circulaire (44), étant relié à cette dernière et étant muni à son extrémité libre d'une partie de paroi conique (47), s'étendant intérieurement audit manchon (46) et destinée à coopérer avec la paroi externe de la partie supérieure conique (16) du récipient primaire (1) et étant entouré par un manchon concentrique (48) de préhension et de rigidification de l'ensemble.
- Appareil, selon la revendication 34, caractérisé en ce que le disque composite supérieur du support rotatif pour l'identification (5) est constitué, d'une part, par une partie de couvercle circulaire (43) et, d'autre part, par une partie inférieure sous forme d'un plateau circulaire (44) pourvu, sur sa face supérieure tournée vers la face inférieure de la partie de couvercle (43), en relief sur sa périphérie, d'alvéoles (45) de réception de l'inoculum et de réactifs de caractérisation, le couvercle (43) étant pourvu d'un rebord (43') s'étendant concentriquement par-dessus la paroi circulaire (44') du plateau circulaire (44), délimitant les alvéoles en relief (45) vers l'extérieur, et fixé à ladite paroi circulaire (44') par collage ou soudage.
- Appareil, selon l'une quelconque des revendications 31 à 35, caractérisé en ce que des moyens de captage de l'inoculum (45"), lors de la centrifugation, prévus, vus en sens radial, devant chaque alvéole (32, 45), respectivement des supports (4 et 5), sont reliés chacun avec l'intérieur d'une alvéole correspondante (32, 45) par l'intermédiaire d'un capillaire (36, 49) et sont ouverts, par ailleurs, sur un espace intérieur (30, 43"), communiquant avec la chambre concentrique (33) du plateau circulaire (31) formant la partie inférieure de corps ou avec l'espace de réception du récipient primaire (1) dans le manchon concentrique (46) s'étendant sous la face inférieure du plateau circulaire (44) formant la partie inférieure du disque composite, les alvéoles en relief (32, 45) étant reliées, par ailleurs, chacune par l'intermédiaire d'un capillaire radial (39, 50) à un capillaire circulaire (40, 51) débouchant, par l'intermédiaire d'un autre capillaire (41, 52), à l'extérieur du plateau circulaire (22) de couvercle ou de la partie de couvercle circulaire (43), l'alvéole de pré-incubation (37) prévue sur le support de mesure (4) pour antibiogramme étant reliée directement, par un trou de passage correspondant, au capillaire circulaire (40), ces différents capillaires étant délimités dans la partie supérieure du plateau circulaire (22) et du couvercle (43) par le film étanche (26 ou 52'), les capillaires (41 et 52) communiquant en leur extrémité la plus proche de l'axe central des disques (31 et 44) avec les chambres intérieures (27 et 43") par des trous percés dans les plateaux circulaires (22 et 43).
- Appareil, selon l'une quelconque des revendications 31 à 33, 35 et 36, caractérisé en ce que le plateau circulaire de couvercle (22) et le couvercle circulaire (43) sont munis, en outre, au-dessus de chaque alvéole (32, 45) et près de son bord, d'une fenêtre de mesure (42, 53), une fenêtre analogue (43, 54) étant prévue sous la face inférieure du plateau circulaire (31, 44) formant la partie inférieure du corps ou du disque composite, en regard de chaque fenêtre de mesure (42, 53) et au moins une zone réfléchissante d'indexation (42', 53'), formée sur la face externe de la paroi périphérique externe des supports (4, 5), étant associée à chaque alvéole (32, 45) avec un décalage angulaire fixe par rapport à cette dernière.
- Appareil, selon la revendication 27, caractérisé en ce que, pour l'introduction automatique d'un inoculum bactérien initial dans un support de mesure pour antibiogramme ou analyse combinée simultanée, le récipient primaire (1') se présente sous forme d'un réceptacle muni, d'une part, d'une pipette (11) identique à celle associée au récipient primaire (1) et, d'autre part, d'une macropipette (73) de transfert de la totalité du contenu du récipient (1'), cette macropipette pouvant être détachée du récipient primaire (1'), utilisée pour vider son contenu dans le support (4), puis replacée dans le récipient primaire (1), la pipette (11) étant ensuite détachée et utilisée pour obturer le support (4) en étant déposée dans le puits (25).
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/647,233 US5863754A (en) | 1995-05-12 | 1996-05-09 | Process for bacteria identification and for determination of the sensitivity of bacteria to antibiotics and apparatus and measuring supports for carrying out this process |
| JP8151462A JPH09117300A (ja) | 1995-05-12 | 1996-05-10 | 細菌を同定し、抗生物質に対する細菌の感度を測定する方法並びに該方法を実施するための装置及び測定サポート |
| CA002176324A CA2176324A1 (fr) | 1995-05-12 | 1996-05-10 | Procede d'identification bacterienne et de determination de la sensibilite de bacteries a des antibiotiques et appareil et supports de mesure pour la mise en oeuvre de ce procede |
| AU52215/96A AU726241B2 (en) | 1995-05-12 | 1996-05-13 | Process for bacteria identification and for determination of the sensitivity of bacteria to antibiotics and apparatus and measuring supports for carrying out this process |
| US09/177,611 US6107082A (en) | 1995-05-12 | 1998-10-23 | Process for bacteria identification and for determination of the sensitivity of bacteria to antibiotics and apparatus and measuring supports for carrying out this process |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9505817 | 1995-05-12 | ||
| FR9505817A FR2733996B1 (fr) | 1995-05-12 | 1995-05-12 | Procede d'identification bacterienne et de determination de la sensibilite de bacteries a des antibiotiques et appareil et consommables pour la mise en oeuvre de ce procede |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0742284A2 true EP0742284A2 (fr) | 1996-11-13 |
| EP0742284A3 EP0742284A3 (fr) | 1999-09-22 |
| EP0742284B1 EP0742284B1 (fr) | 2002-07-17 |
Family
ID=9479051
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP96440034A Expired - Lifetime EP0742284B1 (fr) | 1995-05-12 | 1996-04-29 | Procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques et appareil et supports de mesure pour la mise en oeuvre de ce procédé |
Country Status (5)
| Country | Link |
|---|---|
| EP (1) | EP0742284B1 (fr) |
| AT (1) | ATE220713T1 (fr) |
| DE (1) | DE69622320D1 (fr) |
| FR (1) | FR2733996B1 (fr) |
| ZA (1) | ZA963734B (fr) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1198587A1 (fr) * | 1999-07-30 | 2002-04-24 | Akzo Nobel N.V. | Appareil et technique de detection, de quantification et de caracterisation de micro-organismes |
| CN117721005A (zh) * | 2023-12-23 | 2024-03-19 | 木蕊(上海)医药科技有限公司 | 一种细菌耐药性变化测试装置及其测试方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2013202805B2 (en) * | 2013-03-14 | 2015-07-16 | Gen-Probe Incorporated | System and method for extending the capabilities of a diagnostic analyzer |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3832532A (en) * | 1972-08-18 | 1974-08-27 | Pfizer | Method and apparatus for testing antibiotic susceptibility |
| EP0211334A1 (fr) * | 1985-08-05 | 1987-02-25 | Martin Marietta Energy Systems, Inc. | Méthode et appareil pour procéder et aliquoter automatiquement des échantillons de sang total pour une analyse dans un analyseur centrifugeur rapide |
| US4812411A (en) * | 1984-12-21 | 1989-03-14 | Jean Guigan | Method of performing medical analyses, and a conditioning strip and apparatus for performing the method |
| US5314825A (en) * | 1992-07-16 | 1994-05-24 | Schiapparelli Biosystems, Inc. | Chemical analyzer |
-
1995
- 1995-05-12 FR FR9505817A patent/FR2733996B1/fr not_active Expired - Fee Related
-
1996
- 1996-04-29 EP EP96440034A patent/EP0742284B1/fr not_active Expired - Lifetime
- 1996-04-29 AT AT96440034T patent/ATE220713T1/de not_active IP Right Cessation
- 1996-04-29 DE DE69622320T patent/DE69622320D1/de not_active Expired - Lifetime
- 1996-05-10 ZA ZA963734A patent/ZA963734B/xx unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3832532A (en) * | 1972-08-18 | 1974-08-27 | Pfizer | Method and apparatus for testing antibiotic susceptibility |
| US4812411A (en) * | 1984-12-21 | 1989-03-14 | Jean Guigan | Method of performing medical analyses, and a conditioning strip and apparatus for performing the method |
| EP0211334A1 (fr) * | 1985-08-05 | 1987-02-25 | Martin Marietta Energy Systems, Inc. | Méthode et appareil pour procéder et aliquoter automatiquement des échantillons de sang total pour une analyse dans un analyseur centrifugeur rapide |
| US5314825A (en) * | 1992-07-16 | 1994-05-24 | Schiapparelli Biosystems, Inc. | Chemical analyzer |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1198587A1 (fr) * | 1999-07-30 | 2002-04-24 | Akzo Nobel N.V. | Appareil et technique de detection, de quantification et de caracterisation de micro-organismes |
| EP1198587A4 (fr) * | 1999-07-30 | 2006-06-07 | Bio Merieux Inc | Appareil et technique de detection, de quantification et de caracterisation de micro-organismes |
| CN117721005A (zh) * | 2023-12-23 | 2024-03-19 | 木蕊(上海)医药科技有限公司 | 一种细菌耐药性变化测试装置及其测试方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP0742284A3 (fr) | 1999-09-22 |
| ZA963734B (en) | 1996-11-21 |
| DE69622320D1 (de) | 2002-08-22 |
| ATE220713T1 (de) | 2002-08-15 |
| EP0742284B1 (fr) | 2002-07-17 |
| FR2733996A1 (fr) | 1996-11-15 |
| FR2733996B1 (fr) | 1997-06-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2176324A1 (fr) | Procede d'identification bacterienne et de determination de la sensibilite de bacteries a des antibiotiques et appareil et supports de mesure pour la mise en oeuvre de ce procede | |
| EP0054262B1 (fr) | Dispositif autonome d'analyse simultanée et procédé de mise en oeuvre | |
| EP0352689B1 (fr) | Dispositif pour la réalisation d'analyses biologiques par détection immuno-enzymatique d'anticorps ou d'antigènes dans un sérum | |
| EP0180511B1 (fr) | Procédé et appareil de préparation d'échantillons à des fins d'analyse | |
| EP1913403B1 (fr) | Analyseur automatique plurisisciplinaire pour le diagnostic in vitro | |
| EP0385902B1 (fr) | Dispositif pour remplir des boîtes de Pétri | |
| EP0286536B1 (fr) | Transporteur rotatif à avance pas-à-pas et installation de prélèvement d'échantillons liquides comportant un tel transporteur | |
| EP0738395A1 (fr) | Appareil automatique de dosage immunologique | |
| EP0197866B1 (fr) | Procédé pour la réalisation d'analyses médicales d'un échantillon liquide à l'aide de réactifs secs, et dispositif pour la mise en oeuvre du procédé | |
| WO2011117523A1 (fr) | Procédé automatique et automate de préparation et d'analyse d'une pluralité de suspensions cellulaires | |
| FR2953932A1 (fr) | Procede de separation et de detection d'un analyte | |
| FR2948945A1 (fr) | Dispositif et procede de distribution d'un produit dans une boite de petri | |
| EP2233560B1 (fr) | Dispositif de culture cellulaire ou tissulaire et ensemble associé. | |
| EP2917741A1 (fr) | Dispositif d'analyse pour diagnostic in vitro | |
| EP0742284B1 (fr) | Procédé d'identification bactérienne et de détermination de la sensibilité de bactéries à des antibiotiques et appareil et supports de mesure pour la mise en oeuvre de ce procédé | |
| EP1893123B1 (fr) | Procede pour conditionner dans une paillette une dose predeterminee de substance liquide et dispositif pour le mettre en oeuvre | |
| EP0511097B1 (fr) | Installation de prélèvement d'échantillons fluides dans une zone confinée | |
| EP1352049B1 (fr) | Boite sterile pour la culture de micro-organismes, ensemble et distributeur de boites | |
| EP3423840B1 (fr) | Système d'analyse automatique pour diagnostic in vitro | |
| EP3692354B1 (fr) | Dispositif et procede de coloration d'un materiau organique sur une lame | |
| FR2915488A1 (fr) | Appareil et procedes d'etalement a l'interieur de receptacles, de toutes solutions contenant un echantillon. | |
| EP0189724A1 (fr) | Barrette de conditionnement, dispositif et procédé pour la mis en oeuvre de cette barrette | |
| WO2021089956A1 (fr) | Dispositifs de cytocentrifugation | |
| EP0208611A1 (fr) | Conteneur pour déchets radioactifs de moyenne ou faible activité | |
| FR2698375A1 (fr) | Dispositif pour le transport et le stockage de liquides utilisable, notamment, pour réaliser des kits pour test in vitro. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19960522 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI LU MC NL PT SE |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI LU MC NL PT SE |
|
| 17Q | First examination report despatched |
Effective date: 20010514 |
|
| GRAG | Despatch of communication of intention to grant |
Free format text: ORIGINAL CODE: EPIDOS AGRA |
|
| GRAG | Despatch of communication of intention to grant |
Free format text: ORIGINAL CODE: EPIDOS AGRA |
|
| GRAG | Despatch of communication of intention to grant |
Free format text: ORIGINAL CODE: EPIDOS AGRA |
|
| GRAH | Despatch of communication of intention to grant a patent |
Free format text: ORIGINAL CODE: EPIDOS IGRA |
|
| GRAH | Despatch of communication of intention to grant a patent |
Free format text: ORIGINAL CODE: EPIDOS IGRA |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI LU MC NL PT SE |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20020717 Ref country code: IT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRE;WARNING: LAPSES OF ITALIAN PATENTS WITH EFFECTIVE DATE BEFORE 2007 MAY HAVE OCCURRED AT ANY TIME BEFORE 2007. THE CORRECT EFFECTIVE DATE MAY BE DIFFERENT FROM THE ONE RECORDED.SCRIBED TIME-LIMIT Effective date: 20020717 Ref country code: IE Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20020717 Ref country code: GR Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20020717 Ref country code: GB Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20020717 Ref country code: FI Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20020717 Ref country code: AT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20020717 |
|
| REF | Corresponds to: |
Ref document number: 220713 Country of ref document: AT Date of ref document: 20020815 Kind code of ref document: T |
|
| REG | Reference to a national code |
Ref country code: GB Ref legal event code: FG4D Free format text: NOT ENGLISH |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: EP |
|
| RAP2 | Party data changed (patent owner data changed or rights of a patent transferred) |
Owner name: BIO-RAD PASTEUR |
|
| REG | Reference to a national code |
Ref country code: IE Ref legal event code: FG4D Free format text: FRENCH |
|
| REF | Corresponds to: |
Ref document number: 69622320 Country of ref document: DE Date of ref document: 20020822 |
|
| NLT2 | Nl: modifications (of names), taken from the european patent patent bulletin |
Owner name: BIO-RAD PASTEUR |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20021017 Ref country code: PT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20021017 Ref country code: DK Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20021017 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20021018 |
|
| NLV1 | Nl: lapsed or annulled due to failure to fulfill the requirements of art. 29p and 29m of the patents act | ||
| GBV | Gb: ep patent (uk) treated as always having been void in accordance with gb section 77(7)/1977 [no translation filed] |
Effective date: 20020717 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: ES Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20030130 |
|
| REG | Reference to a national code |
Ref country code: IE Ref legal event code: FD4D Ref document number: 0742284E Country of ref document: IE |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: LU Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20030429 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: MC Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20030430 Ref country code: LI Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20030430 Ref country code: CH Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20030430 Ref country code: BE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20030430 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed |
Effective date: 20030422 |
|
| BERE | Be: lapsed |
Owner name: *PASTEUR SANOFI DIAGNOSTICS Effective date: 20030430 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20031231 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |