CN1842350A - 包含胶原和脱矿骨基质的交联组合物 - Google Patents
包含胶原和脱矿骨基质的交联组合物 Download PDFInfo
- Publication number
- CN1842350A CN1842350A CNA2004800246858A CN200480024685A CN1842350A CN 1842350 A CN1842350 A CN 1842350A CN A2004800246858 A CNA2004800246858 A CN A2004800246858A CN 200480024685 A CN200480024685 A CN 200480024685A CN 1842350 A CN1842350 A CN 1842350A
- Authority
- CN
- China
- Prior art keywords
- compositions
- dbm
- crosslinked
- collagen
- carbodiimide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/3683—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix subjected to a specific treatment prior to implantation, e.g. decellularising, demineralising, grinding, cellular disruption/non-collagenous protein removal, anti-calcification, crosslinking, supercritical fluid extraction, enzyme treatment
- A61L27/3687—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix subjected to a specific treatment prior to implantation, e.g. decellularising, demineralising, grinding, cellular disruption/non-collagenous protein removal, anti-calcification, crosslinking, supercritical fluid extraction, enzyme treatment characterised by the use of chemical agents in the treatment, e.g. specific enzymes, detergents, capping agents, crosslinkers, anticalcification agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L24/00—Surgical adhesives or cements; Adhesives for colostomy devices
- A61L24/0005—Ingredients of undetermined constitution or reaction products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L24/00—Surgical adhesives or cements; Adhesives for colostomy devices
- A61L24/04—Surgical adhesives or cements; Adhesives for colostomy devices containing macromolecular materials
- A61L24/10—Polypeptides; Proteins
- A61L24/102—Collagen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/22—Polypeptides or derivatives thereof, e.g. degradation products
- A61L27/227—Other specific proteins or polypeptides not covered by A61L27/222, A61L27/225 or A61L27/24
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/3604—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix characterised by the human or animal origin of the biological material, e.g. hair, fascia, fish scales, silk, shellac, pericardium, pleura, renal tissue, amniotic membrane, parenchymal tissue, fetal tissue, muscle tissue, fat tissue, enamel
- A61L27/3608—Bone, e.g. demineralised bone matrix [DBM], bone powder
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/3641—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix characterised by the site of application in the body
- A61L27/3645—Connective tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/02—Materials or treatment for tissue regeneration for reconstruction of bones; weight-bearing implants
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- Dermatology (AREA)
- Transplantation (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Botany (AREA)
- Surgery (AREA)
- Molecular Biology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Urology & Nephrology (AREA)
- Zoology (AREA)
- Vascular Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Materials For Medical Uses (AREA)
- Prostheses (AREA)
Abstract
描述了一种包含胶原蛋白和脱矿骨基质的组合物,其中,组合物与碳二亚胺如N-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐(EDC)化学交联。交联反应可以在N-羟基琥珀酰亚胺(NHS)的存在下进行。胶原可以是多孔基质或支架。DBM可以是分散在胶原中的颗粒形式。还描述了一种制备上述组合物的方法,其中,将胶原浆液浇铸成所需形状,冷冻,形成多孔支架,并渗入包含交联剂的溶液。该组合物可用作组织(例如软组织或骨)工程植入物。
Description
相关申请的交叉引用
本申请要求2003年7月25日提交的美国专利申请10/626,571的优先权,该申请被全文纳入本文作为参考。
背景
技术领域
本发明一般涉及生物假体装置,具体涉及包含脱矿骨基质(DBM)的基于化学交联胶原的载体,并涉及这些材料作为植入物如骨诱导植入物的应用。
背景技术
已使用各种材料来修复或再生由于创伤或疾病而缺失的骨或软组织。通常,可植入的骨修复材料提供多孔基质(例如支架(scaffolding)),用于负责骨发生的细胞的移植、增殖和后续的分化。虽然这种方法提供的组合物产生骨侵入性生长的稳定结构,它们不能促进骨增殖或骨再生。
后来的方法使用含有生物活性蛋白的骨修复基质,将其植入骨缺损部位,不仅能够提供骨侵入性向内生长的支撑还能主动诱导骨细胞复制和分化。一般来说,这些骨诱导组合物包含提供骨侵入性生长的支撑的基质、依赖贴壁细胞和骨诱导蛋白源。基质可选自多种材料,包括:胶原、聚乳酸或无机材料如生物可降解多孔陶瓷。已发现可通过骨发生过程诱导新骨形成的两种具体物质包括脱矿物质骨颗粒或粉末和骨形成蛋白(BMP)。
虽然已有多种组合物用于组织工程,仍然存在对可促进和提高骨和软组织修复和再生进行改进或增强的需要,以加快接受植入物的患者的复原和较佳结果。
发明概述
根据本发明的第一方面,提供了一种含有脱矿骨基质(DBM)和胶原蛋白的组合物,其中,该组合物是交联的。组合物可与碳二亚胺化学交联。碳二亚胺可以是N-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐(EDC)。组合物可在N-羟基琥珀酰亚胺(NHS)的存在下与碳二亚胺化学交联。所述组合物还可包含一种或多种生长因子。胶原蛋白可在多孔支架中。DBM可以是颗粒的形式。例如,该组合物可含有分散在含胶原蛋白的多孔支架中的DBM颗粒。DBM颗粒的平均粒度可大到5mm。例如,DBM颗粒的平均粒度可为53-850μm。
根据本发明的第二方面,提供了一种制备包含胶原蛋白和脱矿骨基质的组合物的方法,该方法包括使组合物交联。组合物可与碳二亚胺化学交联。碳二亚胺可以是N-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐(EDC)。组合物可在N-羟基琥珀酰亚胺(NHS)的存在下与碳二亚胺化学交联。使用NHS时,NHS可以EDC/NHS比为1∶2、2∶3或2∶5的比例存在。反应可在或不在pH恒定的环境下如缓冲溶液中发生。本发明此方面方法还包括:将脱矿物质骨颗粒分散在胶原浆液中,将浆液浇铸入模具腔,将铸模浆液冻干,形成含有脱矿骨基质颗粒的多孔胶原支架。例如,浆液可以是含有胶原蛋白和DBM颗粒的水性浆液。浆液可以是酸性pH。根据本发明的这一方面,交联可包括将碳二亚胺交联剂过滤进入多孔胶原支架的孔中并使碳二亚胺交联剂与胶原蛋白分子反应形成交联。
根据本发明的第三方面,提供了一种治疗方法,该方法包括将包含脱矿骨基质(DBM)和胶原蛋白的组合物植入哺乳动物,其中组合物是交联的。组合物可与碳二亚胺化学交联。该组合物可在矫形应用中使用。例如,可将该组合物植入哺乳动物的脊柱或哺乳动物的椎间隙。哺乳动物可以是人。
根据本发明的第四方面,提供了一种包含脱矿骨基质(DBM)和胶原蛋白的组合物,其中组合物通过亚胺键交联。组合物可包括分散在胶原蛋白中的DBM颗粒。胶原蛋白可以在多孔支架中。DBM颗粒的平均粒度可大到5mm。例如,DBM颗粒的平均粒度可为53-850μm。
附图简要说明
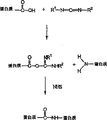
图1阐述了使用本发明的碳二亚胺交联剂形成酰胺交联蛋白基质的过程。
图2-7是已经植入大鼠中的胶原/DBM海绵材料组织切片的图片。
发明详述
根据本发明的一个实施方式,提供了一种包含在胶原载体中的DBM的组合物,该组合物提供细胞迁移的骨传导基质且植入患者后的持续时间延长。根据本发明的另一个实施方式,提供了一种交联含有胶原和DBM的组合物的化学交联方法。交联中,胶原分子可通过胶原分子上存在的反应性基团交联在一起。也是在交联中,由于DBM上反应性表面基团的存在,胶原分子可与DBM交联。结果,产生了一种植入后存在时间更长且随着骨的形成体内还可反转的骨传导基质。这种方法也可控制加入到基质中的DBM的量并最优化最终组合物的材料处置特性。
根据本发明的另一个实施例,可使用碳二亚胺如N-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐(EDC)来化学交联组合物。图1阐述了使用碳二亚胺形成酰胺交联蛋白质基质的过程。如图1所示,第一蛋白质分子上的自由羧酸基团与碳二亚胺反应,形成O-酰基异脲基团。例如,羧酸基团可以在胶原分子的谷氨酸或天冬氨酸残基上。然后,所得O-酰基异脲基团可与第二蛋白质分子的胺基反应,形成交联。例如,胺基可在胶原分子的羟基酪氨酸残基上。
虽然上面讨论了胶原分子间的交联,交联也可在DBM和胶原之间形成。例如,脱矿骨基质表面上的羧酸基团可与碳二亚胺反应,所得O-酰基异脲基团再与胶原分子上的胺基反应。
根据本发明的又一个实施方式,胶原基质可在N-羟基琥珀酰亚胺(NHS)的存在下与碳二亚胺(如EDC)交联。交联反应中加入NHS可增加交联反应速率,因而使得胶原/DBM组合物比不使用NHS的组合物具有更高的交联密度。
根据本发明的又一个实施方式,胶原基质可在缓冲的或恒定pH条件下与EDC交联。多种交联条件公开于国际出版号WO 85/04413。交联条件的例子包括但不限于,碳二亚胺浓度10-300mM,反应温度2-40℃,pH 2-11,反应时间约1-96小时。另一个反应条件的例子包括:碳二亚胺浓度20-200mM,反应温度10-35℃,pH 3-9,反应时间约为2-48小时。其它反应条件包括:碳二亚胺浓度50-150mM,反应温度20-30℃,pH 4-6.5,反应时间4-24小时。
虽然上文描述了EDC,但根据本发明的一个实施方式,也可使用其它碳二亚胺交联剂,包括但不限于氨腈。
根据本发明的一个实施方式,骨诱导组合物中还可加入生长因子、细胞、增塑剂和含钙或磷的化合物。
化学交联方法使得加入到基质中DBM的量和材料处置特性最优化而不明显影响DBM的骨诱导能力。交联法使得产生胶原/DBM组合物,该组合物水合时能维持其形状且水合压缩后能再获得其高度。
根据本发明的一个实施方式,可将胶原/DBM组合物切割成各种形状,并且当卷起以匹配植入物各种构型时能维持其结构。组合物可保留在植入部位中6-10周的时间。然后,该时间范围金枪鱼植入部位和患者个体差异。天然成分胶原可使细胞附着和迁移,并且可被缺损部位存在的细胞重塑。
根据又一个实施方式,组合物可以是小胶原海绵材料的形式。这些海绵材料可单独填充入缺损部位或与用于骨或软组织修复的同种异体移植组织联用。例如,小胶原海绵材料可以是立方体或矩形固体形式。海绵材料的大小可为2-10mm。并且,可将海绵材料研磨成较细大小,与盐水或另一种稀释剂组合,产生糊状材料。这种糊状材料可被注射或填充入伤口部位,用于骨或软组织的修复。
此外,根据本发明的一个实施方式,包含DBM和胶原的组合物的植入物可提供具有骨诱导和骨传导特性的组合物,以促进骨形成。
根据本发明的示例性实施方式,胶原蛋白在多孔支架中。例如,胶原基质可以是多孔或半多孔海绵材料的形式。或者,胶原基质可以是膜、纤维样结构、粉末、羊毛状、颗粒或纤维的形式。多孔支架可提供骨向内生长的骨传导基质。
DBM可以是任何粒度或形状的颗粒形式。例如,根据本发明的一个实施方式,可使用平均之间最多5mm的DBM颗粒。根据本发明的再一个实施方式,可使用平均之间2-4mm的DBM颗粒。根据本发明的另一个实施方案,DBM可以是平均直径为53-850μm的颗粒形式。然而也可使用较大或较小的颗粒,这取决于组合物的所需特性。组合物中的DBM也可以是块或条带的形式。
根据接受植入物的哺乳动物,胶原的来源可以是同种或异种的。胶原可来自人类或动物来源,或者可以是细胞系或细菌表达的重组形式。重组胶原可来自酵母或来自任何原核细胞。可通过任何已知方法从组织提取胶原。胶原蛋白可以是任何类型的胶原。
根据本发明的一个实施方式,组合物可包括任何量的脱矿骨基质(DBM)。可改变DBM的量以获得组合物所需的性质。根据本发明的一个实施方式,以DBM和胶原固体的结合重量计,组合物可包含2-95重量%的DBM。根据本发明的另一个实施方式,以DBM和胶原固体的结合重量计,组合物可包含55-85重量%的DBM。
根据本发明的另一个实施方式,骨诱导性骨修复组合物还可包含一种或多种生长因子。一种或多种生长因子可存在于胶原基质内或在胶原基质上。例如,细胞因子或前列腺素可存在于多孔或半多孔胶原基质内或在其上,或存在于DBM颗粒内或在DBM颗粒上。生长因子可以是天然来源或是使用常规方法重组产生的。生长因子也可以是市售的。两种或多种生长因子的组合可应用于骨诱导组合物,以进一步促进植入物的骨诱导或生物活性。
可使用的生长因子的例子包括但不限于:转化生长因子-β(TGF-β)、例如TGF-β1、TGF-β2和TGF-β3;转化生长因子-α(TGF-α);表皮生长因子(EGF);胰岛素样生长因子-I或II;白介素-I(IL-I);干扰素;肿瘤坏死因子;成纤维细胞生长因子(FGF);血小板衍生生长因子(PDGF);神经生长因子(NGF);和其它显示生长因子或生长因子样作用的分子。根据本发明的一个实施方式,生长因子可以是可溶性生长因子。
可在胶原基质形成之前将生长因子掺入到胶原中。或者,可在水溶液或非水溶液中,使生长因子吸收在胶原基质上。例如,可使含有生长因子的溶液渗入胶原基质。根据本发明的另一个实施方式,可采用真空渗入方法使含有生长因子的溶液渗入胶原基质中。
可以液体形式将生长因子递送至胶原脱矿骨基质组合物中。然而,在重建及吸收或渗入胶原脱矿骨基质组合物之前,生长因子也可以是干燥状态。胶原基质上或胶原基质内存在的生长因子可保留在多孔或半多孔基质的空体积内。也可将控释载体中包含的生长因子掺入胶原脱矿骨基质组合物中。
可使用任何已知的形成多孔胶原支架的方法。例如,可将浆液形式的DBM和胶原(例如水性浆液)浇铸入所需形状的模具空穴中,冻干形成支架。将支架从模具中取出后,使碳二亚胺交联剂渗入组合物的孔中,使其与胶原基质和DBM反应,形成交联。
下面描述了可用于形成交联胶原/DBM组合物的反应方法的非限制性例子。
反应方法1
将10-300mM的EDC水溶液加入到多孔胶原/DBM组合物中,反应1-48小时以使胶原交联。
反应方法2
将用pH 4.0-6.5的MES缓冲液配的浓度为10-300mM的EDC加入到多孔胶原/DBM组合物中,反应1-48小时以使胶原交联。
反应方法3
将含有NHS的浓度为10-300mM的EDC水溶液(EDC/NHS比为1∶2-至2∶5(例如1∶2、2∶3或2∶5))加入到多孔胶原/DBM组合物中,反应1-48小时以使胶原交联。
反应方法4
将用pH 4.0-6.5的MES缓冲液配的含有NHS的浓度为10-300mM的EDC(EDC/NHS比为1∶2-至2∶5(例如1∶2、2∶3或2∶5))溶液加入到多孔胶原/DBM组合物中,反应1-48小时以使胶原交联。
根据本发明的示例性实施方式,可使用化学交联胶原/DBM组合物作为骨移植替代物(例如,作为空隙填充物)。例如,可将化学交联胶原/DBM组合物植入哺乳动物(例如人)中。根据本发明的一个实施方式,可将化学交联胶原/DBM组合物植入哺乳动物的脊柱中。根据本发明的另一个实施方式,可将化学交联胶原/DBM组合物植入哺乳动物的椎间隙中。
试验
胶原海绵材料由60%DBM、40%胶原浆液构成。将胶原浆液和DBM颗粒混合并掺合至均一。将混合物倒入模具中,冷冻,并冻干。室温下使干的海绵材料接触交联溶液。交联溶液由100mM EDC水溶液构成。交联后,用水冲洗海绵材料5次。冷冻海绵材料,然后冻干。然后,将海绵材料封装在陷凹中E-射线照射灭菌。
然后,将海绵材料植入无胸腺大鼠肌内陷凹模型(后肢)中4周。然后取出样品,制备组织切片,切片用Hemotoxylin & Eosin染色。样品的组织切片图片如图2-7所示。
图2是第一种海绵材料的切片图。图片放大倍数为20×。海绵材料1由80%DBM和20%胶原组成。通过使DBM颗粒与胶原浆液结合来制备海绵材料。将所得混合物倒入模具中,冷冻并冻干,形成海绵材料构型。使海绵材料与100mM EDC水溶液接触过夜。用水将所得交联的海绵材料冲洗几遍,冷冻并冻干。通过照射剂量为25kGy的E-射线照射灭菌所得产物。然后将植入样品切割成3毫米的立方体。用几滴盐水水合这些立方体,并将其植入无胸腺大鼠后肢的肌陷凹中。缝合肌陷凹,使动物在无限制条件下维持4周。然后,处死动物,将样品与周围的肌肉组织一起取出。将取出物固定在10%中性缓冲甲醛溶液中。采用标准石蜡包埋技术处理样品,切片并用Hematoxylin和Eosin染色。在标准光镜下,用20×目镜观察切片,分析成骨活性或软骨形成活性。
在图2中,可以看到DBM颗粒内存在软骨形成活性(C)。还可看到一小块新生骨(N)和残留的胶原海绵残留(S)。
图3是第二种海绵材料的切片图。图3中的图片的放大倍数为20×。海绵材料2由80%DBM和20%胶原组成。通过使DBM颗粒与胶原浆液结合来制备海绵材料2。将所得混合物倒入模具中,冷冻并冻干,形成海绵材料构型。海绵材料与10mM EDC水溶液接触过夜。用水将所得交联的海绵材料冲洗几遍,冷冻并冻干。通过照射剂量为25kGy的E-射线照射灭菌所得产物。然后将植入样品切割成3毫米的立方体。用几滴盐水水合这些立方体,并将其植入无胸腺大鼠后肢的肌陷凹中。缝合肌陷凹,使动物在无限制条件下维持4周。然后,处死动物,将样品与周围的肌肉组织一起取出。将取出物固定在10%中性缓冲甲醛溶液中。采用标准石蜡包埋技术处理样品,切片并用Hematoxylin和Eosin染色。在标准光镜下,用20×目镜观察切片,分析成骨活性或软骨形成活性。
在图3中,可以看到成纤维组织(F)和DBM颗粒(DBM)。并且,图3中还可以看到巨细胞骨再塑DBM(G)。
图4是第二种海绵材料的另一个切片图(海绵材料2)。放大倍数也是20×。在图4中,可以看到DBM颗粒(DBM)内的血管(BV)。还可看到残留的胶原海绵材料(S)。
图5是第二种海绵材料的又一个切片图(海绵材料2)。放大倍数也是20×。在图5中,可以看到DBM颗粒(DBM)之间的未发育骨髓形成(C)。
图6是第三种海绵材料的切片图。图片的放大倍数为20×。海绵材料由60%DBM和40%胶原组成。通过使DBM颗粒与胶原浆液结合来制备海绵材料3。将所得混合物倒入模具中,冷冻并冻干,形成海绵材料构型。海绵材料与100mM EDC水溶液接触过夜。用水将所得交联的海绵材料冲洗几遍,冷冻并冻干。通过照射剂量为25kGy的E-射线照射灭菌最终产物。然后将植入样品切割成3毫米的立方体。用几滴盐水水合这些立方体,并将其植入无胸腺大鼠后肢的肌陷凹中。缝合肌陷凹,使动物在无限制条件下维持4周。然后,处死动物,将样品与周围的肌肉组织一起取出。将取出物固定在10%中性缓冲甲醛溶液中。采用标准石蜡包埋技术处理样品,切片并用Hematoxylin和Eosin染色。在标准光镜下,用20×目镜观察切片,分析成骨活性或软骨形成活性。
在图6中,可以看到脱矿骨基质(DBM)颗粒,周围排列着成骨细胞样细胞(O)。
图7是第四种海绵材料的切片图。图片的放大倍数也是20×。图7中所示的海绵材料由60%DBM和40%胶原组成。通过使DBM颗粒与胶原浆液结合来制备海绵材料。将所得混合物倒入模具中,冷冻并冻干,形成海绵材料构型。海绵材料与100mM EDC水溶液接触过夜。用水将所得交联的海绵材料冲洗几遍,冷冻并冻干。通过照射剂量为25kGy的E-射线照射灭菌最终产物。然后将植入样品切割成3毫米的立方体。用几滴盐水水合这些立方体,并将其植入无胸腺大鼠后肢的肌陷凹中。缝合肌陷凹,使动物在无限制条件下维持4周。然后,处死动物,将样品与周围的肌肉组织一起取出。将取出物固定在10%中性缓冲甲醛溶液中。采用标准石蜡包埋技术处理样品,切片并用Hematoxylin和Eosin染色。在标准光镜下,用20×目镜观察切片,分析成骨活性或软骨形成活性。
在图7中,可以看到带有一小块新生骨(N)的脱矿骨基质(DBM)。另外,图7中还可以看到残留的胶原海绵材料(R)。
图2-7表明,本文所述交联胶原/DBM组合物可用作植入物,提供骨诱导和骨传导组合物以促进骨形成。
根据本发明的另一个实施方式,提供了含有脱矿骨基质(DBM)和胶原蛋白的组合物,其中,该组合物可与选自以下的化合物化学交联:戊二醛、甲醛、1,4-丁二醇二甘油醚、羟基吡啶、羟赖氨酰吡啶和甲醛溶液。
还提供了一种含有脱矿骨基质(DBM)和胶原蛋白的组合物,其中,使用照射(例如,e-射线或γ射线照射)、光照(例如,采用合适的发生器的紫外光或其它波长的光)或通过光氧化,使该组合物交联。当使用光照交联时,可使用脉冲光。也可在脱水加热(dehydrothermal)条件下或酸性条件下交联胶原基质。例如,通过在升高的温度下将组合物抽真空,在无水加热条件下交联组合物。
也可使用酶加工使组合物交联。例如,使用赖氨酰氧化酶或组织转谷氨酰胺酶使胶原交联。赖氨酰氧化酶是一种金属蛋白,通过赖氨酸ε氨基的氧化脱氨反应使胶原交联而起效。
也可通过糖化作用(glycation,即通过还原糖如葡萄糖和核糖使胶原氨基非酶交联)或糖基化作用(即葡萄糖非酶连接至胶原,产生一系列化学反应,使相邻蛋白分子之间形成不可逆交联),使胶原基质交联。例如,交联可以是戊糖苷(pentosidine)交联(例如,由赖氨酸和精氨酸残基的非酶糖化作用导致的交联)。或者,胶原中的交联可以是ε(γ-谷氨酰)赖氨酸交联。
交联也可以是细胞驱动的。例如,交联可以是体内培养非交联基质,使胶原通过细胞机制交联的结果。
可将交联胶原/DBM组合物植入哺乳动物,促进组织形成。例如,将交联胶原/DBM组合物植入哺乳动物,促进骨形成。或者,可将交联胶原/DBM组合物植入哺乳动物,促进软组织形成。胶原/DBM组合物可用作矫形应用,颅颌面(cranionmaxillofacial)应用和创伤损伤。
交联过程中,可将一段间隔基(spacer)掺入到胶原/DBM组合物中。间隔基的例子包括但不限于,聚氧亚烷基胺(例如,Huntsman Corporation的注册商标Jeffamine)、聚乙二醇或聚合间隔基。
交联胶原/DBM组合物中也可掺入乙烯吡咯烷酮和甲基丙烯酸甲酯。
交联胶原/DBM组合物中还可掺入胶原酶抑制剂、生长因子、抗体、金属蛋白酶、细胞附着片段或是它们的组合。例如,可在交联前或交联时将一种或多种上述添加剂掺入到组合物中,使添加剂与胶原或DBM交联。
虽然上述说明书公开了本发明的原理,其中实施例是说明的目的,但是,本领域技术人员通过阅读本说明书应明白,不背离本发明的真实范围可对形式和细节进行各种改变。
Claims (57)
1.一种组合物,其包含:
脱矿骨基质(DBM);和
胶原蛋白;
其中,所述组合物是交联的。
2.如权利要求1所述的组合物,其特征在于,所述组合物与碳二亚胺交联剂化学交联。
3.如权利要求2所述的组合物,其特征在于,所述碳二亚胺交联剂是N-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐(EDC)。
4.如权利要求2所述的组合物,其特征在于,所述组合物在N-羟基琥珀酰亚胺(NHS)的存在下化学交联。
5.如权利要求1所述的组合物,其还包含一种或多种生长因子。
6.如权利要求1所述的组合物,其特征在于,所述组合物包含2-95重量%的DBM。
7.如权利要求1所述的组合物,其特征在于,所述组合物包含55-85重量%的DBM。
8.如权利要求1所述的组合物,其特征在于,所述DBM包含分散在胶原中的DBM颗粒。
9.如权利要求1所述的组合物,其特征在于,所述胶原蛋白在多孔支架中。
10.如权利要求9所述的组合物,其特征在于,所述DBM包含分散在多孔支架中的DBM颗粒。
11.如权利要求8所述的组合物,其特征在于,所述DBM颗粒的平均粒度最大为5mm。
12.如权利要求8所述的组合物,其特征在于,所述DBM颗粒的平均粒度为53-850μm。
13.如权利要求1所述的组合物,其特征在于,所述组合物与选自以下的化合物化学交联:戊二醛、甲醛、1,4-丁二醇二甘油醚、羟基吡啶鎓、羟赖氨酰吡啶鎓和甲醛溶液。
14.如权利要求1所述的组合物,其特征在于,所述组合物通过照射进行交联。
15.如权利要求1所述的组合物,其特征在于,所述组合物通过光氧化进行交联。
16.如权利要求1所述的组合物,其特征在于,所述组合物通过酶加工进行交联。
17.如权利要求16所述的组合物,其特征在于,所述胶原蛋白通过组织转谷氨酰胺酶的作用进行交联。
18.如权利要求16所述的组合物,其特征在于,所述组合物与赖氨酰氧化酶交联。
19.如权利要求1所述的组合物,其特征在于,所述组合物通过脱水加热处理进行交联。
20.如权利要求1所述的组合物,其特征在于,所述组合物在酸性条件下交联。
21.如权利要求1所述的组合物,其特征在于,使用e-射线照射、γ照射或光照使所述胶原蛋白交联。
22.如权利要求21所述的组合物,其特征在于,使用脉冲光使所述胶原蛋白交联。
23.如权利要求1所述的组合物,其还包含间隔基。
24.如权利要求23所述的组合物,其特征在于,所述间隔基是聚氧亚烷基胺间隔基或聚乙二醇间隔基。
25.如权利要求1所述的组合物,其特征在于,所述组合物还包含乙烯基吡咯烷酮或甲基丙烯酸甲酯。
26.如权利要求1所述的组合物,其还包含选自以下的添加剂:胶原酶抑制剂、生长因子、抗体、金属蛋白酶、细胞附着片段和它们的组合。
27.如权利要求26所述的组合物,其特征在于,所述添加剂与胶原或DBM结合。
28.如权利要求26所述的组合物,其特征在于,所述添加剂不与胶原或DBM结合。
29.如权利要求1所述的组合物,其特征在于,所述组合物通过糖化或糖基化作用进行交联。
30.如权利要求1所述的组合物,其特征在于,所述交联是戊糖苷交联。
31.如权利要求1所述的组合物,其特征在于,所述交联是ε(γ-谷氨酰)赖氨酸交联。
32.一种制备包含胶原蛋白和脱矿骨基质的组合物的方法,所述方法包括:
交联所述组合物。
33.如权利要求32所述的方法,其特征在于,所述组合物与碳二亚胺交联剂化学交联。
34.如权利要求33所述的方法,其特征在于,所述碳二亚胺是N-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐(EDC)。
35.如权利要求33所述的方法,其特征在于,所述组合物在N-羟基琥珀酰亚胺(NHS)的存在下化学交联。
36.如权利要求35所述的方法,其特征在于,所述NHS以EDC/NHS为1∶2至2∶5的比例存在。
37.如权利要求35所述的方法,其特征在于,所述NHS以EDC/NHS为1∶2、2∶3或2∶5的比例存在。
38.如权利要求32所述的方法,其还包括将脱矿骨基质颗粒分散在胶原浆液中,将所述浆液浇铸入模具腔,并将所述浇铸浆液冻干,以形成含胶原蛋白和脱矿骨基质颗粒的多孔支架。
39.如权利要求38所述的方法,其特征在于,所述浆液是水性浆液。
40.如权利要求38所述的方法,其特征在于,交联包括:
将碳二亚胺交联剂渗入所述多孔支架的孔中;和
使碳二亚胺交联剂与胶原蛋白和/或DBM反应以形成交联。
41.如权利要求32所述的组合物,其特征在于,所述交联是由体内培养非交联基质从而使得胶原通过细胞机制交联而产生的。
42.一种治疗方法,所述方法包括将包含脱矿骨基质(DBM)和胶原蛋白的组合物植入哺乳动物,其中,所述组合物是交联的。
43.如权利要求42所述的方法,其特征在于,所述组合物与碳二亚胺交联剂化学交联。
44.如权利要求42所述的方法,其特征在于,将所述组合物植入哺乳动物的脊柱。
45.如权利要求42所述的方法,其特征在于,将所述组合物植入哺乳动物的椎间隙。
46.如权利要求42所述的方法,其特征在于,将所述组合物植入哺乳动物的创伤损伤部位。
47.如权利要求42所述的方法,其特征在于,将所述组合物植入颅颌面腔。
48.如权利要求42所述的方法,其特征在于,所述哺乳动物是人。
49.一种组合物,其包含:
脱矿骨基质(DBM);和胶原蛋白;
其中,所述组合物通过酰胺键交联。
50.如权利要求49所述的组合物,其还包含一种或多种生长因子。
51.如权利要求49所述的组合物,其特征在于,所述组合物包含2-95重量%的DBM。
52.如权利要求49所述的组合物,其特征在于,所述组合物包含55-85重量%的DBM。
53.如权利要求49所述的组合物,其特征在于,所述组合物包含分散在胶原蛋白中的DBM颗粒。
54.如权利要求49所述的组合物,其特征在于,所述胶原蛋白在多孔支架中。
55.如权利要求54所述的组合物,其特征在于,所述组合物包含分散在多孔支架中的DBM颗粒。
56.如权利要求55所述的组合物,其特征在于,所述DBM颗粒的粒径最大为5mm。
57.如权利要求55所述的组合物,其特征在于,所述DBM颗粒的粒径为53-850μm。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/626,571 US20050020506A1 (en) | 2003-07-25 | 2003-07-25 | Crosslinked compositions comprising collagen and demineralized bone matrix, methods of making and methods of use |
| US10/626,571 | 2003-07-25 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1842350A true CN1842350A (zh) | 2006-10-04 |
Family
ID=34080454
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA2004800246858A Pending CN1842350A (zh) | 2003-07-25 | 2004-07-22 | 包含胶原和脱矿骨基质的交联组合物 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20050020506A1 (zh) |
| EP (1) | EP1648530A1 (zh) |
| JP (1) | JP2007500043A (zh) |
| KR (1) | KR20060052891A (zh) |
| CN (1) | CN1842350A (zh) |
| AU (1) | AU2004261150A1 (zh) |
| CA (1) | CA2533758A1 (zh) |
| WO (1) | WO2005011764A1 (zh) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102284083A (zh) * | 2011-07-07 | 2011-12-21 | 中山大学 | 一种细胞外基质的改性方法 |
| CN101496911B (zh) * | 2008-01-28 | 2012-10-03 | 烟台正海生物技术有限公司 | 一种骨支架材料及其制备方法与应用 |
| CN102716516A (zh) * | 2012-05-11 | 2012-10-10 | 天津大学 | 虎杖甙修饰的胶原支架及其制备方法和应用 |
| CN108210985A (zh) * | 2018-01-22 | 2018-06-29 | 陕西科技大学 | 一种基于人源胶原蛋白的高强度医用水凝胶及其制备方法 |
| CN114502207A (zh) * | 2019-08-26 | 2022-05-13 | 赛特博恩医疗有限公司 | 包含多种硬化状态的植入物 |
Families Citing this family (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7918899B2 (en) * | 2002-01-25 | 2011-04-05 | Biomedical Design, Inc. | Variably crosslinked tissue |
| US20070231788A1 (en) * | 2003-12-31 | 2007-10-04 | Keyvan Behnam | Method for In Vitro Assay of Demineralized Bone Matrix |
| WO2005065396A2 (en) | 2003-12-31 | 2005-07-21 | Osteotech, Inc. | Improved bone matrix compositions and methods |
| US20050266390A1 (en) * | 2004-06-01 | 2005-12-01 | Yuichiro Ueda | Processes for removing cells and cell debris from tissue and tissue constructs used in transplantation and tissue reconstruction |
| EP1796693A2 (en) * | 2004-08-26 | 2007-06-20 | Chandrashekhar P. Pathak | Implantable tissue compositions and method |
| US8445278B2 (en) * | 2005-03-01 | 2013-05-21 | Medtronic, Inc. | Process for producing decellularized biological tissues |
| US20070087059A1 (en) * | 2005-10-17 | 2007-04-19 | Frank Everaerts | Bioactive delivery matrix compositions and methods |
| CN101365499A (zh) | 2005-11-01 | 2009-02-11 | 骨骼技术股份有限公司 | 骨基质组合物和方法 |
| US20070248575A1 (en) * | 2006-04-19 | 2007-10-25 | Jerome Connor | Bone graft composition |
| US20100209470A1 (en) * | 2006-05-01 | 2010-08-19 | Warsaw Orthopedic, Inc. An Indiana Corporation | Demineralized bone matrix devices |
| US7838022B2 (en) * | 2006-05-01 | 2010-11-23 | Warsaw Orthopedic, Inc | Malleable implants containing demineralized bone matrix |
| US8506983B2 (en) * | 2006-05-01 | 2013-08-13 | Warsaw Orthopedic, Inc. | Bone filler material |
| US7771741B2 (en) * | 2006-05-01 | 2010-08-10 | Warsaw Orthopedic, Inc | Demineralized bone matrix devices |
| US20070287991A1 (en) * | 2006-06-08 | 2007-12-13 | Mckay William F | Devices and methods for detection of markers of axial pain with or without radiculopathy |
| CN105327393A (zh) | 2006-06-22 | 2016-02-17 | 南佛罗里达大学 | 胶原支架、具有其的医用植入物以及使用方法 |
| WO2008033505A1 (en) * | 2006-09-13 | 2008-03-20 | University Of South Florida | Biocomposite for artificial tissue design |
| US8048857B2 (en) | 2006-12-19 | 2011-11-01 | Warsaw Orthopedic, Inc. | Flowable carrier compositions and methods of use |
| US8114428B2 (en) * | 2007-03-08 | 2012-02-14 | Sbf Synthetic Bone Factory Gmbh | Methods for manufacturing a composition for treating bone and/or cartilage defects |
| WO2008147867A2 (en) * | 2007-05-23 | 2008-12-04 | Allergan, Inc. | Cross-linked collagen and uses thereof |
| AU2008265852B2 (en) * | 2007-06-15 | 2014-04-17 | Warsaw Orthopedic, Inc. | Method of treating tissue |
| US9554920B2 (en) | 2007-06-15 | 2017-01-31 | Warsaw Orthopedic, Inc. | Bone matrix compositions having nanoscale textured surfaces |
| US8357384B2 (en) | 2007-06-15 | 2013-01-22 | Warsaw Orthopedic, Inc. | Bone matrix compositions and methods |
| WO2008157492A2 (en) * | 2007-06-15 | 2008-12-24 | Osteotech, Inc. | Osteoinductive demineralized cancellous bone |
| WO2009009684A1 (en) * | 2007-07-10 | 2009-01-15 | Osteotech, Inc. | Delivery system |
| US20110054408A1 (en) * | 2007-07-10 | 2011-03-03 | Guobao Wei | Delivery systems, devices, tools, and methods of use |
| WO2009052492A2 (en) | 2007-10-19 | 2009-04-23 | Osteotech, Inc. | Demineralized bone matrix compositions and methods |
| WO2009076594A1 (en) * | 2007-12-12 | 2009-06-18 | Osteotech, Inc. | Bone/collagen composites and uses thereof |
| US8293813B2 (en) * | 2008-03-05 | 2012-10-23 | Biomet Manufacturing Corporation | Cohesive and compression resistant demineralized bone carrier matrix |
| US9616153B2 (en) | 2008-04-17 | 2017-04-11 | Warsaw Orthopedic, Inc. | Rigid bone graft substitute |
| US20090263507A1 (en) * | 2008-04-18 | 2009-10-22 | Warsaw Orthopedic, Inc. | Biological markers and response to treatment for pain, inflammation, neuronal or vascular injury and methods of use |
| US20100119605A1 (en) * | 2008-11-12 | 2010-05-13 | Isenburg Jason C | Compositions for tissue stabilization |
| CH700138B1 (it) * | 2008-12-19 | 2012-12-14 | Ind Biomediche Insubri S A | Matrice per impianto osseo e procedimento di preparazione della stessa. |
| EP2387424A2 (en) * | 2009-01-16 | 2011-11-23 | Geistlich Pharma AG | Method and membrane for tissue regeneration |
| US9011537B2 (en) * | 2009-02-12 | 2015-04-21 | Warsaw Orthopedic, Inc. | Delivery system cartridge |
| GB0907323D0 (en) * | 2009-04-29 | 2009-06-10 | Dynea Oy | Composite material comprising crosslinkable resin of proteinous material |
| US8968785B2 (en) * | 2009-10-02 | 2015-03-03 | Covidien Lp | Surgical compositions |
| FR2952306B1 (fr) * | 2009-11-09 | 2012-03-30 | Creaspine | Composition aqueuse utilisee dans le traitement de la reparation de tissu conjonctif fibreux par laser |
| EP2380601B1 (en) * | 2010-04-15 | 2013-03-20 | National University of Ireland, Galway | Multichannel collagen nerve conduit for nerve repair |
| KR20110117382A (ko) * | 2010-04-21 | 2011-10-27 | 주식회사 메가젠임플란트 | 표면에 콜라겐이 결합된 이상인산칼슘 골대체재의 제조방법 및 그 방법에 의해 제조된 골대체재 |
| US8658711B2 (en) * | 2010-09-29 | 2014-02-25 | Rutgers, The State University Of New Jersey | Process for the synthesis of methacrylate-derivatized type-1 collagen and derivatives thereof |
| PL3505531T3 (pl) | 2011-04-22 | 2024-03-11 | Wyeth Llc | Kompozycje związane ze zmutowaną toksyną Clostridium difficile i sposoby ich wytwarzania |
| BR122016023101B1 (pt) | 2012-10-21 | 2022-03-22 | Pfizer Inc | Polipeptídeo, composição imunogênica que o compreende, bem como célula recombinante derivada de clostridium difficile |
| WO2014065863A1 (en) * | 2012-10-22 | 2014-05-01 | The Regents Of The University Of California | Compositions and methods for promoting collagen-crosslinking |
| CN103920187B (zh) * | 2013-04-16 | 2016-05-25 | 北京航空航天大学 | 一种丝素蛋白和脱钙骨基质复合的骨修复材料 |
| CN107596443A (zh) * | 2016-07-11 | 2018-01-19 | 复旦大学附属华山医院 | 一种无创性可示踪生物材料及其制备方法 |
| US10743996B2 (en) | 2017-03-24 | 2020-08-18 | Robert L. Bundy | Amnion putty for cartilage repair |
| US20220193309A1 (en) * | 2019-04-30 | 2022-06-23 | The General Hospital Corporation | Systems and methods for magnet-induced assembly tissue grafts |
| CN111825859A (zh) * | 2020-07-23 | 2020-10-27 | 陕西科技大学 | 一种具有自修复功能的仿生电子皮肤医用支架材料及其制备方法 |
Family Cites Families (66)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4430760A (en) * | 1981-12-18 | 1984-02-14 | Collagen Corporation | Nonstress-bearing implantable bone prosthesis |
| US4472840A (en) * | 1981-09-21 | 1984-09-25 | Jefferies Steven R | Method of inducing osseous formation by implanting bone graft material |
| US4394370A (en) * | 1981-09-21 | 1983-07-19 | Jefferies Steven R | Bone graft material for osseous defects and method of making same |
| US4440750A (en) * | 1982-02-12 | 1984-04-03 | Collagen Corporation | Osteogenic composition and method |
| US4485097A (en) * | 1982-05-26 | 1984-11-27 | Massachusetts Institute Of Technology | Bone-equivalent and method for preparation thereof |
| US4722948A (en) * | 1984-03-16 | 1988-02-02 | Dynatech Corporation | Bone replacement and repair putty material from unsaturated polyester resin and vinyl pyrrolidone |
| US4789663A (en) * | 1984-07-06 | 1988-12-06 | Collagen Corporation | Methods of bone repair using collagen |
| US5273964A (en) * | 1985-03-20 | 1993-12-28 | Lemons J E | Inorganic and organic composition for treatment of bone lesions |
| US6311690B1 (en) * | 1986-03-27 | 2001-11-06 | Gensci Orthobiologics, Inc. | Bone repair material and delayed drug delivery system |
| US4863732A (en) * | 1987-12-16 | 1989-09-05 | Collagen Corporation | Injectable composition for inductive bone repair |
| US5162114A (en) * | 1989-02-23 | 1992-11-10 | Stryker Corporation | Bone collagen matrix for xenogenic implants |
| DE68929453T2 (de) * | 1988-04-08 | 2003-11-20 | Stryker Corp., Kalamazoo | Osteogene Vorrichtungen |
| US5124273A (en) * | 1988-06-30 | 1992-06-23 | Kabushiki Kaisha Toshiba | Automatic wiring method for semiconductor integrated circuit devices |
| US5290558A (en) * | 1989-09-21 | 1994-03-01 | Osteotech, Inc. | Flowable demineralized bone powder composition and its use in bone repair |
| US5236456A (en) * | 1989-11-09 | 1993-08-17 | Osteotech, Inc. | Osteogenic composition and implant containing same |
| US5645591A (en) * | 1990-05-29 | 1997-07-08 | Stryker Corporation | Synthetic bone matrix |
| US6197325B1 (en) * | 1990-11-27 | 2001-03-06 | The American National Red Cross | Supplemented and unsupplemented tissue sealants, methods of their production and use |
| US5275954A (en) * | 1991-03-05 | 1994-01-04 | Lifenet | Process for demineralization of bone using column extraction |
| US5356629A (en) * | 1991-07-12 | 1994-10-18 | United States Surgical Corporation | Composition for effecting bone repair |
| US5513662A (en) * | 1991-12-31 | 1996-05-07 | Osteotech, Inc. | Preparation of bone for transplantation |
| US5314476A (en) * | 1992-02-04 | 1994-05-24 | Osteotech, Inc. | Demineralized bone particles and flowable osteogenic composition containing same |
| FR2706768B1 (zh) * | 1993-05-13 | 1995-12-01 | Inoteb | |
| US5531791A (en) * | 1993-07-23 | 1996-07-02 | Bioscience Consultants | Composition for repair of defects in osseous tissues, method of making, and prosthesis |
| JP3420634B2 (ja) * | 1994-04-14 | 2003-06-30 | テルモ株式会社 | コラーゲン製材および骨欠損部補綴材 |
| IL110367A (en) * | 1994-07-19 | 2007-05-15 | Colbar Lifescience Ltd | Collagen-based matrix |
| US5516532A (en) * | 1994-08-05 | 1996-05-14 | Children's Medical Center Corporation | Injectable non-immunogenic cartilage and bone preparation |
| US5707962A (en) * | 1994-09-28 | 1998-01-13 | Gensci Regeneration Sciences Inc. | Compositions with enhanced osteogenic potential, method for making the same and therapeutic uses thereof |
| US6180606B1 (en) * | 1994-09-28 | 2001-01-30 | Gensci Orthobiologics, Inc. | Compositions with enhanced osteogenic potential, methods for making the same and uses thereof |
| US6027742A (en) * | 1995-05-19 | 2000-02-22 | Etex Corporation | Bioresorbable ceramic composites |
| US5676976A (en) * | 1995-05-19 | 1997-10-14 | Etex Corporation | Synthesis of reactive amorphous calcium phosphates |
| US6287341B1 (en) * | 1995-05-19 | 2001-09-11 | Etex Corporation | Orthopedic and dental ceramic implants |
| MXPA97009909A (es) * | 1995-06-06 | 2004-08-23 | Gensci Regeneration Lab Inc | Materiales osteogenicos modificados. |
| US5811401A (en) * | 1995-11-30 | 1998-09-22 | The Picower Institute For Medical Research | Advanced glycosylation endproducts and methods of use therefor |
| US5869527A (en) * | 1995-12-29 | 1999-02-09 | Alteon Inc. | 6-(N-carboxymethylamino)caproate, salts thereof and methods of use therefor |
| US6200606B1 (en) * | 1996-01-16 | 2001-03-13 | Depuy Orthopaedics, Inc. | Isolation of precursor cells from hematopoietic and nonhematopoietic tissues and their use in vivo bone and cartilage regeneration |
| US6368356B1 (en) * | 1996-07-11 | 2002-04-09 | Scimed Life Systems, Inc. | Medical devices comprising hydrogel polymers having improved mechanical properties |
| US6165487A (en) * | 1996-09-30 | 2000-12-26 | Children's Medical Center Corporation | Methods and compositions for programming an organic matrix for remodeling into a target tissue |
| ATE239514T1 (de) * | 1997-02-07 | 2003-05-15 | Stryker Corp | Matrixlose osteogene vorrichtungen und implantate und verfahren zu deren verwendung |
| WO1998035653A1 (en) * | 1997-02-13 | 1998-08-20 | Benedict, James, A. | Implantable collagen-containing putty material |
| US6045579A (en) * | 1997-05-01 | 2000-04-04 | Spinal Concepts, Inc. | Adjustable height fusion device |
| US5948426A (en) * | 1997-05-03 | 1999-09-07 | Jefferies; Steven R. | Method and article to induce hematopoietic expansion |
| US5972368A (en) * | 1997-06-11 | 1999-10-26 | Sdgi Holdings, Inc. | Bone graft composites and spacers |
| US6117979A (en) * | 1997-08-18 | 2000-09-12 | Medtronic, Inc. | Process for making a bioprosthetic device and implants produced therefrom |
| US6309659B1 (en) * | 1997-09-02 | 2001-10-30 | Gensci Orthobiologics, Inc. | Reverse phase connective tissue repair composition |
| US20010014667A1 (en) * | 1998-01-05 | 2001-08-16 | Chen Charles C. | Compositions with enhanced osteogenic potential, methods for making the same and therapeutic uses thereof |
| US20020076429A1 (en) * | 1998-01-28 | 2002-06-20 | John F. Wironen | Bone paste subjected to irradiative and thermal treatment |
| US20020018796A1 (en) * | 1998-01-28 | 2002-02-14 | John F. Wironen | Thermally sterilized bone paste |
| US6123731A (en) * | 1998-02-06 | 2000-09-26 | Osteotech, Inc. | Osteoimplant and method for its manufacture |
| US6326018B1 (en) * | 1998-02-27 | 2001-12-04 | Musculoskeletal Transplant Foundation | Flexible sheet of demineralized bone |
| US6437018B1 (en) * | 1998-02-27 | 2002-08-20 | Musculoskeletal Transplant Foundation | Malleable paste with high molecular weight buffered carrier for filling bone defects |
| US6030635A (en) * | 1998-02-27 | 2000-02-29 | Musculoskeletal Transplant Foundation | Malleable paste for filling bone defects |
| US6458375B1 (en) * | 1998-02-27 | 2002-10-01 | Musculoskeletal Transplant Foundation | Malleable paste with allograft bone reinforcement for filling bone defects |
| US6293970B1 (en) * | 1998-06-30 | 2001-09-25 | Lifenet | Plasticized bone and soft tissue grafts and methods of making and using same |
| US6444252B1 (en) * | 1998-11-20 | 2002-09-03 | General Mills, Inc. | Methods of preparation of gel products fortified with calcium |
| US6328765B1 (en) * | 1998-12-03 | 2001-12-11 | Gore Enterprise Holdings, Inc. | Methods and articles for regenerating living tissue |
| US6294187B1 (en) * | 1999-02-23 | 2001-09-25 | Osteotech, Inc. | Load-bearing osteoimplant, method for its manufacture and method of repairing bone using same |
| US20020090725A1 (en) * | 2000-11-17 | 2002-07-11 | Simpson David G. | Electroprocessed collagen |
| AU6406700A (en) * | 1999-03-16 | 2000-10-04 | Regeneration Technologies, Inc. | Molded implants for orthopedic applications |
| US7371408B1 (en) * | 1999-06-07 | 2008-05-13 | Wright Medical Technology, Inc. | Bone graft substitute composition |
| EP1203074A4 (en) * | 1999-06-29 | 2003-09-10 | J Alexander Marchosky | BONE FORMATION AND STRENGTHENING COMPOSITIONS AND METHOD |
| US6340477B1 (en) * | 2000-04-27 | 2002-01-22 | Lifenet | Bone matrix composition and methods for making and using same |
| DK177997B1 (da) * | 2000-07-19 | 2015-02-23 | Ed Geistlich Söhne Ag Für Chemische Ind | Knoglemateriale og collagenkombination til opheling af beskadigede led |
| WO2002024241A2 (en) * | 2000-09-20 | 2002-03-28 | Regeneration Technologies, Inc. | Combination biological-non-biological material prosthetic implant and method |
| US6752831B2 (en) * | 2000-12-08 | 2004-06-22 | Osteotech, Inc. | Biocompatible osteogenic band for repair of spinal disorders |
| US20020082697A1 (en) * | 2000-12-22 | 2002-06-27 | Damien Christopher J. | Implantable osteogenic material |
| CA2412012C (en) * | 2001-11-20 | 2011-08-02 | Ed. Geistlich Soehne Ag Fuer Chemische Industrie | Resorbable extracellular matrix containing collagen i and collagen ii for reconstruction of cartilage |
-
2003
- 2003-07-25 US US10/626,571 patent/US20050020506A1/en not_active Abandoned
-
2004
- 2004-07-22 WO PCT/US2004/023557 patent/WO2005011764A1/en active Application Filing
- 2004-07-22 CA CA002533758A patent/CA2533758A1/en not_active Abandoned
- 2004-07-22 CN CNA2004800246858A patent/CN1842350A/zh active Pending
- 2004-07-22 JP JP2006521921A patent/JP2007500043A/ja active Pending
- 2004-07-22 KR KR1020067001784A patent/KR20060052891A/ko not_active Application Discontinuation
- 2004-07-22 EP EP04778878A patent/EP1648530A1/en not_active Withdrawn
- 2004-07-22 AU AU2004261150A patent/AU2004261150A1/en not_active Abandoned
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101496911B (zh) * | 2008-01-28 | 2012-10-03 | 烟台正海生物技术有限公司 | 一种骨支架材料及其制备方法与应用 |
| CN102284083A (zh) * | 2011-07-07 | 2011-12-21 | 中山大学 | 一种细胞外基质的改性方法 |
| CN102284083B (zh) * | 2011-07-07 | 2013-12-18 | 中山大学 | 一种细胞外基质的改性方法 |
| CN102716516A (zh) * | 2012-05-11 | 2012-10-10 | 天津大学 | 虎杖甙修饰的胶原支架及其制备方法和应用 |
| CN102716516B (zh) * | 2012-05-11 | 2014-02-26 | 天津大学 | 虎杖甙修饰的胶原支架及其制备方法和应用 |
| CN108210985A (zh) * | 2018-01-22 | 2018-06-29 | 陕西科技大学 | 一种基于人源胶原蛋白的高强度医用水凝胶及其制备方法 |
| CN114502207A (zh) * | 2019-08-26 | 2022-05-13 | 赛特博恩医疗有限公司 | 包含多种硬化状态的植入物 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2004261150A1 (en) | 2005-02-10 |
| EP1648530A1 (en) | 2006-04-26 |
| JP2007500043A (ja) | 2007-01-11 |
| WO2005011764A1 (en) | 2005-02-10 |
| US20050020506A1 (en) | 2005-01-27 |
| CA2533758A1 (en) | 2005-02-10 |
| KR20060052891A (ko) | 2006-05-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1842350A (zh) | 包含胶原和脱矿骨基质的交联组合物 | |
| US20200323617A1 (en) | Flowable tissue products | |
| AU2014253753B2 (en) | Demineralized bone fibers having controlled geometry and shapes and methods thereof | |
| CN107073170B (zh) | 用于再生口腔粘膜的生物材料支架 | |
| US20070003525A1 (en) | Hydrogel compositions comprising nucleus pulposus tissue | |
| Murata et al. | Human acid-insoluble dentin with BMP-2 accelerates bone induction in subcutaneous and intramuscular tissues | |
| US20110059178A1 (en) | Tissue Engineered Meniscus Repair Composition | |
| CN104771785A (zh) | 具有神经多肽诱导陈骨活性的骨修复材料的制造方法 | |
| AU2012355466B2 (en) | Flowable tissue products | |
| Zhao | Biomaterial and Cell Based Cartilage Repair | |
| JP2007050084A (ja) | 骨再建材の製造方法および骨再建材ならびに骨組織誘導方法 | |
| JP2004173995A (ja) | 骨修復材および骨原性細胞培養基材 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| ASS | Succession or assignment of patent right |
Owner name: WARSAW ORTHOPEDICS INC. Free format text: FORMER OWNER: SDGI HOLDINGS, INC. Effective date: 20061215 |
|
| C41 | Transfer of patent application or patent right or utility model | ||
| TA01 | Transfer of patent application right |
Effective date of registration: 20061215 Address after: indiana Applicant after: Warsaw Orthopedic Inc. Address before: Delaware Applicant before: SDGI Holding, Inc. |
|
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |