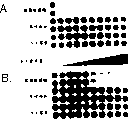CN1642496A - 细菌生物薄膜的酶破坏 - Google Patents
细菌生物薄膜的酶破坏 Download PDFInfo
- Publication number
- CN1642496A CN1642496A CNA038071274A CN03807127A CN1642496A CN 1642496 A CN1642496 A CN 1642496A CN A038071274 A CNA038071274 A CN A038071274A CN 03807127 A CN03807127 A CN 03807127A CN 1642496 A CN1642496 A CN 1642496A
- Authority
- CN
- China
- Prior art keywords
- lysostaphin
- biofilm
- enzyme
- conduit
- antibacterial
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N63/00—Biocides, pest repellants or attractants, or plant growth regulators containing microorganisms, viruses, microbial fungi, animals or substances produced by, or obtained from, microorganisms, viruses, microbial fungi or animals, e.g. enzymes or fermentates
- A01N63/50—Isolated enzymes; Isolated proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/48—Hydrolases (3) acting on peptide bonds (3.4)
- A61K38/482—Serine endopeptidases (3.4.21)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L29/00—Materials for catheters, medical tubing, cannulae, or endoscopes or for coating catheters
- A61L29/14—Materials characterised by their function or physical properties, e.g. lubricating compositions
- A61L29/16—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/20—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing organic materials
- A61L2300/252—Polypeptides, proteins, e.g. glycoproteins, lipoproteins, cytokines
- A61L2300/254—Enzymes, proenzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/404—Biocides, antimicrobial agents, antiseptic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/404—Biocides, antimicrobial agents, antiseptic agents
- A61L2300/406—Antibiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/45—Mixtures of two or more drugs, e.g. synergistic mixtures
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmacology & Pharmacy (AREA)
- Biotechnology (AREA)
- Virology (AREA)
- Environmental Sciences (AREA)
- Wood Science & Technology (AREA)
- Dentistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Plant Pathology (AREA)
- Dermatology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Agronomy & Crop Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Pest Control & Pesticides (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Materials For Medical Uses (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Prostheses (AREA)
Abstract
治疗患者的方法,在这些患者中,受损组织或埋藏的假器官装置或导管中长有细菌生物薄膜,为了至少能部分地破坏该生物薄膜,可以至少施用一种抗细菌的酶,这种酶对形成生物薄膜的细菌是致命的或能损害它,施加的数量足以有效地破坏,至少是部分破坏与之相联系的生物薄膜。本发明也公开了预防治疗患者的方法,以及离体对表面进行消毒或杀菌,从而去掉生物薄膜或抑制生物薄膜生长的方法,此外,本发明还公开了容易生长生物薄膜的可植入性物体,在这些植入性物体上预防性地涂上了抗细菌的酶。
Description
相关申请的相互参照
本申请根据35U.S.C.§119(e)要求美国临时申请No.60/368112的在先权益,该申请是2002年3月26日提交的,它的公开内容在此被引作参考。
发明背景
1.发明领域
本发明涉及抗细菌酶对细菌生物薄膜(biofilm)的破坏。更具体而言,本发明涉及用溶葡球菌酶(lysostaphin)破坏葡萄球菌生物薄膜。
2.技术背景
A.生物薄膜
粘附到植入的医疗器械或受损组织上的细菌用水合的多糖和蛋白基质将自己围住,形成粘液层,也就是已知的生物薄膜。生物薄膜会造成严重的公共卫生问题,因为它能使和生物薄膜相关的器官对抗微生物剂的抗性增加,并且使埋藏有医疗器械或组织受损的患者的器官的感染机会上升。生长在生物薄膜中的细菌对抗生素的抗性导致感染的持续和慢性化,这样的感染如和植入性医疗器械相关的感染。生物薄膜的抗性机制和现在熟知的对单个细菌细胞赋予内在的抗性的质粒、转座子、以及突变体的抗性机制不一样。在生物薄膜中,这种抗性看起来取决于多细胞策略(multicellular strategies)。
生物薄膜是一种复杂的微生物群落,它粘附在表面,或者和界面或受损组织相关。尽管现在微生物学研究的焦点在纯培养的浮游细菌(自由游动)上,但现在广泛意识到,绝大部分在自然界,临床上和工业上发现的细菌以生物薄膜的形式和表面保持联系。此外,微生物群落通常由不同种属的微生物组成,这些微生物之间以及它们与环境之间相互作用。生物薄膜构造的确定,尤其是微菌落(细胞簇)在空间的相对排列对这些复杂群落的功能有深刻的含义。
生物薄膜基质是个动态的环境,在这个环境中,微生物细胞成分达到了动态平衡,组织优化,以利用所有可获得的营养。因此,该基质表示出巨大的微观不均一性,在这种不均一性中,存在不同的微环境。一般认为生物薄膜通过两步形成,首先是细菌细胞粘附到表面,接着细菌生长,进而积累形成多层细胞簇。尽管细胞外聚多糖能提供基质框架,但在生物薄膜中能发现大范围的酶活性,这些酶中的一些能显著的影响结构的统一性和稳定性。
更具体地说,在生物薄膜形成的第一个阶段,假设宿主原生质的纤维蛋白原和纤连蛋白覆盖植入的医疗器械和受损组织的表面,并被组成型表达的微生物表面成份所识别,从而能介导细菌最初粘附到生物材料或受损组织上。在第二步中,细菌细胞中叫胞内粘附(ica)位点的特异基因位点能激活细菌细胞间的相互粘连,形成生物薄膜的次级各层。Ica位点负责荚膜多糖操纵子的表达,通过一种1,6连接的葡糖胺聚糖,聚-N-琥珀酰葡糖胺(PNSG)激活细胞间脂多糖粘附素(PIA)。由于这层多糖,使得在电子显微镜下观察时,生物薄膜外表呈粘液状。
金黄色葡萄球菌是一种高致命的人类病原菌。金黄色葡萄球菌和凝固酶阴性葡萄球菌都是在植入的医疗器械和受损组织形成生物薄膜的过程中伴随出现的主要院内病原菌。这些生物位于人皮肤和粘膜的正常carriage flora中,使得它成为侵入性外科手术或延长住院时间的并发症。因为健康和患病的人中都携带有细菌,而葡萄球菌能通过开放的伤口和植入的生物材料侵入患者,因此被认为是机会致病菌。
伴随金黄色葡萄球菌出现的生物薄膜感染是致病和死亡的一个重要原因,尤其是在诸如医院,疗养院和养老院等地方。处在危险中的患者包括婴儿,老人,免疫受损的人,免疫抑制的人以及那些患慢性疾病,而必须经常待在医院的人。那些在血管或其他地方有植入性假器官(prosthetic)装置的患者受到葡萄球菌感染的危险甚至更大,因为受损的免疫系统和异物的导入损害了组织,以及/或者成为形成生物薄膜的表面。这种传染,如果不是致命的,就是慢性的。
导管(catheter)相关感染仍然是进行导管插入术患者致病率和死亡率的重要原因。在美国,报告的致病率和死亡率是4%,等于每年200,000人。此外,导管相关感染的致死率是14-24%,而且由于延长住院治疗,医疗费用上升。因此,预防或甚至减少导管相关感染病例会带来显著的保健好处。
导管感染最普通的是由葡萄球菌引起的,不管是凝固酶阴性葡萄球菌(CoNS)或金黄色葡萄球菌。由CoNS引起的感染可能是温和的,有些可以通过去掉导管或适当地用抗生素处理导管进行治疗。金黄色葡萄球菌引发的感染通常更严重,而且除了进行抗生素治疗外,还必须去掉导管或其他假器官装置。
金黄色葡萄球菌是一个巨大的毒素制造者和高毒性的人类病原菌。它是不同人类疾病的起因,从局部的皮肤感染到威胁生命的菌血症和一些至关重要器官的感染。如果不迅速控制,金黄色葡萄球菌引发的感染会从最初的感染位点向其他器官快速扩散。尽管感染的中心并不明显,但对感染特别敏感的器官包括心瓣膜,肾,肺,骨骼,脑膜以及灼伤患者的皮肤。
尽管开发了一些抗微生物剂,这些药剂对抗生素敏感葡萄球菌所引发的感染有效,但为了消除持续和慢性的葡萄球菌感染,仍然需要那些能持续和彻底杀死具抗生素抗性的金黄色葡萄球菌,尤其是那些和生物薄膜相关的葡萄球菌的药剂,其中生物薄膜是在植入的假器官装置和受损组织上。不幸的是,生物薄膜上的金黄色葡萄球菌(甚至那些处于浮游状态,对抗生素敏感的葡萄球菌)对抗生素敏感性低,因此感染更难清除。
生物薄膜对抗生素具抗性的原因包括:一些抗微生物剂不能穿透各层生物薄膜,某些生物薄膜细胞生长速率缓慢,而抗微生物剂对活跃生长的细菌有作用,从而使得它们对这些药剂的敏感性比较低,以及包含在生物薄膜中的细菌细胞基因表达类型与它们浮游状态(自由游泳)时的基因表达方式不一样。生物薄膜相关细菌细胞的这些差异使得能有效杀死浮游细菌的抗微生物剂不能有效地杀死生物薄膜相关细菌。通常治疗伴随有生物薄膜的导管或假器官装置的唯一方法是去掉污染的装置,而这要求额外的手术,这会进一步增加患者的危险。
在导管或假器官装置上涂上抗微生物剂是控制和预防异物相关感染的有前途的方法。目前,临床上已经测试了六种灭菌的导管,分别是涂了头孢唑啉,替考拉宁,万古霉素,银,氯己啶-磺胺嘧啶银和米诺环素-利福平的导管。然而,只有涂了米诺环素-利福平的导管能减少导管相关血液感染(CRBI’s)的发生,但它的长期效力没研究过。很明显有必要寻找一种新的抗微生物剂,它能降低CBI’s,从而提高导管的持久性,而且这种药剂还能适当清除导管,假器官装置和受损组织中生物薄膜相关葡萄球菌感染,而不用进行手术。
B.溶葡球菌酶
最初认为对生物薄膜无效的抗微生物剂是溶葡球菌酶。溶葡球菌酶是模仿葡萄球菌(以前叫Staphylococcus staphylolyticus)中确定的第一个有效的抗细菌酶。溶葡球菌酶是一种细菌甘氨酰丙氨酸内肽酶,能剪切葡萄球菌细胞壁中的特异交联聚甘氨酸键,因此对活跃生长和静息的葡萄球菌都是高致命的。溶葡球菌酶以单一多肽链表达,分子量大约是27kDa。
溶葡球菌酶对裂解金黄色葡萄球菌特别有效,因为金黄色葡萄球菌的细胞壁键中含有高比例的甘氨酸。溶葡球菌酶也表示出裂解表皮葡萄球菌的能力,表皮葡萄球菌是医院中最常见的凝固酶阴性细菌。然而,由于生物薄膜构造以及溶葡球菌酶裂解葡萄球菌机制的复杂性,并不希望溶葡球菌酶能有效地抵抗已经生成的生物薄膜中的葡萄球菌。
Clim等人的美国专利No.6028051公开了一种用溶葡球菌酶治疗由葡萄球菌引起的疾病的方法。在治疗中使用了相对高剂量的溶葡球菌酶,每千克体重至少是50,优选的是100毫克溶葡球菌酶。溶葡球菌酶可以进行单剂量治疗或多剂量治疗,它可以单独使用,也可以和其他抗生素药剂一块使用。’051专利也公开了溶葡球菌酶基因的克隆和测序,从而能分离出和野生型溶葡球菌酶基因性质相似或不同的变异基因。
O’Callagham的美国专利No.6315996公开了一种方法,在这种方法中,溶葡球菌酶作为一种抗生素,能有效地局部治疗由葡萄球菌引起的角膜感染。Blackburn等人的美国专利No.5760026公开了一种方法,这种方法利用溶葡球菌酶消除和治愈由葡萄球菌引起的感染,包括通过乳房内输液治愈乳用牛乳腺炎。
已经公布的,由Goldstein等人提出申请的美国专利No.2002/0006406公开认为低剂量溶葡球菌酶以及诸如变异和相关酶这样的相似物,按0.5-45mg/kg/天这样的顺序,“足以”根除绝大部分由葡萄球菌所引起的感染,包括和导管或假器官装置“相关”的感染。因此,在本或其他出版物中没有公开引导本领域技术人员期望溶葡球菌酶对破坏由葡萄球菌或其他细菌引起的生物薄膜有效,这些细菌生长在植入的假器官装置,导管或受损的组织表面。应该注意到,并不是所有和导管或假器官装置“相关”的细菌都能形成生物薄膜,以及并不是所有生物薄膜都和导管或假器官装置“相关”。
发明概述
现在发现,诸如溶葡球菌酶这样的抗细菌酶出人意料地不仅杀死生物薄膜中的所有细菌,而且完全破坏生物薄膜基质,将其从它形成的表面根除。这使得不通过手术而治疗生物薄膜相关感染,尤其是在受损的组织或植入的假器官装置和导管表面的生物薄膜相关的感染成为可能。
因此,根据本发明的一个方面,对于受损组织或植入的假器官装置或导管中生长有细菌生物薄膜的患者,本发明提供了一种治疗方法,至少能部分破坏所述生物薄膜,该方法包括给所述患者至少施用一定量的一种抗细菌酶,这种酶对形成生物薄膜的细菌是致命的或使其受到损伤,施加的数量能有效地破坏,至少是部分破坏与之相联系的生物薄膜。对于葡萄球菌或其他细菌所引发的生物薄膜,溶葡球菌酶和溶葡球菌酶类似物被证明对预防生物薄膜生长和根除已经生成的生物薄膜特别有效。
本发明也包括抗细菌酶的预防性给药,能预防生物薄膜在组织受损或带有假器官装置或导管的易感患者中生长。因此,根据本发明的另一方面,通过预防性地施用有效量的抗细菌酶,能预防易感患者中生物薄膜的生长,这种酶对形成生物薄膜的细菌是致命或使其受损的。例如,可以预防性地施用溶葡球菌酶和溶葡球菌酶类似物给易感患者,从而预防由葡萄球菌所引起的生物薄膜的生长。
本发明也包括对离体(ex-vivo)表面进行灭菌和消毒,不必和患者接触。换句话说,本发明的方法基本上适合对任何表面进行灭菌和消毒,包括任何植入体内的东西如聚合物和金属如钛,生物薄膜在这些植入的物质上生长,或者在这些物质上可能生长但不是所需的。出入实际的目的,发明的方法将主要用在这样的环境中,在这些环境中,为了去掉或预防生物薄膜而进行严格的灭菌和消毒是不合适的,包括残留痕量的有害烈性化学物质这样的情况。因此,本发明的方法对预防生物薄膜生长或在生物薄膜开始生长之前消除污染是特别有用的,其中生物薄膜在患者植入的医疗装置表面生长。
因此,根据本发明的另一方面,提供了一种对生长了细菌生物薄膜的离体表面进行灭菌和消毒的方法,至少能部分地去掉其上生长的生物薄膜,在这种方法中,该表面和至少一种抗细菌酶接触,一定数量的这种酶对形成生物薄膜的细菌是致命的或使其受损,它能有效地破坏,至少是部分破坏和它接触的生物薄膜。本发明的这方面对预防或去掉生物薄膜生长而对表面进行的灭菌和消毒特别有效。
本发明也包括离体方法,它能预防生物薄膜在易感表面的生长。因此,根据本发明的另一方面,提供了一种通过对离体表面进行灭菌,保护和消毒,从而抑制形成生物薄膜的细菌生长的方法,预防性地在表面包被上有效量的至少一种酶,这种酶对形成生物薄膜的细菌是致命的或使其受损。实际上本发明的这方面对易感受生物薄膜的表面消毒,保护或灭菌是有效的,用于将医疗设备如导管和假器官装置植入患者。
把诸如溶葡球菌酶这样的抗细菌酶原位电离,带上一定程度的电荷,使其具有粘附到表面,尤其是聚合物表面的趋势。因此,这样处理的表面保留了酶的涂层,这样就能在体内保持消毒或灭菌的状态,从而抑制生物薄膜的形成。因此本发明进一步包括假器官装置和导管,它们可植入需要这些装置的患者中,并且具有至少一个容易招致细菌生物薄膜生长的表面,这些假器官装置和导管涂了至少一种抗细菌酶,这种酶对形成生物薄膜的细菌是致命的,酶包被的数量足以有效地抑制生物薄膜的形成。
表面涂层可以通过酶的离子电荷这样的物理手段得以保持。对于聚合物表面,可以利用酶对聚合物表面的共价粘附来保持涂层,或者可以利用使酶出现在聚合物表面但基本上不会从聚合物表面释放下来这样的技术,混合涂层和表面聚合物。因此,本发明进一步包括制备聚合物组合物的方法,这种组合物是将聚合物和至少一种有效量的抗细菌酶混合而成,它对表面上生长的细菌生物薄膜具有抗性,抗细菌酶对形成生物薄膜的细菌是致命的。本发明也包括制作假器官装置或导管的聚合物组合物,在这个组合物中,聚合物和至少一种有效量的抗细菌酶混合,这种酶对生物薄膜形成细菌是致命的,能有效地抑制生物薄膜在表面形成。
假器官装置的实例基本上包括任何用来插入体内的装置,它包括但不限于分流器,支架,组织构造的台架,胃饲管,punctual plugs,人工关节,心跳节律器,人工心瓣等。这个定义的意思基本上包括任何有生长细菌生物薄膜危险的表面。
本发明前述和其他目的,特征和优点从下面详细描述以及附图中表现得更明显。
附图简述
图1是两种放大倍数的SEM照片(左边是放大2000倍,而右边是放大660倍),显示的是金黄色葡萄球菌生物薄膜在未经溶葡球菌酶处理的细胞培养盘内件(inserts)中的生长。
图2显示的是用溶葡球菌酶处理的细胞培养盘内件的SEM照片,左边的放大倍数是6600,而右边的放大倍数是660;所有金黄色葡萄球菌已经被根除了。
图3是16孔细胞培养板的扫描图,在这种平板上,金黄色葡萄球菌菌株MBT5040生物薄膜用(+)或没用(-)50μg/ml溶葡球菌酶处理,每种处理8个孔。
图4是30孔细胞培养板的扫描图,在这种平板上,为了比较,不同金黄色葡萄球菌菌株,包括两个抗溶葡球菌酶的的金黄色葡萄球菌(LysoR)突变株的生物薄膜用(+)或没用(-)50μg/ml溶葡球菌酶处理。
图5A和5B是放大倍数为4000时的SEM照片,描述的是小鼠颈静脉导管在体生长的生物薄膜,这种小鼠在用溶葡球菌酶处理之前感染了金黄色葡萄球菌。
图6A和6B是放大倍数为4000时的SEM照片,描述的是从溶葡球菌酶处理的小鼠颈静脉导管中清除生物薄膜,该小鼠在用溶葡球菌酶处理之后感染了金黄色葡萄球菌。
图7是个图表,它显示的是随着时间的变化,溶葡球菌酶(6.25cg/ml)能引起金黄色葡萄球菌生物薄膜吸光度立即和持续的下降,而万古霉素(800cg/ml)和苯唑西林(400cg/ml)对生物薄膜没有作用。
图8A和B是扫描图,显示的是苯唑西林(1.6-400cg/ml)或万古霉素(3.2-800cg/ml)在PBS(A)或细菌培养基(B)培养24小时后,对金黄色葡萄球菌生物薄膜没有作用,而当PBS和TSB+0.25%葡萄糖溶液中的溶葡球菌酶是0.8cg/ml(A)和12.5cg/ml(B)是能清除生物薄膜。
图9是扫描图,它显示的是溶葡球菌酶能破坏表皮葡萄球菌生物薄膜,金黄色葡萄球菌做对照(A),表皮葡萄球菌菌株Hay(B),表皮葡萄球菌ATCC35984(C)或表皮葡萄球菌SE1175(D)。两个放大的部分反映的是表皮葡萄球菌菌株ATCC35984(上图)的多层生物薄膜,以及同一个菌株用溶葡球菌酶处理后残余的糖萼,该菌株已没有完整的葡萄球菌(下图)。
图10显示的是作为溶葡球菌酶包被用时函数的导管抗微生物效力。
图11显示的是溶葡球菌酶包被的导管对金黄色葡萄球菌的长期抗微生物效果,以及
图12显示的是在血清蛋白存在的情况下包被溶葡球菌酶的导管抗微生物的效力。
发明详述
本发明能用抗细菌的酶治疗和预防细菌生物薄膜感染。就本发明的目的而言,术语“生物薄膜感染”定义是指在受损的组织和植入的导管或假器官装置表面形成生物薄膜。这个定义与持续和慢性感染不同,并且排除了这层意思,这种慢性感染是患者形成生物薄膜的二次感染。这些二次感染会暂时性地对常规治疗以及本发明的抗细菌酶的剂量做出反应,这些酶不可能有效地完全清除生物薄膜。
“抗细菌酶”是根据本领域普通技术人员给出的意思定义的,指的是任何蛋白水解的,形成孔的,有降解活性的或抑制活性的酶,它能杀死或损害细菌或特定的菌株。这种结果可以通过损坏细菌细胞壁,破坏和细胞壁相联系或位于细胞内的细胞膜,抑制细菌蛋白合成,破坏糖骨架来达到,也可以通过任何本领域普通技术人员想到的,能有助于肽或蛋白成为抗细菌酶的机制来达到。这种酶可以是天然的酶,野生型的酶,用常规技术修饰的酶,和其他分子交联的酶,重组表达的酶,或合成构建的酶。
这是有限的一类材料。通过本说明书,申请者发现了抗细菌酶既能杀死细菌,也能破坏由细菌形成的生物薄膜的能力,本领域普通的技术人员能轻易地确定合适用于本发明的酶,而不用做过多的实验。抗细菌酶的一个例子是溶葡球菌酶。溶葡球菌酶很重要,因为它能有效地治疗由葡萄球菌引起的疾病和由葡萄球菌形成的生物薄膜。
“溶葡球菌酶”和“溶葡球菌酶类似物”的定义包括溶葡球菌酶(野生型),任何突变或变异以及重组的溶葡球菌酶,或与溶葡球菌酶相关的酶(类似物),或任何合成的溶葡球菌酶或其片段(不管是合成的还是其他方式获得的),这些酶在体外和体内都能保持蛋白水解能力,剪切葡萄球菌细胞壁肽聚糖的多聚甘氨酸键。这些酶可以通过蛋白翻译后加工(可以利用产蛋白菌株中的酶或利用在加工的任何阶段导入的酶或药剂)或通过对结构基因进行突变而获得。突变包括位点缺失,插入,结构域删除和置换突变。
本发明的溶葡球菌酶可以是合成构建的,在哺乳动物细胞,昆虫,细菌,酵母,爬行动物或真菌中表达,从细胞培养物或诸如小鼠或其他更高的物种中表达。这个酶包括保持活性的合成构建的蛋白和嵌合的蛋白,合成的蛋白包括合成的肽和多肽,或负责溶葡球菌酶抗葡萄球菌活性部分的重组表达,这部分作为更大蛋白或肽的一部分,而嵌合蛋白含有一或多个其他抗细菌酶的活性位点,这些抗细菌酶对葡萄球菌有效,也对其他形成生物薄膜的细菌有效。
异源溶葡球菌酶的重组表达,以及从表达蛋白中制备的,含有同质的,活性完全的含溶葡球菌酶的组合物在美国专利申请中公开了,该专利申请题为“葡萄球菌水解活性增强的溶葡球菌酶分子”,由Jeffery Richard Stinson,Lioubov Grinberg,Jon Kokai-Kun,Andrew Lees和James Jacob Mond在2002年12月21日提出申请,它的公开内容完整地被引作本申请的参考。本申请要求2001年12月21日提出申请的美国临时申请No.60/341804的在先权益。
为了用适合肠胃外递送活性药剂的液体进行重构(reconstitution),有药效的抗微生物酶的剂型包括含水溶液或干制剂(例如冻干的晶体或非晶体形式,含或不含其他用于渗透平衡的溶质)。剂型可以是,或重构成小体积的液体形式,这样适合大丸剂静脉注射,肌内注射或外周注射,或者添加到大体积的静脉滴注液中,剂型还可以是,或重构成更大体积,这样可以通过缓慢的静脉滴注给药。
递送优选的是通过静脉(iv),肌内,皮下或腹膜内途径,或鞘内注射或利用吸入剂,或者直接滴到感染位点(如果是为了预防,也可以是受损组织或植入的导管或假器官装置中容易形成生物薄膜的位点),从而使得血和组织水平超过活性药剂要达到的最小抑制浓度(MIC)或最小细菌浓度(MBC),因此能使细菌滴价(titers)减少,破坏形成的生物薄膜,或抑制潜在的生物薄膜形成。
当本发明的抗微生物酶对细菌的物种(species)有特异性时,或在一些情况下,对这种微生物的一或多个菌株特异时,药用制剂可以含有许多酶,从而产生抗生物薄膜感染的广谱活性。然而,本发明的抗微生物的酶可以单独给药,从而治疗生物薄膜感染,这些酶的效力已在这种情况下得到证明。
合适的抗微生物酶的剂量和方法根据患者的物种,生物薄膜感染的严重程度,感染生物的敏感性而变化,而组合治疗取决于组合使用的特定抗细菌剂。候选的患者并不限于人,基本上包括所有冷血或温血的脊椎动物,这些生物容易遭受或有感染生物薄膜的危险,这些生物将会从抗微生物酶的治疗中获得好处。假设剂量是单独或分开的,剂量范围则大约是0.1-100mg/kg/天,典型的是大约5-50mg/kg/天。剂药可以通过许多方式给药,包括通过连续的输注,或每天分成许多剂量。为了预防生物薄膜形成,低剂量可能是有效的。
此外,抗微生物酶可以和其他抗微生物剂共同给药,同时或轮流给药,这样能更有效地破坏生物薄膜,并抑制它的再生。例如,溶葡球菌酶和它的类似物能和干扰或抑制细胞壁合成的抗生素共同给药,其中抗生素如青霉素,萘夫西林,苯唑西林以及其他β内酰胺抗生素,诸如头孢噻吩这样的头孢菌素类,诸如万古霉素这样的糖肽以及其他多肽。或者,溶葡球菌酶和它的类似物也可以和能抑制蛋白合成的抗生素共同给药,这类抗生素包括氨基糖苷类抗生素,如链霉素,四环素和链阳菌素。溶葡球菌酶和它的类似物也可以和单克隆抗体一起给药,或者和其他抗细菌的酶,如溶菌酶,变溶菌素,以及cellozyl胞壁质酶;诸如防卫素这样的肽,以及诸如乳链菌肽这样的羊毛硫抗生素,或任何和枯草菌素一样含lanthione的分子一起给药。与溶葡球菌酶及其类似物一起给药的抗葡萄球菌剂可以与之配制成合剂,或者可以随意采用能获得的和有实际意义的任何剂型,并且可以采用任何已知能在感染部位提供足够水平的给药途径。
抗细菌的酶也可以涂在植入的金属或塑料导管或假器官装置上,这些植入装置至少具有一个容易形成生物薄膜的表面,因此,将这些导管或装置浸入酶溶液中,浸泡时间足以在易感表面形成一层抑制生物薄膜形成的酶涂层。即便是最少浓度的酶也能提供一定的保护。使用的浓度典型的是大约10μg/ml-100mg/ml。将酶和装置表面共价结合也能形成酶涂层。对于聚合物装置,可以通过技术将酶和表面聚合物混合,该技术能导致酶在表面螯合或定位在表面上,而基本上不会从上面释放下来。溶葡球菌酶和其他抑制因子也可以通过导管和植入装置直接导入,无论是在植入前还是在植入后,导入的速率有助于溶葡球菌酶和其他抑制因子包被在装置或导管的表面,从而防止生物薄膜的形成。导入的速率包括:用溶葡球菌酶和其他抑制因子填充导管,并密封导管,容许溶葡球菌酶和其他抑制因子有时间去包被导管表面;或者通过导管用泵抽吸溶葡球菌酶和其他抑制因子,既可以是密封的环,也可以是植入的导管,速率足以使溶葡球菌酶和其他抑制因子涂在导管表面。这些技术对植入装置制作领域普通技术人员都是众所周知的,没必要进一步介绍。
本发明通过下列实施例进一步说明,这些实施例能告诉本领域普通技术人员怎样去实践本发明。下列实施例仅仅是例证本发明,并公开本发明某些实施方案的有利的性质。下列实施例不构成对本发明的限制。
实施例
实施例1.用100μg/ml溶葡球菌酶体外破坏金黄色葡萄球菌生物薄膜
葡萄球菌菌株保存在胰酶大豆肉汤培养基(TSB,Difco Bacto)中,分装成~0.5ml保存在-70℃。在每次实验前,从冰柜中取出一份,铺在绵羊血液琼脂平板上(Remel),并在37℃过夜培养。
表1:使用的细菌菌株
| 菌种 | 名称 | 信息 |
| 金黄色葡萄球菌 | ATCC49521(SA5) | 5型荚膜 |
| 金黄色葡萄球菌 | Col | MRSA |
| 金黄色葡萄球菌 | Col-lysoR | 上述的抗溶葡球菌酶的突变株 |
| 金黄色葡萄球菌 | MBT 5040 | MRSA |
| 金黄色葡萄球菌 | MBT 5040 lysoR | 上述的抗溶葡球菌酶的突变株 |
| 金黄色葡萄球菌 | ATCC35556 | 野生型,如下 |
| 金黄色葡萄球菌 | dltA阴性 | 不能产生生物薄膜 |
| 表皮葡萄球菌 | SE380 | 临床分离株 |
| 表皮葡萄球菌 | HAY | 临床分离株 |
| 表皮葡萄球菌 | SE1175 | 临床分离株 |
| 表皮葡萄球菌 | ATCC35984 | 高产量粘液产生菌 |
生物薄膜实验
用5个分离的葡萄球菌克隆接种5ml的TSB,TSB中补充有0.25%的葡萄糖(Sigma-Aldrich)。培养物在37℃过夜震荡培养。
用Spectronic20D+将~3ml PBS(Bio Whittaker)过夜培养物调整到Abs578等于0.1。24个灭菌的0.02mm的Anopore Membrane聚苯乙烯培养板内件(Nalge Nunc International),每一个含有1mlTSB+0.25%葡萄糖,并且被安装在24孔的组织培养板上(Nalge NuncInternational),这些内件或含有200μl TSB+0.25%葡萄糖的96孔培养板用调节好的过夜培养物接种,过夜培养物按1∶200稀释。培养板在37℃过夜培养,形成生物薄膜。
处理
生长大约24个小时后,在半数的孔或内件注入100μg/ml的溶葡球菌酶(AMBI,now Nutrition21,或Biosynexus Incorprated)。培养板然后在37℃培养过夜。
生物薄膜检测
培养48小时后,孔或内件用PBS轻轻地冲洗两遍。冲洗过的96孔培养板或24内件在室温下完全风干。96孔培养板用番红(Remel)染色,检测生物薄膜,而内件用3×戊二醛缓冲液(0.7M NaCl,0.014MKCl,0.007M KH2PO4,0.039M Na2HPO4,1M OHC(CH2)3CHO)固定,制备用于扫描电子显微镜(SEM)的样品。
图1是两种放大倍数下(2000×和660×)的SEM照片,描绘的是在没有用溶葡球菌酶处理的内件中生长的生物薄膜。
图2是在放大倍数为6600×和660×下的SEM照片,描绘的是用溶葡球菌酶处理的内件。溶葡球菌酶破坏生长了24小时的生物薄膜的能力立即就明显了。
实施例2:用50μg/ml溶葡球菌酶体外破坏金黄色葡萄球菌生物薄膜
如实施例1那样,抗对甲氧苯青霉素金黄葡萄球菌菌株MBT5040在加有葡萄糖的TSB上过夜生长。24小时后,含有200μl加有葡萄糖的TSB的96孔组织培养板用过夜培养物接种,过夜培养物按1∶200稀释,也和实施例1介绍的一样。96孔培养板在37℃过夜震荡培养,然后转移到静止的37℃培养箱中再培养24小时。第二次培养后,用PBS冲洗两遍孔,去掉浮游的细胞,并用不含溶葡球菌酶的PBS(-)或含50μg/ml溶葡球菌酶的PBS(+)在室温下培养3个小时。再培养3小时后,用PBS冲洗两遍孔,然后在布安氏固定液(Sigma-Aldrich)中固定5分钟。孔用番红染色1分钟,然后用PBS再冲洗一遍。结果如图3所示,它表明生物薄膜破坏是由于溶葡球菌酶的处理。没有处理的孔中含有生物薄膜,而处理的孔中生物薄膜则完全被破坏。
实施例3:包被有溶葡球菌酶,抗生物薄膜形成的导管的制备
300μl用PBS稀释的10mg/ml,1mg/ml或100μg/ml溶葡球菌酶溶液在6个孔中培养。所有的样品重复两遍。培养板在4℃过夜培养。第二天早上,用1ml PBS冲洗孔10遍,利用真空吸入将孔清扫干净。金黄色葡萄球菌菌株SA5用PBS稀释到透光百分数为40。将这种溶液做成1∶10000稀释度,在每个孔中加入300μl。将培养板放入震荡培养箱,在37℃以75rpm震荡培养2小时。2个小时后,从每个孔中取出40μl,并涂在血液琼脂平板,然后在培养箱中37℃过夜培养。第二天早上对平板上的克隆进行计数。
两个静脉留置针(Angiocath)导管(Becton Dickinson)和200μl的100μl/mL溶葡球菌酶溶液共培养,而另外两个导管在PBS中培养。导管在4℃过夜培养。第二天早上,通过泵,以1.5ml/分钟的流速用50ml PBS冲洗导管。冲洗完导管后,用PBS将金黄色葡萄球菌稀释到透光百分数为40。将这种溶液做成1∶10000稀释度,在每个导管中加入100μl。导管在37℃培养2小时。培养后,将导管流出物涂在血液琼脂平板,然后在培养箱中37℃过夜培养。第二天早上对平板上的克隆进行计数。
表2
| 表面 | 样品 | 涂层 | CFU |
| 聚苯乙烯 | 1 | 没有 | 625 |
| 2 | 没有 | 594 | |
| 1 | 10mg/ml溶葡球菌酶 | 2 | |
| 2 | 10mg/ml溶葡球菌酶 | 0 | |
| 1 | 1mg/ml溶葡球菌酶 | 1 | |
| 2 | 1mg/ml溶葡球菌酶 | 0 | |
| 1 | 100μg/ml溶葡球菌酶 | 4 |
| 2 | 100μg/ml溶葡球菌酶 | 1 | |
| 静脉留置针 | 1 | 没有 | 288 |
| 2 | 没有 | 475 | |
| 1 | 100μg/ml溶葡球菌酶 | 0 | |
| 2 | 100μg/ml溶葡球菌酶 | 0 |
结果
溶葡球菌酶在两种不同的表面能有效地杀死细菌(金黄色葡萄球菌SA5)。聚苯乙烯表面和三种不同浓度的溶葡球菌酶共培养,浓度分别是10mg/ml,lmg/ml和100μg/ml。在这三种浓度的溶葡球菌酶溶液中,聚合物表面都联结有足够的酶,从而在37℃,2小时内杀死更多的金黄色葡萄球菌,而没包被酶的对照孔计数的细菌显著高。
静脉留置针导管的内部和100μg/ml的溶葡球菌酶溶液共培养。包被有溶葡球菌酶的导管能在37℃,2小时内杀死金黄色葡萄球菌,而没有包被酶的对照导管不能完全有效地杀死导管中的细菌。
比较实施例
金黄色葡萄球菌在加有葡萄糖的胰蛋白酶大豆培养基(TSB)过夜生长。24小时后,含有200μl加有葡萄糖的TSB的96孔组织培养板用过夜培养物接种,过夜培养物按1∶200稀释。96孔培养板在37℃过夜震荡培养,然后转移到静止的37℃培养箱中再培养24小时。第二次培养后,用PBS冲洗两遍孔,去掉浮游的细胞,并用不含溶葡球菌酶的PBS(-)或含50μg/ml溶葡球菌酶的PBS(+)在室温下培养3个小时。再培养3小时后,用PBS冲洗两遍孔,然后在布安氏固定液(Sigma-Aldrich)中固定5分钟。孔用番红染色1分钟,然后用PBS再冲洗一遍。溶葡球菌酶不能破坏金黄色葡萄球菌抗溶葡球菌酶菌株,结果如图4所示,从而证明溶葡球菌酶对对其敏感的细菌是特异的。这种发现也表明溶葡球菌酶作用在生物薄膜中现存的细菌细胞中,而破坏这些和生物薄膜相关的细胞能有效地完全地破坏生物薄膜。
实施例4:溶葡球菌酶能立即破坏金黄色葡萄球菌,并且比其他抗生素更有效。
苯唑西林和万古霉素通常用于金黄色葡萄球菌生物薄膜的抗生素敏感性研究中。把这些抗生素和溶葡球菌酶比较,从而确定溶葡球菌酶在破坏金黄色葡萄球菌菌株ATCC35556生物薄膜中是否比其他常规抗生素更有效。在96孔的聚苯乙烯组织培养板上生长了24小时的生物薄膜用连续稀释的溶葡球菌酶,苯唑西林和万古霉素处理(图7)。
为了检查溶葡球菌酶,苯唑西林和万古霉素在生物薄膜上的动力学效果,检测一段时间内(0-3小时和24小时)96孔组织培养板上已经生长的生物薄膜的吸光率。含有金黄色葡萄球菌SA113的组织培养孔和连续稀释的溶葡球菌酶(0.8g/ml-200g/ml),苯唑西林(1.6g/ml-400g/ml)和万古霉素(3.2g/ml-800g/ml)溶液培养24小时,然后在第一个3小时内,每隔20分钟监测一次650nM的吸光率,然后在24小时时又监测一次。当用含有1剂6.25μg/ml溶葡球菌酶的PBS处理时,溶葡球菌酶处理的生物薄膜的吸光率从0小时的大约0.35下降到处理3小时后的0.125,而到24小时时下降到底线(0.04)附近(图7)。尽管生物薄膜用了含多达400μg/ml苯唑西林或800μg/ml万古霉素的PBS处理,但是用苯唑西林和万古霉素处理24小时的生物薄膜的吸光率变化较少,保持在0.325左右(图7)。因为诸如苯唑西林和万古霉素这样的抗菌素抵抗代谢活跃的细菌有效,因此,作了一个相似的试验,生物薄膜和三种抗生素在细菌培养基(TSB)中共培养。当实验在TSB,而不是PBS中进行时,也发现了非常相似的结果。通过24小时处理,溶葡球菌酶能将生物薄膜的吸光率降低到底线附近,而苯唑西林和万古霉素即便在24小时后,效果很低或没效果(数据没有表示)。
三种药剂在聚苯乙烯孔中破坏金黄色葡萄球菌生物薄膜的能力可以通过比较处理孔和对照孔(缓冲液处理的)的染色密度来显示。上述动力学实验中的生物薄膜处理24小时,能将孔的底部染黑,而清除了生物薄膜的孔用番红染不上色(图8)。含溶葡球菌酶低达0.8μg/ml的PBS(图8A)以及含溶葡球菌酶低达12.5g/ml的TSB+0.25%葡萄糖(图8B)能清除跨膜中的生物薄膜,而含多达400μg/ml苯唑西林或800μg/ml万古霉素的PBS或TSB即便是在处理24小时后,对已经生成的生物薄膜也没有明显的效果(图8A和B)。
实施例5:溶葡球菌酶破坏表皮葡萄球菌生物薄膜
尽管溶葡球菌酶表示出抗金黄色葡萄球菌生物薄膜的活性,而已知表皮葡萄球菌生物薄膜对溶葡球菌酶敏感性较低,因此探究表皮葡萄球菌生物薄膜是否也对溶葡球菌酶破坏生物薄膜的作用敏感是有意思的。检查了三种不同的糖萼(粘液)产生能力相异的表皮葡萄球菌菌株,它们包括:表皮葡萄球菌Hay(低产量粘液产生菌),表皮葡萄球菌菌株SE1175(适中的粘液产生菌),以及表皮葡萄球菌ATCC35984(高产量粘液产生菌)。这三种表皮葡萄球菌都能在载玻培养皿上产生生物薄膜,而ATCC35984产生的生物薄膜如预料的那样是最厚,染色是最黑的。200g/ml溶葡球菌酶和这些表皮葡萄球菌生物薄膜共培养三小时能破坏所有这三种表皮葡萄球菌的生物薄膜(图9)。这个实验把金黄色葡萄球菌菌株SA113作为对照。显微镜检查破坏的生物薄膜发现没有剩下和人造表面相联接的完整细菌(数据没有表示)。在溶葡球菌酶处理的孔中,可以看见的染色的物质是胞外的糖萼,它被番红染成粉红色,并且不含有完整的革兰氏阳性表皮葡萄球菌细胞,只剩下细胞碎片。
实施例6:对已经感染的小鼠的处理
使用了颈静脉插有导管的小鼠(Charles River Labs)。用金黄色葡萄球菌通过尾静脉攻击小鼠(103-104CFU,比感染没插导管的小鼠所必需的典型剂量5×106CFU或更多要少得多)。攻击后4天开始处理,这时已经感染。通过植入的导管将含有溶葡球菌酶的200μl PBS施用给小鼠(对于抗甲氧西林金黄葡萄球菌,在处理中加入了萘夫西林)。在最后处理的那天后,含有溶葡球菌酶(使用时还有萘夫西林)的50μl栓液(50%灭菌的葡萄糖溶液)被放入导管,添加的浓度和处理使用的浓度一样。对照小鼠接受了同样的PBS以及单独的栓液处理。
在最后一次处理后的一天,收获肝,心和心脏中的一部分导管。导管部分用超声波破碎释放细菌。细菌(金黄色葡萄球菌)回收的数量(CFU’s)如表3-11所示。
表3MASS 20mg/kg t.i.d 4天
| 实验组 | 小鼠 | 肝 | 导管 |
| 对照 | 1 | 239 | TNTC |
| 对照 | 2 | TNTC | TNTC |
| 对照 | 3 | 1494 | TNTC |
| 对照 | 4 | TNTC | TNTC |
| 溶葡球菌酶 | 1 | 0 | 0 |
| 溶葡球菌酶 | 2 | 27 | 1 |
| 溶葡球菌酶 | 3 | 43 | 0 |
| 溶葡球菌酶 | 4 | 148 | 387* |
| 溶葡球菌酶 | 5 | 8 | 1339* |
*溶葡球菌酶抗性的
MSSA=对二甲氧基苯青霉素敏感的金黄色葡萄球菌
TNTC=数量太多,没法计数
表4MASS 10mg/kg b.i.d 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | >1600 | TNTC | TNTC |
| 对照 | 2 | 209 | >1500 | >1600 |
| 对照 | 3 | 0 | 0 | 4 |
| 溶葡球菌酶 | 1 | 0 | 0 | 0 |
| 溶葡球菌酶 | 2 | TNTC* | TNTC* | >1700* |
| 溶葡球菌酶 | 3 | 0 | 0 | 0 |
| 溶葡球菌酶 | 4 | 0 | 1 | 5 |
| 萘夫西林(50) | 1 | 0 | 0 | 0 |
| 萘夫西林 | 2 | 5 | 0 | 303 |
| 萘夫西林 | 3 | 0 | 0 | 0 |
| 萘夫西林 | 4 | 0 | 0 | 3 |
*溶葡球菌酶抗性的
表5MRSA 10mg/kg+/ Naf b.i.d 3天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 1004 | 961 | TNTC |
| 对照 | 2 | 17 | TNTC | TNTC |
| 对照 | 3 | 13 | 435 | TNTC |
| 对照 | 4 | TNTC | TNTC | TNTC |
| 溶葡球菌酶 | 1 | 32 | 3 | 981 |
| 溶葡球菌酶 | 2 | 23 | 19 | 310 |
| 溶葡球菌酶 | 3 | 87 | 74 | 593 |
| 溶葡球菌酶 | 4 | 115 | 112 | 83 |
| +萘夫西林(50) | 1 | 7 | 3 | 1125 |
| +萘夫西林 | 2 | 15 | 1 | 1 |
| +萘夫西林 | 3 | 5 | 39 | 1086 |
MRSA=抗二甲氧基苯青霉素的金黄色葡萄球菌
表6MRSA 10mg/kg+/ Naf b.i.d 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 583 | 81 | TNTC |
| 对照 | 2 | 0 | 0 | 334 |
| 对照 | 3 | 67 | TNTC | TNTC |
| 对照 | 4 | 0 | 0 | 693 |
| 溶葡球菌酶 | 1 | 0 | 0 | 0 |
| 溶葡球菌酶 | 2 | 263 | 10 | 932 |
| 溶葡球菌酶 | 3 | 28 | 0 | 523 |
| 溶葡球菌酶 | 4 | 0 | 0 | 0 |
| +萘夫西林(50) | 1 | 18 | 1 | 15 |
| +萘夫西林 | 2 | 0 | 9 | 675 |
| +萘夫西林 | 3 | 0 | 0 | 0 |
| +萘夫西林 | 4 | 0 | 0 | 0 |
表7MRSA 溶葡球菌酶 t.i.d 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 0 | 0 | TNTC |
| 对照 | 2 | 337 | TNTC | TNTC |
| 对照 | 3 | 0 | 0 | TNTC |
| 10mg/ml | 4 | 0 | 0 | 0 |
| 10mg/ml | 1 | 0 | 0 | 115 |
| 10mg/ml | 2 | 395 | 3 | 558 |
| 20mg/ml | 3 | 0 | 0 | 0 |
| 20mg/ml | 4 | 0 | 0 | 0 |
| 20mg/ml | 1 | 0 | 0 | 13 |
| 40mg/ml | 2 | 0 | 0 | 0 |
| 40mg/ml | 3 | 0 | 0 | 0 |
| 40mg/ml | 4 | 1 | 0 | 1 |
表8MRSA 15mg/kg+/ Naf t.i.d 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 0 | 0 | 0 |
| 对照 | 2 | 105 | 11 | TNTC |
| 对照 | 3 | 1740 | 80 | TNTC |
| 对照 | 4 | 0 | 0 | 49 |
| 溶葡球菌酶 | 1 | 183 | 2 | 1298 |
| 溶葡球菌酶 | 2 | 147 | 0 | 64 |
| 溶葡球菌酶 | 3 | 0 | 0 | 0 |
| 溶葡球菌酶 | 4 | 245 | 6 | 26 |
| +萘夫西林(50) | 1 | 0 | 0 | 0 |
| +萘夫西林 | 2 | 1 | 0 | 0 |
| +萘夫西林 | 3 | 0 | 0 | 0 |
| +萘夫西林 | 4 | 2 | 0 | 0 |
表9MRSA 15mg/kg+/ Naf t.i.d 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 279 | 149 | TNTC |
| 对照 | 2 | 1286 | TNTC | TNTC |
| 对照 | 3 | 1218 | 62 | TNTC |
| 对照 | 4 | 1718 | 104 | TNTC |
| 溶葡球菌酶 | 1 | 250 | 8 | 35 |
| 溶葡球菌酶 | 2 | 10 | 0 | 0 |
| 溶葡球菌酶 | 3 | 120 | 0 | 58 |
| 溶葡球菌酶 | 4 | 215 | 4 | >1200 |
| +萘夫西林(50) | 1 | 2 | 0 | 0 |
| +萘夫西林 | 2 | 0 | 0 | 0 |
| +萘夫西林 | 3 | 1 | 0 | 0 |
| +萘夫西林 | 4 | 0 | 0 | 0 |
表10MRSA 溶葡球菌酶 Naf 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 0 | 5 | 4 |
| 对照 | 2 | 0 | 0 | 1040 |
| 对照 | 3 | 802 | 490 | TNTC |
| 对照 | 4 | 152 | 114 | TNTC |
| 15mg/kg b.i.d. | 1 | 0 | 9 | 9 |
| 15mg/kg b.i.d. | 2 | 7 | 0 | 53 |
| 15mg/kg b.i.d. | 3 | 18 | 2 | 2 |
| 15mg/kg b.i.d. | 4 | 16 | 6 | 10 |
| 10mg/kg b.i.d. | 1 | 1144 | 58 | 175 |
| 10mg/kg b.i.d. | 2 | 0 | 0 | 2 |
| 10mg/kg b.i.d. | 3 | 73 | 9 | 15 |
| 10mg/kg b.i.d. | 4 | 0 | 0 | 0 |
表11MRSA Lyso+ Naf t.i.d 4天
| 实验组 | 小鼠 | 肝 | 心脏 | 导管 |
| 对照 | 1 | 103 | 92 | TNTC |
| 对照 | 2 | 306 | 394 | TNTC |
| 对照 | 3 | 0 | 2 | 66 |
| 对照 | 4 | 187 | 272 | TNTC |
| 40(1×)-5mg/kg | 1 | 20 | 10 | 114 |
| 40(1×)-5mg/kg | 2 | 0 | 0 | 0 |
| 40(1×)-5mg/kg | 3 | 0 | 0 | 0 |
| 40(1×)-5mg/kg | 4 | 16 | 9 | 807 |
| 15(3×)-5mg/kg | 1 | 0 | 0 | 0 |
| 15(3×)-5mg/kg | 2 | 0 | 0 | 570 |
| 15(3×)-5mg/kg | 3 | 3 | 0 | 50 |
| 15(3×)-5mg/kg | 4 | 32 | 124 | 237 |
清除小鼠导管中二甲氧基苯青霉素敏感的金黄色葡萄球菌感染需要20mg/kg的溶葡球菌酶,而清除抗二甲氧基苯青霉素的金黄色葡萄球菌感染需要15mg/kg的溶葡球菌酶+50mg/kg的萘夫西林,一日三次,持续4天(注意:已知溶葡球菌酶和萘夫西林对金黄色葡萄球菌有协同的杀死作用)。更低的溶葡球菌酶剂量或不同的剂量方案(如一种剂量先是40mg/kg,然后是5mg/kg,或三种剂量第一天先是15mg/kg,然后是5mg/kg)并不能完全清除金黄色葡萄球菌感染。单独用溶葡球菌酶处理抗二甲氧基苯青霉素的金黄色葡萄球菌两次都出现了溶葡球菌酶抗性,但用溶葡球菌酶和萘夫西林组合处理抗二甲氧基苯青霉素的金黄色葡萄球菌检测不到任何溶葡球菌酶抗性。已知溶葡球菌酶抗性和β内酰胺抗性是相互排斥的。SEM表示金黄色葡萄球菌在植入的导管中生长成生物薄膜(图5),而溶葡球菌酶能清除这些导管中的金黄色葡萄球菌生物薄膜(图6)。
实施例7:用溶葡球菌酶预处理插入导管的小鼠
如实施例4所介绍的那样,在用金黄色葡萄球菌攻击之前,用1或2个剂量的溶葡球菌酶通过导管预处理颈静脉插有导管的小鼠。小鼠在攻击前24小时接受一个剂量的溶葡球菌酶(40mg/kg),或者在攻击前24小时或2小时接受两个剂量的溶葡球菌酶(40mg/kg)。攻击时,导管中留有溶葡球菌酶溶液。对照小鼠接受标准的磷酸缓冲液(PBS)。攻击后4天杀死小鼠。
三只对照小鼠中有两只的导管,肝和心脏受到感染。而所有处理的8只小鼠都没有感染金黄色葡萄球菌。
在上面的实施例中,攻击时,导管中留有溶葡球菌酶溶液,因此这有争论认为是溶葡球菌酶溶液保护导管免受金黄色葡萄球菌感染。为了做一个更严格的试验,用一次200μl剂量的含有40mg/kg溶葡球菌酶的PBS通过导管滴注插有导管的小鼠。一组随后也接受了50μl的栓液,它含有的溶葡球菌酶浓度和滴注前的剂量一样。24小时后,所有这些小鼠的导管用PBS彻底漂洗。漂洗后2小时,用104金黄色葡萄球菌攻击动物。金黄色葡萄球菌攻击后4天,杀死动物,并处理导管和器官中的细菌。如表12所示,在颈静脉导管中仍然保留了足够的溶葡球菌酶,从而能保护导管免受金黄色葡萄球菌的感染,即便过多的溶葡球菌酶被冲洗走。
表12
| 实验组 | 感染的动物 | 导管的CFU | 心脏的CFU | 肝脏的CFU |
| 对照 | 4/4 | >2000 | 880 | 251 |
| 导管滴注溶葡球菌酶,不含栓剂 | 1/4 | 0 | (287)a | (341)a |
| 导管滴注溶葡球菌酶,不含栓剂 | 0/4 | 0 | 0 | 0 |
a来自一种感染动物的结果
上面的在体实施例证明了溶葡球菌酶能清除导管感染小鼠模型中感染的导管中的金黄色葡萄球菌生物薄膜。在这些实施例中,每天给药最少40mg/kg的剂量,一天三次,持续四天,对于清除小鼠导管中的生物薄膜是必需的。上面的实施例还证明了在小鼠导管中预滴注一次40mg/kg的溶葡球菌酶剂量将会保护导管不形成金黄色葡萄球菌生物薄膜,即便过多的溶葡球菌酶被冲洗出导管。这些实施例的意思并不是限制这个专利的权利要求,而是因为清除或保护小鼠免受生物薄膜感染所必需的溶葡球菌酶剂量可能和处理人和其他动物所必需的剂量是不同的。
这些结果和实施例3的结果相关,实施例3介绍了溶葡球菌酶结合在导管上,并能保持它的抗葡萄球菌活性,这两个结果相关表明对导管进行预处理可能比把溶葡球菌酶用作导管感染的治疗手段更有实际意义。
实施例8:包被有溶葡球菌酶的静脉内导管在体外的效力
材料与方法
材料:24孔的聚苯乙烯细胞培养板购自Costar公司(Acton,MA)。静脉留置针导管和胰酶大豆肉汤培养基购自Becton Dickinson公司(Sparks,MD)。磷酸缓冲液,pH7.2,购自Gibco生物技术公司(Rockville,MD)。血液琼脂平板购自Remel公司(Lenexa,KS)。溶葡球菌酶(Ambicin L)购自AMBJ有限公司。细菌菌株金黄色葡萄球菌荚膜型5(SA5)和8(临床分离株);二甲氧基苯青霉素抗性金黄色葡萄球菌菌株MBT5040(WRAMC的临床分离株),表皮葡萄球菌SE380(临床分离株),1175(临床分离株),ATCC35984(购自ATCC公司)用在不同的实验中。
聚苯乙烯孔的包被:分别把300μl 10mg/ml,1mg/ml或0.1mg/ml的溶葡球菌酶稀释在PBS中,然后涂在孔上。平板在4℃过夜培养。用1ml PBS冲洗孔10次,并通过真空吸入去掉冲洗液。在每个孔中加入300μl的5×104CFU/ml的金黄色葡萄球菌溶液。平板在37℃以75rpm震荡培养2个小时。从每个孔中取出40μl,在血液琼脂平板上划线,于37℃过夜培养。
导管的包被:从静脉留置针导管中取走针,并把它处理掉。利用1ml的注射器,将200μl 0.1mg/ml的溶葡球菌酶溶液涂在导管上。导管在室温下培养1小时,除非特别说明。然后利用蠕动泵以1.5ml/分钟的流速冲洗导管,所用的是50ml磷酸缓冲液。然后,导管用300μl~5×104CFU/ml的细菌溶液(稀释在TSB中)接种,并在37℃培养2小时。然后导管流出液在血液琼脂平板上划线,在37℃过夜培养。
溶葡球菌酶的淋洗:为了检测溶葡球菌酶是否缓慢地从导管中释放到内腔溶液中,包被有溶葡球菌酶的导管和100μl PBS在37℃培养2小时。然后将PBS转移到Eppendorf管中,然后在流出物中加入105CFU的SA5,并在37℃培养1小时。从样品中取出40μl,并在血液琼脂平板上划线,在37℃过夜培养。此外,包被有溶葡球菌酶的导管和PBS在37℃培养2小时。第二天早上,冲洗掉PBS,导管用~5×104CFU/ml的SA5在37℃接种2小时。然后导管流出液在血液琼脂平板上划线,在37℃过夜培养。用10,1和0.1mg/ml溶葡球菌酶涂在孔上60分钟,希望淋洗聚苯乙烯表面。然后冲洗孔,往孔中加入300μl PBS2个小时,然后去掉。在PBS冲洗液中加入300μl5×104CFU/ml的SA5溶液,然后在37℃培养1小时。然后取出40μl,并在血液琼脂平板上划线,在37℃过夜培养。
溶葡球菌酶的长期淋洗:10个包被有溶葡球菌酶的导管(包被浓度是10mg/ml)在37℃和PBS共培养2小时。然后冲洗导管,10个包被有溶葡球菌酶的导管中的2个和200μl 5×104CFU/ml的SA5溶液在37℃培养2小时。流出液在血液琼脂平板上划线,在37℃过夜培养。其它导管和新鲜的PBS共培养,并在37℃过夜。第二天,冲洗所有8个导管,其中2个用上述的方法和细菌共培养。剩余的6个导管再次和新鲜的PBS共培养,并在37℃过夜。这个程序每天重复,持续4天。
细菌吸附到导管上。包被有溶葡球菌酶的导管放在2ml 0.1mg/ml的溶葡球菌酶溶液中,然后在37℃震荡培养2小时,从而将导管的外面包被住。然后冲洗导管,并放在5×104CFU/ml的SA5溶液中,在37℃培养3小时。40μl细菌溶液在血液琼脂平板上划线,并在37℃过夜培养。导管在2ml TSB,37℃过夜培养,并检查它的生长。没有处理的导管用50ml PBS冲洗,然后用120μl 5×106CFU/ml的细菌溶液接种,并培养2或24小时。导管流出液在血液琼脂平板上划线,在37℃过夜培养。用50ml PBS冲洗导管,收集最后1ml冲洗液,并用100μl在血液琼脂平板上划线,37℃过夜培养。然后把导管放在1ml TSB中37℃过夜培养,并观察它的生长。
血清蛋白存在时的溶葡球菌酶活性:用0.1mg/ml溶葡球菌酶在室温下包被导管60分钟。然后冲洗导管,并在人血清或TSB中,37℃培养24小时。冲洗导管,然后用5×106CFU/ml的细菌溶液在37℃接种2小时。导管流出液在血液琼脂平板上划线,在37℃过夜培养。
固定的溶葡球菌酶能有效地清除聚苯乙烯和导管表面的细菌。平均而言,从对照孔中能回收610CFU的细菌,而在包被有溶葡球菌酶的孔中只剩下3CFU的细菌,细菌数量减少了99.5%。在这个范围之内的灭活并不是浓度依赖型的,因为所有三种浓度抗细菌的活性都十分大。和对照导管相比,包被有溶葡球菌酶的导管的细菌被完全清除,从对照导管中回收了493CFU的细菌。这些结果表明即便溶葡球菌酶结合在塑料表面,它仍然保持抗金黄色葡萄球菌的活性。
为了确定灭活活性是不是溶葡球菌酶包被时间的函数,用0.1mg/ml溶葡球菌酶包被导管5,10或15分钟,并检测它们灭活金黄色葡萄球菌的能力。如图10所示,即便是刚涂上溶葡球菌酶5分钟,导管就有很高水平的灭活活性,但是,随着包被时间的延长,效力是增长的。包被后5分钟,细菌数减少98.7%,10分钟以后减少99.4%,而包被15分钟后,细菌完全被清除。
从包被表面淋洗溶葡球菌酶:
包被溶葡球菌酶的导管中的PBS冲洗液的细菌数只是微量减少(表14)。和未处理的导管相比,用PBS过夜冲洗包被溶葡球菌酶的导管能完全清除细菌,而从未处理的导管中能回收1500CFU的细菌。这些数据表明如果溶葡球菌酶从导管中淋洗下来,那在数量上发挥作用的溶葡球菌酶就会减少,因此不能有效地抵抗细菌攻击。
溶葡球菌酶从聚苯乙烯表面淋洗下来导致细菌的清除依赖包被浓度。和对照相比,10mg/ml的冲洗液将SA5滴价降低1.4log,而用1mg/ml的冲洗液能将SA5的滴价降低1.3log。然而,因为淋洗导致在0.1mg/ml的包被浓度时,细菌数目只减少0.33log。相反,将细菌滴价直接添加到包被有0.1mg/ml的溶葡球菌酶孔中,能使细菌数目减少到2.4log(表13)。
表13:表面结合的溶葡球菌酶抗金黄色葡萄球菌的效力
表面 涂层浓度 CFU(n=2)
聚苯乙烯 10mg/ml 1
1mg/ml 1
0.1mg/ml 3
0mg/ml 610
静脉留置针 0.1mg/ml 0
0mg/ml 493
表14:结合的溶葡球菌酶的稳定性,以及淋洗对抗微生物效力的作
用
表面 涂层浓度 培养时间 CFU(n=3) 杀死场所
静脉留置针 0.1mg/ml 2小时 219 冲洗液1
0mg/ml 2小时 323 冲洗液
0.1mg/ml 24小时 0 导管2
0mg/ml 24小时 1503 导管
聚苯乙烯 10mg/ml 2小时 26 冲洗液
1mg/ml 2小时 33 冲洗液
0.1mg/ml 2小时 291 冲洗液
0mg/ml 2小时 627 冲洗液
1:加入PBS冲洗液中的细菌
2:加入导管的细菌
连续淋洗溶葡球菌酶对包被导管灭活活性的影响如图11所示。导管在PBS中培养达96小时,PBS每隔24小时更新。然后用细菌攻击导管,以确定导管能否保持对金黄色葡萄球菌的灭活活性。如图11所示,在PBS中培养24小时后,和没有溶葡球菌酶包被的导管相比,从包被有溶葡球菌酶的导管中回收的细菌减少了2.8log。在第24小时,细菌数减少1.8log,48小时后减少1.5log,72小时减少0.7log,而96小时后细菌数减少0.3log。
不同菌株对包被有溶葡球菌酶的导管的易感性:
表15描述的是在体外导管模型中测试的若干金黄色葡萄球菌和表皮葡萄球菌菌株的易感性,包括MRSA菌株和一种产生原始生物薄膜的表皮葡萄球菌菌株。
表15:不同菌株对包被有溶葡球菌酶导管的易感性
涂层浓度 细菌菌株 CFU(n=2)
0.1mg/ml 表皮葡萄球菌380 4
0mg/ml 表皮葡萄球菌380 678
0.1mg/ml 表皮葡萄球菌1175 68
0mg/ml 表皮葡萄球菌1175 824
0.1mg/ml 表皮葡萄球菌35984 16
0mg/ml 表皮葡萄球菌35984 757
0.1mg/ml SA5 1
0mg/ml SA5 785
0.1mg/ml SA8 0
0mg/ml SA8 1593
0.1mg/ml MRSA 1
0mg/ml MRSA 910
以前的研究表明溶葡球菌酶抗表皮葡萄球菌活性比抗金黄色葡萄球菌活性要弱,然而,包被溶葡球菌酶的导管能有效地杀死表皮葡萄球菌的三种菌株,尽管和金黄色葡萄球菌菌株相比效果较弱。表皮葡萄球菌380型是最易感的表皮葡萄球菌,降低了2.2log。产生生物薄膜的表皮葡萄球菌ATCC35984降低了1.8log,而表皮葡萄球菌1175在对照样品中降低了1.1log。包被溶葡球菌酶的导管抵抗金黄色葡萄球菌MBT5040(MRSA)和金黄色葡萄球菌8型荚膜(SA8)非常活跃。和没包被溶葡球菌酶的导管中回收的1250CFU细菌相比,平均而言,从MRSA培养的导管中回收了1CFU细菌,而用SA8培养的导管细菌完全清除。
细菌粘附到导管上。
没包被溶葡球菌酶的导管流出液中的细菌数不胜数,然而,可以收集最后1ml冲洗液,并在血液琼脂平板上划线。冲洗液中的细菌数和培养时间成比例,在24小时内粘附更多的细菌。平均而言,从24小时的冲洗液中回收了1000CFU的细菌,而从2小时的冲洗液中只回收了30CFU的细菌。冲洗液中的细菌数可能是导管中粘附的细菌数的指征。然后培养没包被溶葡球菌酶的导管,检测细菌生长。在培养基中过夜培养显示导管被克隆化,而细菌生长在培养基上。这些数据表明细菌确实粘附到了导管的表面,并且能引起感染。包被有溶葡球菌酶的导管在高接种量的细菌中培养3小时,清除该溶液。过夜培养后,清除培养基,表明包被有溶葡球菌酶的导管在3个小时内能清除细菌溶液,而导管保持无菌。
血清蛋白存在时的溶葡球菌酶活性:如图12所示,包被有0.1mg/ml溶葡球菌酶的导管在人血清蛋白培养,细菌数减少99%,而包被有10和1mg/ml溶葡球菌酶的导管在人血清蛋白培养时,能完全清除细菌。这些结果表明血清蛋白的存在并不能显著地影响溶葡球菌酶对导管的活性。
前面的实施例证明了将溶葡球菌酶包被在人造表面的效力。包被有溶葡球菌酶的表面可以成为预防导管和植入性相关感染的一种新的治疗手段。
容易理解,在不偏离权利要求中所给出的本发明前提下,可以利用上文中提到的特征的变异形式和组合形式。这些变异形式不应被视为偏离本发明的精神和范围,所有这样的修饰都包括在下列权利要求的范围之中。
Claims (92)
1.治疗患者的方法,在所述患者受损组织或植入性假器官装置或导管中,生长有细菌生物薄膜,所述治疗至少部分破坏所述生物薄膜,所述方法包括给所述患者施用至少一种抗细菌的酶,这种酶对形成生物薄膜的细菌是致命的,或者能损害它,施加的数量足以有效地至少部分破坏和它接触的生物薄膜。
2.根据权利要求1所述的方法,其中抗细菌酶的所述数量足以有效地将生物薄膜从它生长的表面完全地清除。
3.根据权利要求1所述的方法,其中抗细菌酶和至少一种其他抗细菌剂共同施用。
4.根据权利要求1所述的方法,其中所述生物薄膜是由葡萄球菌产生的。
5.根据权利要求4所述的方法,其中所述生物薄膜包含金黄色葡萄球菌。
6.根据权利要求4所述的方法,其中所述生物薄膜包含表皮葡萄球菌。
7.根据权利要求4所述的方法,其中所述生物薄膜包含金黄色葡萄球菌和表皮葡萄球菌。
8.根据权利要求4所述的方法,其中所述方法包括施用溶葡球菌酶或溶葡球菌酶类似物。
9.根据权利要求1所述的方法,其中所述方法包括施用溶葡球菌酶或溶葡球菌酶类似物或嵌合分子,该嵌合分子具有和溶葡球菌酶同样的酶学活性。
10.根据权利要求8所述的方法,其中施用重组表达的,具有完全活性的同质的溶葡球菌酶。
11.根据权利要求8所述的方法,其中所述溶葡球菌酶是合成构建的。
12.根据权利要求1所述的方法,其中抗细菌酶是合成构建的。
13.根据权利要求8所述的方法,其中所述溶葡球菌酶是天然来源的。
14.根据权利要求8所述的方法,其中所述溶葡球菌酶和其他能有效地抵抗葡萄球菌的抗生素共同施用。
15.根据权利要求14所述的方法,其中所述其他抗生素能干扰或抑制细胞壁合成。
16.根据权利要求15所述的方法,其中所述抗生素选自β内酰胺,头孢菌素,糖肽,氨基糖苷,sulfonomide,大环内酯抗生素,叶酸,多肽及其组合物。
17.根据权利要求14所述的方法,其中所述其他抗生素干扰蛋白的合成。
18.根据权利要求17所述的方法,其中所述其他抗生素包括糖苷,四环素和链阳菌素。
19.防止生物薄膜在易感患者植入性表面或受损组织上生长的方法,所述方法是通过施用预防有效量的至少一种抗细菌酶而实现的,所述抗细菌酶对形成生物薄膜的细菌是致命的,或能损害它。
20.根据权利要求19所述的方法,其中所述患者植入了表面容易生长生物薄膜的导管或假器官装置。
21.根据权利要求19所述的方法,其中所述生物薄膜是葡萄球菌生物薄膜。
22.根据权利要求21所述的方法,其中所述生物薄膜包含金黄色葡萄球菌。
23.根据权利要求21所述的方法,其中所述生物薄膜包含表皮葡萄球菌。
24.根据权利要求21所述的方法,其中所述生物薄膜包含金黄色葡萄球菌和表皮葡萄球菌。
25.根据权利要求21所述的方法,其中所述施用步骤包括施用至少一种溶葡球菌酶或溶葡球菌酶类似物或嵌合分子,该嵌合分子具有和溶葡球菌酶同样的酶学活性。
26.根据权利要求19所述的方法,其中所述施用步骤包括施用至少一种溶葡球菌酶或溶葡球菌酶类似物或嵌合分子,该嵌合分子具有和溶葡球菌酶同样的酶学活性。
27.根据权利要求25所述的方法,其中施用重组表达的,具有完全活性的同质的溶葡球菌酶。
28.根据权利要求25所述的方法,其中所述溶葡球菌酶是合成构建的。
29.根据权利要求19所述的方法,其中抗细菌酶是合成构建的。
30.根据权利要求25所述的方法,其中所述溶葡球菌酶是天然来源的。
31.根据权利要求19所述的方法,其中所述溶葡球菌酶和其他能有效地抵抗葡萄球菌的抗生素共同施用。
32.根据权利要求19所述的方法,其中所述其他抗生素能干扰或抑制细胞壁合成。
33.根据权利要求19所述的方法,其中所述抗生素选自β内酰胺,头孢菌素,氨基糖苷,sulfonomide,大环内酯,叶酸,糖肽,多肽及其组合物。
34.根据权利要求19所述的方法,其中所述其他抗生素干扰蛋白的合成。
35.根据权利要求19所述的方法,其中所述其他抗生素包括糖苷,四环素和链阳菌素。
36.根据权利要求20所述的方法,其中所述的溶葡球菌酶在导管或假器官装置植入之前导入。
37.根据权利要求36所述的方法,其中所述溶葡球菌酶通过泵入溶液导入导管。
38.根据权利要求20所述的方法,其中所述溶葡球菌酶在导管被插入后导入所述导管。
39.根据权利要求38所述的方法,其中所述溶葡球菌酶通过药团注射导入导管。
40.根据权利要求38所述的方法,其中所述溶葡球菌酶通过慢速输注导入导管。
41.灭菌或消毒离体表面,从而防止形成生物薄膜的细菌在表面上生长的方法,该方法包括将预防有效量的至少一种抗细菌酶和所述表面接触,所述抗细菌酶对所述形成生物薄膜的细菌是致命的,或能损害它。
42.根据权利要求41所述的方法,其中所述形成生物薄膜的细菌包括葡萄球菌。
43.根据权利要求42所述的方法,其中所述形成生物薄膜的细菌包括金黄色葡萄球菌。
44.根据权利要求42所述的方法,其中所述形成生物薄膜的细菌包括表皮葡萄球菌。
45.根据权利要求42所述的方法,其中所述形成生物薄膜的细菌包括金黄色葡萄球菌和表皮葡萄球菌。
46.根据权利要求42所述的方法,其中所述接触步骤包括将至少一种溶葡球菌酶或溶葡球菌酶类似物或嵌合分子和所述表面接触,所述嵌合分子具有和溶葡球菌酶同样的酶学活性。
47.根据权利要求41所述的方法,其中所述接触步骤包括将至少一种溶葡球菌酶或溶葡球菌酶类似物或嵌合分子和所述表面接触,所述嵌合分子具有和溶葡球菌酶同样的酶学活性。
48.根据权利要求41所述的方法,其中所述表面和重组表达的,具有完全活性的同质的溶葡球菌酶接触。
49.根据权利要求48所述的方法,其中所述溶葡球菌酶是合成构建的。
50.根据权利要求41所述的方法,其中抗细菌酶是合成构建的。
51.根据权利要求48所述的方法,其中所述溶葡球菌酶和其他能有效地抵抗葡萄球菌的抗生素共同施用。
52.根据权利要求51所述的方法,其中所述其他抗生素能干扰或抑制细胞壁合成。
53.根据权利要求52所述的方法,其中所述抗生素选自β内酰胺,头孢菌素,糖肽,多肽及其组合物。
54.根据权利要求51所述的方法,其中所述其他抗生素干扰蛋白的合成。
55.根据权利要求54所述的方法,其中所述其他抗生素包括糖苷,四环素和链阳菌素。
56.假器官装置或导管,它可植入到有需要的患者中,并具有至少一个容易生长细菌生物薄膜的表面,其包被有至少一种抗细菌酶,该酶对形成生物薄膜的细菌是致命的,施加的数量足以有效地防止生物薄膜的形成。
57.根据权利要求56所述的装置或导管,其中所述的酶涂层是共价连接在所述表面的。
58.根据权利要求56所述的装置或导管,其中所述的至少一种表面包括聚合物和所述酶的混合物,以至所述酶能在所诉聚合物表面表达,而基本上不从上面释放出来。
59.根据权利要求56所述的装置或导管,其中所述装置选自分流管,支架,组织构建的台架,胃饲管,punctual plug,人工关节,起搏器,和人工瓣膜。
60.根据权利要求59所述的装置或导管,其中所述装置或导管是植入性的金属装置。
61.根据权利要求60所述的装置或导管,其中所述金属是钛。
62.制备聚合物组合物的方法,所述组合物对在由其形成的表面生长的能形成生物薄膜的细菌具有抗性,所述方法包括将聚合物和有效量的至少一种抗细菌酶混合,所述酶对形成生物薄膜的细菌是致命的。
63.根据权利要求62所述的方法,其中所述形成生物薄膜的细菌是葡萄球菌。
64.根据权利要求63所述的方法,其中所述形成生物薄膜的细菌包括金黄色葡萄球菌。
65.根据权利要求63所述的方法,其中所述形成生物薄膜的细菌包括表皮葡萄球菌。
66.根据权利要求63所述的方法,其中所述形成生物薄膜的细菌包括金黄色葡萄球菌和表皮葡萄球菌。
67.根据权利要求62所述的方法,其中所述酶包括溶葡球菌酶或溶葡球菌酶类似物或嵌合分子,该嵌合分子具有和溶葡球菌酶同样的酶学活性。
68.根据权利要求67所述的方法,其中所述溶葡球菌酶或溶葡球菌酶类似物是重组表达的具完全活性的同质溶葡球菌酶。
69.根据权利要求67所述的方法,其中所述溶葡球菌酶是天然来源的。
70.根据权利要求67所述的方法,其中所述溶葡球菌酶是合成的。
71.根据权利要求67所述的方法,其中所述溶葡球菌酶和其他能有效地抵抗葡萄球菌的抗生素共同施用。
72.根据权利要求62所述的方法,其中所述酶包括溶葡球菌酶或溶葡球菌酶类似物。
73.根据权利要求72所述的方法,其中所述溶葡球菌酶是天然来源的。
74.根据权利要求72所述的方法,其中所述溶葡球菌酶是合成的。
75.根据权利要求62所述的方法,其中所述溶葡球菌酶和其他能有效地抵抗葡萄球菌的抗生素共同施用。
76.根据权利要求62所述的方法,其中所述抗生素能干扰或抑制细胞壁的合成。
77.根据权利要求76所述的方法,其中所述抗生素选自β内酰胺,头孢菌素,糖肽,多肽及其组合物。
78.根据权利要求62所述的方法,其中所述其他抗生素干扰蛋白的合成。
79.根据权利要求62所述的方法,其中所述其他抗生素包括糖苷,四环素和链阳菌素。
80.用于构造假器官装置或导管的聚合物组合物,它包括适合使用的聚合物,所述聚合物和至少一种抗细菌酶混合,所述酶对形成生物薄膜的细菌是致命的,施加的数量足以有效地防止生物薄膜在所述聚合物组合物形成的表面上形成。
81.根据权利要求80所述的聚合物组合物,其中所述形成生物薄膜的细菌是葡萄球菌。
82.根据权利要求81所述的聚合物组合物,其中所述形成生物薄膜的细菌包括金黄色葡萄球菌。
83.根据权利要求81所述的聚合物组合物,其中所述形成生物薄膜的细菌包括表皮葡萄球菌。
84.根据权利要求81所述的聚合物组合物,其中所述形成生物薄膜的细菌包括金黄色葡萄球菌和表皮葡萄球菌。
85.根据权利要求81所述的聚合物组合物,其中所述酶包括溶葡球菌酶、溶葡球菌酶类似物或嵌合分子,该嵌合分子具有和溶葡球菌酶同样的酶学活性。
86.根据权利要求85所述的聚合物组合物,其中所述溶葡球菌酶或溶葡球菌酶类似物是重组表达的具完全活性的同质溶葡球菌酶。
87.根据权利要求85所述的聚合物组合物,其中所述溶葡球菌酶是天然来源的。
88.根据权利要求85所述的聚合物组合物,其中所述溶葡球菌酶是合成的。
89.根据权利要求85所述的聚合物组合物,其中所述溶葡球菌酶和其他能有效地抵抗葡萄球菌的抗生素混合。
90.根据权利要求80所述的聚合物组合物,其中所述酶包括溶葡球菌酶或溶葡球菌酶类似物。
91.根据权利要求90所述的方法,其中所述溶葡球菌酶是天然来源的。
92.根据权利要求90所述的方法,其中所述溶葡球菌酶是合成的。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US36781902P | 2002-03-26 | 2002-03-26 | |
| US60/367,819 | 2002-03-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1642496A true CN1642496A (zh) | 2005-07-20 |
Family
ID=28675404
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA038071274A Pending CN1642496A (zh) | 2002-03-26 | 2003-03-26 | 细菌生物薄膜的酶破坏 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US7572439B2 (zh) |
| EP (1) | EP1494614A4 (zh) |
| JP (1) | JP2006507850A (zh) |
| CN (1) | CN1642496A (zh) |
| AU (1) | AU2003237789A1 (zh) |
| BR (1) | BR0308285A (zh) |
| CA (1) | CA2476288A1 (zh) |
| WO (1) | WO2003082148A1 (zh) |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2003241279A1 (en) * | 2002-03-26 | 2003-10-13 | Biosynexus Incorporated | Antimicrobial polymer conjugates |
| US7488757B2 (en) * | 2003-03-24 | 2009-02-10 | Becton, Dickinson And Company | Invisible antimicrobial glove and hand antiseptic |
| US20090191254A1 (en) * | 2004-12-06 | 2009-07-30 | The Govt. Of The U.S.A., Centers For Disease Control And Prevention | Inhibition of biofilm formation using bacteriophage |
| CA2495138C (en) * | 2005-01-20 | 2012-10-23 | Alison Jane Basile | Multiplexed analysis for determining a serodiagnosis of viral infection |
| US20070140990A1 (en) * | 2005-12-21 | 2007-06-21 | Nataly Fetissova | Oral Compositions Comprising Propolis |
| US8512294B2 (en) * | 2006-07-28 | 2013-08-20 | Becton, Dickinson And Company | Vascular access device antimicrobial materials and solutions |
| US8262645B2 (en) * | 2007-11-21 | 2012-09-11 | Actuated Medical, Inc. | Devices for clearing blockages in in-situ artificial lumens |
| CA2715266A1 (en) * | 2008-02-08 | 2009-08-13 | Prothera, Inc. | Inhibition and treatment of gastrointestinal biofilms |
| US20110044968A1 (en) * | 2008-03-10 | 2011-02-24 | Pharmal N Corporation | Compositions for treatment with metallopeptidases, methods of making and using the same |
| US8821455B2 (en) * | 2009-07-09 | 2014-09-02 | Becton, Dickinson And Company | Antimicrobial coating for dermally invasive devices |
| US20110065798A1 (en) * | 2009-09-17 | 2011-03-17 | Becton, Dickinson And Company | Anti-infective lubricant for medical devices and methods for preparing the same |
| US20110135703A1 (en) * | 2009-12-08 | 2011-06-09 | Shipp John I | Antimicrobial Coating for Surgical Implants and Method of Use |
| US20110135704A1 (en) * | 2009-12-08 | 2011-06-09 | Shipp John I | Infection Control for Surgical and Trauma Patients |
| EP2680866A1 (en) | 2011-03-01 | 2014-01-08 | Quorum Innovations, LLC | Materials and methods for treating conditions associated with pathogenic biofilm |
| US20140303060A1 (en) * | 2011-12-14 | 2014-10-09 | Fraunhofer Gesellschaft Zur Foerderung der angewan Forschung E.V. | Process for degrading a biofilm on surfaces of objects |
| US9750928B2 (en) | 2013-02-13 | 2017-09-05 | Becton, Dickinson And Company | Blood control IV catheter with stationary septum activator |
| US9695323B2 (en) | 2013-02-13 | 2017-07-04 | Becton, Dickinson And Company | UV curable solventless antimicrobial compositions |
| US9750927B2 (en) | 2013-03-11 | 2017-09-05 | Becton, Dickinson And Company | Blood control catheter with antimicrobial needle lube |
| US9327095B2 (en) | 2013-03-11 | 2016-05-03 | Becton, Dickinson And Company | Blood control catheter with antimicrobial needle lube |
| EP2996746B1 (en) | 2013-05-13 | 2020-09-30 | Ouyang, Yannan | Flushable catheter affixed to a wash line activated by a microfluidic pressure switch |
| CA2934670A1 (en) * | 2013-12-28 | 2015-07-02 | StaphRx, LLC | Ultra-low dose lysostaphin for treating mrsa |
| US9789279B2 (en) | 2014-04-23 | 2017-10-17 | Becton, Dickinson And Company | Antimicrobial obturator for use with vascular access devices |
| US10376686B2 (en) | 2014-04-23 | 2019-08-13 | Becton, Dickinson And Company | Antimicrobial caps for medical connectors |
| US9675793B2 (en) | 2014-04-23 | 2017-06-13 | Becton, Dickinson And Company | Catheter tubing with extraluminal antimicrobial coating |
| US10358636B2 (en) | 2014-05-14 | 2019-07-23 | Stealth Biologics, Llc | Deimmunized lysostaphin and methods of use |
| US10232088B2 (en) | 2014-07-08 | 2019-03-19 | Becton, Dickinson And Company | Antimicrobial coating forming kink resistant feature on a vascular access device |
| US10493244B2 (en) | 2015-10-28 | 2019-12-03 | Becton, Dickinson And Company | Extension tubing strain relief |
| US20210112816A1 (en) * | 2017-04-26 | 2021-04-22 | Phagelux (Canada) Inc. | Plasma immobilization of bacteriophages and applications thereof |
| US11524098B2 (en) * | 2018-09-14 | 2022-12-13 | Avent, Inc. | Systems and methods for biofilm inoculation |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| US4931390A (en) | 1986-04-16 | 1990-06-05 | Public Health Research Institute Of The City Of New York, Inc. | Expression of the cloned lysostaphin gene |
| US5858962A (en) | 1987-05-11 | 1999-01-12 | Ambi Inc. | Composition for treating mastitis and other staphylococcal infections |
| US4847325A (en) | 1988-01-20 | 1989-07-11 | Cetus Corporation | Conjugation of polymer to colony stimulating factor-1 |
| US4980163A (en) | 1989-03-01 | 1990-12-25 | Public Health Research Institute Of The City Of New York | Novel bacteriocin compositions for use as enhanced broad range bactericides and methods of preventing and treating microbial infection |
| EP0388115A1 (en) * | 1989-03-13 | 1990-09-19 | Nalco Chemical Company | Controlling industrial slime |
| JPH02299663A (ja) * | 1989-05-15 | 1990-12-11 | Unitika Ltd | 抗感染性カテーテル |
| US5234903A (en) | 1989-11-22 | 1993-08-10 | Enzon, Inc. | Chemically modified hemoglobin as an effective, stable non-immunogenic red blood cell substitute |
| US5219564A (en) | 1990-07-06 | 1993-06-15 | Enzon, Inc. | Poly(alkylene oxide) amino acid copolymers and drug carriers and charged copolymers based thereon |
| US5820607A (en) | 1995-06-05 | 1998-10-13 | Board Of Regents, University Of Texas Systems | Multipurpose anti-microbial silastic sheath system for the prevention of device-related infections |
| US6028051A (en) * | 1997-07-23 | 2000-02-22 | Ambi Inc. | Method for the treatment of staphylococcal disease |
| EP1001804B1 (en) * | 1997-07-23 | 2006-02-01 | AMBI Inc. | Pharmaceutical compositions containing lysostaphin alone or in combination with an antibiotic for the treatment of staphylococcal infections |
| US20020037260A1 (en) * | 1997-10-16 | 2002-03-28 | Budny John A. | Compositions for treating biofilm |
| US6315996B1 (en) | 1999-04-09 | 2001-11-13 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Topical lysostaphin therapy for staphylococcus ocular infections |
| EP1198565A1 (en) | 1999-07-07 | 2002-04-24 | Maxygen Aps | A method for preparing modified polypeptides |
| US7151139B2 (en) * | 2001-04-23 | 2006-12-19 | Massachusetts Institute Of Technology | Antimicrobial polymeric surfaces |
| AU2003241279A1 (en) * | 2002-03-26 | 2003-10-13 | Biosynexus Incorporated | Antimicrobial polymer conjugates |
| US7427408B2 (en) * | 2002-06-06 | 2008-09-23 | The Regents Of The University Of California | Quorum sensing and biofilm formation |
-
2003
- 2003-03-26 JP JP2003579694A patent/JP2006507850A/ja active Pending
- 2003-03-26 US US10/401,342 patent/US7572439B2/en not_active Expired - Fee Related
- 2003-03-26 AU AU2003237789A patent/AU2003237789A1/en not_active Abandoned
- 2003-03-26 CA CA002476288A patent/CA2476288A1/en not_active Abandoned
- 2003-03-26 BR BR0308285-7A patent/BR0308285A/pt not_active IP Right Cessation
- 2003-03-26 CN CNA038071274A patent/CN1642496A/zh active Pending
- 2003-03-26 EP EP03736447A patent/EP1494614A4/en not_active Withdrawn
- 2003-03-26 WO PCT/US2003/009354 patent/WO2003082148A1/en active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| US7572439B2 (en) | 2009-08-11 |
| EP1494614A4 (en) | 2010-08-11 |
| BR0308285A (pt) | 2005-04-12 |
| JP2006507850A (ja) | 2006-03-09 |
| EP1494614A1 (en) | 2005-01-12 |
| WO2003082148A1 (en) | 2003-10-09 |
| CA2476288A1 (en) | 2003-10-09 |
| AU2003237789A1 (en) | 2003-10-13 |
| US20030215433A1 (en) | 2003-11-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1642496A (zh) | 细菌生物薄膜的酶破坏 | |
| Wu et al. | Lysostaphin disrupts Staphylococcus aureus and Staphylococcus epidermidis biofilms on artificial surfaces | |
| TWI235656B (en) | A pharmaceutical composition for the treatment of vancomycin-resistant staphylococcal infection | |
| Hanke et al. | Targeting macrophage activation for the prevention and treatment of Staphylococcus aureus biofilm infections | |
| CN101977616B (zh) | 制备噬菌体混合物的方法以及该噬菌体混合物在抗生素抗性葡萄球菌治疗中的用途 | |
| CN1617746A (zh) | 抗感染的医用器材 | |
| CN104189898A (zh) | 铜绿假单胞菌疫苗及其制备方法 | |
| CN110144333B (zh) | 一株铜绿假单胞菌噬菌体及其应用 | |
| US11690885B2 (en) | Anti-bacterial compositions and uses thereof | |
| CN1895666A (zh) | 奶牛乳房炎多联灭活菌苗 | |
| CN105963680B (zh) | 用于抑制/瓦解生物被膜的抑制剂及其应用 | |
| US20100221237A1 (en) | Enzyme disruption of bacterial biofilms | |
| CN109529045A (zh) | 利福霉素-喹嗪酮偶联分子及其药学上可接受的盐的应用 | |
| JP2005525849A (ja) | バクテリアの生息する表面の処理 | |
| CN1520881A (zh) | 一种用于防治奶牛乳腺炎的杀菌制剂及其制备方法 | |
| US7662607B2 (en) | Chalaropsis lysozyme protein and its method of use in anti-bacterial applications | |
| CN1583170A (zh) | 用于抗病毒抗耐药菌的人溶菌酶药物及其制法 | |
| WO2016146037A1 (zh) | 用于抑制/瓦解生物被膜的抑制剂及其应用 | |
| Schinabeck et al. | Biofilm-related indwelling medical device infections | |
| CN1911442A (zh) | 一种用于防治创面感染的溶葡萄球菌酶冻干粉剂 | |
| CN113321707B (zh) | 一种人工合成抗菌肽及其应用 | |
| Mukherjee et al. | 13 Bacteriophage-Associated Inhibition of | |
| US20190282677A1 (en) | Method of preventing or reducing biofilm formation | |
| CN1268211C (zh) | 利用微生物防治白蚁的方法 | |
| Liu | Activity of antibiotics and non-antibiotics substances on Staphylococcus aureus biofilms |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |