CN116096428A - 鸟氨酸氨甲酰基转移酶(otc)构建体及其使用方法 - Google Patents
鸟氨酸氨甲酰基转移酶(otc)构建体及其使用方法 Download PDFInfo
- Publication number
- CN116096428A CN116096428A CN202080089266.1A CN202080089266A CN116096428A CN 116096428 A CN116096428 A CN 116096428A CN 202080089266 A CN202080089266 A CN 202080089266A CN 116096428 A CN116096428 A CN 116096428A
- Authority
- CN
- China
- Prior art keywords
- otc
- polynucleotide construct
- mrna
- lnp
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1003—Transferases (2.) transferring one-carbon groups (2.1)
- C12N9/1018—Carboxy- and carbamoyl transferases (2.1.3)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6905—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion
- A61K47/6911—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion the form being a liposome
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/0008—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition
- A61K48/0025—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition wherein the non-active part clearly interacts with the delivered nucleic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
- A61K48/0066—Manipulation of the nucleic acid to modify its expression pattern, e.g. enhance its duration of expression, achieved by the presence of particular introns in the delivered nucleic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/67—General methods for enhancing the expression
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/8509—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells for producing genetically modified animals, e.g. transgenic
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y201/00—Transferases transferring one-carbon groups (2.1)
- C12Y201/03—Carboxy- and carbamoyltransferases (2.1.3)
- C12Y201/03003—Ornithine carbamoyltransferase (2.1.3.3)
Abstract
除其他外,本公开内容提供了治疗鸟氨酸氨甲酰基转移酶缺乏症的多核苷酸构建体、组合物和方法,所述方法包括向有此需要的受试者施用包含多核苷酸构建体的组合物,所述构建体包含5’UTR、编码鸟氨酸氨甲酰基转移酶的密码子优化的mRNA和3’UTR。
Description
相关申请的交叉引用
本申请要求于2019年10月22日提交的美国临时申请第62/924,567号的优先权,其内容通过引用整体并入本文。
序列表
以电子方式提交的ASCII文本文件形式的序列表(名称:4170_021PC01_Seqlisting_ST25;大小:13,467字节;创建日期:2020年10月21日)与本申请一起提交,且其内容通过引用整体并入本文。
背景技术
鸟氨酸氨甲酰基转移酶缺乏症(OTC缺乏症或OTCD)是一种X连锁遗传疾病,其特征是完全或部分缺乏功能性鸟氨酸氨甲酰基转移酶(OTC),这通常是OTC基因突变的结果。OTC基因的突变可以消除或降低OTC酶催化由氨甲酰磷酸(CP)和鸟氨酸(Orn)合成瓜氨酸(Cit)和磷酸(Pi)(在肝脏和小肠中)的能力。尿素循环中的这种功能障碍会导致氨过量,氨会积聚在血液中(高氨血症)并传输至神经系统,由此导致与OTC缺乏症相关的症状。
OTC缺乏症是尿素循环障碍最常见的类型。据报道,人类OTC中存在数百种突变。OTC缺乏症的严重程度和发病年龄因人而异,即使是在同一个家庭中和/或具有相同的致病突变。这种病症的严重形式会影响一些出生后不久的婴儿,通常是男性。这种病症的较温和形式会影响婴儿后期的一些儿童。男性和女性都可能在儿童时期出现OTC缺乏症的症状。
目前,对于OTC缺乏症患者,除了肝移植之外没有其他治疗方法,长期治疗包括蛋白质摄入的终生限制和氮清除剂治疗(例如苯乙酸钠或苯丁酸钠和/或苯甲酸钠)。对于严重的新生儿期发病的OTC缺乏症或具有频繁高氨血症发作的患者,也可以考虑肝移植。
RNA分子具有作为体外和体内基因表达的有效调节剂的能力,因此具有作为基于核酸的药物的潜力。这些分子可以通过多种机制发挥作用,这些机制利用与细胞蛋白的特异性相互作用,或与其他RNA分子的碱基互补配对相互作用。对于以蛋白质产生不足或有缺陷为特征的疾病,治疗性mRNA有可能为核糖体提供指令以产生缺失或有缺陷的蛋白质。向细胞内高效且有效的递送RNA治疗剂是困难的,因为这些治疗剂容易在血流中快速降解并排出,并且不能自由地通过细胞膜。
外源性多核苷酸(如RNA分子)和其他膜不可渗透的化合物向活细胞中的递送受到细胞的复杂膜系统的高度限制。通常,反义和基因疗法中使用的分子是大的、带负电荷的亲水分子。这些特性可以阻止它们直接扩散穿过细胞膜进入细胞质。因此,多核苷酸用于调节基因表达的治疗用途的主要障碍是将多核苷酸递送至细胞质。转染剂通常包含阳离子性质的多肽、聚合物和脂质以及纳米颗粒和微粒。这些转染剂已成功用于体外反应。然而,在体内的功效和毒性方面存在挑战。此外,这些系统的阳离子电荷导致其与血清成分的相互作用,从而致使多核苷酸-转染试剂相互作用的不稳定以及较差的生物利用度和靶向性。当在体内转染核酸时,递送剂应保护核酸有效载荷对抗早期细胞外降解,例如,对抗核酸酶。此外,递送剂不应被适应性免疫系统识别(免疫原性)并且不应刺激急性免疫应答。
发明内容
本公开提供了多核苷酸构建体,其从5’至3’包含:5’UTR,其包含SEQ ID NO:2的序列;mRNA序列,其包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),其中ORF包含与SEQ ID NO:1至少约95%相同的密码子优化的序列;以及3’UTR,其包含SEQ IDNO:3的序列。
在某些方面,本公开提供了包含mRNA序列的多核苷酸构建体,所述mRNA序列编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),其中所述mRNA序列包含具有不超过五个不同于SEQ ID NO:4的核酸的序列。在一些方面,多核苷酸构建体从5’至3’包含:5’UTR;包含编码OTC的ORF的mRNA序列;和3’UTR。在某些方面,5’UTR包含SEQ ID NO:2的序列和/或3’UTR包含SEQ ID NO:3的序列。在一些方面,功能性OTC包含SEQ ID NO:7的氨基酸序列。在一些方面,ORF序列包含SEQ ID NO:1。
在一些方面,mRNA序列具有不超过四个、三个、两个或一个不同于SEQ ID NO:4的核酸。在某些方面,多核苷酸构建体包含SEQ ID NO:4的序列。
在一些方面,多核苷酸构建体还包含5’末端帽子,例如Cap1。在一些方面,多核苷酸构建体还包含polyA尾。在某些方面,polyA尾是80至1000个核酸长,例如100至500个核酸长。
在一些方面,mRNA包含至少一个化学修饰的尿苷。在某些方面,尿苷的至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约95%或约100%被化学修饰。在一些方面,化学修饰的尿苷选自假尿苷(ψ)、N1-甲基假尿苷(N1-me-ψ)和/或其组合。
本公开的某些方面还涉及一种组合物,其包含:本公开的多核苷酸构建体;和递送剂。在一些方面,递送剂包括脂质纳米颗粒(LNP)、脂质体、聚合物、胶束、质粒、病毒或其任何组合。
在某些方面,LNP选自下组:LNPl(PEG2000-C-DMA:13-B43:胆固醇:DSPC)、LNP2(PEG2000-S:13-B43:胆固醇:DSPC或PEG2000-S:18-B6:胆固醇:DSPC)和LNP3(PEG750-C-DLA:18-B6:胆固醇:DSPC)内的组合物。在一些方面,多核苷酸构建体被封装在LNP中。在一些方面,组合物还包含药学上可接受的载体。在一些方面,多核苷酸构建体被完全封装在LNP中。在一些方面,多核苷酸构建体的至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或更多被LNP封装。
本公开的某些方面涉及用于增加细胞中OTC表达的量的方法,其包括向细胞施用包含本公开的多核苷酸构建体的组合物或本公开的组合物。在一些方面,细胞是肝细胞。
本公开的某些方面涉及用于治疗或减轻与鸟氨酸氨甲酰基转移酶缺乏症(OTCD)相关的症状的方法,其包括向有此需要的受试者施用治疗有效量的包含本公开的多核苷酸构建体的组合物或本公开的组合物。
本公开的某些方面涉及一种用于在患有OTCD的受试者中治疗高氨血症或降低其风险的方法,其包括向有此需要的受试者施用治疗有效量的包含本公开的多核苷酸构建体的组合物或本公开的组合物。
本公开的某些方面涉及一种表达盒,其包含与SEQ ID NO:8具有至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或100%序列同一性的DNA序列。在一些方面,表达盒还包含启动子,例如T7启动子。本公开的一些方面涉及包含本公开的表达盒的质粒。在一些方面,表达盒转录本公开的mRNA(例如,包含SEQ ID NO:1或SEQ ID NO:4)。本公开的一些方面涉及包含本公开的表达盒或本公开的质粒的宿主细胞。
本公开的某些方面涉及本公开的多核苷酸构建体,或本公开的组合物,或本公开的表达盒,或本公开的质粒,或本公开的宿主细胞在制备用于在有此需要的受试者中治疗OTCD或用于在患有OTCD的受试者中治疗高氨血症或用于降低其风险的药物中的用途有此需要。
本公开的某些方面涉及用于核酸的体内递送的方法,该方法包括:向哺乳动物受试者施用本公开的多核苷酸构建体,或本公开的组合物,或本公开的表达盒,或本公开的质粒,或本公开的宿主细胞。
本公开的某些方面涉及用于在有此需要的哺乳动物受试者中治疗疾病或病症的方法,该方法包括:向哺乳动物受试者施用治疗有效量的本公开的多核苷酸构建体,或本公开的组合物,或本公开的表达盒,或本公开的的质粒,或本发明的宿主细胞。在某些方面,疾病或病症是尿素循环障碍。
通过阅读以下详细描述,这些和其他方面将是显而易见的。
附图说明
在一些情况下,结合附图考虑以下对本公开的各个方面的详细描述,可以更全面地理解本公开,其中:
图1显示第一次给药后6小时,与PBS对照组相比,在被施用封装具有不同Poly(A)尾长度(80、161、208、262、322或440个核苷酸)的密码子优化的OTC构建体(OTC mRNA)的LNP的大鼠中的MCP-1诱导。80个核苷酸的Poly(A)是编码的,而其他测试的Poly(A)是酶促合成的(enz)。
图2A显示在第0、7和14天,分别第一次、第二次和第三次给药后6小时,与PBS对照组相比,在被施用封装具有不同Poly(A)尾长度(80、161、208、262、322或440个核苷酸)的密码子优化的OTC构建体(OTC mRNA)的LNP的大鼠中的MCP-1诱导。80个核苷酸的Poly(A)是编码的,而其他测试的Poly(A)是酶促合成的(enz)。
图2B显示在第0、7和14天,分别第一次、第二次和第三次给药后6小时,与PBS对照组相比,在被施用封装具有不同Poly(A)尾长度(80、161、208、262、322或440个核苷酸)的密码子优化的OTC构建体(OTC mRNA)的LNP大鼠中的IP-1诱导。80个核苷酸的Poly(A)是编码的,而其他测试的Poly(A)是酶促合成的(enz)。
图3A显示在单剂量施用封装具有不同Poly(A)尾长度(80、161、208、262、322或440个核苷酸)的密码子优化的OTC构建体(OTC mRNA)的LNP后,与PBS对照组相比,大鼠肝脏中的hOTC蛋白表达。80个核苷酸的Poly(A)是编码的,而其他测试的Poly(A)是酶促合成的(enz)。
图3B显示在单剂量与多剂量施用携带具有不同Poly(A)尾长度(80、161、208、262、322或440个核苷酸)的密码子优化的OTC构建体(OTC mRNA)的LNP后,与PBS对照组相比,大鼠肝脏中的hOTC蛋白表达。80个核苷酸的Poly(A)是编码的,而其他测试的Poly(A)是酶促合成的(enz)。
图4显示在第一次给药后6小时,与PBS对照组相比,在被施用封装具有不同修饰:PsU、N1MePsU或5MoU的OTC构建体(OTC mRNA)的LNP1或LNP2(可电离脂质:13-B43)组的小鼠中的MCP-1诱导。
图5显示给药后24小时,与PBS对照相比,在被施用封装具有不同修饰:PsU、N1MePsU或SMoU的OTC构建体的LNP1或LNP2(可电离脂质:13-B43)组的小鼠中的hOTC表达。
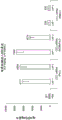
图6A显示与EPO和Luc有效载荷相比,在被施用封装密码子优化的OTC构建体(OTCmRNA)的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组的大鼠中的抗PEG IgG抗体应答。
图6B显示与EPO和Luc有效载荷相比,在被施用封装密码子优化的OTC构建体(OTCmRNA)的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组的大鼠中的抗PEG IgM抗体应答。
图7显示在0、7和14天,与EPO和Luc有效载荷以及PBS相比,在被施用封装密码子优化的OTC构建体的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组6小时的大鼠中的MCP-1诱导(OTC mRNA)。
图8显示在1和3次给药后,在被施用封装密码子优化的OTC构建体(OTC mRNA)的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组的大鼠中的OTC蛋白表达。
图9显示在1和3次给药后,在被施用封装密码子优化的OTC构建体(OTC mRNA)的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组后的大鼠肝脏中的脂质浓度(清除率)。
图10A显示在1和3次给药后,在被施用封装密码子优化的OTC构建体(OTC mRNA)的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组后的大鼠中的ALT水平。
图10B显示在1和3次给药后,在被施用封装密码子优化的OTC构建体(OTC mRNA)的不同LNP(LNP1、LNP2(可电离脂质:13-B43)、LNP2(可电离脂质:18-B6)或LNP3)组后的大鼠中的AST水平。
图11A-11C显示在每周重复给药后,施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物后的细胞因子应答。图11A显示给药后6小时的MCP-1诱导。图11B显示了给药后6小时的IP-10诱导。图11C显示给药后6小时的MIP-1a诱导。
图12显示在每周重复给药后,与PBS对照相比,在施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物后的抗-PEG IgM抗体应答。
图13显示在每周重复给药后,与PBS对照相比,施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物后的抗-PEG IgG抗体应答。
图14显示在每周重复给药后,与PBS对照相比,施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物后的抗-OTC IgM抗体应答。
图15显示在每周重复给药后,与PBS对照相比,施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物后的抗-OTC IgM抗体应答。
图16显示在每周重复给药后,在被施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物的大鼠中的OTC蛋白表达。
图17A-17B显示在被施用封装密码子优化的OTC构建体的LNP2(可电离脂质:13-B43)组合物的大鼠(A)肝脏和(B)血浆中的人OTC mRNA(hOTC mRNA)。
图18A显示在被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠肝脏中给药后24小时的平均ALT水平。
图18B显示在被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠肝脏中给药后24小时的平均AST水平。
图18C显示在被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠肝脏中给药后24小时的个体(R1、R2或R3)和平均ALT水平。
图18D显示在被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠肝脏中给药后24小时的个体(R1、R2或R3)和平均AST1水平。
图19A-19D显示被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠给药后24小时的(A)平均GGT水平,(B)总胆红素水平,(C)个体(R1、R2或R3)和平均GGT水平,和(D)个体(R1、R2或R3)和平均总胆红素水平。
图20A-20C显示被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠给药后24小时的(A)中性粒细胞水平、(B)单核细胞水平和(C)血小板水平。
图21A-21C显示被施用封装密码子优化的OTC构建体的LNP1、LNP2(可电离脂质:13-B43)或LNP2(可电离脂质:18-B6)组合物的大鼠给药后6小时的(A)MCP-1水平,(B)MIP-1a水平和(C)IP-10水平。
图22显示被施用封装密码子优化的OTC构建体的LNP1或LNP2(可电离脂质:13-B43)组合物的大鼠给药后24小时的OTC表达。
图23A-23C显示在以0.25mg/kg、1mg/kg和3mg/kg被施用封装密码子优化的OTCmRNA构建体的LNP1的非人灵长类动物的肝脏中的(A)人OTC(hOTC),(B)MCP-1和(C)IL-6蛋白表达水平。hOTC蛋白表达显示为内源性表达的%,并且与0mg/kg对照相比显示MCP-1和IL-6蛋白表达。
具体实施方式
本公开涉及用于在细胞中表达的功能性酶鸟氨酸氨甲酰基转移酶(OTC)的改进的多核苷酸(例如mRNA)、组合物和方法,以及这些多核苷酸、组合物和方法用于治疗患有OTC缺陷的受试者的用途。除非另有定义,否则本文使用的所有技术和科学术语具有与本文所述方法和组合物相关的本领域普通技术人员的通常理解相同的含义。本文提供的定义是为了便于理解本文中经常使用的某些术语。
除非内容另有明确规定,在本说明书和所附权利要求中使用的,单数形式“一(a)”、“一个(an)”和“该(the)”涵盖指代复数的方面。
如本文所用术语“核酸”在其最广义上是指,例如通过磷酸二酯键掺入或可以掺入多核苷酸链中的任何化合物和/或物质。在一些方面,“核酸”是指单个核酸残基(例如,核苷酸和/或核苷)。在一些方面,“核酸”是指包含单个核酸残基的多核苷酸链。在一些方面,“核酸”包括RNA,例如mRNA,以及单链和/或双链DNA和/或cDNA。
如本文所用,术语“多核苷酸”或“寡核苷酸”是指包含7-20,000个核苷酸单体单元(即,从7个核苷酸单体单元到20,000个核苷酸单体单元,包括端值)的聚合物。多核苷酸包括脱氧核糖核酸(DNA)和核糖核酸(RNA)或它们的衍生物,以及DNA和RNA的组合。例如,DNA可以是cDNA、体外聚合的DNA、质粒DNA、质粒DNA的部分、表达载体、表达盒、嵌合序列、重组DNA、染色体DNA或其任何衍生物的形式。在进一步的示例中,RNA可以是信使RNA(mRNA)、体外聚合的RNA、重组RNA、转移RNA(tRNA)、核小RNA(snRNA)、核糖体RNA(rRNA)、嵌合序列、重组RNA或其任何衍生物。此外,DNA和RNA可以是单链、双链、三链或四链。
如本文所用,多核苷酸的进一步示例包括但不限于经修饰的或未修饰的单链mRNA。经修饰的mRNA包括具有至少两个修饰和可翻译区的那些。修饰可以位于核酸分子的主链和/或核苷上。修饰也可以位于核苷和主链键上。
如本文所用,术语“信使RNA(mRNA)”是指编码至少一种多肽的多核糖核苷酸。如本文所用的mRNA包括经修饰的和未修饰的RNA。mRNA可以包含一个或多个编码区和非编码区。mRNA可以从天然来源纯化、使用重组表达系统产生和任选地纯化、体外转录、化学合成等。在适当的情况下,例如,在化学合成分子的情况下,mRNA可以包含核苷类似物,例如具有化学修饰碱基或糖、骨架修饰等的类似物。除非另有说明,mRNA序列以5’至3’方向呈现。在一些方面,mRNA是或包含天然核苷(例如,腺苷、鸟苷、胞苷、尿苷);核苷类似物(例如,2-氨基腺苷、2-硫代胸苷、肌苷、吡咯并嘧啶、3-甲基腺苷、5-甲基胞苷、C-5丙炔基-胞苷、C-5丙炔基-尿苷、2-氨基腺苷、C5-溴尿苷、C5-氟尿苷、C5-碘尿苷、C5-丙炔基-尿苷、C5-丙炔基-胞苷、C5-甲基胞苷、2-氨基腺苷、7-脱氮腺苷、7-脱氮鸟苷、8-氧代腺苷、8-氧代鸟苷、O(6)-甲基鸟嘌呤和2-硫胞苷);化学修饰的碱基;生物修饰的碱基(例如甲基化碱基);插入碱基;改性糖(例如,2’-氟代核糖、核糖、2’-脱氧核糖、阿拉伯糖和己糖);和/或经修饰的磷酸基团(例如硫代磷酸酯和5’-N-亚磷酰胺键)。
如本文所用,核酸序列的“表达”是指将多核苷酸(例如mRNA)翻译成多肽,多个多肽组装成完整蛋白质(例如酶)和/或多肽或完全组装的蛋白质(例如酶)的翻译后修饰。在本公开中,术语“表达”和“产生”在语法上是等同的,可互换使用。
如本文所用,术语“氨基酸”在其最广义上是指可以并入多肽链中的任何化合物和/或物质。在一些方面,氨基酸具有一般结构H2N-C(H)(R)-COOH。氨基酸包括肽中的羧基和/或氨基末端氨基酸,可以通过甲基化、酰胺化、乙酰化、保护基团和/或用可以改变肽的循环半衰期而不会对它们的活性产生其他不利影响的其他化学基团的取代进行修饰。氨基酸可以参与二硫键。氨基酸可以包含一种或多种翻译后修饰例如与一种或多种化学实体(例如甲基、乙酸基、乙酰基、磷酸基、甲酰基部分、类异戊二烯基团、硫酸基团、聚乙二醇部分、脂质部分、糖类部分、生物素部分等)的缔合。术语“氨基酸”与“氨基酸残基”可互换使用,并且可以指游离氨基酸和/或肽的氨基酸残基。从使用该术语的上下文中可以明显看出它是指游离氨基酸还是肽的残基。
“多肽”是由肽键连接的氨基酸残基的聚合物,无论是天然产生的还是合成的。
如本文所用,术语“肽”是指具有2-100个氨基酸单体的多肽。
“蛋白质”是包含一条或多条多肽链的大分子。蛋白质还可以包含非肽成分,例如糖类基团。糖类和其他非肽取代基可以通过产生蛋白质的细胞被添加至蛋白质中,并且会随细胞类型而变化。一些蛋白质在本文中是根据它们的氨基酸骨架结构来定义。
如本文所用,“功能性”生物分子,例如蛋白质,是一种形式的生物分子,其在该形式中表现出其所被表征的特性和/或活性。
如本文所用,术语“递送”包括局部递送和全身递送。例如,多核苷酸(例如mRNA)的递送包括将多核苷酸递送至靶组织且编码的蛋白质在靶组织内表达并保留的情形(也称为“局部分布”或“局部递送”)。其他示例性情形包括将多核苷酸递送至靶组织且编码的蛋白质被表达并被分泌到患者的循环系统(例如血清)中,并全身性分布且被其他组织吸收的情形(也称为“全身分布”或“全身递送”)。在其他示例性情形下,多核苷酸被全身递送,并在体内被多种细胞和组织吸收。在一些示例性情形下,递送是静脉内、肌内或皮下。
如本文所用,术语“体外”是指在人工环境中发生的事件,例如在试管或反应容器中、在细胞培养物中等,而不是在多细胞生物体中。
如本文所用,术语“体内”是指在多细胞生物体内发生的事件,例如人类和非人类动物。在基于细胞系统的背景下,该术语可用于指代在活细胞内发生的事件(而不是例如体外系统)。
本文使用的短语“药学上可接受的”是指在合理的医学判断范围内,适用于与人类和动物的组织接触,而没有过度的毒性、刺激、过敏反应或其他问题或并发症,具有合理的收益/风险比的那些化合物、材料、组合物和/或剂型。
如本文所用,术语“治疗”是指部分或全部消除、减轻任何一种待治疗的疾病和病症的一个或多个病理特征或症状,或抑制或逆转其进展的递送剂和核酸的施用。此类疾病包括但不限于鸟氨酸氨甲酰基转移酶缺乏症(OTCD)。
如本文所用,短语“治疗有效”旨在限定多核苷酸或药物组合物的量,或在联合治疗的情况下活性成分的组合量。该量或组合量将实现治疗相关疾病或病症的目标。
如本文所用,术语“受试者”是指人类或任何非人类动物(例如,小鼠、大鼠、兔、狗、猫、牛、猪、羊、马或灵长类动物)。人类包括出生前和出生后形态。在许多方面,受试者是人。受试者可以是患者,是指向医疗机构寻求疾病诊断或治疗的人。术语“受试者”在本文中可以与“个体”或“患者”互换使用。受试者可能患有或易患疾病或病症,但可能或可能不表现出疾病或病症的症状。
术语“脂质”是指一组是脂肪酸的酯的有机化合物,其特征在于不溶于水,但可溶于许多有机溶剂。它们通常至少分为三类:(1)“简单脂质”,其包括脂肪和油以及蜡;(2)“复合脂质”,其包括磷脂和糖脂;(3)“衍生脂质”,例如类固醇。
术语“两亲性脂质”部分地是指任何合适的材料,其中脂质材料的疏水部分取向为疏水相,而亲水部分取向为水相。两亲性脂质通常是脂质LNP的主要成分。亲水性特征源于极性或带电基团的存在,例如糖类、磷酸根、羧基、硫酸根、氨基、巯基、硝基、羟基和其他类似基团。疏水性可以通过包含非极性基团来赋予,所述非极性基团包括但不限于,长链饱和及不饱和脂肪族烃基以及被一个或多个芳族、脂环族或杂环基团取代的此类基团。两亲性化合物的示例包括但不限于磷脂、氨基脂和鞘脂。磷脂的代表性示例包括但不限于磷脂酰胆碱、磷脂酰乙醇胺、磷脂酰丝氨酸、磷脂酰肌醇、磷脂酸、棕榈酰油酰磷脂酰胆碱、溶血磷脂酰胆碱、溶血磷脂酰乙醇胺、二棕榈酰磷脂酰胆碱、二油酰磷脂酰胆碱、二硬脂酰磷脂酰胆碱或二亚油酰磷脂酰胆碱。其他缺乏磷的化合物(例如鞘脂、鞘糖脂家族、二酰基甘油和β-酰氧基酸)也属于被命名为两亲性脂质的组。此外,上述两亲性脂质可以与其他脂质混合,其中包括甘油三酯和甾醇。
术语“阴离子脂质”是指在生理pH值下带负电荷的任何脂质。这些脂质包括但不限于磷脂酰甘油、心磷脂、二酰基磷脂酰丝氨酸、二酰基磷脂酸、N-十二烷酰基磷脂酰乙醇胺、N-琥珀酰磷脂酰乙醇胺、N-戊二酰磷脂酰乙醇胺、赖氨酰磷脂酰甘油和其他与中性脂质连接的阴离子修饰基团。
术语“阳离子脂质”是指在选择性的pH下(例如生理pH下)携带净正电荷的多种脂质种类中的任何一种。此类脂质包括但不限于N,N-二油基-N,N-二甲基氯化铵(“DODAC”);N-(2,3-二油氧基)丙基)-N,N,N-三甲基氯化铵(“DOTMA”);N,N-二硬脂基-N,N-二甲基溴化铵(“DDAB”);N-(2,3-二油酰氧基)丙基)-N,N,N-三甲基氯化铵(“DOTAP”);3-(N-(N’,N’-二甲氨基乙烷)-氨甲酰)胆固醇(“DC-Chol”)和N-(1,2-二肉豆蔻氧基丙酸-3-基)-N,N-二甲基-N-羟乙基溴化铵(“DMRIE”)。此外,可获得用于本公开的许多商业阳离子脂质制剂。这些包括例如,(市售阳离子脂质体,其包含DOTMA和1,2-二油酰-sn-3-磷酸乙醇胺(“DOPE”),来自GIBCO/BRL,Grand Island,N.Y.,USA);(市售阳离子脂质体,其包含N-(1-(2,3-二油基氧基)丙基)-N-(2-(精胺甲酰胺基)乙基)-N,N-二甲基三氟乙酸铵(“DOSPA”)和(“DOPE”),来自GIBCO/BRL);和(市售阳离子脂质,其包含乙醇中的双十八烷基氨基甘氨酰羧基精胺(“DOGS”),来自Promega Corp.,Madison,Wis.,USA)。以下是阳离子脂质,并且在低于生理pH时具有正电荷:DODAP、DODMA、DMDMA等。
术语“脂质纳米颗粒”是指可用于递送化合物(例如,多核苷酸构建体)的任何脂质组合物,其包括但不限于脂质体,其中水体积被两亲脂质双层封装;或随着水性内部减少,其中脂质包被包含大分子组分的内部,例如质粒;或脂质聚集体或胶束,其中封装的组分被包含在相对无序的脂质混合物内。
如本文所用,术语“脂质封装的”或“脂质封装”是指可以指提供具有完全封装、部分封装或两者的化合物(例如多核苷酸构建体)的脂质制剂。本文理解“完全封装”或“完全封装的”是指脂质制剂中至少90%的化合物(例如多核苷酸构建体)被脂质(例如LNP)封装。在一些方面,脂质制剂中的化合物(例如,多核苷酸构建体)的至少95%、至少96%、至少97%、至少98%、至少99%或更多被脂质(例如LNP)封装。
多核苷酸构建体
本文公开的多核苷酸构建体可用作治疗剂,以提高细胞(体外或体内)中OTC蛋白的水平至高于在不存在本公开的多核苷酸构建体时获得和/或观察到的水平。
在某些方面,多核苷酸构建体包含核酸序列,例如mRNA序列,其包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)蛋白的开放阅读框(ORF)。ORF可以编码全长OTC蛋白或其功能性片段。在一些方面,ORF编码与SEQ ID NO:7具有至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%、至少99.5%或100%序列同一性的氨基酸序列。在一些方面,全长OTC包含SEQ ID NO:7的氨基酸序列。
在一些方面,多核苷酸构建体包含mRNA序列,所述mRNA序列包含被密码子优化的ORF。在一些方面,ORF包含与SEQ ID NO:1具有至少95%、至少96%、至少97%、至少98%、至少99%、至少99.5%或100%序列同一性的序列。在一些方面,ORF包含SEQ ID NO:1的核酸序列。
在一些方面,多核苷酸构建体包含5’UTR。5’UTR包含SEQ ID NO:2的序列。
在一些方面,多核苷酸构建体包含3’UTR。3’UTR包含SEQ ID NO:3的序列。
在一些方面,本公开的多核苷酸构建体从5’至3’包含:(i)5’UTR,其例如,包含SEQID NO:2的序列;(ii)核酸序列,例如mRNA,其包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),其中ORF包含与SEQ ID NO:1至少约95%、96%、97%、98%、99%、99.5%或100%相同的序列;和3’UTR,其包含SEQ ID NO:3的序列。
在一些方面,多核苷酸构建体包含不超过五个不同于SEQ ID NO:4的核酸的序列。在一些方面,多核苷酸构建体包含与SEQ ID NO:4具有五个、四个、三个、两个或一个核苷酸差异的序列。在一些方面,核酸差异可存在于SEQ ID NO:4的核苷酸2至1221内。多核苷酸构建体可包含SEQ ID NO:4的序列。
多核苷酸构建体可以进一步包含polyA尾。在一些方面,polyA尾长于80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、110、115、120、125、130、135、140、145或150个核酸。在一些方面,polyA尾是80至1000、85至1000、90至1000、95至1000、100至1000、105至1000、110至1000、115至1000、120至1000、125至1000、130至1000、135至1000、140至1000、145至1000、150至1000、155至1000、160至1000、80至800、85至800、90至800、95至800、100至800、105至800、110至800、115至800、120至800、125至800、130至800、135至800、140至800、145至800、150至800、155至800或160至800个核酸长。在一些方面,polyA尾是100至500个核酸长。
在一些方面,多核苷酸构建体在ORF的5’末端包含起始密码子。在一些方面,多核苷酸构建体在ORF的3’末端包含终止密码子。
在某些方面,多核苷酸构建体包含经修饰的核苷酸。在一些方面,多核苷酸构建体包含mRNA序列,所述mRNA序列包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),其中所述mRNA序列包含经修饰的核苷酸。在一些方面,经修饰的核苷酸是尿苷。在一些方面,尿苷的至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约99%或100%被化学修饰。
在一些方面,化学修饰的尿苷选自假尿苷(ψ)、N1-甲基假尿苷(N1-me-ψ)、5-甲氧基尿苷(5moU)及其任何组合。在一些方面,化学修饰的尿苷选自假尿苷(ψ)、N1-甲基假尿苷(N1-me-ψ)及其任何组合。在某些方面,ORF,例如包含SEQ ID NO:1,包含至少95%、至少98%、至少99%或约100%经修饰的尿苷,例如,假尿苷(ψ)修饰的或N1-甲基假尿苷(N1-me-ψ)修饰的。
在某些方面,可以使用表达盒制备多核苷酸构建体,所述表达盒包含与SEQ IDNO:8具有至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或100%序列同一性的序列。在一些方面,表达盒还包含启动子,例如T7启动子。在一些方面,T7启动子包含以下5’至3’序列:TAATACGACTCACTATA(SEQ ID NO:9)。在一些方面,表达盒的5’UTR包含紧邻启动子(例如T7启动子)下游的腺嘌呤(A)。一些方面涉及包含表达盒的质粒。在一些方面,质粒还包含抗生素抗性基因。在一些方面,使用体外转录制备多核苷酸构建体。
示例性OTC氨基酸序列和编码核苷酸序列显示于本文表1中。
表1:与多核苷酸构建体相关的序列
在一些方面,本公开的多核苷酸构建体与递送剂(例如LNP)一起配制。
递送剂
本文公开的递送剂可以在体外和体内有效地将本文公开的多核苷酸构建体、表达盒和mRNA转运到细胞中。
在某些方面,递送剂是脂质纳米颗粒、脂质体、聚合物、胶束、质粒、病毒递送剂或其任何组合。
不受任何特定理论的束缚,通过递送剂对本文公开的多核苷酸构建体、表达盒和/或mRNA的转运可以通过将多核苷酸构建体递送至细胞的细胞溶质而发生。因为基因表达和mRNA翻译发生在细胞的细胞溶质中,所以多核苷酸必须进入细胞溶质以有效调节靶基因或有效翻译转运的mRNA。如果多核苷酸不进入细胞溶质,它们很可能被降解或保留在细胞外基质中。
用于将具有生物活性的多核苷酸在细胞内递送至靶细胞的方法的示例包括,细胞在哺乳动物中的那些,所述哺乳动物包括例如人、啮齿动物、鼠、牛、犬、猫、绵羊、马和猿类哺乳动物。在一些方面,用于细胞内递送的靶细胞是肝细胞。
在一些方面,递送剂是脂质纳米颗粒(LNP)。本公开的多核苷酸构建体可以在LNP内配制。在某些方面,多核苷酸构建体被封装在LNP内。如本文所用,“封装的”是指在LNP的内部空间内包含分子,例如多核苷酸。在一些方面,通过将多核苷酸构建体(例如,包含mRNA)封装在递送剂(例如LNP)内,可以保护核酸(例如,本公开的多核苷酸构建体)免受环境影响,所述环境可以包含降解核酸的酶或化学物质和/或导致核酸快速排泄的系统或受体。脂质纳米颗粒通常包含可电离的(例如,阳离子)脂质、非阳离子脂质(例如,胆固醇和磷脂)和PEG脂质(例如,缀合的PEG脂质),它们可以与目标有效载荷(例如,本文公开的多核苷酸构建体)一起配制。本公开的多核苷酸构建体(例如mRNA)可被封装在脂质颗粒中,从而保护它免受酶促降解。在一些方面,分子(例如,多核苷酸构建体)被LNP完全封装。在一些方面,脂质制剂中分子(例如,多核苷酸构建体)的至少95%、至少96%、至少97%、至少98%、至少99%或更多被LNP封装。
某些方面涉及一种组合物,其包含:本公开的多核苷酸构建体;和递送剂。递送剂可以包含LNP,例如LNP1(PEG2000-C-DMA:13-B43:胆固醇:DSPC)、LNP2(PEG2000-S:13-B43:胆固醇:DSPC或PEG2000-S:18-B6:胆固醇:DSPC)或LNP3(PEG750-C-DLA:18-B6:胆固醇:DSPC)组中的LNP组合物。
在一些方面,本公开的LNP包含选自PEG2000-C-DMA、PEG2000-S和PEG750-C-DLA的PEG脂质。在一些方面,LNP包含PEG脂质,其是PEG2000-C-DMA。在一些方面,LNP包含PEG脂质,其是PEG2000-S。在一些方面,LNP包含PEG脂质,其是PEG750-C-DLA。
在一些方面,本公开的LNP包含可电离脂质,所述可电离脂质是13-B43或18-B6。
在一些方面,可电离脂质是式13-B43的化合物或其盐。此类脂质被描述于例如WO2013/126803(PCT/US2013/027469)中。
在一些方面,可电离脂质是式18-B6的化合物或其盐。
在一些方面,本公开的LNP包含非阳离子脂质。在某些方面,非阳离子脂质是胆固醇、二硬脂酰磷脂酰胆碱(DSPC)或其组合。在一些方面,LNP包含胆固醇。在一些方面,LNP包含二硬脂酰磷脂酰胆碱(DSPC)。在一些方面,LNP包含胆固醇和二硬脂酰磷脂酰胆碱(DSPC)。
在一些方面,本公开的LNP包含(a)PEG脂质(例如,PEG2000-C-DMA、PEG2000-S或PEG750-C-DLA);(b)可电离脂质(13-B43或18-B6);(c)胆固醇;和(d)二硬脂酰磷脂酰胆碱(DSPC)。
在某些方面,本公开的LNP包含的PEG脂质的量为LNP的0.1-4mol%;0.5-4mol%、2-3.5mol%、0.1-2mol%;0.5-2mol%,或1-2mol%。在某些方面,LNP包含的可电离脂质的量为LNP的50-85mol%;50-65mol%,或50-60mol%。在某些方面,LNP包含的非阳离子脂质的量为45-50mol%或多至约50mol%。在某些方面,LNP包含的胆固醇的量为LNP的30-40mol%或30-35mol%。在某些方面,LNP包含的DSPC的量为LNP的3-15mol%或6-12mol%。
在一些方面,本公开的LNP包含(a)1-4mol%PEG脂质(例如,PEG2000-C-DMA、PEG2000-S或PEG750-C-DLA);(b)50-60mol%可电离脂质(13-B43或18-B6);和(c)45-50mol%的非阳离子脂质。
在一些方面,本公开的LNP包含(a)1-4mol%PEG脂质(例如,PEG2000-C-DMA、PEG2000-S或PEG750-C-DLA);(b)50-60mol%可电离脂质(13-B43或18-B6);(c)30-35mol%胆固醇;和(d)6-12mol%二硬脂酰磷脂酰胆碱(DSPC)。
在一些方面,LNP的尺寸为直径约为50-200nm。在一些方面,LNP粒径在约50-150nm、约50-100nm、约50-120nm或约50-90nm的范围内。
LNP制备
本领域技术人员将理解,以下描述仅用于说明目的。本公开的方法适用于广泛的脂质纳米颗粒类型和尺寸。其他颗粒包括胶束、脂质-核酸颗粒、病毒体等。本领域技术人员将知道本公开的方法和装置将适用的其他脂质LNP。
在一个方面,本公开的多核酸构建体的封装方法提供脂质溶液,例如根据良好生产规范(GMP)合成的临床级脂质,然后将其溶解在有机溶液(例如乙醇)中。类似地,治疗性产品(例如有治疗活性的试剂,例如核酸或其他试剂)是根据GMP制备的。之后,将含有缓冲剂(例如柠檬酸或乙醇)的治疗剂溶液(例如mRNA)与溶解在低级链烷醇中的脂质溶液混合以形成脂质体制剂。在本公开的优选方面,在基本上与脂质体的形成同时,治疗剂“被动地包埋”在脂质体中。然而,本领域技术人员将认识到本公开的方法和装置同样适用于在LNP形成之后脂质体的主动包埋或装载。
根据本公开的方法和装置,将脂质和缓冲溶液连续引入混合环境(例如混合室)中的动作导致脂质溶液用缓冲溶液的连续稀释,从而在混合后基本上立即产生脂质体。如本文所用,短语“用缓冲溶液连续稀释脂质溶液”(和变体)通常是指在水合过程中,以足够的力充分快速地稀释脂质溶液以实现LNP产生。通过混合水溶液与有机脂质溶液混合,有机脂质溶液在缓冲(水溶液)溶液的存在下经历连续的逐步稀释以产生脂质体。
在制备溶液(例如脂质溶液和水性治疗剂(例如多核苷酸构建体))之后,使用例如蠕动泵混合器将它们混合在一起。在一个方面,将溶液以基本相等的流速泵送到混合环境中。在某些方面,混合环境包括“T”形的连接器或混合室。在这种情况下,优选地是,流体管线以及因此流动的流体,在“T”形连接器内的窄孔中相遇,因为相对于彼此以大约180°的反向流动。可以使用其他相对引入角度,例如27°至90°以及90°至180°。当溶液流在混合环境中相遇和混合时,脂质LNP基本上立即形成。当包含溶解脂质的有机溶液和水溶液(例如缓冲液)同时连续混合时,会形成脂质LNP。有利且令人惊讶的是,通过混合水溶液和有机脂质溶液,有机脂质溶液经历连续的逐步稀释,基本上立即产生脂质体。泵机制可被配置为向混合环境中提供相等或不同流速的脂质和水溶液,这能够在高级链烷醇环境中产生脂质LNP。
有利地是,如本文提供的用于混合脂质溶液和水溶液的方法和装置,提供了用于在基本上与脂质体形成的同时,在形成的脂质体中的治疗剂的封装,其封装率至少为90-95%。如果需要,本文讨论的进一步处理步骤可用于通过浓缩或稀释样品来靶向特定的mRNA浓度。
在一些方面,形成的LNP具有小于约150nm(例如,约50-90nm)的平均直径,其不需要通过高能过程(例如膜挤出、超声或微流化)进一步缩小尺寸。
在某些方面,当通过与水溶液(例如缓冲液)混合的方式逐步稀释溶解在有机溶剂(例如乙醇)中的脂质时,形成LNP。这种控制的逐步稀释是通过将水性和脂质流在孔(例如T型连接器)中一起混合来实现的。所得的脂质、溶剂和溶质浓度可以在整个LNP形成过程中保持恒定。
在一个方面,使用本公开的方法,通过无梯度的两阶段逐步稀释制备LNP。例如,在第一次逐步稀释中,LNP在高级链烷醇(例如乙醇)的环境(例如约30%至约50%v/v乙醇)中形成。然后可以通过逐步降低链烷醇(例如乙醇)浓度至小于或等于约25%v/v(例如约17%v/v至约25%v/v)的方式来稳定这些LNP。在优选的方面,当水溶液或脂质溶液中存在治疗剂时,在与脂质体形成的同时,封装治疗剂。
在某些方面,可以在100%乙醇中制备脂质原液,然后通过T型连接器在醋酸缓冲液中与mRNA LNP混合。脂质和mRNA原液可以在T型连接器处以400mL/min的流速混合至含有PBS的收集容器中。在一些方面,脂质最初溶解在约40%v/v至约90%v/v,更优选约65%v/v至约90%v/v,且最优选约80%v/v至约90%v/v(A)的链烷醇环境中。接下来,通过与水溶液混合来逐步稀释脂质溶液,导致在约37.5-50%(B)之间的链烷醇(例如乙醇)浓度下的LNP的形成。通过将水溶液与有机脂质溶液混合,有机脂质溶液经历连续的逐步稀释以产生脂质体。此外,可以通过LNP的额外的逐步稀释至小于或等于约25%,优选约15-25%(C)的链烷醇浓度来进一步稳定脂质LNP。
在一些方面,对于两种逐步稀释(A→B和B→C),所得乙醇、脂质和溶质浓度在接收容器中保持在恒定水平。在初始混合步骤之后的这些较高乙醇浓度下,与通过在较低乙醇浓度下稀释形成的LNP相比,脂质单体重排成双层的方式更有序。不受任何特定理论的束缚,据信这些较高的乙醇浓度促进核酸与双分子层中的阳离子脂质的缔合。在某些方面,核酸封装发生在22%以上的链烷醇(例如乙醇)浓度范围内。
在某些方面,在脂质LNP形成之后,它们被收集在另一个容器中,例如不锈钢容器。在一个方面,可以例如以约100-200mL/min的速率进行第二次稀释。
在一个方面,在混合步骤之后,脂质浓度为约1-10mg/mL(例如约7mg/mL),且治疗剂(例如mRNA)浓度为约0.1-4mg/mL。
在混合步骤之后,如果任选地稀释脂质LNP悬浮液,则可以提高治疗剂(例如核酸)的封装程度。例如,在稀释步骤之前,如果治疗剂包埋为约30-40%,则可在稀释步骤之后孵育后增加至约70-80%。在步骤中,通过与例如缓冲液(例如,PBS)的水溶液混合,脂质体制剂被稀释至约10%至约40%,优选约20%链烷醇。这种进一步的稀释优选用缓冲液完成。在某些方面,这种进一步稀释脂质体溶液是连续逐步稀释。然后任选地允许稀释的样品在室温下孵育。
在任选的稀释步骤之后,约70-80%或更多的治疗剂(例如,核酸)被包埋在脂质LNP中。在某些方面,使用了阴离子交换色谱。
在某些情况下,使用例如超滤(例如,切向流透析)的方法,将脂质体溶液任选地浓缩约2-6倍,优选约4倍。在一个方面,将样品转移到超滤系统的进料储库中,并去除缓冲液。也可以使用各种方法(例如超滤)去除缓冲液。
在一些方面,然后渗滤浓缩的制剂以去除链烷醇。步骤完成时的链烷醇浓度小于约1%。优选地,脂质和治疗剂(例如核酸)浓度保持不变并且治疗剂包埋水平也保持恒定。
去除链烷醇后,然后通过用另一种缓冲液渗滤代替水溶液(例如缓冲液)。优选地,脂质与治疗剂(例如核酸)的浓度比例保持不变并且核酸的包埋水平大致恒定。在某些情况下,可以通过用大约10%体积的浓缩样品的缓冲液冲洗柱体来提高样品产量。在某些方面,然后将该冲洗液添加至浓缩样品中。
在某些方面,可以任选地对样品进行无菌过滤。在某些方面,使用胶囊过滤器和带有加热夹套的加压分配容器,在低于约40psi的压力下进行过滤。略微加热样品可以提高过滤的容易程度。
可以使用用于常规脂质体制剂的方法进行无菌填充步骤。在一些方面,本公开的方法导致最终产品中约50-60%的输入治疗剂(例如核酸)。在某些优选的方面,最终产品的治疗剂与脂质的比例约为0.04至0.07。
然后,封装的LNP的制备可以在无菌条件下过滤、等分并在-80℃下储存。
共聚物
在一些方面,本公开的组合物还包含共聚物。在一些方面,本文公开的共聚物是“膜不稳定聚合物”或“膜破坏性聚合物”。膜不稳定聚合物或膜破坏性聚合物可以直接或间接引起细胞膜结构(例如核内体膜)的变化,例如渗透性变化,例如从而允许试剂(例如寡核苷酸或共聚物或两者)都通过这种膜结构。在一些方面,膜破坏性聚合物可以直接或间接引起细胞囊泡的溶解或以其他方式破坏细胞膜,如对于大部分细胞膜中所观察到的。
本文公开的递送剂、共聚物和组合物可用于将本公开的多核苷酸构建体细胞内递送至靶细胞的方法,其中包括体外、离体和体内的靶细胞。在一些方面,将多核苷酸构建体(例如,包含mRNA)递送至靶细胞的方法包括递送至细胞的细胞溶质。
组合物
本文公开的递送剂可以在体外和体内有效地将多核苷酸构建体转运到细胞中。在一些方面,本公开的多核苷酸构建体与递送剂(例如LNP)一起配制。在一些方面,组合物还包含药学上可接受的载体。
本公开的某些方面涉及用于增加细胞中OTC蛋白的量的组合物或方法。在一些方面,包含核酸序列的多核苷酸构建体与LNP和/或共聚物一起配制为组合物,所述核酸序列包含密码子优化的mRNA序列,所述mRNA序列包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF)。在某些方面,mRNA分子编码OTC蛋白,所述OTC蛋白包含与SEQ IDNO:7具有至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或100%序列同一性的氨基酸序列。为了将编码的OTC蛋白引导至细胞的线粒体中,编码OTC蛋白的mRNA分子可包含编码线粒体靶向信号肽的序列(在本文中也称为“线粒体前导序列”)。线粒体前导序列可以是天然OTC蛋白的序列(例如,包含SEQ ID NO:7的残基1-32(天然人线粒体前导序列)),也可以衍生自包含线粒体靶向信号肽的另一种蛋白质或从头合成。可以在线粒体前导序列和多肽的剩余部分之间的连接处引入工程化切割位点以优化细胞中的蛋白水解加工。线粒体前导序列被可操作地连接到编码成熟OTC蛋白的mRNA序列,即,这两个序列以正确的阅读框连接并定位,以将新合成的多肽引导至细胞的线粒体。线粒体前导序列通常位于蛋白质的氨基末端。在特定变体中,具有线粒体前导序列的编码的OTC蛋白具有如SEQ ID NO:7所示的氨基酸序列。编码SEQ ID NO:7的OTC蛋白并且可被配制为本公开的组合物的合适的mRNA序列可包含如SEQ ID NO:1或SEQ ID NO:4中所示的序列。编码SEQ IDNO:7的OTC蛋白并且可被配制为本公开的组合物的合适的mRNA序列可包含如SEQ ID NO:1或SEQ ID NO:4中所示的序列。用于本公开中的制剂的编码OTC的mRNA通常还包括位于其3’末端的Poly(A)(例如,大于80,例如,100至800个腺嘌呤残基的PolyA尾),可使用众所周知的基因工程化技术(例如,通过PCR或酶促Poly-A尾)将其添加到构建体中。可用于插入合适的DNA载体中的示例性DNA序列,用于生产和制备本公开的多核苷酸构建体。
使用方法
本公开的某些方面涉及通过使细胞与包含本文公开的多核苷酸构建体和药学上可接受的稀释剂或载体的组合物接触,来增加细胞中鸟氨酸氨甲酰基转移酶(OTC)的量。在一些方面,多核苷酸构建体与本文公开的LNP一起配制。在其他方面,多核苷酸可以与共聚物一起配制。
一些方面涉及用于增加细胞中OTC表达的量的方法,其包括向细胞施用包含本公开的多核苷酸构建体的组合物,所述细胞是肝细胞。
一种治疗鸟氨酸氨甲酰基转移酶缺乏症(OTCD)的方法,其包括向有此需要的受试者施用治疗有效量的包含本公开的多核苷酸构建体的组合物。
一种用于在患有OTCD的受试者中治疗高氨血症或降低其风险的方法,其包括向有此需要的受试者施用治疗有效量的包含本公开的多核苷酸构建体的组合物。
本公开的其他方面涉及本公开的多核苷酸构建体或本公开的组合物,或本公开的载体,或本公开的宿主细胞在制备用于在有此需要的受试者中治疗OTCD的药物中或在制备用于在患有OTCD受试者中治疗高氨血症或降低其风险的药物中的用途。
可通过本文公开的方法治疗的受试者中与缺陷基因表达和/或活性相关的疾病或病症包括鸟氨酸氨甲酰基转移酶缺乏症(OTCD)。
在某些方面,与缺陷基因表达相关的疾病或病症是以功能性多肽的缺乏为特征的疾病(在本文中也称为“与蛋白质缺乏相关的疾病”)。本公开的递送剂(例如LNP)可以配制为包含信使RNA(mRNA)分子的组合物,所述信使RNA分子编码对应于导致蛋白质缺乏的遗传缺陷的蛋白。对于与蛋白质缺乏相关的疾病的治疗,多核酸构建体(例如,包含mRNA)制剂可被施用于受试者(例如,哺乳动物,例如小鼠、非人灵长类动物或人)以用于将mRNA递送至适当的靶组织,其中mRNA在蛋白质合成过程中被翻译并且所编码的蛋白质的产生量足以治疗疾病。
用于治疗受试者(例如哺乳动物)中与缺陷基因表达和/或活性相关的疾病或病症的方法,例如包括向有此需要的哺乳动物施用治疗有效量的包含核酸序列的多核苷酸构建体,所述核酸序列包含密码子优化的mRNA序列,所述mRNA序列包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),所述多核苷酸构建体与LNP和/或共聚物一起配制成组合物。在某些方面,mRNA分子编码包含与SEQ ID NO:7具有至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或100%序列同一性的氨基酸序列的OTC蛋白。为了将编码的OTC蛋白引导至细胞的线粒体,编码OTC蛋白的mRNA分子可以包含编码线粒体靶向信号肽的序列(在本文中也称为“线粒体前导序列”)。线粒体前导序列可以是天然OTC蛋白的序列(例如,包含SEQ ID NO:7的残基1-32(天然人线粒体前导序列)),也可以衍生自包含线粒体靶向信号肽的另一种蛋白质或从头合成。可以在线粒体前导序列和多肽的剩余部分之间的连接处引入工程化切割位点以优化细胞中的蛋白水解加工。线粒体前导序列被可操作地连接到编码成熟OTC蛋白的mRNA序列,即,这两个序列以正确的阅读框连接并定位,以将新合成的多肽引导至细胞的线粒体。线粒体前导序列通常位于蛋白质的氨基末端。在特定变体中,具有线粒体前导序列的编码的OTC蛋白具有如SEQ ID NO:7所示的氨基酸序列。编码SEQ ID NO:7的OTC蛋白并且可被配制成本公开的组合物的合适的mRNA序列可包含如SEQ ID NO:1或SEQ ID NO:4中所示的序列。编码SEQ ID NO:7的OTC蛋白并且可被配制为本公开的组合物的合适的mRNA序列可包含如SEQ ID NO:1或SEQ ID NO:4中所示的序列。用于本公开中的制剂的编码OTC的mRNA通常还包括位于其3’末端的Poly(A)(例如,大于80,例如,100至800个腺嘌呤残基的Poly-A尾)。
用于治疗与缺陷基因表达相关的疾病或病症的方法的另一个示例包括治疗功能性多肽缺乏的受试者的方法,该方法包括向受试者施用包含至少一种mRNA分子的组合物,所述mRNA分子的至少一部分编码功能性多肽其中施用后功能性多肽的表达高于施用前。在一些方面,mRNA编码功能性鸟氨酸氨甲酰基转移酶(OTC)蛋白。
在特定变体中,包含编码鸟氨酸氨甲酰基转移酶(OTC)蛋白的mRNA的组合物被用于治疗鸟氨酸氨甲酰基转移酶缺乏症(OTCD)的方法。OTCD是一种尿素循环障碍,其可引发高氨血症,这是一种危及生命的疾病,可导致脑损伤、昏迷甚至死亡。这是由于OTC的活性不足所致,OTC是尿素循环中的一种关键酶,其主要产生在肝脏中且负责从体内清除氨。氨是由摄入蛋白质和体内蛋白质分解产生的。在肝脏中,通过尿素循环中的酶将这种氨转化为尿素。尿素是无毒的且通常很容易通过肾脏在尿液中清除。然而,当缺乏OTC酶时,血液中的氨水平会升高,并可导致严重的脑损伤。患有严重OTC缺乏症的患者通常在出生后2-3天被发现,此时患者的血氨水平显著升高并最终陷入昏迷。患有轻度OTC缺乏症的患者在应激期间可出现危机,导致也可能导致昏迷的氨水平升高。目前治疗方法包括用于高氨血症患者的氨清除剂药物(Buphenyl,Ravicti)。
OTC基因是X连锁的。该疾病存在于具有一个突变等位基因的男性中和具有突变等位基因的纯合子或杂合子的女性。具有非常严重OTC缺乏症的男性患者通常在出生后立即被发现。除了血氨水平升高外,尿乳清酸水平也升高。在严重OTC缺乏的患者中,OTC酶活性低于正常水平的2%。在轻度OTC缺乏症患者中,OTC酶活性达到正常水平的30%。
用本公开的多核苷酸构建体或包含本公开的编码OTC的mRNA的组合物治疗OTCD的方法通常包括向患有OTCD的受试者施用治疗有效量的组合物,由此编码OTC的mRNA被递送至肝细胞并在蛋白质合成过程中被翻译以产生OTC蛋白质。编码OTC的mRNA可以是如上文所述的关于用于增加细胞中OTC蛋白的组合物或方法的mRNA。
用于治疗疾病的mRNA组合物的功效可以在疾病的动物模型体内进行评估。例如,用于评估用于治疗OTCD的mRNA组合物的功效的合适动物模型包括已知的具有肝脏中OTC酶缺乏的小鼠模型。一种小鼠模型为Otcspf-ash(稀疏的皮毛且皮肤和毛发异常)小鼠,其包含R129H突变,导致OTC蛋白水平降低,并且肝脏中酶活性只有正常水平的5-10%(参见Hodges等,PNAS 86:4142-4146,1989)。另一种小鼠模型为Otcspf小鼠,其包含H117N突变,导致酶活性水平降低至正常水平的5-10%(参见Rosenberg等,Science 222:426-428,1983)。与野生型的同窝小鼠相比,这两种小鼠模型的尿乳清酸水平均有所升高。第三种用于OTC缺乏的小鼠模型是在Otcspf或Otcspf-ash小鼠中诱导高氨血症(Cunningham等,Mol Ther19(5):854-859,2011)。用OTC siRNA或AAV2/8载体/OTC shRNA处理这些小鼠,以敲低残留的内源性OTC表达和活性。血浆氨水平升高,小鼠约在2-14天死亡。
一旦特定分析物的检测缩小了诊断的可能性,在淋巴细胞或培养的成纤维细胞中测定缺乏酶的活性作为证实试验。对于许多途径,没有单一的酶测定可以建立诊断。对于其他,需要进行补充研究等测试。
在某些方面,治疗的目标是恢复生化和生理的稳态。新生儿可能需要紧急诊断和治疗,这取决于具体的生化病变、代谢阻断的位置和有毒化合物的作用。治疗策略包括:(1)前体氨基酸的饮食限制和(2)使用辅助化合物以(a)处理有毒代谢物或(b)增加缺乏酶的活性。肝移植在少数受影响的个体中取得了成功。即使采用目前的临床管理方法,患有有机酸血症的个体具有更大的感染风险和更高的胰腺炎发病率,这可能是致命的。
在某些方面,本公开的多核苷酸构建体和组合物可用于制备治疗与受试者中缺陷基因表达和/或活性相关的疾病或病症的药物。
本公开的多核苷酸构建体和组合物可以通过多种施用途径施用,例如肠胃外、口服、局部、直肠、吸入等。制剂将根据所选择的施用途径改变。在一些方面,施用途径是静脉内、肌内、皮内、皮下、十二指肠内或腹膜内。
特定情况下适当剂量的确定在本领域技术范围内。本公开的组合物的有效剂量的变化取决于许多不同的因素,其中包括给药方式、靶部位、患者的生理状态、患者是人还是动物、所施用的其他药物以及组合物自身的比活性和其在个体中产生所需应答的能力。通常,患者是人类,但在某些疾病中,患者可以是非人类的哺乳动物。
实施例
实施例1.OTC多核苷酸构建体的制备
通过使用质粒DNA构建体的体外转录(IVT)制备包含SEQ ID NO:4的序列的OTC多核苷酸构建体。质粒DNA构建体包含5’UTR、ORF和3’UTR的指令,而化学修饰(例如假尿苷)是通过向IVT反应中添加所需的核苷酸来确定的。首先,使用5单位的XbaI限制性内切酶/ug质粒DNA对质粒DNA进行线性化切割。在37度孵育过夜后,通过苯酚/氯仿萃取纯化DNA。在37度下,使用T7聚合酶和CleanCap进行除共转录加帽(例如,Cap1)之外的IVT反应3小时。在IVT反应后,通过DNase处理纯化所得mRNA产物,然后进行渗滤。然后,用300单位多聚腺苷酸聚合酶/mg RNA进行酶促多聚腺苷酸化纯化的mRNA,并孵育15至60分钟,具体取决于所需的Poly A长度。然后在调节至所需浓度、无菌过滤和等分之前,通过渗滤和HPLC纯化mRNA产物。
实施例2.Poly(A)尾长度对效力和耐受性的影响
如实施例1所述,用具有可变长度的Poly(A)尾制备OTC mRNA构建体。在第一个实验中,OTC mRNA被转录,粗转录物被用作与预热或预冷的PolyA聚合酶反应的模板。在第二个实验中,OTC mRNA被转录、纯化,并将纯化的转录物用作与预热或预冷的PolyA聚合酶反应的模板。在第三个实验中,确定了产生正确PolyA尾长度的反应时间。
PolyA实验1和2导致所产生的PolyA尾的长度没有显著差异。此外,酶的温度不影响运行性能。在实验1和2中,反应时间为30分钟。在实验3中,测试了45、60和75分钟的反应时间。60和75分钟的反应时间能够产生长度超过300个核苷酸(nts)的PolyA尾。虽然较长的反应时间能够产生较长的尾巴,但反应时间也会影响产品的纯度。
为评估不同Poly(A)尾长度(编码的或酶促的)对效力和耐受性的影响,进行了大鼠重复给药研究。在D0、7和14,将封装在LNP2(PEG2000-S:13-B43:胆固醇:DSPC)中的具有不同Poly(A)尾长度(80、161、208、262、322或440nts)的mRNA的OTC构建体施用于雄性Srague Dawley大鼠(7-8周龄)(表2A)。实验在D1(给药后24小时)或D15(末次给药后24小时)终止。表2B中提供了每种施用的制剂的Z-Avg、PDI和封装率%。所有制剂均通过内部LAL分析测试了内毒素。当0.5mg/mL时,所有制剂均低于2EU/mL。
表2A LNP2制剂的施用和剂量
表2B.LNP2制剂特征
在第一次给药后6小时,分析各种polyA构建体的单核细胞趋化蛋白-1(MCP-1)诱导水平,结果显示在图1中。
为了分析在重复给药后对用含有具有不同polyA尾长度的mRNA的OTC构建体配制的LNP的施用的免疫应答的诱导,在每个给药日给药后6小时取尾戳,并量化大鼠的细胞因子诱导。分析给药后6小时(第0天、第7天和第14天)的单核细胞趋化蛋白-1(MCP-1)诱导水平(图2A)。与具有161、208、262、322或440nt酶促Poly(A)尾的OTC mRNA构建体相比,具有80nts编码的Poly(A)的OTC mRNA产生更高的MCP-1诱导水平。在D0、D7和D14天给药后6小时分析MCP-1和干扰素γ诱导的蛋白10(IP-10)的诱导水平(图2B)。所有应答均与PBS对照组进行比较。与具有大于80个核苷酸的酶促Poly(A)尾的测试OTC mRNA构建体相比,具有80nt编码的Poly(A)尾的OTC mRNA构建体显示出更高的MCP-1(图2A)和IP-10(图2B)诱导。
为了分析OTC蛋白的表达情况,在末次给药后24小时获取大鼠肝脏样品并快速冷冻。与具有大于80个核苷酸的酶促Poly(A)尾的OTC构建体相比,具有80个核苷酸编码的Poly(A)的OTC构建体在肝脏中具有最低的hOTC蛋白表达(图3A和图3B)。
实施例3.经修饰的OTC mRNA构建体
为了评估化学修饰对效力和耐受性的影响,进行一项小鼠研究。通过TriLink方法,使用假尿苷(PsU)、N1-甲基-假尿苷(N1MePsU)或5-甲氧基尿苷(5MoU)(表3A)对实施例1中制备的OTC mRNA(具有~180-480个核苷酸长的PolyA尾范围)进行化学修饰。
将化学修饰的mRNA配制成LNP1或LNP2(PEG2000-S:13-B43:胆固醇:DSPC)(表3B)并施用于小鼠(0.5mg/kg)(表3C)。
表3A.mRNA的化学修饰
表3B.化学修饰的mRNA的LNP制剂
表3C.化学修饰的mRNA的施用
在施用经修饰的OTC mRNA制剂后分析MCP-1水平(图4)。不同的测试的OTC mRNA的化学修饰之间,MCP-1应答没有显著差异。与LNP1相比,LNP2(PEG2000-S:13-B43:胆固醇:DSPC)略微更刺激。
接下来,通过ELISA分析人OTC表达(图5)。两种LNP中OTC mRNA的PsU和N1MePsU修饰之间的OTC表达水平相似。在OTC mRNA 5MoU-LNP治疗的动物中检测到最低的OTC表达。OTC mRNA N1MePsU-LNP1治疗的动物比OTC mRNA PsU-LNP1治疗的动物具有更高的OTC表达。OTC mRNA PsU-LNP2治疗的动物比OTC mRNA N1MePsU治疗的动物具有更高的OTC表达。
实施例4.大鼠中OTC mRNA-LNP耐受性和OTC表达
利用大鼠重复给药研究评估OTC mRNA-PsU效力和耐受性。在LNP1(PEG2000-C-DMA:13-B43:胆固醇:DSPC)、LNP2(PEG2000-S:13-B43:胆固醇:DSPC或PEG2000-S:18-B6:胆固醇:DSPC)或LNP3(PEG750-C-DLA:18-B6:胆固醇:DSPC)中配制OTC mRNA-PsU(0.25mg/kg),并在第0、7和14天施用于大鼠(表4A)。在LNP1中携带EPO和LUC并作为对照组施用。
表4A.OTC mRNA构建体-PsU的施用和给药
表4B中提供了施用的每种制剂的Z-Avg、PDI和封装率%。输入批量大小为3mg。用100mM醋酸、pH5配制LNP并在TFU上进行处理。等分试样储存在-80℃,并在给药的每一天制备测试制品。
表4B.LNP1、LNP2和LNP3制剂特征
为了检测PEG抗体水平,在每个给药日(D0、7和14天)的给药前收集血液。对抗-PEGIgG(图6A)和抗-PEG IgM(图6B)抗体应答进行了量化。在仅用LNP1治疗的大鼠中观察到抗-PEG抗体。测试的OTC mRNA构建体的免疫原性低于EPO和LUC有效载荷。用LNP1产生抗-PEG抗体导致血液清除加速和重复给药后效力丧失(数据未显示)。
为了检测MCP-1的诱导作用,在每次给药后6小时收集血液。在含有与较低免疫原性相关的OTC mRNA构建体的LNP的重复给药后,MCP-1几乎没有增加(图7)。
为了检测OTC表达水平,在每个给药日的给药前收集血液。LNP2制剂是最有效的,而LNP1制剂是效力最差的(图8)。OTC蛋白的积累最高的是LNP2制剂。该数据得到免疫原性数据的支持,该免疫原性数据显示没有抗体产生并且没有加速血液清除。OTC mRNA构建体-LNP2组合物也具有较低的重复给药MCP-1水平。
给药后24小时通过质谱法量化脂质清除率。单剂量研究表明LNP1和LNP2(13-B43)在给药后14天出现,而LNP2(18-B6)和LNP3在给药后6小时明显迅速出现(数据未显示)。OTCmRNA构建体-LNP1或OTC mRNA构建体-LNP2(13-B43)的重复给药导致肝脏中的脂质积累(图9)。即使在重复给药时(所有水平<500ng/g的LLOQ),依旧没有观察到OTC mRNA构建体-LNP2(18-B6)或OTC mRNA构建体-LNP3的积累。
为了分析肝损伤的标志物,量化丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)水平。在给药的第一天和最后一天的24小时收集血清。重复给药(每周施用0.25mg/kgx 3剂;总共0.75mg/kg)后ALT/AST水平没有显著变化(图10A和10B)。第三剂后,与LNP2(18-B6)和LNP3制剂相比,LNP1和LNP2(13-B43)制剂组都具有相对较高的AST。
实施例5.大鼠中单剂量vs.重复剂量的脂质清除
评估单次和重复剂量施用OTC mRNA构建体-LNP后的脂质清除。在LNP2(PEG2000-S:13-B43:胆固醇:DSPC)中配制OTC mRNA,并以0.25mg/kg/剂施用于大鼠。对于单次剂量,在D0向大鼠施用制剂,终止时间点为给药后30分钟、1小时、3小时、6小时和24小时(表5A)。在D0施用高单剂量(2mg/kg),终止时间点为D1。对于重复给药,每7天向大鼠施用一次制剂,持续最多49天(第7、14、21、28、35、42和49天)。第8次治疗后(第49天)在给药后30分钟、1小时、3小时、6小时和24小时(第50天)收集终止时间点。在D0、7、14、21、28、35、42和49施用PBS(5mL/kg)作为对照。表5B中提供了所给予的每种制剂的Z-Avg、PDI和封装率%。
表5A.OTC mRNA构建体-LNP2的单次和重复给药
表5B.OTC mRNA构建体-LNP2(13-B43)制剂特征
为了测量细胞因子应答,在所有终止时间点收集血液。测量的细胞因子是MCP-1、IP-10和巨噬细胞炎症蛋白1α(MIP-1α)。每周重复给药0.25mg/kg时,没有产生细胞因子应答(图11A-11C)。2mg/kg的单剂量给药后,产生显著的细胞因子应答。
为了检测PEG和OTC抗体水平,在每次给药前收集血液。重复施用后,抗PEG IgM水平没有增加的趋势(图12)。类似地,重复施用OTC mRNA构建体-LNP2后,抗-PEG IgG水平没有增加(图13)。重复施用后,未检测到抗-OTC IgM抗体(图14)。同样,对于重复施用OTCmRNA构建体-LNP2,未检测到抗-OTC IgG抗体(图15)。
在每次给药后24小时,在肝脏中也检测到hOTC(图16)。在治疗1或8(第49天)后,随着时间(30分钟、1小时、3小时、6小时和24小时)量化肝脏和血浆中的OTC mRNA水平(图17A和17B)。
实施例6.SD大鼠中的单剂量范围探索研究
接下来是在采用SD大鼠的剂量响应研究中评估用OTC mRNA构建体配制的LNP1(PEG2000-C-DMA:13-B43:胆固醇:DSPC)、LNP2(PEG2000-S:13-B43:胆固醇:DSPC)和LNP2(PEG2000-S:18-B6:胆固醇:DSPC)的效力和耐受性。以不同浓度(0.5mg/kg、1mg/kg或1.5mg/kg)向大鼠施用OTC mRNA构建体-LNP2并在6小时或24小时进行分析(表6A)。作为对照,一些大鼠被施用5mL/kg PBS、1.5mg/kg LNP1或1.5mg/kg LNP2。表6B中提供了被施用的每种制剂的Z-Avg、PDI和封装率%。
表6A.LNP1和LNP2的剂量响应研究
表6B.用于剂量范围研究的LNP制剂
为了分析对肝脏损伤,在末次给药后24小时收集肝脏样本,并分析ALT、AST、GGT和总胆红素水平。与空载相比,mRNA LNP的ALT/AST水平更高(图18A-18D和表7)。随着LNP1、LNP2(13-B43)或LNP2(18-B6)的剂量增加,ALT/AST水平有升高的趋势。1.5mg/kg LNP2(13-B43)的施用诱导的ALT/AST水平高于相同量的LNP1。
表7.施用不同量LNP2的大鼠的ALT和AST水平
分析末次给药后24小时采集的样品中GGT和总胆红素的水平。随着LNP1或LNP2OTC mRNA制剂剂量的增加,GGT和总胆红素水平有增加的趋势(图19A-19D)。与相同量的OTCmRNA构建体-LNP1相比,1.5mg/kg OTC mRNA构建体-LNP2(13-B43)的施用诱导了相似水平的GGT。与相同量的OTC mRNA构建体-LNP1相比,1.5mg/kg OTC mRNA构建体-LNP2的施用诱导了更高水平的总胆红素。
从末次给药后24小时的采集的血液中获得全血细胞计数。与被施用1.5mg/kg OTCmRNA构建体-LNP2(13-B43)的大鼠相比,被施用1.5mg/kg OTC mRNA构建体-LNP1的大鼠具有相似数量的中性粒细胞、单核细胞和血小板(图20A-20C)。OTC mRNA构建体-LNP2的剂量的增加会增加中性粒细胞的量,但会减少单核细胞和血小板的量。
为了检测细胞因子水平,在给药后6小时收集血液,并对MCP-1、MIP-1α和IP-10的水平进行量化。空载和OTC mRNA构建体-LNP组合物之间的MCP-1和MIP-1α水平没有显著差异(图21A-21C)。与空载相比,LNP1和LNP2 OTC mRNA制剂诱导更高水平的IP-10。对于施用OTC mRNA构建体-LNP2(13-B43),细胞因子水平也呈现剂量依赖性增加。
在末次给药后24小时通过蛋白质印迹检测hOTC表达。随着OTC mRNA构建体-LNP2(13-B43)剂量的增加,OTC表达出现剂量依赖性增加(图22)。与1.5mg/kg的OTC mRNA构建体-LNP1相比,1.5mg/kg的OTC mRNA构建体-LNP2(13-B43)提供了更高的OTC表达。
实施例7.非人灵长类动物剂量范围研究
在非人灵长类动物(NHP)的剂量响应研究中评估了用OTC mRNA构建体配制的LNP1(PEG2000-C-DMA:13-B43:胆固醇:DSPC)的效力。OTC mRNA构建体包括:具有5’的核苷酸序列、开放阅读框和SEQ ID NO:4的3’序列、长度为80个核苷酸至440个核苷酸(即284个核苷酸)的polyA尾,并且是假尿苷(ψ)修饰的。在不同的三天中(第1、8和15天),以不同浓度(0.25mg/kg、1mg/kg、3mg/kg或5mg/kg)向非人灵长类动物施用一剂量的OTC mRNA构建体-LNP1(表8)。在第16天分析结果。作为对照,向非人灵长类动物施用5mg/kg空载LNP1。
表8.用于非人灵长类动物剂量范围研究的LNP制剂
在第16天,在非人灵长类动物肝脏样本中分析了人OTC表达。相对于内源性表达,用0.25mg/kg剂量检测到最低OTC表达,并且用3mg/kg剂量检测到最高表达(图23A)。在最低剂量(0.25mg/kg)时实现初始目标hOTC表达(8%)。
为了检测细胞因子水平,在第1天,第一次给药后6小时收集样品并分析MCP-1和IL-6的水平(图23B和23C)。在0.25mg/kg剂量中未检测到MCP-1和IL-6。在3mg/kg剂量下观察到MCP-1和IL-6的短暂升高。
这些结果表明具有低免疫刺激的高hOTC表达。
因此,公开了各个方面。上述实施方式和其他实施方式均在所附权利要求的范围内。本领域的技术人员将理解,本公开可以用于不同于所公开的方面。所公开的方面是出于说明而非限制的目的而呈现的,并且本公开仅由所附权利要求限制。
Claims (38)
1.一种多核苷酸构建体,其从5’至3’包含:
(a)5’UTR,其包含SEQ ID NO:2的序列;
(b)mRNA序列,其包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),其中ORF包含与SEQ ID NO:1至少约95%相同的密码子优化的序列;和
(c)3’UTR,其包含SEQ ID NO:3的序列。
2.一种包含mRNA序列的多核苷酸构建体,所述mRNA序列包含编码功能性人鸟氨酸氨甲酰基转移酶(OTC)的开放阅读框(ORF),其中所述mRNA序列包含具有不超过五个不同于SEQID NO:4的核酸的序列。
3.根据权利要求2所述的多核苷酸构建体,其从5’至3’包含:
(a)5’UTR;
(b)mRNA序列,其包含编码OTC的ORF;和
(c)3’UTR。
4.根据权利要求3所述的多核苷酸构建体,其中所述5’UTR包含SEQ ID NO:2的序列。
5.根据权利要求3或4所述的多核苷酸构建体,其中所述3’UTR包含SEQ ID NO:3的序列。
6.根据权利要求1-5中任一项所述的多核苷酸构建体,其中所述功能性OTC包含SEQ IDNO:7的氨基酸序列。
7.根据权利要求1-6中任一项所述的多核苷酸构建体,其中所述OFR序列包含SEQ IDNO:1。
8.根据权利要求1-7中任一项所述的多核苷酸构建体,其中所述mRNA序列具有不超过四个、三个、两个或一个不同于SEQ ID NO:4的核酸。
9.根据权利要求1-8中任一项所述的多核苷酸构建体,其包含SEQ ID NO:4的序列。
10.根据权利要求1-9中任一项所述的多核苷酸构建体,其还包含5’末端帽子。
11.根据权利要求10所述的多核苷酸构建体,其中所述5’末端帽子是Cap1。
12.根据权利要求1-11中任一项所述的多核苷酸构建体,其还包含polyA尾。
13.根据权利要求12所述的多核苷酸构建体,其中所述polyA尾是80至1000个核酸长。
14.根据权利要求12所述的多核苷酸构建体,其中所述polyA尾是100至500个核酸长。
15.根据权利要求1-14中任一项所述的多核苷酸构建体,其中所述mRNA包含至少一个化学修饰的尿苷。
16.根据权利要求15所述的多核苷酸构建体,其中所述尿苷的至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约95%或约100%被化学修饰。
17.根据权利要求15或16所述的多核苷酸构建体,其中所述化学修饰的尿苷选自假尿苷(ψ)、N1-甲基假尿苷(N1-me-ψ)及其组合。
18.一种组合物,其包含:
(a)根据权利要求1-17中任一项所述的多核苷酸构建体;和
(b)递送剂。
19.根据权利要求18所述的组合物,其中所述递送剂包括脂质纳米颗粒(LNP)、脂质体、聚合物、胶束、质粒、病毒或其任何组合。
20.根据权利要求19所述的组合物,其中所述LNP选自下组:PEG2000-C-DMA:13-B43:胆固醇:DSPC、PEG2000-S:13-B43:胆固醇:DSPC、PEG2000-S:18-B6:胆固醇:DSPC和PEG750-C-DLA:18-B6:胆固醇:DSPC。
21.根据权利要求19或20所述的组合物,其中所述多核苷酸构建体被封装在所述LNP中。
22.根据权利要求21所述的组合物,其中所述多核苷酸构建体被完全封装在所述LNP中。
23.根据权利要求22所述的组合物,其中所述多核苷酸构建体的至少95%被封装在所述LNP中。
24.根据权利要求18-23中任一项所述的组合物,其还包含药学上可接受的载体。
25.一种用于增加细胞中OTC表达的量的方法,其包括向细胞施用包含根据权利要求1-17中任一项所述的多核苷酸构建体,或根据权利要求18-24中任一项所述的组合物。
26.根据权利要求25所述的方法,其中所述细胞是肝细胞。
27.一种用于治疗或减轻与鸟氨酸氨甲酰基转移酶缺乏症(OTCD)相关的症状的方法,其包括向有此需要的受试者施用治疗有效量的包含根据权利要求1-17中任一项所述的多核苷酸构建体的组合物或根据权利要求18-24中任一项所述的组合物。
28.一种用于在患有OTCD的受试者中治疗高氨血症或降低其风险的方法,其包括向有此需要的受试者施用治疗有效量的包含根据权利要求1-17中任一项所述的多核苷酸构建体的组合物或根据权利要求18-24中任一项所述的组合物。
29.一种表达盒,其包含与SEQ ID NO:8具有至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或100%序列同一性的序列。
30.根据权利要求29所述的表达盒,其还包含启动子。
31.根据权利要求30所述的表达盒,其中所述启动子为T7启动子。
32.一种质粒,其包含根据权利要求29-31中任一项所述的表达盒。
33.一种宿主细胞,其包含根据权利要求29-31中任一项所述的表达盒,或根据权利要求32所述的质粒。
34.根据权利要求1-17中任一项所述的多核苷酸构建体,或根据权利要求18-24中任一项所述的组合物,或根据权利要求29-31中任一项所述的表达盒,或根据权利要求32所述的质粒,或根据权利要求33所述的宿主细胞在制备用于在有此需要的受试者中治疗OTCD的药物中的用途。
35.根据权利要求1-17中任一项所述的多核苷酸构建体,或根据权利要求18-24中任一项所述的组合物,或根据权利要求29-31中任一项所述的表达盒,或根据权利要求32所述的质粒,或根据权利要求33所述的宿主细胞在制备用于在患有OTCD的受试者中治疗高氨血症或用于降低其风险的药物中的用途。
36.一种用于核酸的体内递送的方法,所述方法包括:
向哺乳动物受试者施用根据权利要求1-17中任一项所述的多核苷酸构建体,或根据权利要求18-24中任一项所述的组合物,或根据权利要求29-31中任一项所述的表达盒,或根据权利要求32所述的质粒,或根据权利要求33所述的宿主细胞。
37.一种用于在有此需要的哺乳动物受试者中治疗疾病或病症的方法,所述方法包括:
向所述哺乳动物受试者施用治疗有效量的根据权利要求1-17中任一项所述的多核苷酸构建体,或根据权利要求18-24中任一项所述的组合物,或根据权利要求29-31中任一项所述的表达盒,或根据权利要求32所述的质粒,或根据权利要求33所述的宿主细胞。
38.根据权利要求37所述的方法,其中所述疾病或病症是尿素循环障碍。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962924567P | 2019-10-22 | 2019-10-22 | |
| US62/924,567 | 2019-10-22 | ||
| PCT/US2020/056890 WO2021081225A1 (en) | 2019-10-22 | 2020-10-22 | Ornithine transcarbamylase (otc) constructs and methods of using the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116096428A true CN116096428A (zh) | 2023-05-09 |
Family
ID=75620841
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202080089266.1A Pending CN116096428A (zh) | 2019-10-22 | 2020-10-22 | 鸟氨酸氨甲酰基转移酶(otc)构建体及其使用方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20230001021A1 (zh) |
| EP (1) | EP4048317A4 (zh) |
| JP (1) | JP2022553375A (zh) |
| CN (1) | CN116096428A (zh) |
| AU (1) | AU2020371697A1 (zh) |
| CA (1) | CA3158626A1 (zh) |
| IL (1) | IL292420A (zh) |
| WO (1) | WO2021081225A1 (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112021006539A2 (pt) | 2018-10-09 | 2021-07-06 | Univ British Columbia | composições e sistemas competentes de vesículas competentes para transfecção isentas de solventes e detergentes orgânicos e métodos relacionados às mesmas |
| EP4330404A1 (en) * | 2021-04-28 | 2024-03-06 | Genevant Sciences Gmbh | Mrna delivery constructs and methods of using the same |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2919828C (en) * | 2013-07-30 | 2022-07-19 | Phaserx, Inc. | Block copolymers and their conjugates or complexes with oligonucleotides |
| CN114642735A (zh) * | 2015-01-21 | 2022-06-21 | 菲泽尔克斯公司 | 用于将治疗剂和诊断剂递送到细胞中的方法、组合物和系统 |
| CN109312313A (zh) * | 2016-06-13 | 2019-02-05 | 川斯勒佰尔公司 | 用于治疗鸟氨酸转氨甲酰酶缺乏症的信使rna疗法 |
| US11938197B2 (en) * | 2017-01-10 | 2024-03-26 | The Sydney Children's Hospitals Network (Randwick And Westmead (Incorporating The Royal Alexandra Hospital For Children) | Polynucleotides and vectors for the expression of transgenes |
| JP7423522B2 (ja) * | 2017-11-22 | 2024-01-29 | モダーナティエックス・インコーポレイテッド | 尿素サイクル異常症の治療のためのオルニチントランスカルバミラーゼをコードするポリヌクレオチド |
-
2020
- 2020-10-22 US US17/771,421 patent/US20230001021A1/en active Pending
- 2020-10-22 AU AU2020371697A patent/AU2020371697A1/en active Pending
- 2020-10-22 JP JP2022523854A patent/JP2022553375A/ja active Pending
- 2020-10-22 CA CA3158626A patent/CA3158626A1/en active Pending
- 2020-10-22 CN CN202080089266.1A patent/CN116096428A/zh active Pending
- 2020-10-22 WO PCT/US2020/056890 patent/WO2021081225A1/en unknown
- 2020-10-22 IL IL292420A patent/IL292420A/en unknown
- 2020-10-22 EP EP20878326.6A patent/EP4048317A4/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP4048317A4 (en) | 2023-11-22 |
| JP2022553375A (ja) | 2022-12-22 |
| WO2021081225A1 (en) | 2021-04-29 |
| US20230001021A1 (en) | 2023-01-05 |
| CA3158626A1 (en) | 2021-04-29 |
| IL292420A (en) | 2022-06-01 |
| EP4048317A1 (en) | 2022-08-31 |
| AU2020371697A1 (en) | 2022-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20190321295A1 (en) | Method of Encapsulating a Nucleic Acid in a Lipid Nanoparticle Host | |
| CN110114058B (zh) | 用于递送mrna的改进的基于ice的脂质纳米颗粒制剂 | |
| JP6990176B2 (ja) | メッセンジャーリボ核酸薬物の治療投与のための方法 | |
| US10155945B2 (en) | Method of producing lipid nanoparticles for drug delivery | |
| JP6442551B2 (ja) | 薬物送達用の脂質ナノ粒子の生成方法 | |
| EP3060257B1 (en) | Lipid formulations for delivery of messenger rna | |
| JP2007112768A (ja) | 肝指向性リポソーム組成物 | |
| CN116096428A (zh) | 鸟氨酸氨甲酰基转移酶(otc)构建体及其使用方法 | |
| US20230263819A1 (en) | Lipid Composition and Use Thereof for Delivery of a Therapeutically Active Agent to Endothelium | |
| EP4268808A1 (en) | Lipid nanoparticles comprising mannose or uses thereof | |
| EP4330404A1 (en) | Mrna delivery constructs and methods of using the same | |
| WO2023009499A1 (en) | Polynucleotides encoding glucose-6-phosphatase for the treatment of glycogen storage disease type 1a (gsd1a) | |
| WO2023287751A1 (en) | Polynucleotides encoding propionyl-coa carboxylase alpha and beta subunits for the treatment of propionic acidemia | |
| CN115025247A (zh) | 包载促血小板生成素mRNA的组合物及其用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |