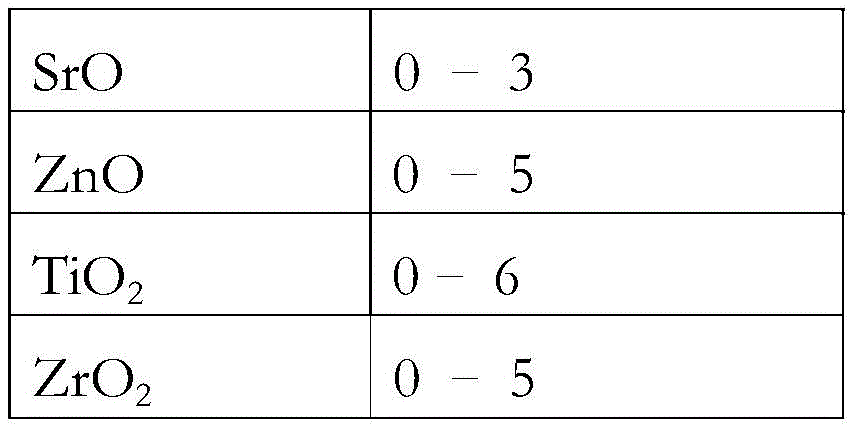CN115771994A - 玻璃陶瓷及用于生产玻璃陶瓷的方法 - Google Patents
玻璃陶瓷及用于生产玻璃陶瓷的方法 Download PDFInfo
- Publication number
- CN115771994A CN115771994A CN202211100581.7A CN202211100581A CN115771994A CN 115771994 A CN115771994 A CN 115771994A CN 202211100581 A CN202211100581 A CN 202211100581A CN 115771994 A CN115771994 A CN 115771994A
- Authority
- CN
- China
- Prior art keywords
- glass
- ceramic
- melt
- fining
- oxygen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000002241 glass-ceramic Substances 0.000 title claims abstract description 165
- 238000004519 manufacturing process Methods 0.000 title claims description 17
- 239000011521 glass Substances 0.000 claims abstract description 82
- 238000000034 method Methods 0.000 claims abstract description 79
- 238000007670 refining Methods 0.000 claims abstract description 22
- 238000002844 melting Methods 0.000 claims abstract description 21
- 230000008018 melting Effects 0.000 claims abstract description 20
- 239000000155 melt Substances 0.000 claims description 75
- 229910052760 oxygen Inorganic materials 0.000 claims description 63
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 60
- 239000001301 oxygen Substances 0.000 claims description 60
- 239000006025 fining agent Substances 0.000 claims description 55
- 238000006243 chemical reaction Methods 0.000 claims description 51
- 239000000203 mixture Substances 0.000 claims description 49
- 230000036961 partial effect Effects 0.000 claims description 39
- 239000000446 fuel Substances 0.000 claims description 18
- 239000002994 raw material Substances 0.000 claims description 17
- 230000002829 reductive effect Effects 0.000 claims description 17
- 239000006060 molten glass Substances 0.000 claims description 16
- 238000010438 heat treatment Methods 0.000 claims description 14
- 229910006404 SnO 2 Inorganic materials 0.000 claims description 12
- 238000002485 combustion reaction Methods 0.000 claims description 11
- 229910018072 Al 2 O 3 Inorganic materials 0.000 claims description 6
- 229910018068 Li 2 O Inorganic materials 0.000 claims description 6
- 229910004298 SiO 2 Inorganic materials 0.000 claims description 6
- 239000000470 constituent Substances 0.000 claims description 6
- 229910052700 potassium Inorganic materials 0.000 claims description 6
- 229910010413 TiO 2 Inorganic materials 0.000 claims description 5
- 230000003647 oxidation Effects 0.000 claims description 5
- 238000007254 oxidation reaction Methods 0.000 claims description 5
- 229910052708 sodium Inorganic materials 0.000 claims description 5
- 229910052684 Cerium Inorganic materials 0.000 claims description 4
- 229910052785 arsenic Inorganic materials 0.000 claims description 4
- 239000007858 starting material Substances 0.000 claims description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 20
- 239000000156 glass melt Substances 0.000 description 15
- 239000003795 chemical substances by application Substances 0.000 description 13
- 238000005352 clarification Methods 0.000 description 11
- 239000008395 clarifying agent Substances 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 6
- 238000010923 batch production Methods 0.000 description 6
- 238000010924 continuous production Methods 0.000 description 6
- 230000001419 dependent effect Effects 0.000 description 6
- 239000007789 gas Substances 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 238000001816 cooling Methods 0.000 description 4
- 239000013078 crystal Substances 0.000 description 4
- 238000002425 crystallisation Methods 0.000 description 4
- 230000008025 crystallization Effects 0.000 description 4
- 239000002803 fossil fuel Substances 0.000 description 4
- 238000000265 homogenisation Methods 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000001393 microlithography Methods 0.000 description 3
- -1 naF Substances 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 238000004040 coloring Methods 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 238000007571 dilatometry Methods 0.000 description 2
- 238000007599 discharging Methods 0.000 description 2
- 238000005868 electrolysis reaction Methods 0.000 description 2
- 230000002349 favourable effect Effects 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 238000001459 lithography Methods 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 229910001404 rare earth metal oxide Inorganic materials 0.000 description 2
- 230000035484 reaction time Effects 0.000 description 2
- 238000004611 spectroscopical analysis Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 229910015902 Bi 2 O 3 Inorganic materials 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 229910005793 GeO 2 Inorganic materials 0.000 description 1
- 229910008556 Li2O—Al2O3—SiO2 Inorganic materials 0.000 description 1
- 229910017493 Nd 2 O 3 Inorganic materials 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229910006406 SnO 2 At Inorganic materials 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 229910000272 alkali metal oxide Inorganic materials 0.000 description 1
- 229910000287 alkaline earth metal oxide Inorganic materials 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 238000002468 ceramisation Methods 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- 239000012459 cleaning agent Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 150000002222 fluorine compounds Chemical class 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 238000005305 interferometry Methods 0.000 description 1
- 230000016507 interphase Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000005398 lithium aluminium silicate glass-ceramic Substances 0.000 description 1
- 238000003754 machining Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000010309 melting process Methods 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 239000013081 microcrystal Substances 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 230000006911 nucleation Effects 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 239000013307 optical fiber Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000003303 reheating Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000007711 solidification Methods 0.000 description 1
- 230000008023 solidification Effects 0.000 description 1
- 238000000411 transmission spectrum Methods 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C1/00—Ingredients generally applicable to manufacture of glasses, glazes, or vitreous enamels
- C03C1/004—Refining agents
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03B—MANUFACTURE, SHAPING, OR SUPPLEMENTARY PROCESSES
- C03B32/00—Thermal after-treatment of glass products not provided for in groups C03B19/00, C03B25/00 - C03B31/00 or C03B37/00, e.g. crystallisation, eliminating gas inclusions or other impurities; Hot-pressing vitrified, non-porous, shaped glass products
- C03B32/02—Thermal crystallisation, e.g. for crystallising glass bodies into glass-ceramic articles
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03B—MANUFACTURE, SHAPING, OR SUPPLEMENTARY PROCESSES
- C03B5/00—Melting in furnaces; Furnaces so far as specially adapted for glass manufacture
- C03B5/16—Special features of the melting process; Auxiliary means specially adapted for glass-melting furnaces
- C03B5/225—Refining
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03B—MANUFACTURE, SHAPING, OR SUPPLEMENTARY PROCESSES
- C03B5/00—Melting in furnaces; Furnaces so far as specially adapted for glass manufacture
- C03B5/16—Special features of the melting process; Auxiliary means specially adapted for glass-melting furnaces
- C03B5/235—Heating the glass
- C03B5/2353—Heating the glass by combustion with pure oxygen or oxygen-enriched air, e.g. using oxy-fuel burners or oxygen lances
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C10/00—Devitrified glass ceramics, i.e. glass ceramics having a crystalline phase dispersed in a glassy phase and constituting at least 50% by weight of the total composition
- C03C10/0018—Devitrified glass ceramics, i.e. glass ceramics having a crystalline phase dispersed in a glassy phase and constituting at least 50% by weight of the total composition containing SiO2, Al2O3 and monovalent metal oxide as main constituents
- C03C10/0027—Devitrified glass ceramics, i.e. glass ceramics having a crystalline phase dispersed in a glassy phase and constituting at least 50% by weight of the total composition containing SiO2, Al2O3 and monovalent metal oxide as main constituents containing SiO2, Al2O3, Li2O as main constituents
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C2204/00—Glasses, glazes or enamels with special properties
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Geochemistry & Mineralogy (AREA)
- Ceramic Engineering (AREA)
- Crystallography & Structural Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Combustion & Propulsion (AREA)
- Physics & Mathematics (AREA)
- Thermal Sciences (AREA)
- Glass Compositions (AREA)
Abstract
本发明涉及一种用于熔融和澄清玻璃、玻璃陶瓷或可陶瓷化成玻璃陶瓷的玻璃的方法以及一种根据该方法生产的玻璃或一种根据该方法生产的玻璃陶瓷。
Description
技术领域
本发明涉及一种用于生产玻璃陶瓷的方法以及一种玻璃陶瓷。
背景技术
在玻璃陶瓷的生产过程中,需要使用大量的能量,以便能够达到生产所需的高温。
在此,特别提及熔融非玻璃质起始材料的步骤以及后续的澄清步骤。这主要适用于低膨胀和零膨胀的玻璃陶瓷,其在间歇工艺在几天内生产。
目前,该工艺所需的能量主要从化石燃料获得。然而,出于生态原因,期望转向更环保的能源或扩大环保技术的比例,以减少与生产相关的CO2排放。
同样出于生态原因,需要在澄清过程中以更少的程度使用多价氧化物。对于关键的澄清剂、例如Sb2O3和As2O3尤其如此。
如上所述,在玻璃和玻璃陶瓷的生产过程中,通常在熔融后进行澄清过程。此外,由此应从玻璃熔体中去除在熔融过程中例如由于基于碳酸盐或氢氧化物的原材料的分解而形成的CO2和H2O气泡。在玻璃生产的澄清阶段,玻璃熔体中的气泡会变大,使得其可以上升并且通过表面离开熔体。
在传统的澄清过程中,在熔槽熔融的一部分中、使得在熔槽熔融的澄清部分中或者在下游区域、如澄清室中将玻璃熔体加热至高的温度。如果熔体含有澄清剂,则会释放澄清气体、例如O2。澄清气体扩散至存在的气泡中并且将这些气泡扩大至这样的程度,使得这些气泡可以在熔体中上升并离开熔体。
对于一些经典的澄清剂、例如多价氧化物澄清剂Sb2O5和As2O5,如今适用法律规定是为了不使用或仅以环保方式使用这些澄清剂,但也有客户要求减少这种澄清剂的使用。
可接受的环保澄清剂、如SnO2在过高的浓度会对某些玻璃性质、例如透射率和结晶敏感性产生不利影响。
发明内容
因此,本发明的目的是提供一种这样的方法。
在第一方面,本发明涉及一种用于生产玻璃陶瓷的方法,包括以下步骤
-提供原材料的混合物,
-加热混合物直至获得熔体,其中将混合物至少部分地加热至高于T3的温度,T3对应于103dPa*s的熔融玻璃粘度,
-澄清熔体,其中将熔体至少部分地加热至高于T2.5的温度,T2.5对应于102.5dPa*s的熔融玻璃粘度,和
-获得澄清的可陶瓷化成玻璃陶瓷的玻璃,
-将可陶瓷化成玻璃陶瓷的玻璃陶瓷化,
其中在借助H2和O2燃烧的加热下进行熔融和/或澄清。
在第二方面,本发明涉及一种通过根据本发明的方法生产的玻璃陶瓷。
在第三方面,本发明涉及一种玻璃陶瓷,其中通过生产绿色玻璃,释放的CO2少于500kg/吨玻璃、优选地少于100kg/吨玻璃。
在第四方面,本发明涉及一种精密组件,其包括根据本发明的玻璃陶瓷和/或根据本发明的方法生产的玻璃陶瓷。
在第五方面,本发明涉及根据本发明的精密组件的用途。
定义和方法
“气泡”是玻璃或玻璃熔体内的气态夹杂物,其直径通常为至少10μm。在此,“直径”是指球当量直径。如果在本说明书中提及气泡的“尺寸”,则是指球当量直径。在本说明书中,术语“气泡”既可以理解为广义上的气态夹杂物,也可以理解为特殊含义上的“CO2气泡”或“O2气泡”。
“氧气与燃料当量比λ”定义了燃料完全反应或转化为燃烧产物、如H2O、CO2或NOx所需的氧气量。与此相应地,λ=1.00是化学计量的,其中富燃料混合物λ<1.00,贫燃料混合物具λ>1.00。因此,λ>1.00的贫燃料混合物能够借助过量(多余)氧气实现燃料的完全转化。
当本说明书涉及与固体或液体相关的“ppm”时,应理解为“质量/重量”;就气体而言,“ppm”是指“体积/体积”。。
“停留时间”是玻璃熔体的特定部分在其从特定容器或局部容器(例如熔融器或澄清器)中移出之前在连续过程中在特定容器或局部容器中保留的时间。“最短停留时间”是玻璃熔体的特定部分在以最快路径通过容器或局部容器时在连续过程中在容器或局部容器中保留的时间。“平均停留时间”定义为“(部分)容器容积[m3]”与“(部分)容器吞吐量[m3h-1]”之间的比。
“澄清时间”是玻璃熔体的特定部分在其从特定容器或局部容器(例如澄清器)中移除之前在间歇过程中用于澄清目的而在容器或局部容器中保留的时间。在此,熔体至少部分地具有高于T2.5的温度,T2.5对应于102.5dPa*s的熔融玻璃粘度。
在第一方面,本发明涉及一种用于生产玻璃陶瓷的方法,包括以下步骤
-提供原材料的混合物,
-加热混合物直至获得熔体,其中将混合物至少部分地加热至高于T3的温度,T3对应于103dPa*s的熔融玻璃粘度,
-澄清熔体,其中将熔体至少部分地加热至高于T2.5的温度,T2.5对应于102.5dPa*s的熔融玻璃粘度,和
-获得澄清的可陶瓷化成玻璃陶瓷的玻璃,
-将可陶瓷化成玻璃陶瓷的玻璃陶瓷化,
其中在借助H2和O2燃烧的加热下进行熔融和/或澄清。
根据本发明,在借助H2和O2燃烧的加热下进行该方法。在该方法的一实施例中,通过H2和O2燃烧提供该方法所需能量的至少10%、至少25%、至少50%、至少75%、至少90%或至少99%。
在该方法的一实施例中,进行加热混合物直至获得熔体的步骤,其中将混合物至少部分地加热至高于T3的温度,T3对应于103dPa*s的熔融玻璃粘度,其中将混合物最多加热至温度T2.5,T2.5对应于102.5dPa*s的熔融玻璃粘度。
在该方法的一实施例中,进行加热混合物直至获得熔体的步骤,其中将混合物至少部分地加热至高于T7.6的温度,T7.6对应于107.6dPa*s的粘度的温度。在该方法的一优选的实施例中,进行加热混合物直至获得熔体的步骤,其中将整个混合物加热至高于T7.6的温度。
在该方法的一实施例中,进行澄清熔体的步骤,其中将熔体至少部分地加热至高于T2.5的温度,T2.5对应于102.5dPa*s的熔融玻璃粘度,其中优选地将熔体至少加热至温度T2.2,T2.2对应于102.2dPa*s的熔融玻璃粘度,和/或其中将熔体最多加热至温度T2,T2对应于102dPa*s的熔融玻璃粘度。
在一实施例中,在借助H2和O2燃烧的加热下进行该方法,其中由H2O的电解提供至少50%、至少80%、至少90%或至少99%的H2和O2。优选地,通过可再生能源为H2O的电解供能。这是有利的,因为这最小化对环境的影响,避免使用化石燃料,进而减少CO2的排放。
在一实施例中,以氧气与燃料当量比λ小于1.05进行该方法。在经济地使用氧气、即氧气可以(几乎)完全反应方面,这是特别有利的。在一实施例中,以氧气与燃料当量比λ为至少1.00进行该方法。同样有利的是,保持低的额外氧气输入,以在澄清熔体期间促进氧分压p(O2)的降低。
在一实施例中,本发明涉及一种方法,其中在借助H2和O2燃烧的加热下进行熔融和/或澄清,其中以氧气与燃料当量比λ>1.00、特别是>1.05进行熔融和/或以氧气与燃料当量比λ<1.05、特别是<1.00进行澄清。
这样的方法是有利的,因为其利用了熔融期间氧气与燃料当量比λ>1.00的(上述)优点并结合了澄清期间氧气与燃料当量比λ<1.00、特别是<1.05的优点,特别是在澄清阶段保持低的额外氧气输入,以便在澄清熔体期间促进氧分压p(O2)的降低。
与通过化石燃料和O2燃烧借助加热进行熔融和/或澄清的传统工艺相比,由于燃烧不完全,在熔融期间无法以氧气与燃料当量比λ约>1.00工作。作为不完全燃烧的结果,CO和/或C的输入导致熔体和工艺设备中许多不期望的问题。如果在氧气与燃料的当量比λ<1.05、特别是<1.00进行澄清,则在使用化石燃料加热时,所述缺点具有更大的影响。
在本发明的一实施例中,玻璃陶瓷为透明的玻璃陶瓷、优选地Li2O-Al2O3-SiO2(LAS)玻璃陶瓷。
根据本发明的一个方面,提供一种LAS玻璃陶瓷,其在0至50℃范围的平均热膨胀系数CTE为至多0.1×10-6/K,即零膨胀LAS玻璃陶瓷。
根据本发明的一个方面,提供一种LAS玻璃陶瓷,其在0至50℃范围的平均热膨胀系数CTE为至少0.001×10-6/K、至少0.005×10-6/K或至少0.01×10-6/K。
根据本发明,玻璃陶瓷是指具有结晶相和玻璃相的无机无孔材料,其中基质、即连续相通常为玻璃相。为了生产玻璃陶瓷,首先将玻璃陶瓷的组分混合、熔融和澄清,然后例如将如此获得的玻璃熔体、即可陶瓷化成玻璃陶瓷的玻璃、即所谓的绿色玻璃浇铸至模具中。在冷却和凝固之后,通过再加热以受控的方式使可陶瓷化成玻璃陶瓷的玻璃结晶(所谓的“受控的体积结晶”)。可陶瓷化成玻璃陶瓷的玻璃和由其制成的玻璃陶瓷的化学成分(分析)是相同的,陶瓷化仅改变材料的内部结构。因此,在下文述及玻璃陶瓷的成分时,上述内容同样适用于玻璃陶瓷的前体、即可陶瓷化成玻璃陶瓷的玻璃或绿色玻璃。
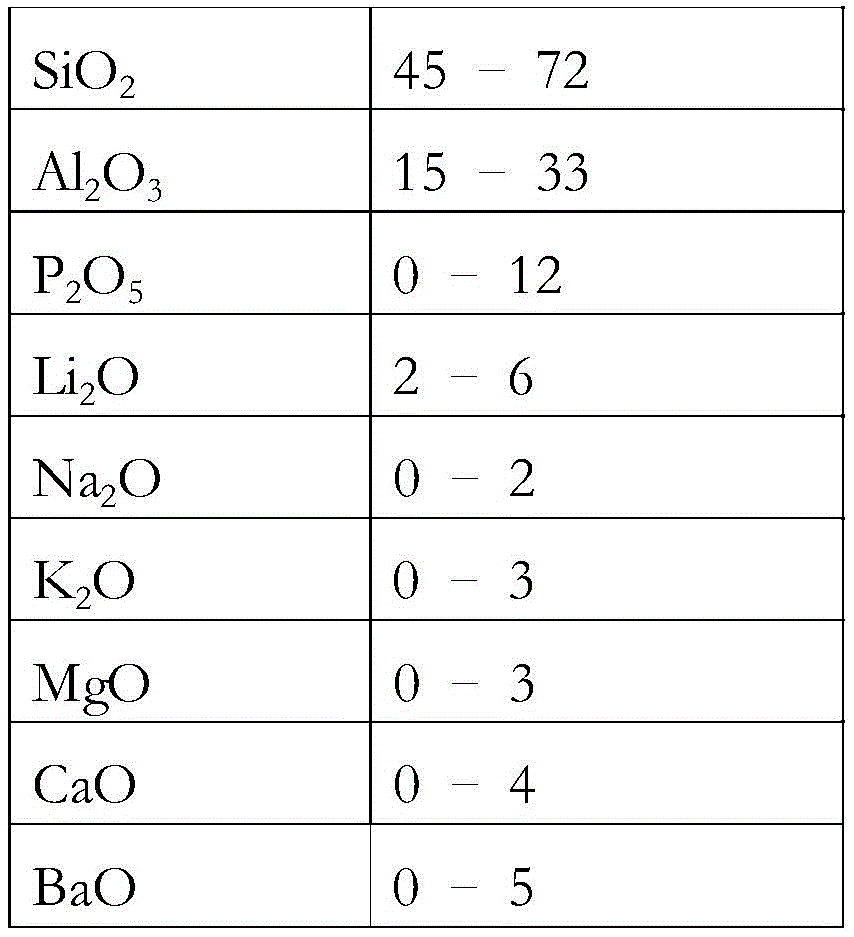
在一实施例中,可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷包括以下成分(基于氧化物的wt%):
| SiO<sub>2</sub> | 35–72,优选地45-72 |
| Al<sub>2</sub>O<sub>3</sub> | 15–33 |
| P<sub>2</sub>O<sub>5</sub> | 0–12 |
| Li<sub>2</sub>O | 2–6 |
| Na<sub>2</sub>O | 0–2 |
| K<sub>2</sub>O | 0–3 |
| MgO | 0–3 |
| CaO | 0–4 |
| BaO | 0–5 |
| SrO | 0–3 |
| ZnO | 0–8 |
| TiO<sub>2</sub> | 1–6 |
| ZrO<sub>2</sub> | 0–5 |
在一实施例中,可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷包括以下成分(基于氧化物的wt%):
在另一实施例中,可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷包括以下成分(基于氧化物的wt%):
| SiO<sub>2</sub> | 50–70 |
| Al<sub>2</sub>O<sub>3</sub> | 17–32 |
| P<sub>2</sub>O<sub>5</sub> | 3–12 |
| Li<sub>2</sub>O | 2–5 |
| Na<sub>2</sub>O | 0–2 |
| K<sub>2</sub>O | 0–2 |
| MgO | 0–2 |
| CaO | 0–4 |
| BaO | 0–5 |
| SrO | 0–2 |
| ZnO | 0–4 |
| TiO<sub>2</sub> | 0–5 |
| ZrO<sub>2</sub> | 0–5 |
玻璃陶瓷优选地具有35wt%至72wt%的SiO2。SiO2更优选地为至多62wt%、更优选地至多60wt%。SiO2更优选地为至少45wt%、更优选地至少50wt%、更优选地至少54wt%。
Al2O3优选地为15wt%至33wt%。玻璃陶瓷更优选地包含至少17wt%、优选地至少20wt%、甚至更优选地至少22wt%的Al2O3。Al2O3更优选地为至多32wt%,更优选地至多28wt%。
玻璃陶瓷的磷酸盐含量P2O5为0wt%至12wt%。玻璃陶瓷更优选地包含至少3wt%、更优选地至少4wt%、甚至更优选地至少5wt%的P2O5。P2O5优选地限制为至多10wt%,更优选地至多8wt%。
玻璃陶瓷优选地还包含0wt%至6wt%、优选地至少1wt%、优选地至少1.5wt%的TiO2。然而,TiO2优选地限制为至多4wt%,更优选地至多3wt%。
玻璃陶瓷还可以包含至多5wt%、优选地至多4wt%的ZrO2。ZrO2优选地以至少0.5wt%、更优选地至少1wt%的比例存在。
此外,玻璃陶瓷可以包含碱金属氧化物、如Li2O、Na2O和K2O。Li2O优选地以至少2wt%、优选地至少3wt%的比例存在。Li2O优选地限制为至多6wt%、更优选地至多5wt%、更优选地至多4wt%。Na2O和K2O可选地存在于玻璃陶瓷中。Na2O优选地以至多2wt%、优选地至多1wt%的比例存在。K2O优选地为至多3wt%、优选地至多2wt%、最优选地至多1wt%。Na2O和K2O在任何情况都可以彼此独立以至少0.01wt%、优选地至少0.02wt%、更优选地至少0.05wt%的比例存在于玻璃陶瓷中。
玻璃陶瓷还可以包含碱土金属氧化物、如MgO、CaO、BaO和/或SrO以及其他二价金属、如ZnO。CaO优选地为至多4wt%、更优选地至多3wt%、甚至更优选地至多2wt%。玻璃陶瓷优选地包含至少0.1wt%、更优选地至少0.5wt%的CaO。MgO可以以至多3wt%、优选地至多2wt%和/或优选地至少0.1wt%的比例存在于玻璃陶瓷中。玻璃陶瓷可以包含小于5wt%、优选地至多4wt%和/或优选地至少0.1wt%的BaO。在个别实施例中,玻璃陶瓷不含BaO。玻璃陶瓷可以包含至多3wt%和/或优选地至少0.1wt%的SrO。在个别实施例中,玻璃陶瓷不含SrO。玻璃陶瓷优选地包含优选至少1wt%、更优选地至少1.5wt%的ZnO作为另外的金属氧化物。ZnO限制为至多8wt%、优选地至多5wt%、优选地至多4wt%。一些实施例不含ZnO。
为了调制光学特性、如折射率,在一些有利的变体中例如可以包含Gd2O3、Y2O3、HfO2、Bi2O3和/或GeO2。
上述玻璃组合物可以可选地添加着色氧化物、例如Nd2O3、Fe2O3、CoO、NiO、V2O5、MnO2、CuO、CeO2、Cr2O3、稀土氧化物,含量分别或总共为0-3wt%。优选的变体不含着色氧化物。
在一些实施例中,根据本发明的玻璃陶瓷包含1.5wt%至6wt%的至少一种选自由TiO2、ZrO2、Ta2O5、Nb2O5、SnO2、MoO3和WO3组成的组的组分。
根据本发明一有利的实施例,组合物不含上文未提及的组分。
根据本发明的一实施例,生产透明的玻璃陶瓷。由于透明性,可以更好地评估这种玻璃陶瓷的许多特性、当然特别是其内部质量。根据本发明的玻璃陶瓷是透明的,即其在350至650nm的波长范围具有至少70%的内部透射率。B2O3和/或更高含量的氟会降低透明度。因此,有利的变体不包含上述组分中的一个或两个。
此外,在本发明范围内生产的玻璃陶瓷是无孔的和无裂纹的。在本发明的范围中,“无孔的”是指孔隙率小于1%、优选地小于0.5%、更优选地小于0.1%。裂纹是在连续的结构中的间隙、即不连续性。
热膨胀系数CTE
根据本发明生产的玻璃陶瓷是零膨胀的,即在特别是0至50℃的范围其平均热膨胀系数CTE为至多0.1×10-6/K。一些有利的变体在特别是0至50℃的范围甚至具有至多0.05×10-6/K的平均CTE。对于特定应用有利的是,在更大的温度范围、例如在-30℃至+70℃的范围、优选地在-40℃至+80℃的范围平均CTE为至多0.1×10-6/K,即零应变。
为了确定根据本发明生产的玻璃陶瓷和由其制成的精密组件的CTE-T曲线,首先确定微分CTE(T)。微分CTE(T)确定为温度的函数。然后根据以下公式(1)定义CTE:
为了创建Δl/l0-T曲线或应变曲线或者描绘测试样品(玻璃陶瓷或精密组件)相对于温度的长度变化Δl/l0,可以测量测试样品从初始温度t0的初始长度l0到温度t的长度lt的温度相关长度变化。在此,优选地选择小的温度间隔、例如5℃或3℃或1℃来确定测量点。例如,可以通过膨胀测定法、干涉测量法(如法布里-珀罗法、即分析耦合到材料中的激光束的谐振峰的偏移)或者通过其他合适的方法进行这类测量。在本发明的范围内,在选择的长度100mm且直径6mm的棒状测试样品上以1℃的温度间隔进行膨胀测定法来确定CTE。所选择的用于确定CTE的方法具有优选地至少±0.05ppm/K、优选地至少±0.03ppm/K的精度。当然也可以使用具有至少±0.01ppm/K、优选地至少±0.005ppm/K或根据一些实施例甚至至少±0.003ppm/K或至少±0.001ppm/K的精度的方法来确定CTE。根据Δl/l0-T曲线,计算对于例如0到50℃温度范围在特定温度间隔的平均CTE。通过推导Δl/l0-T曲线获得CTE-T曲线。根据CTE-T曲线可以确定温度间隔内CTE-T曲线的过零和斜率。通过CTE-T曲线确定在一些变体中形成的有利的CTE平台的类型和位置。
根据一实施例,通过根据本发明的方法生产的玻璃陶瓷组件中的一个是具有高CTE均匀性的精密组件(特别是基板形式)。在此,CTE均匀性(CTE的总空间变化)的值是指所谓的峰谷值,即取自精密组件的样品的相应最高CTE值与相应最低CTE值之间的差。因此,CTE均匀性并非指组件材料的CTE,而是指在所考虑的局部或整个精密组件上CTE的空间变化。为了确定CTE均匀性,从精密组件的不同位置取得多个样品并分别确定CTE值,单位为ppb/K,其中1ppb/K=0.001×10-6/K。CTE均匀性、即CTE的空间变化在整个精密组件上有利地为至多5ppb/K、优选地至多4ppb/K、最优选地至多3ppb/K。在WO2015/124710A中描述了一种确定CTE均匀性的方法以及实现CTE均匀性的措施,其公开内容全部并入本申请中。
另一方面,本发明涉及一种精密组件,其包含根据本发明的方法生产的玻璃陶瓷或根据本发明的玻璃陶瓷。
另一方面涉及根据本发明的精密组件的用途,特别是用于计量学、光谱学、测量技术、光刻、天文学或从宇宙进行地球观测,例如用作分段或单片天文望远镜的镜片或镜架,或者用作例如用于太空望远镜的轻质或超轻镜面基底,或者用作用于例如在太空中进行距离测量的高精度结构部件或用于地球观测的光学器件,作为精密组件,例如用于精密测量技术的标准、精密测量杆、干涉仪中的基准板,作为机械精密零件,例如用于环形激光陀螺仪、用于钟表行业的螺旋弹簧,用作例如LCD光刻中的镜片和棱镜,以及例如用作微光刻和EUV微光刻中的掩模支架、晶片工作台、基准板、参考框架和网格板以及用作EUV微光刻中的镜片和/或光掩模衬底或光掩模基板。
在一实施例中,根据本发明的方法允许在保持优秀的产品质量的同时减少所需的多价氧化物澄清剂的量。根据本发明的方法通过增加由澄清剂释放的O2的量进而在相应所需的澄清温度提高所使用的澄清剂的转化率实现上述情形。因此,根据本发明的方法借助少量的所使用的澄清剂实现了改善的澄清、即仅具有少量气泡的玻璃或玻璃陶瓷。
在一实施例中,在根据本发明的方法中,基于原材料的混合物的总质量,以2wt%或更低的浓度使用至少一种化学式XnOm的澄清剂,其中n=1或2,其中m=2或5,其中X=As、Sb、Sn或Ce,和/或至少一种化学式MnSO4的澄清剂,其中n=1或2,并且M=Na、K、Li、Mg、Ca、Sr、Ba和/或Zn。替代地或另外地,基于原材料的混合物的总质量,以2wt%或更低的浓度使用一种或多种澄清剂,和/或基于原材料的混合物的总质量,以至少0.05wt%、至少0.1wt%或至少0.2wt%的浓度使用一种或多种澄清剂。在一实施例中,基于原材料的混合物的总质量,以0.05wt%至2wt%、0.1wt%至1wt%或0.2wt%至0.5wt%的浓度使用一种或多种澄清剂。
在该方法的一实施例中,使用两种或多种澄清剂的组合,其中两种或多种澄清剂选自化学式XnOm的化合物的组合,其中n=1或2,其中m=2或5,其中X=As、Sb、Sn或Ce,和/或化学式MnSO4的化合物的组合,其中n=1或2,并且M=Na、K、Li、Mg、Ca、Sr、Ba和/或Zn。如果使用两种或多种澄清剂的组合,则在此所做的说明相应地适用于这些澄清剂的组合。
在一实施例中,使用选自氯化物和氟化物列表的额外澄清剂,如NaCl、KCl、NaF、KF。
在一实施例中,澄清剂具有热力学性质,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,从较高氧化态至较低氧化态的至少30%的澄清剂转化率、或者至少35%澄清剂转化率、至少40%澄清剂转化率、至少45%澄清剂转化率或至少50%澄清剂转化率,特别是根据反应XnOm→XnOm-1+1/2O2和/或XnOm→XnOm-2+O2和/或根据反应MnSO4→mnO+SO2+1/2O2,其中温度T2对应于102dPa*s的熔融玻璃粘度。在一实施例中,澄清剂具有热力学性质,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,至多99%的澄清剂转化率、至多95%的澄清剂转化率、至多90%的澄清剂转化率或至多80%的澄清剂转化率,特别是根据反应XnOm→XnOm-1+1/2O2和/或XnOm→XnOm-2+O2和/或根据反应MnSO4→mnO+SO2+1/2O2,其中温度T2对应于102dPa*s的熔融玻璃粘度。澄清剂的转化率受各种因素影响、例如熔体的温度和熔体中的氧分压。在此,在1bar的氧分压p(O2)和温度T2,给定澄清剂的相应转化率(单位为%)与化学平衡条件相关。例如,根据反应XnOm→XnOm-1+1/2O2,至少30%的转化率意味着,基于XnOm和XnOm-1的总物质的量,在化学平衡时存在至少30mol%的还原形态XnOm-1。上述说明优选地作如下理解:在熔体中1bar的氧分压和温度T2,澄清剂具有转化率程度的热力学性质并不表征任何方法步骤,而是澄清剂在假设的熔融条件下的性质。这优选地并不意味着熔体必须在特定时间点处于T2温度和/或必须存在1bar的氧分压。相反,这个特征优选描述了澄清剂在特定条件下的行为。因此,其根据熔体的成分规定了澄清剂的选择规则。可以实验地确定澄清剂的这个性质。实际进行的方法步骤和实际存在的条件必须与此区分开来。因此,可以如在此所述影响澄清剂的实际转化率,特别是可以通过降低氧分压来提高转化率。
在一实施例中,以足够长的时间进行该方法并且特别是澄清步骤,使得在1bar的氧分压p(O2)和温度T2,在熔体中发生至少30%、至少35%、至少40%或至少45%的澄清剂转化率。如果使用多种澄清剂的混合物,则这意味着为至少30%、至少35%、至少40%或至少45%的转化率的总转化率(单位为mol%),其与所使用的澄清剂的摩尔分数的总和相关。
这意味着在化学平衡时,基于还原和氧化形态的总物质的量,存在至少30mol%的所有还原形态的总和。在此,本领域技术人员能够理论地评估并且计量学地测定和确认所需的时间(参见例如图3),其是在温度T2下澄清剂的期望转化率所需的。该时间可以对应于在连续过程中熔体在澄清器或澄清区域中2至18小时的平均停留时间。类似地,该时间可以对应于间歇过程中2至96小时的澄清时间。
在一实施例中,根据本发明的方法包括在澄清熔体期间调节氧分压p(O2)的步骤,基于温度T3下熔体中的O2饱和度,氧分压降低至少60%、优选地至少70%。熔体中的O2饱和度和在澄清熔体期间降低的氧分压p(O2)与相应设定温度下的化学平衡条件相关。
在一实施例中,该方法的特征在于,在澄清熔体期间调节氧分压p(O2),基于温度T3下熔体中的O2饱和度,氧分压降低至少60%、优选地至少70%(参见例如图2)。熔体中的O2饱和度和在澄清熔体期间降低的氧分压p(O2)与相应设定温度下的化学平衡条件相关。在此,对温度T3下熔体中的O2饱和度的引用仅用作参考值。这并不意味着必须在该温度下实际达到平衡状态。例如可以通过调节适当选择的温度和/或使用小的氧气与燃料当量比λ来实现这个方法特征。替代地或另外地,例如可以通过在玻璃熔体上方的区域中使用0.5bar或更低、0.4bar或更低、0.3bar或更低、0.2bar或更低、0.1bar或更低或0.05bar或更低的绝对压力来实现这个方法特征。然而,在澄清期间熔体上方的绝对压力优选地为至少0.5bar。
基于温度T3下熔体中的O2饱和度,玻璃熔体中的氧分压p(O2)降低至少60%、优选地至少70%,导致根据反应XnOm→XnOm-1+1/2O2和/或XnOm→XnOm-2+O2或者根据反应MnSO4→MnO+SO2+1/2O2的相应平衡向有利于产物方向、即有利于还原的澄清剂并产生O2移动。
在一实施例中,使用化学式XnOm的澄清剂,其中n=1或2,其中m=2或5,其中X=As、Sb、Sn或Ce。在一实施例中,使用化学式MnSO4的澄清剂,其中n=1或2,并且M=Na、K、Li、Mg、Ca、Sr、Ba和/或Zn。在一既依赖又独立于其的实施例中,基于原材料的混合物的总质量,以2wt%或更低的浓度使用澄清剂,和/或基于原材料的混合物的总质量,以至少0.05wt%、至少0.1wt%或至少0.2wt%的浓度使用澄清剂。在一实施例中,基于原材料的混合物的总质量,以0.05wt%至2wt%、0.1wt%至1wt%或0.2wt%至0.5wt%的浓度使用澄清剂。
在一实施例中,选择具有热力学性质的澄清剂,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,根据反应XnOm→XnOm-1+1/2O2和/或XnOm→XnOm-2+O2和/或根据反应MnSO4→mnO+SO2+1/2O2,具有至少30%、至少35%、至少40%、至少45%或至少50%的澄清剂转化率,其中温度T2对应于102dPa*s的熔融玻璃粘度。在一实施例中,选择具有热力学性质的澄清剂,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,根据反应XnOm→XnOm-1+1/2O2和/或XnOm→XnOm-2+O2和/或根据反应MnSO4→mnO+SO2+1/2O2,具有至多99%、至多95%、至多90%或至多80%的澄清剂转化率,其中温度T2对应于102dPa*s的熔融玻璃粘度。
在该方法的一实施例中,该方法包括调节玻璃熔体中的氧分压p(O2)的步骤,基于温度T3下熔体中的O2饱和度,氧分压降低至少60%、优选地至少70%、优选地至少80%。在该方法的一实施例中,该方法包括调节玻璃熔体中的氧分压p(O2)的步骤,基于温度T3下熔体中的O2饱和度,氧分压降低至多99%、优选地至多95%或至多90%。在该方法的一实施例中,该方法包括调节玻璃熔体中的氧分压p(O2)的步骤,基于温度T3下熔体中的O2饱和度,氧分压降低60%至99%、优选地70%至95%或80%至90%。
在一实施例中,可陶瓷化成玻璃陶瓷的玻璃中或玻璃陶瓷中Fe2+与Fe3+之比为至少0.01、至少0.02或至少0.05。在一实施例中,可陶瓷化成玻璃陶瓷的玻璃中或玻璃陶瓷中Fe2+与Fe3+之比为至多1.00、至多0.50、至多0.20或至多0.10。在一实施例中,可陶瓷化成玻璃陶瓷的玻璃中或玻璃陶瓷中Fe2+与Fe3+之比为0.01至1.0、0.02至0.50或0.05至0.20或0.05至0.10。该方法有利于由相应所使用的澄清剂释放氧气,进而允许在可陶瓷化成玻璃陶瓷的玻璃中或玻璃陶瓷中就待达到的Fe2+与Fe3+之比来调节期望的氧化还原比。该方法特别是有利于还原条件,根据原始的Fe2+与Fe3+之比,还原条件使平衡向有利于Fe2+移动,从而改善澄清结果。
在一实施例中,既涉及该方法又涉及玻璃陶瓷,在(澄清的)可陶瓷化成玻璃陶瓷的玻璃中,XnOm-1与XnOm之比或XnOm-2与XnOm之比为至少0.6、至少0.7、至少0.8、至少1.0或至少2.0。在一实施例中,在(澄清的)可陶瓷化成玻璃陶瓷的玻璃中,XnOm-1与XnOm之比或XnOm-2与XnOm之比为至多99.0、至多90.0、至多50.0、至多10.0或至多5.0。在一实施例中,在(澄清的)可陶瓷化成玻璃陶瓷的玻璃中,XnOm-1与XnOm之比或XnOm-2与XnOm之比为0.6至99.0、0.7至90.0、0.8至50.0、1.0至10.0或2.0至5.0。该方法有利于由相应所使用的澄清剂释放氧气,进而允许在(澄清的)可陶瓷化成玻璃陶瓷的玻璃中调节相应使用的澄清剂的还原形式与氧化形式之间预期的或期望的比。
在一实施例中,澄清剂选自Na2SO4、K2SO4、Li2SO4、MgSO4、CaSO4、SrSO4、ZnSO4、Sb2O5、As2O5、CeO2和SnO2的列表或其混合物。。
在原材料的混合物中,开始时通常以其最低氧化态提供澄清剂Sb2O5、As2O5、CeO2和SnO2。例如,原材料的混合物中的澄清剂Sb2O5和As2O5通常以Sb2O3和As2O3的形式提供。以重量百分数(wt%)表示的信息是指相应澄清剂Sb2O5、As2O5、CeO2和SnO2的所有氧化和还原形态的总和,因此包括Sb2O3、As2O3、CeO和SnO。
在一实施例中,澄清剂为SnO2,特别地,澄清剂为SnO2,并且基于原材料的混合物的总质量以0.05wt%至2wt%、0.1wt%至1wt%或0.2wt%至0.5wt%的浓度使用澄清剂。
在一实施例中,澄清剂为As2O5,特别地,澄清剂为As2O5,并且基于原材料的混合物的总质量以0.05wt%至2wt%、0.1wt%至1wt%或0.2wt%至0.5wt%的浓度使用澄清剂。
在一实施例中,澄清剂为Sb2O5,特别地,澄清剂为Sb2O5,并且基于原材料的混合物的总质量以0.05wt%至2wt%、0.1wt%至1wt%或0.2wt%至0.5wt%的浓度使用澄清剂。
在一实施例中,澄清剂为Na2SO4,特别地,澄清剂为Na2SO4,并且基于原材料的混合物的总质量以0.05wt%至2wt%、0.1wt%至1wt%或0.2wt%至0.5wt%的浓度使用澄清剂。
在一实施例中,通过根据本发明的方法生产的玻璃陶瓷具有良好的内部质量。
优选地,玻璃陶瓷具有至多5个夹杂物/100cm3、更优选地至多3个夹杂物/100cm3、最优选地至多1个夹杂物/100cm3。根据本发明,夹杂物是指气泡和微晶、优选地直径大于0.3mm的气泡。根据本发明的一个变体,提供玻璃陶瓷或由其制成的精密组件,其具有至多800mm的直径或边缘长度和至多100mm的厚度,并且具有至多5个/100cm3、优选地至多3个/100cm3、更优选地至多1个/100cm3直径大于0.03mm的夹杂物。除了夹杂物的数量之外,检测到的夹杂物的最大直径也可以作为内部质量的量度。在直径小于500mm的精密组件的总体积中,单个夹杂物的最大直径优选地为至多0.6mm,对于应用的关键体积、例如表面附近,优选地为至多0.4mm。在直径500mm至小于2m的玻璃陶瓷组件中,单个夹杂物的最大直径优选地为至多3mm,对于应用的关键体积、例如表面附近,优选地为至多1mm。
在一实施例中,(澄清的)可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷(以下称为“玻璃陶瓷”)具有每10kg玻璃陶瓷少于80个尺寸0.03mm至0.05mm的气泡和/或每10kg玻璃陶瓷少于80个尺寸0.05mm至0.1mm的气泡和/或每10kg玻璃陶瓷少于80个尺寸0.1mm至0.2mm的气泡和/或每10kg玻璃陶瓷少于2个尺寸大于0.2mm的气泡。
在一实施例中,(澄清的)可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷具有每10kg玻璃陶瓷少于80个尺寸0.03mm至0.05mm的气泡、每10kg玻璃陶瓷少于40个尺寸0.03mm至0.05mm的气泡、每10kg玻璃陶瓷少于10个尺寸0.03mm至0.05mm的气泡、每10kg玻璃陶瓷少于5个尺寸0.03mm至0.05mm的气泡或每10kg玻璃陶瓷少于2个尺寸0.03mm至0.05mm的气泡。
在一实施例中,(澄清的)可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷具有每10kg玻璃陶瓷少于80个尺寸0.05mm至0.1mm的气泡、每10kg玻璃陶瓷少于40个尺寸0.05mm至0.1mm的气泡、每10kg玻璃陶瓷少于10个尺寸0.05mm至0.1mm的气泡、每10kg玻璃陶瓷少于5个尺寸0.05mm至0.1mm的气泡或每10kg玻璃陶瓷少于2个尺寸0.05mm至0.1mm的气泡。
在一实施例中,(澄清的)可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷具有每10kg玻璃陶瓷少于80个尺寸0.1mm至0.2mm的气泡、每10kg玻璃陶瓷少于40个尺寸0.1mm至0.2mm的气泡、每10kg玻璃陶瓷少于10个尺寸0.1mm至0.2mm的气泡、每10kg玻璃陶瓷少于5个尺寸0.1mm至0.2mm的气泡或每10kg玻璃少于2个尺寸0.1mm至0.2mm的气泡和/或每10kg玻璃少于2个尺寸大于0.2mm的气泡。
在一实施例中,(澄清的)可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷具有每10kg玻璃少于0.1个尺寸0.1mm至0.2mm的气泡或每10kg玻璃少于0.5个尺寸0.1mm至0.2mm的气泡和/或每10kg玻璃少于0.1个尺寸大于0.2mm的气泡。
对每10kg玻璃特定数量气泡的引用同样适用于10kg玻璃陶瓷或10kg可陶瓷化成玻璃陶瓷的玻璃,并且应作类似理解。此外,每10kg玻璃特定数量气泡的特性并非是指玻璃陶瓷或可陶瓷化成玻璃陶瓷的玻璃必须具有10kg的质量。10kg的参考质量仅用于以比较的方式确定不同质量的玻璃陶瓷或可陶瓷化成玻璃陶瓷的玻璃中的气泡数量。
气泡的尺寸指的是气泡的直径。对于非球形气泡,尺寸是指跨视场的最短距离与最长距离之间的平均值。
在一实施例中,间歇地进行该方法。这是有利的,特别是结合H2和O2的燃烧,因为这允许以此方式延长澄清阶段,使得可以随着在澄清熔体期间提高澄清剂转化率而特别好地控制和调节氧分压p(O2)的降低。
在该方法的一实施例中,在间歇过程中的澄清时间为至少2小时、至少8小时、至少16小时或至少24小时,但至多96小时、至多72小时或至多48小时。在该方法的一实施例中,在间歇过程中澄清时间为2至96小时、8至72小时、16至72小时或24至48小时。
在间歇过程中调整特定的澄清持续时间允许足够的反应时间或所使用的澄清剂充分的转化率以及(与此同时)由熔体充分释放O2并调节所基于的化学平衡。特别地,这意味着(玻璃)熔体中所使用的澄清剂的还原形式与氧化形式之间的化学平衡以及玻璃熔体中的氧分压p(O2)与玻璃熔体上方的氧分压p(O2)之间的化学平衡(依赖于温度)。
在该方法的一实施例中,以连续过程进行澄清,其中熔体在澄清期间的平均停留时间为至少2小时、至少4小时、至少6小时或至少8小时。然而,熔体在澄清期间的平均停留时间为至多18小时、至多16小时、至多14小时或至多12小时。在该方法的一实施例中,以连续过程进行澄清,其中熔体在澄清期间的平均停留时间为2至18小时、4至16小时、6至14小时或8至12小时。
在连续过程中调整熔体在澄清期间的特定平均停留时间能够实现足够的反应时间或所使用的澄清剂充分的转化率以及(与此同时)由熔体充分释放O2并调节所基于的化学平衡。特别地,这意味着熔体中所使用的澄清剂的还原形式与氧化形式之间的化学平衡以及熔体中的氧分压p(O2)与熔体上方的氧分压p(O2)之间的化学平衡(依赖于温度)。
在另一方面,本发明涉及一种根据前述方法可生产或生产的玻璃陶瓷。
在另一方面,本发明涉及一种玻璃陶瓷,其中通过生产绿色玻璃,释放的CO2少于500kg/吨玻璃、优选地少于250kg/吨玻璃、更优选地少于100kg/吨玻璃、更优选地小于50kg/吨玻璃、特别是优选地少于10kg/吨玻璃。
在玻璃陶瓷或可陶瓷化成玻璃陶瓷的玻璃的一实施例中,玻璃或玻璃陶瓷具有中和的CO2平衡。
在一实施例中,根据本发明的玻璃陶瓷具有至少0.01的Fe2+与Fe3+之比,其中玻璃陶瓷具有每10kg玻璃陶瓷少于80个尺寸0.03mm至0.05mm的气泡和/或少于80个尺寸0.05mm至0.1mm的气泡和/或每10kg玻璃陶瓷少于80个尺寸0.1mm至0.2mm的气泡和/或每10kg玻璃陶瓷少于2个尺寸大于0.2mm的气泡。结合根据本发明的玻璃陶瓷,类似地适用于根据本发明的生产方法产生的实施例。
有利地,借助电流进行H2O的电解,其具有中和的CO2平衡。
在本发明的范围内,产生电流视为中和的CO2平衡,其中产生电流不会增加存在的CO2总量。因此,通过太阳能、风能、水力和/或核能产生的电流视为具有中和的CO2平衡的电流。
在玻璃陶瓷或可陶瓷化成玻璃陶瓷的玻璃的一实施例中,玻璃包括澄清剂XnOm,其具有热力学性质,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,由澄清剂释放至多30%、至多20%或至多10%的O2。
附图说明
图1示出了在可陶瓷化成玻璃陶瓷的玻璃中澄清剂Sb2O3、As2O3和SnO2与温度相关的氧释放。
图2示出了可陶瓷化成玻璃陶瓷的玻璃的借助SnO2澄清的熔体的氧分压p(O2)的曲线。
图3示出了在SnO2澄清的玻璃陶瓷中基于锡总量、即SnO和SnO2的SnO含量(mol%)与熔融和澄清过程的温度和时间的关系。
具体实施方式
图1示出了在可陶瓷化成玻璃陶瓷的玻璃中澄清剂Sb2O3、As2O3和SnO2与温度相关的氧释放。
图2示出了借助SnO2澄清的玻璃陶瓷的氧分压p(O2)的曲线。如果借助氧化物澄清剂来达到玻璃的澄清温度,则熔体的p(O2)通常为约1bar。在此,将一部分氧化物澄清剂从氧化态转化为还原态。p(O2)曲线从1600℃变平,并且从1650℃,p(O2)曲线几乎恒定在1bar左右。从1700℃的温度,由于与大气进行交换,p(O2)急剧降低并且下降约0.2bar。通过降低p(O2)进一步提高澄清剂有利于Sn2+或SnO的转化率。
图3示出了在SnO2澄清的玻璃陶瓷中基于锡总量、即SnO和SnO2的SnO含量(单位为mol%)与熔融和澄清过程的温度和时间的关系。在澄清步骤之前,锡总量的SnO含量为约35%(SnO与SnO和SnO2的摩尔比)。通过将澄清温度升高至1700℃,SnO含量增加至约42.5%。通过将该过程保持在该澄清温度和下降的p(O2)值(参见图2),SnO含量增加至44.5%。
在此情况下,澄清步骤中的锡转化率对于澄清的成功(即关于减少澄清的玻璃陶瓷中的气泡)而言尤为重要。通过升高至1700℃(在t=1.5h的情况下),附加的锡转化率约为7.5%SnO。通过在1700℃下保持约8小时并将熔体与气体气氛进行交换致使熔体中的pO2降低并且将现存的另外的2%的锡转化为SnO。在1700℃下,玻璃陶瓷的粘度比在1600℃下低2倍。借此,余留的气泡在1700℃下上浮的速度比在1600℃下快2倍。因此,在澄清期间保持的1700℃的温度下,主要通过发生的SnO转化来去除气泡。
通常如下生产玻璃陶瓷:合适的原材料以合适的成分进行熔融、澄清、均匀化,然后热成型为玻璃毛坯或生坯或绿色玻璃。玻璃陶瓷的“生坯”是指由合适的成分熔融的玻璃体,其可以通过借助合适的温度程序的处理转化成玻璃陶瓷。
在对组分进行称重之后,借助常规的搅拌器对混合物进行混合,然后输送至熔融槽并放入其中。
绿色玻璃的熔融分成多个步骤:
-熔融;
-视情况均匀化;
-澄清;
-视情况进一步均匀化;
-视情况静置阶段;
-浇铸。
在混合物完全熔融后,优选地进行第一均匀化。可以通过气泡以热或机械的方式均匀化。在此,热均匀化是指通过升高温度或对熔融槽表面进行不同程度的加热来促进熔体的对流。然后将用于澄清过程的熔体温度升高至约1600℃。随后进行第二均匀化阶段。例如,可以将熔体在高温下保持几天,其中保持时间的持续取决于熔体的体积。假设在这种保持或静置阶段期间,熔体在分子水平上发生进一步均匀化。
然后,将绿色玻璃浇铸到金属模具中,如例如在DE102004052514A1中所述的。然后将模具横向地移出熔融槽下方的区域并移至炉中用于受控的冷却。以足够慢的冷却速度受控地冷却至室温,以避免应力以及裂纹形成。
如此制成的玻璃块优选地经受光学检测以确保没有气泡、裂纹等。然后,在生坯陶瓷化成玻璃陶瓷之前,进行第一次机械加工、特别是去除表面区域。
在称为陶瓷化的热处理中,绿色玻璃或玻璃或生坯通过受控的体积结晶转化为玻璃陶瓷。在此热处理期间,在第一转化步骤(“结晶成核”)中,在玻璃中形成相同或不同类型的晶核。晶核或晶种是指具有特征尺寸的亚微观结晶聚集体。在第二转化步骤(“晶体生长”)中,视情况在稍高的温度下,由晶核生长出晶体或微晶。
粘度
例如,可以借助旋转粘度法、例如通过DIN ISO 7884-2:1998-2确定黏度。粘度对温度的依赖性通过VFT公式说明。
铁含量
根据DIN 51001:2003-08,通过光谱分析确定所获得的玻璃产品中的铁含量。特别地,通过UV-Vis透射光谱的解卷积定量确定所获得的玻璃产品中Fe2+与Fe3+之间的比。
Claims (17)
1.一种用于生产玻璃陶瓷的方法,包括以下步骤:
-提供原材料的混合物,
-加热混合物直至获得熔体,其中将混合物至少部分地加热至高于T3的温度,T3对应于103dPa*s的熔融玻璃粘度,
-澄清熔体,其中将熔体至少部分地加热至高于T2.5的温度,T2对应于102.5dPa*s的熔融玻璃粘度,
-获得澄清的可陶瓷化成玻璃陶瓷的玻璃,和
-将可陶瓷化成玻璃陶瓷的玻璃陶瓷化,
其中在通过H2和O2燃烧的加热下进行熔融和/或澄清。
2.根据权利要求1所述的方法,其中可陶瓷化成玻璃陶瓷的玻璃或玻璃陶瓷包括以下成分(基于氧化物wt%):
3.根据前述权利要求中任一项所述的方法,其中以氧气与燃料当量比λ小于1.05进行所述方法。
4.根据前述权利要求中任一项所述的方法,其中以氧气与燃料当量比λ>1.00、特别是>1.05进行熔融,和/或以氧气与燃料当量比λ<1.05、特别是<1.00进行澄清。
5.根据前述权利要求中任一项所述的方法,其中基于原材料的混合物的总质量,以2wt%或更低的浓度使用至少一种化学式XnOm的澄清剂,其中n=1或2,其中m=2或5,其中X=As、Sb、Sn或Ce,和/或至少一种化学式MnSO4的澄清剂,其中n=1或2,并且M=Na、K、Li、Mg、Ca、Sr、Ba和/或Zn。
6.根据前述权利要求中任一项所述的方法,其中澄清剂具有热力学性质,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,具有从较高氧化态至较低氧化态的至少30%的澄清剂转化率,特别是根据反应XnOm→XnOm-1+1/2O2和/或XnOm→XnOm-2+O2和/或根据反应MnSO4→mnO+SO2+1/2O2,其中温度T2对应于102dPa*s的熔融玻璃粘度。
7.根据前述权利要求中任一项所述的方法,包括在澄清熔体期间调节氧分压p(O2)的步骤,基于温度T3下熔体中的O2饱和度,氧分压降低至少60%,优选地至少70%。
8.根据前述权利要求中任一项所述的方法,其中在玻璃陶瓷或澄清的可陶瓷化成玻璃陶瓷的玻璃中,Fe2+与Fe3+之比为至少0.01。
9.根据前述权利要求中任一项所述的方法,其中在澄清的可陶瓷化成玻璃陶瓷的玻璃中或玻璃陶瓷中,XnOm-1与XnOm之比或XnOm-2与XnOm之比为至少0.6。
10.根据前述权利要求中任一项所述的方法,其中澄清剂选自Na2SO4、K2SO4、Li2SO4、MgSO4、CaSO4、SrSO4、ZnSO4、Sb2O5、As2O5、CeO2和SnO2的列表。
11.根据前述权利要求中任一项所述的方法,其中间歇地进行所述方法。
12.一种玻璃陶瓷,其根据前述权利要求中任一项所述的方法可生产或生产。
13.根据权利要求12所述的玻璃陶瓷,其中通过生产绿色玻璃释放的CO2少于500kg/吨玻璃、优选少于100kg/吨玻璃;
优选地,其中在玻璃或由玻璃制成的玻璃陶瓷中,Fe2+与Fe3+之比为至少0.01。
14.根据权利要求12或13所述的玻璃陶瓷,其中玻璃陶瓷在0至50℃范围的平均热膨胀系数CTE为至多0.1×10-6/K。
15.根据权利要求12至14中任一项所述的玻璃陶瓷,其中玻璃陶瓷具有中和的CO2平衡。
16.根据权利要求12至15中任一项所述玻璃陶瓷,其中玻璃包括澄清剂XnOm,所述澄清剂具有热力学性质,即在与澄清步骤中的熔体成分相同的熔体中,在1bar的氧分压p(O2)和温度T2,由澄清剂释放至多30%的O2。
17.一种精密组件,其包括根据权利要求12至15中任一项所述的玻璃陶瓷,其在整个精密组件上的CTE均匀性为至多5ppb/K、优选地至多4ppb/K、最优选地至多3ppb/K。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102021123303.8 | 2021-09-08 | ||
| DE102021123304.6 | 2021-09-08 | ||
| DE102021123303.8A DE102021123303A1 (de) | 2021-09-08 | 2021-09-08 | Glas oder Glaskeramik sowie Verfahren zum Schmelzen und Läutern von Glas oder Glaskeramik |
| DE102021123304 | 2021-09-08 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115771994A true CN115771994A (zh) | 2023-03-10 |
Family
ID=85388496
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202211100581.7A Pending CN115771994A (zh) | 2021-09-08 | 2022-09-08 | 玻璃陶瓷及用于生产玻璃陶瓷的方法 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US20230081248A1 (zh) |
| JP (1) | JP2023039442A (zh) |
| CN (1) | CN115771994A (zh) |
-
2022
- 2022-09-08 JP JP2022142759A patent/JP2023039442A/ja active Pending
- 2022-09-08 US US17/940,639 patent/US20230081248A1/en active Pending
- 2022-09-08 CN CN202211100581.7A patent/CN115771994A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20230081248A1 (en) | 2023-03-16 |
| JP2023039442A (ja) | 2023-03-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6899938B2 (ja) | 高均一性ガラスセラミック素子 | |
| EP1707541B1 (en) | Optical glass, press-molding preform, process for the production thereof, optical element and process for the production thereof | |
| KR101927555B1 (ko) | 높은 열적 및 화학적 안정성을 갖는 유리 조성물 | |
| US5200858A (en) | Uni-directional gradient index of refraction glasses | |
| US20050085371A1 (en) | Optical glass and process for the production of optical products | |
| KR101831480B1 (ko) | 기판용 무알칼리 유리 및 기판용 무알칼리 유리의 제조 방법 | |
| JP4522392B2 (ja) | 光学ガラス及びそれを用いた光学製品 | |
| JP2011136884A (ja) | 光学ガラスの製造方法及び光学機器 | |
| EP4059903A1 (en) | Glass ceramic having specific thermal expansion characteristics | |
| JP2012012282A (ja) | 光学ガラス、光学素子およびプリフォーム | |
| JP2010006675A (ja) | 光学ガラス、プリフォーム、及び光学素子 | |
| KR20030043636A (ko) | 고변형점 유리 | |
| KR20230158021A (ko) | 특정 열 팽창 거동을 갖는 정밀 부품 | |
| JP2024511745A (ja) | 高屈折率ホウ酸塩ガラス | |
| DE102022122790A1 (de) | Glaskeramik sowie Verfahren zur Herstellung einer Glaskeramik | |
| CN115771994A (zh) | 玻璃陶瓷及用于生产玻璃陶瓷的方法 | |
| US3528828A (en) | Glass,ceramics,and method | |
| JP2012144416A (ja) | 光学ガラス、光学素子およびプリフォーム | |
| JP2010053013A (ja) | ガラス | |
| US20220396521A1 (en) | Multicomponent oxide glass, optical element, optical fiber, and method of producing multicomponent oxide glass | |
| WO2024128293A1 (ja) | 低周波数光透過材料及びガラス | |
| AU603903B2 (en) | Glass-ceramic article, process for its production and thermally crystallizable glass | |
| JPS63501559A (ja) | 異常な正の部分分散のある光学弗燐酸塩ガラスおよびその製造方法 | |
| WO1991017464A1 (en) | Uni-directional gradient index of refraction glasses | |
| KR20020029758A (ko) | 착색제 유리 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |