CN113597312A - 用于改善的免疫疗法的方法 - Google Patents
用于改善的免疫疗法的方法 Download PDFInfo
- Publication number
- CN113597312A CN113597312A CN201980091985.4A CN201980091985A CN113597312A CN 113597312 A CN113597312 A CN 113597312A CN 201980091985 A CN201980091985 A CN 201980091985A CN 113597312 A CN113597312 A CN 113597312A
- Authority
- CN
- China
- Prior art keywords
- cells
- immune
- cell
- immune cell
- subject
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims abstract description 276
- 238000009169 immunotherapy Methods 0.000 title claims description 64
- 230000001976 improved effect Effects 0.000 title description 11
- 210000002865 immune cell Anatomy 0.000 claims abstract description 741
- 230000014509 gene expression Effects 0.000 claims abstract description 165
- 101710089372 Programmed cell death protein 1 Proteins 0.000 claims abstract description 163
- 239000002858 neurotransmitter agent Substances 0.000 claims abstract description 147
- 108090000189 Neuropeptides Proteins 0.000 claims abstract description 120
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 94
- 102000004310 Ion Channels Human genes 0.000 claims abstract description 89
- 102000003797 Neuropeptides Human genes 0.000 claims abstract description 88
- 230000001965 increasing effect Effects 0.000 claims abstract description 69
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 19
- 238000001514 detection method Methods 0.000 claims abstract description 14
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 273
- 210000004027 cell Anatomy 0.000 claims description 212
- 206010028980 Neoplasm Diseases 0.000 claims description 161
- 102100040678 Programmed cell death protein 1 Human genes 0.000 claims description 161
- 201000011510 cancer Diseases 0.000 claims description 150
- 208000027418 Wounds and injury Diseases 0.000 claims description 118
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 claims description 114
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 109
- 108090000623 proteins and genes Proteins 0.000 claims description 106
- 201000010099 disease Diseases 0.000 claims description 105
- 108090000862 Ion Channels Proteins 0.000 claims description 88
- 208000014674 injury Diseases 0.000 claims description 85
- 230000006378 damage Effects 0.000 claims description 72
- 230000035755 proliferation Effects 0.000 claims description 72
- 102000004169 proteins and genes Human genes 0.000 claims description 70
- 230000006870 function Effects 0.000 claims description 66
- 235000018102 proteins Nutrition 0.000 claims description 66
- 230000028327 secretion Effects 0.000 claims description 64
- 210000002966 serum Anatomy 0.000 claims description 62
- 230000000694 effects Effects 0.000 claims description 61
- 229960003638 dopamine Drugs 0.000 claims description 57
- 102000004127 Cytokines Human genes 0.000 claims description 51
- 108090000695 Cytokines Proteins 0.000 claims description 51
- 206010052428 Wound Diseases 0.000 claims description 49
- 230000007423 decrease Effects 0.000 claims description 44
- 238000011282 treatment Methods 0.000 claims description 44
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 42
- 238000003501 co-culture Methods 0.000 claims description 41
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 claims description 39
- 230000005012 migration Effects 0.000 claims description 38
- 238000013508 migration Methods 0.000 claims description 38
- 230000008569 process Effects 0.000 claims description 38
- 238000012258 culturing Methods 0.000 claims description 36
- 229930195712 glutamate Natural products 0.000 claims description 36
- 229940044601 receptor agonist Drugs 0.000 claims description 33
- 239000000018 receptor agonist Substances 0.000 claims description 33
- 230000002062 proliferating effect Effects 0.000 claims description 32
- 239000002609 medium Substances 0.000 claims description 31
- 230000009467 reduction Effects 0.000 claims description 31
- 230000030833 cell death Effects 0.000 claims description 30
- 230000004083 survival effect Effects 0.000 claims description 30
- 102400001226 Gonadoliberin-2 Human genes 0.000 claims description 29
- 101710112036 Gonadoliberin-2 Proteins 0.000 claims description 29
- 210000001519 tissue Anatomy 0.000 claims description 25
- 101710151321 Melanostatin Proteins 0.000 claims description 24
- 102400000064 Neuropeptide Y Human genes 0.000 claims description 24
- URPYMXQQVHTUDU-OFGSCBOVSA-N nucleopeptide y Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=C(O)C=C1 URPYMXQQVHTUDU-OFGSCBOVSA-N 0.000 claims description 24
- 238000002560 therapeutic procedure Methods 0.000 claims description 23
- 108090000932 Calcitonin Gene-Related Peptide Proteins 0.000 claims description 22
- 230000001024 immunotherapeutic effect Effects 0.000 claims description 20
- 229940044551 receptor antagonist Drugs 0.000 claims description 20
- 239000002464 receptor antagonist Substances 0.000 claims description 20
- MGRVRXRGTBOSHW-UHFFFAOYSA-N (aminomethyl)phosphonic acid Chemical compound NCP(O)(O)=O MGRVRXRGTBOSHW-UHFFFAOYSA-N 0.000 claims description 19
- 230000004611 cancer cell death Effects 0.000 claims description 19
- 230000003915 cell function Effects 0.000 claims description 19
- 230000035515 penetration Effects 0.000 claims description 19
- 230000008733 trauma Effects 0.000 claims description 17
- 230000000735 allogeneic effect Effects 0.000 claims description 16
- 208000015181 infectious disease Diseases 0.000 claims description 16
- 230000008439 repair process Effects 0.000 claims description 16
- 230000002829 reductive effect Effects 0.000 claims description 15
- 230000000284 resting effect Effects 0.000 claims description 15
- 208000029462 Immunodeficiency disease Diseases 0.000 claims description 14
- 230000002708 enhancing effect Effects 0.000 claims description 14
- 210000000056 organ Anatomy 0.000 claims description 14
- 230000001172 regenerating effect Effects 0.000 claims description 14
- 206010061598 Immunodeficiency Diseases 0.000 claims description 13
- 102000005157 Somatostatin Human genes 0.000 claims description 13
- 108010056088 Somatostatin Proteins 0.000 claims description 13
- 239000006143 cell culture medium Substances 0.000 claims description 13
- 239000003136 dopamine receptor stimulating agent Substances 0.000 claims description 13
- 239000001963 growth medium Substances 0.000 claims description 13
- 230000007813 immunodeficiency Effects 0.000 claims description 13
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 claims description 13
- 229960000553 somatostatin Drugs 0.000 claims description 13
- 230000000638 stimulation Effects 0.000 claims description 13
- 229940121891 Dopamine receptor antagonist Drugs 0.000 claims description 12
- 102000004108 Neurotransmitter Receptors Human genes 0.000 claims description 12
- 108090000590 Neurotransmitter Receptors Proteins 0.000 claims description 12
- 239000003210 dopamine receptor blocking agent Substances 0.000 claims description 12
- 230000000903 blocking effect Effects 0.000 claims description 11
- 230000004936 stimulating effect Effects 0.000 claims description 11
- 229940098747 AMPA receptor antagonist Drugs 0.000 claims description 10
- 229940099567 Dopamine D4 receptor agonist Drugs 0.000 claims description 10
- 230000002147 killing effect Effects 0.000 claims description 10
- 229940087102 Dopamine D3 receptor agonist Drugs 0.000 claims description 9
- 102400000932 Gonadoliberin-1 Human genes 0.000 claims description 9
- 101710112034 Gonadoliberin-1 Proteins 0.000 claims description 9
- 239000002298 dopamine 3 receptor stimulating agent Substances 0.000 claims description 9
- XLXSAKCOAKORKW-AQJXLSMYSA-N gonadorelin Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 XLXSAKCOAKORKW-AQJXLSMYSA-N 0.000 claims description 9
- 208000023275 Autoimmune disease Diseases 0.000 claims description 8
- 208000035473 Communicable disease Diseases 0.000 claims description 8
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims description 8
- 102000003734 Voltage-Gated Potassium Channels Human genes 0.000 claims description 8
- 108090000013 Voltage-Gated Potassium Channels Proteins 0.000 claims description 8
- 230000003213 activating effect Effects 0.000 claims description 8
- 229960002724 fenoldopam Drugs 0.000 claims description 8
- TVURRHSHRRELCG-UHFFFAOYSA-N fenoldopam Chemical compound C1=CC(O)=CC=C1C1C2=CC(O)=C(O)C(Cl)=C2CCNC1 TVURRHSHRRELCG-UHFFFAOYSA-N 0.000 claims description 8
- 239000004220 glutamic acid Substances 0.000 claims description 8
- 235000013922 glutamic acid Nutrition 0.000 claims description 8
- 230000002458 infectious effect Effects 0.000 claims description 8
- 239000000774 AMPA receptor agonist Substances 0.000 claims description 7
- 108091006146 Channels Proteins 0.000 claims description 7
- 229940096895 Dopamine D2 receptor agonist Drugs 0.000 claims description 7
- 229940123603 Dopamine D2 receptor antagonist Drugs 0.000 claims description 7
- 229940088353 Dopamine D3 receptor antagonist Drugs 0.000 claims description 7
- 229940124243 Dopamine D4 receptor antagonist Drugs 0.000 claims description 7
- 239000000442 dopamine 2 receptor blocking agent Substances 0.000 claims description 7
- 239000002288 dopamine 2 receptor stimulating agent Substances 0.000 claims description 7
- 239000002300 dopamine 3 receptor blocking agent Substances 0.000 claims description 7
- JUDKOGFHZYMDMF-UHFFFAOYSA-N 1-phenyl-2,3,4,5-tetrahydro-1H-3-benzazepine-7,8-diol Chemical compound C1=2C=C(O)C(O)=CC=2CCNCC1C1=CC=CC=C1 JUDKOGFHZYMDMF-UHFFFAOYSA-N 0.000 claims description 6
- 239000000775 AMPA receptor antagonist Substances 0.000 claims description 6
- 208000026350 Inborn Genetic disease Diseases 0.000 claims description 6
- HOKKHZGPKSLGJE-GSVOUGTGSA-N N-Methyl-D-aspartic acid Chemical compound CN[C@@H](C(O)=O)CC(O)=O HOKKHZGPKSLGJE-GSVOUGTGSA-N 0.000 claims description 6
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 claims description 6
- 208000016361 genetic disease Diseases 0.000 claims description 6
- 208000030159 metabolic disease Diseases 0.000 claims description 6
- 239000003706 n methyl dextro aspartic acid receptor stimulating agent Substances 0.000 claims description 6
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 6
- 230000000926 neurological effect Effects 0.000 claims description 6
- 239000011591 potassium Substances 0.000 claims description 6
- 229910052700 potassium Inorganic materials 0.000 claims description 6
- 208000029483 Acquired immunodeficiency Diseases 0.000 claims description 5
- 229940127523 NMDA Receptor Antagonists Drugs 0.000 claims description 5
- 229940099433 NMDA receptor antagonist Drugs 0.000 claims description 5
- 230000008014 freezing Effects 0.000 claims description 5
- 238000007710 freezing Methods 0.000 claims description 5
- 230000002068 genetic effect Effects 0.000 claims description 5
- 239000003102 growth factor Substances 0.000 claims description 5
- 239000003703 n methyl dextro aspartic acid receptor blocking agent Substances 0.000 claims description 5
- YOILXOMTHPUMRG-JSGCOSHPSA-N (4as,10bs)-4-propyl-3,4a,5,10b-tetrahydro-2h-chromeno[4,3-b][1,4]oxazin-9-ol Chemical group C1=C(O)C=C2[C@@H]3OCCN(CCC)[C@H]3COC2=C1 YOILXOMTHPUMRG-JSGCOSHPSA-N 0.000 claims description 4
- RPXVIAFEQBNEAX-UHFFFAOYSA-N 6-Cyano-7-nitroquinoxaline-2,3-dione Chemical group N1C(=O)C(=O)NC2=C1C=C([N+](=O)[O-])C(C#N)=C2 RPXVIAFEQBNEAX-UHFFFAOYSA-N 0.000 claims description 4
- BLYMJBIZMIGWFK-UHFFFAOYSA-N 7-(dipropylamino)-5,6,7,8-tetrahydronaphthalen-2-ol Chemical compound C1=C(O)C=C2CC(N(CCC)CCC)CCC2=C1 BLYMJBIZMIGWFK-UHFFFAOYSA-N 0.000 claims description 4
- 101000774828 Dendroaspis polylepis polylepis Kunitz-type serine protease inhibitor homolog dendrotoxin K Proteins 0.000 claims description 4
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 claims description 4
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 claims description 4
- 230000007547 defect Effects 0.000 claims description 4
- 230000002939 deleterious effect Effects 0.000 claims description 4
- 208000016097 disease of metabolism Diseases 0.000 claims description 4
- 210000003162 effector t lymphocyte Anatomy 0.000 claims description 4
- 239000007850 fluorescent dye Substances 0.000 claims description 4
- 230000002757 inflammatory effect Effects 0.000 claims description 4
- 239000003226 mitogen Substances 0.000 claims description 4
- 238000012544 monitoring process Methods 0.000 claims description 4
- PFIWYJNBKGCVFM-UHFFFAOYSA-N n-[4-[4-(2,3-dichlorophenyl)piperazin-1-yl]butyl]-9h-fluorene-2-carboxamide;hydrochloride Chemical group Cl.ClC1=CC=CC(N2CCN(CCCCNC(=O)C=3C=C4C(C5=CC=CC=C5C4)=CC=3)CC2)=C1Cl PFIWYJNBKGCVFM-UHFFFAOYSA-N 0.000 claims description 4
- 230000001717 pathogenic effect Effects 0.000 claims description 4
- 108020001213 potassium channel Proteins 0.000 claims description 4
- 210000003289 regulatory T cell Anatomy 0.000 claims description 4
- 229950011111 sumanirole Drugs 0.000 claims description 4
- RKZSNTNMEFVBDT-MRVPVSSYSA-N sumanirole Chemical group C([C@H](C1)NC)C2=CC=CC3=C2N1C(=O)N3 RKZSNTNMEFVBDT-MRVPVSSYSA-N 0.000 claims description 4
- APFMVAHRFWBCDG-JUOYHRLASA-N (6as,13br)-11-chloro-7-methyl-5,6,6a,8,9,13b-hexahydronaphtho[1,2-a][3]benzazepin-12-ol;hydrochloride Chemical group Cl.CN1CCC2=CC(Cl)=C(O)C=C2[C@H]2C3=CC=CC=C3CC[C@H]12 APFMVAHRFWBCDG-JUOYHRLASA-N 0.000 claims description 3
- 108090000312 Calcium Channels Proteins 0.000 claims description 3
- 102000003922 Calcium Channels Human genes 0.000 claims description 3
- 108010062745 Chloride Channels Proteins 0.000 claims description 3
- 102000011045 Chloride Channels Human genes 0.000 claims description 3
- 101710084146 Dendroaspin Proteins 0.000 claims description 3
- 229940123915 Ion channel antagonist Drugs 0.000 claims description 3
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 claims description 3
- 239000012595 freezing medium Substances 0.000 claims description 3
- 210000004475 gamma-delta t lymphocyte Anatomy 0.000 claims description 3
- 229960002989 glutamic acid Drugs 0.000 claims description 3
- 210000002443 helper t lymphocyte Anatomy 0.000 claims description 3
- 210000003071 memory t lymphocyte Anatomy 0.000 claims description 3
- 210000004877 mucosa Anatomy 0.000 claims description 3
- 210000000581 natural killer T-cell Anatomy 0.000 claims description 3
- 238000002054 transplantation Methods 0.000 claims description 3
- 210000003171 tumor-infiltrating lymphocyte Anatomy 0.000 claims description 3
- 229940098778 Dopamine receptor agonist Drugs 0.000 claims description 2
- 102000016913 Voltage-Gated Sodium Channels Human genes 0.000 claims description 2
- 108010053752 Voltage-Gated Sodium Channels Proteins 0.000 claims description 2
- -1 a77636 Chemical compound 0.000 claims description 2
- 102100025588 Calcitonin gene-related peptide 1 Human genes 0.000 claims 1
- 102000004257 Potassium Channel Human genes 0.000 claims 1
- 102100023990 60S ribosomal protein L17 Human genes 0.000 abstract 2
- 230000009286 beneficial effect Effects 0.000 description 47
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 34
- 239000012894 fetal calf serum Substances 0.000 description 34
- 238000000338 in vitro Methods 0.000 description 23
- 102000004414 Calcitonin Gene-Related Peptide Human genes 0.000 description 21
- 230000008901 benefit Effects 0.000 description 18
- 102000005962 receptors Human genes 0.000 description 17
- 108020003175 receptors Proteins 0.000 description 17
- 230000004913 activation Effects 0.000 description 16
- 108091008874 T cell receptors Proteins 0.000 description 11
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 11
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 11
- 238000005259 measurement Methods 0.000 description 11
- 238000002619 cancer immunotherapy Methods 0.000 description 10
- 201000007270 liver cancer Diseases 0.000 description 10
- 208000014018 liver neoplasm Diseases 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 9
- 239000008280 blood Substances 0.000 description 9
- 230000003247 decreasing effect Effects 0.000 description 9
- 238000003556 assay Methods 0.000 description 8
- 238000011534 incubation Methods 0.000 description 8
- 230000001575 pathological effect Effects 0.000 description 8
- 230000004044 response Effects 0.000 description 8
- 235000001014 amino acid Nutrition 0.000 description 7
- 229940024606 amino acid Drugs 0.000 description 7
- 150000001413 amino acids Chemical class 0.000 description 7
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 239000008194 pharmaceutical composition Substances 0.000 description 7
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 6
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 6
- 101000600434 Homo sapiens Putative uncharacterized protein encoded by MIR7-3HG Proteins 0.000 description 6
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 description 6
- 102100037401 Putative uncharacterized protein encoded by MIR7-3HG Human genes 0.000 description 6
- 230000006044 T cell activation Effects 0.000 description 6
- 210000001124 body fluid Anatomy 0.000 description 6
- 238000002659 cell therapy Methods 0.000 description 6
- 230000001939 inductive effect Effects 0.000 description 6
- 210000002569 neuron Anatomy 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 102100034355 Potassium voltage-gated channel subfamily A member 3 Human genes 0.000 description 5
- 101100289792 Squirrel monkey polyomavirus large T gene Proteins 0.000 description 5
- 239000002671 adjuvant Substances 0.000 description 5
- 238000011467 adoptive cell therapy Methods 0.000 description 5
- 230000001363 autoimmune Effects 0.000 description 5
- 231100000433 cytotoxic Toxicity 0.000 description 5
- 230000001472 cytotoxic effect Effects 0.000 description 5
- 230000003013 cytotoxicity Effects 0.000 description 5
- 231100000135 cytotoxicity Toxicity 0.000 description 5
- 239000003937 drug carrier Substances 0.000 description 5
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 239000011148 porous material Substances 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- 239000000556 agonist Substances 0.000 description 4
- 210000004748 cultured cell Anatomy 0.000 description 4
- 239000003085 diluting agent Substances 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 210000000987 immune system Anatomy 0.000 description 4
- 230000002163 immunogen Effects 0.000 description 4
- 238000007918 intramuscular administration Methods 0.000 description 4
- 230000002601 intratumoral effect Effects 0.000 description 4
- 230000001681 protective effect Effects 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 230000017423 tissue regeneration Effects 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 3
- 102100025137 Early activation antigen CD69 Human genes 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 101000934374 Homo sapiens Early activation antigen CD69 Proteins 0.000 description 3
- 102000004868 N-Methyl-D-Aspartate Receptors Human genes 0.000 description 3
- 108090001041 N-Methyl-D-Aspartate Receptors Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 3
- 239000000427 antigen Substances 0.000 description 3
- 102000036639 antigens Human genes 0.000 description 3
- 108091007433 antigens Proteins 0.000 description 3
- 230000006907 apoptotic process Effects 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 230000034994 death Effects 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 229940049906 glutamate Drugs 0.000 description 3
- 239000003823 glutamate receptor agonist Substances 0.000 description 3
- 230000028993 immune response Effects 0.000 description 3
- 230000037451 immune surveillance Effects 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 238000007917 intracranial administration Methods 0.000 description 3
- 238000007912 intraperitoneal administration Methods 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 108020004999 messenger RNA Proteins 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 230000017074 necrotic cell death Effects 0.000 description 3
- 230000001338 necrotic effect Effects 0.000 description 3
- 239000000712 neurohormone Substances 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 230000037361 pathway Effects 0.000 description 3
- 210000005259 peripheral blood Anatomy 0.000 description 3
- 239000011886 peripheral blood Substances 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 230000004853 protein function Effects 0.000 description 3
- 238000011069 regeneration method Methods 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 208000011580 syndromic disease Diseases 0.000 description 3
- 238000001262 western blot Methods 0.000 description 3
- 208000030507 AIDS Diseases 0.000 description 2
- 102000003678 AMPA Receptors Human genes 0.000 description 2
- 108090000078 AMPA Receptors Proteins 0.000 description 2
- 229940124118 AMPA receptor agonist Drugs 0.000 description 2
- 208000024827 Alzheimer disease Diseases 0.000 description 2
- 102000014468 Calcitonin Gene-Related Peptide Receptors Human genes 0.000 description 2
- 108010078311 Calcitonin Gene-Related Peptide Receptors Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 2
- 101800004866 G protein-coupled receptor ligand Proteins 0.000 description 2
- 229940117892 Glutamate receptor agonist Drugs 0.000 description 2
- 101710118786 Gonadotropin-releasing hormone II receptor Proteins 0.000 description 2
- 208000023105 Huntington disease Diseases 0.000 description 2
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 description 2
- 102000000588 Interleukin-2 Human genes 0.000 description 2
- 108010002350 Interleukin-2 Proteins 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 206010027476 Metastases Diseases 0.000 description 2
- 208000012902 Nervous system disease Diseases 0.000 description 2
- 108070000018 Neuropeptide receptor Proteins 0.000 description 2
- 102000028517 Neuropeptide receptor Human genes 0.000 description 2
- 229940084576 Neurotransmitter agonist Drugs 0.000 description 2
- 229940123247 Neurotransmitter antagonist Drugs 0.000 description 2
- 238000000636 Northern blotting Methods 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 102100033845 Putative gonadotropin-releasing hormone II receptor Human genes 0.000 description 2
- 108020004511 Recombinant DNA Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229940123051 Somatostatin receptor agonist Drugs 0.000 description 2
- 229940121856 Somatostatin receptor antagonist Drugs 0.000 description 2
- 230000006786 activation induced cell death Effects 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 238000011374 additional therapy Methods 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 238000011319 anticancer therapy Methods 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- 230000005784 autoimmunity Effects 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 230000021164 cell adhesion Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000003399 chemotactic effect Effects 0.000 description 2
- 238000002512 chemotherapy Methods 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000012636 effector Substances 0.000 description 2
- MMXKVMNBHPAILY-UHFFFAOYSA-N ethyl laurate Chemical compound CCCCCCCCCCCC(=O)OCC MMXKVMNBHPAILY-UHFFFAOYSA-N 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 238000012239 gene modification Methods 0.000 description 2
- 230000005017 genetic modification Effects 0.000 description 2
- 235000013617 genetically modified food Nutrition 0.000 description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-L glutamate group Chemical group N[C@@H](CCC(=O)[O-])C(=O)[O-] WHUUTDBJXJRKMK-VKHMYHEASA-L 0.000 description 2
- 239000003825 glutamate receptor antagonist Substances 0.000 description 2
- 230000009931 harmful effect Effects 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 210000005260 human cell Anatomy 0.000 description 2
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 description 2
- 230000005847 immunogenicity Effects 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000001361 intraarterial administration Methods 0.000 description 2
- 238000007913 intrathecal administration Methods 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- 230000009401 metastasis Effects 0.000 description 2
- 238000010369 molecular cloning Methods 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 201000006938 muscular dystrophy Diseases 0.000 description 2
- 108040002669 neuropeptide hormone activity proteins Proteins 0.000 description 2
- 102000008434 neuropeptide hormone activity proteins Human genes 0.000 description 2
- BPGXUIVWLQTVLZ-OFGSCBOVSA-N neuropeptide y(npy) Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=C(O)C=C1 BPGXUIVWLQTVLZ-OFGSCBOVSA-N 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 230000000770 proinflammatory effect Effects 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 208000020016 psychiatric disease Diseases 0.000 description 2
- 238000003753 real-time PCR Methods 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 2
- 230000002269 spontaneous effect Effects 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 239000003104 tissue culture media Substances 0.000 description 2
- 230000003442 weekly effect Effects 0.000 description 2
- DMJWENQHWZZWDF-PKOBYXMFSA-N (6aS,13bR)-11-chloro-7-methyl-5,6,6a,8,9,13b-hexahydronaphtho[1,2-a][3]benzazepin-12-ol Chemical compound CN1CCC2=CC(Cl)=C(O)C=C2[C@H]2C3=CC=CC=C3CC[C@H]12 DMJWENQHWZZWDF-PKOBYXMFSA-N 0.000 description 1
- RBTBFTRPCNLSDE-UHFFFAOYSA-N 3,7-bis(dimethylamino)phenothiazin-5-ium Chemical compound C1=CC(N(C)C)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 RBTBFTRPCNLSDE-UHFFFAOYSA-N 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 208000019901 Anxiety disease Diseases 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 206010003594 Ataxia telangiectasia Diseases 0.000 description 1
- 102000008096 B7-H1 Antigen Human genes 0.000 description 1
- 108010074708 B7-H1 Antigen Proteins 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 238000007809 Boyden Chamber assay Methods 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 102100032937 CD40 ligand Human genes 0.000 description 1
- 102100032912 CD44 antigen Human genes 0.000 description 1
- 210000001266 CD8-positive T-lymphocyte Anatomy 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- 208000037088 Chromosome Breakage Diseases 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 206010010071 Coma Diseases 0.000 description 1
- 206010010099 Combined immunodeficiency Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 108050006400 Cyclin Proteins 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 206010012289 Dementia Diseases 0.000 description 1
- 201000010374 Down Syndrome Diseases 0.000 description 1
- 101100234002 Drosophila melanogaster Shal gene Proteins 0.000 description 1
- 206010058314 Dysplasia Diseases 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 206010017533 Fungal infection Diseases 0.000 description 1
- 208000015872 Gaucher disease Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000001398 Granzyme Human genes 0.000 description 1
- 108060005986 Granzyme Proteins 0.000 description 1
- 102000018713 Histocompatibility Antigens Class II Human genes 0.000 description 1
- 108010027412 Histocompatibility Antigens Class II Proteins 0.000 description 1
- 238000010867 Hoechst staining Methods 0.000 description 1
- 101000868215 Homo sapiens CD40 ligand Proteins 0.000 description 1
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 1
- 101001018097 Homo sapiens L-selectin Proteins 0.000 description 1
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 description 1
- 206010022489 Insulin Resistance Diseases 0.000 description 1
- 108010038453 Interleukin-2 Receptors Proteins 0.000 description 1
- 102000010789 Interleukin-2 Receptors Human genes 0.000 description 1
- 102100033467 L-selectin Human genes 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 102000002274 Matrix Metalloproteinases Human genes 0.000 description 1
- 108010000684 Matrix Metalloproteinases Proteins 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 206010027457 Metastases to liver Diseases 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 208000031888 Mycoses Diseases 0.000 description 1
- GXCLVBGFBYZDAG-UHFFFAOYSA-N N-[2-(1H-indol-3-yl)ethyl]-N-methylprop-2-en-1-amine Chemical compound CN(CCC1=CNC2=C1C=CC=C2)CC=C GXCLVBGFBYZDAG-UHFFFAOYSA-N 0.000 description 1
- 208000028389 Nerve injury Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 201000007142 Omenn syndrome Diseases 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 239000012270 PD-1 inhibitor Substances 0.000 description 1
- 239000012668 PD-1-inhibitor Substances 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 102000009339 Proliferating Cell Nuclear Antigen Human genes 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 108091027981 Response element Proteins 0.000 description 1
- 201000007737 Retinal degeneration Diseases 0.000 description 1
- 235000019485 Safflower oil Nutrition 0.000 description 1
- 244000166071 Shorea robusta Species 0.000 description 1
- 235000015076 Shorea robusta Nutrition 0.000 description 1
- 108010052164 Sodium Channels Proteins 0.000 description 1
- 102000018674 Sodium Channels Human genes 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 230000009809 T cell chemotaxis Effects 0.000 description 1
- 201000001322 T cell deficiency Diseases 0.000 description 1
- 210000000662 T-lymphocyte subset Anatomy 0.000 description 1
- 208000002903 Thalassemia Diseases 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 206010044688 Trisomy 21 Diseases 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 208000006110 Wiskott-Aldrich syndrome Diseases 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 239000002411 allomone Substances 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 230000001668 ameliorated effect Effects 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000036506 anxiety Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 230000003305 autocrine Effects 0.000 description 1
- 210000003050 axon Anatomy 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 210000003969 blast cell Anatomy 0.000 description 1
- 210000004958 brain cell Anatomy 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 230000035605 chemotaxis Effects 0.000 description 1
- 230000005886 chromosome breakage Effects 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 206010015037 epilepsy Diseases 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 208000007345 glycogen storage disease Diseases 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 239000008241 heterogeneous mixture Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 235000020256 human milk Nutrition 0.000 description 1
- 210000004251 human milk Anatomy 0.000 description 1
- 238000012606 in vitro cell culture Methods 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 239000008176 lyophilized powder Substances 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 208000002780 macular degeneration Diseases 0.000 description 1
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 1
- 239000000347 magnesium hydroxide Substances 0.000 description 1
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229960000907 methylthioninium chloride Drugs 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 238000010232 migration assay Methods 0.000 description 1
- 230000001617 migratory effect Effects 0.000 description 1
- 208000012268 mitochondrial disease Diseases 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000003032 molecular docking Methods 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 230000008764 nerve damage Effects 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 230000002611 ovarian Effects 0.000 description 1
- 230000003076 paracrine Effects 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 229940121655 pd-1 inhibitor Drugs 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 230000002263 peptidergic effect Effects 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002203 pretreatment Methods 0.000 description 1
- 210000004986 primary T-cell Anatomy 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 238000012342 propidium iodide staining Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 238000012514 protein characterization Methods 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000003716 rejuvenation Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004258 retinal degeneration Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 235000005713 safflower oil Nutrition 0.000 description 1
- 239000003813 safflower oil Substances 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 201000000980 schizophrenia Diseases 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 210000002955 secretory cell Anatomy 0.000 description 1
- 210000000582 semen Anatomy 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 1
- 230000008054 signal transmission Effects 0.000 description 1
- 208000019116 sleep disease Diseases 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 229940054269 sodium pyruvate Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 238000011301 standard therapy Methods 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 230000003319 supportive effect Effects 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 238000002626 targeted therapy Methods 0.000 description 1
- 238000010257 thawing Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 230000003827 upregulation Effects 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
- G01N33/5047—Cells of the immune system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/46—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the cancer treated
- A61K2239/53—Liver
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Cell Biology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Toxicology (AREA)
- Pathology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Physics & Mathematics (AREA)
- Zoology (AREA)
- Virology (AREA)
- Developmental Biology & Embryology (AREA)
- Communicable Diseases (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
提供了过继性神经免疫疗法、选择适合过继性神经免疫疗法的对象、选择用于提高治疗性免疫细胞潜力的分子或分子的组合、和降低免疫细胞表面上的PD‑1的表达的方法,包括使免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触。还提供了包含那些分子中的至少一种或包含那些分子中的至少两种和任选地PD‑1检测剂的试剂盒。
Description
相关申请的交叉引用
本申请要求于2018年1月25日提交的美国临时专利申请号62/621,805的优先权的权益,其内容通过引用以其整体并入本文。
技术领域
本发明涉及免疫疗法领域。
背景技术
T细胞对于正常持续的身体功能以及对于克服各种不同类型的多种疾病和其它病理状况,其中包括:癌症、传染病、自身免疫性疾病、退行性疾病、免疫缺陷疾病、代谢疾病、遗传疾病、损伤和创伤等至关重要。T细胞对于识别和根除癌症和传染性介质(agents)尤其重要。
然而,在许多病理中,由于各种不同因素导致的数量次优或功能次优,所急需的T细胞处于次优状态。
在所有这些状况下,提高有益的T细胞功能,特别是以安全、无痛和生理学方式并且在每当有所需要时,是一个巨大的期望临床目标,如果成功,则能够帮助克服疾病、损伤或创伤,因此挽救生命,或至少使疾病变得不那么严重且易于控制,并通过这样做提高患者的生活质量。
提高癌症患者有益的T细胞功能尤为重要,因为在癌症患者中,急需的T细胞无法充分发挥作用,从而“允许”癌症传播和转移,这是由于以下所有因素对T细胞造成的多种不利影响所致:癌细胞(分泌对T细胞有敌意的因子)、应激、焦虑、睡眠障碍和各种感染。此外,用于治疗性破坏癌细胞的各种材料和程序也对有益的T细胞产生不期望的不利影响,其中包括:用于化学疗法的分子、各种其它药物、辐射、外科手术等。此外,患者的肿瘤特异性T细胞由于持续性/慢性暴露于肿瘤抗原而耗尽,当癌细胞增殖时,肿瘤抗原的数量/负荷会增加。这种由肿瘤抗原引起的连续性T细胞活化,通过“活化诱导的细胞死亡(AICD)”导致T细胞死亡。此外,据报道,在许多类型的人类癌症,其中包括:头颈癌、黑素瘤、卵巢癌、前列腺癌、宫颈癌、肾细胞癌、肝结直肠癌转移、结直肠癌和其它各种肿瘤中,T细胞中的CD3ζ表达显著下调。重要的是,CD3ζ损失被认为是癌症患者T细胞的一种关键缺陷,因为该损失削弱T细胞根除癌症的能力。
过继性免疫细胞疗法,通常被称为过继性免疫疗法,是目前正在进行科学和临床研究的癌症治疗的主要途径之一,并且处于其临床应用的第一步。过继性免疫疗法有多种不同的模式,在以下许多参数上彼此不同,其中包括:1)免疫疗法聚焦、靶向或限制的癌症的类型;2)从患者体内纯化,然后在体外操纵以供后续治疗使用的免疫细胞的类型;3)用于增强患者的免疫细胞治疗潜力的精确的体外程序和试剂;4)“体外停放”的时长——免疫细胞体外操纵和扩增以增加其治疗潜力和数量所需的时间;5)癌症患者在治疗性免疫细胞可被注射入其体内之前必须经历的预先免疫疗法治疗,6)癌症患者在治疗性免疫细胞被注射入其体内后必须经历的支持性免疫疗法后治疗,从而它们在患者体内更好地发挥作用并持续更长的时间段,7)向患者注射的治疗性免疫细胞的数量,8)向患者注射的治疗性细胞的次数,以及注射间的频率,9)治疗细胞是否与所给予患者的或对患者执行的其它治疗分子或程序一起或在其它治疗分子或程序之间注射。
在大多数过继性免疫疗法的情况下,免疫细胞,主要是T细胞的体外操纵和培养并非专门用于增加它们的数量。确切地说,患者的T细胞的体外操纵,如基因工程改造或其它操纵用于通过赋予细胞其以前没有的能力来增强它们识别和根除癌细胞的能力。大多数类型的T细胞介导的过继性免疫疗法需要通过其T细胞受体(TCR)经典活化T细胞以进行自身操纵,然后扩增被操纵的T细胞,以获得足够多数量的治疗性T用于向患者注射。
在T细胞介导的免疫疗法的某些模式中,选择特异性的T细胞亚群,例如细胞毒性CD8+T细胞。在其它一些情况下,培养的细胞通过人工的非生理学试剂和程序进行处理以提高它们的功能性。
患有癌症的患者通常对癌症的免疫应答受损。这可能是由于免疫系统减弱或由于肿瘤逃避免疫监视。已知许多肿瘤表达高水平的PD-L1,一种在细胞毒性免疫细胞表面发现的程序性细胞死亡-1(PD-1)蛋白的配体。一般而言,所有过继性免疫细胞疗法都旨在提高免疫细胞的功能,以便在向宿主给予时能够启动针对肿瘤的有益免疫应答。
一种尚未在临床环境下进行测试的建议的过继性免疫细胞疗法涉及在免疫细胞处于体外组织培养时向它们给予神经递质或神经肽。神经递质是尺寸非常小的化学信使(尺寸约一个氨基酸),其协调信号从一个神经细胞(主要是神经元)到另一个脑细胞的传输。神经递质对T细胞和其它免疫细胞也有非常强力和重要的作用。此外,神经递质对各种各样的其它身体细胞和系统也有很强的作用。所有神经递质都通过与其靶细胞的细胞表面上表达的其高度特异性神经递质受体结合来诱导其特异性作用。神经肽,有时也被称为神经激素,是较大的肽能神经递质。神经肽还具有许多高强力且重要的作用。各种单一的神经递质和神经肽已被证明通过增加T细胞的ζ链表达、趋化和自发性迁移、粘附、细胞因子分泌和其它特征和功能,重新(de novo)诱导和/或提高T细胞功能。然而,在了解哪些神经递质和神经肽最能提高给定患者的免疫细胞功能上仍然存在困难。由于个体在特定神经递质受体的表达量/水平及其对特定神经递质的响应方面存在差异。此外,不知道哪些患者最适合这种疗法,或者何时是通过神经递质和/或神经肽增加某些个体的细胞的好时机和条件。最后,虽然已知神经递质和神经肽可以诱导和/或增强T细胞功能,但可克服免疫监视逃避的其它方式则不知晓。极大地需要诱导和/或提高免疫细胞功能和治疗潜力,以及为被称为过继性神经免疫疗法的神经递质/神经肽-诱导的过继性免疫细胞疗法选择患者和选择待使用的神经递质、神经肽或其组合的方法。
发明内容
本发明提供了用于任何疾病、损伤、或创伤,其中总体而言,改善的免疫细胞,并且具体是T细胞,能够对患者有治疗性和益处的过继性神经免疫疗法的方法;用于选择适合神经免疫疗法的对象、选择用于提高治疗性免疫细胞潜力的分子或分子的组合、和降低免疫细胞表面上的PD-1表达的方法,包括使免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触。还提供了包含那些分子中至少一种或包含那些分子中至少两种和任选地PD-1检测剂以用于测试和选择患者的T细胞对哪种分子或分子的组合响应性最好的试剂盒。
本发明部分地基于以下令人惊讶的发现:电压门控离子通道的神经递质、神经肽和调节剂可以降低免疫细胞表面上的PD-1的表达,从而提高它们有益地发挥作用的能力,并改善它们的治疗有效性。此外,在用这些分子对对象的免疫细胞进行体外处理后,PD-1表达是一种用于确定对象是否适合于改善的免疫疗法和疗法的时机,和用于选择分子或分子的组合用于所述疗法的有用的读数。
本发明的方法有效地降低T细胞中的PD-1、提高免疫细胞的免疫治疗潜力、改善患者的病理状况、改善诱导此类效果的分子和/或分子的组合的预先选择以及选择对此类方法有响应的候选患者,和疗法的时机,即患者的T细胞何时对分子或分子的组合有响应。
本发明的方法使用患者自身的T细胞,或对患者有利的不同来源的T细胞,或可通过使用用于T细胞的方法而具有/变得有治疗性的除T细胞以外的免疫细胞。T细胞或其它免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子孵育。
所述方法可以包括两个阶段。第一阶段是诊断阶段,揭示了那些经测试的最好的分子和/或它们的组合,这些分子降低PD-1并随后提高T细胞功能及其免疫治疗潜力。第二阶段是治疗阶段,将诊断结果转化为实际治疗。因此,治疗方案取决于诊断结果并根据诊断结果设计。诊断阶段教导了使用哪些分子在体外孵育/处理T细胞是有利的,以及哪些类型的经处理的T细胞应该在之后向患者注射。诊断阶段也可以在不同的时间点和条件下执行若干次,且只有当患者的T细胞对经测试的分子有响应时,患者才会继续进入治疗阶段。
在诊断阶段中,T细胞在体外对分子的响应决定了:1)在执行诊断时对象是否能够受益于,并因此是否应该用过继性神经免疫疗法治疗;2)应该使用哪些经测试的分子或它们的组合来处理/增强T细胞,从而提高它们的免疫治疗潜力;和3)最终应该向患者注射哪些类型的经处理的T细胞。治疗方法可以以任何期望的频率和整个治疗期重复地使用。治疗方法可用于治疗处于疾病、或损伤或创伤的任何阶段的各种类型的疾病和损伤,作为单独治疗,或处于其它治疗之间或一直(ever)与其它治疗同时进行。诱导或改善T细胞的特征和功能及其治疗潜力的方法可用于改善任何T细胞或其它免疫细胞,用于任何科学、医疗和/或商业目的。
根据第一方面,提供了在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使第一免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的程序性细胞死亡1(PD-1)表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
d.提供与第一免疫细胞来源相同的第二免疫细胞;
e.使第二免疫细胞与至少一种分子接触,其中所述至少一种分子降低第一免疫细胞中的PD-1表达或功能、增加第一免疫细胞的增殖、增加与第一免疫细胞共培养的癌细胞死亡或其组合;和
f.将接触的第二免疫细胞给予所述对象;
从而在所述对其有需要的对象中执行过继性神经免疫疗法。
根据另一方面,提供了在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使第一免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或至少一种电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的PD-1表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对至少一种细胞因子的分泌;
xi.所述免疫细胞对至少一种治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
d.提供与第一免疫细胞来源相同的第二免疫细胞;
e.使第二免疫细胞与至少两种分子接触,其中所述至少两种分子降低第一免疫细胞中的PD-1表达水平或功能水平、增加第一免疫细胞的增殖、增加仅与第一免疫细胞共培养的癌细胞死亡或共培养的癌细胞死亡、增加第一免疫细胞中的ζ链表达、增加第一免疫细胞的迁移、增加第一免疫细胞对细胞因子的分泌、增加第一免疫细胞的粘附、增加第一免疫细胞的归巢、增加所述免疫细胞对至少一种治疗性蛋白质的分泌、提高参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平、或其组合;和
f.将接触的第二免疫细胞向所述对象给予;
从而在所述需要其的对象中执行过继性神经免疫疗法。
根据另一方面,提供了选择适合神经免疫疗法的对象的方法,所述方法包括,
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的程序性细胞死亡1(PD-1)表达;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
其中PD-1表达或功能的降低、增殖的增加、癌细胞死亡的增加及其组合中的至少一个指示所述对象适合神经免疫疗法。
根据另一方面,提供了选择适合神经免疫疗法的对象的方法,所述方法包括,
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或至少一种电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的PD-1表达或活性;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对细胞因子的分泌;
xi.所述免疫细胞对治疗性蛋白质的分泌;和
xii.参与过程i至xi的蛋白质和基因的表达水平和功能水平;
其中PD-1表达或活性的降低、单独或共培养的所述免疫细胞的增殖的增加、癌细胞死亡的增加、ζ链表达的增加、迁移的增加、细胞因子分泌的增加、粘附的增加、归巢的增加、至少一种治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因的表达或功能的降低、或参与过程ii至xi的至少一种蛋白质或基因的表达或功能的提高中的至少一个指示所述对象适合神经免疫疗法。
根据另一方面,提供了选择用于提高免疫治疗潜力的分子的方法,所述方法包括:
a.提供免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的程序性细胞死亡1(PD-1)表达;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
其中PD-1表达或功能的降低、增殖的增加、癌细胞死亡的增加及其组合中的至少一个指示所述至少一种分子提高了所述免疫细胞的治疗潜力。
根据另一方面,提供了选择用于提高治疗性免疫细胞潜力的分子的组合的方法,所述方法包括:
a.提供免疫细胞;
b.使所述第一免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.免疫细胞上的PD-1表达或活性;
ii.与癌细胞共培养的免疫细胞的增殖;和
iii.与免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的免疫细胞的增殖;
v.免疫细胞中CD3ζ链的表达;
vi.免疫细胞的迁移;
vii.免疫细胞的粘附;
viii.免疫细胞的归巢;
ix.免疫细胞的穿透;
x.免疫细胞对细胞因子的分泌;
xi.免疫细胞对治疗性蛋白质的分泌;和
xii.参与以上过程的蛋白质和基因的表达水平和功能水平;
其中PD-1表达或活性的降低、单独或共培养的免疫细胞的增殖的增加、癌细胞死亡的增加、ζ链表达的增加、迁移的增加、细胞因子分泌的增加、粘附的增加、归巢的增加、至少一种治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因的表达或功能的降低、或参与过程ii至xi的至少一种蛋白质或基因的表达或功能的提高中的至少一个指示所述至少一种分子提高了所述免疫细胞的治疗潜力。
根据另一方面,提供了降低免疫细胞的表面上的PD-1表达的方法,所述方法包括向所述免疫细胞给予选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子。
根据另一方面,提供了增强免疫细胞功能的方法,所述方法包括:
a.提供免疫细胞;和
b.使免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少两种分子接触。
根据另一方面,提供了包含至少一种神经递质或其类似物、至少一种神经肽或其类似物和至少一种电压门控离子通道的调节剂的试剂盒。在一些实施方式中,所述试剂盒进一步包含PD-1检测剂。
根据一些实施方式,所述对象遭受具有或疑似具有次优的T细胞数量、活性或两者的疾病、状况、损伤或创伤。根据一些实施方式,所述疾病、状况、损伤或创伤选自:癌症、传染病、遗传免疫缺陷、获得性免疫缺陷、退行性疾病、自身免疫疾病、代谢疾病、遗传疾病、神经或神经精神疾病、和器官移植后伴有免疫功能不全。根据一些实施方式,所述疾病、状况、损伤或创伤是传染病。根据一些实施方式,所述疾病、状况、损伤或创伤是癌症。根据一些实施方式,所述疾病、状况、损伤或创伤需要组织或器官修复,或T细胞衍生因子的递送。
根据一些实施方式,免疫细胞是表达PD-1的免疫细胞。根据一些实施方式,所述免疫细胞是T细胞。根据一些实施方式,第一和第二免疫细胞来自患者。根据一些实施方式,第一和第二免疫细胞来自健康供体。根据一些实施方式,第一提供的免疫细胞在接触之前未被预先活化。
根据一些实施方式,第一提供的免疫细胞是多种免疫细胞并且还包括从所述第一提供的免疫细胞中选择免疫细胞的亚群。根据一些实施方式,所述免疫细胞的亚群选自:效应T细胞、辅助T细胞、细胞毒性T细胞、调节T细胞、抑制T细胞、自然杀伤T细胞、炎性T细胞、记忆T细胞、γδT细胞、组织/器官浸润T细胞、肿瘤浸润T细胞、修复T细胞和促再生T细胞、黏膜相关T细胞、修复T细胞、促再生T细胞、活化T细胞和灭活T细胞。
根据一些实施方式,本发明的方法进一步包括在免疫细胞培养基中培养所提供的免疫细胞。根据一些实施方式,所述免疫细胞培养基包含人血浆或血清。
根据一些实施方式,本发明的方法进一步包括扩大所提供的免疫细胞。根据一些实施方式,所述扩大包括所述免疫细胞的刺激,并且所述方法进一步包括培养足以使至少50%的所提供的免疫细胞进入静息状态的时间段。根据一些实施方式,所述进一步培养持续1和7天之间。根据一些实施方式,所述刺激包括活化所述免疫细胞。根据一些实施方式,所述刺激是通过CD3、CD28、促细胞分裂原、生长因子和细胞因子中的至少一个进行的。
根据一些实施方式,所述接触是使所述免疫细胞与所述分子或分子的组合孵育。根据一些实施方式,所述第一免疫细胞是多种免疫细胞,并且所述第一免疫细胞是单独分裂和培养的;不同的分子或分子的组合与所分裂的免疫细胞的每一种接触,并且实现最大增加或减少的分子或分子的组合被接触。根据一些实施方式,所述第二免疫细胞是多种免疫细胞,并且所述第二免疫细胞被分裂并与不同的分子或分子的组合接触并按顺序向所述对象给予。根据一些实施方式,所述按顺序给予到达所述对象中的至少一个部位并且通过至少一种给予方式进行。
根据一些实施方式,神经递质的类似物是神经递质受体激动剂或神经递质受体拮抗剂。根据一些实施方式,所述神经递质或其类似物选自:多巴胺、谷氨酸、多巴胺受体激动剂、谷氨酸/AMPA/NMDA受体激动剂、谷氨酸/AMPA/NMDA受体拮抗剂、和多巴胺受体拮抗剂。根据一些实施方式,所述多巴胺受体激动剂选自多巴胺D1/5受体激动剂、多巴胺D2受体激动剂、多巴胺D3受体激动剂、和多巴胺D4受体激动剂。根据一些实施方式,所述多巴胺D1/5受体激动剂选自多巴胺、非诺多泮(fenoldopam)、非诺多潘(corlopam)、A77636、和SKF38393。根据一些实施方式,所述多巴胺D2受体激动剂是舒马尼罗(sumanirole)。根据一些实施方式,所述多巴胺D3受体激动剂选自PD 128907和7-OH-DPAT。根据一些实施方式,所述多巴胺D4受体激动剂选自PD 168077和A412997。根据一些实施方式,所述谷氨酸/AMPA/NMDA受体激动剂选自谷氨酸、AMPA和NMDA。根据一些实施方式,所述谷氨酸/AMPA/NMDA受体拮抗剂选自CNQX、MK801。根据一些实施方式,所述多巴胺受体拮抗剂选自多巴胺D1/5受体拮抗剂、多巴胺D2受体拮抗剂、多巴胺D3受体拮抗剂、和多巴胺D4受体拮抗剂。根据一些实施方式,所述多巴胺D1/5受体拮抗剂是SCH39166。根据一些实施方式,所述多巴胺D2受体拮抗剂是L-741626。根据一些实施方式,所述多巴胺D3受体拮抗剂是NGB 2904。根据一些实施方式,所述多巴胺D4受体拮抗剂是L-741742。
根据一些实施方式,所述神经肽或其类似物选自GnRH-I、GnRH-II、CGRP、生长抑素、和神经肽Y。根据一些实施方式,所述电压门控离子通道选自电压门控钠通道、钙通道、钾通道(Kv)和氯通道。根据一些实施方式,所述电压门控离子通道是电压门控钾通道。根据一些实施方式,所述电压门控钾通道是亚家族A的钾电压门控通道。根据一些实施方式,所述亚家族A的钾电压门控通道是Kv1.1。根据一些实施方式,所述电压门控离子通道的调节剂是离子通道阻断剂。根据一些实施方式,所述离子通道拮抗剂是电压门控Kv1.l离子通道阻断剂。根据一些实施方式,所述Kv1.1离子通道阻断剂选自树眼镜蛇毒素K(DTX-K)和抗Kv1.1阻断抗体。
根据一些实施方式,所述给予包括选择和给予第二接触的免疫细胞的亚群。根据一些实施方式,给予所述接触的第二免疫细胞包括给予2X10^6与10^9个之间的免疫细胞。根据一些实施方式,所述给予包括重复给予接触的免疫细胞。根据一些实施方式,所述给予包括无限期地(indefinitely)给予。
根据一些实施方式,所述第一免疫细胞在步骤b之前已经被冷冻和解冻。根据一些实施方式,被冷冻的免疫细胞在包含人血浆或血清的冷冻培养基中冷冻。
根据一些实施方式,所述治疗是所述疾病、状况、损伤或创伤的一线治疗或专有(exclusive)治疗。根据一些实施方式,所述治疗在所述疾病、状况、损伤或创伤的不同疗法之前、期间、与其同时或在其之后。
根据一些实施方式,所述免疫细胞的免疫治疗潜力是所述细胞治疗存在或疑似是次优的T细胞数量、活性或两者的疾病、状况、创伤或损伤的潜力。根据一些实施方式,所给予的细胞在所述对象中执行以下功能中的至少一种:
a.杀死致病细胞;
b.杀死传染性生物体;
c.治愈所述疾病或状况;
d.修复组织或器官;
e.替换受损的细胞,或组织;
f.补偿损失或缺陷;
g.预防所述疾病或状况;和
h.使组织或器官再生。
根据一些实施方式,所述试剂盒用于选择用于提高治疗性免疫细胞潜力的分子。根据一些实施方式,所述试剂盒用于在神经免疫疗法期间提高免疫细胞功能。根据一些实施方式,所述试剂盒用于确定对其有需要的对象是否适合神经免疫疗法。根据一些实施方式,所述试剂盒用于治疗对其有需要的对象中存在或疑似是次优的T细胞活性、数量或两者的疾病、状况、创伤或损伤或预防其复发。
根据一些实施方式,所述PD-1检测剂是抗PD-1抗体。根据一些实施方式,所述PD-1检测剂包括标签。根据一些实施方式,所述标签是荧光标签。
根据一些实施方式,本发明的试剂盒包含所述分子中的至少两种。根据一些实施方式,所述神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂以至多10^-7摩尔(M)的浓度被提供。
根据一些实施方式,所述试剂盒进一步包含至少一种神经递质或其类似物、至少一种神经肽或其类似物、和至少一种电压门控离子通道的调节剂的至少一种组合。根据一些实施方式,所述试剂盒进一步包含组织培养板,其中所述板的单独孔容纳单独的分子或分子的组合。
根据另一方面,提供了选择适合过继性免疫疗法的对象的方法,所述方法包括,
a.提供健康的免疫细胞;
b.将所述健康的免疫细胞与对象的血浆或血清接触;和
c.测量所述免疫细胞的存活;
其中所述健康的免疫细胞的存活的降低指示在所述对象的身体内,其免疫细胞暴露于其血浆或血清内的因子所诱导的有害作用,因此所述对象适合过继性免疫疗法。
根据另一方面,提供了在对其有需要的对象中的免疫疗法的方法,所述方法包括:
a.提供来自所述对象的免疫细胞;
b.在包含来自健康的同种异体个体的血浆或血清的培养基中培养所述免疫细胞;
c.将培养的免疫细胞返回给所述对象;
从而在所述对其有需要的对象中执行免疫疗法。
根据另一方面,提供了选择适合免疫疗法的对象的方法,所述方法包括:
a.提供免疫细胞;
b.在包含来自所述对象的血浆或血清的培养基中培养所述免疫细胞;和
c.监测所述免疫细胞的存活;
其中与在不包含来自所述对象的血浆或血清的培养基中所培养的免疫细胞相比,所述免疫细胞的存活的降低指示所述对象适合免疫疗法。
根据另一方面,提供了用于储存用于免疫疗法的免疫细胞的方法,所述方法包括在包含人血浆或血清的培养基中培养或冷冻免疫细胞。
根据一些实施方式,所述人血浆或血清来自提供所述免疫细胞的对象。根据一些实施方式,所述人血浆或血清来自健康的同种异体个体。
根据一些实施方式,所述免疫细胞来自健康供体。根据一些实施方式,所述免疫细胞是大的增殖T细胞。根据一些实施方式,所述免疫细胞是多种免疫细胞,并且其中降低的存活包括存活的免疫细胞的数量减少至少30%。根据一些实施方式,所述培养持续至少两天半。根据一些实施方式,所述免疫疗法是神经免疫疗法并且包括本发明的任一种方法。
根据下文给出的详细描述,本发明的进一步的实施方式和全部适用范围将变得显而易见。然而,应当理解,详细描述和具体实例虽然指示出了本发明的优选实施方式,但仅作为示例给出,因为通过此详细说明,本发明的精神和范围内的各种变化和修改对于本领域技术人员来说将变得显而易见。
附图说明
本发明的一些实施方式在此仅通过示例并参考附图来描述。现在详细地具体参考附图,要强调的是细节是通过实例的方式并且出于对本发明的实施方式的示例性讨论的目的来显示的。对此,描述连同附图使本领域技术人员清楚可以如何实践本发明的实施方式。
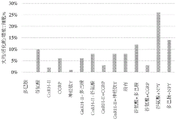
图1:神经递质增强癌症患者T细胞的增殖。条形图显示了在与各种神经递质或神经递质的组合培养60小时后肝癌患者L.F.的CD3阳性细胞的数量。
图2A-图2E:神经递质增加了癌症患者的T细胞的数量。(A-C)点图显示了患者L.F.的T细胞的前向散射(forward scatter)(大小)和杂乱散射(side scatter)(粒度)。显示了对照未处理(2A)、谷氨酸处理(2B)和多巴胺+NPY处理(2C)的T细胞。提供了非健康的(上框)、小且可能未活化的和非增殖的(中三角形)以及大且活跃的(下四边形)细胞的百分比。(2D)条形图显示了患者L.F.的T细胞的表面上CD25的平均表达。(2E)条形图显示了患者A.G.的T细胞的百分比,这些T细胞是大的、可能被活化的和增殖的T细胞。
图3A-图3C:神经递质降低癌症患者T细胞上的PD-1。条形图显示了(3A)患者L.F.的T细胞上的PD-1的细胞表面表达的水平(由各自的PD-1荧光染色的几何平均值反映)、(3B)来自患者L.F.的PD-1阳性的T细胞的百分比、和(3C)来自患者A.G.的T细胞上的PD-1的相对表达。
图4A-图4E:神经递质提高癌症杀伤能力,即癌症患者的T细胞的抵抗癌症的细胞毒性。条形图显示了(4A)与患者L.F.的T细胞共培养4天后培养的HepG2细胞的数量、(4B)与患者L.F.的T细胞共培养1周后培养的Huh7细胞的数量、(4C)与患者L.F.的T细胞共培养1周后活的Huh7细胞的百分比、(4D)与患者L.F.的T细胞共培养1周后坏死的Huh7细胞的百分比、和(4E)与Huh7细胞共培养1周后培养的T细胞的数量。
图5A-图5I:在体外保持人细胞的生长培养基中用人血浆代替胎牛血清(FCS)。对生长在含有FCS的培养物中(5A)5天和(5C)9天的细胞、生长在含有健康对象(血液供体)的人血浆的培养物中(5B)5天和(5D)9天的细胞、和生长在含有癌症患者的血浆的培养物中(5E)5天和(5F)9天的细胞的前向和杂乱散射FACS分析的代表性点图。表格总结了来自健康供体的总T细胞以及小和大的T细胞在含有FCS或来自健康对象和活的癌症对象的人血浆的组织培养基中培养(5G)2.5天和(5H)6天的存活。(5I)条形图显示了在培养6天后大的且可能的增殖性T细胞的存活。
具体实施方式
本发明在一些实施方式中提供了过继性神经免疫疗法、选择适合过继性神经免疫疗法的对象、选择用于提高治疗性免疫细胞潜力的分子或分子的组合、以及降低免疫细胞的表面上的PD-1表达的方法,包括使免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触。还提供了包含那些分子中的至少一种、或包含那些分子中的至少两种,和任选地PD-1检测剂的试剂盒。
通过第一方面,提供了选择用于提高治疗性免疫细胞潜力的分子的方法,所述方法包括:
a.提供免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的程序性细胞死亡1(PD-1)表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
其中PD-1表达的降低、所述免疫细胞的增殖的增加、和癌细胞死亡的增加指示所述至少一种分子提高了所述免疫细胞的治疗潜力。
通过另一方面,提供了选择用于提高治疗性免疫细胞潜力的分子的组合的方法,所述方法包括:
a.提供免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的PD-1表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对至少一种细胞因子的分泌;
xi.所述免疫细胞对至少一种治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
其中PD-1表达水平或功能水平的降低、单独或共培养的所述免疫细胞的增殖的增加、癌细胞死亡的增加、ζ链表达的增加、迁移的增加、细胞因子分泌的增加、粘附的增加、归巢的增加、至少一种治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平的降低、或参与过程ii至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平的提高中的至少一个指示至少两种分子的组合提高了所述免疫细胞的治疗潜力。
通过另一方面,提供了选择适合过继性神经免疫疗法的对象的方法,所述方法包括,
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的程序性细胞死亡1(PD-1)表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
其中PD-1表达水平或功能水平的降低、增殖的增加、癌细胞死亡的增加及其组合中的至少一个指示所述对象适合过继性神经免疫疗法。
通过另一方面,提供了选择适合过继性神经免疫疗法的对象的方法,所述方法包括,
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的PD-1表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对至少一种细胞因子的分泌;
xi.所述免疫细胞对至少一种治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
其中PD-1表达水平或功能水平的降低、单独或共培养的所述免疫细胞的增殖的增加、癌细胞死亡的增加、ζ链表达的增加、迁移的增加、细胞因子分泌的增加、粘附的增加、归巢的增加、至少一种治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因的表达水平或功能水平的降低、或参与过程ii至xi的至少一种蛋白质或基因的表达水平或功能水平的提高中的至少一个指示所述对象适合过继性神经免疫疗法。
在一些实施方式中,本发明的方法在体外执行。然而,应当理解,不能在体外执行任何包括向对象给予的步骤。在一些实施方式中,本发明方法的所有不包括向对象给予的步骤均在体外执行。在一些实施方式中,与癌细胞的共培养可以是与任何患病细胞的共培养。在一些实施方式中,患病细胞是被传染性生物体感染的细胞。在一些实施方式中,本发明的测量还可以是测量与免疫细胞共培养的患病细胞的细胞死亡。本文描述的本发明的所有方法也可以包括此测量作为可以执行的测量之一。
通过另一方面,提供了在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使第一免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的程序性细胞死亡1(PD-1)表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
d.提供与第一免疫细胞来源相同的第二免疫细胞;
e.使第二免疫细胞与至少一种分子接触,其中所述至少一种分子降低第一免疫细胞中的PD-1表达水平或功能水平、增加第一免疫细胞的增殖、增加与第一免疫细胞共培养的癌细胞死亡或其组合;和
f.将接触的第二免疫细胞向所述对象给予;
从而在所述对其有需要的对象中执行过继性神经免疫疗法。
通过另一方面,提供了在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使第一免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的PD-1表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对至少一种细胞因子的分泌;
xi.所述免疫细胞对至少一种治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
d.提供与第一免疫细胞来源相同的第二免疫细胞;
e.使第二免疫细胞与所述至少两种分子接触,其中所述至少两种分子降低第一免疫细胞中的PD-1表达水平或功能水平、增加第一免疫细胞的增殖、增加仅与第一免疫共细胞培养的癌细胞死亡或共培养的癌细胞死亡、增加第一免疫细胞中的ζ链表达、增加第一免疫细胞的迁移、增加第一免疫细胞对细胞因子的分泌、增加第一免疫细胞的粘附、增加第一免疫细胞的归巢、增加第一免疫细胞对至少一种治疗性蛋白质的分泌、降低参与过程i的至少一种蛋白质或基因在第一免疫细胞中的表达水平或功能水平、提高参与过程ii至xi的至少一种蛋白质或基因在第一免疫细胞中的表达水平或功能水平或其组合;和
f.将接触的第二免疫细胞向所述对象给予;
从而在所述对其有需要的对象中执行过继性神经免疫疗法。
通过另一方面,提供了在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使第一免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的PD-1表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对至少一种细胞因子的分泌;
xi.所述免疫细胞对至少一种治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
d.提供与第一免疫细胞来源相同的至少第二和第三免疫细胞;
e.使至少第二免疫细胞和第三免疫细胞与不同的至少一种分子接触,其中所述至少一种分子降低第一免疫细胞中的PD-1表达水平或功能水平、增加第一免疫细胞的增殖、增加仅与第一免疫共细胞培养的癌细胞死亡或共培养的癌细胞死亡、增加第一免疫细胞中的ζ链表达、增加第一免疫细胞的迁移、增加第一免疫细胞对细胞因子的分泌、增加第一免疫细胞的粘附、增加第一免疫细胞的归巢、增加所述免疫细胞对至少一种治疗性蛋白质的分泌、降低参与过程i的至少一种蛋白质或基因在第一免疫细胞中的表达水平或功能水平、提高参与过程ii至xi的至少一种蛋白质或基因在第一免疫细胞中的表达水平或功能水平或其组合;和
f.至少将至少接触的第二免疫细胞给予所述对象并在随后将接触的第三免疫细胞给予所述对象;
从而在所述对其有需要的对象中执行过继性神经免疫疗法。
通过另一方面,提供了与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触的免疫细胞在对其有需要的对象中用于过继性神经免疫疗法的用途。通过另一方面,提供了与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触的免疫细胞用于治疗、预防对其有需要的对象中具有或疑似具有次优T细胞活性的疾病、状况、创伤或损伤或预防其复发的用途。
在一些实施方式中,接触的细胞包含以下中的至少一个:与癌细胞共培养时降低PD-1表达水平或功能水平,增加增殖;和对与其共培养的癌细胞的增加的细胞毒作用。在一些实施方式中,接触的细胞与神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的组合接触。在一些实施方式中,所组合的接触的细胞包含以下中的至少一个:与癌细胞共培养时PD-1表达水平或功能水平降低,增殖增加;和对与其共培养的癌细胞的细胞毒性作用增加、单独培养时增殖增加、CD3ζ链的表达增加、增加的迁移、增加的粘附、增加的归巢、增加的穿透、至少一种细胞因子的分泌增加、至少一种治疗性蛋白质的分泌增加、参与PD-1表达和/或功能的至少一种蛋白质或基因的表达水平或功能水平降低、参与和癌细胞共培养的增殖的至少一种蛋白质或基因的表达水平或功能水平提高、对癌细胞的细胞毒性作用、培养中的增殖、CD3ζ链的表达、迁移、粘附、归巢、穿透、至少一种细胞因子的分泌、和至少一种治疗性蛋白质的分泌。
在一些实施方式中,接触的细胞与通过本发明方法中的一种选择的分子或分子的组合接触。
在一些实施方式中,第二免疫细胞与引起最大的经测量的作用的分子或分子的组合接触。在一些实施方式中,第二免疫细胞与引起最大的经测量的和/或期望的作用的分子或分子的组合接触,所述作用与所述细胞的有益活性的增加相关、或导致所述细胞的有益活性增加,并导致其治疗潜力增加。在一些实施方式中,第二免疫细胞与引起最大的经测量的和/或期望的作用的分子或分子的组合接触,并且第三免疫细胞与具有第二大作用的分子组合的分子或分子的组合接触。在一些实施方式中,第二免疫细胞与对一个测量的标准产生最大作用的分子或分子的组合接触,并且第三免疫细胞与对不同测量的标准具有最大作用的分子组合的分子接触。在一些实施方式中,将第四或更多免疫细胞与不同的分子或分子的组合接触并按顺序给予。
在一些实施方式中,所述至少一种分子是至少一种神经递质或其类似物。在一些实施方式中,所述至少一种分子是至少一种神经肽或其类似物。在一些实施方式中,所述至少一种分子是至少一种电压门控离子通道的调节剂。
在一些实施方式中,两种分子或分子的组合不仅仅是神经递质或其类似物。在一些实施方式中,两种分子或分子的组合不仅仅是神经肽或其类似物。在一些实施方式中,两种分子或分子的组合不仅仅是神经递质或其类似物,或者不仅仅是神经肽或其类似物。在一些实施方式中,两种分子或分子的组合是至少一种神经递质和一种神经肽。在一些实施方式中,两种分子或分子的组合是至少一种神经递质和一种电压门控离子通道的调节剂。在一些实施方式中,两种分子或分子的组合是至少一种神经肽和一种电压门控离子通道的调节剂。
在一些实施方式中,本发明的方法用于选择适合改善的免疫疗法的对象,其中免疫细胞来自所述对象。在一些实施方式中,本发明的方法用于选择可受益于过继性神经免疫疗法的对象,其中免疫细胞来自所述对象。在一些实施方式中,本发明的方法用于在对其有需要的对象中的免疫治疗期间提高免疫细胞功能。
在一些实施方式中,所述测量是测量所述免疫细胞的表面上的程序性细胞死亡1(PD-1)表达水平,并且其中PD-1表达水平的降低指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述测量是测量所述免疫细胞的表面上的程序性细胞死亡1(PD-1)表达水平,并且其中PD-1表达水平的降低指示所述对象适合改善的免疫疗法。在一些实施方式中,所述测量是测量所述免疫细胞上的PD-1表达水平。在一些实施方式中,所述测量是测量所述免疫细胞中的PD-1功能水平。测量PD-1功能是本领域公知的,并且测量PD-1功能的方法包括但不限于测量下游标志物,如IL-2和TNF-a,以及PD-1报道基因测定,如采用NFAT(活化T细胞核因子)响应元件的测定。
在一些实施方式中,所述测量是测量与癌细胞共培养的免疫细胞的增殖。在一些实施方式中,所述测量是测量单独培养的免疫细胞的增殖。增殖可以通过本领域已知的任何手段来测量,包括但不限于通过FACS、细胞分选、显微镜下的细胞计数、自动细胞计数器,或通过检测与细胞数量成比例增加的各种标志物的水平。在一些实施方式中,增加的增殖指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述测量是测量与所述免疫细胞共培养的癌细胞的细胞死亡。在一些实施方式中,死的癌细胞的数量被测量。在一些实施方式中,癌细胞死亡的速率被测量。在一些实施方式中,对死亡速率和死细胞数量两者进行计数。测量细胞死亡是本领域公知的,并且可以通过但不限于诸如碘化丙啶染色、亚甲蓝染色、Hoechst染色、或本领域已知的任何活体/死体测定的测定来执行。在一些实施方式中,共培养的癌细胞的细胞死亡增加指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述测量是测量CD3ζ链表达水平。在一些实施方式中,所述测量是测量蛋白质或mRNA表达。测量蛋白质、基因和/或mRNA表达的方法是本领域公知的,并且可以采用任何已知的方法。此类方法的非限制性实例包括实时PCR、测序、蛋白质印迹法、RNA印迹法、和ELISA。在一些实施方式中,提高的CD3ζ链表达水平指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述测量是测量所述免疫细胞的迁移、粘附、归巢和穿透中的至少一个。在一些实施方式中,所述测量是测量所述免疫细胞的迁移。在一些实施方式中,所述测量是测量所述免疫细胞的粘附。在一些实施方式中,所述测量是测量所述免疫细胞的归巢。在一些实施方式中,所述测量是测量所述免疫细胞的穿透。在一些实施方式中,迁移包括自发迁移、趋化迁移和向癌细胞和/或组织迁移中的至少一个。测量归巢、粘附、迁移和穿透的方法是本领域公知的,并且可以使用任何已知方法。此类方法的非限制性实例包括Boyden室测定、间隙封闭(Gap Closure)测定、和板结合测定。在一些实施方式中,免疫细胞的增加的迁移、粘附、归巢或穿透指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述测量是测量所述免疫细胞对至少一种细胞因子的分泌。在一些实施方式中,所述细胞因子是促炎细胞因子。在一些实施方式中,所述细胞因子是抗炎细胞因子。在一些实施方式中,所述细胞因子是促炎或抗炎细胞因子。在一些实施方式中,细胞因子分泌通过ELISA测量。在一些实施方式中,增加的细胞因子分泌通过蛋白质印迹法测量。在一些实施方式中,所述免疫细胞对至少一种细胞因子的分泌指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述测量是测量所述免疫细胞对至少一种治疗分子的分泌。在一些实施方式中,所述治疗性分子是治疗性蛋白质。如本文所用,“治疗分子”是指由免疫细胞产生的对分泌它的同一细胞(自分泌)或对其它细胞(旁分泌)具有有益作用,从而增强所述免疫细胞的治疗潜力的分子。治疗分子的实例包括但不限于生长因子、细胞因子、金属蛋白酶、基质降解酶和粒酶。在一些实施方式中,所述免疫细胞对至少一种治疗分子的增加的分泌指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述测量是测量参与上述过程的至少一种基因或蛋白质的表达水平、或功能水平、或状态,其证明免疫细胞增强。在一些实施方式中,那些过程是i至xi的过程。测量蛋白质、基因和/或mRNA表达的方法是本领域公知的并且可以采用任何已知的方法。此类方法的非限制性实例包括实时PCR、测序、蛋白质印迹法、RNA印迹法、和ELISA。参与这些过程的基因和蛋白质也是公知的。例如,已知粘附分子,如整联蛋白还有ICAM参与粘附和归巢,Ki67和PCNA是已知的增殖标志物,并且细胞因子基因表达的上调是增加的细胞因子分泌的标志物。测量蛋白质功能也是本领域公知的并且将根据该蛋白质而变化。在某些情况下,可以通过检查活化标志物,如分子的磷酸化或定位来测量蛋白质功能。测量蛋白质功能的测定也是蛋白质依赖性的并且是本领域已知的,并且可以包括但不限于粘附测定、细胞杀伤测定、增殖测定和迁移测定。在一些实施方式中,所述免疫细胞对至少一种细胞因子的分泌指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。在一些实施方式中,参与共培养的免疫细胞的增殖、共培养的癌细胞的细胞死亡、增殖、CD3ζ链表达、迁移、粘附、归巢、穿透、至少一种细胞因子的分泌、或至少一种治疗性蛋白质的分泌的至少一种基因或蛋白质的增加的表达水平、或功能水平、或状态指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。在一些实施方式中,参与PD-1表达或功能的至少一种基因或蛋白质的降低的表达水平、或功能水平、或状态指示所述至少一种分子提高了所述免疫细胞对癌症免疫疗法的适用性、提高了所述免疫细胞的免疫治疗潜力、提高了所述免疫细胞对任何疾病、损伤、或创伤的免疫治疗的适用性,其中有益的免疫细胞的提高或增强的功能能够改善所述对象的状况。每种可能性代表本发明的单独实施方式。
通过另一方面,提供了治疗、预防对其有需要的对象中具有或疑似具有次优T细胞活性的疾病、状况、创伤或损伤或预防其复发的方法,所述方法包括:
a.提供来自对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子接触,其中所述分子实现以下中的至少一个:
i.降低所述免疫细胞上的PD-1表达水平或功能水平;
ii.增加与和癌症相关的癌细胞共培养的所述免疫细胞的增殖;和
iii.增加所述免疫细胞的细胞毒性;和
c.将接触的免疫细胞向所述对象给予;
从而治疗、预防疾病、状况、创伤或损伤或预防其复发。
通过另一方面,提供了治疗、预防对其有需要的对象中具有或疑似具有次优T细胞活性的疾病、状况、创伤或损伤或预防其复发的方法,所述方法包括:
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与通过本发明的方法选择的至少一种分子接触;和
c.将接触的免疫细胞向所述对象给予;
从而治疗、预防疾病、状况、创伤或损伤或预防其复发。
通过另一方面,提供了治疗、预防对其有需要的对象中具有或疑似具有次优T细胞活性的疾病、状况、创伤或损伤或预防其复发的方法,所述方法包括:
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与通过本发明的方法选择的至少两种分子接触;和
c.将接触的免疫细胞向所述对象给予;
从而治疗、预防疾病、状况、创伤或损伤或预防其复发。
在一些实施方式中,所述免疫细胞与降低所述免疫细胞上PD-1表达水平的至少一种分子接触。在一些实施方式中,所述方法进一步包括选择所述至少一种神经递质的步骤。在一些实施方式中,所述选择是通过本发明方法中的一种进行的。
通过另一方面,提供了降低免疫细胞的细胞表面上的PD-1表达水平的方法,所述方法包括向所述免疫细胞给予选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子。
通过另一方面,提供了选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子用于降低免疫细胞的细胞表面上PD-1表达水平的用途。
在一些实施方式中,对所述免疫细胞的给予是在体外执行的。在一些实施方式中,对所述免疫细胞的给予是离体执行的。在一些实施方式中,对所述免疫细胞的给予是在体内执行的。在一些实施方式中,所述免疫细胞是免疫系统的任意细胞。在一些实施方式中,所述免疫细胞选自T细胞、自然杀伤(NK)细胞、B细胞、树突细胞、巨噬细胞、和神经胶质细胞。在一些实施方式中,所述免疫细胞选自T细胞和NK细胞。在一些实施方式中,所述免疫细胞是免疫系统的表达PD-1的任意细胞。在一些实施方式中,所述免疫细胞是T细胞。在一些实施方式中,所述T细胞是大的增殖T细胞。技术人员将能够通过诸如显微术、FACS和细胞分选的技术区分大的和较小的T细胞。当使用流式细胞仪时,前向散射或前向和杂乱散射可用于区分这些大小不同的T细胞。大T细胞被认为是T细胞母细胞,并且这些是活化和增殖的T细胞。这些大T细胞具有更高的前向散射,并且也往往具有通过杂乱散射测量的更低的粒度。以这种方式,具有高前向散射和较低杂乱散射的大的增殖的T细胞群可以很容易地鉴别,如图5A-图5F所示例。在一些实施方式中,所述免疫细胞是有益T细胞。在一些实施方式中,所述免疫细胞来自患有疾病、状况、创伤或损伤的对象,所述疾病、状况、创伤或损伤的特征在于,或者其中存在或疑似是次优的T细胞数量和/或活性,或者其中通过增加的有益T细胞的数量和/或功能实现了临床益处。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述免疫细胞来自患有癌症的对象。在一些实施方式中,所述免疫细胞来自健康供体。在一些实施方式中,所述免疫细胞具有再生或修复潜力。在一些实施方式中,所述免疫细胞来自患有疾病、状况、损伤或创伤的对象的亲属,所述疾病、状况、损伤或创伤的特征在于,或者其中存在或疑似是次优的T细胞活性或数量,或者可受益于提高的或增强的有益免疫细胞的功能。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述免疫细胞对于患有疾病或状况的对象是自体的,所述疾病或状况的特征在于,或者其中存在或疑似是次优的有益T细胞活性或数量。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述免疫细胞对于所述对象是同种异体的。在一些实施方式中,所述免疫细胞来自无限增殖化免疫细胞系。在一些实施方式中,所述免疫细胞来自通用供体细胞系。这样的品系将被繁殖以用于向对其有需要的任何对象进行治疗性供给。在一些实施方式中,所述通用供体细胞系不表达,或者低表达MHC分子。在一些实施方式中,所述MHC分子是MHC II类分子。在一些实施方式中,通用供体系没有免疫原性或者是低免疫原性。在一些实施方式中,所述细胞系是健康的免疫细胞系。在一些实施方式中,所述细胞系是非免疫原性细胞系。在一些实施方式中,所述免疫细胞没有免疫原性。在一些实施方式中,所述免疫细胞没有经过遗传修饰。在一些实施方式中,所述免疫细胞已被遗传修饰。在一些实施方式中,所述遗传修饰提高所述免疫细胞的治疗潜力。在一些实施方式中,所述遗传修饰降低所述免疫细胞的免疫原性。本发明的方法可对在给予时可与为对象提供益处的任何免疫细胞一起使用。在一些实施方式中,所述免疫细胞是培养的。在一些实施方式中,所述免疫细胞在对象中。在一些实施方式中,本发明的方法是在体外执行的。
如本文所用,术语“有益T细胞”是指在通过自身或与身体的其它细胞进行组合来克服病理状况和/或改善对象的状况方面可使所述对象受益的T细胞。在一些实施方式中,所述有益T细胞通过根除引起疾病的传染性生物体或癌症,或通过以再生或修复性治疗细胞操作/充当再生或修复治疗细胞而发挥作用。在一些实施方式中,所述有益T细胞通过根除引起疾病的传染性生物体或癌症发挥作用。在一些实施方式中,所述有益T细胞充当再生或修复性治疗细胞/作为再生或修复性治疗细胞操作。在一些实施方式中,有益T细胞不是自身免疫T细胞、癌性T细胞,也不是可能伤害对象的任何其它病理T细胞。在一些实施方式中,有益T细胞是健康T细胞。
如本文所用,“神经递质”是由神经元分泌以与其它细胞通信的小分子。在一些实施方式中,神经递质是化学品。在一些实施方式中,神经递质具有至多1、2、3、4或5个氨基酸的大小。每种可能性代表本发明的单独实施方式。在一些实施方式中,神经递质具有至多1个氨基酸的大小。在一些实施方式中,神经递质不包含氨基酸。在一些实施方式中,神经递质是天然存在的分子。
如本文所用,神经递质和/或神经肽的“类似物”是能够与神经递质或神经肽同源受体结合的任何分子。在一些实施方式中,所述类似物修饰受体功能。在一些实施方式中,所述类似物阻断所述受体。在一些实施方式中,所述类似物活化所述受体。在一些实施方式中,所述类似物是模拟物。在一些实施方式中,所述类似物是受体激动剂。在一些实施方式中,所述类似物是完全或部分受体拮抗剂。在一些实施方式中,所述类似物是受体激动剂或拮抗剂。在一些实施方式中,所述类似物是受体激动剂和拮抗剂。在一些实施方式中,所述类似物是结合所述受体的抗体。在一些实施方式中,所述类似物是受体阻断抗体。在一些实施方式中,所述类似物是受体活化抗体。在一些实施方式中,所述类似物的功能取决于情况(上下文,context)和/或特定的细胞和/或细胞状况。
术语“激动剂”通常是指在与天然配体相同的位点与受体结合并完全或部分地活化所述受体的分子、化合物或剂。术语“拮抗剂”通常是指在与激动剂相同的位点或另一位点与受体结合并实现以下中的一个或多个的分子、化合物或剂:不活化所述受体、干扰或阻断天然配体对所述受体的活化、和干扰或阻断受体激动剂对所述受体的活化。
术语“模拟物”通常是指与神经肽的受体结合并完全或部分地驾驭(激活,aviates)所述受体,进而诱导与所述神经肽相同的细胞功能的分子、化合物或剂。在一些实施方式中,所述模拟物像所述神经肽一样活化所述受体。在一些实施方式中,所述模拟物像所述神经肽一样阻断所述受体。
如本文所用,“神经肽”是由神经元分泌以与其它细胞通信的肽。在一些实施方式中,所述神经肽的长度为至少5、10、15、20、30、35或40个氨基酸。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述神经肽的长度至少为40个氨基酸。在一些实施方式中,所述神经肽的长度为至多40、50、60、70、80、90或100个氨基酸。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述神经肽是神经激素。如本文所用,“神经激素”是由神经元分泌以与其它靶细胞通信的激素。在一些实施方式中,所述靶细胞远离分泌细胞。
如本文所用,术语“免疫疗法”和“免疫细胞疗法”是同义词且可互换,并且是指通过向对象给予在所述对象中具有有益治疗活性的免疫细胞而对疾病障碍或状况的治疗。在一些实施方式中,所述免疫细胞攻击病理细胞。在一些实施方式中,所述免疫细胞杀伤所述病理细胞或传染性生物体。在一些实施方式中,所述免疫细胞来自所述对象。在一些实施方式中,所述免疫细胞被增强以提高它们诱导免疫应答的功效。在一些实施方式中,所述免疫细胞具有再生活性、修复活性、或保护活性。
如本文所用,术语“过继性神经免疫疗法”和“神经免疫疗法”是同义词且可互换,并且是指这样的的免疫疗法,其中免疫细胞与选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的分子接触以提高其治疗潜力,然后将改善的免疫细胞给予对其有需要的对象。在一些实施方式中,神经免疫疗法是过继性神经免疫疗法。在一些实施方式中,神经免疫疗法是细胞神经免疫疗法。神经免疫疗法不应被解释为仅在大脑中或神经元上执行的免疫疗法,而是用本文所述的分子对免疫细胞的处理。在一些实施方式中,本发明的方法用于选择用于神经免疫疗法的分子。在一些实施方式中,本发明的方法用于改善或增强免疫细胞,因此其可用于神经免疫疗法。在一些实施方式中,本发明的方法用于在神经免疫疗法期间改善或增强免疫细胞。在一些实施方式中,本发明的方法用于提高或增加免疫细胞数量,使得所述免疫细胞可用于神经免疫疗法。在一些实施方式中,本发明的方法用于在神经免疫疗法期间提高或增加免疫细胞数量。在一些实施方式中,本发明的方法用于选择适合神经免疫疗法的对象。
如本文所用,术语“治疗潜力”是指细胞治疗和/或预防疾病、障碍或病理状况以及改善对象的整体状况的能力。如本文所用,术语“免疫治疗潜力”和“治疗性免疫细胞潜力”是同义词,并且是指成为或变得对对象的病理具有治疗性的有益T细胞的定性和/或定量的治疗潜力。在一些实施方式中,治疗潜力包括杀伤病理细胞的能力、杀伤病原体的能力、增殖的能力、CD3ζ链的表达、迁移、细胞因子分泌、细胞粘附和细胞归巢中的至少一个。
在一些实施方式中,提高的治疗潜力是免疫细胞的提高的细胞毒性、免疫细胞的提高的增殖、免疫细胞响应靶标的提高的增殖、降低的PD-1表达、增加的CD3ζ链表达、增加的迁移、增加的细胞因子分泌、增加的细胞粘附和增加的归巢中的至少一个。在一些实施方式中,所述治疗潜力是再生、修复、替换、预防、或保护潜力中的任一种或其组合。
在一些实施方式中,降低的PD-1表达包括免疫细胞的表面上PD-1表达水平的降低。
在一些实施方式中,降低的PD-1表达包括表达PD-1的免疫细胞数量的减少。在一些实施方式中,降低的PD-1表达包括免疫细胞表面上PD-1表达水平的降低和表达PD-1的免疫细胞数量的降低。在一些实施方式中,降低的PD-1表达包括免疫细胞表面上PD-1表达水平的降低或表达PD-1的免疫细胞数量的降低。在一些实施方式中,降低的PD-1表达包括免疫细胞表面上PD-1表达水平的降低、表达PD-1的免疫细胞数量的降低或两者。在一些实施方式中,PD-1功能的降低包括降低的PD-1功能,或降低的所述细胞中与PD-1偶联的下游途径或分子的功能。
在一些实施方式中,细胞死亡的增加包括细胞凋亡、坏死或两者的增加。在一些实施方式中,细胞死亡的增加包括细胞凋亡的增加。在一些实施方式中,细胞死亡的增加包括坏死的增加。在一些实施方式中,细胞死亡的增加包括细胞凋亡和坏死的增加。
在一些实施方式中,免疫细胞的治疗潜力是其治疗具有或疑似具有次优T细胞数量和/或活性的疾病、状况、损伤或创伤的潜力。在一些实施方式中,免疫细胞的治疗潜力是其治疗以次优的T细胞数量和/或活性为特征的疾病、状况、损伤或创伤的潜力。在一些实施方式中,免疫细胞的治疗潜力是其治疗其中可通过增加的T细胞数量和/或活性实现临床益处的疾病、状况、损伤或创伤的潜力。在一些实施方式中,免疫细胞的治疗潜力是其在任何方面有益于患者的潜力。这样的益处可在临床上转化为对致病细胞或传染性生物体增加的杀伤,或对损失或缺陷的任何治愈、修复、替换、补偿,或改善患者的状况的再生或预防,或者可通过对致病细胞或传染性生物体增加的杀伤,或通过对损失或缺陷的任何治愈、修复、替换、补偿,或改善患者的状况的再生或预防而被记录(documented)。
在一些实施方式中,对其有需要的对象是能够以任何方式受益于本发明的方法或过继性神经免疫疗法的对象。在一些实施方式中,所述对象遭受具有或疑似具有次优T细胞数量和/或活性的疾病、状况、损伤或创伤。在一些实施方式中,所述对象遭受可受益于治疗性免疫细胞的疾病、状况、损伤或创伤。在一些实施方式中,所述对象遭受以次优的T细胞数量和/或活性为特征或与之相关的疾病、状况、损伤或创伤。在一些实施方式中,所述对象遭受其中可以通过T细胞活化实现临床益处的疾病、状况、创伤或损伤。在一些实施方式中,所述对象遭受其中可以通过增加有益T细胞的数量和/或功能实现临床益处的疾病、状况、创伤或损伤。如本文所用,“存在或疑似是次优T细胞活性或数量的疾病、状况、创伤或损伤”是任何疾病、障碍、状况或损伤,其导致遭受其的人的T细胞在至少一种T细胞功能和/或数量方面受损,或者由遭受其的人的在至少一种T细胞功能和/或数量方面受损的T细胞引起。如本文所用,“其中可通过增加的有益T细胞的数量和/或功能实现临床益处的疾病、状况、创伤或损伤”是以任何可测量的方式通过活化或增加疾病的遭受内的有益T细胞来改善的疾病。此类疾病和状况是本领域公知的并且可以通过测试来自对象的T细胞的至少一种特征,或通过测量外周血中或组织中的T细胞数量凭经验确定。在一些实施方式中,减少的T细胞数量在外周血中。在一些实施方式中,减少的T细胞数量在组织中。在一些实施方式中,减少的T细胞数量在受所述疾病、状况、创伤或损伤影响的组织中。此类T细胞功能的测试包括但不限于测量靶标的T细胞细胞毒性、测量T细胞炎性细胞因子分泌、测量T细胞趋化性、测量T细胞迁移能力、和测量T细胞CD3ζ链表达。
在一些实施方式中,所述疾病、创伤、损伤或状况是可由健康T细胞治疗的疾病或状况。在一些实施方式中,所述疾病、状况、创伤或损伤是可以通过免疫疗法治疗的疾病或状况。
如本文所用,术语“活化”是指T细胞通过其T细胞受体(TCR)的经典活化。在一些实施方式中,活化包括其它受体和/或途径的共同刺激。在一些实施方式中,所述其它受体和/或途径是本领域已知的。T细胞活化不应被认为包括通过过继性神经免疫疗法或本发明的方法对T细胞功能的增强。在一些实施方式中,所提供的细胞尚未使其TCR活化。
在一些实施方式中,所提供的细胞已使其TCR活化,但随后已培养足以使所述细胞恢复到静息状态的时间。在一些实施方式中,这发生在所述免疫细胞与所述分子接触之前。
在一些实施方式中,疾病、状况、创伤或损伤选自:癌症、传染病、遗传免疫缺陷、获得性免疫缺陷、退行性疾病、自身免疫疾病、代谢疾病、遗传疾病、神经或神经精神疾病、和器官移植后伴有免疫功能不全。在一些实施方式中,所述疾病是神经或神经精神疾病。在一些实施方式中,所述神经或精神疾病或损伤需要更好的有益T细胞功能。在一些实施方式中,所述神经或精神疾病选自:阿尔茨海默病、精神分裂症、昏迷、脑癌、肌萎缩性侧索硬化(ALS)、痴呆、癫痫、杭廷顿舞蹈病、脑膜炎、多发性硬化(MS)和帕金森病。在一些实施方式中,神经损伤选自神经系统轴突横切术(axotomy)和CNS创伤。
在一些实施方式中,疾病、状况、创伤或损伤是癌症。
在一些实施方式中,所述疾病是传染病。在一些实施方式中,所述传染病选自病毒感染、细菌感染、和真菌感染。在一些实施方式中,所述疾病是免疫缺陷。在一些实施方式中,所述免疫缺陷是获得性免疫缺陷。在一些实施方式中,所述免疫缺陷是遗传免疫缺陷。
在一些实施方式中,所述免疫缺陷是遗传免疫缺陷或获得性免疫缺陷。在一些实施方式中,所述免疫缺陷选自,T细胞缺陷、重度联合免疫缺陷症(SCID)、欧门综合征(Omennsyndrome)、软骨-毛发发育不全、获得性免疫缺陷综合征(AIDS)、迪乔治综合征、染色体断裂综合征、共济失调-毛细血管扩张、威斯科特-奥尔德里奇综合征、癌症诱发的免疫缺陷、化疗诱发的免疫缺陷、和糖皮质激素疗法诱发的免疫缺陷。
在一些实施方式中,所述疾病是自身免疫疾病。在一些实施方式中,所述疾病是自身免疫疾病,其中有益的T细胞可以改善对象的状况。在一些实施方式中,其中所述疾病是自身免疫疾病,所述对象的自身免疫细胞不应该用作有益的免疫细胞。在一些实施方式中,其中所述疾病是自身免疫疾病,可以使用所述对象的自身免疫细胞。在这样的实施方式中,所述自身免疫细胞仍然具有治疗功能,如“保护性自身免疫”。如本文所用,“保护性自身免疫”是指过继性免疫系统的细胞,主要是自身免疫T细胞,在主要对脑和/或脊髓的侵害或损伤后有助于组织的完整性,或促进其修复的状况。
在一些实施方式中,所述疾病是退行性疾病。退行性疾病的实例包括但不限于阿尔茨海默病、视网膜变性、帕金森病、黄斑变性、骨关节炎、肌营养不良、ALS、骨质疏松症和心脏病。
在一些实施方式中,所述疾病是代谢疾病。代谢疾病的实例包括但不限于糖尿病、胰岛素抗性、代谢综合征、线粒体疾病、和糖原贮积病。
在一些实施方式中,所述疾病是遗传疾病。遗传疾病的实例包括但不限于囊性纤维化、杭廷顿舞蹈病、唐氏综合症、肌营养不良、高歇病和地中海贫血。
如本文所用,“创伤”是指任何身体损伤或病变。在一些实施方式中,创伤是这样的损伤,其愈合包括向创伤部位募集免疫细胞或T细胞。在一些实施方式中,所述疾病、状况、损伤或创伤需要组织或器官修复、替换或再生,或递送将导致治疗活性的T细胞衍生因子。
在一些实施方式中,所述癌症是任何癌症。在一些实施方式中,所述癌症是实体癌症。在一些实施方式中,所述癌症是血癌。在一些实施方式中,所述癌症是头颈癌、黑素瘤、卵巢癌、前列腺癌、宫颈癌、肾细胞癌、肝结直肠癌、结直肠癌、肝细胞癌、肝癌、及其转移中的任一种。在一些实施方式中,所述癌症选自肝细胞癌和其它类型的肝癌。在一些实施方式中,所述癌症是肝癌。在一些实施方式中,所述癌症是癌。在一些实施方式中,所述癌症是肝细胞癌。在一些实施方式中,所述癌症是表达PD-1L的癌症。在一些实施方式中,所述癌症高度表达PD-1L。在一些实施方式中,所述对象先前已经经历基于PD-1的疗法。在一些实施方式中,基于PD-1的疗法是以下中的任一种:PD-1阻断抗体、PD-1配体(PD-1L)阻断抗体、和PD-1阻断。在一些实施方式中,基于PD-1的疗法是涉及PD-1/PD-1L轴的任何疗法。在一些实施方式中,所述对象对基于PD-1的疗法没有响应或响应低。在一些实施方式中,所述对象对基于PD-1的疗法有响应或高度响应。在一些实施方式中,所述对象先前未接受过任何抗癌疗法。在一些实施方式中,本发明的方法进一步包括标准癌症疗法。在一些实施方式中,本发明的方法进一步包括给予另一种抗癌治疗剂。在一些实施方式中,抗癌治疗剂是PD-1或PD-1L阻断抗体。
在一些实施方式中,本发明的方法是离体执行的。在一些实施方式中,本发明的方法是在体外执行的。在一些实施方式中,本发明的方法是在体内执行的。在一些实施方式中,本发明的方法是在免疫细胞生长培养基中执行的。在一些实施方式中,本发明的方法是在体液中执行的。在一些实施方式中,本发明的方法是在血液中执行的。在一些实施方式中,本发明的方法是在包含人血浆的溶液中执行的。在一些实施方式中,本发明的方法是在包含人血清的溶液中执行的。
在一些实施方式中,所述共培养的癌细胞是原代癌细胞。在一些实施方式中,所述共培养的癌细胞来自所述对象的癌症。在一些实施方式中,所述共培养的癌细胞来自所述患者的癌症的原代细胞的子代细胞或后代细胞。在一些实施方式中,所述原代细胞来自所述对象。在一些实施方式中,所述原代细胞来自所述对象的组织活检。在一些实施方式中,所述共培养的癌细胞是细胞系的细胞。在一些实施方式中,所述细胞系来自与所述对象的癌症类型相同的癌症。在一些实施方式中,所述细胞系是与所述对象的癌症类型相比另一种类型癌症的癌细胞系。在一些实施方式中,所述细胞系来自与所述对象的癌症相同的组织来源。在一些实施方式中,所述细胞系具有与所述对象的癌症相似的PD-1L表面水平。在一些实施方式中,尽管PD-1L表面水平相似,但所述癌细胞系细胞仍可被其活性通过神经免疫疗法程序提高的免疫细胞在体外根除。在一些实施方式中,所述共培养的癌细胞与所述对象的癌症无关。在一些实施方式中,所述对象没有癌症并且测量所述免疫细胞杀伤癌细胞的能力。本领域技术人员将理解,本发明的方法寻求确定免疫细胞是否以任何可能的方式得到改善。因此,如果所述方法与所述患者的状况无关,则可以使用监测所述免疫细胞的治疗潜力的任何方法。因此,即使对于没有癌症的对象,也可以测量癌症杀伤以检查所述免疫细胞的治疗潜力。
在一些实施方式中,所述提供包括提取体液。在一些实施方式中,所述提供包括从体液中分离免疫细胞。免疫细胞分离的方法是本领域公知的,并且包括例如Ficol分离、离心、FACS细胞分选和磁珠偶联抗体分离。在一些实施方式中,所述体液选自血液、血清、淋巴液、脑脊髓液、胃液、唾液、母乳、肿瘤分泌物、从实体器官中提取的流体以及精液。在一些实施方式中,所述体液是血液。在一些实施方式中,在从体液中分离免疫细胞后,将它们冷冻以备后用。在一些实施方式中,所述提供包括对冷冻的免疫细胞解冻。在一些实施方式中,所述免疫细胞在与至少一种分子接触之前被冷冻。在一些实施方式中,本发明的方法包括在给予前冷冻所述接触的免疫细胞。
在一些实施方式中,分离CD3阳性T细胞。在一些实施方式中,所提供的免疫细胞未被活化。在一些实施方式中,所提供的免疫细胞在接触之前未被预先活化。在一些实施方式中,分离无活性免疫细胞。在一些实施方式中,分离静息免疫细胞。在一些实施方式中,分离幼稚免疫细胞。在一些实施方式中,分离静息的幼稚无活性免疫细胞。在一些实施方式中,此活化是TCR的经典活化。在一些实施方式中,所提供的免疫细胞通过TCR被活化以诱导增殖和细胞数量,使其静息足以使所述免疫细胞恢复到静息的幼稚状态的时间段,然后用所述至少一种或至少两种分子处理。在一些实施方式中,所提供的免疫细胞对癌症是幼稚的。技术人员将理解,通过分离外周免疫细胞,如从血液中分离,假定所分离的大部分免疫细胞没有与癌症接触,因为它们没有归巢到癌症生态位。在一些实施方式中,本发明的方法进一步包括在执行接触之前从所提供的免疫细胞中选择未活化的免疫细胞。
在一些实施方式中,所提供的免疫细胞在接触之前在培养基中体外培养。在一些实施方式中,所述培养基是合适的细胞培养基。在一些实施方式中,所述培养基是免疫细胞培养基。在一些实施方式中,所述培养持续最多1小时、4小时、6小时、12小时、24小时、36小时、48小时、60小时、72小时、84小时或96小时。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述培养基是免疫细胞培养基。在一些实施方式中,所述培养持续足以扩大免疫细胞群的时间段。在一些实施方式中,在扩大后,进一步培养持续足以使至少50%、60%、70%、75%、80%、85%、90%、95%、97%、99%或100%的经扩大的免疫细胞进入静息、非活化和/或幼稚状态的时间段。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述进一步培养持续足以使至少50%的经扩大的免疫细胞进入静息状态的时间段。在一些实施方式中,足以使所述细胞恢复到静息、非活化和/或幼稚状态的时间段为至少1、2、3、4、5、6或7天。每种可能性代表本发明的单独实施方式。在一些实施方式中,足以使所述细胞恢复到静息、非活化或幼稚状态的时间段在1和3、1和4、1和5、1和6、1和7、1和8、1之间和9以及1和10天之间。每种可能性代表本发明的单独实施方式。在一些实施方式中,足以使所述细胞恢复到静息状态的时间段在1和7天之间。
在一些实施方式中,所提供的免疫细胞是多种提供的免疫细胞。在一些实施方式中,所述方法进一步包括从第一提供的免疫细胞中选择免疫细胞的亚群。在一些实施方式中,所述亚群是T细胞。在一些实施方式中,所述亚群是CD4阳性T细胞。在一些实施方式中,所述亚群是CD8阳性T细胞。在一些实施方式中,所述亚群是未活化的免疫细胞。在一些实施方式中,所述亚群选自:效应T细胞、辅助T细胞、细胞毒性T细胞、调节T细胞、抑制T细胞、自然杀伤T细胞、炎性T细胞、记忆T细胞、γδT细胞、组织/器官浸润T细胞、肿瘤浸润T细胞、修复T细胞和促再生T细胞、以及黏膜相关T细胞。如本文所用,“修复T细胞”是指能够增强组织修复的T细胞的亚群。如本文所用,“促再生T细胞”是指能够增强组织再生的T细胞的亚群。在一些实施方式中,组织修复和/或再生是肌肉修复和/或再生。在一些实施方式中,修复和/或促再生T细胞表达Foxp3和CD4。
如本文所用,“静息状态”是指免疫细胞目前未被活化的状态。在一些实施方式中,静息状态是幼稚状态。在一些实施方式中,活化是TCR的经典活化。在一些实施方式中,T细胞活化包括CD25或CD69的表面表达增加。CD69是一种非常早期的活化标志物,并且可在TCR连接/活化的数小时内检测到,然后在48-72小时后表达消失。CD25是IL-2受体的α链,并且上调比CD69稍晚些——在第1天可检测到并在TCR连接后大致第2天上调。CD25保持高表达直到第4-5天,然后在第7天开始下降。到第11天,它回到基线。在一些实施方式中,T细胞活化包括选自CD25、CD69、CD44、CD137、CD154和CD27的至少一种表面分子的表面表达。在一些实施方式中,活化包括这些分子的高表面表达。在一些实施方式中,活化包括CD62L或CCR7的表面表达降低。
在一些实施方式中,本发明的方法进一步包括扩大所提供的免疫细胞。在一些实施方式中,本发明的方法进一步包括扩大所提供的第二免疫细胞。在一些实施方式中,执行扩大以增加之后将与本文所述的分子接触以增强免疫治疗潜力的细胞的数量。在一些实施方式中,扩大所述免疫细胞包括刺激所述免疫细胞。在一些实施方式中,扩大所述免疫细胞包括刺激所述免疫细胞并进一步培养所述免疫细胞一段时间,使得它们恢复到静息状态。在一些实施方式中,扩大所述免疫细胞包括刺激所述免疫细胞并进一步培养所述免疫细胞直到它们恢复到静息状态。在一些实施方式中,刺激所述免疫细胞包括使所述免疫细胞与选自细胞因子和生长因子的刺激分子接触。在一些实施方式中,刺激所述免疫细胞包括使所述免疫细胞与损伤/创伤诱导因子、应激诱导因子、T细胞活化酶、T细胞活化离子、病毒传播的(viral-borne)T细胞活化分子、细菌传播的(bacteria-borne)T细胞活化分子中的至少一种接触。在一些实施方式中,所述细胞因子是IL-2。在一些实施方式中,刺激所述免疫细胞包括活化所述免疫细胞。在一些实施方式中,刺激所述免疫细胞包括CD3刺激和CD28刺激中的至少一个。在一些实施方式中,刺激所述免疫细胞包括抗原刺激、促细胞分裂原刺激和细胞因子刺激中的至少一个。在一些实施方式中,所述刺激是通过CD3、CD28、促细胞分裂原、生长因子和细胞因子中的至少一种进行的。在一些实施方式中,刺激不是通过结合神经递质或神经肽受体的分子进行的。在一些实施方式中,刺激不是通过结合电压门控离子通道的分子进行的。在一些实施方式中,刺激不是通过结合神经递质或神经肽受体或电压门控离子通道的分子进行的。
在一些实施方式中,所述神经递质或其类似物选自:多巴胺、谷氨酸、多巴胺受体激动剂、多巴胺受体拮抗剂、谷氨酸受体激动剂、AMPA受体激动剂、NMDA受体激动剂、谷氨酸/AMPA/NMDA受体激动剂、谷氨酸受体拮抗剂、AMPA受体拮抗剂、NMDA受体拮抗剂、和谷氨酸/AMPA/NMDA受体拮抗剂。在一些实施方式中,所述神经递质或其类似物选自:多巴胺、谷氨酸、多巴胺受体激动剂、谷氨酸/AMPA/NMDA受体激动剂、谷氨酸/AMPA/NMDA受体拮抗剂、和多巴胺受体拮抗剂。在一些实施方式中,所述神经递质或其类似物选自:多巴胺、谷氨酸、多巴胺受体激动剂、和谷氨酸/AMPA/NMDA受体激动剂。
在一些实施方式中,所述神经递质类似物是多巴胺受体激动剂。在一些实施方式中,所述多巴胺受体激动剂选自多巴胺D1/5受体激动剂、多巴胺D2受体激动剂、多巴胺D3受体激动剂、和多巴胺D4受体激动剂。在一些实施方式中,所述多巴胺受体激动剂是多巴胺D1/5受体激动剂。在一些实施方式中,所述多巴胺受体激动剂是多巴胺D2受体激动剂。在一些实施方式中,所述多巴胺受体激动剂是多巴胺D3受体激动剂。在一些实施方式中,所述多巴胺受体激动剂是多巴胺D4受体激动剂。
在一些实施方式中,所述多巴胺D1/5受体激动剂选自非诺多泮、非诺多潘、A77636和SKF38393。在一些实施方式中,所述多巴胺D1/5受体激动剂选自非诺多泮、A77636和SKF38393。在一些实施方式中,所述神经递质是多巴胺。在一些实施方式中,多巴胺D1/5受体激动剂是非诺多泮。在一些实施方式中,所述多巴胺D1/5受体激动剂是A77636。
在一些实施方式中,所述多巴胺D1/5受体激动剂是SKF38393。
在一些实施方式中,所述多巴胺D2受体激动剂是舒马尼罗。在一些实施方式中,所述多巴胺D3受体激动剂选自PD 128907和7-OH-DPAT。在一些实施方式中,所述多巴胺D3受体激动剂是PD 128907。在一些实施方式中,所述多巴胺D3受体激动剂是7-OH-DPAT。在一些实施方式中,所述多巴胺D4受体激动剂选自PD 168077和A412997。在一些实施方式中,所述多巴胺D4受体激动剂是PD 168077。在一些实施方式中,所述多巴胺D4受体激动剂是A412997。
在一些实施方式中,所述神经递质类似物是多巴胺受体拮抗剂。在一些实施方式中,所述多巴胺受体拮抗剂选自多巴胺D1/5受体拮抗剂、多巴胺D2受体拮抗剂、多巴胺D3受体拮抗剂、和多巴胺D4受体拮抗剂。在一些实施方式中,所述多巴胺受体拮抗剂是多巴胺D1/5受体拮抗剂。在一些实施方式中,所述多巴胺受体拮抗剂是多巴胺D2受体拮抗剂。在一些实施方式中,所述多巴胺受体拮抗剂是多巴胺D3受体拮抗剂。在一些实施方式中,所述多巴胺受体拮抗剂是多巴胺D4受体拮抗剂。
在一些实施方式中,所述多巴胺D1/5受体拮抗剂是SCH 39166。在一些实施方式中,所述多巴胺D2受体拮抗剂是L-741626。在一些实施方式中,所述多巴胺D3受体拮抗剂是NGB 2904。在一些实施方式中,所述多巴胺D4受体拮抗剂是L-741742。
在一些实施方式中,所述神经递质类似物是谷氨酸受体激动剂。在一些实施方式中,所述神经递质类似物是AMPA受体激动剂。在一些实施方式中,所述神经递质类似物是NMDA受体激动剂。在一些实施方式中,所述神经递质类似物是谷氨酸/AMPA/NMDA受体激动剂。在一些实施方式中,所述神经递质是谷氨酸。在一些实施方式中,所述AMPA受体激动剂是α-氨基-3-羟基-5-甲基-4-异唑丙酸(AMPA)。在一些实施方式中,所述NMDA受体激动剂是N-甲基-D-天冬氨酸(NMDA)。在一些实施方式中,所述谷氨酸受体激动剂选自AMPA和NMDA。在一些实施方式中,所述谷氨酸/AMPA/NMDA受体激动剂选自AMPA和NMDA。
在一些实施方式中,所述神经递质类似物是谷氨酸受体拮抗剂。在一些实施方式中,所述神经递质类似物是AMPA受体拮抗剂。在一些实施方式中,所述神经递质类似物是NMDA受体拮抗剂。在一些实施方式中,所述神经递质类似物是谷氨酸/AMPA/NMDA受体拮抗剂。在一些实施方式中,所述谷氨酸/AMPA/NMDA受体拮抗剂选自CNQX和MK801。
在一些实施方式中,所述神经肽是G蛋白偶联受体配体。在一些实施方式中,所述神经肽选自GnRH-I、GnRH-II、降钙素基因相关肽(CGRP)、生长抑素、和神经肽Y(NPY)。在一些实施方式中,所述G蛋白偶联受体配体选自GnRH-I、GnRH-II、降钙素基因相关肽(CGRP)、生长抑素和NPY。在一些实施方式中,所述神经肽是CGRP。在一些实施方式中,所述神经肽是NPY。在一些实施方式中,所述神经肽是GnRH-I或GnRH-II。在一些实施方式中,所述神经肽是GnRH-1。在一些实施方式中,所述神经肽是GnRH-II。在一些实施方式中,所述神经肽是生长抑素。
在一些实施方式中,所述神经肽类似物是GnRH-1受体激动剂或拮抗剂。在一些实施方式中,所述神经肽类似物是GnRH-II受体激动剂或拮抗剂。在一些实施方式中,所述神经肽类似物是CGRP受体激动剂或拮抗剂。在一些实施方式中,所述神经肽类似物是生长抑素受体激动剂或拮抗剂。在一些实施方式中,所述神经肽类似物是NPY受体激动剂或拮抗剂。在一些实施方式中,所述神经肽类似物选自GnRH-I受体激动剂或拮抗剂、GnRH-II受体激动剂或拮抗剂、CGRP受体激动剂或拮抗剂、生长抑素受体激动剂或拮抗剂、和NPY受体激动剂或拮抗剂。
在一些实施方式中,所述离子通道选自钠通道、钙通道、钾通道和氯通道。在一些实施方式中,所述离子通道是钾通道。在一些实施方式中,所述电压门控钾通道(Kv)选自亚家族A、Shab相关亚家族、亚家族C、Shal相关亚家族、亚家族F、亚家族G、亚家族G、亚家族KQT、亚家族V、亚家族S、和亚家族H的钾电压门控通道。在一些实施方式中,所述电压门控钾通道是亚家族A的钾电压门控通道。在一些实施方式中,亚家族A也被称为Kv1亚家族并且包括Kv1.1、Kv1.2、Kv1.3、Kv1.4、Kv1.5、Kv1.6、Kv1.7、和Kv1.8。
在一些实施方式中,亚家族A也被称为Kv1亚家族并且由Kv1.1、Kv1.2、Kv1.3、Kv1.4、Kv1.5、Kv1.6、Kv1.7、和Kv1.8构成。在一些实施方式中,所述电压门控钾通道是Kv1.1。
在一些实施方式中,所述离子通道是缓慢失活的离子通道。在一些实施方式中,所述电压门控钾通道是振荡器相关(shaker-related)通道。
在一些实施方式中,所述电压门控离子通道的调节剂是离子通道阻断剂。在一些实施方式中,所述电压门控离子通道的调节剂是离子通道开放剂(opener)。在一些实施方式中,所述电压门控离子通道的调节剂阻断离子通道的打开。在一些实施方式中,所述电压门控离子通道的调节剂打开所述离子通道。在一些实施方式中,离子通道阻断剂是电压门控Kv1.1离子通道拮抗剂。在一些实施方式中,所述电压门控Kv1.1离子通道阻断剂选自树眼镜蛇毒素K(DTX-K)和抗Kv1.1阻断抗体。在一些实施方式中,所述电压门控Kv1.1离子通道阻断剂是DTX-K。在一些实施方式中,所述电压门控Kv1.1离子通道阻断剂是抗Kv1.l阻断抗体。在一些实施方式中,所述抗Kv1.1阻断抗体结合Kv1.1的胞外结构域。此类抗体的非限制性实例包括由Allomone Labs(以色列)制造的抗体APC-161和由GeneTex(美国)制造的抗体GTX54875。
在一些实施方式中,分子的组合被接触。在一些实施方式中,所述组合是至少两种神经递质或其类似物。在一些实施方式中,所述组合是至少两种神经递质或其类似物。在一些实施方式中,所述组合是至少两种电压门控离子通道的调节剂。在一些实施方式中,所述组合是至少一种神经递质或其类似物,和至少一种神经递质或其类似物。在一些实施方式中,所述组合是至少一种神经递质或其类似物,和至少一种电压门控离子通道的调节剂。在一些实施方式中,所述组合是至少一种神经肽或其类似物和至少一种电压门控离子通道的调节剂。
在一些实施方式中,所述组合是GnRH-II+多巴胺、GnRH-II+CGRP、GnRH-II+NPY、GnRH-II+谷氨酸、GNRH-II+多巴胺+CGRP+NPY、GNRH-II+多巴胺+谷氨酸+CGRP+NPY、多巴胺+谷氨酸、多巴胺+生长抑素、多巴胺+CGRP、多巴胺+GnRH-II、多巴胺+GnRH-I、多巴胺+NPY、多巴胺+GnRH-I+GnRH-II、多巴胺+谷氨酸+、GnRH-I+GnRH-II+生长抑素+CGRP、多巴胺+SCH39166、多巴胺+L-741626、多巴胺+NGB 2904、多巴胺+L-741742、MK 801+CNQX、谷氨酸+CGRP、或谷氨酸+NPY。每种可能性代表本发明的单独实施方式。
在一些实施方式中,接触的分子处于非常低的浓度。在一些实施方式中,所述接触分子的浓度不超过10^-5摩尔(M)、0.5x10^-5M、10^-6M、0.5x10^-6M、10^-7M、0.5x10^-7M、或10^-8M。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述接触分子的浓度为约10^-5M、0.5x10^-5M、10^-6M、0.5x10^-6M、10^-7M、0.5x10^-7M、或10^-8M。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述接触分子的浓度在10^-5M与10^-9M、0.5x10^-5M与10^-9M、10^-6M与10^-9M、0.5x10^-6M与10^-9M、10^-7M与10^-9M、0.5x10^-7M与10^-9M、10^-8与10^-9、10^-5M与0.5x10^-8M、0.5x10^-5M与0.5x10^-8M、10^-6M与0.5x10^-8M、0.5x10^-6M与0.5x10^-8M、10^-7M与0.5x10^-8M、0.5x10^-7M与0.5x10^-8M、10^-8与0.5x10^-8、10^-5M与10^-8M、0.5x10^-5M与10^-8M、10^-6M与10^-8M、0.5x10^-6M与10^-8M、10^-7M与10^-8M、或0.5x10^-7M与10^-8M之间。每种可能性代表本发明的单独实施方式。
在一些实施方式中,所述接触是使所述免疫细胞与所述分子或分子的组合孵育。在一些实施方式中,所述孵育持续足以降低所述免疫细胞表面上的PD-1表达的时间。在一些实施方式中,所述孵育持续至少30秒,1、3、5、10、15、20、25、30、45分钟,1、2、4、6、12、24、36、48、60、72、84或96小时。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述孵育持续不超过30秒,1、3、5、10、15、20、25、30、45分钟,1、2、4、6、12、24、36、48、60、72、84或96小时。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述接触持续30秒与30分钟之间。在一些实施方式中,所述接触持续30秒与60分钟之间。在一些实施方式中,所述接触持续30分钟与60分钟之间。在一些实施方式中,所述接触持续至少1天。在一些实施方式中,所述接触持续至少2天。在一些实施方式中,所述接触持续最多60小时。
在一些实施方式中,所述第一提供的免疫细胞是单独分裂和培养的。在一些实施方式中,单独培养的细胞被不同的分子或分子的组合接触。在一些实施方式中,选择对增加或减少影响最大的分子或分子的组合。在一些实施方式中,选择对治疗潜力的提高影响最大的分子或分子的组合。在一些实施方式中,使单独培养的细胞接触不同的时间量。在一些实施方式中,选择对增加或减少影响最大的孵育时间。在一些实施方式中,选择对治疗潜力的提高影响最大的孵育时间。
在一些实施方式中,所述第二提供的免疫细胞是单独分裂和培养的。在一些实施方式中,单独培养的细胞被不同的分子或分子的组合接触。在一些实施方式中,使单独培养的细胞接触不同的时间量。在一些实施方式中,按顺序将单独接触的细胞向所述对象给予。在一些实施方式中,每次给予间的间隔为至多1、5、10、15、20、25、30、35、40、45、50、55或60分钟。每种可能性代表本发明的单独实施方式。在一些实施方式中,给予包括重复给予更多的接触的免疫细胞。在一些实施方式中,给予包括无限期地给予。
在一些实施方式中,本发明的方法在一定时间间隔内对同一对象执行多于一次。在一些实施方式中,所述对象在一次给予时接受与一种分子或分子的组合接触的免疫细胞并在第二次给予时接受与不同分子或分子的组合接触的免疫细胞。在一些实施方式中,本发明方法的执行间的间隔为至少1天、2天、3天、1周、2周、1个月、2个月、或3个月。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述对象至少每年一次、每年两次、每六个月一次、每三个月一次、每两个月一次、每月一次、每月两次、每周一次、或每周两次被治疗。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述对象每周两次被治疗。
在一些实施方式中,仅一种分子被接触。在一些实施方式中,至少两种分子被接触。在一些实施方式中,接触发生在体外。在一些实施方式中,所述接触发生在将所述细胞给予所述对象前。在一些实施方式中,步骤c.中的测量进一步包括测量以下至少一项:
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对细胞因子的分泌;
xi.所述免疫细胞对治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
并且其中增殖的增加、ζ链表达的增加、迁移的增加、粘附的增加、归巢的增加、穿透的增加、细胞因子分泌的增加、治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因的表达或功能的降低、或参与过程ii至xi的至少一种蛋白质或基因的表达或功能的提高中的至少一个指示所述分子或分子的组合提高了所述免疫细胞的治疗潜力。在一些实施方式中,本发明的方法包括测量免疫细胞上的PD-1细胞表面表达和测量以下至少一项:与和所述癌症相关的癌细胞共培养的免疫细胞的增殖、与所述免疫细胞共培养的和所述癌症相关的癌细胞的细胞死亡、单独培养的所述免疫细胞的增殖、所述免疫细胞中的ζ链表达、所述免疫细胞的趋化迁移、所述免疫细胞对细胞因子的分泌、所述免疫细胞的粘附和所述免疫细胞的归巢或迁移。
在一些实施方式中,接触的免疫细胞的给予包括给予至少10^6、5x10^6、10^7、5x10^7、10^8、5x10^8或10^9个免疫细胞。每种可能性代表本发明的单独实施方式。在一些实施方式中,接触的免疫细胞的给予包括给予至少10^8个免疫细胞。在一些实施方式中,接触的免疫细胞的给予包括给予约10^8个免疫细胞。在一些实施方式中,接触的免疫细胞的给予包括给予10^6与10^10、2x10^6与10^10、5x10^6与10^10、7x10^6与10^10、10^7与10^10、5x10^7与10^10、10^8与10^10、5x10^8与10^10、10^6与10^9、2x10^6与10^9、5x10^6与10^9、7x10^6与10^9、10^7与10^9、5x10^7与10^9、10^8与10^9、或5x10^8与10^9个之间的免疫细胞。每种可能性代表本发明的单独实施方式。在一些实施方式中,约10^8个接触的免疫细胞每周两次给予。在一些实施方式中,所述给予包括针对给定对象选择最有益的免疫细胞和/或具有最高免疫治疗潜力的免疫细胞并将所选择的细胞向所述对象给予。在一些实施方式中,给予效应细胞而非调节细胞。在一些实施方式中,给予效应T细胞而非调节T细胞。在一些实施方式中,给予调节细胞而非效应细胞。在一些实施方式中,所述过继性神经免疫疗法持续所述患者的一生。在一些实施方式中,所述过继性神经免疫疗法无限期地持续。在一些实施方式中,只要对所述对象有益,所述过继性神经免疫疗法就持续进行。在一些实施方式中,预防性地执行所述过继性神经免疫疗法。在一些实施方式中,执行所述过继性神经免疫疗法防止复发。
在一些实施方式中,所提供的免疫细胞在包含人血清或血浆的细胞培养基中。在一些实施方式中,所述人是所述对象。在一些实施方式中,所述人血清或血浆在加入培养基之前经历热灭活过程。在一些实施方式中,所述人是所述对象的亲属。在一些实施方式中,所述人对于所述对象是同种异体的。在一些实施方式中,所述血浆或血清对于所提供的免疫细胞是同种异体的。在一些实施方式中,所述血浆或血清对于所提供的免疫细胞是自体的。在一些实施方式中,在本发明的任何步骤中,用于体外细胞培养或共培养的培养基含有人血清或血浆。在一些实施方式中,所述细胞培养基含有胎牛血清(FCS)。在一些实施方式中,所述培养基中的FCS已被人血清或血浆替代。在一些实施方式中,所述人血清或血浆是所述对象的血清或血浆。在一些实施方式中,FCS的全部、FCS的一些或FCS的大部分已被替代。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述接触发生在包含所述人血清或血浆的培养基中。在一些实施方式中,所述测量发生在包含人血清或血浆的培养基中。在一些实施方式中,以包含所述人血清或血浆的组合物给予接触的免疫细胞。在一些实施方式中,所述方法的所有步骤在包含人血清或血浆的培养基中执行。在一些实施方式中,所述细胞被冷冻,并且冷冻培养基包含人血清或血浆。
在一些实施方式中,所述治疗是所述疾病或状况的一线治疗。在一些实施方式中,所述对象在执行本发明的方法之前未接受所述疾病或状况的治疗。在一些实施方式中,所述对象在用本发明的方法治疗之前已经接受了针对所述疾病、状况、损伤或创伤的治疗。在一些实施方式中,所述对象已经接受了基于PD-1的疗法。在一些实施方式中,所述基于PD-1的疗法是检查点抑制剂。在一些实施方式中,所述检查点抑制剂是抗PD-1或抗PD-1L抗体。在一些实施方式中,基于PD-a的疗法包括其它PD-1/PD-1L靶向疗法。在一些实施方式中,所述给予包括给予另一种疗法。在一些实施方式中,所述其它疗法是针对用本发明的方法治疗的任何疾病、状况、损伤或创伤的任何治疗。在一些实施方式中,所述其它疗法不靶向PD-1或PD-1L。在一些实施方式中,所述其它疗法是抗癌疗法。在一些实施方式中,本发明的方法进一步包括给予另一种疗法。在一些实施方式中,所述其它疗法是针对所述疾病或状况的标准疗法。本领域技术人员将理解,对疾病的标准护理将取决于多种因素,如疾病的类型、疾病的阶段/严重程度、患者的年龄和健康状况以及在治疗时医师可获得的其它信息。
在一些实施方式中,给予包括给予包含接触的细胞的药物组合物。在一些实施方式中,所述药物组合物包含治疗有效量的接触的细胞。在一些实施方式中,所述药物组合物包含载体、赋形剂或佐剂。
如本文所用,术语“给予(administering)”、“给予(administration)”和类似术语是指在合理的医学实践中以提供治疗效果的方式向对象递送含有活性剂的组合物的任何方法。本主题的一个方面提供了向对其有需要的对象静脉内给予治疗有效量的增强的神经免疫治疗性免疫细胞。其它合适的给予途径可以包括肠胃外、皮下、颅内、肌肉内、肿瘤内、口服、局部、膀胱内、脊柱内或腹膜内。在一些实施方式中,所述给予到达所述疾病、状况或损伤的部位。在一些实施方式中,所述给予到达多于一个的部位。在一些实施方式中,所述给予按顺序到达多于一个的部位。在一些实施方式中,通过以下方法中的至少一种进行所述给予:静脉内、肠胃外、皮下、颅内、肌肉内、肿瘤内或腹膜内。在一些实施方式中,免疫细胞的多次给予被给予到多个位置或通过多个途径给予。给予的剂量将取决于接受者的年龄、健康状况和体重、疾病的类型和严重程度/阶段、同时治疗的种类(如果有的话)、治疗的频率、以及所期望效果的性质。在一些实施方式中,给予包括静脉内给予、肌肉内给予、鼻内给予、鞘内给予、纹状体内给予、颅内给予、动脉内给予、肿瘤内给予和皮下给予中的至少一种。在一些实施方式中,接触的细胞通过至少一种给予模式给予。在一些实施方式中,接触的细胞通过多种给予模式按顺序给予。在一些实施方式中,所述按顺序给予到达所述对象中的至少一个部位并通过至少一种给予模式进行。
术语“治疗有效量”是指有效治疗哺乳动物中的疾病或障碍的药物的量。在一些实施方式中,治疗有效量是以必要的剂量和时间段有效实现期望的治疗或预防结果的量。确切的剂型和方案将由医师根据患者的状况确定。
如本文所用,术语“载体”、“赋形剂”或“佐剂”是指药物组合物的不是活性剂的任何组分。如本文所用,术语“药学上可接受的载体”是指无毒的惰性固体、半固体液体填充剂、稀释剂、包封材料、任何类型的制剂助剂,或就只是无菌水性介质,如盐水。可充当药学上可接受的载体的材料的一些实例是糖类,如乳糖、葡萄糖和蔗糖,淀粉类,如玉米淀粉和马铃薯淀粉,纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和醋酸纤维素;黄蓍胶粉;麦芽、明胶、滑石;赋形剂,如可可脂和栓剂蜡;油类,如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和豆油;二醇类,如丙二醇,多元醇类,如甘油、山梨糖醇、甘露醇、聚乙二醇;酯类,如油酸乙酯和月桂酸乙酯,琼脂;缓冲剂,如氢氧化镁和氢氧化铝;海藻酸;无热原水;等渗盐水,林格氏溶液;乙醇和磷酸盐缓冲溶液,以及药物制剂中使用的其它无毒相容性物质。
所述载体可总共占本文呈现的药物组合物重量的约0.1%至约99.99999%。
应当注意,接触的免疫细胞可以作为组合物给予,并且可以单独给予或作为活性成分与药学上可接受的载体、稀释剂、佐剂和赋形剂组合给予。所述组合物也可以皮下或肠胃外给予,包括静脉内、动脉内、肌肉内、肿瘤内、腹膜内、扁桃体内、和鼻内给予以及鞘内和输注技术。所述组合物的植入物也是有用的。被治疗的患者是温血动物,具体是包括人在内的哺乳动物。所述药学上可接受的载体、稀释剂、佐剂和媒介物以及植入物载体通常是指不与本发明的活性成分反应的惰性的无毒固体或液体填充剂、稀释剂或包封材料。
所述剂量可以是在几天、几周、几个月或甚至几年或只要对所述对象有益的时期内的单剂量或多剂量。治疗的长度通常与疾病过程的长度和治疗效果以及被治疗的患者种属成比例。
通过另一方面,提供了药物组合物,其包含本发明的改善的神经免疫治疗性免疫细胞和药学上可接受的载体、佐剂或赋形剂。
通过另一方面,提供了过继性细胞疗法的方法,包括向对其有需要的对象给予至少10^8个免疫细胞。通过另一方面,提供了至少10^8个免疫细胞用于过继性细胞疗法的使用。在一些实施方式中,所述免疫细胞每周两次给予。在一些实施方式中,所述疗法持续所述患者的一生。在一些实施方式中,所述免疫细胞被无限期地给予。在一些实施方式中,所述过继性细胞疗法是改善的免疫细胞疗法。在一些实施方式中,所述改善的免疫细胞疗法包括本发明的任何治疗方法。
通过另一方面,提供了选择适合免疫疗法的对象的方法,所述方法包括,
a.提供健康的免疫细胞;
b.使所述健康免疫细胞与所述对象的血浆或血清接触;和
c.测量所述免疫细胞的存活;
其中所述免疫细胞存活的降低指示所述对象适合免疫疗法。在一些实施方式中,所述方法是在体外执行的。
在一些实施方式中,所述对象遭受存在或疑似是次优T细胞活性和/或数量的疾病、状况、创伤或损伤。在一些实施方式中,所述对象遭受其中可通过增加有益的T细胞数量和/或功能实现临床益处的疾病。在一些实施方式中,所述对象遭受以次优T细胞活性和/或数量为特征的疾病。在一些实施方式中,所述对象遭受癌症。
在一些实施方式中,所述接触包括在包含所述对象的血浆或血清的细胞培养基中培养所述健康的免疫细胞。在一些实施方式中,所述接触包括在其中FCS被所述对象的血浆或血清替代的培养基中培养所述健康的免疫细胞。在一些实施方式中,全部的FCS都被替代。在一些实施方式中,至少10、20、30、40、50、60、70、80、90、95、97或99%的所述血清被替代。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述人血清或血浆在加入所述细胞培养基之前被热灭活。
在一些实施方式中,与未与所述对象的血浆或血清接触的健康的免疫细胞相比,所述免疫细胞的存活降低。在一些实施方式中,与在具有含有FCS且不含所述对象的血浆或血清的培养基的培养物中生长的健康的免疫细胞相比,存活降低。在一些实施方式中,与在具有含有健康供体的血浆或血清的培养基的培养物中生长的健康的免疫细胞相比,存活降低。
通过另一方面,提供了储存用于过继性细胞疗法的免疫细胞的方法,所述方法包括在包含人血清或血浆的培养基中培养或冷冻免疫细胞。通过另一方面,提供了储存用于免疫疗法的免疫细胞的方法,所述方法包括在包含人血清或血浆的培养基中培养或冷冻免疫细胞。
通过另一方面,提供了选择适合免疫疗法的对象的方法,所述方法包括:
a.提供免疫细胞;
b.在包含来自所述对象的血浆或血清的培养基中培养所述免疫细胞;
c.监测所述免疫细胞的存活;
其中所述免疫细胞的存活的降低指示所述对象适合免疫疗法。
在一些实施方式中,与在不包含所述对象的血浆或血清的培养基中培养的免疫细胞的存活相比,存活降低。在一些实施方式中,不包含所述对象的血浆或血清的培养基包含FCS。在一些实施方式中,不包含所述对象的血浆或血清的培养基包含来自同种异体健康对象的血浆或血清。在一些实施方式中,所提供的免疫细胞来自健康供体。在一些实施方式中,所提供的免疫细胞来自所述对象。在一些实施方式中,所述免疫细胞是大的增殖免疫细胞。
在一些实施方式中,所述免疫细胞是多种免疫细胞,并且存活的降低包括存活的免疫细胞的数量减少至少20%、25%、30%、35%、40%、45%或50%。每种可能性代表本发明的单独实施方式。在一些实施方式中,存活的降低是存活细胞的数量的至少30%的降低。在一些实施方式中,存活的降低是存活细胞的数量的至少50%的降低。
通过另一方面,提供了在对其有需要的对象中的免疫疗法的方法,所述方法包括:
a.提供所述对象的免疫细胞;
b.在包含健康同种异体个体的血浆或血清的培养基中培养所述免疫细胞;
c.将培养的免疫细胞返回给所述对象;
从而在所述对其有需要的对象中执行免疫疗法。
通过另一方面,提供了在包含来自健康个体的血浆或血清的培养基中培养的免疫细胞用于对其有需要的对象中的免疫疗法的用途。在一些实施方式中,所述健康个体对于所述对象是同种异体的。
在一些实施方式中,所述免疫疗法是过继性神经免疫疗法。在一些实施方式中,所述过继性细胞疗法是过继性神经免疫疗法。在一些实施方式中,所述免疫疗法是任意免疫疗法。在一些实施方式中,所述神经免疫疗法包括本发明的任何方法。
在一些实施方式中,所述免疫细胞在包含人血清或血浆的培养基中。在一些实施方式中,所述人是所述对象。在一些实施方式中,所述人是所述对象的亲属。在一些实施方式中,所述人对于所述对象是同种异体的。在一些实施方式中,所述血浆或血清对于所述免疫细胞是同种异体的。在一些实施方式中,所述血浆或血清对于所述免疫细胞是自体的。在一些实施方式中,所述培养基中的胎牛血清(FCS)已被人血清或血浆替代。在一些实施方式中,所述人血清或血浆是所述对象的血清或血浆。在一些实施方式中,FCS的全部、FCS的影响或FCS的大部分已被替代。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述FCS、人血清或血浆经历热灭活。
在一些实施方式中,所述人血浆或血清来自提供所述免疫细胞的所述对象。在一些实施方式中,所述人血浆或血清来自健康的同种异体个体。
在一些实施方式中,所述培养持续至少1、2、3、4、5、6、7、8或9天。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述培养持续2.5与9、2.5与8、2.5与7或2.5与6之间的天数。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述培养持续至少2.5天。在一些实施方式中,所述培养持续至少6天。在一些实施方式中,所述培养持续至少2.5天并且所述免疫细胞的存活的降低至少是30%。在一些实施方式中,所述培养持续至少6天并且所述免疫细胞的存活的降低至少是50%。
试剂盒
通过另一方面,提供了包含至少一种神经递质或其类似物、至少一种神经肽或其类似物和至少一种电压门控离子通道的调节剂的试剂盒。通过另一方面,提供了包含至少一种神经递质或其类似物、和至少一种神经肽及其类似物、以及所述至少一种神经肽和至少一种神经递质的组合的试剂盒。
通过另一方面,提供了包含PD-1检测剂和选自神经递质或其类似物、神经肽或其模拟物、或电压门控离子通道的调节剂的至少一种分子的试剂盒。
在一些实施方式中,所述试剂盒用于选择用于提高免疫细胞对过继性神经免疫疗法的适用性的分子。在一些实施方式中,所述试剂盒用于选择用于提高治疗性免疫细胞潜力的分子。在一些实施方式中,所述试剂盒用于在免疫疗法期间提高免疫细胞功能。在一些实施方式中,所述试剂盒用于提高免疫细胞功能以供免疫治疗。在一些实施方式中,所述试剂盒用于确定对其有需要的对象是否适合过继性神经免疫疗法。在一些实施方式中,所述试剂盒用于治疗、预防对其有需要的对象中具有或疑似具有次优T细胞活性和/或数量的疾病、创伤、损伤、或状况或预防其复发。在一些实施方式中,所述试剂盒用于修复、再生或补偿由于所述疾病、创伤、损伤或状况引起的损失或缺陷。在一些实施方式中,所述试剂盒用于揭示和选择分子或其组合中的哪些对对象的免疫细胞引发最大的有益效果,从而提高/增强针对所述对象的免疫治疗潜力。
在一些实施方式中,所述PD-1检测剂不是PD-1抑制剂。在一些实施方式中,所述PD-1检测剂包含抗PD-1抗体。在一些实施方式中,所述PD-1检测剂是抗PD-1抗体。在一些实施方式中,所述抗PD-1抗体不是PD-1阻断抗体。在一些实施方式中,所述PD-1检测剂包含标签。在一些实施方式中,所述标签是荧光标签。在一些实施方式中,所述抗PD-1抗体是FACS抗体。在一些实施方式中,所述PD-1检测剂是作为非抗体的PD-1传感器。
在一些实施方式中,所述试剂盒包含至少2、3、4、5、6、7、8、9或10种分子。每种可能性代表本发明的单独实施方式。在一些实施方式中,所述试剂盒包含至少2种神经递质或其类似物。在一些实施方式中,所述试剂盒包含至少2种神经肽或其模拟物。在一些实施方式中,所述试剂盒包含至少一种神经递质或其类似物和一种神经肽或其模拟物。在一些实施方式中,所述试剂盒包含至少一种神经递质或其类似物和一种电压门控离子通道的调节剂。在一些实施方式中,所述试剂盒包含至少一种神经肽或其模拟物和一种电压门控离子通道的调节剂。在一些实施方式中,所述试剂盒包含神经递质或其类似物、神经肽或其模拟物、或电压门控离子通道的调节剂中的至少两种,并且其中这两种来自不同的类别。可用于本发明试剂盒的分子的实例和实施方式可在上文中找到。在一些实施方式中,所述试剂盒包含神经递质或神经递质激动剂、神经递质拮抗剂、神经肽或神经肽激动剂、神经肽拮抗剂、和电压门控离子通道的调节剂。在一些实施方式中,所述试剂盒包含神经递质或神经递质激动剂、神经递质拮抗剂、神经肽或神经肽激动剂和电压门控离子通道阻断剂。
在一些实施方式中,所述试剂盒中的分子以至多10^-7M的浓度提供。在一些实施方式中,所述试剂盒中的分子以本文所述的适合执行本发明方法的浓度提供。在一些实施方式中,提供了本文描述的分子的组合。在一些实施方式中,所述组合是所述分子的混合物。在一些实施方式中,混合至少两种神经递质或其类似物。在一些实施方式中,混合至少两种神经肽或其类似物。在一些实施方式中,将至少一种神经递质或其类似物、至少一种神经肽或其类似物和至少一种电压门控离子通道的调节剂混合。
在一些实施方式中,本发明的试剂盒还包括组织培养板,其中所述板的单独孔容纳单独的分子或分子的组合。这样的板可用于最有益分子(一种或多种)的快速测试,因为培养基中的细胞可以移入已经容纳待测试且处于适当浓度的分子的每个孔中。最有益的分子(一种或多种)将是对对象的免疫细胞或非对象供体的免疫细胞引发最佳有益效果并将提高它们对所述对象的治疗潜力的分子。由于使用的分子浓度非常低,并且这些分子每次都需要从高浓度的冷冻储液或从冻干粉以所需浓度新鲜地制备,因此每次向小的组织培养孔添加适当的量都可能是困难且耗时的。技术人员将理解对孔预先装载分子的益处。在一些实施方式中,这些孔被单独密封。在一些实施方式中,正确量的所述分子附贴至孔壁,以便在打开培养皿时不会损失。在一些实施方式中,所述分子被提供为处于所述孔中的膜,所述膜可溶解在介质中以达到所需浓度但不雾化。在一些实施方式中,所述分子可以以确保所述分子不会丢失,或所述分子的浓度不会改变,但是当将所述分子添加到所述孔时将允许其溶解并分散在介质中的任何方式提供在所述孔中以便达到所需浓度。在一些实施方式中,所述分子可被配置使得它们保留在所述孔的壁上而不分散到介质中。在一些实施方式中,所述分子被锚定或嵌入或以任何其它方式束缚至所述壁而不分散在介质中。在一些实施方式中,正确浓度的所述分子在载体上或在载体中,在与介质或所需缓冲液接触时,将所述分子释放到介质或缓冲液中。这种载体的实例可以是滤纸、或纤维素、或所述分子可以从其解离的任何载体。
在一些实施方式中,所述试剂盒由以下分子和组合构成或包含以下分子和组合:多巴胺、多巴胺+谷氨酸、多巴胺+GnRH-II、多巴胺+NPY、多巴胺+生长抑素、多巴胺+CGRP、谷氨酸、谷氨酸+GnRH-II、谷氨酸+NPY、谷氨酸+生长抑素、谷氨酸+CGRP、GnRH-II、GnRH-II+NPY、GnRH-II+生长抑素、GnRH-II+CGRP、NPY、NPY+生长抑素、NPY+CGRP、生长抑素、生长抑素+CGRP、和多巴胺+谷氨酸+GnRH-II+NPY+生长抑素+CGRP。
如本文所用,当与数值组合时,术语“约”是指参考值的正负10%。例如,约1000纳米(nm)的长度是指1000nm+-100nm的长度。
注意,如本文和所附权利要求书中所使用的,单数形式“一”、“一个”和“所述”包括复数指代,除非上下文另有明确规定。因此,例如,对“多核苷酸”的提及包括多种这样的多核苷酸,并且对“多肽”的提及包括对本领域技术人员已知的一种或多种多肽及其等同物的提及等等。进一步注意,权利要求书的撰写可以排除任何任选要素。因此,此声明意图作为如“仅”、“只有”等排他术语与权利要求要素的叙述结合使用或“否定”限定的使用的先行基础。
在那些使用类似于“A、B和C等中的至少一个”的惯例(convention)的情况下,一般而言,这样的构句意图表示为本领域技术人员会对该惯例理解的含义(例如,“具有A、B和C中的至少一个的系统”将包括但不限于只有A、只有B、只有C、具有A和B一起、具有A和C一起、具有B和C一起、和/或具有A、B和C一起等等的系统)。本领域技术人员将进一步理解,实际上任何呈现两个或多个可选术语的反意连接词和/或短语,无论是在说明书、权利要求书、或附图中,都应被理解为考虑到包括这些术语中的一个、术语中的任一个、或这两个术语的可能性。例如,短语“A或B”将被理解为包括“A”或“B”或“A和B”的可能性。
应当理解,为了清楚起见,在单独的实施方式的背景下描述的本发明的某些特征也可以在单个实施方式中以组合方式提供。相反,为了简洁起见,在单个实施方式的背景下描述的本发明的各种特征也可以单独提供或以任何合适的子组合的方式提供。涉及本发明的实施方式的所有组合都被本发明具体地包含并且在本文中被公开,就好像每个组合被单独地且明确地公开一样。此外,各种实施方式及其要素的所有子组合也被本发明具体地包含并且在本文中被公开,就好像每个这样的子组合在本文中被单独且明确地公开一样。
在查看以下并非意图进行限制的实例后,本发明的其它目的、优点和新颖特征将变得对本领域普通技术人员显而易见。此外,上文描述的和以下权利要求部分要求保护的本发明的各个实施方式和方面中的每一个都会在以下实例中找到实验上的支持。
上文描述的和以下权利要求部分要求保护的本发明的各种实施方式和方面会在以下实例中找到实验上的支持。
实施例
总体上,本文使用的命名法和本发明中使用的实验室程序包括分子、生物化学、微生物、和重组DNA技术。此类技术在文献中有详尽的解释。参见,例如,"Molecular Cloning:A laboratory Manual"Sambrook等人(1989);"Current Protocols in MolecularBiology"第I-III卷Ausubel,R.M.,ed.(1994);Ausubel等人,"Current Protocols inMolecular Biology",John Wiley and Sons,Baltimore,Maryland(1989);Perbal,"APractical Guide to Molecular Cloning",John Wiley&Sons,New York(1988);Watson等人,"Recombinant DNA",Scientific American Books,New York;Birren等人(eds)"Genome Analysis:A Laboratory Manual Series",第1-4卷,Cold Spring HarborLaboratory Press,New York(1998);如美国专利号4,666,828;4,683,202;4,801,531;5,192,659和5,272,057中列出的方法;"Cell Biology:A Laboratory Handbook",VolumesI-III Cellis,J.E.,ed.(1994Mishell and Shiigi(eds)),"Strategies for ProteinPurification and Characterization-A Laboratory Course Manual"CSHL Press(1996);其全部都以引用并入。本文件的全文中提供了其它一般性文献。
实施例1:神经递质降低健康供体的T细胞中的PD-1表达
通过Ficol分离,从健康供体的正常人白细胞分离外周血淋巴细胞(PBL),并且通过抗CD3抗体偶联的磁珠分离CD3阳性T细胞。CD3+T细胞在补充有10%热灭活胎牛血清(FCS)、1%F-谷氨酰胺、1%丙酮酸钠、1%非必需氨基酸、和1%抗生素的RPMI 1640培养基中培养。这些细胞在它们分离后,在加入各种分子并测量它们对T细胞的作用之前通常平均维持24小时。许多肿瘤能够通过表达PD-1配体(PD-1L)来逃避免疫监视。PD-1L与T细胞上表达的PD-1结合,因此这样做不会使T细胞活化、发挥功能并附着癌细胞。因此测试了神经递质、神经肽和/或电压门控离子通道的调节剂是否可以减少T细胞的细胞表面上的PD-1。这种减少将使T细胞逃离肿瘤诱导的T细胞抑制,然后活化的T细胞可以附着癌细胞。因此,监测了这些经处理和未经处理的T细胞的表面上PD-1的表达。提供了用神经递质处理1小时(表1)、18小时(表2)和24小时(表3)对PD-1表面表达的结果。测试的每种神经递质产生了T细胞的表面上PD-1的总表达水平以及表达PD-1的T细胞总数的降低,然而却取决于所改变的神经递质、最佳浓度和处理的持续时间。例如,浓度为10^-7M的多巴胺D4受体激动剂PD168077在处理24小时后诱导了表达PD-1的T细胞的平均百分比的最大降低。相比之下,谷氨酸盐在较短的处理时间后产生了更强的效果(33.0降低vs.20.2%降低,10^-8M下1小时vs.24小时;10^-7M下31.7vs.22.64,10^-7M下18小时vs.24小时)。事实上,在某些情况下,神经递质或它们的受体激动剂(多巴胺、非诺多泮、SKF38393)在较短的孵育时间引起强烈的降低,但在孵育24小时时则不产生积极的效果。当细胞将随后被返回给对象时,较短的体外孵育时间常常是优选的,因为它们的结束降低了不利反应的风险。这些结果证明,用神经递质、神经递质受体激动剂、和阻断Kv1.l离子通道的分子进行处理有效降低了T细胞中的表面PD-1表达并减少了表达PD-1的T细胞的数量,还证明了PD-1表达可用作优化T细胞的增强或活化的有效读数(readout)。
表1:神经递质、神经递质受体激动剂、和Kv1.1离子通道的调节剂处理(1Hr)对表达PD-1的CD3+正常人T细胞的百分比的影响
表2:神经递质、神经递质受体激动剂、和Kv1.1离子通道的调节剂处理(18Hr)对表达PD-1的CD3+正常人T细胞的百分比的影响
表3:神经递质、神经递质受体激动剂、和Kv1.1离子通道的调节剂处理(24Hr)对表达PD-1的CD3+正常人T细胞的百分比的影响
实施例2:神经递质、神经肽、它们的类似物及其组合减少大的增殖和小的非增殖T细胞中的PD-1
患者的CD3阳性T细胞是不同类型T细胞的异质混合物。即使在没有任何染色的情况下,流式细胞术分析也会通过被称为前向散射(FSC)的参数显示细胞的大小,并通过被称为杂乱散射(SSC)的参数显示细胞的粒度。利用这种FCS和SSC分析,T细胞可以被区分并按大小分为大的增殖T细胞和较小的非增殖T细胞。发现呈PD-1阳性的较小T细胞比大的增殖T细胞的部分更多,并且单独检查了神经递质和神经肽对这两个群体的影响。表4总结了用各种分子和分子的组合对大的增殖T细胞进行1小时处理的影响。表5总结了相同处理对较小的非增殖T细胞的影响。处理前PD-1水平高于较大T细胞的较小T细胞对各种分子的响应降低,正如通过表达PD-1的细胞的百分比降低来测量的,然而,哪些分子是最有效的这一趋势在这两个群体之间总体上是一致的,这表明对任一群体的检查对于确定最有益的分子是提供有用信息的。
表4:神经递质、神经肽、它们的类似物及其组合处理(1小时)对表达PD-1的大的增殖CD3+正常人T细胞的百分比的影响
表5:神经递质、神经肽、它们的类似物及其组合处理(1小时)对表达PD-1的较小非增殖CD3+正常人T细胞的百分比的影响
实施例3:神经递质、神经肽及其组合增强肝癌患者的CD3+T细胞的增殖
在确立了神经递质、神经肽、它们的类似物、Kv1.1离子通道阻断剂及其组合对降低健康对象的正常人T细胞中PD-1表达及增强其增殖的功效后,在癌症患者的T细胞上测试这些分子。血液是从患有肝癌的两名患者身上抽取的,患者L.F.和患者A.G.都患有肝细胞癌。15mL血液获得大约2.5x10^7个外周血白细胞,从中分离出大约6x10^6个CD3阳性T细胞。如上所述对这些细胞进行培养,并检查各种分子及其组合对那些T细胞的影响。
在分子(一种或多种)给予后,监测培养物中的细胞增殖60小时(图1)。测试的所有神经递质和神经肽(多巴胺、谷氨酸、GnRH-II、CGRP、神经肽Y[NPY])和所有组合(GnRH-II+多巴胺、GnRH-II+CGRP、GnRH-II+神经肽Y、所有神经递质)都增加了培养物中存在的T细胞数量。多巴胺、谷氨酸和GnRH-II+NPY是最有效的。有趣的是,所有分子的组合对这些患者的T细胞无效,导致增殖的增加低于任何单独的神经递质。这加强了对每名患者进行测试的逻辑和需要,哪些分子或其组合会对他/她自己的T细胞诱发最佳有益效果。
不仅培养物中存在更多的T细胞,而且在流式细胞仪中分析细胞时,观察到大的增殖CD3阳性细胞的数量显著增加(表6)。通过此测量,谷氨酸(图2A-图2B)、GnRH-II、和GnRH-II+多巴胺或+NPY(图2C)是最有效的。所有神经递质的混合再次是最不有效的。还注意到单独的GnRH-II或与几种神经肽(CGRP、NPY)组合增加了CD25的表面表达,已知其在T细胞活化时上调(图2D)。
表6:神经递质、神经肽及其组合增加肝癌患者的大的增殖T细胞的数量
用各种分子(一种或多种)对患者A.G.的T细胞进行了相同的处理,尽管一些神经递质和神经肽(谷氨酸、CGRP)及其组合(谷氨酸+多巴胺、谷氨酸+NPY)导致了大的增殖T细胞的百分比少量提高,但它从未提高大于30%(图2E)。从L.F.所看到的数倍提高对于A.G.则无法实现。这些结果加强了测试每名患者的T细胞其对这些分子的响应,以及确定患者是否可以从过继性神经免疫疗法中受益,或者是否是过继性神经免疫疗法的候选者的逻辑和需要。
实施例4:神经递质、神经肽及其组合降低肝癌患者的T细胞上的PD-1
接下来研究了神经递质降低癌症患者的T细胞上的PD-1表达的能力。将培养的L.F的T细胞暴露于各种神经递质、神经肽及其组合共60小时,并通过FACS分析来测量总PD-1表面表达(图3A)。与采用健康供体T细胞的结果相似,单独的神经递质和神经肽具有不同水平的有效性,然而,最有效或最无效的神经递质和神经肽则不然,这表明分子(一种或多种)的作用的量级可能具有人特异性。此外,当神经递质和神经肽组合时,L.F.的T细胞显示出强烈的协同作用。与总PD-1表达相反,当测量PD-1阳性细胞的百分比时,获得了类似的结果(图3B)。
以同样的方式测试A.G.的T细胞。几种神经肽(GnRH-II)或分子的组合(GnRH-II+谷氨酸、谷氨酸+多巴胺、多巴胺+NPY)再次降低了此肝癌患者的T细胞中PD-1的表达(图3C),然而,再一次又未从患者L.F.观察到同样大小的降低,最大降低仅为减少15%。
实施例5:神经递质、神经肽及其组合提高癌症患者的T细胞的癌症杀伤能力
现在研究神经递质、神经肽、和它们的组合提高癌症患者的T细胞杀伤患者所患的同一癌症类型的癌细胞的能力。再次从血液样品中分离肝细胞癌患者L.F.的T细胞,然后用各种分子预处理60小时,之后与HepG2肝细胞癌的细胞共培养。4天后,对存活的HepG2细胞的总数计数(图4A)。未处理的T细胞使癌细胞总数减少了47%,但用神经递质处理能够提高T细胞的细胞毒性,从而使癌细胞的数量减少多达62%。
当L.F.的经神经递质/神经肽增强的T细胞与Huh7肝癌细胞孵育时,获得了类似的结果。共培养一周后,未处理的T细胞使存活的肝癌细胞总数减少了31%,而用分子(一种或多种)处理能够增加杀伤,使得发生41%的减少(图4B)。然后用SYTOX绿染色1周后仍在培养中的肝癌细胞以确定活细胞和坏死细胞的百分比。存活的降低也与活细胞的减少(图4C)、坏死细胞的增加(图4D)相关。令人兴奋的是,在一周的共培养后,观察到培养后存活的T细胞的数量增加(图4E)。具体来说,大约15000个未处理的T细胞与Huh7细胞共培养后存活下来,但相比之下,经神经递质增强的细胞在共培养后剩余多达超过20000个细胞。这些结果非常好且令人鼓舞,因为它们显示了用神经递质、神经肽及它们的组合对肝细胞癌患者的T细胞进行预处理会增加其随后因遇到肝细胞癌的细胞而对其的响应以及增殖。因此,这些分子增强了T细胞对癌细胞的响应。
实施例6:FCS可用健康人对象的人血浆代替用以培养T细胞
体外培养人细胞,通常被称为“细胞停放”,如果打算将这些细胞返回给人对象,则会产生多种有害影响。具体而言,细胞培养基中使用的胎牛血清(FCS)可能存在问题,因为其批次之间的差异性、刺激不期望的免疫原性的倾向以及可能导致被所培养细胞内化的外来不期望的物质。因此,尝试使培养基尽可能类似于人生理条件并用人衍生的材料/因子代替FCS是有益的。
为此,从健康供体的血液中分离健康的正常人原代CD3阳性T细胞,并在含有10%热灭活FCS的标准组织培养基中或在代替地含有10%热灭活人血浆的培养基中培养。本实验中使用的人血浆来自与T细胞相同的供体。5天和9天后,监测细胞的存活率以及大小T细胞之间的区别。5天后,含FCS的培养物中平均(n=3)存在12218个大的增殖T细胞和4924个小T细胞(图5A)。含人血浆的培养物平均(n=3)有13455个大的增殖T细胞和5583个小T细胞(图5B)。9天后,在含FCS的培养物中,这些数字已变为平均(n=4)10101和11672(图5C),而含人血浆的培养物中平均(n=4)为6012和9441(图5D)。
这些结果证实了用健康人对象的人血浆替代FCS对正常人T细胞的短期体外培养是有效的,至少长达9天。对于针对不超过5天的神经递质/神经肽/离子通道增强的免疫疗法进行的培养,由于FCS的不期望的影响,因此人血浆是可行的,并且确实可以是FCS的优选替代品。
实施例7:需要免疫治疗的患者的血浆不适合培养T细胞
与上述实验平行,将健康对象的相同的正常人原代T细胞在含有10%热灭活的患者L.F.的人血浆的培养基中孵育。5天和9天,监测这些细胞的存活率以及小T细胞与大T细胞间的区别。5天后,培养物中存在平均(n=3)8392个大的增殖T细胞和6449个小T细胞(图5E)。这是大的增殖T细胞数量31%减少。9天后,这些数字甚至进一步减少至培养物中平均(n=4)1603个大的增殖T细胞和14366个小T细胞(图5F)。这代表大的增殖T细胞减少了84%。
为了确保这种减少不仅仅是由于血浆来自同种异体的人来源,也不是具体是因为它与癌症有关,进行了以下实验:从健康对象#1中分离CD3+T细胞。这些细胞在含有FCS、对象#1的血浆、另一个健康对象#2的血浆、第三个健康对象#3的血浆、癌症患者L.F.的血浆、癌症患者A.G.的血浆和第三个癌症患者B.S.的血浆中任一个的培养基中培养。所有类型的血清/血浆在将其加入细胞培养基之前都被热灭活(56℃,30分钟)。2.5天(60小时)和6天后,通过FACS对T细胞的总数以及仅小T细胞或大T细胞的数量进行计数。结果总结在表7中,并显示正常人T细胞可以在含有健康人对象的同基因或同种异体热灭活血浆的培养基中于组织培养下存活至少6天。
表7:癌症患者的血浆对增殖T细胞的有害影响
2.5天后,健康的人对象(同基因或同种异体)的血浆能够替代FCS,其中大的增殖T细胞仅略有减少,而事实上,当培养延长至6天时,来自健康的人对象的血浆在支持培养的大的增殖T细胞方面如果没有比FCS更好,那也是同样好的(图5G-图5H)。相比之下,癌症患者的血浆对大的增殖T细胞的存活产生强烈的负面影响,并且仅在6天后,所有三名被测试的癌症患者的血浆就使大的增殖T细胞的数量减少了大于50%(图5I)。
综上所述,这些结果表明肝癌患者的血浆本身可能对T细胞存活有害。这加强了癌症患者接受免疫疗法以补偿他们自身普遍对T细胞的缺乏和/或补偿那些次优T细胞的需要。此外,这将使他们的“恢复活力”的T细胞战斗以克服他们的癌症,这可能是其血浆中存在的敌对/有害抗T细胞因子的起源。最后,随着时间的推移,它进一步强化了持续免疫疗法的必要,因为这种有害的环境可能会在短短一周内开始损害所给予的T细胞。
尽管已经结合其具体实施方式描述了本发明,但是很明显,多种可选方案、修改和变化对于本领域技术人员来说将是显而易见的。因此,意图包括落入所附权利要求的精神和广泛范围内的所有此类可选方案、修改和变化。
Claims (87)
1.在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使所述第一免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的程序性细胞死亡1(PD-1)表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
d.提供与所述第一免疫细胞来源相同的第二免疫细胞;
e.使所述第二免疫细胞与所述至少一种分子接触,其中所述至少一种分子降低所述第一免疫细胞中的PD-1表达或功能、增加所述第一免疫细胞的增殖、增加与所述第一免疫细胞共培养的癌细胞死亡或其组合;和
f.将所述接触的第二免疫细胞向所述对象给予;
从而在所述对其有需要的对象中执行过继性神经免疫疗法。
2.在对其有需要的对象中的过继性神经免疫疗法的方法,所述方法包括:
a.提供第一免疫细胞;
b.使所述第一免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或至少一种电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞中的PD-1表达水平或功能水平;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对至少一种细胞因子的分泌;
xi.所述免疫细胞对至少一种治疗性蛋白质的分泌;和
xii.参与过程i至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平;
d.提供与所述第一免疫细胞来源相同的第二免疫细胞;
e.使所述第二免疫细胞与所述至少两种分子接触,其中所述至少两种分子降低所述第一免疫细胞中的PD-1表达水平或功能水平、增加所述第一免疫细胞的增殖、增加仅与所述第一免疫共细胞培养的癌细胞死亡或共培养的癌细胞死亡、增加所述第一免疫细胞中的ζ链表达、增加所述第一免疫细胞的迁移、增加所述第一免疫细胞对细胞因子的分泌、增加所述第一免疫细胞的粘附、增加所述第一免疫细胞的归巢、增加所述免疫细胞对至少一种治疗性蛋白质的分泌、降低参与过程i的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平、提高参与过程ii至xi的至少一种蛋白质或基因在所述免疫细胞中的表达水平或功能水平、或其组合;和
f.将所述接触的第二免疫细胞向所述对象给予;
从而在所述对其有需要的对象中执行过继性神经免疫疗法。
3.根据权利要求1或2所述的方法,其中所述对象遭受具有或疑似具有次优的T细胞数量、活性或两者的疾病、状况、损伤或创伤。
4.根据权利要求3所述的方法,其中所述疾病、状况、损伤或创伤选自:癌症、传染病、遗传免疫缺陷、获得性免疫缺陷、退行性疾病、自身免疫疾病、代谢疾病、遗传疾病、神经或神经精神疾病、和器官移植后伴有免疫功能不全。
5.根据权利要求4所述的方法,其中所述疾病、状况、损伤或创伤是传染病。
6.根据权利要求4所述的方法,其中所述疾病、状况、损伤或创伤是癌症。
7.根据权利要求4所述的方法,其中所述疾病、状况、损伤或创伤需要组织或器官修复,或T细胞衍生因子的递送。
8.根据权利要求1至7中任一项所述的方法,其中所述免疫细胞是表达PD-1的免疫细胞。
9.根据权利要求1至8中任一项所述的方法,其中所述免疫细胞是T细胞。
10.根据权利要求1至9中任一项所述的方法,其中所述第一和第二免疫细胞来自所述患者。
11.根据权利要求1至10中任一项所述的方法,其中所述第一和第二免疫细胞来自健康供体。
12.根据权利要求1至11中任一项所述的方法,其中所述第一提供的免疫细胞在所述接触之前未被预先活化。
13.根据权利要求1至12中任一项所述的方法,其中所述第一提供的免疫细胞是多种免疫细胞并且进一步包括从所述第一提供的免疫细胞中选择免疫细胞的亚群。
14.根据权利要求13所述的方法,其中所述免疫细胞的亚群选自:效应T细胞、辅助T细胞、细胞毒性T细胞、调节T细胞、抑制T细胞、自然杀伤T细胞、炎性T细胞、记忆T细胞、γδT细胞、组织/器官浸润T细胞、肿瘤浸润T细胞、修复T细胞和促再生T细胞、黏膜相关T细胞、修复T细胞、促再生T细胞、活化T细胞、和灭活T细胞。
15.根据权利要求1至14中任一项所述的方法,进一步包括在免疫细胞培养基中培养所提供的免疫细胞。
16.根据权利要求15所述的方法,其中所述免疫细胞培养基包含人血浆或血清。
17.根据权利要求1至16中任一项所述的方法,进一步包括扩大所述提供的免疫细胞。
18.根据权利要求17所述的方法,其中所述扩大包括所述免疫细胞的刺激,并且所述方法进一步包括培养足以使至少50%的所述提供的免疫细胞进入静息状态的时间段。
19.根据权利要求18所述的方法,其中所述进一步培养持续1和7天之间。
20.根据权利要求18或19所述的方法,其中所述刺激包括活化所述免疫细胞。
21.根据权利要求18至20中任一项所述的方法,其中所述刺激通过CD3、CD28、促细胞分裂原、生长因子和细胞因子中的至少一个进行。
22.根据权利要求1至21中任一项所述的方法,其中所述接触是使所述免疫细胞与所述分子或分子的组合孵育。
23.根据权利要求1至22中任一项所述的方法,其中所述第一免疫细胞是多种免疫细胞,并且所述第一免疫细胞是单独分裂和培养的;不同的分子或分子的组合与所述分裂的免疫细胞的每一种接触,并且实现最大增加或减少的分子或分子的组合被接触。
24.根据权利要求1至23中任一项所述的方法,其中所述第二免疫细胞是多种免疫细胞,并且所述第二免疫细胞被分裂并与不同的分子或分子的组合接触并按顺序向所述对象给予。
25.根据权利要求24所述的方法,其中所述按顺序给予到达所述对象中的至少一个部位并且通过至少一种给予方式进行。
26.根据权利要求1至25中任一项所述的方法,其中所述神经递质的类似物是神经递质受体激动剂或神经递质受体拮抗剂。
27.根据权利要求1至26中任一项所述的方法,其中所述神经递质或其类似物选自:多巴胺、谷氨酸、多巴胺受体激动剂、谷氨酸/AMPA/NMDA受体激动剂、谷氨酸/AMPA/NMDA受体拮抗剂、和多巴胺受体拮抗剂。
28.根据权利要求27所述的方法,其中所述多巴胺受体激动剂选自多巴胺D1/5受体激动剂、多巴胺D2受体激动剂、多巴胺D3受体激动剂、和多巴胺D4受体激动剂。
29.根据权利要求28所述的方法,其中所述多巴胺D1/5受体激动剂选自多巴胺、非诺多泮、非诺多潘、A77636、和SKF38393。
30.根据权利要求28所述的方法,其中所述多巴胺D2受体激动剂是舒马尼罗。
31.根据权利要求28所述的方法,其中所述多巴胺D3受体激动剂选自PD 128907和7-OH-DPAT。
32.根据权利要求28所述的方法,其中所述多巴胺D4受体激动剂选自PD 168077和A412997。
33.根据权利要求27所述的方法,其中所述谷氨酸/AMPA/NMDA受体激动剂选自谷氨酸、AMPA和NMDA。
34.根据权利要求27所述的方法,其中所述谷氨酸/AMPA/NMDA受体拮抗剂选自CNQX、MK801。
35.根据权利要求27所述的方法,其中所述多巴胺受体拮抗剂选自多巴胺D1/5受体拮抗剂、多巴胺D2受体拮抗剂、多巴胺D3受体拮抗剂、和多巴胺D4受体拮抗剂。
36.根据权利要求28所述的方法,其中所述多巴胺D1/5受体拮抗剂是SCH 39166。
37.根据权利要求28所述的方法,其中所述多巴胺D2受体拮抗剂是L-741626。
38.根据权利要求28所述的方法,其中所述多巴胺D3受体拮抗剂是NGB 2904。
39.根据权利要求28所述的方法,其中所述多巴胺D4受体拮抗剂是L-741742。
40.根据权利要求1至39中任一项所述的方法,其中所述神经肽或其类似物选自GnRH-I、GnRH-II、CGRP、生长抑素、和神经肽Y。
41.根据权利要求1至40中任一项所述的方法,其中所述电压门控离子通道选自电压门控钠通道、钙通道、钾通道(Kv)和氯通道。
42.根据权利要求41所述的方法,其中所述电压门控离子通道是电压门控钾通道。
43.根据权利要求42所述的方法,其中所述电压门控钾通道是亚家族A的钾电压门控通道。
44.根据权利要求43所述的方法,其中所述亚家族A的钾电压门控通道是Kv1.1。
45.根据权利要求1至44中任一项所述的方法,其中所述电压门控离子通道的调节剂是离子通道阻断剂。
46.根据权利要求45所述的方法,其中所述离子通道拮抗剂是电压门控Kv1.l离子通道阻断剂。
47.根据权利要求46所述的方法,其中所述Kv1.1离子通道阻断剂选自树眼镜蛇毒素K(DTX-K)和抗Kv1.1阻断抗体。
48.根据权利要求1至47中任一项所述的方法,其中所述给予包括选择和给予所述第二接触的免疫细胞的亚群。
49.根据权利要求1至48中任一项所述的方法,其中给予所述接触的第二免疫细胞包括给予2X10^6与10^9个之间的免疫细胞。
50.根据权利要求1至49中任一项所述的方法,其中所述给予包括重复给予接触的免疫细胞。
51.根据权利要求1至50中任一项所述的方法,其中所述给予包括无限期地给予。
52.根据权利要求1至51中任一项所述的方法,其中所述第一免疫细胞在步骤b之前已经被冷冻和解冻。
53.根据权利要求52所述的方法,其中所述被冷冻的免疫细胞在包含人血浆或血清的冷冻培养基中冷冻。
54.根据权利要求1至53中任一项所述的方法,其中所述治疗是所述疾病、状况、损伤或创伤的一线治疗或专有治疗。
55.根据权利要求1至54中任一项所述的方法,其中所述治疗在针对所述疾病、状况、损伤或创伤的不同疗法之前、期间、与其同时或在其之后。
56.根据权利要求1至55中任一项所述的方法,其中所述给予的细胞在所述对象中执行以下功能中的至少一种:
a.杀死致病细胞;
b.杀死传染性生物体;
c.治愈所述疾病或状况;
d.修复组织或器官;
e.替换受损的细胞、或组织;
f.补偿损失或缺陷;
g.预防所述疾病或状况;和
h.使组织或器官再生。
57.选择适合神经免疫疗法的对象的方法,所述方法包括,
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的程序性细胞死亡1(PD-1)表达;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
其中PD-1表达或功能的降低、增殖的增加、癌细胞死亡的增加及其组合中的至少一个指示所述对象适合神经免疫疗法。
58.选择适合神经免疫疗法的对象的方法,所述方法包括,
a.提供来自所述对象的免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或至少一种电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的PD-1表达或活性;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对细胞因子的分泌;
xi.所述免疫细胞对治疗性蛋白质的分泌;和
xii.参与过程i至xi的蛋白质和基因的表达水平和功能水平;
其中PD-1表达或活性的降低、单独或共培养的所述免疫细胞的增殖的增加、癌细胞死亡的增加、ζ链表达的增加、迁移的增加、细胞因子分泌的增加、粘附的增加、归巢的增加、至少一种治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因的表达或功能的降低、或参与过程ii至xi的至少一种蛋白质或基因的表达或功能的提高中的至少一个指示所述对象适合神经免疫疗法。
59.选择用于提高免疫治疗潜力的分子的方法,所述方法包括:
a.提供免疫细胞;
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的程序性细胞死亡1(PD-1)表达;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
其中PD-1表达或功能的降低、增殖的增加、癌细胞死亡的增加及其组合中的至少一个指示所述至少一种分子提高了所述免疫细胞的治疗潜力。
60.选择用于提高治疗性免疫细胞潜力的分子的组合的方法,所述方法包括:
a.提供免疫细胞;
b.使所述第一免疫细胞与选自神经递质或其类似物、和神经肽或其类似物、或电压门控离子通道的调节剂的至少两种分子接触;
c.测量以下至少一项:
i.所述免疫细胞上的PD-1表达或活性;
ii.与癌细胞共培养的所述免疫细胞的增殖;和
iii.与所述免疫细胞共培养的癌细胞的细胞死亡;
iv.单独培养的所述免疫细胞的增殖;
v.所述免疫细胞中CD3ζ链的表达;
vi.所述免疫细胞的迁移;
vii.所述免疫细胞的粘附;
viii.所述免疫细胞的归巢;
ix.所述免疫细胞的穿透;
x.所述免疫细胞对细胞因子的分泌;
xi.所述免疫细胞对治疗性蛋白质的分泌;和
xii.参与以上过程的蛋白质和基因的表达水平和功能水平;
其中PD-1表达或活性的降低、单独或共培养的所述免疫细胞的增殖的增加、癌细胞死亡的增加、ζ链表达的增加、迁移的增加、细胞因子分泌的增加、粘附的增加、归巢的增加、至少一种治疗性蛋白质的分泌的增加、参与过程i的至少一种蛋白质或基因的表达或功能的降低、或参与过程ii至xi的至少一种蛋白质或基因的表达或功能的提高中的至少一个指示所述至少一种分子提高了所述免疫细胞的治疗潜力。
61.根据权利要求59或60所述的方法,其中所述免疫细胞的免疫治疗潜力是所述细胞治疗存在或疑似是次优的T细胞数量、活性或两者的疾病、状况、创伤或损伤的潜力。
62.降低免疫细胞表面上的PD-1表达的方法,所述方法包括向所述免疫细胞给予选自神经递质或其类似物、神经肽或其类似物、或电压门控离子通道的调节剂的至少一种分子。
63.增强免疫细胞功能的方法,所述方法包括:
a.提供免疫细胞;和
b.使所述免疫细胞与选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少两种分子接触。
64.选择适合过继性免疫疗法的对象的方法,所述方法包括,
a.提供健康的免疫细胞;
b.将所述健康的免疫细胞与来自所述对象的血浆或血清接触;和
c.测量所述免疫细胞的存活;
其中所述健康的免疫细胞的存活的降低指示在所述对象的身体内,其免疫细胞暴露于由其血浆或血清内的因子所诱导的有害作用,因此所述对象适合过继性免疫疗法。
65.试剂盒,其包含至少一种神经递质或其类似物、至少一种神经肽或其类似物和至少一种电压门控离子通道的调节剂。
66.试剂盒,其包含PD-1检测剂和选自神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂的至少一种分子。
67.根据权利要求65或66所述的试剂盒,其用于选择用于提高治疗性免疫细胞潜力的分子。
68.根据权利要求65或66所述的试剂盒,其用于在神经免疫疗法期间提高免疫细胞功能。
69.根据权利要求65或66所述的试剂盒,其用于确定对其有需要的对象是否适合神经免疫疗法。
70.根据权利要求65或66所述的试剂盒,其用于治疗对其有需要的对象中存在或疑似是次优的T细胞活性、数量或两者的疾病、状况、创伤或损伤或预防其复发。
71.根据权利要求65至70中任一项所述的试剂盒,其中所述PD-1检测剂是抗PD-1抗体。
72.根据权利要求65至71中任一项所述的试剂盒,其中所述PD-1检测剂包括标签。
73.根据权利要求72所述的试剂盒,其中所述标签是荧光标签。
74.根据权利要求65至73中任一项所述的试剂盒,其包含所述分子中的至少两种。
75.根据权利要求65至74中任一项所述的试剂盒,其中所述神经递质或其类似物、神经肽或其类似物、和电压门控离子通道的调节剂以至多10^-7摩尔(M)的浓度被提供。
76.根据权利要求65至75中任一项所述的试剂盒,其进一步包含至少一种神经递质或其类似物、至少一种神经肽或其类似物、和至少一种电压门控离子通道的调节剂的至少一种组合。
77.根据权利要求65至76中任一项所述的试剂盒,其进一步包含组织培养板,其中所述板的单独孔容纳单独的分子或分子的组合。
78.用于储存用于免疫疗法的免疫细胞的方法,所述方法包括在包含人血浆或血清的培养基中培养或冷冻免疫细胞。
79.根据权利要求78所述的方法,所述人血浆或血清来自提供所述免疫细胞的对象。
80.根据权利要求78所述的方法,其中所述人血浆或血清来自健康的同种异体个体。
81.在对其有需要的对象中的免疫疗法的方法,所述方法包括:
a.提供来自所述对象的免疫细胞;
b.在包含来自健康的同种异体个体的血浆或血清的培养基中培养所述免疫细胞;
c.将所述培养的免疫细胞返回给所述对象;
从而在所述对其有需要的对象中执行免疫疗法。
82.选择适合免疫疗法的对象的方法,所述方法包括:
a.提供免疫细胞;
b.在包含来自所述对象的血浆或血清的培养基中培养所述免疫细胞;和
c.监测所述免疫细胞的存活;
其中与在不包含来自所述对象的血浆或血清的培养基中培养的免疫细胞相比,所述免疫细胞的存活的降低指示所述对象适合免疫疗法。
83.根据权利要求82所述的方法,其中所述免疫细胞来自健康供体。
84.根据权利要求82或83所述的方法,其中所述免疫细胞是大的增殖T细胞。
85.根据权利要求82至84中任一项所述的方法,其中所述免疫细胞是多种免疫细胞,并且其中降低的存活包括存活的免疫细胞的数量减少至少30%。
86.根据权利要求82至85中任一项所述的方法,其中所述培养持续至少两天半。
87.根据权利要求78至86中任一项所述的方法,其中所述免疫疗法是神经免疫疗法并且包括权利要求1-60所述的任一种方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862621805P | 2018-01-25 | 2018-01-25 | |
| PCT/IL2019/050104 WO2019145956A1 (en) | 2018-01-25 | 2019-01-24 | Methods for improved immunotherapy |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113597312A true CN113597312A (zh) | 2021-11-02 |
Family
ID=65729410
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980091985.4A Pending CN113597312A (zh) | 2018-01-25 | 2019-01-24 | 用于改善的免疫疗法的方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20220072042A1 (zh) |
| EP (1) | EP3914267A1 (zh) |
| JP (1) | JP2022513330A (zh) |
| KR (1) | KR20210126556A (zh) |
| CN (1) | CN113597312A (zh) |
| AU (1) | AU2019211777A1 (zh) |
| BR (1) | BR112021014546A2 (zh) |
| CA (1) | CA3127176A1 (zh) |
| IL (1) | IL284816A (zh) |
| SG (1) | SG11202106249QA (zh) |
| WO (1) | WO2019145956A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116617222A (zh) * | 2023-05-10 | 2023-08-22 | 徐州医科大学 | 小分子离子通道阻滞剂mk-801在制备治疗肿瘤或抗感染药物的应用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101296943A (zh) * | 2005-08-03 | 2008-10-29 | 米亚·利维特 | 通过多巴胺d1r激动剂杀伤人类淋巴瘤和白血病癌细胞和tcr活化的人类正常细胞 |
| WO2015104711A1 (en) * | 2014-01-09 | 2015-07-16 | Hadasit Medical Research Services And Development Ltd. | Improved cell compositions and methods for cancer therapy |
| WO2017015427A1 (en) * | 2015-07-21 | 2017-01-26 | Novartis Ag | Methods for improving the efficacy and expansion of immune cells |
| CN108463547A (zh) * | 2015-10-28 | 2018-08-28 | 生命技术股份公司 | 通过改变细胞表面信号和信号比选择性扩增不同的t细胞亚群 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4666828A (en) | 1984-08-15 | 1987-05-19 | The General Hospital Corporation | Test for Huntington's disease |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US4801531A (en) | 1985-04-17 | 1989-01-31 | Biotechnology Research Partners, Ltd. | Apo AI/CIII genomic polymorphisms predictive of atherosclerosis |
| US5272057A (en) | 1988-10-14 | 1993-12-21 | Georgetown University | Method of detecting a predisposition to cancer by the use of restriction fragment length polymorphism of the gene for human poly (ADP-ribose) polymerase |
| US5192659A (en) | 1989-08-25 | 1993-03-09 | Genetype Ag | Intron sequence analysis method for detection of adjacent and remote locus alleles as haplotypes |
| WO2006111967A2 (en) * | 2005-04-18 | 2006-10-26 | Mia Levite | Method for augmenting the ability of t-cells and other cells for fighting disease and invade diseased organs, for elevating cd3 zeta and tnf-alpha expression in t-cells, and mixing t-cell boosting devices and kit particularly useful in such method |
| EP1917277A4 (en) * | 2005-08-03 | 2009-08-05 | Mia Levite | BRAZING HUMAN LYMPHOMA AND LEUKEMIA CANCER CELLS, AND TCR-ACTIVATED NORMAL HUMAN CELLS BY DOPAMIN D1R AGONISTS |
| US20140065096A1 (en) * | 2012-09-05 | 2014-03-06 | Regen BioPharma, Inc. | Cancer therapy by ex vivo activated autologous immune cells |
-
2019
- 2019-01-24 EP EP19710502.6A patent/EP3914267A1/en active Pending
- 2019-01-24 AU AU2019211777A patent/AU2019211777A1/en not_active Abandoned
- 2019-01-24 BR BR112021014546-0A patent/BR112021014546A2/pt unknown
- 2019-01-24 KR KR1020217022540A patent/KR20210126556A/ko not_active Application Discontinuation
- 2019-01-24 SG SG11202106249QA patent/SG11202106249QA/en unknown
- 2019-01-24 CN CN201980091985.4A patent/CN113597312A/zh active Pending
- 2019-01-24 CA CA3127176A patent/CA3127176A1/en active Pending
- 2019-01-24 JP JP2021543486A patent/JP2022513330A/ja active Pending
- 2019-01-24 WO PCT/IL2019/050104 patent/WO2019145956A1/en active Application Filing
- 2019-01-24 US US17/424,499 patent/US20220072042A1/en active Pending
-
2021
- 2021-07-13 IL IL284816A patent/IL284816A/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101296943A (zh) * | 2005-08-03 | 2008-10-29 | 米亚·利维特 | 通过多巴胺d1r激动剂杀伤人类淋巴瘤和白血病癌细胞和tcr活化的人类正常细胞 |
| WO2015104711A1 (en) * | 2014-01-09 | 2015-07-16 | Hadasit Medical Research Services And Development Ltd. | Improved cell compositions and methods for cancer therapy |
| WO2017015427A1 (en) * | 2015-07-21 | 2017-01-26 | Novartis Ag | Methods for improving the efficacy and expansion of immune cells |
| CN108463547A (zh) * | 2015-10-28 | 2018-08-28 | 生命技术股份公司 | 通过改变细胞表面信号和信号比选择性扩增不同的t细胞亚群 |
Non-Patent Citations (4)
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116617222A (zh) * | 2023-05-10 | 2023-08-22 | 徐州医科大学 | 小分子离子通道阻滞剂mk-801在制备治疗肿瘤或抗感染药物的应用 |
| CN116617222B (zh) * | 2023-05-10 | 2024-05-03 | 徐州医科大学 | 小分子离子通道阻滞剂mk-801在制备治疗肿瘤或抗感染药物的应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022513330A (ja) | 2022-02-07 |
| CA3127176A1 (en) | 2019-08-01 |
| US20220072042A1 (en) | 2022-03-10 |
| IL284816A (en) | 2021-08-31 |
| EP3914267A1 (en) | 2021-12-01 |
| WO2019145956A1 (en) | 2019-08-01 |
| AU2019211777A1 (en) | 2021-09-16 |
| BR112021014546A2 (pt) | 2021-10-05 |
| SG11202106249QA (en) | 2021-07-29 |
| KR20210126556A (ko) | 2021-10-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Garris et al. | Successful anti-PD-1 cancer immunotherapy requires T cell-dendritic cell crosstalk involving the cytokines IFN-γ and IL-12 | |
| US20210040215A1 (en) | Methods for enhancing the potency of the immune checkpoint inhibitors | |
| Strater et al. | CD95 (APO-1/Fas)-mediated apoptosis in colon epithelial cells: a possible role in ulcerative colitis | |
| Arora et al. | Invariant natural killer T cells coordinate removal of senescent cells | |
| US20230340099A1 (en) | Composition comprising chemokine inhibitor, colony stimulating factor inhibitor, and cancer immunotherapy agent for prevention or treatment of cancer and combination therapy | |
| JP2021167345A (ja) | Gvhd又は腫瘍を治療するための骨髄系由来サプレッサー細胞のインフラマソーム活性化の調節 | |
| CN113597312A (zh) | 用于改善的免疫疗法的方法 | |
| KR20190059304A (ko) | Tim-3 상승을 치료하는 방법 | |
| Wu et al. | Osteoclast-derived apoptotic bodies inhibit naive CD8+ T cell activation via Siglec15, promoting breast cancer secondary metastasis | |
| Tang et al. | Anti-CD20 monoclonal antibody combined with adenovirus vector-mediated IL-10 regulates spleen CD4+/CD8+ T cells and T-bet/GATA-3 expression in NOD mice | |
| WO2020027832A1 (en) | Chemokine responsive activated natural killer cells with secondary homing activation for verified targets | |
| US20230054656A1 (en) | Diagnostic and prognostic utility of exosomes in immunotherapy | |
| US20230072528A1 (en) | Methods for discontinuing a treatment with a tyrosine kinase inhibitor (tki) | |
| US20180228775A1 (en) | Methods of treating cancer | |
| CN116421720A (zh) | 抗肿瘤联用细胞产品和抗肿瘤细胞产品 | |
| CN115212231A (zh) | 调节间充质干细胞免疫调节功能方法和试剂 | |
| AU2021329838A1 (en) | B-cell based immunotherapy for the treatment of glioblastoma and other cancers | |
| CN111670040A (zh) | Aldh1抗原冲击树突状细胞 | |
| CN116139275A (zh) | Cd300ld抑制剂在制备预防、诊断或治疗肿瘤产品中的用途 | |
| KR20230044315A (ko) | 췌장 암 평가 및 치료를 위한 방법 및 조성물 | |
| JP2021526826A (ja) | ウイルス検出アッセイ | |
| Durham et al. | Cancer Immunotherapy: Chapter 18. Dendritic Cell Vaccines: Sipuleucel-T and Other Approaches | |
| Kar et al. | Novel CCL21-Vault Nanocapsule Intratumoral Delivery Inhibits Lung Cancer | |
| US20130338080A1 (en) | Compositions and methods for treating an activated b-cell diffuse large b-cell lymphoma | |
| WO2017011352A1 (en) | Methods for treating pain |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |