CN108367109B - 用于体外循环肺支持的方法 - Google Patents
用于体外循环肺支持的方法 Download PDFInfo
- Publication number
- CN108367109B CN108367109B CN201680063827.4A CN201680063827A CN108367109B CN 108367109 B CN108367109 B CN 108367109B CN 201680063827 A CN201680063827 A CN 201680063827A CN 108367109 B CN108367109 B CN 108367109B
- Authority
- CN
- China
- Prior art keywords
- blood
- oxygen
- dialysis
- dialysis liquid
- liquid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/14—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis
- A61M1/16—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis with membranes
- A61M1/1698—Blood oxygenators with or without heat-exchangers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/14—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis
- A61M1/16—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis with membranes
- A61M1/1654—Dialysates therefor
- A61M1/1676—Dialysates therefor containing proteins, e.g. albumin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/14—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis
- A61M1/16—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis with membranes
- A61M1/1694—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis with membranes with recirculating dialysing liquid
- A61M1/1696—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis with membranes with recirculating dialysing liquid with dialysate regeneration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/14—Dialysis systems; Artificial kidneys; Blood oxygenators ; Reciprocating systems for treatment of body fluids, e.g. single needle systems for hemofiltration or pheresis
- A61M1/32—Oxygenators without membranes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3666—Cardiac or cardiopulmonary bypass, e.g. heart-lung machines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/369—Temperature treatment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/02—Gases
- A61M2202/0208—Oxygen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/02—Gases
- A61M2202/0225—Carbon oxides, e.g. Carbon dioxide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/03—Gases in liquid phase, e.g. cryogenic liquids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/04—Liquids
- A61M2202/0468—Liquids non-physiological
- A61M2202/0476—Oxygenated solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/06—Solids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2230/00—Measuring parameters of the user
- A61M2230/20—Blood composition characteristics
- A61M2230/202—Blood composition characteristics partial carbon oxide pressure, e.g. partial dioxide pressure (P-CO2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2230/00—Measuring parameters of the user
- A61M2230/20—Blood composition characteristics
- A61M2230/205—Blood composition characteristics partial oxygen pressure (P-O2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2230/00—Measuring parameters of the user
- A61M2230/20—Blood composition characteristics
- A61M2230/208—Blood composition characteristics pH-value
Abstract
本发明一般地涉及一种适于体外循环肺支持的方法。所述方法包括使血液与由半渗透膜隔开的透析液体接触。在使血液与由半渗透膜隔开的透析液体接触之前,向血液中和/或向透析液体中引入氧。所述方法是多功能的,其允许血液氧合以及从血液中去除血液中存在的至少一种不期望的物质,所述物质选自二氧化碳、碳酸氢根和氢阳离子。由此,本发明在体外循环接触步骤中利用了Haldane效应。不期望的物质可通过半渗透膜高效地转运到透析液体中。与现有技术的体外循环二氧化碳去除方法(ECCO2R)相比,本发明采用多功能透析液体,取决于病症和需要,其允许调节透析液体的pH和缓冲能力、向透析液体和/或向血液添加流体以及在体外循环回路中从血液中去除物质。本发明还提供了透析液体的再生和再循环以使其重复使用。本发明适于治疗患有肺衰竭或肺病的人或动物对象。
Description
本发明一般地涉及一种适于体外循环肺支持的方法。所述方法包括使血液经由半渗透膜与透析液体接触。在所述接触步骤之前、之后或同时,血液或透析液体或二者变得富氧。对于透析液体的富氧,氧从透析液体到血液的净转移通过半渗透膜进行。接触步骤还允许将不期望的物质通过半渗透膜从血液直接去除到透析液体中。由此提供了高效的体外循环肺支持。
引言
代谢物在血液中的转运
为了人或动物的生存,整个有机体的适当氧合是重要的。分子氧O2对于所有好氧生物体的细胞呼吸都是必不可少的。血红细胞(红细胞)在肺中吸收氧并负责运载氧遍及全身。血红细胞中结合肺中氧的化学实体是蛋白质血红蛋白,特别是血红蛋白的亚铁血红素部分。
由于代谢活动,人体或动物体会产生二氧化碳、H+离子和其他代谢物。一般来说,在脊椎动物(人或动物)体内,由于代谢活动,将在外周组织中产生二氧化碳。在外周组织的毛细血管中,组织中产生的二氧化碳将沿着其降低的分压梯度向血液中、主要是向红细胞中扩散。在脊椎动物体内,二氧化碳在血液中的转运有三种主要途径:(a)溶解的CO2(二氧化碳远比氧更可溶于血液中),(b)与血液蛋白如血红蛋白和血浆蛋白结合,和(c)以离子对形式:碳酸氢根离子和H+离子。在静息的成年人体内,每分钟会产生大约10mmol的CO2。此外,红细胞中每分钟会产生大约8mmol H+离子(大约15000mmol/天)。基于成年人血液量(5l)计算,每分钟会有10mmol CO2负载到5l血液中,即每l血液2mmol H+离子。
肾通常承担大约100mmol H+离子/天的去除。
在分子水平上,与蛋白结合的二氧化碳(b)通过与血液蛋白例如血红蛋白的氨基基团缔合形成氨甲酰蛋白如氨甲酰血红蛋白而可逆地结合到血液蛋白如血红蛋白和血浆蛋白。因此,二氧化碳通常不会像氧那样与铁结合,而是与血红蛋白蛋白质的氨基基团和其他血液蛋白、特别是血浆蛋白的多肽链上的氨基基团结合。碳酸氢根离子(c)来源于二氧化碳,其在进入血红细胞(红细胞)中后将与水结合形成碳酸(H2CO3)。该反应主要由碳酸酐酶催化,碳酸酐酶尤其见于血红细胞中。该酶也见于肺内皮中及身体的其他部位处。碳酸然后解离形成碳酸氢根离子(HCO3 -)和氢阳离子:
该反应的反应物(离析物和产物)以动态平衡存在——如由上面方程式中的箭头定性所示。根据Le Chatelier的原理,添加或去除一种或多于一种反应物(无论是在体内还是在体外)将导致反应根据平衡而移动。对于该反应的发生本身,碳酸酐酶不是严格需要的;然而,其对于高效的转化来说是重要的。
氧、二氧化碳和H+离子主要在血液中转运,与周围空气的气体交换(氧、二氧化碳、水)发生在肺中。
在人体或动物体内,如血液的流体必须保持在窄的pH范围内,例如,在人体中优选保持在pH为7.35至7.45,即微碱性的范围内。血液中转运的代谢物,如二氧化碳(CO2)可影响血液pH。
作为代谢活动的结果,人体或动物体不仅产生二氧化碳,而且产生酸性有机分子。酸性有机分子是H+离子的又一来源。H+离子的存在影响血液pH。然而,在人体或动物体内,如血液的流体必须保持在窄的pH范围内,例如,在人体中保持在pH为7.35至7.45,即微碱性的范围内。因此血液的缓冲是重要的。当对象患有与过量H+离子相关的病症时,血液的缓冲能力通常会不足以使血液保持在该pH范围内。
通常,在碳酸解离成氢阳离子和碳酸氢根离子时形成的氢阳离子可与血液中、特别是红细胞中的蛋白质结合。主要的细胞内氢阳离子受体或用于结合氢阳离子的缓冲剂是蛋白质血红蛋白。血红蛋白和较低程度的血浆蛋白能够缓冲血液的pH,例如过量的氢阳离子。当血液穿过组织毛细血管时,氢阳离子的缓冲将使血液的pH变化最小化。然而,缓冲能力不是无限的,并因此可能发生酸中毒。氢阳离子主要与血红蛋白的组氨酸侧链结合。
碳酸氢根在生理pH缓冲体系中起着关键的生物化学作用。在健康的脊椎动物(人或动物)体内,(a)约5%的二氧化碳溶解在血浆中来不变地转运;(b)约10%的二氧化碳与血液蛋白、特别是血红蛋白和血浆蛋白相结合来转运;和(c)大部分二氧化碳以碳酸氢根离子和氢阳离子的形式转运;氢阳离子主要与蛋白质结合。
在健康的人体或动物体的呼吸器官——肺中,二氧化碳被释放;从而使CO2的分压(pCO2)减小。(人)对象动脉血中pCO2的正常值在35mmHg至45mmHg范围内。超过45mmHg的pCO2在本文中称为“高pCO2”或“增加的pCO2”。换气不足是导致高pCO2的一个可能原因。如果对象动脉血中的pCO2高于45mmHg,则对象可能需要治疗以降低pCO2。
术语酸中毒指哺乳动物体内酸度的增加。酸中毒可通过测量对象的体液、特别是血浆、更特别是动脉血浆的pH来确定。在哺乳动物、特别是人中,酸中毒的特征在于动脉血浆的pH低于7.35。人体或动物体通常不能耐受血液pH值低于6.8,因为超出此范围的pH通常会导致不可逆的细胞损伤。因此,酸中毒的特征在于动脉血浆的pH为6.8至低于7.35。
通常,根据血浆中酸度的分子原因,患有酸中毒的对象可分为两大亚类:呼吸性酸中毒和代谢性酸中毒。在分子水平上,代谢性酸中毒是由酸性有机分子数量的增多所致,酸性有机分子数量的增多是由于代谢活动增加导致产生的有机酸(例如,乳酸)增多和/或经由肾排泄酸的能力失调引起的。在分子水平上,呼吸性酸中毒是由于通气减少(换气不足)导致血液中二氧化碳的积聚所致。其通常由肺功能失常引起。颅脑损伤、药物(尤其是麻醉剂和镇静剂)以及中枢神经系统异常如脑肿瘤也可能导致这种情况。其还可能作为慢性代谢性碱中毒的代偿性反应发生。如果呼吸性酸中毒持续,例如在削弱肺功能的疾病如晚期肺气肿和肌营养不良的情况下,这样的代偿机制,即外源性碳酸氢根输注,将不能高效地逆转与未代偿的呼吸性酸中毒相关的二氧化碳积聚。在这种情况下,可能需要使用肺支持。
在实践中,存在表现出两种病症的症状的患者。给定的对象可能患有(i)代谢性酸中毒、或(ii)呼吸性酸中毒、或(iii)代谢性和呼吸性酸中毒的组合中的任何一种。
用于肺支持的现有技术系统
医学领域的一项重大突破是对患呼吸衰竭的对象进行机械通气的发明及后来的使用。在德国,每年有超过240000名对象机械通气,平均治疗时间为10天。这些对象的平均死亡率为35%。如果其他器官功能障碍与呼吸衰竭一起发生,则死亡率可能增至最高75%。
机械通气是一种机械辅助或替代自主呼吸的方法,即一种肺支持的方法。机械通气可能涉及机器(呼吸机),或呼吸可能由医疗保健专业人员如护士或医生辅助。在任一情况下,机械通气都可能涉及穿透到对象身体中的装置(“有创机械通气”),即穿透口腔(如气管内导管)或穿透皮肤(如气管造口管)。有两种主要的机械通气模式:气体(例如,空气)被推入气管中的正压通气,以及负压通气,例如,通过将患者的胸部置于低压室中,这将使得胸部扩张,并由此将空气吸入患者的肺中。除了机械通气的所有积极效果外,还存在不期望的缺点:不期望的后果可包括但不限于以下:内脏器官例如肝的血液灌注减少多达30%、血压降低、腹内压升高、肾排泄功能降低、呼吸机引起的肺损伤(VILI)、气压伤、容积伤、肺不张伤和生物创伤、急性呼吸窘迫综合征(ARDS)、肺炎、在重症监护室(ICU)中治疗的镇静对象的呼吸困难、在约48小时通气后撤除(参见例如Larsen and Ziegenfuβ,Beatmung,Springer,Berlin Heidelberg,2013;和Schmidt等人,Intensive Care Med.,第40卷,第1–10页,2014)。
机械通气的一些不期望的后果可通过体外循环肺支持系统解决。这些系统以体外循环血液氧合或体外循环血液二氧化碳去除为目标。目前,体外循环膜式氧合(ECMO)是用来辅助或替代肺的功能的体外循环肺支持最常用的治疗之一。血液从身体被取出并引入到具有分离血液与气相(氧或包含氧的气体混合物)的膜(用于短期治疗的多孔膜或用于长期治疗的无孔膜)的装置中,这将允许血液的氧合。由于ECMO过程中的体外循环血液流量类似于最高约7l/分钟的心输出量,因此可以通过在系统中引入泵来结合ECMO与心脏支持(ECLS,体外循环生命支持)。作为膜式氧合的替代方案,可将氧直接引入到体外循环血液中,例如通过氧(超)饱和液体,如US 6344489 B1(Wayne State University)和US 6607698B1(Therox/Wayne State University)中所述。然而,液体的体外循环引入通常会增大血液的量;因此需要在将富含气体的血液重新引入到人体或动物体中之前将量减小。引入气体饱和或气体超饱和的液体会增加气泡形成的风险。然而,通常,气泡(特别是氧气泡)的存在会引起血液蛋白不期望的变性,因此,为了最大限度地减少气泡形成,这些方法和系统的应用需要极其小心。或者,血液可以直接氧合,即在无气体交换膜的情况下,例如通过气泡氧合器向血液中注入氧。该方法伴随着不期望的泡沫形成以及气体栓塞的风险。该方法不适合治疗酸中毒。
一些现有技术方法依赖于高血液流量以及特别是高速吹扫气流;然而,这可能导致血液侧的气体栓塞。作为补救措施,可以考虑动脉过滤器;然而,这将增加异物反应的风险。
单通过氧合治疗肺功能受损的对象并不能完全代替肺的功能。已经开发了主要用于体外循环二氧化碳去除(ECCO2R)的系统和方法。在例如呼吸性酸中毒的情况下可能需要做这种治疗。如Baker等人,J.Intens.Care Soc.,13:232-236(2012)中所评述,ECCO2R系统通常依赖于气体交换膜的使用,二氧化碳穿过该膜从体外循环血液扩散到气体室中。根据该文章,AV-ECCO2R系统(Novalung,德国)是目前使用最广泛的ECCO2R技术。该系统依靠使体外循环回路中的血液与气体可渗透膜接触,在膜的另一侧具有作为“吹扫气体”的气体(氧气或包含氧气的气体混合物),由此允许二氧化碳气体穿过该膜并由吹扫气流将其从气体室中移除。例如,WO 2010/091867 A1(Novalung)描述了一种在三室系统中处理生物液体的装置。第一室适于容纳生物液体如血液,第二室由气体可渗透但液体不可渗透的膜与第一室隔开,并能够任选地容纳气体如氧气。由于膜的气体渗透性,二氧化碳气体可从第一室扩散到第二室中(由此提供ECCO2R),并且任选地,氧气可从第二室扩散到第一室中,并因此提供体外循环肺支持。小分子如水可从第一室通过液体可渗透膜去除到第三室中。此三室系统较复杂,并且可能与不利地高的流动阻力相关联。此外,Respiratory(ALungTechnologies)正在被商业化推广。这种方法依赖于吹扫气体而不是透析液体。该方法不适于调节血液的酸-碱平衡和/或电解质平衡,并且不适用于传统的透析装置(Cove等人Critical Care 2012,16:232)。
通常,血液氧合和血液二氧化碳去除这两者的效率取决于血液流量,并且以下情况成立:血液流量越高,整个对象(例如,患者)的氧合越好,而血液流量越低,二氧化碳从血液的去除越好(ECCO2R)。通常,高流量(适用于ECMO)是指>2400ml/分钟;中流量(适用于ECMO和ECCO2R)是指800至2400ml/分钟,而低流量(适用于ECCO2R)是指<800ml/分钟。对于现有技术的ECCO2R,血液流量低于ECMO(即约2l/分钟以下)的血液流量是合适的。这样的血液流量在例如常用的pECLA(无泵体外循环肺辅助)中实现。
液体呼吸是现有技术中肺支持的一种替代形式。在此方法中,在TLV(完全液体通气)或PLV(部分液体通气)方法中,生物体(例如,人)呼吸富氧液体(如全氟化碳)而不是呼吸空气,通过该方法,含PFC(全氟化碳)的液体通过用于输送呼吸气体如氧和二氧化碳的机械通气机涌入肺中(Lachmann等人,Intensivmed.und Notfallmed.,第34卷,第513-526页(1997))。尚未建立液体呼吸的标准应用模式。
在现有技术中,将对象的血液抽出到体外循环回路中不仅出于肺支持(氧合和/或CO2去除)的目的实施,而且还出于支持其他器官如肝或肾的目的实施。这样的方法通常涉及使血液与透析液体通过半渗透膜而接触,从而允许不期望的物质沿着浓度梯度从血液转移到透析液体,并任选地在相反的方向上转移期望的物质。这些现有技术系统针对的是其他目的,即肾支持和/或肝支持。例如,在可能由慢性肾衰竭(CRF)导致的酸中毒的情况下,可能需要针对肾支持的透析。WO 03/094998 A1(Hepa Wash)描述了一种用于从血液去除蛋白质结合物质(特别是毒素)的装置和方法,其依赖于适合作为用于肝透析的透析液体的吸收剂液体,其中所述透析液体包含白蛋白,并可任选地包含咖啡因,二者均出于使毒素结合到白蛋白的目的。然而,这些现有技术方法并非针对二氧化碳(CO2)、氢阳离子(H+)和碳酸氢根(HCO3 -)的高效去除,也不针对氧合血液。因此,这样的方法不适于代替肺的功能不全;特别是,它们不适于氧合血液和从血液去除二氧化碳。
待解决的问题
本发明的目的在于提供一种适于体外循环肺支持的新方法,其提供氧合以及二氧化碳去除(ECCO2R)。还希望克服在传统膜气体交换装置(例如,ECCO2R和ECMO)中与血液空气接触相关的缺点。本发明的另一个目的在于提供具有优异定量能力的肺支持:对于肺支持,CO2的去除(或者或另外,H+/碳酸氢根离子对的去除)必须在mmol范围内。因此,一个目的在于以优异的量实现H+离子和碳酸氢根的组合去除,即在该范围内的去除。又一个目的在于提供能够实现这些目的的单个装置。本发明人发现,这些及其他目的可通过权利要求中限定的特征来实现。
作为这些目的以及与现有技术相关的问题的解决方案,本发明提供了一种用于体外肺支持的优异方法。本发明的其他优点与下文的详细描述中描述的本发明的要素相关联。
术语和定义
每当本文使用术语“包含”时,这允许可以存在比实际列出的更多的项目。然而,在一些实施方案中,如本文所使用的,“包含”应更狭义地理解,使得其与术语“基本上由……构成”或“由……构成”是同义的。
酸中毒是指血液和其他身体组织中酸度增加(即氢阳离子浓度的增大)。如果没有进一步指出,则其通常是指血浆酸度增加。酸度增加通常意味着动脉血浆的pH低于7.35,通常为6.8至低于7.35。
碳酸氢根平衡是指碳酸和碳酸氢根/氢阳离子的平衡:
该平衡是动态的,并且解离自发发生(即不依赖于通过酶如碳酸酐酶的催化)。
Bohr效应:一般来说,氧与血红蛋白的结合亲和力受pH(以及因此受氢阳离子的浓度的影响)和二氧化碳分压(pCO2)的影响。因此,血红蛋白的氧合和二氧化碳从血红蛋白中的去除将相互影响。此现象被称为Bohr效应。作为参考,以及关于Bohr效应的其他方面,参见R.F.Schmidt,F.Lang,and M.Heckmann,编著,Physiologie des Menschen.Berlin,Heidelberg:Springer Berlin Heidelberg,2011;和J.B.West,Respiratory Physiology:The Essentials.Lippincott Williams&Wilkins,2012。
缓冲剂在本文中用于指即便添加了酸性或碱性化合物,也适于使溶液的酸度(pH)保持在特定的值附近(例如,接近弱酸或弱碱的pKa值,例如,pH=pKa±1)的弱酸或弱碱。术语缓冲剂可用于固体,同样地可用于溶解的化合物。缓冲剂通常可溶于溶液中,优选含水溶液中。缓冲剂的功能是在向所述溶液中加入酸性或碱性化合物时防止pH发生不期望的变化。也可将适于使溶液的酸度(pH)保持在一定的值附近的弱酸或弱碱的盐称为缓冲剂。
碳酸酐酶是指催化溶解的二氧化碳向碳酸的可逆转化的酶:
碳酸酐酶天然存在于人体或动物体的血红细胞(红细胞)中和其他部位处。
透析液体和透析液在本文中可互换使用。
红细胞或血红细胞或RBC同义地指脊椎动物生物体的血细胞,其以细胞质中存在血红蛋白为特征。RBC在肺中吸收氧并将其释放到外周组织中,同时吸收外周组织中不期望的物质如氢阳离子和二氧化碳并在肺中释放它们。外周组织中的释放/吸收主要发生在红细胞穿过这些组织的毛细血管时。
体外循环是指在人体或动物体外存在或进行的任何过程、活动、物质或装置。如果过程、活动、物质或装置部分地在人体或动物体外存在或进行,则该术语是指身体外的部分。
流体通常是指物质的非固体状态。通常,流体为液体或气体。
Haldane效应:通常,脱氧血红蛋白具有比氧合血红蛋白结合更多H+离子的能力。这方面涉及可称为Haldane效应的现象。Haldane效应的意义在于血红蛋白的氧合(通常在肺中)将促进H+从血红蛋白(Hb)中解离的事实,这将使碳酸氢根平衡向着CO2的形成移动;因此,在血红蛋白氧合部位从红细胞中释放CO2。作为参考,以及关于Haldane效应的其他方面,参见R.F.Schmidt,F.Lang,and M.Heckmann,编著,Physiologie desMenschen.Berlin,Heidelberg:Springer Berlin Heidelberg,2011;和J.B.West,Respiratory Physiology:The Essentials.Lippincott Williams&Wilkins,2012。Haldane效应的其他方面在本发明的详细描述中描述。
亚铁血红素或血红素是指包含Fe2+(亚铁)离子的卟啉部分(杂环有机环),所述亚铁离子包含在其杂环有机环体系(卟啉)的中心。亚铁血红素包含在血红蛋白中。
血红蛋白,或简称Hb,是典型地存在于脊椎动物生物体的血红细胞中的蛋白质。血红蛋白的肽链含有大量的氨基和羧基基团。通常,血红蛋白分子由四个球蛋白亚单位构成。每一个亚单位由与非蛋白亚铁血红素基团相关的蛋白链(球蛋白)构成。血红蛋白能够可逆地结合小分子如代谢物,最显著的是氧(O2)、氢阳离子(H+)和二氧化碳(CO2)或任何这些的溶剂化物。通常,氧可以可逆地与亚铁血红素基团结合。相比之下,二氧化碳通常可以可逆地与氨基基团(通常在血红蛋白中精氨酸和赖氨酸残基的N-端处及侧链处)结合,这将导致氨甲酰基团的形成。具有一个或多于一个氨甲酰基团的血红蛋白被称为氨甲酰血红蛋白。氨甲酰血红蛋白是Haldane效应的主要贡献者。通常,氨甲酰血红蛋白被认为承担哺乳动物中约10%的二氧化碳转运。最后,血红蛋白的羧基基团能够结合并因此缓冲氢阳离子(这种氢阳离子通常由于CO2解离和碳酸氢根平衡而形成)。在正常的生理pH范围内,血红蛋白对氢阳离子的许多结合发生在球蛋白链中存在的氨基酸组氨酸的咪唑基团处。脱氧血红蛋白是比氧合血红蛋白更好的氢阳离子受体。
碳酸氢根(hydrogen carbonate)或碳酸氢根(bicarbonate)可互换使用,其指具有化学式HCO3 -的阴离子。碳酸氢根是碳酸去质子化的中间体形式。它是多原子阴离子。除非上下文另有规定,否则该术语在本文中用于指氢阴离子(HCO3 -)和任何碳酸氢盐,例如碳酸氢钠。
氢阳离子或氢离子或H+在本文中可互换使用以指原子氢的阳离子形式。所有这些术语共同包括氢的所有同位素的阳离子,特别是质子、氘核和氚核。在水性溶液中,氢阳离子通常通过加合一种或多于一种水分子而形成溶剂化物。这样的溶剂化物被称为水合氢离子并可用通式H+(H2O)n描述;n为整数,如0、1、2、3、4或大于4;最通常为1或4。术语氢阳离子也可在本文中用于指溶液中的氢阳离子或氢阳离子的溶剂化态。
如本文所使用的,代谢物是指人或动物代谢的任何中间体或产物。本发明中重要的特定代谢物为二氧化碳、碳酸氢根和氢阳离子。
氧在本文中指分子氧(O2),除非上下文另有规定。氧对于包括哺乳动物在内的所有好氧生物体的细胞呼吸都是必不可少的。
氧合/脱氧血红蛋白是指血红蛋白的氧合状态。由于血红蛋白通常由四个血红蛋白蛋白亚单位构成,其每一个都可以被可逆地氧合/脱氧,故可以有五种氧合状态:完全脱氧形式(所有四个亚单位均脱氧)总是被称为“脱氧的”;完全氧合形式(所有四个亚单位均氧合)总是被称为“氧合的”。术语“氧合的”和“脱氧的”也在本文中用作相对的术语:例如,相对于具有一个氧合的亚单位的血红蛋白形式,具有两个或三个或四个氧合的亚单位的形式都可以称为“氧合的”血红蛋白。相反,具有一个氧合的亚单位的相同形式相对于不具有氧合的亚单位的形式(即,所有亚单位均脱氧)可称为“氧合的”血红蛋白。脱氧的血红蛋白也被称为脱氧血红蛋白。氧合的血红蛋白也被称为氧合血红蛋白。在本文中,术语血红蛋白同时用于氧合血红蛋白和脱氧血红蛋白,除非上下文另有规定。术语氧合血红蛋白/脱氧血红蛋白并不特别需要与氧合血红蛋白/脱氧血红蛋白蛋白质结合特定量的氢阳离子。然而,结合的氢阳离子的量通常与氧合状态相关(参见Haldane效应和Bohr效应)。
pCO2 是指流体例如血浆或透析液体中二氧化碳(CO2)的分压。
pO2 是指流体例如血浆或透析液体中氧(O2)的分压。
外周组织在本文中指脊椎动物的任何非肺组织(非鳃组织),特别是哺乳动物的非肺组织。
血浆在本文中指血液血浆,即血液的细胞外血管内液体部分。
pH或pH值是指氢离子活性以10为底的负对数。pH小于7的溶液是酸性的,pH大于7的溶液是碱性的。
pKa是表示弱酸酸度的指标,其中pKa定义如下。通常,弱酸会根据以下平衡在水性溶液中部分解离:
pKa=-log10Ka。
通常,pKa值越小,酸越强。
碳酸氢钠(sodium bicarbonate)或碳酸氢钠(sodium hydrogen carbonate)可互换地指呈任何形式例如结晶(例如,无水或任何水合物)或溶解于溶液例如,含水溶液中的具有式NaHCO3的(水溶性)化合物(也称发酵粉或苏打或小苏打)。
碳酸钠是指呈任何形式例如结晶(例如无水或任何水合物如七水合物或十水合物)或溶解于溶液例如,含水溶液中的碳酸的(水溶性)二钠盐(Na2CO3,也称洗涤苏打或苏打灰)。
溶剂化物是指被溶剂分子包围或络合的溶质。溶剂化是溶质(例如,离子如氢阳离子(H+)、碳酸氢根(HCO3 -))与溶剂(例如,水)的相互作用。在溶剂化状态下,溶剂化物通常是稳定的(与非溶剂化状态相对)。除非上下文另有规定,否则溶剂化物在本文中优选指在水中溶剂化的溶质。
对象或患者是指个体的人或动物,优选人。对象可以是健康的或患有至少一种医疗病症、疾病或病。患者是患有至少一种医学病症、疾病或病的对象。在本说明书的上下文中,术语患者可指患有本文公开的任何一种或多于一种特定病症的个体。
附图简要说明:
图1:包含碳酸氢根和/或白蛋白的溶液的缓冲能力结果(详情参见实施例1)。
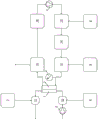
图2:本发明的实施方案的示意性概览。
图2a:具有健全肾功能的患者的肺支持。
图2B:用于治疗患有肾衰竭的患者的肺支持。
图2C:用于治疗患有肾衰竭和肝衰竭的患者的肺支持(即,具有毒素和/或液体去除和/或电解质代偿)。
图2D:需要肺支持和/或肾支持和/或肝支持和/或电解质Na、K、Ca、Cl......代偿的患者的单程透析。
图2A至图2D中使用的数字具有以下含义:
1 血液室(第一室)
2 透析液体室(第二室)
3 pH测量单元
4 用于透析液体的循环泵
5 体外循环血液回路中的血泵
6 氧/富氧液体和/或固体
7 氧/富氧液体和/或固体
8 氧/富氧液体和/或固体
9 H+和/或OH-
10 向体外循环血液回路中加入6
11 向体外循环血液回路中加入7
12 向透析液体中加入8
13 向透析液体中加入9
14 吸收器
15 CO2、HCO3 -、CO3 2-和/或液体和/或透析液体的去除
16 透析液体再处理单元
17 单程入口(泵)
18 单程出口(泵)
不必将所有项目1至18都组合实现。然而,本发明的方法至少需要血液室(第一室)和透析液体室(第二室)。具体实施方案在详细描述中提供。
具体的说明性且非限制性实施方案如下:
在一个单程实施方案中,17和18号如单程平衡系统的现有技术那样以泵、阀、流量计、平衡室或这里提及的这些的组合实现。从透析回路和/或体外循环血液回路中去除额外的液体,例如,可通过18号或18号前和2号后的单独装置实现超滤。
可实现12至15号或其中之一在16号中的集成。12至14号可由一个单元组合或单独实现。6至8号和10至12号可实现仅一个、两个或这些的任意组合。5号可位于10号之前、位于10号和1号之间、1号和11号之间以及11号之后。4号可位于2号、3号和12号至16号之间。12号可位于透析液体流路中13号之前或之后,但优选位于14号之后。14号优选在透析液体流路中的13号之后。
在该附图的各幅图片中示出的实施方案中,二氧化碳和/或碳酸氢根和/或碳酸根和/或氢阳离子通过隔开第一室与第二室的半渗透膜去除。根据以下中的任一情况直接或间接进行氧合:(B)通过向透析液体中引入氧(例如,富氧溶液),产生富氧透析液体;和/或(C)通过在血液经过透析器(用于透析的装置)之前向血液中引入氧(例如,富氧溶液)和/或(D)通过在血液经过透析器(用于透析的装置)之前向血液中引入氧(例如,富氧溶液)。该附图还示出了其中所用透析液体被再循环(回收利用)的实施方案。这种回收利用是任选但优选的实施方案。典型地,透析液体的再循环通过至少一个泵实现,优选地具有10ml/分钟至11000ml/分钟的可调节流量。图3:透析液体和血液中的Ca2+水平随时间的变化(详情参见实施例2)。
图4:氧合结果(详情参见实施例3)。
O2Hb[%]:血红蛋白的氧饱和度(%);
O2Hb前:在血液进入第一室中之前测得的血红蛋白的氧饱和度;
O2Hb后:在血液从第一室离开后测得的血红蛋白的氧饱和度。
具体实施方式
这些目的通过根据本发明的过程和方法来解决。由此克服了现有技术方法或过程的缺点。特别地,本发明人发现,通过在体外循环肺支持的方法中使用液体透析流体(透析液体),可以实现优于依赖于气相进行肺支持的体外循环肺支持的常规方法或过程的优点。该方法允许高效地氧合血液、从血液中去除二氧化碳和/或调节血液pH至期望值或正常值和/或调节(增大或减少)血液中的碳酸氢根浓度。因此,该方法能实现高效且多用途的肺支持,并可基于个体对象的需要支持其他器官。
本发明人发现,在本发明的液体/液体透析方法中,可以利用Haldane效应和/或Bohr效应。然而,本发明不限于特定选择的效应,也不限于解释任何这些效应的特定理论。更通常而言,本发明尤其基于如下发现:当血液与如本文所定义的透析液体接触并且血液如本文所述直接或间接氧合时,可以有利地利用某些物质与血红蛋白的结合。
在根据本发明的血液氧合的方法中,可在体外系统地利用各自的效应来从血液中去除代谢物。这允许比常规方法更高效的体外循环肺支持。
Haldane效应先前曾被描述为是脊椎动物身体中发生的一种现象。在本文中以及在现有技术中,Haldane效应通常是指血红蛋白配体特别是氧、二氧化碳和氢阳离子(H+)对血红蛋白的结合亲和力不是静态的、即不是在所有条件下都相同的现象,因此,一般而言,当配体从血红蛋白中释放或与血红蛋白结合时,可能导致对另一配体的结合亲和力的增加或降低。在健康的脊椎动物(人或动物)身体中,在外周组织中、特别是在外周组织的毛细血管中(从血红蛋白中释放氧的地方)和肺中(氧与血红蛋白结合的地方)观察到Haldane效应。为了进一步说明本发明,本文通过如下对健康人体或动物体的(1)外周组织中和(2)肺中发生的现象的说明性描述来大体解释Haldane效应:
(1)一般而言,在脊椎动物(人或动物)身体中,由于代谢活动而将在外周组织中产生二氧化碳。在外周组织的毛细血管中,组织中产生的二氧化碳将沿着其降低的分压梯度向血液中、主要是向红细胞中扩散。如上所述,二氧化碳以碳酸和碳酸氢根/氢阳离子对的动态平衡存在。氢阳离子又可与血液中、特别是红细胞中的蛋白质结合。主要的细胞内氢阳离子受体或用于结合氢阳离子的缓冲剂是蛋白质血红蛋白。氢阳离子主要与血红蛋白的组氨酸侧链结合。当从血红蛋白的亚铁血红素中释放氧时,即当氧合血红蛋白变为脱氧的时,血红蛋白对氢阳离子的亲和力将增大。因此,在这个阶段,血红蛋白变为更强的碱或更弱的酸,使更多的位点可用于缓冲氢阳离子。换句话说,脱氧血红蛋白比氧合血红蛋白对质子具有更高的亲和力。因此,氢阳离子在氧释放后与血红蛋白(脱氧血红蛋白)结合。根据LeChatelier的原理,氢阳离子与血红蛋白的结合以及因此游离的氢阳离子从血液中的分离会导致反应
向右移动。此外,脱氧血红蛋白有利于氢阳离子的结合,并因此有利于碳酸氢根的形成。碳酸氢根的形成将增大血液携带二氧化碳的能力。
(2)一般而言,在健康的人或动物的肺中,当氧与血红蛋白的亚铁血红素结合(即脱氧血红蛋白变为氧合的)时,Haldane效应将造成上述反应的逆转:不久,血红蛋白的氧合将促进氢阳离子从血红蛋白中解离,这将使碳酸氢根缓冲液平衡向着形成CO2的方向移动;使得从红细胞中释放CO2。在呼吸道上皮中,二氧化碳将沿着其分压梯度从呼吸面向环境中扩散。该扩散和由此导致的细胞内二氧化碳张力的减小将造成碳酸氢根和二氧化碳的反应的失衡,因此,碳酸氢根脱水成二氧化碳(通常由红细胞中的酶碳酸酐酶辅助)。该反应所需的氢阳离子从血红蛋白中释放。因此,在结合氧后从血红蛋白中释放氢阳离子。解离的氢阳离子与碳酸氢根(HCO3 -)反应形成碳酸(H2CO3),所述碳酸进一步反应——通常由红细胞中存在的酶碳酸酐酶辅助——形成水和CO2,氧与血红蛋白的结合有利于碳酸氢根缓冲液平衡向着形成CO2的方向移动。在健康的脊椎动物(人或动物)体的肺中,由于血红蛋白的氧合,通常然后会从血红细胞中释放CO2。
氧与血红蛋白的结合亲和力受pH影响(并因此受氢阳离子浓度影响)和受二氧化碳分压(pCO2)影响的事实也被称为Bohr效应。
因此,一般而言,脱氧血红蛋白可比氧合血红蛋白结合更多的氢阳离子(对氢阳离子具有更高的亲和力):普遍认为,这种现象的分子原因在于脱氧血红蛋白的氢受体部分如组氨酸侧链的咪唑比脱氧血红蛋白的相同或相当的氢受体部分更能结合氢阳离子(对结合氢阳离子具有更高的亲和力)。不希望受特定理论的限制,认为球蛋白肽链的电子结构将在氧的结合或释放过程中改变,从而引起氢阳离子亲和力的改变。允许血红蛋白脱氧的此现象将促进氢阳离子与血红蛋白的缔合,这将使碳酸氢根缓冲液平衡向形成碳酸氢根(HCO3 -)的方向移动;使得血液的CO2转运能力增大,反之亦然,这称为“Haldane效应”。由于Haldane效应,脱氧的血红蛋白(脱氧血红蛋白)比氧合的血红蛋白(氧合血红蛋白)具有更高的中和(缓冲)H+离子的能力。在健康的脊椎动物(人或动物)体中,Haldane效应是通过最大限度地减少游离H+或血液pH的变化来促进CO2的转运的重要机制。
在本发明中,可利用Haldane效应,使得氧合和二氧化碳去除以积极的方式相互影响。然而,本发明在人体或动物体外使用Haldane效应的有益效果。用于体外循环肺支持的本发明方法包括两个功能:二氧化碳去除和血液氧合,这对于完整的肺支持来说是必需的。然而,在本发明的方法中二氧化碳去除单元和血液氧合单元是空间上隔开的。
本发明允许从血液中去除至少一种不期望的物质,其中不期望的物质选自二氧化碳(CO2)、氢阳离子(H+)、碳酸氢根(HCO3 -)。为了从血液中去除至少一种不期望的物质,本发明的方法不需要气体交换膜(即,在至少一侧上为血液而在另一侧上为气相的膜)。相反,不期望的物质的去除通过半渗透膜的两侧都为液体的半渗透膜进行,即一侧上为血液而在相应的另一侧上为透析液体。本发明能够分别调节和控制氧合和至少一种不期望的物质的去除。此外,本发明能够调节二氧化碳比去除速率、血液的氧合或(过)氧合速率及调节血液pH至期望的水平。
本发明还允许稳定血液pH或调节血液pH至期望值或正常值。通常,血液pH的期望值或正常值在pH 7.35至7.45的范围内,优选地7.36至7.44,更优选地7.37至7.43,更优选地7.38至7.42,更优选地7.39至7.41,最优选地约7.40。更一般地,可接受pH为6.8至8.0的血液pH范围。
从广义上讲,本发明因此提供了(i)氧合血液的方法,其包括将血液暴露于由半渗透膜隔开的透析液体的步骤,其中所述透析液体具有本文限定的性质或优选性质;和(b)氧合血液的方法,其包括步骤:(i)向装置的第一室中引入血液,所述包括第一室和第二室,其中第一室和第二室被半渗透膜隔开,(ii)向所述装置的第二室中引入透析液体,其中透析液体被引入到第二室中。在本说明书中,术语第一室通常用来指配置为或适于容纳血液的室,术语第二室通常用来指配置为或适于容纳透析液体的室;通常,第一室和第二室被如本文定义的半渗透膜彼此隔开。通常,第一室和第二室不存在直接连接(管道等)。因此,只有那些能够穿过半渗透膜的物质才能从第一室迁移到第二室中和/或从第二室迁移到第一室中。
血液和透析液体是水性流体。术语水性在本文中通常用来指水或含水流体,特别是但不限于其液体状态。术语水性在本文中用来指包含水的流体,特别是包含水的液体或液相。通常,水性液体包含超过50%(体积/体积)的水,并且是亲水的。血液和透析液体是这样的水性液体。
特别地,本文提供了允许血液的体外循环氧合的体外循环肺支持方法,其特征在于以下步骤:
(i)向血液中和/或向透析液体中引入氧,
其中透析液体的特征在于pH为6.8至11;并且其中透析液体包含白蛋白,优选地10g/l至60g/l的白蛋白;
从而产生富氧血液和/或富氧透析液体;和
(ii)暴露所述血液于被半渗透膜隔开的透析液体。
理想的是,步骤(i)先于步骤(ii)进行。或者,可以同时进行步骤(i)和(ii)。在任一情况下,血液或透析液体或二者都在步骤(i)中变为富氧的。对于透析液体的富氧,接触步骤过程中通过半渗透膜将发生氧从透析液体到血液的净转移。接触步骤还允许将不期望的物质从血液直接去除到透析液体中。
无论如何,在步骤(ii)中,血液的流动和透析液体的流动优选不以逆流模式实现;即,血液和透析液体不以彼此相反的方向流动。换句话说,优选透析液体和血液以相同的方向流动通过本发明的装置(顺流)。当血液被冷却至37℃以下的温度时,顺流模式是特别优选的。
在血液同时与透析液体和氧接触的情况下,例如,如果除了用于容纳血液的第一室和用于容纳透析液体的第二室之外,本发明的装置还包括用于容纳氧(例如,氧气、包含氧的气态混合物或富氧液体)的第三室,则第三室和第一室经由气体渗透膜彼此接触,然后氧优选以相对于第一室逆流的模式通过第三室。
本发明采用透析液体是本发明与现有技术的基于气体的体外循环二氧化碳去除方法(ECCO2R)之间的根本区别。
本发明人发现,本发明的方法特别适合于氧合血液、体外循环二氧化碳去除和调节碳酸氢根水平的目的。这些目标可在个性化医疗中实现,即取决于个体患者的需要。由于本发明允许增加或减少人体或动物体外血红蛋白的氧亲和力,故可以通过在本发明的限制内改变条件来根据个体患者的需要调节氧吸收,这将在下文中描述。在本说明书和所附权利要求中提供了本发明具体的、优选的和有利的实施方案。还可以(a)通过在本发明的框架内使用适宜的透析液体和(b)通过氧合血液来调节血浆中的血浆碳酸根浓度、血浆碳酸氢根浓度和碳酸根与碳酸氢根的比率,从而导致不期望的物质从血液中的去除。例如,血浆中的碳酸根与碳酸氢根的比率取决于pH并可通过选择具有适宜pH的透析液体来影响。
血液
在脊椎动物(人或动物)体内,血液由血细胞和血液血浆(也称为“血浆”)构成,使得血细胞悬浮在血浆中。在脊椎动物体内,血浆的主要组分为水,血细胞的主要类型是红细胞。本发明的方法适于向人或动物的所有血液类型应用,优选脊椎动物,优选哺乳动物,最优选人类。
本文中在第一室、或透析单元或透析器的情况下或在任何其他体外循环的情况下提及到血液的任何时候,其不一定指取自人体或动物体的纯血。在一些实施方案中,术语血液可指取自人体或动物体的血液与可接受的量的可接受的添加剂的混合物。如果血液的功能不会受到显著不利的影响,则添加剂是可接受的。如果添加剂的加入不会导致取自人体或动物体的血量的显著增多以致血量增多不超过50%、优选不超过40%、不超过30%、不超过20%、不超过10%、不超过5%,则添加剂的量是可接受的。
在一些实施方案中,本发明的方法专门涉及体外活性。在替代的实施方案中,该方法被利用来满足活体对象的医疗需要,这将在下文中详细描述;在这些替代的实施方案中,血液经由半渗透膜与透析液体的接触也在体外(即,在人或动物的身体外)或体外循环中进行。另外,如下文所述,发生与人体或动物体的相互作用。
血液和/或透析液体的富氧
本发明的方法包括向血液中和/或向根据本发明的透析液体中引入氧的步骤。
如果向透析液体中引入氧,通常是在将血液暴露于被半渗透膜隔开的透析液体的步骤之前或同时的步骤中,向透析液体中引入氧。由此,发生至少一部分所述氧从透析液体到血液的净转移。
经受氧富集的血液通常是氧含量低的血液。这样的血液被称为脱氧血液。脱氧血液通常来源于人或动物对象的静脉。
向(所述脱氧)血液中和/或透析液体中引入氧的步骤之后或同时,进行在使血液经由半渗透膜与透析液体接触的步骤,允许包括氧在内的小分子通过半渗透膜转移。氧合步骤的任一阶段(向脱氧血液中引入氧或是向透析液体中引入氧)都可产生氧合的血液,即,具有增大的氧浓度的血液。换句话说,向脱氧血液中引入氧提供了血液的“直接”氧化步骤;向透析液体中引入氧提供了血液的“间接”氧化步骤。无论如何,通常沿例如透析液体或血液的流路提供至少一个用于引入氧的位点。
对于如本文所述通过向透析液体中引入氧(而不是直接向血液中引入)、然后暴露富氧透析液体于被半渗透膜隔开的血液的间接血液氧合,血液的氧过饱和通常是不可能的,因为氧的扩散由浓度梯度驱动。这在很多情况下是期望的。在对流转运富氧透析液体的情况下,血液的氧过饱和是可能的。
通常,氧可以许多不同的方式被引入到血液和/或透析液体中。其优选实例在下文更详细地描述。
然而,优选向血液中引入的氧(即,在“直接”氧合中)不为气态氧。优选地,“气态”氧理解为氧以气相形式呈现,而不以含有气态氧的液体或固体形式呈现(例如,处于溶解态/相中)。具体而言,优选在本文描述的方法的步骤(i)中向血液中引入氧并且引入血液中的氧不为气态氧。更优选地,“气态”氧还理解为包括含有气态氧的气泡的液体。
还优选向透析液体中引入氧。例如,气态氧可被引入到透析液体中以溶解。通过这些措施,避免了血液与气体的直接接触。血液与气体的直接接触可能导致气泡,其可能在血液中引起紊乱,如泡沫形成,并且其甚至可能导致气体栓塞。此外,血液与气体的直接接触还可能导致凝血和/或炎症反应。因此,优选避免血液与气体的直接接触。然而,在根据本发明的方法中,可使血液与包含气态氧的液体接触。换句话说,可使气态氧溶解在液体中,所述液体特别是富氧液体。
因此,优选引入到血液中和/或透析流体中的氧借助于液态氧(如下文所说明,参见下面的选项(2))或富氧液体(如下文所说明,参见例如下面的选项(1)和(6))和/或固体(如下文所说明,参见例如下面的选项(5))引入。特别地,“富氧”液体可理解为包括其中溶解了分子氧的(均匀)液体和/或含有气泡(气态氧“溶解于”其中)的液体。更优选地,“富氧”液体指其中溶解了分子氧的均匀液相,即没有气泡(气态氧“溶解于”其中)。关于氧的引入,在任一情况下,引入可通过以下任一种情况实现:
(1)分别向血液和/或透析液体中引入(优选输注)包含溶解氧的液体。该液体可以是氧饱和的或氧过饱和的。
(2)分别向血液和/或透析液体中引入(优选输注)液态氧;优选向透析液体中引入。
(3)分别通过氧可渗透膜向血液和/或透析液体中引入氧。
(4)分别向血液和/或透析液体中引入(优选输注)气态氧。引入可例如借助于气泡氧合器来实施。
(5)引入含氧固体。这样的固体含有被固定的氧,当固体被引入到液体中时,可以释放被固定的氧。合适的含氧固体包括例如干凝胶和液凝胶或冷冻的富含气体的液体。可向血液和/或透析液体中引入这样的含氧固体。
(6)富氧液体的对流转运。
在本文中,输注通常是指流体(液体或气体,视情况而定)向另一流体中即向透析液体中或向血液中的引入。
下面将描述实施方案(1)至(6)的一些方面。
对于选项(1),使用的液体可以是水、反渗透水、NaCl水溶液如缓冲盐水、葡萄糖溶液、透析液体、全氟化碳和油。氧可溶解在液体中或超过在相应液体中的最大溶解度而存在(这将使得液体为氧超饱和液体),或者氧可以以与液体中溶解的氧结合物质结合的方式存在。对于该实施方案,PFC(全氟化碳)是特别合适的。因此,可引入具有与PFC结合的氧的含PFC液体。
当通过特别是向血液中引入任何这种液体而进行氧合时,将实现血红蛋白和氧的良好接触,并可避免气体栓塞的风险。一般来说,氧在液体中的溶解度取决于压力、温度和盐度(Weiss(1970),Deep Sea Res.Oceanogr.Abstr.,第17卷,第4期,第721–735页)。通过改变这些参数,可制备并提供所期望氧合程度的富氧液体。所述液体后续可用于氧合血液和/或透析液体。可以使用具有增加的氧分压的氧超饱和或氧过饱和液体。这样的液体在高压下、通常显著高于标准大气压下制备。为此,为了避免在较低的压力例如大气压力下此类氧超饱和液体释放的过程中形成气泡,可使氧超饱和液体通过一个或多于一个毛细管。合适的毛细管具有0.012μm至1000μm的内径(ID)和0.1mm至1100mm的长度。通常,在毛细管的一端有高压力,而在毛细管的另一端有较低的压力。由于任何毛细管都具有取决于其内径、长度、压力差和液体的特定氧超饱和液体流量,故可通过使用若干平行的毛细管来增大总流量。可优选通过改变富氧液体的压力来调节流量和由此获得的氧合。这影响了各液体中溶解氧的浓度。优选通过增大气体压力、升高或降低温度、降低所用气体的离子浓度和离子化来增大液体中的氧溶解度。此外,对于选项(1),特别是如果直接向血液中引入富氧液体,则体外循环血液的量通常会增大。通常不期望增大正被治疗的人或动物的血液总量。因此,在这样的情况下期望后续的血量减少。因此,在这样的情况下通常在将血液重新引入到对象中之前的任何阶段减少血量。血量的减少可例如通过过滤实现。由此,可以不使人或动物对象富含液体,即不使人或动物对象超水合或水过多。这在长期治疗中尤为重要。
对于选项(2),优选直接向透析液体中引入液态氧。可以设想,这样的引入有助于透析液体的冷却。这对于这样的实施方案可能是优选的。可使氧通过一个或多于一个细管或毛细管。
对于选项(3),即,经由氧可渗透膜引入氧,氧通常呈气态形式。因此,通常不设想血液氧过饱和的情形,因为氧气扩散由浓度梯度驱动。
对于选项(4),还可以通过直接向血液中引入氧来氧合血液。氧或以纯氧引入,或以包含氧的气体混合物例如空气引入。这样的血液氧合模式通常通过气泡氧合器实现。还可以通过引入和/或产生氧细小气泡(微米/纳米气泡)来使相应的液体富含氧和/或氧(超)饱和。这样的细小气泡可优选由多孔材料产生。由于氧会与血红蛋白结合,故H+离子将从血红蛋白中释放并与碳酸氢根反应形成二氧化碳。这样的二氧化碳可通过使血液经由半渗透膜与透析液体接触的步骤来去除。在这样的情况下,直接氧合优选先于所述接触步骤进行。或者或另外,可以预期气泡捕集器从氧合血液中去除不期望的二氧化碳气泡。然而,这可能较不优选,因为气泡在其去除之前可能在血液中引起紊乱,如泡沫形成;当引入到人或动物对象中时,残留的气泡甚至可能导致气体栓塞。
选项(3)和(6)可组合地实现。因此,可通过使富氧液体通过对流转运穿过膜而使血液或透析液体富氧。富氧液体可以是透析液,并且穿过膜的步骤与使血液通过半渗透膜与透析液体接触的步骤同时进行。
在经由膜进行血液氧合的任何时候——包括选项(3),进行本发明的方法的步骤(ii)中的借助于预先氧合的透析液体通过半渗透膜向血液中引入氧或使血液氧合,经由相应的膜与血液接触的富氧流体(例如,透析液体)的氧浓度或氧分压优选是已知的。透析液体的氧浓度优选可调节至0mol/kg至0.42mol/kg的浓度。为此,优选可以增大氧分压。氧的浓度可根据氧分压和流体性质例如流体的温度和盐度/离子浓度来确定。无论如何,在本发明的方法中与血液接触的透析液体和/或血液以外的任何富氧液体(例如,血浆)的氧浓度优选至少与血浆的期望氧浓度一样高。由此将避免氧从血液到相应的其他液体的净再扩散。
对于所有实施方案(即(1)至(6)中的任何一个),优选在使透析液体与血液经由半渗透膜接触的步骤之前、即在透析液体穿过用于透析的装置之前实现氧的引入。或者或另外,与使透析液体与血液经由半渗透膜接触的步骤平行地实现氧的引入。在该情况下,最优选根据上述(3)通过氧可渗透膜引入氧。对于这样的实施方案,可优选在用于透析的装置中提供单独的(第三)室。该第三室被至少一个半渗透膜与第二室(透析液体室)和/或第一室(血液室)隔开。为了平行接触,除了用于容纳血液的第一室和用于容纳透析液体的第二室外,本发明的装置优选还包括用于容纳氧(例如,氧气、包含氧的气态混合物、富氧液体或溶解在液体中的氧)的第三室。由此,第三室和第一室经由气体渗透膜彼此接触。
通常,当血液的氧饱和度是已知的时,可以使血液氧合至期望的饱和水平。应优选避免血液的气态氧过饱和。
优选地,一旦从人或动物对象的静脉取出血液,测量血液的总氧含量[ml/dl]和/或血红蛋白结合氧的量和/或血液的氧饱和度。
血液血红蛋白浓度通常以克每分升[g/dl]给出。在用于加氧的装置之前或在进入用于透析的装置之前,通过测量体外循环血液回路中血液的血液血红蛋白浓度[g/dl]、氧合血红蛋白饱和水平[%]和氧分压[mmHg],可根据下式计算血液的总氧含量[ml/dl]:
cO2=(Hb·1.34)·(O2Hb/100)+(pO2·0.003)
优选地,在血液被重新引入到人或动物对象中之前,测量血液的总氧含量[ml/dl]。这样的过程允许复核本发明的方法的性能并确保对象被提供了氧合血液。
还可以在使透析液体经由半渗透膜与血液接触之前和/或之后测量透析液体的总氧含量[ml/dl]。
为了便于进行实现血液的目标氧水平[ml/dl]的调整,应调节氧向体外循环血液中的引入,即优选调节至体外循环血液流量。如果向透析液体中引入氧,则应调节透析液体流量和引入的氧的量,即优选调节至体外循环血液流量。
作为上述任何情况的替代或补充,还可以通过如上(1)至(6)中所述的任何措施在使血液与透析液体经由半渗透膜接触的步骤之后的步骤中向血液中引入氧。然而,在此阶段引入的氧将不会与透析液体接触:因此,它不会导致利用体外循环环境中的Haldane效应。因此,强烈优选在使血液与透析液体经由半渗透膜接触的步骤之前的步骤中引入氧。因此,通常根本不预期在使血液与透析液体经由半渗透膜接触的步骤之后(即晚于该步骤)的步骤中向血液中引入氧,或仅预期为附加措施,即除在使血液与透析液体经由半渗透膜接触的步骤之前的步骤中引入之外预期的引入。在该附加的实施方案中,氧在至少两个位点处被引入,即在血液/透析液体接触步骤之前的一个位点和在血液/透析液体接触步骤之后的一个位点。
如下文详细描述的,在使血液经由半渗透膜与透析液体接触的步骤中通常从血液中去除至少一种不期望的物质。由于Haldane效应,透析液体或血液或二者中加入的氧的存在有助于使不期望的物质从血液中高效地转移至透析液体。
图2中示出在本发明的实施方案中可能的血液或透析液体的氧合位置。简言之,可在经由半渗透膜接触血液之前制备富氧透析液体(在图2中位置10号处引入氧,还参见实施例3)或者可在经由半渗透膜接触透析液体之前制备富氧血液(在图2中位置12号处引入氧)。如上所述,在所述接触步骤之后引入氧是可能的,但优选不作为唯一的氧合位点。
优选地,在使血液经由半渗透膜与透析液体接触的步骤过程中不存在气泡(例如,不存在氧气泡)。这种偏好的分子上的原因在于,在不存在任何气泡的情况下,膜可渗透物质通过膜的交换通常更高效。对于向透析液体中引入氧,优选的是,在所述引入氧的步骤后但在使血液与透析液体经由半渗透膜接触的步骤之前使透析液体经过至少一个气泡捕集器或沿至少一个气泡捕集器通行。在此情况下,气泡捕集器适当地位于体外循环血液流路中在向透析液体中引入氧的地方后面(之后)但用于透析的装置前面(之前)的位置处。另一方面,对于向血液中引入氧,气泡捕集器可能并不必要,因为通常氧在血液中足够良好或足够快地溶解。
或者或另外,优选在将血液重新引入到患者中之前,使血液经过至少一个气泡捕集器或沿至少一个气泡捕集器通行。在这样的情况下,气泡捕集器适当地位于体外循环血液流路中用于透析的装置之后的位点处,并且还位于引入氧的位点后面(之后)。
优选地,在步骤(i)中向透析液体中引入氧(即,优选“间接”氧合)。更优选地,在步骤(i)中不向血液中引入氧。
相应地,在又一个方面,本发明提供了一种氧合透析液体的方法,其包括以下步骤(i)
(i)向透析液体中引入氧,
其中透析液体的pH为6.8至11并且其中透析液体包含白蛋白,优选10g/l至60g/l的白蛋白;
从而产生富氧透析液体。
上面描述了向透析液体中引入氧的各种优选选择。例如,优选通过液态氧(如上文所说明,参见上面的选项(2))或富氧液体(如上文所说明,参见例如上面的选项(1)和(6))和/或固体(如上文所说明,参见例如上面的选项(5))向透析流体中引入氧。
优选地,根据本发明的这种氧合透析液体的方法还包括在步骤(i)之后的步骤(ii),其中在步骤(ii)中,氧合的透析液体流经第二室,从而进入、经过并离开第二室,该第二室由半渗透膜与第一室隔开。半渗透膜、第一室和第二室及其优选实施方案将在下文更详细地描述(特别是在涉及“半渗透膜”和“包含半渗透膜的装置”的段落中)。优选地,第一室、半渗透膜和第二室包括在一个装置中,该装置为透析单元或透析器。同样,透析单元或透析器及其优选实施方案将在下文更详细地描述(特别是在涉及“包含半渗透膜的装置”的段落中)。优选地,步骤(i)在装置外的位点处并在透析液体进入所述装置中之前进行,使得透析液体以富氧形式进入装置中。特别地,这意味着透析液体在如上所述装置(例如,透析器)外氧合。优选地,进入如上所述装置(例如,透析器)的透析流体是氧合的。
如上所述,以及在根据本发明的使透析液体氧合的方法的情况下,优选在步骤(i)中通过以下任一种或多于一种情况向所述透析液体中引入氧:
(1)输注富氧(优选地,氧饱和或氧过饱和)液体(参见上文描述的选项(1));
(2)输注液态氧(参见上文描述的选项(2));
(3)通过氧可渗透膜引入氧(参见上文描述的选项(3));
(4)输注气态氧(参见上文描述的选项(4));
(5)引入含氧固体,例如,干凝胶和液凝胶或冷冻的富氧液体(参见上文描述的选项(5));和
(6)富氧液体的对流转运(参见上文描述的选项(6))。
优选地,除白蛋白外,所述透析液体还包含一种或多于一种缓冲剂,其特征在于至少一个pKa值为7.0至11.0,这将在下文更详细地描述,并且其中所述一种或多于一种缓冲剂优选选自:三(羟甲基)氨基甲烷(Tris,THAM)和碳酸根/碳酸氢根,如下文更详细描述的。
优选地,透析液体对于H+离子具有12mmol/l或更高的缓冲能力,如下文更详细描述的。
还优选透析液体的特征为pH为8.0至9.0,如下文更详细描述的。
优选地,透析液体包含2,3-二磷酸甘油酯(2,3-DPG),如下文更详细描述的。还优选透析液体包含10mmol/l至40mmol/l的碳酸根/碳酸氢根(碳酸根和碳酸氢根浓度的总量),如下文更详细描述的。优选地,透析液体包含5mmol/l至20mmol/l的Tris,如下文更详细描述的。
优选地,在根据本发明的氧合透析液体的方法中,离开第二室的透析液体经受至少一个处理步骤(iii)。如果方法包括如上所述的步骤(ii),则处理步骤(iii)优选在步骤(ii)之后进行。这样的“处理步骤”在下文更详细地描述。例如,这样的“处理步骤”可包括以下子步骤中的一个或多于一个,优选全部:
(a')将透析液体流分离为第一流和第二流;
(b')向透析液体的第一流中添加酸性流体;
(c')通过对透析液体的酸化的第一流过滤、透析、沉淀或渗滤来去除毒素;
(d')向透析液体的第二流中添加碱性流体;
(e')通过对透析液体的碱化的第二流过滤、透析、沉淀或渗滤来去除毒素;和
(f')汇合透析液体的第一流和第二流。
说明该处理步骤的示例性实施方案包括在图2A至图2D中。
优选地,在步骤(iii)之后,使透析液体再次进入(再循环到)第二室。
还优选至少一个处理步骤(iii)选自(1)暴露于吸附剂;(2)与(优选半渗透的)膜接触,优选去除二氧化碳;和/或(3)暴露于酸性pH和/或碱性pH,如下文更详细描述的。
优选地,所述处理步骤(iii)包括酸化透析液体至酸性pH以形成二氧化碳和任选地去除二氧化碳。
此外,还优选根据本发明的氧合透析液体的方法另外包括测量透析液体的至少一个参数的步骤,参数选自pH、二氧化碳分压、氧分压、碳酸氢根(HCO3 -)浓度、缓冲能力、脱氧血红蛋白浓度或饱和度(HHb)和氧合血红蛋白饱和度(O2Hb)中的一个或多于一个,如下文更详细描述的。更优选地,根据本发明的氧合透析液体的方法另外包括测量透析液体的至少一个参数的步骤,参数选自pH、二氧化碳分压、氧分压、碳酸氢根(HCO3 -)浓度、缓冲能力和脱氧血红蛋白中的一个或多于一个,如下文更详细描述的。
优选地,透析液体所包含的白蛋白选自人血清白蛋白和/或牛血清白蛋白,如下文更详细描述的。
还优选透析液体包含超过1.7mmol/l的钙(Ca2+)离子、优选地2mmol/l至4mmol/l的钙(Ca2+)离子、更优选地2.4mmol/l至2.6mmol/l的钙离子,如下文更详细描述的。
优选地,在将透析液体重新引入到第二室中之前调节透析液体的pH和/或缓冲能力,如下文更详细描述的。
优选地,根据本发明的氧合透析液体的方法还包括以下步骤:
(a)将透析液体流分离为第一流和第二流;
(b)向透析液体的第一流中添加酸性流体;
(c)通过对透析液体的酸化的第一流过滤、透析、沉淀或渗滤来去除毒素;
(d)向透析液体的第二流中添加碱性流体;
(e)通过对透析液体的碱化的第二流过滤、透析、沉淀或渗滤来去除毒素;
(f)汇合透析液体的第一流和第二流。
这些其他步骤在下文更详细地描述,特别是在涉及“再循环”和“酸/碱处理”的段落中。相应地,其优选实施方案在下文描述,特别是在涉及“再循环”和“酸/碱处理”的段落中。另外,所述步骤(a)至(f)及其优选实施方案还在WO 2009/071103 A1中描述。
优选地,步骤(a)至(f)先于步骤(i)进行。换句话说,透析液体优选在用酸性和碱性流体处理之后氧合。
还优选步骤(a)至(f)在步骤(ii)之后、即透析液体经过透析器之后进行。在优选的实施例中,透析流体被再循环/再生并因此可多次通过透析器(所谓的多程透析)。在这种情况下,优选在进行以再循环/再生透析流体的步骤(a)至(f)之后进行步骤(i),即透析液体在再循环/再生之后氧合。其后,再循环和氧合的透析流体通过透析器(步骤(ii))。
如上所述,步骤(a)至(f)优选作为处理步骤(iii)的子步骤进行,然而,它们尤其也可独立于处理步骤(iii)进行。
此外,还优选根据本发明的方法还包括定期切换多个开关阀,使得经酸化的透析液体流被交替地供给到第一解毒单元和第二解毒单元,而经碱化的透析液体流被交替地供给到第二解毒单元和第一解毒单元。WO 2009/071103 A1中提供了其详细描述和优选实施方案。
还优选方法还包括以下中的一个或多于一个步骤:
-调节酸化透析液的温度;
-因酸化而沉淀去除毒素;
-调节碱化透析液的温度;和
-因碱化而沉淀去除毒素,
例如如下文和/或WO 2009/071103 A1中所述。
透析液体
本发明的透析液体为水性液体,即包含水的液体。适于本发明的透析液体的特征在于pH为6.8至11.0并且存在白蛋白。白蛋白的合适浓度为10g/l至60g/l(即,1g/100ml至6g/100ml)。在本说明书中,g/l和g/100ml是指每体积(含白蛋白的液体的最终体积)的克数。
这些条件在本文中也被称为“框架条件”。在框架内,可以适当选择更具体的条件,如下文所述。
如上文所限定的,透析液体的特征在于pH为6.8至11;并包含白蛋白,优选10g/l至60g/l的白蛋白。通常,白蛋白具有缓冲水性液体的能力,并且认为白蛋白的某些氨基酸残基(例如,组氨酸的咪唑基团、半胱氨酸的硫醇基团)是重要的(Caironi等人,BloodTransfus.,2009;7(4):259–267),并且在更高的pH值下,赖氨酸侧链的氨基基团和N-端的氨基基团可有助于缓冲。然而,白蛋白的缓冲能力已在血液中被常规地利用(其在人体或动物体内天然存在),并且含有白蛋白的液体对于体外循环肺支持的适用性在本领域尚未被认识或利用。
在本发明中,白蛋白优选为人或动物的血清白蛋白,例如人血清白蛋白、动物白蛋白(例如,牛血清白蛋白),或者基因工程白蛋白,或者这些中任何一种或多于一种的混合物。含有白蛋白和至少一种其他载体物质的混合物也是可能的。在任何情况下,本文中指定的白蛋白浓度是指白蛋白的总浓度,不管采用的是单一类型的白蛋白(例如,人血清白蛋白)还是多种类型的白蛋白的混合物。本发明中使用的透析液体包含10g/l至60g/l的白蛋白,优选10g/l至40g/l的白蛋白,优选15g/l至30g/l的白蛋白,优选20至25g/l的白蛋白,最优选30g/l或约30g/l的白蛋白。白蛋白的浓度也可用%值表示;即,2g/100ml的白蛋白对应于2%的白蛋白(重量/体积)。白蛋白是根据本发明的透析液体中的第二缓冲剂。透析液体中的白蛋白有助于其缓冲能力,并以氨甲酰基团的形式结合碳酸根。其中白蛋白可适当地缓冲液体如血液的pH范围是本领域众所周知的,例如,从生物化学教科书。透析液体中白蛋白的存在促进蛋白质结合物质从血液中去除。考虑到其吸附或结合化合物如氢阳离子、二氧化碳和毒素的性质,白蛋白也可更一般地称为吸附剂或吸附剂分子。
除了白蛋白对于结合上述类型的不期望的物质的适用性及因此其在用于体外循环肺支持和血液pH调节的方法中的适用性之外,透析液体中白蛋白的存在,如在本发明中,将进一步允许或增强蛋白质结合毒素的去除。为此目的,可以利用透析液体中存在的白蛋白的能力:一般来说,已知白蛋白与未结合的毒素结合,故当透析液体中存在白蛋白时可以利用这种性质,从而使得能够结合从血液中穿过半渗透膜进入到透析液体中的毒素。此方法被称为“白蛋白透析”(参见例如WO 2009/071103 A1,其全部内容以引用方式并入本文)。
通常优选透析液体在与血液接触的步骤中处于富氧状态。透析液体的富氧可通过本文描述的任何手段实现。
透析液体通常包含水。通常,透析液体中超过50%(体积/体积)、超过60%(体积/体积)、超过70%(体积/体积)、超过80%(体积/体积)或超过90%(体积/体积)为水。透析液体中也可包含其他可与水混溶的液体。
本发明不仅提供了用于去除不期望的物质的方法,而且提供了适用于所述目的的透析液体本身。本文描述的任何和所有特定的透析液体都是本发明的主题。
透析液体中包含的缓冲剂
本发明人发现,透析液体(与常规CO2去除系统中的吹扫气体相对)的使用适于保持透析液体的pH为可接受的pH水平。
优选地,白蛋白不是透析液体中存在的唯一缓冲剂。合适地,透析液体包含至少一种额外的缓冲剂,其中缓冲剂的特征在于至少一个pKa值为7.0至11.0。一般的缓冲透析液体和特别是本发明的特定透析液体的使用允许在不损害血液的pH范围内进行二氧化碳去除,而该透析液体对于离子的实际能力远高于不含缓冲剂的情况。所述至少一种缓冲剂提供或有助于透析液体的缓冲能力。
待包含在透析液体中的合适缓冲剂包括特别是以下中的任何一种或多于一种:三(羟甲基)氨基甲烷(Tris,THAM)和碳酸根/碳酸氢根。
-碳酸氢根的特征在于酸度(pKa)为10.3(共轭碱碳酸根)。因此,在含有碳酸氢根的水性溶液中,取决于溶液的pH也可能存在碳酸根。为方便起见,本文使用表述“碳酸根/碳酸氢根”来指碳酸氢根及其相应的碱碳酸根。“碳酸根/碳酸氢根浓度”或“(组合的)碳酸根/碳酸氢根浓度”等在本文中是指碳酸根和碳酸氢根的总浓度。例如,“20mM碳酸根/碳酸氢根”是指碳酸氢根及其相应的碱碳酸根的总浓度为20mM的组合物。碳酸氢根对碳酸根的比率通常由组合物的pH决定。
-碳酸根/碳酸氢根是合适的额外缓冲剂。已知碳酸根/碳酸氢根对提供生理pH缓冲体系。现有技术中先前已经描述不含白蛋白的含碳酸氢根的透析液体。
碳酸氢根和氢阳离子以及其他小分子,包括可影响水性液体的pH的离子或物质,可在本发明的方法过程中穿过半渗透膜。因此,确切地说,如本说明书中所限定的,透析液体中(组合的)碳酸根/碳酸氢根浓度优选针对处于即将接触血液的阶段的透析液体限定,例如,处于透析液体如本文所述进入透析单元的第二室的阶段。碳酸根/碳酸氢根的合适总浓度(两种物质一起的组合浓度)为0mmol/l至40mmol/l。透析液体中碳酸根/碳酸氢根的存在有助于透析液体的缓冲能力。然而,碳酸根/碳酸氢根的浓度越低,CO2从血液中的去除将越好。因此,可能期望使用不含碳酸根/碳酸氢根的透析液体,或者不添加碳酸根/碳酸氢根。碳酸氢根可适当地缓冲液体如血液的pH范围是本领域众所周知的,例如,从生物化学教科书。在制备本发明的透析液体时,碳酸氢根可以以其任何盐的形式添加,如碳酸氢钠、碳酸氢钾等,或者可通过任选地在碳酸酐酶的存在下引入二氧化碳而间接添加,并根据需要通过加入合适的碱如氢氧化钠或氢氧化钾来调节pH,强烈优选氢氧化钠。在以盐的形式添加的情况下,强烈优选碳酸氢钠或碳酸钠。或者,可使用钾盐或钠盐与钾盐的混合物。特别用于在高pH(例如,最高pH为11)下加入透析液体中的盐为碳酸钠或碳酸钾。通常,参考本发明的方法中进入第二室的阶段,透析液体中优选的(组合的)碳酸根/碳酸氢根浓度为超过0mmol/l(例如1mmol/l)至40mmol/l,优选10mmol/l至35mmol/l,更优选15mmol/l至30mmol/l,最优选20mmol/l至30mmol/l或约20mmol/l至30mmol/l。注意这些只是一般的优选范围和子范围是重要的。对于特定的目的,如为了处理来自特定患者亚组的血液,可能优选替代的、不同的或部分偏离的范围,如下文所述。替代的合适的(组合的)碳酸根/碳酸氢根浓度为0mmol/l至40mmol/l、或超过0mmol/l至40mmol/l,优选5mmol/l至35mmol/l,优选10mmol/l至30mmol/l,更优选15mmol/l至25mmol/l,最优选25mmol/l或约25mmol/l。当透析液体被再循环时,在透析液体进入第二室中之前确定(组合的)碳酸根/碳酸氢根浓度,并进行调节,如果需要的话。一般来说,鉴于可能的副作用,不期望(组合的)碳酸根/碳酸氢根浓度高于40mmol/l。
-三(羟甲基)氨基甲烷,常被称为“Tris”。三(羟甲基)氨基甲烷还被称为“THAM”。Tris是具有式(HOCH2)3CNH2的有机化合物。Tris的酸度(pKa)为8.07。Tris是无毒的并且先前已用于体内治疗酸中毒(例如,Kallet等人,Am.J.of Resp.and Crit.Care Med.161:1149–1153;Hoste等人,J.Nephrol.18:303–7)。在包含Tris的水性溶液中,取决于溶液的pH,也可存在相应的碱。为方便起见,除非上下文另有指出,否则表述“Tris”在本文中用来指三(羟甲基)氨基甲烷及其相应的碱二者。例如,“20mM Tris”是指Tris及其相应的碱的总浓度为20mM的组合物。三(羟甲基)氨基甲烷与其相应的碱的比率将由组合物的pH决定。Tris和其共轭碱以及其他小分子,包括可影响水性液体的pH的离子或物质,可在本发明的方法过程中穿过半渗透膜。因此,确切地说,如本说明书中所限定的,透析液体的Tris浓度优选针对处于即将接触血液的阶段的透析液体限定,例如,处于透析液体如本文所述进入透析单元的第二室的阶段。合适的Tris浓度为0mmol/l至40mmol/l、或超过0mmol/l至30mmol/l,优选5mmol/l至25mmol/l,优选10mmol/l至20mmol/l,更优选15mmol/l。替代的合适的Tris浓度为0mmol/l至38mmol/l或0mmol/l至20mmol/l。
-如果水溶性蛋白质具有至少一个咪唑(组氨酸侧)链和/或至少一个氨基基团(赖氨酸)侧链或至少一个巯基(半胱氨酸)侧链,则除白蛋白外,水溶性蛋白质也适合于本发明的目的。这些侧链通常具有7.0至11.0的pKa值。如果pH在本发明的透析液体的范围内、例如pH为8.0的每升水性溶液中可溶解至少10克蛋白质,则该蛋白质落在水溶性的定义内。在本发明的情况下强烈优选的水溶性蛋白质为白蛋白,如下文限定的。优选地,除白蛋白外,还存在碳酸根/碳酸氢根或Tris。根据本发明的优选透析液体包含(i)碳酸根/碳酸氢根和(ii)白蛋白两者;或(i)Tris和(ii)白蛋白两者。特别地,当没有向透析液体中加入碳酸根/碳酸氢根(即,透析液体中碳酸根/碳酸氢根浓度为0mmol/l或接近0mmol/l)时,优选的是Tris和白蛋白都存在于透析液体中。或者,Tris是透析液体中包含的唯一缓冲剂。
Tris、碳酸根/碳酸氢根和白蛋白的所有上述范围和浓度在本发明中是可组合的。根据本发明的优选透析液体包含(i)碳酸根/碳酸氢根和(ii)白蛋白两者;或(i)Tris和(ii)白蛋白两者。一种替代的优选透析液体包含Tris作为唯一缓冲剂,即不含添加的碳酸根/碳酸氢根或白蛋白。
与先前使用含碳酸根的透析液体相比,本发明是有利的,尤其是因为可以利用白蛋白的缓冲能力。
可用于本发明的第一特定透析液体包含0mmol/l至40mmol/l的碳酸根/碳酸氢根(优选10mmol/l至40mmol/l的碳酸根/碳酸氢根)、10g/l至60g/l的白蛋白(即,1g/100ml至6g/100ml的白蛋白)并具有7.75至11.0、优选8.0至10.0、更优选8.0至9.0的pH。优选的碳酸根/碳酸氢根浓度为如上文所指定的。
可用于本发明的第二特定透析液体包含0mmol/l至40mmol/l的Tris(优选1mmol/l至20mmol/l的Tris)、10g/l至60g/l的白蛋白(即,1g/100ml至6g/100ml的白蛋白)并具有7.75至11.0、优选8.0至10.0、更优选8.0至9.0的pH。优选的Tris浓度为如上文所指定的。
任选地,存在其他无机或有机缓冲剂。优选地,这样的缓冲剂具有至少一个为7.0至9.0的pKa值。更优选地,可采用两种或三种这样的缓冲剂,每一种具有为7.0至9.0的pKa值。合适的额外有机缓冲剂包括蛋白质,特别是水溶性蛋白质,或氨基酸,或Tris;合适的额外无机缓冲分子包括HPO4 2-/H2PO4 -。
对H+离子的缓冲能力
合适地,本发明中使用的透析液体对H+离子具有高的缓冲能力,例如,对H+离子为12mmol/l H+离子或更高的缓冲能力。对H+离子为12mmol/l H+离子或更高的缓冲能力通常是超过血浆(pH 7.45;参见实施例1)的缓冲的缓冲能力。因此,在本发明中,透析液体的缓冲能力通常超过血浆(pH 7.45)的缓冲。换句话说,透析液体的缓冲能力通常为12mmol/l H+离子或更高的缓冲能力。
在本发明的情况下,术语“对H+离子的缓冲能力”或简称“缓冲能力”是表示给定液体缓冲添加H+离子的能力的抽象值。术语“对H+离子的缓冲能力”是相应液体(水性溶液)的固有性质。血浆也是这样的液体。血浆缓冲能力的确定需要离心步骤;离心导致包括血小板在内的血细胞的沉降,上清液被称为血浆。实施例1中描述了这种离心。用于血液离心并因此用于制备血浆的合适条件是本领域已知的。
准确地说,术语“对H+离子的缓冲能力”是指缓冲一定量的H+离子而不达到低于6.5的pH的能力。“不达到低于6.5的pH”是指适当混合的液体的pH不达到低于6.5的pH值。因此,在缓冲能力的实际评估中充分混合是重要的。因此,如本文所使用的,在本发明的透析液体的情况下,术语“对H+离子的缓冲能力”可仅用于pH为6.5或更高的液体。如本文所定义的,pH为6.5的溶液对H+离子的缓冲能力为零毫摩尔每升(0mmol/l)。本发明的透析液体通常具有高于6.5的pH,即如本文所限定的;因此,它们对H+离子确实具有缓冲能力。优选地,缓冲能力为12mmol/l H+离子或更高。甚至更优选高于此的缓冲能力,即对H+离子的缓冲能力为12mmol/l或更高、14mmol/l或更高、16mmol/l或更高、18mmol/l或更高、20mmol/l或更高、22mmol/l或更高、24mmol/l或更高、26mmol/l或更高、28mmol/l或更高、30mmol/l或更高、32mmol/l或更高、34mmol/l或更高、36mmol/l或更高、38mmol/l或更高、40mmol/l或更高、42mmol/l或更高、44mmol/l或更高、46mmol/l或更高、48mmol/l或更高、50mmol/l或更高。因此,根据本发明的透析液体通常对H+离子的缓冲能力为12mmol/l或更高、如超过12mmol/l。优选的缓冲能力为12mmol/l至50mmol/l、超过12mmol/l至40mmol/l、13mmol/l至30mmol/l、14mmol/l至25mmol/l、15mmol/l至24mmol/l、16mmol/l至23mmol/l、17mmol/l至22mmol/l、18mmol/l至21mmol/l、19mmol/l至20mmol/l。
缓冲能力不仅仅取决于相应液体的pH,而且还受液体组成(所述液体中缓冲化合物的存在和浓度)的影响。
对H+离子的缓冲能力以数值表示,单位为“mmol/l”。根据本发明,对H+离子的缓冲能力(以mmol/l表示的缓冲能力)通过以下四步测定法确定:
1.作为导言,该测定法适于确定pH在本发明的透析液体的pH范围内、即pH为6.8至11.0或在其子范围内的给定液体(透析液体或候选透析液体)对H+离子的缓冲能力。因此,在第一步中,测试给定的液体的pH是否在该范围内。如果情况并非如此,则给定的液体不是根据本发明的透析液体(不需要进一步的测试)。然而,如果是在该范围内的情况,则通过以下步骤2和3确定给定液体的缓冲能力:
2.用HCl滴定该液体。特别地,加入0.1M HCl,搅动溶液以确保混合,连续监测pH,并且确切地在所滴定的液体的pH达到pH 6.5的最终值时终止滴定。换句话说,当pH达到6.5的值时停止滴定。基于pH达到6.5之前添加的HCl的量计算缓冲能力(H+离子,单位mmol/l)。这是可能的,因为根据常识,HCl是一种强酸,它可以完全溶解在水性溶液中。因此,0.1MHCl(0.1mol/l)含有0.1mol/l溶解的Cl-离子和0.1mol/l溶解的H+离子。基于给定液体滴定达到pH为6.5所需的HCl的体积,可以计算由所述体积的透析液体缓冲的H+离子的量。如果测定法中所用给定液体的量为1升,则将直接获得由1升透析液体(以mmol/l表示缓冲能力)缓冲的H+离子的量。如果测定法中所用给定液体的量为超过1升或少于1升的限定量,则可由1升透析液体(以mmol/l表示缓冲能力)缓冲的H+离子的量可通过简单数学计算获得。
3.将步骤2中确定的缓冲能力(mmol/l)与参考值相比较。合适的参考值为10mmol/l、11mmol/l、12mmol/l、13mmol/l、14mmol/l;强烈优选12mmol/l。或者,参考值由人或动物(猪、小鼠)血液的缓冲能力表示;在此情况下,如上面步骤2中所述确定血浆的缓冲能力。
4.如果给定溶液的缓冲能力(mmol/l)超过参考值(mmol/l),则确定该给定溶液具有根据本发明的缓冲能力。
在确定缓冲能力的测试法中,所有pH测量以及滴定均在室温(所有溶液和装置的温度;环境温度)下进行。基于本文的指导和普通常识,上述测试法是简单明了的,技术人员付出极小的努力即可实现。由此,给定液体的缓冲能力可容易且可靠地确定而没有不适当的负担。
下文在实施例1中给出了确定如本发明所定义的缓冲能力的一个实例。如该实施例所示,具有pH为7.45的血浆通常具有12mmol/l的缓冲能力。
然而,可以想到,来自其他来源(其他物种和/或其他个体)的血浆具有不同的缓冲能力。其他可以想到的血浆缓冲能力为3mmol/l至30mmol/l、优选4mmol/l至25mmol/l、优选5mmol/l至20mmol/l、优选6mmol/l至19mmol/l、优选7mmol/l至18mmol/l、优选8mmol/l至17mmol/l、优选9mmol/l至16mmol/l、优选10mmol/l至15mmol/l、优选11mmol/l至14mmol/l、优选12mmol/l至13mmol/l。
优选根据本发明的透析液体通常具有超过血浆的缓冲能力的缓冲能力。当在本发明的过程或方法中处理个体例如患者的血液时,对H+离子的缓冲能力优选选择为使得其超过该个体例如该患者的血液的缓冲能力。
透析液体的pH
透析液体的优选pH范围包括pH为8.0至10.5、8.0至10.0、8.0至9.5、优选pH为8.0至9.0。在这样的pH值下,可以去除H+(质子)而不会使透析液体所包含的白蛋白不稳定。
因此,透析液体中存在的至少一种缓冲剂的至少一个pKa值为pH为7.0至11.0、8.0至10.5、8.0至10.0、8.0至9.5、优选地8.0至9.0。如果存在多于一种缓冲剂,则优选其各自具有为上述范围或子范围的pKa值。如果至少一种缓冲剂具有多于一个pKa值,则至少一个所述pKa值、优选多于一个所述pKa值为上述范围或子范围。理论上,任何具有至少一个pKa值为7.0至11.0的缓冲剂都适于在期望的pH范围内进行缓冲。然而,在本发明的情况下,缓冲剂必须选择为使得其是无毒的或者不会对经受透析的人或动物引起不期望的副作用。特别合适的缓冲剂为碳酸根/碳酸氢根体系、Tris和水溶性蛋白质(优选白蛋白),其全部如上文所定义。透析液体的另一合适的pH值为7.75至9.0。通常,优选的pH值为7.75至9.0,优选8.0至9.0,优选8.1至8.9,优选8.2至8.8,优选8.3至8.7,更优选8.4至8.6,最优选8.5或约8.5。注意这些只是一般的优选范围和子范围是重要的。对于特定的目的,如为了处理来自特定患者亚组的血液,可能优选替代的、不同的或部分偏离的范围,如下文描述的。可通过在本文预期的范围内的缓冲物质如碳酸氢根和血红蛋白的量或浓度来调节pH,和/或通过加入酸或碱如盐酸或氢氧化钠来调节pH。
碳酸氢根和氢阳离子以及其他小分子,包括可影响水性液体的pH的离子或物质,可在本发明的方法过程中穿过半渗透膜。因此,在使血液与透析液体接触的整个过程步骤中,透析液体的pH不一定保持恒定。因此,确切地说,如本说明书中所限定的,透析液体的pH优选针对处于即将接触血液的阶段的透析液体限定,例如,处于透析液体如本文所述进入透析单元的第二室的阶段。
无需使透析液体始终保持在开始暴露于血液(进入第二室中)时期望的pH下。特别是当透析液体被再循环时,如下文所述,pH和(组合的)碳酸根/碳酸氢根浓度可随时间变化。然而,在进入第二室中的阶段,将透析液体调节为符合指定的pH和碳酸氢根/白蛋白浓度。例如,可在透析液体进入第二室之前通过至少一个pH测量装置测量pH。任选地,pH可另外通过至少一个pH测量装置来测量。
透析液体的其他组分
一般而言,除上述方面外,适于本发明的生理学目的的透析液体优选包含适当浓度的期望电解质、营养物和缓冲剂,从而可调节其在患者血液中的水平,例如,到正常的生理值,或到任何其他期望或指示的值。根据本发明的透析液体的任选组分包括电解质,优选地选自糖和/或盐(阴离子/阳离子/两性离子)。典型的阳离子包括钙、镁、钾和钠离子;典型的阴离子包括氯、HCO3 -、H2CO3、HPO4 2-、H2PO4 -;典型的两性离子包括氨基酸(例如,组氨酸)和肽或有机酸的盐。
优选地,透析液体不含添加的乙酸,也不含添加的乙酸盐。优选地,透析液体中乙酸的组合浓度低于4mmol/l、低于3mmol/l、低于2mmol/l、低于1mmol/l、最优选为0mmol/l。
如果需要,透析液体还可包含其他用于转移到血液的膜可渗透的小分子,例如,葡萄糖。
还通常优选透析液体具有低的或可忽略的溶解二氧化碳和氮的含量。
优选地,透析液体包含钙(Ca2+)离子。与仅含游离钙离子的现有技术透析液体相比,本发明的透析液体的典型特征在于钙离子至少部分地与白蛋白结合。一般来说,在较高的pH值下,更多的钙与白蛋白结合,并且与血液交换的可用量更少。因此,根据本发明的含有白蛋白的透析液体中的总钙含有比从根据现有技术的透析液体已知的更高的钙浓度。特别地,含有白蛋白的透析液体的钙离子浓度为1.7mmol/l或更高。为了可获得足够的游离钙即不降低血液中的游离钙离子浓度,这是所期望的(参见实施例2)。
优选地,透析液体包含2mmol/l至4mmol/l的钙(Ca2+)离子,更优选地2.4mmol/l至2.6mmol/l的钙离子。钙离子可以任何合适的盐的形式添加,例如,氯化钙。向透析液体中添加钙是有利的,因为血液也包含钙;透析液体中钙的存在将防止钙离子从血液向透析液体中不期望的净通量(泄漏)。已知钙离子可在非常碱性的pH下沉淀。鉴于经由半渗透膜与血液接触时透析液体的最大pH值为9.0,故钙的存在不会与本发明不相容。任何时候当透析液体的pH高于10时,一些离子如钙离子(以及其他离子)通常就会变得不可溶。因此,如果透析液体的pH大于9,则优选不存在钙离子(和其他不溶性离子)。如果透析液体的pH在该范围内,为了不使患者缺少这种离子,则应将其直接输注到患者的血液中。
优选地,透析液体的特征在于与正被透析的血液的摩尔渗透压浓度基本上相同的摩尔渗透压浓度。
除上述外,可向透析液体中添加碳酸酐酶这种酶,或者透析液体中可存在碳酸酐酶。碳酸酐酶是促进二氧化碳向碳酸氢根(HCO3 -)和H+离子的可逆反应的酶。碳酸酐酶可被加到体外循环血液回路中。还可以用碳酸酐酶包覆第一室或第二室的内表面。
任选地,透析液体包含2,3-二磷酸甘油酯(2,3-DPG或也称为2,3-二磷酸甘油酸、2,3-BPG)。已知2,3-DPG会通过降低它们对氧的亲和力而与脱氧的血红蛋白β亚单位相互作用,因此其将别构地促进与血红蛋白结合的剩余氧分子的释放,从而增强RBC在最需要氧的组织附近释放氧的能力。2,3-DPG因此是别构效应物。红细胞中2,3-DPG的浓度通常为约4mmol/l至5mmol/l。在本发明的透析液体中,取决于目的,2,3-DPG的浓度可为0mmol/l至4mmol/l、4mmol/l至5mmol/l或大于5mmol/l。可向透析液体中添加2,3-DPG的一个原因是为了避免血液中2,3-DPG的净损失,即防止2,3-DPG从血液扩散到透析液体中。酸中毒患者的治疗通常需要添加2,3-DPG。
血液中包含的不期望的物质;不期望的物质的去除
本发明的方法允许从血液去除至少一种不期望的物质。从广义上讲,至少一种待去除的不期望的物质是由代谢活动产生的物质。优选地,至少一种不期望的物质选自二氧化碳(CO2)、氢阳离子(H+)、碳酸氢根(HCO3 -)、碳酸(H2CO3)和它们中任何一种的溶剂化物以及这些的任何组合。已知在水性环境(例如,水性溶液或水性悬浮液,如血液或透析液体)中,这些不期望的物质彼此相互关联,如由以下平衡方程式所表示:
该反应的反应物(离析物和产物)以动态平衡存在——如由上面方程式中的箭头定性所示。碳酸的解离通常由存在于红细胞中的酶碳酸酐酶催化或辅助。根据动态平衡的一般原理,按Le Chatelier原理,一种反应物的去除将引起反应的移动。现有技术的ECCO2R系统依赖于气体交换膜的使用,一种反应物二氧化碳将通过气体交换膜从体外循环血液扩散到气体室中。相比之下,本发明能够将至少一种不期望的物质从一种液体(血液)直接去除到另一液体(透析液体)中。因此,本发明不限于气态的不期望的物质(如CO2)的去除,并且不需要将不期望的物质转移到气相。因此预期在本发明的方法中二氧化碳不转移到气相。
通常,CO2在血液中转运的形式之一是氨甲酰基团形式,其中二氧化碳连接到血液中蛋白质的端氨基基团上,主要是连接到血红蛋白的端氨基基团上(然后称为氨甲酰血红蛋白)。通常,应理解,氨甲酰基团的形成是快速且可逆的并且不需要任何酶的催化。因此,当由于二氧化碳扩散进入透析液体中,其浓度在其周围降低时,呈氨甲酰形式的二氧化碳也迅速从血液蛋白质如血红蛋白的氨基基团释放,从而根据Le Chatelier原理,将建立一个新的平衡。如上所述,氨甲酰血红蛋白和溶解的二氧化碳也以与碳酸氢根(HCO3 -)/H+离子对平衡,但经由H2CO3的迅速转化需要碳酸酐酶这种酶。碳酸酐酶天然存在于红细胞中。
因此,在本发明中,血液中存在的所有三种主要形式的碳酸根:(i)呈氨甲酰血红蛋白形式的蛋白质(血红蛋白)结合CO2,(ii)游离的CO2和(iii)碳酸氢根(HCO3 -)/H+可直接或间接地通过半渗透膜去除。虽然游离的CO2和碳酸氢根离子可沿浓度梯度穿过半渗透膜进入透析液体中,但当例如游离的CO2的浓度因向透析液体中的扩散而降低时,血红蛋白结合CO2将优先从血红蛋白中释放,以使根据Le Chatelier原理,将建立血液中存在的三种主要形式的碳酸根(转运形式)的新平衡。重要的是,在本发明中二氧化碳的不同转运形式不必转移到待去除的气相中。因此,不需要血液-气体接触,并优选不预期。本发明能够在液体介质中从血液完全去除二氧化碳的所有主要转运形式。取决于透析液体和血液的碳酸氢根(HCO3 -)浓度,碳酸氢根可沿半渗透膜一侧的透析液体和另一侧的血液的浓度梯度从血液中去除。
在本发明的情况下,这些不期望的物质可通过沿浓度梯度转移到透析液体而直接去除(直接去除)。或者或另外,不期望的物质可通过与从透析液体转移到血液的物质反应而间接去除,这也导致不期望的物质从血液的净去除(间接去除):例如,氢阳离子可通过从透析液体向血液转移OH-离子而间接去除,其实现是因为本发明中使用的透析液体的pH通常比待处理的血液的pH更碱性。还可通过从透析液体向血液转移物质及其对碳酸氢根平衡的影响来间接去除其他不期望的物质,如碳酸、碳酸根、碳酸氢根。
与去除气相中的二氧化碳的现有技术系统相比,本发明能够去除可溶于液体中的物质。这些物质包括任何类型的离子,只要它们可溶于水即可,特别是氢阳离子和碳酸氢根阴离子。本发明因此能够比现有技术的ECCO2R方法更完全并因此更高效地从血液中去除代谢物。根据本发明的二氧化碳去除机制允许溶解的气体从一个液相扩散到另一个液相。
如下文详细描述的,在本发明的方法中可适当地使用包括两个室的透析单元或装置。第一室适于容纳血液。第一室适当地具有入口(用于使血液进入)和出口(用于使血液离开)。
当本发明的方法中使用透析单元时,期望在血液离开第一室(出口)时其pH为7.35至7.45,优选7.36至7.44,更优选7.37至7.43,更优选7.38至7.42,更优选7.39至7.41,最优选约7.40。
优选地,血液在离开第一室(出口)后返回到人体或动物体内。合适的管道和连接件是本领域已知的并可在本发明的情况下采用。
任选地,预期从血液中去除气泡(如果有的话),即在从第一室(出口)离开之后并且在血液被重新引入到人体或动物体内之前的阶段。为此目的,可在第一室后面设置一个或至少一个气泡捕集器。如果在方法的至少一部分的过程中,血液还暴露于气体或气体饱和的或气体过饱和的液体,则这是特别合适的。
从血液中去除二氧化碳的方面
二氧化碳去除不仅可以替代肺支持,而且可以保持血液基本无气泡。理论上,向血液中引入溶解氧但不去除二氧化碳会增大形成二氧化碳气泡的可能性和/或血液中溶解的二氧化碳浓度的增加和/或血液pH的降低。在本发明的方法中,预期将二氧化碳的去除与氧合一起进行;从而避免此类不期望的副作用。
pCO2的增大将降低血红蛋白的氧亲和力,因此可以在本发明的透析回路中实现的二氧化碳从血液中去除将提高血红蛋白的氧亲和力。但pCO2变化的影响并不大,因为40mmHg的pCO2变化仅使P50改变约10mmHg pO2。H+离子变化具有大得多的影响,该变化反映在pH的变化上。血液中pH升高将导致血红蛋白与氧的总结合能力的增大。本发明通过向透析液体中或向血液中引入OH-离子来实现血液pH的升高。
从血液中去除氢阳离子的方面
由于透析液体的pH和缓冲能力,故可在接触步骤过程中从血液中去除H+。由于游离的H+离子从血液中的去除,故更多的H+将从血红蛋白中解离并也将被去除。此外,由于在血液与透析液体经由半渗透膜接触的步骤中利用的Haldane效应,故血红蛋白结合H+离子的去除将导致血红蛋白结合氧的亲和力的增大。
为此,在接触步骤之前或与接触步骤同时的步骤中向血液中和/或透析液体中引入富氧液体是有利的。氧的存在改善了血红蛋白结合H+离子的释放,这促进了其从血液中的去除。氧合血红蛋白(O2Hb)与H+结合脱氧血红蛋白(HHb)的比率不仅与氧或H+离子的浓度有关,而且还取决于pH。因此,血液中引入的pH变化可影响H+离子与血红蛋白的结合。血液的pH又可在血液与透析液体接触的步骤中受影响;在本发明的框架内,这适宜通过调节透析液体的pH和缓冲能力来实现。
使透析液体与调节血液至一定pH的目标相适应
除了在体外循环肺支持中的功能,包括从血液中去除CO2和/或碳酸氢根离子以及血液的氧合,本发明的方法还能够调节血液的pH至期望的水平。这适合于例如酸性血液的处理,酸性血液例如来自酸中毒患者的血液。期望将血液pH调节至6.8至8.5的预定值或预定范围。鉴于不期望的副作用,如血液蛋白质的变性和/或血液组分的沉淀,故不期望血液pH值在该范围之外。通常,调节血液pH值或范围意味着在从第一室离开的阶段血液以所述调节值或调节范围为特征。
考虑到健康的人对象的生理血液pH通常为7.35至7.45,即约7.40,故在一些实施方案中期望调节血液pH至涵盖该范围的范围或值,即7至8.5、7.0至7.8、7.2至7.6或7.3至7.5。在优选的实施方案中,当意图使血液pH接近健康的人对象的生理血液值时,期望调节血液pH至7.35至7.45的值或范围,优选7.36至7.44,更优选7.37至7.43,更优选7.38至7.42,更优选7.39至7.41,最优选约7.40。
如下文详细描述的,本发明还特别适于治疗患有酸中毒的对象(酸中毒患者),即患有代谢性和/或呼吸性酸中毒的对象。在针对或适于处理来自酸中毒患者的血液的本发明实施方案中,可能期望调节血液pH至比7.40更碱性、超过7.40至8.0、7.5至7.9或7.6至7.8的范围或值,优选pH为7.65至7.75,例如7.7。
由于所用透析液体的缓冲能力并由于H+和OH-离子的半渗透膜渗透性,故本发明的方法中血液pH的调节是技术上可行的。因此,通过使用缓冲的透析液体,可实现血液的pH调节。H+和OH-离子可穿过半渗透膜,并将沿着相应的浓度梯度进行。
不希望受任何特定理论的束缚,应理解,主要鉴于本发明的透析液体优异的缓冲能力,H+离子将从血液中消除。除此之外,认为少量的H+离子通过与透析液体在半渗透膜的任一侧或全部两侧提供的OH-离子反应去除。不仅从血液消除二氧化碳而且还从血液中消除H+离子(通过与OH-离子的反应)能够调节血液的酸-碱平衡。本发明中使用的透析液体可基于需要加以调节,例如,基于正经受透析治疗的患者的需要。本发明因此能够优先去除二氧化碳,或优先调节血液pH,或二者。这种多功能性由调节透析液体的pH和调节透析液体中缓冲物质(特别是白蛋白和碳酸氢根)的浓度的可能性提供,这两种调节彼此独立地在本文限定的一般范围内进行。
使透析液体与氧合血液至一定的值的目标相适应
由于血红蛋白的氧亲和力取决于温度、pCO2、pH和2,3-二磷酸甘油酯(2,3-DPG或也称为2,3-双磷酸甘油酸、2,3-BPG)的浓度,故可根据本发明改变这些参数中的任何一个或多于一个来实现期望的氧合程度。可独立地调节这四个参数中的每一个。这还能够促进氧吸收或递送,其对于重症监护室(ICU)中的患者可能是必需的。例如,在标准血液条件(pH7.4,37℃,2,3-DPG 13μmol/g Hb,pCO2 40mmHg)下,P50(意指50%的血红蛋白饱和度)在pO2为27mmHg下实现。
血液通过第一室时的温度不受特别限制,只要血液成分不变性并且血液保持液态即可。合适的温度在1.2℃至45℃的范围内,例如37℃。优选地,血液温度降低。这可优选通过冷却用于透析的装置中的透析液体和/或通过体外循环血液回路中的另一外部冷却单元和/或内部冷却单元和/或通过向体外循环血液回路中引入温度为1.2℃至低于37℃的溶液来实现。已知20℃(20开尔文)的血液温度变化可将P50改变30mmHg pO2。
在较高的温度(例如,37℃)下,血红蛋白的氧亲和力较低。通常,20℃的血液温度变化可使P50改变30mmHg pO2。为了实现血红蛋白氧亲和力的增加,在根据本发明的引入氧的体外循环步骤中,可或直接或间接地降低血液温度。在优选的实施方案中,实施本发明的方法使得该方法的至少一部分在低于37℃、优选4℃至20℃的温度下进行。温度的间接降低可通过例如降低透析液体的温度、或通过体外循环血液回路中的外部冷却单元和/或内部冷却单元和/或通过向血液或透析液体中引入温度为1.2℃至低于37℃的溶液来实现。合适地,在经由半渗透膜与透析液体接触的步骤中血液的温度为1.2℃至37℃,如5℃至35℃、10℃至30℃、15℃至25℃或约17℃或约20℃。优选地,冷却如下进行:
(a)步骤(i)的特征在于向血液中输注低于37℃的富氧液体或液氧;和
(b)步骤(ii)的特征在于与血液接触的透析液体的温度低于30℃,例如低于28℃,优选低于26℃、低于24℃、低于22℃或低于20℃。
在本发明中,可以以与正被治疗的对象的血液中的浓度相等或比其更高的浓度包含2,3-DPG。由此,可调节血红蛋白的氧亲和力。或者,根据本发明的透析液体包含比其低、即低于血液的2,3-DPG浓度。由此,可从血液中去除2,3-DPG,这导致氧解离曲线的左移并使P50降低至pO2为18mmHg。
鉴于本发明中采用的透析液体的一般通用性,即调节血液pH的适用性以及肺支持的适用性及它们的组合,可选择透析液体以专门或主要解决特定的目标。例如,可针对调节血液pH的目标或针对提供肺支持的目标选择透析液体。在这种情况下,术语透析液体的设计和适应可互换使用,并且是指即将经由半渗透膜暴露于血液、即在进入第二室的阶段的透析液体。
例如,当正被治疗的对象不仅患有低血氧症而且患有呼吸性酸中毒时,则通常期望调节血液pH,这可在本发明中通过直接或间接地去除二氧化碳来实现。凭借Haldane效应,这进一步提高了血红蛋白的氧结合。可在如本文所述的透析液体的一般框架内使本发明中使用的透析液体适应这样的目的。
取决于透析液体和血液的碳酸氢根(HCO3 -)浓度,碳酸氢根可沿半渗透膜一侧的透析液体和另一侧的血液的浓度梯度从血液中去除。换句话说,只要透析液体中(组合的)碳酸根/碳酸氢根浓度低于血液中(组合的)碳酸根/碳酸氢根浓度,则碳酸氢根将沿浓度梯度从血液去除到透析液体中。如果不期望或未指示从血液去除碳酸氢根,则选择透析液体的(组合的)碳酸根/碳酸氢根浓度使得其不低于血液的(组合的)碳酸根/碳酸氢根浓度。在这种情况下,“不低于”是指等于或高于,如略高于,但通常是指约等于或等于。
一般来说,用于患有呼吸性酸中毒的对象的血液处理而调节的透析液体包含优选0mmol/l至40mmol/l、或者5mmol/l至40mmol/l或10mmol/l至40mmol/l的浓度的碳酸氢根。用于这样的目的的(组合的)碳酸根/碳酸氢根浓度的优选实施方案包括15mmol/l至35mmol/l、20mmol/l至30mmol/l或(约)25mmol/l。
半渗透膜
在本发明中,至少一种不期望的物质从血液向透析液体的转移通过半渗透膜发生。在本发明的方法的接触步骤中将血液与透析液体隔开的膜适合可渗透氧、二氧化碳和液体。该膜形成分离表面或接触表面,化合物可以通过其转移。该膜可渗透液体,特别是水和水性溶液。理想的是,该膜可渗透氧、二氧化碳、碳酸氢根、H+离子和液体。在包括用于容纳血液的第一室和用于容纳透析液体的第二室的装置中,半渗透膜的位置使得其将第一室与第二室隔开。这使得能够将膜可渗透物质从第一室转移到第二室或从第二室转移到第一室。通常,这些物质,只要它们是膜可渗透的,就将优先沿其浓度梯度迁移。
半渗透膜对具有白蛋白大小或性质的蛋白质不可渗透。然而,碳酸氢根和氢阳离子以及其他小分子,包括可影响水性液体的pH的离子或物质,可在本发明的方法过程中穿过半渗透膜。因此,在使血液与透析液体接触的整个过程步骤中,透析液体的pH不一定保持恒定。因此,确切地说,如本说明书中所限定的,透析液体的pH和(组合的)碳酸根/碳酸氢根浓度优选针对处于即将进行所述接触的阶段的透析液体限定,即,处于透析液体进入第二室的阶段。换句话说,在进入第二室时,透析液体具有6.8至11.0的pH(或如本说明书中限定的任何优选的值或其子范围)。
虽然物质通过半渗透膜的转移是被动的,即沿浓度梯度,但通过例如这些液体经过相应的室的恒定流动并任选地通过搅拌、振动、压力梯度(导致对流)或其他合适的机械活动,血液和/或透析液体将优先移动。认为这种机械活动有助于物质高效地暴露于半渗透膜的表面,并从而有助于通过膜迁移的效率。
包括半渗透膜和两个室的装置
适于本发明的装置包括适于容纳血液的第一室和适于容纳透析液体的第二室。第一室和第二室由至少一个半渗透膜隔开。
合适地,第一室被分成多个第一室。“多个”是指多于一个的任何整数。因此,通常,装置中存在多个第一室。优选地每个第一室经由半渗透膜与第二室接触。所述第一室优选以毛细管的形式存在。这能够使血液在经由半渗透膜与透析液体接触的同时流过毛细管。
任选地,装置中存在多个第二室。优选地,每个第二室经由半渗透膜与第一室接触。
在装置中,(多个)第二室的总体积与(多个)第一室的总体积的比率可为10:1至1:10。优选地,(多个)第二室的总体积大于(多个)第一室的总体积。优选的比率为约2:1。
通常,在适于本发明的装置中,半渗透膜的暴露表面积可为0.01m2至6m2。当平行使用两个透析单元时,通常存在最高6m2的(组合)表面积。在本发明的一个实施方案中预期这种两个透析单元的平行使用。通常,任何一个透析单元的暴露表面积为0.01m2至3m2,如0.1m2至2.2m2。通常,在这些范围的较低部分中的表面积特别适合儿童的治疗。暴露表面积是指在一侧暴露于第一室、同时在另一侧暴露于第二室的半渗透膜的面积。没有同时暴露于两个室但例如固定在固定机构中或以其他方式未暴露的任何另外的膜部分不应视为是暴露表面积的一部分。本发明的方法还可以在同一透析单元中或在多于一个透析单元中使用多于一个这样的膜。如果使用了多于一个透析单元,则从体外循环血液流路的角度看,这样的多于一个的透析单元可成排或平行地存在。优选地,存在两个用于透析的装置,每一个具有如上所公开的暴露表面积。
本发明的方法因此能够使二氧化碳和其他化合物如氢阳离子和碳酸氢根(通过透析膜)转移到透析液体。因此,本发明的方法适于CO2去除。与常规方法相比,这允许更高效地从血液去除代谢物,如CO2。
虽然氨甲酰血红蛋白和溶解的二氧化碳与碳酸氢根(HCO3 -)/H+离子对平衡,但迅速的转化需要碳酸酐酶这种酶。任选地,半渗透膜含有碳酸酐酶活性。这可通过用碳酸酐酶涂覆膜的朝向血液的侧和/或朝向透析液体的侧来实现。
合适地,在半渗透膜的任一侧提供一个室,即在半渗透膜的一侧提供第一室并在半渗透膜的另一侧提供第二室。换句话说,适宜使用包括两个隔室的装置,所述隔室由半渗透膜隔开。优选地,第一室、半渗透膜和第二室包括在一个装置中。因此,血液存在于第一室中,透析液体存在于第二室中,这些室由所述半渗透膜隔开。也可以用酶碳酸酐酶涂覆半渗透膜。
合适地,存在多个第一室,每一个经由半渗透膜与第二室接触。这种多个第一室可呈毛细管的形式;因此,在该实施方案的方法中,血液流过毛细管。
在静态系统中采用本发明的方法并非不可能。在这样的情况下,血液稳定地存在于第一室中,即没有流动(进入、经过和离开该室)。透析液体还稳定地存在于第二室中,即没有流动(进入、经过和离开该室)。然而,优选半静态和非静态实施方案。在非静态实施方案中,血液流经第一室,以使其进入、经过并离开第一室,而透析液体流经第二室,以使其进入、经过并离开第二室。其中仅这些液体中之一流经其相应的室而另一液体稳定地存在于其相应的另一室中,即相应的另一液体不流动(进入、经过和离开)通过该相应的另一室的实施方案被称为半静态。因此,优选地,在本发明的方法中,血液流过第一室并且透析液体同时流过第二室。因此,优选的是血液通过血液隔室(第一室)并且透析液体通过透析液体隔室(第二室)。
本发明的方法使得可以高效地去除如上所定义的一种或多于一种不期望的物质,包括CO2,而不需要如现有技术中的气流(吹扫气体)。特别地,既不期望也不需要将不期望的CO2带入气相中。通常,本发明中使用的透析单元不包括其中气体(吹扫气体)经由膜(例如,气体交换膜)与血液接触的室。
合适地,包括第一室、第二室和半渗透膜的装置为透析单元,其任选地包括在透析器中。透析单元是这样的单元,其包括如本文所定义的第一室、如本文所定义的第二室、和半渗透膜以及用于使流体(例如,血液)进入第一室和从第一室中去除流体(例如,血液)的机构(入口和出口)及用于流体(例如,透析液体)进入第二室和从第二室中去除流体(例如,透析液体)的机构(入口和出口)。因此,第一室包含入口和出口,并且第二室包含入口和出口。因此,在本发明中,透析单元包括为生物流体回路的一部分的生物流体隔室(第一室)、为透析液体回路的一部分的透析液体隔室(第二室)和隔开生物流体隔室与透析液体隔室的半渗透膜。在使用透析单元时,血液通过第一室,透析液体通过第二室。
或者,装置为用于透析、过滤或渗滤的装置。
优选地,在本发明的方法过程中,第二室基本上不包含任何气相,即基本上仅填充呈液相的透析液体。因此,血液的气体接触可被完全排除,或被限制到最低限度,在这种情况下需要例如气泡捕捉器或类似装置。
本发明中使用的半渗透膜不受特别限制,只要其可渗透水和溶解于水中的无机分子即可。对于本发明合适的半渗透膜能够使至少一种不期望的物质通过半渗透膜转移。膜可例如选自目前用于例如血液透析的常规半渗透膜。然而,也可想到考虑比目前用于透析的那些具有更大孔的膜。通过膜的扩散可任选地借助于过滤由对流转运支持。
透析器包括如上所述的透析单元及另外的管道(入口和出口),其与用于分别使流体进入所述第一室和第二室和从所述第一室和第二室中去除流体的相应机构相连:连接到第一室的管道(入口和出口)适于连接到人或动物的血液系统。透析器基本上包括由透析膜隔开的两个室,其每一个连接用于待使用的流体的管道系统。任选地,连接到第二室的管道(入口和出口)适于连接到再生单元。后一设置允许透析液体的再生(再循环、回收利用),如下文以及在WO 03/094998 A1和WO 2009/071103 A1中所述,二者均以引用方式全文并入本文。本发明中使用的透析器不受特别限制,并可以是目前用于例如血液透析的常规透析器。在一个特别的实施方案中,本发明中可与如本文所述的用于氧合血液的装置一起使用系统。
如果需要,可以从血液中去除液体。例如,可以从血液中去除与在本发明的方法的步骤(i)和(ii)过程中引入(如果引入了任何液体的话)的体积相同或基本近似的液体。或者,如果需要,可以去除甚至更多的液体。
透析单元
优选地,平行地使用两个用于透析的装置或两个透析单元。这允许增加暴露的膜表面积,并因此能够使一种或多于一种不期望的物质更高效地通过半渗透膜交换。
其他方法特征和参数
以下其他特征和参数适合与透析单元结合使用,即在包括第一室、第二室和半渗透膜的装置中使用。
透析器的常规部件如压力计、空气检测器、泵送装置如肝素泵、血泵等形成根据本发明的装置或装置的一部分。
一次性使用
可以在从第二室(出口)离开后弃去透析液体。这样的实施方案被称为“一次性使用”或“单程”方法。一次性使用实施方案需要在方法的基本上整个持续过程中(向第二室的入口中)加入新鲜的透析液体。
在本发明的情况下,一次性使用是可能的。然而,它不如下文描述的再循环方便。因此,一次性使用在本发明的情况下较不优选。
再循环
与一次性使用相对,透析液体也可被再循环(“回收利用”或“多次使用”或“多程”)。为此,从第二室(出口)离开的透析液体(“用过的透析液体”)被收集并返回到第二室(入口)中。白蛋白相对昂贵。因此通常希望再循环含白蛋白的透析液体。换句话说,再循环可以节省大量成本。
再循环还允许最高4000ml/分钟的高透析液体流量。
通常,透析液体的再循环需要清洗或再生透析液体。这种清洗或再生通过至少一种类型的处理步骤实现,以在再次进入第二室中之前从透析液体(即,用过的透析液体)中去除不期望的物质。所述步骤在第二室外进行,即在与血液接触位点不同的位点处进行。所述至少一个处理步骤选自(i)暴露于吸附剂和/或(ii)暴露于渗滤和/或(iii)暴露于酸性pH和/或碱性pH和/或(iv)暴露于渗透膜或半渗透膜(即,与位于透析单元中隔开第一室和第二室的膜不同的膜)。所述吸附剂通常是不同于白蛋白的实体;即,对于含白蛋白的透析液,所述吸附剂是其他的或另外的吸附剂。在特别合适的实施方案中,所述吸附剂能够结合钠离子(Na+)和/或氯离子(Cl-)。
此类处理步骤中的任何一个或多于一个可连续地或平行地(即在分离透析液体后)进行。可以预期在透析液体暴露于由半渗透膜隔开的血液之后、即在从第二室中离开后使透析液体经受处理或纯化。处理或纯化透析液体的合适装置包括一个或多于一个吸附单元、一个或多于一个pH变化单元和/或一个或多于一个渗滤单元。这样的单元并不互相排斥,而是可成排或平行地存在。特别是,本发明的透析液体的再循环可能还需要并因此涉及(总的)碳酸根/碳酸氢根浓度和/或pH的调节,以确保在被(重新)引入到第一室中时透析液体的pH与如本文所限定的本发明的情况下所期望的性质相符。(重新)引入是指再循环后的引入。
流量
血液通过第一室,透析液体通过第二室。血液和透析液体的流量或流速可从恒定或随时间改变(变化)中选择。
由于血液氧合和二氧化碳去除都取决于血液流量,故通常期望适应性地改变流量。以下情况成立:血液流量越高,被治疗的对象的氧合越好;血液流量越低,二氧化碳去除越好。
通常调节血液流量到50ml/分钟至7000ml/分钟的范围。
在本发明中,流量一般不受限制。例如,可能的是,血液以低流量(小于800ml/分钟;优选100ml/分钟至800ml/分钟)、以中等流量(800ml/分钟至2400ml/分钟)或以高流量(大于2400ml/分钟)流过第一室。通常控制和调整血液流量并可根据处理条件和透析液体进行调节。
在一个实施方案中,最优选低流量。
在一个替代的实施方案中,最优选中等流量。
通常,低流量和/或中等流量处理对于操作者来说比高流量更容易操作,并且对于患者而言比高流量风险小。另外,当在中等流量下实施本发明的方法时,另外的肺保护性通气(LPV)不是必需的;与通常需要另外的LPV的现有技术中等流量装置相比,这是一大优势。由于不期望的物质如二氧化碳向液相的转移,并且由于可能向血液中引入过量的氧(使血液为氧超饱和的),故根据本发明在中等流量下高的氧合速率是可能的。在不同于本发明的方法的方法中,过量的氧会引起血红蛋白结合H+离子的释放,并会产生游离的二氧化碳气体。这将构成气体栓塞的风险,或者由于二氧化碳的溶解度比氧高约20倍,故将构成溶解的二氧化碳被逆向转运回正接受治疗的对象中的风险。鉴于这些考虑,由于中等血液流量更安全的操作,故中等血液流量在本发明中是有利的。在中等流量下,本发明中肺可得到最高100%的支持而不需要任何其他的通气装置。与现有技术的用于体外循环肺支持的中等流量系统相比,这是显著的改进。这种现有技术的中等流量系统是不利的,首先是因为它们通常必须与肺保护性通气(LPV)结合使用。然而,机械通气方法与血小板活化、炎症、血凝固的风险相关并可能由此导致致命(Assmann等人,Zeitschrift für Herz-,Thorax-und第23卷,第4期,第229-234页,2009年7月)。现有技术系统与LPV的组合的另一个缺点在于医院的人员和空间容量及护理人员是有限的;然而,保护性通气和体外循环肺支持的组合会需要至少两个平行的装置。相比之下,本发明的方法有利地在没有平行的LPV的情况下实施。换句话说,通常用于现有技术中等流量装置的另外的肺保护性通气(LPV)不是必需的。
在本发明中高流量也是可能的。然而,为了获得高流量系统的血液流量,需要更大容器的插管插入术,这必须由专家进行并与某些健康风险相关联。这就是本发明中中等流量被认为有利的原因之一。
可提供泵以引导或控制血液的流量。
通常提供泵来引导或控制透析液体的流量。
在本发明的方法中,透析液体流量可为10ml/分钟至11000ml/分钟(即,0.1667ml/h至183.333ml/h)。更通常地,透析液体流量选自以下:对于每个透析器,慢的透析液体流量(1l/h至2l/h)和正常透析液体流量(25l/h至60l/h)以及中间速率(大于2l/h至小于25l/h)。因此可根据需要适应性地改变流量。较高的透析液体流量通常允许碳酸氢根/碳酸根的高效转移。
通常,优选血液的流量低于透析液体的流量。从而可实现对血液的高效处理。
在透析单元中,即在包括第一室、第二室和半渗透膜的装置中,血液和透析液体优选不以逆流传送,即优选以顺流传送。然而,通常可以想到,血液和透析液体可以相同的方向或逆流通过用于透析的装置。
从透析液体中去除CO2
在本发明的方法的优选实施方案中,预期从透析液体(图2C的15号)中去除二氧化碳和/或碳酸和/或其解离产物(H+/HCO3 -)的可能性。这理想地在不连续的步骤中预期,即在透析液体离开第二室(出口)之后的步骤中。针对这些目的的措施不受特别限制,只要它们合适即可。对于该处理,二氧化碳和/或碳酸和/或其解离产物(H+/HCO3 -)适合通过脱气(减压、加热或冷却、超声波、膜脱气、用惰性气体置换、添加还原剂、冷冻-抽真空-解冻循环、降低pH、离心力或添加脱气添加剂)、过滤、吸附或化学键合从透析液体中去除。例如,所述去除可通过脱气(例如,减压、加热或冷却、超声波、膜脱气、用惰性气体置换、添加还原剂、冷冻-抽真空-解冻循环、降低pH、离心力或添加脱气添加剂)、过滤、吸附或化学键合和/或这些措施的组合实现。理想地可以在透析液体从第二室离开后,测量透析液体中二氧化碳和/或碳酸和/或碳酸氢根的浓度和/或测量pH。二氧化碳和/或碳酸和/或其解离产物的所述去除在如本文所述的透析液体被再循环的那些实施方案中是特别合适的。
在一个特别合适的实施方案中,实施本发明的方法使得再循环包括将透析液体酸化至酸性pH以形成二氧化碳和借助于气泡捕集器通过二氧化碳可渗透膜从透析液体中去除二氧化碳。合适地,膜是气体可渗透的,并且二氧化碳在气相中去除。
酸/碱处理
白蛋白可商购获得但相对昂贵。因此,基于白蛋白的透析液体可能招致高的方法成本。在现有技术中,例如在WO 03/094998 A1中已针对肝透析的情况描述了含有白蛋白的透析液体的再循环,其通过引用全文并入本文。如该专利申请中所述,可基于载体蛋白(如白蛋白)对结合物质如毒素的结合亲和力可通过某些措施如pH-变化来改变这一原理而使白蛋白再循环。包含白蛋白的透析液体的pH的选择性降低和后续升高(反之亦然)将允许经由透析(扩散)或过滤(对流)或两种方法的组合(后文称为渗滤)高效地去除结合物质。一般来说,渗滤是稀释方法,其涉及通过使用可渗透溶液的组分的过滤器基于其分子大小去除或分离溶液的组分(可渗透分子如盐、小蛋白质、溶剂等)。以渗滤为媒介去除此类组分将允许白蛋白的后续再循环。如现有技术中所述,白蛋白可在具有两个平行的透析液体流路、即平行的酸性流路和碱性流路的透析再生单元中高效地再生(WO 09/071103 A1)。WO 09/071103 A1中描述的方法和装置(例如,透析液体再生单元、透析单元)也适合于在本发明的方法中再循环含有白蛋白的透析液体;因此,WO 09/071103 A1通过引用全文并入本文。
通过在改变的pH下处理(清洗、再生)透析液体的步骤,结合到例如白蛋白的毒素可被去除。为了高效地去除所述毒素,根据本发明的实施方案的透析液体再生单元包括平行操作的两个流路。待再生的透析液体被分离并通过两个流路传送。在第一流路中,(从酸性流体供给单元)向透析液体中添加酸性流体。对于可溶于酸性溶液中的毒素,溶液中游离毒素的浓度将增高。在位于酸性流体供给单元下游的解毒单元中,游离毒素从在第一流路中流动的酸化透析液体中去除。通过向透析液体中添加酸性流体,可允许酸性可溶性毒素的去除。此外,通过降低pH,碱性可溶性毒素例如可沉淀并由此从透析液体流体中去除。在平行于第一流路延伸的第二流路中,(从碱性流体供给单元)向在第二流路中流动的透析液体中添加碱性流体。由于pH的升高,游离的碱性可溶性毒素的浓度将增高,并因此允许碱性可溶性毒素的去除。这些毒素由位于碱性流体供给单元下游的另一解毒单元去除。另一解毒单元适于从在第二流路中流动的碱化透析液体中去除毒素。此外,通过升高pH,酸性可溶性毒素例如可沉淀并由此从透析液体流体去除。通过平行提供酸性流路和碱性流路,酸性可溶性毒素和碱性可溶性毒素都可(更)高效地从透析液体中去除。因此,根据本发明的实施方案的透析液体再生单元能够高效地去除蛋白质结合毒素。术语“毒素”在本文中应非常宽泛地理解并涵盖所有的蛋白质结合物质,即便它们本身通常不是直接毒性的(引起健康问题),如药物、电解质、H+、激素、脂肪、维生素、气体和代谢降解产物如胆红素。在统称为“pH处理单元”(或解毒单元)的酸处理单元和碱处理单元的下游,来自第一流路的再生酸化透析液体可与来自第二流路的再生碱化透析液体汇合,由此来自第一流路的酸化透析液体和来自第二流路的碱化透析液体可至少部分地彼此中和。因此,通过汇合来自第一流路的酸化透析液体流与来自第二流路的碱化透析液体流,可提供处于生理pH值的再生透析液体流。
根据优选的实施方案,由第一供给单元添加的酸性流体包含盐酸、硫酸和乙酸中的至少一种。在优选的实施方案中,第一供给单元适于调节第一流路中透析液体的pH为1至7、优选2.5至5.5。
优选地,由第二供给单元添加的碱性流体包含以下中的至少一种:氢氧化钠溶液和氢氧化钾溶液。在优选的实施方案中,第二供给单元适于调节第二流路中透析液体的pH为7至13、优选8至13、更优选8至11。
进一步优选地,酸性流体和碱性流体选择为使得在中和过程中产生“生理”中和产物。例如,一定浓度的所形成的中和产物可能已经存在于相应的生物流体中。例如,在使用盐酸水溶液和氢氧化钠水溶液时,通过酸化流和碱化流的中和将产生一定量的NaCl。NaCl通常也存在于生物流体如血液或血清中。
根据优选的实施方案,通过降低第一流路中透析液体的pH,对于透析液体中的至少一些毒素,毒素-载体-复合物与游离毒素和游离载体物质的浓度比率将以有利于游离毒素的方式改变,从而增大透析液体中游离毒素的浓度。通过降低第一流路中透析液体的pH,酸性可溶性毒素(如镁或铜)的溶解度将增加,而酸性可溶性毒素对载体物质的结合亲和力将降低。相应地,溶液中游离毒素的浓度将增大。
进一步优选地,解毒单元适于至少部分地去除所述游离毒素。由于游离毒素浓度的增大,故所述毒素可以增大的速率去除。
此外,通过降低第一流路中透析液体的pH值,一些碱性可溶性毒素例如可沉淀,并由此从透析液体流体中去除。
在优选的实施方案中,通过升高第二流路中透析液体的pH,对于透析液体中的至少一些毒素,毒素-载体-复合物与游离毒素和游离载体物质的浓度比率将以有利于游离毒素的方式改变,从而增大透析液体中游离毒素的浓度。通过升高第二流路中透析液体的pH,碱性可溶性物质(如胆红素)的溶解度将增加,而碱性可溶性毒素对载体物质的结合亲和力将降低。相应地,溶液中游离毒素的浓度将增大。
优选地,另一解毒单元适于至少部分地去除所述游离毒素。由于游离毒素浓度的增大,故所述毒素可以增大的速率去除。
此外,通过升高第二流路中透析液体的pH值,一些酸性可溶性毒素例如可沉淀,并由此从透析液体流体中去除。
根据进一步优选的实施方案,通过升高透析液体的温度,对于透析液体中的至少一些毒素,毒素-载体-复合物与游离毒素和游离载体物质的浓度比率将以有利于游离毒素的方式改变,从而增大透析液体中游离毒素的浓度。相应地,游离毒素可由解毒单元以增大的速率去除。
使含有白蛋白的透析液体再循环的又一个方面在WO 2009/071103 A1中描述,其通过引用全文并入本文,包括附图中的说明。除了WO 2009/071103 A1中描述的发现外,白蛋白还有助于根据本发明的透析液体的优异缓冲能力。
吸附剂处理/吸附
为了提取或去除过量或不期望的物质,如电解质(例如,阳离子如钾阳离子、钠阳离子和钙阳离子;或阴离子如氯阴离子、碳酸根阴离子或碳酸氢根阴离子),可使吸附剂与透析液体接触。一般来说,吸附剂能够吸附患者血液中存在的至少一种不期望的物质(例如,尿素、尿酸、电解质、钠阳离子、钙阳离子或钾阳离子;氯阴离子)。通常,吸附剂存在于吸附剂单元中,即存在于透析液体将通过其中的固定单元中。吸附剂的类型或组成或材料不受特别限制,只要其具有结合至少一种待从透析液体中去除的物质的能力即可。本领域中已知不同的吸附剂类型。通过吸附剂的适当选择,可根据实际需要例如根据个体患者的需要调整方法。吸附剂在再循环实施方案中、即当意图使透析液体再循环时特别有用。
透析液体的再生方面
过量或不期望的物质可通过膜即可渗透膜或半渗透膜从透析液体(用过的透析液体)中去除。例如,溶解在透析液体中的气体和/或溶质/离子可通过这样的膜处理来去除。在一个优选的实施方案中,二氧化碳以气体或以溶解于液体中的状态去除。去除二氧化碳的一种特别合适的方式为使透析液体与可渗透二氧化碳的膜接触。透析液体具有一定的压力p1,并且所述膜另一侧的流体(液体或气体)的压力p2较低,即p2<p1。如果在所述膜另一侧的流体中CO2的分压较低,则也可以或替代地实现从用过的透析液体中去除CO2这一目的。类似地,可以沿浓度梯度去除碳酸氢根,即通过使用过的透析液体与碳酸氢根可渗透的膜接触,只要膜另一侧的流体(液体)中(总的)碳酸根/碳酸氢根浓度低于用过的透析液体的(组合的)碳酸根/碳酸氢根浓度即可。在任何情况下,使用的膜都对白蛋白不可渗透。这可通过选择具有适宜孔尺寸的膜来实现。这样的膜处理对于再循环实施方案特别有用。
医学用途
可以并希望针对医学目的利用如上所述的本发明的方法。针对通过手术或疗法治疗人体或动物体的任何活动,特别是旨在预防或改善活体对象内的病症、即服务于医学目的的那些活动可被称为医学方法或医学用途。一般来说,术语方法(method)和过程(process)在本文中可互换使用。然而,有时候,术语方法被用来特别指医学方法;本发明的医学方法可涉及上述从血液中去除不期望的物质的过程的任何和所有方面。特别是,本发明提供了一种用于体外循环处理来自需要这类处理的患者的血液的方法。使体外循环血液经受如本文所述的透析方法,即——通常来说——暴露于由半渗透膜隔开的透析液体。为此,从对象中取出血液,经受本发明的方法,并适当地返回到对象。通常,在这样的方法中,从患者中取出静脉血液并使之进入本发明的方法的第一室。在本文所述的任何和所有方面,这允许血液以本发明的方法处理。然后,血液(“经处理的血液”)离开第一室并可返回到患者。最通常的是使经处理的血液进入患者的静脉,但作为替代方案,可返回到动脉,然而后者适当地局限于其中血液还经历氧合的方法。由从身体取出患者血液到将经处理的患者血液返回到身体的所有这些方面对于本文所述的所有适应症而言都是常见的医学方法。
本发明的发现允许其利用于通过疗法对人体或动物体的治疗中(通常称为医学用途)。可以根据相应患者的实际需要具体定制本发明的医学用途。尽管在本质上,气体交换不限于具有肺的生物体,还在具有鳃的生物体(如鱼)中也同样发生,但本发明的医学用途集中在肺支持这一目标上,即用于治疗或预防具有肺的生物体如优选哺乳动物、更优选人类中的某些病症。因此,本说明书中没有详细讨论鳃和/或具有鳃的生物体。
优选地,在医学方法中,透析液体的特征在于摩尔渗透压浓度,其与血液即正在透析单元中透析的物种(例如,人)的血液的摩尔渗透压浓度基本相同。
任选地,通常适合于血液的体外循环处理的本发明方法不(或至少不一定)包括侵入性步骤和/或不包括代表对身体的实质性物理干预的步骤和/或不包括其进行需要专业的专门医学知识的步骤和/或不包括即便在使用专业的护理和专门知识进行时也牵涉到实质性健康风险的步骤。优选地,本发明的方法不包括代表对身体的实质性物理干预的侵入性步骤,这样的步骤的进行需要专业的医学专门知识并且即便在使用所需的专业护理和专门知识进行时也牵涉到实质性的健康风险。例如,本发明的方法任选地不包括连接透析系统与人体或动物体和/或断开透析系统与人体或动物体的连接的侵入性步骤。在另一个实施例中,体外循环装置与活体对象的静脉血液的接触以及由此相应的医学方法不会牵涉到实质性的健康风险。
本发明的医学方法用于或适用于治疗至少一种选自呼吸性酸中毒、代谢性酸中毒、肺衰竭或肺病、肾衰竭、多器官衰竭以及这些中任何一种或多于一种的组合的病症。方法可根据待治疗的病症或根据待治疗的个体具体配置(个性化医疗)。虽然以下部分讨论的是这些病症的治疗,但相应的预防方法同样涵盖在本发明中。
所有这些治疗方法都涉及从对象中抽取静脉血液,从而产生体外循环血液;如本发明的方法的情况所述的,使体外循环血液暴露以经由半渗透膜与如本文所述的透析液体接触,从而产生经处理的血液;和将经处理的血液返回到同一对象,优选返回到对象的静脉中,在较不优选的实施方案中返回到对象的动脉中。下面描述具体的配置。
肺衰竭或肺病的治疗
本发明的方法适于治疗患有急性或慢性呼吸性衰竭(肺衰竭)的患者。患有肺衰竭但通常不患其他器官衰竭如肾衰竭或肝衰竭的患者会发生呼吸性酸中毒或有发生呼吸性酸中毒的风险。这是因为二氧化碳的去除不像健康对象那样高效,或根本不会发生。该患者组包括患有哮喘、换气不足、肺病如肺癌、与吸烟和与暴露于其他空气中毒素或颗粒物有关的并发症、或肌营养不良症或肺气肿、特别是晚期肺气肿的患者。许多患有此类肺病的患者具有完全健全的肾(肾功能健全)。本发明允许体外循环氧合以及至少一种不期望的物质如二氧化碳或碳酸氢根或氢阳离子的体外循环去除。因此,本发明提供了全肺支持并且特别适合于该患者组。
透析液体或被弃去或优选被再循环。在后一情况下优选使透析液体经受膜处理。通过膜处理,二氧化碳和/或碳酸氢根和/或碳酸根和/或碳酸可被去除或部分地去除。这将允许透析液体的再循环。对于二氧化碳的去除,膜处理优选在低的pH下进行,即在透析液的酸化之后进行。
合并肺衰竭/肾衰竭的治疗
除肺外,肾也在维持体液pH方面起着重要作用。在健康的人或动物对象中,肾与肺协作调节碳酸根/碳酸氢根比率和调节血液pH。因此,一般来说,肾通过调节血浆的pH而在维持健康个体的酸-碱平衡中起着重要作用:主要功能包括从尿液中重吸收碳酸氢根和将氢阳离子排泄到尿液中。肾的这些功能对于维持酸-碱平衡很重要,并且还可有助于控制血液pH。
现代重症监护室/重症监护病房(ICU)正在广泛使用肾替代疗法(RRT)来治疗此类对象。在重症监护病房中的对象(ICU对象)中,作为多器官功能障碍综合征(MODS)的一部分,急性肾衰竭(ARF)在术后状态中和介入性研究后在已经易感的个体中频繁发生。一般来说,ICU对象需要不同的器官支持,如连续肾替代疗法(CRRT)、肝透析和机械通气。与传统上需要至少三个不同装置来治疗这类对象的肾、肝和肺衰竭(或者除了用于治疗肝衰竭的装置外,还需要使用组合的三室装置来治疗肾/肺衰竭,PrismaLungTM,DE 10 2009 008601A1;WO 2010/091867 A1;Novalung)的现有技术相比,本发明提供了显著的改进。
在患有肾衰竭的患者中,肾的正常功能受到影响。与常规的体外循环肺支持例如仅允许气体交换并且不支持肾的ECMO相比,本发明还能够治疗肾衰竭和多器官衰竭。因此,本发明允许治疗患有尤其是急性或慢性肾脏(肾)功能不全或慢性肾衰竭(CRF)的对象。本发明还允许治疗患有肾病如肾癌以及与中毒和与暴露于某些药物有关的并发症的患者。
为了治疗多器官衰竭,例如肺和肾衰竭,本发明相对于现有技术提供了进一步的优点,因为其仅使用一个单一装置,而不是两个单独的装置——一个用于治疗肺衰竭,一个用于治疗肾衰竭。在本发明的方法中,所述单一装置包括用于使血液与由半渗透膜隔开的透析液体接触的第一室和第二室。
在本发明中,条件(进入第二室的透析液体的(组合的)碳酸根/碳酸氢根浓度;离开第一室的血液的pH;离开第一室的血液的碳酸氢根浓度)适当地选自本文针对任何呼吸性或代谢性酸中毒描述的那些条件,优选地针对代谢性酸中毒描述的那些。另外,优选包括适于结合或吸附患者血液中存在的至少一种不期望的物质(例如,尿素、尿酸、电解质、钠阳离子、钙阳离子或钾阳离子;氯阴离子)的吸附剂。例如,在患有肾衰竭的患者中,通常肾不能够维持血液中溶质的生理浓度或所需浓度,所述溶质包括:钠阳离子、钙阳离子或钾阳离子;和/或氯阴离子。本发明解决了这些缺点。具体而言,可专门适应性地改变透析液体以维持相应溶质的期望水平。为此,透析液体含有比相应溶质的期望血液浓度(i)更多或(ii)更少的相应溶质,这取决于是期望(i)增大还是(ii)减小正接受治疗的对象的血液中相应溶质的浓度。本发明提供了一种多功能的肾支持:例如,如果希望肾支持来从血液去除过量的碳酸氢根,则优选透析液体选择为使得其不包含外加的碳酸氢根;优选地,碳酸根和碳酸氢根的(组合)浓度低于5mmol/l;更优选地为0mmol/l。在又一个实例中,如果希望肾支持来调节血液pH(例如,用于治疗酸中毒),则优选透析液体选择为使得其pH和/或缓冲能力适应于这样的目标:例如,pH可为8.0至11.0,和/或对H+离子的缓冲能力可为12mmol/l或更高。下文描述了治疗酸中毒的其他方面。
合并肾衰竭/肝衰竭/肺衰竭的治疗
本发明还允许治疗除肺衰竭和/或肾衰竭外,还患有急性或慢性肝衰竭的对象。根据本发明的典型治疗涉及体外循环毒素去除。为了治疗此类对象,可以修改WO 2009/071103 A1和/或WO 03/094998 A1中描述的方法或通过Hepa Wash公司(德国慕尼黑)提供的方法使得透析液体与本发明的透析液体框架或与其任何实施方案相符。在这样的方法中,白蛋白具有双重或协同作用:其不仅结合毒素(解决肝功能不全),而且与碳酸根一起缓冲透析液体(解决肺功能不全)。这意味着,除了WO 2009/071103 A1和/或WO 03/094998 A1中描述的功能外,还可以实现肺支持和/或修正血液pH至生理水平或其他期望的水平。该治疗允许在一个单一装置中组合肾透析、肝透析及包括二氧化碳去除和血液氧合在内的肺支持。
上面针对肾衰竭的治疗所述的修改或配置,如吸附剂的存在,也适于在本实施方案中采用。
呼吸性酸中毒的治疗
本发明的方法适于治疗患有急性或慢性呼吸性酸中毒的患者。患者组包括患有换气不足、肺肿瘤、哮喘、肌营养不良症或肺气肿、特别是晚期肺气肿的患者。为了治疗患有呼吸性酸中毒的对象,透析液体在进入第二室的阶段适合含有低的(组合的)碳酸根/碳酸氢根浓度,其为0mmol/l至最大40mmol/l。事实上,对于呼吸性酸中毒,优选的(组合的)碳酸根/碳酸氢根浓度应尽可能低,即0mmol/l或大于0mmol/l。子范围包括1mmol/l至35mmol/l、2mmol/l至30mmol/l、3mmol/l至25mmol/l、4mmol/l至20mmol/l、5mmol/l至15mmol/l,例如10mmol/l。
通常,处于上述范围或子范围的较低端值的(组合的)碳酸根/碳酸氢根浓度允许高效地从血液去除不期望的物质,如碳酸氢根、CO2和碳酸根。
呼吸性酸中毒的治疗需要调节血液pH。因此,用于治疗该患者组的透析液体适当地调节至具有至少12mmol/l的缓冲能力,如本文所定义。如上所述,酸中毒患者的治疗以及血液氧合通常需要向透析液体中加入2,3-DPG。这是因为酸中毒患者产生的2,3-DPG通常比健康对象少。
当透析液体中(组合的)碳酸根/碳酸氢根浓度低(例如,0mmol/l或0mmol/l至10mmol/l)时,则所需的缓冲能力适当地主要由透析液体中足够量的其他缓冲剂提供,通常是白蛋白和任选地Tris。特别地,当没有向透析液体中加入碳酸根/碳酸氢根(即,透析液体中碳酸根/碳酸氢根浓度为0mmol/l或接近0mmol/l)时,优选的是Tris和白蛋白都存在于透析液体中。这些缓冲剂的浓度选择为使得缓冲能力超过血浆的缓冲能力。这将允许血液pH的高效调节。
还可以在治疗的过程中增大(组合的)碳酸根/碳酸氢根浓度。这允许使治疗适应于个体的需要(个性化医疗)。
在经由半渗透膜暴露于这样的透析液体后,血液pH通常为7.40或更高;如高于7.40但不高于8.0,如7.5至7.9、或7.6至7.8、或7.65至7.75,例如7.7。这样的血液被返回到对象中。
已知在患有呼吸性酸中毒的对象(即,由于肺中的低效去除而导致体液中CO2过量溶解)中,肾经常因增加的量的碳酸氢根的产生而延迟一些时间作出反应,例如延迟3周。本发明允许在整个疾病过程中治疗患有呼吸性酸中毒的对象,即在早期阶段主要希望从体液去除过量CO2以及在晚期阶段(还)希望从体液去除过量碳酸氢根。此外,可以在疾病的所有阶段从体液去除过量的H+离子。在治疗的过程中,医生可以根据本文提供的指导改变透析液体的构成和pH。还可以在治疗的过程中在本发明的范围(0mmol/l至40mmol/l)内逐渐增大(组合的)碳酸根/碳酸氢根浓度。
本发明的方法步骤的氧合有助于从血红蛋白释放H+离子和CO2。分子原因在于如上所述Haldane效应在体外循环中的利用。因此,由于Haldane效应,氧合步骤使得这些不期望的物质非常高效地从血液去除。这是相对于现有技术方法的一大改进。
代谢性酸中毒的治疗
本发明还包括治疗代谢性酸中毒的方法。在分子水平上,代谢性酸中毒是由酸性有机分子数量的增多所致,酸性有机分子数量的增多是由于代谢活动增加导致产生的有机酸(例如,乳酸)增多和/或经由肾排泄酸的能力失调引起。慢性肾衰竭(CRF)中的代谢性酸中毒是由于排泄非挥发性酸的能力下降及碳酸氢根的肾合成减少并因此导致体内氢阳离子的增加所致。不限于此,有机酸可源自例如蛋白质分解代谢的氨基酸残基或者来自饥饿期间或糖尿病性酸中毒中酮酸的积累(酮症)。虽然在许多情况下,受影响的身体会试图通过呼吸来补偿代谢性酸中毒(呼吸补偿),但非挥发性代谢物不会通过该途径排泄,并且受影响的对象有力竭的风险,这会导致呼吸衰竭。本发明提供了一种解决方案:其或作为预防措施,或作为治疗措施,即当代谢性酸中毒严重并且不再能由肺适当补偿时,可能需要本发明方法的治疗:
对于患有代谢性酸中毒的对象的治疗,需要高pH的透析液体,例如,pH为8.0至11.0,优选8.0至9.0。透析液体的缓冲能力高于血浆的缓冲能力。透析液体的高pH与透析液体的高缓冲能力的组合允许高效地调节血液pH及血液的碳酸氢根、CO2和碳酸根物质的最小净通量(添加或去除)。特别地,与标准透析方法相比,该通量可增大。
如上所述,酸中毒患者的治疗以及血液氧合通常需要向透析液体中加入2,3-DPG。这是因为酸中毒患者产生的2,3-DPG通常比健康对象少。在经由半渗透膜暴露于这样的透析液体后,血液pH通常在希望调节血液pH所至的范围内或为该范围涵盖的值,即7.0至7.8、7.2至7.6、或7.3至7.5、7.35至7.45,最优选地确切地为或约为7.40。
对于患有急性或慢性代谢性酸中毒并且肺功能正常的对象的治疗,透析液体在进入第二室的阶段适当地含有作为附加缓冲剂的碳酸根。合适的(组合的)碳酸根/碳酸氢根浓度为20mmol/l至40mmol/l、优选地25mmol/l至35mmol/l,更优选地确切地为或约为30mmol/l。
本发明还允许治疗以呼吸性酸中毒和代谢性酸中毒的组合为特征的病症。因为透析液体、特别是透析液体的pH和(组合的)碳酸根/碳酸氢根浓度可根据个体需要进行调节,因此该治疗是可能的。
然而,对于以急性或慢性代谢性酸中毒为特征但肺功能受损的对象亚组的治疗,透析液体优选地不含任何外加的碳酸根/碳酸氢根。对于该类型患者合适的透析液体适当地含有0mmol/l至5mmol(优选地0mmol)的(组合的)碳酸根/碳酸氢根浓度。缓冲能力由白蛋白单独提供;或由白蛋白与在上文定义的浓度范围内的其他合适的非碳酸根/非碳酸氢根缓冲剂例如Tris提供。例如,如果透析液体中(组合的)碳酸根/碳酸氢根浓度与患者血液中(组合的)碳酸根/碳酸氢根浓度相同,则不会发生碳酸根/碳酸氢根的净转移(即,去除)。
合并器官功能不全的治疗和心血管疾病的治疗
在许多情况下,患有肺衰竭和/或肺中气体交换不良的对象也受到其他器官功能障碍的影响。本发明的方法也适于治疗这样的对象,并因此支持这些器官。
特别地,在患有心血管疾病、特别是心脏功能受损并因此血液流动受损的对象中,血液向肺的输送通常效率低下。因此,作为所述心血管病症的后果,患有这种心血管病症的患者还患有肺中气体交换受损,即肺中二氧化碳释放受损和/或肺中血液氧合受损。
本发明不仅能够治疗所述后果(肺中气体交换受损),而且还能治疗导致该后果的原因(心血管疾病,例如心脏功能受损并因此血流受损)。这通过从待治疗的对象的静脉取出血液、根据本发明使所述血液经受体外循环肺支持和通过泵送血液通过第一室并将血液返回到对象的动脉中来实现。为此,在第一室之前或在第一室之后提供泵。所述泵将使血液通过体外循环回路移动并因此至少部分地替代心脏的受损功能。
鉴于上述内容,本发明在又一个方面提供一种透析液体,其用于治疗和/或预防选自肺衰竭、呼吸性酸中毒、代谢性酸中毒、肾衰竭、心血管疾病或它们的任何组合的疾病,其中所述透析液体
(i)包含白蛋白,优选地10g/l至60g/l的白蛋白,
(ii)具有6.8至11的pH;和
(iii)是氧合的。
用于根据本发明使用的这种透析液体的优选实施方案对应于如上所述透析液体的优选实施方案以及如上所述过程和/或方法的优选实施方案。例如,这样的透析液体优选由如本文所述用于氧合透析流体的方法进行氧合。
优选地,“氧合的”透析液体含有溶解氧。更优选地,“氧合的”透析液体中溶解氧的量超过标准条件下(即,293.15K的温度和14.696psi的压力下)水中溶解氧的量。
此外,本发明还提供了一种透析液体,其在通过疗法治疗人或动物对象的方法中使用,其中所述透析液体的pH为6.8至11;并且其中所述透析液体包含白蛋白,优选地10g/l至60g/l的白蛋白;
并且其中所述使用优选地包括步骤:
(i)从所述对象的静脉或动脉取出血液;
(ii)使血液经受根据权利要求1至29中任一项所述的方法,由此使用所述透析液体;和
(iii)将血液重新引入到所述对象的动脉或静脉中。更优选地,所述透析液体是氧合的。
实施例:
以下实施例为说明的目的提供。这些实施例不限制本发明。
实施例1:包含一种或多于一种缓冲剂的溶液的缓冲能力
通过实验测试包含一种或多于一种缓冲剂的各种水性溶液的缓冲能力。这些水性溶液是示例性的液体,其缓冲能力对应于根据本发明的透析液体(透析液)或用于比较目的的透析液体(透析液)。
1A:液体的制备
这些示例性液体如下制备:
为了制备根据本发明的示例性透析液体和参考液体,使用纯水(渗透品质)作为基础,并加入根据本发明的一种或多于一种缓冲剂(白蛋白和/或碳酸氢钠(“苏打”)和/或三(羟甲基)氨基甲烷(Tris/THAM))。特别地,将白蛋白(以下面所示的浓度)和/或碳酸氢根(以下面所示的浓度)和/或Tris(以下面所示的浓度)溶解于水中。然后或同时,调节pH至下面所示的值。如果需要,白蛋白的加入和pH的调节可同时进行。在一些情况下,如下表中所示,白蛋白在期望pH下或接近期望pH下将更快地溶解。无论如何,在所有缓冲剂已溶解后,立即对pH进行复核,如果必要,进行调节。pH的调节通常通过加入酸性浓缩物(HCl水溶液)和/或通过加入碱性浓缩物(NaOH水溶液)来完成。
出于比较目的,还制备不添加缓冲剂(白蛋白、碳酸根/碳酸氢根、Tris)的溶液。如下表中所示,分别调节这些溶液的pH至7.45和9。
为了进一步的比较,还制备两种在现有技术描述的范围内的含乙酸根示例性液体,其还含有碳酸氢钠。详情参见下表。
另外,制备四种仅含有Tris的示例性液体。为此,制备两种Tris(三(羟甲基)-氨基甲烷)溶液:
-Tris 38mmol/l:溶解后的初始pH:10.45。
-Tris 20mmol/l:溶解后的初始pH:10.14。
如下表中所示,加入HCl(0.1M或0.2M)直至达到下表中所示的pH值(分别为7.45或9.0)。由此制得含Tris的示例性液体。
在制备示例性液体时,不加入碳酸根(例如,碳酸钠)。然而,应理解,碳酸根和碳酸氢根取决于pH以动态平衡存在。因此,通过添加一定量的碳酸氢根(例如,20mmol/l)和调节至一定的pH(例如,pH 9)所制得的任何示例性液体将包含组合浓度的碳酸氢根和碳酸根(例如,在该情况下20mmol/l)。
具体而言,制备以下示例性液体:
表1:
在图1中,所有这些液体都被称为“透析液”。示出了各自的缓冲剂和pH。
作为参考(内标),测定了血液血浆(“血浆”)的缓冲能力。为此,如下测试猪血。首先,测定碳酸氢根浓度和pH,发现平均碳酸氢根浓度为24.2mmol/l,pH为7.45。其次,使所述血液经受离心以获得无细胞的上清液。此无细胞的上清液被称为血浆。
在图1中,其被称为“血液血浆”。
1B:缓冲能力的测定
通过实验测试1A部分中描述的所有液体(根据1A部分表1的液体;如1A部分中描述的血浆)对H+离子的缓冲能力。为此,用HCl滴定所有液体(参考用示例性液体和根据本发明的示例性液体及血浆)。具体而言,加入0.1M HCl,连续监测pH,搅动溶液以确保混合,并在pH达到pH 6.5的最终值时终止滴定。换句话说,当pH达到6.5的值时停止滴定。基于pH达到6.5时所加入的HCl的量计算缓冲能力(H+离子,单位mmol/l)。
图1中示出了通过该测定法测得的缓冲能力。
测得血浆的缓冲能力为12.00mmol/l H+离子。
优选根据本发明的示例性液体(在表1中以编号3至8提供)的特征在于,如通过该测定法所测得,缓冲能力(单位mmol/l)优于血液血浆的缓冲能力。
因此,根据本发明的透析液体提供优异的缓冲能力,特别是在其中本发明的透析液体的pH高于正常人血液pH的实施方案中。
实施例2:钙浓度
使用包含钙(Ca2+离子)的透析液体,并且该透析液体的pH从7.45至9变化(参见图3)。使透析液体经由半渗透膜与血液接触。测定血液中的钙浓度。如从图3可以看出,即便透析液体中钙浓度高于1.70mmol/l,血液中的钙离子浓度也保持在1.00mmol/l至1.70mmol/l的期望范围。这证明根据本发明的透析液体中钙离子浓度适当地为高于1.70mmol/l。
实施例3:血液的氧合
将五升肝素化猪血以200ml/分钟的血液流量连续地通过体外循环血液回路模型(Hepa Wash LK2001透析装置)泵送。示意性地,血液通过第一室(由图2A中的1号表示)。血液通过半渗透膜与透析液体接触。
使血液再循环。然而,为了模拟来自需要肺支持的患者的脱氧血液,并为了使进入第一室的血液的血红蛋白的氧饱和度保持恒定,血液被连续地脱氧。这确保了进入第一室的血液具有约60至70%的氧饱和度(O2Hb前)(参见图4)。
该透析液体具有7.45的pH。透析液体流量设定为1000ml/分钟。示意性地,透析液体通过第二室(由图2A中的2号表示)。进入第二室的透析液体构成如下:
| Na<sup>+</sup> | 138.00 | mmol/l |
| K<sup>+</sup> | 4.00 | mmol/l |
| Ca<sup>2+</sup> | 2.50 | mmol/l |
| Mg<sup>2+</sup> | 0.50 | mmol/l |
| Cl<sup>-</sup> | 110.00 | mmol/l |
| HCO<sub>3</sub><sup>-</sup> | 20.00 | mmol/l |
| 葡萄糖 | 1.00 | g/l |
| 白蛋白 | 20.00 | g/l |
为了氧合,在透析液体进入第二室(在图2A中由12号示意性地表示的位置)之前不断地向透析液体中引入富氧渗透水。调节氧浓度和引入速率以取得约99%的目标氧合血红蛋白饱和度。渗透水的富氧可通过本文描述的任一种方法实现。在特定的情况下,渗透水的富氧通过在升高的压力下暴露于氧、然后通过毛细管将该富氧的渗透水在图2A中由12号示意性地表示的位置处释放到透析液体中。
图4示出了该实验的成功:
测量了血红蛋白的氧饱和度(%)(在图4中表示为O2Hb[%])。
O2Hb前:在血液进入第一室中之前测得的血红蛋白的氧饱和度。
O2Hb后:在血液从第一室离开后测得的血红蛋白的氧饱和度。
本实施例表明,本发明的方法允许非常高效且连续的血液氧合。如图4中所示,从第一室离开的血液中血红蛋白的氧饱和度恒定地高于95%,通常在99%左右。
Claims (81)
1.液态氧或富氧液体和/或富氧固体在制备用于氧合血液用于体外循环肺支持的制剂中的用途,其中通过包括以下步骤的方法来氧合血液:
(i)向血液中和/或向透析液体中引入氧,
其中所述透析液体的pH为6.8至11;并且其中所述透析液体包含白蛋白;
从而产生富氧血液和/或富氧透析液体;和
(ii)使所述血液经由半渗透膜与所述透析液体接触,
其中向所述血液中和/或向所述透析液体中引入的氧以液态氧或富氧液体和/或富氧固体引入。
2.根据权利要求1所述的用途,其中所述透析液体包含10g/l至60g/l的白蛋白。
3.根据权利要求1或2所述的用途,其中在步骤(i)中将氧引入到所述透析液体中和所述血液中。
4.根据权利要求1或2所述的用途,其中在步骤(i)中将氧引入到所述透析液体中,但不引入到所述血液中。
5.根据权利要求1或2所述的用途,其中所述接触步骤包括所述血液流经第一室,从而进入、通过并离开所述第一室,所述透析液体流经第二室,从而进入、通过并离开所述第二室,其中所述第一室和第二室由所述半渗透膜彼此隔开。
6.根据权利要求5所述的用途,其中所述第一室、半渗透膜和第二室包括在一个装置中,所述装置为透析单元或透析器。
7.根据权利要求1或2所述的用途,其中通过步骤(i)将氧引入到所述血液中。
8.根据权利要求7所述的用途,其中步骤(i)在权利要求6限定的装置外部的位置并且在血液或透析液体进入所述装置中之前进行,使得血液或透析液体或其二者以富氧形式进入装置中。
9.根据权利要求1或2所述的用途,其中通过以下任何一种或多于一种情况将氧引入到所述血液中和/或所述透析液体中:
(a)输注富氧液体;
(b)输注液态氧;
(e)引入富氧固体;和
(f)富氧液体的对流输送。
10.根据权利要求9所述的用途,其中所述富氧固体为干凝胶和液凝胶或冷冻的富氧液体。
11.根据权利要求1或2所述的用途,其中除白蛋白外,所述透析液体还包含一种或多于一种缓冲剂,所述缓冲剂的特征在于至少一个pKa值为7.0至11.0。
12.根据权利要求11所述的用途,其中所述一种或多于一种缓冲剂选自:三(羟甲基)氨基甲烷和碳酸根/碳酸氢根。
13.根据权利要求6所述的用途,其中选自二氧化碳、氢阳离子和碳酸氢根的至少一种不期望的物质从存在于权利要求6限定的透析器或透析单元中的所述血液中去除。
14.根据权利要求13所述的用途,其中所述至少一种不期望的物质从所述血液至少部分地通过所述半渗透膜输送到所述透析液体中。
15.根据权利要求1或2所述的用途,其中所述透析液体具有对氢阳离子12mmol/l或更高的缓冲能力。
16.根据权利要求1或2所述的用途,其中所述透析液体的特征在于pH为8.0至9.0。
17.根据权利要求1或2所述的用途,其中所述透析液体包含2,3-二磷酸甘油酯。
18.根据权利要求1或2所述的用途,其中所述方法的至少一部分在低于37℃的温度下进行。
19.根据权利要求18所述的用途,其中所述方法的一个或多于一个步骤在低于37℃的温度下进行。
20.根据权利要求18所述的用途,其中所述方法的至少一部分在4℃至20℃的温度下进行。
21.根据权利要求18所述的用途,其特征在于步骤(i)包括向血液中输注低于37℃的富氧液体或液态氧;和/或
步骤(ii)提供温度低于30℃的与血液接触的透析液体。
22.根据权利要求5所述的用途,其中所述血液以100ml/分钟至800ml/分钟的低流量、以800ml/分钟至2400ml/分钟的中等流量或以大于2400ml/分钟的高流量流经所述第一室。
23.根据权利要求13所述的用途,其中所述透析液体的pH和组成根据待向血液中加入的氧的量来选择和/或根据待从血液中去除的不期望的物质的量来选择。
24.根据权利要求23所述的用途,其中所述不期望的物质选自二氧化碳、氢阳离子和碳酸氢根。
25.根据权利要求11所述的用途,其中所述透析液体包含10mmol/l至40mmol/l的碳酸根/碳酸氢根,以碳酸根和碳酸氢根浓度的总量计。
26.根据权利要求11所述的用途,其中所述透析液体包含5mmol/l至20mmol/l的三(羟甲基)氨基甲烷。
27.根据权利要求5所述的用途,其中使离开所述第二室的透析液体经受至少一个处理步骤,然后再次进入第二室。
28.根据权利要求27所述的用途,其中所述至少一个处理步骤选自(i)暴露于吸附剂;和/或(ii)与膜接触;和/或(iii)暴露于酸性pH和/或碱性pH。
29.根据权利要求28所述的用途,其中所述膜为半渗透膜。
30.根据权利要求28所述的用途,其中所述至少一个处理步骤选自(i)暴露于吸附剂;和/或(ii)与膜接触以去除二氧化碳。
31.根据权利要求28所述的用途,其中所述处理步骤包括酸化所述透析液体至酸性pH以形成二氧化碳和任选地去除二氧化碳。
32.根据权利要求1或2所述的用途,其中所述方法还包括测量所述血液和/或所述透析液体的至少一个参数的步骤,所述参数选自pH、二氧化碳分压、碳酸氢根浓度、缓冲能力、脱氧血红蛋白浓度或饱和度和氧合血红蛋白饱和度中的一个或多于一个。
33.根据权利要求1或2所述的用途,其中所述白蛋白选自人血清白蛋白和/或牛血清白蛋白。
34.根据权利要求1或2所述的用途,其中所述透析液体包含大于1.7mmol/l的钙离子。
35.根据权利要求34所述的用途,其中所述透析液体包含2mmol/l至4mmol/l的钙离子。
36.根据权利要求35所述的用途,其中所述透析液体包含2.4mmol/l至2.6mmol/l的钙离子。
37.根据权利要求27所述的用途,其中在将所述透析液体重新引入到所述第二室中之前调节透析液体的pH和/或缓冲能力。
38.根据权利要求1或2所述的用途,其中整个所述方法或至少所述方法的步骤(i)和/或(ii)在人体或动物体外进行。
39.液态氧或富氧液体和/或富氧固体在制备用于体外循环肺支持的用于体外循环处理来自人或动物对象的血液的制剂中的用途,其中通过包括以下步骤的方法来体外循环处理血液:
(i)从所述对象的静脉或动脉取出血液;
(ii)使步骤(i)的血液经受权利要求1至38中任一项所限定的方法;和
(iii)将步骤(ii)的血液重新引入到所述对象的动脉或静脉中。
40.根据权利要求39所述的用途,其中所述对象选自患有肺衰竭的对象、患有呼吸性酸中毒的对象、患有代谢性酸中毒的对象、患有肾衰竭的对象、患有心血管疾病的对象、或患有这些中任何两种或多于两种的组合的对象。
41.根据权利要求40所述的用途,其中所述对象患有肺衰竭或肺病。
42.一种在通过疗法治疗人或动物对象的方法中所使用的用于体外循环肺支持的透析液体,
其中所述透析液体的pH为6.8至11;其中所述透析液体包含白蛋白;并且其中所述透析液体是氧合的,且向所述透析液体中引入的氧以液态氧或富氧液体和/或富氧固体引入。
43.根据权利要求42所述使用的透析液体,其中所述透析液体包含10g/l至60g/l的白蛋白。
44.根据权利要求42所述使用的透析液体,其中所述使用包括步骤:
(i)从所述对象的静脉或动脉中取出血液;
(ii)使血液经受权利要求1至38中任一项所限定的方法,由此使用所述透析液体;和
(iii)将血液重新引入到所述对象的动脉或静脉中。
45.根据权利要求42至44中任一项所述使用的透析液体,其中所述对象选自患有肺衰竭的对象、患有呼吸性酸中毒的对象、患有代谢性酸中毒的对象、患有肾衰竭的对象、患有心血管疾病的对象、或患有这些中任何两种或多于两种的组合的对象。
46.根据权利要求45所述使用的透析液体,其中所述对象患有肺衰竭或肺病。
47.一种在治疗和/或预防选自肺衰竭、呼吸性酸中毒、代谢性酸中毒、肾衰竭、心血管疾病或其任意组合的疾病中所使用的用于体外循环肺支持的透析液体,其中所述透析液体
(i)包含白蛋白,
(ii)具有6.8至11的pH;和
(iii)是氧合的,其中向所述透析液体中引入的氧以液态氧或富氧液体和/或富氧固体引入。
48.根据权利要求47所述使用的透析液体,其中所述透析液体包含10g/l至60g/l的白蛋白。
49.液态氧或富氧液体和/或富氧固体在制备用于氧合透析液体用于体外循环肺支持的制剂中的用途,其中通过包括以下步骤的方法来氧合透析液体:
(i)向所述透析液体中引入氧,
其中所述透析液体的pH为6.8至11,其中所述透析液体包含白蛋白;由此产生富氧透析液体;
其中向所述透析液体中引入的氧以液态氧或富氧液体和/或富氧固体引入。
50.根据权利要求49所述的用途,其中所述透析液体包含10g/l至60g/l的白蛋白。
51.根据权利要求49或50所述的用途,所述方法包括步骤(i)之后的步骤(ii),其中在步骤(ii)中,所述氧合的透析液体流经第二室,从而进入、经过并离开所述第二室,第二室由半渗透膜与第一室隔开。
52.根据权利要求51所述的用途,其中所述第一室、半渗透膜和第二室包括在一个装置中,所述装置为透析单元或透析器。
53.根据权利要求52所述的用途,其中步骤(i)在权利要求52中限定的装置外并在透析液体进入所述装置中之前进行,使得所述透析液体以富氧形式进入装置中。
54.根据权利要求49或50所述的用途,其中在步骤(i)中通过以下任何一种或多于一种情况将氧引入到所述透析液体中:
(a)输注富氧液体;
(b)输注液态氧;
(e)引入富氧固体;和
(f)富氧液体的对流输送。
55.根据权利要求54所述的用途,其中所述富氧固体为干凝胶和液凝胶或冷冻的富氧液体。
56.根据权利要求49或50所述的用途,其中除白蛋白外,所述透析液体还包含一种或多于一种缓冲剂,所述缓冲剂的特征在于至少一个pKa值为7.0至11.0。
57.根据权利要求56所述的用途,其中所述一种或多于一种缓冲剂选自:三(羟甲基)氨基甲烷和碳酸根/碳酸氢根。
58.根据权利要求49或50所述的用途,其中所述透析液体具有对氢阳离子12mmol/l或更高的缓冲能力。
59.根据权利要求49或50所述的用途,其中所述透析液体的特征在于pH为8.0至9.0。
60.根据权利要求49或50所述的用途,其中所述透析液体包含2,3-二磷酸甘油酯。
61.根据权利要求49或50所述的用途,其中所述透析液体包含10mmol/l至40mmol/l的碳酸根/碳酸氢根,以碳酸根和碳酸氢根浓度的总量计。
62.根据权利要求49或50所述的用途,其中所述透析液体包含5mmol/l至20mmol/l的三(羟甲基)氨基甲烷。
63.根据权利要求51所述的用途,其中在步骤(ii)之后使离开所述第二室的透析液体经受至少一个处理步骤(iii)。
64.根据权利要求63所述的用途,其中在步骤(iii)之后,所述透析液体再次进入所述第二室。
65.根据权利要求63所述的用途,其中所述至少一个处理步骤(iii)选自(1)暴露于吸附剂;(2)与膜接触;和/或(3)暴露于酸性pH和/或碱性pH。
66.根据权利要求65所述的用途,其中所述膜为半渗透膜。
67.根据权利要求65所述的用途,其中所述至少一个处理步骤(iii)选自(1)暴露于吸附剂;(2)与膜接触以去除二氧化碳。
68.根据权利要求63所述的用途,其中所述处理步骤(iii)包括酸化所述透析液体至酸性pH以形成二氧化碳和任选地去除二氧化碳。
69.根据权利要求49或50所述的用途,其还包括测量所述透析液体的至少一个参数的步骤,所述参数选自pH、二氧化碳分压、碳酸氢根浓度、缓冲能力、脱氧血红蛋白浓度或饱和度和氧合血红蛋白饱和度中的一个或多于一个。
70.根据权利要求49或50所述的用途,其中所述白蛋白选自人血清白蛋白和/或牛血清白蛋白。
71.根据权利要求49或50所述的用途,其中所述透析液体包含大于1.7mmol/l的钙离子。
72.根据权利要求71所述的用途,其中所述透析液体包含2mmol/l至4mmol/l的钙离子。
73.根据权利要求72所述的用途,其中所述透析液体包含2.4mmol/l至2.6mmol/l的钙离子。
74.根据权利要求51所述的用途,其中在将所述透析液体重新引入到所述第二室中之前调节透析液体的pH和/或缓冲能力。
75.根据权利要求49所述的用途,其中所述方法还包括以下步骤:
(a)将所述透析液体流分离为第一流和第二流;
(b)向透析液体的第一流中添加酸性流体;
(c)通过对所述透析液体的酸化的第一流过滤、透析、沉淀或渗滤来去除毒素;
(d)向所述透析液体的第二流中添加碱性流体;
(e)通过对所述透析液体的碱化的第二流进行过滤、透析、沉淀或渗滤来去除毒素;
(f)汇合所述透析液体的第一流和第二流。
76.根据权利要求75所述的用途,其中步骤(a)至(f)先于步骤(i)进行。
77.根据权利要求75所述的用途,其中步骤(a)至(f)在步骤(ii)之后进行。
78.根据权利要求63所述的用途,其中权利要求75所限定的步骤(a)至(f)作为步骤(iii)的子步骤进行。
79.根据权利要求75所述的用途,其中所述方法还包括定期切换多个开关阀,使得酸化的透析液体流被交替地供给到第一解毒单元和第二解毒单元,而碱化的透析液体流被交替地供给到所述第二解毒单元和所述第一解毒单元。
80.根据权利要求75所述的用途,其中所述方法还包括以下中的一个或多于一个步骤:
-调节酸化透析液的温度;
-通过所述酸化产生的沉淀去除毒素;
-调节碱化透析液的温度;和
-通过所述碱化产生的沉淀去除毒素。
81.根据权利要求42或47所述使用的透析液体,其中所述透析液体通过权利要求49至80中任一项所限定的方法氧合。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EPPCT/EP2015/002331 | 2015-11-20 | ||
| PCT/EP2015/002331 WO2017084683A1 (en) | 2015-11-20 | 2015-11-20 | Method for extracorporeal lung support |
| PCT/EP2016/078198 WO2017085292A1 (en) | 2015-11-20 | 2016-11-18 | Method for extracorporeal lung support |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN108367109A CN108367109A (zh) | 2018-08-03 |
| CN108367109B true CN108367109B (zh) | 2022-01-28 |
Family
ID=54608483
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680063827.4A Active CN108367109B (zh) | 2015-11-20 | 2016-11-18 | 用于体外循环肺支持的方法 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US11583620B2 (zh) |
| EP (2) | EP3377139B1 (zh) |
| JP (1) | JP6983793B2 (zh) |
| KR (1) | KR20180084125A (zh) |
| CN (1) | CN108367109B (zh) |
| AU (1) | AU2016356068B2 (zh) |
| BR (1) | BR112018007200A2 (zh) |
| CA (1) | CA3000927A1 (zh) |
| DK (1) | DK3377139T3 (zh) |
| ES (1) | ES2905621T3 (zh) |
| IL (1) | IL258481B (zh) |
| MX (1) | MX2018006089A (zh) |
| PL (1) | PL3377139T3 (zh) |
| WO (2) | WO2017084683A1 (zh) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017084683A1 (en) | 2015-11-20 | 2017-05-26 | Hepa Wash Gmbh | Method for extracorporeal lung support |
| WO2017084682A1 (en) | 2015-11-20 | 2017-05-26 | Hepa Wash Gmbh | Method for extracorporeal carbon dioxide removal |
| US11351291B2 (en) | 2016-03-14 | 2022-06-07 | Advitos Gmbh | Systems or apparatuses and methods for performing dialysis |
| IL270771B2 (en) * | 2017-05-22 | 2023-12-01 | Advitos Gmbh | Methods and systems for removing carbon dioxide |
| MX2020002828A (es) * | 2017-09-17 | 2020-07-22 | Steven Paul Keller | Sistemas, dispositivos, y métodos para la eliminación extracorpórea de dióxido de carbono. |
| CN108211032B (zh) * | 2018-02-01 | 2023-11-17 | 南方医科大学珠江医院 | 组合型生物人工肝支持系统 |
| JP7301509B2 (ja) * | 2018-09-06 | 2023-07-03 | 聡 安斎 | 治療装置 |
| US11633525B2 (en) | 2019-01-29 | 2023-04-25 | Transonic Systems Inc. | Method and apparatus for assessing cardiac output in veno-arterial extracorporeal blood oxygenation |
| US20220031921A1 (en) * | 2019-04-29 | 2022-02-03 | Verthermia Acquisition, Inc. | Method and System for Controlled Hyperthermia |
| US11065379B2 (en) * | 2019-04-30 | 2021-07-20 | Veryhermia Acquistion, Inc. | Method and system for controlled hyperthermia |
| JP7347857B2 (ja) * | 2019-05-02 | 2023-09-20 | トランソニック システムズ インク | 静脈-静脈体外血液酸素化を受けている患者の心拍出量の計算 |
| DE102019007144A1 (de) * | 2019-10-15 | 2021-04-15 | ProMedTec Germany GmbH | Verfahren und Anordnung zur Verbesserung des Austausches von Gasen über semipermeable Membranen im wässrigen Milieu |
| WO2022119951A1 (en) * | 2020-12-01 | 2022-06-09 | Boundless Science, Llc | Method and apparatus for enhanced transport |
| US11219551B1 (en) * | 2021-04-25 | 2022-01-11 | Verthermia Acquisition, Inc. | Method and system for controlled hyperthermia |
| JP7458605B1 (ja) | 2022-07-28 | 2024-04-01 | 国立大学法人 東京大学 | 血漿交換システム、及び血漿交換システムの制御方法 |
| WO2024090508A1 (ja) * | 2022-10-28 | 2024-05-02 | 株式会社ジェイ・エム・エス | 血液浄化システム及び中間システム |
Family Cites Families (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4375414A (en) | 1971-05-20 | 1983-03-01 | Meir Strahilevitz | Immunological methods for removing species from the blood circulatory system and devices therefor |
| US3771658A (en) * | 1971-10-20 | 1973-11-13 | R Brumfield | Blood transport membrane pump |
| US3846236A (en) * | 1971-10-22 | 1974-11-05 | Wisconsin Alumni Res Found | Method and apparatus for dialysis |
| SE7403799L (zh) | 1974-03-21 | 1975-09-22 | Gambro Ab | |
| DE3230540A1 (de) | 1982-08-17 | 1984-02-23 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V., 8000 München | Verfahren und vorrichtung zur entfernung von protein- oder lipidgebundenen toxinen aus blut oder blutfraktionen |
| US4663049A (en) | 1984-07-05 | 1987-05-05 | University Of Utah | Process for therapeutic dissociation of immune complexes and removal of antigens |
| IT8504923V0 (it) | 1985-06-07 | 1985-06-07 | Miren Srl | Dispositivo per il controllo del bilancio idrico di un paziente durante il trattamento di emodialisi |
| FR2651438A1 (fr) | 1989-09-07 | 1991-03-08 | Fondation Nale Transfusion San | Procede d'inactivation par ultrasons d'agents infectieux ou parasitaires dans des milieux biologiques et applications du procede. |
| US6344489B1 (en) | 1991-02-14 | 2002-02-05 | Wayne State University | Stabilized gas-enriched and gas-supersaturated liquids |
| DE4309410A1 (de) | 1993-03-19 | 1995-02-16 | Stange Jan | Material, Verfahren und Einrichtung zur selektiven Trennung frei gelöster und stoffgebundener Stoffe aus flüssigen Stoffgemischen sowie Verfahren zur Herstellung des Materials |
| US5753227A (en) | 1993-07-23 | 1998-05-19 | Strahilevitz; Meir | Extracorporeal affinity adsorption methods for the treatment of atherosclerosis, cancer, degenerative and autoimmune diseases |
| US5561115A (en) | 1994-08-10 | 1996-10-01 | Bayer Corporation | Low temperature albumin fractionation using sodium caprylate as a partitioning agent |
| US6607698B1 (en) | 1997-08-15 | 2003-08-19 | Therox, Inc. | Method for generalized extracorporeal support |
| WO1999037335A1 (en) | 1998-01-23 | 1999-07-29 | Hemotherm, Inc. | Apparatuses and processes for whole-body hyperthermia |
| JP4061775B2 (ja) | 1998-05-21 | 2008-03-19 | ニプロ株式会社 | アルブミン含有腹膜透析液 |
| DE69929555T8 (de) | 1998-06-17 | 2007-05-31 | Nipro Corp. | Verwendung einer Flüssigkeit zur Herstellung einer Dialyselösung für die kontinuierliche rezirkulierende Peritonealdialyse |
| JP2000072658A (ja) | 1998-06-17 | 2000-03-07 | Nissho Corp | 腹膜透析液および腹膜透析法 |
| DE19831061A1 (de) | 1998-07-10 | 2000-01-13 | Rotkreuzstiftung Zentrallab | Herstellung von Proteinpräparationen mit verringertem Aggregatgehalt |
| US7670491B2 (en) | 1998-10-20 | 2010-03-02 | Advanced Renal Technologies | Buffered compositions for dialysis |
| DE60127657T8 (de) | 2000-01-11 | 2008-04-17 | Nephros, Inc. | Blutreinigungssystem |
| US6716356B2 (en) | 2000-01-11 | 2004-04-06 | Nephros, Inc. | Thermally enhanced dialysis/diafiltration system |
| AU2002226209A1 (en) | 2000-12-20 | 2002-07-01 | Dialysis Solutions Inc. | Sterile low bicarbonate dialysis concentrate solutions |
| US7241272B2 (en) | 2001-11-13 | 2007-07-10 | Baxter International Inc. | Method and composition for removing uremic toxins in dialysis processes |
| US7455771B2 (en) | 2002-05-14 | 2008-11-25 | Hepa Wash Gmbh | Means for removing protein-bound substances |
| EP1362605A1 (de) | 2002-05-14 | 2003-11-19 | Bernhard Dr. Kreymann | Dialysevorrichtung zur Entfernung proteingebundener Substanzen |
| US7112273B2 (en) | 2002-09-27 | 2006-09-26 | Nxstage Medical, Inc. | Volumetric fluid balance control for extracorporeal blood treatment |
| US7686778B2 (en) | 2003-01-15 | 2010-03-30 | Nxstage Medical, Inc. | Waste balancing for extracorporeal blood treatment systems |
| ITMI20030212A1 (it) | 2003-02-07 | 2004-08-08 | Gambro Lundia Ab | Metodo per il trattamento extracorporeo di sangue |
| WO2004105589A2 (en) | 2003-05-28 | 2004-12-09 | Hemocleanse Technologies, Llc | Sorbent reactor for extracorporeal blood treatment systems, peritoneal dialysis systems, and other body fluid treatment systems |
| AU2004279280B2 (en) | 2003-10-13 | 2009-11-26 | Fresenius Medical Care Deutschland Gmbh | A device for carrying out a peritoneal dialysis treatment |
| CN1897993B (zh) | 2003-12-24 | 2012-02-08 | 凯米卡技术有限公司 | 用于便携式人类透析的透析液再生系统 |
| EP1649883A1 (en) | 2004-10-19 | 2006-04-26 | MRI S.r.l. Società Unipersonale | A CO2 removal device for removing carbon dioxide from blood or from a fluid taken from patient's cardio-circulatory system |
| JP4908044B2 (ja) | 2006-04-14 | 2012-04-04 | 株式会社ジェイ・エム・エス | 重量検出装置及びバランス制御装置 |
| US20090018484A1 (en) * | 2007-07-11 | 2009-01-15 | Levitov Alexander B | System device and method for oxygenation |
| CN101883594B (zh) * | 2007-12-03 | 2012-10-10 | Hepa净化有限公司 | 透析液再生单元 |
| DE102009008601A1 (de) | 2009-02-12 | 2010-08-19 | Novalung Gmbh | Vorrichtung zur Behandlung einer biologischen Flüssigkeit |
| PL2416770T3 (pl) | 2009-04-06 | 2017-06-30 | Crearene Ltd. | Roztwory do hemodializy i dializy otrzewnowej zawierające jeden lub więcej związków kreatyny |
| DK177144B1 (en) * | 2009-06-19 | 2012-02-06 | Aquaporin As | A liquid membrane suitable for water extraction |
| CN102107031A (zh) * | 2009-12-28 | 2011-06-29 | 天津市海河医院 | 血液血浆中毒素滤过吸附器及其制备方法和应用 |
| DE102010023635A1 (de) | 2010-06-14 | 2011-12-15 | Fresenius Medical Care Deutschland Gmbh | Vorrichtung und Verfahren zum Fördern von Flüssigkeiten in die Behandlungseinheit einer medizinischen Behandlungsvorrichtung, insbesondere in den Dialysator einer Dialysevorrichtung |
| JP2012228285A (ja) * | 2011-04-23 | 2012-11-22 | Sunceramics Corp | 酸素濃度を高めた透析液 |
| PL2644215T3 (pl) | 2012-03-28 | 2015-04-30 | Gambro Lundia Ab | Aparat do pozaustrojowej obróbki krwi |
| EP2653178A1 (de) | 2012-04-16 | 2013-10-23 | Zentrum für biomedizinische Technologie der Donau- Universität Krems | Sicherheitseinrichtung für eine extrakorporale Blutbehandlung |
| GB201207543D0 (en) * | 2012-05-01 | 2012-06-13 | Haemair Ltd | Treatment of transfusion blood |
| CN102940886B (zh) | 2012-12-13 | 2015-02-18 | 鼎正动物药业(天津)有限公司 | 一种生物屏障渗透剂及其制备方法 |
| US10322221B2 (en) | 2013-01-18 | 2019-06-18 | University of Pittsburgh—of the Commonwealth System of Higher Education | Removal of carbon dioxide via dialysis |
| DE112014001309T5 (de) | 2013-03-13 | 2016-01-07 | Nxstage Medical, Inc. | Single-Pass-Dialyse in Kombination mit Multiple-Pass-Albumin-Dialyse |
| DE102013019356A1 (de) | 2013-11-19 | 2015-06-03 | Fresenius Medical Care Deutschland Gmbh | Vorrichtung und Verfahren zum Bilanzieren von Flüssigkeiten für eine extrakorporale Blutbehandlungsvorrichtung |
| WO2017084682A1 (en) | 2015-11-20 | 2017-05-26 | Hepa Wash Gmbh | Method for extracorporeal carbon dioxide removal |
| WO2017084683A1 (en) | 2015-11-20 | 2017-05-26 | Hepa Wash Gmbh | Method for extracorporeal lung support |
| IL270771B2 (en) | 2017-05-22 | 2023-12-01 | Advitos Gmbh | Methods and systems for removing carbon dioxide |
-
2015
- 2015-11-20 WO PCT/EP2015/002331 patent/WO2017084683A1/en active Application Filing
-
2016
- 2016-11-18 US US15/777,639 patent/US11583620B2/en active Active
- 2016-11-18 MX MX2018006089A patent/MX2018006089A/es unknown
- 2016-11-18 ES ES16797952T patent/ES2905621T3/es active Active
- 2016-11-18 PL PL16797952T patent/PL3377139T3/pl unknown
- 2016-11-18 AU AU2016356068A patent/AU2016356068B2/en active Active
- 2016-11-18 BR BR112018007200A patent/BR112018007200A2/pt not_active Application Discontinuation
- 2016-11-18 DK DK16797952.5T patent/DK3377139T3/da active
- 2016-11-18 CA CA3000927A patent/CA3000927A1/en active Pending
- 2016-11-18 CN CN201680063827.4A patent/CN108367109B/zh active Active
- 2016-11-18 KR KR1020187017421A patent/KR20180084125A/ko not_active Application Discontinuation
- 2016-11-18 EP EP16797952.5A patent/EP3377139B1/en active Active
- 2016-11-18 WO PCT/EP2016/078198 patent/WO2017085292A1/en active Application Filing
- 2016-11-18 EP EP21207826.5A patent/EP4011416A1/en not_active Withdrawn
- 2016-11-18 JP JP2018545683A patent/JP6983793B2/ja active Active
-
2018
- 2018-04-02 IL IL258481A patent/IL258481B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CN108367109A (zh) | 2018-08-03 |
| DK3377139T3 (da) | 2022-01-24 |
| EP3377139A1 (en) | 2018-09-26 |
| IL258481B (en) | 2021-08-31 |
| EP4011416A1 (en) | 2022-06-15 |
| US11583620B2 (en) | 2023-02-21 |
| CA3000927A1 (en) | 2017-05-26 |
| EP3377139B1 (en) | 2021-12-29 |
| KR20180084125A (ko) | 2018-07-24 |
| BR112018007200A2 (pt) | 2018-10-16 |
| MX2018006089A (es) | 2018-11-09 |
| WO2017085292A1 (en) | 2017-05-26 |
| US20190030232A1 (en) | 2019-01-31 |
| ES2905621T3 (es) | 2022-04-11 |
| IL258481A (en) | 2018-06-28 |
| PL3377139T3 (pl) | 2022-05-16 |
| JP2018538118A (ja) | 2018-12-27 |
| AU2016356068A1 (en) | 2018-04-12 |
| AU2016356068B2 (en) | 2021-07-01 |
| JP6983793B2 (ja) | 2021-12-17 |
| WO2017084683A1 (en) | 2017-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108367109B (zh) | 用于体外循环肺支持的方法 | |
| US11833282B2 (en) | Method for extracorporeal carbon dioxide removal | |
| US11344656B2 (en) | Methods and systems for removing carbon dioxide | |
| WO2014113740A1 (en) | Removal of carbon dioxide via dialysis | |
| RU2783826C2 (ru) | Способы и системы для удаления двуокиси углерода | |
| Minnie et al. | THE USE OF HOLLOW FIBRE MEMBRANE DIALYSERS IN A LIQUID-LIQUID CONFIGURATION FOR RESPIRATORY SUPPORT | |
| Minnie et al. | DEVELOPMENT OF AN ULTRAVIOLET C IRRADIATION DEVICE: INITIAL FINDINGS FOR THE TREATMENT OF SPIKED WHOLE BLOOD |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| CB02 | Change of applicant information | ||
| CB02 | Change of applicant information |
Address after: Munich, Germany Applicant after: Advitos Ltd. Address before: Munich, Germany Applicant before: HEPA WASH GmbH |
|
| GR01 | Patent grant | ||
| GR01 | Patent grant |