CN107430123B - 用于在传感器表面上检测分析物-配体结合的方法 - Google Patents
用于在传感器表面上检测分析物-配体结合的方法 Download PDFInfo
- Publication number
- CN107430123B CN107430123B CN201580074734.7A CN201580074734A CN107430123B CN 107430123 B CN107430123 B CN 107430123B CN 201580074734 A CN201580074734 A CN 201580074734A CN 107430123 B CN107430123 B CN 107430123B
- Authority
- CN
- China
- Prior art keywords
- analyte
- sensor surface
- seconds
- ligand
- sample solution
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/558—Immunoassay; Biospecific binding assay; Materials therefor using diffusion or migration of antigen or antibody
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54373—Apparatus specially adapted for solid-phase testing involving physiochemical end-point determination, e.g. wave-guides, FETS, gratings
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54393—Improving reaction conditions or stability, e.g. by coating or irradiation of surface, by reduction of non-specific binding, by promotion of specific binding
Abstract
本发明提供针对第一分析物的存在而测定样品溶液的方法,该方法包括:(a)提供传感器表面,该传感器表面具有固定化于该传感器表面的配体;(b)使样品溶液流过传感器表面;以及(c)在传感器表面上检测分析物与配体的结合的存在与否;其中,样品溶液与固定化的配体之间的接触时间不到15秒钟。
Description
发明领域
本发明涉及在传感器表面处确定分子结合相互作用的方法,且更具体地,涉及使用生物传感器来确定分析物与配体之间的相互作用的方法。
发明背景
能够实时地对分子(诸如,生物分子)之间的相互作用进行监测的分析传感器系统越来越受到关注。这些系统通常基于光学生物传感器,并且,一般被称为相互作用分析传感器或生物特异相互作用分析传感器。具有代表性的这样的生物传感器系统为GEHealthcare所销售的BIACORE®仪表,该仪表使用表面等离子体共振(SPR),用于检测样品中的分子和固定化于传感表面上的分子结构之间的相互作用。随着样品经过传感器表面,结合的进程直接地反映出发生相互作用的速率。样品的注入随后是缓冲液流动,在此期间,检测器响应反映出表面上的复合物的离解的速率。来自BIACORE®系统的典型输出是描述随着时间推移而变化的分子相互作用的进程(包括缔合相部分和离解相部分)的图表或曲线。一般显示于计算机屏幕上的该结合曲线通常被称为“传感图”。
在BIACORE®系统(及类似的传感器系统)的情况下,因而,有可能在不使用标记的情况下,且通常无需纯化所涉及的物质的情况下,不仅实时地检测样品中的特定分子(分析物)的存在和浓度,而且还实时地检测另外的相互作用参数(包括分子相互作用中的结合(缔合)和离解的动力速率常数以及表面相互作用的亲和力)。通过使许多不同的样品分析物浓度的所得动力学数据与表现为微分方程的形式的相互作用模型的数学描述拟合,能够获得缔合速率常数(ka)和离解速率常数(kd)。能够根据缔合速率常数和离解速率常数而计算亲和力(表示为亲和常数KA或离解常数KD)。还有可能通过平衡结合分析而测量亲和力值,平衡结合分析涉及针对一系列的分析物浓度测定平衡或稳态下的结合的水平,假定在结合相互作用的缔合相结束时或临近结束时已达到该水平。
在当前的方法中,方法学力图获得可高度重复且高质量的响应信号。这通过例如以下的几个耗时的措施而实现:长的注入或接触时间(超过30秒钟),从而具有高而稳定的响应值;对流控系统进行冲洗,从而避免干扰;携带(carry-over)控制注入,从而对来自流控装置的污染的响应贡献进行监测;以及再生,从而在每一个循环中,使传感器表面达到同一起始条件。这些步骤可能非常耗时,并且,得到的循环时间可能通常达到600秒钟或更久。这样的长循环时间可能导致相当长的运行时间,特别是当需要在单个实验中评估多个分析物样品的情况下如此。
本发明至少部分地旨在克服与使用生物传感器来评估分析物与配体之间的相互作用的当前的方法相关联的问题。
发明概要
根据本发明的第一方面,提供针对第一分析物的存在而测定样品溶液的方法,该方法包括:
(a)提供传感器表面,该传感器表面具有固定化于该传感器表面的配体;
(b)使样品溶液流过传感器表面;以及
(c)在传感器表面上检测分析物与配体的结合的存在与否;
其中,样品溶液与固定化的配体之间的接触时间不到15秒钟。
本申请证实,有可能在显著地缩短包含分析物的溶液与配体之间的接触时间的同时,提供涉及表面结合的配体和分析物的结合的有意义且可重复的结合数据。如前所述,在本领域中,标准的做法是,采用长的注入或接触时间(典型地,超过30秒钟),以确保高而稳定的响应值。然而,本发明的发明者已识别出,将接触时间显著地缩短至例如两秒钟或更短,仍然产生有用且可重复的信息。这一发现提供分析物分析的领域(例如,包括抗体筛选和基于片段的筛选的药物开发的多方面)中的显著的优点。具体地,缩短接触时间能够显著地增强生产能力。这能够通过排除如下的更耗时的措施而进一步增强:诸如,对流控系统进行冲洗(采用这一措施,以避免干扰);携带控制注入,从而对来自流控装置的污染的响应贡献进行监测;以及再生,从而在每一个循环中,使传感器表面达到同一起始条件。例如,通过与短的接触时间组合而使用足够高的配体密度,能够排除再生表面的需要,因为,在提供足够的游离的配体,以在彼此之后检测几个样品的同时,配体密度确保充分的分析物结合。这是可能的,因为,仅一小部分的容量用于每个结合,且意味着,对于筛选运行中的典型数量的结合剂,没必要进行再生。
在一个实施方案中,接触时间不到10秒钟。在另一实施方案中,接触时间不到5秒钟。在另一实施方案中,接触时间不到3秒钟。在另一实施方案中,接触时间不到2秒钟。
在另一实施方案中,传感器表面处的检测基于倏逝波传感。
在另一实施方案中,传感器表面处的检测基于表面等离子体共振(SPR)。
在另一实施方案中,在步骤(c)之后,通过使第二样品溶液流过表面,以检测配体与另一分析物之间的结合的存在与否,重复步骤(b)和(c)。另一分析物可以与第一分析物相同。备选地,另一分析物可以与第一分析物不同。在又一实施方案中,针对第三样品溶液而重复步骤(b)和(c)。在另一实施方案中,将步骤(b)和(c)重复至少十次,以测定至少十种另外的溶液。
在另一实施方案中,开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间的时间(循环时间)不到40秒钟。在另一实施方案中,循环时间不到15秒钟。
在另一实施方案中,在开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间,不实行再生步骤。
在另一实施方案中,在开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间,不实行冲洗步骤和/或携带控制注入步骤。
在另一实施方案中,传感器表面上的配体密度为至多50000 RU。在另一实施方案中,传感器表面上的配体密度在5000 RU至15000 RU的范围内。
在另一实施方案中,步骤(c)包含确定样品溶液中的分析物浓度。
在另一实施方案中,步骤(c)包含确定分析物对配体的亲和力。
在另一实施方案中,方法包含确定不同的样品溶液之间的分析物浓度和/或分析物亲和力的差异(相对或绝对)。
在另一实施方案中,配体或分析物是抗体或其片段。在另一实施方案中,所述方法用于筛选抗体。
在另一实施方案中,所述方法用作基于片段的筛选,以鉴定非特异性的结合剂或聚集体。
在另一实施方案中,所述方法用作基于片段的筛选,以鉴定针对配体的特异性的结合剂。
根据本发明的第二方面,提供一种计算机程序,该计算机程序包含程序代码手段,该程序代码手段用于使传感器装置运行,从而根据包含以下的步骤的方法在传感器表面上检测分析物与配体之间的相互作用:(a)提供传感器表面,该传感器表面具有固定化于该传感器表面的配体;
(b)使样品溶液流过传感器表面;以及(c)在传感器表面上检测分析物与配体的结合的存在与否;其中,样品溶液与固定化的配体之间的接触时间不到15秒钟;并且,其中,在计算机上运行程序。所述方法可以具有在上文中关于本发明的第一方面而描述的任何实施方案中所描述的特征。
附图简述
图1是基于SPR的生物传感器系统的示意侧视图。
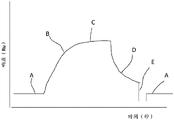
图2是示出针对分析物与用于分析物的固定化的结合剂之间的相互作用,随时间变化的检测器响应的具有代表性的传感图。
图3和图4示出在BIACORE T200仪器上执行的实验的结果,这些结果表明采用2秒钟的接触时间,在分析物(β2μ球蛋白)的各种浓度下,配体(抗β2μ)之间的相互作用。图3示出随循环次数而变化的注入之后的响应。图4示出当未将命令加到注入时,随着循环时间而变化的对应的传感图。
图5用图表示出针对每个循环而在各种时间下使带有4针系统的384板运行所耗费的时间。
发明详述
如上文所提到的,在第一方面,本发明涉及针对第一分析物的存在而测定样品溶液的方法,该方法包含:(a)提供传感器表面,该传感器表面具有固定化于该传感器表面的配体;(b)使样品溶液流过传感器表面;以及(c)在传感器表面上检测分析物与配体的结合的存在与否;其中,样品溶液与固定化的配体之间的接触时间不到15秒钟。典型地,通过基于传感器的技术而获得实验结合数据,该技术研究分子相互作用,并且,随着相互作用进程而实时地呈现结果。在更详细地描述本发明之前,然而,将描述旨在使用本发明的一般背景。
除非另有定义,否则本文中所使用的所有的技术术语和科学术语都具有与本发明有关的领域的技术人员普遍地理解的相同含义。同样地,除非另有说明,否则单数形式“一”、“一个”以及“这个”旨在包括复数的参考物。
本文中所提到的所有的出版物、专利申请、专利及其他参考文献通过引用整体地并入。
化学传感器或生物传感器典型地基于无标记的技术,检测传感器表面的性质(诸如,例如,固定化的层的质量、折射率或厚度)的改变,但是,也存在依赖于某种标记的传感器。典型的传感器检测技术包括(但不限于)质量检测方法(诸如,光学方法、热光学方法以及压电或声波方法(包括例如表面声波(SAW)和石英晶体微天平(QCM)方法))和电化学方法(诸如,电位式方法、电导式方法、电流式方法以及电容/阻抗式方法)。关于光学检测方法,具有代表性的方法包括检测质量表面浓度的方法,诸如,角、波长、极化或相分辨式的反射光学方法(包括外反射方法和内反射方法两者),例如,倏逝波椭圆光度法和倏逝波光谱(EWS或内反射光谱),这两者都可以包括经由表面等离子体共振(SPR)、布儒斯特角折射测定法、生物层干涉(BLI)、临界角折射测定法、受抑全反射(FTR)、散射式全内反射(STIR)(可以包括散射增强标记)、光学波导传感器而实现的倏逝场增强;外反射成像、基于倏逝波的成像,诸如,临界角分辨成像、布儒斯特角分辨成像、SPR角分辨成像等。而且,可以提到基于例如表面增强型拉曼光谱(SERS)、表面增强型共振拉曼光谱(SERRS)、倏逝波荧光(TIRF)以及磷光的“本身”或与反射方法组合的光度法和成像/显微技术方法,以及波导干涉仪、波导泄漏模式光谱、反射干涉光谱(RIfS)、透射干涉、全息光谱以及原子力显微技术(AFR)。
市场上可买到的生物传感器包括由GE Healthcare, Uppsala, Sweden制造且推向市场的前面提到的BIACORE®系统仪器,BIACORE®系统仪器基于表面等离子体共振(SPR),并且,允许在感兴趣的结合配体与分析物之间实时地监测表面结合相互作用。在此背景下,“配体”是具有对给定的分析物的已知的或未知的亲和力的分子,且包括固定化于表面上的任何捕获或捕收剂,而“分析物”包括配体的任何特异性的结合配偶体。
能够在本发明中使用的典型的配体包括(但不限于)蛋白(例如,抗体、亲和体或适体)、酶、受体、抗原、半抗原、肽或化学分子(例如,候选药物或其片段)。
能够在本发明中使用的典型的分析物包括(但不限于)蛋白和糖蛋白(例如,抗体或其片段、亲和体或适体)、脂质、碳水化合物、酶、受体、抗原、半抗原、肽或化学分子(例如,候选药物或其片段、特异性的或非特异性的结合剂、螯合剂或聚集体)。
术语“抗体”描述不管是天然的,还是部分地或完全地合成产生的免疫球蛋白。抗体可以是单克隆或多克隆的,并且,可以通过在本领域中众所周知的技术制备,例如,宿主的免疫和血清的收集(多克隆),或通过制备连续的杂交细胞系且收集分泌蛋白(单克隆),或通过克隆且表达编码至少针对天然抗体的特异性结合所要求的氨基酸序列的核苷酸序列或其诱变形式。术语“抗体”还涵盖包含抗体抗原结合位点的任何多肽或蛋白。包含抗体抗原结合位点的抗体片段包括(但不限于)分子例如Fab、Fab’、Fab’-SH、scFv、Fv、dAb、Fd;和双特异抗体。
在本领域中,众所周知生成用于在生物传感器系统中使用的传感表面的方法。例如,在US 5492840和US 5242828中,陈述这样的方法的多个示例,通过引用而将这些专利的内容合并于本文中。
虽然在随后的详述和实施例中,在SPR光谱(且更具体地,BIACORE®系统)的背景下说明了本发明,但要理解到,本发明不限于该检测方法。而是,可以采用其中分析物与固定化于传感表面上的配体结合的任何基于亲和力的检测方法,只要能够测量在数量上指示分析物与固定化于传感表面上的配体的结合的传感表面处的改变。
众所周知SPR的现象,不用多说,当在不同的折射率的两种介质之间的分界面处,在一定的条件下反射光时,出现SPR,并且,分界面被金属膜(典型地,银或金)覆盖。在BIACORE®仪器中,介质为样品和传感器芯片的玻璃,玻璃通过微流控流动系统而与样品接触。金属膜是芯片表面上的薄层的金。SPR导致以特定反射角反射的光的强度降低。这一最小的反射光强度的角随着接近于与反射光相对的一侧(在BIACORE®系统中,为样品侧)的表面的折射率而变化。
在图1中,示出BIACORE®系统的示意图示。传感器芯片1具有支撑捕获分子(配体)3(例如,抗体)的金膜2,金膜2暴露于通过流动通道5的带有分析物4(例如,抗原)的样品流。来自光源7(LED)的单色p偏振光6通过棱镜8而与玻璃/金属分界面9耦合,在玻璃/金属分界面9处,光被全反射。反射的光束10的强度由光学检测单元11(光电检测器阵列)检测。
可以在美国专利号5313264中找到BIACORE®仪器的技术方面和SPR的现象的详细讨论。例如,在美国专利号5242828和5436161中,给出关于用于生物传感器的传感表面的基质涂层的更详细的信息。另外,可以在美国专利号5492840中找到结合BIACORE®仪器而使用的生物传感器芯片的技术方面的详细讨论。
当样品中的分子与传感器芯片表面上的捕获分子结合时,浓度改变,且因此,表面处的折射率改变,并且,检测到SPR响应。相互作用的过程期间响应对比时间的作图将提供相互作用的进程的定量测量。这样的图或动力或结合曲线(结合等温线)一般被称为传感图,在本领域中,有时也被称为“亲和力轨迹”或“亲和力图”。在BIACORE®系统中,SPR响应值以共振单位(RU)表示。1 RU表示最小的反射光强度的角的0.0001º的改变,对于大部分的蛋白及其他生物分子,这一改变与传感器表面上的大约1 pg/mm2的浓度的改变相对应。在被称为“缔合”的步骤中,当含有分析物的样品接触传感器表面时,与传感器表面结合的捕获分子(配体)与分析物相互作用。在传感图上通过在样品与传感器表面初步接触时的RU的增加指示该步骤。相反地,通常,当样品流被例如缓冲液流所替换时,发生“离解”。在传感图上通过当分析物从表面结合的配体离解时随着时间的推移的RU的降低指示该步骤。
在图2中呈现传感器芯片表面处的可逆的相互作用的具有代表性的传感图(结合曲线),传感表面具有与样品中的结合配偶体(因此,或分析物)相互作用的固定化的捕获分子或配体(例如,抗体)。基于在上文中提到的其他的检测原理的由生物传感器系统产生的结合曲线将具有类似的表现。竖直轴(y轴)指示响应(在此,以共振单位RU为单位),并且,水平轴(x轴)指示时间(在此,以秒钟为单位)。首先,缓冲液经过传感表面,在传感图中,显示出基线响应A。在样品注入的期间,由于分析物的结合而观察到信号的增强。结合曲线的该部分B一般被称为“缔合相”。最后,在缔合相结束时或临近结束时,达到稳态条件,其中在C处,共振信号达到平稳状态(然而,可能不总是实现该状态)。要注意到,在本文中,术语“稳态”与术语“平衡”同义地使用(在其他背景下,可以保留术语“平衡”,以描述理想的相互作用模型,因为,实际上,即使系统不处于平衡,结合也可能随着时间的推移而恒定)。在样品注入结束时,以缓冲液的连续流取代样品,并且,信号的减弱反映出分析物从表面离解或释放。结合曲线的该部分D一般被称为“离解相”。分析以再生步骤结束,在再生步骤中,将溶液注入传感器表面上,其中,该溶液能够在(理想地)维持配体的活性的同时,从表面去除结合的分析物。这在传感图的部分E中指示。然而,在已经完成离解或在下一次分析之前,预期完成离解的情况下,能够避免再生,这具有增强配体保存且减少操作的次数的优点。缓冲液的注入恢复基线A,并且,现在,表面准备好进行新的分析。
分别从缔合相B和离解相D的分布图获得关于结合动力和离解动力的信息,并且,C处的共振信号的高度表示亲和力(起因于与表面上的质量浓度的改变有关的相互作用而导致的响应)。在US2012/0244637 A1中,公开了用于确定诸如表面结合速率、动力速率常数ka和kd、亲和力常数(缔合常数KA和离解常数KD)之类的参数及其他参数的方法的详细解释。
在市场上可买到用于分析动力和亲和力数据的软件。因而,例如,一般利用专用的BIA评价软件(由Biacore AB, Uppsala, Sweden提供)来执行对BIACORE®仪器所产生的动力及亲和力数据的评价,BIA评价软件使用数值积分来计算微分速率方程和非线性回归,从而通过查找赋予最接近的拟合的变量的值而拟合动力和亲和力参数,导致平方残差的和降低至最小值。
利用BIA评价软件,根据所测量到的稳态结合水平而确定亲和力常数可以例如包括以下的步骤:
(i)在曲线的稳态区域中,根据传感图上的报告点而获得稳态结合水平(Req,平衡时的响应);
(ii)创建随着C而变化的Req的图,其中,C是溶液中的游离的分析物的初始或体积浓度;以及
(iii)使该图与一般的“稳态亲和力”拟合模型拟合,以获得KA/KD和Rmax(其中,Rmax为在分析物已与表面上的所有的配体结合的情况下获得的以RU为单位的响应,也被称为饱和响应)。
接触时间
根据本发明的第一方面,样品溶液与固定化的配体之间的接触时间不到15秒钟。在本领域中,众所周知术语“接触时间”,并且,如本文中所使用的,术语“接触时间”意指样品溶液流过配体结合的传感器表面的任一个固定点所耗费的总时间。例如,能够从检测表面的第一部分被样品溶液接触时的开始时间至表面的第一部分与随后的缓冲液溶液接触时的停止时间确定该时间。
生物传感器装置(诸如,但不限于,BIACORE®系统)许可用户设置优选的接触时间。例如,通过指定具体的接触时间和流动速率,PC软件能够计算适当的样品体积,然后经由仪器软件以所指定的流动速率执行体积。例如,如果接触时间设置于2秒钟,并且,流动速率设置于60 μl/min,则能够采用样品体积60/60 x 2 = 2 μl。
本申请证实,有可能在显著地缩短包含分析物的溶液与配体之间的接触时间的同时,提供有意义的涉及表面结合的配体和分析物的结合的结合数据。如前所述,在本领域中,标准的做法是,采用长的注入或接触时间(典型地,超过30秒钟),以确保高而稳定的响应值。然而,本发明的发明者已识别出,显著地缩短接触时间仍然产生有用且可重复的信息。例如,接触时间可以少于15秒钟、少于14秒钟、少于13秒钟、少于12秒钟、少于11秒钟、少于10秒钟、少于9秒钟、少于8秒钟、少于7秒钟、少于6秒钟、少于5秒钟、少于4秒钟、少于3秒钟、少于2秒钟或少于1秒钟。接触时间可以在15秒钟至2秒钟、14秒钟至2秒钟、13秒钟至2秒钟、12秒钟至2秒钟、11秒钟至2秒钟、10秒钟至2秒钟、9秒钟至2秒钟、8秒钟至2秒钟、7秒钟至2秒钟、6秒钟至2秒钟、5秒钟至2秒钟、4秒钟至2秒钟、3秒钟至2秒钟或大约2秒钟的范围内。接触时间可以在3秒钟至0.1秒钟、3秒钟至0.2秒钟、3秒钟至0.3秒钟、3秒钟至0.4秒钟、3秒钟至0.5秒钟、3秒钟至0.6秒钟、3秒钟至0.7秒钟、3秒钟至0.8秒钟、3秒钟至0.9秒钟、3秒钟至1秒钟的范围内。接触时间的下限可以是0.1秒钟、0.2秒钟、0.3秒钟、0.4秒钟、0.5秒钟、0.6秒钟、0.7秒钟、0.8秒钟、0.9秒钟、0.1秒钟、1秒钟、1.1秒钟、1.2秒钟、1.3秒钟、1.4秒钟、1.5秒钟、1.6秒钟、1.7秒钟、1.8秒钟、1.9秒钟或2秒钟。
在根据本发明的方法中能够使用显著地如此短的接触时间这一发现提供分析物分析的领域(例如,药物开发的多方面,包括抗体筛选和基于片段的筛选(在下文中更详细地描述))中的显著的优点。例如,接触时间的缩短可能导致更快的结果,并且,能够通过缩短循环时间而显著地增强生产能力。
在另一实施方案中,继步骤(c)之后,使第二样品溶液流过表面,以检测配体与另一分析物之间的结合的存在与否,在同一表面上,重复步骤(b)和(c)。另一分析物可以与第一分析物相同。备选地,另一分析物可以与第一分析物不同。然后,可以针对第三样品溶液而重复步骤(b)和(c)。在另一实施方案中,将步骤(b)和(c)重复至少两次、三次、四次、五次、六次、七次、八次、九次、十次、十一次、十二次、十三次、十四次、十五次、十六次、十七次、十八次、十九次或二十次,以测定相对应的数量的另外的溶液。
在另一实施方案中,开始使至少一个样品溶液流过(例如,注入)传感器表面与开始使下一个相继的样品溶液流过传感器表面之间的时间(循环时间)不到40秒钟。在另一实施方案中,循环时间不到30秒钟。在另一实施方案中,循环时间不到20秒钟。在另一实施方案中,循环时间不到15秒钟。在另一实施方案中,循环时间不到10秒钟。在另一实施方案中,循环时间在10秒钟至40秒钟的范围内,优选地,在10秒钟至30秒钟的范围内。
在另一实施方案中,开始使每个样品溶液流过(例如,注入)传感器表面与开始使下一个相继的样品溶液流过传感器表面之间的时间(循环时间)不到40秒钟。在另一实施方案中,每个循环时间不到30秒钟。在另一实施方案中,每个循环时间不到20秒钟。在另一实施方案中,每个循环时间不到15秒钟。在另一实施方案中,每个循环时间不到10秒钟。在另一实施方案中,每个循环时间在10秒钟至40秒钟的范围内,优选地,在10秒钟至30秒钟的范围内。
通过排除典型地在基于生物传感器的分析物结合技术中采用的更耗时的措施(例如,冲洗流控系统、携带控制和/或再生),能够进一步缩短分析物溶液之间的循环时间。如在本申请的实施例中所表明的,不采用这样的冲洗、携带控制或再生步骤,针对多个分析物结合循环获得有用且可重复的结合数据。
典型地,实行冲洗步骤,以确保不存在粘在流控系统上的剩余的分析物,这样的分析物可能促成结合数据中的干扰。
携带控制是经施行以处理如下的事实的典型步骤:某些分析物“较粘”,且可能难以从流控系统洗掉,导致将材料“携带”至下一个分析循环。这能够通过常规地包括样品注入之后的缓冲液的“携带注入”而检测:来自“较粘的”化合物的响应将被携带至该缓冲液注入中。因而,携带控制注入能够监测来自流控系统的污染的响应贡献。
再生是如下的过程:在新的循环的制备中,在分析循环之后,从表面去除结合的分析物,而不损伤配体。在本领域中,众所周知再生技术,并且,所采用的特定方法可以取决于所采用的配体和/或分析物而变化。对于使用定制的抗体来进行的测定开发,以低的pH(甘氨酸-HCl,pH 1.5至3)进行的再生通常为有效的。
在本发明的一个实施方案中,在开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间,不实行冲洗步骤。
在一个实施方案中,在开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间,不实行携带控制注入步骤。
在一个实施方案中,在开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间,不实行再生步骤。
在一个实施方案中,在开始使至少一个样品溶液流过传感器表面与开始使下一个相继的样品溶液流过传感器表面之间,不实行再生步骤和携带控制和/或系统冲洗步骤。
在一个实施方案中,在开始使第一样品溶液流过传感器表面与开始使每个随后的样品溶液流过传感器表面之间,不实行再生步骤和/或携带控制和/或系统冲洗步骤。
能够通过采用高密度的固定化的配体而增强短的接触时间的使用且避免应用再生步骤。高密度的配体能够使能够接触配体的分析物的量最大化,这可能在接触时间(且因此,可用于结合的时间)短的情况下特别有利,因而确保良好的水平的配体分析物结合。此外,通过与短的接触时间组合而采用高密度的配体,仅一小部分的传感器容量(可用于分析物的结合位点)用于每个分析物注入,从而规避再生的要求。
在本发明的实施方案中,传感器表面上的配体密度为至多50000 RU。在另一实施方案中,传感器表面上的配体密度在5000 RU至15000 RU的范围内。在固定化的配体为抗体的情况下,这些数量特别地优选。考虑到抗体的典型的近似的分子量为150000 g/摩尔,对于具有分子量X的其他分子,必须如下计算固定化水平:
然而,配体密度的选择还可能取决于分析物,且具体地,配体与分析物的分子量比。
在另一实施方案中,步骤(c)包含确定样品溶液中的分析物浓度。在另一实施方案中,步骤(c)包含确定分析物对配体的亲和力(例如,结合常数)。
然而,如上所述的短的接触时间和/或短的循环时间的使用意味着,在需要在短的或更易于管理的时段期间,针对配体结合而对大量的样品分析物溶液进行测定的方法中,本方法特别有利。以这种方式,用户能够例如迅速地确定给定的样品溶液中的分析物的存在与否,或例如,确定不同的样品溶液之间的分析物浓度和/或分析物亲和力的定性或定量的差异。例如,响应的水平能够用于得出关于抗体的相对亲和力和/或抗体的浓度的结论。
在本发明的优选的实施方案中,配体或分析物是抗体或其片段。例如,配体可以是抗体,并且,分析物可以是能够(或被认为是潜在地能够)与抗体结合的分子。备选地,配体可以是能够与靶抗体(例如,抗原)结合的分子,并且,分析物溶液可以包含能够结合配体(或为了测试其结合配体的能力)的候选抗体。以这种方式,可以在抗体筛选程序(例如,初步筛选)中采用本发明的方法,从而针对与靶抗原(配体)结合的能力而测试不同的杂交瘤(存在于例如384孔板上)。在本发明的测定中显示结合(通过响应信号的增加)的那些能够被识别为产生结合靶抗原的抗体。此外,响应的水平能够用于得出关于抗体的相对亲和力和/或抗体的浓度的结论。
本发明的方法还能够在基于片段的筛选中有利地采用,以识别非特异性的结合剂或聚集体。基于片段的药物开发是用于开发针对例如靶蛋白的高亲和力的结合剂的强有力的方法。虽然对于指定为“片段”的化合物,不存在严格的尺寸要求,但该术语通常用于具有小于大约25重原子或小于300 Da的分子量的小的有机分子。然而,在开始基于片段的筛选之前,去除可能行为失常的片段是重要的,因为,这样的分子的存在可能使筛选结果模糊或干扰筛选结果。这样的筛选有时被称为“彻底筛选”,并且,是片段筛选活动中的推荐的第一步骤。这样的“行为失常的”分子能够包括非特异性的结合剂、螯合剂或聚集体。选出这样的行为失常的分子可能是一项富有挑战性的任务,因为,在筛选之前,并非所有的这样的化合物都是已知的。然而,本发明的方法能够用于有效地针对这样的行为失常的分子而“预先筛选”片段库。能够通过监测与分子的结合相关联的信号而识别这些分子。例如,这样的分子将由于起因于不需要的结合相互作用而导致的缓慢离解而可识别。于是,本发明的方法可以进一步用于筛选优化的基于片段的库。
根据本发明的第二方面,提供计算机程序,该计算机程序包含程序代码手段,该程序代码手段用于使传感器装置运行,从而根据包含以下的步骤的方法而在传感器表面上检测分析物与配体之间的相互作用:(a)提供传感器表面,该传感器表面具有固定化于该传感器表面的配体;
(b)使样品溶液流过传感器表面;以及(c)在传感器表面上检测分析物与配体的结合的存在与否;其中,样品溶液与固定化的配体之间的接触时间不到15秒钟;并且,其中,在计算机上运行程序。该方法可以具有在上文中关于本发明的第一方面而描述的任何实施方案中所描述的特征。
现在,将参考以下的非限制性的实施例而描述本发明。
实施例
超高的生物传感器生产能力
1. 利用10 mM醋酸盐pH 5.0来将来自GE Healthcare的配体抗β2µ从1 mg/ml的储备溶液稀释至30 µg/ml。
2. 配体为使用来自GE Healthcare的胺偶联试剂盒中的试剂通过BIACORE T200系统中的预编程序的设置而与传感器芯片CM7偶联的胺。注入配体溶液达7分钟,导致43319RU的固定化水平。运行缓冲液:来自GE Healthcare的HBS-EP+。
3. 利用运行缓冲液将来自GE Healthcare的分析物β2µ储备液从100 µg/ml稀释至1600 ng/ml,且然后,进一步稀释至800、400、200和100 ng/ml。
4. 将每个分析物浓度注入10次,接触时间2 s,流动速率60 µl/分钟,从低浓度变成高浓度。在不同的浓度之间,通过将来自GE Healthcare的10 mM甘氨酸pH 2.5注入达30s而再生芯片。
在图3和图4中,示出上文中的实验的结果。这些图表明,2秒钟的注入时间足以检测下降到至少100 ng/ml的样品中的蛋白结合剂。
图3显示随循环次数而变化的注入之后的响应,表明针对分析物的每个浓度,响应在多个循环之间是可重现的,并且,相对响应反映出分析物的浓度增加。图4显示在未将命令加到注入时,随着循环时间而变化的对应的传感图。数据证实,极短的接触时间能够产生高度地有用且可重复的信息。
图5是示出对于给定循环的各种时间下带有4针系统的384孔板上的所计算出的总实验时间的信息图。如果采用仅2秒钟的接触时间,并且,避免所有的其他命令,则能够显著地缩短样品时间。例如,12秒钟的循环时间将允许4针系统在少于20分钟(96 x 12s)内运行384板。
Claims (23)
1.一种针对第一分析物的存在而测定样品溶液的方法,包括:
(a)提供传感器表面,该传感器表面具有固定化于该传感器表面的配体,其中所述传感器表面上的配体密度为至多50000 RU;
(b)使所述样品溶液流过所述传感器表面;以及
(c)在所述传感器表面上检测所述分析物与所述配体的结合的存在与否;
其中,所述样品溶液与所述固定化的配体之间的接触时间不到15秒钟,
其中在步骤(c)之后,通过使第二样品溶液流过所述表面,以检测配体与另一分析物之间的结合的存在与否,来重复步骤(b)和(c),
和其中开始使至少一个所述样品溶液流过所述传感器表面与开始使下一个相继的样品溶液流过所述传感器表面之间的时间不到40秒钟。
2.如权利要求1所述的方法,其中,所述接触时间不到10秒钟。
3.如权利要求1所述的方法,其中,所述接触时间不到5秒钟。
4.如权利要求1所述的方法,其中,所述接触时间不到3秒钟。
5.如权利要求1所述的方法,其中,所述接触时间不到2秒钟。
6.如前述权利要求中的任一项所述的方法,其中,所述传感器表面处的检测基于倏逝波传感。
7.如权利要求1至5中的任一项所述的方法,其中,所述传感器表面处的检测基于表面等离子体共振(SPR)。
8.如权利要求1所述的方法,其中,所述另一分析物与所述第一分析物相同。
9.如权利要求1所述的方法,其中,所述另一分析物与所述第一分析物不同。
10.如权利要求1至5中的任一项所述的方法,其中,针对第三样品溶液而重复步骤(b)和(c)。
11.如权利要求1所述的方法,其中,将步骤(b)和(c)重复至少十次,以测定至少十种另外的溶液。
12.如权利要求1所述的方法,其中,开始使至少一个所述样品溶液流过所述传感器表面与开始使下一个相继的样品溶液流过所述传感器表面之间的时间不到15秒钟。
13.如权利要求1至5中的任一项所述的方法,其中,在开始使至少一个所述样品溶液流过所述传感器表面与开始使下一个相继的样品溶液流过所述传感器表面之间,不实行再生步骤。
14.如权利要求1至5中的任一项所述的方法,其中,在开始使至少一个所述样品溶液流过所述传感器表面与开始使下一个相继的样品溶液流过所述传感器表面之间,不实行冲洗步骤和/或携带控制注入步骤。
15.如权利要求1至5中的任一项所述的方法,其中,所述传感器表面上的配体密度在5000 RU至15000 RU的范围内。
16.如权利要求1至5中的任一项所述的方法,其中,步骤(c)包括确定所述样品溶液中的分析物浓度。
17.如权利要求1至5中的任一项所述的方法,其中,步骤(c)包括确定分析物对所述配体的亲和力。
18.如权利要求1至5中的任一项所述的方法,包括确定不同的样品溶液之间的分析物浓度和/或分析物亲和力的差异。
19.如权利要求1至5中的任一项所述的方法,其中,所述配体或分析物是抗体或其片段。
20.如权利要求1至5中的任一项所述的方法,其中,所述方法用于筛选抗体。
21.如权利要求1至5中的任一项所述的方法,其中,所述方法用作基于片段的筛选,以鉴定非特异性的结合剂或聚集体。
22.如权利要求1至5中的任一项所述的方法,其中,所述方法用作基于片段的筛选,以鉴定针对所述配体的特异性的结合剂。
23.一种计算机可读介质,具有存储在其上的计算机程序,所述计算机程序包含程序代码手段,该程序代码手段用于当在计算机上运行所述程序时,使传感器装置运行,从而根据如权利要求1至18中的任一项所述的方法而在传感器表面上检测分析物与配体之间的相互作用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SE1451456 | 2014-11-28 | ||
| SE1451456-6 | 2014-11-28 | ||
| PCT/EP2015/077568 WO2016083417A1 (en) | 2014-11-28 | 2015-11-24 | Method for determining analyte-ligand binding on a sensor surface |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN107430123A CN107430123A (zh) | 2017-12-01 |
| CN107430123B true CN107430123B (zh) | 2020-04-14 |
Family
ID=54754613
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201580074734.7A Active CN107430123B (zh) | 2014-11-28 | 2015-11-24 | 用于在传感器表面上检测分析物-配体结合的方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US10725030B2 (zh) |
| EP (1) | EP3224622B1 (zh) |
| JP (3) | JP2017535783A (zh) |
| CN (1) | CN107430123B (zh) |
| WO (1) | WO2016083417A1 (zh) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020028396A1 (en) * | 2018-07-30 | 2020-02-06 | Georgetown University | Chirality sensing with molecular click chemistry probes |
| WO2020056012A1 (en) | 2018-09-11 | 2020-03-19 | Georgetown University | Quantitative auxiliary-free chirality sensing with a metal probe |
| EP3969910A1 (en) * | 2019-05-17 | 2022-03-23 | Creoptix AG | Methods for determining kinetic parameters of a reaction between analyte and ligands |
| DE102020107645A1 (de) * | 2020-03-19 | 2021-09-23 | Bruker Daltonics GmbH & Co. KG | Betrieb einer Mikrofluidik-Vorrichtung bei der Analyse von Probesubstanzen |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996009532A1 (en) * | 1994-09-22 | 1996-03-28 | Abbott Laboratories | Optical waveguide method for detecting specific binding events by light scattering |
| WO2004109284A1 (en) * | 2003-06-06 | 2004-12-16 | Biacore Ab | Method and system for determination of molecular interaction parameters |
| CN101743465A (zh) * | 2007-04-19 | 2010-06-16 | Sru生物系统公司 | 应用生物传感器检测与固定化靶标分子直接结合的小分子的方法 |
| CN102652259A (zh) * | 2010-03-12 | 2012-08-29 | 小利兰·斯坦福大学托管委员会 | 基于磁性传感器的定量结合动力学分析 |
| CN102667448A (zh) * | 2009-11-30 | 2012-09-12 | 通用电气健康护理生物科学股份公司 | 用于相互作用分析的方法和系统 |
| CN103748467A (zh) * | 2011-05-11 | 2014-04-23 | Ssens有限责任公司 | 用于测定分析物与配体的固有结合参数的方法、用于从一群分析物中选择分析物的方法、所选择的配体或分析物及传感器 |
| EP2770058A1 (en) * | 2013-02-26 | 2014-08-27 | Université de Perpignan | Ligand and method for detection of okadaic acid |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9816441D0 (en) | 1998-07-28 | 1998-09-23 | Hartley Frank R | Analysis of liquids |
| WO2003091706A1 (fr) * | 2002-04-24 | 2003-11-06 | Hitachi, Ltd. | Microreacteur pour reaction d'interface solide-liquide et procede de realisation de mesure concernant la reaction d'interface solide-liquide |
| JP2004251807A (ja) | 2003-02-21 | 2004-09-09 | Nipro Corp | エンドトキシン測定用センサ、測定方法、診断方法、製造方法およびセンサ再生方法 |
| WO2004092840A1 (ja) | 2003-04-17 | 2004-10-28 | Nissan Chemical Industries, Ltd. | 多孔質下層膜及び多孔質下層膜を形成するための下層膜形成組成物 |
| MX343228B (es) * | 2009-11-30 | 2016-10-26 | Biotest Ag | Anticuerpos anti-il-10humanizados para el tratamiento de lupus sistémico eritematoso. |
| US9447193B2 (en) | 2013-03-24 | 2016-09-20 | Development Center For Biotechnology | Methods for suppressing cancer by inhibition of TMCC3 |
-
2015
- 2015-11-24 EP EP15802025.5A patent/EP3224622B1/en active Active
- 2015-11-24 WO PCT/EP2015/077568 patent/WO2016083417A1/en active Application Filing
- 2015-11-24 CN CN201580074734.7A patent/CN107430123B/zh active Active
- 2015-11-24 JP JP2017528219A patent/JP2017535783A/ja active Pending
- 2015-11-24 US US15/529,466 patent/US10725030B2/en active Active
-
2020
- 2020-07-17 US US16/932,453 patent/US11796536B2/en active Active
- 2020-11-18 JP JP2020191572A patent/JP7345790B2/ja active Active
-
2022
- 2022-08-18 JP JP2022130703A patent/JP7456653B2/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996009532A1 (en) * | 1994-09-22 | 1996-03-28 | Abbott Laboratories | Optical waveguide method for detecting specific binding events by light scattering |
| WO2004109284A1 (en) * | 2003-06-06 | 2004-12-16 | Biacore Ab | Method and system for determination of molecular interaction parameters |
| CN101743465A (zh) * | 2007-04-19 | 2010-06-16 | Sru生物系统公司 | 应用生物传感器检测与固定化靶标分子直接结合的小分子的方法 |
| CN102667448A (zh) * | 2009-11-30 | 2012-09-12 | 通用电气健康护理生物科学股份公司 | 用于相互作用分析的方法和系统 |
| CN102652259A (zh) * | 2010-03-12 | 2012-08-29 | 小利兰·斯坦福大学托管委员会 | 基于磁性传感器的定量结合动力学分析 |
| CN103748467A (zh) * | 2011-05-11 | 2014-04-23 | Ssens有限责任公司 | 用于测定分析物与配体的固有结合参数的方法、用于从一群分析物中选择分析物的方法、所选择的配体或分析物及传感器 |
| EP2770058A1 (en) * | 2013-02-26 | 2014-08-27 | Université de Perpignan | Ligand and method for detection of okadaic acid |
Non-Patent Citations (5)
| Title |
|---|
| Analysis of Fibril Elongation Using Surface Plasmon Resonance Biosensors;DAVID G. MYSZKA et al.;《METHODS IN ENZYMOLOGY》;19991231;第309卷;第386页引言部分,第387页第4段,第388页第4-6段,391页第3段,第392页第5段,第394页第1段,第398页第5段,图1-2 * |
| Chip-Based Protein–Protein Interaction Studied by Atomic Force Microscopy;Feng-Sheng Kao et al.;《Biotechnology and Bioengineering》;20121031;第109卷(第10期);摘要 * |
| From Experimental Design to Validated Hits: A Comprehensive Walk-Through of Fragment Lead Identification Using Surface Plasmon Resonance;Anthony M. Giannetti;《Methods in Enzymology》;20111231;第493卷;全文 * |
| Langmuir-Blodgeet Composite Films for the Selective Determination of Calcium in Aqueous Solutions;M.A.Kalinina et al.;《Russian Journal of Physical Chemistry A》;20080831;第82卷(第8期);摘要,第1336页左栏第2段、第5-6段 * |
| Quantitative Analysis of Mitoxantrone by Surface-Enhanced Resonance Raman Scattering;Clare McLaughlin et al.;《Anal. Chem.》;20020701;第74卷(第13期);摘要 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3224622A1 (en) | 2017-10-04 |
| JP7456653B2 (ja) | 2024-03-27 |
| US11796536B2 (en) | 2023-10-24 |
| CN107430123A (zh) | 2017-12-01 |
| US10725030B2 (en) | 2020-07-28 |
| JP2017535783A (ja) | 2017-11-30 |
| US20200348295A1 (en) | 2020-11-05 |
| JP7345790B2 (ja) | 2023-09-19 |
| JP2022171673A (ja) | 2022-11-11 |
| WO2016083417A1 (en) | 2016-06-02 |
| EP3224622B1 (en) | 2019-08-07 |
| US20170261502A1 (en) | 2017-09-14 |
| JP2021036245A (ja) | 2021-03-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210215613A1 (en) | Concentration assay | |
| US11796536B2 (en) | Method for determining analyte-ligand binding on a sensor surface | |
| JP5855246B2 (ja) | 校正不要分析による活性濃度の決定方法 | |
| WO2006135309A9 (en) | Method and system for affinity analysis | |
| DK2507618T3 (en) | Method and system for interaction analysis | |
| JP5714023B2 (ja) | 結合の挙動の分析のための方法及びシステム | |
| EP2726875A1 (en) | Method of determining active concentration | |
| JP2007506967A (ja) | 分子相互作用分析の方法及びシステム | |
| Nilvebrant | Kinetic analysis and epitope binning using surface plasmon resonance | |
| US20110152120A1 (en) | method of characterizing antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant | ||
| CP01 | Change in the name or title of a patent holder |
Address after: uppsala Patentee after: Stoivan Sweden Limited Address before: uppsala Patentee before: GE HEALTHCARE BIO-SCIENCES AB |
|
| CP01 | Change in the name or title of a patent holder |