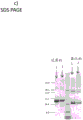CN106604929B - 新型过敏原 - Google Patents
新型过敏原 Download PDFInfo
- Publication number
- CN106604929B CN106604929B CN201580038584.4A CN201580038584A CN106604929B CN 106604929 B CN106604929 B CN 106604929B CN 201580038584 A CN201580038584 A CN 201580038584A CN 106604929 B CN106604929 B CN 106604929B
- Authority
- CN
- China
- Prior art keywords
- protein
- equ
- ige
- horse
- allergy
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/35—Allergens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6854—Immunoglobulins
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Organic Chemistry (AREA)
- Urology & Nephrology (AREA)
- Biochemistry (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Microbiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Biotechnology (AREA)
- General Physics & Mathematics (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Pathology (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pulmonology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本发明涉及由以下组成的新型马过敏原:具有第一肽链和第二肽链(其一起与SEQ ID NO:3和SEQ ID NO:4的组合序列具有至少70%的总体序列同一性)的异源二聚蛋白,以及与根据SEQ ID NO:3和SEQ ID NO:4的组合氨基酸序列具有至少70%、诸如75%、80%、85%、90%、95%或98%的总体序列同一性的单链蛋白。本发明还涉及所述蛋白在I型过敏的诊断和治疗方法中的用途,以及用于此类方法中的试剂盒和组合物。
Description
发明领域
本发明涉及过敏的领域。更具体地,本发明涉及鉴定来自哺乳动物的新型过敏原以及诊断和治疗对哺乳动物的过敏。
背景
工业化世界的约20%的人群在暴露于来自各种环境来源的抗原后变得超敏(过敏)。诱导立即和/或延迟型超敏反应的那些抗原被称为过敏原(Breiteneder, Hoffmann-Sommergruber等人,1997)。这些包括草、树、杂草、动物皮屑、昆虫、食物、药物和化学品的产物。参与特应性过敏的抗体主要属于免疫球蛋白E同种型(IgE)。IgE经由特异性高亲和力受体FcεRI与嗜碱性粒细胞肥大细胞和树突状细胞结合。在暴露于过敏原后,细胞表面上的过敏原特异性IgE抗体发生交联,导致炎性介体诸如组胺和白三烯的释放,导致过敏的生理表现(Akdis 2006)。
过敏的诊断测试涉及检测对来自过敏原来源的蛋白具有特异性的患者的IgE抗体。然而,阳性IgE测试,即IgE致敏,并不总是导致过敏的临床表现,并且该差异是试图开发新的和更好的诊断程序的主要原因之一。在典型测试中,这些测试中使用来自过敏原来源的含有蛋白混合物的含水提取物。对于大多数过敏原来源,仅部分地鉴定和表征存在于粗提取物中的过敏原蛋白。用于检测患者中的特异性IgE抗体的诊断测试程序可以利用使用来自患者的血清的体外免疫测定,或者是通过将特定提取物局部施用于患者皮肤上进行的皮肤点刺试验(SPT)(Wainstein,Yee等人 2007)。在临床实践中,医生对过敏的诊断通常基于对相关过敏原来源的IgE致敏的阳性测试和对该过敏原的过敏反应的令人信服的临床史。
近年来,已经鉴定和表征了过敏原提取物中的许多重要的过敏原蛋白。这已经使得能够对针对这些个别过敏组分中的每者的特异性IgE抗体进行定量,通常被称为组分分辨的诊断(CRD)(Hiller,Laffer等人,2002)(Valenta,Lidholm等人,1999)或基于分子的过敏(MA)诊断(Canonica,Ansotegui等人,2013)。
现在广泛认识到,与使用过敏原提取物的常规IgE分析(Canonica,Ansotegui等人,2013)相比,基于分子的过敏(MA)诊断具有几个明显优点。来自过敏原来源的所有相关过敏原组分的分析已经显示显著增加IgE测试的临床效用,如小麦、花生和榛子所例举。(Nicolaou, Poorafshar等人,2010;Codreanu, Collignon等人,2011;Ebisawa, Moverare等人,2012) (Masthoff, Mattsson等人,2013)。如果可以应用MA,则必要条件是已经鉴定和表征了来自过敏原来源的大部分单独过敏原组分。
MA诊断的最重要意义之一是区分真正的IgE致敏与由于交叉反应性导致的致敏,这可以帮助临床医生确定单个、几个紧密相关或几个广泛不同的过敏原来源是否导致过敏症状。这可以导致改进对花粉(Stumvoll, Westritschnig等人,2003)、毒液(Müller,Schmid-Grendelmeier等人,2012)超敏和食物过敏(Matsuo, Dahlstrom等人,2008;Ebisawa, Shibata等人,2012)的诊断。具体而言,对于花生和榛子过敏,使用过敏原组分IgE测试在预测过敏的临床结果方面比使用经典提取物IgE测试更好(Nicolaou,Poorafshar等人,2010;Codreanu, Collignon等人,2011;Masthoff, Mattsson等人,2013)。其中一个原因是一些组分可能是低丰度的,因此仅表明由于与来自其它物种的同源组分的交叉反应性导致的IgE反应性。因此,对此类交叉反应性组分仅具有IgE反应性的个体不太可能具有对该过敏原的临床症状(Asarnoj, Moverare等人,2010;Asarnoj,Nilsson等人,2012)。尽管其临床相关性低,但在过敏原提取物中鉴定所有那些低丰度的交叉反应性组分是非常重要的,因为在患者的临床检查中,重要的是对所有组分的IgE反应性的总和合计等于对整个提取物的IgE反应性的总和,以便排除对提取物中其它次要或未知组分的IgE反应性。因此,MA诊断的结果可以导致最佳免疫疗法治疗的改进选择和不同食物过敏的更好风险评价。
过敏原组分的另一种用途是使用这些以通过用组分掺入提取物来提高提取物的诊断灵敏度。这在小型化或非实验室免疫测定法诸如过敏原微阵列或医生办公室测试(其中不太有利的测定条件、抗体结合过敏原试剂的能力较低和效力有限的天然过敏原提取物的组合可以引起诊断灵敏度不足)中是特别重要的。
总之,因此,鉴定和表征每种过敏原来源中的所有重要过敏原蛋白是非常重要的。
过敏的治疗最经常是通过例如抗组胺剂减少过敏的症状,但过敏的更长期和治疗性治疗可以用特异性免疫疗法进行。应用引起疾病的过敏原提取物(最通常皮下或舌下),其引起对过敏原蛋白的保护性免疫应答的特异性激活。尽管确切机制尚不完全清楚,但此类免疫系统的特异性激活减轻了相同过敏原的随后环境暴露后过敏的症状(Akdis和Akdis2007)。常规免疫疗法的进一步开发是使用一种或几种纯化的过敏原蛋白替代粗天然提取物。已经成功地对草花粉过敏患者进行了此类免疫疗法(Jutel, Jaeger等人,2005)(Cromwell, Fiebig等人,2006) (Saarne, Kaiser等人,2005),并且还建议其用于治疗针对动物皮屑的过敏(Valenta, Lidholm等人,1999;Gronlund, Saarne等人,2009)。
近年来,对过敏原特异性IgG抗体的关注日益增加。这些可直接通过充当过敏原上的阻断抗体或间接通过经由Fc受体作用而直接调节IgE抗体的作用(Akdis和Akdis 2007;Uermosi,Beerli等人,2010; Uermosi, Zabel等人,2014)。
因此,相比仅测量IgE应答,通过评价对过敏原的特异性IgE和特异性IgG应答可能更具临床上相关性(Custovic, Soderstrom等人,2011; Caubet, Bencharitiwong等人,2012; Du Toit, Roberts等人,2015)。众所周知的是,免疫疗法诱导主要由IgG4亚类组成的特异性IgG应答。由于该抗体应答是成功免疫疗法的机制的一部分(Uermosi, Beerli等人,2010;Uermosi, Zabel等人,2014),过敏原特异性IgG抗体的分析可以是监测治疗效力的方式。
总之,测量过敏原特异性IgG水平可以反映通过环境暴露或免疫疗法治疗对过敏原的天然或诱导的耐受性,并且可以与IgE水平组合提高诊断测试的临床相关性。
马皮屑是呼吸道过敏的一种日渐普遍的原因(Liccardi,D'Amato等人,2011),其中症状包括鼻炎、结膜炎、支气管炎症和哮喘。职业性暴露于马过敏原是过敏性致敏的重要风险因素(Tutluoglu, Atis等人,2002),但在其它地方诸如学校也可以检测到相当浓度的过敏原(Kim, Elfman等人,2005)。在一项研究中显示,对马皮屑的IgE致敏与发生哮喘的高风险相关(Ronmark, Perzanowski等人,2003)。
马毛和皮屑的提取物含有复杂的过敏原蛋白,并且迄今已经鉴定了4种马过敏原:Equ c 1、Equ c 2、Equ c 3和Equ c 4。前两者都是脂质运载蛋白家族的成员,并且已从其天然来源纯化(Dandeu, Rabillon等人,1993;Goubran Botros, Rabillon等人,1998),而仅Equ c 1已被表达为重组蛋白(Gregoire, Rosinski-Chupin等人,1996)。Equ c 1的氨基酸序列与猫过敏原Fel d 4的氨基酸序列67%相似(Smith,Butler等人,2004)。Equ c 3,马血清白蛋白,是一种相对保守的蛋白,其显示与其它哺乳动物白蛋白广泛的交叉反应性(Goubran Botros, Gregoire等人,1996)。Equ c 4首先被纯化(Goubran Botros,Rabillon等人,1998; Goubran Botros, Poncet等人,2001),并且后来才被鉴定为马汗latherin(McDonald,Fleming等人,2009)。近来,已经表征了来自分泌球蛋白家族的C-D亚家族的新型马过敏原(Equ c 15k, WO2011/133105)。
Equ c 1被认为是已知马过敏原中最重要的一种(Dandeu,Rabillon等人,1993),并且重组蛋白的IgE抗体识别存在于所研究的马过敏个体的群体的76%中(Saarelainen,Rytkonen-Nissinen,等人2008)。在使用纯化的天然过敏原的另一项研究中,仅33%的马过敏患者被Equ c 2致敏,而23%的马过敏患者被Equ c 4致敏(Goubran Botros,Rabillon等人,1998)。已经在几项研究中探讨了IgE与马血清白蛋白结合的频率,表明在高达40%的马过敏性个体中的反应性(Spitzauer等人,1993;Cabañas等人,2000)。然而,由于对血清白蛋白的致敏通常伴有针对其它过敏原组分的更高浓度的IgE抗体,所以其特异性临床相关性是不确定的(Spitzauer, Schweiger等人,1993; Cabañas, López-Serrano等人,2000)。近来的研究证实了这些马过敏原组分的相对流行性,并且显示了对Equ c 15k具有IgE反应性的马过敏患者的48%的患病率。(WO2011/133105).
发明概述
通过使用不与任何已知的马过敏原组分反应的血清,纯化了新型马过敏原并鉴定为分泌球蛋白。使用N-末端测序和MALDI ToF MS部分鉴定序列。通过3’RACE验证完整氨基酸序列,且在大肠杆菌中产生重组单链蛋白,其具有与天然纯化蛋白类似的IgE反应性。还公开了过敏原在诊断和治疗中的用途,以及诊断试剂盒和含有所述过敏原的药物组合物。
在第一个方面,本发明涉及具有第一肽链和第二肽链的分离的异源二聚蛋白,所述第一肽链和第二肽链一起与SEQ ID NO:3和SEQ ID NO:4的组合序列具有至少70%,诸如75%、80%、85%、90%、95%或98%的总体序列同一性。
在另外的方面,本发明涉及单链蛋白,其与根据SEQ ID NO:3和SEQ ID NO:4的组合氨基酸序列具有至少70%,诸如75%、80%、85%、90%、95%或98%的总体序列同一性。
在另外的方面,本发明涉及分离蛋白,其与SEQ ID NO:3的序列具有至少70 %,诸如75%、80%、85%、90%、95%或98%的序列同一性。
在另外的方面,本发明涉及分离蛋白,其与SEQ ID NO:4的序列具有至少70 %,诸如75%、80%、85%、90%、95%或98%的序列同一性。
在另外的方面,本发明涉及根据上述方面中任一项的蛋白的片段,其包含异源二聚蛋白的至少一个IgE抗体表位,所述异源二聚蛋白具有第一肽链和第二肽链,所述第一肽链具有根据SEQ ID NO:3的序列且所述第二肽链具有根据SEQ ID NO:4的序列。
在另外的方面,本发明涉及根据上述方面的蛋白或蛋白片段,其已经固定化至固体或可溶性支持物。适合于固定化蛋白和肽的支持物是本领域众所周知的,且本发明在该方面涵盖任何支持物,其不在任何实质性程度上负面影响蛋白或蛋白片段的免疫原性质。在本上下文中,应当理解术语“固定化”可以是适合于特定支持物的任何种类的附接。在一个实施方案中,根据本发明的蛋白或蛋白片段已经固定化至适合用于诊断方法诸如ImmunoCAP、EliA或VarelisA中的固体支持物。在一个替代实施方案中,根据本发明的蛋白或蛋白片段已经固定化至溶液中的天然或合成聚合结构,诸如溶液中的一种或多种树状结构。
在另外的方面,本发明涉及根据上述方面的蛋白或蛋白片段,其已经提供有标记或标记元件。因此,在一个实施方案中,本发明是根据本发明的蛋白或蛋白片段,其已经提供有发光标记,诸如光致发光标记,诸如荧光或磷光标记、化学发光标记或放射性发光标记。在一个替代实施方案中,根据本发明的蛋白或蛋白片段已经用可鉴定的元件(诸如亲和力功能)衍生化。用于标记蛋白和肽的亲和功能是本领域众所周知的,并且技术人员将能够选择任何合适的功能,诸如生物素。
在另外的方面,本发明涉及编码根据上述方面的蛋白或蛋白片段的核酸分子、以及包含所述核酸分子的载体、包含所述载体的宿主细胞,以及用于重组产生根据上述方面的蛋白或蛋白片段的方法,其包括在适合于表达所述蛋白的条件下培养所述宿主细胞。
在另外的方面,本发明涉及用于体外评价1型过敏的方法,其包括以下步骤:
- 使来自疑似具有1型过敏的患者的含有免疫球蛋白的体液样品与根据上述方面的蛋白、肽链或蛋白片段接触;并且
- 检测所述样品中特异性结合所述蛋白、肽链或蛋白片段的抗体诸如IgE抗体的存在;
其中抗体诸如IgE抗体的存在指示所述患者具有1型过敏。
在一个实施方案中,根据本发明的方法包括检测特异性结合所述蛋白、肽链或蛋白片段的IgE和/或IgG抗体的存在。在其它实施方案中,本发明使用其它或额外同种型的抗体诸如IgA;IgD;和/或IgM。在该实施方案中,特异性IgE抗体的存在指示所述患者具有对马的1型过敏,并且特异性IgG抗体的水平提供了有关天然的或通过环境暴露或免疫疗法治疗诱导的对马的耐受性的信息。
在一个实施方案中,根据该方面的该方法还包括以下步骤:
-使来自疑似具有1型过敏的患者的含有免疫球蛋白的体液样品与来自马的至少一种进一步纯化的过敏原组分接触;并且
-检测所述样品中特异性结合来自马的所述纯化的过敏原组分的IgE抗体的存在;
其中特异性结合所述蛋白、肽链或蛋白片段的IgE抗体的存在和特异性结合来自马的所述过敏原组分的IgE抗体的不存在的组合指示所述患者具有对猫的1型过敏。
在该实施方案中,所述来自马的进一步纯化的过敏原组分优选选自天然和重组的Equ c 1、Equ c 2、Equ c 3、Equ c 4/5和Equ c 15k。
在另外的方面,本发明涉及使用如本申请中所述的标记和/或固定的蛋白和/或蛋白片段的测定法。在一个实施方案中,本发明是包括以下步骤的测定法:(i)在如上所讨论的固体或可溶性支持物上捕获目标抗体同种型;(ii)添加根据本发明的蛋白或蛋白片段;和(iii)直接或间接检测蛋白或蛋白片段与所述抗体的结合。在一个实施方案中,所述蛋白或蛋白片段已经用荧光团标记,在所述情况下,所述检测是直接检测。在另一个实施方案中,所述蛋白或蛋白片段已经如上所述衍生化,例如,通过酶缀合的元件诸如抗生物素蛋白或链霉抗生物素蛋白。
因此,本发明可用于许多不同类型的IgE和IgG测定法,诸如在反向测定法中,其中例如将从IgE致敏个体获得的IgE抗体捕获在支持物上,并通过与标记的过敏原结合来检测,如上所述。
在另外的方面,本发明涉及用于进行根据上述方面的方法的试剂盒,所述试剂盒包括固定化在固体支持物上的根据本发明的蛋白、肽链或蛋白片段。
在该方面的一个实施方案中,所述固体支持物选自硝化纤维素、玻璃、硅和塑料,和/或是微阵列芯片。
在该方面的一个实施方案中,所述试剂盒还包括与固定化的蛋白、肽链或蛋白片段结合的能够结合抗体诸如IgE抗体和/或IgG抗体的检测剂。此类检测剂可以例如是用如免疫测定领域中已知的可检测标记诸如染料、荧光团或酶标记的抗IgE抗体。
本发明的方面还包括根据上述方面的蛋白或蛋白片段,其用于在人或动物体上实践的治疗或诊断、诸如在人或动物体上实践的1型过敏的治疗或诊断的方法,以及用于治疗1型过敏的方法中,所述方法包括向易受此类治疗影响的个体施用根据上述方面的蛋白、肽链或蛋白片段。
定义
术语“蛋白”和“肽”应当被解释为具有它们在本领域中的通常含义。如果没有另外说明,所述术语在本文中可互换使用。
蛋白的“长度”是蛋白中的氨基酸残基的数目。
蛋白的“片段”应当被解释为意指由至少10个氨基酸组成或具有初始蛋白的长度的至少10%的长度的蛋白片段。片段包括具有初始蛋白的全长的至少20%、30%、40%、50%、60%、70%、80%和90%的长度的蛋白片段。
蛋白的“变体”涉及经初始蛋白的整个长度计算与所述初始蛋白具有至少70%、优选超过75%、80%、85%、90%、95%或98%的序列同一性的初始蛋白的变体。用于比对初始和变体蛋白和计算序列同一性的许多软件工具是可商购的,诸如由EuropeanBioinformatics Institute (Cambridge, United Kingdom)提供的Clustal Omega。蛋白变体可以具有初始蛋白的10%、20%、30%、40%、50%、60%、70%、80%、90%、95%、98%、100%、105%或110%的长度。因此,蛋白变体可以由于其产生而包含额外的氨基酸,诸如六组氨酸标签、接头序列或源自载体的氨基酸。为了作为初始过敏蛋白的“变体”,所述变体蛋白应当优选还包含初始过敏蛋白的至少一个IgE抗体表位,即结合来自初始过敏蛋白致敏的代表性患者的血清样品的IgE抗体。初始过敏蛋白的变体是否包含初始过敏蛋白的IgE抗体表位可以通过使用实施例10中描述的抑制测定法来测定。包含初始IgE结合表位的IgE结合表位的变体是引起与初始蛋白的结合的“显著抑制”的那些分子,其应当被解释为与单独的缓冲液(IgE稀释剂,Thermo Fisher Scientific)的抑制相比可以将所述结合抑制至少10%、20%、30%、40%或50%的那些分子。优选地,所述变体以与初始过敏蛋白实质上相同的水平结合IgE抗体。可以通过将所述变体或片段固定化在固相上并测量个体血清的IgE反应性来测量结合水平,如实施例8中所述。为了该定义的目的,“实质上相同的水平”应当被解释为意指所述变体的结合水平与初始蛋白的结合水平相差至多25%、20%、15%、10%或5%。
“异源二聚蛋白”涉及这样的蛋白,其以天然形式包含通过共价或非共价键结合在一起的具有不同氨基酸序列的两条蛋白链。单体单元,即蛋白链,可以由来源生物体中的一种基因或单独的基因编码。
“序列同一性”涉及两个(核苷酸或氨基酸)序列在比对中在相同位置具有相同残基的程度,其表示为百分比。在这方面,为了评价相似性程序和同源性可能性的目的,“比对”涉及匹配两个或更多个生物序列的核苷酸或氨基酸残基以达到最大水平的同一性和(在氨基酸序列的情况下)保守性的过程或结果。在异源二聚蛋白的情况下,可以在比对中连接和使用各链的氨基酸序列或编码它们的核酸序列,以确定“总体”序列同一性。还参见Fassler和Cooper, “BLAST Glossary”, BLAST® Help, Bethesda (MD):NationalCenter for Biotechnology Information (US); 2008-。
术语“载体”涉及用作将外来遗传物质人工携带至其中其可以复制和/或表达的另一细胞中的载体的DNA分子。
附图简述
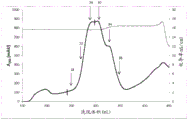
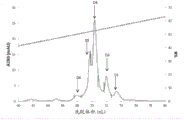
图1显示通过尺寸排阻色谱法(SEC)分离马皮屑蛋白,其中A280吸光度由实线指示,而电导率由阴影线指示。箭头指示测试IgE反应性的级分的位置。垂直条指示含有经受进一步纯化的活性级分的合并物。
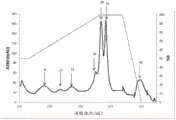
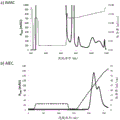
图2显示通过疏水相互作用色谱法的未知马皮屑组分的第二纯化步骤,其中A280吸光度由实线指示,而泵B中Tris pH 8.0缓冲液的百分比(%B)由阴影线指示。箭头指示测试IgE反应性的级分的位置。垂直条指示含有经受进一步纯化的活性级分的合并物。
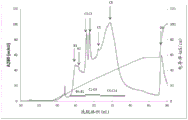
图3显示通过阴离子交换色谱法的未知马皮屑组分的第三纯化步骤,其中A280吸光度由实线指示,而电导率由阴影线指示。箭头指示测试IgE反应性的级分的位置。水平条指示进一步测试的合并物,其中之一含有经受进一步纯化的活性级分。
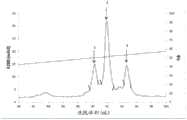
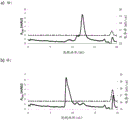
图4显示通过反相色谱法的未知马皮屑组分的第四纯化步骤,其中A280吸光度由实线指示,而泵B中0.05% TFA 90%乙腈缓冲液的百分比(%B)由阴影线指示。垂直条指示三个峰(标记为1、2和3)的合并,每个峰均经受SDS PAGE分析并测试IgE反应性。
图5显示来自RPC纯化步骤的三个峰的还原和非还原样品的SDS-PAGE分析。泳道M含有分子量标记蛋白,其中分子量在左侧指示。
图6显示全长蛋白Equ c s链1的假设核苷酸(a)和氨基酸(b)序列。(c)中显示来自猫的同源分子Fel d 1 链1的氨基酸比对。
图7显示全长蛋白Equ c s链2的假设核苷酸(a)和氨基酸(b)序列。(c)中显示来自猫的同源分子Fel d 1 链2的氨基酸比对。
图8显示阴离子交换色谱合并物的RPC纯化步骤,其使用更陡梯度进行以提高级分中的蛋白浓度。垂直条指示经受MS/MS溶液中消化分析的级分D4和D5。
图9显示通过IMAC(a)纯化重组Equ c s,其中A280吸光度由实线指示,而电导率由阴影线指示。咪唑洗脱梯度范围为800-1200 mL。箭头指示合并且进行阴离子交换色谱(b)的峰。箭头指示峰1和2,且垂直条指示这些合并物的限值。
图10显示重组Equ c s ab的分析型凝胶过滤分析,其中A280吸光度由实线指示,而电导率由阴影线指示。在(a)中,显示来自AIEC的rEqu c s ab,峰1的分析,而在(b)中,显示来自AIEC的 rEqu c s ab,峰2的分析。在(c)中,显示在还原和非还原条件下来自AIEC的峰1和峰2的重组Equ c s ab的SDS PAGE分析。
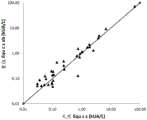
图11显示35个马皮屑致敏个体中天然和重组Equ c s的IgE反应性之间的相关性。0.35 kUA/L和0.1 kUA/L水平由虚线指示。
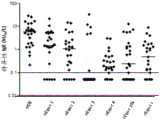
图12显示25个马皮屑过敏性个体的组群中针对马皮屑提取物(HDE)的IgE抗体的水平,Equ c 1、nEqu c 2、nEqu c 3、nEqu c 4、rEqu c 15k和rEqu c s。对于每种组分,在括号中标明了低于0.1 kUA/L的观察数。虚线指示0.35 kUA/L水平,而实线指示0.1 kUA/L水平。水平条指示IgE的中值水平。
图13比较马皮屑致敏个体的组群中IgE抗体与rEqu c s和rFel d 1的结合。0.35kUA/L和0.1 kUA/L水平由虚线指示。
序列表
以下序列列于序列表中。
| SEQ ID NO: | 描述 |
| 1 | 包含信号肽的Equ c s的5 kDa链的氨基酸序列 |
| 2 | 包含信号肽的Equ c s的10 kDa链的预测氨基酸序列 |
| 3 | Equ c s的5 kDa链的预测氨基酸序列 |
| 4 | Equ c s的10 kDa链的预测氨基酸序列 |
| 5 | 整个重组蛋白rEqu c s ab的氨基酸序列 |
| 6 | 编码整个重组蛋白rEqu c s ab的核酸序列 |
| 7 | 替代重组蛋白rEqu c s ba的氨基酸序列 |
| 8 | 编码替代重组蛋白rEqu c s ba的核酸序列 |
| 9 | 密码子优化的编码链1的核酸分子 |
| 10 | 密码子优化的编码链2的核酸分子 |
| 11 | 链1的正向引物,PCR 1 |
| 12 | 链2的正向引物,PCR 1 |
| 13 | 链1的正向引物,PCR 2 |
| 14 | 链2的正向引物,PCR 2 |
| 15 | 链1的反向引物,PCR 2 |
| 16 | 链2的反向引物,PCR 2 |
| 17-33 | 表7中公开的肽片段 |
| 34-43 | 表8中公开的肽片段 |
| 44 | 通过经由RPC峰2的Edman降解的N-末端测序分析给出的双重序列 |
| 45 | 表示为Equ c s,链1的假设序列的完整DNA序列 |
| 46 | 表示为Equ c s,链2的假设序列的完整DNA序列 |
| 47 | Fel d 1 链1 |
| 48 | Fel d 1 链2 |
发明详述
在一个方面,本发明涉及分离的马过敏原,其在本文中表示为Equ c s,属于分泌球蛋白家族,显示出对应于在非还原条件下约18 kDa的电泳迁移率(表观分子量),并且包含通过一个或多个二硫键连接在一起的具有大约5 kDa的分子量的第一肽链和具有大约10kDa的分子量的第二肽链。本发明的该方面还包含与如上所定义的天然Equ c s具有特定序列同一性且优选包含天然Equ c s的至少一个IgE抗体表位的Equ c s的变体和片段。此类变体和片段优选具有与Equ c s反应性血清的IgE反应性,并且此类变体或片段可以抑制IgE与初始rEqu c s分子的结合的至少10%,如通过实施例10中描述的测定法所测定。此外在下面描述的本发明的其它方面中,为了简单起见,术语“Equ c s”还用于包括此类变体和其片段。
在另一个方面,本发明涉及编码根据第一所述方面的过敏原的分离的核酸分子,以及含有所述核酸分子的载体和含有所述载体的宿主细胞。取决于所使用的宿主细胞,由此类含有载体的宿主细胞产生的重组蛋白或肽可以是糖基化的或不是糖基化的。
在另外的方面,本发明涉及用于评价患者中的I型过敏的体外方法,其中使体液样品,诸如来自患者的血液或血清样品,与Equ c s或根据前述方面的组合物接触,由此可以确定患者样品是否含有特异性结合Equ c s的IgE抗体。此类方法可以本领域已知的任何方式实施。Equ c s可以例如固定化在固体支持物上,诸如在常规实验室免疫测定中,在微阵列中或在侧向流测定中,或用作流体相试剂。
在又另外的方面,本发明涉及用于评价患者中的I型过敏的体外方法,其中使体液样品,诸如来自患者的血液或血清样品,与Equ c s接触,由此可以确定患者样品是否含有特异性结合Equ c s、但不结合其它马过敏原组分诸如Equ c 1、Equ c 2、 Equ c 3、Equ c4/5或Equ c 15k的IgE抗体。显示出针对Equ c s、而不针对其它马过敏原组分的IgE反应性的患者可能主要对猫敏感,而不是对马敏感。
在上述方面,野生型Equ c s分子可以如上所述被天然或人造的包含来自野生型蛋白的IgE抗体表位的Equ c s片段或变体替代。
本发明还涉及治疗I型过敏的方法,其包括向需要此类治疗的患者施用如下所解释的Equ c s或修饰的Equ c s。本发明的该方面还涉及Equ c s在此类免疫疗法、包括例如组分分辨的免疫疗法(Valenta和Niederberger 2007)中的用途。在该方面的一个实施方案中,可以其天然形式或以展现与天然分子类似的生物化学和免疫学性质的重组形式使用Equ c s。在另一个实施方案中,可以化学或遗传方式产生的修饰形式使用Equ c s,以便消除或减弱其IgE抗体结合能力,同时优选能够在治疗个体中引发IgG反应。修饰的实例包括但不限于分子的片段化、截短、串联或聚集、内部片段的缺失、氨基酸残基的取代、结构域重排或通过破坏二硫键或其与另一大分子结构或其它低分子量化合物的结合而破坏至少部分三级结构。在该方面的又另一个实施方案中,Equ c s的单独的10 kDa和/或5 kDa亚基被用作修饰的Equ c s。
在本发明的所有上述方面,Equ c s蛋白可以从来自马的其天然来源(诸如从尿液、唾液或其它体液)或组织(诸如毛发或毛皮)纯化。如上所述,其还可以通过重组DNA技术产生或通过本领域技术人员已知或本申请中描述的方法化学合成。
本文所述的过敏性马蛋白Equ c s属于分泌球蛋白家族,具体来讲是包含由两个异源二聚亚基形成的四聚蛋白的一个亚家族。异源二聚体由通过二硫键连接在一起的源自不同基因的两条链组成(Klug等人2000)。本文所述的马分泌球蛋白是18±2 kDa异源二聚体,本文称为Equ c s,分别由5±2 kDa亚基和10±2 kDa亚基(其为了本发明的目的被称为5和10 kDa亚基)组成。分子量分配是根据它们在SDS-PAGE中观察到的表观分子量,如下面实施例3中所述。应当理解,表观分子量将根据分离条件(包括电泳分离介质及其浓度,所使用的线性或梯度缓冲液等)而变化。此外,10 kDa亚基含有N-糖基化位点,当其被聚糖结构占据时可影响表观分子量。
5 kDa链的氨基酸序列具有以下预测氨基酸序列
(SEQ ID NO:3)以及7.9 kDa的理论分子量。
10 kDa链的氨基酸序列具有以下预测氨基酸序列
(SEQ ID NO:4)以及9.6 kDa的理论分子量。
应当注意,结构相关的蛋白已经描述于广泛范围的哺乳动物物种中,但仅两种蛋白已被定义为过敏原,主要猫过敏原Fel d 1 (登录号P30438和P30440)和Equ c 15k(WO2011/133105)。
尽管马皮屑过敏原Equ c 1、Equ c 2、Equ c 3、Equ c 4/5和Equ c 15k涵盖了在马过敏患者中观察到的与马皮屑提取物的大部分IgE反应性,但我们遇到了几种猫过敏性个体的情况,其表现出与马皮屑提取物的IgE反应性,而没有与五种已知马过敏原组分中任一种的伴随反应性。本发明描述了对这种引起与马皮屑提取物的未知IgE反应性的马过敏原的鉴定和表征,其导致发现猫过敏原Fel d 1的蛋白同源物。
在来自猫致敏个体的血清的集合中,许多血清可以被表征为与马皮屑提取物具有反应性,而无法检测到与已知马皮屑过敏原中任一种的反应性。使用上述血清,IgE与马皮屑提取物的结合可以被重组Fel d 1抑制,表明IgE反应性涉及与Fel d 1免疫学相似的马蛋白。
借助于这些血清,可以从马皮屑纯化出新的主要过敏原并鉴定为分泌球蛋白家族的成员。这种在本文中被称为Equ c s的新型马蛋白由通过二硫键连接在一起的一条5 kDa氨基酸链和一条10/11 kDa氨基酸链组成。考虑到这两条多肽链由单独的基因编码的事实,本研究证实了存在先前通过马基因组的生物信息学研究未预期的异源二聚蛋白。其不同于先前已知的马过敏原。该过敏原代表对已知马过敏原组的重要补充,并且可用于诊断马过敏。由于这是与主要猫过敏原Fel d 1交叉反应的过敏原,所以与该分子的IgE反应性可以反映马皮屑的交叉反应性致敏,其可能或可能不与临床症状相关。
以下实施例以来自马的称为Equ cs的分泌球蛋白的分离和使用举例说明了本发明。所述实施例仅仅是说明性的,而不应被认为限制本发明,本发明由所附权利要求的范围所限定。
实施例1:检测马皮屑提取物中类似于Fel d 1的未知过敏原组分的血清的鉴定
使用马皮屑提取物、猫皮屑提取物和Fel d 1常规ImmunoCAP测试。基本上如专利WO2011/133105中所述得到使用重组Equ c 1和Equ c 15k以及从马皮屑纯化的Equ c 2和Equ c 4和从马血清纯化的Equ c 3的实验immunoCAP测试结果。
针对对猫和马皮屑组分的IgE反应性测试了对猫皮屑提取物具有高水平致敏的血清的集合。此处鉴定的五种血清的特征在于对猫皮屑提取物、Fel d 1和马皮屑提取物的高IgE反应性,而对五种已知马过敏原组分中任一种均没有伴随的反应性(表1)。这些血清因此检测了马皮屑提取物中未知的过敏原组分。
所选择的血清用于使用马皮屑提取物和猫皮屑提取物作为固相的抑制试验中(表2)。作为抑制剂,以100 µg/ml的最终浓度分别使用重组Equ c 15k、Fel d 1和Fel d 7。作为抑制对照缓冲液,使用含有0.3%人血清白蛋白的0.1 M磷酸钠缓冲液,pH 7.4。计算每种抑制的重复测定的平均值,并且计算抑制分数作为可以用每种抑制剂淬灭的抑制对照缓冲液的结合的分数。在这些选择的血清中,与猫皮屑提取物的结合可以几乎完全被Fel d 1抑制(表2a)。所测试的其它抑制剂无一显示任何抑制。这表明与猫皮屑提取物的IgE结合由与Fel d 1的反应性支配。同样,与马皮屑提取物固相的结合(表2b)可以被rFel d 1(但没有被其它抑制剂)完全抑制。这表明这些血清与马皮屑提取物的结合针对与猫过敏原Fel d 1免疫学相似的马皮屑组分。尽管Equ c 15k属于分泌球蛋白家族,但该蛋白未表现出对马皮屑提取物的结合的任何抑制,表明所搜索的马组分不是Equ c 15k。这可以通过以下事实来解释:这两种蛋白属于不同的分泌球蛋白亚家族,Fel d 1属于B-E亚家族,而Equ c 15k属于C-D亚家族(Laukaitis和Karn 2005),WO2011/133105。
实施例2:与猫过敏原Fel d 1同源的马皮屑过敏原组分的纯化
通过使用实施例1中描述的血清,可以在马皮屑提取物中检测到类似于Fel d 1的未知过敏原组分,并且通过经由色谱程序分离马皮屑提取物并将这些级分固定在ImmunoCAP固相上,可以在几个色谱步骤期间追踪未知组分。
尺寸排阻色谱
在20 mM MOPS, pH 7.6, 0.15 M NaCl (MBS = MOPS-缓冲盐水)中提取马皮屑(Allergon, Välinge, Sweden),通过离心澄清,并过滤通过0.45μm混合纤维素酯过滤器(Millipore, Billerica, MA, USA)。作为第一纯化步骤,将澄清的提取物施加至Superdex™ 75柱(XK26/100, Vt= 505 mL, GE Healthcare Bio-Sciences AB, Uppsala, Sweden)用于尺寸排阻色谱(SEC),且以2 mL/min的流速用MBS进行洗脱。
色谱图显示于图1中,其中如先前所述将由箭头指示的六个级分固定在固相上(Marknell DeWitt, Niederberger等人 2002)。使用上述血清与固定化级分的IgE结合显示于表3中,其表明测试级分18、22和26含有最高量的未知过敏原组分。将级分16-27(图1中用垂直条指示)合并,并经受疏水相互作用色谱法。
疏水相互作用色谱法
将来自SEC的合并物调节至1 M NH4SO4,并施加至用20 mM tris pH 8.0中的1 MNH4SO4平衡的Phenyl Sepharose™ HP柱(HR10/10, Vt= 8.0 mL, GE Healthcare LifeSciences)。在1M至0 M NH4SO4的线性NH4SO4 梯度(指示为图2的色谱图中在洗脱体积140至260 mL之间的50%-100%B)中进行洗脱。为了洗脱强结合的蛋白,洗涤泵A,并将缓冲液改为20mM Tris pH 8.0中的30%异丙醇。然后使用0-30%异丙醇的异丙醇梯度洗脱柱上的剩余蛋白(指示为色谱图上在洗脱体积285和325mL之间的100%-0%B的梯度)。将色谱图中指示的七个峰1:2稀释于偶联缓冲液(0.1M NaHCO3, pH8.0)中,固定在ImmunoCAP固相上,并使用先前描述的检测血清测试IgE反应性(表4)。在级分60中的异丙醇洗涤梯度中获得最高的IgE反应性。将级分58-66合并并经受阴离子交换色谱法。
阴离子交换色谱法
通过将半体积的Tris pH 8.5的合并物添加至HIC合并物中来调节HIC合并物。随后将合并物施加至用20 mM Tris, pH 8.5平衡的阴离子交换柱Source™ 15Q (PE4.6/100, Vt= 1.66 mL, GE Healthcare Life Sciences)。在相同缓冲液中在线性0-0.50 MNaCl梯度中洗脱后,将蛋白分成几个峰(图3),其中七个在1:4稀释于偶联缓冲液中后固定化。由于在该稀释度的大多数级分中检测到与未知组分的IgE反应性(表5a),将三个合并物B4-B1、C1-C4和C1-C11基于SDS PAGE上的蛋白条带模式合并,并在1:20稀释于偶联缓冲液中之后固定化。稀释度更高的合并级分的IgE分析揭示在第一合并物B4-B1中发现最高活性(表5b),使所述第一合并物B4-B1经受最终色谱RPC纯化步骤。
反相色谱法
通过将TFA添加至0.065%的最终浓度来调节阴离子交换合并物,并通过将样品施加至用水中的0.065% TFA平衡的Source™ 15 RPC柱(Resource, Vt= 3.2 mL; GEHealthcare Life Sciences)来进行最终的RPC纯化步骤。在缓冲液B的线性0-60%梯度中进行洗脱,所述缓冲液B由90%乙腈中的0.05%TFA组成。在梯度结束附近洗脱三个峰(图4),将其固定化在固相上并测试。根据表6,两个第一峰含有高水平的未知组分,其中编号2的峰的含量略多于第一峰。
实施例3:通过SDS PAGE、N-末端测序和MALDI TOF MS分析纯化的级分
RPC级分的SDS PAGE分析揭示前两个RPC峰具有类似模式:在还原条件下,一个5kDa条带和在10/11 kDa的双条带,这些条带在非还原条件下呈现为一个18 kDa的宽条带。该条带模式与来自分泌球蛋白家族的蛋白一致,所述来自分泌球蛋白家族的蛋白通常含有在还原条件下在5和10 kDa的两个条带,以及在非还原条件下在15-20 kDa的一个条带。两个条带中最大的条带是糖基化的,因此可以表现为扩散的,或者在这种情况下表现为双条带。
通过基本上如(Mattsson, Lundgren等人2009)中所述进行的RPC峰2的Edman降解的N-末端测序分析揭示在七个残基之后变得不太清楚的双重序列:
氨基酸残基NO:1 2 3 4 5 6 7
第一备选方案 D P S F Y A V
第二备选方案 - I R P A V -
由于每个循环中氨基酸的相对量是相似的,所以不可能从这些数据建立一级和二级序列。双重序列作为SEQ ID NO:44也显示于序列表中。
用胰蛋白酶对来自一维SDS PAGE凝胶电泳条带5、10和11kDa的斑点进行凝胶中消化,随后通过使用Bruker Daltonics Autoflex 2仪器(Bruker Daltonics, Bremen,Germany)的基质辅助激光解吸电离飞行时间质谱(MALDI TOF MS),随后肽质量指纹(PMF)分析,除了与未表征的马蛋白(XP_005596696)的预测序列相匹配的5kDa条带之外,没有得到与NCBI-NR数据库中任何已知蛋白的显著匹配。然而,尽管该记录的序列的一部分与分泌球蛋白同源,但分子量对于该分子家族太高,并且与从其中挑出的条带不匹配。这个预测的记录被假定是错误的。
实施例4:鉴定与Fel d 1的链1和链2同源的氨基酸序列的马基因组序列的生物信
息学分析
链1
如实施例1中所示与未知马皮屑蛋白免疫学相似的猫过敏原蛋白Fel d 1由通过二硫键连接在一起的两条氨基酸链链1和链2(登录号分别是NP_001041618和NP_001041619)组成。
用Fel d 1,链1(NP_001041618)的序列对马基因组数据库(wsg)的TBLASTN检索得到:aa 17-79与登录号AAWR02030062(马基因组序列的105199 bp区段)的(反向链的)核苷酸位置77633-77453的翻译相匹配。
使围绕该序列的更大区段,登录号AAWR02030062的90000-70021,与Fel d 1链1的前体序列一起进入基因测定程序FGENESH+。该程序在基因组序列内搜索同源基因。
结果是由登录号AAWR02030062的三个外显子组成的假设序列:
77850 -> 77790
77632 -> 77445
76428 -> 76399
该假设序列的完整DNA序列(表示为Equ c s,链1)显示于图6a(SEQ ID NO:45)中,其编码92个氨基酸残基(SEQ ID NO:1,图6b),其前22个残基通过SignalP预测形成信号肽。从克隆的cDNA推导的成熟蛋白由70个氨基酸残基组成,包含三个半胱氨酸,并且具有7.9kDa的预测分子量和4.96的等电点。使用该预测序列的蛋白BLAST同源性检索揭示与分泌球蛋白具有同源性的氨基酸序列。所述预测序列与Fel d 1链1(SEQ ID NO:47)具有67%氨基酸同一性(图6c)。
链2
与上述类似,用Fel d 1,链2(NP_001041619)的序列对马基因组数据库(wsg)的TBLASTN检索得到:aa 21-85与登录号AAWR02030062(马基因组序列的105199 bp区段)的(正向链的)核苷酸位置82588-82782的翻译相匹配。
使围绕该序列的更大区段,登录号AAWR02030062的70021-94020,与Fel d 1链2的前体序列一起进入基因测定程序FGENESH+。该程序在基因组序列内搜索同源基因。
结果是由来自登录号AAWR02030062的两个外显子组成的不完全假设序列:
82004 -> 82064
82589 -> 82770
基于与Fel d 1链2的序列的同源性,在该假定序列中缺失最后一个外显子。比较Fel d 1链2的外显子3与核苷酸82770之后的翻译的基因组序列的蛋白BLAST搜索鉴定了与Feld 1链2的外显子3具有同源性的基因组序列。Equ cs的该假设的外显子3可以与前面外显子同框连接,并在Fel d 1链2的外显子3的同源位置处含有终止密码子。该最终外显子的序列见于:
基因组序列登录号AAWR02030062的90025-90127。
该假设序列的完整DNA序列(表示为Equ c s,链2)显示于图7a(SEQ ID NO:46)中,其编码114个氨基酸残基(SEQ ID NO:2,图7b),其前23个残基通过SignalP预测形成信号肽。从克隆的cDNA推导的成熟蛋白由91个氨基酸残基组成,包含三个半胱氨酸,并且具有9.6 kDa的预测分子量和4.84的等电点。使用该预测序列的蛋白BLAST同源性检索揭示与分泌球蛋白具有同源性的氨基酸序列。所述预测序列与Fel d 1链2(SEQ ID NO:48)具有47%氨基酸同一性(图7c)。
实施例5:来自马皮肤的Equ c s链1和链2 mRNA的PCR扩增和测序
使用RNAqueous试剂盒(Ambion, Austin, TX, USA)从马皮肤制备总RNA。使用mRNA纯化试剂盒从总RNA分离多聚腺苷酸化的RNA,使用第一链cDNA合成试剂盒(均来自Thermo Fisher Scientific))制备第一链cDNA。根据Frohman (Frohman 1993)使用以下来自起始密码子之前的非翻译序列的基因特异性正向寡核苷酸引物进行3’ RACE。
5’-ATAAAAGGGCTGCAGAATTG-3’(SEQ ID NO:11,链1)和
5’-GCAGCAGAAACCCTGCCCTG-3’ (SEQ ID NO:12,链2)。
使用以下来自起始密码子之前的非翻译序列的第二基因特异性正向寡核苷酸引物进行第二PCR,
5’-GTGAGCACCTGCCACCTG-3’ (SEQ ID NO:13,链1)和
5’-GAAGAGCATTCTAGCAGTTG-3’ (SEQ ID NO:14,链2)
其携带用于克隆的末端NdeI限制性位点,以及以下特异性反向寡核苷酸引物,
5’-GAATCTTCTAATCAGACAC-3’ (SEQ ID NO:15,链1)和
5’-GGTAGAGGAGACAGGTGTC-3’ (SEQ ID NO:16,链2)。
分离出链1的四个独立的3’ RACE克隆和链2的三个独立的3’ RACE克隆,并以其整体测序,由此可以验证Equ c s的假设链的编码序列。使用Applied Biosystems 3130Genetic Analyzer (Applied Biosystems, Foster City, CA, USA)进行DNA测序。使用GCG Wisconsin Package (Accelrys, San Diego, CA, USA)的程序进行DNA和氨基酸序列分析和计算。
实施例6:使用Equ c s链1和链2的假设序列的N-末端测序和MALDI TOF分析
使用Equ c s的假设序列进行实施例3中所述的双氨基酸序列的重新评估。双重序列现在可以解释为DICPAV (SEQ ID NO:3的残基1-6)和CPSFYAV (SEQ ID NO:4的残基1-7),其与Equ cs蛋白的成熟链1和链2的假设N-末端序列相同。
图5中的峰2的还原样品的5、10和11 kDa条带以及相同峰的非还原样品的18 kDa条带的凝胶中消化经受MALDI ToF肽质量指纹(PMF)分析,基本上如(Mattsson, Lundgren等人2009)中所述。在5 kDa条带中,检测到8种不同的肽,其质量与假设的Equ c s链1序列中的假设的胰蛋白酶切割的肽相匹配(表7a)。这些肽覆盖了假设的成熟序列的89%,包括氨基酸链的N-末端和C-末端。
在11 kDa条带中,检测到两种不同的肽,其与假设的Equ c s链2序列中的假设的胰蛋白酶切割的肽的质量相匹配(表7b)。这些肽覆盖了假设的成熟序列的32%,包括氨基酸链的N-末端。仅可以鉴定链2序列的小部分的原因在于其含有N-糖基化并且胰蛋白酶切割位点分布使得事实上产生过大或过小的肽。在18 kDa条带中,可以发现来自链1和链2两者的肽。
为了增加这些肽的信号强度以使得能够进行MS/MS分析,使用来自RPC色谱纯化的两个级分,所述RPC色谱纯化类似于实施例2中所述的RPC色谱纯化,但使用更陡的梯度(图8),从而使得前两个峰变得无法完全分辨。将来自前两个峰的级分(级分D5和D4)还原,用碘乙酰胺烷基化,并通过胰蛋白酶进行溶液中消化。使用这些样品,可以通过MS/MS分析来验证由5和10 kDa条带的PMF分析c所覆盖的全部氨基酸序列具有与假设片段相同的序列(表8)。对该样品的进一步分析假定半胰蛋白酶切割位点(即,允许每个肽的仅一个末端被胰蛋白酶切割)鉴定出在链2的C末端附近的大肽片段(表8)。
上述SDS-PAGE分析(图5)和质谱分析提供了5和10 kDa氨基酸链可以分别被鉴定为Equ c s链1和2的证据。在天然非还原状态下,这些氨基酸链通过一个或多个二硫键连接在一起,从而形成异源二聚蛋白。因此,所述分析将由一个基因编码的序列SEQ ID No 3与由另一个不同的基因编码的SEQ ID No 4连接在一起,其一起构成先前未知的异源二聚分泌球蛋白。
实施例7:产生并免疫表征重组Equ c s
重组Equ c s的克隆和纯化
通过将编码5 kDa和10 kDa亚基的氨基酸序列的核苷酸序列与编码包含3x (Gly-Gly-Gly-Gly-Ser,SEQ ID NO:5的残基72-94)的接头肽的序列组合来设计合成Equ cs单链基因。将全长合成基因克隆至载体pET23a(+) (Novagen, Madison, WI, USA)的NdeI和XhoI位点,添加C-末端六组氨酸标签以能够通过固定化金属离子亲和色谱法(IMAC)纯化蛋白。
整个重组蛋白(命名为rEqu cs ab)的氨基酸序列是
(SEQ ID NO:5)。
针对大肠杆菌中的最佳密码子使用设计核苷酸序列(DNA2.0, Menlo Park, CA,USA)。
编码整个重组蛋白的核酸序列是
(SEQ ID NO:6)。
编码链1的核酸序列是
(SEQ ID NO:9)。
编码链2的核酸是
(SEQ ID NO:10)。
设计了替代构建体,其在N-末端具有10 kDa亚基,随后是接头和5 kDa亚基,从而连接每个氨基酸链的另一端的两个亚基。替代重组蛋白(命名为rEqu c s ba)的氨基酸序列是
(SEQ ID NO:7)。
而编码相同蛋白的核酸序列是
(SEQ ID NO:8)。
将质粒DNA构建体转化至大肠杆菌菌株BL21-AI (Invitrogen)中,并且使用3-升生物反应器(Belach Bioteknik, Skogås, Sweden)产生重组Equ c s单链蛋白。
重组Equ c s的纯化方法对于所述蛋白的两种变体几乎是相同的。将收获的细胞重悬浮于20 mM Tris-HCl pH 8.0中,并通过使悬浮液在10000-15000 kPa下通过Emulsiflex C5匀浆器(Avestin, Ottawa, Ontario, Canada)来裂解。在通过离心和过滤来澄清之后,将上清液施加至装填有NiSO4的Chelating Sepharose FF柱(GE HealthcareLife Sciences)。用20 mM Tris-HCl pH 8.0, 0.15 M NaCl中的20 mM咪唑进行柱洗涤,并将重组蛋白洗脱于相同缓冲液中的咪唑的线性20-500 mM梯度中(图9a)。通过20 mM Tris-HCl pH 8.0中的AIEC使用Q Sepharose™ FF柱(GE Healthcare Life Sciences)进行重组蛋白的进一步纯化。使用线性0-0.6 M NaCl梯度洗脱蛋白,产生双峰,其中分别合并两个峰(图9b)。使用0.34/mg/mL的计算消光系数从280 nm处的吸光度测定制备物的蛋白浓度。
重组Equ c s的生物化学表征
rEqu c s ab的峰1和峰2的分析型凝胶过滤表明峰1含有rEqu c s的二聚和单体形式的混合物(图10a),而峰2主要含有聚集物质(图10b)。该结果对于其它重组形式rEqu cs ba也是如此(数据未显示)。
单链重组Equ c s的SDS PAGE分析表明对于还原条件在19 kDa处的单一条带和对于非还原条件在16 kDa处的略低的表观分子量条带(图10c)。在非还原条件期间,还存在主要在39 kDa的更高分子量条带,其被认为代表所述蛋白的二聚形式。
rEqu c s (rEqu c s ab)的第一变体的N-末端序列分析得到清楚和明确的序列读出值,而没有偏离预期序列,并且其中完全保留起始甲硫氨酸。在第二变体rEqu c s ba的制备物中,约一半的样品中保留了起始甲硫氨酸,而制备物的剩余部分开始于第二氨基酸链。总之,两种重组制备物均含有完整的rEqu cs。
评价IgE与重组Equ c s的结合
如所述(Marknell DeWitt, Niederberger等人2002)将两种形式的重组Equ cs的峰1和2各自固定化至实验性ImmunoCAP™,并且使用与实施例1中描述的血清的IgE反应性来评价这些制备物各自的IgE反应性。根据表9,所有制备物均与这些血清具有类似的IgE反应性,这也与含有天然蛋白的纯化级分(表6,级分2)的IgE反应性一致。
使用来自35名马皮屑致敏个体的血清进行IgE反应性的进一步分析,将重组Equ cs ab与来自RPC的天然纯化蛋白级分2进行比较(图4)。
IgE与纯化的天然Equ c s和重组Equ c s的结合之间存在良好的一致性(r=0.99)(图11),表明所述重组蛋白是免疫活性的并且在结构上类似于天然蛋白。这些数据为以下结论提供了强有力的证据:如从鉴定的基因组序列信息所预测,Equ c s的5 kDa (SEQ IDNO:3)和10 kDa (SEQ ID NO:4)亚基的氨基酸序列是正确的,且代表纯化的马皮屑过敏原Equ c s的氨基酸序列。
实施例8:在马过敏患者组群中评价nEqu c 1、nEqu c 2、nEqu c 3、nEqu c 4、Equ
c 15k和Equ c s的IgE结合活性
来自西班牙(n=20)和瑞典(n=5)的25名马过敏个体的血清被用于研究中。所有患者都被医生诊断为具有症状诸如哮喘、鼻结膜炎和荨麻疹的马过敏,以及对马皮屑提取物的皮肤点刺试验呈阳性。所有样品和临床数据均在每个中心的地方伦理委员会的批准下收集,所述中心对保藏样品和数据的生物库有贡献。
使用ImmunoCAP™测定25名马过敏个体中对马皮屑提取物nEqu c 1、nEqu c 2、nEqu c 3和nEqu c 4、rEqu c 15k和rEqu c s ab的特异性IgE抗体的水平(图12,表10)。在表10中,所有ImmunoCAP™水平都显示为kUA/L,且每个患者的来源由ES(西班牙)或SE(瑞典)指示。所记录的暴露于马的过敏症状是鼻炎(rhin)、哮喘(astm)、荨麻疹(urt)或过敏反应(anaph)。
在测试的25份血清中,13份(52%)显示对rEqu c s的≥0.35 kUA/L的IgE反应,而12份(48%)对rEqu c 15k具有IgE反应性,16份(64%)对nEqu c 2具有IgE反应性,且19份(76%)对nEqu c 1具有IgE反应性。nEqu c 3和nEqu c 4/5两者在所研究的个体中呈现为次要过敏原,分别结合来自仅5份(20%)和7份(28%)的测试血清中的IgE ab。在该研究组群中,无一患者专门对rEqu c s反应,而25份血清中的四份(16%)和两份分别对Equ c 15k和Equc 1反应。平均在所有Equ c 15k-反应性血清中,针对Equ c s的IgE抗体的浓度相当于对马皮屑的IgE抗体的浓度的30%。针对nEqu c 1的IgE抗体的相应相对浓度为52%,而对于nEqu c 2、nEqu c 3、nEqu c 4/5和Equ c 15k,在对那些过敏原特异性反应的血清中,相对浓度分别为35%、69%、9%和37%。25份血清中的24份显示IgE抗体与马皮屑提取物的结合。所有那些血清都显示与所测试的五种个体马过敏原中的至少一种结合。IgE与各个组分的结合水平的总和匹配或超过与马皮屑提取物的结合水平。
实施例9:Equ c s和来自猫的分泌球蛋白、主要猫过敏原Fel d 1之间的交叉反应
性
由于作为该研究的起点的未知IgE反应性被Fel d 1抑制,所以研究了重组Equ cs和Fel d 1之间的关系。在35名马皮屑致敏的个体(包括实施例8中描述的那些25名马致敏患者)的血清中评估IgE与Fel d 1结合的水平。在针对重组Equ cs的IgE水平和rFel d 1之间存在显著相关性(r=0.92)(图13),并且对于几乎所有个体,针对Fel d 1的IgE反应性均高于Equ c s。
为了进一步研究Equ cs和Fel d 1之间的关系,使用固相上的马皮屑提取物rFeld 1和rEqu c s以及rEqu c 15k、rEqu c s和rFel d 1作为抑制剂(以100 µg/mL的最终浓度),测试实施例1中使用的5种血清的交叉抑制。作为抑制对照缓冲液,使用含有0.3%人血清白蛋白的0.1 M磷酸钠缓冲液,pH 7.4。计算每种抑制的重复测定的平均值,并且将抑制分数计算为可以用每种抑制剂淬灭的使用抑制对照缓冲液的结合分数。
在所选的这些血清中,抑制与马皮屑提取物的结合仅可通过Fel d 1和Equ c s来实现,表明Equ c s确实是马皮屑提取物中的未知蛋白,其负责这些血清的结合(表11A)。与Fel d 1 immunoCAP的结合可以被Fel d 1本身抑制,但不可被Equ cs抑制(表11B),而与Equ c s的结合可以被Fel d 1和Equ c s两者抑制(表11C)。这表明Fel d 1和Equ cs之间的IgE结合确实是交叉反应的,正如这两种蛋白之间的高度序列同源性(图6C和7C)以及IgE结合与马皮屑致敏血清群体的高度相关性所提示的。此外,Fel d 1可以抑制与Equ c s固相的结合、但Equ c s不能抑制与Fel d 1的结合的事实,以及马皮屑致敏血清群体中IgE与Fel d 1的结合总是高于与Equ c s的结合的事实,表明这些血清最初是Fel d 1致敏,而与Equ c s的结合是交叉反应性的结果。
实施例10:评价过敏原蛋白的变体或片段(被分析物)的IgE结合性质
将初始过敏原蛋白,在这种情况下是Equ c s,固定化在固体支持物上。将来自对相关物种致敏的至少三名代表性人患者且对来自该物种的初始过敏原蛋白表现出IgE反应性的血清样品在室温下与100 μg/mL的最终浓度的被分析物温育2小时,并平行地与单独的缓冲液和大肠杆菌的非过敏性麦芽糖结合蛋白(MBP)温育2小时作为阴性对照。然后分析样品的IgE与携带固定化Equ c s的固体支持物的结合,以研究与Equ c s的变体或片段的预温育是否特异性抑制或显著降低IgE结合。
表1 用于检测未知马皮屑组分的血清的IgE结合特征。
CDE-猫皮屑提取物
HDE–马皮屑提取物。
表2 使用抑制剂Equ c 15k、Fel d 1和Fel d 7抑制IgE与a)猫皮屑提取物和b)马皮屑提取物的结合。
a) 与猫皮屑提取物固相的结合
b) 与马皮屑提取物固相的结合
表3 检测血清与固定化的来自马皮屑提取物的SEC色谱的级分的IgE结合
表4 检测血清与固定化的来自马皮屑提取物的富集级分的HIC色谱的级分的IgE结合
表5 检测血清与固定化的来自马皮屑提取物的富集级分的阴离子交换色谱的级分的IgE结合
a) 1:4稀释的固定化的级分
b) 1:20稀释的固定化的合并物
表6 检测血清与固定化的来自马皮屑提取物的富集级分的RPC色谱的级分的IgE结合
表7 与来自还原样品的a) 5 kDa条带和b) 10 kDa条带以及非还原样品的c) 18kDa条带的凝胶中消化的胰蛋白酶切割的Equ c s的理论质量相匹配的肽片段。
表8 来自RPC的溶液中消化的级分的通过MS/MS鉴定的肽。
*通过蛋白的半胰蛋白酶切割鉴定的肽。
表9 rEqu s c制备物的IgE反应性
表10 25名马过敏患者的IgE反应性
表11 使用抑制剂Equ c 15k、Equ c s和Fel d 1抑制IgE与a)马皮屑提取物、b)rFel d 1和c) rEqu c s固相的结合。
a) 与马皮屑提取物固相的结合
b) 与rFel d 1固相的结合
c) 与rEqu c s固相的结合
参考文献
Akdis, C. A. (2006). "Allergy and hypersensitivity: mechanisms ofallergic disease." Curr Opin Immunol 18(6): 718-726.
Akdis, M. and C. A. Akdis (2007). "Mechanisms of allergen-specificimmunotherapy." J Allergy Clin Immunol 119(4): 780-791.
Asarnoj, A., R. Moverare,等人,(2010). "IgE to peanut allergencomponents: relation to peanut symptoms and pollen sensitization in 8-year-olds." Allergy.
Asarnoj, A., C. Nilsson,等人,(2012). "Peanut component Ara h 8sensitization and tolerance to peanut." J Allergy Clin Immunol 130(2): 468-472.
Breiteneder, H., K. Hoffmann-Sommergruber,等人,(1997). "Recombinantallergens; basic and practical considerations." Arbeiten aus dem Paul Ehrlich Institut - Bundesamt fur Sera und Impfstoffe - Zu Frankfurt Am(91): 80-86.
Cabañas, R., M. C. López-Serrano,等人,(2000). "Importance of albuminin cross-reactivity among cat, dog and horse allergens." Journal of Investigational Allergology and Clinical Immunology 10(2): 71-77.
Canonica, G. W., I. J. Ansotegui,等人,(2013). "A WAO - ARIA - GA2LENconsensus document on molecular-based allergy diagnostics." World Allergy Organ J 6(1): 17.
Caubet, J. C., R. Bencharitiwong,等人,(2012). "Significance ofovomucoid- and ovalbumin-specific IgE/IgG(4) ratios in egg allergy." J Allergy Clin Immunol 129(3): 739-747.
Codreanu, F., O. Collignon,等人,(2011). "A novel immunoassay usingrecombinant allergens simplifies peanut allergy diagnosis." Int Arch Allergy Immunol 154(3): 216-226.
Cromwell, O., H. Fiebig,等人,(2006). "Strategies for recombinantallergen vaccines and fruitful results from first clinical studies." Immunol Allergy Clin North Am 26(2): 261-281, vii.
Custovic, A., L. Soderstrom,等人,(2011). "Allergen-specific IgGantibody levels modify the relationship between allergen-specific IgE andwheezing in childhood." J Allergy Clin Immunol 127(6): 1480-1485.
Dandeu, J. P., J. Rabillon,等人,(1993). "Hydrophobic InteractionChromatography for Isolation and Purification of Equ.Cl, the Horse MajorAllergen." Journal of Chromatography-Biomedical Applications 621(1): 23-31.
Du Toit, G., G. Roberts,等人,(2015). "Randomized trial of peanutconsumption in infants at risk for peanut allergy." N Engl J Med 372(9): 803-813.
Ebisawa, M., R. Moverare,等人,(2012). "Measurement of Ara h 1-, 2-,and 3-specific IgE antibodies is useful in diagnosis of peanut allergy inJapanese children." Pediatr Allergy Immunol 23(6): 573-581.
Ebisawa, M., R. Shibata,等人,(2012). "Clinical utility of IgEantibodies to omega-5 gliadin in the diagnosis of wheat allergy: a pediatricmulticenter challenge study." Int Arch Allergy Immunol 158(1): 71-76.
Goubran Botros, H., C. Gregoire,等人,(1996). "Cross-antigenicity ofhorse serum albumin with dog and cat albumins: study of three short peptideswith significant inhibitory activity towards specific human IgE and IgGantibodies." Immunology 88(3): 340-347.
Goubran Botros, H., P. Poncet,等人,(2001). "Biochemicalcharacterization and surfactant properties of horse allergens." Eur J Biochem268(10): 3126-3136.
Goubran Botros, H., J. Rabillon,等人,(1998). "Thiophilic adsorptionchromatography: purification of Equ c2 and Equ c3, two horse allergens fromhorse sweat." Journal of Chromatography. B, Biomedical Sciences & Applications 710(1-2): 57-65.
Gregoire, C., I. Rosinski-Chupin,等人,(1996). "cDNA cloning andsequencing reveal the major horse allergen Equ c1 to be a glycoprotein memberof the lipocalin superfamily." Journal of Biological Chemistry 271(51):32951-32959.
Gronlund, H., T. Saarne,等人,(2009). "The Major Cat Allergen, Fel d1, in Diagnosis and Therapy." Int Arch Allergy Immunol 151(4): 265-274.
Hiller, R., S. Laffer,等人,(2002). "Microarrayed allergen molecules:diagnostic gatekeepers for allergy treatment." FASEB Journal 16(3): 414-416.
Jutel, M., L. Jaeger,等人,(2005). "Allergen-specific immunotherapywith recombinant grass pollen allergens." J Allergy Clin Immunol 116(3): 608-613.
Kim, J. L., L. Elfman,等人,(2005). "Current asthma and respiratorysymptoms among pupils in relation to dietary factors and allergens in theschool environment." Indoor Air 15(3): 170-182.
Laukaitis, C. and R. Karn (2005). "evolution of the secretoglobins: agenomic and proteomic view." biol J Linnean Soc 84: 493-501.
Liccardi, G., G. D'Amato,等人,(2011). "Sensitization to HorseAllergens in Italy: A Multicentre Study in Urban Atopic Subjects withoutOccupational Exposure." Int Arch Allergy Immunol 155(4): 412-417.
Marknell DeWitt, Å., V. Niederberger,等人,(2002). "Molecular andimmunological characterization of a novel timothy grass (Phleum pratense)pollen allergen, Phl p 11." Clinical & Experimental Allergy 32(9): 1329-1340.
Masthoff, L. J., L. Mattsson,等人,(2013). "Sensitization to Cor a 9and Cor a 14 is highly specific for a hazelnut allergy with objectivesymptoms in Dutch children and adults." J Allergy Clin Immunol 132(2): 393-399.
Matsuo, H., J. Dahlstrom,等人,(2008). "Sensitivity and specificity ofrecombinant omega-5 gliadin-specific IgE measurement for the diagnosis ofwheat-dependent exercise-induced anaphylaxis." Allergy 63(2): 233-236.
Mattsson, L., T. Lundgren,等人,(2009). "Prostatic kallikrein: A newmajor dog allergen." J Allergy Clin Immunol 123(2): 362-368.
McDonald, R. E., R. I. Fleming,等人,(2009). "Latherin: a surfactantprotein of horse sweat and saliva." PLoS One 4(5): e5726.
Müller, U., P. Schmid-Grendelmeier,等人,(2012). "IgE to recombinantallergens Api m 1, Ves v 1, and Ves v 5 distinguish double sensitization fromcrossreaction in venom allergy." Allergy 67(8): 1069-1073.
Nicolaou, N., M. Poorafshar,等人,(2010). "Allergy or tolerance inchildren sensitized to peanut: prevalence and differentiation usingcomponent-resolved diagnostics." J Allergy Clin Immunol 125(1): 191-197 e191-113.
Ronmark, E., M. Perzanowski,等人,(2003). "Different sensitizationprofile for asthma, rhinitis, and eczema among 7-8-year-old children: reportfrom the Obstructive Lung Disease in Northern Sweden studies." Pediatr Allergy Immunol 14(2): 91-99.
Saarelainen, S., M. Rytkonen-Nissinen,等人,(2008). "Animal-derivedlipocalin allergens exhibit immunoglobulin E cross-reactivity." Clin Exp Allergy 38(2): 374-381.
Saarne, T., L. Kaiser,等人,(2005). "Rational design of hypoallergensapplied to the major cat allergen Fel d 1." Clin Exp Allergy 35(5): 657-663.
Smith, W., A. J. Butler,等人,(2004). "Fel d 4, a cat lipocalinallergen." Clinical & Experimental Allergy 34(11): 1732-1738.
Spitzauer, S., C. Schweiger,等人,(1993). "Characterisation of dogallergens by means of immunoblotting." International Archives of Allergy and Immunology 100: 60-67.
Stumvoll, S., K. Westritschnig,等人,(2003). "Identification of cross-reactive and genuine Parietaria judaica pollen allergens." Journal of Allergy and Clinical Immunology 111(5): 974-979.
Tutluoglu, B., S. Atis,等人,(2002). "Sensitization to horse hair,symptoms and lung function in grooms." Clin Exp Allergy 32(8): 1170-1173.
Uermosi, C., R. R. Beerli,等人,(2010). "Mechanisms of allergen-specific desensitization." J Allergy Clin Immunol 126(2): 375-383.
Uermosi, C., F. Zabel,等人,(2014). "IgG-mediated down-regulation ofIgE bound to mast cells: a potential novel mechanism of allergen-specificdesensitization." Allergy 69(3): 338-347.
Wainstein, B. K., A. Yee,等人,(2007). "Combining skin prick,immediate skin application and specific-IgE testing in the diagnosis ofpeanut allergy in children." Pediatr Allergy Immunol 18(3): 231-239.
Valenta, R., J. Lidholm,等人,(1999). "The recombinant allergen-basedconcept of component-resolved diagnostics and immunotherapy (CRD and CRIT)."Clinical and Experimental Allergy 29(7): 896-904.
Valenta, R. and V. Niederberger (2007). "Recombinant allergens forimmunotherapy." J Allergy Clin Immunol 119(4): 826-830。
序列表
<110> Phadia AB
<120> 新型过敏原
<130> P10607SE00
<160> 48
<170> PatentIn version 3.5
<210> 1
<211> 92
<212> PRT
<213> 家马(Equus caballus)
<220>
<221> 信号
<222> (1)..(22)
<220>
<221> 成熟肽
<222> (23)..(92)
<400> 1
Met Lys Arg Ala Gly Ala Leu Val Leu Leu Trp Thr Thr Leu Leu Leu
-20 -15 -10
Ile Pro Gly Arg Asn Cys Asp Ile Cys Pro Ala Val Lys Glu Asp Val
-5 -1 1 5 10
Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr Val Lys Lys Val Ser
15 20 25
Gln Tyr Gln Arg Asn Pro Val Ile Leu Ala Asn Ala Glu Lys Leu Lys
30 35 40
Asn Cys Ile Asp Lys Lys Leu Thr Ala Glu Asp Lys Glu Asn Ala Leu
45 50 55
Ser Val Leu Glu Lys Ile Tyr Ser Ser Asp Phe Cys
60 65 70
<210> 2
<211> 114
<212> PRT
<213> 家马(Equus caballus)
<220>
<221> 信号
<222> (1)..(23)
<220>
<221> 成熟肽
<222> (24)..(114)
<400> 2
Met Lys Gly Ala Leu Leu Val Leu Ala Leu Leu Val Thr Arg Glu Leu
-20 -15 -10
Gly Ile Lys Met Ala Glu Ala Cys Pro Ser Phe Tyr Ala Val Leu Gly
-5 -1 1 5
Val Leu Ser Leu Gly Ser Lys Thr Leu Leu Asp Thr Ser Leu Asn Leu
10 15 20 25
Val Asn Ala Thr Glu Pro Glu Lys Val Ala Met Gly Lys Ile Gln Asp
30 35 40
Cys Tyr Asn Glu Ala Gly Val Ile Thr Lys Ile Ser Asp Leu Ile Ile
45 50 55
Met Gly Thr Ile Thr Thr Ser Pro Glu Cys Ile Ser His Ala Leu Ser
60 65 70
Thr Leu Thr Thr Asp Val Gln Glu Gly Ile Ser Lys Leu Asn Pro Leu
75 80 85
Gly Arg
90
<210> 3
<211> 70
<212> PRT
<213> 家马(Equus caballus)
<400> 3
Asp Ile Cys Pro Ala Val Lys Glu Asp Val Asn Ile Phe Leu Thr Gly
1 5 10 15
Thr Pro Asp Asp Tyr Val Lys Lys Val Ser Gln Tyr Gln Arg Asn Pro
20 25 30
Val Ile Leu Ala Asn Ala Glu Lys Leu Lys Asn Cys Ile Asp Lys Lys
35 40 45
Leu Thr Ala Glu Asp Lys Glu Asn Ala Leu Ser Val Leu Glu Lys Ile
50 55 60
Tyr Ser Ser Asp Phe Cys
65 70
<210> 4
<211> 91
<212> PRT
<213> 家马(Equus caballus)
<400> 4
Cys Pro Ser Phe Tyr Ala Val Leu Gly Val Leu Ser Leu Gly Ser Lys
1 5 10 15
Thr Leu Leu Asp Thr Ser Leu Asn Leu Val Asn Ala Thr Glu Pro Glu
20 25 30
Lys Val Ala Met Gly Lys Ile Gln Asp Cys Tyr Asn Glu Ala Gly Val
35 40 45
Ile Thr Lys Ile Ser Asp Leu Ile Ile Met Gly Thr Ile Thr Thr Ser
50 55 60
Pro Glu Cys Ile Ser His Ala Leu Ser Thr Leu Thr Thr Asp Val Gln
65 70 75 80
Glu Gly Ile Ser Lys Leu Asn Pro Leu Gly Arg
85 90
<210> 5
<211> 185
<212> PRT
<213> 人工序列
<220>
<223> 合成单链蛋白
<220>
<221> INIT_MET
<222> (1)..(1)
<220>
<221> MISC_FEATURE
<222> (72)..(86)
<223> 接头肽
<220>
<221> MISC_FEATURE
<222> (180)..(185)
<223> 六组氨酸标签
<400> 5
Met Asp Ile Cys Pro Ala Val Lys Glu Asp Val Asn Ile Phe Leu Thr
1 5 10 15
Gly Thr Pro Asp Asp Tyr Val Lys Lys Val Ser Gln Tyr Gln Arg Asn
20 25 30
Pro Val Ile Leu Ala Asn Ala Glu Lys Leu Lys Asn Cys Ile Asp Lys
35 40 45
Lys Leu Thr Ala Glu Asp Lys Glu Asn Ala Leu Ser Val Leu Glu Lys
50 55 60
Ile Tyr Ser Ser Asp Phe Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly
65 70 75 80
Ser Gly Gly Gly Gly Ser Cys Pro Ser Phe Tyr Ala Val Leu Gly Val
85 90 95
Leu Ser Leu Gly Ser Lys Thr Leu Leu Asp Thr Ser Leu Asn Leu Val
100 105 110
Asn Ala Thr Glu Pro Glu Lys Val Ala Met Gly Lys Ile Gln Asp Cys
115 120 125
Tyr Asn Glu Ala Gly Val Ile Thr Lys Ile Ser Asp Leu Ile Ile Met
130 135 140
Gly Thr Ile Thr Thr Ser Pro Glu Cys Ile Ser His Ala Leu Ser Thr
145 150 155 160
Leu Thr Thr Asp Val Gln Glu Gly Ile Ser Lys Leu Asn Pro Leu Gly
165 170 175
Arg Leu Glu His His His His His His
180 185
<210> 6
<211> 555
<212> DNA
<213> 人工序列
<220>
<223> 编码合成单链肽的DNA
<400> 6
atggacattt gccctgcggt taaagaggac gtcaacattt ttctgaccgg taccccagat 60
gattacgtca aaaaagtgag ccagtaccag cgtaacccgg ttattctggc aaatgccgag 120
aaactgaaga attgtatcga caaaaagctg acggctgagg ataaggaaaa cgccctgtct 180
gtcttggaga agatttacag cagcgacttc tgtggtggcg gtggcagcgg tggtggtggt 240
tcgggcggtg gcggcagctg cccgtccttc tatgcggtgc tgggtgttct gagcttaggt 300
agcaagaccc tgttggacac gagcctgaat ttggtgaatg cgactgaacc ggagaaagtc 360
gcaatgggca agatccaaga ttgctataac gaagcgggcg ttatcaccaa gatcagcgat 420
ctgatcatta tgggtacgat cacgaccagc ccggaatgta tctctcacgc gctgtccacc 480
ctgaccaccg acgtgcaaga gggcattagc aaactgaacc cgctgggtcg cctcgagcac 540
caccaccacc accac 555
<210> 7
<211> 185
<212> PRT
<213> 人工序列
<220>
<223> 合成单链肽
<220>
<221> INIT_MET
<222> (1)..(1)
<220>
<221> MISC_FEATURE
<222> (93)..(107)
<223> 接头肽
<220>
<221> MISC_FEATURE
<222> (180)..(185)
<223> 六组氨酸标签
<400> 7
Met Cys Pro Ser Phe Tyr Ala Val Leu Gly Val Leu Ser Leu Gly Ser
1 5 10 15
Lys Thr Leu Leu Asp Thr Ser Leu Asn Leu Val Asn Ala Thr Glu Pro
20 25 30
Glu Lys Val Ala Met Gly Lys Ile Gln Asp Cys Tyr Asn Glu Ala Gly
35 40 45
Val Ile Thr Lys Ile Ser Asp Leu Ile Ile Met Gly Thr Ile Thr Thr
50 55 60
Ser Pro Glu Cys Ile Ser His Ala Leu Ser Thr Leu Thr Thr Asp Val
65 70 75 80
Gln Glu Gly Ile Ser Lys Leu Asn Pro Leu Gly Arg Gly Gly Gly Gly
85 90 95
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Cys Pro Ala
100 105 110
Val Lys Glu Asp Val Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr
115 120 125
Val Lys Lys Val Ser Gln Tyr Gln Arg Asn Pro Val Ile Leu Ala Asn
130 135 140
Ala Glu Lys Leu Lys Asn Cys Ile Asp Lys Lys Leu Thr Ala Glu Asp
145 150 155 160
Lys Glu Asn Ala Leu Ser Val Leu Glu Lys Ile Tyr Ser Ser Asp Phe
165 170 175
Cys Leu Glu His His His His His His
180 185
<210> 8
<211> 555
<212> DNA
<213> 人工序列
<220>
<223> 编码合成单链肽的DNA
<400> 8
atgtgcccgt cgttttatgc agtcctgggt gttctgtctt tgggttctaa aactttgctg 60
gacacgagcc tgaatctggt gaatgcaacg gagcctgaaa aggtcgcgat gggcaagatt 120
caggactgtt acaacgaagc gggcgttatt accaagatca gcgacctgat cattatgggc 180
acgatcacca cgagcccaga gtgcatcagc cacgctttgt ccaccctgac caccgatgtc 240
caagagggca ttagcaagct gaacccgctg ggtcgcggtg gtggcggtag cggtggtggt 300
ggctccggtg gcggtggcag cgatatttgt ccggcggtga aagaagatgt caacatcttc 360
ctgaccggta ccccggatga ttatgtgaaa aaagttagcc aataccagcg taatccggtt 420
atcctggcca atgccgagaa actgaagaac tgcatcgaca aaaagctgac cgcagaggac 480
aaagaaaacg cgctgagcgt gctggagaag atttacagca gcgacttctg tctcgagcac 540
caccaccacc accac 555
<210> 9
<211> 210
<212> DNA
<213> 人工序列
<220>
<223> 密码子优化链1
<400> 9
gacatttgcc ctgcggttaa agaggacgtc aacatttttc tgaccggtac cccagatgat 60
tacgtcaaaa aagtgagcca gtaccagcgt aacccggtta ttctggcaaa tgccgagaaa 120
ctgaagaatt gtatcgacaa aaagctgacg gctgaggata aggaaaacgc cctgtctgtc 180
ttggagaaga tttacagcag cgacttctgt 210
<210> 10
<211> 273
<212> DNA
<213> 人工序列
<220>
<223> 密码子优化链2
<400> 10
tgcccgtcgt tttatgcagt cctgggtgtt ctgtctttgg gttctaaaac tttgctggac 60
acgagcctga atctggtgaa tgcaacggag cctgaaaagg tcgcgatggg caagattcag 120
gactgttaca acgaagcggg cgttattacc aagatcagcg acctgatcat tatgggcacg 180
atcaccacga gcccagagtg catcagccac gctttgtcca ccctgaccac cgatgtccaa 240
gagggcatta gcaagctgaa cccgctgggt cgc 273
<210> 11
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> 链1的正向引物,PCR 1
<400> 11
ataaaagggc tgcagaattg 20
<210> 12
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> 链2的正向引物,PCR 1
<400> 12
gcagcagaaa ccctgccctg 20
<210> 13
<211> 18
<212> DNA
<213> 人工序列
<220>
<223> 链1的正向引物
<400> 13
gtgagcacct gccacctg 18
<210> 14
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> 链2的正向引物
<400> 14
gaagagcatt ctagcagttg 20
<210> 15
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> 链1的反向引物
<400> 15
gaatcttcta atcagacac 19
<210> 16
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> 链2的反向引物
<400> 16
ggtagaggag acaggtgtc 19
<210> 17
<211> 23
<212> PRT
<213> 家马(Equus caballus)
<400> 17
Asp Ile Cys Pro Ala Val Lys Glu Asp Val Asn Ile Phe Leu Thr Gly
1 5 10 15
Thr Pro Asp Asp Tyr Val Lys
20
<210> 18
<211> 16
<212> PRT
<213> 家马(Equus caballus)
<400> 18
Glu Asp Val Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr Val Lys
1 5 10 15
<210> 19
<211> 17
<212> PRT
<213> 家马(Equus caballus)
<400> 19
Glu Asp Val Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr Val Lys
1 5 10 15
Lys
<210> 20
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<400> 20
Lys Val Ser Gln Tyr Gln Arg
1 5
<210> 21
<211> 6
<212> PRT
<213> 家马(Equus caballus)
<400> 21
Val Ser Gln Tyr Gln Arg
1 5
<210> 22
<211> 10
<212> PRT
<213> 家马(Equus caballus)
<400> 22
Asn Pro Val Ile Leu Ala Asn Ala Glu Lys
1 5 10
<210> 23
<211> 15
<212> PRT
<213> 家马(Equus caballus)
<400> 23
Leu Thr Ala Glu Asp Lys Glu Asn Ala Leu Ser Val Leu Glu Lys
1 5 10 15
<210> 24
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<400> 24
Ile Tyr Ser Ser Asp Phe Cys
1 5
<210> 25
<211> 16
<212> PRT
<213> 家马(Equus caballus)
<400> 25
Cys Pro Ser Phe Tyr Ala Val Leu Gly Val Leu Ser Leu Gly Ser Lys
1 5 10 15
<210> 26
<211> 13
<212> PRT
<213> 家马(Equus caballus)
<400> 26
Ile Gln Asp Cys Tyr Asn Glu Ala Gly Val Ile Thr Lys
1 5 10
<210> 27
<211> 23
<212> PRT
<213> 家马(Equus caballus)
<400> 27
Asp Ile Cys Pro Ala Val Lys Glu Asp Val Asn Ile Phe Leu Thr Gly
1 5 10 15
Thr Pro Asp Asp Tyr Val Lys
20
<210> 28
<211> 16
<212> PRT
<213> 家马(Equus caballus)
<400> 28
Glu Asp Val Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr Val Lys
1 5 10 15
<210> 29
<211> 17
<212> PRT
<213> 家马(Equus caballus)
<400> 29
Glu Asp Val Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr Val Lys
1 5 10 15
Lys
<210> 30
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<400> 30
Lys Val Ser Gln Tyr Gln Arg
1 5
<210> 31
<211> 10
<212> PRT
<213> 家马(Equus caballus)
<400> 31
Asn Pro Val Ile Leu Ala Asn Ala Glu Lys
1 5 10
<210> 32
<211> 15
<212> PRT
<213> 家马(Equus caballus)
<400> 32
Leu Thr Ala Glu Asp Lys Glu Asn Ala Leu Ser Val Leu Glu Lys
1 5 10 15
<210> 33
<211> 13
<212> PRT
<213> 家马(Equus caballus)
<400> 33
Ile Gln Asp Cys Tyr Asn Glu Ala Gly Val Ile Thr Lys
1 5 10
<210> 34
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<400> 34
Asp Ile Cys Pro Ala Val Lys
1 5
<210> 35
<211> 16
<212> PRT
<213> 家马(Equus caballus)
<400> 35
Glu Asp Val Asn Ile Phe Leu Thr Gly Thr Pro Asp Asp Tyr Val Lys
1 5 10 15
<210> 36
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<400> 36
Lys Val Ser Gln Tyr Gln Arg
1 5
<210> 37
<211> 6
<212> PRT
<213> 家马(Equus caballus)
<400> 37
Val Ser Gln Tyr Gln Arg
1 5
<210> 38
<211> 10
<212> PRT
<213> 家马(Equus caballus)
<400> 38
Asn Pro Val Ile Leu Ala Asn Ala Glu Lys
1 5 10
<210> 39
<211> 15
<212> PRT
<213> 家马(Equus caballus)
<400> 39
Leu Thr Ala Glu Asp Lys Glu Asn Ala Leu Ser Val Leu Glu Lys
1 5 10 15
<210> 40
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<400> 40
Ile Tyr Ser Ser Asp Phe Cys
1 5
<210> 41
<211> 13
<212> PRT
<213> 家马(Equus caballus)
<400> 41
Ile Gln Asp Cys Tyr Asn Glu Ala Gly Val Ile Thr Lys
1 5 10
<210> 42
<211> 16
<212> PRT
<213> 家马(Equus caballus)
<400> 42
Cys Pro Ser Phe Tyr Ala Val Leu Gly Val Leu Ser Leu Gly Ser Lys
1 5 10 15
<210> 43
<211> 24
<212> PRT
<213> 家马(Equus caballus)
<400> 43
Ile Ser Asp Leu Ile Ile Met Gly Thr Ile Thr Thr Ser Pro Glu Cys
1 5 10 15
Ile Ser His Ala Leu Ser Thr Leu
20
<210> 44
<211> 7
<212> PRT
<213> 家马(Equus caballus)
<220>
<221> 不确定
<222> (1)..(1)
<223> Asp或Cys
<220>
<221> 不确定
<222> (2)..(2)
<223> Pro, Ile或Cys
<220>
<221> 不确定
<222> (3)..(3)
<223> Ser, Arg,或Cys
<220>
<221> 不确定
<222> (4)..(4)
<223> Phe, Pro,或Cys
<220>
<221> 不确定
<222> (5)..(5)
<223> Tyr, Ala,或Cys
<220>
<221> 不确定
<222> (6)..(6)
<223> Ala, Val,或Cys
<220>
<221> 不确定
<222> (7)..(7)
<223> Val,或Cys
<400> 44
Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 45
<211> 279
<212> DNA
<213> 家马(Equus caballus)
<400> 45
atgaagcggg ctggtgctct cgtgctgctc tggaccacct tgcttctgat cccaggcaga 60
aattgtgaca tttgcccagc cgtgaaggaa gatgttaata tattcctgac aggaacccct 120
gatgactatg ttaaaaaagt ttcacagtac caacgcaatc ctgtaatatt ggccaatgct 180
gaaaagctaa agaactgcat tgataagaaa ttgacagccg aggataagga gaatgccctc 240
agtgtgctgg agaaaatata ctcaagtgat ttttgttaa 279
<210> 46
<211> 345
<212> DNA
<213> 家马(Equus caballus)
<400> 46
atgaaggggg cactgcttgt gctggccttg ctggtgacca gagagctggg catcaagatg 60
gcggaagctt gcccgagttt ttatgcagtc cttggtgtgt tgtcccttgg aagcaagaca 120
ctgttggaca cctccctcaa tctggtcaat gctactgaac cggaaaaagt agccatggga 180
aaaatccagg attgctacaa tgaggcggga gtcataacca agatctcgga tctgatcatc 240
atgggtacta tcaccaccag cccagaatgc atcagccacg cactgagcac attgacgacg 300
gatgttcaag aaggcatttc taagctgaac cctctgggga gatga 345
<210> 47
<211> 88
<212> PRT
<213> 家猫(Felis catus)
<220>
<221> 信号
<222> (1)..(18)
<400> 47
Met Leu Asp Ala Ala Leu Pro Pro Cys Pro Thr Val Ala Ala Thr Ala
1 5 10 15
Asp Cys Glu Ile Cys Pro Ala Val Lys Arg Asp Val Asp Leu Phe Leu
20 25 30
Thr Gly Thr Pro Asp Glu Tyr Val Glu Gln Val Ala Gln Tyr Lys Ala
35 40 45
Leu Pro Val Val Leu Glu Asn Ala Arg Ile Leu Lys Asn Cys Val Asp
50 55 60
Ala Lys Met Thr Glu Glu Asp Lys Glu Asn Ala Leu Ser Leu Leu Asp
65 70 75 80
Lys Ile Tyr Thr Ser Pro Leu Cys
85
<210> 48
<211> 109
<212> PRT
<213> 家猫(Felis catus)
<220>
<221> 信号
<222> (1)..(23)
<400> 48
Met Arg Gly Ala Leu Leu Val Leu Ala Leu Leu Val Thr Gln Ala Leu
1 5 10 15
Gly Val Lys Met Ala Glu Thr Cys Pro Ile Phe Tyr Asp Val Phe Phe
20 25 30
Ala Val Ala Asn Gly Asn Glu Leu Leu Leu Asp Leu Ser Leu Thr Lys
35 40 45
Val Asn Ala Thr Glu Pro Glu Arg Thr Ala Met Lys Lys Ile Gln Asp
50 55 60
Cys Tyr Val Glu Asn Gly Leu Ile Ser Arg Val Leu Asp Gly Leu Val
65 70 75 80
Met Thr Thr Ile Ser Ser Ser Lys Asp Cys Met Gly Glu Ala Val Gln
85 90 95
Asn Thr Val Glu Asp Leu Lys Leu Asn Thr Leu Gly Arg
100 105
Claims (14)
1.分离的异源二聚蛋白,其具有根据SEQ ID NO:3的序列的一个肽链和根据SEQ IDNO:4的序列的另一个肽链,其中所述分离的异源二聚蛋白是具有IgE反应性的过敏原。
2.单链蛋白,其由根据SEQ ID NO:3和SEQ ID NO:4所示的氨基酸序列经由接头组合而成。
3.根据权利要求1或2所述的蛋白,其已被固定化至固体或可溶性支持物并且/或者已提供有可检测标记。
4.核酸分子,其编码根据权利要求1或2所述的蛋白。
5.载体,其包含根据权利要求4所述的核酸分子。
6.宿主细胞,其包含根据权利要求5所述的载体。
7.由权利要求6所述的宿主细胞表达的重组蛋白或肽。
8.根据权利要求1的分离的异源二聚蛋白或根据权利要求2的单链蛋白或根据权利要求7的重组蛋白或肽在制备用于通过如下方法体外评估1型过敏的试剂中的用途,其中所述方法包括以下步骤:
- 使来自疑似具有1型过敏的患者的含有免疫球蛋白的体液样品与所述试剂接触;并且
- 检测所述样品中特异性结合所述蛋白或肽的抗体的存在;
其中此类结合的抗体的存在指示所述患者具有1型过敏。
9.根据权利要求8所述的用途,其中所述方法包括检测所述样品中特异性结合所述蛋白或肽的IgE和/或IgG抗体的存在;
其中特异性IgE抗体的存在指示所述患者具有对马的1型过敏,而特异性IgG抗体的水平提供了有关天然的或通过环境暴露或免疫疗法治疗诱导的对马的耐受性的信息。
10.根据权利要求8或9所述的用途,其中所述方法还包括以下步骤:
-使来自疑似具有1型过敏的患者的含有免疫球蛋白的体液样品与来自马的至少一种进一步纯化的过敏原组分接触;并且
-检测所述样品中特异性结合来自马的所述纯化的过敏原组分的IgE抗体的存在;
其中特异性结合所述蛋白或肽的IgE抗体的存在和特异性结合来自马的所述过敏原组分的IgE抗体的不存在的组合指示所述患者具有对猫的1型过敏。
11.根据权利要求10所述的用途,其中所述来自马的进一步纯化的过敏原组分选自天然和重组的Equ c 1、Equ c 2、Equ c 3、Equ c 4/5和Equ c 15k。
12.试剂盒,用于实施根据权利要求8-11中任一项所限定的方法,其包括固定化在固体支持物上的根据权利要求1的分离的异源二聚蛋白或根据权利要求2的单链蛋白或根据权利要求7的重组蛋白或肽。
13.根据权利要求1的分离的异源二聚蛋白或根据权利要求2的单链蛋白或根据权利要求7的重组蛋白或肽在制备用于诊断1型过敏的试剂中的用途。
14.根据权利要求1的分离的异源二聚蛋白或根据权利要求2的单链蛋白或根据权利要求7的重组蛋白或肽在制备用于治疗1型过敏的试剂中的用途。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SE1450907 | 2014-07-21 | ||
| SE1450907-9 | 2014-07-21 | ||
| PCT/SE2015/050828 WO2016013971A1 (en) | 2014-07-21 | 2015-07-20 | Novel allergen |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN106604929A CN106604929A (zh) | 2017-04-26 |
| CN106604929B true CN106604929B (zh) | 2021-11-05 |
Family
ID=53872123
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201580038584.4A Active CN106604929B (zh) | 2014-07-21 | 2015-07-20 | 新型过敏原 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US10753946B2 (zh) |
| EP (1) | EP3171890B1 (zh) |
| JP (1) | JP6785216B2 (zh) |
| CN (1) | CN106604929B (zh) |
| AU (1) | AU2015294723B2 (zh) |
| CA (1) | CA2955348A1 (zh) |
| DK (1) | DK3171890T3 (zh) |
| ES (1) | ES2856128T3 (zh) |
| RU (1) | RU2017104910A (zh) |
| WO (1) | WO2016013971A1 (zh) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011133105A1 (en) * | 2010-04-23 | 2011-10-27 | Phadia Ab | Novel allergen |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6019972A (en) * | 1989-11-03 | 2000-02-01 | Immulogic Pharmaceutical Corporation | Peptides of human T cell reactive feline protein (TRFP) |
| EP1195606A1 (en) | 2000-10-03 | 2002-04-10 | VBC-Genomics Forschungsges.m.b.H. | Allergen-microarray assay |
-
2015
- 2015-07-20 AU AU2015294723A patent/AU2015294723B2/en active Active
- 2015-07-20 RU RU2017104910A patent/RU2017104910A/ru not_active Application Discontinuation
- 2015-07-20 CN CN201580038584.4A patent/CN106604929B/zh active Active
- 2015-07-20 JP JP2017503551A patent/JP6785216B2/ja active Active
- 2015-07-20 EP EP15750835.9A patent/EP3171890B1/en active Active
- 2015-07-20 ES ES15750835T patent/ES2856128T3/es active Active
- 2015-07-20 US US15/327,253 patent/US10753946B2/en active Active
- 2015-07-20 CA CA2955348A patent/CA2955348A1/en active Pending
- 2015-07-20 WO PCT/SE2015/050828 patent/WO2016013971A1/en active Application Filing
- 2015-07-20 DK DK15750835.9T patent/DK3171890T3/da active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011133105A1 (en) * | 2010-04-23 | 2011-10-27 | Phadia Ab | Novel allergen |
| CN103108883A (zh) * | 2010-04-23 | 2013-05-15 | 法蒂亚公司 | 新型变应原 |
Non-Patent Citations (4)
| Title |
|---|
| Cabañas R等.Importance of albumin in cross-reactivity among cat,dog and horse allergens.《Journal of Investigational Allergology and Clinical Immunology》.2000, * |
| Predicted: major allergen I polypeptide chain 1-like [Equus przewalskii];GenBank;《GenBank Database》;20140714;Accession NO.XP_008513295.1 * |
| Predicted: major allergen I polypeptide chain 2-like isoform X1[Equus przewalskii];GenBank;《GenBank Database》;20170714;Accession NO.XP_008513296.1 * |
| 马主要过敏原Equ c1的重组表达及其低过敏原性的改造;彭俊玲;《中国优秀硕士学位论文全文数据库医药卫生科技辑》;20121015;E059-185 * |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2015294723B2 (en) | 2021-05-06 |
| US20170219602A1 (en) | 2017-08-03 |
| JP6785216B2 (ja) | 2020-11-18 |
| AU2015294723A1 (en) | 2017-02-16 |
| CN106604929A (zh) | 2017-04-26 |
| ES2856128T3 (es) | 2021-09-27 |
| US10753946B2 (en) | 2020-08-25 |
| JP2017524358A (ja) | 2017-08-31 |
| EP3171890B1 (en) | 2020-12-02 |
| WO2016013971A1 (en) | 2016-01-28 |
| DK3171890T3 (da) | 2021-02-22 |
| EP3171890A1 (en) | 2017-05-31 |
| CA2955348A1 (en) | 2016-01-28 |
| RU2017104910A (ru) | 2018-08-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9274114B2 (en) | Prostate kallikrein allergen | |
| US20220241406A1 (en) | Novel allergen | |
| CN106604929B (zh) | 新型过敏原 | |
| US9724407B2 (en) | Horse allergen and methods | |
| RU2592674C2 (ru) | Аллергены, полученные рекомбинантными способами |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |