CN102711769A - 甾体化合物在炎性和自身免疫疾病中的应用 - Google Patents
甾体化合物在炎性和自身免疫疾病中的应用 Download PDFInfo
- Publication number
- CN102711769A CN102711769A CN2010800404946A CN201080040494A CN102711769A CN 102711769 A CN102711769 A CN 102711769A CN 2010800404946 A CN2010800404946 A CN 2010800404946A CN 201080040494 A CN201080040494 A CN 201080040494A CN 102711769 A CN102711769 A CN 102711769A
- Authority
- CN
- China
- Prior art keywords
- optional substituted
- alkynyl
- alkyl
- optional
- amino
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/575—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of three or more carbon atoms, e.g. cholane, cholestane, ergosterol, sitosterol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/04—Drugs for disorders of the muscular or neuromuscular system for myasthenia gravis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/14—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Pulmonology (AREA)
- Physical Education & Sports Medicine (AREA)
- Hematology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Dermatology (AREA)
- Endocrinology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Ophthalmology & Optometry (AREA)
- Obesity (AREA)
- Transplantation (AREA)
- Emergency Medicine (AREA)
- Gastroenterology & Hepatology (AREA)
- Neurology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Steroid Compounds (AREA)
Abstract
Description
技术领域
本发明涉及甾体化合物的应用,包括螺环甾体类似物在治疗、预防或改善炎性状态的症状,例如哮喘。免疫系统的作用机理表明,甾体化合物能用于治疗一系列的炎性状态,包括但不限于哮喘、肺部炎症、视网膜炎性状态,自身免疫疾病如类风湿性关节炎、多发性硬化症和全身性红斑狼疮,炎性肠疾病和肌病。
背景技术
炎症是多种伤害刺激和状态触发的适应性反应。炎症触发粒性白细胞和血浆蛋白到感染的组织位点的募集。其成为许多人类免疫系统相关疾病的基础。炎性状态的范围继续扩张到包括最初认为不是炎性但是退化成为炎性的常规疾病。炎症分为外源性炎症,其引起外源性炎症相关的疾病(感染、变态反应、毒物接触、药品、化学物质、吸烟、污染、谷蛋白、胆固醇、葡萄糖),和内源性炎症(自发炎症与自身免疫炎症相对)。自发炎症疾病(FMF,HIDS,TRAPS)是先天免疫疾病,而自身免疫性疾病(全身性红斑狼疮、类风湿性关节炎、多发性硬化症、重症肌无力、再生障碍性贫血、自身免疫性溶血性贫血、顽固性硬皮病、皮炎、获得性天疱疮、格雷夫斯病、自身免疫性肝炎、银屑病、克隆氏病,溃疡性结肠炎)是遗传的和继承性的免疫疾病。
对病原体的免疫是通过诱导抗原特异性的辅助性T淋巴细胞(Th)Th1,Th2和Th17介导的。Th 1免疫对抗细胞内病原体给予保护和当其过度时产生自身免疫性。异常的Th 1)-和Th 17细胞激活会导致自身免疫,当抗环境中的抗原过度的Th2细胞激活,可能诱发变态反应和哮喘。Th1细胞产生γ-干扰素(IFN-γ)和激活MΦs以对抗细胞内的病原体。Th2细胞产生细胞因子如白介素-4(IL-4),白介素-5(IL-5)和白介素-13(IL-13),刺激肥大细胞和嗜酸性粒细胞并增强B细胞产生的免疫球蛋白E(IgE)。Th17细胞调节遗传性和继承性的免疫应答以对抗病原体,如真菌和细菌。T调控细胞(Treg)是一种不同的T细胞亚群,其通过过度增生的Th1,Th2或Th17细胞限制免疫病理学。Th的免疫性的激活和分化依赖于Th细胞和抗体内存在的细胞间的相互作用,例如树状突细胞(DCs)和在这个过程中起到关键作用的细胞因子。
过度增生的Th1,Th2或Th17的免疫应答通过抑制机制(免疫抑制)受到限制。这些机制包括细胞因子如转化生长因子-β(TGF-β)的局部分泌,以及通过与细胞表面分子结合直接细胞接触,如抑制性T细胞上的细胞溶解性T淋巴细胞相关抗原cDN(CTLA-4)与在效应器T细胞上的CD80和CD86分子结合。抑制作用需要在不同组织的抑制器和效应器T细胞适当的共区域化和可能包含T细胞受体干扰,表明触发转录因子在调节效应细胞功能中是重要的。T调控细胞显示了重要的抑制活性。T调控细胞在保持对自身抗原的免疫无应答性上和在抑制对宿主有害的过度免疫应答起了必不可少的作用。T调控细胞作为T细胞的一个功能性成熟的亚群在胸腺中产生,也能够从在外周的初始T细胞被诱导。最近研究揭示了T调控细胞发育和功能的细胞和分子基础,与T调控细胞在免疫疾病中和调节异常的关联。
糖皮质激素,是内源性类固醇,其中许多很可能是最强效的抗感染药物,然而这些药物具有许多不希望的副作用(如向心性肥胖、高血糖、骨质疏松)使它们的应用必须严格控制。
脱氢表雄酮(DHEA)的合成衍生物,如5-雄烯-116α-氟-17-酮(HE2500)和确定的自然代谢产物在自身免疫和代谢性疾病的各种动物模型显示具有作用。但是,像脱氢表雄酮一样,这些化合物的低效价和低的口服生物利用度使他们在人类中的应用被限制。HE3286是一种新的脱氢表雄酮的17-乙炔基衍生物,在小鼠上和在胶原诱导关节炎(CIA)的DBA小鼠模型中的口服生物利用度显示达到25%;接受用HE3286(50mg/kg)口服治疗的动物,在疾病的开始,表现CIA峰值和关节炎分数的每日严重度明显地降低。HE3286在人任何经典模型的测试中没有发现免疫抑制,包括分裂素诱导的细胞增殖、延迟性过敏或混合淋巴细胞反应。反而,这些优势与CD4+CD25+FOXp3+CD127-调控T细胞(T reg)的数量和功能的增加有关。
新的治疗炎性状态的开发是一种持久性的需要。天然类固醇如脱氢表雄酮(DHEA)在实验动物上具有重要的免疫抑制剂的性质。然而,天然来源的类固醇在人体内代谢为雌激素、雄激素或黄体酮,产生全身的和重要的激素样副反应,包括激素依赖性瘤的形成Front.Neuroendocrinol.21,1(2000)(神经内分泌学前言.21.(2000)),从而限制了它们的临床应用。
美国专利US 3,365,475(1968)公开了17α-(3’-羟基-丙基)-4-雄甾烯-3β,17β-二醇的制备方法,其可用于制备甾体17-螺环四氢呋喃,后者作为醛固酮抑制剂具有有效的治疗效用。
美国专利US 4,026,918(1977)描述了某些被认为具有抗炎活性的D高甾类的制备。(3β,11α,17α)-螺环[雄甾-5-烯-17,2′-环氧乙烷]-3,11-二醇作为化学中间体被公开。
美国专利US 4,054,563(1977)公开了制备某些17-螺环-(2’-氧杂环丙烷)甾体化合物的方法,该化合物被认为是用于制备醛固酮拮抗剂的有用的中间体。
WO 98/33506公开了某些化合物在抑制雄激素合成中的应用,所述化合物被认为可用于治疗前列腺癌和良性前列腺肥大。所列的比较化合物之一是17β,20β-乙烯亚氨基-孕甾-5-烯-3β-醇。
在Journal of Medicinal Chemistry 10(4),546-551(1967)(药物化学杂志,10(4),546-551(1967))中,提及如下式B所示的甾族环醚作为中间体用于制备具有抗雌激素性质的甾族化合物。
WO 2008/155534中公开了神经甾体化合物及其在治疗与神经元凋亡或神经元损伤相关的神经变性状态中的应用,包括埃尔茨海默病和帕金森病。
发明内容
在第一方面,本发明涉及一种预防或治疗炎性状态的方法,包括给予患者有效量的式I化合物或其药学上可接受的酯、盐或酸加成盐:
其中R1、R2、R3、R4、R5、R6、R7、A、B、X、Y和Z如以下具体说明书中所定义的。
仅作为例举,所述的炎性状态可以是以下中的任何一种:哮喘、肺部炎症、视网膜炎性状态、自身免疫疾病如类风湿性关节炎、I型糖尿病、全身性红斑狼疮,重症肌无力、再生障碍性贫血,自身免疫性溶血性贫血、顽固性硬皮病、皮炎、获得性天疱疮、格雷夫斯病、自身免疫性肝炎、银屑病、克隆氏病,溃疡性结肠炎和炎性肠疾病和肌病。多发性硬化症是另一种状态,可以根据本发明的方法治疗。
在另一方面,本发明涉及式I的化合物或其药学上可接受的酯、盐或酸加成盐,用于预防或治疗炎性状态。所述状态是,例如上面列出这些中的任意一种。
在另一方面,本发明涉及式I的化合物,或其药学上可接受的酯、盐或酸加成盐在制备预防或治疗炎性状态的药物中的应用。所述状态可以是,例如上面列出这些中的任意一种。
在另一方面,本发明涉及式I的化合物,或其药学上可接受的酯、盐或酸加成盐在控制或抑制人类或非人类动物体免疫应答中的应用。
在另一方面,本发明涉及式I的化合物,或其药学上可接受的酯、盐或酸加成盐在控制或抑制人类或非人类动物体T细胞活性中的应用。
如在说明书和例证性的具体实施方案中所描述和举例说明的,通过下列产品和所需特征、性质、特性,以及要素与工序关系、彼此相对关系的详细描述,本发明将得到更好的理解。
附图说明
图1是显示在实验研究中,几种甾体化合物对受刺激的培养小鼠淋巴结细胞的影响柱状图。
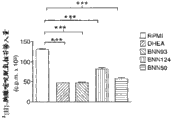
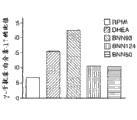
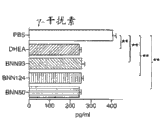
图2包含柱状图形式的实验研究结果,显示几种甾体化合物对某些未接触抗原的纯的培养小鼠CD4+T细胞的影响(图2a),和对白介素-2和γ-干扰素的增殖和分泌的影响(分别为图2b和2c)。
图3是显示在实验研究中,几种甾体化合物对受刺激的培养小鼠的纯的CD4+T细胞影响的柱状图。
图4是显示在实验研究中,几种甾体化合物对经过流式细胞检测分析后培养中的CD4+7AAD-细胞数量影响的柱状图。
图5是显示粗略的实验记录时间表,该实验记录是用于研究几种甾体化合物防止MOG肽诱导的实验性自身免疫脑脊髓炎(EAE)的能力。
图6是显示在根据图5所显示的实验记录的实验研究中,几种甾体化合物随时间对小鼠平均临床EAE值影响的图。
图7包含根据图5所显示的实验记录的实验研究结果,以柱状图的形式显示几种甾体化合物对小鼠在EAE病的发生率方面(图7a),平均最大临床分数(图7b)和病初起的天数(图7c)的影响。
图8包含染色切片,是显示在实验研究中根据图5所显示的实验记录中,几种甾体化合物对小鼠脊索感染的影响。
图9包含以柱状图的形式显示的几种甾体化合物对某些经过诱导发展成EAE的小鼠的淋巴结细胞的影响的实验研究结果,在对MOG35-55肽的细胞增殖方面(图9a),在产生γ-干扰素和白介素-10的数量方面(图9b和图9c),在细胞因子白介素-17分泌方面(图9d),在γ-干扰素/白介素-17的比例方面(图9e)。
图10是显示粗略的实验记录时间表,该实验记录是用于研究几种甾体化合物在实验性自身免疫脑脊髓炎(EAE)病初发后的保护效应。
图11是显示在根据图10所显示的实验记录的实验研究中,几种甾体化合物随时间对小鼠平均临床EAE值影响的图。
图12是显示在根据图10所显示的实验记录的实验研究中,几种甾体化合物对小鼠在平均最大临床分数方面的影响的柱状图。
图13包含以柱状图的形式显示的几种甾体化合物对经过诱导发展成EAE的某些小鼠的淋巴结细胞的影响的实验研究结果,在产生白介素-10的数量方面(图13a),和在γ-干扰素(图13b)和细胞因子白介素-17(图13c)的分泌方面。
图14包含某些小鼠的实验研究结果,以柱状图的形式显示,几种甾体化合物在支气管肺泡灌洗中对不同类型粒细胞的数量的影响(图14a),对肺部白细胞浸润的影响(图14b)和对卵清蛋白特异性T细胞的分化的影响(14c)。
图15是显示粗略的实验记录时间表,该实验记录是用于研究几种甾体化合物在抑制建立的MOG肽诱导的实验性自身免疫脑脊髓炎(EAE)的能力。
图16是显示在根据图15所显示的实验记录的实验研究中,几种甾体化合物随时间对小鼠平均临床EAE值影响的图。
图17是显示在根据图15所显示的实验记录的实验研究中,几种甾体化合物对小鼠在平均最大临床分数方面影响的柱状图。
图18包含染色切片,显示在根据图5所显示的实验记录的实验研究中,某些甾体化合物对小鼠脊索感染的影响。
图19包含以柱状图的形式显示的几种甾体化合物对经过诱导发展成EAE的某些小鼠的淋巴结细胞的影响的实验研究结果,在对MOG35-55肽的细胞增殖方面(图19a),在产生γ-干扰素和白介素-17的数量方面(图19b和图19c),和在细胞因子白介素-10分泌方面(图19d)。
图20是显示在实验研究中,几种甾体化合物对经过流式细胞检测分析后培养中的CD3+CD4+IL10+T细胞数量影响的柱状图。
图21是显示在实验研究中,某些甾体化合物随时间对小鼠平均临床EAE值影响图。
图22是显示在实验研究中,某些甾体化合物对小鼠在平均最大临床分数方面影响的柱状图。
图23包含以柱状图的形式显示的某种甾体化合物对经过诱导发展成EAE的某些小鼠的淋巴结细胞影响的实验研究结果,在对MOG35-55肽的细胞增殖方面(图23a),和在产生γ-干扰素和白介素-17的数量方面(图23b和图23c)。
图24是显示在实验研究中,某些甾体化合物随时间对小鼠平均临床EAE值影响图。
图25是显示在实验研究中,某些甾体化合物对小鼠在平均最大临床分数方面影响的柱状图。
图26包含以柱状图的形式显示的某些甾体化合物对经过诱导发展成EAE的某些小鼠的淋巴结细胞影响的实验研究结果,在对MOG35-55肽的细胞增殖方面(图26a),和在产生γ-干扰素和白介素-17的数量方面(图26b和图26c)。
图27包含在实验研究中,以柱状图的形式显示的某些甾体化合物对经过流式细胞检测分析后培养中细胞数量的影响的实验研究结果,CD11c+细胞(图27a)、CD3+CD4+IL17+T细胞(图27b)和CD4+Foxp3+T细胞。
图28是显示在实验研究中,某些甾体化合物随时间对小鼠平均临床EAE值影响图。
图29是显示在实验研究中,某些甾体化合物对小鼠在平均最大临床分数方面影响的柱状图。
图30是显示某些甾体化合物对经过诱导发展成EAE的某些小鼠的淋巴结细胞在对MOG35-55肽的细胞增殖方面影响的柱状图。
图31是显示在实验研究中,某些甾体化合物随时间对小鼠平均临床EAE值影响图。
图32是显示在实验研究中,某些甾体化合物对小鼠在平均最大临床分数方面影响的柱状图。
图33包含以柱状图的形式显示的某些甾体化合物对经过诱导发展成EAE的某些小鼠的淋巴结细胞影响的实验研究结果,在对MOG35-55肽的细胞增殖方面(图33a),和在产生γ-干扰素和白介素-17的数量方面(图33b和33c)。
图34是显示在实验研究中,某些甾体化合物随时间对小鼠平均临床EAE值影响图。
图35是显示在实验研究中,某些甾体化合物对小鼠在平均最大临床分数方面影响的柱状图。
图36是显示某些甾体化合物对经过流式细胞检测分析后培养中CD4+IL-17+细胞数量影响的柱状图。
图37是显示某些甾体化合物对经过流式细胞检测分析后培养中CD4+IL-10+细胞数量影响的柱状图。
图38包含通过流式细胞计量法得到的输出图和显示在实验研究中几种甾体化合物对培养中的CD25和Foxp3+细胞数量的影响。
图39是显示在实验研究中某些甾体化合物对经过培养的初始CD4+细胞影响的柱状图。
图40是显示某些甾体化合物对首先经过诱导发展成EAE,用甾体化合物治疗和然后用OVA/CFA进行免疫(弗氏完全佐剂)的某些小鼠的淋巴结细胞影响的柱状图。
附图的更详细讨论见以下实施例1-8。
具体实施方式
本发明涉及式I的化合物的应用
(I)
其中
R1是羟基、烷氧基、烷酰氧基、氨基碳酰氧基或烷氧基碳酰氧基;
R2是氢、任选取代的烷基、任选取代的烯基、任选取代的烷氧基烷基、任选取代的氨烷基、氰基、任选取代的氰烷基、任选取代的硫氰烷基、异硫氰基、任选取代的叠氮烷基、任选取代的烷酰氧基烷基、任选取代的芳基烷基、任选取代的杂芳基烷基、任选取代的芳基烯基、任选取代的杂芳基烯基、任选取代的芳基、任选取代的芳基炔基(arylkynyl)、任选取代的芳基烷基炔基(arylkylalkynyl)、任选取代的烷酰氧炔基、任选取代的杂芳基氧基炔基、任选取代的酮炔基或其缩酮、任选取代的氰基炔基、任选取代的杂芳基炔基、任选取代的羟基炔基、任选取代的烷氧基炔基、任选取代的氨基炔基、任选取代的酰氨基炔基、任选取代的巯基炔基、任选取代的羟基炔基二酸半酯或其盐、或任选取代的炔氧基炔基;
或
R1是氧,且R2是烷基或烯基或炔基,其与R1键合形成可被任选取代的氧化环;
R3是氢,或当甾环系统的C5和C6之间存在双键时,R3不存在;
R4是氢或低级烷基;
R5是氢、氨基、任选取代的烷基氨基、任选取代的二烷基氨基、任选取代的烯基氨基、任选取代的二烯基氨基、任选取代的炔基氨基、任选取代的二炔基氨基、酰胺基、硫代、亚磺酰基、磺酰基、亚磺酰氨基、卤素、羟基、任选取代的烷氧基、任选取代的烯基氧基、任选取代的炔基氧基烷基、任选取代的烯基、任选取代的炔基、任选取代的芳基、叠氮基、任选取代的杂芳基、肟=N-O-R8、羧甲基肟、羧乙基肟、或羧丙基肟;
R6是氢、氨基、硫代、亚磺酰基、磺酰基、亚磺酰氨基、卤素、羟基、任选取代的烷氧基、任选取代的烷基、任选取代的烯基、或任选取代的炔基;
R7是氢、氨基、任选取代的烷基氨基、任选取代的二烷基氨基、任选取代的烯基氨基、任选取代的二烯基氨基、任选取代的炔基氨基、任选取代的二炔基氨基、酰胺基、硫、亚磺酰基、磺酰基、亚磺酰氨基、卤素、羟基、任选取代的烷氧基、任选取代的烯基氧基、任选取代的炔基氧基烷基、任选取代的烯基、任选取代的炔基、任选取代的芳基、叠氮基、任选取代的杂芳基、肟=N-O-R8、羧甲基肟、羧乙基肟、或羧丙基肟;
X是化合价键,亚甲基(-CH2-)或选自氧、硫的杂原子,或-NH、-S(O)、-SO2、-NR8、-NC(O)R8、-N-甲苯-4-磺酰基氧;
A是-(CH2)n-、C2-5亚烯基、或C2-5亚炔基,其中n是整数,且可取值为0或1或2或3或4或5;
B是-(CH2)y-、C2-5亚烯基、或C2-5亚炔基,其中y是整数,且可取值为1或2或3或4或5;
Y可键合到在甾体骨架C17处的螺环取代基的任何碳原子上,且独立地是H、任选取代的C1-10烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的C2-10炔基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、甲酰基、羧基、-NC(O)R8、NC(S)R8、-NR8R9、任选取代的C(O)-W、任选取代的C(O)O-W、或任选取代的C(S)O-W;
Z可键合到在甾体骨架C17处的螺环取代基的任何碳原子上,且独立地是H、任选取代的C1-10烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的C2-10炔基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、甲酰基、羧基、-NC(O)R8、NC(S)R8、-NR8R9、任选取代的C(O)-W、任选取代的C(O)O-W、任选取代的C(S)O-W;
Y和Z可键合到C17处螺环取代基的同一碳原子上;
W是任选取代的C1-10烷基、任选取代的杂环烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的杂环烯基、任选取代的C2-10炔基、任选取代的杂环炔基、任选取代的芳基、或任选取代的杂芳基;
R8和R9独立地是任选取代的C1-10烷基、任选取代的杂环烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的杂环烯基、任选取代的C2-10炔基、任选取代的杂环炔基、任选取代的芳基、或任选取代的杂芳基;
以及点线表示可能存在的单键或双键。
式I的化合物及其药学上可接受的酯、盐或酸加成盐可用于治疗、预防或改善炎性状态的症状,特别是那些与免疫系统相关的。仅作为例举,可被治疗的状态包括哮喘、肺部炎症、视网膜炎性状态、自身免疫疾病如类风湿性关节炎、I型糖尿病、全身性红斑狼疮,重症肌无力、再生障碍性贫血,自身免疫性溶血性贫血、顽固性硬皮病、皮炎、获得性天疱疮、格雷夫斯病、自身免疫性肝炎、银屑病、克隆氏病,溃疡性结肠炎和炎性肠疾病和肌病。多发性硬化症是另一种状态,可以根据本发明的方法治疗。
在本发明优选的实施方案中,上述式I中的X是亚甲基、氧原子或-NH。更优选地,X是氧原子。
在本发明还优选的实施方案中,上述式I中的双键位于甾环系统的C5和C6之间,以致R3不存在。
在本发明还优选的实施方案中,上述式I中的R1=OH;R2=R5=R6=R7=Y=H且R4=Me。
在本发明更优选的实施方案中,上述式I中的R1=OH;R2=R5=R6=R7=Y=H,A=-(CH2)n-且B=-(CH2)y-;甾环系统的C1和C2之间不存在双键;双键位于甾环系统的C5和C6之间,以致R3不存在;且R4=Me。还更优选的是其中n=0且y=1的化合物。
在本发明最优选的实施方案中,其中式I的化合物选自下述化合物,包括它们药学上可接受的酯、盐及酸加成盐:
17β-螺环-[5-雄甾烯-17,2’-环氧乙烷基]-3β-醇;
(20S)-3β,21-二羟基-17β,20-环氧-5-孕烯;
(20S)-3β-羟基-17β,20-环氧-20-(2-溴乙炔基)-5-雄甾烯;和
3β,21-二羟基-17α,20-环氧-5-孕烯。
单独或组合使用的下列术语在此定义如下:
术语“烷基”在此表示直链或支链或环状饱和的烃基团。优选的是C1-C16烷基。除非另有特别限定,烷基可以是未被取代、单取代、或如果可能的话是多取代的,其取代基位于任何能够取代的位置。除非另有特别限定,环烷基包括单环、双环、三环和多环,例如金刚烷基、降莰基(norbornyl)和相关的萜烯。
术语“杂环烷基”在此表示包含1、2、3或4个O、N或S原子或O、N、S原子组合的环烃基团,例如环氧乙基、氧杂环丁基、四氢呋喃基、四氢-2H-吡喃基、吗啉基、乙烯亚氨基、氮杂环丁基、吡咯烷基、哌啶基、四氢噻吩基、四氢-2H-硫吡喃基。除非另有特别限定,杂环烷基可以是未被取代、单取代、或者如果可能的话是多取代的,其取代基位于任何能够取代的位置。
术语“卤素烷基”在此表示用一个或多个卤素取代的烷基。
术语“烯基”,单独或组合使用,在此表示包含至少一个碳-碳双键的直链或支链或环状不饱和的烃基团。除非另有特别限定,烯基可以是未被取代、单取代、或者如果可能的话是多取代的,其取代基位于任何能够取代的位置。优选的是C2-C16烯基。烯基意在包括具有两个相邻的双键的丙二烯基。
术语“杂环烯基”在此表示含有至少一个包含1、2、3或4个O、N或S原子或O、N、S原子组合的碳-碳双键的环状不饱和的烃基团。除非另有特别限定,杂环烯基基团可以是未被取代、单取代、或者如果可能的话是多取代的,其取代基位于任何能够取代的位置。
术语“炔基”,单独或组合使用,在此表示包含至少一个碳-碳三键的直链或支链或环状不饱和的基团。除非另有特别限定,炔基可以是未被取代、单取代、或者如果可能的话是多取代的,其取代基位于任何能够取代的位置。优1选的是C2-C16炔基。
术语“芳基”,单独或联合使用,在此表示包含至少一个具有共轭π电子的环的芳香基团、碳环芳基和联芳基,其可以是未被取代、单取代、或者如果可能的话是多取代的,其取代基位于任何能够取代的位置。优选的是C2-C10芳基基团。典型的芳基基团包括苯基、萘基、菲基、蒽基、茚基、薁基、联苯基、亚联苯基和芴基。
术语“联芳基”表示被其它芳基取代的芳基。
术语“碳环芳基”指其中芳香环上的原子是碳原子的基团。
术语“硫代”在此表示-SR10,其中R10是氢、烷基、烯基、炔基、芳基、芳基烷基或杂芳基,上述基团均为任选取代的。
术语“亚磺酰基”在此表示-SOR10,其中R10是氢、烷基、烯基、炔基、芳基、芳基烷基或杂芳基,上述基团均为任选取代的。
术语“磺酰基”在此表示-SO2R10,其中R10是氢、烷基、烯基、炔基、芳基、芳基烷基或杂芳基,上述基团均为任选取代的。
术语“亚磺酰氨基”在此表示-SO2NR10R11,其中R10和R11独立地是氢、烷基、烯基、炔基、芳基、芳基烷基或杂芳基,上述基团均为任选取代的。
术语“任选取代的”或“取代的”指被下述取代基在任何可能的位置取代的基团。对于上述部分,在本发明中有用的取代基是那些不会明显削弱本发明化合物生物活性的基团。不会明显削弱本发明化合物生物活性的取代基包括例如,低级烷基(脂肪族和环状的)、芳基(碳环芳基和杂芳基)、烯基、炔基、烷氧基、卤素、卤素烷基、氨基、烷基氨基、二烷基氨基、巯基、烷基硫基、烷基亚磺酰基、烷基磺酰基、硝基、烷酰基、烷酰氧基、烷酰氧烷酰基、烷氧基羧基、烷酯基、甲酰胺基、甲酰基、羧基、羟基、氰基、叠氮基、异氰基、异硫氰基、肟、酮及其环缩酮、烷酰基氨基、杂芳基氧、O-芳酰基、O烷基OH、O烯基OH、O炔基OH、O烷基NX1X2、O烯基NX1X2、O炔基NX1X2、NH-酰基、NH-芳酰基、CF3、COOX3、SO3H、PO3X1X2、OPO3X1X2,,SO2NX1X2、CONX1X2,其中X1和X2各自独立地表示H或烷基或烯基或炔基,或X1和X2共同包含具有大约4到大约7个环原子的杂环的一部分,和任选的选自O、N或S的一个额外的杂原子,或X1和X2共同包含具有大约5到6个环原子的酰亚胺环的一部分,且X3表示H、烷基、烯基、炔基、羟基-低级烷基或烷基-NX1X2。
术语“低级”与有机基团或化合物连用时在此表示包含1个,至多6个碳原子。这样的基团可以是直链、支链或环。
术语“杂芳基”指含碳的5-14元环状不饱和基团,其包含1、2、3或4个O、N或S原子并含有在一个或多个环上不定域的6、10或14个π电子,例如,噻吩基、苯并[b]噻吩基、石脑油[2,3-b]噻吩基、噻蒽基(thianthrenyl)、呋喃基、吡喃基、异苯并呋喃基、色烯基(chromenyl)、呫吨基、苯黄嘌呤基(phenoxanthinyl)、2H-吡咯基、咪唑基、吡唑基、吡啶基、嘧啶基、哒嗪基、中氮茚基、异吲哚基、3H-吲哚基、吲哚基、吲唑基、嘌呤基、4H-喹嗪基、异喹啉基、喹啉基、酞嗪基、萘啶基、喹唑啉基、噌啉基、蝶啶基、5aH-肼基甲酰基、肼基甲酰基、β-咔啉基、菲啶基、吖啶基、噁唑基、嘧啶基、苯并咪唑基、三唑基,上述任一基团都可以是如上述讨论中所述任选取代的。
本发明还包括式I化合物的药学上可接受的酯和盐,包括酸加成盐。
本领域技术人员将会确认存在于式I化合物的立体中心。由此,本发明包括作为混合物或纯的非对映异构体的式I所有可能的立体异构体和几何异构体。当需要一种单一的非对映异构体的式I化合物时,可通过终产物的分解或立体定向合成来获得,其中立体定向合成可从异构体纯的起始原料或使用任何合适的中间体进行合成。
包括于本发明范围内的是在此定义的式I化合物及其药学上可接受的盐或酸加成盐的结晶形式(例如多晶型物)、对映体形式和互变异构体形式。
一些式I的具体化合物是:
1)17β-螺环-[5-雄甾烯-17,2’-环氧乙烷基]-3β-醇(“BNN-50”)
2)(20S)-3β,21-二羟基-17β,20-环氧-5-孕烯(“BNN-124”)
3)(20S)-3β-羟基-17β,20-环氧-20-(2-溴乙炔基)-5-雄甾烯
4)3β,21-二羟基-17α,20-环氧-5-孕烯(“BNN-93”)
式I的化合物可以采用本领域技术人员熟知的常规合成反应通过市售的甾体化合物进行制备。其中X是氧原子的本发明优选的实施方案可通过重要的中间体(20S)-3β-(叔丁基二苯基甲硅烷基氧)-21-羟基-17β,20-环氧-5-孕烯进行制备,以合适的顺序采用了一系列的合成步骤,包括但不限于氧化、Wittig反应、还原、加氢、肟化、卤化、碳-碳偶联反应和去除C3上的保护基团。可使用除叔丁基二苯基甲硅烷基氧之外的其它合适的羟基保护基团。WO2008/155534描述了许多制备方法,其实施例中包含了BNN-50,BNN-93,BNN-124,(20S)-3β-羟基-17β,20-环氧-20-(2-溴乙炔基)-5-雄甾烯,3β,22-二羟基-17β,21-氧杂环丁基-5-孕烯和17β-螺环-[3β-羟基-5-雄甾烯-17,2’-环氧乙烷基-7-亚基氨基氧]-乙酸的具体的制备方法。
根据本发明的制剂可以标准方式给药用于治疗所述状态,包括但不限于口服、肠胃外、舌下、经皮、直肠、或通过吸入或含服给药。另外,本发明的组合物可配制成通过注射或连续输注的肠胃外给药的剂型。根据本发明的组合物可作为缓释剂型或长效制剂进行配制。给药途径可以是任何有效传递活性化合物至目标位置用以发挥其抗炎的效果的途径。任何本领域技术人员都可以将之前的描述扩展为任何其它的给药方法,而不会损害受试者。
当在本文中使用时,术语“治疗(treat)”或“治疗方法(treatment)”包括预防。通过根据公认步骤以足以在受试者、动物或人中产生期望药效活性无毒的量,将本发明的活性化合物或这种化合物的混合物与无毒的药学载体混合,以常规剂量单位形式制备本发明的药物化合物。优选地,组合物中包含活性成分的量为有活性而无毒性的,取决于期望的特定生物活性和患者的状态。
所使用的药学载体可以是,例如固体或液体。代表性的固体载体是乳糖、白土、蔗糖、滑石粉、明胶、琼脂、果胶、阿拉伯树胶、硬脂酸镁、硬脂酸、微晶纤维素、高分子水凝胶以及类似物。典型的液体载体是丙二醇、β-环糊精水溶液、糖浆、花生油和橄榄油以及类似乳状剂。同样地,载体或稀释剂可包括任何本领域公知的延时材料,例如单独使用单硬脂酸甘油酯或二硬脂酸甘油酯或联用蜡、微胶囊、微球体、脂质体、和/或水凝胶。
对于固体载体,其制备可以是简单研磨、微粉化或纳米化、油包、成片剂、硬明胶包被或在肠溶胶囊中以微粉化或丸剂的形态存在、或以含片、锭剂或栓剂的形式存在。对于液体载体,其制备可以是液体的形式,例如置于安瓿管中;或以混合有药学上可接受的防腐剂的水溶液或非水性悬液以及类似的形式进行。当需要低剂量时,也可以采用鼻腔喷雾、舌下施用和延时释放的皮肤药膏途径作为局部用药的给药形式。
实验部分
下列实施例用于更好地理解本发明,并不以任何方式作为对本发明范围的限制。
下列实施例用于研究在实验性自身免疫性脑脊髓炎和过敏性气管发炎过程中,脱氢表雄酮(DHEA)和其相关的螺环化合物BNN-50、BNN-93和BNN-124(上面定义的)是否在体外抑制对抗T细胞应答,以及在体内抑制对抗免疫-介导的疾病和应答。
实施例1
合成螺环甾体体外抑制T细胞应答的活性
由没有接触抗原的DO11.10T细胞受体转基因(DO11.10TCR Tg)小鼠(其对OVA肽323-329应答),培养淋巴结(LN)细胞,在DHEA或螺环化合物BNN-50,BNN-93和BNN-124或对照RPMI存在下用OVA进行刺激。用DHEA和螺环-类似物处理的结果是显著减少了对抗原应答的T细胞的增殖(图1)。
为了测定DHEA和其类似物是否对CD4+T细胞直接发挥其免疫抑制作用,由带有丝裂霉素C处理的脾细胞和OVA肽323-329的未接触抗原的DO11.10T细胞受体转基因(DO11.10TCR Tg)小鼠培养纯的CD4+T细胞。此外,用DHEA和螺环化合物处理的结果是显著减少白介素-2和γ-干扰素的分泌和增殖(图2)。当未接触抗原的BALB/c小鼠的纯CD4+T细胞用α-CD3/α-CD28(非抗原特异性)刺激时,检测到DHEA和螺环化合物具有相同的抑制作用(图3)。CD4+T细胞的增殖应答减少不是由于细胞死亡增加,通过在流式细胞检测分析后所有培养中的具有相似数量的CD4+7AAD-细胞得到证实(图4)。
总的来说,DHEA和螺环化合物BNN-93,BNN-124,BNN-50一般对T细胞应答具有免疫抑制作用。
实施例2
合成甾体化合物在防止MOG肽-诱导的实验性自身免疫脑脊髓炎(EAE)的能力。
为了评价DHEA和螺环化合物在体外的免疫抑制作用,进行了一项研究以确定DHEA及其螺环类似物是否能防止实验性自身免疫脑脊髓炎(EAE)。EAE是中枢神经系统(CNS)的自免疫状态,是由通过毁坏的自身反应T淋巴细胞和随后的脱髓鞘作用以及轴突与神经元变性的中枢神经系统的浸润引起的。
通过使小鼠免疫致病的鞘磷脂少突神经胶质细胞糖蛋白(MOG)肽(第35-55氨基酸),对C57BL/6小鼠诱导急性EAE。从EAE诱导的那天到第26天小鼠被处以安乐死为止,每天腹膜内给予BNN-93,BNN-124,BNN-50或DHEA(2mg/鼠)或PBS(对照)(图5)。小鼠的日常看护在临床表征(麻痹)采用盲式。收集组织(脑、脊索、DLNs)以进行组织学评价(用苏木素-伊红染色法(H&E)对脑和脊索切片进行染色)和体外培养用于测定T细胞应答和细胞因子的释放。
给予DHEA和螺环化合物导致麻痹水平的降低。总的来说,临床过程得到了改善和平均最大分数下降(图6和7)。与对照进行比较(图7),减少的临床分数与延缓发生和低的发病率相关。DHEA和螺环化合物的保护作用也与脊索内减少的炎症相关((图8)。
总的来说,螺环化合物和DHEA能防止EAE诱导的MOG肽,并有助于减少临床分数和发病率,延迟的疾病发生和降低在中枢系统的炎症。
在经过诱导发展成EAE的小鼠上,也测定了淋巴样细胞(T细胞)对MOG35-55肽的增殖反应和细胞因子分泌。来自用DHEA和螺环化合物处理的小鼠的引流淋巴结细胞,表明显著地降低了对MOG35-55肽的增殖(图9a)和γ-干扰素和白介素-10产生的数量大量地升高(图9b和图9c),通过最近几项研究表明其具有调控性质。另外,炎性细胞因子白介素-17的分泌增加(图9d),但是其绝对增加量与γ-干扰素的增加量相比是非常低。事实上,DHEA和螺环化合物显著增加γ-干扰素/白介素-17的比例(图9e),该结果与对EAE的保护效应一致。因此,DHEA和螺环化合物通过转移对高致病性Th17的应答向对较低致病性Th1的应答的平衡可以抑制EAE。
总的来说,这些结果表明用DHEA及其螺环类似物处理的结果是显著抑制致病性免疫应答。
进行试验以发现DHEA及其螺环类似物在实验性自身免疫脑脊髓炎(EAE)病初发后是否具有保护作用。对于这些试验,在C57BL/6小鼠上诱导急性的EAE与前面描述的相同。从EAE病症初起的那天到第26天小鼠被处以安乐死为止,每天腹膜内给予BNN-93,BNN-124,BNN-50或DHEA(2mg/只鼠)或PBS(图10)。小鼠的日常看护对临床表征(麻痹)采用盲式。收集组织(脑、脊索、DLNs)进行组织学评价(用苏木素-伊红染色法对脑和脊索切片进行染色)和体外培养用于测定T细胞应答和细胞因子的释放。给予DHEA和螺环化合物导致麻痹水平的降低。总的来说,临床过程得到了改善/逆转和平均最大分数下降(图11和12)。
在经过诱导发展成EAE的小鼠上,也测定了淋巴样细胞(T细胞)对MOG35-55肽的细胞因子分泌。来自用DHEA和螺环化合物处理的小鼠的引流淋巴结细胞,产生白介素-10的数量大大地增加(图13a)。另外,γ-干扰素以及细胞因子白介素-17的分泌也大量地增加(图13b和13c)。因此,DHEA和螺环化合物可以通过转移从高致病性Th17的应答向主要以生产白介素-10为特征的T调控细胞应答的平衡对EAE初发起后进行保护。
实施例3
合成甾体化合物在抑制TH-2免疫应答和防止过敏性气管炎症的活性。
使用建立的过敏性哮喘小鼠模型,在TH-2介导的免疫反应和随后疾病发展过程中,对DHEA和螺环化合物的体内效应进行了研究。BALB/c小鼠的致敏是通过在0和12天向腹膜内给予含0.01mg的鸡卵清白蛋白(OVA)的0.2ml明矾,和在第18-20天暴露在雾化OVA中(5%20min)。在第0,1,2,12,13,14,18,19和20.天,给予小鼠2mg/鼠的DHEA或螺环化合物(BNN-93或BNN-124或BNN-50)或PBS。
用DHEA或螺环化合物处理的小鼠在支气管肺泡灌洗(BAL)中,与PBS处理的小鼠相比,嗜酸性粒细胞和淋巴单核细胞的数量显著减少(图14a)。用DHEA和螺环化合物处理的小鼠的肺部白细胞浸润也显著减少(图14b)。此外,当检测来自于引流淋巴结的免疫反应时,发现用DHEA或螺环化合物处理导致OVA-特异性T细胞增殖的显著降低(图14c)。另外,用DHEA或螺环化合物处理的小鼠的OVA-特异性IgE,IgG1和IgG2a的水平显著降低。而且,用DHEA或螺环化合物处理的小鼠的CD3+CD4+CD25+Foxp3+T细胞(T调控细胞)和抑制CD11c+PDCA-1+的类浆树突状细胞(pDCs)的数量大量地增加。总的来说,这些结果提供证据证明了DHEA和螺环化合物抑制过敏性气管炎症,Th2应答和B细胞应答并发调控免疫细胞亚型的诱导。
实施例4
合成甾体化合物在抑制建立的MOG肽诱导的实验性自身免疫脑脊髓炎(EAE)的活性
进行了一项研究用于确定DHEA以及其螺环类似物对在小鼠种群中已经建立的EAE是否具有抑制效应
通过使动物免疫致病的鞘磷脂少突神经胶质细胞糖蛋白(MOG)肽(第35-55氨基酸),对C57BL/6小鼠诱导急性EAE。直到大约第12天出现疾病的症状(分数1-2),才对小鼠进行处理。从EAE诱导后的第13天起至第26-28天小鼠被处以安乐死为止,每天腹膜内给予BNN-93,BNN-124,BNN-50或DHEA(2mg/鼠)或PBS(对照)(图15)。小鼠的日常看护在临床表征(麻痹)上采用盲式。收集组织(脑、脊索、DLNs)以进行组织学评价(用苏木素-伊红染色法对脑和脊索切片进行染色)和体外培养用于测定T细胞应答和细胞因子的释放。
在疾病初起后开始给予的DHEA和螺环化合物导致麻痹水平的显著降低。总的来说,临床过程得到了显著改善和平均最大分数下降(图16和17)。DHEA和螺环化合物的保护作用也与脊索内减少的炎症相关((图18)。
总的来说,螺环化合物和DHEA抑制病程中的MOG肽诱导的EAE,并有助于减少临床分数和中枢神经系统的炎症。
在经过诱导发展成EAE的小鼠上,也测定了淋巴样细胞(T细胞)对MOG35-55肽的增殖反应和细胞因子分泌。来自用DHEA和螺环化合物处理的小鼠的引流淋巴结细胞,表明显著地降低了对MOG35-55肽的增殖(图19a)和γ-干扰素和白介素-10产生的数量大量地减少(19b和图19c),其具有炎性性质。这伴随引流淋巴结内和脑部内的Th17和Th1细胞的数量显著降低。另外,免疫调节细胞因子白介素-10的分泌增加(图19d)。此外,DHEA和螺环化合物显著增加IL-10+Treg细胞,该结果与对EAE的保护效应一致(图20)。因此,DHEA和螺环化合物通过减少致病性的Th1和Th17的免疫应答且增加Treg细胞从而可以抑制病程中的EAE。当疾病达到高峰(第17天)小鼠被处以安乐死时,获得了相似的结果(图21,22和23a,b,c)
总的来说,这些结果表明用DHEA及其螺环类似物治疗患有病程中的EAE的小鼠,结果是显著抑制了致病性免疫应答和症状。
实施例5
合成甾体化合物在转移的免疫细胞中抑制疾病的活性
进行了实验以确定已经被DHEA以及其螺环类似物抑制EAE的免疫细胞从一个小鼠种群继承性转移到另一个种群时是否还具有抗EAE的活性。
从在病初起之后(第12-17天)用DHEA或BNN-93处理患有EAE的小鼠中获得的引流淋巴结(DLN)细胞,将其继承性转移至患有病程中的EAE(大约在第12天)的受体上。与继承性转移有由PBS-处理的供体提供的DLN细胞的患有EAE的小鼠相比,发现这些DLN细胞对EAE的发展给予抑制,并导致快速的恢复和在平均最大疾病分数上的显著降低(图24和25)。供体DLN细胞在第17天时取得,相对于对照小鼠该天疾病达到了高峰。可以观察到这种保护,直到第28-30天小鼠被处以安乐死。从继承性转移有用DHEA或BNN-93处理的患有EAE的供体提供的DLN细胞的小鼠上获得的DLN细胞,显示对MOG35-55的体外增殖的显著降低和产生上层清液中γ-干扰素和白介素-17的减少(图26a,b,c)。另外,在分化和激活Th应答中起到支配性作用的CD11c+树突状细胞的募集,和高感染性的IL-17分泌T细胞,在引流淋巴结中大量地增加,且CD4+Foxp3+调控T细胞的募集增加(图27a,b,c)。
上面的结果表明用DHEA和螺环化合物治疗的小鼠发育了“带有”免疫调节能力的免疫细胞,通过在受体的转移能够调控和抑制病程中的疾病。
也进行了研究确定从用DHEA,BNN-93或PBS处理的EAE诱导的小鼠得到的CD4+T细胞(T辅助淋巴细胞)是否能够转移疾病抑制。从用DHEA或BNN-93处理的EAE诱导的小鼠获得的CD4+T细胞继承性转移到患有病程中的EAE的受体,在平均最大EAE分数上具有明显的降低(图28和29)。相反的,继承性转移从PBS-处理的EAE小鼠获得的CD4+T细胞,没有减少疾病。相应地,从继承性转移有用DHEA或BNN-9处理EAE供体获得的DLN细胞的小鼠中得到的DLN细胞和脾细胞,显示显著降低了对MOG35-55的体外增殖(图30)。
这些结果表明在EAE期用DHEA和螺环化合物处理,导致了CD4+T细胞的发育,其能够单独抑制病程中的EAE。
继承性转移从EAE诱导并用DHEA或BNN-93处理的小鼠获得的CD4+T细胞至不含有T和B细胞(C57BL/6Rag-/-)的受体小鼠,在百日咳毒素注射后诱导非常低的EAE分数使得没有疾病(BNN-93)(图31和32)。相反,继承性转移从PBS-处理的EAE诱导小鼠获得的CD4+T细胞在C57BL/6Rag-/-受体上导致了疾病的发展。从继承性转移有由DHEA或BNN-93处理的EAE供体提供的CD4+T细胞的受体小鼠中获得的DLN细胞,显示大量地降低了对MOG35-55的体外增殖和减少了γ-干扰素和白介素-17的产生(图33a,b,c)。这些结果表明来自处理的小鼠的CD4+T细胞具有显著的更低的致病性。
实施例6
合成甾体化合物在中断治疗后抑制疾病的活性
进行了实验以研究已经被DHEA和螺环化合物抑制EAE的免疫细胞是否可以在鼠种群中持续,即使在治疗中断后。
通过上述描述相同的方式对C57BL/6鼠进行EAE诱导,接着在病初起(大约13天)后用DHEA,BNN-93或PBS处理15天,然后终止治疗。在之后的另外45天内每天继续检测EAE的临床表征。之前用DHEA和BNN-93治疗只有15天的小鼠保持防止EAE的发展,而且它们的疾病分数保持没有变化,与继续表现高的分数疾病过程的对照小鼠相比,没有任何的恶化,(图34和35)
实施例7
合成甾体化合物在Th17分化和Foxp3+Treg细胞形成中的效应
在Th17细胞极化条件下(含有重组转化因子-β1和重组白介素-6)体外培养初始CD4+T细胞,用DHEA,BNN-93,BNN-124,BNN-50或RPMI(对照培养基)处理4天。用DHEA和螺环类似物的处理导致了CD4+IL-17-分泌T细胞数量的增加(图36)和CD4+IL-10-分泌T细胞数量的显著增加(图37),在Th17的分化细胞中,这些被认为具有重要的免疫调节性质。
另外,在Treg细胞形成条件下(含有重组转化因子-β1和重组白介素-2)体外培养初始CD4+T细胞,用DHEA或BNN-93,BNN-124,BNN-50或RPMI处理5天。用DHEA和螺环类似物,有或甚至没有重组转化因子-β1处理,导致了在Foxp3+Treg细胞数量的显著增加和增殖的增加(图38和39)。
这些结果表明DHEA和螺环化合物影响具有免疫抑制能力的CD4+T细胞亚群的分化和形成。
实施例8
对其他抗原(不是MOG)应答的界定实验
进行实验以研究免疫细胞对EAE发展中涉及的不同抗体的应答,其中免疫细胞中的EAE被DHEA和螺环类似物抑制。
C57BL/6鼠被诱导发展成EAE,并在疾病初起后很快开始用DHEA,BNN93或RPMI(对照)进行治疗15天。治疗停止后给小鼠注射OVA/CFA(弗氏完全佐剂)。每天监测小鼠的EAE临床表征,与对照小鼠相比,用DHEA或BNN93对其进行治疗,可以明显防止EAE,具有稳定的表型没有任何恶化。
在OVA/CFA免疫后,用DHEA或BNN93治疗的小鼠在体外显示T细胞对OVA应答的大量地增加(用3H-胸腺嘧啶脱氧核苷掺入量表示)(图40),γ-干扰素的产生量也增加。结果表明神经甾体抑制EAE,但是他们不能预防免疫细胞对除了这些包含在EAE发展中的抗原的应答。对小鼠暴露的新的抗原的应答是加强的。
Claims (24)
1.一种预防或治疗炎性状态的方法,包括给予患者有效量的式I化合物或其药学上可接受的酯、盐或酸加成盐:
其中
R1是羟基、烷氧基、烷酰氧基、氨基碳酰氧基或烷氧基碳酰氧基;
R2是氢、任选取代的烷基、任选取代的烯基、任选取代的烷氧基烷基、任选取代的氨烷基、氰基、任选取代的氰烷基、任选取代的硫氰烷基、异硫氰基、任选取代的叠氮烷基、任选取代的烷酰氧基烷基、任选取代的芳基烷基、任选取代的杂芳基烷基、任选取代的芳基烯基、任选取代的杂芳基烯基、任选取代的芳基、任选取代的芳基炔基、任选取代的芳基烷基炔基、任选取代的烷酰氧炔基、任选取代的杂芳基氧基炔基、任选取代的酮炔基或其缩酮、任选取代的氰基炔基、任选取代的杂芳基炔基、任选取代的羟基炔基、任选取代的烷氧基炔基、任选取代的氨基炔基、任选取代的酰氨基炔基、任选取代的巯基炔基、任选取代的羟基炔基二酸半酯或其盐、或任选取代的炔氧基炔基;或
R1是氧,且R2是烷基或烯基或炔基,其与R1键合形成可被任选取代的氧化环;
R3是氢,或当甾环系统的C5和C6之间存在双键时,R3不存在;
R4是氢或低级烷基;
R2是氢、氨基、任选取代的烷基氨基、任选取代的二烷基氨基、任选取代的烯基氨基、任选取代的二烯基氨基、任选取代的炔基氨基、任选取代的二炔基氨基、酰胺基、硫代、亚磺酰基、磺酰基、亚磺酰氨基、卤素、羟基、任选取代的烷氧基、任选取代的烯基氧基、任选取代的炔基氧基烷基、任选取代的烯基、任选取代的炔基、任选取代的芳基、叠氮基、任选取代的杂芳基、肟=N-O-R8、羧甲基肟、羧乙基肟、或羧丙基肟;
R6是氢、氨基、硫代、亚磺酰基、磺酰基、亚磺酰氨基、卤素、羟基、任选取代的烷氧基、任选取代的烷基、任选取代的烯基、或任选取代的炔基;
R7是氢、氨基、任选取代的烷基氨基、任选取代的二烷基氨基、任选取代的烯基氨基、任选取代的二烯基氨基、任选取代的炔基氨基、任选取代的二炔基氨基、酰胺基、硫、亚磺酰基、磺酰基、亚磺酰氨基、卤素、羟基、任选取代的烷氧基、任选取代的烯基氧基、任选取代的炔基氧基烷基、任选取代的烯基、任选取代的炔基、任选取代的芳基、叠氮基、任选取代的杂芳基、肟=N-O-R8、羧甲基肟、羧乙基肟、或羧丙基肟;
X是化合键,亚甲基(-CH2-)或选自氧、硫的杂原子,或-NH、-S(O)、-SO2、-NR8、-NC(O)R8、-N-甲苯-4-磺酰基氧;
A是-(CH2)n-、C2-5亚烯基、或C2-5亚炔基,其中n是整数,且可取值为0或1或2或3或4或5;
B是-(CH2)y-、C2-5亚烯基、或C2-5亚炔基,其中y是整数,且可取值为1或2或3或4或5;
Y可键合到在甾体骨架C17处的螺环取代基的任何碳原子上,且独立地是H、任选取代的C1-10烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的C2-10炔基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、甲酰基、羧基、-NC(O)R8、NC(S)R8、-NR8R9、任选取代的C(O)-W、任选取代的C(O)O-W、或任选取代的C(S)O-W;
Z可键合到在甾体骨架C17处的螺环取代基的任何碳原子上,且独立地是H、任选取代的C1-10烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的C2-10炔基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、甲酰基、羧基、-NC(O)R8、NC(S)R8、-NR8R9、任选取代的C(O)-W、任选取代的C(O)O-W、任选取代的C(S)O-W;
Y和Z可键合到C17处螺环取代基的同一碳原子上;
W是任选取代的C1-10烷基、任选取代的杂环烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的杂环烯基、任选取代的C2-10炔基、任选取代的杂环炔基、任选取代的芳基、或任选取代的杂芳基;
R8和R9独立地是任选取代的C1-10烷基、任选取代的杂环烷基、任选取代的稠双环系、任选取代的桥双环系、任选取代的桥三环系、任选取代的C2-10烯基、任选取代的杂环烯基、任选取代的C2-10炔基、任选取代的杂环炔基、任选取代的芳基、或任选取代的杂芳基;
以及点线表示可能存在的单键或双键。
2.根据权利要求1的方法,其中X是氧原子。
3.根据权利要求1的方法,其中X是亚甲基。
4.根据权利要求1的方法,其中X是-NH。
5.根据前述权利要求任一项的方法,其中甾环系统的C5和C6之间存在双键,以致R3不存在。
6.根据前述权利要求任一项的方法,其中R1=OH;R2=R5=R6=R7=Y=H且R4=Me。
7.根据权利要求1-4任一项的方法,其中R1=OH;R2=R5=R6=R7=Y=H,A=-(CH2)n-,B=-(CH2)y-;甾环系统的C1和C2之间不存在双键;甾环系统的C5和C6之间存在双键,以致R3不存在;R4=Me;n=0且y=1。
8.根据权利要求1的方法,其中式I的化合物选自下述化合物,包括它们药学上可接受的酯、盐及酸加成盐:
17β-螺环-[5-雄甾烯-17,2’-环氧乙烷基]-3β-醇;
(20S)-3β,21-二羟基-17β,20-环氧-5-孕烯;
(20S)-3β-羟基-17β,20-环氧-20-(2-溴乙炔基)-5-雄甾烯;
3β,21-二羟基-17α,20-环氧-5-孕烯。
9.根据前述权利要求任一项的方法,其中状态选自如下状态组成的组:哮喘、肺部炎症或视网膜炎性状态。
10.根据权利要求1-8任一项的方法,其中状态是自身免疫疾病。
11.根据权利要求10的方法,其中自身免疫疾病是类风湿性关节炎、I型糖尿病、全身性红斑狼疮,溃疡性结肠炎、炎性肠疾病或肌病。
12.根据权利要求10的方法,其中自身免疫疾病是重症肌无力、再生障碍性贫血,自身免疫性溶血性贫血、顽固性硬皮病、皮炎、获得性天疱疮、格雷夫斯病、自身免疫性肝炎、银屑病或克隆氏病。
13.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐,用于预防或治疗炎性状态。
14.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐,用于预防或治疗哮喘、肺部炎症或视网膜炎性状态。
15.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐,用于预防或治疗自身免疫疾病。
16.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐,用于预防或治疗类风湿性关节炎、I型糖尿病、全身性红斑狼疮,溃疡性结肠炎、炎性肠疾病或肌病。
17.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐,用于预防或治疗重症肌无力、再生障碍性贫血,自身免疫性溶血性贫血、顽固性硬皮病、皮炎、获得性天疱疮、格雷夫斯病、自身免疫性肝炎、银屑病或克隆氏病。
18.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐在制造用于预防或治疗炎性状态的药物中的应用。
19.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐在制造用于预防或治疗哮喘、肺部炎症或视网膜炎性状态的药物中的应用。
20.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐在制造用于预防或治疗自身免疫疾病的药物中的应用。
21.如权利要求20的应用,其中自身免疫疾病是类风湿性关节炎、I型糖尿病、全身性红斑狼疮,溃疡性结肠炎、炎性肠疾病或肌病。
22.如权利要求20的应用,其中自身免疫疾病是重症肌无力、再生障碍性贫血,自身免疫性溶血性贫血、顽固性硬皮病、皮炎、获得性天疱疮、格雷夫斯病、自身免疫性肝炎、银屑病或克隆氏病。
23.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐在控制或抑制人类或非人类动物体的免疫应答中的应用。
24.如权利要求1-8任一项定义的式I的化合物,或其药学上可接受的酯,盐或酸加成盐在控制或抑制人类或非人类动物体的T细胞活性中的应用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0916020.1 | 2009-09-11 | ||
| GB0916020A GB0916020D0 (en) | 2009-09-11 | 2009-09-11 | Use of steroid compounds |
| GBGB1009342.5A GB201009342D0 (en) | 2010-06-03 | 2010-06-03 | Use of steroid compounds |
| GB1009342.5 | 2010-06-03 | ||
| PCT/GB2010/001727 WO2011030116A1 (en) | 2009-09-11 | 2010-09-13 | Use of steroid compounds for inflammatory and autoimmune disorders |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102711769A true CN102711769A (zh) | 2012-10-03 |
Family
ID=43063384
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2010800404946A Pending CN102711769A (zh) | 2009-09-11 | 2010-09-13 | 甾体化合物在炎性和自身免疫疾病中的应用 |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US20120225852A1 (zh) |
| EP (1) | EP2475369A1 (zh) |
| JP (1) | JP5826750B2 (zh) |
| KR (1) | KR20120068026A (zh) |
| CN (1) | CN102711769A (zh) |
| AU (1) | AU2010293960B2 (zh) |
| BR (1) | BR112012008352A2 (zh) |
| CA (1) | CA2773600A1 (zh) |
| EA (1) | EA021840B1 (zh) |
| IL (1) | IL218503A0 (zh) |
| IN (1) | IN2012DN02613A (zh) |
| MX (1) | MX2012002834A (zh) |
| SG (1) | SG179049A1 (zh) |
| WO (1) | WO2011030116A1 (zh) |
| ZA (1) | ZA201202022B (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104027302A (zh) * | 2013-03-07 | 2014-09-10 | 中国医药工业研究总院 | 17α-乙炔基雄甾-5-烯-3β,7β,17β-三醇眼用制剂 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20210137960A1 (en) * | 2018-02-01 | 2021-05-13 | Yale University | Compositions and methods for inhibition of nuclear-penetrating antibodies |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0162330A1 (en) * | 1984-04-30 | 1985-11-27 | Roecar Holdings (Netherlands Antilles) N.V. | Use of sterolins and spiroketalins in the production of medicaments for the treatment of psoriasis |
| CN1021445C (zh) * | 1986-03-26 | 1993-06-30 | 鲁索-艾克勒夫公司 | 制备在位置17含有螺环的新的甾族化合物的方法 |
| WO2007025780A2 (en) * | 2005-09-02 | 2007-03-08 | Recordati Ireland Limited | Aldosterone receptor antagonists |
| WO2007103162A2 (en) * | 2006-03-01 | 2007-09-13 | Samaritan Pharmaceuticals, Inc. | Structure based drug design of steroidogenesis inhibitors |
| WO2008155534A2 (en) * | 2007-06-20 | 2008-12-24 | Bionature E.A. Ltd. | Neurosteroid compounds |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3365475A (en) | 1966-07-22 | 1968-01-23 | Merck & Co Inc | Process for the preparation of 17alpha-(3'-hydroxy-propyl)-4-androstene-3beta, 17beta-diol |
| DE2349023A1 (de) * | 1973-09-26 | 1975-04-10 | Schering Ag | Neue d-homo-steroide |
| DE2349022A1 (de) * | 1973-09-26 | 1975-04-10 | Schering Ag | Neue d-homo-steroide |
| US4054563A (en) | 1975-04-25 | 1977-10-18 | Ciba-Geigy Corporation | Process for the manufacture of spiro compounds of the steroid series |
| US4243586A (en) * | 1980-01-18 | 1981-01-06 | E. R. Squibb & Sons, Inc. | Steroidal-17-spiro-dihydrofuranones |
| US5846963A (en) * | 1995-06-07 | 1998-12-08 | University Of Utah Research Foundation | Methods for preventing progressive tissue necrosis, reperfusion injury, bacterial translocation and adult respiratory distress syndrome |
| US5994334A (en) | 1997-02-05 | 1999-11-30 | University Of Maryland | Androgen synthesis inhibitors |
| US20060004076A1 (en) * | 2004-06-30 | 2006-01-05 | Inflabloc Pharmaceuticals, Inc. | Co-administration of dehydroepiandrosterone (DHEA) congener with pharmaceutically active agents for treating inflammation |
-
2010
- 2010-09-13 SG SG2012016416A patent/SG179049A1/en unknown
- 2010-09-13 KR KR1020127009258A patent/KR20120068026A/ko not_active Application Discontinuation
- 2010-09-13 MX MX2012002834A patent/MX2012002834A/es active IP Right Grant
- 2010-09-13 BR BR112012008352A patent/BR112012008352A2/pt not_active IP Right Cessation
- 2010-09-13 EP EP10757115A patent/EP2475369A1/en not_active Withdrawn
- 2010-09-13 JP JP2012528448A patent/JP5826750B2/ja not_active Expired - Fee Related
- 2010-09-13 CN CN2010800404946A patent/CN102711769A/zh active Pending
- 2010-09-13 IN IN2613DEN2012 patent/IN2012DN02613A/en unknown
- 2010-09-13 AU AU2010293960A patent/AU2010293960B2/en not_active Ceased
- 2010-09-13 CA CA2773600A patent/CA2773600A1/en not_active Abandoned
- 2010-09-13 EA EA201270399A patent/EA021840B1/ru not_active IP Right Cessation
- 2010-09-13 WO PCT/GB2010/001727 patent/WO2011030116A1/en active Application Filing
- 2010-09-13 US US13/395,381 patent/US20120225852A1/en not_active Abandoned
-
2012
- 2012-03-06 IL IL218503A patent/IL218503A0/en unknown
- 2012-03-19 ZA ZA2012/02022A patent/ZA201202022B/en unknown
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0162330A1 (en) * | 1984-04-30 | 1985-11-27 | Roecar Holdings (Netherlands Antilles) N.V. | Use of sterolins and spiroketalins in the production of medicaments for the treatment of psoriasis |
| CN1021445C (zh) * | 1986-03-26 | 1993-06-30 | 鲁索-艾克勒夫公司 | 制备在位置17含有螺环的新的甾族化合物的方法 |
| WO2007025780A2 (en) * | 2005-09-02 | 2007-03-08 | Recordati Ireland Limited | Aldosterone receptor antagonists |
| WO2007103162A2 (en) * | 2006-03-01 | 2007-09-13 | Samaritan Pharmaceuticals, Inc. | Structure based drug design of steroidogenesis inhibitors |
| WO2008155534A2 (en) * | 2007-06-20 | 2008-12-24 | Bionature E.A. Ltd. | Neurosteroid compounds |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104027302A (zh) * | 2013-03-07 | 2014-09-10 | 中国医药工业研究总院 | 17α-乙炔基雄甾-5-烯-3β,7β,17β-三醇眼用制剂 |
Also Published As
| Publication number | Publication date |
|---|---|
| EA201270399A1 (ru) | 2012-10-30 |
| MX2012002834A (es) | 2012-04-10 |
| EP2475369A1 (en) | 2012-07-18 |
| BR112012008352A2 (pt) | 2016-03-22 |
| WO2011030116A1 (en) | 2011-03-17 |
| JP2013504551A (ja) | 2013-02-07 |
| SG179049A1 (en) | 2012-04-27 |
| CA2773600A1 (en) | 2011-03-17 |
| AU2010293960A1 (en) | 2012-04-12 |
| ZA201202022B (en) | 2013-05-29 |
| IL218503A0 (en) | 2012-07-31 |
| US20120225852A1 (en) | 2012-09-06 |
| IN2012DN02613A (zh) | 2015-09-04 |
| KR20120068026A (ko) | 2012-06-26 |
| AU2010293960B2 (en) | 2015-03-19 |
| JP5826750B2 (ja) | 2015-12-02 |
| EA021840B1 (ru) | 2015-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2773079T3 (es) | Métodos para el uso de progestágeno como sensibilizador de glucocorticoides | |
| Canonica et al. | Sub-lingual immunotherapy: World Allergy Organization position paper 2009 | |
| US20090214474A1 (en) | Compounds, methods, and treatments for abnormal signaling pathways for prenatal and postnatal development | |
| CN104159911A (zh) | 作为免疫调节剂的模拟肽化合物 | |
| TW200413374A (en) | Novel adenine derivative and its use | |
| JPS6075454A (ja) | 鎮痛用新規化合物および組成物 | |
| JPS6318600B2 (zh) | ||
| AU2008259864B2 (en) | Methods and compositions for administration of Oxybutynin | |
| CN103739647A (zh) | 用于治疗疾病的NF-κB的非激素甾体调节剂 | |
| CN102711769A (zh) | 甾体化合物在炎性和自身免疫疾病中的应用 | |
| Ye et al. | Strategies of mucosal immunotherapy for allergic diseases | |
| US20240124409A1 (en) | Guaianolide sesquiterpene lactone derivatives and pharmaceutical use thereof | |
| MX2015002898A (es) | Derivados de isoxazolidina. | |
| US7592327B2 (en) | Asthma/allergy therapy that targets T-lymphocytes and/or eosinophils | |
| Duan et al. | Dehydroepiandrosterone therapy ameliorates experimental autoimmune myasthenia gravis in Lewis rats | |
| GB1604644A (en) | Biologically active pentapeptide amides | |
| TW561141B (en) | Compounds for the treatment or prophylaxis of disorders mediated by s-CD23, the preparation and the pharmaceutical composition thereof | |
| CA2668580A1 (en) | Compounds, methods, and treatments for abnormal signaling pathways for prenatal and postnatal development | |
| US11352392B2 (en) | Artificially synthesized peptide H-473 and use thereof | |
| ES2267505T3 (es) | Tratamiento de asma/alergia teniendo como objetivo los linfocitos t y/o eosinofilos. | |
| CN115873062B (zh) | 一种熊果酸吡嗪衍生物及其应用、制备方法 | |
| RU2652752C1 (ru) | Способ лечения бронхиальной астмы | |
| Stanhope et al. | Problems in the use of pulsatile gonadotrophin-releasing hormone for the induction of puberty | |
| US20230124142A1 (en) | New therapeutic targets with an anti-inflammatory and anti-interferon effect | |
| US20160168190A1 (en) | C-20 steroid compounds, compositions and uses thereof to treat traumatic brain injury (tbi), including concussions |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| AD01 | Patent right deemed abandoned |
Effective date of abandoning: 20161019 |
|
| C20 | Patent right or utility model deemed to be abandoned or is abandoned |