CN102132160A - 与转移有关的信号和决定子以及它们的使用方法及用途 - Google Patents
与转移有关的信号和决定子以及它们的使用方法及用途 Download PDFInfo
- Publication number
- CN102132160A CN102132160A CN2009801331437A CN200980133143A CN102132160A CN 102132160 A CN102132160 A CN 102132160A CN 2009801331437 A CN2009801331437 A CN 2009801331437A CN 200980133143 A CN200980133143 A CN 200980133143A CN 102132160 A CN102132160 A CN 102132160A
- Authority
- CN
- China
- Prior art keywords
- determinant
- kinds
- host
- sample
- tumour
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6809—Methods for determination or identification of nucleic acids involving differential detection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/112—Disease subtyping, staging or classification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/118—Prognosis of disease development
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/56—Staging of a disease; Further complications associated with the disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/60—Complex ways of combining multiple protein biomarkers for diagnosis
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Analytical Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Physics & Mathematics (AREA)
- Biochemistry (AREA)
- Pathology (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- Biophysics (AREA)
- Hematology (AREA)
- Hospice & Palliative Care (AREA)
- Urology & Nephrology (AREA)
- Biomedical Technology (AREA)
- Cell Biology (AREA)
- General Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本发明提供了使用生物标记物检测癌症的方法。
Description
相关申请
本申请要求享有申请日为2008年6月26日的U.S.S.N.61/075933的权益,上述文献的全部内容在本发明中被引入作为参考。
发明的领域
本发明总体而言涉及到对生物信号以及遗传决定子的识别,其中所述的生物信号与癌症的转移有关,所述的遗传决定子能够影响癌症的转移,以及使用这样的生物信号和决定子的方法,用于进行癌症的筛选,预防,诊断,治疗,监测,以及预后。
发明的背景
转移是大多数致命性的固体肿瘤所具有的最重要的特征,并且表现为一种复杂的多步骤的生物学过程,这种生物学过程是由遗传性改变或者后成性改变的总体来驱动的,从而为肿瘤细胞赋予了这样的能力,使其能够绕过局部的控制并且经由周围的基质进行侵袭,在存活状态下转移过脉管系统或者淋巴腺,最终定植于外来的土地上并且生长(参见Gaorav P.Gupta以及Joan Massague(于2006年)在Cell《细胞》中发表的文章)。普遍的理论是:伴随着肿瘤的生长以及扩大,这种带来转移的遗传性事件可以通过随机的方式获得;的确,整体的肿瘤负荷是转移危险的阳性预测因素。从另外一个方面来说,越来越多的证据提出了这样的论题:某些肿瘤可能在所述的最初阶段被赋予了(或者不被赋予)转移的能力。通过对具有相当的早期阶段的肿瘤(即,类似的肿瘤负荷)之间存在的广泛变化的结果所进行的临床观察,对下述观点进行了支持:某些肿瘤在其生命史的早期对于转移而言是不可能发生的(“hard-wired”)。因此,已经表明,与其他的转移相比,一种转移的转录组学状态同与其相匹配的转移更为相似(参见Perou等人于2000年发表的文章)。除此之外,已经证明了在一个癌症基因组中,大规模的基因组失常在从良性阶段到恶性阶段的转化的早期发生(参见Chin,K.,de Solorzano,C.O.,Knowles,D.,Jones,A.,Chou,W.,Rodriguez,E.G.,Kuo,W.L.,Liung,B.M.,Chew,K.,Myambo,K.等人(于2004年)在Nat Genet《自然遗传学》36,984-988中发表的文章In situ analyses of genome instability in breast cancer《在乳腺癌中对基因组的不稳定性进行的原位分析》;Rudolph,K.L.,Millard,M.,Bosenberg,M.W.,以及DePinho,R.A.(于2001年)在Nat Genet《自然遗传学》28,155-159中发表的文章Telomere dysfunction and evolution of intestinal carcinoma in mice and human《在小鼠以及人类体内的端粒功能紊乱以及肠癌的演变》)。其他的作者包括Marcus Bosenberg,提出:在演变的早期阶段获得的遗传性事件的特定的补体将最终指定所述肿瘤的生物学行为,至少在一定程度上指定,其中所述的生物学行为包括它的转移的可能性。因此,我们断定,一个肿瘤的转移可能性的遗传性决定子预先存在于早期阶段的原发性恶性肿瘤之中,并且这样的决定子在恰好负责转移分配的过程中是功能上活化的。因此,这样的转移决定子不仅仅是可能的治疗靶向,而且是所述的癌症性疾病的侵蚀性的决定子,因此所述的转移决定子同样是预后决定子。
发明概述
本发明的一部分内容涉及到下述的发现:某些生物标记物(在本发明中被称之为“决定子(DETERMINANT)”)存在于宿主中或者在宿主中发生了改变,所述的宿主具有发展成为一种转移性肿瘤的增加的危险,其中所述的生物标记物例如是蛋白质,核酸,多形体,代谢物,以及其他的被分析物,以及某些生理学条件以及状态。
因此在一个方面本发明提供了一种方法,用以评价宿主中的一种转移性肿瘤的形成的危险。转移性肿瘤的形成的危险是通过下述方式来确定的:对存在于来自于所述宿主的样本之中的有效剂量的决定子(DETERMINANT)所具有的水平进行测量。转移性肿瘤的形成的增加的危险是通过下述方式来确定的:对存在于所述的样本之中的决定子(DETERMINANT)所具有的水平所发生的临床意义上显著的改变进行测量。或者可供选择的,转移性肿瘤的形成的增加的危险是通过下述方式来确定的:将所述的有效剂量的决定子(DETERMINANT)所具有的水平与一种参考值进行比较。在一些方面所述的参考值是一个指数。
在另外一个方面本发明提供了一种方法,用以评价宿主体内的肿瘤的恶化,所述的方法是通过下述方式来实现的:在第一个时间段内,对来自于所述宿主的第一个样本中的一种有效剂量的决定子(DETERMINANT)所具有的水平进行检测,在第二个时间段内对来自于所述宿主的第二个样本中的一种有效剂量的决定子(DETERMINANT)所具有的水平进行检测并且将检测到的所述决定子(DETERMINANT)所具有的水平与一种参考值进行比较。在一些方面所述的第一个样本是在接受针对所述肿瘤的治疗之前从所述的宿主处获取的并且所述的第二个样本是在接受了针对所述肿瘤的治疗之后从所述的宿主处获取的。
在一个进一步的方面本发明提供了一种方法,用以对治疗的有效性进行监测或者对治疗方案进行筛选,其中所述的治疗或者治疗方案是针对一种转移性肿瘤而言的,所述的方法是通过下述方式来实现的:在第一个时间段内,对来自于所述宿主的第一个样本中的一种有效剂量的决定子(DETERMINANT)所具有的水平进行检测并且任选的在第二个时间段内,对来自于所述宿主的第二个样本中的一种有效剂量的决定子(DETERMINANT)所具有的水平进行检测。将在所述的第一个时间段内检测到的所述的有效剂量的决定子(DETERMINANT)所具有的水平与在所述的第二个时间段内检测到的所述的水平进行比较,或者可供选择的将其与一种参考值进行比较。通过对来自于所述宿主的所述的有效剂量的决定子(DETERMINANT)所具有的水平的变化对治疗的有效性进行监测。
在另外一个方面本发明提供了一种方法,用以对患有肿瘤的患者进行治疗,所述的方法是通过下述方式来实现的:对患有肿瘤的患者进行识别,其中当在来自于所述肿瘤的样本中进行测量时,一种有效剂量的决定子(DETERMINANT)以一种临床意义上的显著的方式发生改变,并且利用一种治疗方案对所述的患者进行治疗,从而预防或者降低肿瘤的转移。
在一个方面本发明提供了一种方法,用以对需要接受辅佐治疗的肿瘤患者进行筛选,所述的方法是通过下述方式来实现的:通过对一种有效剂量的决定子(DETERMINANT)进行测量的方式来评价所述的患者发生转移的危险,其中在来自于所述患者的肿瘤样本之中的两种或者多种(DETERMINANT)所发生的临床意义上的显著的改变表明所述的患者需要接受辅佐治疗。
在一个进一步的方面本发明提供了一种方法,用以告知一种针对肿瘤患者的治疗决定,所述的方法是通过下述方式来实现的:获得关于存在于一个肿瘤样本之中的一种有效剂量的决定子(DETERMINANT)的信息,其中所述的肿瘤样本来自于所述的患者,并且选定一种能够在所述的患者体内预防或者降低肿瘤转移的治疗方案,其中在所述的治疗方案中两种或者更多种决定子(DETERMINANT)以一种临床意义上显著的方式发生了改变。
在各种不同的实施方式中,所述的评价/监测以一种预先确定水平的可预测性被得以实现。预先确定水平的可预测性指的是所述的方法提供了一种可以接受的水平的临床准确率或者诊断准确率。临床准确率以及诊断准确率是通过本领域已知的方法来确定的,例如通过在本发明中所描述的方法来确定的。
一个决定子(DETERMINANT)包括例如在本发明中所描述的决定子(DETERMINANT)1-360。对一个,两个,三个,四个,五个,十个或者更多个决定子(DETERMINANT)进行测量。优选的,对至少两个决定子(DETERMINANT)进行测量,所述的决定子选自决定子(DETERMINANT)1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271。任选的,本发明中所述的方法进一步的包括对至少一种与肿瘤有关的标准参数进行测量。
通过电泳的方式或者免疫化学的方式对一种决定子(DETERMINANT)所具有的水平进行测量。例如通过放射性免疫检测,免疫荧光检测或者通过酶联免疫吸附检测对所述的决定子所具有的水平进行检测。
所述的宿主患有一种原发性肿瘤,复发性肿瘤,或者转移性肿瘤。在一些方面所述的样本是在宿主先前已经接受过针对所述肿瘤的治疗的情况下获取的。或者可供选择的,所述的样本是在宿主接受针对所述肿瘤的治疗之前获取的。所述的样本是一种肿瘤的活组织切片例如核心活组织切片,一种切离组织的活组织切片或者一种切口组织的活组织切片,或者是一种带有流通的肿瘤细胞的血液样本。
同样被包括在本发明之中的是一种转移性肿瘤的参考表达曲线,所述的曲线中含有有效剂量的两种或者更多种标记物所具有的标记物水平的图案,其中所述的标记物选自决定子(DETERMINANT)1-360。优选的,所述的曲线中含有下述决定子(DETERMINANT)的标记物水平的图案:1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271。同样被包括在内的是一种计算机可读形式的介质,所述的介质中含有一个或者多个转移性肿瘤的参考表达曲线以及任选的,另外的测试结果以及宿主信息。在另外一个方面本发明提供了一种试剂盒,所述的试剂盒中包括大量的决定子(DETERMINANT)检测试剂,所述的试剂能够对相应的决定子(DETERMINANT)进行检测。所述的检测试剂例如是抗体或其片段,寡核苷酸或者适配子(aptamer)。
在一个进一步的方面本发明提供了一种决定子(DETERMINANT)小组(panel),所述的小组中含有一种或者多种决定子(DETERMINANT),所述的决定子(DETERMINANT)指示着肿瘤所发生的与生理学或者生物化学途径有关的转移或者肿瘤的恶化。所述的生理学或者生物化学途径包括例如,
在另外一个方面,本发明提供了一种识别生物标记物的方式,所述的生物标记物对于一种疾病而言是具有预后性的,所述的方式是通过下述来实现的:对一种或者多种基因进行识别,其中所述的基因与一种对照相比在所述的疾病中是发生了差异化的表达的,从而建立一个基因靶向列表;并且对存在于所述的靶向列表之中的一种或者多种基因进行识别,其中所述的基因与所述疾病的功能方面的进展是有关的。所述的功能方面例如是,细胞迁移,血管生成,细胞外基质降解或者失巢凋亡抗性。任选的,所述的方法包括对存在于所述的靶向列表之中的一种或者多种基因进行识别,其中所述的基因包括进化保守性的变化,从而建立了第二个基因靶向列表。所述的疾病例如是癌症例如是转移性癌症。
对能够调节一种决定子(DETERMINANT)所具有的活性或者表达的化合物进行识别,所述的识别是通过下述方式来实现的:提供一种表达所述决定子(DETERMINANT)的细胞,使所述的细胞与一种组合物发生接触(例如,体内,或者体外),其中所述的组合物中包括一种备选的化合物;并且确定所述的物质是否对所述的决定子(DETERMINANT)所具有的活性的表达进行了改变。如果在存在有所述化合物的条件下能够观察到所述的改变,而当所述的细胞与一种缺乏所述化合物的组合物发生接触时不能够观察到所述的改变,那么识别出所述的化合物能够对决定子(DETERMINANT)所具有的活性或者表达进行调节。
通过下述方式在宿主体内对癌症进行治疗:向所述的宿主施用一种化合物,所述的化合物能够对一种决定子(DETERMINANT)所具有的活性或者表达进行调节,或者向所述的宿主施用一种试剂,所述的试剂能够对一种化合物所具有的活性或者表达进行调节,其中所述的化合物受到一种决定子(DETERMINANT)的调节。所述的化合物可以是,例如,(i)一种决定子(DETERMINANT)多肽;(ii)编码一种决定子(DETERMINANT)的核酸;(iii)一种核酸,所述的核酸能够降低编码决定子(DETERMINANT)的核酸所具有的表达或者活性,其中所述的编码决定子(DETERMINANT)的核酸例如是,以及它的衍生物,片段,类似物和同系物;(iv)能够降低一种决定子(DETERMINANT)所具有的表达或者活性的多肽,例如是一种对所述的决定子(DETERMINANT)具有特异性的抗体。当在本发明中进行使用时所述的术语“抗体”(Ab)包括单克隆抗体,多克隆抗体,多重特异性抗体(例如,双重特异性抗体),人源化抗体或者人类抗体,Fv抗体,双功能抗体以及抗体片段,只要它们能够表现出所期望的生物活性即可。例如所述的化合物是转化生长因子β(TGFβ)并且所述的试剂是一种转化生长因子β(TGFβ)抑制剂。另外一个例子是趋化因子受体4(CXCR4)并且所述的试剂是一种趋化因子受体4(CXCR4)拮抗剂。
除非另外定义,当在本发明中进行使用时所有的技术术语以及科学术语具有与本发明所属领域的普通技术人员通常所理解的相同的含义。尽管与本发明中所描述的那些相类似的或者等价的方法以及材料可以被用在本发明的实践中,但适合的方法以及材料是下文中所描述的。在本发明中所提及的全部公开出版物,专利申请,专利,以及其他的参考文献均明确的以全部内容被引入作为参考。如果出现矛盾,本说明书,包括定义,将占主导地位。除此之外,在本发明中所描述的材料,方法,以及例子仅仅是说明性的并且并不意在构成限制。
本发明的其他特征以及优点将通过下述的详细描述以及权利要求而变得显而易见并且被涵盖在下述的详细描述以及权利要求的范围之内。
附图的简要描述
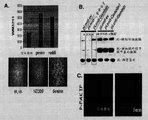
附图1表示的是黑素细胞特异性MET表达对皮肤恶性黑素瘤的形成的促进。(A)从指定的动物处收集黑素细胞并且使其适于进行培养。从经过培养的黑素细胞中提取总RNA,其中所述的黑素细胞是在存在或者不存在强力霉素(DOX)的条件下生长的,并且使用转基因特异性引物通过逆转录-聚合酶链式反应(RT-PCR)对MET的表达(Tg MET)进行检测。R15,核糖体蛋白R15内部对照;-RT,非逆转录聚合酶链式反应(PCR)对照(B)从存在强力霉素的iMet动物处收集原发性肿瘤(T1-T6)并且使用基因特异性引物通过逆转录-聚合酶链式反应(RT-PCR)对所述的黑素细胞标记物酪氨酸酶TRP1以及Dct的表达进行评价。XB2,小鼠角化细胞细胞系;B16F10,小鼠恶性黑素瘤细胞系;R15,核糖体蛋白R15内部对照;-RT,非逆转录聚合酶链式反应(PCR)对照。(C)在一个MET诱发的原发性恶性黑素瘤中,S100的黑素细胞特异性免疫组织化学染色。t,肿瘤;f,卵泡;fm,卵泡黑素细胞;a,脂肪细胞。(D)在一个MET诱发的原发性恶性黑素瘤中,全部的c-Met以及磷酸化的c-MET的免疫组织化学染色。(E)进行逆转录-定量聚合酶链式反应(RT-qPCR),用以分析人类生长因子(HGF)在MET诱发的原发性恶性黑素瘤(T1-T6)中的表达。对肿瘤的表达数据进行了正态化处理,使其在两种Ink4a/Arf-/-黑素细胞细胞系中表达。
附图2表示的是M的活化作用驱动了转移性恶性黑素瘤的形成并且促进了在肺部的接种。(A)在勃顿小室(Boyden chamber)内接种存在于不合有血清的培养基中的5x 104个iMet肿瘤细胞(BC014细胞系)。将小室放置于化学引诱剂(含有10%血清的培养基)中并且进行24小时的培养,其中在所述的化学引诱剂中不含有以及含有50纳克/毫升的重组人类生长因子(HGF)。通过利用结晶紫进行染色的方式使得入侵的细胞进行显现。(B)存在于一个iMet转基因小鼠的背部皮肤上的一种原发性皮肤梭形细胞恶性黑素瘤的苏木素-伊红染色(H&E)切片,这是通过强力霉素诱导的,以及发生在淋巴结肾上腺以及肺脏的远端转移。(C)向SCID小鼠的尾部静脉内注射5x105个细胞,在此之后经过肺部小结的形成,这与转移的播种有关联。左侧组:从SCID动物的尾部静脉内收集到的不含有小结的肺部组织的苏木素-伊红(H&E)染色切片,其中在所述动物的尾部静脉内注射有一种HRAS*恶性黑素瘤细胞系(0/4小鼠);右侧组:从SCID动物的尾部静脉内收集到的渗透有小结的肺部组织的苏木素-伊红(H&E)染色切片,其中在所述动物的尾部静脉内注射有所述的MET驱动的BC014细胞系(iMet)(3/4小鼠)。t,肿瘤。
附图3表示的是多维交叉品系的基因组分析,其中所述的分析与一种低复杂性的功能性遗传学筛选进行了偶联,用以识别转移决定子,其中所述的筛选针对的是细胞的入侵。(A)通过对来自于iHRAS*以及iMet皮肤恶性黑素瘤的表达曲线的微阵列显著性(SAM)分析的差异化表达的基因(1597个探针组)的相交,所述的相交是通过直系同源标定(ortholog mapping)来实现的,利用的是存在于人类转移性恶性黑素瘤的扩增区域以及缺失区域内的基因,或者利用的是存在于人类的原发性恶性黑素瘤与转移性恶性黑素瘤之间的差异化表达的基因,从而定义了360个备选物。(B)在iHRAS*与iMet小鼠恶性黑素瘤之间进行的差异化表达基因的Ingenuity途径分析(IPA)(1597个探针组,顶端)并且将交叉品系的整体的基因列表(360个过滤出的基因列表,底端)与9个随机抽取的基因组进行比较,其中所述的9个随机抽取的基因组具有相同的大小。所表示出的是前四位重要的功能性分类。虚线代表的是由Ingenuity途径分析(IPA)确定的显著性。(C)流程图描述的是关于入侵的低复杂性的遗传学筛选。230个克隆代表的是所述的295个经过上调节的备选物/扩增的备选物中的199个被分别转导至经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)中并且在96孔基质胶入侵培养板内对入侵作用进行检测,其中所述的备选物在一个慢病毒系统中进行了表达。经由荧光素介导的量化对入侵作用进行了测量并且利用绿色荧光蛋白(GFP)对照对所述的数值进行了正态化处理。在HMEL468或者在WM3211中,对在两项独立的筛选中(n=45)得分偏离向量对照超过两倍的标准偏差的备选物进行第二次的验证筛选,其中使用到标准的24孔基质胶入侵小室。(D)前侵基因的低复杂性遗传学筛选的柱状图概述。单独利用前转移性备选物cDNA病毒对经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)致敏的黑素细胞进行转导,在此之后将其装载于96孔transwell入侵检测培养板上。经由荧光素介导的量化对入侵作用进行了测量并且利用空白载体对照对所述的数值进行了正态化处理。在两次独立的筛选中出现的产生偏离绿色荧光蛋白(GFP)对照两倍标准偏差的入侵作用的备选cDNA被认为是第一次筛选所选中的(n=45)。(E)相对于对照31验证的转移性决定子而言,在入侵活性方面的增加倍数的柱状图概述。
附图4表示的是对代表性的决定子(A)Fascin1(FSCN1)以及(B)人热休克转录因子1(HSF1)的蛋白质表达所进行的自动化定量分析所述的自动化定量分析是在色素痣组织微阵列(TMA)上进行的,正如所述,所述的色素痣是原发性以及转移性恶性黑素瘤的肿瘤范例【参见Camp,R.L.,Chung,G.G.,& Rimm,D.L.(于2002年)在Nat Med《天然药物学》8(11),1323-1327中发表的文章Automated subcellular localization and quantification of protein expression in tissue microarrays《组织微阵列中的自动化的亚细胞定位以及蛋白质表达的量化》】。对自动化定量分析的得分进行信息核心的评价,其中所述的得分是分别对发生在所述的细胞质以及细胞核的细胞间隔内的FSCN1以及人热休克转录因子1(HSF1)的染色而言的。显著性(S;5%)是基于Fisher’s测试而言的。参见表格2中对于结果的概述。
附图5表示的是(A)K-均值聚类以及(B)卡普兰-迈耶(Kaplan-Meier)分析,所述的卡普兰-迈耶分析针对的是两个亚类别的整体存活组(顶端)以及不发生转移的存活组(底端),所述的亚类别来自于上文中所述的295个处于第I-II阶段的乳腺癌小组【乳腺癌数据来自于:van de Vijver,M.J.等人(于2002年)在N Engl J Med《新英格兰药物学杂志》347(25),1999-2009中发表的文章A gene-expression signature as a predictor of survival in breast cancer《作为乳腺癌存活的预测剂的基因表达信号》;van’t Veer,L.J.等人(于2002年)在Nature《自然》415(6871),530-536中发表的文章Gene expression profiling predicts clinical outcome of breast cancer《基因表达曲线对乳腺癌的临床结果所进行的预测》】。
附图6表示的是所述的体外失巢凋亡(anoikis)筛选方法。(A)体外失巢凋亡的筛选策略。(B)当被放置在具有低附着性的培养板上时,大鼠的肠道上皮(RIE)细胞具有降低的存活能力。将大鼠的肠道上皮(RIE)细胞放置在96孔超低聚集度(ULC)培养板上或者附着性培养板(adherent plate)上24小时。对用于表征细胞的存活能力的三磷酸腺苷(ATP)所具有的水平进行测量并且将其以在时间24小时/0小时下的水平的比率的形式给出。(C)大鼠的肠道上皮细胞(RIE)对V5-mTrkB的表达。大鼠的肠道上皮(RIE)细胞发生了感染并且在48小时时对细胞的溶解物进行分离并且利用十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)对其进行处理。利用α-V5抗体完成western印迹分析。
附图7表示的是各种不同的基因向大鼠的肠道上皮(RIE)细胞提供的失巢凋亡抗性。利用逆转录病毒对大鼠的肠道上皮(RIE)细胞进行感染,其中所述的逆转录病毒表达所述的备选基因中的一种,将上述细胞放置于超低聚集度培养板上并且在放置之后的24小时时对细胞所具有的存活能力进行测量。给出的数值是相对于0小时时的存活能力。对所有的读数均进行三次读取。高亮显示的是空白载体的读数,脑源性神经营养因子(BDNF)的读数或者mTrkB的读数(阳性对照)。
附图8表示的是二十个备选基因,其中所述的备选基因向大鼠的肠道上皮(RIE)细胞所提供的失巢凋亡抗性超过了所述中间值的两倍的标准偏差。在两次独立的筛选中,九个备选基因(HNRPR,CDC20,PRIM2A,HRSP12,ENY2,MGC14141,RECQL,STK3,以及MX2)给出了超过所述中间值的一倍的标准偏差。这些基因位于所述的被指定的染色体之中。
附图9表示的是在被保持在悬浮液中之后,基因为大鼠的肠道上皮(RIE)细胞提供的发生附着的能力。将表达一种备选基因的大鼠的肠道上皮(RIE)细胞放置在超低聚集度(ULC)培养板上24小时。将存在于悬浮液中的细胞转移到附着性培养板中并且在经过24小时之后利用结晶紫对发生附着的细胞进行染色。以24小时/0小时的形式给出细胞的存活能力。对所有的读数均进行三次读取。
附图10表示的是转移决定子对致肿瘤性的促进(A)经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)向SCID小鼠(n=6)中进行的皮下注射,其中所述的经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)细胞能够稳定的表达绿色荧光蛋白(GFP)或者指定的转移决定子,通过临床检查对所述小鼠的肿瘤形成进行监测。所表示出的是经过苏木素-伊红(H&E)染色的代表性的原发性肿瘤(t),所述的原发性肿瘤(t)表现出经过周围的肌肉纤维(m)以及脂肪细胞(a)而进行的局部入侵。(B)表格概括的是通过决定子驱动的致肿瘤性检测中收集到的数据。
附图11描述的是决定子HOXA1对细胞的入侵能力以及肺部的播种能力的促进。(A)HOXA1在经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)中的异常表达导致了粘附斑激酶(FAK)(Tyr 397;左侧组)的活化作用的增强,以及在transwell入侵检测中相应的入侵作用的增强,其中所述的入侵是进入基质胶的入侵(右侧组;在附图11C中对其进行了量化)。(B)对HOXA1-V5进行的western印迹分析,用以证实HOXA1在WM115以及WM3211转导细胞系中的表达(左侧组)以及所述的transwell入侵检测的代表性的图像(右侧组),其中所述的检测在附图11C中进行了量化。(C)对入侵小室数据的量化,其中所述的数据在附图11A-B中被呈现。(D)将稳定的表达绿色荧光蛋白(GFP)或者HOXA1的经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)细胞通过静脉内的方式注射至SCID小鼠(n=6)的尾部静脉内,并且在经过注射后的12周时对尸体进行肺部小结的检查。在50%的HOXA1组中(n=3)检测到了肉眼可见的(以及显微镜可见的)肺部小结但是在所述的对照中没有检测到肺部小结。从一种注射了经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)-HOXA1的动物处切离的肺部小结(t)以及周围的肺部软组织(1)的代表性的苏木素-伊红(H&E)显微镜照片。(E)将表达空白载体(EV)或者HOXA1的WM115恶性黑素瘤细胞通过皮下的方式注射至裸鼠体内并且在经过注射之后的46天时进行测量。(F)从裸鼠中分离出来的肺脏的代表性的转移,其中所述的裸鼠接受了皮层内注射的WM115-HOXA1细胞。
附图12表示的是HOXA1驱动的转录物组分析对Smad3网络的识别,所述的网络是由Ingenuity途径分析(IPA)来定义的。使用Iugenuity途径分析(IPA)(Ingenuity Systems Inc.)生成一个分子网络。所述的网络通过绘图的方式被显示为小结(基因)以及边缘(存在于小结之间的生物关联)。实线代表的是直接的相互作用而虚线代表的是间接的相互作用。红色以及绿色分别代表的是在所述的转录物组分析中发生过表达的基因或者低表达(under-expressed)的基因。所述的物体的形状代表着所述的蛋白质所属的功能家族。关于基因家族内容请参阅补充表格s3以及说明书。(B)使用逆转录-定量聚合酶链式反应(RT-qPCR)对指定的HOXA1转导细胞系进行SMAD3表达的评价。根据甘油醛磷酸脱氢酶(GAPDH)内部对照以及绿色荧光蛋白(GFP)试验对照对数值进行计算。误差条代表的是标准误差。
附图13表示的是HOXA1的异常表达对细胞入侵作用的增强,其中所述的入侵作用是经由所述的转化生长因子β(TGFβ)信号应答的上调节作用来实现的。(A)利用转化生长因子β(TGFβ)可诱导型3TP-Lux荧光素酶报告基因对WM115细胞进行转染,其中所述的WM115细胞能够异常的表达HOXA1,在此之后利用或者不利用转化生长因子β(TGFβ)进行处理,用以对与所述的绿色荧光蛋白(GFP)表达对照相比而言的应答性进行评价。误差条代表的是标准误差;双尾t-检验:-转化生长因子β(TGFβ):p=0.003;+转化生长因子β(TGFβ):p<0.0001。(B)使用指定的抗体,通过western印迹对来自于WM115细胞的全细胞溶解物进行分析,其中所述的WM115细胞能够稳定的表达绿色荧光蛋白(GFP)或者HOXA1,并且是在存在或者不存在转化生长因子β(TGFβ)的条件下在10%的血清或者1%的血清中繁殖的。(C)利用SMAD3 shRNA(shSMAD3)或者非靶向的shRNA(shNT)对WM115细胞进行转导,其中所述的WM115细胞能够稳定的表达HOXA1,并且将所述的细胞装载于基质胶transwell入侵小室之上,从而对细胞的入侵作用进行检测,所述的检测是与所述的WM115亲本细胞系进行比较而言的,其中所述的WM115亲本细胞系是利用绿色荧光蛋白(GFP)对照病毒(GFP)进行转导的。在右侧组中表示出的是入侵小室的代表性的图像。双尾t-检验:绿色荧光蛋白(GFP)vs.shNT,p=0.0008;shNT vs.shSMAD3,p=0.0022。(D)将能够表达空白载体(EV)或者HOXA1的WM115恶性黑素瘤细胞通过皮下的方式注射至裸鼠体内。利用抗-膦-SMAD3对上述得到的异种移植物的肿瘤切片进行免疫染色,用以证实在HOXA1肿瘤范例中SMAD3的活化作用。
附图14。在经过向SCID小鼠进行的静脉内尾部静脉注射之后,利用HRAS*进行转导的来自于Ink4a/Arf-/-小鼠的黑素细胞(M3HRAS)表现出下述性质,其中HRAS*能够对FSCN1或者HOXA1进行过表达:(A)在tranwell入侵检测中向基质胶中的增强的入侵作用(B)在裸鼠中增强的皮下肿瘤的生长以及(C)增强的肺部小结的形成。需要注意的是在C中,所述的FSCN1组的肺脏/体重指数的差异不显著,这归因于在所述的检测终点时这些动物具有的相对良好的健康状况,其中所述的检测终点是由极端病态的HOXA1组所指定的。
附图15表示的是利用RNA来进行定量的聚合酶链式反应(qPCR),其中使用RT2Profiler聚合酶链式反应(PCR)阵列(Supperarray)对与转移有关的一组基因的表达进行分析,其中所使用的RNA是从下述细胞中分离得到的:(A)WM115恶性黑素瘤细胞以及(B)转化的人类黑素细胞(HMEL468),所述的黑素细胞能够表达空白载体(对照组)或者HOXA1(组1)。利用抗趋化因子受体4(CXCR4)对上述得到的异种移植物的肿瘤切片进行免疫染色,用以证实在HOXA1肿瘤范例中的过表达(附图13)。所表示出的是符合差异化表达的阈值的基因,其中所述的差异化表达是存在于对照组与试验组之间的差异化表达。
附图16表示的是将WM115恶性黑素瘤细胞以及经过转化的人类黑素细胞(HMEL468)通过皮下的方式向裸鼠体内的注射,其中所述的经过转化的人类黑素细胞(HMEL468)能够表达空白载体(EV)或者HOXA1。利用抗趋化因子受体4(CXCR4)对上述得到的异种移植物的肿瘤切片进行免疫染色,用以证实在HOXA1肿瘤范例中的过表达。
附图17表示的是(A)在Spitz色素痣组以及恶性黑素瘤的福尔马林固定石蜡包埋(FFPE)的样本组中对UBE2C的RNA表达所进行的QuantiGene分析。(B)利用指定的载体对原发性的Ink4a/Arf-缺陷型小鼠胚胎成纤维细胞(MEF)进行转染,其中所述的载体能够表达HRASV12,MYC以及UBE2C。Vec=LacZ载体对照;条状代表的是+/-标准偏差。
附图18表示的是(A)在transwell入侵检测中对WM3211恶性黑素瘤细胞向基质胶中的入侵作用进行检测,其中所述的WM3211恶性黑素瘤细胞能够稳定的表达空白载体(ev),Geminin或者Nedd9(阳性对照)。(B)对从WM3211细胞中提取出来的整体的细胞溶解物进行免疫印迹分析,其中所述的WM3211细胞能够稳定的表达空白载体(ev),Geminin或者小窝蛋白(Caveolin)1(阴性对照)。抗-膦粘附斑激酶(FAK)以及抗-膦细胞外信号调节蛋白激酶(ERK)分别代表的是被活化的粘附斑激酶(FAK)以及细胞外信号调节蛋白激酶(ERK)物种。(C)针对膦-粘附斑激酶(FAK)(P-FAK;红色)对能够稳定的表达空白载体(EV)或者Geminin(GEMN)的WM3211细胞进行免疫染色,用以证实在附图18B中观察到的粘附斑激酶(FAK)的活化作用的增强。
发明的详细说明
本发明涉及到对信号以及决定子的识别,其中所述的信号与转移性肿瘤或者发展成为一种转移性肿瘤的危险有关,并且所述的决定子意味着宿主具有一种转移性肿瘤或者宿主具有发展成为一种转移性肿瘤的危险。
已经证实了在人类和小鼠的数据组之间进行的交叉品系的比较能够提供一种生物过滤器,用于对诱因性的癌症基因进行识别,其中所述的癌症基因与人类的恶性黑素瘤生物学相关。在现在的研究中,使用两个恶性黑素瘤的小鼠模型来进行基因的识别,其中所述的基因在转移中发生了差异化的表达,所述的小鼠模型所具有的原发性肿瘤表现出明显的发生转移的可能性。在原发性肿瘤之间进行的表达曲线的比较识别出了一份1597个差异化表达的基因的列表,其中所述的基因已经通过生物过滤被区分了优先次序,并且与扩增以及缺失的图案发生了重叠,其中所述的原发性肿瘤来自于转移性的(iMet)以及非转移性的(iHRAS*)遗传工程化小鼠(GEM)模型,所述的生物过滤是通过交叉品系分析来实现的,所述的扩增以及缺失的图案是通过阵列-比较基因组杂交(CGH)来获得的。可以设想,进化保守性变化(例如,在小鼠以及人类中)更为可能是至关重要的;因此,利用基因组数据对来自于所述的遗传工程化小鼠(GEM)模型(其优点在于具有定义的遗传学背景以及清楚的表型关系)的表达数据进行的三角剖分能够允许进行优先次序的排列并且指定了人类与所述的1597个备选物之间的关联。
已经识别出由295个上调节/扩增的基因以及65个下调节/缺失的基因组成的一种受表型驱动的进化保守型转移备选物列表,所述的列表是通过下述方式来进行识别的:对两个经过基因工程化处理的小鼠皮肤癌恶性黑素瘤模型所具有的转录物组进行比较,其中所述的两个小鼠模型具有差异化的转移可能性,在此之后利用人类原发性恶性黑素瘤以及转移性恶性黑素瘤所具有的基因组曲线以及转录物组曲线进行三角剖分。使这些备选物纳入到低复杂性的遗传学筛选之中,所述的筛选针对的是入侵作用,失巢凋亡抗性或者在流通以及定植作用中的存活,它们对应的是在转移性蔓延中的三个主要的步骤(即,从所述的原发性肿瘤位点处的逃离,流通,最终在远端的外源位点上发生定植以及增殖)。到目前为止,所述的入侵筛选已经定义了三十一种(31)有效的转移决定子,所述的转移决定子能够为经过端粒酶逆转录酶(TERT)永生化处理的人类黑素细胞468以及恶性黑素瘤细胞提供前侵活性。可以预料到的是,通过对失巢凋亡抗性或者定植作用的筛选,所述的转移备选物的独立的子集将被定义为另外的决定子,所述的决定子仅仅在一定程度上,如果还会的话,与来自于所述的入侵筛选的决定子发生重叠。到目前为止,所述的失巢凋亡抗性筛选已经定义了九种(9)有效的决定子,所述的决定子能够为悬浮液提供存活性,而不与所述的入侵作用决定子发生重叠。这些决定子将共同或者作为一个子集来适用于在转移分配作用中所涉及到的主要步骤。
已经认识到,原发性肿瘤在遗传学意义上是多样化的。如果在一个原发性肿瘤之中的亚群体中的转移决定子能够为所述的原发性肿瘤提供增殖的益处并且最终驱动其向远端位点处的分配,那么可以预料到的是,相对于其原发性的副本而言,所述的转移性衍生物将更为均一化并且因此对于这样的转移决定子而言将出现一种与恶化相关联的表达类型。为了对25种这样的决定子所具有的表达类型进行评价,我们利用在Oncomine上的表达曲线数据一览表(参见Rhodes D.R.等人于2004年在Neoplasia《瘤的形成》6,1-6中发表的文章ONCOMINE:a cancer microarray database and integrated data-mining platform《ONCOMINE:一个癌症微阵列数据库以及综合的数据采集平台》)。然而,尽管这25种转移决定子中的绝大部分还没有被明确的包含在入侵或者或者转移之中,但是它们中的每一种均在恶性黑素瘤以及非恶性黑素瘤固体肿瘤中表现出一种表达类型,所述的表达类型与增加的肿瘤级别或者预后具有显著的关联。例如,相对于原发性疾病而言,在所述的25种决定子中有12种在转移性疾病中表现出了增加的表达。在脑(神经胶质瘤)肿瘤中,有13种所述的转移决定子表现出了与恶化相关的表达类型,即,在更高阶段的神经胶质瘤中的增加的表达,其中所述的脑(神经胶质瘤)肿瘤是类似于恶性黑素瘤的另外一种间叶细胞样肿瘤。在这些决定子中,有6种表现出与结果的阳性相关性。在前列腺腺癌中,从原发性到转移性,所述的转移决定子中有十种表现出了在表达方面的显著的增加。在肺部,有五种表现出了与增加的肿瘤级别之间的相关性。在乳腺癌中观察到了最为显著的重叠,其中在所述的25种转移决定子中有13种表现出了与肿瘤恶化的阶段或者肿瘤恶化的级别之间的相关性;此外,有13种所述的决定子被报告为与预后存在相关性。
因此,本发明提供了用以对宿主进行识别的方法,其中所述的宿主患有一种转移性肿瘤,或者存在经历一种转移性肿瘤的危险,所述的方法是通过下述方式来实现的:对与所述的转移性肿瘤有关的决定子进行检测,包括那些对于所述的转移性肿瘤而言是无症状的宿主。这些信号以及决定子同样可以被有效的用于对宿主进行监测,其中所述的宿主正在接受针对癌症的处置以及治疗,并且可以被有效的用于对治疗以及处置方案进行筛选或者修饰,其中所述的治疗以及处置方案对于患有癌症的宿主而言应当是有效的,其中对这些处置方案以及治疗的筛选以及使用能够减慢所述肿瘤的恶化,或者在本质上延缓或者阻止其发作,或者降低或阻止所述的肿瘤发生转移的发病率。
定义
“准确率”指的是一种被测量得到的质量或者被计算得到的质量(一种测试所报告的数值)与其实际(或者真实)值之间的一致性程度。临床准确率涉及到所述的真实结果(真实阳性(TP)或者真实阴性(TN))占错误分类结果(假阳性(FP)或者假阴性(FN))的比例,并且其可以被称为敏感度,特异性,阳性预测值(PPV)或者阴性预测值(NPV),或者除了其他的测量物之外,作为一种可能性,还可以被称为让步比。
“决定子”在本发明的上下文中涵盖了,但不局限于,蛋白质,核酸,以及代谢产物,以及它们的多形体,变异形式,变体,修饰形式,亚单元,片段,蛋白-配体复合物,以及降解产物,蛋白-配体复合物,元素,相关的代谢产物,以及其他的分析物或者来源于样本的测量物。决定子同样可以包括变异的蛋白质或者变异的核酸。决定子同样能够涵盖非血液中产生的因子或者健康状态的非分析物生理学标记物,例如在本发明中所定义的“临床参数”,以及同样在本发明所定义的“传统实验室危险因素”。决定子同样包括任何通过计算得到的指数,其中所述的指数是通过数学的方法或者通过前述测量方法中的任意一种或者多种的组合而建立的,包括暂时性的趋势以及差异。在可以利用的情况中,并且除非在本发明中另有描述,当决定子是基因产物时,可以根据所述的官方的字母缩略语或者被指定的基因符号对所述的决定子进行识别,其中所述的基因符号是由国际人类基因命名委员会(international Human Genome Organization Naming Committee(HGNC))指定的,以及在本申请日前在所述的美国生物技术信息中心(US National Center for Biotechnology Information(NCBI))网页(http://www.ncbi.nlm.nih.gov/sites/entrez?db=gene)上所列出的,其同样被称之为Entrez基因(Entrez Gene)。
“决定子(DETERMINANT)”或者“DETERMINANTS”涵盖了全部的核酸或者多肽中的一种或者多种,其中所述的核酸或者多肽所具有的水平在宿主体内发生了变化,所述的宿主患有一种转移性的肿瘤或者存在发展成为一种转移性肿瘤的倾向,或者存在形成一种转移性肿瘤的危险。在表格1中对各种决定子(DETERMINANT)进行了概括并且在本发明中尤其将它们统称为“转移性肿瘤相关性蛋白质”,“决定子(DETERMINANT)多肽”,或者“决定子(DETERMINANT)蛋白质”。编码所述多肽的相应的核酸被称之为“转移性肿瘤相关性核酸”,“转移性肿瘤相关性基因”,“决定子(DETERMINANT)核酸”,或者“决定子(DETERMINANT)基因”。除非另外指明,“决定子(DETERMINANT)”,“转移性肿瘤相关性蛋白质”,“转移性肿瘤相关性核酸”意在指的是在本发明中所公开的序列中的任意一个。所述的决定子(DETERMINANT)蛋白质或者核酸所具有的相应的代谢物同样是可以被测量的,以及上述提及的传统危险标记物代谢物中的任意一种。
健康状态的生理学标记物(例如,年龄,家族历史,以及普遍被用来作为传统的危险因素的其他测量值)被称之为“决定子(DETERMINANT)生理学”。经过计算得到的指数被称之为“决定子(DETERMINANT)指数”,其中所述的指数是通过数学的方法将一种或者多种测量值进行组合来建立的,其中所述的测量值优选为两种或者多种,是针对前述提及的决定子(DETERMINANT)类型所进行的测量。
“临床参数”涵盖了所有的宿主健康状态的非样本生物标记物或者非分析物生物标记物或者其他的特征,例如,但不局限于,年龄(Age),种族(RACE),性别(Sex),或者家族历史(FamHX)。
“循环内皮细胞”(“CEC”)是一种来自于血管内壁的内皮细胞,所述的内皮细胞能够在某些条件下散落在血流之中,所述的条件包括炎症,并且促成了与癌症的发病机理有关的新的脉管系统的形成。循环内皮细胞(CEC)能够被有效的用来作为一种肿瘤恶化的标记物和/或针对抗血管生成治疗的应答的标记物。
“循环肿瘤细胞”(“CTC”)是一种来源于上皮的肿瘤细胞,所述的肿瘤细胞能够在发生转移时从所述的原发性肿瘤处散落,并且进入到所述的循环之中。在患有转移性癌症的患者体内,存在于外周血之中的所述循环肿瘤细胞的数量与预后有关。可以对这些细胞进行分离并且使用能够检测上皮细胞的免疫方法对其进行量化。
“FN”指的是假阴性,当其被用在一种疾病状态的测试中时,指的是将一个患有疾病的宿主错误的分类为未患有疾病或者正常。
“FP”指的是假阳性,当其被用在一种疾病状态的测试中时,指的是将一个正常的宿主错误的分类为患有疾病。
“公式”、“运算法则”、或者“模型”指的是任何的数学等式,算法,解析过程或者程序化的过程,或者统计学技术,其能够进行一个或者多个连续的或者分类的输入(在本发明中被称为“参数”)并且计算出一个输出值,有时其被称之为“指数”或者“指数值”。“公式”的非限制性的例子包括求和操作,比例操作,以及回归操作,例如系数或者指数,生物标记物值的转化以及正态化(包括,但不局限于,那些基于临床参数的正态化方案,其中所述的临床参数是例如性别,年龄,或者种族),标准以及指导方针,统计学分类模型,以及已经在历史群体中训练得到的神经网络。当在组合的决定子(DETERMINANT)以及其他的决定子中进行特定的使用时,其是线性等式以及非线性等式,以及统计学分类分析,用以确定存在于一个宿主样本中的所述决定子(DETERMINANT)所具有的水平与所述的宿主所存在的发生转移性疾病的危险之间存在的关系。在评判小组(panel)以及混合结构中,特别感兴趣的是结构以及合成统计分类运算法则,以及用来进行危险指数构建的方法,其中所述的方法利用到了图案识别的特征,包括已经建立的技术例如交叉相关,主成分分析(PCA),因素轴转,吉斯回归(LogReg),线性判断分析(LDA),Eigengene线性判断分析(ELDA),支持向量机(SVM),随机森林(RF),递归分割树(RPART),以及除此之外的其他相关的决策树分类技术,缩小重心(SC),StepAIC,K最近邻取样,Boosting,决策树,神经网络,贝叶斯网络,支持向量机,以及隐式马可夫模型。可以被用在存活率以及事件时机危险分析中的其他技术包括Cox比例风险模型,可靠性和寿命数据分析(Weibull),卡普兰-迈耶(Kaplan-Meier)模型以及Greenwood模型,这些均是本领域技术人员所熟知的。这些技术中的许多在用来与一种决定子(DETERMINANT)筛选技术进行组合使用时同样是有效的,其中所述的决定子(DETERMINANT)筛选技术例如是前向选择,后向选择,或者逐步选择,在一种给定大小的范围内对所有可能的小组进行的全数调查,遗传运算法则,或者它们本身可以包括以它们自己的技术来完成的生物标记物筛选方法。可以将这些与信息准则进行偶联,其中所述的信息准则是例如赤池信息准则(Akaike’s Information Criterion)(AIC)或者贝叶斯信息准则(Bayes Information Criterion)(BIC),其目的在于对存在于另外的生物标记物与模型改进之间的折衷进行量化,并且帮助对这种过度拟合进行最小化。上述得到的预测模型可以在其他的研究中对其进行验证,或者在它们最初进行训练的研究中对其进行交叉验证,其中所述的验证或者交叉验证使用的是这样的技术例如Bootstrap仿真程序,留一法(LOO)以及10倍交叉验证(10-Fold CV)。在各种不同的步骤中,可以通过数值的置换检验对错误发现率进行估算,这可以依照本领域已知的技术来实现。“健康经济利用率函数(health economic utility function)”是一种来自于一定范围内的临床结果的预期概率的组合的一个公式,其中所述的临床结果来自于一个理想化的可以适用的患者群体,其得自于在向所述的标准治疗过程中插入诊断性干预或者治疗性干预之前以及之后。其涵盖了对这种干预所具有的下述参数的估算:准确率,有效性以及性能特征,以及与每一种结果相关的成本和/或价值测量(利用率),所述的结果可以来自于真实的医疗卫生系统成本(服务,补给,设备以及药物,等等)和/或一种估算得到的可以被接受的在每一个质量调整生命年(QALY)中的价值,其中所述的价值是能够产生每一种结果的价值。将产生一种结果的参与预测的所述群体的大小乘以各自结果的预期可利用率,将所有的预测结果的上述乘积求和,就得到了对于一种给定的标准治疗而言的整体的健康经济利用率。在(i)存在所述干预的情况下,计算得到的所述标准治疗所具有的总体的健康经济利用率与(ii)不存在所述干预的情况下,计算得到的所述标准治疗所具有的总体的健康经济利用率之间所存在的差异产生了对所述的干预而言的健康经济成本或者价值的整体测量值。可以将该数值除以参与进行分析的整体的患者组(或者单独的除以所述的干预组),从而获得了每一个单位干扰所具有的成本,并且能够对下述决策起到指导作用,其中所述的决策是:市场定位,定价,以及对健康系统的接受程度的设想。这样的健康经济利用率函数是普遍被使用的,用以对所述的干预所具有的成本-有效性进行比较,但是同样可以对上述函数进行转化,用以估算在每一个质量调整生命年(QALY)中有意愿对所述的健康治疗系统进行购买的可接受值,或者用以估算一种新的干预所需要具有的可接受的成本-有效性临床性能特征。
对于本发明中所述的诊断性的(或者预后性的)干预而言,由于每一种结果(这在一项疾病分类诊断性测试中可以是一种真阳性,假阳性,真阴性,或者假阴性)承受着不同的成本,一个健康经济利用率函数可能对敏感度而不是特异性进行优先的证明,或者可能对阳性预测值(PPV)而不是阴性预测值(NPV)进行优先的证明,这是根据所述的临床状况以及各个结果所具有的成本以及价值来决定的,并且因此提供了另外一种健康经济性能以及价值的测量值,所述的测量值可能与更直接的临床性能测量值或者分析性能测量值存在差异。这些不同的测量值及其相关的折衷值一般而言仅仅在一种完美的测试中才能会聚在一点,具有零错误率(或者换句话说,有零个被预测的宿主的结果是被错误分类的或者是假阳性的以及假阴性的),其中所有的性能测量值都将偏向于不完整性,只是在程度上有所不同。
“测量”或者“测量方法”,或者可供选择的“检测”或者“检测方法”,指的是在一个临床样本或者来自于宿主的样本中,对一种任意给定的物质的存在、不存在、质量、活性或者剂量(其可能是一种有效剂量)所进行的评价,包括这样的物质所具有的定性的浓度水平或者定量的浓度水平的衍生,或者另外的对一种宿主的非分析物临床参数所具有的价值或者分类所进行的评价。
“阴性预测值”或者“NPV”是由真阴性(TN)/(真阴性+假阴性)计算得到的,或者是由所述的真阴性部分占全部的阴性测试结果的比例计算得到的。其同样会固有的受到所述疾病的流行程度的影响,以及所述群体所具有的测试前概率的影响,其中所述的群体是意在接受测试的群体。
参见,例如,O’Marcaigh AS,Jacobson RM于1993年在Clin.Ped.《儿科临床学》32(8):485-491中发表的文章“Estimating The Predictive Value Of A Diagnostic Test,How To Prevent Misleading Or Confusing Results《对一种诊断性测试所具有的预测值的估算,怎样防止误导或者混乱的结果》”,其中对一种测试所具有的特异性、敏感度、以及阳性预测值和阴性预测值进行了讨论,所述的测试例如是一种临床诊断性测试。通常情况下,对于使用了一种连续性的诊断性测试的测量方法的二元疾病状态分类方法而言,通过接受者操作特性(ROC)曲线对所述的敏感度以及特异性进行了总结,并且通过所述的曲线下面积(AUC)或者c-统计量进行了总结,其中所述的接受者操作特性(ROC)曲线是依照Pepe等人于2004年在Am.J.Epidemiol《美国流行病学杂志》159(9):882-890中发表的文章“Limitations of the Odds Ratio in Gauging the Performance of a Diagnostic,Prognostic,or Screening Marker《让步比在测定一种诊断性、预兆性、或者筛选性标记物的性能中所存在的局限性》”所描述的,所述的曲线下面积(AUC)或者c-统计量是一种允许用来仅使用一个单一的数值对一种测试、检测、或者方法在全体范围的测试(或者检测)分割点上所具有的敏感度以及特异性进行代表的指示剂。同样可以参见,例如,Shultz于1996年在由Burtis以及Ashwood(编辑)的Teitz,Fundamentals of Clinical Chemistry《临床化学基础》第4版第14章中发表的文章“Clinical Interpretation Of Laboratory Procedures《实验室操作的临床干预》”,W.B.Saunders公司,第192-199页;以及Zweig等人于1992年在Clin.Chem.《临床化学》38(8):1425-1428中发表的文章“ROC Curve Analysis:An Example Showing The Relationships Among Serum Lipid AndApolipoprotein Concentrations In Identifying Subjects With Coronory Artery Disease《接受者操作特性曲线分析:在对患有冠心病的患者进行识别时,一种能够表现出所述的血清血脂与阿朴脂蛋白之间的关系的例子》”。依照Cook于2007年在Circulation《循环》115:928-935中发表的文章“Use and Misuse of the Receiver Operating Characteristic Curve in Risk Prediction《在危险预测中,对所述的接受者操作性特征曲线的使用以及滥用》”中的内容,对一种可供选择的方法进行了概述,其中在所述的方法中使用到了似然函数,让步比,信息论,预测值,校验(包括吻合度),以及重新分类的测量方法。
最终,由一项测试来进行定义的危险比例以及在宿主组内的绝对危险比例及相对危险比例成为一项对临床准确率以及可利用率的进一步的测量方法。多种方法被频繁的用来对异常的或者疾病的值进行定义,其中所述的值包括引用极限,判定极限,以及危险阈值。
“分析准确率”指的是所述的测量方法过程本身所具有的可再现性以及可预测性,并且可以在如下这样的测量方法中对其进行总结:变异系数,以及所述的相同样本或者对照所具有的一致性以及校验测试,其中在所述的测量方法中使用到的是不同的时间、使用者、仪器和/或试剂。同样在Vasan于2006年发表的文章中总结概括了在评价新的生物标记物的过程中的这些考虑以及其他的考虑。
“性能”是一个术语,所述的术语指的是一种诊断性的测试或者预后性的测试所具有的整体的有效性以及质量,其中包括临床准确率以及分析准确率,其他的分析特征以及加工特征,例如使用特征(例如,稳定性,使用的便利性),健康经济值,以及所述的测试中的组分所具有的相对成本。这些因素中的任何一个都可能是所述的优异性能产生的源泉以及因此使所述的测试具有有效性的源泉,并且可以通过适宜的“性能度量体系”来对其进行测量,其中所述的“性能度量体系”例如是曲线下面积(AUC),获得结果的时机,货架期,等等,只要相关即可。
“阳性预测值”或者“PPV”是由真阳性(TP)/(真阳性+假阳性)计算得到的,或者是由所述的真阳性部分占全部的阳性测试结果的比例计算得到的。其同样会固有的受到所述疾病的流行程度的影响,以及所述群体所具有的测试前概率的影响,其中所述的群体是意在接受测试的群体。
在本发明的上下文中,“危险”指的是在一个指定的时间段内一种事件将发生的概率,正如在向转移性事件进行转化的方面,并且能够意味着所述宿主的“绝对”危险或者“相对”危险。绝对危险可以根据下述来进行测量:在进行测量之后的所述相关的时间组之后实际的观察情况,或者根据从统计学有效的历史组中得来的指数值来进行测量,其中所述的历史组是在所述的相关的时间段内被跟进的组。相对危险指的是一个宿主所具有的绝对危险与所述的低危险组所具有的绝对危险之间的比值,或者是一个宿主所具有的绝对危险与一种平均的群体危险之间的比值,这种比值可能因为临床危险因素的评价方式而存在变化。对于非转化的情况而言,让步比同样是被普遍使用的,让步比指的是对于一个给定的测试结果而言,所述的阳性事件与所述的阴性事件之间的比例(让步比是根据所述的公式p/(1-p)计算得到的,其中p指的是所述事件所具有的概率并且(1-p)指的是所述的未发生事件所具有的概率)。
在本发明的上下文中,“危险评估”或者“对危险进行的评估”涵盖了对所述的概率、让步、或者可能性所进行的一种预测,其中所述的概率、让步、或者可能性指的是:一种事件或者疾病状态可能发生,所述的事件所具有的出现几率或者从一种疾病状态向另外一种疾病状态进行的转化,即,从一种原发性肿瘤到一种转移性肿瘤的转化,或者从一种原发性肿瘤到存在发展成为一种转移的危险的转化,或者从存在一种原发性转移事件的危险到一种更为次级的转移性事件的转化。危险评估同样能够包括对下述内容所进行的预测:未来的临床参数,传统实验室危险因素值,或者癌症的其他指数,无论它们是以绝对的形式或者是相对的形式在先前已经被测量的群体中出现的。本发明中所述的方法可以被用来对针对一种转移性肿瘤的危险进行连续性的测量或者分类的测量,并且因此对一种类型的宿主所具有的危险谱进行诊断以及定义,其中所述的这种类型的宿主被定义为存在形成转移性肿瘤的危险。在进行所述的分类测量的情况中,本发明可以被用来在正常的宿主与具有较高的形成转移性肿瘤的危险的其他宿主组之间进行判定。这种不同的用途可能需要不同的决定子(DETERMINANT)的组合以及有各自特点的评判小组,数学运算法则,和/或截止点,但是可以被进行相同的上述提及的测量,其中所述的测量针对的是对于各自的指定用途而言所具有的准确率以及性能。
在本发明的上下文中,“样本”指的是一种从宿主中分离得到的生物学样本,并且可以包括,通过举例的方式而不构成限制,组织活切片,全血,血清,血浆,血细胞,内皮细胞,淋巴液,腹腔积液,间质流体(同样被称为“细胞外流体”并且涵盖了在细胞之间的间隙内被发现的所述流体,包括,尤其是,牙龈沟液),骨髓,脑脊髓液(CSF),唾液,粘液,痰液,汗液,尿液,循环肿瘤细胞,循环内皮细胞或者任意其他的分泌物,排泄物,或者其他的体液。
“敏感度”是由真阳性(TP)/(真阳性+假阴性)计算得到的,或者是通过所述的疾病宿主所具有的真阳性比例计算得到的。
“特异性”是由真阴性(TN)/(真阴性+假阳性)计算得到的,或者是通过所述的非疾病宿主或者正常宿主所具有的真阴性比例计算得到的。
“统计学显著的”指的是所述的变化要比可能预期到的仅仅在偶然情况下发生的情况(其可能是一种“假阳性”)具有更高的程度。统计学显著性是可以通过本领域中已知的任何方法来确定的。普遍被使用的显著性的测量值包括所述的p值,其中所述的p值代表的是:假定一个数据点仅仅是由偶然的原因所产生的结果,获得一个至少像所述给定的数据点一样极端的结果所具有的概率。如果所述的p值为0.05或者更小,则认为所述的结果是具有高度的显著性的。
在本发明的上下文中,“宿主”优选是一种哺乳动物。所述的哺乳动物可以是人类,非人类的灵长动物,小鼠,大鼠,狗,猫,马,或者牛,但是并不局限于这些例子。除了人类之外的哺乳动物可以被有利的用来作为代表肿瘤转移的动物模型的宿主。宿主可以是雄性的或者是雌性的。宿主可以是这样的一个宿主,其在之前已经被诊断为或者被识别出患有原发性肿瘤或者转移性肿瘤,并且任选的已经接受过,或者正在接受,针对所述肿瘤的一种治疗性的干预。或者可供选择的,宿主同样可以是这样的一个宿主,其在之前并没有被诊断为患有一种转移性的肿瘤。例如,宿主可以表现出一种或者多种危险因素,其中所述的危险因素是针对一种转移性的肿瘤而言的。
“TN”指的是真阴性,当其被用在一种疾病状态的测试中时,意味着对未患有疾病的宿主或者正常的宿主进行了正确的分类。
“TP”指的是真阳性,当其被用在一种疾病状态的测试中时,意味着对患有疾病的宿主进行了正确的分类。
“传统实验室危险因素”对应着从宿主样本中分离出来的生物标记物或者从宿主样本中得到的生物标记物,并且已经在所述的临床实验室中对这些生物标记物进行了普遍的评价,并且在传统性的全球危险评价运算法则中对它们进行了使用。针对肿瘤转移的传统实验室危险因素包括例如垂直厚度,溃疡形成,增殖指数,肿瘤浸润淋巴细胞。针对肿瘤复发的其他传统实验室危险因素对于本领域技术人员而言是已知的。
本发明的方法以及用途
在本发明中所公开的方法是针对这样的宿主进行使用的,所述的宿主存在发展成为一种转移性肿瘤的危险,所述的宿主可能已经被诊断出患有一种转移性肿瘤或者可能还没有被诊断出患有一种转移性肿瘤,以及所述的宿主正在接受针对一种原发性肿瘤或者一种转移性肿瘤的处置和/或治疗。本发明中所述的方法同样可以被用来为宿主进行治疗方案的监测或者筛选,其中所述的宿主患有一种原发性肿瘤或者一种转移性肿瘤,以及用来对宿主进行筛选,其中所述的宿主之前并没有被诊断为患有一种转移性肿瘤,例如那些表现出针对转移的危险因素的宿主。优选的,本发明中所述的方法被用来对宿主进行诊断和/或识别,其中所述的宿主对于一种转移性肿瘤而言是无症状的。“无症状的”意味着不能够表现出所述的传统的症状。
本发明中所述的方法同样可以被用来对宿主进行识别和/或诊断,其中所述的宿主已经存在发展成为一种转移性肿瘤的较高的危险,这是单独基于所述的传统危险因素而言的。
可以通过下述方式对患有一种转移性肿瘤的宿主进行识别:对存在于一种来源于宿主的样本之中的有效数量(其可以是两种或者是更多种)的决定子(DETERMINANT)所具有的剂量(包括它的存在或者不存在)进行测量并且之后将所述的剂量与一种参考值进行比较。在此之后,可以对那些相对于所述的参考值而言发生的改变进行识别,其中所述的改变指的是所述的存在于宿主样本之中的生物标记物在剂量以及表达类型上的改变,或者所述的存在于宿主样本之中的代谢物或者其他被分析物所具有的分子质量的改变,其中所述的生物标记物例如是蛋白质,多肽,核酸以及多核苷酸,蛋白质、多肽、核酸以及多核苷酸的多形体,变异的蛋白质、多肽、核酸、以及多核苷酸。
一个参考值可以与来自于群体研究中的数量或者数值有关,包括但不局限于,这样的宿主,所述的宿主具有相同的癌症,所述的宿主具有相同或者相似的年龄范围,所述的宿主具有相同或者相似的种族集团,所述的宿主具有癌症的家族历史,或者所述的参考值可以与来自于宿主的起始样本有关,其中所述的宿主正在接受针对癌症所进行的治疗。这样的参考值可以从对群体进行的统计分析和/或群体的危险预测数据中得到,其中所述的统计分析和/或群体的危险预测数据是通过数学的运算法则以及对癌症转移的计算机计算得到的指数中获得的。同样可以对参考的决定子(DETERMINANT)指数进行构建以及使用,其中所述的构建以及使用是利用了运算法则以及统计学分类和结构分类中的其他方法。
在本发明的一种实施方式中,所述的参考值指的是存在于一种对照样本之中的所述的决定子(DETERMINANT)所具有的剂量,其中所述的对照样本来自于一个或者多个宿主,所述的宿主不存在发展成为转移性肿瘤的危险或者存在发展成为转移性肿瘤的较低的危险。在本发明的另外一种实施方式中,所述的参考值指的是存在于一种对照样本之中的所述的决定子(DETERMINANT)所具有的剂量,其中所述的对照样本来自于一个或者多个宿主,所述的宿主对于一种转移性肿瘤而言是无症状的和/或缺乏传统危险因素。在一种进一步的实施方式中,在经过这样的测试之后,在一个诊断学上相应的时间段内对这样的宿主进行监测和/或周期性的重复测试(“纵向研究”),用以验证一种转移性肿瘤的持续性的不存在(未发生疾病或者未发生事件的存活)。这样的时间段可以是一年,两年,两年至五年之间,五年,五年至十年之间,十年,或者十年至更多年之间,其中所述的时间是从为了确定所述的参考值而进行的初始测试的日期开始计算的。此外,在建立这些参考值时,可以对存在于被适当堆积的历史性的宿主样本中的决定子(DETERMINANT)进行追溯性的测量,因此可以缩短所述的研究所需要的时间。
一种参考值同样可以包括来自于宿主的所述的决定子(DETERMINANT)所具有的剂量,其中所述的宿主表现出在转移性的危险因素方面的改善,这种改善是针对所述的癌症所进行的处置和/或治疗方法所产生的结果。一种参考值同样可以包括来自于宿主的所述的决定子(DETERMINANT)所具有的剂量,其中已经通过已知的入侵性技术或者非入侵性技术证实了所述的宿主患有的疾病,或者所述的宿主存在发展成为一种转移性肿瘤的较高的危险,或者所述的宿主已经经受着一种转移性的肿瘤。
在另外一种实施方式中,所述的参考值是一个指数值或者是一个基线值。一种指数值或者基线值指的是一种有效剂量的决定子(DETERMINANT)的综合样本,其中所述的决定子(DETERMINANT)来自于一个或者多个宿主,所述的宿主并不存在转移性肿瘤,或者所述的宿主对于转移而言是无症状的。一种基线值同样可以包括来自于宿主的样本中所述的决定子(DETERMINANT)所具有的剂量,其中所述的宿主已经表现出在转移性肿瘤的危险因素方面的改善,这种改善是针对所述的癌症所进行的处置和/或治疗方法所产生的结果。在这种实施方式中,为了与所述的来自于宿主的样本进行比较,采用类似的方法对所述的决定子(DETERMINANT)所具有的剂量进行计算并且将其与所述的指数值进行比较。任选的,对这样的宿主进行选择,所述的宿主被识别出患有转移性肿瘤,或者具有发展成为一种转移性肿瘤的增加的危险,使所述的宿主接受一种治疗方案,从而对所述的癌症的恶化进行减慢,或者对所述的发展成为一种转移性肿瘤的危险进行降低或者阻止。
可以通过下述方式,对所述的转移性肿瘤的恶化或者一种癌症治疗方案所具有的有效性进行监测,所述的方式是:在一段时间内,对来自于一个宿主的样本中的有效剂量的决定子(DETERMINANT)(其可以是两种或者更多种)进行检测并且将所检测到的所述的决定子(DETERMINANT)的剂量进行比较。例如,可以在所述的宿主接受治疗之前获得第一个样本,并且在所述的宿主接受治疗之后或者在治疗的过程中获取一个或者多个随后的样本。如果随着时间的过去所述的决定子(DETERMINANT)所具有的剂量相对于所述的参考值而言发生了变化,则认为所述的癌症发生了恶化(或者,可供选择的,所述的治疗并没有对恶化进行阻止),而如果所述的决定子(DETERMINANT)所具有的剂量随着时间的过去仍然保持恒定,则所述的癌症并没有发生恶化(相对于所述的参考群体而言,或者相对于在本发明中所使用的“恒定”而言)。当被用在本发明的上下文中时,所述的术语“恒定”被解释为包括随着时间的过去伴随着所述的参考值所发生的变化。
例如,本发明中所述的方法可以被用来对所述肿瘤所具有的入侵性进行区别和/或对所述肿瘤所处于的阶段(例如,第I阶段,第II阶段,第III阶段或者第IV阶段)进行评价。这将允许对患者进行分级,使其分为高危险组或者低危险组,并且据此进行治疗。
除此之外,可以通过下述方式对适于向一个特定的宿主进行施用的治疗试剂或者预防试剂进行识别:对存在于一种样本之中的有效剂量的决定子(DETERMINANT)(其可以是两种或者更多种)进行检测,其中所述的样本来自于一个宿主,将所述的来自于宿主的样本暴露在一种受试化合物之下,并且测定存在于所述的来自于宿主的样本之中的所述决定子(DETERMINANT)所具有的剂量(其可以是两种或者更多种)。因此,可以根据存在于样本之中的所述决定子(DETERMINANT)所具有的剂量并且将其与一种参考值进行比较的方式,对适合在宿主中使用的处置方案或者治疗方案进行筛选,其中所述的样本来自于所述的宿主,所述的宿主患有一种癌症,或者所述的宿主存在发展成为一种转移性肿瘤的危险。可以对两种或者多种处置方案或者治疗方案进行平行的评价,从而确定哪一种处置方案或者治疗方案在对宿主进行使用时应当是最为有效的,用以延缓所述癌症的发作,或者减慢所述癌症的恶化。
本发明进一步的提供了一种用于对标记物的表达变化进行筛选的方法,其中所述的标记物的表达与一种转移性的肿瘤有关,所述的方法通过下述方式来实现:对存在于一种来自于宿主的样本中的所述的决定子(DETERMINANT)所具有的剂量(其可以是两种或者是更多种)进行测定,将其与存在于一种参考样本中的所述决定子(DETERMINANT)所具有的剂量进行比较,并且对与所述的参考样本相比而言在所述的宿主样本中发生的剂量的变化进行识别。
本发明进一步的提供了一种对患有肿瘤的患者进行治疗的方法,所述的方法是通过下述方式来实现的:对患有肿瘤的患者进行识别,其中在对来自于所述的肿瘤的样本进行测量时,一种有效剂量的决定子(DETERMINANT)以一种临床意义上显著的方式发生了改变,并且利用一种治疗方案对所述的患者进行治疗,其中所述的治疗方案能够阻止或者减慢肿瘤的转移。
除此之外,本发明提供了一种用以对肿瘤患者进行筛选的方法,其中所述的肿瘤患者需要接受辅助治疗,所述的方法是通过下述方式来实现的:通过对一种有效剂量的决定子(DETERMINANT)进行测量的方式来对所述患者所具有的转移危险进行评价,其中,在来自于所述患者的肿瘤样本之中的两种或者更多种决定子(DETERMINANT)所发生的临床意义上显著的改变预示着所述的患者需要接受辅助的治疗。
关于针对一个肿瘤患者的治疗决定的信息是通过下述方式获得的:获得一种有效剂量的决定子(DETERMINANT)的信息,其中所述的决定子(DETERMINANT)存在于来自于所述患者的肿瘤样本之中,并且对一种能够阻止或者减慢所述患者体内的肿瘤转移的治疗方案进行选择,当两种或者更多种决定子(DETERMINANT)以一种临床意义上显著的方式发生改变时。
如果所述的参考样本,例如是一种对照样本,来自于一个没有患有转移性肿瘤的宿主,或者如果所述的参考样本反映出的数值与这样的一个人相关,所述的人具有快速恶化成为一种转移性肿瘤的高度可能性,则存在于所述的测试样本以及所述的参考样本之中的决定子(DETERMINANT)所具有的剂量上的相似性表明着所述的治疗是有效的。然而,存在于所述的测试样本以及所述的参考样本之中的决定子(DETERMINANT)所具有的剂量上的差异表明着这是一种不太适合的临床结果或者预后。
“有效的”意味着所述的治疗导致了在一种决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物、或者其他分析物所具有的剂量或者活性方面的降低。可以使用标准的临床方案来实现对本发明所公开的危险因素的评价。可以与用于对一种转移性疾病进行诊断、识别、或者治疗的任何已知的方法联合起来,对有效性进行确定。
本发明同样提供了决定子(DETERMINANT)小组,所述的小组包括一种或者多种决定子(DETERMINANT),其中所述的决定子(DETERMINANT)指示着与一种转移有关的一般性的生理学途径。例如,所述的决定子(DETERMINANT)是可以被用来排除或者区分不同的疾病状态或者与转移有关的后遗症的一种或者多种决定子(DETERMINANT)。一个单个的决定子(DETERMINANT)可能具有根据本发明中上述提及的特征中的几种,并且可供选择的,对于一种给定的本发明的应用而言,当适宜时,可以被用来对一种或者多种其他的决定子(DETERMINANT)进行替代。
本发明同样包括一种带有检测试剂的试剂盒,其中所述的检测试剂能够与两种或者多种所述的决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物、或者其他的分析物进行结合。在本发明中同样提供的是一种检测试剂的阵列,其中所述的检测试剂是例如抗体和/或寡核苷酸,其中所述的抗体和/或寡核苷酸能够分别与两种或者多种决定子(DETERMINANT)蛋白质或者核酸进行结合。在一种实施方式中,所述的决定子(DETERMINANT)是蛋白质以及阵列,其中所述的阵列中含有能够与一种有效剂量的决定子(DETERMINANT)1-360发生结合的抗体,所述的有效剂量足以能够对发生在决定子(DETERMINANT)表达中的一种统计学意义上显著的改变进行测量,其中所述的改变是相较于一种参考值而言的。在另外一种实施方式中,所述的决定子(DETERMINANT)是核酸以及阵列,其中所述的阵列中含有能够与一种有效剂量的决定子(DETERMINANT)1-360发生结合的寡核苷酸或者适配子,所述的有效剂量足以能够对发生在决定子(DETERMINANT)表达中的一种统计学意义上显著的改变进行测量,其中所述的改变是相较于一种参考值而言的。
在另外一种实施方式中,所述的决定子(DETERMINANT)是蛋白质以及阵列,其中所述的阵列中含有能够与一种有效剂量的决定子(DETERMINANT)1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271发生结合的抗体,所述的有效剂量足以能够对发生在决定子(DETERMINANT)表达中的一种统计学意义上显著的改变进行测量,其中所述的改变是相较于一种参考值而言的。在另外一种实施方式中,所述的决定子(DETERMINANT)是核酸以及阵列,其中所述的阵列中含有能够与一种有效剂量的决定子(DETERMINANT)1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271发生结合的寡核苷酸或者适配子,所述的有效剂量足以能够对发生在决定子(DETERMINANT)表达中的一种统计学意义上显著的改变进行测量,其中所述的改变是相较于一种参考值而言的。
在本发明中同样提供的是一种用于对一个或者多个宿主进行治疗的方法,其中所述的宿主存在发展成为一种转移性肿瘤的危险,所述的方法是通过下述方式来实现的:对存在于一个样本中的有效剂量的所述决定子(DETERMINANT)是否存在剂量上的改变进行检测,其中所述的样本来自于所述的一个或者多个宿主;并且利用一种或者多种癌症调节药物对所述的一个或者多个宿主进行治疗,直至所述的决定子(DETERMINANT)所具有的剂量的改变或者活性的改变恢复至一种基线值,其中所述的基线值是在一个或者多个宿主中测量得到的,所述的宿主存在较低的发展成为一种转移性肿瘤的危险,或者可供选择的,所述的宿主没有表现出针对转移性疾病的任何一种所述的传统危险因素。
在本发明中同样提供的是一种用于对一个或者多个宿主进行治疗的方法,其中所述的宿主患有一种转移性肿瘤,所述的方法是通过下述方式来实现的:对存在于一个样本中的有效剂量的所述决定子(DETERMINANT)是否存在剂量上的改变进行检测,其中所述的样本来自于所述的一个或者多个宿主;并且利用一种或者多种癌症调节药物对所述的一个或者多个宿主进行治疗,直至所述的决定子(DETERMINANT)所具有的剂量的改变或者活性的改变恢复至一种基线值,其中所述的基线值是在一个或者多个宿主中测量得到的,所述的宿主存在较低的发展成为一种转移性肿瘤的危险。
在本发明中同样提供的是一种对宿主所存在的发展成为一种转移性肿瘤的危险方面的变化进行评价的方法,其中所述的宿主被诊断为患有癌症,所述的方法是通过下述的方式来实现的:对存在于第一个样本之中的所述有效剂量的决定子(DETERMINANT)(其可以是两种或者是更多种)进行检测,其中所述的第一个样本是在第一个时间段内来自于所述宿主的,对存在于第二个样本之中的所述决定子(DETERMINANT)的剂量进行检测,其中所述的第二个样本是在第二个时间段内来自于所述宿主的,并且将在上述的第一个时间段以及第二个时间段内检测到的所述决定子(DETERMINANT)的剂量进行比较。
本发明的诊断指示以及预后指示
本发明允许对一种转移性肿瘤进行诊断以及预后。可以通过下述方式对发展成为一种转移性肿瘤的危险进行检测:对存在于一种受试样本(例如,一种来自于宿主的样本)中的一种有效剂量的决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物、以及其他的分析物(其可以是两种或者是更多种)进行测量,并且将所述的有效剂量与参考值或者指数值进行比较,通常利用数学运算法则或者公式,其目的在于对来自于多种不同的决定子(DETERMINANT)的结果的信息以及来自于非分析性的临床参数的信息进行组合,使其成为一个单一的测量值或者指数。任选的,可以对被识别出存在一种转移性肿瘤的增加的危险的宿主进行筛选,使其接受治疗方案,其中所述的治疗方案例如是进行预防性化合物或者治疗性化合物的施用,从而阻止或者延缓所述的转移性肿瘤的发作。
可以对存在于一种受试样本中的所述的决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物、或者其他的分析物所具有的剂量进行测量,并且将其与所述的“正常的对照水平”进行比较,利用诸如引用极限,判定极限,或者危险定义阈值这样的技术,从而对截止点以及异常值进行定义。所述的“正常的对照水平”指的是一般情况下在一个没有患有转移性肿瘤的宿主体内发现的所述一种或者多种决定子(DETERMINANT)所具有的水平或者综合的决定子(DETERMINANT)指数。这样的正常的对照水平以及截止点可能存在变化,这取决于决定子(DETERMINANT)是否是单独进行使用的,还是在一个公式中与其他的决定子(DETERMINANT)进行组合成为一个指数。或者可供选择的,所述的正常的对照水平可以是一个决定子(DETERMINANT)类型的数据库,其中所述的类型来自于先前接受过测试的宿主,所述的宿主在经过一段临床学上相关的时间范围之后没有发展成为一种转移性的肿瘤。
本发明可以被用来针对转化成为一种转移性肿瘤的危险进行连续性的测量或者分类的测量,并且因此对一种类型的宿主所具有的危险谱进行诊断以及定义,其中所述的这种类型的宿主被定义为存在患有一种转移性肿瘤的危险。在进行所述的分类测量的情况中,本发明中所述的方法可以被用来在正常宿主组与疾病宿主组之间进行判定。在其他的实施方式中,可以对本发明进行使用,从而对存在发展成为一种转移性事件的危险的宿主进行判定,使其与存在较为快速的恶化成为一种转移性事件的宿主(或者可供选择的与那些具有较短的可能的时间范围来发展成为一种转移性事件的宿主)进行区分,与存在较为缓慢的恶化(或者具有较长的时间范围来发展成为一种转移性事件的宿主)成为一种转移性事件的宿主进行区分,或者使患有一种转移性肿瘤的宿主与正常宿主进行区分。这种不同的用途可能需要存在于各个小组中的不同的决定子(DETERMINANT)的组合,数学运算法则,和/或截止点,但是可以被进行相同的上述提及的测量,其中所述的测量针对的是对于各自的指定用途而言所具有的准确率以及性能度量体系。
对那些将存在发展成为一种转移性事件的宿主所进行的识别使得能够对各种不同的治疗性干预或者治疗方案进行筛选以及激发,其目的在于延缓、减慢或者阻止宿主向一种转移性的疾病状态的转化。一种决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物、或者其他的分析物所具有的有效剂量的水平同样能够允许对所述的治疗过程进行监测,其中所述的治疗是针对转移性疾病或者转移性事件而进行的。在这个方法中,可以从一个宿主中获得一种生物学样本,其中所述的宿主正在接受针对癌症的治疗方案,例如,药物的治疗。如果期望的话,生物学样本是在各种不同的时间点处从所述的宿主处获得的,其中所述的时间点是在治疗之前、治疗的过程中、或者治疗之后。
由于所述的决定子(DETERMINANT)在其功能上而言是被活化的,通过对其功能进行阐明,可以利用试剂和/或药物对具有高水平的决定子(DETERMINANT)的宿主进行处理,其中所述的试剂和/或药物能够优先的作用于这样的途径,例如经由转化生长因子β(TGFβ)的HOXA1功能化,因此,可以利用转化生长因子β(TGFβ)抑制剂对具有高水平的HOXA1宿主进行治疗。或者HOXA1能够对趋化因子受体4(CXCR4)进行活化,因此,可以使用对趋化因子受体4(CXCR4)产生拮抗作用的试剂/药物,其中所述的趋化因子受体4(CXCR4)是一种已知的在转移作用中涉及到的趋化因子轴,并且已经报导其可以作用于转化生长因子b(TGFb)的上游。
本发明同样可以被用来在任何不同的环境中对患者或者宿主的群体进行筛选。例如,一个健康维护组织,公共卫生单位或者学校健康计划可以对一组宿主进行筛选,从而按照上文中所描述的方法对它们中需要进行干预的那部分进行识别,或者用于收集所述的流行病学数据。保险公司(例如,健康保险,人寿保险或者残疾保险)可以在确定所述的保险范围或者定价的过程中对申请者进行筛选,或者对现有的客户所需要进行的可能的干预进行筛选。对从这样的群体中收集到的数据进行筛选,特别是当所述的数据与任何的临床病症的恶化例如癌症或者转移性事件相关联时,这对于例如健康维护组织、公共健康计划以及保险公司的运作而言将是有价值的。这样的数据阵列或者数据收集可以被存储在计算机可读形式的介质之中并且在许多的与健康相关的数据管理系统中对其进行使用,从而提供改进的卫生保健服务,成本有效的卫生保健,改进的保险运作,等等。参见,例如,美国专利申请No.2002/0038227;美国专利申请No.2004/0122296;美国专利申请No.2004/0122297;以及美国专利No.5018067。这样的系统能够直接从内部数据存储中对所述的数据进行存取,或者从一个或者多个数据存储站点中对所述的数据进行远程的存取,这将在本发明中进行进一步的详细描述。
一种计算机可读形式的存储介质可以包括一种数据存储材料,所述的数据存储材料是由计算机可读形式的数据或者数据阵列来编码的,当使用用于这些数据的说明书对一种计算机进行编程时,所述的数据或者数据阵列能够用于各种不同的目的,例如,但不局限于,宿主的信息,其中所述的信息涉及到在一段时间内的转移性疾病的危险因素或者对药物治疗的应答。可以在计算机程序中执行对本发明中所述的生物标记物的有效剂量的测量和/或通过这些生物标记物对危险进行的评价,其中所述的计算机程序是在可编程的计算机上运行的,其包括,尤其是,一种处理器,一种数据存储系统(包括易失性存储器以及非易失性存储器和/或存储元件),至少一个输入设备,以及至少一个输出设备。可以应用程序代码进行数据的输入从而实现如上所述的功能并且生成输出信息。根据本领域中已知的方法,可以将所述的输出信息应用至一个或者多个输出设备上。所述的计算机可以是,例如,个人电脑,微电脑,或者具有传统设计的工作站。
每一种程序都可以以一种高水平的程序性语言或者面向对象的程序设计语言来进行执行,从而使其能够与一种计算机系统进行交流。然而,如果期望的话,可以通过汇编语言或者计算机语言对所述的程序进行执行。所述的语言可以是一种经过编译的语言或者经过翻译的语言。每一种这样的计算机程序可以被存储在一个存储介质或者存储设备之上(例如,只读内存(ROM)或者磁性软盘或者在本公开物的其他内容中所定义的那些其他介质或者设备),其中所述的存储介质或者存储设备可以利用一种具有一般性目的或者特殊性目的的可编程的计算机来进行阅读,当所述的存储介质或者存储设备被所述的计算机进行阅读用以完成本发明中所描述的操作程序时,其能够对所述的计算机进行配置以及运行。本发明中所述的健康相关数据管理系统同样可以被用来作为一种计算机可读形式的存储介质来进行执行,利用一种计算机程序对其进行配置,其中被进行了这样的配置的所述的存储介质能够引发计算机以一种特定的方式或者预先定义的方式来进行运行,从而实现在本发明中所描述的各种不同的功能。
在此之后,可以对一种有效剂量的决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物、或者其他分析物所具有的水平进行测定并且将其与一种参考值或者指数值或者基线值进行比较,其中所述的参考值是例如一个对照的宿主或者群体,所述的宿主或者群体所具有的转移状态是已知的。所述的参考样本或者指数值或者基线值可以从一个或者多个宿主处获取或者获得,其中所述的宿主已经接受过所述的治疗,或者可以从一个或者多个宿主处获取或者获得,其中所述的宿主存在较低的发展成为癌症或者转移性事件的危险,或者可以从这样的宿主处获取或者获得,其中所述的宿主已经表现出进展,这种进展是一种接受治疗的结果。可供选择的,所述的参考样本或者指数值或者基线值可以从一个或者多个宿主处获取或者获得,其中所述的宿主并没有接受过治疗。例如,样本可以从这样的宿主处进行收集,所述的宿主已经接受过针对癌症或者转移性事件所进行的初始治疗以及随后的针对癌症或者转移性事件所进行的治疗,用以对所述的治疗所取得的进展进行监测。一种参考值同样能够包括这样的值,所述的值来自于危险预测运算法则或者计算机计算得到的指数,例如在本发明中所公开的那些,这些运算法则或者指数是来自于群体研究的。
本发明中所述的决定子(DETERMINANT)因此可以被用来生成一种宿主的“参考决定子(DETERMINANT)曲线”,其中所述的宿主不存在癌症或者不存在发生一种转移性事件的危险,并且被认为不能够发展成为癌症或者一种转移性事件。本发明中公开的所述决定子(DETERMINANT)同样可以被用来生成一种“宿主的决定子(DETERMINANT)曲线”,其中所述的曲线来自于这样的宿主,所述的宿主患有癌症或者存在发生一种转移性事件的危险。可以将所述的宿主决定子(DETERMINANT)曲线与一种参考决定子(DETERMINANT)曲线进行比较,从而对存在发展成为癌症或者一种转移性事件的危险的宿主进行诊断或者识别,用以对所述疾病的恶化情况进行监测,以及对所述疾病所具有的恶化速率进行监测,并且对所述的治疗形式所具有的有效性进行监测。本发明中所述的参考决定子(DETERMINANT)曲线以及宿主决定子(DETERMINANT)曲线可以被容纳在一种计算机可读形式的介质中,所述的介质是例如但不局限于,模拟磁带,其中,像那些能够被一种盒式磁带录像机(VCR)、只读光盘(CD-ROM)、数字视盘(DVD-ROM)、通用串行总线(USB)闪存进行阅读的介质。这样的计算机可读形式的介质中同样可以容纳其他的测试结果,例如,但不局限于,对临床参数以及传统实验室危险因素的测量。可供选择的或者除此之外的,所述的计算机可读形式的介质中同样可以包括宿主信息,例如病历以及任何相关的家族历史。所述的计算机可读形式的介质中同样可以容纳与其他的疾病危险运算法则以及计算机计算得到的指数相关的信息,例如那些在本发明中所描述的。
宿主在所述的遗传组成方面所存在的差异能够导致他们在代谢各种不同的药物方面所具有的相对能力上的差异,这种代谢药物的能力能够对癌症或者转移性事件所具有的症状或者危险因素进行调节。患有癌症的宿主、或者存在发展成为癌症或者转移性事件的危险的宿主可以在年龄、种族、以及其他的参数方面存在变化。因此,本发明中公开的所述决定子(DETERMINANT)的使用,无论是单独使用还是与药物代谢方面已知的遗传因素共同进行组合使用,使得存在一种具有预先确定的水平的可预测性,使需要在一个被选定的宿主体内进行测试的一种推定的治疗剂或者预防剂将能够适合于对所述的宿主进行治疗或者预防,其中所述的治疗或者预防针对的是癌症或者是一种转移性的事件。
为了对那些能够适合于一个具体宿主的治疗剂或者药物进行识别,同样可以将一个来自于所述宿主的测试样本暴露于一种治疗试剂或药物之中,并且对所述的一种或者多种决定子(DETERMINANT)蛋白质、核酸、多形体、代谢产物或者其他的分析物所具有的水平进行测定。可以将所述的一种或者多种决定子(DETERMINANT)所具有的水平与来自于所述宿主的样本进行比较,其中所述的样本是在接受治疗之前以及接受治疗之后获得的,或者所述的样本是在被暴露于一种治疗剂或者药物之前以及被暴露于一种治疗剂或者药物之后获得的,或者可以将所述的一种或者多种决定子(DETERMINANT)所具有的水平与来自于一个或者多个宿主的样本进行比较,其中所述的宿主在危险因素(例如,临床参数或者传统实验室危险因素)方面已经表现出了改善,这种改善是这样的治疗或者暴露所产生的结果。
可以在存在有一种备选试剂的条件下对一个宿主细胞(即,一个从宿主中分离得到的细胞)进行培养,并且对存在于所述的测试样本中的所述决定子(DETERMINANT)的表达类型进行测量并且将其与一种参考曲线或者一种指数值或者基线值进行比较,其中所述的参考曲线是例如,一种转移性疾病参考表达曲线或者非疾病参考表达曲线。所述的测试试剂可以是任何的化合物或者组合物或者两者的混合物,包括,膳食补充剂。例如,所述的测试试剂是那些被频繁的用于癌症治疗方案中的试剂以及在本发明中所公开的试剂。
前述提及的本发明所述的方法可以被用来对宿主的恶化和/或改善进行评价或者监测,其中所述的宿主已经被诊断为患有一种癌症,并且所述的宿主已经接受了外科手术的干预。
本发明的性能测量以及准确度测量
按照上文中所记载的,可以通过多种方式对本发明所具有的性能以及因此所产生的绝对临床有效性以及相对临床有效性进行评价。在这些对所述的性能进行的各种不同的评价方法中,本发明意在提供在临床诊断以及预后方面所具有的准确率。一种诊断性或者预后性的测试、检测、或者方法所具有的准确率关系到所述的测试、检测、或者方法在辨别宿主的方面所具有的能力,其中所述的需要辨别的宿主是那些患有癌症、或者存在形成癌症或者一种转移性事件的危险的宿主,这种辨别是以下述为基础的:所述的宿主是否在所述的决定子(DETERMINANT)的水平上发生了“显著性的改变”(例如,临床意义上的显著,诊断意义上的显著)。“有效剂量”意味着能够产生一种“显著性改变”(例如,一种决定子所具有的表达水平或者活性水平)的适合数量的决定子(DETERMINANT)(其可以是一种或者是更多种)的测量值与针对该决定子(DETERMINANT)的预先确定的截止点(或者阈值)之间存在差异并且因此表明所述的宿主患有癌症或者存在发生一种转移性事件的危险,其中在上述情况中所述的决定子(DETERMINANT)是一种决定性因素。存在于正常与异常的所述的决定子(DETERMINANT)的水平之间的差异优选的是具有统计学显著性的。正如将在下文中进行记载的,并且并不构成对本发明的任何限制,达到统计学显著性,并且因此而被优选的分析准确率以及临床准确率,一般而言但不总是需要将几种决定子(DETERMINANT)的组合共同用于小组中并且将其与数学运算法则进行结合,其目的在于获得一个具有统计学显著性的决定子(DETERMINANT)指数。
在对一种疾病状态进行类别诊断时,一项测试(或者检测)的分割点或者阈值的改变通常会改变所述的敏感度以及特异性,但是是以一种相反的定性关系来进行改变的。因此,在对一种被提议的用以对宿主的情况进行评价的医学测试、检测、或者方法所具有的准确率以及有效性进行评价的时候,应当总是同时将敏感度以及特异性纳入考虑范围,并且注意到在对所述的敏感度以及特异性进行报告时当时所述的分割点为多少,因为敏感度以及特异性可能在一定的分割点的范围内存在显著性的变化。对于使用本发明的大部分分类的危险测量而言,统计学方法的使用是优选的,其中所述的统计学方法例如是曲线下面积(AUC),其涵盖了所有可能的分割点值,而对于连续性的危险测量而言,拟合度的统计学方法以及对观察到的结果所进行的校验或者其他的金标准是优选的。
预先确定水平的可预测能力意味着所述的方法能够提供一种具有可接受水平的临床准确率或者诊断准确率。使用了这样的统计学方法,“可接受程度的诊断准确率”在本发明中被定义为对一种测试或者检测(例如是本发明中所述的测试,用以确定所述的决定子(DETERMINANT)的临床意义上的显著性是否存在,从而指示着所述癌症的存在和/或发生一种转移性事件的危险的存在)所具有的AUC(对于所述的测试或者检测而言,存在于所述的接受者操作特性曲线之下的面积)为至少0.60,期望的为至少0.65,更加期望的为至少0.70,优选的为至少0.75,更加优选的为至少0.80,并且最为优选的为至少0.85。
“非常高程度的诊断准确率”意味着在一项测试或者检测中,所述的AUC(对于所述的测试或者检测而言,存在于所述的接受者操作特性曲线之下的面积)为至少0.75,0.80,期望的为至少0.85,更加期望的为至少0.875,优选的为至少0.90,更加优选的为至少0.925,并且最为优选的为至少0.95。
或者可供选择的,所述的方法以至少75%的准确率对所述癌症的存在或者不存在、转移性癌症的存在或者不存在、或者针对治疗的应答的存在或者不存在进行预测,其中所述的准确率更加优选的为80%,85%,90%,95%,97%,98%,99%或者更高的准确率。
对于任何一项测试而言,所述测试的预测值取决于所述的测试所具有的敏感度以及特异性,并且取决于所述的病症在接受测试的所述群体中的普遍程度。这种想法是以贝叶斯定理为依据,假定被进行筛选的所述病症在一个个体中或者在所述的群体中存在的可能性越大(测试前的概率),一种阳性测试所具有的有效性越高,并且所述的结果是一种真阳性的可能性就越大。因此,当一个任意的群体中存在所述的病症的可能性小时,在这个群体中使用一项测试所产生的问题是一种阳性的结果具有有限的价值(即,更为可能是一种假阳性)。与之相类似的,在具有非常高的危险的群体中,一种阴性的测试结果更为可能是一种假阴性。
作为结果,在具有低的疾病普遍性的受试群体中(被定义为每年具有低于1%的发生率(发病率)的群体,或者在一段特定的时间范围内具有低于10%的累积普遍性的群体),关于测试所具有的临床可利用率方面,接受者操作特性曲线(ROC)以及曲线下面积(AUC)可能是容易令人误解的。或者可供选择的,在本公开物的其他内容中定义的绝对危险以及相对危险的比例可以被用来确定所述的临床可利用率的程度。用于进行测试的宿主群体可以被分类为四分位数,所述的分类是通过所述的测试测量值来进行的,其中所述的顶端的四分位数(占所述群体中的25%)包括这样的宿主组,所述的宿主存在发展成为癌症或者转移性事件的最高的相对危险性,而所述的底端的四分位数包括这样的宿主组,所述的宿主存在发展成为癌症或者转移性事件的最低的相对危险性。一般而言,在一个具有低普遍性的群体之中,当来自于测试或者检测中的从顶端四分位数至底端四分位数的相对危险数值超过2.5倍时,我们认为其具有“高程度的诊断准确率”,并且那些对每一个四分位数而言所述的相对危险在五倍至七倍之间的,我们认为其具有“非常高度的诊断准确率”。虽然如此,当来自于测试或者检测中的每一个四分位数的相对危险数值仅仅为1.2倍至1.5倍时,其仍然具有临床意义上的有效性,能够被广泛的用来作为一种疾病的危险因素;这对于总胆固醇以及许多炎性生物标记物在它们对未来事件所进行的预测而言是常见的事情。通常情况下,这样的具有较低的诊断准确率的测试必须要与其他的参数进行结合,其目的在于得到有意义的临床阈值用以进行治疗性的干预,正如利用前述提及的全球性危险评价指数来完成的。
一个健康经济利用率函数是另外一种方式,用于测量一种给定的测试所具有的性能以及临床价值,所述的方式是通过对所述的可能的分类测试结果进行加权处理来构成的,这种加权处理依据的是对每一种结果的临床价值以及经济价值所进行的实际测量。健康经济性能与准确率紧密相关,因为健康经济利用率函数能够为对受试宿主的正确分类所产生的利益指定一个经济学价值,并且能够为对受试宿主的错误分类所产生的成本指定一个经济学价值。作为一种性能的测量,需要一种能够达到一定的性能水平的测试并非不寻常的,其中所述的性能水平使得能够在每一次测试中产生一次在健康经济价值上的增加(在测试成本之前),使之超过所述的测试的目标价格。
一般而言,在下述情况中,用于测定诊断准确率的可供选择的方法普遍被用来进行连续性的测量:当一种疾病的类型或者危险的类型还没有被明确的定义出来的时候(例如那些存在发生一种转移性事件的危险的类型),其中所述的定义是通过相关的医学学会以及医学实践来完成的,当治疗性用途的阈值还没有被确立出来的时候,或者当目前还没有已有的金标准用来对所述的未疾病(pre-disease)进行诊断的时候。为了对危险进行连续性的测量,对于一种经过计算得到的指数而言,对诊断准确率的测量一般而言是基于曲线拟合以及在所述的经过预测的连续值与实际观察值(或者是一个历史指数计算得到的值)之间所进行的校验并且利用诸如下述的测量值:R平方值,Hosmer-Lemeshow拟合度校验,P值统计学方法以及置信区间。使用这样的被报道的运算法则以一种历史观察组的预测为依据对于所预测的值而言并非不寻常的,其中所述的运算法则包括置信区间(一般而言是90%或者95%的置信区间(CI)),正如被Genomic Health,Inc(红杉市,加利福尼亚)商业化的用于对未来的乳腺癌复发的危险所进行的测试中。
一般而言,通过对所述的诊断准确率所具有的程度进行定义,即,存在于一条接受者操作特性曲线(ROC)曲线上的分割点,对一种可接受的曲线下面积(AUC)值进行定义,以及通过对构成本发明中的有效剂量的所述决定子(DETERMINANT)的相对浓度的可接受范围的确定,可以使得本领域技术人员利用所述的决定子(DETERMINANT)对宿主进行识别,诊断,或者预后,其中所述的识别、诊断、或者预后是在具有一种预先确定的水平的可预测性以及性能的条件下完成的。
本发明的危险标记物(决定子(DETERMINANT))
本发明中所述的生物标记物以及方法允许本领域技术人员对那些宿主进行识别,诊断,或者评价,其中所述的宿主是那些没有表现出任何的癌症症状或者转移性事件的症状的宿主,但是虽然如此,所述的宿主可能存在发展成为癌症或者一种转移性事件的危险。
已经识别出一千五百九十三种生物标记物,因为已经发现在患有转移性疾病的宿主体内所述的生物标记物具有改变的或者经过修饰的存在水平或者浓度水平。
表格I中包括了本发明所述的三百六十种(360)过表达的/扩增的或者去调节的/缺失的表型驱动的进化保守型决定子(DETERMINANT)。决定子(DETERMINANT)1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271已经被识别为前侵决定子。
表格I
| 基因ID | 基因符号 | 决定子编号: |
| 54 | ACP5 | 1 |
| 54443 | ANLN | 2 |
| 55723 | ASF1B | 3 |
| 23397 | BRRN1 | 4 |
| 699 | BUB1 | 5 |
| 79019 | CENPM | 6 |
| 55635 | DEPDC1 | 7 |
| 64123 | ELTD1 | 8 |
| 6624 | FSCN1 | 9 |
| 64151 | HCAP-G | 10 |
| 3146 | HMGB1 | 11 |
| 3198 | HOXA1 | 12 |
| 3297 | HSF1 | 13 |
| 23421 | ITGB3BP | 14 |
| 10112 | KIF20A | 15 |
| 11004 | KIF2C | 16 |
| 10403 | KNTC2 | 17 |
| 4176 | MCM7 | 18 |
| 10797 | MTHFD2 | 19 |
| 11156 | PTP4A3 | 20 |
| 6045 | RNF2 | 21 |
| 10615 | SPAG5 | 22 |
| 11065 | UBE2C | 23 |
| 51377 | UCHL5 | 24 |
| 11326 | VSIG4 | 25 |
| 79575 | ABHD8 | 26 |
| 1636 | ACE | 27 |
| 8038 | ADAM12 | 28 |
| 101 | ADAM8 | 29 |
| 23600 | AMACR | 30 |
| 80833 | APOL3 | 31 |
| 410 | ARSA | 32 |
| 22901 | ARSG | 33 |
| 259266 | ASPM | 34 |
| 477 | ATP1A2 | 35 |
| 6790 | AURKA | 36 |
| 9212 | AURKB | 37 |
| 26053 | AUTS2 | 38 |
| 627 | BDNF | 39 |
| 638 | BIK | 40 |
| 332 | BIRC5 | 41 |
| 672 | BRCA1 | 42 |
| 701 | BUB1B | 43 |
| 80135 | BXDC5 | 44 |
| 29902 | C12ORF24 | 45 |
| 55839 | C16ORF60 | 46 |
| 56942 | C16ORF61 | 47 |
| 116496 | C1ORF24 | 48 |
| 719 | C3AR1 | 49 |
| 57002 | C7ORF36 | 50 |
| 84933 | C8ORF76 | 51 |
| 152007 | C90RF19 | 52 |
| 781 | CACNA2D1 | 53 |
| 857 | CAV1 | 54 |
| 6357 | CCL13 | 55 |
| 6347 | CCL2 | 56 |
| 6354 | CCL7 | 57 |
| 890 | CCNA2 | 58 |
| 947 | CD34 | 59 |
| 948 | CD36 | 60 |
| 983 | CDC2 | 61 |
| 991 | CDC20 | 62 |
| 995 | CDC25C | 63 |
| 990 | CDC6 | 64 |
| 8317 | CDC7 | 65 |
| 83540 | CDCA1 | 66 |
| 83461 | CDCA3 | 67 |
| 55536 | CDCA7L | 68 |
| 81620 | CDT1 | 69 |
| 1058 | CENPA | 70 |
| 1062 | CENPE | 71 |
| 1063 | CENPF | 72 |
| 55165 | CEP55 | 73 |
| 23177 | CEP68 | 74 |
| 1070 | CETN3 | 75 |
| 1111 | CHEK1 | 76 |
| 26586 | CKAP2 | 77 |
| 1163 | CKS1B | 78 |
| 1164 | CKS2 | 79 |
| 1180 | CLCN1 | 80 |
| 7122 | CLDN5 | 81 |
| 23601 | CLEC5A | 82 |
| 9918 | CNAP1 | 83 |
| 10664 | CTCF | 84 |
| 1565 | CYP2D6 | 85 |
| 1601 | DAB2 | 86 |
| 10926 | DBF4 | 87 |
| 23564 | DDAH2 | 88 |
| 1719 | DHFR | 89 |
| 55355 | DKFZP762E1312 | 90 |
| 27122 | DKK3 | 91 |
| 9787 | DLG7 | 92 |
| 1769 | DNAH8 | 93 |
| 30836 | DNTTIP2 | 94 |
| 51514 | DTL | 95 |
| 1854 | DUT | 96 |
| 1894 | ECT2 | 97 |
| 51162 | EGFL7 | 98 |
| 56943 | ENY2 | 99 |
| 54749 | EPDR1 | 100 |
| 51327 | ERAF | 101 |
| 2115 | ETV1 | 102 |
| 2131 | EXT1 | 103 |
| 2162 | F13A1 | 104 |
| 51647 | FAM96B | 105 |
| 2230 | FDX1 | 106 |
| 2235 | FECH | 107 |
| 63979 | FIGNL1 | 108 |
| 51303 | FKBP11 | 109 |
| 2289 | FKBP5 | 110 |
| 55110 | FLJ10292 | 111 |
| 79805 | FLJ12505 | 112 |
| 84935 | FLJ14834 | 113 |
| 54908 | FLJ20364 | 114 |
| 54962 | FLJ20516 | 115 |
| 2350 | FOLR2 | 116 |
| 2305 | FOXM1 | 117 |
| 2530 | FUT8 | 118 |
| 51809 | GALNT7 | 119 |
| 64096 | GFRA4 | 120 |
| 2740 | GLP1R | 121 |
| 51053 | GMNN | 122 |
| 2775 | GNAO1 | 123 |
| 2792 | GNGT1 | 124 |
| 4076 | GPIAP1 | 125 |
| 2894 | GRID1 | 126 |
| 2936 | GSR | 127 |
| 2966 | GTF2H2 | 128 |
| 51512 | GTSE1 | 129 |
| 3045 | HBD | 130 |
| 50810 | HDGFRP3 | 131 |
| 3082 | HGF | 132 |
| 3012 | HIST1H2AB | 133 |
| 3142 | HLX1 | 134 |
| 3148 | HMGB2 | 135 |
| 3161 | HMMR | 136 |
| 10236 | HNRPR | 137 |
| 10247 | HRSP12 | 138 |
| 3313 | HSPA9B | 139 |
| 51501 | HSPC138 | 140 |
| 10808 | HSPH1 | 141 |
| 25998 | IBTK | 142 |
| 3384 | ICAM2 | 143 |
| 80173 | IFT74 | 144 |
| 3570 | IL6R | 145 |
| 3684 | ITGAM | 146 |
| 6453 | ITSN1 | 147 |
| 10008 | KCNE3 | 148 |
| 3776 | KCNK2 | 149 |
| 9768 | KIAA0101 | 150 |
| 9694 | KIAA0103 | 151 |
| 56243 | KIAA1217 | 152 |
| 84629 | KIAA1856 | 153 |
| 3832 | KIF11 | 154 |
| 81930 | KIF18A | 155 |
| 3833 | KIFC1 | 156 |
| 55220 | KLHDC8A | 157 |
| 3912 | LAMB1 | 158 |
| 3915 | LAMC1 | 159 |
| 55915 | LANCL2 | 160 |
| 11025 | LILRB3 | 161 |
| 4005 | LMO2 | 162 |
| 150084 | LOC150084 | 163 |
| 345711 | LOC345711 | 164 |
| 91614 | LOC91614 | 165 |
| 26018 | LRIG1 | 166 |
| 54892 | LUZP5 | 167 |
| 4085 | MAD2L1 | 168 |
| 6300 | MAPK12 | 169 |
| 4147 | MATN2 | 170 |
| 4172 | MCM3 | 171 |
| 4174 | MCM5 | 172 |
| 4175 | MCM6 | 173 |
| 9833 | MELK | 174 |
| 4232 | MEST | 175 |
| 4233 | MET | 176 |
| 85014 | MGC14141 | 177 |
| 79971 | MIER1 | 178 |
| 4288 | MK167 | 179 |
| 8028 | MLLT10 | 180 |
| 4317 | MMP8 | 181 |
| 4318 | MMP9 | 182 |
| 4353 | MPO | 183 |
| 51678 | MPP6 | 184 |
| 219928 | MRGPRF | 185 |
| 64968 | MRPS6 | 186 |
| 10335 | MRVI1 | 187 |
| 10232 | MSLN | 188 |
| 4600 | MX2 | 189 |
| 4678 | NASP | 190 |
| 4751 | NEK2 | 191 |
| 23530 | NNT | 192 |
| 4846 | NOS3 | 193 |
| 4855 | NOTCH4 | 194 |
| 84955 | NUDCD1 | 195 |
| 11163 | NUDT4 | 196 |
| 53371 | NUP54 | 197 |
| 4928 | NUP98 | 198 |
| 51203 | NUSAP1 | 199 |
| 4999 | ORC2L | 200 |
| 116039 | OSR2 | 201 |
| 5019 | OXCT1 | 202 |
| 56288 | PARD3 | 203 |
| 55872 | PBK | 204 |
| 11133 | PDAP1 | 205 |
| 5138 | PDE2A | 206 |
| 5156 | PDGFRA | 207 |
| 5157 | PECAM1 | 208 |
| 5218 | PFTK1 | 209 |
| 25776 | PGEA1 | 210 |
| 26227 | PHGDH | 211 |
| 83483 | PLVAP | 212 |
| 57125 | PLXDC1 | 213 |
| 5425 | POLD2 | 214 |
| 5427 | POLE2 | 215 |
| 5446 | PON3 | 216 |
| 5557 | PRIM1 | 217 |
| 5558 | PRIM2A | 218 |
| 5578 | PRKCA | 219 |
| 23627 | PRND | 220 |
| 9265 | PSCD3 | 221 |
| 5743 | PYGS2 | 222 |
| 5885 | RAD21 | 223 |
| 5888 | RAD51 | 224 |
| 5889 | RAD51C | 225 |
| 3516 | RBPSUH | 226 |
| 5965 | RECQL | 227 |
| 5984 | RFC4 | 228 |
| 5985 | RFC5 | 229 |
| 23179 | RGL1 | 230 |
| 64407 | RGS18 | 231 |
| 5997 | RGS2 | 232 |
| 8490 | RGS5 | 233 |
| 9584 | RNPC2 | 234 |
| 6091 | ROBO1 | 235 |
| 6118 | RPA2 | 236 |
| 6119 | RPA3 | 237 |
| 6222 | RPS18 | 238 |
| 6236 | RRAD | 239 |
| 22800 | RRAS2 | 240 |
| 6240 | RRM1 | 241 |
| 6241 | RRM2 | 242 |
| 340419 | RSPO2 | 243 |
| 10371 | SEMA3A | 244 |
| 143686 | SESN3 | 245 |
| 85358 | SHANK3 | 246 |
| 79801 | SHCBP1 | 247 |
| 8036 | SHOC2 | 248 |
| 23517 | SKIV2L2 | 249 |
| 7884 | SLBP | 250 |
| 6509 | SLC1A4 | 251 |
| 115286 | SLC25A26 | 252 |
| 6526 | SLC5A3 | 253 |
| 8467 | SMARCA5 | 254 |
| 8243 | SMC1L1 | 255 |
| 10592 | SMC2L1 | 256 |
| 10051 | SMC4L1 | 257 |
| 6629 | SNRPB2 | 258 |
| 64321 | SOX17 | 259 |
| 6662 | SOX9 | 260 |
| 57405 | SPBC25 | 261 |
| 60559 | SPCS3 | 262 |
| 6741 | SSB | 263 |
| 6742 | SSBP1 | 264 |
| 26872 | STEAP1 | 265 |
| 6788 | STK3 | 266 |
| 10460 | TACC3 | 267 |
| 23435 | TARDBP | 268 |
| 25771 | TBC1D22A | 269 |
| 6899 | TBX1 | 270 |
| 7052 | TGM2 | 271 |
| 90390 | THRAP6 | 272 |
| 8914 | TIMELESS | 273 |
| 7077 | TIMP2 | 274 |
| 7083 | TK1 | 275 |
| 55273 | TMEM100 | 276 |
| 55161 | TMEM33 | 277 |
| 55706 | TMEM48 | 278 |
| 54543 | TOMM7 | 279 |
| 7153 | top2A | 280 |
| 22974 | TPX2 | 281 |
| 54209 | TREM2 | 282 |
| 4591 | TRIM37 | 283 |
| 9319 | TRIP13 | 284 |
| 95681 | TSGA14 | 285 |
| 7371 | UCK2 | 286 |
| 83878 | USHBP1 | 287 |
| 10894 | XLKD1 | 288 |
| 51776 | ZAK | 289 |
| 221527 | ZBTB12 | 290 |
| 346171 | ZFP57 | 291 |
| 23414 | ZFPM2 | 292 |
| 79830 | ZMYM1 | 293 |
| 7705 | ZNF146 | 294 |
| 84858 | ZNF503 | 295 |
| 79026 | AHNAK | 296 |
| 360 | AQP3 | 297 |
| 622 | BDH1 | 298 |
| 219738 | C10ORF35 | 299 |
| 726 | CAPN5 | 300 |
| 999 | CDH1 | 301 |
| 51673 | CGI-38 | 302 |
| 1159 | CKMT1B | 303 |
| 85445 | CNTNAP4 | 304 |
| 1303 | COL12A1 | 305 |
| 9244 | CRLF1 | 306 |
| 1410 | CRYAB | 307 |
| 1428 | CRYM | 308 |
| 113878 | DTX2 | 309 |
| 10278 | EFS | 310 |
| 79993 | ELOVL7 | 311 |
| 2041 | EPHA1 | 312 |
| 2045 | EPHA7 | 313 |
| 2051 | EPHB6 | 314 |
| 10205 | EVA1 | 315 |
| 2125 | EVPL | 316 |
| 2159 | F10 | 317 |
| 375061 | FAM89A | 318 |
| 8857 | FCGBP | 319 |
| 2261 | FGFR3 | 320 |
| 56776 | FMN2 | 321 |
| 2770 | GNAI1 | 322 |
| 7107 | GPR137B | 323 |
| 64388 | GREM2 | 324 |
| 3098 | HK1 | 325 |
| 688 | KLF5 | 326 |
| 5655 | KLK10 | 327 |
| 11202 | KLK8 | 328 |
| 10748 | KLRA1 | 329 |
| 10219 | KLRG1 | 330 |
| 4135 | MAP6 | 331 |
| 5603 | MAPK13 | 332 |
| 4312 | MMP1 | 333 |
| 4486 | MST1R | 334 |
| 4692 | NDN | 335 |
| 5092 | PCBD1 | 336 |
| 10158 | PDZK1IP1 | 337 |
| 5317 | PKP1 | 338 |
| 26499 | PLEK2 | 339 |
| 58473 | PLEKHB1 | 340 |
| 5366 | PMAIP1 | 341 |
| 79983 | POF1B | 342 |
| 5453 | POU3F1 | 343 |
| 5579 | PRKCB1 | 344 |
| 5745 | PTHR1 | 345 |
| 5792 | PTPRF | 346 |
| 57111 | RAB25 | 347 |
| 6095 | RORA | 348 |
| 6337 | SCNN1A | 349 |
| 6382 | SDC1 | 350 |
| 5268 | SERPINB5 | 351 |
| 11254 | SLC6A14 | 352 |
| 6578 | SLCO2A1 | 353 |
| 6586 | SLIT3 | 354 |
| 10653 | SPINT2 | 355 |
| 6768 | ST14 | 356 |
| 7070 | THY1 | 357 |
| 23650 | TRIM29 | 358 |
| 23555 | TSPAN15 | 359 |
| 11197 | WIF1 | 360 |
本领域技术人员将能够认识到,存在于本发明中的所述的决定子(DETERMINANT)涵盖了所有的形式以及变体,包括但不局限于,多形体,同型体,突变体,衍生物,前体包括核酸以及尿蛋白(pro-protein),裂解产物,受体(包括可溶性受体以及跨膜受体),配体,蛋白-配体复合物,以及翻译后的修饰变体(例如交联或者糖基化),片段,以及降解产物,以及任何的多单元的核酸,蛋白质,以及糖蛋白结构,其中所述的糖蛋白结构是由任意的所述决定子(DETERMINANT)作为所述的完整组配结构中的组成部分亚单元而构成的。
本领域技术人员将能够注意到,上述列出的所述决定子(DETERMINANT)来自于一套不同的生理学途径以及生物学途径,包括许多还没有被普遍接受认为与转移性疾病相关的途径。这些不同决定子(DETERMINANT)的分组,即使是在那些具有高显著性的片段中,可能预示着所述疾病的状态中的不同的信号或者所述疾病的不同的恶化速率。这样截然不同的决定子(DETERMINANT)的分组可能允许出现一种来自于所述决定子(DETERMINANT)的更为生物学详尽的以及临床学有效的信号,以及在所述的决定子(DETERMINANT)运算法则中进行类型识别的可能性,期中在所述的决定子(DETERMINANT)运算法则中对多种决定子(DETERMINANT)信号进行了组合。
本发明在一个方面涉及到一种决定子(DETERMINANT)子集;其他决定子(DETERMINANT)以及甚至是没有在上述的表格I中所列出的生物标记物可能被证实能够有效的给出由这些研究所提供的所述信号以及信息,期中所述的其他决定子(DETERMINANT)以及生物标记物与这些生理学途径以及生物学途径是相关的。如果达到了下述的程度:其他的生物标记物途径参与者(即,与那些在上述的表格I中的决定子列表中含有的生物标记物存在于共同途径中的其他的生物标记物参与者)同样是癌症或者转移性事件中的相关的途径参与者,则它们可以成为所述的生物标记物的功能等价物,期中所述的生物标记物是目前为止在表格I中所公开的例如趋化因子受体4(CXCR4)的生物标记物。这些其他的途径参与者在本发明的上下文中同样被认为是决定子(DETERMINANT),只要它们额外的与一种良好的生物标记物共享某些定义的特征即可,其中所述的特征应当包括参与本发明公开的生物学过程以及同样在分析意义上重要的特征例如所述的生物标记物所具有的以一种有效的信噪比的水平存在的生物可利用率,以及存在于一种有效的并且容易获得的样本基质例如血清中。这样的需求通常情况下会对一种生物学途径中的许多成员所具有的诊断有效性产生限制,并且仅仅频繁的发生在这样的途径成员中:构成分泌性物质的,那些容易在细胞的原生质膜上获取的,以及那些通过细胞死亡而被释放到所述的血清中的,这归因于细胞凋亡或者出于其他的原因,所述的原因例如是内皮重塑或者其他细胞的转换或者细胞坏死的过程,无论它们是否与癌症或者转移性事件的疾病恶化有关。然而,符合这一决定子(DETERMINANT)的高标准的其余生物标记物以及未来的生物标记物可能是非常有价值的。
此外,其他未被列出的生物标记物将与在表格I中所列出的作为决定子(DETERMINANT)的所述生物标记物具有非常高度的关联(出于本申请中的目的,当任意两个变量所具有的决定系数(R2)为0.5或者更高时,它们将被认为是“非常高度相关的”)。本发明涵盖了上述提及的决定子(DETERMINANT)的功能等价物以及统计学等价物。此外,这些额外的决定子(DETERMINANT)所具有的统计学效用在本质上取决于多种生物标记物之间的相互关系,并且任何新的生物标记物将通常被需要在一个小组内进行运作,其目的在于对基础生物学的意义进行精细描述。
在本发明的实践中,可以对上述列出的一种或者多种决定子(DETERMINANT)进行检测,优选的对两种或者多种决定子(DETERMINANT)进行检测。例如,可以对两种(2),三种(3),四种(4),五种(5),十种(10),十五种(15),二十种(20),四十种(40),五十种(50),七十五种(75),一百种(100),一百二十五种(125),一百五十种(150),一百七十五种(175),两百种(200),两百一十种(210),两百二十种(220),两百三十种(230),两百四十种(240),两百五十种(250),两百六十种(260)或者更多种,两百七十种(270)或者更多种,两百八十种(280)或者更多种,两百九十种(290)或者更多种决定子(DETERMINANT)进行检测。
在一些方面,可以对本发明中所列出的全部的三百六十种决定子(DETERMINANT)进行检测。优选的开始进行检测的所述决定子(DETERMINANT)的数量范围包括选自一至三百六十之间的任意最小值的界限范围,特别是两种,五种,十种,二十种,五十种,七十五种,一百种,一百二十五种,一百五十种,一百七十五种,两百种,两百一十种,两百二十种,两百三十种,两百四十种,两百五十种,所述的最小值与任意的最大值相配合,其中所述的最大值直至全部已知的决定子(DETERMINANT),特别是五种,十种,二十种,五十种,以及七十五种。特别优选的范围包括两种至五种(2-5),两种至十种(2-10),两种至五十种(2-50),两种至七十五种(2-75),两种至一百种(2-100),五种至十种(5-10),五种至二十种(5-20),五种至五十种(5-50),五种至七十五种(5-75),五种至一百种(5-100),十种至二十种(10-20),十种至五十种(10-50),十种至七十五种(10-75),十种至一百种(10-100),二十种至五十种(20-50),二十种至七十五种(20-75),二十种至一百种(20-100),五十种至七十五种(50-75),五十种至一百种(50-100),一百种至一百二十五种(100-125),一百二十五种至一百五十种(125-150),一百五十种至一百七十五种(150-175),一百七十五种至两百种(175-200),两百种至两百一十种(200-210),两百一十种至两百二十种(210-220),两百二十种至两百三十种(220-230),两百三十种至两百四十种(230-240),两百四十种至两百五十种(240-250),两百五十种至两百六十种(250-260)。
决定子(DETERMINANT)小组的构建
决定子(DETERMINANT)的分组可以被包含在“小组(panel)”中。在本发明的上下文中一个“小组”意味着一组生物标记物(无论它们是否是决定子,临床参数,或者传统实验室危险因素),其中包括不止一种的决定子(DETERMINANT)。一个小组中同样可以包括额外的生物标记物,例如,临床参数,传统实验室危险因素,其中所述的额外的生物标记物是已知的存在于癌症或者癌症转移中的,或者与癌症或癌症的转移有关,这些生物标记物与在表格I中列出的所述决定子(DETERMINANT)的一个选定的组之间发生了组合。
正如上文中所提到的,所列出的各种决定子(DETERMINANT)、临床参数、以及传统实验室危险因素中的许多,当在单独使用或者不是单独使用,被用来作为一个多重生物标记物决定子(DETERMINANT)小组中的成员时,在对存在于一个选定的普通群体中的各个宿主进行可靠的判定方面具有甚微的作用或者不具有临床上的作用,其中需要对彼此间进行判定的所述宿主为:正常的宿主,存在发生一种转移性事件的危险的宿主,以及患有癌症的宿主,并且因此不能够被可靠的单独用来对存在于上述三种状态之中的任何宿主进行分类。在每一个这样的群体中,即使当它们的平均测量值中存在统计学意义上显著的差异,正如在具有充足能力的研究中所普遍发生的那样,这样的生物标记物可能仍然被局限于它们在一个个体宿主中的适用性,并且在针对该宿主进行的诊断性预测或者预后性预测方面起到了微小的促进作用。统计学显著性的一个普遍的测量值是所述的p值,其代表的是:单独由偶然的原因引发出一个观察值所具有的概率;优选的,这样的p值为0.05或者更小,这代表着所述的目标观察值是由偶然原因所引发的机会为5%或者更小。这样的p值显著的取决于所完成的研究所具有的能力。
不管这种个体决定子(DETERMINANT)的表现如何,所述公式所具有的全面表现仅仅将所述的传统临床参数与几种传统实验室危险因素进行了组合,本发明人已经注意到两种或者更多种决定子(DETERMINANT)所形成的某些特异性的组合同样可以被用来作为多重生物标记物的小组,其中在所述的小组中包括那些已知被包含到一种或者多种生理学途径或者生物学途径之中的决定子(DETERMINANT)的组合,并且可以对这样的信息进行组合并且通过各种不同的公式的使用使其成为临床意义上有效的,其中所述的公式包括统计学分类运算法则以及其他,将它们进行组合并且在很多情况下所述的组合所具有的性能特征超越了所述的个体决定子(DETERMINANT)所具有的性能特征。这些特异性的组合表现出了一种可接受水平的诊断准确率,并且,当在一种接受过训练的公式中结合来自于多种决定子(DETERMINANT)的足够的信息时,通常能够可靠的生成一种高水平的诊断准确率,其中所述的诊断准确率可以由一个群体传送到另外一个群体。
本发明中的一个关键的方面是下述的一般概念:怎样将两种具有较低特异性或者具有较差表现的决定子(DETERMINANT)组合成为一个新的并且对于所述指定的适应症而言更为有效的组合。当使用了适宜的数学运算法则以及临床运算法则时,多重生物标记物通常能够产生比所述的个体组分更好的表现;这在敏感度以及特异性方面通常均是明显的,并且产生了一个更大的曲线下面积(AUC)。其次,在所述现有的生物标记物中通常存在有新的未被注意到的信息,因为为了通过所述的新的公式来达到一种提高的敏感度或者特异性水平,这是必要的。这种隐藏的信息甚至对于某些生物标记物而言可以保持真实性,所述的生物标记物在通常情况下被认为在单独使用时具有不是最理想的临床表现。事实上,在高的假阳性比例方面,在单独测量的一种单一的生物标记物中的所述不是最理想的表现可能非常好的成为一种指示:在所述的生物标记物的结果中含有某种重要的附加信息——在不存在与另外一种生物标记物以及一种数学公式进行组合的情况下不会被阐明的信息。
可以使用本领域中已知的几种统计学运算法则以及模拟运算法则来同时帮助进行决定子(DETERMINANT)筛选的选择以及对运算法则进行优化,其中在所述的运算法则中对这些选择进行了组合。统计学工具允许使用用于进行小组构建的更为合理的方式,其中所述的统计学工具例如是因素以及交叉生物标记物的关联性/协方差分析。表现出存在于所述的决定子(DETERMINANT)之间的欧几里得标准距离(Euclidean standardized distance)的数学聚类以及分类树可以被有利的使用。同样可以使用的是这种统计学分类技术的途径告知的播种,这可能是合理的方式,这种方式是以对个体决定子(DETERMINANT)所进行的筛选为基础的,其中所述的筛选是以所述的决定子在特定的途径或者生理学功能中的参与为基础的。
最终,例如统计学分类运算法则这样的公式可以被直接用来对决定子(DETERMINANT)进行筛选以及生成并且训练所述的最佳公式,其中所述的公式对于将来自于多个决定子(DETERMINANT)的结果组合成为一个单一的指数而言是必要的。通常,例如前向(从零个潜在的解释参数开始)选择以及后向选择(从所有可以利用的潜在的解释参数开始)这样的技术是可以使用的,并且信息准则被用来对在所述小组的性能与诊断准确性之间的折衷进行量化,以及对所使用的所述决定子(DETERMINANT)的数量进行量化,其中所述的信息准则例如是赤池信息准则(AIC)或者贝叶斯信息准则(BIC)。在一个前向选择的小组或者后向选择的小组中,各个决定子(DETERMINANT)所存在的位置可能与其向运算法则进行的增量信息含量的提供紧密相关,因此所述的贡献次序高度取决于存在于所述小组之中的其他的组成型决定子(DETERMINANT)。
临床运算法则的构建
可以使用任何的公式对决定子(DETERMINANT)的结果进行结合从而得到能够有效的用于进行本发明的实践的指数。正如在上文中所指示出的,并且并不局限于此,除了所述的各种不同的其他的指标之外,这样的指数能够对从一种疾病状态向另一种疾病状态所进行的转化所具有的概率、可能性、绝对危险或者相对危险、时机或者速率进行指示,或者对转移性疾病的未来的生物标记物的测量值进行预测。这可以针对的是在一段特定的时间段内或者时间范围内,或者针对剩余的终生危险,或者简单的作为一种指数被提供,其中所述的指数与另外一个参考宿主群体有关。
尽管在此描述了各种不同的优选的公式,但在本发明中提及的范围之外以及在上文中进行定义的若干其他模型以及公式类型是本领域技术人员熟知的。所使用的实际的模型类型或者公式本身可以从所述的可能的模型组中被筛选出来,这种筛选依据的是其在一种训练群体中所取得的结果所具有的性能以及诊断准确率的特征。所述的公式本身所具有的细节通常可以来自于决定子(DETERMINANT)的结果,其中所述的结果是在所述的相关性的训练群体中获得的结果。在其他的用途之中,这样的公式可能被打算用来将所述的特征空间在一组宿主类别中进行定位(map),其中所述的特征空间来自于一个或者多个决定子(DETERMINANT)输入(例如,能够有效的用于预测宿主的类别属籍,将所述的宿主分为正常、存在发生一种转移性事件的危险,患有癌症的类别),使用一种贝叶斯方法得到对危险的概率函数所进行的评估(例如,所述的患有癌症的危险或者出现一种转移性事件的危险),或者用以对所述的类别-条件概率进行评估,此后按照在先前的情况中那样,使用贝叶斯定理生成所述的类别概率函数。
优选的公式包括很多类型的统计学分类运算法则,并且特别是所述的判断分析的使用。所述的判断分析的目标在于通过一组先前被识别出的特征来预测类别的属籍。在使用线性判断分析(LDA)的情形中,通过某种标准对所述特征的线性结合进行识别,其中所述的线性结合能够使得组之间的分割最大化。可以使用一种基于eigengene的方法利用不同的阈值(ELDA)对用于线性判定分析(LDA)的特征进行识别,或者使用一种基于多变量方差分析(MANOVA)的梯度运算法则对所述的特征进行识别。可以进行前向、后向、以及逐步的运算法则,从而基于所述的Hotelling-Lawley统计学方法使没有产生分割的概率最小化。
基于Eigengene的线性判断分析(ELDA)是一种特征筛选技术,是由Shen等人(于2006年)研发的。所述的公式能够在一个多变量的框架内进行特征(例如,生物标记物)的筛选,其中使用一种经过修饰的本征分析(eigen analysis)对与所述的最为重要的本征向量有关的特征进行识别。“重要的”被定义为那些能够对存在于样本的差异中的最重要的变化进行解释的本征向量,其中所述的样本是那些被试图进行分类的样本,所述的分类是相对于某个阈值而言所进行的分类。
支持向量机(SVM)是一种分类公式,试图在寻找一个能够将两种类别进行分割的超平面。这种超平面上含有支持向量,数据点,其中所述的数据点正是距离所述超平面的空白距离。在适合的事件中,在所述数据的当前维度内不存在分割的超平面,通过将所述的数据投射至更大的维度内的方式使所述的维度发生很大的扩张,其中所述的数据的投射是通过采取初始变量的非线性函数的方式来实现的(参见Venables以及Ripley于2002年发表的文章)。尽管不是必需的,对支持向量机(SVM)的特征进行过滤通常能够对预测进行提高。可以通过使用一种非参数性的Kruskal-Wallis(KW)测试对所述的最佳单变量特征进行筛选的方式对支持向量机的特征(例如,生物标记物)进行识别。随机森林(RF,参见Breiman于2001年发表的文章)或者递归分割树(RPART,参见Breiman等人于1984年发表的文章)同样可以被单独进行使用或者进行组合使用,用以对生物标记物的组合进行识别,其中所述的生物标记物的组合是最为重要的。Kruskal-Wallis(KW)以及随机森林(RF)同样需要从所述的总体中筛选出许多的特征。递归分割树(RPART)能够通过使用一个可利用的生物标记物亚组建立一个单一的分类树。
为了对各个决定子(DETERMINANT)的测量方法所得到的结果进行预处理,使其在被呈递到所述的预测公式之前被处理成为更具价值的信息形式,可以使用其他的公式。最为显著的,关于一种群体所具有的平均值而言,对生物标记物的结果所进行的正态化处理,使用常用的数学转化方法例如对数函数或者逻辑斯蒂函数,作为正常的或者其他的分配位置,等等,这些都是本领域技术人员所熟知的。格外令人感兴趣的是基于临床参数的一组正态化处理,其中所述的临床参数是例如年龄,性别(gender),种族,或者性别(sex),其中特定的公式仅仅被用在同一类别的宿主上或者对一个临床参数进行连续性的合并从而作为一个输入值。在其他的情况中,可以将基于分析物的生物标记物结合到经过计算得出的变量之中,在此之后将所述的变量呈递到一个公式中去。
除了可以对来自于一个宿主的所述的个体参数值进行可能的正态化处理之外,一个针对所有宿主或者任意已知类别的宿主而言的整体预测公式本身是可以进行重复校验的,或者依据对一个群体预期普遍性以及平均生物标记物参数值的调整方法对其进行调整,其中使用的是在D’Agostino等人(于2001年)在JAMA《美国医学学会杂志》286:180-187中发表的文章中概述的技术,或者其他相类似的正态化技术以及重新校验技术。可以经由下述的方式对这样的流行病学调整的统计学方法进行连续的获取、证实、改进以及更新,其中所述的方式是:经由呈递在所述的模型之上的过往数据的登记,其中所述的数据可以是计算机可读形式的或者是另外的形式,或者偶然的经由对存储的样本所进行的追溯性的查询,或者经由对这样的参数以及统计学方法所进行的历史研究的参考。能够成为所述的公式校验或者其他调整方式的主题的另外的例子包括那些在Pepe,M.S.等人于2004年在对所述的让步比所具有的局限性进行的研究中所使用到的统计学方法;Cook,N.R.于2007年在涉及接受者操作特性曲线(ROC)曲线的研究中所使用到的统计学方法。最终,一个分类公式所得到的数字结果本身能够被转化进行后处理,其中所述的转化是通过对一个实际的临床群体以及研究结果以及所观察到的端点进行的参考而实现的,其目的在于对绝对危险进行校验并且为所述的分类公式或者危险公式所得到的存在变化的数字结果提供置信区间。这方面的一个例子是所述的绝对危险的呈递,以及这个危险的置信区间的呈递,所述的绝对危险以及置信区间是通过使用一种实际的临床研究而得来的,并且在Genomic Health,Inc.(红杉市,加利福尼亚)的Oncotype Dx产品中根据所述的参考得分公式得到的输出量对其进行了选择。一种进一步的修饰是使其调整为适合进行较小的亚群体的研究,这种调整是基于所述的分类公式或者危险公式所得到的输出值来完成的,并且通过它们的临床参数进行了定义以及筛选,其中所述的临床参数是例如年龄或者性别。
与临床参数以及传统实验室危险因素所进行的结合
前述提及的临床参数中的任何一个可以被用在本发明的实践当中作为一种决定子(DETERMINANT)输入值输入到一个公式中去或者作为一种进行预先筛选的标准,用于对一个需要进行测量的相关群体进行定义,其中所述的测量使用到的是一种特定的决定子(DETERMINANT)小组以及公式。正如上文中所记载的,临床参数同样可以被有效的用于所述的生物标记物的正态化处理以及预处理中,或者用于决定子(DETERMINANT)的筛选,小组的构建,公式类型的筛选以及推导,以及公式结果的后处理中。可以利用所述的传统实验室危险因素实现类似的方法,作为一个公式的输入值或者作为一种进行预先筛选的轨范。
决定子(DETERMINANT)的测量方法
可以使用本领域中任何已知的方法,在所述的蛋白质水平或者核酸水平的条件下对所述的决定子(DETERMINANT)所具有的水平或者剂量进行实际的测量。例如,在所述的核酸水平的条件下,Northern杂交分析以及Southern杂交分析,以及使用探针的核糖核酸酶保护检测可以被用来对基因表达进行确定,其中所述的探针能够对这些序列中的一个或者多个进行特异性的识别。或者可供选择的,可以使用基于逆转录-聚合酶链式反应检测(RT-PCR)对决定子(DETERMINANT)所具有的剂量进行测量,例如,使用对所述基因的差异性表达的序列具有特异性的引物,或者通过支链RNA的扩增作用以及Panomics,Inc.的检测方法。同样可以在所述的蛋白质水平的条件下对所述的决定子(DETERMINANT)所具有的剂量进行测定,例如,通过对所述肽的水平进行测量的方式,其中所述的肽是由本发明中所描述的基因产物来进行编码的,或者使用技术平台进行亚细胞的定位或者它们的活动,其中所述的技术平台例如是AQUA。这样的方法是本领域中熟知的并且包括,例如,基于抗体的免疫检测,适配子或者分子烙印,其中所述的抗体是由所述的基因所编码的蛋白质的抗体。任何的生物学材料均可以被用来进行所述蛋白质或其活性的检测/量化。或者可供选择的,可以筛选出一种适当的方法,用以对蛋白质所具有的活性进行测定,其中所述的蛋白质是由所述的标记物基因来进行编码的,所述的方法的选择依据的是被分析的每一种蛋白质所具有的活性。
可以以任何适当的方式对所述的决定子(DETERMINANT)蛋白质、多肽、变异体、及其多形体进行检测,但是通常情况下是通过下述方式来进行检测的:将一种来自于所述宿主的样本与一种抗体进行接触,其中所述的抗体能够与所述的决定子(DETERMINANT)蛋白质、多肽、变异体、或者多形体进行结合并且在此之后检测一种反应产物的存在或者不存在。所述的抗体可以是单克隆的,多克隆的,嵌合抗体,或者前述抗体的片段,正如在上文中进行过详细讨论的,并且可以使用任何适当的免疫检测来实现对所述的反应产物的检测。所述的来自于所述宿主的样本通常情况下是一种生物学流体,正如在上文中所描述的,并且可以与那些被用来实现上文中所描述的方法的生物学流体样本相同。
依照本发明进行实施的免疫检测可以是同源性检测或者是异源性检测。在一项同源性检测中,所述的免疫学反应通常涉及到所述的特异性抗体(例如,抗决定子(DETERMINANT)蛋白质抗体),一种被标记的分析物,以及所述的目标样本。当所述的抗体与所述的被标记的分析物进行结合的时候,来自于所述的标记之中的所述信号被进行了直接的或者间接的修饰。可以在一个同源性溶液中同时进行所述的免疫学反应以及对所述反应所具有的程度的检测。可以使用的免疫化学标记包括自由基,放射性同位素,荧光染料,酶,抗菌素,或者辅酶。
在一项异源性检测方法中,所述的试剂通常是所述的样本,所述的抗体,以及用以生成一种可检测性信号的工具。在上文中所描述的抗体是可以被使用的。所述的抗体可以被固定在一个支持物,培养板或者载玻片之上,其中所述的支持物例如是一个珠子(例如蛋白质A以及蛋白质G琼脂糖珠子),并且将其在一种液相中与所述的样本进行接触,其中所述的样本是被怀疑为含有所述抗原的样本。在此之后将所述的支持物从所述的液相中分离出来并且对所述的支持相或者所述的液相进行一种可检测性信号的检查,其中使用工具以生成这样的信号。所述的信号与所述的样本中的分析物的存在有关。用于生成一种可检测性信号的工具包括下述物质的使用:放射性标记,荧光标记,或者酶标记。例如,如果将要被检测的所述抗原含有第二个结合位点,可以将能够在这个位点上进行结合的一种抗体与一种可检测性的基团进行共轭并且将其在所述的分离步骤之前添加到所述的液相反应溶液中去。在所述的固体支持物上,所述的可检测性基团的存在标志着在所述的测试样本中所述抗原的存在。适合的免疫检测的例子是寡核苷酸法,免疫印迹法,免疫荧光法,免疫沉淀反应,化学发光方法,电化学发光方法(ECL)或者酶联免疫吸附检测。
本领域技术人员将熟知多种特异性的免疫检测形式及其变化形式,这些形式及其变化形式能够有效的用于实现本发明所公开的方法。大体上可以参见E.Maggio(于1980年)所著的Enzyme-Immunoassay《酶-免疫检测》(CRC Press,Inc.,Boca Raton,Fla.);同样可以参见Skold等人的美国专利No.4727022,其名称为“Methods for Modulating Ligand-Receptor Interactions and their Application《用于调节配体-受体相互作用的方法以及它们的应用》”;Forrest等人的美国专利No.4658678,其名称为“Immunoassay ofAntigens《抗原的免疫检测》”;David等人的美国专利申请No.4376110,其名称为“Immunometric Assays Using Monoclonal Antibodies《使用单克隆抗体的免疫量度检测》”;Litman等人的美国专利No.4275149,其名称为“Macromolecular Environment Control in Specific Receptor Assays《在特异性受体检测中的大分子环境的控制》”;Maggio等人的美国专利No.4233402,其名称为“Reagents and Method Employing Channeling《利用通道的试剂以及方法》”;以及Boguslaski等人的美国专利No.4230767,其名称为“Heterogenous Specific Binding Assay Employing a Coenzyme as Label《利用辅酶作为标记的异源特异性结合检测》”。
根据已知的技术,例如被动结合,可以将抗体与一种固体支持物进行共轭,其中所述的固体支持物适合进行一种诊断性的检测(例如,珠子,例如蛋白质A或者蛋白质G琼脂糖,微球体,培养板,载玻片或者孔,上述支持物是使用例如乳胶或者聚苯乙烯这样的材料来形成的。依照已知的技术,在本发明中所描述的抗体同样能够与可检测性的标记物或者基团进行共轭,其中所述的可检测性的标记物或者基团是例如放射性标记(例如,35硫,125碘,131碘),酶标记(例如,辣根过氧化物酶,碱性磷酸酶),以及荧光标记(例如荧光素,Alexa,绿色荧光蛋白,若丹明)。
抗体同样能够有效的用来对决定子(DETERMINANT)蛋白质、多肽、变异体、以及多形体的翻译后修饰进行检测,其中所述的修饰例如是酪氨酸的磷酸化作用,苏氨酸的磷酸化作用,丝氨酸的磷酸化作用,糖基化作用(例如,氧-乙酰葡萄糖胺)。这样的抗体能够特异性的检测到存在于一种目标蛋白质中的所述发生磷酸化的氨基酸,并且可以被用在本发明中所描述的免疫印迹法,免疫荧光法,以及酶联免疫吸附检测(ELISA)中。这些抗体是本领域技术人员熟知的,并且是可以通过商业购买获得的。同样可以使用亚稳定离子在反射基质辅助的激光解析电离飞行时间质谱(MALDI-TOF)中对翻译后的修饰进行测定(参见Wirth,U.等人(于2002年)在Proteomics《蛋白质组学》2(10):1445-51中发表的文章)。
对于已知具有酶活性的决定子(DETERMINANT)蛋白质、多肽、变异体、以及多形体而言,可以使用本领域已知的酶检测方法对所述的活性进行体外的检测。这样的检测包括,但不局限于,除了许多其他检测以外,激酶检测,磷酸酶检测,还原酶检测。可以通过使用已知的运算法则对所述的速率常数KM进行测量的方式,确定出所述的酶活性动力学的修饰作用,其中所述的运算法则是例如希尔标绘法(Hill plot),米氏方程(Michaelis-Menten),线性回归标绘法例如Lineweaver-Burk分析,以及Scatchard标绘法。
通过使用序列信息能够对所述的决定子(DETERMINANT)序列的表达(如果存在的话)进行检测并且使用本领域普通技术人员所熟知的技术对其进行测量,其中所述的序列信息是由所述的决定子(DETERMINANT)序列的数据库条目来进行提供的。例如,存在于相对于决定子(DETERMINANT)序列的序列数据库条目之中的序列,或者存在于本发明中公开的所述序列之中的序列,可以被用来构建探针,用于在例如下述方法中检测决定子(DETERMINANT)的RNA序列:Northern印迹杂交分析或者方法,所述的方法能够特异性的,并且优选的,定量的扩增特异性的核酸序列,其中所述的序列数据库条目相对应于所述的决定子(DETERMINANT)序列。作为另外一个例子,所述的序列可以被用来构建引物,用于在例如下述方法中对所述的决定子(DETERMINANT)序列进行特异性的扩增:基于扩增的检测方法例如基于逆转录-聚合酶链式反应(RT-PCR)。当存在于基因表达之中的改变与基因的扩增、缺失、多形体、以及变异有关时,可以通过对存在于所述的测试以及参考细胞群体中的接受检查的DNA序列的相对数量进行比较的方式,在测试以及参考群体之间进行序列的比较。
可以使用任何本领域已知的方法在所述的RNA水平上对本发明中公开的所述基因的表达进行测量。例如,使用探针的Northern杂交分析可以被用来确定基因的表达,其中所述的探针能够对这些序列中的一个或者多个进行特异性的识别。或者可供选择的,可以使用基于逆转录的聚合酶链式反应检测(RT-PCR)对表达进行测量,例如,使用对所述的差异化表达的序列具有特异性的引物。同样可以使用例如其他的目标扩增方法(例如,转录介导扩增法(TMA),链置换扩增法(SDA),核酸序列依赖性扩增(NASBA)),或者信号扩增方法(例如,支链DNA杂交方法),以及类似的方法对RNA进行量化。
可供选择的,可以对决定子(DETERMINANT)蛋白质以及核酸的代谢产物进行测量。所述的术语“代谢产物”包括在一种代谢过程中存在的任意的化学产物或者生物化学产物,例如有一种生物分子(例如,蛋白质,核酸,碳水化合物,或者脂质体)的加工、断裂或者消耗而产生出的任何化合物。可以使用本领域技术人员已知的各种不同的方式对代谢产物进行检测,所述的方式包括所述的折射率光谱(RI),紫外光谱(UV),荧光分析,放射化学分析,近红外光谱(near-IR),核磁共振光谱(NMR),光散射分析(LS),质谱,高温分解质谱,比浊法,色散型拉曼光谱,质谱联用的气相色谱,质谱联用的液相色谱,质谱联用的基质辅助的激光解析电离飞行时间质谱(MALDI-TOF),质谱联用的离子喷雾色谱,毛细管电泳,核磁共振光谱(NMR)以及红外光谱(IR)检测。(参见WO 04/056456以及WO 04/088309,上述文章中的全部内容均在此被引入作为参考)。就这一点而言,可以使用上述提及的检测方法或者本领域技术人员已知的其他方法对其他的决定子(DETERMINANT))分析物进行测量。例如,可以使用荧光染料对存在于一个样本之中的流动的钙离子(Ca2+)进行检测,其中所述的荧光染料除了其他之外,例如是所述的氟系列,例如是Fura-2A,Rhod-2。可以使用试剂对其他的决定子(DETERMINANT)代谢产物进行类似性的检测,其中所述的试剂是经过特意的设计或者剪裁过的,用以对这样的代谢产物进行检测。
试剂盒
本发明同样包括一种决定子(DETERMINANT)检测试剂,例如是一种核酸,所述的试剂能够通过具有同源性的核酸序列而对一个或者多个决定子(DETERMINANT)核酸进行特异性的识别,例如是一个寡核苷酸序列,所述的决定子(DETERMINANT)核酸的一部分的互补物或者由所述决定子(DETERMINANT)核酸编码的蛋白质的抗体一同被包裹在所述的试剂盒形式中。所述的寡核苷酸可以是所述决定子(DETERMINANT)基因的片段。例如,所述的寡核苷酸可以具有200、150、100、50、25、10或者更少个寡核苷酸的长度。所述的试剂盒中可以在各自分离的容器内装有一种核酸或者抗体(可以是已经与以一种固体基质进行结合的,或者与试剂进行单独的包装,其中所述的试剂能够将它们与所述的基质进行结合),对照制剂(阳性的和/或阴性的),和/或一种可检测性的标记例如荧光素,绿色荧光蛋白,若丹明,花青染料,Alexa染料,荧光素酶,放射性标记,除其他之外。用以实现所述检测的说明书(例如,书写形式的,录音形式的,盒式磁带录像机(VCR),只读光盘(CD-ROM),等等)可以被包含在所述的试剂盒之中。所述的检测可以是以例如一种Northern杂交或者夹心酶联免疫吸附检测(ELISA)的形式来进行的,这在本领域是已知的。
例如,可以将决定子(DETERMINANT)检测试剂固定在一种固体的基质上,其中所述的固体基质例如是一种多孔的条带,从而形成至少一个决定子(DETERMINANT)检测位点。所述的多孔条带上的测量区域或者检测区域内可以包括许多个含有核酸的位点。一个测试条带上同样可以含有用于进行阴性对照和/或阳性对照的位点。或者可供选择的,对照位点可以定位于一个与所述的测试条带相分离的条带之上。任选的,所述的不同的检测位点上可以含有不同剂量的固定化的核酸,例如,在所述的第一个检测位点上具有一种较高的剂量而在随后的位点上具有较低的剂量。当加入了所述的测试样本时,所述的位点的数量呈现出一种可检测性的信号,从而为存在于所述样本之中的所述决定子(DETERMINANT)的剂量提供了定量的指示。所述的检测位点可以被配置成任意适当的可检测的形状,并且在通常情况下被配置成为一种条状或者圆点状,其跨越了所述测试条带的宽度。
可供选择的,所述的试剂盒中含有一种核酸底物阵列,其中包括一个或者多个核酸序列。存在于所述阵列之上的所述核酸能够特异性的识别一个或者多个由决定子(DETERMINANT)1-360所代表的核酸序列。在各种不同的实施方式中,可以凭借与所述阵列的结合来识别出2个、3个、4个、5个、6个、7个、8个、9个、10个、15个、20个、25个、40个、50个、100个、125个、150个、175个、200个、250个、275个或者更多个序列的表达,其中所述的序列是由决定子(DETERMINANT)1-360所代表的。所述的底物阵列可以存在于例如一种固体底物之上,例如是在美国专利No.5744305中所描述的一个“芯片”之上。或者可供选择的,所述的底物阵列可以是一种溶液阵列,例如xMAP(Luminex,Austin,TX),Cyvera(Illumina,San Diego,CA),CellCard(Vitra Bioscience,Mountain View,CA)以及Quantum Dots’Mosaic(Invitrogen,Carlsbad,CA)。
用以对所述的决定子(DETERMINANT)进行检测的所述抗体的适合来源包括可商业购买获得的来源例如,Abazyme,Abnova,Afrinity Biologicals,AntibodyShop,Biogenesis,Biosense Laboratories,Calbiochem,Cell Sciences,Chemicon International,Chemokine,Clontech,Cytolab,DAKO,Diagnostic BioSystems,eBioscience,Endocrine Technologies,Enzo Biochem,Eurogentec,Fusion Antibodies,Genesis Biotech,GloboZymes,Haematologic Technologies,Immunodetect,Immunodiagnostik,Immunometrics,Immunostar,Immunovision,Biogenex,Invitrogen,Jackson ImmunoResearch Laboratory,KMI Diagnostics,Koma Biotech,LabFrontier Life Science Institute,Lee Laboratories,Lifescreen,Maine Biotechnology Services,Mediclone,MicroPharm Ltd.,ModiQuest,Molecular Innovations,Molecular Probes,Neoclone,Neuromics,New England Biolabs,Novocastra,Novus Biologicals,Oncogene Research Products,Orbigen,Oxford Biotechnology,Panvera,PerkinElmer Life Sciences,Pharmingen,Phoenix Pharmaceuticals,Pierce Chemical Company,Polymun Scientific,Polysiences,Inc.,Promega Corporation,Proteogenix,Protos Immunoresearch,QED Biosciences,Inc.,R & D Systems,Repligen,Research Diagnostics,Roboscreen,Santa Cruz Biotechnology,Seikagaku America,Serological Corporation,Serotec,SigmaAldrich,StemCell Technologies,Synaptic Systems GmbH,Technopharm,Terra Nova Biotechnology,TiterMax,Trillium Diagnostics,Upstate Biotechnology,US Biological,Vector Laboratories,Wako Pure Chemical Industries,以及Zeptometrix。然而,本领域技术人员能够通过常规方法制备抗体,核酸探针,例如,作用于表格I中的任何一种所述决定子(DETERMINANT)的寡核苷酸,适配子,siRNA,反义寡核苷酸。
实施例
实施例1:一般方法
转基因小鼠以及原发性肿瘤
按照描述(参见Ganss,Montoliu等人于1994年发表的文章;Chin,Pomerantz等人于1997年发表的文章;Chin,Tam等人于1999年发表的文章),对所述的反义四环素转录激活子,Tet启动子以及所述的酪氨酸酶增强剂/启动子转基因进行使用。按照与描述相类似的方式,在所述的Tet启动子的调控下对小鼠的c-MetcDNA(一个来自于George F Vande-Woude,Grand Rapids,MI的礼物)进行克隆。以一种可以预料的频率生成了多个转基因生成品系(founder line)。所述的被精确定义的活化品系(activator line)(酪氨酸酶/反义四环素转录激活子,品系37,参见Chin于1999年在Nature《自然》中发表的文章)以及三种独立的报告品系(reporter line)(Met15,Met28以及Met40)被用来进行这些研究。
为了在体内对转基因的表达进行活化,在饮用水中给MET转基因小鼠饲喂强力霉素(以2微克/毫升的水平存在于糖水中),并且对自然发生的肿瘤的形成进行观察,其中所述的MET转基因小鼠正处于断奶年龄。通过利用三溴乙醇(0.5克/千克体重)进行腹腔内注射的方式对一小组动物(3周)进行麻醉,并且在其背部造成一个20毫米的椭圆形伤口,在此之后对伤口进行缝合。对动物进行两周的观察,观察其肿瘤的形成或者不健康状况的出现。对premoribund动物或者存在显著的肿瘤负荷的动物进行处死,在此之后对其进行详细的尸体解剖。将肿瘤样本固定在10%的福尔马林中并且利用石蜡对其进行包埋,用于按照先前所描述的(参见Chin,L等人于1997年在Genes and Dev《基因与发展》中发表的文章)进行组织学分析。在可以获得足够的样本的情况下,对原发性肿瘤进行闪冻用于进行后续的分析并且生成细胞系。
细胞培养。通过下述方式从小鼠的肿瘤中获得恶性黑素瘤细胞系:利用胶原酶+透明质酸酶(2毫克/毫升;Sigma)进行2小时的消化,在此之后利用RPMI 1640培养基(Gibco BRL)对其进行培养,其中在所述的培养基中含有10%的胎牛血清(FBS)以及1%的盘尼西林/链霉素。按照描述10从新生小鼠的表皮处生成黑素细胞培养物并且将其保持在RPMI 1640中,其中在所述的RPMI 1640中含有5%的胎牛血清(FBS),1%的盘尼西林/链霉素,200匹摩的霍乱毒素,200纳摩的12-十四烷佛波酯-13-乙酸酯(TPA)。通过以2微克/毫升的水平进行强力霉素的添加,在上述培养的细胞内诱导转基因c-Met的表达。将M3 BRAF黑素细胞,经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)启动的(primed)黑素细胞,WM3211以及WM115保持在RPMI 1640中,在所述的RPMI 1640中含有10%的胎牛血清(FBS),1%的盘尼西林/链霉素。按照Garraway等人11的描述,经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)能够对PMEL/hTERT/CDK4(R24C)/p53DD/BRAFV600E细胞的亚克隆进行识别。
组织学分析以及免疫组织化学染色。根据学院的指导对小鼠进行处死并且将器官固定在10%的经过缓冲的福尔马林之中并且进行石蜡的包埋。利用苏木素-伊红(H&E)对组织切片进行染色,从而能够进行对所述损伤的分类以及对肿瘤转移的检测。为了对c-Met蛋白质进行检测并且对其活化状态进行确定,利用全部的c-Met以及磷酸化的c-Met(Tyr1349)抗体对肿瘤的样本进行免疫染色,其中所述的抗体来自于Cell Signaling Technology。利用来自于Sigma的S100抗体对肿瘤进行免疫染色。
通过逆转录-聚合酶链式反应(RT-PCR)以及实时定量聚合 酶链式反应(PCR)进行的基因表达。为了对基因的表达进行分析,根据制造商给出的方案,使用Trizol(Gibco BRL)从原发性的皮肤恶性黑素瘤中或者从经过培养的细胞中分离出总RNA。利用RQ1脱氧核糖核酸酶(DNAse)(Promega)对总RNA进行处理并且利用1微克的总RNA来进行逆转录反应,其中在所述的逆转录反应中使用了Superscript II聚合酶(Invitrogen),其中所述的聚合酶利用oligo(dT)作为引物。通过聚合酶链式反应(PCR)或者定量实时聚合酶链式反应(PCR)对编码区域进行扩增,其中使用到SYBR Green(Applied Biosystems)在一个Mx3000P实时聚合酶链式反应(PCR)系统上(Stratagene)进行。核糖体蛋白质R15被用来作为一种内部表达对照。引物序列如下:c-Met:5’-TCTGTTGCCATCCCAAGACAACATTGATGG,5’-AAATCTCTGGAGGAGGTTGG;人类生长因子(HGF):5’-CAAGGCCAAGGAGAAGGTTA,5’-TTTGAAGTTCTCGGGAGTGA;酪氨酸(Tyr):5’-CCAGAAGCCAATGCACCTAT,5’-AGCAATAACAGCTCCCACCA;酪氨酸酶TRP1:5’-ATTCTGGCCTCCAGTTACCA,5’-GGCTTCATTCTTGGTGCTTC;酪氨酸酶DCT:5’-AACAACCCTTCCACAGATGC,5’-TCTCCATTAAGGGCGCATAG;R15:5’-CTTCCGCAAGTTCACCTACC,反义-TACTTGAGGGGGATGAATCG。SMAD3引物来自于超级阵列。
基因表达曲线以及数据分析。按照上文中描述的方法对Met驱动以及HRas驱动的小鼠肿瘤的RNA进行提取,对其进行标记并且依照制造商的方案通过所述的Dana-Farber癌症研究所微阵列核心设备将其杂交至Affymetrix GeneChip Mouse Genome(Affymetrix基因芯片小鼠基因组)4302.0阵列中。使用所述的R/bioconductor软件包(www.bioconductor.org)对表达数据进行处理。按照描述12进行分析。简要的说,所述的背景校正方法是MAS(版本4.5),正态化方法是常数,PM调整方法是MAS(版本4.5),表达数值的概述方法是中位数平滑(RMA)。P/M/A命名方法(call method)是MAS5。对带有至少2个已存在的命名(present call)的探针组(16434个探针组)进行选择,用以进行进一步的差异化表达的分析,其中所述的已存在的命名是存在于所有的12个肿瘤样本之中的,所述的差异化的表达分析是发生在六个iMet肿瘤与六个iHRas肿瘤之间的。微阵列的显著性分析(SAM 2.0;http://www-stat.stanford.edu/~tibs/SAM/)被用来进行差异化的表达分析13。对两种类型的未发生配对的样本进行分析,在此之后针对最小两倍的改变以及delta值的调整进行过滤,这样一来所述的假发现率应当小于0.05。按照上文中所描述的,通过微阵列显著性分析(SAM)来实现对所述的HOXA1诱导的转录的分析,其中使用了从细胞(HMEL468,WM115,WM3211)中提取的RNA,其中所述的细胞被绿色荧光蛋白(GFP)或者HOXA1进行了转导,在此之后依照制造商的方案通过所述的Dana-Farber癌症研究所微阵列核心设备将经过标记的cDNA杂交至Affymetrix GeneChip Human Genome U133Plus 2.0(Affymetrix基因芯片人类基因组)上。所述的Ingenuity途径分析程序(http://www.ingenuity.com/index.html)被用来对所述的细胞功能以及途径进行进一步的分析,其中所述的细胞功能以及途径在转移性恶性黑素瘤中被进行了显著性的调节。
小鼠的基因表达与人类阵列比较基因组杂交(CGH)数据之 间的比较。在人类直系同源基因上对非冗余的差异化表达的探针组进行标定,其中所述的探针组是从小鼠肿瘤的表达分析中获得的(如上文中所述),其中所述的人类直系同源基因在人类转移性恶性黑素瘤中表现出拷贝数量的异常,这种异常是通过阵列-比较基因组杂交(CGH)(GEO Accession #GSE7606)来识别的。同源基因数据库(美国国立生物技术信息中心NCBI)被用来对直系同源性的人类基因进行识别,识别它们在iMet肿瘤与iRas肿瘤中所进行的差异化表达。分别对在iMet肿瘤(与iRas肿瘤)中发生了上调节或者去调节的基因以及在人类的转移性疾病中发生了扩增或者删除的基因进行筛选。
无监督式聚类以及卡普兰-迈耶(Kaplan-Meriers)存活分析。转移性决定子所具有的表达曲线被用来将295种乳腺癌肿瘤14;15聚类至两组中,其中所述的聚类是通过使用R的k-均值聚类(http://www.r-project.org/)来实现的。针对所述的两个聚类组进行卡普兰-迈耶(Kaplan-Meier)的存活分析,其中使用了以R来表示的存活包,并且使用以R来表示的存活统计包对p值进行计算。
DNA构建体以及低复杂性文库。pRetrosuperSmad3以及p3TPLux来自于Addgene(分别为#15726以及11767)。对于所述的低复杂性的cDNA文库而言,从所述的ORFeome保藏中心(Dana-Farber癌症研究所)处获得代表199个基因的230个cDNA,并且以高通量的水平将其转移至pLenti6/V5DEST(Invitrogen)中,其中所述的转移是按照制造商的建议经由Gateway重组来实现的。对在所述的入侵筛选中备选的cDNA得分进行排序并且使用所述的V5表位对表达进行验证,并且在所有的入侵验证研究中使用同源性的克隆制剂。
96孔病毒的生成、转导以及transwell入侵检测。在进行转染之前的24小时,以每孔100微升的水平在96孔平底培养板内进行大约3x104个293T细胞的接种,在此之后在添加有10%的胎牛血清(FBS)(抗生素)的DMEM中进行转染(大约90%的融合度)。为了进行每个孔内的转染,使用Opti-MEM(Invitrogen)将150纳克的病毒骨架以及110纳克的慢病毒包装载体稀释至15微升。将上述得到的载体混合物与15微升Opti-MEM进行混合,其中在所述的Opti-MEM中含有0.6微升的Liptofectamine 2000(Invitrogen),在室温(RT)下进行20分钟的培养并且将其添加到100微升的培养基中从而覆盖所述的293T细胞。经过转染的大约10小时之后,利用添加有10%的胎牛血清(FBS)以及P/S的DMEM对所述的培养基进行取代,并且在经过转染的36小时之后开始获取4个病毒的上清液收集物并且将它们进行混合。将含有8微克/毫升凝聚胺的150微升的病毒上清液添加到靶向细胞(经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468))中,其中所述的靶向细胞在进行感染(70-80%的融合度)的24小时前被接种至96孔平底培养板内。对细胞进行两次感染并且在经过所述的第二次感染之后允许其在RPMI中进行24小时的恢复,其中在所述的RPMI中添加有10%的胎牛血清(FBS)以及P/S,经过上述的恢复之后,对细胞进行胰蛋白酶化处理并且按照制造商的推荐将其放置在96孔肿瘤入侵培养板(BD Bioscience)中。通过体内标记的方式对发生入侵的细胞进行检测,其中所述的体内标记使用的是4微摩的钙黄绿素AM(BD Bioscience),并且在494/517纳米下通过荧光性对其进行测量(Abs/Em)。对阳性得分的备选物进行识别,因为它们的得分偏离所述的向量对照两倍的标准偏差。
Transwell入侵检测。按照制造商的建议,利用标准的24孔入侵小室(BD Biosciences)对入侵作用进行评价。简要的说,对细胞进行胰蛋白酶化处理,利用磷酸盐缓冲液(PBS)进行两次漂洗,将其重新悬浮在不含有血清的RPMI 1640培养基中,并且对其进行接种,其中经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)的接种水平为7.5x104个细胞/孔,WM3211的接种水平为2.0x104并且WM115的接种水平为5.0x104。对小室进行一式三份或者一式四份的接种并且将其放置在含有10%的血清的培养基中作为一种化学诱导剂,同时也将其一式两份的放置在细胞培养板中作为输入对照。经过22小时的培养之后,将小室固定在10%的福尔马林之中,利用结晶紫对其进行染色用于进行手工的计数或者像素的量化,其中所述的像素量化是利用Adobe Photoshop(Adobe)来实现的。对数据进行正态化处理,将细胞输入为与对照值在细胞数量上的差异(负载对照)。为了对SMAD3在由HOXA1介导的入侵作用中的解体(knock-down)进行评价,一种经过验证的shRNA构建体以SMAD3为靶向(pSUPER-shSMAD3),并且使用标准的逆转录酶病毒制备方案来生成病毒。平行的利用非靶向性的shRNA(pSUPER-shNT)对对照细胞进行转导,用以进行入侵作用的比较。
异种移植物以及尾部静脉注射的研究。利用绿色荧光蛋白(GFP)或者HOXA1病毒对经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)进行稳定的转导。为了进行异种移植物的研究,以1x106个细胞/位点的水平通过皮下的方式将细胞植入到CB-17-scid(C.B-Igh-lb/IcrTac-Prkdcscid;Taconic)小鼠的双侧。为了对肺部的播种能力进行评价,向所述的CB-17-scid小鼠的尾部静脉内注射5.0x105个细胞。对所有动物的肿瘤的形成进行监测,在此之后进行尸体解剖以及肿瘤的组织学分析。
转化生长因子β(TGFβ)报告基因的检测。在利用所述的3TPLux报告基因(每孔1微克)以及对照报告基因(珊瑚虫荧光素酶,每孔20微克)进行转染之前的24小时,将细胞以每孔2x105个细胞的水平一式三份的接种至6孔培养板中。经过24小时的培养之后,利用转化生长因子β(TGFβ)(20纳克/毫升,R & D Systems)对细胞进行24小时的处理并且按照制造商的方案对其进行荧光素酶的分析(Promega),在所述的分析中使用的是Lumat LB9507光度计,用以取得报告基因的活化作用,这种活化作用是通过所述的萤火虫/珊瑚虫荧光素酶的比例来指示的。使用双尾t检验对p值进行计算。
免疫印迹分析。当需要时,利用20纳克/毫升的转化生长因子b(TGFb)(R & D Systems)对细胞进行处理,在此之后利用磷酸盐缓冲液(PBS)对其进行两次洗涤并且对其进行裂解,其中裂解使用的是含有1毫摩苯甲基磺酰氯(PMSF)的RIPA缓冲液(150毫摩的氯化钠,50毫摩的Tris盐酸,pH为7.5,500微摩的乙二胺四乙酸,100微摩的乙二醇二乙醚四乙酸,1.0%的Triton-X,以及1%的脱氧胆酸钠),1倍的蛋白酶抑制剂混合物(Sigma)以及1倍的磷酸酶抑制剂(Calbiochem)。在4℃下,经过在裂解缓冲液中进行的30分钟的培养之后,对全细胞提取物进行分离,通过在4℃下以10k 10分钟的条件进行离心对其进行清除,之后通过DC蛋白质检测(BioRad)对蛋白质的浓度进行确定。通过在NuPAGE 4-12%Bis-Tris凝胶(Invitrogen)上的分离使所述的蛋白质呈现出来,在聚偏氟二乙烯(PVDF)(Millipore,Billerica,MA)上对其进行印迹处理,之后利用所述的指定抗体对其进行了培养,其中利用存在于磷酸盐缓冲液(PBS)+吐温-20的5%的乳对所述的聚偏氟二乙烯(PVDF)进行了阻滞。下述的抗体被用来进行免疫印迹:pSmad3以及总Smad3(Cell Signaling Technology),α-微管蛋白(Sigma),V5(Invitrogen),膦-粘附斑激酶(FAK)(pY397;Invitrogen)。
通过平行定量技术进行的基于RNA表达的检测。作为一个可以替代基于蛋白质表达的分析的可供选择项,QuantiGene Plex技术(Panomics)同样可以被利用来评价PD的RNA表达。所述的QuantiGene平台是以所述的分支DNA技术为基础的,分支DNA技术是一种夹心核酸杂交检测,能够提供一种独特的方式用于进行RNA的检测以及量化,其中所述的检测以及量化是通过对所述的报告基因信号的扩增而不是对所述序列的扩增来实现的(参见Flagella,M.,Bui,S.,Zheng,Z.,Nguyen,C.T.,Zhang,A.,Pastor,L.,Ma,Y.,Yang,W.,Crawford,K.L.,McMaster,G.K.,等人(于2006年)在Anal Biochem《分析生物化学》352,50-60中发表的文章A multiplex branched DNA assay for parallel quantitative gene expression profiling《一种用于平行定量的基因表达曲线的多元分支DNA检测》)。这种技术能够可靠的定量测量RNA的表达,其中所述的RNA的表达发生在新鲜的、冷冻的或者福尔马林固定、石蜡包埋的(FFPE)组织匀浆中(参见Knudsen,B.S.,Allen,A.N.,McLerran,D.F.,Vessella,R.L.,Karademos,J.,Davies,J.E.,Maqsodi,B.,McMaster,G.K.,以及Kristal,A.R.(于2008年)在J Mol Diagn《分子诊断学杂志》10,169-176中发表的文章Evaluation of the branched-chain DNA assay for measurement of RNA in formalin-fixed tissues《对用于在福尔马林固定的组织中进行RNA测量的支链DNA检测的评估》)。正如在附图17A中所表示出的,一种可行性的引导已经表明,我们能够可靠的对在21个色素痣以及22个恶性黑素瘤样本中发生的UBE2C的RNA表达进行测量,其中所述的色素痣以及恶性黑素瘤样本处于福尔马林固定、石蜡包埋的状态中。对每一个基因所进行的分析达到了优秀的再现性,具有存在于8-9%的范围之内的变异系数(CV),因此满足了最高程度的质量控制的标准。这种方法因此为我们提供了一种理想的可供选择的方式,用以收集首先观察到的一种目标备选物所具有的表达类型,而不需要可以利用的抗体。著名的是,对UBE2C所进行的QuantiGenePlex分析对标志着UBE2C具有致肿瘤活性的结果进行了验证。特别的,使用所述的经典的共转化检测,我们发现UBE2C与活化的HRASV12进行合作从而增加了转化焦点在Ink4a/Arf-缺陷型原发性小鼠胚胎纤维原细胞中的形成(附图17B)。
自动化定量分析 允许对存在于亚细胞间隔之内的蛋白质的浓度进行精确的测量,正如在其他处所详细描述的那样[参见Camp,R.L.,Chung,G.G.,& Rimm,D.L.,(于2002年)在Nat Med《天然药物学》8(11),1323-1327中发表的文章Automated subcellular localization and quantification of protein expression in tissue microarrays《组织微阵列中的自动化亚细胞定位以及蛋白质表达的量化》]。简要的说,通过所述的PM-2000显微镜捕获到一系列高分辨率的单色波图像。对于每一个histospot而言,使用来自于所述的4’,6-二脒基-2-苯基吲哚(DAPI)的信号可以获得焦点内图像以及焦点外图像,其中所述的信号是对细胞角蛋白以及原发性抗体具有特异性的信号。通过建立一种与细胞角蛋白以及S100信号之间的肿瘤“掩蔽”的方式,将肿瘤区分为基质性元素以及非基质性元素。这形成了一种以强度阈值为基础的二元的掩蔽(每一个像素是“开启”或者“关闭”的),其中所述的强度阈值是通过对histospot的视觉检查来设定的。通过下述方式对存在于每一个亚细胞间隔之中的所述目标蛋白质所得到的自动化定量分析得分进行计算:利用所述的具体的间隔所具有的面积除以所述的信号强度(以从0-255的数值范围进行打分)。在每一个点上具有小于5%的肿瘤面积的样本不被包含在自动化定量分析之内,因为它不能够作为所述的相应肿瘤样本的代表。
实施例2:一种表型驱动的进化保守型转移信号的识别
具有非常不同的转移可能性的遗传工程化小鼠(GEM)的恶性黑素瘤模型被用在这里作为一种生物学系统,用以减少在所述的人类癌症的分析中所固有的混乱的不确定性,其中所述的混乱的不确定性除了其他因素之外,包括,与微转移或者大转移的文件中涉及到的变量以及继续发展的持续时间。被利用的所述的两种小鼠的恶性黑素瘤模型是(i)一种新近研发的Met驱动的遗传工程化小鼠(GEM)模型,所述的模型是由在所述的Ink4a/Arf空白背景上的酪氨酸酶驱动的rtTA以及tet-Met转基因构成的(Tyr-rtTA;Tet-Met;Ink4a/Arf/-,在本发明中被称为“iMet”)以及(ii)之前描述过的HRASV12G驱动的小鼠恶性黑素瘤模型(Tyr-rtTA;Tet-HRASV12G;Ink4a/Arf/-,在本发明中被称为“iHRAS*”)12。表型鉴定已经表明:有75%的所述iMet小鼠在活组织检查的位点处形成了恶性黑素瘤,其具有平均为12周的潜伏期。这些肿瘤是黑素细胞标记物阳性的,表现出磷活化的Met受体以及人类生长因子(HGF)的表达(附图5A-E);除此之外,衍生的iMet恶性黑素瘤细胞在transwell小室入侵性检测中表现出了强劲的入侵活性,这种活性是对重组的人类生长因子(HGF)所进行的应答(附图2A)。与存在于人类中的高级别的转移性恶性黑素瘤中的人类生长因子(HGF)-MET信号的活化作用13相协调的是,除了在所述的肾上腺以及肺部软组织中的偶然的扩散之外,存在于重生(de novo)的转基因动物中的iMet恶性黑素瘤一律向所述的淋巴结内进行转移,其中所述的肾上腺以及肺部软组织属于在人类恶性黑素瘤的转移性播种中的常见的位点(附图2B)。这种高度渗透性的转移性表型与所述的iHRAS*恶性黑素瘤模型形成了鲜明的对比,所述的iHRAS*恶性黑素瘤模型的特征在于非转移性的原发性皮肤恶性黑素瘤12;14。通过下述证实对这种形成对照的转移可能性进行了加强:iMet细胞系而不是iHRAS*细胞系能够在尾部静脉检测中对所述的肺部进行播种,其中所述的细胞系来自于原发性的恶性黑素瘤(附图2C)。
在iHRAS*与iMet所具有的转移倾向性之间所存在的清晰的差别允许生成一种表型驱动的原发性肿瘤的转移信号,这种转移信号的产生是以转录组学的比较为基础的,其中所述的比较是发生在所述的iHRAS*模型以及iMet模型的原发性皮肤恶性黑素瘤之间的。这种小鼠的转移信号接下来与具有下述性质的大量的基因互相配合,其中所述的基因(i)存在于人类转移性恶性黑素瘤的拷贝数量异常(CNA)之中和/或(ii)在人类原发性恶性黑素瘤与转移性恶性黑素瘤之间表现出差异化的表达,从而生成了295个上调节/扩增的基因以及65个下调节/缺失的基因(附图3A;表格4),其中所述的小鼠转移信号是由1597个探针组所构成的,其中所述的探针组在假发现率小于0.05的条件下具有大于等于2倍的差异化表达。为了对早期观察到的由这些基因所赋予的生物学活性的类型进行收集,我们实施了基于知识的途径分析,用以对获得显著性得分的基因功能进行定义,其中所述的显著性得分是通过所述的360个经过过滤的基因列表而产生的,所述的经过过滤的基因列表是与更大的1597个鼠科动物的转移信号相对而言的,其中所述的基于知识的途径分析是通过使用Ingenuity途径分析(IPA)(Ingenuity Systems Inc.,Redwood City,CA)得以实现的。为了对所述的Ingenuity途径分析(IPA)访问(call)所具有的显著性进行评价,我们生成了具有相等大小的用于进行平行分析的随机抽取的基因列表。正如在附图3B中所表示出的,我们发现所述的鼠科动物的转移表达信号表现出在基因功能方面的某种程度上的过分表达,这种过分表达是相对于所述的随机抽取的列表而言的,其中所述的基因功能是在DNA复制以及重组、癌症、细胞周期以及细胞死亡中所涉及到的。通过进行比较,除了一种仅仅被称之为“细胞的聚集以及组织”的新的功能网络的出现之外,所述的交叉品系/交叉平台过滤的列表表现出在这些相同功能方面的显著增强的富集作用,其中所述的新的功能网络病没有在所述的鼠科动物的表达信号中出现(附图3B)。这种比较表明:一种表型驱动的转移信号的三角化以及交叉品系的比较能够提供基因网络的富集,其中所述的基因网络与肿瘤形成以及转移的过程之间有着强烈的联系。
实施例3:针对转移以及决定子而进行的功能性遗传学筛选
特别的,所述的细胞聚集以及组织基因的强烈富集被鼓励性的给出了其与细胞运动以及入侵作用之间的相关性,其中所述的细胞运动以及入侵作用是一种负责散播癌症细胞的能力。这种观察促使我们执行一种低复杂性的遗传学筛选,用以对驱动入侵作用的基因进行识别(附图3C);此外,这些筛选专门聚焦于显示出它们可能所具有的治疗性潜力的经过上调节的基因。具体的,从所述的人类开放阅读框框架组(ORFeome)(http://horfdb.dfci.harvard.edu/)处获得230个可以利用的开放阅读框(ORF)并且将它们转移到一种用于向HMEL468中进行转导的慢病毒表达系统中,其中所述的230个可以利用的开放阅读框(ORF)对应着所述的295个独特的经过上调节/扩增的备选物中的199种(表格5),所述的HMEL468是一种经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞15。为了进行第一次的筛选,我们利用了带有荧光计量读数器的96孔transwell入侵作用检测,用以对备选的决定子基因所具有的增强经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)的迁移作用以及入侵作用的能力进行测量,其中所述的迁移作用以及入侵作用是向基质胶中进行的,所述的基质胶能够对细胞外的基质进行刺激。作为阴性对照以及阳性对照,分别使用到绿色荧光蛋白(GFP)以及NEDD916慢病毒。对所述的第一次筛选重复进行两次并且将45种备选物认定为被第一次筛选所选中,其中所述的备选物能够重复性的出现两次这样的得分,所述的得分距离所述的绿色荧光蛋白(GFP)对照有两倍的标准偏差(附图3C-D)。在此之后以一式三份的方式对上述第一次选中的45种备选物进行第二次的验证筛选,其中使用到标准的24孔基质胶transwell入侵小室,生成了25个基因,所述的基因能够产生至少1.5倍的入侵作用的增强,这种增强是相较于在经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)的黑素细胞中的绿色荧光蛋白(GFP)对照而言的(附图3E以及表格3)。除此之外,将已知能够与这25种决定子中的一种形成复合体的相关基因同样纳入到功能性检测之内,从而识别出6种另外的决定子。
实施例4:在人类原发性恶性黑素瘤组织微阵列(TMA)以
及转移性恶性黑素瘤组织微阵列(TMA)中的表达与恶化之间的
相关性
在为了确定转移决定子的表达与恶性黑素瘤的恶化之间所存在的相关性方面所作出的努力中,我们进行了组织微阵列(TMA)的免疫组织化学(IHC)检测,其中按照描述(参见Camp,R.L.,Dolled-Filhart,M.,King,B.L.,以及Rimm,D.L.(于2003年)发表的文章)通过自动化定量分析(AQUA)使用了可商业购买获得的作用于代表性决定子的抗体,在所述的组织微阵列(TMA)中含有良性色素痣,原发性肿瘤以及肿瘤转移物。对乳腺癌组织微阵列所进行的定量分析表明,高水平的人类表皮生长因子受体(HER)2表达以及正常水平的人类表皮生长因子受体(HER)2表达均与差的结果有关(参见Cancer Res《癌症研究》63,1445-1448中发表的文章)。正如在表格2中所概括的以及在附图4A-B中的代表性的数据,除了BRRN1之外,其他所有的参与测试的决定子(人热休克转录因子1(HSF1),MCM7,HOXA1,FSCN1,ACP5,UBE2C以及KNTC2)在原发性的转移物种表现出了明显更高的表达,这种表达是相对于良性色素痣而言的。
表格2
实施例5:转移性决定子是非种属特异性的以及预后性的
已经明确的确定出基因组的不稳定性能够驱动肿瘤的形成,生成原发性肿瘤,其中所述的原发性肿瘤是由异源性的细胞亚群体所组成的,这些细胞亚群体具有共同的以及独特的遗传学曲线。因此显而易见的是:如果存在于一个原发性肿瘤之中的能够表达一种转移性决定子的亚群体被赋予了一种增殖方面的优点并且最终发生散播,所述的转移性决定子所进行的表达将会增加,这归因于存在于所述的更为同源的衍生的转移性损伤中被强化的表现。为了对这种与恶化相关的表达进行评价,我们在Oncomine24中的表达曲线数据一览表内对所述的25种决定子进行检查。除了七种决定子表现出相对于原发性肿瘤而言在转移性事件中的增加的表达之外,所有的25种均在一个或者多个非恶性黑素瘤固体瘤中表现出一种与恶化相关的表达类型(表格3),即使这25种转移性决定子中的绝大部分之前没有被涵盖在肿瘤的恶化过程中。例如,在较高级别的神经胶质瘤中,有9种决定子表现出在表达方面的具有统计学显著性的增加。在前列腺腺癌中,从原发性事件到转移性事件中,有9种所述的转移性决定子表现出在表达方面的显著增加。相类似的,在肺部,有5种表现出与增加的肿瘤级别的相关性。在乳腺癌中观察到了最为显著的重叠,其中在所述的25种转移性决定子中有12种表现出了与肿瘤恶化的阶段或者级别之间所具有的相关性。
给出了在乳腺癌曲线中的显著的重叠之后,我们接下来利用在乳腺中公开的标注有结果的转录组数据5;6,对这些决定子所具有的潜在的更为广泛的预后显著性进行探索。所述的乳腺癌转录组数据组中包含了这样的探针,所述的探针作用于所述的20种转移性决定子中的19种,这样的探针被用来作为信号,从而对一个有295个乳腺肿瘤的组进行分级,其中所述的分级是通过利用k-均值无监督式分类的运算法则来进行的(附图5A;表格7)。已经发现上述得到的亚组在整体存活(p=2.6-9)以及不存在转移性事件的存活(p=2.1-6)中具有显著的差异(附图5B)。当进行分类时,获得了相类似的区分,其中在所述的分类中使用到的是分级聚类(数据未示出)。
在早期的乳腺癌中所具有的强劲的预后潜力以及在多发性非恶性黑素瘤的癌症类型中进行的与恶化相关的表达所具有的广泛的类型表明:这25种转移性的决定子不是种属特异性的并且可能能够对在多种多样的肿瘤类型中的核心过程进行驱动,尽管它们中的大部分之前在文献中并没有被涉及到入侵作用或者转移中。取而代之的是,在基因本体论(Gene-Ontology)中对许多进行了注解,将其注解为细胞周期或者增殖基因,所述的基因在纺锤体检查调节或者染色体浓缩方面具有已知的作用。例如,已知几种决定子(例如,BRRN1,KNTC2,SPAG5,UBE2C,CENPM以及MCM7)能够对DNA有丝分裂的进行、有丝分裂纺锤体以及DNA的复制过程进行调节。从另外一个方面看,BRRN1、KNTC2以及UBE2C被包含在一种20个基因的功能模块之内,在与发生了转移的原发性乳腺肿瘤相关的一种转移性乳腺癌信号中发生了所述模块的富集,这种富集是相较于没有发生转移的原发性肿瘤而言的25。相类似的,MCM7已经被认定为是一种对于多种入侵性癌症而言差的预后性标记物,其中所述的癌症包括前列腺癌26。将它们一并考虑,尽管尚不清楚这些蛋白质通过怎样的方式直接或者间接的促进对于细胞入侵作用以及转移作用的驱动,我们推测这些有丝分裂检查点蛋白质可能在控制所述的细胞骨架机构方面提供了双重的作用,其中所述的细胞骨架机构是用于进行细胞运动的。
实施例6:对提供失巢凋亡抗性的基因所进行的识别
转移是一项复杂的、多步骤的过程(参见Gupta,G.P.,以及Massague J.(于2006年)在Cell《细胞》127,679-69中发表的文章Cancer metastasis:building a framework《癌症的转移:一种骨架的建立》)。为了能够使全面的转移作用发生,肿瘤细胞必需能够在所述的原发性肿瘤位点上进行增殖,向内入侵(intravasate)至所述的循环系统或者淋巴系统中去,在循环的过程中保持存活,向外入侵(extravasate)并且形成第二个肿瘤。为了使之完成,循环的肿瘤细胞必需能够克服失巢凋亡,或者由基质连接的缺失而诱导的细胞凋亡(参见Simpson,C.D.,Anyiew,K.,以及Schimmer,A.D.(于2008年)在Cancer Lett《癌症学》272,177-185中发表的文章Anoikis resistance and tumor metastasis《失巢凋亡抗性以及肿瘤的转移》)。为了对能够向失巢凋亡敏感性细胞提供失巢凋亡抗性的基因进行识别,我们对一种体外筛选进行了最优化处理,其中所述的筛选针对的是失巢凋亡敏感性(附图6A)。我们假设,被播种在一种培养板(超低水平的聚集)之上的细胞能够在循环的过程中在一定程度上在体外对所述的细胞的体内悬浮进行重现,其中所述的培养板上覆盖有一种水凝胶层,所述的水凝胶层用以防止细胞表面上发生的连接。
在前导性研究中,我们对一组恶性黑素瘤细胞系进行了筛选并且发现全部具有失巢凋亡抗性,不论恶性黑素瘤处于何种阶段(例如,定位的,入侵的)。取而代之的是,我们以及其他人发现大鼠的肠内上皮(RIE)细胞在发生粘附性的缺失时具有降低的存活率(附图6B)(参见Douma,S.,Van Laar,T.,Zevenhoven,J.,Meuwissen,R.,Van Garderen,E.,以及Peeper,D.S.(于2004年)在Nature《自然》430,1034-1039中发表的文章Suppression of anoikis and induction of metastasis by the neurotrophic receptor TrkB《通过神经营养受体TrkB对失巢凋亡的抑制以及对转移的诱导》)。大鼠肠内上皮(RIE)细胞是经过固定化的但没有经过转化的细胞系。经历着失巢凋亡的细胞触发了细胞凋亡的途径,同时那些在附着性的缺失中能够存活的细胞证明了具有失巢凋亡的抗性。因此,我们对三磷酸腺苷(ATP)的生成进行了测量,所述的三磷酸腺苷(ATP)的生成标志着细胞的代谢作用,作为对细胞的存活能力所进行的一种可量化的以及敏感的测量。
使用所述的Gateway重组系统,将所述的199种备选的开放阅读框(ORF)克隆至所述的逆转录病毒载体之中,其中所述的开放阅读框(ORF)是经过我们的交叉品系肿瘤基因组分析识别出的,所述的逆转录病毒载体是MSCV/V5。当通过Western印迹进行分析时,mTrkB以及一种克隆物的随机取样在大鼠的肠内上皮(RIE)细胞中进行了表达,其中所述的克隆物具有改变的cDNA的大小,从而证明了我们的表达系统所具有的功能性(附图6C并且数据未示出)。
为了进行所述的失巢凋亡抗性的筛选,将293T细胞放置在6孔培养板中并且利用所述的MSCV/V5与所述的包装载体对其进行共转染,其中在所述的MSCV/V5中含有一个开放阅读框(ORF)并且所述的包装载体是pCL-Eco(附图6A)。利用脂质体(Lipofectamine)2000(Invitrogen)对细胞进行转染并且在多个时间点上对病毒进行收集。将大鼠的肠内上皮(RIE)细胞放置在6孔培养板上并且放置后的24小时时利用48小时以及72小时的病毒上清液进行连续的感染。经过最终的感染之后的24小时时对大鼠的肠内上皮(RIE)细胞进行收集并且当形成了单个细胞的悬浮液之后,以7000个细胞/孔的水平一式三份的将其放置在96孔的超低聚集度(ULC)培养板中(时间0小时)。为了确定基线的细胞数量,在0小时时对细胞进行溶解并且对三磷酸腺苷(ATP)的水平进行测量(Cell Titer Glo,Promega)。在经过超低聚集度(ULC)培养后的24小时时,利用Cell Titer Glo对细胞进行溶解并且将溶解物转移至96孔不透明孔的照度计培养板中用以进行读取。在我们的分析中,在24小时时将所述的三磷酸腺苷(ATP)的水平与0小时下的水平进行比较,从而给出在三磷酸腺苷(ATP)水平上发生的倍数的变化(附图7)。
所述的神经营养受体TrkB已经被证实能够在体外向失巢凋亡敏感性细胞提供失巢凋亡抗性并且促进肿瘤的形成以及体内的肺部播种(3)。我们对我们的筛选具有增强了的信心,因为鼠科动物的TrkB(m TrkB以及所述TrkB的人类配体,BDNF,向大鼠的肠内上皮(RIE)细胞提供了失巢凋亡抗性,所提供的抗性强于抗体单独所能提供的抗性(附图7)。在相同的两次筛选中,平均有21%的基因提供了高于1倍的标准偏差,其中所述的标准偏差是相对于偏离所有的备选基因所具有的中间值而言的。在至少经过一次的筛选时,有二十种基因超过了两倍的标准偏差,其中所述的标准偏差是相对于偏离所有的备选基因所具有的中间值而言的(附图8)。这些基因中有九种在两次的筛选中均提供了偏离所述中间值超过1倍的标准偏差,而这九种基因中有七种在至少一次的筛选中给出了偏离所述中间值超过2倍的标准偏差(HNRPR,CDC20,PRIMA2A,HRSP12,ENY2,MGC14141,RECQL)。有趣的是,在所述的九种基因中,STK3,PRIM2A,CDC20,RECQL,HNRPR,ENY2以及MGC14141已经表现出在恶性黑素瘤样本中的更高的表达,无论是在正常与恶性黑素瘤之间所进行的比较中,还是在原发性事件与肿瘤性事件之间所进行的比较中(Oncomine,GEO)。除此之外,所有的九种基因已经表现出在乳腺肿瘤、肺部肿瘤或者脑瘤中的增加的表达,这证明了我们的优先列表在其他的癌症类型中同样是有效的(Oncomine)。
为了在非附着性条件下对所述细胞所具有的增加的存活能力进行证实,我们对经过一段时间的连接作用的缺失之后所述的连接能力的保持力进行了检查,其中所述的细胞是能够表达我们的九种备选基因的细胞。将能够表达目标基因的大鼠肠内上皮(RIE)细胞转移到超低聚集度(ULC)培养板中并且经过24小时之后将存在于悬浮液中的全部细胞转移到附着性培养板内。利用结晶紫对发生附着的细胞进行染色,用以对存活的细胞进行量化。正如在附图9中所表示出的,经过在悬浮液中的24小时之后,大鼠的肠内上皮(RIE)细胞具有降低的能力来连接到附着性培养板上。然而,当细胞已经存在于悬浮液中之后,所有的九种基因向大鼠的肠内上皮(RIE)细胞提供了增强的能力,其中所述的能力指的是发生重新连接并且保持存活的能力(附图9)。这样的一种能力将成为循环的肿瘤细胞所具有的一种必要的特征,其中所述的肿瘤细胞注定需要在另外一个位点上进行存留。
实施例7:转移性决定子是致肿瘤性的
因为转移性决定子是早期从所述的转化过程中获得的并且预先存在于原发性肿瘤之中,已经假定出这些转移性的基因可能同样是真实的癌症基因,向所述的原发性肿瘤提供了一种增殖方面的好处2;22。为了致力于此,我们查询了这些转移性的决定子是否能够向经过端粒酶逆转录酶(TERT)永生化处理的黑素细胞HMEL468提供直接的致肿瘤性。除了HOXA1之外,我们同样筛选了三种其他的决定子用于测试,它们是ANLN,BRRN1以及KNTC2,因为它们被包含在一个254个基因的信号中,所述的信号能够抵抗与存在于恶性黑素瘤中的不存在转移的存活之间所具有的相关性23。的确,经过12周之后,HOXA 1转导的经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)形成了一个大的肿瘤(2厘米),所述的肿瘤具有局部入侵作用的组织病理学迹象(附图10A),其具有33%的外显率(n=2,具有6个皮下移植位点),而载体转导的对照经过注射之后的21周后没有形成任何的肿瘤(附图10B)。相类似的,相对于载体对照而言,ANLN、BRRN1以及KNTC2转导的细胞表现出增强的致肿瘤性(附图3B)。将它们一并进行考虑,我们推断出转移性决定子本身的确是真实的致癌基因,它们同样能够对入侵性的行为进行驱动。
实施例8:对HOXA1以及FSCN1的体外以及体内验证数据
为了进一步的验证这种综合性的方法能够作为一种对转移性决定子进行识别的方式,我们接下来对所述的同源转换盒转录因子HOXA1进行了全面深入的验证。已经在多种癌症中报道了HOXA1的上调节作用,其中所述的癌症包括乳腺癌,非小细胞腺癌(NSCLC)以及恶性黑素瘤17;18;19,尽管其在入侵作用以及转移事件中所起到的作用还没有被提到。在过表达的研究中,被强制的HOXA1显现出了粘附斑激酶FAK的磷酸化作用的戏剧性的增强(附图11A),其中所述的粘附斑激酶FAK是存在于所述的生长因子的调节作用以及整联蛋白刺激的细胞运动作用以及入侵作用中的一种关键的信号分子20。因此,过表达HOXA1的经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)表现出在体外的入侵作用方面的10倍的增强并且获得了体内的肺部播种的能力(附图11A,D)。重要的是,这种前侵作用并不特异于所述的经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)黑素细胞细胞系,因为HOXA1能够类似的对WM115以及WM3211人类恶性黑素瘤细胞的入侵作用进行增强(附图11B-C)。的确,正如在表格3中所概括出的,进行了入侵作用检测的所述决定子中有许多在WM115以及WM3211恶性黑素瘤细胞中同样表现出了超越经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)黑素细胞的前侵活性。使用虚弱的致肿瘤性恶性黑素瘤细胞系WM115进行的另外的验证试验,目的在于对所述的HOXA1所具有的致肿瘤性以及转移的可能性进行测试,所述的试验表明,HOXA1的过表达显著的增加了存在于裸鼠中的异种移植细胞的肿瘤生长(附图11E),这与使用其他的人类细胞系以及小鼠细胞系所得到的数据相一致。当在真皮内向所述的裸鼠的双侧植入WM115细胞时,HOXA1的过表达同样导致了WM115细胞的增加的肿瘤生长,并且上述得到的原发性肿瘤在经过肿瘤的形成之后轻易的转移到了肺部(附图11F),而对照(空白的载体细胞)没有形成原发性的肿瘤。
除了在人类细胞系中进行的这些研究之外,我们同样使用小鼠的细胞系对HOXA1以及Fascin1(FSCN1)进行了测试。与使用人类细胞系统所得到的入侵作用结果相一致(附图11A-C),两种备选物所进行的表达显著的增强了来源于Ink4a/Arf/-小鼠d的黑素细胞所具有的基质入侵能力(附图12A),其中所述的黑素细胞是经过HRAS*进行转导的细胞(被称之为M3HRAS细胞,参见Kim,M.,Gans,J.D.,Nogueira,C.,Wang,A.,Paik,J.H.,Feng,B.,Brennan,C.,Hahn,W.C.,Cordon-Cardo,C.,Wagner,S.N.,等人(于2006年)在Cell《细胞》125,1269-1281中发表的文章Comparative oncogenomics identifies NEDD9 as a melanoma metastasis gene《比较肿瘤基因组学将NEDD9认定为一种恶性黑素瘤的转移性基因》。除此之外,当被异种移植在所述的裸鼠的两侧之上时,HOXA1以及Fascin1的过表达均增强了所述的M3HRAS细胞所具备的生长能力(附图12B)并且在经过静脉内的尾部静脉注射之后形成了肉眼可见的肺部结节,其中所述的静脉内的尾部静脉注射是一种针对转移事件的替代性检测(附图12C)。
实施例9:HOXA1是一种致癌基因,所述的致癌基因能够经
由对转化生长因子β(TGFβ)信号的调节作用来对入侵作用进
行促进
接下来,为了对HOXA1的入侵性活性所具有的分子基础进行探究,我们对所述的HOXA1转录组进行了测定,其中所述的测定是以对照组以及经过HOXA1转导的经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)、WM115以及WM3211细胞所具有的表达曲线为基础的(附图11B)。对所述的差异化表达的基因列表所进行的基于知识的途径分析揭示了一种转化生长因子β(TGFβ)信号基因网络在SMAD3上制定了一个中心作为一个主要的节点(附图13A以及表格6)。给出了它在转移中的已知作用21,我们因此评价所述的转化生长因子β(TGFβ)信号是否受到HOXA1的调节。使用一种转化生长因子β(TGFβ)应答性报告基因构建体(p3TP-Lux),我们发现HOXA1所进行的异常表达不仅仅能够增强基础报告基因的活性(11.0倍,p=0.003),与对照组相比而言(p=0.0001),同样能够导致对转化生长因子β(TGFβ)配体的应答发生9.3倍的增强(附图14A)。因此,在10%以及1%的血清培养条件下,当发生转化生长因子β(TGFβ)的刺激作用时,所述的经过活化的p-SMAD3以及总SMAD3被得到的了提升(附图14B),这得到了RNA表达分析的确证(附图13B)。而且,通过SMAD3的knockdown对由HOXA1介导的入侵作用进行了废除(附图14C),因而将HOXA1的前侵活性与转化生长因子β(TGFβ)-SMAD的信号进行了功能上的联系,其中所述的转化生长因子β(TGFβ)-SMAD信号是一种由中心途径支配的癌症转移21。
为了检查HOXA1的过表达能否对存在于肿瘤之中的SMAD3的磷酸化状态产生影响,我们利用了异种移植物的肿瘤样本,用以进行免疫组织化学的分析,其中在所述的免疫组织化学分析中使用到了一种作用于SMAD3的磷-特异性抗体,其中所述的异种移植物的肿瘤样本来自于能够表达空白载体或者HOXA1的WM115恶性黑素瘤细胞(附图11E)。与我们的观察相一致的是,HOXA1的过表达导致了SMAD3的磷酸化作用的增加(附图14B),我们在HOXA1过表达的肿瘤中发现了增加的SMAD3的磷酸化作用(附图14D)。
实施例:趋化因子受体4
为了获得对所述的HOXA1所具有的生物学功能的观察,我们准备来来自于空白载体中的cDNA以及HOXA1过表达的WM115恶性黑素瘤细胞以及经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468),用于在RT2Profiler聚合酶链式反应(PCR)阵列(超级阵列)中使用,从而对一组与转移有关的基因所产生的表达进行分析。所述的两种细胞系所共享的最为过表达的基因是所述的趋化因子受体CXCR4(附图15),它是一种对趋化因子基质衍生因子-1(SDF-1)具有特异性的受体。在许多类型的癌症中,通过肿瘤细胞所进行的趋化因子受体4(CXCR4)的表达已经与差的预后存在关联并且所述的趋化因子受体4(CXCR4)的表达在细胞的转移中起到了至关重要的作用,其中所述的所用是经过向器官进行一种趋化现象梯度的建立的方式来实现的,其中所述的器官能够表达基质衍生因子-1(SDF-1)(参见Fulton AM.于2009年三月在Curr Oncol Rep.《当代肿瘤学报导》11(2):125-31中发表的文章)。为了进一步的检查存在于所述的HOXA1与趋化因子受体4(CXCR4)之间的关系,我们使用免疫组织化学的方法,对空白载体过表达的异种移植物肿瘤以及HOXA1过表达的异种移植物肿瘤中的趋化因子受体4(CXCR4)的表达进行评价。与所述的RT2Profiler分析相一致的是,我们发现在WM115-HOXA1以及经过端粒酶逆转录酶(TERT)永生化处理的人类原发性黑素细胞468(HMEL468)-HOXA1异种移植物肿瘤中,趋化因子受体4(CXCR4)的表达都发生了显著的增加(附图16)。这些数据与一个模型相一致,在所述的模型中HOXA1导致了趋化因子受体4(CXCR4)的增加的表达,这种表达继而对转移性的信号程序产生了影响,其中这种转移性的信号程序是通过HOXA1的过表达来触发的。
概括的说,一种综合性的功能性基因组的方法能够进行所述的转移性决定子的识别,其中所述的转移性决定子对于入侵作用以及真实的致癌基因而言都是有活性的驱动器。这些在恶性黑素瘤的情形中发现的转移性的决定子,在早期阶段的乳腺癌中证实了具有预后性并且在多种多样的非恶性黑素瘤的肿瘤类型中表现出了与恶化相关的表达。这些发现提供了试验证据:转移性决定子存在于某些早期阶段的原发性肿瘤之中并且能够规划这些肿瘤进行有侵略性的行为,因此提供了差的临床结果。尽管这些决定子中的绝大部分都没有与癌症或者转移事件发生联系,它们能够为基于功能的预后性标记物以及新的治疗剂的侵袭提供一种基础。
表格3
参考文献
1.Cupta,G.P.&Massague,J.(于2006年)在Cell《细胞》127,679-95中发表的文章Cancer metastasis:building a framework《癌症的转移:一种框架的建立》。
2.Bernards,R.&Weinberg,R.A.(于2002年)在Nature《自然》418,823中发表的文章A progression puzzle《恶化方面的一个难题》。
3.Perou,C.M.等人(于2000年)在Nature《自然》406,747-52中发表的文章Molecular portraits of human breast tumours《人类乳腺肿瘤的分子肖像》。
4.Ramaswamy,S.,Ross,K.N.,Lander,E.S.&Golub,T.R.(于2003年)在Nat Genet《自然遗传学》33,49-54中发表的文章A molecular signature of metastasis in primary solid tumors《原发性固体肿瘤的转移的一种分子信号》。
5.Van’t Veer,L.J.等人(于2002年)在Nature《自然》415,530-6中发表的文章Gene expression profiling predicts clinical outcome of breast cancer《基因表达曲线对乳腺癌的临床结果所进行的预测》。
6.Van de Vijver,M.J.等人(于2002年)在N Engl J Med《新英格兰药物学杂志》347,1999-2009中发表的文章Agene-expression signature as a predictor of survival in breast cancer《作为乳腺癌存活的预测剂的基因表达信号》。
7.Chin,K.等人(于2004年)在Nat Genet《自然遗传学》36,984-8中发表的文章In situ analyses of genome instability in breast cancer《在乳腺癌中对基因组的不稳定性所进行的原位分析》。
8.Rudolph,K.L.,Millard,M.,Bosenberg,M.W.&DePinho,R.A.(于2001年)在Nat Genet《自然遗传学》28,155-9中发表的文章Telomere dysfunction and evolution of intestinal carcinoma in mice and human《在小鼠以及人类体内的端粒功能紊乱以及肠癌的演变》。
9.Breslow,A.(于1970年)在Ann Surg《外科学年报》172,902-8中发表的文章Thickness,cross-sectional areas and depth of invasion in the prognosis of cutaneous melanoma《在皮肤恶性黑素瘤的预后过程中入侵作用的厚度、相交区域的面积以及深度》。
10.Gimotty,P.A.等人(于2005年)在J Clin Oncol《临床肿瘤学杂志》23,8048-56中发表的文章Biologic and prognostic significance of dermal Ki67 expression,mitoses,and tumorigenicity in thin invasive cutaneous melanoma《在入侵性的皮肤恶性黑素瘤中发生的真皮Ki67的表达、有丝分裂、以及致肿瘤性所具有的生物学意义以及预后性意义》。
11.Gimotty,P.A.等人(于2007年)在J Clin Oncol《临床肿瘤学杂志》25,1129-34中发表的文章Identification of high-risk patients among those diagnosed with thin cutaneous melanomas《在那些被诊断为患有薄皮层恶性黑素瘤的患者中对高危险患者所进行的识别》。
12.Chin,L.等人(于1997年)在Genes and Development《基因及其发展》11,2822-34中发表的文章Cooperative effects of INK4a and ras in melanoma susceptibility in vivo《INK4a与ras在恶性黑素瘤的体内易感性方面所产生的协同作用》。
13.Natali,P.G.等人(于1993年)在Br J Cancer《英国癌症杂志》68,746-50中发表的文章Expression of the c-Met/HGFreceptor in human melanocytic neoplasms:demonstration of the relationship to malignant melanoma tumour progression《c-Met/人类生长因子受体在人类黑素细胞肿瘤中的表达:对其与恶性黑素瘤肿瘤的恶化所存在的相关性进行的证明》。
14.Chin,L.等人(于1999年)在Nature《自然》400,468-72中发表的文章Essential role for oncogenic Ras in tumour maintenance《致癌基因Ras在肿瘤的维持方面所具有的至关重要的作用》。
15.Garraway,L.A.等人(于2005年)在Nature《自然》436,117-22中发表的文章Integrative genomic analyses identify MITF as a lineage survival oncogene amplified in malignantmelanoma《综合性的基因组分析将MITF认定为一种在恶性黑素瘤中发生扩增的种属存活性致癌基因》。
16.Kim,M.等人(于2006年)在Cell《细胞》125,1269-81中发表的文章Comparative oncogenomics identifies NEDD9as a melanoma metastasis gene《比较肿瘤基因组学将NEDD9认定为一种恶性黑素瘤转移性基因》。
17.Chariot,A.&Castronovo,V.(于1996年)在Biochem BiophysRes Commun《生物化学与生物物理学研究通讯》222,292-7中发表的文章Detection of HOXA 1expression in human breast cancer《在人类乳腺癌中对HOXA1的表达所进行的检测》。
18.Maeda,K.等人(于2005年)在Int J Cancer《国际癌症杂志》114,436-41中发表的文章Altered expressions of HOX genes in human cutaneous malignant melanoma《在人类皮肤恶性黑素瘤中HOX基因的改变的表达》。
19.Abe,M.等人(于2006年)在Oncol Rep《肿瘤学报告》15,797-802中发表的文章Disordered expression of HOXgenes in human non-small cell lung cancer《HOX基因在人类非小细胞肺癌中的紊乱的表达》。
20.Schlaepfer,D.D.&Mitra,S.K.(于2004年)在Curr Opin GenetDev《遗传学及其发展的当前观点》14,92-101中发表的文章Multiple connections link FAK to cell motility and invasion《将粘附斑激酶与细胞的运动性以及入侵作用进行联系的多种关联》。
21.Bierie,B.&Moses,H.L.(于2006年)在Nat Rev Cancer《癌症的自然回顾》6,506-20中发表的文章Tumourmicroenvironment:TGFbeta:the molecular Jekyll and Hyde ofcancer《肿瘤微环境:转化生长因子β:癌症的双重分子》。
22.Weinberg,R.A.(于2008年)在Carcinogenesis《致癌作用》中发表的文章Mechanisms of Malignant Progression《恶化过程所具有的机制》。
23.Winnepenninckx,V.等人(于2006年)在J Natl Cancer Inst《国家癌症研究中心杂志》98,472-82中发表的文章Geneexpression profiling of primary cutaneous melanoma andclinical outcome《原发性恶性黑素瘤的基因表达曲线以及临床结果》。
24.Rhodes,D.R.等人(于2004年)在Neoplasia《瘤的形成》6,1-6中发表的文章ONCOMINE:a cancer microarraydatabase and integrated data-mining platform《ONCOMINE:一个癌症微阵列数据库以及综合的数据采集平台》。
25.Rhodes,D.R.&Chinnaiyan,A.M.(于2005年)在Nat Genet《自然遗传学》37增刊S31-7中发表的文章Integrativeanalysis of the cancer transcriptome《对癌症转录组的综合性分析》。
26.Ren,B.等人(于2006年)在Oncogene《致癌基因》25,1090-8中发表的文章MCM7 amplification andoverexpression are associated with prostate cancer progression《MCM7的扩增以及过表达与前列腺癌的恶化相关》。
Claims (45)
1.一种具有预先确定的水平的预测能力的方法,用以对宿主体内的一种转移性肿瘤的形成的危险进行评价,所述的方法包括:
a.在一个来自于所述宿主的样本中,对选自由下述决定子所组成的组中的两种或者更多种决定子所具有的水平进行测量:1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271,并且
b.对存在于所述样本之中的所述的两种或者更多种决定子所具有的水平所发生的临床意义上显著的改变进行测量,其中所述的改变意味着在所述的宿主体内形成一种转移性肿瘤的危险的增加。
2.根据权利要求1中所述的方法,其中进一步的包括对选自由下述决定子所组成的组中的一种或者多种决定子所具有的有效剂量进行测量:决定子26-40,42-60,64,65,67-73,75-95,97,98,100-102,104-125,127-134,136,139-176,178-189,191-209,211,213-216,219-226,228-238,240-260,262-270,272-360。
3.根据权利要求1或者2中所述的方法,其中进一步的包括对至少一种与所述肿瘤相关的标准参数进行测量。
4.根据权利要求1中所述的方法,其中通过电泳的方式或者免疫化学的方式对所述的决定子所具有的水平进行测量。
5.根据权利要求4中所述的方法,其中所述的免疫化学检测是通过放射性免疫检测、免疫荧光检测或者通过一种酶联免疫吸附检测来实现的。
6.根据权利要求1中所述的方法,其中所述的宿主患有一种原发性的肿瘤,一种复发性的肿瘤,或者一种转移性的肿瘤。
7.根据权利要求1中所述的方法,其中所述的样本是一个肿瘤的活组织切片。
8.根据权利要求1中所述的方法,其中所述的活组织切片是一种核心活组织切片,一种切离组织的活组织切片或者是一种切口组织的活组织切片。
9.根据权利要求1中所述的方法,其中对五种或者更多种所述的决定子所具有的表达水平进行测量。
10.一种具有预先确定的水平的预测能力的方法,用以对宿主体内的一种转移性肿瘤的形成的危险进行评价,所述的方法包括:
a.在一个来自于所述宿主的样本中,对选自由下述决定子所组成的组中的两种或者更多种决定子所具有的水平进行测量:1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271,并且
b.将所述的两种或者更多种决定子所具有的水平与一种参考值进行比较。
11.根据权利要求10中所述的方法,其中所述的参考值是一种指数值。
12.一种具有预先确定的水平的预测能力的方法,用以对宿主体内的一种肿瘤的恶化进行评价,所述的方法包括:
a.在第一个时间段内,对来自于所述宿主的第一个样本之中的选自由下述决定子所组成的组中的两种或者更多种决定子所具有的水平进行测量:1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271;
b.在第二个时间段内,对来自于所述宿主的第二个样本之中的上述两种或者更多种决定子所具有的水平进行检测;
c.将在步骤(a)中检测到的所述的两种或者更多种决定子所具有的水平与在步骤(b)中检测到的所述的剂量进行比较,或者将其与一种参考值进行比较。
13.根据权利要求12中所述的方法,其中所述的第一个样本是在所述的宿主接受针对所述肿瘤所进行的治疗之前从所述的宿主处获取的。
14.根据权利要求12中所述的方法,其中所述的第二个样本是在所述的宿主经历过针对所述肿瘤所进行的治疗之后从所述的宿主处获取的。
15.一种具有预先确定的水平的预测能力的方法,用以对针对一种转移性肿瘤所进行的治疗所具有的有效性进行监测:
a.在第一个时间段内,对来自于所述宿主的第一个样本之中的选自由下述决定子所组成的组中的两种或者更多种决定子所具有的水平进行测量:1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271;
b.在第二个时间段内,对来自于所述宿主的第二个样本之中的上述两种或者更多种决定子所具有的水平进行检测;
c.将在步骤(a)中检测到的所述的两种或者更多种决定子所具有的水平与在步骤(b)中检测到的所述的剂量进行比较,或者将其与一种参考值进行比较,其中通过对来自于所述宿主的两种或者更多种决定子所具有的水平所发生的变化对所述治疗所具有的有效性进行监测。
16.根据权利要求15中所述的方法,其中所述的宿主之前已经接受过针对所述的转移性肿瘤所进行的治疗。
17.根据权利要求15中所述的方法,其中所述的第一个样本是在所述的宿主接受针对所述转移性肿瘤所进行的治疗之前从所述的宿主处获取的。
18.根据权利要求15中所述的方法,其中所述的第二个样本是在所述的宿主接受针对所述转移性肿瘤所进行的治疗之后从所述的宿主处获取的。
19.一种具有预先确定的水平的预测能力的方法,用以为一个宿主进行治疗方案的筛选,其中所述的宿主被诊断为患有肿瘤,所述的方法包括:
a.在第一个时间段内,对来自于所述宿主的第一个样本之中的选自由下述决定子所组成的组中的两种或者更多种决定子所具有的水平进行测量:1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271;
b.任选的在第二个时间段内,对来自于所述宿主的第二个样本中的上述两种或者多种决定子所具有的有效剂量的水平进行检测;
c.将在步骤(a)中检测到的所述的两种或者多种决定子所具有的水平与一种参考值进行比较,或者任选的,将其与在步骤(b)中探测到的所述剂量进行比较。
20.根据权利要求19中所述的方法,其中所述的宿主之前已经接受过针对所述的肿瘤所进行的治疗。
21.根据权利要求19中所述的方法,其中所述的第一个样本是在所述的宿主接受针对所述肿瘤所进行的治疗之前从所述的宿主处获取的。
22.根据权利要求19中所述的方法,其中所述的第二个样本是在所述的宿主接受针对所述肿瘤所进行的治疗之后从所述的宿主处获取的。
23.一种转移性肿瘤的参考表达曲线,所述的曲线中含有有效剂量的两种或者更多种标记物所具有的标记物水平的图案,其中所述的标记物选自由下述决定子所组成的组中:决定子1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271。
24.一种试剂盒,所述的试剂盒中包括大量的决定子检测试剂,所述的试剂能够对相应的决定子进行检测,并且足以生成权利要求23中所述的曲线,其中所述的决定子选自由下述决定子所组成的组中:决定子1-25,41,61,62,63,66,74,96,99,103,126,135,137,138,177,190,210,212,217,218,227,239,261,以及271。
25.根据权利要求24中所述的试剂盒,其中所述的检测试剂包括一种或者多种抗体或其片段。
26.根据权利要求24中所述的试剂盒,其中所述的检测试剂包括一种或者多种寡核苷酸。
27.根据权利要求24中所述的试剂盒,其中所述的检测试剂包括一种或者多种适配子。
28.一种计算机可读形式的介质,其中含有根据权利要求23中所述的一种或者多种转移性肿瘤的参考表达曲线,并且任选的,含有另外的测试结果以及宿主的信息。
29.一种决定子小组,其中包括一种或者多种决定子,所述的决定子能够代表一种或者多种与转移相关的生理学途径或者生物化学途径。
30.根据权利要求29中所述的小组,其中所述的生理学途径或者生物化学途径包括细胞迁移,血管生成,细胞外基质降解或者失巢凋亡抗性。
31.一种决定子小组,其中包括一种或者多种决定子,所述的决定子能够代表一种肿瘤的恶化。
32.一种用以识别生物标记物的方法,其中所述的生物标记物是对于一种疾病的预后,所述的方法包括:
a)对一种或者多种基因进行识别,所述的基因在所述疾病中发生了差异化的表达,这种差异化的表达是相较于一种对照而言的,从而生成一个基因靶向列表;并且
b)对存在于所述的靶向列表中的一种或者多种基因进行识别,其中所述的基因与所述疾病的恶化的功能方面存在关联;
从而对对于所述疾病的预后的生物标记物进行识别。
33.根据权利要求32中所述的方法,其中进一步的包括下述步骤:对存在于所述的基因靶向列表中的一种或者多种基因进行识别,其中所述的基因包括一种进化保守的改变,从而生成第二个基因靶向列表。
34.根据权利要求32中所述的方法,其中所述的疾病是癌症。
35.根据权利要求34中所述的方法,其中所述的癌症是转移性的癌症。
36.根据权利要求32中所述的方法,其中所述的功能方面是细胞迁移,血管生成,细胞外基质降解或者失巢凋亡抗性。
37.一种用以识别化合物的方法,其中所述的化合物能够对一种决定子所具有的活性或者表达进行调节,所述的方法包括:
(a)提供一种表达所述决定子的细胞;
(b)将所述的细胞与一种组合物进行接触,所述的组合物中包括一种备选的化合物;并且
(c)确定所述的物质是否能够对所述决定子所具有的表达或者活性产生改变;
其中,如果在存在有所述化合物的条件下能够观察到所述的改变,而当所述的细胞与一种缺乏所述化合物的组合物发生接触时不能够观察到所述的改变,那么识别出所述的化合物能够对决定子所具有的活性或者表达进行调节。
38.根据权利要求37中所述的方法,其中所述的细胞是在体内、或者在体外发生接触的。
39.一种用以对宿主的癌症进行治疗的方法,所述的方法包括向所述的宿主施用一种化合物,其中所述的化合物能够对一种决定子所具有的活性或者表达进行调节。
40.一种用以对宿主的癌症进行治疗的方法,所述的方法包括向所述的宿主施用一种制剂,其中所述的制剂能够对一种化合物所具有的活性或者表达进行调节,其中所述的化合物是受到一种决定子的调节的。
41.根据权利要求40中所述的方法,其中所述的化合物是转化生长因子β或者趋化因子受体4。
42.根据权利要求41中所述的方法,其中所述的化合物是一种转化生长因子β抑制剂或者是一种趋化因子受体4抑制剂。
43.一种用以对患有肿瘤的患者进行治疗的方法,所述的方法包括:
对患有肿瘤的患者进行识别,其中通过对在来自于所述肿瘤的样本所进行的测量,决定子1-360中的两种或者更多种发生了一种临床意义上显著形式的改变,并且
利用一种治疗方案对所述的患者进行治疗,从而阻止或者减慢肿瘤的转移。
44.一种用以对需要进行辅助治疗的肿瘤患者进行筛选的方法,所述的方法包括:
通过对决定子1-360中的两种或者更多种进行测量的方式,对存在于所述患者中的转移的危险进行评价,其中,存在于来自所述患者的肿瘤样本中的所述两种或者多种决定子所发生的临床意义上显著的改变标志着所述的患者需要进行辅助治疗。
45.一种用以告知针对一个肿瘤患者的治疗决定的方法,所述的方法包括:
获得关于存在于来自于所述患者的一个肿瘤样本之中的两种或者更多种决定子1-360的信息,并且
选定一种能够在所述的患者体内预防或者降低肿瘤转移的治疗方案,其中在所述的治疗方案中所述的两种或者更多种决定子以一种临床意义上显著的方式发生了改变。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US7593308P | 2008-06-26 | 2008-06-26 | |
| US61/075,933 | 2008-06-26 | ||
| PCT/US2009/048862 WO2009158620A2 (en) | 2008-06-26 | 2009-06-26 | Signatures and determinants associated with metastasis methods of use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102132160A true CN102132160A (zh) | 2011-07-20 |
Family
ID=41445345
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2009801331437A Pending CN102132160A (zh) | 2008-06-26 | 2009-06-26 | 与转移有关的信号和决定子以及它们的使用方法及用途 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20110182881A1 (zh) |
| EP (1) | EP2307886A2 (zh) |
| JP (1) | JP2011526693A (zh) |
| KR (1) | KR20110036056A (zh) |
| CN (1) | CN102132160A (zh) |
| AU (1) | AU2009262022A1 (zh) |
| BR (1) | BRPI0914734A2 (zh) |
| CA (1) | CA2728674A1 (zh) |
| IL (1) | IL210245A0 (zh) |
| MX (1) | MX2010014280A (zh) |
| NZ (1) | NZ590385A (zh) |
| RU (1) | RU2011102743A (zh) |
| WO (1) | WO2009158620A2 (zh) |
| ZA (1) | ZA201100225B (zh) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018077225A1 (en) * | 2016-10-28 | 2018-05-03 | Mao Ying Genetech Inc. | The primary site of metastatic cancer identification method and system thereof |
| WO2019015549A1 (en) * | 2017-07-17 | 2019-01-24 | Mao Ying Genetech Inc. | METHOD AND SYSTEM OF CELLULAR TYPE IDENTIFICATION |
| CN109932510A (zh) * | 2017-12-18 | 2019-06-25 | 天津云检医学检验所有限公司 | 一种宫颈癌生物标志物及其检测试剂盒 |
| TWI800847B (zh) * | 2020-06-15 | 2023-05-01 | 日商三菱動力股份有限公司 | 預兆判定裝置、預兆判定方法及記憶媒體 |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20120041274A1 (en) | 2010-01-07 | 2012-02-16 | Myriad Genetics, Incorporated | Cancer biomarkers |
| US20100248269A1 (en) * | 2009-03-30 | 2010-09-30 | New York Blood Center | Detection of fibrin and fibrinogen degradation products and associated methods of production and use for the detection and monitoring of cancer |
| SG183304A1 (en) | 2010-02-17 | 2012-09-27 | Takeda Pharmaceutical | Heterocyclic compound |
| JP2013533960A (ja) | 2010-06-01 | 2013-08-29 | トドス メディカル リミテッド | がんの診断 |
| EP3812469A1 (en) | 2010-07-07 | 2021-04-28 | Myriad Genetics, Inc. | Gene signatures for cancer prognosis |
| WO2012030840A2 (en) | 2010-08-30 | 2012-03-08 | Myriad Genetics, Inc. | Gene signatures for cancer diagnosis and prognosis |
| WO2012061721A1 (en) * | 2010-11-05 | 2012-05-10 | Alleghney-Singer Research Institute | Method and system for recommending a decision based on combined entity modeling |
| WO2012153326A1 (en) | 2011-05-11 | 2012-11-15 | Todos Medical Ltd. | Diagnosis of cancer |
| US20140302042A1 (en) * | 2011-07-01 | 2014-10-09 | Dana-Farber Cancer Institute, Inc. | Methods of predicting prognosis in cancer |
| US9535065B2 (en) | 2011-09-06 | 2017-01-03 | Becton, Dickinson And Company | Methods and compositions for cytometric detection of rare target cells in a sample |
| CA2882388C (en) | 2012-08-31 | 2020-10-20 | Sloan-Kettering Institute For Cancer Research | Particles, methods and uses thereof |
| JP6164678B2 (ja) * | 2012-10-23 | 2017-07-19 | 国立研究開発法人科学技術振興機構 | ネットワークエントロピーに基づく生体の状態遷移の予兆の検出を支援する検出装置、検出方法及び検出プログラム |
| EP4190918A1 (en) | 2012-11-16 | 2023-06-07 | Myriad Genetics, Inc. | Gene signatures for cancer prognosis |
| CA2894719C (en) | 2012-12-19 | 2019-10-22 | Sloan-Kettering Institute For Cancer Research | Multimodal particles, methods and uses thereof |
| JP6635791B2 (ja) * | 2013-02-20 | 2020-01-29 | スローン − ケタリング・インスティテュート・フォー・キャンサー・リサーチ | 広視野ラマン撮像装置および関連方法 |
| ES2947946T3 (es) | 2013-03-14 | 2023-08-24 | Castle Biosciences Inc | Métodos para predecir el riesgo de metástasis en melanoma cutáneo |
| EP3004870B1 (en) | 2013-05-28 | 2019-01-02 | Todos Medical Ltd. | Differential diagnosis of benign tumors |
| GB201317609D0 (en) | 2013-10-04 | 2013-11-20 | Cancer Rec Tech Ltd | Inhibitor compounds |
| US10912947B2 (en) | 2014-03-04 | 2021-02-09 | Memorial Sloan Kettering Cancer Center | Systems and methods for treatment of disease via application of mechanical force by controlled rotation of nanoparticles inside cells |
| AU2015225867B2 (en) * | 2014-03-07 | 2020-02-06 | University Health Network | Methods and compositions for modifying the immune response |
| CA2947624A1 (en) | 2014-05-13 | 2015-11-19 | Myriad Genetics, Inc. | Gene signatures for cancer prognosis |
| US10688202B2 (en) | 2014-07-28 | 2020-06-23 | Memorial Sloan-Kettering Cancer Center | Metal(loid) chalcogen nanoparticles as universal binders for medical isotopes |
| EP3259578B1 (en) * | 2015-02-17 | 2019-10-23 | Siemens Healthcare Diagnostics Inc. | Model-based methods and testing apparatus for classifying an interferent in specimens |
| GB201505658D0 (en) | 2015-04-01 | 2015-05-13 | Cancer Rec Tech Ltd | Inhibitor compounds |
| US10919089B2 (en) | 2015-07-01 | 2021-02-16 | Memorial Sloan Kettering Cancer Center | Anisotropic particles, methods and uses thereof |
| GB201617103D0 (en) | 2016-10-07 | 2016-11-23 | Cancer Research Technology Limited | Compound |
| WO2023107329A1 (en) * | 2021-12-08 | 2023-06-15 | Mayo Foundation For Medical Education And Research | Assessing and treating melanoma |
| CN116204890B (zh) * | 2023-04-28 | 2023-07-21 | 浙江鹏信信息科技股份有限公司 | 一种自适应增强人工智能算法安全的算法组件库 |
| CN117171678B (zh) * | 2023-11-02 | 2024-01-12 | 北京建工环境修复股份有限公司 | 一种微生物修复过程中土壤微生物菌群调控方法及系统 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4230767A (en) * | 1978-02-08 | 1980-10-28 | Toyo Boseki Kabushiki Kaisha | Heat sealable laminated propylene polymer packaging material |
| US4275149A (en) * | 1978-11-24 | 1981-06-23 | Syva Company | Macromolecular environment control in specific receptor assays |
| US4233402A (en) * | 1978-04-05 | 1980-11-11 | Syva Company | Reagents and method employing channeling |
| US4376110A (en) * | 1980-08-04 | 1983-03-08 | Hybritech, Incorporated | Immunometric assays using monoclonal antibodies |
| US4659678A (en) * | 1982-09-29 | 1987-04-21 | Serono Diagnostics Limited | Immunoassay of antigens |
| US4727022A (en) * | 1984-03-14 | 1988-02-23 | Syntex (U.S.A.) Inc. | Methods for modulating ligand-receptor interactions and their application |
| US5018067A (en) * | 1987-01-12 | 1991-05-21 | Iameter Incorporated | Apparatus and method for improved estimation of health resource consumption through use of diagnostic and/or procedure grouping and severity of illness indicators |
| US5744101A (en) * | 1989-06-07 | 1998-04-28 | Affymax Technologies N.V. | Photolabile nucleoside protecting groups |
| US20020038227A1 (en) * | 2000-02-25 | 2002-03-28 | Fey Christopher T. | Method for centralized health data management |
| US20040002071A1 (en) * | 2001-09-19 | 2004-01-01 | Intergenetics, Inc. | Genetic analysis for stratification of cancer risk |
| US20040122296A1 (en) * | 2002-12-18 | 2004-06-24 | John Hatlestad | Advanced patient management for triaging health-related data |
| US7468032B2 (en) * | 2002-12-18 | 2008-12-23 | Cardiac Pacemakers, Inc. | Advanced patient management for identifying, displaying and assisting with correlating health-related data |
| US20030232398A1 (en) * | 2002-03-28 | 2003-12-18 | Macmurray James P. | Use of ROC plots of genetic risk factor to predict risk of sporadic breast cancer |
| WO2004079014A2 (en) * | 2003-03-04 | 2004-09-16 | Arcturus Bioscience, Inc. | Signatures of er status in breast cancer |
| CA2562310A1 (en) * | 2004-04-30 | 2005-11-17 | Yale University | Methods and compositions for cancer diagnosis |
| US20060063190A1 (en) * | 2004-09-22 | 2006-03-23 | Tripath Imaging, Inc | Methods and compositions for evaluating breast cancer prognosis |
| WO2007059313A1 (en) * | 2005-11-16 | 2007-05-24 | Children's Medical Center Corporation | Method to assess breast cancer risk |
| US8445198B2 (en) * | 2005-12-01 | 2013-05-21 | Medical Prognosis Institute | Methods, kits and devices for identifying biomarkers of treatment response and use thereof to predict treatment efficacy |
| US20090069196A1 (en) * | 2006-03-22 | 2009-03-12 | Mathias Gehrmann | Prediction of Breast Cancer Response to Chemotherapy |
| ES2484142T3 (es) * | 2006-09-06 | 2014-08-11 | The Regents Of The University Of California | Diagnóstico molecular y clasificación del melanoma maligno |
| CA2662508A1 (en) * | 2006-09-19 | 2008-07-10 | Novartis Ag | Biomarkers of target modulation, efficacy, diagnosis and/or prognosis for raf inhibitors |
| EP2092075A2 (en) * | 2006-11-06 | 2009-08-26 | Source Precision Medicine, Inc. | Gene expression profiling for identification, monitoring and treatment of melanoma |
| WO2008121132A2 (en) * | 2007-03-30 | 2008-10-09 | Source Precision Medicine, Inc. D/B/A Source Mdx | Gene expression profiling for identification, monitoring, and treatment of prostate cancer |
| EP3056576B1 (en) * | 2007-10-23 | 2019-02-13 | Clinical Genomics Pty Ltd | A method of diagnosing neoplasms |
| WO2009101639A1 (en) * | 2008-02-14 | 2009-08-20 | Decode Genetics Ehf. | Susceptibility variants for lung cancer |
| US20110053804A1 (en) * | 2008-04-03 | 2011-03-03 | Sloan-Kettering Institute For Cancer Research | Gene Signatures for the Prognosis of Cancer |
| EP2288728A4 (en) * | 2008-05-15 | 2011-11-02 | Univ Southern California | ANALYSIS OF GENOTYPE AND EXPRESSION TO PREDICT THE EVOLUTION OF A DISEASE AND CHOOSE THE MOST SUITABLE THERAPY |
| EP4350001A2 (en) * | 2009-11-23 | 2024-04-10 | Genomic Health, Inc. | Methods to predict clinical outcome of cancer |
-
2009
- 2009-06-26 NZ NZ590385A patent/NZ590385A/xx not_active IP Right Cessation
- 2009-06-26 RU RU2011102743/15A patent/RU2011102743A/ru not_active Application Discontinuation
- 2009-06-26 US US13/001,203 patent/US20110182881A1/en not_active Abandoned
- 2009-06-26 CN CN2009801331437A patent/CN102132160A/zh active Pending
- 2009-06-26 KR KR1020117001619A patent/KR20110036056A/ko not_active Application Discontinuation
- 2009-06-26 WO PCT/US2009/048862 patent/WO2009158620A2/en active Application Filing
- 2009-06-26 EP EP09771151A patent/EP2307886A2/en not_active Withdrawn
- 2009-06-26 MX MX2010014280A patent/MX2010014280A/es not_active Application Discontinuation
- 2009-06-26 CA CA2728674A patent/CA2728674A1/en not_active Abandoned
- 2009-06-26 AU AU2009262022A patent/AU2009262022A1/en not_active Abandoned
- 2009-06-26 JP JP2011516713A patent/JP2011526693A/ja not_active Withdrawn
- 2009-06-26 BR BRPI0914734A patent/BRPI0914734A2/pt not_active IP Right Cessation
-
2010
- 2010-12-23 IL IL210245A patent/IL210245A0/en unknown
-
2011
- 2011-01-07 ZA ZA2011/00225A patent/ZA201100225B/en unknown
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018077225A1 (en) * | 2016-10-28 | 2018-05-03 | Mao Ying Genetech Inc. | The primary site of metastatic cancer identification method and system thereof |
| WO2019015549A1 (en) * | 2017-07-17 | 2019-01-24 | Mao Ying Genetech Inc. | METHOD AND SYSTEM OF CELLULAR TYPE IDENTIFICATION |
| CN109932510A (zh) * | 2017-12-18 | 2019-06-25 | 天津云检医学检验所有限公司 | 一种宫颈癌生物标志物及其检测试剂盒 |
| TWI800847B (zh) * | 2020-06-15 | 2023-05-01 | 日商三菱動力股份有限公司 | 預兆判定裝置、預兆判定方法及記憶媒體 |
Also Published As
| Publication number | Publication date |
|---|---|
| NZ590385A (en) | 2012-11-30 |
| AU2009262022A1 (en) | 2009-12-30 |
| IL210245A0 (en) | 2011-03-31 |
| ZA201100225B (en) | 2011-10-26 |
| RU2011102743A (ru) | 2012-08-10 |
| KR20110036056A (ko) | 2011-04-06 |
| WO2009158620A3 (en) | 2010-06-03 |
| EP2307886A2 (en) | 2011-04-13 |
| MX2010014280A (es) | 2011-05-23 |
| WO2009158620A2 (en) | 2009-12-30 |
| CA2728674A1 (en) | 2009-12-30 |
| BRPI0914734A2 (pt) | 2015-10-20 |
| US20110182881A1 (en) | 2011-07-28 |
| JP2011526693A (ja) | 2011-10-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102132160A (zh) | 与转移有关的信号和决定子以及它们的使用方法及用途 | |
| US10253368B2 (en) | Molecular signatures of ovarian cancer | |
| Stratford et al. | A six-gene signature predicts survival of patients with localized pancreatic ductal adenocarcinoma | |
| O'Brien et al. | CENP‐F expression is associated with poor prognosis and chromosomal instability in patients with primary breast cancer | |
| Krop et al. | A putative role for psoriasin in breast tumor progression | |
| Generali et al. | Role of carbonic anhydrase IX expression in prediction of the efficacy and outcome of primary epirubicin/tamoxifen therapy for breast cancer | |
| CN102159727A (zh) | 与前列腺癌有关的信号和胆碱磷酸决定子以及它们的使用方法 | |
| Matsuoka et al. | The tumour stromal features are associated with resistance to 5‐FU‐based chemoradiotherapy and a poor prognosis in patients with oral squamous cell carcinoma | |
| CN102439168A (zh) | 用以对头颈癌进行识别、监测、以及治疗的生物标记物 | |
| JP2013520958A (ja) | 上皮間葉転換のバイオマーカーとしてaxlを使用する方法 | |
| Holm et al. | Elevated levels of chemokine receptor CXCR4 in HER-2 negative breast cancer specimens predict recurrence | |
| Chen et al. | The predictive role of E2-EPF ubiquitin carrier protein in esophageal squamous cell carcinoma | |
| CN104981697B (zh) | 促染色质转录复合物(fact)在癌症中的用途 | |
| CN105214077A (zh) | Usp33在肿瘤中的应用 | |
| Yu et al. | Transcriptomic Analysis of LNCaP Tumor Xenograft to Elucidate the Components and Mechanisms Contributed by Tumor Environment as Targets for Dietary Prostate Cancer Prevention Studies | |
| Marfizo et al. | Intensity and features of acute postoperative pain after mastectomy and breast-conserving surgery | |
| Guo et al. | Overexpression of VEGFA mediated by HIF‐1 is associated with higher rate of spread through air spaces in resected lung adenocarcinomas | |
| Kim et al. | Metabolic coupling in phyllodes tumor of the breast and its association with tumor progression | |
| Sharp et al. | A randomised controlled trial of the psychoneuroimmunological effects of reflexology in women with early-stage breast cancer | |
| Lamers et al. | Microarray based expression profiling of BRCA1 mutated human tumours using a breast-specific platform to identify a profile of BRCA1 deficiency | |
| Patel et al. | Psychosocial impact of breast cancer diagnosis and treatment in African, Caribbean and South Asian women | |
| Morris et al. | New regulators of the BRCA1 response to genotoxic stress | |
| Sneddon et al. | Opticin: a potent anti-angiogenic/antiproliferative agent for breast cancer therapy | |
| Lau | Validation of putative prognostic markers for non-small cell lung carcinoma | |
| Kamal et al. | Loss of CSMD1 disrupts mammary epithelial morphogenesis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20110720 |