CN101896815A - 肠疾病中的新的治疗靶标 - Google Patents
肠疾病中的新的治疗靶标 Download PDFInfo
- Publication number
- CN101896815A CN101896815A CN2008801210743A CN200880121074A CN101896815A CN 101896815 A CN101896815 A CN 101896815A CN 2008801210743 A CN2008801210743 A CN 2008801210743A CN 200880121074 A CN200880121074 A CN 200880121074A CN 101896815 A CN101896815 A CN 101896815A
- Authority
- CN
- China
- Prior art keywords
- pxr
- gene
- cell
- sequence
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/566—Immunoassay; Biospecific binding assay; Materials therefor using specific carrier or receptor proteins as ligand binding reagents where possible specific carrier or receptor proteins are classified with their target compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/12—Antidiarrhoeals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70567—Nuclear receptors, e.g. retinoic acid receptor [RAR], RXR, nuclear orphan receptors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/04—Screening involving studying the effect of compounds C directly on molecule A (e.g. C are potential ligands for a receptor A, or potential substrates for an enzyme A)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/06—Gastro-intestinal diseases
- G01N2800/065—Bowel diseases, e.g. Crohn, ulcerative colitis, IBS
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- General Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本发明涉及用于检测、诊断和治疗肠疾病(BD)的新的序列。本发明提供其表达与BD有关的BD相关多核苷酸序列。本文提供用于检测BD的诊断组合物和方法。本发明提供对BD多肽有特异性的单克隆和多克隆抗体。本发明还提供用于筛选、预防和治疗BD的诊断工具和治疗组合物及方法。
Description
相关申请
本申请要求2008年10月17日申请的美国临时申请60/999,234的权益。上述申请的全部内容都通过引用结合到本文中。
发明背景
2004年,FDA批准将(利福昔明(Rifaximin),RIFax)用于治疗旅行者腹泻(Laustsen and Wimmett,2005)。研究表明,RIFax是对抑制细菌RNA合成起作用的通用抗生素。并不完全了解促成RIFax在慢性胃肠疾病中起有益作用的机制。
因此,在本领域中存在对提供涉及肠疾病(BD),特别是肠易激综合征(IBS)的多核苷酸和多肽序列的需求。在本领域中还存在对提供与各种BD有关的抗原(BD相关多肽)作为诊断和/或治疗化合物和组合物的靶标的需求,包括对提供抗体的需求。这些抗原还可用于药物开发(例如小分子),以及用于细胞调节、生长和分化的进一步表征。还存在对鉴定和表征可以用作药剂或药物靶标,或者可以在预防、改善或纠正功能障碍或疾病中起作用的基因和相关蛋白质的需求。
发明概述
一方面,本文提供筛选调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐的方法,所述方法包括使PXR受体与一种或多种候选化合物接触。
在一个实施方案中,候选化合物包含利福霉素类似物。
在一个相关实施方案中,利福霉素类似物包含利福昔明。
在一个实施方案中,调节包括调节由PXR蛋白或其片段与利福霉素类似物的结合所诱导的信号转导。
在一个实施方案中,PXR受体与膜缔合、在转基因小鼠中、在测定板中、在细胞中和/或在人工膜中。
在一个实施方案中,PXR蛋白包含由序列登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP 003880或NP 071285所表示的氨基酸序列或其片段或变体或者由序列登录号NM 033013、NM 009803、NM 022002、NM 003889、CS618137、CS618135、CS618133所表示的核酸或其片段或变体。
在另一个实施方案中,CYP3A11、GSTA1、MRP2和OATP2上调。
在一个实施方案中,所述方法还可包括用利福昔明、利福霉素类似物或候选化合物的一种或多种预治疗。
在一个实施方案中,用候选化合物预治疗不会影响CYP3A底物咪达唑仑的药代动力学特征。
在另一个实施方案中,用候选化合物预治疗提高1′-羟基咪达唑仑的Cmax并降低1′-羟基咪达唑仑的Tmax。
在一个实施方案中,在用候选化合物治疗后与对照相比,CYP3A11增加约1倍~约4倍。
在另一个实施方案中,GSTA1mRNA在候选化合物治疗后上调。
在另一个实施方案中,上调范围介于约65%~约200%之间。
在一个实施方案中,肠MRP2mRNA在候选化合物治疗之后上调。
一方面,本文提供用于筛选(I)调节PXR受体或其片段的化合物或其盐的试剂盒,所述试剂盒包括PXR受体蛋白或其活性片段和利福霉素类似物。
一方面,本文提供用于治疗PXR相关疾病的药物,所述药物包含调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐,或者调节由PXR蛋白或其片段与利福霉素类似物的结合所诱导的信号转导的化合物或其盐。
一方面,本文提供治疗、预防或减轻受治疗者的PXR相关疾病的方法,所述方法包括给予调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐。
在一个实施方案中,调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐不是利福昔明。
在一个实施方案中,调节包括调节由PXR蛋白或其片段与利福霉素类似物的结合所诱导的信号转导。
在另一个实施方案中,PXR受体与膜缔合、在转基因小鼠中、在测定板中、在细胞中和/或在人工膜中。
在一个实施方案中,PXR蛋白包含由序列登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880或NP_071285表示的氨基酸序列或其片段或变体或者由序列登录号NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133表示的核酸或其片段或变体。
一方面,本文提供包含有效量的产生治疗效果的PXR蛋白激动剂组合物。
一方面,本文提供包含纯合破坏(homozygous disruption)的内源孕烷X受体(PXR)基因的转基因小鼠。
在另一个实施方案中,小鼠包含人PXR基因。
一方面,本文提供从本文所述转基因小鼠中分离的细胞或组织。
一方面,本文提供鉴定能够调节PXR基因的活性或PXR基因表达产物的活性的调节剂的方法,所述方法包括给予本文所述的转基因小鼠推定的调节剂;给予野生型对照小鼠所述调节剂;将转基因小鼠的生理反应与对照小鼠的生理反应进行比较;其中在转基因小鼠与对照小鼠之间生理反应上的差异表示所述调节剂能够调节基因或基因表达产物的活性。
一方面,本文提供筛选具有抗炎性肠病活性的候选药物的方法,所述方法包括提供表达PXR基因或其片段或变体的细胞,所述PXR基因由选自以下序列的核酸序列编码:NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133或O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880、NP_071285;使细胞与候选药物接触;以及监测组织样品中候选药物对BD多核苷酸表达的作用。
一方面,本文提供与PXR多肽结合的分离抗体或其抗原结合片段。
在一个实施方案中,抗体或其片段与固相支持体连接;其中抗体是单克隆抗体;其中抗体是多克隆抗体;和/或其中抗体或其片段另包含可检测标记。
本发明部分是基于这样的发现,即BD易感性与核受体家族的成员PXR基因的遗传变异强相关。PXR是一种调节参与异生素(xenobiotic)和限制抗生素沉积(deposition)及解毒的基因的核受体。本发明还部分基于人PXR的RIFax特异性活化。PXR是构成参与内源性解毒和异生素解毒的机体防御机制的固有组分(Kliewer等,2002)。PXR被包括处方药、草药补充剂、农药、内分泌破坏物和其它环境污染物在内的广谱异生素激活(Carnahan和Redinbo,2005)。PXR活化调节参与异生素(包括毒性化学物质)代谢和分泌的多种基因(Kliewer,2003;Rosenfeld等,2003;Sonoda等,2005)。本文还公开了一种新的动物模型PXR人源化小鼠(hPXR),其中将完整人PXR基因重新导入Pxr失效背景中(Ma等,2007)。
本发明提供用于筛选调节炎性肠病的组合物的方法。本发明还提供用于筛选调节炎性肠病的组合物的方法。本文还提供抑制肠及相关组织和器官的炎症的方法。本文还提供治疗炎性肠病的方法。
本公开内容总的来讲涉及转基因动物,以及与基因功能的表征有关的组合物和方法。
一方面,筛选候选药物的方法包括提供表达炎性肠病相关(BD)基因或其片段的细胞系。BD基因的某些实施方案是在BD中进行差异性表达的基因。用于本文方法的BD基因的某些实施方案包括但不限于选自NCBI登录号NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133的核酸或其相当于由其产生的人mRNA的片段。所述方法另包括将候选药物加到细胞中,并测定候选药物对BD基因的表达、结合、作用方式的作用。
在一个实施方案中,筛选候选药物的方法包括将候选药物不存在时的表达水平与候选药物存在时的表达水平进行比较。
本文还提供筛选能够与BD蛋白(BDP)结合的生物活性剂的方法,所述方法包括将BDP与候选生物活性剂混合,并测定候选生物活性剂与BDP的结合。
本文另外还提供用于筛选能够调节BDP活性的生物活性剂的方法。在一个实施方案中,所述方法包括将BDP与候选生物活性剂混合,并测定候选生物活性剂对BDP的生物活性的作用。
本文还提供评价候选BD药物的作用的方法,所述方法包括给予受治疗者药物,并从受治疗者体内提取细胞样品。然后测定细胞的表达谱。该方法可另外包括将受治疗者的表达谱与健康个体的表达谱进行比较。
例如,BD蛋白包含选自NCBI登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880、NP_071285所示序列的蛋白质。本文所使用的BDP蛋白包括例如被配体活化后在信号转导途径中的蛋白质。
例如,BD蛋白包含由选自NCBI登录号NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133所示序列的核酸编码的蛋白质;所述核酸相当于由其产生的人mRNA。
此外,本文提供包含编码BD蛋白的核酸区段的生物芯片,所述核酸选自NCBI登录号NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133所示序列;相当于由其产生的人mRNA。
本文还提供通过对受治疗者的至少一种BD基因进行测序来诊断或确定BD倾向性的方法。在本发明的又一个方面,提供确定受治疗者的BD(包括基因拷贝数)的方法。
在一些实施方案中,多核苷酸或其互补序列或其片段另包含可检测标记,所述多核苷酸或其互补序列或其片段与固相支持体连接、至少部分通过化学合成法制备、是反义片段、是单链、是双链或包含微阵列。
本文提供分离多肽,所述多肽在选自下述多核苷酸序列或互补序列的BD序列的可读框内编码。本文提供分离多肽,其中所述多肽包含由选自下述序列的多核苷酸编码的氨基酸序列。本文提供分离多肽,其中所述多肽包含由选自下述序列的多肽编码的氨基酸序列。在某些实施方案中,所述多肽或其片段可与固相支持体连接。在一个实施方案中,本文提供与这类多肽结合的分离抗体(单克隆或多克隆抗体)或其抗原结合片段。分离抗体或其抗原结合片段可与固相支持体连接,或另包含可检测标记。
在一个实施方案中,本文提供筛选抗BD活性的方法,所述方法包括:(a)提供表达BD相关基因或其片段的细胞,所述基因由选自以下登录号的BD序列的核酸序列编码:NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133或登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880、NP_071285;(b)使从BD细胞中得到的组织样品与抗BD候选药物(例如候选组合物)接触;(c)监测组织样品中抗BD候选药物对BD多核苷酸的表达的作用,并任选(d)将候选药物不存在时的表达水平与候选药物存在时的表达水平进行比较。候选药物可以是转录抑制剂、G蛋白偶联受体拮抗剂、生长因子拮抗剂、丝氨酸-苏氨酸激酶拮抗剂、酪氨酸激酶拮抗剂。
在一个实施方案中,化合物包括例如利福霉素衍生物,该衍生物带有在3,4-位上稠合的杂环。示例性组合物包括例如公开于以下专利的化合物:南非专利第68/0903号(吡咯并[5,4-c]利福霉素SV衍生物)、德国专利公布号2,739,671和2,739,623(咪唑并[5,4-c]利福霉素SV化合物,其在1位和2位上带有取代基)。德国专利公布号2,741,066中报告了噻唑并[5,4-c]利福霉素SV(利福霉素P)衍生物。其它利福霉素类似物包括例如本领域技术人员熟知的利福霉素-O和利福霉素-P,并且可与其它组合物及其衍生物一起提供,例如USPN 4,341,785或USPN4,200,574。
本文提供用于筛选能够调节BD蛋白(BDP)活性的生物活性剂的方法,其中BDP由包含下述核酸序列的核酸编码,所述方法包括:将BDP与候选生物活性剂混合;测定候选生物活性剂对BDP的生物活性的作用。按照该方法,生物活性剂可影响BD蛋白(BDP)的表达;影响BD蛋白(BDP)的活性。
本发明提供优先与BD蛋白(BDP)结合、任选与治疗剂连接或人源化的单克隆抗体,其中BD蛋白选自本文所述的BD蛋白。本文还提供用于检测受治疗者体内存在或不存在BD细胞且包含这类抗体的的试剂盒和药物组合物。
本公开内容提供转基因细胞,所述转基因细胞包含PXR基因中的破坏。本公开内容的转基因细胞包括能够进行同源重组的任何细胞。优选本公开内容的细胞是干细胞,更优选胚胎干(ES)细胞,最优选鼠ES细胞。按照一个实施方案,通过将寻靶构建体导入干细胞以产生导致PXR基因突变的同源重组,来制备转基因细胞。在另一个实施方案中,转基因细胞由下述转基因动物获得。由转基因动物得到的细胞包括分离的细胞或存在于组织或器官及任何细胞系中的细胞或其任何子代。
本公开内容还提供寻靶构建体和当导入干细胞时产生同源重组的产生寻靶构建体的方法。在一个实施方案中,本公开内容的寻靶构建体包含与PXR基因同源的第一多核苷酸序列和第二多核苷酸序列。寻靶构建体还包含编码选择标记的多核苷酸序列,所述选择标记优选位于构建体中两个不同的同源多核苷酸序列之间。寻靶构建体还可包含可以提高同源重组的其它调节元件。
本公开内容另外提供非人类转基因动物和产生这类包含PXR基因中的破坏的非人类转基因动物的方法。本公开内容的转基因动物包括在PXR基因中对于突变是杂合和纯合的转基因动物。一方面,本公开内容的转基因动物在PXR基因的功能方面有缺陷。另一方面,本公开内容的转基因动物包括与PXR基因上具有突变有关的表型。
本公开内容还提供鉴定能够影响转基因动物表型的作用剂(agent)的方法。例如,将推定的作用剂给予转基因动物,测定转基因动物对推定的作用剂的反应,与“正常”或野生型小鼠的反应进行比较,又或者与转基因动物对照(未给予作用剂)进行比较。本公开内容另外提供按照这类方法鉴定出的作用剂。本公开内容还提供鉴定用作治疗PXR基因破坏相关疾病的治疗剂的作用剂的方法。
本公开内容另外提供鉴定对PXR表达或功能起作用的作用剂的方法。所述方法包括给予转基因动物(例如小鼠)有效量的作用剂。例如,所述方法包括测定转基因动物对作用剂的反应,对转基因动物的反应与对照动物的反应进行比较,对照动物可为例如野生型动物又或者为转基因动物对照。可能对PXR表达或功能起作用的化合物也可在基于细胞的测定法中针对细胞进行筛选,例如以鉴定这类化合物。所述细胞可以是从本文所述的PXR转基因小鼠中得到的细胞。
本公开内容还提供包含PXR基因的核酸序列的细胞系。这类细胞系能够通过与功能性启动子有效连接,在细胞系中表达这类序列。在一个实施方案中,PXR基因序列的表达在诱导型启动子的控制下。本文还提供鉴定与PXR基因相互作用的作用剂的方法,所述方法包括使PXR基因与作用剂接触并检测作用剂/PXR基因复合物的步骤。例如可通过测定有效连接的选择标记的表达,来检测这类复合物。
本公开内容另外提供治疗与PXR基因中的破坏有关,更准确地讲与PXR基因表达或功能的破坏有关的疾病或病症的方法。在一个实施方案中,本公开内容的方法涉及治疗与PXR基因表达或功能的破坏有关的疾病或病症,所述方法包括给予有需要的受治疗者实现PXR表达或功能的治疗剂。按照这个实施方案,所述方法包括给予治疗有效量的天然、合成、半合成或重组的PXR基因、PXR基因产物或其片段以及天然、合成、半合成或重组的类似物。
本公开内容另外提供治疗与受破坏的靶定基因表达或功能有关的疾病或病症的方法,其中所述方法包括检测并通过基因疗法置换突变的PXR基因。
在另一个实施方案中,与PXR基因中的破坏有关的表型(或表型改变)用于预测拮抗PXR基因产物的药物的可能作用和副作用。在该实施方案中,使用小鼠评价作为“药物性靶标”的基因,以确定例如靶向PXR基因产物的药物的开发是否值得集中进行药物研究。
下文中公开了其它实施方案。
附图简述
图1表示RIF和RIFax的LC-MS/MS分析。(A)RIF的结构;(B)RIFax的结构;(C)RIF和RIFax的典型层析谱。通过LC-MS/MS对RIF和RIFax进行检测,对于RIF(1)m/z为823.5/791.5,对于RIFax(2)m/z为786.3/754.5。
图2表示在单剂量的10mg/kg RIF或RIFax治疗之后,小鼠中RIF和RIFax的代谢分布曲线和肠道分布。(A)在口服治疗后血清RIF和RIFax的浓度-时间曲线图。数据用平均值±SD表示,在每个时间点上n=3。(B、C、D)在口服治疗后小肠(S.intestine)、盲肠和结肠中RIF和RIFax的时程。分别在给药后1.5、3、6、9、12、24和48小时,从小肠(B)、盲肠(C)和结肠(D)中采集内容物。从肠道内容物提取RIF和RIFax,并通过LC-MS/MS进行分析。数据用平均值±SD表示,在每个时间点上n=3。(E)在口服治疗后,对野生型小鼠、Pxr失效小鼠和hPXR小鼠进行了RIFax Cmax比较。数据用平均值表示(n=3)。(F)通过静脉内、腹膜内和口服治疗的血清RIFax的浓度-时间曲线图。数据用平均值表示(n=3)。(G)腹膜内注射后血清RIFax和RIF的浓度-时间曲线图。数据用平均值表示(n=3)。(H)静脉内注射后血清RIFax和RIF的浓度-时间曲线图。数据用平均值表示(n=3)。
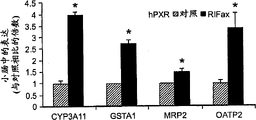
图3表示RIF和RIFax对野生型小鼠、Pxr失效小鼠和hPXR小鼠的小肠和肝中的PXR靶基因的作用。小鼠用25mg/kg RIF或RIFax经口服治疗3天,通过qPCR对CYP3A11、GSTA1、MRP2和OATP2的表达进行了分析。采用比较CT法对对数值进行了量化,使样品归一化至β-肌动蛋白。数据用平均值±SD表示,n=3。与对照相比*p<0.05。(A)RIFax对hPXR小鼠小肠的PXR靶基因的作用;(B)RIFax对野生型小鼠小肠的PXR靶基因的作用;(C)RIFax对Pxr失效小鼠小肠的PXR靶基因的作用;(D)RIF对hPXR小鼠小肠的PXR靶基因的作用;(E)RIF对hPXR小鼠肝的PXR靶基因的作用;(F)RIFax对hPXR小鼠肝的PXR靶基因的作用。
图4表示基于细胞的报道分子测定法测定各种异生素核受体的RIFax活化。数据用平均值±SD表示,n=3。与对照相比*p<0.05。(A)RIFax对人PXR的活化的基于细胞的报道分子测定法。分别将10μM RIF;1μM、10μM、100μM RIFax加到培养基中。采用DMSO作为溶媒。24小时后通过测定萤火虫萤光素酶活性,接着通过蛋白质浓度使萤光素酶活性归一化,来确定PXR的活化。(B)RIFax对人PXR、CAR、PPARα、PPARγ和FXR的活化的基于细胞的报道分子测定法。将10μM RIFax加到培养基中孵育24小时。分别使用RIF(10μM)、TCPOBOP(250nM)、Wy-14,643(10μM)、罗格列酮(rosiglitazone)(10μM)和GW4064(25μM)作为人PXR、CAR、PPARα、PPARγ和FXR的阳性对照。采用DMSO作为溶媒。采用标准双重萤光素酶测定法,并归一化至转染的对照报道分子。
发明详述
获准用于治疗旅行者腹泻的利福昔明(RIFax)这种利福霉素类似物,在胃肠疾病或BD的治疗中同样有益。然而,并不完全了解促成利福昔明在慢性胃肠疾病中起作用的机制。本发明部分基于利福昔明在调节参与异生素和限制生物体内生的沉积及解毒的基因的核受体人孕烷X受体(PXR)的特异性活化中的作用。本发明还部分基于PXR-人源化(hPXR)小鼠、Pxr失效小鼠和野生型小鼠的产生。
要了解的是,前面的概述和下面的详述都只是示例性和说明性的,并不限制所要求保护的本发明。在本申请中,使用的单数包括复数,除非另有说明。在本申请中,使用的“或”是指“和/或”,除非另有说明。此外,使用的术语“包括”以及其它形式不是限制性的。同样,术语例如“元件”或“组分”既包括包含一个单位的元件和组分,又包括包含一个以上亚单位的元件和组分,除非另有说明。同样,使用的术语“部分”可包括部分的组成部分或完整部分。
本文所使用的章节标题仅出于组织目的,不得解释为限制所述描述的主题。在本申请中引用的所有文件或文件的部分,包括但不限于专利、专利申请、文章、书和论文,通过引用其全部明确结合到本文中以用于任何目的。
术语“有效量”包括以剂量并经过必需的一段时间有效达到所需结果的量,例如足以治疗或预防患者或受治疗者的BD的量。PXR受体调节剂的有效量可根据受治疗者的疾病状况、年龄和体重等因素,以及PXR受体调节剂在受治疗者体内诱导所需反应的能力而改变。可以调整剂量方案以提供最适宜的治疗反应。有效量也是治疗有益作用胜过其中PXR受体调节剂的任何毒性作用或有害作用(例如副作用)的量。
“改善”、“改进”、“改良”等是指例如与发生在受治疗者中或在至少少部分受治疗者中的改善一致的可检测的改善或可检测的变化,例如至少约2%、5%、10%、15%、20%、25%、30%、40%、50%、60%、70%、75%、80%、85%、90%、95%、98%、100%或在大致任两个数值之间的范围。与未用利福昔明治疗的受治疗者相比,在经治疗的受治疗者中观察到这类改善或变化,其中未接受治疗的受治疗者患有或易发生相同或相似的疾病、病症、症状等。可以通过以下方面来主观或客观地确定疾病、病症、症状或实验参数的改善:受治疗者自我评价;通过临床医生的评价;或者通过进行适当的测定或测量,包括例如生命质量的评价、疾病或病症的进程减慢、疾病或病症的严重程度降低;或者生物分子、细胞的水平或活性的适当测定或者通过检测受治疗者的BD发作。改善可以是短暂的、长期的或永久的,或者在将PXR受体调节剂给予受治疗者或者用于本文或所引用的参考文献描述的测定法或其它方法期间或之后的适当时间,改善是可变的,所述适当时间例如在下述时限内,或者在给药或使用PXR受体调节剂后约1小时至受治疗者接受这类治疗之后约28天或1、3、6、9个月以上。
例如症状、分子的水平或生物活性等的“调节”,是指例如症状或者活性等可测量地提高或降低。与未使用PXR受体调节剂治疗的受治疗者相比,可以在接受治疗的受治疗者中观察到这类加重/提高或减轻/降低,其中未接受治疗的受治疗者患有或易发生相同或相似的疾病、病症、症状等。这类加重/提高或减轻/降低可为至少约2%、5%、10%、15%、20%、25%、30%、40%、50%、60%、70%、75%、80%、85%、90%、95%、98%、100%、150%、200%、250%、300%、400%、500%、1000%以上或在这些值的任两个之间的任何范围内。可通过以下方面主观或客观地确定所述调节:受治疗者的自我评价;通过临床医生评价;或者进行适当的实验或测量,包括例如生命质量评价或分子水平或活性的适当测定法、受治疗者体内的细胞或细胞迁移等。调节可以是短暂的、长期的或永久的,或者在将PXR受体调节剂给予受治疗者或者用于本文或所引用的文献资料描述的测定法或其它方法期间或之后的适当时间,调节是可变的,所述适当时间例如在下述时间内,或者给予或使用PXR受体调节剂约1小时至在受治疗者接受PXR受体调节剂之后约3、6、9个月以上。
术语“调节”还可指细胞在响应暴露于PXR受体调节剂时活性的提高或降低,例如在动物中抑制至少一部分细胞的增殖和/或诱导至少一部分细胞的分化,使得达到所需要的最终结果,例如用于治疗的PXR受体调节剂的治疗结果可随具体治疗的进程增加或减少。
如在“获得PXR受体调节剂”中一样的术语“获得”是指包括购买、合成或以别的方式获取PXR受体调节剂。
本文所使用的术语“胃肠外给药”和“经胃肠外给予”包括例如肠内给药和局部给药以外的给药方式,通常通过注射,包括而不限于静脉内、肌内、动脉内、鞘内、囊内、眶内、心脏内、真皮内、腹膜内、经气管、皮下、表皮下、关节内(intraarticulare)、囊下、蛛网膜下、脊柱内和胸骨内注射和输注。
术语化合物的“预防有效量”是指当以单剂量或多剂量给予受治疗者时有效预防或治疗BD的PXR受体调节剂的量。
本文所使用的术语“药物组合物”(或药剂或药物)是指当适当给予患者时能够诱导所需治疗效果的化合物、组合物、药剂或药物。它不一定需要一种以上类型的成分。
本文所使用的术语“全身给药”、“全身给予”、“外周给药”和“外周给予”是指给予PXR受体调节剂、药物或其它物质,使得它进入受治疗者系统,并因此进行代谢等过程,例如皮下给药。
术语PXR受体调节剂的“治疗有效量”是指当以单剂量或多剂量给予受治疗者时,在受治疗者体内有效抑制细菌生长和/或侵袭、或者减轻与细菌生长相关的症状(例如BD发作)的PXR受体调节剂的量。“治疗有效量”还指足以降低受治疗者的BD严重程度的某一疗法(例如包含PXR受体调节剂的组合物)的量。
本文所使用的术语“预防”、“防止”、“阻止”是指预防BD发作或更多BD症状的复发、起病或发生。预防包括防止BD发作的发生和严重性。
本文所使用的术语“预防有效量”是指某一疗法(例如包含PXR受体调节剂的组合物)的量足以预防BD发作的发生、复发或起病或者提高或改善另一疗法的预防效果。
本文所使用的“受治疗者”包括可能患有肠疾病或用PXR调节剂可治疗的其它病症或者除此外可从给予本文所述的PXR调节剂获益的生物,例如人和非人类动物。优选的人类动物包括人类受治疗者。本发明的术语“非人类动物”包括所有脊椎动物,例如哺乳动物,例如小鼠等啮齿动物,以及非哺乳动物,例如非人类灵长类,例如绵羊、狗、牛、鸡、两栖动物、爬行动物等等。
本发明涉及多种与BD有关的序列。
本文描述了通过将PXR调节剂制剂给予受治疗者以治疗患有或易患胃肠疾病或肠疾病的受治疗者的方法。在患有胃肠疾病的受治疗者中给予本文所述的PXR调节剂制剂加强治疗功效。可用本发明方法治疗的示例性胃肠疾病和肠疾病(PXR相关疾病或PXR蛋白相关疾病)包括但不限于例如肠易激综合征、克罗恩病(Crohn’s disease)、旅行者腹泻、溃疡性结肠炎、肠炎、小肠细菌过度生长、慢性胰腺炎、胰腺功能不全、结肠炎或肝性脑病。可能特别受益于该治疗的受治疗者包括患有或可能易患BD的受治疗者,例如新患上食源性疾病的受治疗者。在一个实施方案中,肠疾病包括肝性脑病。在一个实施方案中,BD包括以下一种或多种疾病:炎性肠病(IBD)、克罗恩病、肝性脑病、肠炎、结肠炎、肠易激综合征(IBS)、纤维肌痛(FM)、慢性疲劳综合征(CFS)、抑郁症、注意力缺陷/多动症(ADHD)、多发性硬化(MS)、系统性红斑狼疮(SLE)、旅行者腹泻、小肠细菌过度生长、慢性胰腺炎或胰腺功能不全。
因此,本发明提供与BD有关的核酸和蛋白质序列,本文称为“BD相关”或“BD”序列。另外,BD基因可能涉及其它疾病,例如但不限于与老化或神经变性相关的疾病。在这个方面的“相关”是指与正常组织相比,在BD中核苷酸或蛋白质序列被差异表达、激活、钝化或改变。
如下所述,BD序列包括在BD中上调(例如以较高水平表达)的序列,以及在BD中下调(例如以较低水平表达)的序列。BD序列还包括发生变化的序列(例如截短序列或具有取代、缺失或插入的序列,包括点突变),以及具有相同表达谱或变化谱的序列。在一个实施方案中,BD序列来自人;然而,正如本领域技术人员应了解的一样,来自其它生物的BD序列可用于疾病和药物评价的动物模型;因此,本文提供得自脊椎动物、包括哺乳动物、包括啮齿动物(大鼠、小鼠、仓鼠、豚鼠等)、灵长类和家畜(包括绵羊、山羊、猪、牛、马等)的其它BD序列。在一些情况下,原核BD序列可能是有益的。可采用下述技术获得其它生物的BD序列。
BD序列包括核酸序列和氨基酸序列。在一个实施方案中,BD序列为重组核酸。在一个实施方案中,BD序列为核酸。正如本领域技术人员应了解并且将在下面更详细描述的一样,BD序列可用于各种应用,包括可以检测天然存在的核酸的诊断应用以及筛选应用;例如,可以制成包含BD序列的核酸探针的生物芯片。从大的方面来看,使用的“核酸”、“多核苷酸”或“寡核苷酸”或等同术语在本文中是指至少两个核苷酸共价连接在一起。在一些实施方案中,寡核苷酸是6、8、10、12、20、30个或多达100个核苷酸的寡聚体。“多核苷酸”或“寡核苷酸”可包含DNA、RNA、PNA或通过磷酸二酯和/或任何更迭键连接的核苷酸的多聚体。
术语“标记”是指例如能够产生表示实验样品中存在靶多核苷酸的可检测信号的组分。合适的标记包括放射性同位素、核苷酸发色团、酶、底物、荧光分子、化学发光部分、磁性颗粒、生物发光部分等。因此,标记是通过分光镜方法、光化学方法、生化方法、免疫生化方法、电学方法、光学方法、化学方法或任何其它适当的方法可检测的任何组分。术语“标记”是用来指具有可检测的生理性质的任何化学基团或部分,或者能够引起化学基团或部分显示可检测的物理性质的任何化合物,例如酶催化底物转化成可检测产物。术语“标记”还包括抑制特定生理性质表达的化合物。标记还可以是作为结合对的一个成员的化合物,其另一个成员则带有可检测的生理性质。
本文所使用的“生物样品”是指例如从受治疗者中分离出来的组织或液体的样品,包括但不限于例如血液、血浆、血清、脊髓液、淋巴液、皮肤、呼吸道、肠道和泌尿生殖道、眼泪、唾液、乳汁、细胞(包括但不限于血液细胞)、BD、器官,以及还有体外细胞培养物组分的样品。
本文所使用的术语“生物源”是指例如从中得到靶多核苷酸的来源。来源可以是如上所述的任何形式的“样品”,包括但不限于细胞、组织或体液。“不同的生物源”可指同一个体的不同细胞/组织/器官,或来自同一物种不同个体的细胞/组织/器官,或来自不同物种的细胞/组织/器官。
术语“基因”是指例如(a)含有至少一个本文所公开的DNA序列的基因;(b)编码由本文所公开的DNA序列编码的氨基酸序列的任何DNA序列;和/或(c)与编码本文所公开的编码序列的互补序列杂交的任何DNA序列。优选该术语包括编码区以及非编码区,优选包括正常基因表达所必需的所有序列,包括启动子、增强子和其它调节序列。
“PXR基因”是指例如Genebank所包括的按以下登录号识别的序列:NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133或登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880、NP_071285。当基因组DNA的片段定位于内源性同源序列内以及与内源性同源序列重组时,便出现PXR基因的“破坏”。这些序列破坏或修饰可包括插入、错义、移码、缺失或取代,或DNA序列的置换,或其任何组合。插入包括可以是动物、植物、真菌、昆虫、原核来源或病毒来源的完整基因的插入。例如,破坏可以改变或置换启动子、增强子或PXR基因的剪接位点,并可通过部分或完全抑制其产生,或者通过提高正常基因产物的活性,来改变正常的基因产物。
术语“转基因细胞”是指例如通过基因打靶方法在其基因组内含有遭完全或部分破坏、修饰、改变或置换的PXR基因的细胞。
术语“转基因动物”是指例如通过基因打靶的方法在其基因组内含有遭破坏的特定基因的动物。转基因动物包括杂合子动物(例如一个缺陷型等位基因和另一个野生型等位基因)和纯合子动物(例如两个缺陷型等位基因)。
本文所使用的术语“选择标记”或“阳性选择标记”是指例如编码某一产物的基因,该基因只能够使携带该基因的细胞在某些条件下存活和/或生长。例如,表达所导入的新霉素抗性(Neor)基因的植物和动物细胞对化合物G418具有抗性。没有携带Neor基因标记的细胞将被G418杀死。其它阳性选择标记为本领域技术人员所知。
“宿主细胞”包括受治疗者细胞或细胞培养物,它们可以是或者就是载体的接受体或掺入的核酸分子和/或蛋白质的接受体。宿主细胞包括单一宿主细胞的子代,并且子代由于天然突变、偶发突变或蓄意突变所致,不一定与原亲本完全相同(在形态上或在整体DNA互补性上)。宿主细胞包括用本公开内容的构建体转染的细胞。
本文所使用的术语“调节”是指例如PXR功能、表达、活性或者与PXR基因的破坏有关的表型的抑制、降低、增加或提高。关于PXR受体,模件还可包括改变受体的结合性质、与受体结合、激活受体、与受体缔合和/或抑制受体的活性或分子与受体的相互作用。
术语“改善”是指例如减少、减轻或消除病况、疾病、病症或表型(包括异常)或与PXR基因中的破坏有关的症状。
术语“异常”是指例如其中涉及PXR基因遭破坏的任何疾病、病症、病况或表型,包括病理病症。
利福霉素类抗生素是例如具有下式I结构的化合物:
其中A可以为结构A1:
或者为结构A2:
其中,-x-为共价化学键或无;R为氢或乙酰基;
R1和R2独立表示氢、(C1-4)烷基、苄氧基、一-(C1-3)烷基氨基-(C1-4)烷基和二-(C1-3)烷基氨基-(C1-4)烷基、(C1-3)烷氧基-(C1-4)烷基、羟基甲基、羟基-(C2-4)-烷基、硝基或者R1和R2与吡啶核的两个连续碳原子结合在一起形成未取代或者被甲基或乙基中的一个或两个取代的苯环;R3为氢原子或无;前提条件是,如果A为A1,则-x-无且R3为氢原子;且前提条件是,如果A为A2,则-x-为共价化学键且R3无。
本文还描述了如上定义的一种化合物,其中A为如上定义的A1或A2,-x-为共价化学键或无,R为氢或乙酰基,R1和R2独立表示氢、(C1-4)烷基、苄氧基、羟基-(C2-4)烷基、二-(C1-3)烷基氨基-(C1-4)烷基、硝基或者R1和R2与吡啶核的两个连续碳原子结合在一起形成苯环,R3为氢原子或无;前提条件是,如果A为A1,则-x无且R3为氢原子;且前提条件是,如果A为A2,则-x-为共价化学键且R3无。
本文还描述了如上定义的一种化合物,其中A为如上定义的A1或A2,-x-为共价化学键或无,R为乙酰基,R1和R2独立表示氢、(C1-4)烷基或者R1和R2与吡啶核的两个连续碳原子结合在一起形成苯环,R3为氢原子或无;前提条件是,如果A为A1,则-x无且R3为氢原子;且前提条件是,如果A为A2,则-x-为共价化学键且R3无。
本文还描述了如上定义的一种化合物,它是4-脱氧-4′-甲基-吡啶并[1′,2′-1,2]咪唑并[5,4-c]利福霉素SV。本文还描述了如上定义的一种化合物,它是4-脱氧-吡啶并[1′,2′:1,2]咪唑并[5,4-c]利福霉素SV。
本文还描述了如上定义的一种化合物,其中A如上定义,-x-为共价化学键或无;R为氢或乙酰基;R1和R2独立表示氢、(C1-4)烷基、苄氧基、一和二(C1-3)烷基氨基(C1-4)烷基、(C1-3)烷氧基-(C1-4)烷基、羟基甲基、羟基-(C2-4)-烷基、硝基或者R1和R2与吡啶核的两个连续碳原子结合在一起形成未取代或者被甲基或乙基中的一个或两个取代的苯环;R3为氢原子或无;前提条件是,如果A为A1,则-x无且R3为氢原子;且前提条件是,如果A为A2,则-x-为共价化学键且R3无。
利福昔明是具有下式II结构的化合物:
BD相关序列
最初可通过与本文所列BD序列同源的大量核酸序列和/或氨基酸序列来鉴定BD序列。这种同源性可以整个核酸序列或氨基酸序列为基础,并且一般按照下述方法采用同源程序或杂交条件来确定。在一个实施方案中,BD序列是在BD中上调的序列;也就是说,这些基因在BD组织中的表达比正常组织的高。本文所使用的“上调”是指表达增加约50%,优选约100%,更优选约150%~约200%,其中上调300%~1000%。
在另一个实施方案中,BD序列是在BD中下调的序列;也就是说,在BD组织中这些基因的表达比同一分化期的正常组织的低。本文所使用的“下调”是指表达降低约50%,优选约100%,更优选约150%~约200%,其下调300%~1000%至无表达。
在又一个实施方案中,BD序列是与同一分化期的正常淋巴组织相比,序列发生改变但具有相同表达谱或经改变的表达谱的序列。本文所使用的“经改变的BD序列”还指例如经过截短的序列、含有插入或含有点突变的序列。
在一个实施方案中,BD序列是跨膜蛋白。跨膜蛋白是跨越细胞的磷脂双层的分子。它们可具有胞内结构域、胞外结构域或两者兼有。这类蛋白质的胞内结构域可具有多种功能,包括已披露的胞内蛋白的功能。该蛋白质还可是胞内蛋白、核内蛋白或分泌蛋白。
一般来讲,本文所使用的术语“多肽”是指例如由所列举的多核苷酸编码的全长多肽和由所列举的多核苷酸所代表的基因编码的多肽两者以及其部分或片段。本发明包括天然存在的蛋白质的变体,其中这类变体与天然存在的蛋白质同源或基本类似,并且可以是来源于相同或不同的物种作为天然存在的蛋白质形式(例如天然表达所列举的多肽的人、鼠或某些其它物种,通常为哺乳动物物种)。一般来讲,多肽变体具有与本文所述的差异表达的多肽有至少约80%、至少约81%、至少约82%、至少约83%、至少约84%、至少约85%、至少约86%、至少约87%、至少约88%、至少约89%、通常至少约90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%以上通常至少约99%序列同一性的序列。
属于本发明范围内的还有变体。多肽的变体包括突变体、片段和融合体。突变体可包括氨基酸取代、加入或缺失。氨基酸取代可以是保守氨基酸取代或以排除非必需氨基酸的取代,例如改变糖基化位点、磷酸化位点或乙酰化位点,或者通过取代或缺失不是功能所必需的一个或多个半胱氨酸残基使错折叠降到最低。保守氨基酸取代是保持被取代氨基酸的正常电荷、疏水性/亲水性和/或空间位阻的取代。可以对变体进行设计以保持或提高蛋白质特定区域(例如功能结构域和/或当多肽是蛋白质家族的成员时与共有序列有关的区域)的生物活性。
变体还包括本文所公开的多肽的片段,特别是生物活性片段和/或相当于功能结构域的片段。目标片段的长度通常可为至少约8个氨基酸(aa)、10aa、15aa、20aa、25aa、30aa、35aa、40aa~至少约45aa,长度通常为至少约50aa、至少约75aa、至少约100aa、至少约125aa、长度至少约150aa、至少约200aa、至少约300aa、至少约400aa,长度可长达500aa或更长,但是长度通常不会超过约1000aa,其中所述片段可具有一氨基酸序列段,该氨基酸序列段与由具有任一种本文所提供的多核苷酸序列的序列的多核苷酸或其同源物编码的多肽具有同一性。本文所述的蛋白质变体由属于本发明范围的多核苷酸编码。可使用遗传密码选择适当的密码子来构建相应的变体。
虽然观察到与BD有关的多核苷酸的表达发生改变,但是由这些多核苷酸编码的多肽表达水平的改变很可能在BD中起作用。
在一个实施方案中,BD蛋白定义中还包括BD家族的其它BD蛋白,以及得自其它生物的如下述方法克隆和表达的BD蛋白。因此,可采用探针或简并聚合酶链式反应(PCR)引物序列从人或其它生物中寻找其它相关的BD蛋白。正如本领域技术人员应了解的一样,特别有用的探针和/或PCR引物序列包括BD核酸序列的独特区域。正如本领域普遍所知的一样,某些PCR引物长度为约15~约35个核苷酸,其中约20~约30个是确定的,并且按需要可含有肌苷。PCR反应的条件是本领域众所周知的。另外,如本文中所述,例如,可以通过说明的额外序列、加入表位或纯化标签、加入其它融合序列等,产生比所述数目的核酸编码的BD蛋白长的BD蛋白。还可鉴定BD蛋白是由BD核酸编码的。因此,BD蛋白由与本文列举的序列表的序列或其互补序列杂交的核酸编码。
最初用与本文所列BD序列同源的实体核酸序列和/或氨基酸序列来鉴定BD序列。这种同源性可以整个核酸序列或氨基酸序列为基础,并且一般按照下述方法采用同源程序或杂交条件来确定。
如果核酸序列相对于本文所述核酸之一的总体同源性优选大于约75%、大于约80%、大于约85%或大于90%,则本文所使用的核酸是“BD核酸”。在一些实施方案中,同源性高达约93%-95%或98%。在一个实施方案中,用来确定序列同一性或相似性的序列选自本文所述核酸的序列。在另一个实施方案中,序列是本文所述的核酸序列的天然存在的等位基因变体。在另一个实施方案中,序列是本文进一步描述的序列变体。
在这个方面的同源性是指序列相似性或同一性。出于同源性目的的比较是将含有测序错误的序列与正确序列进行比较。这种同源性可以应用本领域的标准技术来确定,包括但不限于Smith和Waterman的局部同源性算法(Smith和Waterman,Adv.Appl.Math.2:482(1981));Needleman和Wunsch的同源性比对算法(Needleman和Wunsch,J.Mol.Biol.48:443(1970));Pearson和Lipman的相似性检索方法(Pearson和Lipman,PNAS USA 85:2444(1988));这些算法的计算机执行(Wisconsin遗传学软件包中的GAP、BESTFIT、FASTA和TFASTA,Genetics Computer Group,575Science Drive,Madison,Wis.);Devereux等人的最佳拟合序列程序(Devereux等,Nucl.Acid Res.12:387-395(1984)),优选使用默认设置;或者通过检查。有用的算法的一个实例是PILEUP。PILEUP采用渐进成对比对,从一组相关序列中产生多序列比对。它还可画一个树状图显示用来产生比对的聚类关系。PILEUP应用Feng和Doolittle的渐近比对方法(Feng和Doolittle,J.Mol.Evol.35:351-360(1987))的简化法;该方法类似于Higgins和Sharp CABIOS 5:151-153(1989)描述的方法。有用的PILEUP参数包括默认空位权重(gzp weight)3.00、默认空位长度权重(gap length weight)0.10和加权末端空位。有用算法的另一个实例是BLAST(基本局部比对检索工具(Basic Local Alignment Search Tool))算法,参见Altschul等,J.Mol.Biol.215,403-410,(1990)和Karlin等,PNAS USA90:5873-5787(1993)。一个特别有用的BLAST程序是从Altschul等人获得的WU-BLAST-2程序[Altschul等,Methods in Enzymology,266:460-480(1996);http://blast.wustl.edu/]。WU-BLAST-2采用若干个检索参数,其大多数设置成默认值。可调节参数用下列值设置:重叠跨距(overlap span)=1,重叠部分(overlap fraction)=0.125,字阈值(wordthreshold)(T)=11。HSP S和HSP S2参数是动态值,是由程序本身根据具体序列的组成和针对其进行目标序列检索的具体数据库的组成来设定的;然而,可以调节这些值以提高灵敏度。用匹配的相同残基数除以比对区中“较长”序列的残基总数,求出氨基酸序列同一性百分比值。“较长”序列是在比对区中具有最多实际残基的序列(由WU-Blast-2引入以使比对分值最大化的空位忽略不计)。因此,“百分比(%)核酸序列同一性”定义为候选序列中与以下登录号的核酸的核苷酸残基相同的核苷酸残基的百分比:NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135或CS618133。
在本发明的另一个实施方案中,提供能够在中等严格性条件至高严格性条件下与本文所提供的多核苷酸序列或其片段或其互补序列杂交的多核苷酸组成成分。杂交技术是分子生物学领域众所周知的。出于说明目的,用于测定本发明的多核苷酸与其它多核苷酸杂交的合适的中等严格性条件包括在5X SSC(“柠檬酸钠盐水(saline sodiumcitrate)”;9mM NaCl、0.9mM柠檬酸钠)、0.5%SDS、1.0mM EDTA(pH 8.0)的溶液中预洗涤;在50-60℃、5X SSC中杂交过夜;接着在65℃下用含有0.1%SDS的2X、0.5X和0.2X SSC的每一种洗涤20分钟。本领域技术人员应了解的是可容易地控制杂交的严格性,例如通过改变杂交溶液的含盐量和/或进行杂交的温度。例如,在另一个实施方案中,合适的高严格性杂交条件包括上述条件,只是提高杂交温度至例如60-65℃或65-70℃。还可随着加入去稳定剂(例如甲酰胺)而达到严格性条件。
另外,本发明的BD核酸序列是较大基因的片段,例如,它们是核酸区段。或者,BD核酸序列可用作癌基因位置的标志,例如,BD序列可以是激活原癌基因的增强子。在这个方面的“基因”包括编码区,非编码区以及编码和非编码区的混合区。因此,正如本领域技术人员应了解的一样,应用用于克隆较长序列或全长序列的本领域众所周知的技术,使用本文所提供的序列,可以获得BD基因的额外序列;参见Maniatis等和Ausubel等(同上),特此通过引用明确予以结合。一般来讲,这可采用PCR,例如动力学PCR来进行。
BD表达的检测
一旦鉴定出BD核酸,就可以进行克隆,且必要时可将其组成部分进行重组形成完整的BD核酸。一旦从其天然来源,例如,包含在质粒或其它载体内分离出来,或由其切离,形成线性核酸区段,就可将重组BD核酸进一步用作鉴定和分离其它BD核酸(例如附加编码区)的探针。它还可用作“前体”核酸以获得经修饰的BD核酸和蛋白质或变体BD核酸和蛋白质。在一个实施方案中,一旦鉴定出BD基因,其核苷酸序列便可用来设计对BD基因有特异性的探针。
本发明的BD核酸以若干种方式使用。在第一个实施方案中,制成可与BD核酸杂交的核酸探针,并与将用于筛选和诊断方法或基因疗法和/或反义应用的生物芯片连接。或者,将包括BD蛋白编码区的BD核酸放入表达载体中用于BD蛋白表达,此外用于筛选目的或用于给予受治疗者。
DNA微阵列技术的最新近展使得在单个固相支持体上对大量靶BD核酸分子进行大规模测定成为可能。美国专利第5,837,832号(Chee等)和相关专利申请描述了使一系列寡核苷酸探针固定化以用于样品中特定核酸序列的杂交和检测。使从目标组织分离的目标靶多核苷酸与DNA芯片杂交,根据离散的探针位置上靶多核苷酸的偏好和杂交的程度检出特定序列。阵列的一种用途在于对差异性基因表达进行分析,其中对不同细胞(常常为目标细胞和对照细胞)中基因的表达谱进行比较,并鉴定出相应细胞中基因表达的任何差异。这类信息可用于鉴定在特定细胞或组织类型中表达的基因类型,并根据表达谱对BD病况进行诊断。参见美国专利第6,410,229号(Lockhart等)。例如,采用cDNA微阵列对人类癌症的基因表达形式进行分析可参见DeRisi等(Nature Genetics 14:457-460(1996))。
在某些实施方案中,探针可以是嵌合分子;例如,可包含一种以上类型的碱基或糖亚基,和/或在同一引物内可存在不只一种类型的键。探针可包含促进与其靶序列杂交的部分,正如本领域已知的一样,例如嵌入剂和/或小沟结合物。碱基、糖和核苷酸间主链的变化以及探针上任何侧基的存在,都应与探针以序列特异性方式与其靶序列结合的能力相适应。在这些界限内,大量已知和待开发的结构修饰都是可行的。有利的是,本发明的探针可能具有可供信号放大之用的结构特征,这类结构特征为例如Urdea等(Nucleic Acids Symp.Ser.,24:197-200(1991))或欧洲专利第EP-0225,807号所描述的分支DNA探针。此外,用于制备形成探针的各种杂环碱基、糖、核苷和核苷酸的合成方法,以及预先确定的特定序列的寡核苷酸的制备法都得到充分了开发并且是本领域已知的。用于寡核苷酸合成的一种方法结合了美国专利第5,419,966号的教导。
在一个实施方案中,使用编码BD蛋白的BD核酸以制备各种表达载体,以表达BD蛋白,BD蛋白然后可用于如下所述的筛选实验。表达载体可以是自我复制的染色体外载体或整合到宿主基因组的载体。这些表达载体一般包括与编码BD蛋白的核酸有效连接的转录和翻译的调节核酸。术语“控制序列”是指例如有效连接的编码序列在特定宿主生物中进行表达所必需的DNA序列。例如,适于原核生物的控制序列包括启动子、任选操纵子序列和核糖体结合位点。已知真核细胞利用启动子、聚腺苷酸化信号和增强子。
当核酸被置于与另一核酸序列具有功能关系的位置时,该核酸是“有效连接的”。例如,如果要表达成为参与某一多肽分泌的前蛋白质,则将前序列或分泌前导序列的DNA与该多肽的DNA有效连接;如果要影响某一序列的转录,则将启动子或增强子与该编码序列有效连接;或者如果将某一编码序列定位以促进翻译,则将核糖体结合位点与该编码序列有效连接。“有效连接”一般是指被连接的DNA序列是邻接的,而且在分泌前导序列的情况下,是邻接并在读框(reading phase)中。然而,增强子不必是邻接的。本领域已知用于各种宿主细胞的多种适当表达载体的类型和合适调节序列。
一般来讲,转录和翻译调节序列可包括但不限于启动子序列、核糖体结合位点、转录起始序列和终止序列、翻译起始序列和终止序列以及增强子或激活物序列。在一个实施方案中,调节序列包括启动子及转录起始序列和终止序列。启动子序列编码组成型启动子或诱导型启动子。启动子可以是天然存在的启动子或杂合启动子。结合不只一个启动子的元件的杂合启动子也是本领域已知的,并可用于本发明。
另外,表达载体可包含另外的元件。例如,表达载体可能具有两个复制系统,因此允许它保持在两种生物中,例如在哺乳动物或昆虫细胞中用于表达,以及在原核宿主中用于克隆和扩增。另外,在一个实施方案中,表达载体含有供选择转化的宿主细胞之用的选择标记基因。筛选基因是本领域众所周知的,并随所采用的宿主细胞而变化。
可通过例如在合适的条件下,对用含有BD蛋白编码核酸的表达载体转化的宿主细胞进行培养,诱导或引起BD蛋白的表达,来产生本发明的BD蛋白。适于BD蛋白表达的条件将随选择的表达载体和宿主细胞而变化,并且可由本领域技术人员通过常规实验方法容易地加以确定。例如,在表达载体中,组成型启动子的使用将需要使宿主细胞的生长和增殖最优化,而诱导型启动子的使用则需要适于诱导的适当生长条件。另外,在一些实施方案中,收获时机很重要。例如,用于昆虫细胞表达的杆状病毒系统是裂解病毒,因此收获期选择对于产物产量可能是至关重要的。
还可以采用本领域众所周知的技术,将BD蛋白制成融合蛋白。
在一个实施方案中,本发明的BD核酸、蛋白质和抗体是经标记的。所谓“标记的”在本文中是指化合物是直接或间接标记的,并可具有至少一个提供可检测信号的元件,例如,所连接的同位素或化合物使得能够检出所述化合物。标记一般包括可以是放射性同位素或重同位素的同位素标记、磁性标记、酶标记、可以是抗体或抗原的免疫标记以及着色染料或荧光染料。可将标记掺到BD核酸、蛋白质和抗体的任何位置上。例如,标记应能够直接或间接产生可检测信号。可检测的部分可以是放射性同位素,例如3H、14C、32P、35S或125I;荧光或化学发光化合物,例如异硫氰酸荧光素、罗丹明;或萤光素;或酶,例如碱性磷酸酶、β-半乳糖苷酶或辣根过氧化物酶。可以采用本领域已知的用于将抗体与标记缀合的任何方法,包括以下文献所描述的方法:Hunter等,Nature,144:945(1962);David等,Biochemistry,13:1014(1974);Pain等,J.Immunol.Meth.,40:219(1981);以及Nygren,J.Histochem.and Cytochem.,30:407(1982)。其它标记可包括特异性结合分子。特异性结合分子包括一对,例如生物素和链霉抗生物素、地高辛和抗地高辛(antidigoxin)等。对于特异性结合成员,互补成员通常根据上述已知方法用供检测之用的分子进行标记。该标记可以直接或间接提供可检测信号。
在一个实施方案中,通过竞争性结合测定法确定候选生物活性剂的结合。在该实施方案中,竞争剂是已知与靶分子(例如BD蛋白)结合的结合部分,例如抗体、肽、结合配偶体、配体等。在某些情况下,在生物活性剂和结合部分之间可能存在竞争性结合,其中结合部分置换生物活性剂。
BD抗原和其抗体
在一个实施方案中,本发明提供BD特异性抗体。在一个实施方案中,当使用BD蛋白以产生抗体时,例如对于免疫疗法,BD蛋白应与全长蛋白有共同的至少一个表位或决定子。所谓“表位”或“决定子”在本文中是指在MHC情况下可产生和/或结合抗体或T细胞受体的蛋白质的部分。因此,在多数情况下,针对较小BD蛋白制成的抗体将能够与全长蛋白结合。在一个实施方案中,表位是独特的;也就是说,针对独特表位制成的抗体几乎没有或没有交叉反应性。可对由BD多核苷酸序列编码的任何多肽序列进行分析以确定多肽的某些区域。例如,通过选择代表在某一环境下很可能暴露在多肽表面的多肽区域的数值,经DNASTAR分析由数据确定高抗原性的区域,在所述环境中,在引发免疫应答的过程中可发生抗原识别。例如,采用DNASTAR计算机算法(DNASTAR,Inc.,Madison,Wis.;参见万维网:dnastar.com)的默认参数,对由BD多核苷酸序列编码的多肽的氨基酸序列进行了分析。
在一个实施方案中,术语“抗体”包括本领域已知的抗体片段,包括Fab、Fab2、单链抗体(例如Fv)、嵌合抗体等,或通过完整抗体的修饰产生,或应用重组DNA技术从头合成。制备多克隆抗体的方法为本领域技术人员所知。多克隆抗体可在哺乳动物内产生,例如,通过免疫剂和佐剂(如有需要)的一次或多次注射。或者,抗体可以是单克隆抗体。单克隆抗体可采用杂交瘤方法制备,例如Kohler和Milstein,Nature,256:495(1975)所描述的杂交瘤。在一个实施方案中,抗BD抗体能够降低或消除BD的生物功能,正如下面所描述的一样。也就是说,将抗BD抗体(多克隆或优选单克隆)加到BD(或含有BD的细胞)可降低或消除BD活性。在一个实施方案中,抗BD蛋白的抗体是人源化抗体。“人源化”抗体是这指样一种分子,该分子具有基本上得自非人类物种的免疫球蛋白的抗原结合部位,该分子的其余免疫球蛋白结构以人免疫球蛋白的结构和/或序列为基础。抗BD蛋白的特异性抗体,或为多克隆,或为单克隆,都可通过上面论述的本领域已知的任何合适方法产生。例如,鼠或人单克隆抗体可通过杂交瘤技术产生,或者可将BD蛋白,或其免疫活性片段,或抗独特型抗体,或其片段给予动物以诱导能够识别和结合BD蛋白的抗体的产生。这类抗体可得自任何抗体类别,包括但不限于IgG、IgA、IgM、IgD和IgE,或者在鸟类品种的情况下为IgY,以及得自任何抗体亚类。
在另一确定的实施方案中,产生抗体所针对的BD蛋白为跨膜蛋白。虽然不受理论的束缚,但是用于治疗的抗体与BD蛋白的胞外结构域结合,并阻止它与其它蛋白质结合,例如循环配体或细胞缔合分子。抗体可引起跨膜BD蛋白的下调。正如本领域技术人员所了解的一样,抗体可以是蛋白质与BD蛋白胞外结构域结合的竞争性抑制剂、非竞争性抑制剂或反竞争性抑制剂。抗体还是BD蛋白的拮抗剂。此外,抗体阻止跨膜BD蛋白的活化。一方面,当抗体阻止其它分子与BD蛋白结合时,抗体便阻止了细胞的生长。抗体还可使细胞对细胞毒剂或化疗药物产生敏化,细胞毒剂包括但不限于TNF-α、TNF-β、IL-1、INF-γ和IL-2,化疗药物包括5FU、长春碱、放线菌素D、顺铂、甲氨蝶呤等。在一些情况下,所述抗体属于当与跨膜蛋白复合时便激活血清补体因此介导细胞毒性的亚型。因此,通过给予受治疗者针对跨膜BD蛋白的抗体可以治疗BD。
在另一确定的实施方案中,抗体与治疗部分缀合。一方面,所述治疗部分是调节BD蛋白活性的小分子。另一方面,所述治疗部分调节与BD蛋白缔合或与BD蛋白紧密相邻的分子的活性。所述治疗部分可抑制酶活性,例如与BD有关的蛋白酶或蛋白激酶活性。
在另一确定的实施方案中,产生抗体所针对的BD蛋白是胞内蛋白。在这种情况下,抗体可与有利于进入细胞的蛋白质缀合。在一种情况下,抗体通过胞吞进入细胞。在另一个实施方案中,将编码抗体的核酸给予个体或细胞。此外,其中BD蛋白可被靶定在细胞(例如核)内,其抗体含有用于所述靶定位的信号,例如核定位信号。
本发明的BD抗体与BD蛋白特异性结合。所述“特异性结合”在本文中是指抗体与蛋白质结合的结合常数的范围为104-10-6M,其中一个范围为10-7-10-9M。在一个实施方案中,BD蛋白在表达后进行纯化或分离。可通过本领域已知的各种方法,根据样品中存在的其它组分,来分离或纯化BD蛋白。
本文所述抗体的产生包括例如用于产生能够特异性识别一个或多个表位的抗体的方法。这类抗体可包括但不限于多克隆抗体、单克隆抗体(mAb)、人源化或嵌合抗体、单链抗体、Fab片段、F(ab′)2片段、由Fab表达文库产生的片段、抗独特型(抗Id)抗体以及上述任一种的表位结合片段。例如在检测生物样品中的PXR基因时,又或者作为用于抑制异常PXR基因活性的方法时,都可使用这类抗体。因此,这类抗体可用作疾病治疗方法的组成部分,和/或可用作诊断技术的组成部分,可籍此测出受治疗者PXR基因蛋白的异常水平,或测出这类蛋白质的异常形式的存在。
对于抗体的产生,可通过注射PXR基因、其表达产物或其部分来免疫各种宿主动物。这类宿主动物可包括但不限于兔、小鼠、大鼠、山羊和鸡等等。各种佐剂可用于增强免疫应答,这取决于宿主物种,佐剂包括但不限于弗氏佐剂(完全和不完全)、氢氧化铝等矿物凝胶(mineral gel)、溶血磷脂酰胆碱等表面活性物质、普流罗尼克多元醇、聚阴离子、肽、油乳液、匙孔血蓝蛋白、二硝基苯酚及潜在有益的人用佐剂,例如BCG(卡介苗)和短小棒状杆菌(Corynebacteriumparvum)。
多克隆抗体是从用抗原(例如PXR基因产物)或其抗原功能衍生物免疫的动物的血清中获得的异质群的抗体分子。为了产生多克隆抗体,可通过注射补充了上述佐剂的基因产物,来免疫宿主动物,例如同样如上所述的动物。
单克隆抗体,是抗特定抗原的同质群的抗体,可通过供培养物中的传代细胞系产生抗体分子之用的任何技术获得。这些包括但不限于杂交瘤技术(Kohler和Milstein,Nature,256:495-7(1975)和美国专利第4,376,110号));人B细胞杂交瘤技术(Kosbor等,Immunology Today,4:72(1983);Cote等,Proc.Natl.Acad.Sci.USA,80:2026-30(1983));以及EBV杂交瘤技术(Cole等,Monoclonal Antibodies And BDTherapy,Alan R.Liss,Inc.,New York,第77-96页(1985))。这类抗体可以是任何免疫球蛋白类别,包括IgG、IgM、IgE、IgA、IgD及其任何亚类。产生本公开内容的mAb的杂交瘤可以在体外或体内进行培养。体内产生高效价的mAb构成本发明的某些产生方法。
另外,可采用开发用于产生“嵌合抗体”的技术(Morrison等,Proc.Natl.Acad.Sci.,81:6851-6855(1984);Takeda等,Nature,314:452-54(1985)),该技术通过将得自具有合适抗原特异性的小鼠抗体分子的基因与得自具有合适生物活性的人抗体分子的基因剪接在一起。嵌合抗体是其中不同部分得自不同动物物种的分子,例如具有得自鼠mAb的可变区和人免疫球蛋白恒定区的抗体。
或者,可以采用所述用于产生单链抗体的技术(美国专利第4,946,778号;Bird,Science 242:423-26(1988);Huston等,Proc.Natl.Acad.Sci.USA,,85:5879-83(1988);以及Ward等,Nature,334:544-46(1989))来产生基因-单链抗体。单链抗体通常通过氨基酸桥使Fv区的重链和轻链片段连接形成,从而产生单链多肽。
识别特定表位的抗体片段可通过已知技术产生。例如,这类片段包括但不限于:可通过胃蛋白酶消化抗体分子产生的F(ab′)2片段,以及通过还原F(ab′)2片段的二硫键产生的Fab片段。或者,可以构建Fab表达文库(Huse等,Science,246:1275-81(1989)),以供快速和容易地鉴定具有所需特异性的单克隆Fab片段。
BD表型的检测
一旦经表达和纯化,必要时,BD蛋白和核酸便可用于多种应用。一方面,测定在BD表型中不同细胞状态的基因表达水平;也就是说,评价正常组织中和BD组织中基因的表达水平以提供表达谱。特定细胞状态或发育点的表达谱是所述状态的重要“指纹”;虽然两种状态可能具有进行类似表达的任何特定基因,但是同时评价多种基因可供产生对于所述细胞状态是唯一的基因表达谱。通过比较不同状态中细胞的表达谱,获得在这些状态的每一个中有关该基因的信息(包括基因的上调和下调)。然后,可进行诊断或确定例如得自具体受治疗者的组织是否具有正常组织或BD组织的基因表达谱。
在一个实施方案中,将本文所述的三类蛋白质(分泌蛋白、跨膜蛋白或胞内蛋白)中的任一类用于诊断实验。将BD蛋白、抗体、核酸、修饰蛋白和含有BD序列的细胞用于诊断实验。这可在受治疗者基因水平或相应的多肽水平上进行,或者作为一组实验进行。
在另一个确定的方法中,抗BD蛋白的抗体应用于原位成像技术。在这种方法中,使细胞与多种抗BD蛋白抗体中的一种接触。在洗涤除去非特异性结合的抗体之后,检测一种或多种抗体的存在。在一个实施方案中,通过与含有可检测标记的第二抗体一起孵育来检测抗体。在另一种方法中,第一抗BD蛋白抗体含有可检测标记。在另一确定的实施方案中,多种第一抗体的每一种中含有独特的可检测标记。该方法特别应用于多种BD蛋白的同时筛选。正如本领域技术人员所了解的一样,多种其它组织学成像技术可用于本发明。
要了解的是,在受治疗者和标准之间进行表达指纹比较时,技术人员可做出诊断以及预后。此外还要了解的是,指示诊断结果的基因可不同于指示预后结果的基因。
筛选候选组合物
在一个实施方案中,任一个本文所述的BD序列都可用于药物筛选实验。BD蛋白、抗体、核酸、修饰蛋白和含有BD序列的细胞或用于药物筛选实验,或评价候选药物对“基因表达谱”或多肽表达谱的作用。在一个实施方案中,表达谱优选与高通量筛选技术联用,以供在用候选药剂治疗之后监测表达谱基因(Zlokarnik等,Science 279,84-8(1998),Heid等,Genome Res.,6:986-994(1996))。
在另一个实施方案中,在细胞筛选实验中使用BD蛋白、抗体、核酸、修饰蛋白和含有天然或修饰的BD蛋白。也就是说,本发明提供用于筛选调节BD表型的组合物的新方法。如上所述,这可以通过筛选基因表达的调节剂或蛋白质活性的调节剂来进行。同样,这可在受治疗者的基因水平或蛋白质水平上或者通过评价候选药物对“基因表达谱”的作用来进行。在一个实施方案中,表达谱优选与高通量筛选技术联用,以供在用候选药剂治疗之后监测表达谱基因,参见Zlokarnik,同上。
在鉴定出本文的BD基因后,可以进行多种实验以评价药剂对基因表达的作用。在一个实施方案中,实验可以在受治疗者的基因水平或蛋白质水平上进行。也就是说,鉴定出作为在BD中异常调节的特定基因时,可对候选生物活性剂进行筛选以调节基因的调节。因此,“调节”包括基因表达或活性的增加和降低。特定的调节量将取决于正常组织相对于BD组织的基因表达的起始变化,其中变化至少10%,优选50%,更优选100-300%,在一些实施方案中为300-1000%或更高。因此,如果与正常组织相比,基因在BD中增加4倍,则需要候选药剂降低约4倍;与正常组织相比在BD中得到10倍的降低,则在表达中需要候选药剂增加10倍等。或者,如果BD序列发生了改变却具有相同的表达谱或变化的表达谱,则蛋白质按照本文所述进行检测。
正如本领域技术人员应了解的一样,这可通过在基因水平或蛋白质水平上的评价来进行;也就是说,可以采用核酸探针和基因表达水平的定量测定来监测基因表达的量,又或者,可以通过例如使用抗BD蛋白抗体和标准免疫测定法来监测基因产物本身的水平。或者,可按下述方法进行与蛋白质的结合和生物活性测定。
在一个实施方案中,进行了基因表达监测,同时监测了多种基因(例如表达谱),虽然也可进行多种蛋白质表达监测。
在一个实施方案中,一般在分析之前将候选生物活性剂加到细胞中。此外,提供鉴定调节特定BD类型、调节BD蛋白、结合BD蛋白或干扰BD蛋白与抗体结合的候选生物活性剂的筛选法。
本文所使用的术语“候选生物活性剂”、“候选活性剂”、“候选组合物”或“候选药物”或语法上的等同术语描述了待用于生物活性剂测定的任何分子,例如蛋白质、寡肽、有机小分子或无机小分子、多糖、多核苷酸等,所述生物活性剂能够直接或间接改变BD表型、结合BD蛋白和/或调节BD蛋白的生物活性或BD序列(同时包括核酸序列和蛋白质序列)的表达。在一个特别确定的实施方案中,候选活性剂抑制BD表型以达到例如正常组织指纹。同样,候选活性剂优选抑制严重的BD表型。一般将多种实验混合物与不同浓度的活性剂一起平行进行以获得对各种浓度的不同反应。通常,这些浓度之一用作阴性对照,例如,在0浓度下或在检出水平以下。
一方面,候选活性剂可中和BD蛋白的作用。所谓“中和”是指蛋白质的活性被抑制或被抵消使得基本上对细胞无作用。
候选活性剂包括多种化合物类别,虽然它们通常是有机分子或无机分子,优选分子量大于100道尔顿且小于约2,500道尔顿的有机小分子化合物。小分子可以是例如小于2000D,或小于1500D或小于1000D或小于500D。候选活性剂包含与蛋白质相互作用的结构上所必需的官能团,特别是氢键,通常包括至少胺基、羰基、羟基或羧基,优选至少两个官能化学基团。候选活性剂常常包含环碳或杂环结构和/或被一个或多个上述官能团取代的芳族结构或聚芳结构。还存在于生物分子中的候选活性剂包括肽、糖、脂肪酸、类固醇、嘌呤、嘧啶、衍生物、结构类似物或其组合。
候选活性剂可获自各种来源,包括合成化合物文库或天然化合物文库。例如,可利用多种用于随机和定向合成多种有机化合物和生物分子(包括随机化寡核苷酸的表达)的方法。或者,可获得或容易产生细菌、真菌、植物和动物提取物形式的天然化合物文库。此外,通过常规的化学、物理和生物化学方法,容易对天然文库或经合成产生的文库和化合物进行修饰。可以对已知的药物进行定向或随机化学修饰,例如酰化、烷基化、酯化或酰胺化以产生结构类似物。在一个实施方案中,候选生物活性剂是蛋白质。在一个实施方案中,候选生物活性剂是天然存在的蛋白质或天然存在的蛋白质的片段。因此,例如,可以使用含有蛋白质的细胞提取物,或者随机或定向消化的蛋白质性质的细胞提取物。这样,可以制备原核蛋白和真核蛋白的文库用于本发明方法的筛选。在一些实施方案中,文库由例如细菌、真菌、病毒和哺乳动物蛋白质构成。
在另一个实施方案中,候选生物活性剂是约5~约30个氨基酸、约5~约20个氨基酸或约7~约15个氨基酸的肽。所述肽可以是如上所述的天然存在的蛋白质的消化物、随机肽或“有偏(biased)”随机肽。
在一个实施方案中,候选生物活性剂是核酸。正如对于蛋白质的一般描述中所述,核酸候选生物活性剂可以是天然存在的核酸、随机核酸或“有偏”随机核酸。在另一个实施方案中,候选生物活性剂是有机化学部分,在文献中可获得大量的候选生物活性剂。
在进行测定期间或之后,对数据进行分析以确定表达水平和状态之间各个基因表达水平的变化,以形成基因表达谱。
在一个实施方案中,对于诊断和预测应用,在任一种状态中鉴定出差异表达基因或突变基因时,可以进行筛选以检测各种BD基因表达的变化。也就是说,可以对单一基因表达调控的调节进行筛选。因此,例如,在两种状态之间靶基因的存在或不存在是唯一的情况下,对靶基因表达的调节剂进行筛选。在一个实施方案中,候选生物活性剂是经标记的。将候选生物活性剂或竞争剂或两者先加到蛋白质(如存在的话)中达足够的时间使之结合。孵育可以在有利于最佳活性的任何温度下进行,温度通常介于4℃和40℃之间。选择适于最佳活性的孵育期,但是也可使之最优化以利于快速的高通量筛选。通常在0.1小时和1小时之间便足够。一般除去或洗去过量的试剂。然后加入第二组分,根据标记组分的存在或不存在来说明结合。
在一个实施方案中,首先加入竞争剂,接着加入候选生物活性剂。竞争剂的置换表明候选生物活性剂与BD蛋白结合,因此能够结合BD蛋白并可能调节BD蛋白的活性。在该实施方案中,任一种组分都可以是标记的。因此,例如,如果竞争剂是标记的,洗涤溶液中标记的存在则表明被活性剂置换。或者,如果候选生物活性剂是标记的,支持体上标记的存在则表明置换。
在一个替代性实施方案中,先加入候选生物活性剂,孵育并洗涤,接着加入竞争剂。由竞争剂所引起的结合不存在可表明生物活性剂以较高亲和力与BD蛋白结合。因此,如果候选生物活性剂是标记的,支持体上标记的存在,同缺乏竞争剂结合联系起来,可表明候选活性剂能够与BD蛋白结合。
在一个实施方案中,所述方法包括示差筛选以鉴定(identity)能够调节BD蛋白活性的生物活性剂。在该实施方案中,所述方法包括在第一样品中将BD蛋白和竞争剂混合。第二样品包含候选生物活性剂、BD蛋白和竞争剂。测定两种样品中竞争剂的结合,两种样品之间结合的变化或差异表明存在能够结合BD蛋白和可能调节其活性的活性剂。也就是说,如果与第一样品相比,在第二样品中竞争剂的结合有所不同,则活性剂能够与BD蛋白结合。
还可对调节BD蛋白活性的活性剂进行筛选。在一个实施方案中,用于筛选能够调节BD蛋白活性的生物活性剂的方法包含将候选生物活性剂加到上述BD蛋白的样品中,并测定BD蛋白的生物活性的变化的步骤。“调节BD蛋白活性”包括活性的提高、活性的降低或存在的活性类型或种类的变化。因此,在该实施方案中,候选活性剂应与BD蛋白结合(虽然这可并非是必需的),并如本文所述改变其生物活性或生化活性。所述方法包括如上文中所概述的体外筛选方法,以及体内筛选在BD蛋白的存在、分布、活性或量方面发生变化的细胞。
因此,在该实施方案中,所述方法包括将BD样品和候选生物活性剂混合,并评价对BD活性的作用。所谓“BD活性”或本文语法上的等同术语是指BD蛋白的生物活性之一,包括但不限于其在BD中的作用。
在一个实施方案中,BD蛋白的活性提高;在另一个实施方案中,BD蛋白的活性降低。因此,在一些实施方案中,生物活性剂是拮抗剂,在其它实施方案中,生物活性剂是激动剂。
应用
在一个实施方案中,提供抑制BD的方法。在另一个实施方案中,提供改善BD的方法。在又一个实施方案中,提供治疗具有BD的细胞或患有BD的个体的方法。
所述方法包括给予BD抑制剂。在具体的实施方案中,BD抑制剂为反义分子、药物组合物、治疗剂或小分子、单克隆抗体、多克隆抗体、嵌合抗体或人源化抗体。在具体的实施方案中,治疗剂与抗体、优选单克隆抗体偶联。在具体的实施方案中,BD抑制剂为PXR激活物,例如利福霉素类似物。利福霉素类似物包括例如利福昔明和利福霉素。
在其它实施方案中,提供用于检测或诊断受治疗者的BD细胞的方法。在具体的实施方案中,诊断剂/检测剂是优先结合本发明BDP的小分子。在一个实施方案中,诊断剂/检测剂是抗体,例如任选与可检测试剂连接的单克隆抗体。
在本发明的其它实施方案中,提供动物模型和转基因动物,用于产生BD动物模型。
反义分子(antisense)、核酶和抗体
可用作治疗药的其它物质包括PXR基因、其表达产物及其功能片段。此外,降低或抑制突变型PXR基因活性的物质可用来改善疾病症状。这类物质包括反义分子、核酶和三股螺旋分子。本领域技术人员熟知用于产生和使用这类分子的技术。
核酶是能够催化RNA特异性切割的具有酶特性的RNA分子。核酶的作用机制涉及核酶分子与互补靶RNA的序列特异性杂交,接着进行内核降解切割。核酶分子的组成必须包括一种或多种与PXR基因mRNA互补的序列,并且必需包括众所周知的负责mRNA切割的催化序列。有关该序列可参见美国专利第5,093,246号,所述专利通过引用其全部结合到本文中。因此属于本公开内容的范围的有工程改造的锤头状基序核酶分子,它特异性并有效地催化编码PXR基因蛋白的RNA序列的内核降解切割。
通过仔细研究包括下列序列GUA、GUU和GUC在内的核酶切割位点的目标分子,初步鉴定出任何可能的RNA靶标内的特异性核酶切割位点。一经鉴定,便可以评价介于15个和20个核糖核苷酸之间的短RNA序列(相当于含有切割位点的PXR基因的区域)的预计结构特征,例如可能提供不适当的寡核苷酸序列的二级结构。应用核糖核酸酶保护实验,通过测定候选序列与互补寡核苷酸杂交的可及性,可以评价候选序列的适合性。
用于三股螺旋形成以抑制转录的核酸分子应为单链,并由脱氧核糖核苷酸组成。必需通过Hoogsteen碱基配对法则,设计这些寡核苷酸的碱基组成以促使三股螺旋形成,这一般需要相当大的嘌呤或嘧啶序列段存在于双螺旋的一条上。核苷酸序列可以是基于嘧啶的,这将导致跨过所得到的三股螺旋的3条缔合链的TAT和CGC三联体。富含嘧啶的分子提供与双螺旋单条链的富含嘌呤区互补的碱基,其取向与所述链平行。另外,可以选择富含嘌呤的核酸分子,例如含有一段G残基。这些分子将与富含GC对的DNA双螺旋形成三股螺旋,其中大量的嘌呤残基定位于靶定的双螺旋的一条链上,导致GGC三联体跨过三螺旋的3条链。
或者,可通过产生所谓的“Z型转向(switchback)”核酸分子来增加可以靶定用于三股螺旋形成的可能序列。Z型转向分子以交替的5′-3′、3′-5′方式合成,使得与双螺旋的第一条链进行碱基配对,然后与另一条链进行碱基配对,消除了一条双螺旋上存在相当大的嘌呤或嘧啶序列段的必要性。
有可能的是,本文所述的反义分子、核酶和/或三股螺旋分子可降低或抑制通过正常和突变型PXR基因等位基因产生的mRNA的转录(三股螺旋)和/或翻译(反义分子、核酶)。为了确保维持基本正常的PXR基因活性水平,可将编码和表达具有正常活性的PXR基因多肽的核酸分子导入细胞,所述细胞不含对不论是所要利用的反义分子、核酶还是三股螺旋治疗敏感的序列。或者,可优选将正常的PXR基因蛋白共同给予细胞或组织以维持细胞或组织PXR基因活性所必需的水平。
本公开内容的反义RNA和DNA、核酶和三股螺旋分子可通过本领域已知的用于合成DNA和RNA分子的任何方法制备。这些包括本领域众所周知的用于化学合成寡脱氧核糖核苷酸和寡核糖核苷酸的技术,例如固相亚磷酰胺化学合成法。或者,RNA分子可通过编码反义RNA分子的DNA序列的体外和体内转录来形成。可将这类DNA序列整合到多种整合了合适的RNA聚合酶启动子(例如T7或SP6聚合酶启动子)的载体中。或者,可将经组成型或诱导型(取决于所使用的启动子)合成的反义RNA的反义cDNA构建体稳定导入细胞系中。
可将各种熟知的修饰引入DNA分子中作为提高胞内稳定性和半寿期的手段。可能的修饰包括但不限于将核糖核苷酸或脱氧核糖核苷酸的旁侧序列加到分子的5′端和/或3′端,或者使用硫代磷酸酯或2′O-甲基而不是寡脱氧核糖核苷酸主链内磷酸二酯酶键。
对PXR基因蛋白、特别是突变型基因蛋白有特异性,并干扰其活性的抗体可用来抑制突变型PXR基因功能。应用本领域的标准技术以及按照本文所述方法,可以针对蛋白质本身或针对相当于所述蛋白质的部分的肽,来形成这类抗体。这类抗体包括但不限于多克隆抗体、单克隆抗体、Fab片段、单链抗体、嵌合抗体等。
在其中PXR基因蛋白是胞内的,并且使用完整抗体的情况下,使抗体内化将是确定的。然而,可以使用脂质转染试剂脂质体递送抗体或与PXR基因表位结合的Fab区的片段进入细胞。当使用抗体片段时,结合靶标的最小抑制片段或延伸的靶蛋白的结合结构域是确定的。例如,可以使用具有相当于与PXR基因蛋白结合的抗体可变区结构域的氨基酸序列的肽。可以应用本领域众所周知的方法(参见例如Creighton,Structures and Molecular Principles(1984)W.H.Freeman,New York 1983,同上;以及Sambrook等,1989,同上),用化学方法合成或用重组DNA技术产生这类肽。或者,还可以给予与胞内PXR基因表位结合的单链中和抗体。可通过利用例如文献中披露的技术(例如Marasco等,Proc.Natl.Acad.Sci.USA,90:7889-93(1993)),通过例如在靶细胞群内表达编码单链抗体的核苷酸序列,来给予这类单链抗体。
可以浓度足以产生使疾病症状得到改善的PXR基因蛋白的水平,将编码PXR基因蛋白的RNA序列直接给予患有疾病症状的受治疗者。可通过基因置换疗法对受治疗者进行治疗。除将DNA导入细胞的其它颗粒(例如脂质体)以外,还可使用载体将一个或多个拷贝的正常PXR基因或具有PXR基因功能指导产生正常PXR基因蛋白的基因部分插入细胞中,载体包括但不限于腺病毒、腺伴随病毒和反转录病毒载体。此外,可以应用有关技术(例如上面所述技术)将正常PXR基因序列导入人细胞中。
然后可将含有表达正常PXR基因的基因序列的细胞,优选自体细胞引入或再引入供改善疾病症状的位置。
反义RNA和DNA分子通过与靶定的mRNA杂交并阻止蛋白质翻译,起着直接阻断mRNA翻译的作用。对于反义DNA这种从翻译起始位点衍生的寡脱氧核糖核苷酸(例如目标PXR基因核苷酸序列-10和+10间的区域)是确定的。
在一个实施方案中,BD抑制剂或激活物是反义分子,例如PXR激活物。本文所使用的反义分子包括反义或有义寡核苷酸,所述寡核苷酸包含能够结合BD分子的靶mRNA(有义)或靶DNA(反义)序列的单链核酸序列(RNA或DNA)。本发明的反义或有义寡核苷酸,包含一般为至少约14个核苷酸、优选约14-30个核苷酸的片段。基于编码指定蛋白质的cDNA序列,驱动反义或有义寡核苷酸的能力可参见例如Stein和Cohen,Cancer Res.48:2659,(1988)以及van der Krol等,BioTechniques 6:958,(1988)。
反义分子可以是修饰或未修饰的RNA、DNA或混合多聚体寡核苷酸。这些分子通过与匹配序列特异性结合,通过空间阻断或通过激活RNA酶H酶导致肽合成受抑制而起作用(Wu-Pong,1994年11月,BioPharm,20-33)。反义分子还可通过干扰RNA加工或由核转运到胞质,来改变蛋白质合成(Mukhopadhyay和Roth,1996,Crit.Rev.inOncogenesis 7,151-190)。另外,单链DNA与RNA的结合可导致核酸酶介导的异源双链体降解(Wu-Pong,同上)。迄今显示用作RNA酶H的底物、主链被修饰的DNA化学结构为硫代磷酸酯、二硫代磷酸酯、三氟硼酸酯(borontrifluoridates)及含有2′阿糖寡核苷酸和2′-氟代阿糖的寡核苷酸。
RNA干扰是指例如在动物中由短干扰RNA(siRNA)介导的序列特异性转录后基因沉默的过程(Fire等,Nature,391,806(1998))。植物中相应的过程称为转录后基因沉默或RNA沉默,在真菌中亦称压抑(quelling)。细胞中dsRNA的存在通过尚未充分表征的机制引发RNAi反应。这种机制似乎不同于干扰素反应,所述反应是由dsRNA介导的蛋白激酶PKR和导致由核糖核酸酶L对mRNA非特异性切割的2′,5′-寡腺苷酸合成酶的活化引起的(有关综述参见Sharp,P.A.,RNA interference--2001,Genes&Development 15:485-490(2001))。
本文提供包含分离核酸分子的表达系统,所述核酸分子包含能够与BD序列特异性杂交的序列。在一个实施方案中,所述核酸分子能够抑制BD蛋白的表达。本发明提供通过短RNA的载体定向表达抑制细胞内BD表达的一种方法,所述短RNA本身可折叠并产生具有BD mRNA序列同一性的双链RNA,且能够在细胞内引发BD基因的转录后基因沉默即RNA干扰(RNAi)。在另一种方法中,将具有BDmRNA序列同一性的短的双链RNA递送到细胞内以引发BD基因的转录后基因沉默即RNAi。在各种实施方案中,核酸分子为至少7聚体,至少10聚体,或至少20聚体。在又一个实施方案中,所述序列唯一的。
药物组合物
本文提供的药物组合物包括治疗有效量的本文所公开的小分子多肽、多核苷酸、反义寡核苷酸或抗体作为活性剂。“有效量”是足以引起有益结果或所需结果(包括临床结果)的量。可以一种或多种给药法给予有效量。对于本发明来说,腺病毒载体的有效量是足以减轻、改善、稳定、逆转、减慢或延迟疾病状况的进程的量。
所述组合物可用来治疗BD。本文所使用的术语“治疗”等一般是指获得所需要的药学作用和/或生理作用。该作用从完全或部分预防疾病或其症状来看可以是预防性的和/或从部分或完全稳定或治愈疾病和/或归因于该疾病的不良作用来看可以是治疗性的。本文所使用的“治疗”包括哺乳动物特别是人的疾病的任何治疗,并包括:(a)防止可能易患疾病或症状但还未诊断患有该疾病或症状的受治疗者发生疾病或症状;(b)抑制疾病症状,例如阻止其发展;或(c)缓解疾病症状,例如引起疾病或症状消退。
对本发明来说,“受治疗者”包括人和其它动物,特别是哺乳动物,以及生物体。因此,所述方法适用于人类疗法和兽医应用。在某些实施方案中,受治疗者是哺乳动物,在大多数确定的实施方案中,受治疗者是人。
本文所使用的术语“治疗有效量”是指例如治疗、改善或预防需要治疗的疾病或病症,或具有可检测的治疗或预防效果的治疗剂的量。可通过例如化学标记或抗原水平检测效果。治疗效果还包括生理症状的减轻,例如体温降低。用于受治疗者的确切的有效量将取决于受治疗者的尺寸和健康状况、病症的性质和程度、以及选用于给药的治疗药或治疗药的组合。给定情况下的有效量由常规实验方法确定,并由临床医生予以判断。从本发明来看,给予个体的本发明组合物的有效剂量一般为约0.01mg/kg~约5mg/kg、或约0.01mg/kg~约50mg/kg或约0.05mg/kg~约10mg/kg或约0.1m/kg~约100mg/kg。
药物组合物还可含有药物可接受的载体。术语“药物可接受的载体”是指例如用于给予治疗剂(例如抗体或多肽、基因和其它治疗剂)的载体。该术语是指例如任何药用载体本身不会诱导产生对接受组合物的个体是有害的抗体,并且可以给予而无过度毒性。合适的载体可以是大的缓慢代谢的大分子,例如蛋白质、多糖、聚乙酸(polylaceticacid)、聚乙醇酸、聚合氨基酸、氨基酸共聚物和无活性的病毒颗粒。这类载体是本领域普通技术人员熟知的。治疗组合物中药物可接受的载体可包括液体,例如水、盐水、甘油和乙醇。辅助物质,例如润湿剂或乳化剂、pH缓冲物质等,也可存在于这类溶媒中。治疗组合物通常被制成作为液体溶液剂或混悬剂的注射剂;还可制成固体形式,适于在注射之前混于液体溶媒的溶液剂或混悬剂。脂质体包括在药物可接受的载体的定义内。药物可接受的盐也可存在于药物组合物中,例如无机酸盐,例如盐酸盐、氢溴酸盐、磷酸盐、硫酸盐等;以及有机酸的盐,例如乙酸盐、丙酸盐、丙二酸盐、苯甲酸盐等。有关药物可接受的赋形剂的全面论述可参见Remington:The Science andPractice of Pharmacy(1995)Alfonso Gennaro,Lippincott,Williams,&Wilkins。
可以各种形式制备药物组合物,例如颗粒剂、片剂、丸剂、栓剂、胶囊剂、混悬剂、软膏剂、洗剂等。可以采用适于口服和局部用途的药用级有机或无机载体和/或稀释剂配制含有有治疗活性的化合物的组合物。本领域已知的稀释剂包括水性介质、植物油及动物油和脂肪。稳定剂、润湿剂和乳化剂、用于改变渗透压的盐或用于确保适当pH值的缓冲剂和皮肤渗透促进剂可以用作助剂。
本发明的药物组合物包含适于给予受治疗者的某一形式的BD蛋白。在某些实施方案中,所述药物组合物是水溶性形式,例如作为药物可接受的盐存在,这就意味着同时包括酸加成盐和碱加成盐。“药物可接受的酸加成盐”是指例如保持游离碱基的生物功效以及不是生物学上不良或其它方面不良的与以下无机酸和有机酸形成的盐:无机酸例如盐酸、氢溴酸、硫酸、硝酸、磷酸等,有机酸例如乙酸、丙酸、乙醇酸、丙酮酸、草酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、柠檬酸、苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、对甲苯磺酸、水杨酸等。“药物可接受的碱加成盐”包括由无机碱衍生的盐,例如钠盐、钾盐、锂盐、铵盐、钙盐、镁盐、铁盐、锌盐、铜盐、锰盐、铝盐等。特别确定的是铵盐、钾盐、钠盐、钙盐和镁盐。衍生自药物可接受的有机无毒碱的盐包括伯胺、仲胺和叔胺、取代胺(包括天然存在的取代胺)、环胺的盐和碱性离子交换树脂,例如异丙胺、三甲胺、二乙胺、三乙胺、三丙胺和乙醇胺的盐。
本发明的治疗性多核苷酸和多肽可使用基因递送溶媒递送。基因递送溶媒可以是病毒来源或非病毒来源(一般参见Jolly,BD GeneTherapy(1994)1:51;Kimura,Human Gene Therapy(1994)5:845;Connelly,Human Gene Therapy(1995)1:185;以及Kaplitt,NatureGenetics(1994)6:148)。可以采用内源哺乳动物启动子或异源启动子诱导这类编码序列的表达。编码序列的表达可以是组成型或调节型。
本发明的BD蛋白和调节剂的给药可按上述各种方法进行,包括但不限于口服、皮下、静脉内、鼻内、经皮、腹膜内、肌内、经肺、阴道、直肠或眼内。在一些情况下,例如在创伤和炎症的治疗中,BD蛋白和调节剂可以直接用作溶液剂或喷雾剂。
在一个实施方案中,提供调节细胞或生物体中的BD基因活性的方法。在一个实施方案中,所述方法包括给予细胞降低或消除内源BD蛋白的生物活性的抗BD抗体。或者,所述方法包括给予细胞或生物体编码BD蛋白的重组核酸。正如本领域技术人员应了解的一样,这可以用多种方法来完成。在一个实施方案中,例如当BD序列在BD中下调时,通过增加BD在细胞中的表达来增加BD基因产物的活性,例如采用已知的基因疗法技术,通过内源BD基因过量表达或者通过给予BD序列的编码基因。在一个实施方案中,基因疗法技术包括利用增强型同源重组(enhanced homologous recombination,EHR)掺入外源基因,例如参见PCT/US93/03868(特此通过引用其全部予以结合)。或者,例如当BD序列在BD中上调时,例如通过给予BD反义核酸,降低内源BD基因的活性。
可以提供所述检测方法作为试剂盒的组成部分。因此,本发明另外提供试剂盒,用于在生物样品中,检测BD细胞中差异表达的多核苷酸(例如通过检测由差异表达的目标基因编码的mRNA)和/或由其编码的多肽的存在和/或水平。使用这些试剂盒的方法步骤可通过临床实验室、实验室、开业医生或私营个体进行。用于检测由在BD细胞中差异表达的多核苷酸编码的多肽的本发明试剂盒可包括特异性结合多肽的部分,其可以是结合多肽或其片段的抗体。用于检测在BD细胞中差异表达的多核苷酸的本发明试剂盒可包括与这类多核苷酸特异性杂交的部分。试剂盒可任选提供可用于所述方法步骤的其它组分,包括但不限于缓冲剂、显影剂、标记、反应表面、检测方法、对照样品、标准品、说明书和说明资料。因此,本发明提供用于检测前列腺BD的试剂盒,所述试剂盒包含至少一种如以下NCBI登录号所示序列的多核苷酸或其片段:NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133。
可将经鉴定出的抑制靶突变型基因表达、合成和/或活性的化合物以治疗或改善疾病的治疗有效剂量给予受治疗者。治疗有效剂量是指例如足以引起疾病症状得到改善的化合物的量。
可以通过标准药学规程,在细胞培养或实验动物中测定这类化合物的毒性和治疗功效,例如,测定LD50(50%群体的致死剂量)和ED50(50%群体中治疗有效的剂量)。毒性作用与治疗效果之间的剂量比为治疗指数,它可以用比率LD50/ED50表示。治疗指数大的化合物是确定的。虽然可以使用具有毒副作用的化合物,但是要注意应设计使这类化合物靶向受累组织部位的递送系统,以使对未被感染细胞的损害最小化,从而降低副作用。
可以利用从细胞培养实验和动物研究获得的数据配制一系列剂量用于人体。这类化合物的剂量优选介于包括ED50在内的循环浓度范围内,几乎没有毒性或者没有毒性。剂量可以在这个范围内变化,这取决于所采用的剂型和所利用的给药途径。对于用于本公开内容的方法中的任何化合物,最初可从细胞培养实验中估计治疗有效剂量。可在动物模型中配制某一剂量以达到包括在细胞培养物中测定的IC50在内的循环血浆浓度范围(例如达到症状最大抑制一半的试验化合物的浓度)。可以利用这类信息,更准确地确定人体中的有益剂量。可通过例如高效液相层析法测定血浆中的水平。
用于本公开内容的药物组合物可按常规方式使用一种或多种生理上可接受的载体或赋形剂配制。因此,可以配制化合物及其生理上可接受的盐和溶剂化物用于通过以下方式给药:吸入或吹入(经口或经鼻)或口服、口腔、胃肠外、局部、皮下、腹膜内、静脉内、胸膜内、眼内、动脉内或直肠给药。还预期药物组合物可与增强所述化合物的活性的其它产品一起给予,任选可包括其它治疗成分。
对于口服给药,药物组合物可呈例如通过常规方法与以下药物可接受的赋形剂一起制备的片剂或胶囊剂的形式:例如粘合剂(例如预胶化玉米淀粉、聚乙烯吡咯烷酮或羟丙基甲基纤维素);填充剂(例如乳糖、微晶纤维素或磷酸氢钙);润滑剂(例如硬脂酸镁、滑石粉或硅石);崩解剂(例如马铃薯淀粉或羟基乙酸淀粉钠);或润湿剂(例如十二烷基硫酸钠)。片剂可通过本领域众所周知的方法包衣。口服给药的液体制剂可呈例如溶液剂、糖浆剂或混悬剂的形式,或者可以干制品提供,用前与水或其它合适的溶媒配制。这类液体制剂可通过常规方法与以下药物可接受的添加剂一起制备:例如悬浮剂(例如山梨醇糖浆、纤维素衍生物或氢化食用脂肪);乳化剂(例如卵磷脂或阿拉伯树胶);无水溶媒(例如杏仁油、油性酯、乙醇或分级植物油)和防腐剂(例如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯或山梨酸)。适当时制剂还可含有缓冲盐、矫味剂、着色剂和甜味剂。可适当地配制口服给药的制剂以得到控释的活性化合物。对于口腔给药,组合物可呈以常规方式配制的片剂或糖锭剂的形式。
对于吸入给药,用于本公开内容的化合物可用合适的抛射剂从加压包装或雾化吸入器发出喷雾剂的形式方便地递送,所述抛射剂例如二氯二氟甲烷、三氯氟甲烷、二氯四氟乙烷、二氧化碳或其它合适的气体。在加压气雾剂的情况下,可通过提供递送定量的阀,来确定剂量单位。用于吸入器或吹入器的例如明胶的胶囊和药筒可制成装有化合物和合适粉末基料(例如乳糖或淀粉)的粉末混合物。
可以配制化合物用于通过注射(例如通过推注或连续输注)的胃肠外给药。用于注射的剂型可呈单位剂型,例如装入具有添加防腐剂的安瓿或多次剂量容器中。组合物可呈诸如油性或水性溶媒中的混悬剂、溶液剂或乳剂的这类形式,并且可含有调配剂(formulatory agent),例如悬浮剂、稳定剂和/或分散剂。或者,活性成分可呈粉剂形式,用前用合适的溶媒(例如无菌无热原水)配制。
还可将化合物配制成例如含有常规栓剂基料(例如可可脂或其它甘油酯)的直肠组合物,例如栓剂或滞留型灌肠剂。口服法可能是服用任何药物最简单的方法。这类给药途径从受治疗者的观点来看一般简单易用并且常常是不便或不适最少的给药途径。然而,这包括使药物材料通过胃,这对于包括蛋白质和其它生物活性组合物在内的许多物质来说是不利的环境。由于胃的酸性、水解和蛋白水解环境进化成将蛋白质性质的物质有效地消化成为氨基酸和寡肽用于后续的合成代谢,因此,如果只是口服用药时,不难预料,多种有生物活性的蛋白质性质的物质在经过胃以后极少或没有可能存在并在小肠中被机体吸收。结果是许多蛋白质性质的药物必需通过其它方法摄取,例如经胃肠外,常常通过皮下、肌内或静脉内注射。
为了稳定药物活性,药物组合物还可包括各种缓冲剂(例如Tris、乙酸盐、磷酸盐)、稳定剂(例如吐温、聚山梨酯)、载体(例如人血清白蛋白)、防腐剂(硫柳汞、苯甲醇)和抗氧化剂(例如抗坏血酸)。稳定剂可以是洗涤剂,例如吐温-20、吐温-80、NP-40或曲通X-100。还可将EBP掺入聚合物的粉粒制剂中以在延长的一段时间内有控制地递送给受治疗者。有关药物组合物中各组分的更多论述可参见Remington′sPharmaceutical Sciences,第18版,A.R.Gennaro,主编,MackPublishing,Easton,Pa.(1990)。
除了前述剂型外,也可将化合物制成贮库制剂。这类长效剂型通过植入(例如皮下或肌内)或通过肌内注射给予。因此,例如化合物可与合适的聚合材料或疏水材料(例如作为可接受的油中的乳剂)或离子交换树脂一起配制,或者作为微溶衍生物,例如作为微溶盐。
如有需要,可以在装有一个或多个含有活性成分的单位剂型的小包或分配器中提供组合物。小包可包括例如金属或塑料箔,例如泡罩包装。小包或分配器可随附用药说明书。
孕烷X受体(PXR)
用于本发明的细胞包括真核细胞和原核细胞,包括但不限于细菌细胞、酵母细胞、真菌细胞、昆虫细胞、线虫细胞、植物细胞和动物细胞。合适的动物细胞包括但不限于BDK细胞、HeLa细胞、COS细胞、U20S细胞、CHO-KI细胞和各种哺乳动物原代细胞。
用于本发明的细胞包括表达PXR、未知PXR、修饰PXR的细胞及其组合。表达PXR的细胞在其细胞膜上含有PXR作为功能受体的细胞。细胞可以天然地表达PXR,可以经遗传工程改造以在不同的表达水平上表达PXR,或者可经遗传工程改造以诱导型地表达PXR。正如本领域技术人员容易理解的一样,可以通过遗传工程领域的分子生物学技术标准,对细胞进行遗传工程改造以表达PXR。
另外,用于本发明的细胞可以稳定或瞬时表达用于本文所述方法PXR。本发明的方法可以采用使用以下专利中所描述的非哺乳动物病毒(例如杆状病毒)表达基因的方法:美国专利第4,745,051、4,879,236、5,348,886、5,731,182、5,871,986、6,281,009和6,238,914号。美国专利第4,745,051、4,879,236、5,348,886、5,731,182、5,871,986、6,281,009和6,238,914号的全部内容特此通过引用其全部予以结合。与本发明的方法一起使用的检测方法还可参见美国专利申请顺序号10/095,620、美国专利第5,891,646号和美国专利第6,110,693号,其内容特此通过引用其全部予以结合。
动物模型和转基因动物
在另一个实施方案中,BD基因应用于产生BD的动物模型。正如本领域普通技术人员所了解的一样,当所鉴定的BD基因在BD组织中受抑制或减少时,其中反义RNA针对BD基因的基因疗法技术也将减少或抑制该基因的表达。由此产生的动物用作用于筛选候选生物活性药物的BD动物模型。同样,基因敲除技术,例如由于与适当的基因寻靶载体进行同源重组的结果,将导致缺乏BD蛋白。需要时,BD蛋白的组织特异性表达或敲除可能是必要的。
还有可能的是,在BD中BD蛋白过量表达。因此,可以产生过量表达BD蛋白的转基因动物。根据所需要的表达水平,可以利用各种强度的启动子以表达转基因。同样,可以测定经整合的转基因的拷贝数并进行比较,以确定转基因的表达水平。通过这类方法产生的动物可用作BD的动物模型,此外还可用于筛选治疗BD的生物活性分子。
寻靶构建体的产生
本公开内容的寻靶构建体可采用本领域已知的标准方法产生(参见例如Sambrook等,1989,Molecular Cloning:A Laboratory Manual,第二版,Cold Spring Harbor Laboratory Press,Cold Spring Harbor,N.Y.;E.N.Glover(编著),1985,DNA Cloning:A Practical Approach,第I和II卷;M.J.Gait(编著),1984,Oligonucleotide Synthesis;B.D.Hames和S.J.Higgins(编著),1985,Nucleic Acid Hybridization;B.D.Hames和S.J.Higgins(编著),1984,Transcription and Translation;R.I.Freshney(编著),1986,Animal Cell Culture;Immobilized Cells andEnzymes,IRL Press,1986;B.Perbal,1984,Practical Guide To Molecular克隆;F.M.Ausubel等,1994,Current Protocols in Molecular Biology,John Wiley和Sons,Inc.)。例如,寻靶构建体可以按照常规方法制备,其中序列可以合成、从天然来源分离、操纵、克隆、连接、进行体外诱变、引物修复等。在不同阶段,连接的序列可以进行克隆,并通过限制性分析、测序等进行分析。
可以应用本领域众所周知的技术构建寻靶DNA。例如,可通过寡核苷酸的化学合成、双链DNA模板的切口平移、序列的聚合酶链式扩增(或连接酶链式反应扩增)、带有目标序列(例如克隆cDNA或基因组DNA、合成DNA或上述组合的任一种)的原核载体或靶克隆载体的纯化来合成寻靶DNA,所述载体例如质粒、噬菌粒、YAC、黏粒、噬菌体DNA、其它病毒DNA或复制中间体、或其纯化的限制片段、以及具有所需核苷酸序列的单链和双链多核苷酸的其它来源。此外,可应用本领域已知的方法选择同源性的长度。例如,选择可以序列组成和预定的内源靶DNA序列的复杂性为基础。
在本公开内容的一个实施方案中,采用2004年11月9日授予专利权的美国专利第6,815,185号(其公开内容通过引用其全部结合到本文)中所描述的方法,直接由质粒基因组文库制备寻靶构建体,美国专利第6,815,185号以2001年6月19日申请的美国专利申请顺序号09/885,816为基础,美国专利申请顺序号09/885,816是1998年11月17日申请、现已放弃的美国专利申请顺序号09/193,834的继续申请,美国专利申请顺序号09/193,834要求1998年5月11日申请的临时申请号60/084,949、临时申请号60/084,194以及1997年11月17日申请的已转为临时申请号60/084,194的美国专利申请顺序号08/971,310的权益。一般来讲,应用例如长片段PCR,在单一步骤中从质粒文库鉴定和分离目标序列。分离出该序列之后,可容易地将可破坏靶序列的第二多核苷酸插入编码目标序列的两个区域之间。按照这个方面,构建体以两个步骤产生:(1)扩增(例如使用长片段PCR)与靶序列同源的序列,和(2)将另一多核苷酸(例如选择标记)插入PCR产物中使得它的两侧是同源序列。通常,载体是得自质粒基因组文库的质粒。完成的构建体也通常是环状质粒。
在另一个实施方案中,按照对2001年9月17日申请的美国专利申请顺序号09/954,483,现为已公布的美国专利公布号20030032175(其公开内容通过引用其全部结合到本文中)所描述的阳性选择方法进行的调整,设计寻靶构建体。将寻靶构建体设计成包括具有定位于PGK启动子上的两个lacO位点的PGK-neo融合基因,以及包含lac阻抑蛋白的NLS-lacI基因,所述lac阻抑蛋白与编码得自SV40T抗原的NLS的序列融合。在另一个实施方案中,寻靶构建体还含有一个以上的选择标记基因,包括阴性选择标记,例如单纯疱疹病毒tk(HSV-tk)基因。阴性选择标记可与启动子和聚腺苷酸化信号有效连接。(参见例如美国专利第5,464,764、5,487,992、5,627,059号;以及美国专利第5,631,153号)。
一旦制成合适的寻靶构建体,则可应用本领域已知的任何方法,将寻靶构建体导入合适的宿主细胞中。本公开内容可应用各种技术,包括例如前核显微注射、反转录病毒介导的基因转移至种系、胚胎干细胞中的基因打靶、胚胎的电穿孔、精子介导的基因转移、磷酸钙/DNA共沉淀、将DNA显微注射入核中、细菌原生质体与完整细胞融合、转染、聚阳离子(例如多聚季铵盐、polyomithine)等(参见例如美国专利第4,873,191号;Van der Putten等,1985,Proc.Natl.Acad.Sci.,USA82:6148-6152;Thompson等,1989,Cell56:313-321;Lo,1983,MolCell.Biol.3:1803-1814;Lavitrano等,1989,Cell,57:717-723)。本领域已知转化哺乳动物细胞的各种技术(参见例如Gordon,1989,Intl.Rev.Cytol.,115:171-229;Keown等,1989,Methods in Enzymology;Keown等,1990,Methods and Enzymology,第185卷,第527-537页;Mansour等,1988,Nature,336:348-352)。
然后将选出的细胞注入动物(例如小鼠)的胚泡(或发育的其它阶段以适于产生可生长发育的动物,例如桑葚胚)中以形成嵌合体(参见例如Bradley,A.Teratocarcinomas and Embryonic Stem Cells:APractical Approach,E.J.Robertson,编著,IRL,Oxford,第113-152页(1987))。或者,可使选出的ES细胞与解离的小鼠胚胎细胞聚集形成聚集嵌合体。然后将嵌合胚胎植入合适的假孕雌性代孕动物内,使胚胎达到足孕。可使用在其生殖细胞中具有同源重组DNA的嵌合子代来繁殖动物,其中动物的所有细胞都含有同源重组DNA。在一个实施方案中,使用嵌合子代小鼠产生PXR基因中具有杂合破坏(heterozygous disruption)的小鼠。然后使杂合转基因小鼠交配。本领域众所周知的是,通常这类交配的1/4后代在PXR基因中可具有纯合破坏。
在一个实施方案中,将与PXR基因的破坏有关的表型(或表型改变)接入或存储在数据库中。优选数据库包括:(i)基因型数据(例如被破坏基因的鉴定)和(ii)与基因型数据有关的表型数据(例如因基因破坏而产生的表型)。数据库优选为电子数据库。
本公开内容另还提供条件性转基因动物或敲除动物,例如采用重组方法产生的转基因动物或敲除动物。噬菌体Pl Cre重组酶和得自酵母质粒的flp重组酶是在特定靶位点(cre重组酶的lox P位点和flp重组酶的frt位点)切割DNA并催化该DNA与第二切割位点连接的位点特异性DNA重组酶的两个非限制性实例。已经披露了多个合适的替代性位点特异性重组酶,并且其基因可用于本公开内容的方法。这类重组酶包括噬菌体λ的Int重组酶(含有或不含Xis时)(Weisberg,R.等,Lambda II,(Hendrix,R.等编著),Cold Spring Harbor Press,ColdSpring Harbor,N.Y.,第211-50页(1983),通过引用予以结合);TpnI和β-内酰胺酶转座子(Mercier等,J Bacteriol.,172:3745-57(1990));Tn3解离酶(Flanagan和Fennewald J.Molec.Biol.,206:295-304(1989);Stark等,Cell,58:779-90(1989));酵母重组酶(Matsuzaki等,J Bacteriol.,172:610-18(1990));枯草芽孢杆菌(B.subtilis)SpoIVC重组酶(Sato等,J Bacteriol.172:1092-98(1990));Flp重组酶(Schwartz和Sadowski,JMolec.Biol.,205:647-658(1989);Parsons等,J Biol.Chem.,265:4527-33(1990);Golic和Lindquist,Cell,59:499-509(1989);Amin等,J Molec.Biol.,214:55-72(1990));Hin重组酶(Glasgow等,J Biol.Chem.,264:10072-82(1989));免疫球蛋白重组酶(Malynn等,Cell,54:453-460(1988));以及Cin重组酶(Haffter和Bickle,EMBO J,7:3991-3996(1988);Hubner等,J Molec.Biol.,205:493-500(1989)),所有文献都通过引用予以结合。Echols(J Biol.Chem.265:14697-14700(1990));deVillartay(Nature,335:170-74(1988));Craig,(Ann.Rev.Genet.,22:77-105(1988));Poyart-Salmeron等(EMBO J 8:2425-33(1989));Hunger-Bertling等(Mol Cell.Biochem.,92:107-16(1990))以及Cregg和Madden(Mol.Gen.Genet.,219:320-23(1989))论述了这类系统,所有文献都通过引用结合到本文中。Cre已被纯化成均质,且它与loxP位点的反应得到了广泛深入的表征(Abremski和Hess J Mol.Biol.259:1509-14(1984),通过引用结合到本文)。Cre蛋白的分子量为35,000,可购自New England Nuclear/Du Pont公司。已经对cre基因(其编码Cre蛋白)进行了克隆和表达(Abremski等,Cell 32:1301-11(1983),通过引用结合到本文)。Cre蛋白介导两个loxP序列之间的重组(Sternberg等,Cold Spring Harbor Symp.Quant.Biol.45:297-309(1981)),它可存在于相同或不同的DNA分子上。因为loxP位点的内部间隔序列是不对称的,所以两个loxp位点可具有彼此相对的方向性(Hoess和Abremski Proc.Natl.Acad.Sci.U.S.A.81:1026-29(1984))。因此,当位于相同DNA分子中的两个位点是正向重复取向时,Cre将切下两个位点之间的DNA(Abremski等,Cell 32:1301-11(1983))。然而,如果两个位点彼此是反向的,则在重组之后不会切掉它们之间的DNA,而只是简单地反转。因此,具有正向取向的两个loxP位点的环状DNA分子将重组产生两个较小的环,而具有两个反向取向的loxP位点的环状分子只是将loxP位点两侧的DNA序列反转。另外,当靶标存在于不同DNA分子上时,重组酶作用可导致靶位点的远端区发生相互交换。
在一个实施方案中,通过直接显微注射将将经纯化的重组酶供给细胞。在另一个实施方案中,重组酶是从共转染的构建体或载体中表达的,其中所述重组酶基因与功能启动子有效连接。该实施方案另外的方面是组织特异性或诱导型重组酶构建体的用途,所述构建体允许选择重组发生的时间及位置。
本文所述的基于细胞的系统和基于动物的系统可用作疾病的模型。可以利用任何物种的动物来产生疾病动物模型,包括但不限于小鼠、大鼠、兔、豚鼠、猪、微型猪、山羊和非人类灵长类,例如狒狒、猴和黑猩猩。另外,可以使用人的细胞。这些系统可用于各种应用中。可以利用这类实验作为所设计的鉴定药剂的筛选策略的组成部分,所述药剂例如能够改善疾病症状的化合物。因此,可以采用基于动物的模型和基于细胞的模型鉴定在治疗疾病中将是有效的药物、药品、疗法和干预。可以采用基于细胞的系统鉴定可对改善疾病症状起作用的化合物。例如,可将这类细胞系统暴露在疑似具有能力改善疾病症状的化合物中,所述化合物有足够的浓度并且在暴露的细胞中达到足以引起这种疾病症状改善的一段时间。在暴露之后,对细胞进行分析以确定一种或多种疾病细胞表型是否改变而类似于更加正常或更接近野生型的无疾病表型。
另外,可以采用基于动物的疾病系统(例如本文所述的基于动物的疾病系统)鉴定能够改善疾病症状的化合物。这类动物模型可用作试验基体(substrate)以鉴定在治疗动物的疾病或其它表型特征中将是有用的药物、药品、疗法和干预法。例如,可将动物模型暴露于疑似具有能力改善疾病症状的化合物或药剂中,所述化合物或药剂有足够的浓度并且在暴露的动物中达到足以引起这类疾病症状的改善的一段时间。通过评价所述疾病相关病症的逆转,可以监测动物对暴露的反应。暴露可以包括在本文所述的模型动物怀孕期间治疗母体动物,由此将胚胎或胎儿暴露在可预防或改善疾病或表型的化合物或药剂中。也可暴露新生、幼稚和成年动物。
更具体地讲,本发明提供采用本公开内容的动物模型,特别是转基因小鼠,优选以影响至少一个与PXR基因的破坏有关的表型的能力为基础,来鉴定包括化合物在内的药剂的方法。在一个实施方案中,本公开内容提供鉴定对PXR表达或功能具有作用的药剂的方法。所述方法包括例如测量动物对药剂的生理反应,并将这类动物的生理反应与对照动物的生理反应进行比较,其中与对照动物相比,所述动物的生理反应包括PXR的破坏则表明药剂的特异性。“生理反应”是指可以测量的动物的任何生物学参数或生理学参数。分子实验(例如基因转录、蛋白质产生和降解速率)、生理参数(例如运动生理学测验、各种呼吸参数的测量、心率或血压的测量、出血时间的测量、aPTT.T或TT)以及细胞实验(例如细胞表面标记的免疫组织化学测定,或者细胞聚集或增殖的能力)可以用来评价生理反应。本公开内容的转基因动物和细胞可以用作与PXR破坏相关表型有关的疾病、病症或病况的模型。
本公开内容提供独特的动物模型,用于测定和开发新的与BD相关的疗法。BD表型分析可供开发动物模型,所述动物模型可用于测定例如建议的BD药物疗法的功效。
筛选方法
本公开内容可用于筛选活性剂例如激动剂(例如结合并激活PXR多肽的活性剂)或拮抗剂(例如抑制PXR多肽的活性或PXR多肽与其配体相互作用)的方法中。因此,还可以在例如细胞、不含细胞制备物、化学文库和本领域已知的天然产物混合物中,使用本公开内容的多肽评价小分子底物与配体的结合。可以按照本公开内容应用常规用来鉴定和筛选可以调节受体的调节剂的任何方法。
在一个实施方案中,在与利福昔明比较时,在筛选方法中鉴定出的组合物可以至少根据下列5个特征来进行分类:溶解度、吸收、细菌穿透性、RNA聚合酶抑制和/或PXR特异性。这些特征中的每一个可不同于利福昔明在一个或多个这些特征中的性质,还可以是所述特征的任何组合。
·溶解度:例如,在筛选实验中鉴定出来的示例性分子的溶解度将会提高以促进递送至结肠中。如果需要更多被吸收的分子,则溶解度提高和改进对全身吸收也将会是有益的。
·吸收:最好可提高或改进系统抗细菌活性。例如,在筛选实验中鉴定出来的示例性分子的吸收提高。
·细菌穿透性:最好可增加或改进细菌穿透性,这可导致抗细菌活性提高。如果需要最优化抗炎分子来降低细菌穿透性,则这也将是有益的。
·RNA Pol.抑制:最好可提高或改进抗细菌性能,这可用在筛选中选出的化合物的RNA聚合酶活性提高来衡量。如果需要最优化的抗炎分子降低聚合酶抑制活性,则这也将是有益的。
·PXR特异性:最好可提高或改进特异性,如通过结合、活化和/或下游信号转导途径反应所测定的一样。PXR特异性较高的化合物可能较低水平的剂量给予,或者可诱导较大的PXR作用,或者改进抗炎性能。
获益于本公开内容的本领域技术人员应了解,测定在筛选实验中鉴定出来的化合物的5个特征与利福昔明相比较的实验。一旦通过筛选实验鉴定出少数示例性化合物时,所述化合物也可彼此进行比较。
本公开内容提供用于鉴定和筛选调节PXR表达或功能的治疗剂的方法。更具体地讲,含有和表达PXR基因序列的细胞可用来筛选治疗剂。这类细胞可包括非重组单核细胞细胞系,例如U937(ATCC#CRL-1593)、THP-1(ATCC#TIB-202)和P388D1(ATCC#TIB-63);DPX2;内皮细胞例如HUVEC内皮细胞和牛主动脉内皮细胞(BAEC);以及通用哺乳动物细胞系,例如HeLa细胞和COS细胞,例如COS-7(ATCC#CRL-1651)。此外,这类细胞可包括重组的转基因细胞系。例如,本公开内容的转基因小鼠可用来产生细胞系,它含有涉及某一疾病的一种或多种细胞类型可用作该疾病的细胞培养物模型。虽然可以利用衍生自本公开内容的疾病转基因动物的细胞、组织和原代培养物,但是传代细胞系的产生也是确定的。对于可以应用的由转基因动物获得传代细胞系的技术的实例可参见Small等,Mol.Cell Biol.,5:642-48(1985)。
可将PXR基因序列导入目标细胞的基因组,并在其中过量表达。为了过量表达PXR基因序列,可将PXR基因序列的编码部分与能够驱动基因在目标细胞类型中进行表达的调节序列连接。这类调节区是本领域技术人员熟知的,并且可在不存在过多实验的情况下应用。PXR基因序列也可被破坏或表达不足。例如,可以采用存在PXR基因破坏或PXR基因序列表达不足的细胞来筛选药剂,所述药剂能够影响补偿由破坏或表达不足引起的任何功能丧失的替代途径。
可以设计体外系统以鉴定能够结合PXR基因产物的化合物。这类化合物可包括但不限于由D-构型氨基酸和/或L-构型氨基酸制成的肽(例如在随机肽文库的形成中(参见例如Lam等,Nature,354:82-4(1991))、磷酸肽(例如在随机或部分简并序列、定向磷酸肽文库的形成中;参见例如Songyang等,Cell,72:767-78(1993))、抗体和有机小分子或无机分子。例如,已鉴定出来的化合物可用于调节PXR基因蛋白、优选突变型PXR基因蛋白的活性;精心设计PXR基因蛋白的生物功能;或筛选破坏正常PXR基因相互作用或自身破坏这类相互作用的化合物。
例如,用于鉴定结合PXR基因蛋白的化合物的实验包括在足以允许两种组分相互作用和结合的时间和条件下,制备PXR基因蛋白和试验化合物的反应混合物,因此在反应混合物形成可以提取和/或检测的复合物。这些实验以各种方法进行。例如,进行这类实验的一种方法可包括将PXR基因蛋白或试验物质锚定在固相上,并检测在反应结束时锚定在固相上的靶蛋白/试验物质复合物。在这类方法的一个实施方案中,PXR基因蛋白可锚定在固体表面上,可对未被锚定的试验化合物进行直接或间接的标记。
可方便的利用微量滴定板。可通过非共价或共价连接使锚定组分固定化。仅仅将固体表面用蛋白质溶液包被并干燥,就可实现非共价连接。或者,可以采用对蛋白质具有特异性的固定化抗体、优选单克隆抗体,将该蛋白质固定在固体表面上。可提前制备该表面并保存。
为了进行实验,将非固定化组分加到含有锚定组分的包被表面上。在反应完成后,在使所形成的任何复合物保持固体化在表面上的条件下,除去未反应的组分(例如通过洗涤)。可按多种方法完成锚定在固体表面上的复合物的检测。如果之前未固定化的组分是预先标记的,则测出表面上固定化的标记便表明形成了复合物。如果之前未固定化的组分没预先标记,则可以采用间接标记检查锚定在表面上的复合物;例如,使用对之前非固定化组分有特异性的标记抗体(该抗体进而可用标记的抗Ig抗体直接标记或间接标记)。
或者,可以在液相中进行反应,将反应产物与未反应的组分分离开来,并检测复合物;例如,使用对PXR基因产物有特异性的固定化的抗体或锚定溶液中所形成的任何复合物的试验化合物,以及对可能的复合物的另一组分有特异性的标记抗体,以检测锚定的复合物。
可对通过上述方法之一结合特定PXR基因产物的化合物诱导PXR基因蛋白的生化反应的能力进行进一步的测定。可以利用本领域众所周知的测定法来鉴定表达产物的激动剂、拮抗剂和/或抑制剂。
可以利用多种方法诊断PXR基因相关疾病。具体地讲,可以采用例如用于检测PXR基因突变的存在,或检测PXR基因mRNA过量表达或表达不足的试剂。
下列实施例仅旨在说明本公开内容,不得以任何方式解释为是对主题公开内容的限制。
实施例
材料与方法
化学试剂
利福平(Rifampicin,RIF)即3-(4-甲基哌嗪基亚氨基甲基)利福霉素SV;利福昔明(RIFax)即4-脱氧-4′-甲基吡啶并[1′,2′-1,2]咪唑并[5,4-c]利福霉素SV;以及咪达唑仑(MDZ)获自Sigma-Aldrich(St.Louis,MO)。1′-羟基咪达唑仑(1′-OH-MDZ)购自BD Gentest(Woburn,MA)。其它所有化学试剂都是市售的最高等级。
动物和治疗
将PXR-人源化(hPXR)小鼠、Pxr失效小鼠和野生型(WT)小鼠维持培养在标准12小时光/12小时暗周期下,随意饮食。Pxr失效小鼠和hPXR小鼠如以前文献中所述(Staudinger等,2001;Ma等,2007)。为了研究RIFax在PXR活化中的潜在作用,2-4月龄雄性hPXR小鼠、Pxr失效小鼠和WT小鼠用25mg/kg/天的RIFax口服治疗3天。RIF、特异性人PXR配体用作阳性对照,以25mg/kg/天(口服)给药3天。玉米油用作RIF和RIFax治疗两者的溶媒。在最后一剂之后24小时,用CO2使全部小鼠窒息致死。采集肝和小肠,并在-80℃保存以备进一步分析。
RIFax药代动力学及其在肠道中的分布
对于药代动力学分析,WT小鼠、Pxr失效小鼠和hPXR小鼠经口管饲法用10mg/kg RIF或RIFax治疗。玉米油用作RIF和RIFax治疗两者的溶媒。在给药前、给药后0.25、0.5、1.5、3、6、9、12、24和48小时,使用肝素化管,从框下静脉采集血样。为了比较RIFax和RIF的代谢分布曲线,经静脉内(i.v.)和腹膜内(i.p.)给予10mg/kgRIFax和RIF。对于腹膜内注射,使用玉米油作为RIF和RIFax两者的溶媒,在给药前、给药后0.25、0.5、1、2、4、8、24和48小时,从框下静脉采集血样。对于静脉内注射,使用30%聚乙二醇(PEG,分子量400)作为RIF和RIFax两者的溶媒,在给药前、给药后0.0833、0.25、0.5、1、2、4、8、24和48小时,从框下静脉中采集血样。在8,000g下离心10分钟分离出血清。取50μl血清与150μl甲醇混合,涡旋两次达20秒钟,在4℃下以14,000rpm离心10分钟。然后将上部的有机层转移到自动进样器小瓶中,用于使用API2000SCIEX三重四级杆质谱仪(Applied Biosystems/MDS Sciex,Foster City,CA)的LC-MS/MS对RIF或RIFax进行了检测。通过采用WinNonlin(Pharsight,Mountain View,CA)的非区室分析法(non-compartmentalapproach),由血清浓度-时间数据估算RIF和RIFax的药代动力学参数。从原始数据得出血清中的最大浓度(Cmax)。通过梯形法则计算得到血清浓度-时间曲线下面积(AUC0-48小时)。为了检测在肠道中的分布,小鼠用10mg/kgRIFax或RIF(口服)治疗。在给药后1.5、3、6、9、12、24和48小时,处死小鼠,在肠道的不同区段收集内容物。将肠内容物称重,并在甲醇(100mg/ml)中匀浆。匀浆物在4℃下以14,000rpm离心10分钟。然后将上部的有机层转移到自动进样器小瓶中,用于通过LC-MS/MS对RIF或RIFax进行检测。
通过LC-MS/MS对RIFax和RIF进行分析
通过LC-MS/MS测定了RIFax和RIF,采用高效液相层析系统进行,该系统由PerkinElmer Series 200四元泵、真空脱气器和带有接入上述LC-MS/MS的100μl环的自动进样器构成。在Luna C1850mm x4.6mm(内径)柱(Phenomenex,Torrance,CA)中对RIFax和RIF进行分离。在环境温度下,用含有0.1%甲酸的85%甲醇和15%H2O过柱的流速为0.25ml/分钟。以具有阳离子检测的涡轮离子喷雾模式操作质谱仪。涡轮离子喷雾温度保持在300℃,向喷雾针施加4.8kV的电压。使用N2作为涡轮离子喷雾气体和雾化气体。采用多重反应监测(MRM)模式进行了检测和量化,对于RIFax的m/z为786.3/754.5,对于RIF的m/z为823.5/791.5。
用RIFax预治疗的hPXR小鼠中MDZ的药代动力学分析
hPXR小鼠用或不用10mg/kg RIFax预治疗,一天一次共3天。使用玉米油作为RIFax治疗的溶媒。最后一剂RIFax后24小时,经口管饲法给予小鼠2.5mg/kg MDZ。在给予MDZ之前、之后5、10、20、30、60和90分钟,使用肝素化管,从框下静脉采集血样。在8,000g下离心10分钟分离出血清。对于MDZ和1′-OH-MDZ提取,取50μl血清与150μl磷酸盐缓冲盐水、200μl乙酸乙酯和200μl甲基叔丁基醚混合。混合物在4℃、3,000rpm离心下5分钟。然后将有机层转移到新管内,用N2干燥,并用100μl含有0.1%甲酸的70%甲醇水溶液和30%H2O重配。按照前述方法(Ma等,2007),通过LC-MS/MS对MDZ和1′-OH-MDZ进行了检测。通过采用WinNonlin(Pharsight,Mountain View,CA)的非区室分析法,由血浆浓度-时间数据估算MDZ和1′-OH-MDZ的药代动力学参数。通过梯形法则计算得到血清浓度-时间曲线下面积(AUC0-90分钟)。从原始数据得出血清中的最大浓度(Cmax)及其相应时间(Tmax)。
PXR靶基因的qPCR分析
通过定量实时PCR(qPCR)对下列PXR靶基因进行了分析:细胞色素P4503A11(CYP3A11)、谷胱甘肽S-转移酶α1(GSTA1)、多种药物耐药性蛋白2(MRP2)和有机阴离子转运多肽2(OATP2)(Guo等,2002;Kast等,2002;Rosenfeld等,2003)。使用TRIzol试剂(Invitrogen,Carlsbad,CA),从不同的组织提取RNA。使用由1μg总RNA与SuperScript II逆转录酶试剂盒(Invitrogen)所产生的cDNA进行了qPCR。应用引物表达软件(Applied Biosystems),设计了用于qPCR的引物;引物序列见表1。在ABI Prism 7900HT序列检测系统(AppliedBiosystems,Foster City,CA)中,采用SYBR green PCR master mix(SuperArray)进行了PCR反应。所得数值采用比较CT法量化,将样品归一化至β-肌动蛋白。
表1.用于qPCR分析的引物序列。
引物序列
CYP3A11 正向引物:5’-AGC AGG GAT GGA CCT GG-3’(SEQ ID NO:1)
反向引物:5’-CGG TAG AGG AGC ACC AA-3’(SEQ ID NO:2)
GSTA1 正向引物:5’-CAG CCT GGC AGC CAG AGA-3’(SEQ ID NO:3)
反向引物:5’-TCT GTG GCT CCA TCA ATG CA-3’(SEQ ID
NO:4)
MRP2 正向引物:5’-CGT GGC TGT TGA GCG AAT AA-3’(SEQ ID
NO:5)
反向引物:5’-TCT CAC CTT TTT TGG GCC AAT-3’(SEQ ID
NO:6)
OATP2 正向引物:5’-TGC TGA CTG CAA CAC AAA GTG T-3’(SEQ ID
NO:7)
反向引物:5’-AGC TGA CAT GTA TGA TAG ACC ATT GTC-3’
(SEQ ID NO:8)
基于细胞的报道分子测定法
具有稳定表达的重组人PXR的hepG2细胞系(DPX2)和克隆至萤光素酶载体的PXR反应元件获自Puracyp Inc.(Carlsbad,CA)。以前有研究报告了细胞系的构建和验证(Yueh等,2005)。根据批发商的说明书接种细胞。将RIFax(1μM、10μM、100μM)加到培养基中,使用10μM RIF作为阳性对照。通过测定24小时后萤火虫萤光素酶活性,然后通过蛋白质浓度使萤光素酶活性归一化,来确定PXR的活化。对于核受体CAR、PPARα、PPARγ和FXR的基于细胞的报道分子测定法,将HCT116细胞接种在24孔板(5X 104细胞/孔,在含有10%FBS的DMEM之中培养)中,并使用Fugene转染试剂(Roche,Indianapolis,IN),用各种表达载体转染。以前的报告中描述了小鼠PPAR和CAR载体(Kliewer等,1992;Swales等,2005)。小鼠FXR载体由DrChristopher J.Sinal博士提供。在转染后24小时之后,细胞用溶媒(DMSO)和10μM RIFax孵育24小时。对于小鼠CAR、PPARα、PPARγ和FXR,分别使用TCPOBOP(250nM)、Wy-14,643(10μM)、罗格列酮(10μM)和GW4064(25μM)作为阳性对照。采用标准双重萤光素酶测定法,并归一化至共转染的对照报道分子(Promega,Madison,WI)。每项体外测定都重复进行3次。
统计学分析
所有数值都用平均值±SD表示,并通过双尾斯氏t检验进行了分析。p<0.05视为组间显著不同。
PXR-人源化(hPXR)小鼠、Pxr失效小鼠和野生型小鼠用利福昔明和利福平、充分表征的人PXR配体经口服治疗。当与利福平相比时,利福昔明高度集中在肠道内。利福昔明治疗在hPXR小鼠肠中显著诱导PXR靶基因,但是在野生型小鼠和Pxr失效小鼠中并不如此。然而,在野生型小鼠、Pxr失效小鼠和hPXR小鼠中,利福昔明治疗证实对肝PXR靶基因没有显著作用。与体内数据一致,基于细胞的报道基因实验揭示了利福昔明介导的人PXR的活化,但对于其它异生素核受体CAR、PPARα、PPARγ和FXR却并非如此。用利福昔明进行预治疗不影响CYP3A底物咪达唑仑的药代动力学特征,但却增加1′-羟基咪达唑仑的Cmax,并降低1′-羟基咪达唑仑的Tmax。总的来说,本研究将利福昔明鉴定为肠特异性人PXR配体。
小鼠中RIFax的代谢特征和肠道分布
应用LC-MS/MS研究了RIF和RIFax的药代动力学特征。保留时间对于RIF为2.21分钟,m/z为823.5/791.5(图1C峰值1),对于RIFax,为3.03分钟,m/z为786.3/754.5(图1C峰值2)。检出限对于RIF为0.023pmol,对于RIFax为0.012pmol。在一次口服剂量的RIF或RIFax之后,在治疗后的不同时间点采集小鼠血样和肠内容物长达48小时。在药代动力学研究中,血清RIFax的Cmax为0.04μM,低于RIF(2.75μM)~70倍。血清RIFax的AUC0-48小时低于RIF~300倍(图2A)。然而,对于肠道分布,RIFax浓度显著高于RIF浓度。在小肠中,在所测量的所有时间点上,RIF浓度都低于20μg/g(图2B)。对于RIFax,在给药后浓度为~160μg/g并持续9小时。在盲肠(图2C)和结肠(图2D)中,RIFax肠道分布类似于小肠中的分布。在口服治疗之后,在野生型小鼠、Pxr失效小鼠和hPXR小鼠之间未发现RIFax代谢的显著差异。在野生型小鼠、Pxr失效小鼠和hPXR小鼠中,RIFax(口服治疗)的Cmax如图2E中所示。众所周知,RIFax是通过口服治疗无法吸收的利福霉素。通过腹膜内注射,RIFax无法很好地吸收,且生物利用度显著低于RIF的生物利用度(图2F、图2G)。在静脉内治疗之后,观察到RIFax和RIF之间代谢分布曲线上的差异,当与RIF比较时,RIFax呈超短T1/2和超低AUC(图2H)。
由RIFax所引起的PXR活化
对野生型小鼠和hPXR小鼠的十二指肠、空肠、回肠、盲肠和结肠中的PXR进行了检测,但未检测胃中的PXR(Ma等,2007)。由于RIFax在肠道中的高分布及在肠中PXR的表达,因此通过qPCR研究了RIFax对肠PXR靶基因的作用。在用RIFax治疗的hPXR小鼠小肠中,CYP3A11、GSTA1、MRP2和OATP2全都上调(图3A)。与溶媒治疗的hPXR小鼠相比,肠CYP3A11增加~4倍,虽然在野生型小鼠中表达受到抑制,在Pxr失效小鼠中未观察到显著变化(图3B和图3C)。在RIFax治疗之后,肠GSTA1mRNA在所有3个小鼠品系中都上调,在野生型小鼠、Pxr失效小鼠和hPXR小鼠中记录到增加87%、74%和172%这就表明了Gsta1基因可能不是直接的PXR靶标,但却可能通过间接机制增加。虽无意受任何特定学术理论的束缚,但是RIFax对GSTA1的作用的一种可能解释是RIFax的抗生素活性。RIFax以25mg/kg口服治疗3天,这可能改变肠细菌稳态,并间接影响GSTA1表达。在RIFax治疗之后,在hPXR小鼠中注意到肠MRP2mRNA显著上调,但是在野生型小鼠中其表达显著受到抑制,在Pxr失效小鼠中未观察到变化(图3B和图3C)。据报导,在人和大鼠肝细胞中分别被RIF和PCN激活的MRP2(Kast等,2002),在肝中不被RIF显著诱导,在肠中只被RIF或RIFax适度诱导。其他研究者发现,MRP2不被小鼠PXR配体(例如PCN)显著诱导(Maher等,2005)。在hPXR小鼠中MRP2不被RIF诱导的研究结果表明,在人和小鼠之间,在控制Mrp2基因的顺式元件中存在可能的物种差异。在RIFax治疗之后,在hPXR小鼠中,肠OATP2mRNA增加3.4倍,但是在野生型小鼠和Pxr失效小鼠两者中都未记录到这种mRNA的显著诱导(图3B和图3C)。正如所预期的一样,RIF在肠中也诱导4种mRNA,但是诱导程度都小于用RIFax所观察到的程度(图3D)。相比之下,在肝中RIF显著诱导CYP3A11、GSTA1和OATP2,而在RIFax治疗的hPXR小鼠肝中,仅GSTA1mRNA增加(图3E和3F)。这些数据表明RIFax是肠特异性人PXR配体。
在基于细胞的报道分子测定法中由RIFax所引起的人PXR活化
在由RIFax所引起的hPXR活化的基于细胞的报道分子测定法中观察到萤光素酶活性剂量依赖性的增加。在hPXR报道分子系统中,与1μM、10μM和100μM RIFax一起孵育,相对于DMSO对照,分别产生2.1倍、6.7倍和25.2倍的增加(图4A)。在100nM下的RIFax对hPXR没有显著作用,而在PPARα、PPARγ、CAR和FXR存在下,10μM RIFax在萤光素酶活性方面没有产生显著变化(图4B)。用RIFax预治疗的hPXR小鼠中MDZ的药代动力学特征
在单次口服给予MDZ(2.5mg/kg)之后,测定了hPXR小鼠中MDZ和1′-OH-MDZ的血清浓度-时程。通过非区室分析对药代动力学参数进行了估算。在用或不用RIFax预治疗的hPXR小鼠中,MDZ的Cmax、Tmax和AUC0-90分钟没有显著变化(p>0.05)。在hPXR小鼠中,RIFax预治疗对1′-OH-MDZ这种MDZ的主要代谢物的AUC0-90分钟没有显著作用。然而,在hPXR小鼠预治疗的RIFax中,1′-OH-MDZ的Cmax值比对照组高50%(p<0.05),相应的Tmax比对照组的显著较短(表2)。这些结果表明,在hPXR小鼠肠中RIFax-介导的CYP3A11上调对MDZ的肝外首过代谢产生影响。
表2.在用或不用RIFax,以10mg/kg/天预治疗3天的hPXR小鼠中MDZ的药代动力学特征。通过LC-MS/MS检测了血清MDZ和1′-OH-MDZ。应用WinNonlin(Pharsight,Mountain View,CA)通过非区室分析法,由血浆浓度-时间数据对MDZ和1′-OH-MDZ的AUC0-90 分钟进行了估算。从原始数据得出Cmax和Tmax。数据用平均值±SD表示,n=3。与对照相比*p<0.05。
表2
对照 RIFax RIFax/对照
MDZ
Cmax(nmol/L) 477±40.3 383±19.1 0.8
Tmax(分钟) 10.0±0.0 12.5±10.6 1.3
AUC0-90分种(μmol分钟/L) 8.0±0.4 8.9±0.7 1.1
1′-OH-MDZ
Cmax(nmol/L) 562±4.9 823±55.2* 1.5
Tmax(分钟) 25.0±7.1 7.5±3.5* 0.3
AUC0-90分钟(μmol分钟/L) 32.4±3.0 36.5±4.2 1.1
研究了RIFax对PXR的作用。采用hPXR小鼠、Pxr失效小鼠和野生型小鼠,以及基于细胞的人PXR报道基因实验,鉴定出RIFax为肠特异性人PXR配体。在RIFax的药物开发期间,在人肝细胞模型中记录到由RIFax所引起的CYP3A4诱导。本文所报告的是一个新发现,即RIFax是使包括CYP3A在内的PXR靶基因上调的肠特异性人PXR配体。在具有稳定的重组人PXR表达的DPX2细胞系中,在1μM以上的RIFax浓度下,hPXR被显著激活,因为萤光素酶活性相对于溶媒提高了2.1倍。在DPX2细胞系中,估计由RIFax引起的hPXR活化的EC50约为20μM。在RIFax治疗之后,肠中的RIFax浓度比20μM高出很多。在最新研究中,当小鼠用10mg/kg RIFax(单剂量,口服)治疗时,肠道中的RIFax浓度高达150μg/g(约200μM)肠内容物。在人体中,在3天的RIFax 治疗(每天800mg,口服)之后,RIFax浓度约为8mg/g(约10,000μM)大便(Jiang等,2000),这就表明RIFax暴露于肠中的浓度极高。RIFax对肠PXR的作用(但对肝受体并非如此),可能与吸收差有关。在这项研究中,RIFax的代谢特征与之前的研究一致,因为肠道中RIFax的浓度非常高,而仅有少量分布在血液中(Venturini,1983;Cellai等,1984);这不依赖于肠中的PXR表达,说明了缺乏吸收不是由PXR诱导的代谢所引起的。在人体中,在口服给药后,RIFax吸收也可忽略。在一次口服剂量的RIFax(400mg)之后,血浆RIFax浓度低于检出限(2ng/ml)。在尿中,检测出极少量的未改变的分子,为所给剂量的<0.01%(Descombe等,1994)。因此,本研究表明,在临床应用中,RIFax起抗生素的作用,并且在肠内还起PXR激活物的作用。
将RIFax鉴定为人PXR配体为了解RIFax在药理学和治疗学中的作用提供了新的视野。PXR,这个配体激活的转录因子的核受体家族的成员,是参与异生素解毒的机体防御机制所固有的组分(Kliewer等,2002)。PXR活化调节异生素氧化和缀合酶(xenobiotics oxidationand conjugation enzyme),以及参与代谢并从机体中将潜在的有害化学物质清除掉的转运蛋白的表达。以前的研究揭示了在人肝细胞模型中由RIFax引起的CYP3A4诱导。使用MDZ和含有炔雌醇和诺孕酯的口服避孕药(Trapnell等,2007)的两项临床研究证实,RIFax不会改变这些药物的药代动力学特征,因此表明RIFax对肠或肝CYP3A4没有显著作用。然而,在本文中,在用RIFax治疗的hPXR小鼠中,肠CYP3A11显著上调。在用RIFax预治疗的hPXR小鼠中,对MDZ进行的药代动力学研究发现Cmax降低20%,这与其主要代谢物1′-OHMDZ的Cmax提高一致,虽无意受任何特定学术理论的束缚,但是可用通过肠CYP3A代谢的首过效应来解释。然而,用RIFax预治疗的hPXR小鼠中,没有平行的MDZ AUC的降低。AUC不仅仅与首过消除有关,而且还与其它因素有关,例如吸收。在用RIFax预治疗的hPXR小鼠中,包括转运蛋白在内的若干肠基因上调,例如流入转运蛋白OATP2(influx transporter OATP2),这可能是MDZ吸收增加的原因之一。没有对MDZ的生物利用度进行研究,因为在小鼠中它的生物利用度差,并且变化大(Granvil等,2003)。PXR活化的有益方面是其通过上调参与消除异生素的酶和转运蛋白在解毒中的作用,包括P450s、GST、OATP、MRP等(Kliewer,2003;Saini等,2005;Wagner等,2005)。PXR靶基因是在肠屏障功能中针对异生素和细菌的组分(Langmann等,2004)。在用RIFax治疗的hPXR小鼠小肠中,CYP3A11、GSTA1、MRP2和OATP2等若干PXR靶基因上调。RIFax有益于多发性慢性胃肠疾病的治疗,例如肝性脑病、肠气和肠气相关症状、憩室病、囊炎(pouchitis)和BD(Scarpignato和Pelosini,2005)。不完全了解促成RIFax在慢性胃肠疾病中的有益作用的机制。subject在葡聚糖硫酸钠(DSS)诱发的BD小鼠模型中,PCN介导的PXR活化显著预防DSS诱发的结肠炎(Shah等,2007),这就表明PXR配体作为BD治疗的潜在价值。进一步的人体研究建议在慢性胃肠疾病的治疗学中,对RIFax介导的肠PXR活化的作用进行评价。
虽然为了清楚理解起见,通过实例和实施例对前述发明进行了某种程度的详细描述,按照本发明的教导对于本领域普通技术人员显而易见的是,在不偏离所附权利要求书的精神或范围的情况下,可以对其进行某些改动和修改。
缩略词:RIF,利福平;RIFax,利福昔明;PXR,孕烷X受体;CAR,组成型雄烷受体;PPARα,过氧化物增殖物激活受体α;PPARγ,过氧化物增殖物激活受体γ;FXR,法尼醇X受体;WT,野生型小鼠;hPXR,PXR人源化小鼠;CYP3A,细胞色素P4503A;GSTA,谷胱甘肽S-转移酶α;MRP,多种药物耐药性蛋白;OATP,有机阴离子转运多肽;MDZ,咪达唑仑。
参考文献
Abdelrazeq AS,Kelly SM,Lund JN和Leveson SH(2005)Rifaximin-ciprofloxacin combination therapy is effective in chronic activerefractory pouchitis(利福昔明-环丙沙星联合疗法有效用于慢性活动性难治性囊炎).Colorectal Dis 7:182-186。
Bertilsson G,Heidrich J,Svensson K,Asman M,Jendeberg L,Sydow-Backman M,Ohlsson R,Postlind H,Blomquist P和BerkenstamA(1998)Identification of a human nuclear receptor defines a newsignaling pathway for CYP3A induction(人核受体的鉴定对于CYP3A诱导确定了新的信号转导途径).Proc Natl Acad Sci U S A95:12208-12213。
Carnahan VE和Redinbo MR(2005)Structure and function of thehuman nuclear xenobiotic receptor PXR (人核异生素受体PXR的结构和功能).Curr Drug Metab 6:357-367。
Cellai L,Colosimo M,Marchi E,Venturini AP和Zanolo G(1984)Rifaximin(L/105),a new topical intestinal antibiotic:pharmacokineticstudy after single oral administration of 3H-rifaximin to rats(新的局部肠抗生素利福昔明(L/105):单次口服给予大鼠3H-利福昔明之后的药代动力学研究).Chemioterapia 3:373-377。
Descombe JJ,Dubourg D,Picard M和Palazzini E(1994)Pharmacokinetic study of rifaximin after oral administration in healthyvolunteers(口服给予健康志愿者利福昔明之后的药代动力学研究).IntJ Clin Pharmacol Res 14:51-56。
Di Stefano M,Strocchi A,Malservisi S,Veneto G,Ferrieri A和Corazza GR(2000)Non-absorbable antibiotics for managing intestinalgas production and gas-related symptoms(用于控制肠气产生和肠气相关症状的非吸收性抗生素).Aliment Pharmacol Ther 14:1001-1008。
Doherty MM和Charman WN(2002)The mucosa of the smallintestine:how clinically relevant as an organ of drug metabolism(小肠粘膜:作为药物代谢器官的临床重大意义如何)?Clin Pharmacokinet41:235-253。
Dring MM,Goulding CA,Trimble VI,Keegan D,Ryan AW,Brophy KM,Smyth CM,Keeling PW,O′Donoghue D,O′Sullivan M,O′Morain C,Mahmud N,Wikstrom AC,Kelleher D和McManus R(2006)The pregnane X receptor locus is associated with susceptibility toinflammatory bowel disease(孕烷X受体基因座与炎性肠病易感性有关).Gastroenterology 130:341-348;quiz 592。
Gionchetti P,Rizzello F,Lammers KM,Morselli C,Tambasco R和Campieri M(2006)Antimicrobials in the management of inflammatorybowel disease(在炎性肠病控制中的抗微生物药物).Digestion 73Suppl1:77-85。
Gionchetti P,Rizzello F,Venturi A,Ugolini F,Rossi M,BrigidiP,Johansson R,Ferrieri A,Poggioli G和Campieri M(1999)Antibioticcombination therapy in patients with chronic,treatment-resistant pouchitis(慢性难治性囊炎患者中的抗生素联合疗法).Aliment Pharmacol Ther13:713-718。
Granvil CP,Yu AM,Elizondo G,Akiyama TE,Cheung C,Feigenbaum L,Krausz KW和Gonzalez FJ(2003)Expression ofthehuman CYP3A4gene in the smallintestine of transgenic mice:in vitrometabolism and pharmacokinetics of midazolam(人CYP3A4基因在转基因小鼠小肠中的表达:咪达唑仑的体外代谢和药代动力学特征).DrugMetab Dispos 31:548-558。
Guo GL,Staudinger J,Ogura K和Klaassen CD(2002)Induction ofrat organic anion transporting polypeptide 2 bypregnenolone-16alpha-carbonitrile is via interaction with pregnane Xreceptor(孕烯诺龙-16α-甲腈通过与孕烷X受体相互作用诱导的大鼠有机阴离子转运多肽2).Mol Pharmacol 61:832-839。
Guslandi M,Petrone MC和Testoni PA(2006)Rifaximin for activeulcerative colitis(用于活动性溃疡性结肠炎的利福昔明).InflammBowel Dis 12:335。
Jiang ZD,Ke S,Palazzini E,Riopel L和Dupont H(2000)In vitroactivity and fecal concentration of rifaximin after oral administration(在口服给药后利福昔明的体外活性和粪便浓度).Antimicrob AgentsChemother 44:2205-2206。
Kast HR,Goodwin B,Tarr PT,Jones SA,Anisfeld AM,Stoltz CM,Tontonoz P,Kliewer S,Willson TM和Edwards PA(2002)Regulation ofmultidrug resistance-associated protein 2(ABCC2)by the nuclearreceptors pregnane X receptor,farnesoid X-activated receptor,andconstitutive androstane receptor(通过核受体孕烷X受体、法尼醇X激活的受体和组成型雄烷受体引起的多种药物耐药性相关蛋白2(ABCC2)的调节).J Biol Chem 277:2908-2915。
Kliewer SA(2003)The nuclear pregnane X receptor regulatesxenobiotic detoxification(核孕烷X受体调节异生素解毒).J Nutr133:2444S-2447S。
Kliewer SA,Goodwin B和Willson TM(2002)The nuclearpregnane X receptor:a key regulator of xenobiotic metabolism(核孕烷X受体:异生素代谢的关键调节因子).Endocr Rev 23:687-702。
Kliewer SA,Umesono K,Noonan DJ,Heyman RA和Evans RM(1992)Convergence of 9-cis retinoic acid and peroxisome proliferatorsignalling pathways through heterodimer formation of their receptors(9-顺式维甲酸和过氧化物酶增殖物信号转导途径通过其受体形成异二聚体的会聚).Nature 358:771-774。
Langmann T,Moehle C,Mauerer R,Scharl M,Liebisch G,ZahnA,Stremmel W和Schmitz G(2004)Loss of detoxification ininflammatory bowel disease:dysregulation of pregnane X receptor targetgenes(炎性肠病中解毒作用的丧失:孕烷X受体靶基因失调).Gastroenterology 127:26-40。
Latella G,Pimpo MT,Sottili S,Zippi M,Viscido A,ChiaramonteM和Frieri G(2003)Rifaximin improves symptoms of acquireduncomplicated diverticular disease of the colon(利福昔明改善获得性非复杂性结肠憩室病的症状).Int J Colorectal Dis 18:55-62。
Laustsen G和Wimmett L(2005)2004 drug approval highlights:FDA update(2004药物批准集锦:FDA修订).Nurse Pract 30:14-29;quiz29-31。
Loguercio C,Federico A,De Girolamo V,Ferrieri A和Del VecchioBlanco C(2003)Cyclic treatment of chronic hepatic encephalopathy withrifaximin.Results of a double-blind clinical study(慢性肝性脑病使用利福昔明的循环治疗。双盲临床研究结果).Minerva Gastroenterol Dietol49:53-62。
MaX,Shah Y,Cheung C,Guo GL,Feigenbaum L,Krausz KW,Idle JR和Gonzalez FJ(2007)The PREgnane X receptor gene-humanizedmouse:a model for investigating drug-drug interactionsmediated bycytochromes P4503A(孕烷X受体基因-人源化小鼠:研究细胞色素P4503A介导的药物之间相互作用的模型).Drug Metab Dispos35:194-200。
Maher JM,Cheng X,Slitt AL,Dieter MZ和Klaassen CD(2005)Induction of the multidrug resistance-associated protein family oftransporters by chemical activators of receptor-mediated pathways inmouse liver(小鼠肝中受体介导的途径的化学激活物诱导多种药物耐药性相关蛋白家族的转运蛋白).Drug Metab Dispos 33:956-962。
Mas A,Rodes J,Sunyer L,Rodrigo L,Planas R,Vargas V,CastellsL,Rodriguez-Martinez D,Fernandez-Rodriguez C,Coll I和Pardo A(2003)Comparison of rifaximin and lactitolin the treatment of acutehepatic encephalopathy:results of a randomized,double-blind,double-dummy,controlled clinical trial(在急性肝性脑病的治疗中利福昔明与乳糖醇的比较:随机、双盲、双模拟、对照临床试验的结果).JHepatol 38:51-58。
Miki Y,Suzuki T,Tazawa C,Blumberg B和Sasano H(2005)Steroid and xenobiotic receptor(SXR),cytochrome P4503A4andmultidrug resistance gene 1 in human adult and fetal tissues(成人和人胚胎组织中的类固醇和异生素受体(SXR)、细胞色素P4503A4和多种药物耐药性基因1).Mol Cell Endocrinol 231:75-85。
Papi C,Koch M和Capurso L(2005)Management of diverticulardisease:is there room for rifaximin?(憩室病管理:利福昔明有机会吗?)Chemotherapy 51Suppl 1:110-114。
Pistoia MA,Lombardi L,Rossi M,Vittorini C,Cavaliere GF和Pistoia F(2004)Does rifaximin prevent complications of diverticulardisease?A retrospective study(利福昔明预防憩室病并发症吗?回顾性研究).Eur Rev Med Pharmacol Sci 8:283-287。
Rosenfeld JM,Vargas R,Jr.,Xie W和Evans RM(2003)Geneticprofiling defines the xenobiotic gene networkcontrolled by the nuclearreceptor pregnane X receptor(遗传谱测定限定受控于核受体孕烷X受体的异生素基因网).Mol Endocrinol 17:1268-1282。
Saini SP,Mu Y,Gong H,Toma D,Uppal H,Ren S,Li S,PoloyacSM和Xie W(2005)Dual role of orphan nuclear receptor pregnane Xreceptor in bilirubin detoxification in mice(小鼠中孤儿核受体孕烷X受体在胆红素解毒中的双重作用).Hepatology 41:497-505。
Scarpignato C和Pelosini I(2005)Rifaximin,a poorly absorbedantibiotic:pharmacology and clinical potential(不易吸收的抗生素利福昔明:药理和临床潜力).Chemotherapy 51Suppl 1:36-66。
Shafran I和Johnson LK(2005)An open-label evaluation ofrifaximin in the treatment of active Crohn′s disease(对利福昔明在治疗活动性克罗恩病中的非盲评价).Curr Med Res Opin 21:1165-1169。
Shah YM,Ma X,Morimura K,Kim I和Gonzalez FJ(2007)Pregnane X receptor activation ameliorates DSS-induced inflammatorybowel disease via inhibition of NF-{kappa}B target gene expression(孕烷X受体活化通过抑制NF-{κ}B靶基因表达改善DSS诱发的炎性肠病).Am J Physiol Gastrointest Liver Physiol 292:G1114-1122。
Sonoda J,Chong LW,Downes M,Barish GD,Coulter S,LiddleC,Lee CH和Evans RM(2005)Pregnane X receptor prevents hepatorenaltoxicity from cholesterol metabolites(孕烷X受体预防来自胆固醇代谢物的肝肾毒性).Proc Natl Acad Sci U S A 102:2198-2203。
Staudinger JL,Goodwin B,Jones SA,Hawkins-Brown D,MacKenzie KI,LaTour A,Liu Y,Klaassen CD,Brown KK,ReinhardJ,Willson TM,Koller BH和Kliewer SA(2001)The nuclear receptorPXR is a lithocholic acid sensor that protects against liver toxicity(核受体PXR是防止肝毒性的石胆酸感受器).Proc Natl Acad Sci U S A98:3369-3374。
Swales K,Kakizaki S,Yamamoto Y,Inoue K,Kobayashi K和Negishi M(2005)Novel CAR-mediated mechanism for synergisticactivation of two distinct elements within the human cytochrome P4502B6gene in HepG2cells(HepG2细胞中人细胞色素P4502B6基因内两个不同元件协同活化的新的CAR-介导的机制).J Biol Chem280:3458-3466。
Trapnell CB,Connolly M,Pentikis H,Forbes WP和BettenhausenDK(2007)Absence of effect of oral rifaximin on the pharmacokinetics ofethinyl estradiol/norgestimate in healthy females(健康女性中口服利福昔明对炔雌醇/诺孕酯的药代动力学特征没有影响).Ann Pharmacother41:222-228。
Venturini AP(1983)Pharmacokinetics of L/105,a new rifamycin,inrats and dogs,after oral administration(在大鼠和狗中口服给予一种新的利福霉素L/105后的药代动力学特征).Chemotherapy 29:1-3。
Wagner M,Halilbasic E,Marschall HU,Zollner G,Fickert P,Langner C,Zatloukal K,Denk H和Trauner M(2005)CAR and PXRagonists stimulate hepatic bile acid and bilirubin detoxification andelimination pathways in mice(小鼠中CAR和PXR激动剂刺激肝脏胆汁酸和胆红素解毒和清除途径).Hepatology 42:420-430。
Yueh MF,Kawahara M和Raucy J(2005)High volume bioassays toassess CYP3A4-mediated drug interactions:induction and inhibition in asingle cell line(评价CYP3A4-介导的药物相互作用的高容量生物测定法:在单一细胞系中的诱导和抑制).Drug Metab Dispos 33:38-48。
Claims (28)
1.一种筛选调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐的方法,所述方法包括使PXR受体与一种或多种候选化合物接触,并选出调节PXR受体的化合物或其盐。
2.权利要求1的方法,其中所述候选化合物包含利福霉素类似物。
3.权利要求1的方法,其中调节包括调节由PXR蛋白或其片段与利福霉素类似物的结合所诱导的信号转导。
4.权利要求1的方法,其中所述PXR受体与膜缔合、在转基因小鼠中、在测定板中、在细胞中和/或在人工膜中。
5.权利要求1的方法,其中所述PXR蛋白包含由序列登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880或NP_071285所表示的氨基酸序列或其片段或变体或者由序列登录号NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133所表示的核酸或其片段或变体。
6.权利要求1的方法,其中CYP3A11、GSTA1、MRP2和OATP2全都上调。
7.权利要求1的方法,所述方法另外包括用利福昔明预治疗。
8.权利要求1的方法,所述方法另外包括用PXR受体蛋白与候选化合物预治疗。
9.权利要求8的方法,其中用候选化合物预治疗不会影响CYP3A底物咪达唑仑的药代动力学。
10.权利要求8的方法,其中用候选化合物预治疗提高1′-羟基咪达唑仑的Cmax并降低1′-羟基咪达唑仑的Tmax。
11.权利要求1的方法,其中在用候选化合物治疗后与对照相比,CYP3A11增加约1~约4倍。
12.权利要求1的方法,在候选化合物治疗后,GSTA1mRNA上调。
13.权利要求12的方法,其中上调范围介于约65%~约200%之间。
14.权利要求1的方法,其中在候选化合物治疗之后肠MRP2mRNA上调。
15.一种用于筛选调节PXR受体或其片段的化合物或其盐的试剂盒,所述试剂盒包括PXR受体蛋白或其活性片段和利福霉素类似物。
16.一种用于治疗PXR相关疾病的药物,所述药物包含调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐,或者调节由PXR蛋白或其片段与利福霉素类似物的结合所诱导的信号转导的化合物或其盐。
17.一种治疗、预防或减轻受治疗者的PXR相关疾病的方法,所述方法包括给予调节孕烷X受体(PXR)蛋白或其片段的化合物或其盐。
18.权利要求17的方法,其中调节包括调节由PXR蛋白或其片段与利福霉素类似物的结合所诱导的信号转导。
19.权利要求17的方法,其中所述PXR受体与膜缔合、在转基因小鼠中、在测定板中、在细胞中和/或在人工膜中。
20.权利要求17的方法,其中所述PXR蛋白包含由序列登录号O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880或NP 071285所表示的氨基酸序列或其片段或变体或者由序列登录号NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133所表示的核酸或其片段或变体。
21.一种组合物,所述组合物包含产生治疗效果的有效量的PXR蛋白激动剂。
22.一种转基因小鼠,所述转基因小鼠包含纯合破坏的内源孕烷X受体(PXR)基因。
23.权利要求22的转基因小鼠,其中所述小鼠包含人PXR基因。
24.一种细胞或组织,所述细胞或组织分离自权利要求22的转基因小鼠。
25.一种鉴定能够调节PXR基因活性或PXR基因表达产物活性的调节剂的方法,所述方法包括:
给予权利要求23的转基因小鼠推定的调节剂;
给予野生型对照小鼠所述调节剂;和
将转基因小鼠的生理反应与对照小鼠的生理反应进行比较;其中在转基因小鼠与对照小鼠之间生理反应上的差异表示所述调节剂能够调节基因或基因表达产物的活性。
26.一种筛选具有肠疾病活性的候选药物的方法,所述方法包括:
提供表达PXR基因或其片段或变体的细胞,所述PXR基因由选自以下序列的核酸序列编码:NM_033013、NM_009803、NM_022002、NM_003889、CS618137、CS618135、CS618133或O75469、Q8SQ01、Q9R1A7、O54915、NP_148934、NP_003880、NP_071285;
使所述细胞与候选药物接触;和
监测组织样品中候选药物对BD多核苷酸表达的作用。
27.一种与PXR多肽结合的分离抗体或其抗原结合片段。
28.权利要求27的分离抗体,其中将所述抗体或其片段与固相支持体连接;其中所述抗体是单克隆抗体;其中所述抗体是多克隆抗体;和/或其中所述抗体或其片段另包含可检测标记。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US99923407P | 2007-10-17 | 2007-10-17 | |
| US60/999234 | 2007-10-17 | ||
| PCT/US2008/080115 WO2009052255A2 (en) | 2007-10-17 | 2008-10-16 | Novel therapeutic targets in bowel disease |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN101896815A true CN101896815A (zh) | 2010-11-24 |
Family
ID=40568065
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2008801210743A Pending CN101896815A (zh) | 2007-10-17 | 2008-10-16 | 肠疾病中的新的治疗靶标 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20110055943A1 (zh) |
| EP (1) | EP2201372A4 (zh) |
| JP (1) | JP2011501672A (zh) |
| CN (1) | CN101896815A (zh) |
| AU (1) | AU2008312464A1 (zh) |
| MX (1) | MX2010004333A (zh) |
| WO (1) | WO2009052255A2 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108267522A (zh) * | 2017-12-28 | 2018-07-10 | 北京和合医学诊断技术股份有限公司 | 检测血液中奥氮平药物含量的液相色谱分析方法 |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITBO20050123A1 (it) | 2005-03-07 | 2005-06-06 | Alfa Wassermann Spa | Formulazioni farmaceutiche gastroresistenti contenenti rifaximina |
| ES2509892T3 (es) * | 2008-05-07 | 2014-10-20 | Salix Pharmaceuticals, Ltd. | Administración de un agente para limpieza del intestino y antibiótico para el tratamiento de enfermedad intestinal |
| CN110470771B (zh) * | 2019-09-05 | 2021-06-01 | 清华大学 | 一种评价转基因植物食用安全性的方法 |
| CN117031004B (zh) * | 2023-08-09 | 2024-10-01 | 四川省医学科学院·四川省人民医院 | 一种检测网膜素-1的试剂在制备预测或评估ibs患者生活质量的产品中的应用 |
-
2008
- 2008-10-16 MX MX2010004333A patent/MX2010004333A/es not_active Application Discontinuation
- 2008-10-16 JP JP2010530102A patent/JP2011501672A/ja active Pending
- 2008-10-16 AU AU2008312464A patent/AU2008312464A1/en not_active Abandoned
- 2008-10-16 EP EP08839346A patent/EP2201372A4/en not_active Withdrawn
- 2008-10-16 CN CN2008801210743A patent/CN101896815A/zh active Pending
- 2008-10-16 WO PCT/US2008/080115 patent/WO2009052255A2/en active Application Filing
- 2008-10-16 US US12/682,665 patent/US20110055943A1/en not_active Abandoned
Non-Patent Citations (2)
| Title |
|---|
| HAI-LIN FANG ET AL.: "Positive and Negative Regulation of Human Hepatic Hydroxysteroid Sulfotransferase (SULT2A1) Gene Transcription by Rifampicin: Roles of Hepatocyte Nuclear Factor 4 and Pregnane X Receptor", 《 THE JOURNAL OF PHARMACOLOGY AND EXPERIMENTAL THERAPEUTICS》 * |
| XIAOCHAO MA, ET AL: "Rifaximin Is a Gut-Specific Human Pregnane X Receptor Activator", 《THE JOURNAL OF PHARMACOLOGY AND EXPERIMENTAL THERAPEUTICS》 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108267522A (zh) * | 2017-12-28 | 2018-07-10 | 北京和合医学诊断技术股份有限公司 | 检测血液中奥氮平药物含量的液相色谱分析方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2011501672A (ja) | 2011-01-13 |
| MX2010004333A (es) | 2010-11-30 |
| US20110055943A1 (en) | 2011-03-03 |
| WO2009052255A3 (en) | 2009-06-11 |
| EP2201372A4 (en) | 2010-11-10 |
| AU2008312464A1 (en) | 2009-04-23 |
| EP2201372A2 (en) | 2010-06-30 |
| WO2009052255A2 (en) | 2009-04-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Dean et al. | The human ATP‐binding cassette (ABC) transporter superfamily | |
| Urs et al. | Distinct cortical and striatal actions of a β-arrestin–biased dopamine D2 receptor ligand reveal unique antipsychotic-like properties | |
| Mohn et al. | Mice with reduced NMDA receptor expression display behaviors related to schizophrenia | |
| Wang et al. | Dopamine D2 long receptor-deficient mice display alterations in striatum-dependent functions | |
| Al-Wandi et al. | Absence of α-synuclein affects dopamine metabolism and synaptic markers in the striatum of aging mice | |
| Goren et al. | Glucose homeostasis and tissue transcript content of insulin signaling intermediates in four inbred strains of mice: C57BL/6, C57BLKS/6, DBA/2, and 129X1 | |
| Zhang et al. | The transport of antiepileptic drugs by P-glycoprotein | |
| Rangel et al. | Impaired angiogenesis in aminopeptidase N-null mice | |
| Kroeger Jr et al. | The zebrafish kidney mutant zeppelin reveals that brca2/fancd1 is essential for pronephros development | |
| JP2001520170A (ja) | Nf−at3機能に関連した心肥大動物モデルと治療法 | |
| Albiston et al. | Gene knockout of insulin-regulated aminopeptidase: loss of the specific binding site for angiotensin IV and age-related deficit in spatial memory | |
| CN105008394A (zh) | 治疗结肠直肠癌的方法 | |
| Beumer et al. | Evaluation of eluforsen, a novel RNA oligonucleotide for restoration of CFTR function in in vitro and murine models of p. Phe508del cystic fibrosis | |
| CN101896815A (zh) | 肠疾病中的新的治疗靶标 | |
| JP2023052057A (ja) | リンパ系疾患の診断及び治療のための組成物及び方法 | |
| Seidel et al. | Enhanced Ca2+ signaling, mild primary aldosteronism, and hypertension in a familial hyperaldosteronism mouse model (Cacna1h M1560V/+) | |
| Sartori et al. | GATA factors promote ER integrity and β-cell survival and contribute to type 1 diabetes risk | |
| Leach et al. | Disruption of diacylglycerol kinase delta (DGKD) associated with seizures in humans and mice | |
| Pewzner-Jung et al. | Brain pathology and cerebellar purkinje cell loss in a mouse model of chronic neuronopathic Gaucher disease | |
| Käenmäki et al. | Importance of membrane‐bound catechol‐O‐methyltransferase in L‐DOPA metabolism: a pharmacokinetic study in two types of Comt gene modified mice | |
| Vecchio et al. | N-terminal tagging of the dopamine transporter impairs protein expression and trafficking in vivo | |
| Bayle et al. | Hyperphenylalaninemia and impaired glucose tolerance in mice lacking the bifunctional DCoH gene | |
| Omer et al. | Protein kinase D1 variant associated with human epilepsy and peripheral nerve hypermyelination | |
| Yu et al. | Induction of the Hajdu-Cheney syndrome mutation in CD19 B cells in mice alters B-cell allocation but not skeletal homeostasis | |
| Volpatti | Characterization of a Zebrafish Model of X-linked Centronuclear Myopathy for Therapeutic Drug Development |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20101124 |