PROCEDE DE DEGRADATION ENZYMATIQUE DE POLYETHYLENE TEREPHTALATE
DOMAINE TECHNIQUE DE L’INVENTION
La présente invention concerne un procédé de dépolymérisation par voie enzymatique de polyéthylène téréphtalate (PET), notamment contenu dans un matériau plastique. Le procédé selon l’invention peut notamment être mis en œuvre à l’échelle industrielle ou semi-industrielle.
ARRIERE PLAN TECHNOLOGIQUE
Les produits plastiques sont des matériaux durables et peu chers qui peuvent être utilisés pour la fabrication d’une grande variété de produits pour des applications diverses (emballages alimentaires, textiles d’habillement, etc.). En conséquence, la production de plastiques a drastiquement augmenté depuis les dernières décennies. La plupart d’entre eux sont utilisés pour des applications de courte durée, ce qui a pour effet d’entraîner une accumulation de déchets plastiques et une nécessité de traitement de ces derniers. Parmi les différents polymères constituants ces-dits plastiques, on retrouve notamment le polyéthylène téréphtalate (PET), un polyester aromatique produit à partir d’acide téréphtalique et d’éthylène glycol et qui est utilisé dans de nombreuses applications telles que les emballages alimentaires (bouteilles, flacons, pots, barquettes, poches), mais également dans la production de textiles pour l’habillement, la décoration (moquette), le linge de maison, etc.
Afin de répondre aux problématiques environnementales et économiques d’accumulation des déchets, des technologies de recyclage ou de valorisation énergétique ont été développées. Le procédé de recyclage mécanique reste aujourd’hui le plus utilisé, mais ce dernier présente de nombreux inconvénients. Sa mise en œuvre nécessite en effet de procéder à un tri sophistiqué et coûteux et conduit à la production de plastiques recyclés de qualité diminuée destinés à des applications de moindre valeur (baisse de masse moléculaire, présence incontrôlée d’additifs). En outre, ces plastiques recyclés ne sont pas compétitifs par rapport aux plastiques vierges issus du pétrole.
Récemment, des procédés innovants de recyclage enzymatique de produits plastiques ont été développés et notamment décrits dans les demandes de brevets WO 2014/079844, WO
2015/097104, WO 2015/173265 et WO 2017/198786. Contrairement aux procédés traditionnels de recyclage mécanique, ces procédés enzymatiques permettent, par dépolymérisation enzymatique du polymère contenu dans le plastique, de revenir aux principaux constituants (monomères) du polymère. Les monomères obtenus peuvent ensuite être purifiés et utilisés pour repolymériser de nouveaux polymères. Ces procédés enzymatiques permettent, via la spécificité des enzymes, d’éviter un tri coûteux des plastiques, mais également de proposer un recyclage à l’infini conduisant à des polymères recyclés de qualité équivalente aux polymères issus du pétrole. Ces procédés permettent notamment, à partir de PET, de produire de l’acide téréphtalique et de l’éthylène glycol.
RESUME DE L’INVENTION
En travaillant sur les procédés de dépolymérisation enzymatique du PET, le Demandeur est parvenu à mettre au point un procédé optimisé permettant de dépolymériser par voie enzymatique des plastiques contenant du PET à une température proche de la Tg de ce PET, afin de rendre les chaînes dudit polymère plus facilement accessibles à l’enzyme de dépolymérisation et ainsi augmenter le taux de dépolymérisation.
Pour parvenir à un tel procédé, l’inventeur a dû répondre à des problèmes antinomiques. En effet, les enzymes aptes à dépolymériser les polymères sont majoritairement plus actives sur les polymères amorphes que sur les polymères semi-cristallins. Or, bien qu’un procédé de dépolymérisation à une température proche de la Tg d’un polymère puisse théoriquement permettre d’améliorer l’accessibilité de l’enzyme aux chaînes dudit polymère à dépolymériser, via une augmentation de la mobilité des chaînes de ce polymère, lorsqu’un polymère est soumis à une température proche ou au-dessus de sa Tg ce dernier tend à recristalliser plus rapidement, rendant ainsi le polymère plus difficilement dépolymérisable pour l’enzyme.
L’inventeur a ainsi mis en évidence qu’il est possible de réaliser un procédé de dépolymérisation du PET à une température proche ou au-dessus de la Tg dudit PET, en s’assurant d’une part que le taux de cristallinité du PET est suffisamment bas préalablement à l’étape de dépolymérisation et d’autre part en sélectionnant une enzyme apte à dépolymériser ce PET dans un temps de dépolymérisation inférieur au temps nécessaire audit PET pour atteindre un taux de cristallinité incompatible avec une dépolymérisation enzymatique. Le procédé développé par l’inventeur permet de maintenir des vitesses de dépolymérisation au sein
d’un réacteur compatibles avec une mise en œuvre à l’échelle industrielle. A titre d’exemple, l’inventeur est parvenu à dépolymériser plus de 90% d’un PET en moins de lOh à une température de 72°C. De manière avantageuse, le procédé de l’invention peut être mis en œuvre pour la dépolymérisation et/ou le recyclage de plastiques contenant du PET. L’invention a donc pour objet un procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) par mise en contact dudit PET avec une enzyme apte à dépolymériser ledit PET, caractérisé en ce que le PET présente un degré de cristallinité initial d’au plus 25%, l’étape de dépolymérisation est conduite à une température T égale à la Tg +/- lO°C dudit PET, et l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à ladite enzyme pour dépolymériser au moins 80% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35% à ladite température T.
L’étape de dépolymérisation est préférentiellement conduite à une température T comprise entre 66°C et 80°C, préférentiellement entre 68°C et 73°C, le temps tD étant inférieur ou égal à 20h, préférentiellement inférieur à l6h.
DESCRIPTION DE LA FIGURE
Figure 1 : Cinétique de recristallisation d’un PET contenu dans un matériau plastique lors de l’incubation dudit matériau à différentes températures. DESCRIPTION DETAILLEE DE L’INVENTION
Définitions
Dans le contexte de l’invention l’expression « matériau plastique » désigne les produits plastiques (tels que des feuilles, barquettes, films, tubes, blocs, fibres, tissus, etc.) et les compositions plastiques utilisées pour réaliser les produits plastiques. De manière préférentielle, le matériau plastique est composé de polymères amorphes et/ou semi-cristallins. Le matériau plastique peut contenir en plus du ou des polymères, des substances additionnelles ou des additifs, tels que des plastifiants, des charges minérales ou organiques, des colorants, etc. Ainsi, dans le contexte de l’invention, le matériau plastique fait référence à tout produit
plastique et/ou composition plastique comprenant au moins un polymère sous forme semi- cristalline et/ou amorphe et plus particulièrement au moins un PET.
Les produits plastiques désignent notamment les produits plastiques manufacturés, tels que les emballages rigides ou souples (films, bouteilles, barquettes), films agricoles, sacs, objets jetables, textiles, tissus, non-tissés, revêtements de sols, les déchets plastiques ou déchets fibres, etc.
Le terme « polymère » fait référence à un composé chimique dont la structure est constituée de multiples unités répétées (i.e. « monomères ») liées par des liaisons covalentes chimiques. Dans le contexte de l’invention, le terme « polymère » fait plus précisément référence à de tels composés chimiques entrant dans la composition de matériaux plastiques.
Le terme « polyester » fait référence à un polymère qui contient un groupe fonctionnel ester dans la chaîne principale de sa structure. Le groupe fonctionnel ester est caractérisé par une liaison entre un carbone et trois autres atomes : une liaison unique avec un autre atome de carbone, une double liaison avec un oxygène et une liaison simple avec un autre atome d’oxygène. L’oxygène lié au carbone par une liaison simple est lui-même lié à un autre carbone par une liaison simple. Les polyesters peuvent être constitués d’un seul type de monomères (i.e. homopolymère) ou d’au moins deux monomères différents (i.e. copolymère). Les polyesters peuvent être aromatiques, aliphatiques ou semi-aromatiques. A titre d’exemple, le polyéthylène téréphtalate est un copolymère semi-aromatique composé de deux monomères, l’acide téréphtalique et l’éthylène glycol.
Dans le contexte de l’invention, le terme « polymères semi-cristallins » fait référence à des polymères partiellement cristallins, dans lesquels des régions cristallines et amorphes coexistent. Le degré de cristallinité d’un polymère semi-cristallin peut être estimé par diverses méthodes analytiques, et est généralement compris entre 10% et 90%. Un polymère avec un degré de cristallinité inférieur à 10% peut être considéré comme amorphe.
Un « procédé de dépolymérisation » en relation avec un polymère ou matériau plastique fait référence à un procédé par lequel un polymère ou au moins un polymère d’un matériau plastique est dégradé en molécules plus petites, telles que des monomères et/ou oligomères. Dans le cas de la présente invention, un procédé de dépolymérisation de PET ou d’un matériau plastique
contenant du PET fait référence à un procédé dans lequel le PET est dégradé en monomères tels que l’acide téréphtalique et/ou l’éthylène glycol et/ou en oligomères tels que le diméthyle téréphtalate (DMT), le methyl-2-hydroxyethyl téréphtalate (MHET), bis(2-hydroxyethyl) téréphtalate (BHET).
Sélection du PET
Le procédé de dépolymérisation selon l’invention repose sur une dépolymérisation enzymatique d’un PET, par mise en contact dudit PET avec au moins une enzyme apte à le dépolymériser. Plus particulièrement, l’inventeur a mis au point un procédé de dépolymérisation enzymatique de PET comprenant une étape de dépolymérisation conduite à une température T comprise entre la Tg - l0°C et la Tg + l0°C dudit PET, à partir d’un PET présentant un degré de cristallinité initial d’au plus 25%. Aussi, selon un mode particulier de l’invention, on sélectionne le PET de manière à ce que ce dernier présente un degré de cristallinité initial d’au plus 25%.
Selon l’invention, le PET soumis à l’étape de dépolymérisation est un PET amorphe et/ou semi- cristallin au début de l’étape de dépolymérisation, dont le degré de cristallinité initial est inférieur ou égal à 25%. On entend par « degré de cristallinité initial », le degré de cristallinité du PET au début de l’étape de dépolymérisation, c’est-à-dire avant la mise en contact dudit PET avec une enzyme de dépolymérisation. Ainsi dans le cas où le PET subirait une ou des étape(s) de prétraitement (amorphisation, micronisation), le « degré de cristallinité initial » correspond au degré de cristallinité après ces étapes de prétraitement.
Le degré de cristallinité d’un polymère semi-cristallin peut être estimé par diverses méthodes analytiques, et est généralement compris entre 10% et 90%. Par exemple, la calorimétrie différentielle à balayage (DSC) ou la diffraction des rayons X peuvent être utilisées pour déterminer le degré de cristallinité des polymères. D’autres techniques conviennent également à la détermination de la cristallinité des polymères, mais avec une fiabilité moindre, comme la diffusion des rayons X aux petits angles (SAXS) ou aux grands angles (WAXS) et la spectroscopie infrarouge. Dans la présente demande, la cristallinité est mesurée par l’analyse calorimétrique différentielle (DSC). Plus particulièrement, les expériences de DSC ont été conduites en utilisant le protocole suivant : une petite quantité de matériau plastique (plusieurs mg) est chauffée à une vitesse de chauffe constante, à partir de la température ambiante ou
d’une température inférieure à la température ambiante jusqu’à une température supérieure à la température de fusion (Tf) du polymère. Les données de flux de chaleur sont collectées et tracées en fonction de la température. Le degré de cristallinité (Xc) exprimé en pourcentage (%) est calculé selon la formule suivante :
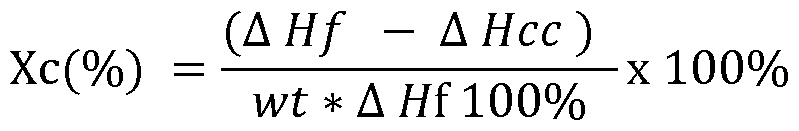
Etant entendu que :
AHf correspond à l'enthalpie de fusion qui peut être déterminée en intégrant le pic de fusion endothermique,
AHcc correspond à l'enthalpie de cristallisation froide et déterminée en intégrant le pic de cristallisation froide exothermique,
wt représente la fraction pondérale de polyester dans le plastique, et
AHfl 00% correspond à l'enthalpie de fusion pour un polymère entièrement cristallin et peut être trouvée dans la littérature. Par exemple, DHO 00% du PET correspond dans la littérature à 125,5 J / g (Polymer Data Handbook, deuxième édition, édité par James E. Mark, OXFORD, 2009).
La marge d’erreur de mesure du degré de cristallinité est d’environ 10%. Ainsi un degré de cristallinité évalué à 25% correspond à un degré de cristallinité compris entre 22,5% et 27,5%.
Selon un mode de réalisation du procédé, on sélectionne un PET qui a un degré de de cristallinité inférieur à 25%, +/- 10%. Dans un mode préféré, le PET a un degré de cristallinité initial inférieur à 20%, +/-l0%. Dans un autre cas préféré, le PET soumis à l’étape de dépolymérisation est un PET amorphe, c’est-à-dire présentant un degré de cristallinité inférieur à 10%, +/- 10%.
Selon l’invention, il est possible de procéder à une étape d’amorphisation du PET en amont de l’étape de dépolymérisation, par tout moyen connu de l’homme de l’art, de manière à atteindre un degré de cristallinité initial inférieur ou égal à 25%. Une telle étape d’amorphisation est notamment décrite dans la demande WO 2017/198786.
Dans un mode de réalisation particulier, le procédé de dépolymérisation selon l’invention est mis en œuvre avec un matériau plastique comprenant au moins du PET. Dans un mode préféré, le PET représente au moins 80% en poids dudit matériau plastique, préférentiellement au moins 85%, 90%, 95%.
Dans un contexte particulier de l’invention, le terme matériau plastique désigne tout produit plastique sous forme de fibres, tels que textiles, tissus, non-tissés, fils etc. Ainsi, dans un mode de mise en œuvre particulier, le matériau plastique est sélectionné parmi des fibres et/ou des déchets fibres et/ou textiles et le PET représente au moins 60% en poids par rapport au poids total dudit matériau plastique, préférentiellement au moins 65%, 70%, 75%, 80%, 85%, 90%, 95%.
Dans un mode de mise en œuvre particulier, le matériau plastique comprend un mélange de PET et d’acide polylactique (PLA), un mélange de PET et polyéthylène (PE), un mélange de PET et polytriméthylène téréphtalate (PTT), un mélange de PET et de polyamide (PA), ou un mélange de PET et de coton. Avantageusement, les matériaux plastiques engagés dans le réacteur sont des déchets plastiques ou déchets fibres. Ces déchets peuvent être issus des filières de collecte destinées au recyclage, mais également être des déchets de la filière de production ou de la filière de recyclage, et peuvent ainsi contenir d’autres composés que les déchets plastiques. Cela implique que le PET peut être engagé dans le réacteur en combinaison d’autres éléments présents dans ces flux (tel que papier, carton, aluminium, colle etc...). Dans un mode de mise en œuvre particulier, le réacteur dans lequel est mis en œuvre l’étape de dépolymérisation est chargé en plusieurs matériaux plastiques contenant au moins du PET, préférentiellement contenant au moins 80% en poids de PET, par rapport au poids total en matériaux plastiques, préférentiellement au moins 85%, 90%, 95%.
Selon l’invention, le PET est caractérisé par sa température de transition vitreuse (Tg) initiale, c’est-à-dire avant la mise en contact dudit PET avec une enzyme de dépolymérisation. Ainsi dans le cas où le PET subirait une étape de prétraitement (amorphisation, micronisation), le PET est caractérisé par sa Tg après ces étapes de prétraitement. Cette température peut être estimée par différentes méthodes analytiques. Par exemple, la calorimétrie différentielle à balayage (DSC) ou l'analyse thermique différentielle (DTA) peuvent être utilisées pour déterminer la Tg d’un polymère. Dans la présente description, la Tg correspond à la température
de transition vitreuse mesurée par DSC lors du premier balayage en température comme indiqué dans les exemples. D’une manière générale, la marge d’erreur de mesure de la Tg est d’environ 2°C.
Dans un mode particulier de l’invention, la Tg initiale du PET est comprise entre 60°C et 90°C, préférentiellement entre 60°C et 85°C. Dans un autre mode particulier, la Tg initiale du PET est comprise entre 65°C+/-l°C et 80°C+/-l°C. Dans un autre mode particulier, la Tg initiale du PET est comprise entre 65°C+/-2°C et 80°C+/-2°C. Dans un autre mode particulier, la Tg initiale du PET est comprise entre 60°C+/-2°C et 70°C+/-2°C.
Selon l’invention, il est possible de procéder à une étape de pré-traitement du PET en amont de l’étape de dépolymérisation, et notamment à une étape de broyage du PET, ou du matériau plastique contenant le PET avant l’étape de dépolymérisation du polyester. Dans un mode préféré, le PET ou le matériau plastique contenant le PET est réduit sous forme de poudre par tout moyen approprié connu de l’homme de l’art. Dans ce cas particulier, le PET, ou le matériau plastique contenant le PET, est avantageusement micronisé de manière à être transformé sous forme de poudre.
Dans un mode de mise en œuvre particulier, le PET ou le matériau plastique contenant le PET engagé dans le réacteur est sous forme de poudre de granulométrie moyenne (d50) inférieure à 2 mm, préférentiellement de granulométrie inférieure à 1 mm. Dans un autre mode de réalisation le PET ou le matériau plastique contenant le PET engagé dans le réacteur est sous forme de poudre de granulométrie moyenne (d50) inférieure à 500mih.
Dans un mode de réalisation particulier, le procédé de dépolymérisation comprend une étape d’amorphisation du PET, suivie d’une étape de broyage et/ou de micronisation du PET ou du matériau plastique contenant le PET avant l’étape de dépolymérisation du PET.
Dans un mode de réalisation particulier, le procédé de dépolymérisation comprend une étape d’amorphisation du PET avant l’étape de dépolymérisation du PET et, le PET ou le matériau plastique contenant le PET est engagé dans le réacteur sous forme de granules issus de l’extrudeuse utilisée pour l’amorphisation. Ainsi le PET ou le matériau plastique contenant le PET est engagé sous forme de granules de taille inférieure à 2 mm, préférentiellement de taille inférieure à 1 mm.
Sélection de l’ enzyme
Selon l’invention, le procédé de dépolymérisation est mis en œuvre avec une enzyme apte à dépolymériser le PET. Plus particulièrement, l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET.
Selon l’invention, on définit par temps de cristallisation « (tR) » du PET, le temps nécessaire audit PET d’une cristallinité initiale Xc pour atteindre un taux, ou degré, de cristallinité de 35% ou moins de 35% à une température T. Ce temps est dépendant de la nature du matériau et/ou de la nature du polymère (i.e. la présence d’additifs et/ou de co-monomères), de son poids moléculaire, de sa Tg et également de son histoire thermique (traitements antérieurs ayant impliqués un refroidissement et/ou un chauffage, comme une amorphisation ou une micronisation). Ce temps est mesuré dans des conditions où la température T est régulée, et n’est pas impactée par l’agitation et/ou le pH pendant la mesure. Selon l’invention, il est possible de mesurer le temps de cristallisation (tR) du PET à une température T par incubation du matériau plastique contenant le PET à cette température T, et par mesure régulière du taux de cristallinité (par DSC) d’échantillons prélevés à différents intervalles de temps.
Selon l’invention, le temps de dépolymérisation « (tD) » représente le temps nécessaire à l’enzyme dégradant le polymère pour dépolymériser au moins 80% dudit polymère à une température T. Dans un mode particulier, ce temps est déterminé au pH optimal de l’enzyme et à une concentration saturante en enzyme, i.e. une concentration au-delà de laquelle la vitesse de réaction n’est pas améliorée par l’ajout d’enzyme. Ainsi, le temps tD correspond au temps nécessaire à l’enzyme pour libérer 80% des monomères présents dans le polymère. Dans le cas particulier de l’invention, le temps tD correspond au temps nécessaire pour obtenir après mise en contact de l’enzyme et du PET, 80% d’équivalent acide téréphtalique (AT) présents dans le PET, l’équivalent AT correspondant à l’AT libre et l’AT présent dans les oligomères de BHET et MHET. Dans un autre cas particulier de l’invention, le temps tD correspond au temps nécessaire pour obtenir après mise en contact de l’enzyme et du PET, 80% d’équivalent monoéthylène glycol (ME G) dans le PET, l’équivalent MEG correspondant au MEG libre et au MEG présent dans les oligomères de BHET et MHET.
Il est précisé que la mesure des temps tD et tR est réalisée à une même température T.
Selon l’invention, l’enzyme est avantageusement sélectionnée parmi les enzymes ayant une température de fusion (Tm) strictement supérieure à la température T à laquelle est conduite l’étape de dépolymérisation. Dans le contexte de l’invention, la température Tm correspond plus particulièrement à la température à laquelle la moitié de la quantité de l'enzyme considérée est dépliée ou mal repliée, de sorte qu’elle perd tout ou partie de son activité par rapport à l’activité de l’enzyme convenablement repliée. La Tm permet notamment d’estimer la thermostabilité de l’enzyme considérée. La Tm peut être mesurée par tout moyen connu de l’homme de l’art, notamment la DSF (analyse fluorimétrique différentielle). De manière alternative, la Tm peut être évaluée par analyse du repliement de la protéine en utilisant la méthode du dichroïsme circulaire. De préférence, la Tm est mesurée en utilisant la DSF telle qu'exposé dans la partie expérimentale.
Dans un mode préféré, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
L’activité de dépolymérisation d’une enzyme sur un polymère peut être évaluée par tous moyens connus de l’homme de l’art. Par exemple, elle peut être évaluée par la perte de masse du polymère ou la mesure du taux de dépolymérisation du polymère, i.e. la quantité de monomères et/ou oligomères produits sur une période de temps. Ainsi dans le contexte de l’invention, l’activité de dépolymérisation d’une enzyme dégradant le PET peut être évaluée en mesurant les quantités d’oligomères (BHET et/ou MHET) et/ou de monomères (acide téréphtalique et/ou éthylène glycol et/ou DMT) relarguées dans des conditions particulières de température et de pH et en mettant en contact le PET ou le matériau plastique contenant le PET avec ladite enzyme. L’activité de dépolymérisation peut également être évaluée par le suivi de l’ajout de base au cours de la réaction de dépolymérisation. Une addition de base est en effet réalisée de manière à neutraliser l’acide téréphtalique produit par la dépolymérisation et ainsi réguler le pH. Aussi la quantité de base ajoutée au cours de la réaction permet de mesurer la quantité d’acide téréphtalique produit lors de la réaction. De manière préférentielle, on ajoute une solution basique de manière à maintenir le milieu réactionnel au pH optimum de l’enzyme.
Avantageusement, ladite enzyme est sélectionnée parmi les cutinases, les lipases et les estérases dégradant ledit PET. Particulièrement, ladite enzyme est sélectionnée parmi les estérases dégradant ledit PET.
Par exemple, l’enzyme peut être sélectionnée parmi les cutinases issues de Thermobifida cellulosityca, Thermobifida halotolerans, Thermobifida fusca, Thermobifida alba, Bacillus subtilis, Fusarium solani pisi, Humicola insolens (telle que celle référencée A0A075B5G4 dans la base Uniprot), Sirococcus conigenus, Pseudomonas mendocina et Thielavia terrestris ou un variant de celles-ci.
Dans un autre cas, la cutinase est sélectionnée parmi les cutinases issues de banques métagénomiques telle que la LC-Cutinase décrite dans Sulaiman et al., 2012 ou des variants de cette dernière.
Dans un autre cas, l’enzyme est une lipase, préférablement issue de Ideonella sakaiensis. De manière alternative, l’enzyme peut être sélectionnée parmi les enzymes commerciales telle que Novozym 51032 ou des variants de ces enzymes.
Il est bien entendu possible de charger le réacteur avec plusieurs enzymes, et notamment au moins deux enzymes parmi celles évoquées ci-dessus.
Dans un cas particulier, l’enzyme (ou les enzymes) est sélectionnée parmi les enzymes ayant une séquence en acides aminés présentant au moins 75% d’identité avec SEQ ID N°l et/ou avec SEQ ID N°2 et/ou avec SEQ ID N°3 et/ou avec SEQ ID N°4 et/ou SEQ ID N°5, et ayant une activité de dépolymérisation du PET. Dans un cas particulier, l’enzyme est sélectionnée parmi les enzymes ayant une séquence en acides aminés présentant au moins 75% d’identité avec SEQ ID N°l, et une activité de dépolymérisation du PET.
Dans un mode particulier l’enzyme est apte à dépolymériser le polymère jusqu’aux oligomères, dans ce cas-là elle est avantageusement associée à une enzyme apte à dépolymériser lesdits oligomères en monomères. Dans un exemple particulier, les deux enzymes sont alors sélectionnées parmi les enzymes ayant une séquence en acides aminés présentant au moins 75% d’identité avec SEQ ID N°4 et/ou SEQ ID N°5.
L’inventeur a identifié que le procédé de l’invention était particulièrement adapté dans le cas particulier où l’enzyme sélectionnée a une séquence en acides aminés présentant au moins 90% d’identité avec SEQ ID N°l et comprenant au moins une combinaison de mutations
sélectionnée parmi F208I + D203C + S248C + Y92G, F208W + D203C + S248C + Y92G ou F208I + D203C + S248C + VI 701 +Y92G par rapport à la SEQ ID N°l.
Avantageusement, le temps tD est inférieur ou égal à 20h, préférentiellement inférieur ou égal à l8h, l6h, l4h, l2h, lOh. Dans un mode de mise en œuvre, le temps tD est compris entre lh et l6h, préférentiellement entre lh et lOh. Inversement, le temps de cristallisation tR est préférentiellement supérieur ou égal à 20h, préférentiellement supérieur ou égal à l8h, l6h, l4h, l2h, lOh.
Dans un mode de mise en œuvre particulier, le temps tR correspond au temps nécessaire pour que ledit PET, présentant une cristallinité initiale inférieure ou égale à 25%, atteigne une cristallinité de 30%, ou moins de 30%, à ladite température T.
Ainsi, dans un mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- le PET présente un degré de cristallinité initial d’au plus 25% ;
- l’étape de dépolymérisation est conduite à une température T égale à la Tg +/- l0°C dudit PET, et
- l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité de 30%, ou moins de 30%, à ladite température T.
Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Ainsi, dans un mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- on sélectionne un PET présentant un degré de cristallinité initial d’au plus 25% ;
- on sélectionne une enzyme apte à dégrader le PET, de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité de 30%, ou moins, à ladite température T ; et
- on réalise une étape de dépolymérisation enzymatique dudit PETpar mise en contact dudit PET avec ladite enzyme à une température T égale à la Tg +/- l0°C dudit PET.
Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Dans un mode préféré, le temps tD correspond au temps nécessaire à ladite enzyme pour dépolymériser au moins 85% dudit PET à ladite température T, préférentiellement au moins 90%.
Ainsi, dans un mode de mise en œuvre préféré, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- le PET présente un degré de cristallinité initial d’au plus 25% ;
- l’étape de dépolymérisation est conduite à une température T égale à la Tg +/- lO°C dudit PET, et
- l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 85% dudit PET à ladite température T, préférentiellement au moins 90%, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35%, préférentiellement au plus 30% à ladite température T.
Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+lO°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Dans un mode de mise en œuvre préféré, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- on sélectionne un PET présentant un degré de cristallinité initial d’au plus 25% ;
- On sélectionne une enzyme apte à dépolymériser le PET, de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 85% dudit PET à ladite température T, préférentiellement au moins 90%, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35%, préférentiellement un taux de cristallinité d’au plus 30% à ladite température T ; et
- on réalise une étape de dépolymérisation dudit PET par mise en contact de ladite enzyme avec ledit PET à une température T égale à la Tg +/- l0°C dudit PET.
Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Plus généralement, le procédé de dépolymérisation enzymatique de PET selon l’invention comprend les étapes selon lesquelles :
- on sélectionne un PET présentant un degré de cristallinité initial d’au plus 25% ;
- on sélectionne une enzyme apte à dégrader le PET, de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à ladite enzyme pour dépolymériser au moins 80% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité de 35%, ou moins de 35%, à ladite température T
- on réalise l’étape de dépolymérisation par mise en contact de l’enzyme avec le PET, à une température T égale à la Tg +/- lO°C dudit PET.
Etape de dépolymérisation
L’étape de dépolymérisation selon l’invention est avantageusement mise en œuvre dans un réacteur dont le volume est supérieur à 500 millilitres (mL), supérieur à 1 litre (L), préférentiellement supérieur à 2 L, 5 L, 10 L. Dans un mode de réalisation particulier, le procédé de l’invention peut être mis en œuvre à l’échelle industrielle et/ou semi-industrielle. Il est ainsi possible d’utiliser un réacteur dont le volume est supérieur à 100L, 150L, 1000L, 10 000 L, 100 000 L, 400 000 L. Selon l’invention, il est possible de charger le réacteur destiné à la réalisation de l’étape de dépolymérisation directement en PET, ou en matériaux plastiques contenant au moins le PET.
Selon l’invention, la quantité d’enzyme engagée pendant l’étape de dépolymérisation est avantageusement suffisante pour permettre une dépolymérisation totale ou quasi-totale dudit PET (i.e., dégradation à hauteur au moins de 80% en poids par rapport au poids dudit PET engagé) dans des temps de réaction compatibles avec une mise en œuvre à l’échelle industrielle.
Dans un mode de réalisation, le ratio en poids quantité d’enzyme engagée sur quantité de PET engagée est compris entre 0,01/1000 et 3/1000. Préférentiellement le ratio quantité d’enzyme engagée sur quantité de PET engagée est compris entre 0,5/1000 et 2,5/1000, plus préférentiellement entre 1/1000 et 2/1000. Dans un cas particulier, la quantité d’enzyme engagée est supérieure ou égale à la quantité d’enzyme nécessaire pour atteindre une concentration saturante en enzyme. Dans un cas particulier, l’enzyme peut être engagée sous la forme d’une composition comprenant en plus de l’enzyme des excipients, pouvant être sélectionnés parmi les tampons communément utilisés en biochimie, des conservateurs, et/ou des agents stabilisants. La quantité d’enzyme désigne alors avantageusement la quantité d’enzyme exempte de tout excipient.
Selon l’invention, l’étape de dépolymérisation du PET est conduite à une température T égale à la Tg +/- l0°C dudit PET, la Tg étant celle dudit PET avant l’étape de dépolymérisation. De manière avantageuse, la température est maintenue en-dessous de la température d’inactivation
de l’enzyme. Dans un mode particulier, l’étape de dépolymérisation du PET est conduite à une température T comprise entre la Tg- lO°C et la Tg +5°C du PET. Dans un autre mode particulier, l’étape de dépolymérisation est conduite à une température T comprise entre la Tg- 8°C et la Tg +2°C du PET. Dans un autre mode particulier, l’étape de dépolymérisation est conduite à une température T comprise entre la Tg- lO°C et la Tg -5°C du PET.
Dans un mode particulier, le PET a une Tg de 78°C+/-2°C et l’étape de dépolymérisation est réalisée à une température T égale à 70°C +/-2°C. Dans un autre mode particulier, le PET a une Tg de 78°C+/-2°C et l’étape de dépolymérisation est réalisée à une température T égale à 72°C +/-2°C. Dans un autre mode particulier, le PET a une Tg de 75°C+/-2°C et l’étape de dépolymérisation est réalisée à une température T égale à 68°C +/-2°C. Dans un autre mode particulier, le PET a une Tg de 75°C+/-2°C et l’étape de dépolymérisation est réalisée à une température T égale à 70°C +/-2°C. Dans un autre mode particulier, le PET a une Tg comprise entre 70°C+/-2°C et 75°C +/-2°C et l’étape de dépolymérisation est réalisée à une température T comprise entre 65°C +/-2°C et 72°C +/-2°C. Dans un mode particulier, le PET est issu d’un matériau plastique sélectionné parmi des fibres et/ou des déchets fibres et/ou textiles et a une Tg comprise entre 60°C+/-l°C et 75°C +/-l°C, et l’étape de dépolymérisation est réalisée à une température T égale à 65°C +/-2°C. Dans un autre mode particulier, le PET est issu d’un matériau plastique sélectionné parmi des fibres et/ou des déchets fibres et/ou textiles et a une Tg comprise entre 60°C+/-l°C et 70°C +/-l°C et l’étape de dépolymérisation est réalisée à une température T égale à 60°C +/-2°C.
Dans un mode particulier, l’étape de dépolymérisation est réalisée à une température T comprise entre 66°C et 80°C, préférentiellement entre 68°C et 73°C. Dans un mode particulier, l’étape de dépolymérisation est réalisée à une température T de 72°C+/- l°C. Dans un autre mode particulier, l’étape de dépolymérisation est réalisée à une température T de 70°C+/- l°C. Ainsi, dans un mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- le PET présente un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 65°C+/-l°C et 80°C+/-l°C ;
- l’étape de dépolymérisation est conduite à une température T comprise entre 66°C et 80°C, préférentiellement entre 68°C et 73°C, et
- l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité de 35%, ou moins de 35%, à ladite température T.
Avantageusement, on sélectionne un PET présentant un taux de cristallinité initial d’au plus 25%, préférentiellement d’au plus 20%. Dans un mode de mise en œuvre particulier, on sélectionne un PET présentant un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 65°C+/-l°C et 80°C+/-l°C.
Dans un autre mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- le PET présente un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 65°C+/-l°C et 80°C+/-l°C;
- l’étape de dépolymérisation est conduite à une température T de 72°C+/- l°C, et
- l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80%, préférentiellement au moins 85%, plus préférentiellement au moins 90% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35% à ladite température T.
Préférentiellement, tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 30% à ladite température T. Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Dans un autre mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- on sélectionne un PET présentant un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 75°C+/-l°C et 80°C+/-l°C;
- l’étape de dépolymérisation est conduite à une température T de 72°C+/- l°C, et
- l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80%, préférentiellement au moins 85%, plus préférentiellement au moins 90% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35% à ladite température T. Préférentiellement, tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 30% à ladite température T. Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Dans un autre mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que - le PET présente un degré de cristallinité initial d’au plus 25% et une Tg comprise entre
65°C+/-l°C et 80°C+/-l°C;
- l’étape de dépolymérisation est conduite à une température T de 70°C+/- l°C, et
- l’enzyme est sélectionnée de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80%, préférentiellement au moins 85%, plus préférentiellement au moins 90% dudit PET
à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35% à ladite température T. Préférentiellement, tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 30% à ladite température T. Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Ainsi, avantageusement, dans ce mode de réalisation, on sélectionne un PET présentant un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 65°C+/-l°C et 80°C+/-l°C et l’étape de dépolymérisation est conduite à une température T de 70°C+/- l°C.
Dans un autre mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- on sélectionne un matériau plastique parmi des fibres et/ou des déchets fibres et/ou textiles comprenant du PET présentant un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 60°C+/-l°C et 75°C+/-l°C;
- on sélectionne une enzyme apte à dégrader le PET, de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80%, préférentiellement au moins 85%, plus préférentiellement au moins 90% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35% à ladite température T, et
- on réalise l’étape de dépolymérisation du PET par mise en contact de ladite enzyme avec ledit matériau plastique à une température T de 65°C+/- l°C.
Préférentiellement, tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité de 30% à ladite température T. Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Dans un autre mode de mise en œuvre particulier, le procédé de dépolymérisation enzymatique de polyéthylène téréphtalate (PET) selon l’invention est caractérisé en ce que
- on sélectionne un matériau plastique parmi des fibres et/ou des déchets fibres et/ou textiles comprenant du PET présentant un degré de cristallinité initial d’au plus 25% et une Tg comprise entre 60°C+/-l°C et 70°C+/-l°C;
- on sélectionne une enzyme apte à dégrader le PET, de manière à ce qu’un temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur à un temps de cristallisation (tR) dudit PET, dans lequel le temps tD représente le temps nécessaire à l’enzyme sélectionnée pour dépolymériser au moins 80%, préférentiellement au moins 85%, plus préférentiellement au moins 90% dudit PET à ladite température T, et le temps tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 35% à ladite température T, et
- on réalise l’étape de dépolymérisation du PET par mise en contact de ladite enzyme avec ledit matériau plastique à une température T de 60°C+/- l°C.
Préférentiellement, tR représente le temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 30% à ladite température T. Avantageusement, l’enzyme est sélectionnée parmi les enzymes ayant une Tm supérieure ou égale à la température T+l0°C, préférentiellement supérieure ou égale à la température T+l5°C, plus préférentiellement supérieure ou égale à la température T+20°.
Dans un mode particulier, le temps de cristallisation (tR) du PET est mesuré préalablement à l’étape de dépolymérisation, sur un échantillon dudit PET.
Selon l’invention, l’enzyme est sélectionnée de manière à ce que le temps de dépolymérisation (tD) du PET par ladite enzyme soit strictement inférieur au temps de cristallisation (tR) dudit PET. Préférentiellement, l’enzyme est sélectionnée de manière à ce que le temps tD corresponde au temps nécessaire à ladite enzyme pour dépolymériser au moins 90% dudit PET à ladite température T, et pour que le temps tR corresponde au temps nécessaire audit PET pour atteindre un taux de cristallinité d’au plus 30% à ladite température T. Dans un mode particulier, le temps tD est inférieur à 20h, préférentiellement inférieur à 18h, l6h, l4h, l2h, lOh. Dans un
autre mode particulier, le temps tD est compris entre lh et l6h, préférentiellement entre lh et lOh.
Selon l’invention, l’étape de dépolymérisation du PET est réalisée par une mise en contact dudit PET et de ladite enzyme sélectionnée à une température T. De manière avantageuse, le pH est régulé afin d’optimiser le rendement du procédé de dépolymérisation en fonction de la solubilité des monomères / oligomères. Dans un mode de réalisation particulier, le pH est régulé pour être maintenu au pH optimal de l’enzyme +/- 1. Particulièrement, le pH est ainsi régulé pour être maintenu entre 6,5 et 9. Dans un mode de mise en œuvre particulier, le pH est régulé entre 6,5 et 8,5 pendant l’étape de dépolymérisation, préférentiellement entre 7 et 8. Dans un autre cas particulier, le pH est régulé entre 7,5 et 8,5.
Selon l’invention, le contenu du réacteur est maintenu sous agitation pendant l’étape de dépolymérisation. La vitesse de l’agitation est régulée par l’homme de l’art de manière à être suffisante pour permettre une suspension du matériau plastique/polyester engagé dans le réacteur, une homogénéité de la température et une précision de la régulation du pH. Par exemple, la vitesse de l’agitation est maintenue entre 50 rpm et 500 rpm, notamment à 80 rpm,
100 rpm, 150 rpm, 200 rpm, 250 rpm, 300 rpm, 350 rpm, 350 rpm, 400 rpm, 450 rpm, 500 rpm.
EXEMPLES
Exemple 1 : Mesure du temps de cristallisation du PET
1 1 Amorphisation du PET du matériau plastique Le procédé de dépolymérisation est réalisé à partir de paillettes plastiques colorées et lavées issues de la filière de recyclage de déchets plastiques en PET. Ces matériaux plastiques, composés à 98% m/m (en poids) de PET avec un taux de cristallinité moyen de 34%, ont subi une étape d’extrusion, suivie d’un refroidissement rapide permettant l’amorphisation du PET contenu dans les déchets. L’extrudeuse utilisée pour l’amorphisation était une extrudeuse double vis KMB ZE 60A équipée d'une pompe à engrenage, d'un changeur de filtre, d'une filière et d’un système de coupe en tête sous eau. La température réglée était à 265°C dans les zones de l'extrudeuse, à 280°C dans la pompe à engrenage, à 280°C dans les zones de changeur de filtre et à 360°C dans la filière. L’eau utilisée dans le système de granulation a été régulée à une
température de 80°C. Pour introduire les paillettes, un système de dosage gravimétrique commercialisé par Brabender a été utilisé. Un débit de 150 kg / h a été utilisé. Pour la granulation, une filière comportant 120 trous de 0,8 mm de diamètre a été utilisée. La vitesse de coupe était de 4500 tr / min. L’amorphisation a permis d’obtenir des granulés de taille inférieure à 1 mm dont le degré de cristallinité a été mesuré à 16% (par DSC). Les granulés ont ensuite subi une étape de réduction en poudre à l’aide d’un pulvérisateur à disques. La poudre a été soumise à un tamis de 400mhi pour ne récupérer que les poudres de taille inférieure. Le taux de cristallinité de cette poudre a été déterminé à 16% conformément à l’exemple 1.2 ci- dessous. L2 Mesure de la Tg et du degré de cristallinité du PET
Pour l’analyse DSC, un appareil Mettler Toledo DSC 3 a été utilisé avec un flux d’air sec. Seul le premier balayage en température a été réalisé pour déterminer les caractéristiques thermiques de la poudre de PET, à partir d’un échantillon de poudre issue de l’Exemple 1.1, en particulier la température de transition vitreuse (Tg) et le niveau de cristallinité initial. La montée en température a été effectuée de 25°C à 280 ° C avec une vitesse de chauffe de 10 ° C / min avec environ 10 mg d’échantillon en utilisant un creuset en aluminium de 40 pL.
La Tg a été déterminée, à l’aide du logiciel STARe Mettler Toledo, au milieu de la transition vitreuse représentée sur le thermogramme de l’échantillon, et le degré de cristallinité initial conformément à l’équation détaillée dans la description. La Tg de la poudre de PET produite dans l’Example 1.1 a été évaluée à 78,4°C.
1.3 Mesure de la cinétique de cristallisation du PET du matériau plastique
5 g de poudre issue de l’Exemple 1.1 (matériaux plastiques contenant du PET) et 20 ml d’eau ont été mélangés dans un flacon de 40 ml. Le flacon fermé a ensuite été immergé dans un bain- marie réglé à la température T voulue d’incubation. Des prélèvements à différents intervalles de temps ont été effectués. La poudre prélevée a été déposée sur un papier absorbant pour un séchage à l’air ambiant pendant au moins l2h. Une analyse DSC a ensuite été effectuée sur environ 10 mg d’échantillon pour évaluer le taux de cristallinité comme indiqué dans l’exemple 1.2.
La Figure 1 montre l’évolution de la cristallinité du PET en fonction du temps, à différentes températures : 65°C, 70°C, 72°C, 75°C.
A 65°C la cristallinité du PET dans la poudre de l’exemple 1.1 évolue très peu et, après 72h à 65°C, la cristallinité reste en dessous de 20% (données non montrées). Ce sera ainsi également le cas pour les températures inférieures à 65°C.
A 70°C, 72°C et 75°C, le PET atteint 35% de cristallinité au bout de respectivement l7,5h ; 11 ,5h et 5h. A 70°C, 72°C et 75°C, le PET atteint 30% de cristallinité au bout de respectivement l6h ; lOh et 4,3 h.
Exemple 2 : Evaluation des températures de fusion (Tm) des enzymes 2 1 Production des enzymes
Les gènes ont été exprimés dans des cellules compétentes de E. coli BL21 (DE3) (New England Biolabs, Ipswich, MA) par culture dans un milieu auto-inductible ZYM (Studier et al., 2005 - Prot. Exp. Pur. 41, 207-234) pendant 23 heures à 2l°C. Les cellules de E. coli ont été récoltées par centrifugation (6 000 x g, 10 min à 4°C) et mises en suspension dans du tampon de lyse (Tris-HCl 20 mM, pH 8, NaCl 300 mM). Les cellules ont été cassées par sonication sur glace et le lysat a été clarifié par centrifugation (10 000 x g, 30 min à 4°C). La fraction soluble a été soumise à une résine à affinité métallique TALON (Clontech, CA). Après lavage des protéines non liées avec le tampon de lyse additionné d'imidazole 10 mM, les protéines liées ont été éluées avec un tampon d'élution (Tris-HCl 20 mM, pH 8, NaCl 300 mM, imidazole 100 mM). Le tampon a finalement été échangé pour un tampon de stockage (Tris-HCl 20 mM, pH 8, NaCl 300 mM) par dialyse. La concentration en protéines purifiées a été déterminée sur la base du coefficient d'extinction molaire calculé à 280 nm.
2 2 Evaluation de la Tm
La DSL a été utilisée pour évaluer les températures de fusion (Tm) des enzymes utilisées. Des échantillons de protéines ont été préparés à une concentration de 14 mM (0,4 mg/mL) et conservés dans un tampon constitué de Tris HCl 20 mM, pH 8,0, NaCl 300 mM. La solution mère SYPRO Orange Dye 5000x DMSO a d’abord été diluée 250 fois dans de l’eau. Les
échantillons de protéines ont été chargés sur une plaque PCR 96 puits (Lifescience Bio-Rad, France, cat# HSP9601), chaque puits contenant un volume final de 25 pL. La concentration finale de protéine et de colorant SYPRO Orange dans chaque puits était respectivement de 5mM (0,14 mg/ml) et 10 x. Les volumes chargés par puits étaient les suivants : 15 pL de tampon, 9 pL de la solution protéique à 0,4 mg/mL et 1 pL de la solution diluée 250 x SYPRO Orange. Les plaques PCR ont ensuite été scellées avec une bande adhésive de qualité optique et centrifugées à 2000 tour/min pendant 1 min à température ambiante. Des expériences DSF ont ensuite été effectuées en utilisant un système PCR en temps réel Bio-Rad CFX96 réglé sur le canal FRET pour utiliser les filtres d'excitation 450/490 et d'émission 560/580. Les échantillons ont été chauffés de 25 à l00°C à une vitesse de l°C/min. Une mesure de fluorescence a été effectuée tous les 0,3°C. La température de fusion a été déterminée à partir du (des) pic (s) des premières dérivées de la courbe de fusion en utilisant le logiciel Bio-Rad CFX Manager. Les valeurs de Tm correspondent à la moyenne de 3 mesures.
Tableau 1 : Température de fusion en fonction des enzymes
Exemple 3 : Procédé de dépolymérisation en réacteur
Le procédé a été réalisé dans un bioréacteur de 500 ml Minibio (Applikon Biotechnology, Delft, Pays-Bas). 0,69 pmol à 1,10 pmol de protéine purifiée (produite conformément à l’Exemple 2.1.) préparée dans 80 ml de tampon phosphate de potassium 100 mM, pH 8, ont été combinés à 20 g de la poudre contenant le PET préparée selon l’Exemple 1 (Xc = 16%, Tg = 78,4°C). La régulation de la température a été effectuée par immersion dans un bain d’eau et une seule turbine marine a été utilisée pour maintenir une agitation constante à 250 tour/min. Le pH a été régulé à 8 avec du NaOH 6 N et assuré par le système de contrôle my-Control bio (Applikon
Biotechnology, Delft, Pays-Bas), et la consommation de base a été enregistrée pendant la durée du procédé.
La caractérisation du taux de dépolymérisation du PET a été réalisée via le prélèvement régulier d’échantillons soumis à une analyse par chromatographie en phase liquide à ultra haute performance (UHPLC) pour mesure de la quantité d’équivalent acide téréphtalique produit selon la méthode décrite ci-dessous. La quantité d’acide téréphtalique produite peut également être estimée via la quantité de base rajoutée dans le milieu au cours de la réaction.
La concentration en équivalent AT a été déterminée par chromatographie (UHPLC). Si nécessaire (en présence d’AT insoluble), les échantillons ont été dilués dans du tampon phosphate de potassium 100 mM, pH 8. 150 pL de méthanol et 6,5 pL de HCl 6 N ont été ajoutés à 150 pL d’échantillon ou de dilution. Après homogénéisation et filtration à travers un filtre à seringue de 0,45 pm, 20 pL d’échantillon ont été injectés dans l’UHPLC, système Ultimate 3000 UHPLC (Thermo Lisher Scientifïc, Waltham, MA) comprenant un module de pompe, un échantillonneur automatique, un four à colonne thermostaté à 25°C et un détecteur UV à 240 nm. L’acide téréphtalique (AT) et les molécules produites (MHET et BHET) ont été séparés en utilisant un gradient de méthanol (30% à 90%) dans du H2S04 1 mM à 1 m/min à travers une colonne HPLC Discovery HS C18 (150 mm x 4,6 mm, 5 pm) équipée d'un précolonne (Supelco, Bellefonte, PA). Le AT, le MHET et le BHET ont été mesurés selon des courbes standard préparées à partir du AT et du BHET du commerce et du MHET synthétisé en interne. L’équivalent AT correspond à la somme du AT mesuré et du AT contenu dans les MHET et BHET mesurés.
Les enzymes de l’exemple 2 ont été testées à différentes températures (70°C +/- l°C et 72°C +/-1 °C) afin d’évaluer lesquelles pouvaient être sélectionnées pour mettre en œuvre le procédé de l’invention à ces différentes températures. Les enzymes ont ainsi été testées à une concentration saturante. Des tests à une température de 60°C ont également été réalisés, la température de 60°C correspondant à la température traditionnellement utilisée dans les procédés de dépolymérisation de l’art antérieur (contrôle négatif).
Pour rappel, les temps de cristallisation tR du PET issu de l’exemple 1.1 pour atteindre 30% et 35% de cristallinité sont respectivement de l6h et l7,5h à 70°C, et lOh et 11 ,5h à 72°C.
Les tableaux 2, 3, 4 et 5 ci-dessous indiquent respectivement la mesure des temps tD des enzymes El, E2, E3, et E4 à différentes températures.
Tableau 2 : Mesure des temps tD de El à 60°C (contrôle) et 72°.
Pour El, tD est ainsi supérieur à tR à 72°C. L’enzyme ne peut donc pas être sélectionnée pour la mise en œuvre du procédé de l’invention. Une des raisons est qu’elle n’est pas suffisamment stable et/ou active pour atteindre 80% de conversion avant que le PET n’ait atteint un taux de cristallinité supérieur à 30%.
Tableau 3 : Mesure des temps tD de E2 à 60°C (contrôle) et 72°C.
L’enzyme E2 peut être sélectionnée pour mettre en œuvre le procédé de l’invention à 72°C permettant une amélioration significative du rendement par rapport à un procédé à 60°C (diminution par 2,3 du temps pour atteindre 90% de dépolymérisation). E2 a à la fois une Tm suffisamment élevée (> T + 20°C) et un tD suffisamment bas pour atteindre 80% de dépolymérisation avant que le PET n’ait atteint une cristallinité trop élevée (tR pour atteindre 30% de cristallinité = lOh) à 72°C.
Tableau 4 : Mesure des temps t
De manière équivalente à E2, E3 peut être sélectionnée pour mettre en œuvre le procédé de l’invention à 72°C.
Tableau 5 : Mesure des temps tD de E4 à 60°C (contrôle), 70°C et 72°C.
De manière équivalente à E2 et E3, E4 peut également être sélectionnée pour mettre en œuvre le procédé de l’invention à 70°C et à 72°C, permettant une amélioration significative du rendement par rapport à un procédé à 60°C. Exemple 4 : Procédé de dégradation d’un matériau plastique issu de déchets textiles comprenant du PET
4.1 Mesure du temps de cristallisation ftR) du PET issu de déchets textiles
4.1.1 Amorphisation du PET du matériau plastique issu de déchets textiles et mesure du degré de cristallinité du PET Le procédé de dépolymérisation est réalisé à partir de rebus de production d’un procédé de tissage à jet d’eau, dont la matière est sous forme d’amas de fils continus et contient environ 100% de PET. Ces matières textiles ont subi une étape de séchage à 60°C pendant l6h puis une étape d’extrusion, suivie d’un refroidissement rapide permettant l’amorphisation du PET contenu dans les déchets. L’extrudeuse utilisée pour l’amorphisation était une extrudeuse double vis ZSE 18 MAXX de chez Leistritz. Les températures des zones de chauffe ont été réglées selon le profil suivant :
265oC-265oC-265oC-255oC-255oC-250oC-250oC-245oC-245oC-245°C
La vitesse de rotation des vis a été réglée à 150 rpm. L’introduction de la matière dans l’extrudeuse a été effectuée manuellement. Le jonc arrivant en tête d’extrudeuse est ensuite immédiatement immergé dans un bain d’eau à l0°C. Le jonc obtenu a été granulé puis réduit à l’état de poudre fine à l’aide d’un microniseur (grille lmm). La poudre a ensuite été soumise à un tamis de 500mhi pour ne récupérer que les poudres inférieures à cette taille. La cristallinité de la poudre a été déterminée, conformément à l’exemple 1.2, comme étant inférieure à 10%.
4.1.2 Mesure de la cinétique de cristallisation du PET du matériau plastique
La mesure du temps de cristallisation (tR) du PET issu de déchets textiles a été réalisé avec le même protocole que l’exemple 1.3. A 68°C la cristallinité du PET dans la poudre obtenue dans l’exemple 4.1 évolue très peu et, après 29h à 68°C, la cristallinité reste inférieure à 20%. Il en est de même à 60°C.
4.1.3 Mesure de la T g du PET
La mesure de la Tg du PET a été réalisée avec le même protocole que l’exemple 1.2. La Tg de la poudre de PET produite dans l’Example 4.1.1 a été évaluée à 75,7°C.
4 2 Sélection de l’enzyme par un procédé de dépolymérisation en réacteur du matériau plastique PET issu de déchets textiles.
Pour les tests de dépolymérisation, un réacteur à fond bombé d’un volume total de 5L (Global Process Concept) a été utilisé. Le réacteur était équipé d’une sonde température et d’une sonde pH (Hamilton, EasyFerm HB BioArc 325). La régulation de ces deux paramètres aux valeurs de consignes était assurée par des contrôleurs PID interne au logiciel C-bio (Global Process Concept). Une pâle marine de diamètre 5.5 cm fixé à l’arbre central tournant à 300 rpm a permis l’agitation du milieu réactionnel.
Pour tous les tests, le pH est régulé à 8.0 par ajout d’hydroxyde de sodium à 20% m.m. L’enzyme E4 a été ajoutée selon un ratio en poids de 1/1000 par quantité de PET engagée. Elle a été produite par fermentation d’un microorganisme recombinant en milieu liquide. Le tableau 6 ci-dessous indique respectivement la mesure des temps tD de l’enzyme E4 sur le matériau plastique défini en 4.1.1 à différentes températures.
Tableau 6 : Mesure des temps tD de E4 à 60°C et à 68°C.
tD restant inférieur à tR à 68°C, E4 peut donc être sélectionnée pour mettre en œuvre le procédé de l’invention à 68°C sur le matériau plastique défini en 4.1.1 tout en permettant une amélioration significative du rendement par rapport à un procédé à 60°C.
Exemple 5 : Procédé de dégradation d’un matériau plastique, issus de déchets plastiques. Sélection et montée en échelle.
5.1 Mesure du temps de cristallisation (tR) du PET issu de déchets plastiques
5.1.1 Amorphisation du PET du matériau plastique issu de déchets plastiques et mesure du degré de cristallinité du PET
L’extrudeuse utilisée pour l’amorphisation était une extrudeuse double vis KMB ZE 60A équipée d'une pompe à engrenage, d'un changeur de filtre, d'une filière et d’un système de coupe en tête sous eau. La température était réglée à 265°C dans les zones de l'extrudeuse, à 275°C dans la pompe à engrenage, à 275°C dans les zones de changeur de filtre et à 350 °C dans la filière. La vitesse de rotation des vis était de 160 rpm. L'eau utilisée dans le système de granulation a été régulée à une température de 80°C. Pour introduire les paillettes, 2 systèmes de dosage gravimétrique commercialisés par Brabender ont été utilisés. Un débit de 300 kg / h a été utilisé. Pour la granulation, une filière comportant 240 trous de 0,75 mm de diamètre a été utilisée. La vitesse de coupe était de 3800 tr / min. L’amorphisation a permis d’obtenir des granulés de taille inférieure à 1 mm dont le degré de cristallinité a été mesuré à 12% (par DSC). Les granulés ont ensuite subi une étape de réduction en poudre à l’aide d’un pulvérisateur à disques. La poudre a été soumise à un tamis de 500mhi pour ne récupérer que les poudres de taille inférieure. La cristallinité de la poudre a été déterminé, conformément à l’exemple 1.2, comme étant égale à 16.5% (DSC).
5.1.2 Mesure de la T g du PET
La mesure de la Tg du PET a été réalisée avec le même protocole que l’exemple 1.2. La Tg de la poudre de PET produite dans l’Example 5.1.1 a été évaluée à 75,2°C.
5.1.3 Mesure de la cinétique de cristallisation du PET du matériau plastique
La mesure du temps de cristallisation (tR) du PET issu du matériau plastique a été réalisée selon le même protocole que l’exemple 1.3. A 60°C et 66°C la cristallinité du PET dans la poudre obtenue dans l’exemple 5.1 évolue très peu et, après 30h à 60°C ou 66°C, la cristallinité reste inférieure à 22%. A 72°C, elle atteint 30% en l8h (tR).
5.2 Sélection de l’enzyme par un procédé de dépolymérisation en réacteur du matériau plastique PET issu de déchets plastiques.
Pour le test A, un réacteur agité à fond plat, d’un volume total de 500 mL (MiniBioréacteurs, Global Process Concept) a été utilisé. Il était équipé d’une sonde température et d’une sonde pH (Hamilton, EAsyFerm HB BioArc 120). La régulation de ces deux paramètres aux valeurs de consignes était assurée par des contrôleurs PID internes au logiciel C-bio (Global Process Concept). Une pâle marine de diamètre 3 cm fixée à l’arbre central tournant à 300 rpm a permis l’agitation du milieu réactionnel.
Pour les tests B et C, un réacteur à fond bombé d’un volume total de 5L (Global Process Concept) a été utilisé comme décrit dans l’Exemple 4.2.
Pour tous les tests, le pH est régulé à 8.0 par ajout d’hydroxyde de sodium à 20% m.m. L’enzyme E4 a été ajoutée selon un ratio en poids de 1/1000 par quantité de PET engagée Elle a été produite par fermentation d’un microorganisme recombinant en milieu liquide.
Le tableau 7 ci-dessous indique respectivement la mesure des temps tD de l’enzyme E4 à différentes températures.
Tableau 7 : Mesure des temps tD de E4 à différentes températures tD restant inférieur à tR, E4 peut donc être sélectionnée pour mettre en œuvre le procédé de l’invention à ces deux températures sur le matériau plastique défini en 5.1.1. On notera que
l’utilisation de E4 à 66°C et72°C devrait permettre une amélioration significative du rendement par rapport à un procédé à 60°C.
5.3 Validation de la montée en échelle
Les étapes précédentes ayant permis de valider que l’enzyme E4 peut être sélectionnée, le procédé peut être mis en œuvre selon l’invention.
Pour ce test (D), un réacteur à fond plat d’un volume total de 1000 L a été utilisé. Le réacteur était équipé d’une sonde température et d’une sonde pH (In Pro3 l00/SG/325, Mettler Toledo). Une pâle marine de diamètre variable a permis l’agitation du milieu réactionnel. Le pH est régulé à 8.0 par ajout d’hydroxyde de sodium à 20% m.m. L’enzyme E4 a été ajoutée selon un ratio en poids de 2/1000 par quantité de PET engagée. Elle a été produite par fermentation d’un microorganisme recombinant en milieu liquide.
La dégradation réalisée à une température de 66°C est suivie selon les mêmes méthodes que décrits précédemment.
Ainsi les taux de 80% et 90% de dégradation sont obtenus respectivement au bout de l4h et 24h.
Les résultats obtenus sur des volumes semi industriels sont ainsi cohérents avec ceux obtenus lors de la sélection de l’enzyme. On notera qu’ avantageusement, l’utilisation de plus gros volumes permet une meilleure agitation et ainsi une amélioration des rendements.






