WO2014133014A1 - 単核ルテニウム錯体およびそれを使用した有機合成反応 - Google Patents
単核ルテニウム錯体およびそれを使用した有機合成反応 Download PDFInfo
- Publication number
- WO2014133014A1 WO2014133014A1 PCT/JP2014/054715 JP2014054715W WO2014133014A1 WO 2014133014 A1 WO2014133014 A1 WO 2014133014A1 JP 2014054715 W JP2014054715 W JP 2014054715W WO 2014133014 A1 WO2014133014 A1 WO 2014133014A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- ruthenium complex
- compound
- carbon atoms
- mononuclear ruthenium
- Prior art date
Links
- 239000012327 Ruthenium complex Substances 0.000 title claims abstract description 99
- 238000003786 synthesis reaction Methods 0.000 title description 8
- 239000003054 catalyst Substances 0.000 claims abstract description 60
- 125000001424 substituent group Chemical group 0.000 claims abstract description 48
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 36
- 125000003118 aryl group Chemical group 0.000 claims abstract description 29
- 125000003710 aryl alkyl group Chemical group 0.000 claims abstract description 28
- 238000006459 hydrosilylation reaction Methods 0.000 claims abstract description 27
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 24
- 238000005984 hydrogenation reaction Methods 0.000 claims abstract description 23
- 239000003446 ligand Substances 0.000 claims abstract description 19
- 150000001728 carbonyl compounds Chemical class 0.000 claims abstract description 16
- 125000005843 halogen group Chemical group 0.000 claims abstract description 12
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 claims abstract description 10
- 238000004132 cross linking Methods 0.000 claims abstract description 9
- 229910000073 phosphorus hydride Inorganic materials 0.000 claims abstract description 5
- 230000000694 effects Effects 0.000 claims abstract description 3
- -1 alkane compound Chemical class 0.000 claims description 214
- 125000004432 carbon atom Chemical group C* 0.000 claims description 75
- 150000001875 compounds Chemical class 0.000 claims description 42
- 238000006243 chemical reaction Methods 0.000 claims description 31
- 238000006722 reduction reaction Methods 0.000 claims description 23
- 125000002947 alkylene group Chemical group 0.000 claims description 17
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 16
- 150000001336 alkenes Chemical class 0.000 claims description 15
- 125000003545 alkoxy group Chemical group 0.000 claims description 15
- 238000000034 method Methods 0.000 claims description 13
- 150000001412 amines Chemical class 0.000 claims description 10
- 229910000077 silane Inorganic materials 0.000 claims description 10
- 150000003573 thiols Chemical class 0.000 claims description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 9
- 125000000611 organothio group Chemical group 0.000 claims description 9
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 claims description 8
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 claims description 8
- 125000001931 aliphatic group Chemical group 0.000 claims description 8
- 230000015572 biosynthetic process Effects 0.000 claims description 7
- 150000002576 ketones Chemical class 0.000 claims description 7
- 125000002030 1,2-phenylene group Chemical group [H]C1=C([H])C([*:1])=C([*:2])C([H])=C1[H] 0.000 claims description 6
- 150000001299 aldehydes Chemical class 0.000 claims description 6
- 150000001345 alkine derivatives Chemical class 0.000 claims description 6
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 claims description 5
- RBFQJDQYXXHULB-UHFFFAOYSA-N arsane Chemical compound [AsH3] RBFQJDQYXXHULB-UHFFFAOYSA-N 0.000 claims description 5
- 125000004429 atom Chemical group 0.000 claims description 5
- 150000002466 imines Chemical class 0.000 claims description 5
- 150000002527 isonitriles Chemical class 0.000 claims description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 150000002825 nitriles Chemical class 0.000 claims description 4
- 229910052707 ruthenium Inorganic materials 0.000 claims description 4
- 230000008569 process Effects 0.000 claims description 3
- 230000009467 reduction Effects 0.000 abstract description 10
- 238000005481 NMR spectroscopy Methods 0.000 description 39
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 30
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 27
- 239000000047 product Substances 0.000 description 25
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 22
- 239000012300 argon atmosphere Substances 0.000 description 21
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 18
- 125000000732 arylene group Chemical group 0.000 description 16
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 15
- 239000012298 atmosphere Substances 0.000 description 14
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 14
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical compound CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 12
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 12
- 229940052810 complex b Drugs 0.000 description 12
- 239000001257 hydrogen Substances 0.000 description 12
- 229910052739 hydrogen Inorganic materials 0.000 description 12
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 11
- 125000004104 aryloxy group Chemical group 0.000 description 11
- 229910002091 carbon monoxide Inorganic materials 0.000 description 11
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 10
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 10
- 239000002904 solvent Substances 0.000 description 10
- 125000002102 aryl alkyloxo group Chemical group 0.000 description 9
- 238000001816 cooling Methods 0.000 description 9
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 9
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 8
- 230000003197 catalytic effect Effects 0.000 description 8
- OIKHZBFJHONJJB-UHFFFAOYSA-N dimethyl(phenyl)silicon Chemical compound C[Si](C)C1=CC=CC=C1 OIKHZBFJHONJJB-UHFFFAOYSA-N 0.000 description 8
- XUKFPAQLGOOCNJ-UHFFFAOYSA-N dimethyl(trimethylsilyloxy)silicon Chemical compound C[Si](C)O[Si](C)(C)C XUKFPAQLGOOCNJ-UHFFFAOYSA-N 0.000 description 8
- 238000010438 heat treatment Methods 0.000 description 8
- ILPBINAXDRFYPL-UHFFFAOYSA-N 2-octene Chemical compound CCCCCC=CC ILPBINAXDRFYPL-UHFFFAOYSA-N 0.000 description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 7
- TVMXDCGIABBOFY-UHFFFAOYSA-N n-Octanol Natural products CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 7
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 7
- 229920001296 polysiloxane Polymers 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 6
- 238000007259 addition reaction Methods 0.000 description 6
- 150000001408 amides Chemical class 0.000 description 6
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cyclohexene Chemical compound C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 5
- 235000002597 Solanum melongena Nutrition 0.000 description 5
- 238000002329 infrared spectrum Methods 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- RGSFGYAAUTVSQA-UHFFFAOYSA-N pentamethylene Natural products C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 5
- 150000003303 ruthenium Chemical class 0.000 description 5
- 125000004434 sulfur atom Chemical group 0.000 description 5
- CTMHWPIWNRWQEG-UHFFFAOYSA-N 1-methylcyclohexene Chemical compound CC1=CCCCC1 CTMHWPIWNRWQEG-UHFFFAOYSA-N 0.000 description 4
- WGLLSSPDPJPLOR-UHFFFAOYSA-N 2,3-dimethylbut-2-ene Chemical compound CC(C)=C(C)C WGLLSSPDPJPLOR-UHFFFAOYSA-N 0.000 description 4
- OCGXPFSUJVHRHA-UHFFFAOYSA-N 4-methoxy-n,n-dimethylbenzamide Chemical compound COC1=CC=C(C(=O)N(C)C)C=C1 OCGXPFSUJVHRHA-UHFFFAOYSA-N 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- 229910052786 argon Inorganic materials 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 239000012043 crude product Substances 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- SWGZAKPJNWCPRY-UHFFFAOYSA-N methyl-bis(trimethylsilyloxy)silicon Chemical compound C[Si](C)(C)O[Si](C)O[Si](C)(C)C SWGZAKPJNWCPRY-UHFFFAOYSA-N 0.000 description 4
- COCAUCFPFHUGAA-MGNBDDOMSA-N n-[3-[(1s,7s)-5-amino-4-thia-6-azabicyclo[5.1.0]oct-5-en-7-yl]-4-fluorophenyl]-5-chloropyridine-2-carboxamide Chemical compound C=1C=C(F)C([C@@]23N=C(SCC[C@@H]2C3)N)=CC=1NC(=O)C1=CC=C(Cl)C=N1 COCAUCFPFHUGAA-MGNBDDOMSA-N 0.000 description 4
- 229910000510 noble metal Inorganic materials 0.000 description 4
- 239000003960 organic solvent Substances 0.000 description 4
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- PJANXHGTPQOBST-VAWYXSNFSA-N trans-stilbene Chemical compound C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 4
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 3
- MUUXBTFQEXVEEI-UHFFFAOYSA-N [2-(dimethyl-$l^{3}-silanyl)phenyl]-dimethylsilicon Chemical compound C[Si](C)C1=CC=CC=C1[Si](C)C MUUXBTFQEXVEEI-UHFFFAOYSA-N 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 3
- 239000003638 chemical reducing agent Substances 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- XNMQEEKYCVKGBD-UHFFFAOYSA-N dimethylacetylene Natural products CC#CC XNMQEEKYCVKGBD-UHFFFAOYSA-N 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 230000001747 exhibiting effect Effects 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 239000011261 inert gas Substances 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 125000004430 oxygen atom Chemical group O* 0.000 description 3
- 229910052763 palladium Inorganic materials 0.000 description 3
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000004344 phenylpropyl group Chemical group 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 229910052703 rhodium Inorganic materials 0.000 description 3
- 238000010898 silica gel chromatography Methods 0.000 description 3
- 150000003568 thioethers Chemical class 0.000 description 3
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 2
- ZGEGCLOFRBLKSE-UHFFFAOYSA-N 1-Heptene Chemical compound CCCCCC=C ZGEGCLOFRBLKSE-UHFFFAOYSA-N 0.000 description 2
- DJGIITKNTHQYPX-UHFFFAOYSA-N 1-benzylazepan-2-one Chemical compound O=C1CCCCCN1CC1=CC=CC=C1 DJGIITKNTHQYPX-UHFFFAOYSA-N 0.000 description 2
- AFFLGGQVNFXPEV-UHFFFAOYSA-N 1-decene Chemical compound CCCCCCCCC=C AFFLGGQVNFXPEV-UHFFFAOYSA-N 0.000 description 2
- LIKMAJRDDDTEIG-UHFFFAOYSA-N 1-hexene Chemical compound CCCCC=C LIKMAJRDDDTEIG-UHFFFAOYSA-N 0.000 description 2
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 2
- 238000005160 1H NMR spectroscopy Methods 0.000 description 2
- NKTDTMONXHODTI-UHFFFAOYSA-N 2-pentyne Chemical compound CCC#CC NKTDTMONXHODTI-UHFFFAOYSA-N 0.000 description 2
- BRRVYBRXLUEEJP-UHFFFAOYSA-N 4-bromo-n,n-dimethylbenzamide Chemical compound CN(C)C(=O)C1=CC=C(Br)C=C1 BRRVYBRXLUEEJP-UHFFFAOYSA-N 0.000 description 2
- HSFWRNGVRCDJHI-UHFFFAOYSA-N Acetylene Chemical compound C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 2
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- 239000005977 Ethylene Substances 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- QQONPFPTGQHPMA-UHFFFAOYSA-N Propene Chemical compound CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- 229910019895 RuSi Inorganic materials 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- PNXKRHWROOZWSO-UHFFFAOYSA-N [Si].[Ru] Chemical compound [Si].[Ru] PNXKRHWROOZWSO-UHFFFAOYSA-N 0.000 description 2
- 125000003158 alcohol group Chemical group 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- KDKYADYSIPSCCQ-UHFFFAOYSA-N but-1-yne Chemical compound CCC#C KDKYADYSIPSCCQ-UHFFFAOYSA-N 0.000 description 2
- IAQRGUVFOMOMEM-UHFFFAOYSA-N but-2-ene Chemical compound CC=CC IAQRGUVFOMOMEM-UHFFFAOYSA-N 0.000 description 2
- NQZFAUXPNWSLBI-UHFFFAOYSA-N carbon monoxide;ruthenium Chemical group [Ru].[Ru].[Ru].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-].[O+]#[C-] NQZFAUXPNWSLBI-UHFFFAOYSA-N 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- 238000007872 degassing Methods 0.000 description 2
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- FDBVFKPSUNQAHK-UHFFFAOYSA-N n,n-dimethyl-3-phenylpropanamide Chemical compound CN(C)C(=O)CCC1=CC=CC=C1 FDBVFKPSUNQAHK-UHFFFAOYSA-N 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- YWAKXRMUMFPDSH-UHFFFAOYSA-N pentene Chemical compound CCCC=C YWAKXRMUMFPDSH-UHFFFAOYSA-N 0.000 description 2
- QMMOXUPEWRXHJS-UHFFFAOYSA-N pentene-2 Natural products CCC=CC QMMOXUPEWRXHJS-UHFFFAOYSA-N 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 230000035484 reaction time Effects 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- PJANXHGTPQOBST-UHFFFAOYSA-N trans-Stilbene Natural products C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 2
- QQQSFSZALRVCSZ-UHFFFAOYSA-N triethoxysilane Chemical compound CCO[SiH](OCC)OCC QQQSFSZALRVCSZ-UHFFFAOYSA-N 0.000 description 2
- GGQQNYXPYWCUHG-RMTFUQJTSA-N (3e,6e)-deca-3,6-diene Chemical compound CCC\C=C\C\C=C\CC GGQQNYXPYWCUHG-RMTFUQJTSA-N 0.000 description 1
- JIZDZCFZPMIBPK-UHFFFAOYSA-N 1,3-bis(methylsulfanyl)propane Chemical compound CSCCCSC JIZDZCFZPMIBPK-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- RFEDQTSVZVRTGH-UHFFFAOYSA-N 1-(4-bromophenyl)-n,n-dimethylmethanamine Chemical compound CN(C)CC1=CC=C(Br)C=C1 RFEDQTSVZVRTGH-UHFFFAOYSA-N 0.000 description 1
- WMWQTUBQTYZJRI-UHFFFAOYSA-N 1-(4-methoxyphenyl)-n,n-dimethylmethanamine Chemical compound COC1=CC=C(CN(C)C)C=C1 WMWQTUBQTYZJRI-UHFFFAOYSA-N 0.000 description 1
- PTIVSZNNOUZBKM-UHFFFAOYSA-N 1-benzylazepane Chemical compound C=1C=CC=CC=1CN1CCCCCC1 PTIVSZNNOUZBKM-UHFFFAOYSA-N 0.000 description 1
- DURPTKYDGMDSBL-UHFFFAOYSA-N 1-butoxybutane Chemical compound CCCCOCCCC DURPTKYDGMDSBL-UHFFFAOYSA-N 0.000 description 1
- CGHIBGNXEGJPQZ-UHFFFAOYSA-N 1-hexyne Chemical compound CCCCC#C CGHIBGNXEGJPQZ-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- IBXNCJKFFQIKKY-UHFFFAOYSA-N 1-pentyne Chemical compound CCCC#C IBXNCJKFFQIKKY-UHFFFAOYSA-N 0.000 description 1
- ZFFMLCVRJBZUDZ-UHFFFAOYSA-N 2,3-dimethylbutane Chemical group CC(C)C(C)C ZFFMLCVRJBZUDZ-UHFFFAOYSA-N 0.000 description 1
- IMSODMZESSGVBE-UHFFFAOYSA-N 2-Oxazoline Chemical compound C1CN=CO1 IMSODMZESSGVBE-UHFFFAOYSA-N 0.000 description 1
- WEQPBCSPRXFQQS-UHFFFAOYSA-N 4,5-dihydro-1,2-oxazole Chemical compound C1CC=NO1 WEQPBCSPRXFQQS-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 101000687448 Homo sapiens REST corepressor 1 Proteins 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 102100024864 REST corepressor 1 Human genes 0.000 description 1
- 229910019832 Ru—Si Inorganic materials 0.000 description 1
- 238000004639 Schlenk technique Methods 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 1
- UORVGPXVDQYIDP-BJUDXGSMSA-N borane Chemical compound [10BH3] UORVGPXVDQYIDP-BJUDXGSMSA-N 0.000 description 1
- 229910000085 borane Inorganic materials 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- 150000001639 boron compounds Chemical class 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000001485 cycloalkadienyl group Chemical group 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000003678 cyclohexadienyl group Chemical group C1(=CC=CCC1)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- LRTZIJCDXOAKRC-UHFFFAOYSA-N cyclopropylphosphane Chemical compound PC1CC1 LRTZIJCDXOAKRC-UHFFFAOYSA-N 0.000 description 1
- ILLHQJIJCRNRCJ-UHFFFAOYSA-N dec-1-yne Chemical compound CCCCCCCCC#C ILLHQJIJCRNRCJ-UHFFFAOYSA-N 0.000 description 1
- 238000006356 dehydrogenation reaction Methods 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 125000004986 diarylamino group Chemical group 0.000 description 1
- 125000004119 disulfanediyl group Chemical group *SS* 0.000 description 1
- 238000000921 elemental analysis Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 150000004678 hydrides Chemical class 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 239000002198 insoluble material Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- AUHZEENZYGFFBQ-UHFFFAOYSA-N mesitylene Substances CC1=CC(C)=CC(C)=C1 AUHZEENZYGFFBQ-UHFFFAOYSA-N 0.000 description 1
- 125000001827 mesitylenyl group Chemical group [H]C1=C(C(*)=C(C([H])=C1C([H])([H])[H])C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- SKTCDJAMAYNROS-UHFFFAOYSA-N methoxycyclopentane Chemical compound COC1CCCC1 SKTCDJAMAYNROS-UHFFFAOYSA-N 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- NMXXDRKTOJAAQS-UHFFFAOYSA-N n,n-dimethyl-3-phenylpropan-1-amine Chemical compound CN(C)CCCC1=CC=CC=C1 NMXXDRKTOJAAQS-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000005184 naphthylamino group Chemical group C1(=CC=CC2=CC=CC=C12)N* 0.000 description 1
- 125000004998 naphthylethyl group Chemical group C1(=CC=CC2=CC=CC=C12)CC* 0.000 description 1
- 125000004923 naphthylmethyl group Chemical group C1(=CC=CC2=CC=CC=C12)C* 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- UMIPWJGWASORKV-UHFFFAOYSA-N oct-1-yne Chemical compound CCCCCCC#C UMIPWJGWASORKV-UHFFFAOYSA-N 0.000 description 1
- 238000006053 organic reaction Methods 0.000 description 1
- 150000003961 organosilicon compounds Chemical class 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 239000010970 precious metal Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- ZJLMKPKYJBQJNH-UHFFFAOYSA-N propane-1,3-dithiol Chemical compound SCCCS ZJLMKPKYJBQJNH-UHFFFAOYSA-N 0.000 description 1
- MWWATHDPGQKSAR-UHFFFAOYSA-N propyne Chemical compound CC#C MWWATHDPGQKSAR-UHFFFAOYSA-N 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 238000006884 silylation reaction Methods 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 150000003613 toluenes Chemical class 0.000 description 1
- 150000003623 transition metal compounds Chemical class 0.000 description 1
- 125000004665 trialkylsilyl group Chemical group 0.000 description 1
- 125000005106 triarylsilyl group Chemical group 0.000 description 1
- 125000002306 tributylsilyl group Chemical group C(CCC)[Si](CCCC)(CCCC)* 0.000 description 1
- 125000000725 trifluoropropyl group Chemical group [H]C([H])(*)C([H])([H])C(F)(F)F 0.000 description 1
- UORVGPXVDQYIDP-UHFFFAOYSA-N trihydridoboron Substances B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 1
- 125000000025 triisopropylsilyl group Chemical group C(C)(C)[Si](C(C)C)(C(C)C)* 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229960003986 tuaminoheptane Drugs 0.000 description 1
- 230000007306 turnover Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/1608—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes the ligands containing silicon
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/20—Carbonyls
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C13/00—Cyclic hydrocarbons containing rings other than, or in addition to, six-membered aromatic rings
- C07C13/02—Monocyclic hydrocarbons or acyclic hydrocarbon derivatives thereof
- C07C13/08—Monocyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with a five-membered ring
- C07C13/10—Monocyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with a five-membered ring with a cyclopentane ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C13/00—Cyclic hydrocarbons containing rings other than, or in addition to, six-membered aromatic rings
- C07C13/02—Monocyclic hydrocarbons or acyclic hydrocarbon derivatives thereof
- C07C13/16—Monocyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with a six-membered ring
- C07C13/18—Monocyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with a six-membered ring with a cyclohexane ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/02—Monocyclic hydrocarbons
- C07C15/067—C8H10 hydrocarbons
- C07C15/073—Ethylbenzene
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/12—Polycyclic non-condensed hydrocarbons
- C07C15/18—Polycyclic non-condensed hydrocarbons containing at least one group with formula
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C209/00—Preparation of compounds containing amino groups bound to a carbon skeleton
- C07C209/44—Preparation of compounds containing amino groups bound to a carbon skeleton by reduction of carboxylic acids or esters thereof in presence of ammonia or amines, or by reduction of nitriles, carboxylic acid amides, imines or imino-ethers
- C07C209/50—Preparation of compounds containing amino groups bound to a carbon skeleton by reduction of carboxylic acids or esters thereof in presence of ammonia or amines, or by reduction of nitriles, carboxylic acid amides, imines or imino-ethers by reduction of carboxylic acid amides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C213/00—Preparation of compounds containing amino and hydroxy, amino and etherified hydroxy or amino and esterified hydroxy groups bound to the same carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/132—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by reduction of an oxygen containing functional group
- C07C29/136—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by reduction of an oxygen containing functional group of >C=O containing groups, e.g. —COOH
- C07C29/14—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by reduction of an oxygen containing functional group of >C=O containing groups, e.g. —COOH of a —CHO group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C5/00—Preparation of hydrocarbons from hydrocarbons containing the same number of carbon atoms
- C07C5/02—Preparation of hydrocarbons from hydrocarbons containing the same number of carbon atoms by hydrogenation
- C07C5/03—Preparation of hydrocarbons from hydrocarbons containing the same number of carbon atoms by hydrogenation of non-aromatic carbon-to-carbon double bonds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C9/00—Aliphatic saturated hydrocarbons
- C07C9/14—Aliphatic saturated hydrocarbons with five to fifteen carbon atoms
- C07C9/16—Branched-chain hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D223/00—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom
- C07D223/02—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom not condensed with other rings
- C07D223/04—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom not condensed with other rings with only hydrogen atoms, halogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0046—Ruthenium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/30—Addition reactions at carbon centres, i.e. to either C-C or C-X multiple bonds
- B01J2231/32—Addition reactions to C=C or C-C triple bonds
- B01J2231/323—Hydrometalation, e.g. bor-, alumin-, silyl-, zirconation or analoguous reactions like carbometalation, hydrocarbation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/60—Reduction reactions, e.g. hydrogenation
- B01J2231/64—Reductions in general of organic substrates, e.g. hydride reductions or hydrogenations
- B01J2231/641—Hydrogenation of organic substrates, i.e. H2 or H-transfer hydrogenations, e.g. Fischer-Tropsch processes
- B01J2231/643—Hydrogenation of organic substrates, i.e. H2 or H-transfer hydrogenations, e.g. Fischer-Tropsch processes of R2C=O or R2C=NR (R= C, H)
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/60—Reduction reactions, e.g. hydrogenation
- B01J2231/64—Reductions in general of organic substrates, e.g. hydride reductions or hydrogenations
- B01J2231/641—Hydrogenation of organic substrates, i.e. H2 or H-transfer hydrogenations, e.g. Fischer-Tropsch processes
- B01J2231/645—Hydrogenation of organic substrates, i.e. H2 or H-transfer hydrogenations, e.g. Fischer-Tropsch processes of C=C or C-C triple bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/821—Ruthenium
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2531/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- C07C2531/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2531/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- C07C2531/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- C07C2531/22—Organic complexes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2531/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- C07C2531/26—Catalysts comprising hydrides, coordination complexes or organic compounds containing in addition, inorganic metal compounds not provided for in groups C07C2531/02 - C07C2531/24
- C07C2531/28—Catalysts comprising hydrides, coordination complexes or organic compounds containing in addition, inorganic metal compounds not provided for in groups C07C2531/02 - C07C2531/24 of the platinum group metals, iron group metals or copper
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/06—Systems containing only non-condensed rings with a five-membered ring
- C07C2601/08—Systems containing only non-condensed rings with a five-membered ring the ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
Definitions
- the present invention relates to a mononuclear ruthenium complex having a ruthenium-silicon bond. More specifically, the present invention relates to a mononuclear ruthenium complex having catalytic activity in three reactions of hydrosilylation reaction, hydrogenation reaction, and reduction reaction of a carbonyl compound.
- Hydrosilylation reaction in which a Si-H functional compound is added to a compound having a carbon-carbon double bond or triple bond, is a useful means for synthesizing organosilicon compounds, and is also an industrially important synthesis. It is a reaction.
- Pt, Pd, and Rh compounds are known. Among them, the most frequently used are Pt compounds represented by Speier catalyst and Karstedt catalyst.
- a problem of the reaction using a Pt compound as a catalyst is that, when a Si—H functional compound is added to a terminal olefin, a side reaction occurs in which the olefin undergoes internal rearrangement. In this system, there is no addition reactivity with internal olefins, and unreacted olefins remain in the addition product. Excess olefin must be used. There is also a problem that the selectivity of the ⁇ adduct and the ⁇ adduct is inferior depending on the type of olefin.
- the biggest problem is that the central metals Pt, Pd, and Rh are all extremely expensive noble metal elements, and a metal compound catalyst that can be used at a lower cost is desired. It is being advanced.
- Ru belongs to a noble metal, it is a metal that can be obtained at a relatively low cost, so that a function as a substitute for Pt, Pd, and Rh is required.
- Patent Document 1 a compound having an ⁇ 6 -arene group and having an organopolysiloxane bonded to a central metal Ru or a vinylsiloxane coordinated has been reported (Patent Document 1). Although this compound has been shown to be effective for the addition reaction of methylhydrogenpolysiloxane and methylvinylpolysiloxane, the yield is low in the reaction at 120 ° C, and 160 ° C in order to obtain a high yield. The reaction must be carried out at high temperatures. In addition, in Patent Document 1, many patents relating to Ru catalysts are cited as prior documents (Patent Documents 2 to 6). I can't say that.
- Non-patent Document 2 Non-patent Document 2
- these reducing agents are ignitable and water-inhibiting substances, they are difficult to handle.
- the present invention has been made in view of such circumstances, and a single compound having a ruthenium-silicon bond capable of exhibiting excellent catalytic activity in three reactions of hydrosilylation reaction, hydrogenation reaction, and reduction reaction of a carbonyl compound. It is an object of the present invention to provide a nuclear ruthenium complex and a method for performing a hydrosilylation reaction, a hydrogenation reaction, and a carbonyl compound reduction reaction under mild conditions using the complex.
- the present inventors have found that a given mononuclear ruthenium complex having a ruthenium-silicon bond can be used in three reactions: hydrosilylation reaction, hydrogenation reaction, and reduction reaction of a carbonyl compound.
- the present inventors have found that the catalyst can exhibit excellent catalytic activity and the hydrosilylation reaction, hydrogenation reaction, and reduction reaction of the carbonyl compound proceed under mild conditions.
- n and m is an integer of 1 to 3 independently of one another, n + m satisfies the 3 or 4.
- L is molecular hydrogen, amine, imine, nitrogen-containing heterocycle, arsine, alcohol, thiol, ether, sulfide, nitrile, isonitrile, aldehyde, ketone, alkene having 2 to 30 carbon atoms, alkyne having 2 to 30 carbon atoms And a mononuclear ruthenium complex which is at least one dielectron ligand selected from triorganohydrosilane, 3. N and m are both 2, and L is at least one selected from sulfide, thiol and triorganohydrosilane (however, two L may be bonded to each other) Nuclear ruthenium complex, 4).
- R 1 to R 6 are each independently an alkyl group, an aryl group, or an aralkyl group (X represents the same meaning as described above), which may be substituted with X, and L is H—SiR 7 R 8 R 9 and H—SiR 10 R 11 R 12 (wherein R 7 to R 12 are each independently an alkyl group, aryl group or aralkyl group optionally substituted with X) X represents the same meaning as described above.), And is represented by any one of R 1 to R 3 and at least one of R 4 to R 6 or R 7 to R 9.
- Any one of R 10 to R 12 together with at least one of any of R 4 to R 6 or at least one of any of R 7 to R 9 together It may form a bridging substituent turned, R 1 ⁇ R 3 Either to form one of the at least one pair or one of the at least one set bridging substituent together the R 7 ⁇ R 9 in R 4 ⁇ R 6, and, with any of R 10 ⁇ R 12 3 mononuclear ruthenium complexes in which at least one set of any of R 4 to R 6 and at least one of any of R 7 to R 9 may be combined to form a bridging substituent, 5.
- R 1 to R 6 are each independently an alkyl group, an aryl group, or an aralkyl group (X represents the same meaning as described above), which may be substituted with X, and L is SR 13 R 14 and SR 15 R 16 (wherein, R 13 to R 16 each independently represents a hydrogen atom, an alkyl group, an aryl group or an aralkyl group which may be substituted with X; It represents the same meaning as described above.), And any one of R 13 and R 14 and at least one of R 15 and R 16 together form a bridging substituent. 3 mononuclear ruthenium complexes which may be 6).
- Nuclear ruthenium complex 10. Any one of R 1 to R 3 and any one of R 4 to R 6 together form an o-phenylene group which may be substituted with Y (Y is a hydrogen atom, a halogen atom, An atom, an alkyl group having 1 to 10 carbon atoms, or an alkoxy group having 1 to 10 carbon atoms, and when a plurality of Y's are present, they may be the same or different from each other), and any of R 13 and R 14 8 mononuclear ruthenium complexes in which one of R 15 and R 16 together forms an alkylene group having 1 to 6 carbon atoms, 11.
- a catalyst comprising any one of mononuclear ruthenium complexes of 1 to 10 and having activity in three reactions of a hydrosilylation reaction, a hydrogenation reaction, and a reduction reaction of a carbonyl compound; 12 A process for producing an addition compound comprising hydrosilylation reaction of a compound having an aliphatic unsaturated bond with a hydrosilane or organohydropolysiloxane having a Si-H bond in the presence of 11 catalyst; 13.
- a process for producing an alkane compound characterized in that a compound having an aliphatic unsaturated bond is hydrogenated in the presence of 11 catalysts; 14 A method for producing an amine compound, wherein the amide compound is reduced with a silane or an organohydropolysiloxane having a Si—H bond in the presence of 11 catalysts; 15. An alcohol compound is produced by reducing an aldehyde compound, a ketone compound or an ester compound with a silane or an organohydropolysiloxane having a Si—H bond in the presence of 11 catalysts.
- the reaction is performed at room temperature to 100 ° C. or less. Addition reaction is possible. Particularly, the addition reaction with industrially useful polysiloxane, trialkoxysilane and dialkoxysilane proceeds well. Furthermore, the known literature shows that in this reaction, the addition reaction to the unsaturated group and the reaction for producing the unsaturated group-containing compound by the dehydrogenation silylation reaction frequently proceed simultaneously, but the catalyst of the present invention When is used, an addition reaction to an unsaturated group proceeds selectively.
- the target reducing compound can be obtained by reacting an amide compound, an aldehyde compound, a ketone compound or an ester compound with a silane or polysiloxane having an Si—H group which is easy to handle. .
- the superiority of the complex compound of the present invention is that the same complex compound exhibits high catalytic activity for a plurality of reactions selected from a hydrosilylation reaction, a hydrogenation reaction, and a reduction reaction of a carbonyl compound. It is extremely useful in organic synthesis reactions.
- FIG. 1 is a view showing a structure of a ruthenium complex A obtained in Example 1.
- FIG. 1 is a 1 H-NMR spectrum diagram of a ruthenium complex A obtained in Example 1.
- FIG. 1 is a 13 C-NMR spectrum diagram of ruthenium complex A obtained in Example 1.
- FIG. 4 is a view showing a structure of a ruthenium complex B obtained in Example 2.
- FIG. 2 is a 1 H-NMR spectrum diagram of a ruthenium complex B obtained in Example 2.
- FIG. 3 is a 13 C-NMR spectrum of ruthenium complex B obtained in Example 2.
- the mononuclear ruthenium complex according to the present invention has a Ru—Si bond and has at least one carbon monoxide (CO) coordinated to Ru as represented by the formula (1). is there.
- the mononuclear ruthenium complex of the formula (1) for example, when there are 2 CO and 2 L (which are distinguished as L 1 and L 2 ), the coordination structure as shown by the following formula Although isomers exist, the mononuclear ruthenium complex of the present invention includes all these coordination structural isomers.
- carbon monoxide is an essential coordination compound for exhibiting catalytic activity
- n is an integer of 1 to 3, but the catalytic activity is further enhanced.
- 1 to 2 is preferable, and 2 is optimal.
- R 1 to R 6 are independently of each other a hydrogen atom or an X group, an alkyl group, an aryl group, an aralkyl group, an organooxy group, a monoorganoamino group, a diorganoamino group, or a monoorgano.
- the alkyl group may be linear, branched or cyclic, and the carbon number thereof is not particularly limited, but is preferably an alkyl having 1 to 30 carbons, more preferably 1 to 10 carbons.
- Specific examples thereof include methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, s-butyl, t-butyl, n-pentyl, n-hexyl, n-heptyl, n-octyl, n-nonyl, n-decyl, n-undecyl, n-dodecyl, n-tridecyl, n-tetradecyl, n-pentadecyl, n-hexadecyl, n-heptadecyl, n-octadecyl, n-nonadecyl, n-eicosanyl group, etc.
- Linear or branched alkyl group cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl, cyclooctyl, Such as cycloalkyl groups such as Kurononiru group.
- the number of carbon atoms of the aryl group is not particularly limited, but is preferably an aryl group having 6 to 30 carbon atoms, more preferably 6 to 20 carbon atoms.
- Specific examples thereof include phenyl, 1- Examples include naphthyl, 2-naphthyl, anthryl, phenanthryl, o-biphenylyl, m-biphenylyl, p-biphenylyl group and the like.
- the number of carbon atoms of the aralkyl group is not particularly limited, but is preferably an aralkyl group having 7 to 30 carbon atoms, more preferably 7 to 20 carbon atoms. Specific examples thereof include benzyl and phenylethyl. , Phenylpropyl, naphthylmethyl, naphthylethyl, naphthylpropyl group and the like.
- the organooxy group is not particularly limited, but RO (R is a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, aryl group having 6 to 30 carbon atoms, or 7 to 30 carbon atoms.
- R is a substituted or unsubstituted alkyl group having 1 to 30 carbon atoms, aryl group having 6 to 30 carbon atoms, or 7 to 30 carbon atoms.
- the alkoxy group is not particularly limited, but is preferably an alkoxy group having 1 to 30 carbon atoms, particularly 1 to 10 carbon atoms.
- aryloxy group is not particularly limited, but is preferably an aryloxy group having 6 to 30 carbon atoms, particularly 6 to 20 carbon atoms. Specific examples thereof include phenoxy, 1-naphthyloxy and 2-naphthyl.
- the aralkyloxy group is not particularly limited, but is preferably an aryloxy group having 7 to 30 carbon atoms, particularly 7 to 20 carbon atoms, such as benzyloxy group, phenylethyloxy, phenylpropyloxy, 1 or 2- Examples thereof include naphthylmethyloxy, 1 or 2-naphthylethyloxy, 1 or 2-naphthylpropyloxy group and the like.
- the organothio group include groups in which the oxygen atom of the organooxy group is substituted with a sulfur atom.
- the mono-organo groups include, but are not particularly limited, is preferably one represented by RNH 2 (R represents the same meaning as above.)
- RNH 2 R represents the same meaning as above.
- a linear or branched monoalkylamino group such as n-heptadecylamino, n-octadecylamino, n-nonadecylamin
- the diorganoamino group is not particularly limited, but is preferably represented by R 2 NH (wherein R independently represents the same meaning as described above), and the preferred carbon number in R is the alkoxy , Aryloxy and aralkyloxy groups. Specific examples thereof include dimethylamino, diethylamino, di-n-propylamino, diisopropylamino, di-n-butylamino, diisobutylamino, di-s-butylamino, di-t-butylamino, di-n-pentyl.
- a dicycloalkylamino group such as N-methylanilino, N-ethylanilino, and Nn-propylanilino groups; diphenylamino, 4,4'-bisnaphthylamino, N-phenyl-1 or 2- And diarylamino groups such as naphthylamino group; and diaralkylamino groups such as dibenzylamino, bis (phenylethyl) amino, bis (phenylpropyl) amino, and bis (1 or 2-naphthylmethyl) amino groups.
- the monoorganophosphino group is not particularly limited, but is preferably RPH (where R represents the same meaning as described above), and the preferred carbon number in R is alkoxy, aryloxy, aralkyloxy. Same as the group. Specific examples thereof include methyl phosphino, ethyl phosphino, n-propyl phosphino, isopropyl phosphino, n-butyl phosphino, isobutyl phosphino, s-butyl phosphino, t-butyl phosphino, n-pentyl phosphino.
- cyclopropylphosphine Monocycloalkyl phosphino groups such as ino, cyclobutyl phosphino, cyclopentyl phosphino, cyclohexyl phosphino, cycloheptyl phosphino, cyclooctyl phosphino, cyclononyl phosphino groups; phenyl phosphino, 1 or 2-naphthyl phosphino And monoarylphosphino groups such as fino groups; monoaralkylphosphino groups such as benzylphosphino groups and the like.
- the diorganophosphino group is not particularly limited, but is preferably represented by R 2 P (wherein R independently represents the same meaning as described above).
- Aryloxy and aralkyloxy groups include dimethylphosphino, diethylphosphino, di-n-propylphosphino, diisopropylphosphino, di-n-butylphosphino, diisobutylphosphino, di-s-butylphosphino, di-t- Butylphosphino, di-n-pentylphosphino, di-n-hexylphosphino, di-n-heptylphosphino, di-n-octylphosphino, di-n-nonylphosphino, di-n-decylphosphino, di- n-undecylphosphino, di-n-dodecylphosphino, di-n-tride
- Mono-organosilyl group but are not particularly limited, but is preferably one represented by the RSiH 2 (R has the same meaning as above.)
- R has the same meaning as above.
- the diorgano silyl group is not particularly limited, but is preferably those represented by R 2 SiH (R independently of one another represent the same meaning as above.)
- R 2 SiH R independently of one another represent the same meaning as above.
- the preferred number of carbon atoms in R of the alkoxy The same as the aryloxy and aralkyloxy groups.
- a branched dialkylsilyl group a dicycloalkylsilyl group such as dicyclopropylsilyl, dicyclobutylsilyl, dicyclopentylsilyl, dicyclohexylsilyl, dicycloheptylsilyl, dicyclooctylsilyl, dicyclononylsilyl, cyclopentylcyclohexylsilyl group, etc.
- Alkylalkylsilyl groups such as (methyl) phenylsilyl, (ethyl) phenylsilyl, (n-propyl) phenylsilyl groups; diphenylsilyl, bis (1 or 2-naphthyl) silyl, phenyl-1 or 2-naphthylsilyl groups And diarylsilyl groups such as dibenzylsilyl, bis (phenylethyl) silyl, bis (phenylpropyl) silyl, and bis (1 or 2-naphthylmethyl) silyl groups.
- R 3 Si (R represents. As defined above independently of each other) is preferably one represented by the preferable number of carbon atoms in R of the alkoxy, The same as the aryloxy and aralkyloxy groups. Specific examples thereof include trimethylsilyl, triethylsilyl, tri-n-propylsilyl, triisopropylsilyl, tri-n-butylsilyl, triisobutylsilyl, tri-s-butylsilyl, tri-t-butylsilyl, tri-n-pentylsilyl.
- Each of the above substituents may have at least one hydrogen atom on R substituted with a substituent X, where X is a halogen atom, an organooxy group, a monoorganoamino group, a diorganoamino group, or Examples include organothio groups, and examples of the organooxy group, monoorganoamino group, diorganoamino group, and organothio group include the same groups as described above.
- halogen atom examples include fluorine, chlorine, bromine and iodine atoms, but a fluorine atom is preferable, and examples of suitable fluorine-substituted alkyl groups include trifluoropropyl group, nonafluorohexyl group, heptadecylfluorodecyl group and the like. .
- R 1 to R 6 are each independently an alkyl group having 1 to 30 carbon atoms, an aryl group having 6 to 30 carbon atoms, or 7 to 7 carbon atoms that may be substituted with X.
- 30 aralkyl groups are preferred, alkyl groups having 1 to 10 carbon atoms and aryl groups having 6 to 10 carbon atoms are more preferred.
- the crosslinking substituent in which at least one of R 1 to R 3 and any one of R 4 to R 6 is bonded is not particularly limited as long as it is a substituent capable of crosslinking two Si atoms.
- —O—, —S—, —NH—, —NR— (R is the same as above), —PR— (R is the same as above), —NH— (CH 2 ) k —NH -(K represents an integer of 1 to 10), -NR- (CH 2 ) k -NR- (k is the same as above, R is the same as above independently), -PH- (CH 2 ) K -PH- (k is the same as above), -PR- (CH 2 ) k -PR- (k is the same as above, R is independently the same as above), -C C-, An alkylene group having 1 to 10 carbon atoms, an arylene group having 6 to 30 carbon atoms, an aralkylene group having 7 to 30 carbon atoms
- alkylene group having 1 to 10 carbon atoms examples include methylene, ethylene, propylene, trimethylene, tetramethylene, pentamethylene and hexamethylene groups.
- arylene group having 6 to 30 carbon atoms examples include o-phenylene (1,2-phenylene), 1,2-naphthylene, 1,8-naphthylene and 2,3-naphthylene groups.
- aralkylene group having 7 to 30 carbon atoms As the aralkylene group having 7 to 30 carbon atoms, — (CH 2 ) k —Ar— (Ar represents an arylene group having 6 to 20 carbon atoms, k represents the same meaning as described above), —Ar— ( CH 2 ) k — (Ar and k are as defined above), — (CH 2 ) k —Ar— (CH 2 ) k — (Ar is as defined above, and k is independently from each other. The same meaning as above).
- at least one of these hydrogen atoms may be substituted with a substituent X (X is the same as above).
- bridging substituent Z When the bridging substituent is represented as Z, the number of Z connecting two silicon atoms is 1 to 3, and a mononuclear ruthenium complex having such a bridging substituent Z is represented by the following formula.
- R 1 , R 2 , R 5 , R 6 , L, n and m represent the same meaning as described above, and Z represents a bridging substituent.
- disila metallacycle structure having a crosslinking substituent include those represented by the following formula, but are not limited thereto.
- R 1 , R 2 , R 4 and R 5 represent the same meaning as described above
- R 17 to R 20 are each independently a hydrogen atom, a halogen atom, a carbon number of 1 to 10 represents an alkyl group or an alkoxy group having 1 to 10 carbon atoms
- R 25 to R 30 each independently represent a hydrogen atom or an unsubstituted or substituted monovalent hydrocarbon group having 1 to 20 carbon atoms.
- R 17 to R 20 and R 25 to R 30 are preferably hydrogen atoms.
- Specific examples of the monovalent hydrocarbon group include an alkyl group, an aryl group, an aralkyl group, and the like, and specific examples thereof include those similar to the above. Examples of the alkyl group, alkoxy group, and halogen atom are the same as those described above.
- L is a two-electron ligand other than CO and phosphine in which two electrons contained in the ligand are coordinated to ruthenium.
- the two-electron ligand is not particularly limited as long as it is other than CO and phosphine, and any ligand other than CO conventionally used as the two-electron ligand of the metal complex can be used.
- amines are typically compounds such as amines, imines, nitrogen-containing heterocycles, arsine, alcohols, thiols, ethers, sulfides, etc., which contain unshared electron pairs (unpaired electrons) such as nitrogen, oxygen and sulfur; Alkenes, alkynes, aldehydes, ketones, nitriles, isonitriles, and other compounds containing both unpaired and ⁇ electrons; molecular hydrogen bonded by agostic interaction Coordination), hydrosilane (sigma electrons contained in Si—H bonds coordinate), and the like.
- unshared electron pairs unpaired electrons
- unpaired electrons such as nitrogen, oxygen and sulfur
- molecular hydrogen bonded by agostic interaction Coordination hydrosilane (sigma electrons contained in Si—H bonds coordinate), and the like.
- Examples of the amine include tertiary amines represented by R 3 N (wherein R independently represents the same meaning as described above).
- Examples of the nitrogen-containing heterocycle include pyrrole, imidazole, pyridine, pyrimidine, oxazoline, isoxazoline and the like.
- Examples of the arsine include those represented by R 3 As (wherein R independently represents the same meaning as described above).
- ROH R represents the same meaning as the above.) Is mentioned, for example.
- Examples of the thiol include those in which the oxygen atom of the alcohol is substituted with a sulfur atom.
- Examples of the ether include those represented by ROR (wherein R independently represents the same meaning as described above).
- Examples of the sulfide include those obtained by substituting the oxygen atom of the ether with a sulfur atom.
- Examples of the ketone include those represented by RCOR (R represents the same meaning as described above independently of each other).
- Examples of the isonitrile include those represented by RNC (R represents the same meaning as described above independently of each other).
- Alkenes include, for example, ethene, propene, 1-butene, 2-butene, 1-pentene, 2-pentene, cyclopentene, 1-hexene, cyclohexene, 1-heptene, 1-octene, 1-nonene, 1-decene, etc.
- alkenes having 2 to 30 carbon atoms examples include, for example, ethyne, propyne, 1-butyne, 2-butyne, 1-pentyne, 2-pentyne, 1-hexyne, 1-heptin, 1-octyne, 1-nonine, 1-decyne, and the like.
- alkyne examples include, for example, ethyne, propyne, 1-butyne, 2-butyne, 1-pentyne, 2-pentyne, 1-hexyne, 1-heptin, 1-octyne, 1-nonine, 1-decyne, and the like.
- the hydrosilane examples include triorganohydrosilane, specifically, trihydrocarbon organohydrosilane having 1 to 30 carbon atoms, and more specifically, R 1 R 2 R 3 SiH (where R 1 to R 3 are the above). It represents the same
- the two-electron ligand L molecular hydrogen, amine, imine, nitrogen-containing heterocycle, arsine, alcohol, thiol, ether, sulfide, nitrile, isonitrile, aldehyde, ketone, having 2 to 30 carbon atoms.
- Alkenes, alkynes having 2 to 30 carbon atoms, and triorganohydrosilane are preferred.
- two Ls When two Ls are present, they may be bonded to each other to form a ligand containing two coordinating two-electron functional groups.
- Representative examples include, but are not limited to, ethylenediamine, ethylene glycol dimethyl ether, 1,3-butadiene, and those represented by the following formula.
- ethylenediamine ethylene glycol dimethyl ether
- 1,3-butadiene 1,3-butadiene
- those represented by the following formula in the mononuclear ruthenium complex of this invention, when three L exists, all of them combine and it does not take the ligand containing three coordinating two-electron functional groups.
- Me means a methyl group and Ph means a phenyl group.
- the coordination number m of the two-electron ligand L represents an integer of 1 to 3, but is preferably 2.
- the sum of the coordination number n of CO and the coordination number m of L satisfies 3 or 4, but is preferably 4.
- thiol, sulfide, and triorganohydrosilane are more preferable among the above preferable L.
- SiHR 7 R 8 R 9 and SiHR 10 R 11 R 12 R 7 to R 12 each independently represents an alkyl group, an aryl group or an aralkyl group, which may be substituted with X, Represents the same meaning as above
- SR 13 R 14 and SR 15 R 16 R 13 to R 16 are each independently substituted with a hydrogen atom or X).
- An alkyl group, an aryl group or an aralkyl group, and X represents the same meaning as described above.
- alkyl group examples include the same groups as those exemplified above, but each of the alkyl group having 1 to 10 carbon atoms, the aryl group having 6 to 20 carbon atoms, Aralkyl groups having 7 to 20 carbon atoms are preferred, alkyl groups having 1 to 10 carbon atoms and aryl groups having 6 to 20 carbon atoms are more preferred.
- a mononuclear ruthenium complex is formed.
- Two or more of the four silicon atoms may be connected by the above-described bridging substituent Z.
- the combination of silicon atoms is silicon atoms having silicon-ruthenium covalent bonds, silicon atoms coordinated by Si—H, silicon-ruthenium covalent bonds, and silicon atoms coordinated by Si—H. Either of these may be used.
- the number of Z connecting two silicon atoms is 1 to 3, while the total number of Z contained in the whole complex is 1 to 12.
- dithia (dithio) metallacycle structures include, but are not limited to, those represented by the following formula.
- Examples of the structure of a mononuclear ruthenium complex having a dithia metallacycle structure include, but are not limited to, those represented by the following formula.
- a mononuclear ruthenium complex in which two COs are coordinated and Si-H of a triorganohydrosilane that is a two-electron ligand is agogotically coordinated is preferable.
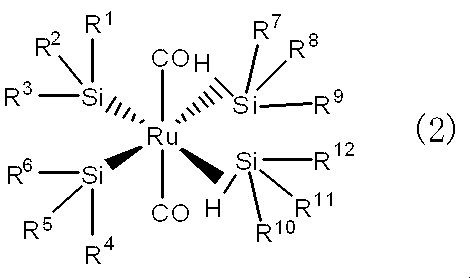
- a structure represented by the formula (2) can be mentioned.
- other coordination structure isomerism is used. It may be a body.
- R 1 to R 12 represent the same meaning as described above, but R 1 to R 6 are each independently an alkyl group, an aryl group, or an aralkyl group (X is as defined above), which may be substituted with X. .) Is preferred.
- specific examples of the alkyl group, the aryl group, and the aralkyl group include the same groups as those exemplified above.
- Aralkyl groups having 7 to 20 carbon atoms are preferred, alkyl groups having 1 to 10 carbon atoms and aryl groups having 6 to 20 carbon atoms are more preferred.
- two or more of the four silicon atoms constituting the mononuclear ruthenium complex may be linked by a bridging substituent, specifically, any one of R 1 to R 3 and R At least one of any of 4 to R 6 or at least one of any of R 7 to R 9 together, or any of R 10 to R 12 and at least any of R 4 to R 6
- One set or at least one of R 7 to R 9 may be combined together to form a bridging substituent such as an alkylene group, an arylene group or an aralkylene group, or any one of R 1 to R 3 ;
- At least one group of any of R 4 to R 6 or at least one group of any of R 7 to R 9 together forms a bridging substituent such as an alkylene group, an arylene group or an aralkylene group, and R 10 one of the ⁇ R 12
- bridging substituent such as an
- alkylene group examples include the same groups as those exemplified above, but each of the alkylene group having 1 to 10 carbon atoms, the arylene group having 7 to 20 carbon atoms, Aralkylene groups having 7 to 20 carbon atoms are preferable, alkylene groups having 1 to 6 carbon atoms, and arylene groups having 7 to 20 carbon atoms are more preferable.
- ruthenium complex in which two COs are coordinated and two sulfides or thiols that are two-electron ligands are coordinated can also be suitably used.
- a ruthenium complex is expressed conveniently using one coordination structure, a structure represented by the formula (3) can be given.
- other coordination structure isomerism is used. It may be a body.
- R 1 to R 6 and R 13 to R 16 represent the same meaning as described above, but R 13 to R 16 are each independently an alkyl group which may be substituted with X, An aryl group or an aralkyl group (X represents the same meaning as described above) is preferable.
- specific examples of the alkyl group, the aryl group, and the aralkyl group include the same groups as those exemplified above.
- Aralkyl groups having 7 to 20 carbon atoms are preferred, alkyl groups having 1 to 10 carbon atoms and aryl groups having 6 to 20 carbon atoms are more preferred.
- two sulfur atoms constituting the mononuclear ruthenium complex may be connected by a bridging substituent, specifically, any one of R 13 and R 14 , R 15 and R 16 At least one of these groups may be combined to form a crosslinking substituent such as an alkylene group, an arylene group or an aralkylene group.
- the two silicon atoms constituting the mononuclear ruthenium complex may also be connected by a bridging substituent.
- any one of R 1 to R 3 and any of R 4 to R 6 At least one of these groups may be combined to form a crosslinking substituent such as an alkylene group, an arylene group or an aralkylene group.
- alkylene group examples include the same groups as those exemplified above, but each of the alkylene group having 1 to 10 carbon atoms, the arylene group having 7 to 20 carbon atoms, Aralkylene groups having 7 to 20 carbon atoms are preferable, alkylene groups having 1 to 6 carbon atoms, and arylene groups having 7 to 20 carbon atoms are more preferable.
- R 1 , R 2 , R 4 , R 5 , R 7 , R 8 , R 10 , R 11 , R 13 and R 16 to R 20 represent the same meaning as described above, and R 21 to R 24 Represents the same meaning as R 17.
- a represents an integer of 1 to 6, but 2 or 3 is preferable.
- a ruthenium complex represented by the above formulas (4) and (6) includes a ruthenium-carbonyl complex having a cycloalkadienyl group such as a cyclohexadienyl group or a cyclooctadienyl group as a ligand, and 1 , 2-bis (dimethylsilyl) benzene and other bissilyl compounds can be obtained by light irradiation in an inert gas atmosphere such as argon gas.
- the amount of the bissilyl compound used can be about 1 to 10 moles, preferably 2 to 5 moles, relative to the ruthenium-carbonyl complex.
- the organic solvent various solvents can be used as long as they do not affect the reaction.
- aliphatic hydrocarbons such as pentane, hexane, heptane, octane, cyclohexane; diethyl ether, diisopropyl ether, dibutyl ether , Ethers such as cyclopentyl methyl ether, tetrahydrofuran, and 1,4-dioxane; aromatic hydrocarbons such as benzene, toluene, xylene, and mesitylene.
- the reaction temperature may be appropriately set within the range from the melting point to the boiling point of the organic solvent, but is preferably 10 to 50 ° C, more preferably 15 to 30 ° C.
- the reaction time is usually about 1 to 48 hours.
- the solvent can be distilled off, and then the desired product can be obtained by a known purification method such as recrystallization, but the prepared ruthenium complex can be used as a catalyst for the desired reaction without isolation. Also good.
- the ruthenium complex having a sulfide ligand as represented by the above formulas (5) and (7) is, for example, a ruthenium complex represented by the formulas (4) and (6) obtained by the above method as a raw material. And obtained by reacting with a dithia hydrocarbon compound such as 2,6-dithiaheptane or a thiol compound such as 1,3-propanedithiol in an organic solvent as exemplified above in an inert gas atmosphere such as argon. Can do.
- the amount of the dithia hydrocarbon compound used can be about 1 to 3 moles, preferably 1 to 1.5 moles, more preferably 1 to 1.2 moles, relative to the ruthenium complex. preferable.
- the reaction temperature may be appropriately set within the range of 0 ° C. to the boiling point of the organic solvent, but is preferably 10 to 50 ° C., and preferably 15 to 30 ° C.
- the reaction time is usually about 1 to 48 hours.
- the solvent can be distilled off, and then the desired product can be obtained by a known purification method such as recrystallization, but the prepared ruthenium complex can be used as a catalyst for the desired reaction without isolation. Also good.
- the mononuclear ruthenium complex of the present invention can exhibit catalytic activity in three reactions of hydrosilylation reaction, hydrogenation reaction, and reduction reaction of a carbonyl compound.
- a catalyst and having an aliphatic unsaturated bond, such as an olefin compound, a silane compound or an organopolysiloxane compound, and a compound having an aliphatic unsaturated bond, and an Si—H bond
- the amount of the catalyst used is not particularly limited, but the reaction is allowed to proceed under mild conditions of room temperature to about 100 ° C.
- the amount of the catalyst used is preferably 0.5 mol% or more. Even when the mononuclear ruthenium complex of the present invention is used as a catalyst and an olefin compound containing an aliphatic unsaturated bond is reduced with hydrogen gas to obtain a saturated compound, the amount of the catalyst used is particularly limited. However, considering that the desired product can be obtained in good yield by proceeding the reaction at room temperature and under a mild condition where the hydrogen pressure is about 1 atm, the amount of catalyst used should be 1 mol% or more. Is preferred. In any reaction, the upper limit of the amount of catalyst used is not particularly limited, but is about 10 mol% from an economical viewpoint.
- the amount of the catalyst used is not particularly limited. In consideration of obtaining the desired product in good yield by advancing the reaction, the amount of the catalyst used is preferably 0.01 mol% or more. In this case, the upper limit of the amount of catalyst used is not particularly limited, but is about 5 mol% from an economic viewpoint.
- Examples of the carbonyl compound that can be subjected to the reduction reaction include compounds having an amide, aldehyde, ketone, ester, carboxylic acid, carboxylate (for example, sodium salt, potassium salt, etc.) group, etc., and these are the ruthenium complex of the present invention.
- a silane or siloxane containing a Si—H group By reacting with a silane or siloxane containing a Si—H group in the presence of a catalyst, it can be led to the corresponding amine or alcohol compound, respectively.
- the reaction mixture was dried under reduced pressure, and the resulting dried product was dissolved in hexane (40 mL), and a small amount of brown insoluble material by-produced by centrifugation was removed. Thereafter, the hexane solution was concentrated to about 25 mL under reduced pressure, and recrystallized at ⁇ 35 ° C. to obtain a ruthenium complex A (274 mg / 0.50 mmol / 27%) typically represented by the formula (6). .
- the structure of the obtained ruthenium complex A is shown in FIG. 1, the measurement result of 1 H-NMR is shown in FIG. 2, and the measurement result of 13 C-NMR is shown in FIG.
- the solution was concentrated to about 5 mL under reduced pressure, recrystallized at ⁇ 35 ° C., and reconstituted with the formula (7
- the ruthenium complex B (82 mg / 0.17 mmol / 94%) typically represented by The structure of the resulting ruthenium complex B is shown in FIG. 4, the measurement result of 1 H-NMR is shown in FIG. 5, and the measurement result of 13 C-NMR is shown in FIG.
- Example 5 Hydrosilylation of 2-octene with triethoxysilane A magnetic stirrer was added to a 20 mL Schlenk tube and dried by heating while reducing the pressure to 5 Pa. Then, the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (8 mg, 0.015 mmol) was added to the Schlenk tube as a catalyst. To this was added 2-octene (78.2 ⁇ L, 0.5 mmol), and further triethoxysilane (92.3 ⁇ L, 0.5 mmol) was added, and the solution was stirred at 80 ° C. for 3 hours. After cooling, anisole was added as an internal standard, and a 1 H-NMR spectrum was measured to determine the structure and yield of the product. These results are shown in Table 1 as entry 3.
- Example 6 Hydrosilylation of 2-octene with triethylsilane A magnetic stirrer was added to a 20 mL Schlenk tube and dried by heating while reducing the pressure to 5 Pa. Then, the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (8 mg, 0.015 mmol) was added to the Schlenk tube as a catalyst. To this was added 2-octene (78.2 ⁇ L, 0.5 mmol), and further triethylsilane (79.8 ⁇ L, 0.5 mmol) was added, and the solution was stirred at 80 ° C. for 3 hours. After cooling, anisole was added as an internal standard, and a 1 H-NMR spectrum was measured to determine the structure and yield of the product. These results are shown in Table 1 as entry 4.
- Example 8 Hydrosilylation of 1-octene with 1,1,1,3,5,5,5-heptamethyltrisiloxane
- a magnetic stirrer was added to a 20 mL Schlenk tube, and the mixture was dried by heating while reducing the pressure to 5 Pa. The inside of the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (8 mg, 0.015 mmol) was added to the Schlenk tube as a catalyst.
- 1-octene (78.2 ⁇ L, 0.5 mmol) was added thereto, and 1,1,1,3,5,5,5-heptamethyltrisiloxane (135.7 ⁇ L, 0.5 mmol) was further added.
- the solution was stirred at 80 ° C. for 3 hours. After cooling, anisole was added as an internal standard, and a 1 H-NMR spectrum was measured to determine the structure and yield of the product.
- Example 11 Hydrogenation of trans-stilbene A magnetic stirrer was added to a 20 mL Schlenk tube and dried by heating while reducing the pressure to 5 Pa. Then, the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (14 mg, 0.025 mmol) was added to the Schlenk tube as a catalyst, and dissolved in toluene (1 mL). To this solution was added trans-stilbene (90 mg, 0.5 mmol). The resulting solution was freeze degassed and the inside of the Schlenk tube was replaced with a hydrogen atmosphere, and then the solution was stirred at room temperature for 6 hours. Anisole was added as an internal standard, and the 1 H-NMR spectrum was measured to determine the structure and yield of the product. The structure of the obtained compound was confirmed by 1 H, 13 C-NMR spectrum. These results are shown in Table 3 as entry 2.
- Example 12 Hydrogenation of cyclohexene A magnetic stirrer was added to a 20 mL Schlenk tube and dried under reduced pressure to 5 Pa, and the inside of the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (14 mg, 0.025 mmol) was added to the Schlenk tube as a catalyst, and dissolved in toluene (1 mL). To this solution was added cyclohexene (54 ⁇ L, 0.5 mmol). The resulting solution was freeze degassed and the inside of the Schlenk tube was replaced with a hydrogen atmosphere, and then the solution was stirred at room temperature for 6 hours. Anisole was added as an internal standard, and the 1 H-NMR spectrum was measured to determine the structure and yield of the product. The structure of the obtained compound was confirmed by 1 H, 13 C-NMR spectrum. These results are shown in Table 3 as entry 3.
- Example 13 Hydrogenation of cyclopentene A magnetic stirrer was added to a 20 mL Schlenk tube and dried under reduced pressure to 5 Pa, and the inside of the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (14 mg, 0.025 mmol) was added to the Schlenk tube as a catalyst and dissolved in toluene (2 mL). To this solution was added cyclopentene (44.2 ⁇ L, 0.5 mmol). The resulting solution was freeze degassed and the inside of the Schlenk tube was replaced with a hydrogen atmosphere, and then the solution was stirred at room temperature for 6 hours. Anisole was added as an internal standard, and the 1 H-NMR spectrum was measured to determine the structure and yield of the product. The structure of the obtained compound was confirmed by 1 H, 13 C-NMR spectrum. These results are shown in Table 3 as entry 4.
- Example 14 Hydrogenation of 1-methyl-1-cyclohexene A magnetic stirrer was added to a 20 mL Schlenk tube and dried under reduced pressure to 5 Pa, and then the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (14 mg, 0.025 mmol) was added to the Schlenk tube as a catalyst, and dissolved in toluene (1 mL). To this solution was added 1-methyl-1-cyclohexene (54 ⁇ L, 1.0 mmol). The resulting solution was freeze degassed and the inside of the Schlenk tube was replaced with a hydrogen atmosphere, and then the solution was stirred at room temperature for 6 hours. Anisole was added as an internal standard, and the 1 H-NMR spectrum was measured to determine the structure and yield of the product. The structure of the obtained compound was confirmed by 1 H, 13 C-NMR spectrum. These results are shown in Table 3 as entry 5.
- Example 15 Hydrogenation of 2,3-dimethyl-2-butene A magnetic stirrer was added to a 20 mL Schlenk tube and dried under reduced pressure to 5 Pa, and then the Schlenk tube was replaced with an argon atmosphere. Ruthenium complex A (14 mg, 0.025 mmol) was added to the Schlenk tube as a catalyst, and dissolved in toluene (1 mL). To this solution was added 2,3-dimethyl-2-butene (54 ⁇ L, 1.0 mmol). The resulting solution was freeze degassed and the inside of the Schlenk tube was replaced with a hydrogen atmosphere, and then the solution was stirred at room temperature for 6 hours. Anisole was added as an internal standard, and the 1 H-NMR spectrum was measured to determine the structure and yield of the product. The structure of the obtained compound was confirmed by 1 H, 13 C-NMR spectrum. These results are shown in Table 3 as entry 6.
- Example 18 Reduction of N, N-dimethyl-3-phenylpropanamide A three-way cock was attached to a 20 mL eggplant flask, a magnetic stirrer was added, and heat drying was performed while reducing the pressure to 5 Pa. Replaced. Ruthenium complex A (0.27 mg, 5.0 ⁇ 10 ⁇ 4 mmol) was added to the flask as a catalyst. To this was added dimethylphenylsilane (681 ⁇ L) with a syringe, followed by N, N-dimethyl-3-phenylpropanamide (177 mg, 1.0 mmol). After stirring the solution at 25 ° C. for 7 hours, the remaining dimethylphenylsilane was distilled off under reduced pressure.
- the obtained crude product was purified by silica gel column chromatography using hexane / ethyl acetate (10/1) as a developing solvent, and 151 mg (0.79 mmol, 79%) of N, N-dimethyl-3-phenylpropylamine was obtained. Got. These results are shown in Table 4 as entry 3. The structure of the obtained amine was confirmed by 1 H, 13 C-NMR spectrum and IR spectrum.
- Example 19 Reduction of N-benzyl- ⁇ -caprolactam A three-way cock was attached to a 20 mL eggplant flask, a magnetic stirrer was added, and the mixture was heated and dried while reducing the pressure to 5 Pa, and then the atmosphere in the flask was replaced with an argon atmosphere. Ruthenium complex A (0.27 mg, 5.0 ⁇ 10 ⁇ 4 mmol) was added to the flask as a catalyst. To this was added dimethylphenylsilane (681 ⁇ L) with a syringe, followed by N-benzyl- ⁇ -caprolactam (203 mg, 1.0 mmol). After stirring the solution at 25 ° C.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Other In-Based Heterocyclic Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Description
このヒドロシリル化反応の触媒としては、Pt、Pd、Rh化合物が知られており、その中でも最も多く用いられているものはSpeier触媒、Karstedt触媒に代表されるPt化合物である。
また、オレフィンの種類により、α付加体とβ付加体の選択性が劣るという問題もある。
また、この特許文献1には先行文献としてRu触媒に関する多くの特許が引用されているが(特許文献2~6)、反応性、選択性、経済性の観点からいずれも貴金属元素系触媒に勝っているとは言えない。
空気中で安定かつ取り扱いが容易なヒドロシラン化合物、メチルハイドロジェンポリシロキサンを還元剤として使用する方法が数多く報告されているが、反応には強い酸またはルイス酸の添加や、高価な貴金属触媒を必要とする。最近、比較的安価なルテニウムを触媒とするカルボニル化合物の還元反応が報告されており、そのうちの一部は、従来法では過酷な条件を必要とするアミドの還元反応に適用した例も出ている。具体的なルテニウム触媒の例として非特許文献3~6が挙げられるが、より高いターンオーバー数を示す高活性触媒が望まれている。
1. 式(1)で表されることを特徴とする単核ルテニウム錯体、
2. 前記Lが、分子状水素、アミン、イミン、含窒素ヘテロ環、アルシン、アルコール、チオール、エーテル、スルフィド、ニトリル、イソニトリル、アルデヒド、ケトン、炭素数2~30のアルケン、炭素数2~30のアルキン、およびトリオルガノヒドロシランから選ばれる少なくとも1種の二電子配位子である1の単核ルテニウム錯体、
3. 前記nおよびmがいずれも2であり、前記Lが、スルフィド、チオールおよびトリオルガノヒドロシランから選ばれる少なくとも1種である(ただし、2つのLは互いに結合していてもよい)1または2の単核ルテニウム錯体、
4. 前記R1~R6が、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基(Xは前記と同じ意味を表す。)であり、かつ、前記Lが、H-SiR7R8R9およびH-SiR10R11R12(式中、R7~R12は、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基を表し、Xは前記と同じ意味を表す。)で表されるトリオルガノヒドロシランであり、R1~R3のいずれかと、R4~R6のいずれかの少なくとも1組もしくはR7~R9のいずれかの少なくとも1組が一緒になって、またはR10~R12のいずれかと、R4~R6のいずれかの少なくとも1組もしくはR7~R9のいずれかの少なくとも1組が一緒になって架橋置換基を形成していてもよく、R1~R3のいずれかと、R4~R6のいずれかの少なくとも1組またはR7~R9のいずれかの少なくとも1組が一緒になって架橋置換基を形成し、かつ、R10~R12のいずれかと、R4~R6のいずれかの少なくとも1組およびR7~R9のいずれかの少なくとも1組が一緒になって架橋置換基を形成していてもよい3の単核ルテニウム錯体、
5. 前記R1~R6が、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基(Xは前記と同じ意味を表す。)であり、かつ、前記Lが、SR13R14およびSR15R16(式中、R13~R16は、互いに独立して、水素原子、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基を表し、Xは前記と同じ意味を表す。)で表されるスルフィドまたはチオールであり、R13およびR14のいずれかと、R15およびR16のいずれかの少なくとも1組が一緒になって架橋置換基を形成していてもよい3の単核ルテニウム錯体、
6. 前記R1~R3のいずれか1つと、R4~R6のいずれか1つとが一緒になって架橋置換基を形成している1~5のいずれかの単核ルテニウム錯体、
7. 前記R1~R3のいずれか1つと、R4~R6のいずれか1つまたはR7~R9のいずれか1つとが一緒になって架橋置換基を形成し、かつ、R10~R12のいずれか1つと、R4~R6のいずれか1つおよびR7~R9のいずれか1つのうち前記架橋置換基の形成に関与してないSi上の置換基とが一緒になって架橋置換基を形成している4の単核ルテニウム錯体、
8. 前記R13およびR14のいずれか1つと、R15およびR16のいずれか1つとが一緒になって架橋置換基を形成している5または6の単核ルテニウム錯体、
9. 前記R1~R3のいずれか1つと、R4~R6のいずれか1つとが一緒になってYで置換されていてもよいo-フェニレン基を形成し(Yは、水素原子、ハロゲン原子、炭素数1~10のアルキル基、または炭素数1~10のアルコキシ基を表し、Yが複数存在する場合それらは互いに同一でも異なっていてもよい)、かつ、R10~R12のいずれか1つと、R7~R9のいずれか1つとが一緒になってYで置換されていてもよいo-フェニレン基(Yは前記を同じ意味を表す。)を形成している7の単核ルテニウム錯体、
10. 前記R1~R3のいずれか1つと、R4~R6のいずれか1つとが一緒になってYで置換されていてもよいo-フェニレン基を形成し(Yは、水素原子、ハロゲン原子、炭素数1~10のアルキル基、または炭素数1~10のアルコキシ基を表し、Yが複数存在する場合それらは互いに同一でも異なっていてもよい)、かつ、R13およびR14のいずれか1つと、R15およびR16のいずれか1つとが一緒になって炭素数1~6のアルキレン基を形成している8の単核ルテニウム錯体、
11. 1~10のいずれかの単核ルテニウム錯体からなる、ヒドロシリル化反応、水素化反応およびカルボニル化合物の還元反応の3つの反応に活性を有する触媒、
12. 11の触媒の存在下、脂肪族不飽和結合を有する化合物と、Si-H結合を有するヒドロシランまたはオルガノヒドロポリシロキサンとをヒドロシリル化反応させることを特徴とする付加化合物の製造方法、
13. 11の触媒の存在下、脂肪族不飽和結合を有する化合物を水素化させることを特徴とするアルカン化合物の製造方法、
14. 11の触媒の存在下、アミド化合物をSi-H結合を有するシランまたはオルガノヒドロポリシロキサンで還元することを特徴とするアミン化合物の製造方法、
15. 11の触媒の存在下、アルデヒド化合物、ケトン化合物またはエステル化合物をSi-H結合を有するシランまたはオルガノヒドロポリシロキサンで還元することを特徴とするアルコール化合物の製造方法
を提供する。
水素化反応は、室温および水素ガス1気圧の温和な条件下で行うことができ、しかも従来の方法では困難であった多置換アルケンの水素化にも有効である。
カルボニル化合物の還元反応では、アミド化合物、アルデヒド化合物、ケトン化合物、エステル化合物を、取り扱いが容易なSi-H基を有するシラン、あるいはポリシロキサンと反応させることによって目的とする還元化合物を得ることができる。
さらに、本発明の錯体化合物の優れている点は、同じ錯体化合物が、ヒドロシリル化反応、水素化反応、カルボニル化合物の還元反応から選択される複数の反応に対して高い触媒活性を示すことにあり、有機合成反応において極めて有用性が高いものである。
本発明に係る単核ルテニウム錯体は、式(1)で表されるように、Ru-Si結合を有し、かつ、Ruに少なくとも1つの一酸化炭素(CO)が配位しているものである。
アルキル基としては、直鎖、分岐鎖、環状のいずれでもよく、また、その炭素数も特に限定されるものではないが、好ましくは炭素数1~30、より好ましくは炭素数1~10のアルキル基であり、その具体例としては、メチル、エチル、n-プロピル、イソプロピル、n-ブチル、イソブチル、s-ブチル、t-ブチル、n-ペンチル、n-ヘキシル、n-ヘプチル、n-オクチル、n-ノニル、n-デシル、n-ウンデシル、n-ドデシル、n-トリデシル、n-テトラデシル、n-ペンタデシル、n-ヘキサデシル、n-ヘプタデシル、n-オクタデシル、n-ノナデシル、n-エイコサニル基等の直鎖または分岐鎖アルキル基;シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、シクロヘプチル、シクロオクチル、シクロノニル基等のシクロアルキル基などが挙げられる。
アラルキル基としても、その炭素数は特に限定されるものではないが、好ましくは炭素数7~30、より好ましくは炭素数7~20のアラルキル基であり、その具体例としては、ベンジル、フェニルエチル、フェニルプロピル、ナフチルメチル、ナフチルエチル、ナフチルプロピル基等が挙げられる。
アルコキシ基としては、特に限定されるものではないが、炭素数1~30、特に炭素数1~10のアルコキシ基が好ましく、その具体例としては、メトキシ、エトキシ、n-プロポキシ、i-プロポキシ、c-プロポキシ、n-ブトキシ、i-ブトキシ、s-ブトキシ、t-ブトキシ、n-ペントキシ、n-ヘキソキシ、n-ヘプチルオキシ、n-オクチルオキシ、n-ノニルオキシ、n-デシルオキシ基等が挙げられる。
アリールオキシ基としては、特に限定されるものではないが、炭素数6~30、特に炭素数6~20のアリールオキシ基が好ましく、その具体例としては、フェノキシ、1-ナフチルオキシ、2-ナフチルオキシ、アントリルオキシ、フェナントリルオキシ基等が挙げられる。
アラルキルオキシ基としては、特に限定されるものではないが、炭素数7~30、特に炭素数7~20のアリールオキシ基が好ましく、ベンジルオキシ基、フェニルエチルオキシ、フェニルプロピルオキシ、1または2-ナフチルメチルオキシ、1または2-ナフチルエチルオキシ、1または2-ナフチルプロピルオキシ基等が挙げられる。
オルガノチオ基としては、上記オルガノオキシ基の酸素原子を硫黄原子で置換した基等が挙げられる。
ハロゲン原子としては、フッ素、塩素、臭素、ヨウ素原子が挙げられるが、フッ素原子が好ましく、好適なフッ素置換アルキル基として、トリフロロプロピル基、ノナフロロヘキシル基、ヘプタデシルフロロデシル基等が挙げられる。
炭素数6~30のアリーレン基としては、o-フェニレン(1,2-フェニレン)、1,2-ナフチレン、1,8-ナフチレン、2,3-ナフチレン基等が挙げられる。
炭素数7~30のアラルキレン基としては、-(CH2)k-Ar-(Arは、炭素数6~20のアリーレン基を表し、kは上記と同じ意味を表す。)、-Ar-(CH2)k-(Arおよびkは上記と同じ意味を表す。)、-(CH2)k-Ar-(CH2)k-(Arは上記と同じ意味を表し、kは互いに独立して上記と同じ意味を表す。)等が挙げられる。
なお、上記アルキレン、アリーレン、アラルキレン基は、それらの水素原子の少なくとも1つが、置換基X(Xは上記と同じ。)で置換されていてもよい。
一価炭化水素基の具体例としては、アルキル基、アリール基、アラルキル基等が挙げられ、これらの具体例としては、上記と同様のものが挙げられる。
なお、アルキル基、アルコキシ基、ハロゲン原子としては、上記と同様のものが挙げられる。
二電子配位子としては、COおよびホスフィン以外であれば特に限定されるものではなく、金属錯体の二電子配位子として従来用いられているCO以外の任意の配位子を用いることができるが、典型的には、窒素、酸素、イオウ等の非共有電子対(不対電子)を含む、アミン、イミン、含窒素ヘテロ環、アルシン、アルコール、チオール、エーテル、スルフィド等の化合物;π電子を含む、アルケン、アルキン;不対電子とπ電子双方を含む、アルデヒド、ケトン、ニトリル、イソニトリル等の化合物;アゴスティック相互作用で結合する、分子状水素(H-H結合に含まれるσ電子が配位する)、ヒドロシラン(Si-H結合に含まれるσ電子が配位する)などが挙げられる。
イミンとしては、RC(=NR)R(Rは互いに独立して上記と同じ意味を表す。)で示されるものが挙げられる。
含窒素へテロ環としては、例えば、ピロール、イミダゾール、ピリジン、ピリミジン、オキサゾリン、イソオキサゾリン等が挙げられる。
アルシンとしては、例えば、R3As(Rは互いに独立して上記と同じ意味を表す。)で示されるものが挙げられる。
アルコールとしては、例えば、ROH(Rは上記と同じ意味を表す。)で示されるものが挙げられる。
チオールとしては、上記アルコールの酸素原子を硫黄原子で置換したものが挙げられる。
スルフィドとしては、上記エーテルの酸素原子を硫黄原子で置換したものが挙げられる。
ケトンとしては、例えば、RCOR(Rは互いに独立して上記と同じ意味を表す。)で示されるものが挙げられる。
イソニトリルとしては、例えば、RNC(Rは互いに独立して上記と同じ意味を表す。)で示されるものが挙げられる。
アルケンとしては、例えば、エテン、プロペン、1-ブテン、2-ブテン、1-ペンテン、2-ペンテン、シクロペンテン、1-ヘキセン、シクロヘキセン、1-ヘプテン、1-オクテン、1-ノネン、1-デセン等の炭素数2~30のアルケンが挙げられる。
アルキンとしては、例えば、エチン、プロピン、1-ブチン、2-ブチン、1-ペンチン、2-ペンチン、1-ヘキシン、1-ヘプチン、1-オクチン、1-ノニン、1-デシン等の炭素数2~30のアルケンが挙げられる。
ヒドロシランとしては、例えば、トリオルガノヒドロシランが挙げられ、具体的にはトリ炭素数1~30オルガノヒドロシランが挙げられ、より具体的には、R1R2R3SiH(R1~R3は上記と同じ意味を表す。)で示されるものが挙げられる。
なお、本発明の単核ルテニウム錯体では、Lが3個存在する場合に、それら全てが結合して3つの配位性2電子官能基を含む配位子はとらない。
また、COの配位数nと、Lの配位数mとの総和は3または4を満たすが、好ましくは4である。
この場合、二電子配位子Lは、ルテニウムと比較的弱く結合するものが触媒活性という点から有利であることから、上記好適なLの中でも、特に、チオール、スルフィド、トリオルガノヒドロシランがより好ましく、特に、SiHR7R8R9およびSiHR10R11R12(R7~R12は、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基を表し、Xは上記と同じ意味を表す。)で表される2つのトリオルガノヒドロシランや、SR13R14およびSR15R16(R13~R16は、互いに独立して、水素原子、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基を表し、Xは上記と同じ意味を表す。)で表される2つのスルフィドまたはチオールがより一層好ましい。
ここで、アルキル基、アリール基、アラルキル基の具体例としては、先に例示した基と同様のものが挙げられるが、それぞれ炭素数1~10のアルキル基、炭素数6~20のアリール基、炭素数7~20のアラルキル基が好ましく、炭素数1~10のアルキル基、炭素数6~20のアリール基がより好ましい。
このような架橋置換基Zを有する単核ルテニウム錯体を1つの配位構造を用いて表現した場合、下記式で示されるような構造が挙げられるが、これらに限定されるものではなく、また、上述のとおりこれ以外の配位構造異性体も存在し、その場合にも同様の架橋置換基Zを有する構造が存在する。
このような架橋置換基Zを有する単核ルテニウム錯体を1つの配位構造を用いて表現した場合、下記式で示されるような構造が挙げられるが、これらに限定されるものではなく、また、上述のとおりこれ以外の配位構造異性体も存在し、その場合にも同様の架橋置換基Zを有する構造が存在する。
なお、この場合に、単核ルテニウム錯体を構成する2つのケイ素原子も、上述した架橋置換基Zにより繋がれていてもよい。
ここで、アルキル基、アリール基、アラルキル基の具体例としては、先に例示した基と同様のものが挙げられるが、それぞれ炭素数1~10のアルキル基、炭素数6~20のアリール基、炭素数7~20のアラルキル基が好ましく、炭素数1~10のアルキル基、炭素数6~20のアリール基がより好ましい。
上記式(2)においても、単核ルテニウム錯体を構成する4つのケイ素原子の2つ以上は架橋置換基により繋がれていてもよく、具体的には、R1~R3のいずれかと、R4~R6のいずれかの少なくとも1組もしくはR7~R9のいずれかの少なくとも1組が一緒になって、またはR10~R12のいずれかと、R4~R6のいずれかの少なくとも1組もしくはR7~R9のいずれかの少なくとも1組が一緒になってアルキレン基、アリーレン基やアラルキレン基といった架橋置換基を形成していてもよく、またはR1~R3のいずれかと、R4~R6のいずれかの少なくとも1組またはR7~R9のいずれかの少なくとも1組が一緒になってアルキレン基、アリーレン基やアラルキレン基といった架橋置換基を形成し、かつ、R10~R12のいずれかと、R4~R6のいずれかの少なくとも1組およびR7~R9のいずれかの少なくとも1組が一緒になってアルキレン基、アリーレン基やアラルキレン基といった架橋置換基を形成していてもよい。
ここで、アルキレン基、アリーレン基、アラルキレン基の具体例としては、先に例示した基と同様のものが挙げられるが、それぞれ炭素数1~10のアルキレン基、炭素数7~20のアリーレン基、炭素数7~20のアラルキレン基が好ましく、炭素数1~6のアルキレン基、炭素数7~20のアリーレン基がより好ましい。
ここで、アルキル基、アリール基、アラルキル基の具体例としては、先に例示した基と同様のものが挙げられるが、それぞれ炭素数1~10のアルキル基、炭素数6~20のアリール基、炭素数7~20のアラルキル基が好ましく、炭素数1~10のアルキル基、炭素数6~20のアリール基がより好ましい。
上記式(3)においても、単核ルテニウム錯体を構成する2つの硫黄原子は架橋置換基により繋がれていてもよく、具体的には、R13およびR14のいずれかと、R15およびR16のいずれかの少なくとも1組が一緒になってアルキレン基、アリーレン基やアラルキレン基といった架橋置換基を形成していてもよい。
また、この場合に、単核ルテニウム錯体を構成する2つのケイ素原子も架橋置換基により繋がれていてもよく、具体的には、R1~R3のいずれかと、R4~R6のいずれかの少なくとも1組が一緒になってアルキレン基、アリーレン基やアラルキレン基といった架橋置換基を形成していてもよい。
ここで、アルキレン基、アリーレン基、アラルキレン基の具体例としては、先に例示した基と同様のものが挙げられるが、それぞれ炭素数1~10のアルキレン基、炭素数7~20のアリーレン基、炭素数7~20のアラルキレン基が好ましく、炭素数1~6のアルキレン基、炭素数7~20のアリーレン基がより好ましい。
本発明で好適に用いることのできる単核ルテニウム錯体を1つの配位構造を用いて表すと、式(4)および(5)で示されるものが挙げられ、より具体的には式(6)および(7)で示されるものが挙げられるが、上述のとおり、これらの配位構造異性体も好適に用いることができる。
例えば、上記式(4),(6)で示されるようなルテニウム錯体は、シクロヘキサジエニル基やシクロオクタジエニル基等のシクロアルカジエニル基を配位子として有するルテニウム-カルボニル錯体と、1,2-ビス(ジメチルシリル)ベンゼン等のビスシリル化合物とを、アルゴンガス等の不活性ガス雰囲気下、光照射して得ることができる。
この場合、ビスシリル化合物の使用量は、ルテニウム-カルボニル錯体に対して、1~10モル倍程度とすることができるが、2~5モル倍が好ましい。
また、有機溶媒としては、反応に影響を及ぼさない限りにおいて各種の溶媒類が使用でき、例えば、ペンタン、ヘキサン、ヘプタン、オクタン、シクロヘキサン等の脂肪族炭化水素類;ジエチルエーテル、ジイソプロピルエーテル、ジブチルエーテル、シクロペンチルメチルエーテル、テトラヒドロフラン、1,4-ジオキサン等のエーテル類;ベンゼン、トルエン、キシレン、メシチレン等の芳香族炭化水素類などを用いることができる。
反応温度は、有機溶媒の融点から沸点の範囲で適宜設定すればよいが、10~50℃が好ましく、15~30℃がより好ましい。
反応時間は、通常、1~48時間程度である。
反応終了後は、溶媒を留去した後、再結晶法等の公知の精製法にて目的物を得ることができるが、調製したルテニウム錯体を単離せずに目的とする反応の触媒として用いてもよい。
この場合、ジチア炭化水素化合物の使用量は、ルテニウム錯体に対して、1~3モル倍程度とすることができるが、1~1.5モル倍が好ましく、1~1.2モル倍がより好ましい。
反応温度は、0℃から有機溶媒の沸点の範囲で適宜設定すればよいが、10~50℃が好ましく、15~30℃が好ましい。
反応時間は、通常、1~48時間程度である。
反応終了後は、溶媒を留去した後、再結晶法等の公知の精製法にて目的物を得ることができるが、調製したルテニウム錯体を単離せずに目的とする反応の触媒として用いてもよい。
本発明の単核ルテニウム錯体を触媒として使用し、脂肪族不飽和結合を含有する、オレフィン化合物、シラン化合物またはオルガノポリシロキサン化合物等の脂肪族不飽和結合を有する化合物と、Si-H結合を有する、シラン化合物またはオルガノポリシロキサン化合物とのヒドロシリル化反応を行う場合、触媒の使用量は特に限定されるものではないが、室温~100℃程度の温和な条件下で反応を進行させて収率よく目的物を得ることを考慮すると、触媒の使用量は0.5モル%以上とすることが好ましい。
本発明の単核ルテニウム錯体を触媒として使用し、脂肪族不飽和結合を含有するオレフィン化合物を水素ガスによって還元し、飽和化合物を得る反応を行う場合も、触媒の使用量は特に限定されるものではないが、室温下、かつ、水素圧が1気圧程度の温和な条件下で反応を進行させて収率よく目的物を得ることを考慮すると、触媒の使用量は1モル%以上とすることが好ましい。
なお、いずれの反応においても、触媒使用量の上限は特に制限はないが、経済的な観点から10モル%程度である。
還元反応に供し得るカルボニル化合物としては、アミド、アルデヒド、ケトン、エステル、カルボン酸、カルボン酸塩(例えば、ナトリウム塩、カリウム塩等)基等を有する化合物が挙げられ、これらを本発明のルテニウム錯体触媒の存在下、Si-H基を含有するシランまたはシロキサンと反応させることによって、それぞれ対応するアミンやアルコール化合物へと導くことができる。
ルテニウム錯体の合成は、シュレンクテクニックもしくはグローブボックスを用いてすべての操作を窒素またはアルゴン雰囲気下で行い、遷移金属化合物の調製に用いた溶媒は、全て公知の方法で脱酸素、脱水を行った後に用いた。
アルケンのヒドロシリル化反応、アミドの還元反応および溶媒精製は、全て不活性ガス雰囲気下で行い、各種反応に用いた溶媒等は、全て予め公知の方法で精製、乾燥、脱酸素を行ったものを用いた。
1H,13C,29Si-NMRの測定は日本電子(株)製JNM-ECA600,JNM-LA400を、IR測定は日本分光(株)製FT/IR-550を、元素分析はPerkin Elmer製2400II/CHNを、X線結晶構造解析は(株)リガク製VariMax、MoKα線0.71069オングストロームを用いてそれぞれ行った。
なお、以下に示す化学構造式においては慣用的な表現法に従って水素原子を省略している。また、Meはメチル基を表す。
[実施例1]ルテニウム錯体Aの合成
アルゴン雰囲気下、100mLのシュレンク管に(η4-1,3-シクロヘキサジエン)ルテニウム(0)トリカルボニル錯体(500mg,1.87mmol)と1,2-ビス(ジメチルシリル)ベンゼン(800mg,4.11mmol)を仕込み、ここへ脱気・脱水処理したヘキサン(50mL)を加え、高圧水銀灯(ウシオ電機(株)製,UM-453B-A(450W))を用いて光照射をしながら室温下で22時間撹拌した。反応終了後、減圧乾燥し、得られた乾燥物をヘキサン(40mL)に溶解させ、遠心分離にて副生した少量の褐色不溶物を取り除いた。その後、ヘキサン溶液を減圧下で約25mLになるまで濃縮し、-35℃で再結晶して式(6)で代表的に示されるルテニウム錯体A(274mg/0.50mmol/27%)を得た。得られたルテニウム錯体Aの構造を図1に、1H-NMRの測定結果を図2に、13C-NMRの測定結果を図3にそれぞれ示す。
13C NMR (CDCl3, 395 MHz) δ = 8.4, 128.9, 131.4, 152.5, 198.4.
IR (KBr pellet): ν = 1975 (νSi-H), 1978 (νRu-CO) cm-1
Anal. Calcd. for C22H34O2RuSi4: C, 48.58; H, 6.30 Found: C, 48.34; H, 6.29
アルゴン雰囲気下、50mLのシュレンク管内で、ルテニウム錯体A(100mg,0.18mmol)を脱気・脱水処理したトルエン(20mL)に溶解させ、ここへ2,6-ジチアヘプタン(26mg,0.19mmol)を加え、室温下で12時間撹拌した。反応終了後、減圧乾燥し、得られた乾燥物をジエチルエーテル(10mL)に溶解させた後、溶液を減圧下で約5mLになるまで濃縮し、-35℃で再結晶をして式(7)で代表的に示されるルテニウム錯体B(82mg/0.17mmol/94%)を得た。得られたルテニウム錯体Bの構造を図4に、1H-NMRの測定結果を図5に、13C-NMRの測定結果を図6にそれぞれ示す。
13C NMR (CDCl3, 395 MHz) δ = 1.53, 6.39, 23.1, 25.6, 37.4, 127.5, 131.6, 157.5.
Anal. Calcd. for C17H28O2RuSi2S2: C, 42.03; H, 5.81 Found: C, 42.21; H, 5.69
[実施例3]2-オクテンの1,1,1,3,3-ペンタメチルジシロキサンによるヒドロシリル化
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここに1-オクテン(78.2μL,0.5mmol)を加え、さらに1,1,1,3,3-ペンタメチルジシロキサン(97.6μL,0.5mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソール(108.6μL,1.0mmol、使用量は以下同じ。)を加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー1として表1に示す。
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここに2-オクテン(78.2μL,0.5mmol)を加え、さらに1,1,1,3,5,5,5-ヘプタメチルトリシロキサン(135.7μL,0.5mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー2として表1に示す。
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここに2-オクテン(78.2μL,0.5mmol)を加え、さらにトリエトキシシラン(92.3μL,0.5mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー3として表1に示す。
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここに2-オクテン(78.2μL,0.5mmol)を加え、さらにトリエチルシラン(79.8μL,0.5mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー4として表1に示す。
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここに1-オクテン(78.2μL,0.5mmol)を加え、さらに1,1,1,3,3-ペンタメチルジシロキサン(97.6μL,1.0mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー1として表2に示す。
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここに1-オクテン(78.2μL,0.5mmol)を加え、さらに1,1,1,3,5,5,5-ヘプタメチルトリシロキサン(135.7μL,0.5mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー2として表2に示す。
20mLのシュレンクチューブに磁気撹拌子を加え、5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(8mg,0.015mmol)を加えた。ここにシクロペンテン(44.2μL,0.5mmol)を加え、さらに1,1,1,3,3-ペンタメチルジシロキサン(97.6μL,0.5mmol)を加えた後、溶液を80℃で3時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。これらの結果をエントリー3として表2に示す。
[実施例10]スチレンの水素化
20mLのシュレンクチューブに磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(14mg,0.02mmol)を加え、トルエン(1mL)に溶解させた。この溶液に、スチレン(57μL,0.5mmol)を加えた。得られた溶液を凍結脱気し、シュレンクチューブ内を水素雰囲気に置換した後、溶液を室温で3時間撹拌した。内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。これらの結果をエントリー1として表3に示す。
13C NMR (100MHz, CDCl3) δ= 15.6, 28.8, 125.6, 127.8, 128.3, 144.3.
20mLのシュレンクチューブに磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(14mg,0.025mmol)を加え、トルエン(1mL)に溶解させた。この溶液に、トランス-スチルベン(90mg,0.5mmol)を加えた。得られた溶液を凍結脱気し、シュレンクチューブ内を水素雰囲気に置換した後、溶液を室温で6時間撹拌した。内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。これらの結果をエントリー2として表3に示す。
13C NMR (CDCl3, 100 MHz) δ= 37.9, 125.9, 128.3, 128.5, 141.8.
20mLのシュレンクチューブに磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(14mg,0.025mmol)を加え、トルエン(1mL)に溶解させた。この溶液に、シクロヘキセン(54μL,0.5mmol)を加えた。得られた溶液を凍結脱気し、シュレンクチューブ内を水素雰囲気に置換した後、溶液を室温で6時間撹拌した。内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。これらの結果をエントリー3として表3に示す。
13C NMR (CDCl3, 100 MHz) δ= 27.0.
20mLのシュレンクチューブに磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(14mg,0.025mmol)を加え、トルエン(2mL)に溶解させた。この溶液に、シクロペンテン(44.2μL,0.5mmol)を加えた。得られた溶液を凍結脱気し、シュレンクチューブ内を水素雰囲気に置換した後、溶液を室温で6時間撹拌した。内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。これらの結果をエントリー4として表3に示す。
13C NMR (CDCl3, 100 MHz) δ= 25.9.
20mLのシュレンクチューブに磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(14mg,0.025mmol)を加え、トルエン(1mL)に溶解させた。この溶液に、1-メチル-1-シクロヘキセン(54μL,1.0mmol)を加えた。得られた溶液を凍結脱気し、シュレンクチューブ内を水素雰囲気に置換した後、溶液を室温で6時間撹拌した。内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。これらの結果をエントリー5として表3に示す。
13C NMR (CDCl3, 100 MHz) δ= 22.9, 26.3, 26.4, 32.7, 35.4.
20mLのシュレンクチューブに磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体A(14mg,0.025mmol)を加え、トルエン(1mL)に溶解させた。この溶液に、2,3-ジメチル-2-ブテン(54μL,1.0mmol)を加えた。得られた溶液を凍結脱気し、シュレンクチューブ内を水素雰囲気に置換した後、溶液を室温で6時間撹拌した。内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。これらの結果をエントリー6として表3に示す。
13C NMR (CDCl3, 100 MHz) δ= 19.4, 33.7.
[実施例16]N,N-ジメチル-4-メトキシベンズアミドの還元
20mLのナスフラスコに三方コックを付け、磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、フラスコ内をアルゴン雰囲気に置換した。そのフラスコに、触媒としてルテニウム錯体A(0.27mg,5.0×10-4mmol)を加えた。ここへ、ジメチルフェニルシラン(681μL)をシリンジで加えた後、N,N-ジメチル-4-メトキシベンズアミド(179mg,1.0mmol)を加えた。溶液を25℃で5時間撹拌した後、残ったジメチルフェニルシランを減圧下で留去した。得られた粗生成物をヘキサン/酢酸エチル(10/1)を展開溶媒としたシリカゲル充填カラムクロマトグラフィーにて精製し、N,N-ジメチル-4-メトキシベンジルアミン149mg(0.90mmol、90%)を得た。これらの結果をエントリー1として表4に示す。得られたアミンは、1H,13C-NMRスペクトル、IRスペクトルによりその構造を確認した。
13C NMR (CDCl3, 395 MHz) δ = 45.22, 55.07, 63.74, 130.23, 113.58, 131.15, 158.71.
IR (neat): ν = 1038, 1241, 1510, 2766, 2813,2941 cm-1
20mLのナスフラスコに三方コックを付け、磁気撹拌子を加えて5Paで減圧しながら加熱乾燥した後、フラスコ内をアルゴン雰囲気に置換した。そのフラスコに、触媒としてルテニウム錯体A(2.4mg,4.5×10-3mmol)を加えた。ここへ、ジメチルフェニルシラン(681μL)をシリンジで加えた後、N,N-ジメチル-4-ブロモベンズアミド(228mg,1.0mmol)を加えた。溶液を25℃で23時間撹拌した後、残ったジメチルフェニルシランを減圧下で留去した。得られた粗生成物をヘキサン/酢酸エチル(20/1)を展開溶媒としたシリカゲル充填カラムクロマトグラフィーにて精製し、N,N-ジメチル-4-ブロモベンジルアミン184mg(0.86mmol、86%)を得た。これらの結果をエントリー2として表4に示す。得られたアミンは、1H,13C-NMRスペクトル、IRスペクトルによりその構造を確認した。
13C NMR (CDCl3, 395 MHz) δ = 45.97, 64.30, 121.45, 131.33, 131.97,138.67.
IR (neat): ν = 1011, 1487, 2767, 2815,2941 cm-1.
20mLのナスフラスコに三方コックを付け、磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、フラスコ内をアルゴン雰囲気に置換した。そのフラスコに、触媒としてルテニウム錯体A(0.27mg,5.0×10-4mmol)を加えた。ここへ、ジメチルフェニルシラン(681μL)をシリンジで加えた後、N,N-ジメチル-3-フェニルプロパンアミド(177mg,1.0mmol)を加えた。溶液を25℃で7時間撹拌した後、残ったジメチルフェニルシランを減圧下で留去した。得られた粗生成物をヘキサン/酢酸エチル(10/1)を展開溶媒としたシリカゲル充填カラムクロマトグラフィーにて精製し、N,N-ジメチル-3-フェニルプロピルアミン151mg(0.79mmol、79%)を得た。これらの結果をエントリー3として表4に示す。得られたアミンは、1H,13C-NMRスペクトル、IRスペクトルによりその構造を確認した。
13C NMR (CDCl3, 395 MHz) δ = 29.57, 33.79, 45.60, 59.41, 125.84, 128.42, 128.50,142.40.
IR (neat): ν = 1030, 1496, 2764, 2942, 3025, 3060 cm-1.
20mLのナスフラスコに三方コックを付け、磁気撹拌子を加えて5Paに減圧しながら加熱乾燥した後、フラスコ内をアルゴン雰囲気に置換した。そのフラスコに、触媒としてルテニウム錯体A(0.27mg,5.0×10-4mmol)を加えた。ここへ、ジメチルフェニルシラン(681μL)をシリンジで加えた後、N-ベンジル-ε-カプロラクタム(203mg,1.0mmol)を加えた。溶液を25℃で7時間撹拌した後、残ったジメチルフェニルシランを減圧下で留去した。得られた粗生成物をヘキサン/酢酸エチル(10/1)を展開溶媒としたシリカゲル充填カラムクロマトグラフィーで精製し、1-ベンジルアゼパン165mg(0.87mmol、87%)を得た。これらの結果をエントリー4として表4に示す。得られたアミンは、1H,13C-NMRスペクトル、IRスペクトルによりその構造を確認した。
13C NMR (CDCl3, 395 MHz) δ = 27.19, 28.40, 55.76, 62.90, 126.79, 128.22, 128.90,140.30.
IR (neat): ν = 1071, 1354, 1452, 2851,2923 cm-1.
[実施例20]エチレンの1,1,1,3,3-ペンタメチルジシロキサンによるヒドロシリル化
20mLのシュレンクチューブに磁気撹拌子を加え、5Paで減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブに、触媒としてルテニウム錯体B(14mg,0.03mmol)を加えた。ここに1,1,1,3,3-ペンタメチルジシロキサン(195.2μL,1.0mmol)を加えた。得られた溶液を凍結脱気した後、シュレンクチューブ内をエチレン雰囲気に置換した。その後、溶液を80℃で16時間撹拌した。冷却後、内標としてアニソールを加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した(収率55%)。得られた化合物は、1H,13C,29Si-NMRスペクトルによりその構造を確認した。
13C NMR (100MHz, CDCl3) δ = -0.28, 1.93, 6.72, 10.03.
29Si NMR (119MHz, CDCl3) δ = 7.05, 8.60.
[実施例21]スチレンの水素化
20mLのシュレンクチューブに、磁気撹拌子を加えて5Paで減圧しながら加熱乾燥した後、シュレンクチューブ内をアルゴン雰囲気に置換した。そのシュレンクチューブ内に、触媒としてルテニウム錯体B(12mg,0.025mmol)を加え、トルエン(1mL)に溶解させた。この溶液に、スチレン(57μL,0.5mmol)を加えた。得られた溶液を凍結脱気した後、シュレンクチューブ内を水素雰囲気に置換した。その後、溶液を100℃で16時間撹拌した。内標としてアニソール(108.6μL,1.0mmol)を加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した(収率71%)。得られた化合物は、1H,13C-NMRスペクトルによりその構造を確認した。
13C NMR (100MHz, CDCl3) δ = 15.6, 28.8, 125.6, 127.8, 128.3, 144.3.
[実施例22]N,N-ジメチル-4-メトキシベンズアミドの還元
20mLのナスフラスコに三方コックを付け、磁気撹拌子を加えて5Paで減圧しながら加熱乾燥した後、フラスコ内をアルゴン雰囲気に置換した。そのフラスコに、触媒としてルテニウム錯体B(12mg,0.025mmol)を加え、トルエン(0.25mL)に溶解させた。この溶液に、1,2-ビス(ジメチルシリル)ベンゼン(238μL)をシリンジで加え、次に、N,N-ジメチル-4-メトキシベンズアミド(90mg,0.5mmol)を加えた。その後、溶液を100℃で16時間撹拌した。冷却後、内標としてフェロセン(18.6mg,1.0mmol)を加え、1H-NMRスペクトルを測定し、生成物の構造および収率を決定した(収率99%)。得られた化合物は、1H,13C-NMRスペクトル、IRスペクトルによりその構造を確認した。
13C NMR (CDCl3, 395 MHz) δ = 45.22, 55.07, 63.74, 130.23,113.58, 131.15,158.71.
IR (neat): ν = 1038, 1241, 1510, 2766, 2813,2941 cm-1
Claims (15)
- 式(1)で表されることを特徴とする単核ルテニウム錯体。
Xは、ハロゲン原子、オルガノオキシ基、モノオルガノアミノ基、ジオルガノアミノ基、またはオルガノチオ基を表し、
Lは、COおよびホスフィン以外の二電子配位子を表し、Lが複数存在する場合、それらは互いに同一でも異なっていてもよく、Lが2個の場合、それらは互いに結合していてもよく、
nおよびmは、互いに独立して1~3の整数を表すが、n+mは3または4を満たす。) - 前記Lが、分子状水素、アミン、イミン、含窒素ヘテロ環、アルシン、アルコール、チオール、エーテル、スルフィド、ニトリル、イソニトリル、アルデヒド、ケトン、炭素数2~30のアルケン、炭素数2~30のアルキン、およびトリオルガノヒドロシランから選ばれる少なくとも1種の二電子配位子である請求項1記載の単核ルテニウム錯体。
- 前記nおよびmがいずれも2であり、
前記Lが、スルフィド、チオールおよびトリオルガノヒドロシランから選ばれる少なくとも1種である(ただし、2つのLは互いに結合していてもよい)請求項1または2記載の単核ルテニウム錯体。 - 前記R1~R6が、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基(Xは前記と同じ意味を表す。)であり、かつ、
前記Lが、H-SiR7R8R9およびH-SiR10R11R12(式中、R7~R12は、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基を表し、Xは前記と同じ意味を表す。)で表されるトリオルガノヒドロシランであり、
R1~R3のいずれかと、R4~R6のいずれかの少なくとも1組もしくはR7~R9のいずれかの少なくとも1組が一緒になって、またはR10~R12のいずれかと、R4~R6のいずれかの少なくとも1組もしくはR7~R9のいずれかの少なくとも1組が一緒になって架橋置換基を形成していてもよく、
R1~R3のいずれかと、R4~R6のいずれかの少なくとも1組またはR7~R9のいずれかの少なくとも1組が一緒になって架橋置換基を形成し、かつ、R10~R12のいずれかと、R4~R6のいずれかの少なくとも1組およびR7~R9のいずれかの少なくとも1組が一緒になって架橋置換基を形成していてもよい請求項3記載の単核ルテニウム錯体。 - 前記R1~R6が、互いに独立して、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基(Xは前記と同じ意味を表す。)であり、かつ、
前記Lが、SR13R14およびSR15R16(式中、R13~R16は、互いに独立して、水素原子、Xで置換されていてもよい、アルキル基、アリール基またはアラルキル基を表し、Xは前記と同じ意味を表す。)で表されるスルフィドまたはチオールであり、
R13およびR14のいずれかと、R15およびR16のいずれかの少なくとも1組が一緒になって架橋置換基を形成していてもよい請求項3記載の単核ルテニウム錯体。 - 前記R1~R3のいずれか1つと、R4~R6のいずれか1つとが一緒になって架橋置換基を形成している請求項1~5のいずれか1項記載の単核ルテニウム錯体。
- 前記R1~R3のいずれか1つと、R4~R6のいずれか1つまたはR7~R9のいずれか1つとが一緒になって架橋置換基を形成し、かつ、R10~R12のいずれか1つと、R4~R6のいずれか1つおよびR7~R9のいずれか1つのうち前記架橋置換基の形成に関与してないSi上の置換基とが一緒になって架橋置換基を形成している請求項4記載の単核ルテニウム錯体。
- 前記R13およびR14のいずれか1つと、R15およびR16のいずれか1つとが一緒になって架橋置換基を形成している請求項5または6記載の単核ルテニウム錯体。
- 前記R1~R3のいずれか1つと、R4~R6のいずれか1つとが一緒になってYで置換されていてもよいo-フェニレン基を形成し(Yは、水素原子、ハロゲン原子、炭素数1~10のアルキル基、または炭素数1~10のアルコキシ基を表し、Yが複数存在する場合それらは互いに同一でも異なっていてもよい)、かつ、R10~R12のいずれか1つと、R7~R9のいずれか1つとが一緒になってYで置換されていてもよいo-フェニレン基(Yは前記を同じ意味を表す。)を形成している請求項7記載の単核ルテニウム錯体。
- 前記R1~R3のいずれか1つと、R4~R6のいずれか1つとが一緒になってYで置換されていてもよいo-フェニレン基を形成し(Yは、水素原子、ハロゲン原子、炭素数1~10のアルキル基、または炭素数1~10のアルコキシ基を表し、Yが複数存在する場合それらは互いに同一でも異なっていてもよい)、かつ、R13およびR14のいずれか1つと、R15およびR16のいずれか1つとが一緒になって炭素数1~6のアルキレン基を形成している請求項8記載の単核ルテニウム錯体。
- 請求項1~10のいずれか1項記載の単核ルテニウム錯体からなる、ヒドロシリル化反応、水素化反応およびカルボニル化合物の還元反応の3つの反応に活性を有する触媒。
- 請求項11記載の触媒の存在下、脂肪族不飽和結合を有する化合物と、Si-H結合を有するヒドロシランまたはオルガノヒドロポリシロキサンとをヒドロシリル化反応させることを特徴とする付加化合物の製造方法。
- 請求項11記載の触媒の存在下、脂肪族不飽和結合を有する化合物を水素化させることを特徴とするアルカン化合物の製造方法。
- 請求項11記載の触媒の存在下、アミド化合物をSi-H結合を有するシランまたはオルガノヒドロポリシロキサンで還元することを特徴とするアミン化合物の製造方法。
- 請求項11記載の触媒の存在下、アルデヒド化合物、ケトン化合物またはエステル化合物をSi-H結合を有するシランまたはオルガノヒドロポリシロキサンで還元することを特徴とするアルコール化合物の製造方法。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14756744.0A EP2963046B1 (en) | 2013-03-01 | 2014-02-26 | Mononuclear ruthenium complex and organic synthesis reaction using same |
| CN201480011637.9A CN105026409B (zh) | 2013-03-01 | 2014-02-26 | 单核钌络合物和使用了该单核钌络合物的有机合成反应 |
| KR1020157026839A KR101807167B1 (ko) | 2013-03-01 | 2014-02-26 | 단핵 루테늄 착물 및 그것을 사용한 유기 합성 반응 |
| JP2015502958A JP6089286B2 (ja) | 2013-03-01 | 2014-02-26 | 単核ルテニウム錯体およびそれを使用した有機合成反応 |
| US14/771,765 US9782762B2 (en) | 2013-03-01 | 2014-02-26 | Substituted mononuclear ruthenium complexes for catalysis of synthetic organic reactions |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013-040906 | 2013-03-01 | ||
| JP2013040906 | 2013-03-01 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014133014A1 true WO2014133014A1 (ja) | 2014-09-04 |
Family
ID=51428276
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/054715 WO2014133014A1 (ja) | 2013-03-01 | 2014-02-26 | 単核ルテニウム錯体およびそれを使用した有機合成反応 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9782762B2 (ja) |
| EP (1) | EP2963046B1 (ja) |
| JP (1) | JP6089286B2 (ja) |
| KR (1) | KR101807167B1 (ja) |
| CN (1) | CN105026409B (ja) |
| WO (1) | WO2014133014A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3323505B1 (en) * | 2015-07-14 | 2024-07-17 | Kyushu University, National University Corporation | Hydrosilylation reaction catalyst |
| JP6956475B2 (ja) * | 2016-09-28 | 2021-11-02 | エルジー ディスプレイ カンパニー リミテッド | 電子部品の実装方法、電子部品の接合構造、基板装置、ディスプレイ装置、ディスプレイシステム |
| EP3645608B1 (en) * | 2017-06-26 | 2024-06-19 | Dow Silicones Corporation | Method for hydrosilylation of aliphatically unsaturated alkoxys i lan es and hydrogen terminated organosiloxane oligomers to prepare alkoxysilyl terminated polymers useful for functionalizing polyorganosiloxanes using a cobalt catalyst |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2810032A1 (de) | 1977-03-23 | 1978-09-28 | Chisso Corp | Verfahren zur herstellung von substituierten dichlorsilanen |
| EP0403706A2 (en) | 1989-05-31 | 1990-12-27 | Tonen Corporation | Process for preparing amino-propyl silanes |
| JPH0532561B2 (ja) | 1985-04-05 | 1993-05-17 | Honda Motor Co Ltd | |
| US5248802A (en) | 1993-02-16 | 1993-09-28 | Dow Corning Corporation | Ruthenim catalyzed process for preparation of β-cyanoalkylsilanes |
| WO1996005207A1 (en) * | 1994-08-15 | 1996-02-22 | The Trustees Of The University Of Pennsylvania | Method of synthesizing arylsilanes |
| US5559264A (en) | 1994-02-24 | 1996-09-24 | Osi Specialities, Inc. | Process for making chloroorganosilicon compounds |
| US20040092759A1 (en) | 2002-11-12 | 2004-05-13 | Westmeyer Mark D. | Process for making haloalkylalkoxysilanes |
| WO2009055912A1 (en) * | 2007-10-30 | 2009-05-07 | Kanata Chemical Technologies Inc. | Cationic transition metal catalysts |
| JP2009533374A (ja) * | 2006-04-13 | 2009-09-17 | ワッカー ケミー アクチエンゲゼルシャフト | 新規のRu−錯体、その製造及び使用 |
| JP2011045798A (ja) * | 2009-08-25 | 2011-03-10 | Osaka City Univ | 脱水素シリル化反応用触媒、及び有機ケイ素化合物の製造方法 |
-
2014
- 2014-02-26 US US14/771,765 patent/US9782762B2/en active Active
- 2014-02-26 WO PCT/JP2014/054715 patent/WO2014133014A1/ja active Application Filing
- 2014-02-26 CN CN201480011637.9A patent/CN105026409B/zh active Active
- 2014-02-26 JP JP2015502958A patent/JP6089286B2/ja active Active
- 2014-02-26 EP EP14756744.0A patent/EP2963046B1/en active Active
- 2014-02-26 KR KR1020157026839A patent/KR101807167B1/ko active Active
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2810032A1 (de) | 1977-03-23 | 1978-09-28 | Chisso Corp | Verfahren zur herstellung von substituierten dichlorsilanen |
| JPH0532561B2 (ja) | 1985-04-05 | 1993-05-17 | Honda Motor Co Ltd | |
| EP0403706A2 (en) | 1989-05-31 | 1990-12-27 | Tonen Corporation | Process for preparing amino-propyl silanes |
| US5248802A (en) | 1993-02-16 | 1993-09-28 | Dow Corning Corporation | Ruthenim catalyzed process for preparation of β-cyanoalkylsilanes |
| US5559264A (en) | 1994-02-24 | 1996-09-24 | Osi Specialities, Inc. | Process for making chloroorganosilicon compounds |
| WO1996005207A1 (en) * | 1994-08-15 | 1996-02-22 | The Trustees Of The University Of Pennsylvania | Method of synthesizing arylsilanes |
| US20040092759A1 (en) | 2002-11-12 | 2004-05-13 | Westmeyer Mark D. | Process for making haloalkylalkoxysilanes |
| JP2009533374A (ja) * | 2006-04-13 | 2009-09-17 | ワッカー ケミー アクチエンゲゼルシャフト | 新規のRu−錯体、その製造及び使用 |
| WO2009055912A1 (en) * | 2007-10-30 | 2009-05-07 | Kanata Chemical Technologies Inc. | Cationic transition metal catalysts |
| JP2011045798A (ja) * | 2009-08-25 | 2011-03-10 | Osaka City Univ | 脱水素シリル化反応用触媒、及び有機ケイ素化合物の製造方法 |
Non-Patent Citations (10)
Also Published As
| Publication number | Publication date |
|---|---|
| JP6089286B2 (ja) | 2017-03-08 |
| EP2963046A4 (en) | 2016-08-17 |
| EP2963046A1 (en) | 2016-01-06 |
| KR20150121721A (ko) | 2015-10-29 |
| US20160023197A1 (en) | 2016-01-28 |
| CN105026409A (zh) | 2015-11-04 |
| CN105026409B (zh) | 2018-12-11 |
| KR101807167B1 (ko) | 2018-01-10 |
| US9782762B2 (en) | 2017-10-10 |
| JPWO2014133014A1 (ja) | 2017-02-02 |
| EP2963046B1 (en) | 2018-10-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3071584B1 (en) | Cobalt catalysts and their use for hydrosilylation and dehydrogenative silylation | |
| JP6327426B2 (ja) | ヒドロシリル化反応触媒 | |
| WO2016024611A1 (ja) | ヒドロシリル化反応触媒 | |
| JP6085892B2 (ja) | 単核鉄錯体およびそれを使用した有機合成反応 | |
| WO2017126562A1 (ja) | 新規イソシアニド化合物及びヒドロシリル化反応触媒 | |
| JP6761997B2 (ja) | ヒドロシリル化鉄触媒 | |
| JP6241966B2 (ja) | 単核ルテニウム錯体およびそれを使用した有機合成反応 | |
| JP6089286B2 (ja) | 単核ルテニウム錯体およびそれを使用した有機合成反応 | |
| JP6617264B2 (ja) | 単核鉄錯体およびそれを使用した有機合成反応 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201480011637.9 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14756744 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015502958 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14771765 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014756744 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 20157026839 Country of ref document: KR Kind code of ref document: A |