5-CHINOLINDERIVATE MIT ANTIBAKTΞRIELLER AKTIVITÄT 5-CHINOLINE DERIVATIVES WITH ANTIBACTERIAL ACTIVITY
In vielen Ländern der Welt hat die Resistenz gegenüber den derzeit gebräuchlichen Antibiotika in den letzten Jahren beträchtlich zugenommen und zum Teil bedrohliche Ausmaße angenommen. Das Hauptproblem dabei ist, dass diese Erreger nicht nur eine, sondern in der Regel mehrfache Resistenzen tragen. Dies gilt insbesondere für einige Gram-positive Erregergruppen, wie Staphylokokken, Pneumokokken und Enterokokken (S. Ewig et al . , Antibiotika-Resistenz bei Erregern ambulant erworbener Atemwegsinfektionen, Chemother. J. 2002, 11, 12-26; F. Tenover, Development and spread of bacterial resistance to antimicrobial agents : an overview, Clin. Infect. Dis. 2001 Sep 15, 33 Suppl . 3, 108- 115).In many countries of the world, resistance to currently used antibiotics has increased considerably in recent years and has in some cases reached alarming proportions. The main problem is that these pathogens carry not only one, but usually multiple resistances. This is especially true for some Gram-positive pathogen groups, such as staphylococci, pneumococci and enterococci (S.Ewig et al., Antibiotic resistance in pathogens from community-acquired respiratory tract infections, Chemother J. 2002, 11, 12-26, F. Tenover, Development and spread of bacterial resistance to antimicrobial agents: an overview, Clin. Infect. Dis. 2001 Sep 15, 33 Suppl. 3, 108-115).
Eine lange befürchtete Entwicklung ist kürzlich eingetreten: In den USA wurde der erste Stamm von Staphylococcus aureus beschrieben, welcher nicht nur Methicillin- resistent, sondern auch gegen Vancomycin hoch-resistent ist (Centers for Disease Control and Prevention, Staphylococcus aureus resistant to vancomycin - United States, 2002, MMWR 2002, 51, 565-567) .A long-feared development has recently occurred: in the USA, the first strain of Staphylococcus aureus has been described, which is not only resistant to methicillin but is also highly resistant to vancomycin (Centers for Disease Control and Prevention, Staphylococcus aureus resistant to vancomycin - United States, 2002, MMWR 2002, 51, 565-567).
Neben hygienischen Maßnahmen in Krankenhäusern sind daher auch verstärkt Anstrengungen erforderlich, neue Antibiotika zu finden, die möglichst eine neue Struktur und einen neuen Wirkungsmechanismus besitzen, um gegen diese Problemkeime wirksam zu sein.In addition to hygienic measures in hospitals, therefore, more efforts are needed to find new antibiotics that have as possible a new structure and a new mechanism of action to be effective against these problematic germs.
Die vorliegende Anmeldung beschreibt neuartige Verbindungen mit antibakterieller Aktivität. Diese Verbindungen sind unter anderem als Inhibitoren von DNA Gyrase und
Topoisomerasen (z.B. Topoisomerase II und IV) von Interesse .The present application describes novel compounds having antibacterial activity. These compounds are, inter alia, as inhibitors of DNA gyrase and Topoisomerases (eg topoisomerase II and IV) of interest.
Die vorliegende Erfindung betrifft Verbindungen der allgemeinen Formel (I) :The present invention relates to compounds of the general formula (I):
R1 ein Wasserstoffatom, ein Halogenatom, eine Hydroxy-, eine Amino-, eine Cyano-, eine Nitro-, eine Thiol-, eineR 1 is a hydrogen atom, a halogen atom, a hydroxy, an amino, a cyano, a nitro, a thiol, a
Ci-C6-Alkyl-, eine C2~C6-Alkenyl- , eine C2-C6-Alkinyl- , eine Heteroalkyl- , eine Alkyloxy-, eine Heteroalkyloxy- , eine Cycloalkyloxy- , eine Alkylcycloalkyloxy- , eine Hetero- cycloalkyloxy- oder eine Heteroalkylcycloalkyloxygruppe ist;Ci-C 6 alkyl, a C 2 ~ C 6 alkenyl group, a C 2 -C 6 alkynyl, a heteroalkyl, an alkyloxy, a Heteroalkyloxy-, a cycloalkyloxy, a Alkylcycloalkyloxy-, a hetero - cycloalkyloxy or a heteroalkylcycloalkyloxy group;
R2 ein Wasserstoffatom, ein Halogenatom, eine Hydroxy-, eine Amino-, eine Cyano-, Ci-Cβ-Alkyl-, C2-C6-Alkenyl-, C2-C6-Alkinyl- oder eine Heteroalkylgruppe ist;R 2 is a hydrogen atom, a halogen atom, a hydroxy, an amino, a cyano, C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl, C 2 -C 6 -alkynyl or a heteroalkyl group;
R3 eine Gruppe der folgenden Formel ist:R 3 is a group of the following formula:
wobei U und V unabhängig voneinander Stickstoffatome oder Gruppen der Formel CH oder CR6 sind;
die Reste R4 unabhängig voneinander ein Halogenatom, eine Hydroxy-, Amino-, Cyano-, Nitro- oder Thiolgruppe, ein Alkyl-, Alkenyl-, Alkinyl- oder Heteroalkylrest sind;wherein U and V are independently nitrogen atoms or groups of the formula CH or CR 6 ; R 4 is independently halogen, hydroxy, amino, cyano, nitro or thiol, alkyl, alkenyl, alkynyl or heteroalkyl;
n gleich 0, 1 oder 2 ist;n is 0, 1 or 2;
R5 ein Alkyl-, Alkenyl-, Alkinyl-, Heteroalkyl-, Aryl-, Heteroaryl-, Cycloalkyl-, Alkylcycloalkyl- , Heteroalkyl- cycloalkyl-, Heterocycloalkyl-, Aralkyl- oder ein Hetero- aralkylrest ist;R 5 is an alkyl, alkenyl, alkynyl, heteroalkyl, aryl, heteroaryl, cycloalkyl, alkylcycloalkyl, heteroalkyl, cycloalkyl, heterocycloalkyl, aralkyl or heteroaralkyl radical;
die Gruppen R6 unabhängig voneinander ein Halogenatom, eine Hydroxy-, Alkyl-, Alkenyl-, Alkinyl- oder eine Heteroalkyl- gruppe sind;the groups R 6 are independently a halogen atom, a hydroxy, alkyl, alkenyl, alkynyl or heteroalkyl group;
A aus folgenden Gruppen ausgewählt ist: -CR10 (OR11) CR12R13-, -CR8R9CR10 (OR11) -, -OCR8R9CR12R13-, -CR8R9CR12R13O-, -CR8R9SO2-, -SO2CR8R9-, -CR8R9NR7-, -NR7CR8R9-, -CR8R9O-, -OCR8R9-, -CR8R9S-, -SCR8R9-, -NR7C (=0)-, -C(=0)NR7- und -CR8R9CR12R13-;A is selected from the following groups: -CR 10 (OR 11 ) CR 12 R 13 -, -CR 8 R 9 CR 10 (OR 11 ) -, -OCR 8 R 9 CR 12 R 13 -, -CR 8 R 9 CR 12 R 13 O-, -CR 8 R 9 SO 2 -, -SO 2 CR 8 R 9 -, -CR 8 R 9 NR 7 -, -NR 7 CR 8 R 9 -, -CR 8 R 9 O-, -OCR 8 R 9 -, -CR 8 R 9 S-, -SCR 8 R 9 -, -NR 7 C (= O) -, -C (= O) NR 7 - and -CR 8 R 9 CR 12 R 13 -;
R7 ein Wasserstoffatom, eine Trifluormethyl-, Ci-Cβ-Alkyl-, C2-C6-Alkenyl-, Ci-C6-Alkoxycarbonyl- , Ci-Cβ-Alkylcarbonyl- oder eine Carbonylaminogruppe ist, wobei die Aminogruppe der Carbonylaminogruppe gegebenenfalls durch eine Ci-Cβ- Alkoxycarbonyl- , Ci-Cε-Alkylcarbonyl- , C2~C6-Alkenyloxy- carbonyl-, C2-C6-Alkenylcarbonyl- , d-C6-Alkyl- , C2-C6- Alkenyl- und gegebenenfalls weiter durch eine Ci-C6-Alkyl- oder eine C2-C6-Alkenylgruppe substituiert sein kann;R 7 is a hydrogen atom, a trifluoromethyl, Ci-Cβ alkyl, C 2 -C 6 alkenyl, Ci-C 6 alkoxycarbonyl, Ci-Cβ-alkylcarbonyl or a carbonylamino group wherein the amino group of carbonylamino optionally carbonyl- 6 alkenyloxy by a Ci-Cβ- alkoxycarbonyl, Ci-Cε alkylcarbonyl, C2 ~ C, C 2 -C 6 -Alkenylcarbonyl-, dC 6 alkyl, C 2 -C 6 - alkenyl, and optionally further substituted by a Ci-C 6 alkyl or a C 2 -C 6 alkenyl group may be substituted;
die Reste R8, R9, R10, R12 und R13 unabhängig voneinander ein Wasserstoffatom, ein Halogenatom, ein Azid, eine Trifluor-
methyl-, Hydroxy- , Amino-, Ci-Cβ-Alkyloxy- , Ci-Cβ-Alkyl- thio-, Ci-C6-Alkyl-, C2-C6-Alkenyl- , Ci-Cβ-Alkoxycarbonyl-, C2-C6-Alkenyloxycarbonyl-, Ci-C6-Alkylsulfonyl- , C2-CO- Alkenylsulfonyl- oder eine Sulfonylaminogruppe sind, wobei die Aminogruppe der Sulfonylaminogruppe gegebenenfalls durch eine Ci-Cβ-Alkyl- oder eine Phenylgruppe substituiert sein kann;the radicals R 8 , R 9 , R 10 , R 12 and R 13 independently of one another represent a hydrogen atom, a halogen atom, an azide, a trifluoro- methyl, hydroxy, amino, Ci-Cβ-alkyloxy, Ci-Cβ alkyl thio, Ci-C 6 alkyl, C 2 -C 6 alkenyl, Ci-Cβ alkoxycarbonyl, C 2 -C 6 -Alkenyloxycarbonyl-, Ci-C 6 alkylsulfonyl, C 2 -C O - alkenylsulfonyl or a sulfonylamino group are wherein the amino group of the sulfonylamino group may be optionally substituted by a Ci-Cβ alkyl or phenyl;
R11 ein Wasserstoffatom, eine Trifluormethyl- , Ci-Cβ-Alkyl-, C2-C6-Alkenyl-, Ci-Cβ-Alkoxycarbonyl- , Ci-C6-Alkylcarbonyl- oder eine Carbonylaminogruppe ist, wobei die Aminogruppe der Carbonylaminogruppe gegebenenfalls durch eine Ci-Cβ- Alkoxycarbonyl-, Ci-Cβ-Alkylcarbonyl- , C2-C6-Alkenyloxy- carbonyl-, C2-C6-Alkenylcarbonyl-, Ci-Cβ-Alkyl- , C2-CO- Alkenyl- und gegebenenfalls weiter durch eine Ci-Cö-Alkyl- oder eine C2-C6-Alkenylgruppe substituiert sein kann;R 11 is a hydrogen atom, a trifluoromethyl, C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl, C 1 -C 6 -alkoxycarbonyl, C 1 -C 6 -alkylcarbonyl or a carbonylamino group, where the amino group of the carbonylamino group is optionally carbonyl by a C Cβ- alkoxycarbonyl, Ci-Cβ-alkylcarbonyl, C 2 -C 6 alkenyloxy, C 2 -C 6 -Alkenylcarbonyl-, Ci-Cβ alkyl, C 2 -C O - alkenyl - And optionally further substituted by a Ci-C ö alkyl or a C 2 -C 6 alkenyl group may be substituted;
oder ein pharmakologisch akzeptables Salz, Solvat, Hydrat oder eine pharmakologisch akzeptable Formulierung derselben.or a pharmacologically acceptable salt, solvate, hydrate or pharmacologically acceptable formulation thereof.
Der Ausdruck Alkyl bezieht sich auf eine gesättigte, geradkettige oder verzweigte Kohlenwasserstoffgruppe, die 1 bis 20 Kohlenstoffatome, vorzugsweise 1 bis 12 Kohlenstoff- atome, besonders bevorzugt 1 bis 6 Kohlenstoffatome aufweist, z.B. die Methyl-, Ethyl-, Propyl-, Isopropyl-, n- Butyl-, Isobutyl-, tert-Butyl-, n-Pentyl-, n-Hexyl-, 2 , 2-Dimethylbutyl- oder n-Octyl-Gruppe.The term alkyl refers to a saturated, straight or branched hydrocarbon group having 1 to 20 carbon atoms, preferably 1 to 12 carbon atoms, more preferably 1 to 6 carbon atoms, e.g. the methyl, ethyl, propyl, isopropyl, n-butyl, isobutyl, tert-butyl, n-pentyl, n-hexyl, 2, 2-dimethylbutyl or n-octyl group.
Die Ausdrücke Alkenyl und Alkinyl beziehen sich auf zumindest teilweise ungesättigte, geradkettige oder verzweigte Kohlenwasserstoffgruppen, die 2 bis 20
Kohlenstoffatome, vorzugsweise 2 bis 12 Kohlenstoffatome, besonders bevorzugt 2 bis 6 Kohlenstoffatome aufweisen, z.B. die Ethenyl-, AlIyI-, Acetylenyl-, Propargyl-, Isoprenyl- oder Hex-2-enyl-Gruppe. Bevorzugt weisen Alkenylgruppen eine oder zwei (besonders bevorzugt eine) Doppelbindungen bzw. Alkinylgruppen eine oder zwei (besonders bevorzugt eine) Dreifachbindungen auf.The terms alkenyl and alkynyl refer to at least partially unsaturated, straight-chain or branched hydrocarbon groups containing 2 to 20 Carbon atoms, preferably 2 to 12 carbon atoms, more preferably 2 to 6 carbon atoms, eg the ethenyl, allyl, acetylenyl, propargyl, isoprenyl or hex-2-enyl group. Alkenyl groups preferably have one or two (particularly preferably one) double bonds or alkinyl groups one or two (particularly preferably one) triple bonds.
Des weiteren beziehen sich die Begriffe Alkyl, Alkenyl und Alkinyl auf Gruppen, bei denen ein oder mehrereFurthermore, the terms alkyl, alkenyl and alkynyl refer to groups in which one or more
Wasserstoffatome durch ein Halogenatom (bevorzugt F oder Cl) ersetzt sind wie z.B. die 2 , 2 , 2-Trichlorethyl- oder die Trifluormethylgruppe .Hydrogen atoms are replaced by a halogen atom (preferably F or Cl), e.g. the 2, 2, 2-trichloroethyl or the trifluoromethyl group.
Der Ausdruck Heteroalkyl bezieht sich auf eine Alkyl-, eine Alkenyl- oder eine Alkinyl-Gruppe, in der ein oder mehrere (bevorzugt 1, 2 oder 3) Kohlenstoffatome durch ein Sauerstoff-, Stickstoff-, Phosphor-, Bor-, Selen-, Siliziumoder Schwefelatom ersetzt sind (bevorzugt Sauerstoff, Schwefel oder Stickstoff) . Der Ausdruck Heteroalkyl bezieht sich des weiteren auf eine Carbonsäure oder eine von einer Carbonsäure abgeleiteten Gruppe wie z.B. Acyl, Acylalkyl, Alkoxycarbonyl , Acyloxy, Acyloxyalkyl , Carboxyalkylamid oder Alkoxycarbonyloxy.The term heteroalkyl refers to an alkyl, an alkenyl or an alkynyl group in which one or more (preferably 1, 2 or 3) carbon atoms are represented by an oxygen, nitrogen, phosphorus, boron, selenium, Silicon or sulfur atom are replaced (preferably oxygen, sulfur or nitrogen). The term heteroalkyl further refers to a carboxylic acid or a carboxylic acid derived group such as e.g. Acyl, acylalkyl, alkoxycarbonyl, acyloxy, acyloxyalkyl, carboxyalkylamide or alkoxycarbonyloxy.
Beispiele für Heteroalkylgruppen sind Gruppen der Formeln Ra-O-Ya-, Ra-S-Ya-, Ra-N(Rb) -Ya-, Ra-CO-Ya- , Ra-O-CO-Ya- , Ra-CO-O-Ya-, Ra-CO-N(Rb)-Ya-, Ra-N (Rb) -CO-Ya- , Ra-O-CO-N(Rb)-Ya-, Ra-N(Rb)-CO-O-Ya-, Ra-N (Rb) -CO-N (Rc) -Ya- , Ra-O-CO-O-Ya-, Ra-N(Rb)-C(=NRd)-N(Rc)-Ya-, Ra-CS-Ya-,Examples of heteroalkyl groups are groups of the formulas R a -OY a , R a -SY a , R a -N (R b ) -Y a , R a -CO-Y a , R a -O-CO- Y a -, R a -CO-OY a -, R a -CO-N (R b) -Y a -, R a -N (R b) -CO-Y a -, R a -O-CO- N (R b ) -Y a -, R a -N (R b ) -CO-OY a -, R a -N (R b ) -CO-N (R c ) -Y a -, R a -O -CO-OY a -, R a -N (R b ) -C (= NR d ) -N (R c ) -Y a -, R a -CS-Y a -,
Ra-O-CS-Ya-, Ra-CS-O-Ya-, Ra-CS-N(Rb)-Ya-, Ra-N (Rb) -CS-Ya- , Ra-O-CS-N(Rb)-Ya-, Ra-N(Rb)-CS-O-Ya-, Ra-N (Rb) -CS-N (Rc) -Ya- ,
Ra-O-CS-O-Ya-, Ra-S-CO-Ya-, Ra-CO-S-Ya-, Ra-S-CO-N (Rb) -Ya- , Ra-N(Rb)-CO-S-Ya-, Ra-S-CO-O-Ya-, Ra-O-CO-S-Ya- , Ra-S-CO-S-Ya-, Ra-S-CS-Ya-, Ra-CS-S-Ya-, Ra-S-CS-N (Rb) -Ya- , Ra-N(Rb)-CS-S-Ya-, Ra-S-CS-O-Ya-, Ra-O-CS-S-Ya- , wobei Ra ein Wasserstoffatom, eine Ci-Cβ-Alkyl-, eine C2-C6-Alkenyl- oder eine C2-C6-Alkinylgruppe; Rb ein Wasserstoffatom, eine C1-C6- Alkyl-, eine C2-C6-Alkenyl- oder eine C2-C6-Alkinylgruppe; Rc ein Wasserstoffatom, eine Ci-C6-Alkyl-, eine C2-C6-Alkenyl- oder eine C2-C6-Alkinylgruppe; Rd ein Wasserstoffatom, eine Ci-C6-Alkyl-, eine C2-C6-Alkenyl- oder eine C2-C6-R a is -O-CS-Y a -, R a is -CS-OY a -, R a is -CS-N (R b ) -Y a -, R a is -N (R b ) -CS-Y a -, R a -O-CS-N (R b ) -Y a -, R a -N (R b ) -CS-OY a -, R a -N (R b ) -CS-N (R c ) -Y a , R a -O-CS-OY a -, R a -S-CO-Y a -, R a -CO-SY a -, R a -S-CO-N (R b ) -Y a -, R a -N (R b ) -CO-SY a -, R a -S-CO-OY a -, R a -O-CO-SY a -, R a -S-CO-SY a -, R a -S -CS-Y a -, R a -CS-SY a -, R a -S-CS-N (R b ) -Y a -, R a -N (R b ) -CS-SY a -, R a -S-CS-OY a -, R a -O-CS-SY a -, wherein R a is a hydrogen atom, a Ci-Cβ-alkyl, a C 2 -C 6 alkenyl or a C 2 -C 6 -alkynyl; R b represents a hydrogen atom, a C 1 -C 6 - alkyl, C2-C6 alkenyl or a C 2 -C 6 alkynyl group; R c is a hydrogen atom, a Ci-C 6 alkyl, a C 2 -C 6 alkenyl or a C 2 -C 6 alkynyl group; R d is a hydrogen atom, a Ci-C 6 alkyl, a C 2 -C 6 alkenyl or a C 2 -C 6 -
Alkinylgruppe und Ya eine direkte Bindung, eine Ci-C6- Alkylen-, eine C2-C6-Alkenylen- oder eine C2-C6- Alkinylengruppe ist, wobei jede Heteroalkylgruppe mindestens ein Kohlenstoffatom enthält und ein oder mehrere Wasserstoffatome durch Fluor- oder Chloratome ersetzt sein können. Konkrete Beispiele für Heteroalkylgruppen sind Methoxy, Trifluormethoxy, Ethoxy, n-Propyloxy, iso- Propyloxy, tert-Butyloxy, Methoxymethyl , Ethoxymethyl , -CH2CH2OH, -CH2OH, Methoxyethyl , Methylamine Ethylamino, Dimethylamino, Diethylamino, iso-Propylethylamino, Methylaminomethyl , Ethylaminomethyl , Di-iso- Propylaminoethyl , Enolether, Dimethylaminomethyl , Dimethylaminoethyl , Acetyl , Propionyl, Butyryloxy, Acetyloxy, Methoxycarbonyl , Ethoxycarbonyl , N-Ethyl-N- Methylcarbamoyl oder N-Methylcarbamoyl . Weitere Beispiele für Heteroalkylgruppen sind Nitril-, Isonitril-, Cyanat-, Thiocyanat-, Isocyanat-, Isothiocyanat- und Alkylnitril- Gruppen. Ein Beispiel für eine Heteroalkylengruppe ist eine Gruppe der Formel -CH2CH(OH)-.Alkynyl group and Y a is a direct bond, a Ci-C 6 - alkylene, a C 2 -C 6 alkenylene or a C 2 -C 6 - alkynylene, wherein each heteroalkyl group at least one carbon atom and one or more hydrogen atoms are replaced by Fluorine or chlorine atoms may be replaced. Specific examples of heteroalkyl groups are methoxy, trifluoromethoxy, ethoxy, n-propyloxy, isopropyloxy, tert-butyloxy, methoxymethyl, ethoxymethyl, -CH 2 CH 2 OH, -CH 2 OH, methoxyethyl, methylamines, ethylamino, dimethylamino, diethylamino, iso- Propylethylamino, methylaminomethyl, ethylaminomethyl, di-iso-propylaminoethyl, enol ether, dimethylaminomethyl, dimethylaminoethyl, acetyl, propionyl, butyryloxy, acetyloxy, methoxycarbonyl, ethoxycarbonyl, N-ethyl-N-methylcarbamoyl or N-methylcarbamoyl. Further examples of heteroalkyl groups are nitrile, isonitrile, cyanate, thiocyanate, isocyanate, isothiocyanate and alkylnitrile groups. An example of a heteroalkylene group is a group of the formula -CH 2 CH (OH) -.
Der Ausdruck Cycloalkyl bezieht sich auf eine gesättigte oder teilweise ungesättigte (z.B. Cycloalkenyl) cyclische
Gruppe, die einen oder mehrere Ringe (bevorzugt 1 oder 2) aufweist und 3 bis 14 Ringkohlenstoffatome, vorzugsweise 3 bis 10 (insbesondere 3, 4, 5, 6 oder 7) Ringkohlenstoff- atome enthält. Der Ausdruck Cycloalkyl bezieht sich weiterhin auf Gruppen, bei denen ein oder mehrere Wasserstoffatome durch Fluor-, Chlor-, Brom- oder Jodatome oder OH, =0, SH, =S, NH2, =NH oder NO2-Gruppen ersetzt sind, also z.B. cyclische Ketone wie z.B. Cyclohexanon, 2-Cyclohexenon oder Cyclopentanon. Weitere konkrete Beispiele für Cycloalkylgruppen sind die Cyclopropyl- , Cyclobutyl-,The term cycloalkyl refers to a saturated or partially unsaturated (eg cycloalkenyl) cyclic Group which has one or more rings (preferably 1 or 2) and contains 3 to 14 ring carbon atoms, preferably 3 to 10 (in particular 3, 4, 5, 6 or 7) ring carbon atoms. The term cycloalkyl furthermore refers to groups in which one or more hydrogen atoms have been replaced by fluorine, chlorine, bromine or iodine atoms or OH, 0O, SH, SS, NH 2 , NHNH or NO 2 groups, For example, cyclic ketones such as cyclohexanone, 2-cyclohexenone or cyclopentanone. Further concrete examples of cycloalkyl groups are the cyclopropyl, cyclobutyl,
Cyclopentyl-, Spiro [4, 5]decanyl-, Norbornyl-, Cyclohexyl-, Cyclopentenyl-, Cyclohexadienyl- , Decalinyl-, Bicyclo [4.3.0] nonyl- , Tetralin-, Cyclopentylcyclohexyl-, Fluorcyclohexyl- oder die Cyclohex-2-enyl-Gruppe.Cyclopentyl, spiro [4,5] decanyl, norbornyl, cyclohexyl, cyclopentenyl, cyclohexadienyl, decalinyl, bicyclo [4.3.0] nonyl, tetralin-, cyclopentylcyclohexyl, fluorocyclohexyl or cyclohex-2- enyl group.
Der Ausdruck Heterocycloalkyl bezieht sich auf eine Cycloalkylgruppe wie oben definiert, in der ein oder mehrere (bevorzugt 1, 2 oder 3) Ringkohlenstoffatome durch ein Sauerstoff-, Stickstoff-, Silizium-, Selen-, Phosphor- oder Schwefelatom (bevorzugt Sauerstoff, Schwefel oder Stickstoff) ersetzt sind. Bevorzugt besitzt eine Heterocycloalkylgruppe 1 oder 2 Ringe mit 3 bis 10 (insbesondere 3, 4, 5, 6 oder 7) Ringatomen. Der Ausdruck Heterocycloalkyl bezieht sich weiterhin auf Gruppen, bei denen ein oder mehrere Wasserstoffatome durch Fluor-,The term heterocycloalkyl refers to a cycloalkyl group as defined above in which one or more (preferably 1, 2 or 3) ring carbon atoms are represented by an oxygen, nitrogen, silicon, selenium, phosphorus or sulfur atom (preferably oxygen, sulfur or sulfur) Nitrogen) are replaced. A heterocycloalkyl group preferably has 1 or 2 rings with 3 to 10 (in particular 3, 4, 5, 6 or 7) ring atoms. The term heterocycloalkyl furthermore refers to groups in which one or more hydrogen atoms are replaced by fluorine,
Chlor-, Brom- oder Jodatome oder OH, =0, SH, =S, NH2, =NH oder NO2-Gruppen ersetzt sind. Beispiele sind die Piperidyl-, Piperazinyl- , Morpholinyl- , Urotropinyl- , Pyrrolidinyl- , Tetrahydrothiophenyl- , Tetrahydropyranyl- , Tetrahydrofuryl- oder 2-Pyrazolinyl-Gruppe sowie Lactame, Lactone, cyclische Imide und cyclische Anhydride.
Der Ausdruck Alkylcycloalkyl bezieht sich auf Gruppen, die entsprechend den obigen Definitionen sowohl Cycloalkyl- wie auch Alkyl-, Alkenyl- oder Alkinylgruppen enthalten, z.B. Alkylcycloalkyl-, Cycloalkylalkyl- , Alkylcycloalkenyl-, Alkenylcycloalkyl- und Alkinylcycloalkylgruppen. Bevorzugt enthält eine Alkylcycloalkylgruppe eine Cycloalkylgruppe, die ein oder zwei Ringe aufweist und 3 bis 10 (insbesondere 3, 4, 5, 6 oder 7) Ringkohlenstoffatome enthält und eine oder zwei Alkyl-, Alkenyl- oder Alkinylgruppen mit 1 oder 2 bis 6 Kohlenstoffatomen.Chlorine, bromine or iodine atoms or OH, = 0, SH, = S, NH 2 , = NH or NO 2 groups are replaced. Examples are the piperidyl, piperazinyl, morpholinyl, urotropinyl, pyrrolidinyl, tetrahydrothiophenyl, tetrahydropyranyl, tetrahydrofuryl or 2-pyrazolinyl group as well as lactams, lactones, cyclic imides and cyclic anhydrides. The term alkylcycloalkyl refers to groups containing both cycloalkyl and alkyl, alkenyl or alkynyl groups according to the above definitions, for example alkylcycloalkyl, cycloalkylalkyl, alkylcycloalkenyl, alkenylcycloalkyl and alkynylcycloalkyl groups. Preferably, an alkylcycloalkyl group contains a cycloalkyl group having one or two rings and containing 3 to 10 (especially 3, 4, 5, 6 or 7) ring carbon atoms and one or two alkyl, alkenyl or alkynyl groups having 1 or 2 to 6 carbon atoms.
Der Ausdruck Heteroalkylcycloalkyl bezieht sich auf Alkyl- cycloalkylgruppen, wie oben definiert, in der ein oder mehrere (bevorzugt 1, 2 oder 3) Kohlenstoffatome durch ein Sauerstoff-, Stickstoff-, Silizium-, Selen-, Phosphor- oder Schwefelatom (bevorzugt Sauerstoff, Schwefel oder Stickstoff) ersetzt sind. Bevorzugt besitzt eine Heteroalkyl- cycloalkylgruppe 1 oder 2 Ringe mit 3 bis 10 (insbesondere 3, 4, 5, 6 oder 7) Ringatomen und eine oder zwei Alkyl-, Alkenyl-, Alkinyl- oder Heteroalkylgruppen mit 1 oder 2 bis 6 Kohlenstoffatomen. Beispiele derartiger Gruppen sind Al- kylheterocycloalkyl, Alkylheterocycloalkenyl , Alkenyl- heterocycloalkyl , Alkinylheterocycloalkyl , Heteroalkylcycloalkyl, Heteroalkylheterocycloalkyl und Heteroalkyl- heterocylcloalkenyl , wobei die cyclischen Gruppen gesättigt oder einfach, zweifach oder dreifach ungesättigt sind.The term heteroalkylcycloalkyl refers to alkylcycloalkyl groups as defined above in which one or more (preferably 1, 2 or 3) carbon atoms are represented by an oxygen, nitrogen, silicon, selenium, phosphorus or sulfur atom (preferably oxygen, Sulfur or nitrogen) are replaced. A heteroalkylcycloalkyl group preferably has 1 or 2 rings having 3 to 10 (in particular 3, 4, 5, 6 or 7) ring atoms and one or two alkyl, alkenyl, alkynyl or heteroalkyl groups having 1 or 2 to 6 carbon atoms. Examples of such groups are alkylheterocycloalkyl, alkylheterocycloalkenyl, alkenyl-heterocycloalkyl, alkynylheterocycloalkyl, heteroalkylcycloalkyl, heteroalkylheterocycloalkyl and heteroalkyl-heterocyclic-alkenyl, where the cyclic groups are saturated or mono-, di- or tri-unsaturated.
Der Ausdruck Aryl bzw. Ar bezieht sich auf eine aromatische Gruppe, die einen oder mehrere Ringe aufweist und 6 bis 14 Ringkohlenstoffatome, vorzugsweise 6 bis 10 (insbesondere 6) Ringkohlenstoffatome enthält. Der Ausdruck Aryl (bzw. Ar) bezieht sich weiterhin auf Gruppen, bei denen ein oder
mehrere Wasserstoffatome durch Fluor-, Chlor-, Brom- oder Jodatome oder OH, SH, NH2, oder NO2-Gruppen ersetzt sind. Beispiele sind die Phenyl-, Naphthyl-, Biphenyl-, 2-Fluor- phenyl-, Anilinyl-, 3-Nitrophenyl oder 4-Hydroxyphenyl- Gruppe .The term aryl or Ar refers to an aromatic group having one or more rings and containing 6 to 14 ring carbon atoms, preferably 6 to 10 (especially 6) ring carbon atoms. The term aryl (or Ar) further refers to groups in which one or several hydrogen atoms are replaced by fluorine, chlorine, bromine or iodine atoms or OH, SH, NH 2 , or NO 2 groups. Examples are the phenyl, naphthyl, biphenyl, 2-fluorophenyl, anilinyl, 3-nitrophenyl or 4-hydroxyphenyl group.
Der Ausdruck Heteroaryl bezieht sich auf eine aromatische Gruppe, die einen oder mehrere Ringe aufweist und 5 bis 14 Ringatome, vorzugsweise 5 bis 10 (insbesondere 5 oder 6) Ringatome enthält und ein oder mehrere (bevorzugt 1, 2, 3 oder 4) Sauerstoff-, Stickstoff-, Phosphor- oder Schwefel- Ringatome (bevorzugt O, S oder N) enthält. Der Ausdruck Heteroaryl bezieht sich weiterhin auf Gruppen, bei denen ein oder mehrere Wasserstoffatome durch Fluor-, Chlor-, Brom- oder Jodatome oder OH, SH, NH2, oder NO2-Gruppen ersetzt sind. Beispiele sind 4-Pyridyl-, 2-Imidazolyl-, 3- Phenylpyrrolyl- , Thiazolyl-, Oxazolyl-, Triazolyl-, Tetrazolyl-, Isoxazolyl-, Indazolyl-, Indolyl-, Benz- imidazolyl-, Pyridazinyl- , Chinolinyl-, Purinyl-, Carbazolyl-, Acridinyl-, Pyrimidyl-, 2 , 3 '-Bifuryl- , 3-Pyrazolyl- und Isochinolinyl-Gruppen.The term heteroaryl refers to an aromatic group which has one or more rings and contains 5 to 14 ring atoms, preferably 5 to 10 (in particular 5 or 6) ring atoms and one or more (preferably 1, 2, 3 or 4) oxygen atoms. , Nitrogen, phosphorus or sulfur ring atoms (preferably O, S or N). The term heteroaryl furthermore refers to groups in which one or more hydrogen atoms have been replaced by fluorine, chlorine, bromine or iodine atoms or OH, SH, NH 2 or NO 2 groups. Examples are 4-pyridyl, 2-imidazolyl, 3-phenylpyrrolyl, thiazolyl, oxazolyl, triazolyl, tetrazolyl, isoxazolyl, indazolyl, indolyl, benzimidazolyl, pyridazinyl, quinolinyl, purinyl , Carbazolyl, acridinyl, pyrimidyl, 2,3'-bifuryl, 3-pyrazolyl and isoquinolinyl groups.
Der Ausdruck Aralkyl bezieht sich auf Gruppen, die entsprechend den obigen Definitionen sowohl Aryl- wie auch Alkyl-, Alkenyl-, Alkinyl- und/oder Cycloalkylgruppen enthalten, wie z.B. Arylalkyl-, Arylalkenyl-, Arylalkinyl- , Arylcycloalkyl-, Arylcycloalkenyl- , Alkylarylcycloalkyl- und Alkylarylcycloalkenylgruppen. Konkrete Beispiele für Aralkyle sind Toluol, Xylol, Mesitylen, Styrol, Benzyl- chlorid, o-Fluortoluol, 1H-Inden, Tetralin, Dihydro- naphthalin, Indanon, Phenylcyclopentyl , Cumol, Cyclohexyl- phenyl, Fluoren und Indan. Bevorzugt enthält eine Aralkyl-
gruppe ein oder zwei aromatische Ringsysteme (1 oder 2 Ringe) mit 6 bis 10 Kohlenstoffatomen und ein oder zwei Alkyl-, Alkenyl- und/oder Alkinylgruppen mit 1 oder 2 bis 6 Kohlenstoffatomen und/oder eine Cycloalkylgruppe mit 5 oder 6 Ringkohlenstoffatomen.The term aralkyl refers to groups containing both aryl and alkyl, alkenyl, alkynyl and / or cycloalkyl groups according to the above definitions, such as arylalkyl, arylalkenyl, arylalkynyl, arylcycloalkyl, arylcycloalkenyl, alkylarylcycloalkyl and alkylarylcycloalkenyl groups. Concrete examples of aralkyls are toluene, xylene, mesitylene, styrene, benzyl chloride, o-fluorotoluene, 1H-indene, tetralin, dihydronaphthalene, indanone, phenylcyclopentyl, cumene, cyclohexylphenyl, fluorene and indane. Preferably, an aralkyl group one or two aromatic ring systems (1 or 2 rings) having 6 to 10 carbon atoms and one or two alkyl, alkenyl and / or alkynyl groups having 1 or 2 to 6 carbon atoms and / or a cycloalkyl group having 5 or 6 ring carbon atoms.
Der Ausdruck Heteroaralkyl bezieht sich auf eine Aralkyl- gruppe wie oben definiert, in der ein oder mehrere (bevorzugt 1, 2, 3 oder 4) Kohlenstoffatome durch ein Sauerstoff-, Stickstoff-, Silizium-, Selen-, Phosphor-,The term heteroaralkyl refers to an aralkyl group as defined above in which one or more (preferably 1, 2, 3 or 4) carbon atoms are represented by an oxygen, nitrogen, silicon, selenium, phosphorus,
Bor- oder Schwefelatom (bevorzugt Sauerstoff, Schwefel oder Stickstoff) ersetzt sind, d. h. auf Gruppen, die entsprechend den obigen Definitionen sowohl Aryl- bzw. Heteroaryl- wie auch Alkyl-, Alkenyl-, Alkinyl- und/oder Heteroalkyl- und/oder Cycloalkyl- und/oder Heterocyclo- alkylgruppen enthalten. Bevorzugt enthält eine Hetero- aralkylgruppe ein oder zwei aromatische Ringsysteme (1 oder 2 Ringe) mit 5 oder 6 bis 10 Kohlenstoffatomen und ein oder zwei Alkyl-, Alkenyl- und/oder Alkinylgruppen mit 1 oder 2 bis 6 Kohlenstoffatomen und/oder eine Cycloalkylgruppe mit 5 oder 6 Ringkohlenstoffatomen, wobei 1, 2, 3 oder 4 dieser Kohlenstoffatome durch Sauerstoff-, Schwefel- oder Stickstoffatome ersetzt sind.Boron or sulfur atom (preferably oxygen, sulfur or nitrogen) are replaced, d. H. to groups which according to the above definitions contain both aryl or heteroaryl and also alkyl, alkenyl, alkynyl and / or heteroalkyl and / or cycloalkyl and / or heterocycloalkyl groups. Preferably, a heteroaralkyl group contains one or two aromatic ring systems (1 or 2 rings) having 5 or 6 to 10 carbon atoms and one or two alkyl, alkenyl and / or alkynyl groups having 1 or 2 to 6 carbon atoms and / or a cycloalkyl group 5 or 6 ring carbon atoms, wherein 1, 2, 3 or 4 of these carbon atoms are replaced by oxygen, sulfur or nitrogen atoms.
Beispiele sind Arylheteroalkyl-, Arylheterocycloalkyl-,Examples are arylheteroalkyl, arylheterocycloalkyl,
Arylheterocycloalkenyl-, Arylalkylheterocycloalkyl-, Aryl- alkenylheterocycloalkyl- , Arylalkinylheterocycloalkyl- , Arylalkylheterocycloalkenyl-, Heteroarylalkyl- , Heteroaryl- alkenyl-, Heteroarylalkinyl-, Heteroarylheteroalkyl- , Heteroarylcycloalkyl-, Heteroarylcycloalkenyl- , Heteroaryl- heterocycloalkyl-, Heteroarylheterocycloalkenyl-, Hetero- arylalkylcycloalkyl- , Heteroarylalkylheterocycloalkenyl- ,
Heteroarylheteroalkylcycloalkyl- , Heteroarylheteroalkyl- cycloalkenyl- und Heteroarylheteroalkylheterocycloalkyl- Gruppen, wobei die cyclischen Gruppen gesättigt oder einfach, zweifach oder dreifach ungesättigt sind. Konkrete Beispiele sind die Tetrahydroisochinolinyl- , Benzoyl-, 2- oder 3-Ethylindolyl-, 4-Methylpyridino-, 2-, 3- oder 4-Methoxyphenyl-, 4-Ethoxyphenyl-, 2-, 3- oder 4-Carboxy- phenylalkylgruppe .Arylheterocycloalkenyl-, Arylalkylheterocycloalkyl-, aryl alkenylheterocycloalkyl-, alkenyl, heterocycloalkyl Arylalkinylheterocycloalkyl-, Arylalkylheterocycloalkenyl-, heteroarylalkyl, heteroaryl heteroarylalkynyl- Heteroarylheteroalkyl-, Heteroarylcycloalkyl-, Heteroarylcycloalkenyl-, heteroaryl, Heteroarylheterocycloalkenyl-, arylalkylcycloalkyl- hetero-, Heteroarylalkylheterocycloalkenyl, Heteroarylheteroalkylcycloalkyl, Heteroarylheteroalkyl- cycloalkenyl and Heteroarylheteroalkylheterocycloalkyl- groups, wherein the cyclic groups are saturated or mono-, di- or triunsaturated. Concrete examples are the tetrahydroisoquinolinyl, benzoyl, 2- or 3-ethyl-indolyl, 4-methylpyridino, 2-, 3- or 4-methoxyphenyl, 4-ethoxyphenyl, 2-, 3- or 4-carboxyphenylalkyl group ,
Die Ausdrücke Cycloalkyl, Heterocycloalkyl, Alkylcyclo- alkyl, Heteroalkylcycloalkyl , Aryl, Heteroaryl , Aralkyl und Heteroaralkyl beziehen sich auch auf Gruppen, in denen ein oder mehrere Wasserstoffatome solcher Gruppen durch Fluor-, Chlor-, Brom- oder Jodatome oder OH, =0, SH, =S, NH2, =NH oder NO2-Gruppen ersetzt sind.The terms cycloalkyl, heterocycloalkyl, alkylcycloalkyl, heteroalkylcycloalkyl, aryl, heteroaryl, aralkyl and heteroaralkyl also refer to groups in which one or more hydrogen atoms of such groups are represented by fluorine, chlorine, bromine or iodine atoms or OH, = 0, SH, = S, NH 2 , = NH or NO 2 groups are replaced.
Der Ausdruck "gegebenenfalls substituiert" bezieht sich auf Gruppen, in denen ein oder mehrere Wasserstoffatome durch Fluor-, Chlor-, Brom- oder Jodatome oder OH, =0, SH, =S, NH2, =NH oder Nθ2-Gruppen ersetzt sind. Dieser Ausdruck bezieht sich weiterhin auf Gruppen, die mit unsubsti- tuierten Ci-C6-Alkyl- , C2-C6-Alkenyl- , C2-C6-Alkinyl- , Ci-C6- Heteroalkyl-, C3-Ci0-Cycloalkyl-, C2-C9-Heterocycloalkyl-, Ce-Cio-Aryl-, Ci-C9-Heteroaryl- , C7-Ci2-Aralkyl- oder C2-Cn- Heteroaralkyl-Gruppen substituiert sind.The term "optionally substituted" refers to groups in which one or more hydrogen atoms are replaced by fluorine, chlorine, bromine or iodine atoms or OH, = O, SH, = S, NH 2 , = NH or NO 2 groups are. This expression further refers to groups-substituted with unsubsti- Ci-C 6 alkyl, C 2 -C 6 alkenyl, C 2 -C 6 alkynyl, Ci-C6 - heteroalkyl, C 3 - are heteroaralkyl groups substituted - Ci 0 cycloalkyl, C 2 -C 9 heterocycloalkyl, Ce-Cio-aryl, Ci-C9 heteroaryl, C7-Ci2 aralkyl or C 2 -C n ,
Bevorzugt sind Verbindungen der Formel (I), wobei A aus folgenden Gruppen ausgewählt ist: -CH(OH)CH2-, -CH2CH(OH)-, -OCH2CH2-, -CH2CH2O-, -CH2SO2-, -SO2CH2-, -CH2N (d-C4-Alkyl) - , -N(Ci-C4-AIkYl) CH2-, -CH2NH-, -NHCH2-, -CH2O-, -OCH2-, -CH2S-,Preference is given to compounds of the formula (I) in which A is selected from the following groups: -CH (OH) CH 2 -, -CH 2 CH (OH) -, -OCH 2 CH 2 -, -CH 2 CH 2 O-, -CH 2 SO 2 -, -SO 2 CH 2 -, -CH 2 N (C 1 -C 4 -alkyl) -, -N (C 1 -C 4 -alkyl) CH 2 -, -CH 2 NH-, -NHCH 2 - , -CH 2 O-, -OCH 2 -, -CH 2 S-,
-SCH2-, -N(Ci-C4-Alkyl)C(=O)-, -C (=0) N (C1-C4-AIkYl )-, -NHC (=0)-, -Ct=O)NH- oder -CH2CH2-.
Besonders bevorzugt sind Verbindungen der Formel (I), wobei A eine Gruppe der Formel -CH(OH)CH2- oder -OCH2CH2- ist.-SCH 2 -, -N (C 1 -C 4 -alkyl) C (= O) -, -C (= O) N (C 1 -C 4 -alkyl) -, -NHC (= O) -, -Ct = O) NH- or -CH 2 CH 2 -. Particular preference is given to compounds of the formula (I) in which A is a group of the formula -CH (OH) CH 2 - or -OCH 2 CH 2 -.
Wiederum bevorzugt ist R1 eine Cyano-, eine Ci-C4-Alkyloxy- oder eine Ci-C4-Heteroalkyloxygruppe, wobei ein oder mehrere Wasserstoffatome dieser Gruppen durch Fluoratome ersetzt sein können.Again preferably R 1 is a cyano, a C 1 -C 4 -alkyloxy or a C 1 -C 4 -Heteroalkyloxygruppe, wherein one or more hydrogen atoms of these groups may be replaced by fluorine atoms.
Besonders bevorzugt ist R1 eine Methoxygruppe .More preferably, R 1 is a methoxy group.
Weiter bevorzugt ist R2 ein Wasserstoff- oder ein H Haallooggeennaattoomm.. BBeessoonnddeerrss bbeevvoorrzzυugt ist R2 ein Wasserstoff-, ein Chlor- oder ein Fluoratom.More preferably, R 2 is a hydrogen or H halo logging ratio. For the sake of convenience, R 2 is a hydrogen, a chlorine or a fluorine atom.
Wiederum bevorzugt ist R3 aus folgenden Gruppen ausgewähltAgain preferably, R 3 is selected from the following groups
Besonders bevorzugt ist R3 aus folgenden Gruppen ausgewählt :R 3 is particularly preferably selected from the following groups:
Wiederum bevorzugt sind die Reste R4 unabhängig voneinander ein Halogenatom, eine Hydroxy-, eine Cyano-, eine Ci-C4- Alkyl- oder eine Ci-C4-Heteroalkylgruppe (z.B. eine Hydroxymethylgruppe) . The radicals R 4 are preferably in turn independently of one another a halogen atom, a hydroxy, a cyano, a Ci-C 4 - alkyl or a Ci-C4 heteroalkyl group (for example, a hydroxymethyl group).
Besonders bevorzugt sind die Reste R4 unabhängig voneinander ein Fluor- oder Chloratom oder eine Ci-C4- Heteroalkylgruppe (z.B. eine Hydroxymethylgruppe).The radicals R 4 are particularly preferably independently of one another a fluorine or chlorine atom or a C 1 -C 4 -heteroalkyl group (for example a hydroxymethyl group).
Bevorzugt ist n gleich 0 oder 1; besonders bevorzugt 0.Preferably, n is 0 or 1; more preferably 0.
Weiter bevorzugt ist R5 eine Heteroalkylcycloalkyl- oder eine Heteroaralkylgruppe .More preferably, R 5 is a heteroalkylcycloalkyl or heteroaralkyl group.
Besonders bevorzugt ist R5 eine Gruppe der Formel -B-Y, wobei B eine Bindung, eine Alkylen- (insbesondere eine Ci- C4-Alkylengruppe) , eine Alkenylen-, eine Alkinylen-, eine -NH-, -NHSO2-, -SO2-, -C(=O)-, eine Heteroalkylen- (insbesondere eine Ci-C4-Heteroalkylengruppe) oder eineR 5 is particularly preferably a group of the formula -BY, where B is a bond, an alkylene (in particular a C 1 -C 4 -alkylene group), an alkenylene, an alkynylene, a -NH-, -NHSO 2 , - SO 2 -, -C (= O) -, a heteroalkylene (especially a Ci-C 4 -Heteroalkylengruppe) or a
Heterocycloalkylengruppe ist und Y eine Aryl-, Heteroaryl-, Aralkyl-, Heteroaralkyl- , Cycloalkyl-, Heterocycloalkyl- , Alkylcycloalkyl- , Heteroalkylcycloalkyl-, Heteroarylhetero- cycloalkyl- oder eine Arylheterocycloalkylgruppe (ins- besondere eine Heterocycloalkyl-, eine Heteroaryl-,Heterocyclicalkylene group and Y is an aryl, heteroaryl, aralkyl, heteroaralkyl, cycloalkyl, heterocycloalkyl, alkylcycloalkyl, heteroalkylcycloalkyl, heteroarylheterocycloalkyl or an arylheterocycloalkyl group (in particular a heterocycloalkyl, a heteroaryl,
Aralkyl-, Heteroaralkyl-, eine Heteroarylheterocycloalkyl- oder eine Arylheterocycloalkylgruppe) ist.Aralkyl, heteroaralkyl, heteroarylheterocycloalkyl or arylheterocycloalkyl group).
Bevorzugt ist B eine Bindung oder eine Gruppe der Formel -NH-, -NHCH2-, -CH2NH-, -NHCH2CH2-, -CH2CH2NH-, -NHCH2CH2CH2-, -CH2CH2CH2NH-, -CH2-, -CH2CH2-, -CH2CH2CH2-, -NHC (=0)-, -C(=O)NH-, -CH(OH)-, -CH2CH(OH)-, -CH(OH)CH2-, -NHSO2-,
-SO2NH-, -SO2-, -C(=S)NH-, -NHC (=S)-, -C(=NOH)-, -CH2C (=NOH)-, -C(=NOH)CH2-, -C(=0)-, -C (=0) -C (=0) - , -CH2C (=0)-, -C (=0) CH2-, -N(C1-C4-AIkYl)CH2-, -CH2N(Ci-C4- Alkyl)- oder eine Piperazingruppe.B is preferably a bond or a group of the formula -NH-, -NHCH 2 -, -CH 2 NH-, -NHCH 2 CH 2 -, -CH 2 CH 2 NH-, -NHCH 2 CH 2 CH 2 -, - CH 2 CH 2 CH 2 NH-, -CH 2 -, -CH 2 CH 2 -, -CH 2 CH 2 CH 2 -, -NHC (= O) -, -C (= O) NH-, -CH ( OH) -, -CH 2 CH (OH) -, -CH (OH) CH 2 -, -NHSO 2 -, -SO 2 NH-, -SO 2 -, -C (= S) NH-, -NHC (= S) -, -C (= NOH) -, -CH 2 C (= NOH) -, -C (= NOH) CH 2 -, -C (= O) -, -C (= O) -C (= O) -, -CH 2 C (= O) -, -C (= O) CH 2 -, -N (C 1 -C 4 -alkyl) CH 2 -, -CH 2 N (Ci-C 4 - alkyl) -, or a piperazine group.
Besonders bevorzugt ist B eine Bindung oder eine Gruppe der Formel -NHCH2-, -CH2NH-, -CH2-, -CH2CH2-, -CH2CH2CH2-, -NHC (=0)-, -C(=O)NH-, -CH2CH(OH)-, -CH(OH)CH2-, -NHSO2-, -SO2NH-, -SO2-, -C(=0)- oder eine Piperazingruppe.B is particularly preferably a bond or a group of the formula -NHCH 2 -, -CH 2 NH-, -CH 2 -, -CH 2 CH 2 -, -CH 2 CH 2 CH 2 -, -NHC (= O) - , -C (= O) NH-, -CH 2 CH (OH) -, -CH (OH) CH 2 -, -NHSO 2 -, -SO 2 NH-, -SO 2 -, -C (= 0) - or a piperazine group.
Bevorzugt ist Y ein bicyclisches System, wobei die beiden Ringe unabhängig voneinander ein Cycloalkyl-, ein Hetero- cycloalkyl-, ein Aryl- (insbesondere ein Phenylring) oder ein Heteroaryl-Ring sind und jeweils 3 bis 8 Ringatome (bevorzugt 5, 6 oder 7 Ringatome) aufweisen (insbesondere bevorzugt weist der Heteroarylring 5 oder 6 Ringatome auf) und das System gegebenenfalls substituiert sein kann (z.B. durch F, =0, Methyl, Trifluormethyl , Methoxy, -C(=O)OH, Cyclopropyl) .Y is preferably a bicyclic system, where the two rings independently of one another are a cycloalkyl, a heterocycloalkyl, an aryl (in particular a phenyl ring) or a heteroaryl ring and in each case 3 to 8 ring atoms (preferably 5, 6 or 7 Ring atoms) (particularly preferably the heteroaryl ring has 5 or 6 ring atoms) and the system may optionally be substituted (eg by F, = 0, methyl, trifluoromethyl, methoxy, -C (= O) OH, cyclopropyl).
Wiederum bevorzugt ist Y eine Gruppe der Formel -Y1-Y2, wobei Y1 eine Bindung, eine Alkylen- (insbesondere eine Ci-C4-Alkylengruppe) , eine Alkenylen- (insbesondere eine Ci-C4-Alkenylengruppe) , eine Alkinylen-, eine -NH-, eine -S-, eine -0-, eine -NHC (=0)-, eine -C(=O)NH- oder eineY is again preferably a group of the formula -Y 1 -Y 2 , where Y 1 is a bond, an alkylene (in particular a C 1 -C 4 -alkylene group), an alkenylene (in particular a C 1 -C 4 -alkenylene group), a Alkynylene, one -NH-, one -S-, one -O-, one -NHC (= O) -, one -C (= O) NH- or one
Heteroalkylengruppe (insbesondere eine Ci-C4-Heteroalkylen- gruppe) ist und Y2 eine Aryl-, Heteroaryl-, Aralkyl-, Heteroaralkyl-, Cycloalkyl-, Heterocycloalkyl- , Alkyl- cycloalkyl-, Heteroalkylcycloalkyl-, Heteroarylhetero- cycloalkyl- oder eine Arylheterocycloalkylgruppe (insbesondere eine Heterocycloalkyl-, eine Aryl-, eine Heteroaryl-, Aralkyl-, Heteroaralkyl-, eine Heteroaryl-
heterocycloalkyl- oder eine Arylheterocycloalkylgruppe) ist. Besonders bevorzugt ist Y1 eine Bindung oder eine Gruppe der Formel -CH=CH-, -CH2CH2-, -S-, -CH2O-, -C(=O)NH-, -NH- oder -CH2C (=0)- und Y2 eine gegebenenfalls substituierte Phenylgruppe oder Heteroarylgruppe mit 5 oder 6 Ringatomen.Heteroalkylene group (in particular a C 1 -C 4 -Heteroalkylen- group) and Y 2 is an aryl, heteroaryl, aralkyl, heteroaralkyl, cycloalkyl, heterocycloalkyl, alkylcycloalkyl, Heteroalkylcycloalkyl-, Heteroarylhetero- cycloalkyl or a Arylheterocycloalkyl group (in particular a heterocycloalkyl, an aryl, a heteroaryl, aralkyl, heteroaralkyl, a heteroaryl) heterocycloalkyl or an arylheterocycloalkyl group). Y 1 is particularly preferably a bond or a group of the formula -CH = CH-, -CH 2 CH 2 -, -S-, -CH 2 O-, -C (= O) NH-, -NH- or -CH 2 C (= 0) - and Y 2 is an optionally substituted phenyl group or heteroaryl group having 5 or 6 ring atoms.
Insbesondere bevorzugt weist Y eine der folgenden Strukturen auf :Most preferably, Y has one of the following structures:
wobei X1, X2 und X3 unabhängig voneinander Stickstoffatome oder Gruppen der Formel CR20 sind, X4 und X5 unabhängig voneinander Sauerstoff- oder Schwefelatome oder Gruppen der Formel NR21 sind, o gleich 0, 1 oder 2 ist, R14, R15, R16, R17, R19 und R20 unabhängig voneinander Wasserstoffatome, Halogenatome, Hydroxy- , Ci-Cβ-Alkyl-, C2-C6-Alkenyl-, C2-C6- Alkinyl- oder Ci-Cβ-Heteroalkylgruppen sind und R18 und R21 unabhängig voneinander Wasserstoffatome, Ci-C6-Alkyl- , C2-C6-Alkenyl-, C2-C6-Alkinyl- oder Ci-C6-Heteroalkylgruppen sind.wherein X 1 , X 2 and X 3 are independently nitrogen atoms or groups of the formula CR 20 , X 4 and X 5 are independently oxygen or sulfur atoms or groups of the formula NR 21 , o is 0, 1 or 2, R 14 , R 15 , R 16 , R 17 , R 19 and R 20 are independently hydrogen atoms, halogen atoms, hydroxy, Ci-Cβ-alkyl, C 2 -C 6 alkenyl, C 2 -C 6 alkynyl or Ci -Cβ-heteroalkyl, and R 18 and R 21 are independently hydrogen, Ci-C 6 alkyl, C 2 -C 6 alkenyl, C 2 -C 6 alkynyl or C 6 heteroalkyl groups are.
Besonders bevorzugt weist Y eine der folgenden Strukturen auf :
Most preferably, Y has one of the following structures:
Insbesondere bevorzugt weist Y eine der folgenden Strukturen auf :Most preferably, Y has one of the following structures:
Weiter bevorzugt sind die Reste R6 unabhängig voneinander ein Halogenatom, eine Hydroxy-, eine Ci-C4-Alkyl- oder eine Ci-C4-Heteroalkylgruppe (z.B. eine Hydroxyethylgruppe) . More preferably, the radicals R 6 independently of one another are a halogen atom, a hydroxy, a C 1 -C 4 -alkyl or a C 1 -C 4 -heteroalkyl group (for example a hydroxyethyl group).
Des weiteren bevorzugt sind die Reste R6 unabhängig voneinander ein Fluor- oder ein Chloratom oder eine Hydroxy-, eine Ci-C4-Alkyloxy- , eine Ci-C4-Heteroalkyl- (z.B. eine Hydroxyethylgruppe) oder eine C3-C6-Dialkylamino- methylgruppe, wobei ein oder mehrere Wasserstoffatome dieser Gruppen durch Fluoratome ersetzt sein können.The radicals R 6 are furthermore preferably, independently of one another, a fluorine or a chlorine atom or a hydroxy, a C 1 -C 4 -alkyloxy, a C 1 -C 4 -heteroalkyl (eg a hydroxyethyl group) or a C 3 -C 6 Dialkylamino- methyl group, wherein one or more hydrogen atoms of these groups may be replaced by fluorine atoms.
Besonders bevorzugt sind die Reste R6 unabhängig voneinander eine Ci-C4-Heteroalkylgruppe (z.B. eine Hydroxyethylgruppe) .The radicals R 6 are particularly preferably independently of one another a Ci-C 4 -Heteroalkylgruppe (eg a hydroxyethyl group).
Besonders bevorzugt sind Verbindungen der Formel (II) :Particular preference is given to compounds of the formula (II):
wobei R2, R4a und R6a unabhängig voneinander ein Wasserstoff- oder Halogenatom oder eine Ci-C4-Heteroalkylgruppe (z.B. eine Hydroxymethyl- oder Hydroxyethylgruppe) sind (insbesondere ist R2 ein Wasserstoffatom und R4a und R6a ein Wasserstoff- oder Fluoratom oder eine Cχ-C4-Heteroalkyl- gruppe) . B und Y sind wie oben definiert. Insbesondere ist B eine Bindung oder eine Gruppe der Formel -NHCH2-, -NHC (=0)- Oder -NHSO2-.
Besonders bevorzugt sind Verbindungen der Formel (III) :wherein R 2 , R 4a and R 6a are independently a hydrogen or halogen atom or a Ci-C 4 -Heteroalkylgruppe (eg a hydroxymethyl or hydroxyethyl group) (in particular R 2 is a hydrogen atom and R 4a and R 6a is a hydrogen or Fluorine atom or a Cχ-C 4 heteroalkyl group). B and Y are as defined above. In particular, B is a bond or group of the formula -NHCH 2 -, -NHC (= O) - or -NHSO 2 -. Particular preference is given to compounds of the formula (III):
wobei R2 ein Wasserstoff- oder Halogenatom ist (insbesondere ist R2 ein Wasserstoffatom) . B und Y sind wie oben definiert. Insbesondere ist B eine Bindung oder eine Gruppe der Formel -CH2CH2-, -CH2CH2CH2- oder -CH2CH(OH)-.wherein R 2 is a hydrogen or halogen atom (in particular, R 2 is a hydrogen atom). B and Y are as defined above. In particular, B is a bond or a group of the formula -CH 2 CH 2 -, -CH 2 CH 2 CH 2 - or -CH 2 CH (OH) -.
Besonders bevorzugt sind Verbindungen der Formel (IV) :Particular preference is given to compounds of the formula (IV):
wobei R2 ein Wasserstoff- oder Halogenatom ist (insbesondere ist R2 ein Wasserstoffatom) . B und Y sind wie oben definiert. Insbesondere ist B eine Bindung oder eine Gruppe der Formel -CH2-, -CH2CH2-, -SO2- oder -C(=0)-.wherein R 2 is a hydrogen or halogen atom (in particular, R 2 is a hydrogen atom). B and Y are as defined above. In particular, B is a bond or a group of the formula -CH 2 -, -CH 2 CH 2 -, -SO 2 - or -C (= 0) -.
Es ist besonders bevorzugt, die bevorzugten Ausführungs- beispiele für jede generische Gruppe in den Formeln (I),
(II) , (III) und (IV) in jeder möglichen Weise zu kombinieren.It is particularly preferred to use the preferred embodiments for each generic group in the formulas (I), (II), (III) and (IV) in any possible way.
Verbindungen der Formeln (I) bis (IV) können aufgrund ihrer Substitution ein oder mehrere Chiralitätszentren enthalten. Die vorliegende Erfindung umfasst daher sowohl alle reinen Enantiomere und alle reinen Diastereomere, als auch deren Gemische in jedem Mischungsverhältnis. Des weiteren sind von der vorliegenden Erfindung auch alle cis/trans-Isomeren der Verbindungen der allgemeinen Formeln (I) bis (IV) sowie Gemische davon umfasst. Des weiteren sind von der vorliegenden Erfindung alle tautomeren Formen der Verbindungen der Formeln (I) bis (IV) umfasst.Compounds of formulas (I) to (IV) may contain one or more chiral centers due to their substitution. The present invention therefore encompasses both all pure enantiomers and all pure diastereomers, as well as their mixtures in any mixing ratio. Furthermore, all cis / trans isomers of the compounds of the general formulas (I) to (IV) and mixtures thereof are also encompassed by the present invention. Furthermore, all tautomeric forms of the compounds of the formulas (I) to (IV) are encompassed by the present invention.
Die therapeutische Verwendung der Verbindungen der Formeln (I) bis (IV), ihrer pharmakologisch akzeptablen Salze bzw. Solvate und Hydrate sowie Formulierungen und pharmazeutischen Zusammensetzungen liegen ebenfalls im Rahmen der vorliegenden Erfindung.The therapeutic use of the compounds of the formulas (I) to (IV), their pharmacologically acceptable salts or solvates and hydrates, as well as formulations and pharmaceutical compositions are also within the scope of the present invention.
Die pharmazeutischen Zusammensetzungen gemäß der vorliegenden Erfindung enthalten mindestens eine Verbindung der Formeln (I) bis (IV) als Wirkstoff und fakultativ Trägerstoffe und/oder Adjuvantien.The pharmaceutical compositions according to the present invention contain at least one compound of formulas (I) to (IV) as active ingredient and optionally excipients and / or adjuvants.
Beispiele für pharmakologisch akzeptable Salze der Verbindungen der Formeln (I) bis (IV) sind Salze von physiologisch akzeptablen Mineralsäuren wie Salzsäure, Schwefelsäure und Phosphorsäure oder Salze von organischen Säuren wie Methansulfonsäure, p-Toluolsulfonsäure,Examples of pharmacologically acceptable salts of the compounds of the formulas (I) to (IV) are salts of physiologically acceptable mineral acids such as hydrochloric acid, sulfuric acid and phosphoric acid or salts of organic acids such as methanesulfonic acid, p-toluenesulfonic acid,
Milchsäure, Essigsäure, Trifluoressigsäure, Zitronensäure, Bernsteinsäure, Fumarsäure, Maleinsäure und Salicylsäure.
Weitere Beispiele für pharmakologisch akzeptable Salze der Verbindungen der Formeln (I) bis (IV) sind Alkali- oder Erdalkalisalze wie z.B. Natrium, Kalium, Lithium, Calcium oder Magnesium Salze, Ammoniumsalze oder Salze von organi- sehen Basen wie z.B. Methylamin, Dirnethylamin, Triethylamin, Piperidin, Ethylendiamin, Lysin, Cholinhydroxid, Meglumin, Morpholin oder Arginin. Verbindungen der Formel (I) bis (IV) können solvatisiert, insbesondere hydratisiert sein. Die Hydratisierung kann z.B. während des Herstellungsverfahrens oder als Folge der hygroskopischen Natur der anfänglich wasserfreien Verbindungen der Formeln (I) bis (IV) auftreten. Wenn die Verbindungen der Formeln (I) bis (IV) asymmetrische C-Atome enthalten, können sie entweder als achirale Verbindungen, Diastereomeren-Gemische, Gemische von Enantiomeren oder als optisch reine Verbindungen vorliegen.Lactic acid, acetic acid, trifluoroacetic acid, citric acid, succinic acid, fumaric acid, maleic acid and salicylic acid. Further examples of pharmacologically acceptable salts of the compounds of formulas (I) to (IV) are alkali or alkaline earth salts such as sodium, potassium, lithium, calcium or magnesium salts, ammonium salts or salts of organic see bases such as methylamine, dimethylamine, triethylamine , Piperidine, ethylenediamine, lysine, choline hydroxide, meglumine, morpholine or arginine. Compounds of formula (I) to (IV) may be solvated, in particular hydrated. The hydration may occur, for example, during the manufacturing process or as a result of the hygroscopic nature of the initially anhydrous compounds of formulas (I) to (IV). When the compounds of formulas (I) to (IV) contain asymmetric C atoms, they may be present either as achiral compounds, diastereomeric mixtures, mixtures of enantiomers or as optically pure compounds.
Die Pro-Drugs (z.B. R. B. Silverman, Medizinische Chemie, VCH Weinheim, 1995, Kapitel 8, S. 361ff ) , die ebenfalls Gegenstand der vorliegenden Erfindung sind, bestehen aus einer Verbindung der Formeln (I) bis (IV) und mindestens einer pharmakologisch akzeptablen Schutzgruppe, die unter physiologischen Bedingungen abgespalten wird, z.B. einer Alkoxy- , Aralkyloxy-, Acyl- oder Acyloxy-Gruppe, wie z.B. einer Methoxy- , Ethoxy-, Benzyloxy-, Acetyl- oder Acetyloxy-Gruppe .The prodrugs (eg RB Silverman, Medizinische Chemie, VCH Weinheim, 1995, Chapter 8, p. 361ff), which are also the subject of the present invention, consist of a compound of formulas (I) to (IV) and at least one pharmacologically acceptable protecting group which is cleaved off under physiological conditions, eg an alkoxy, aralkyloxy, acyl or acyloxy group, e.g. a methoxy, ethoxy, benzyloxy, acetyl or acetyloxy group.
Auch die Verwendung dieser Wirkstoffe zur Herstellung von Arzneimitteln ist Gegenstand der vorliegenden Erfindung. Im allgemeinen werden Verbindungen der Formeln (I) bis (IV) unter Anwendung der bekannten und akzeptablen Modi, entweder einzeln oder in Kombination mit einem beliebigen
anderen therapeutischen Mittel verabreicht. Solche therapeutisch nützlichen Mittel können auf einem der folgenden Wege verabreicht werden: oral, z.B. als Dragees, überzogene Tabletten, Pillen, Halbfeststoffe, weiche oder harte Kapseln, Lösungen, Emulsionen oder Suspensionen; parenteral, z.B. als injizierbare Lösung; rektal als Suppositorien; durch Inhalation, z.B. alsThe use of these active ingredients for the preparation of medicaments is also an object of the present invention. In general, compounds of formulas (I) to (IV) will be prepared using the known and acceptable modes, either alone or in combination with any of them administered to other therapeutic agents. Such therapeutically useful agents may be administered by one of the following routes: orally, eg as dragees, coated tablets, pills, semi-solids, soft or hard capsules, solutions, emulsions or suspensions; parenteral, eg as an injectable solution; rectally as suppositories; by inhalation, eg as
Pulverformulierung oder Spray, transdermal oder intranasal Zur Herstellung solcher Tabletten, Pillen, Halbfeststoffe, überzogenen Tabletten, Dragees und harten Gelatinekapseln kann das therapeutisch verwendbare Produkt mit pharmakologisch inerten, anorganischen oder organischen Arzneimittelträgersubstanzen vermischt werden, z.B. mit Lactose, Sucrose, Glucose, Gelatine, Malz, Silicagel, Stärke oder Derivaten derselben, Talkum, Stearinsäure oder ihrenPowder Formulation or Spray, Transdermal or Intranasal For the preparation of such tablets, pills, semi-solids, coated tablets, dragées and hard gelatin capsules, the therapeutically useful product may be mixed with pharmacologically inert, inorganic or organic excipients, e.g. with lactose, sucrose, glucose, gelatin, malt, silica gel, starch or derivatives thereof, talc, stearic acid or theirs
Salzen, Trockenmagermilch und dgl . Zur Herstellung von weichen Kapseln kann man Arzneimittelträgerstoffe wie z.B. pflanzliche Öle, Petroleum, tierische oder synthetische Öle, Wachs, Fett, Polyole einsetzen. Zur Herstellung von flüssigen Lösungen und Sirups kann man Arzneimittelträger- stoffe wie z.B. Wasser, Alkohole, wässrige Salzlösung, wässrige Dextrose, Polyole, Glycerin, pflanzliche Öle, Petroleum, tierische oder synthetische Öle verwenden. Für Suppositorien kann man Arzneimittelträgerstoffe wie z.B. pflanzliche Öle, Petroleum, tierische oder synthetische Öle, Wachs, Fett und Polyole verwenden. Für Aerosol- Formulierungen kann man komprimierte Gase, die für diesen Zweck geeignet sind, wie z.B. Sauerstoff, Stickstoff und Kohlendioxid einsetzen. Die pharmazeutisch verwendbaren Mittel können auch Zusatzstoffe zur Konservierung, Stabilisierung, Emulgatoren, Süßstoffe, Aromastoffe, Salze zur
Veränderung des osmotischen Drucks, Puffer, Umhüllungszu- satzstoffe und Antioxidantien enthalten.Salts, dry skimmed milk and the like For the preparation of soft capsules, one can use excipients such as vegetable oils, petroleum, animal or synthetic oils, wax, fat, polyols. For the preparation of liquid solutions and syrups, excipients such as water, alcohols, aqueous saline, aqueous dextrose, polyols, glycerine, vegetable oils, petroleum, animal or synthetic oils may be used. For suppositories, one may use excipients such as vegetable oils, petroleum, animal or synthetic oils, wax, fat and polyols. For aerosol formulations, one can use compressed gases that are suitable for this purpose, such as oxygen, nitrogen and carbon dioxide. The pharmaceutically acceptable agents may also contain additives for preservation, stabilization, emulsifiers, sweeteners, flavorings, salts for Change in osmotic pressure, buffer, coating additives and antioxidants.
Die Verbindungen der allgemeinen Formeln (I) , (II) , (III) und (IV) weisen verbesserte Eigenschaften im Vergleich zu den antibakteriellen Verbindungen auf, die im Stand der Technik bekannt sind. Besonders sind hier eine verbesserte antibakterielle Aktivität, eine bessere Löslichkeit und verbesserte PK-Eigenschaften zu nennen.The compounds of the general formulas (I), (II), (III) and (IV) have improved properties as compared with the antibacterial compounds known in the art. Particularly noteworthy here are improved antibacterial activity, better solubility and improved PK properties.
Kombinationen mit anderen therapeutischen Mitteln können andere antimikrobielle und antifungale Wirkstoffe beinhalten.Combinations with other therapeutic agents may include other antimicrobial and antifungal agents.
Zur Vorbeugung und/oder Behandlung der oben beschriebenen Erkrankungen kann die Dosis der erfindungsgemäßen biologisch aktiven Verbindung innerhalb breiter Grenzen variieren und kann auf den individuellen Bedarf eingestellt werden. Im allgemeinen ist eine Dosis von 10 mg bis 4000 mg pro Tag geeignet, wobei eine bevorzugte Dosis 50 bis 3000 mg pro Tag ist. In geeigneten Fällen kann die Dosis auch unter oder über den oben angegebenen Werten liegen. Die tägliche Dosis kann als einfache Gabe oder in mehrfachen Gaben verabreicht werden. Eine typische Einzeldosis beinhaltet etwa 50 mg, 100 mg, 250 mg, 500 mg, 1 g oder 2 g des Wirkstoffs.
BeispieleFor the prevention and / or treatment of the diseases described above, the dose of the biologically active compound of the present invention may vary within wide limits and may be adjusted to individual needs. In general, a dose of 10 mg to 4000 mg per day is suitable, with a preferred dose being 50 to 3000 mg per day. In appropriate cases, the dose may also be below or above the above values. The daily dose may be given as a single dose or in multiple doses. A typical single dose contains about 50 mg, 100 mg, 250 mg, 500 mg, 1 g or 2 g of the active ingredient. Examples
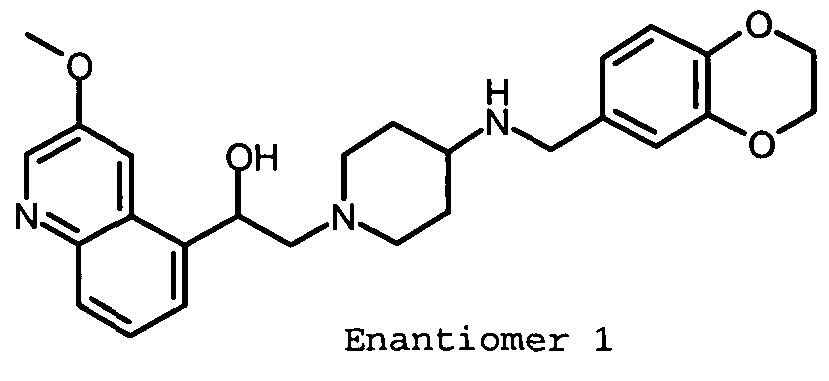
Beispiel Is 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-ylamino}-methyl) -4H-benzo [1, 4] oxazin-3- on (Enantiomer 2)Example Is 6- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [1,4-oxazine] 3-one (enantiomer 2)
Ia) 3, 5-Dibrom-chinolin 3-Bromchinolin (250 g) wurde zu eiskalter konzentrierter Schwefelsäure (625 ml) getropft, so dass die Temperatur nicht über 15°C stieg. Dann wurde N-Bromsuccinimid (240 g) langsam portionsweise zugegeben, so dass die Temperatur nicht über 200C stieg, und das Ganze bei Raumtemperatur über Nacht gerührt. Das Reaktionsgemisch wurde auf Eis (10 kg) gegossen und unter Kühlung mit festem Natriumhydroxid versetzt. Die enstehende Suspension wurde filtriert, der Feststoff mit Wasser gewaschen und bei 400C unter Vakuum getrocknet. Der Feststoff wurde in Methanol (1.5 1) suspendiert und anschliessend unter Rückfluss erhitzt. Nach dem Abkühlen wurde filtriert, mit kaltem Methanol (500 ml) nachgewaschen und das Filtrat eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Heptan 1:29, 1:19, 1:9) gereinigt und lieferte das gewünschte Produkt (151 g) .Ia) 3,5-Dibromoquinoline 3-Bromoquinoline (250 g) was added dropwise to ice-cold concentrated sulfuric acid (625 ml) so that the temperature did not rise above 15 ° C. Then, N-bromosuccinimide (240 g) was added slowly in portions so that the temperature did not rise above 20 ° C., and the whole was stirred at room temperature overnight. The reaction mixture was poured onto ice (10 kg) and treated with solid sodium hydroxide while cooling. The resulting suspension was filtered, the solid washed with water and dried at 40 0 C under vacuum. The solid was suspended in methanol (1.5 L) and then heated under reflux. After cooling, it was filtered, rinsed with cold methanol (500 ml) and the filtrate was concentrated. The crude product was purified by flash chromatography (silica gel, ethyl acetate / heptane 1:29, 1:19, 1: 9) to afford the desired product (151 g).
1H NMR (300 MHz, CDCl3): δ: 8.85 (d, IH), 8.65-8.64 (m, IH), 7.99 (d, IH), 7.78 (d, IH), 7.56-7.49 (m, IH)
Ib) 5-Brom-3-iϊiethoxy-chinolin 1 H NMR (300 MHz, CDCl 3): δ: 8.85 (d, IH), 8.65-8.64 (m, IH), 7.99 (d, IH), 7.78 (d, IH), 7:56 to 7:49 (m, IH ) Ib) 5-bromo-3-iϊiethoxy-quinoline
3 , 5-Dibromchinolin (Ia) (150 g) wurde zu einer gerührten Suspension von Natriummethylat (35.78 g) in trockenem DMPU (1.5 1) bei 1000C gegeben und anschliessend für 90 Minuten auf 125°C erhitzt. Nach dem Abkühlen wurde das Reaktionsgemisch auf Eis (7.5 kg) gegossen und über Nacht gerührt. Der entstandene Feststoff wurde abfiltriert, mit Wasser gewaschen und bei 400C im Vakuum getrocknet. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Heptan 1:19, 1:4) gereinigt und lieferte das gewünschte Produkt (65.2 g) .3, 5-dibromoquinoline (Ia) (150 g) was added to a stirred suspension of sodium methoxide (35.78 g) in dry DMPU (1.5 1) at 100 0 C and then heated for 90 minutes at 125 ° C. After cooling, the reaction mixture was poured onto ice (7.5 kg) and stirred overnight. The resulting solid was filtered off, washed with water and dried at 40 0 C in vacuo. The crude product was purified by flash chromatography (silica gel, ethyl acetate / heptane 1:19, 1: 4) to afford the desired product (65.2 g).
1H NMR (300 MHz, CDCl3): δ: 8.60 (d, IH) , 7.95 (d, IH), 7.72 (d, IH), 7.65 (d, IH), 7.37-7.31 (m, IH), 3.93 (s, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 8.60 (d, IH), 7.95 (d, IH), 7.72 (d, IH), 7.65 (d, IH), 7:37 to 7:31 (m, IH), 3.93 (s, 3H)
Ic) 3-Methoxy-5-vinyl-chinolinIc) 3-methoxy-5-vinyl-quinoline
Unter Stickstoff wurde Tetrakis ( triphenylphosphin) - palladium (0) (1.155 g) zu einer Lösung von Methoxychinolin (Ib) (9.52 g) in trockenem 1 , 2-Dimethoxyethan (450 ml) bei Raumtemperatur gegeben und 20 Minuten gerührt. Dann wurde Kaliumcarbonat (5.57 g) , Wasser (120 ml) und 2,4,6- Trivinylcycloboroxan-Pyridin-Komplex (3.85 g - O'Sheas Reagenz - Siehe J. Org. ehem., Vol. 67 (2002), 4968-4971) zugegeben und für 4 Stunden auf 1000C erhitzt. Nach dem Abkühlen auf Raumtemperatur wurde Wasser (200 ml) zugegeben und mit Essigester extrahiert (4 x 150 ml) . Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Heptan/Essigester 9:1, 3:2) gereinigt und lieferte das gewünschte Produkt (7.41 g) .
1H NMR (300 MHz, CDCl3) : δ: 8.60 (d, IH) , 7.91 (d, IH) , 7.57-7.41 (m, 3H) , 7.28-7.22 (m, IH) , 5.72 (dd, IH) , 5.43 (dd, IH) , 3.87 (s, 3H)Under nitrogen, tetrakis (triphenylphosphine) -palladium (0) (1155 g) was added to a solution of methoxyquinoline (Ib) (9.52 g) in dry 1, 2-dimethoxyethane (450 ml) at room temperature and stirred for 20 minutes. Then, potassium carbonate (5.57 g), water (120 ml) and 2,4,6-trivinylcycloboroxane-pyridine complex (3.85 g - O'Sheas Reagent - See J. Org. Ex., Vol. 67 (2002), 4968 -4971) was added and heated for 4 hours at 100 0 C. After cooling to room temperature, water (200 ml) was added and extracted with ethyl acetate (4 x 150 ml). The combined organic phases were dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, heptane / ethyl acetate 9: 1, 3: 2) to afford the desired product (7.41 g). 1 H NMR (300 MHz, CDCl 3): δ: 8.60 (d, IH), 7.91 (d, IH), 7:57 to 7:41 (m, 3H), 7:28 to 7:22 (m, IH), 5.72 (dd, IH ), 5.43 (dd, IH), 3.87 (s, 3H)
Id) l-(3-Methoxy-chinolin-5-yl)-ethan-l,2-diol (Enantiomer 2)Id) 1- (3-methoxyquinolin-5-yl) ethane-1,2-diol (enantiomer 2)
AD mix alpha (90.2 g) und Methansulfonsäureamid (7.6 g) wurden in Wasser (280 ml) und tert-Butanol (280 ml) bei Raumtemperatur gelöst. Die orange Lösung wurde auf 00C abgekühlt, Vinylchinolin (Ic) (14.4 g) zugegeben und 2 Tage bei 0-40C gerührt. Danach wurde bei 00C Natriumpyrosulfit (108 g) zugegeben und 30 Minuten bei dieser Temperatur gerührt. Nach dem Erwärmen auf Raumtemperatur wurde mit Essigester (5 x 150 ml) extrahiert. Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 29:1, 4:1) gereinigt und lieferte das gewünschte Produkt (14.91 g) .AD mix alpha (90.2 g) and methanesulfonic acid amide (7.6 g) were dissolved in water (280 ml) and tert-butanol (280 ml) at room temperature. The orange solution was cooled to 0 0 C, was added vinylquinoline (Ic) (14.4 g) and stirred for 2 days at 0-4 0 C. Next, sodium pyrosulfite (108 g) was added at 0 ° C. and stirred for 30 minutes at this temperature. After warming to room temperature, it was extracted with ethyl acetate (5 x 150 ml). The combined organic phases were dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, dichloromethane / methanol 29: 1, 4: 1) to afford the desired product (14.91 g).
1H NMR (300 MHz, d6-DMSO) : δ: 8.65 (d, IH), 7.88-7.85 (m, 2H), 7.66 (d, IH), 7.58-7.53 (m, IH), 5.51 (d, IH), 5.31- 5.26 (m, IH), 4.87-4.84 (m, IH), 3.96 (s, 3H), 3.67-3.57 (m, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.65 (d, IH), 7.88-7.85 (m, 2H), 7.66 (d, IH), 7.58-7.53 (m, IH), 5.51 (i.e. , IH), 5.31-5.26 (m, IH), 4.87-4.84 (m, IH), 3.96 (s, 3H), 3.67-3.57 (m, 2H)
Ie) Toluol-4-sulfonsäure-2-hydroxy-2- (3-methoxy-chinolin-5- yl) -ethylester (Enantiomer 2)Ie) Toluene-4-sulfonic acid 2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl ester (enantiomer 2)
Unter Stickstoff wurde zu einer Suspension von Diol (Id) (14.4 g) in trockenem Dichlormethan (150 ml) bei Raum- temperatur unter Rühren Dibutylzinnoxid (0.33 g) , p-Toluol- sulfonsäure (12.78 g) und Triethylamin (9.33 ml) gegeben. Die Reaktionsmischung wurde 14 Stunden gerührt, dann mit
Wasser (150 ml) gequencht und die organische Phase abgetrennt. Die wässrige Phase wurde noch 2 x mit Dichlormethan (jeweils 150 ml) extrahiert. Die vereinigten organischen Phasen wurden mit Wasser (150 ml) und ges . Natriumchloridlösung (150 ml) gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1) gereinigt und lieferte das gewünschte Produkt (16.12 g) .Under nitrogen, dibutyltin oxide (0.33 g), p-toluenesulfonic acid (12.78 g) and triethylamine (9.33 ml) were added to a suspension of diol (Id) (14.4 g) in dry dichloromethane (150 ml) at room temperature with stirring , The reaction mixture was stirred for 14 hours, then with Quenched water (150 ml) and the organic phase separated. The aqueous phase was extracted twice more with dichloromethane (150 ml each time). The combined organic phases were washed with water (150 ml) and sat. Sodium chloride solution (150 ml), dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1) to give the desired product (16.12 g).
1H NMR (300 MHz, d6-DMSO) : δ: 8.63 (d, IH), 7.89 (d, IH) , 7.67-7.62 (m, 2H), 7.58-7.47 (m, 3H), 7.27 (d, 2H), 6.05 (bs, IH), 5.56 (bs, IH), 4.25 (dd, IH), 4.14 (dd, IH), 3.89 (s, 3H), 2.34 (s, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.63 (d, IH), 7.89 (d, IH), 7.67-7.62 (m, 2H), 7.58-7.47 (m, 3H), 7.27 (i.e. , 2H), 6.05 (bs, IH), 5.56 (bs, IH), 4.25 (dd, IH), 4.14 (dd, IH), 3.89 (s, 3H), 2.34 (s, 3H)
If) 3-Methoxy-5-oxiranyl-chinolin (Enantiomer 2) Bei Raumtemperatur wurde eine Lösung von Tosylat (Ie) (15.97 g) in Diethylether (300 ml) unter Rühren mit 2N Natronlauge (110 ml) versetzt. Die zweiphasige Mischung wurde 3 Stunden bei Raumtemperatur gerührt und dann die organische Phase abgetrennt. Die wässrige Phase wurde noch 3 x mit Diethylether (150 ml) extrahiert. Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Heptan 1:1) gereinigt und lieferte das gewünschte Produkt (5.8 g) .If) 3-Methoxy-5-oxiranyl-quinoline (Enantiomer 2) At room temperature, a solution of tosylate (Ie) (15.97 g) in diethyl ether (300 ml) was added under stirring with 2N sodium hydroxide solution (110 ml). The biphasic mixture was stirred at room temperature for 3 hours and then the organic phase separated. The aqueous phase was extracted 3 more times with diethyl ether (150 ml). The combined organic phases were dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, ethyl acetate / heptane 1: 1) to afford the desired product (5.8 g).
1H NMR (300 MHz, CDCl3): δ: 8.64 (d, IH), 7.94 (dd, IH), 7.59 (d, IH), 7.48-7.39 (m, 2H), 4.30 (m, IH), 3.91 (s, 3H), 3.22 (dd, IH), 2.81 (dd, IH)
Ig) {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) -ethyl] - piperidin-4-yl} -carbaminsäure-tert-butylester (Enantiomer 2) 1 H NMR (300 MHz, CDCl 3): δ: 8.64 (d, IH), 7.94 (dd, IH), 7:59 (d, IH), 7:48 to 7:39 (m, 2H), 4.30 (m, IH), 3.91 (s, 3H), 3.22 (dd, IH), 2.81 (dd, IH) Ig) tert-butyl {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-yl} -carbamate (enantiomer 2)
Epoxid (If) (689 mg) und 4- (tert-Butoxycarbonyl- amino)piperidin (686 mg) wurden in DMF (11 ml) gelöst, mit Kaliumcarbonat (497 mg) und Lithiumperchlorat (364 mg) versetzt und bei 800C für 2 Tage gerührt. Die Lösung wurde eingeengt, der Rückstand in Dichlormethan gelöst und mit Wasser und ges . Natriumchloridlösung extrahiert. Die organische Phase wurde über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Dichlormethan/Methanol 97:3) gereinigt und lieferte das gewünschte Produkt (1.22 g) .Epoxide (If) (689 mg) and 4- (tert-butoxycarbonyl amino) piperidine (686 mg) were dissolved in DMF (11 ml), treated with potassium carbonate (497 mg) and lithium perchlorate (364 mg) at 80 0 C. stirred for 2 days. The solution was concentrated, the residue dissolved in dichloromethane and washed with water and sat. Extracted sodium chloride solution. The organic phase was dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 97: 3) to afford the desired product (1.22 g).
1H NMR (300 MHz, CDCl3): δ: 8.56 (d, IH), 7.92 (m, IH), 7.64 (m, IH), 7.48-7.43 (m, IH), 5.72 (bs, IH), 4.51 (m, IH), 3.85 (s, 3H), 3.60-3.46 (m, IH), 3.29-3.26 (m, 2H), 2.84- 2.73 (m, 2H), 2.67-2.40 (m, 2H), 2.09-1.95 (m, 2H), 1.84- 1.64 (m, 2H), 1.38 (s, 9H) 1 H NMR (300 MHz, CDCl 3): δ: 8:56 (d, IH), 7.92 (m, IH), 7.64 (m, IH), 7:48 to 7:43 (m, IH), 5.72 (bs, IH), 4.51 (m, IH), 3.85 (s, 3H), 3.60-3.46 (m, IH), 3.29-3.26 (m, 2H), 2.84-2.73 (m, 2H), 2.67-2.40 (m, 2H), 2.09-1.95 (m, 2H), 1.84- 1.64 (m, 2H), 1.38 (s, 9H)
Ih) 2- (4-Amino-piperidin-l-yl) -1- (3-methoxy-chinolin-5-yl) - ethanol (Enantiomer 2)Ih) 2- (4-amino-piperidin-1-yl) -1- (3-methoxy-quinolin-5-yl) -ethanol (enantiomer 2)
Boc-Amin (Ig) (1.22 g) wurde in Dichlormethan (23 ml) gelöst, bei 0-50C mit Trifluoressigsäuere behandelt (2.3 ml) und bei Raumtemperatur über Nacht gerührt. Die Lösung wurde mit 2N Natronlauge basisch gemacht und die Phasen getrennt. Die wässrige Phase wurde mit Dichlormethan extrahiert. Die vereinigten organischen Phasen wurden mit ges. Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel,
Dichlormethan/Methanol 9:1 + 1% Ammoniak) gereinigt und lieferte das gewünschte Produkt (557 mg) .Boc-amine (Ig) (1.22 g) was dissolved in dichloromethane (23 ml), treated at 0 C with 0-5 Trifluoressigsäuere (2.3 ml) and stirred at room temperature overnight. The solution was basified with 2N sodium hydroxide and the phases separated. The aqueous phase was extracted with dichloromethane. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, Dichloromethane / methanol 9: 1 + 1% ammonia) to afford the desired product (557 mg).
1H NMR (300 MHz, d6-DMSO) : δ: 8.66-8.63 (m, IH), 7.87-7.82 (m, 2H), 7.67 (m, IH) , 7.58-7.51 (m, IH), 5.43-5.39 (m, IH), 5.26-5.23 (m, IH), 3.95 (s, 3H), 2.99-2.85 (m, 2H), 2.62-2.55 (m, IH), 2.19-1.99 (m, 2H), 1.72-1.57 (m, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.66-8.63 (m, IH), 7.87-7.82 (m, 2H), 7.67 (m, IH), 7.58-7.51 (m, IH), 5.43 -5.39 (m, IH), 5.26-5.23 (m, IH), 3.95 (s, 3H), 2.99-2.85 (m, 2H), 2.62-2.55 (m, IH), 2.19-1.99 (m, 2H) , 1.72-1.57 (m, 2H)
Ii) (4-Formyl-2-nitro-phenoxy) -essigsäureethylester 4-Hydroxy-3-nitrobenzaldehyd (25 g) wurde in DMF (250 ml) gelöst. Dann wurde Kaliumcarbonat hinzugegeben (22.7 g) und Chloressigsäureethylester (23.2 ml) zugetropft. Die Lösung wurde zwei Tage bei 500C und zwei weitere Tage bei Raumtemperatur gerührt, dann mit Wasser verdünnt und mit Essigester extrahiert. Die vereinigten organischen Phasen wurden mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt und lieferten das gewünschte Produkt (37.8 g) .Ii) (4-Formyl-2-nitro-phenoxy) -acetic acid ethyl ester 4-Hydroxy-3-nitrobenzaldehyde (25 g) was dissolved in DMF (250 ml). Then, potassium carbonate was added (22.7 g) and ethyl chloroacetate (23.2 ml) was added dropwise. The solution was stirred at 50 ° C. for two days and at room temperature for two more days, then diluted with water and extracted with ethyl acetate. The combined organic phases were washed with water, dried over magnesium sulfate, filtered and concentrated to afford the desired product (37.8 g).
1H NMR (300 MHz, d6-DMSO) : δ: 9.96 (s, IH), 8.44 (s, IH), 8.15 (dd, IH), 7.52 (d, IH), 5.17 (s, 2H), 4.18 (q, 2H), 1.21 (t, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 9.96 (s, IH), 8.44 (s, IH), 8.15 (dd, IH), 7.52 (d, IH), 5.17 (s, 2H), 4.18 (q, 2H), 1.21 (t, 3H)
Ij ) 3-Oxo-3,4-dihydro-2H-benzo[l,4]oxazin-6-carbaldehyd Phenoxyessigsäureethylester (Ii) (37.7 g) wurde inIj) 3-Oxo-3,4-dihydro-2H-benzo [l, 4] oxazine-6-carbaldehyde Phenoxyacetic acid ethyl ester (Ii) (37.7 g) was dissolved in
Essigsäure (1000 ml) gelöst. Dann wurde Eisenpulver (83 g) zugegeben und bei 800C 1.5 Stunden gerührt. Das Reaktions- gemisch wurde durch Decalit filtriert und eingeengt. Der Rückstand wurde in ges . Natriumhydrogencarbonatlösung aufgenommen und mit Essigester extrahiert. Die vereinigten organischen Phasen wurden über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mit Ether
versetzt, der Niederschlag abfiltiert und lieferte das gewünschte Produkt (20 g) .Acetic acid (1000 ml) dissolved. Then, iron powder (83 g) was added and stirred at 80 ° C. for 1.5 hours. The reaction mixture was filtered through decalite and concentrated. The residue was dissolved in sat. Sodium bicarbonate solution and extracted with ethyl acetate. The combined organic phases were dried over magnesium sulfate, filtered and concentrated. The residue was washed with ether the precipitate filtered off and gave the desired product (20 g).
1H NMR (300 MHz, dβ-DMSO) : δ: 11.00 (bs, IH), 9.84 (s, IH), 7.54 (dd, IH), 7.39 (d, IH), 7.14 (d, IH), 4.72 (s, 2H) 1 H NMR (300 MHz, d β -DMSO): δ 11.00 (bs, IH), 9.84 (s, IH), 7:54 (dd, IH), 7:39 (d, IH), 7.14 (d, IH), 4.72 (s, 2H)
Ik) TitelverbindungIk) title compound
Amin (Ih) (100 mg) wurde in 1 , 2-Dichlorethan (6 ml) und Methanol (2 ml) gelöst, mit 3A Molsieb (1.00 g) und Aldehyd (Ij) (71 mg) versetzt. Die Mischung wurde bei Raumtemperatur über Nacht gerührt . Dann wurde Natriumborhydrid (13 mg) hinzugefügt und die Mischung für 4 Stunden bei Raumtemperatur gerührt. Das Molsieb wurde abfiltriert und das Filtrat mit ges . Natriumhydrogencarbonatlösung und ges . Natriumchloridlösung gewaschen. Die organische Phase wurde über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1 + 1% Ammoniak) gereinigt und lieferte das gewünschte Produkt (70 mg) .Amine (Ih) (100 mg) was dissolved in 1,2-dichloroethane (6 ml) and methanol (2 ml), added with 3A molecular sieves (1.00 g) and aldehyde (Ij) (71 mg). The mixture was stirred at room temperature overnight. Then, sodium borohydride (13 mg) was added and the mixture was stirred for 4 hours at room temperature. The molecular sieve was filtered off and the filtrate with sat. Sodium bicarbonate solution and sat. Washed sodium chloride solution. The organic phase was dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1 + 1% ammonia) to afford the desired product (70 mg).
1H NMR (300 MHz, d6-DMSO) : δ: 10.78 (S, IH), 8.66 (d, IH), 7.96 (s, IH), 7.88-7.84 (m, 2H), 7.70-7.68 (m, IH), 7.59- 7.54 (m, IH), 7.00-6.91 (m, 3H), 5.75 (s, IH), 5.49-5.46 (m, IH), 4.56 (s, 2H), 3.96 (s, 3H), 2.82 (s, 2H), 3.12- 3.03 (m, 2H), 2.72-2.60 (m, 2H), 2.30-2.10 (m, 2H), 2.00- 1.85 (m, 2H), 1.58-1.36 (m, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.78 (S, IH), 8.66 (d, IH), 7.96 (s, IH), 7.88-7.84 (m, 2H), 7.70-7.68 (m , IH), 7.59-7.54 (m, IH), 7.00-6.91 (m, 3H), 5.75 (s, IH), 5.49-5.46 (m, IH), 4.56 (s, 2H), 3.96 (s, 3H ), 2.82 (s, 2H), 3.12- 3.03 (m, 2H), 2.72-2.60 (m, 2H), 2.30-2.10 (m, 2H), 2.00- 1.85 (m, 2H), 1.58-1.36 (m , 3H)
Beispiel 2: 6- ( {1- [2-Hydroacy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-ylamino} -methyl) -4H-pyrido [3, 2- b] [1,4] thiazin-3-on (Enantiomer 2)
Example 2: 6- ({1- [2-Hydroacy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4 H -pyrido [3, 2-b ] [1,4] thiazine-3-one (enantiomer 2)
2a) N-(6-Methyl-pyridin-2-yl)-acetamid2a) N- (6-methyl-pyridin-2-yl) -acetamide
Eine Lösung von 3-Amino-6-picolin (39 g) in Essigsäureanhydrid (200 ml) wurde für 90 Minuten auf 700C erhitzt und anschliessend eingeengt. Der Rückstand wurde in Wasser (500 ml) aufgenommen, mit festem Natriumhydrogencarbonat auf pH 8 gebracht und mit Essigester extrahiert (2 x 200 ml) . Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt und lieferten das gewünschte Produkt (53.3 g) .A solution of 3-amino-6-picoline (39 g) in acetic anhydride (200 ml) was heated for 90 minutes at 70 0 C and subsequently concentrated. The residue was taken up in water (500 ml), brought to pH 8 with solid sodium bicarbonate and extracted with ethyl acetate (2 x 200 ml). The combined organic phases were washed with sat. Sodium chloride solution, dried over magnesium sulfate, filtered and concentrated to afford the desired product (53.3 g).
1H NMR (300 MHz, CDCl3): δ: 8.43 (bs, IH), 8.00 (d, IH), 7.62-7.57 (m, IH), 6.89 (d, IH), 2.45 (s, 3H), 2.18 (s, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 8:43 (bs, IH), from 8.00 (d, IH), 7.62-7.57 (m, IH), 6.89 (d, IH), 2:45 (s, 3H), 2.18 (s, 3H)
2b) 6-Acetylamino-pyridin-2-carbonsäure2b) 6-acetylamino-pyridine-2-carboxylic acid
Eine Suspension des Acetamides (2a) (53.3 g) in Wasser (530 ml) wurde auf 75°C erhitzt, bis sich eine homogene Lösung gebildet hatte. Kaliumpermanganat (133 g) wurde in kleinen Portionen über 1.25 Stunden hinzugegeben (die Reaktiontemperatur im Innern des Kolbens wurde sorgfältig kontrolliert) . Nach 3 Stunden Rühren bei 75°C wurde die Reaktionslösung heiss durch Celit filtriert und mit heissem Wasser nachgewaschen. Das FiItrat wurde auf etwa 100 ml eingeengt und konz . Salzsäure zugegeben, bis sich ein weisser Niederschlag bildete. Der weisse Feststoff wurde abfiltriert, getrocknet und lieferte das gewünschte Produkt (32 g) .
1H NMR (300 MHz, d6-DMSO) : δ: 10.85 (s, IH) , 8.26 (d, IH) , 7.97-7.72 (m, IH) , 7.73 (dd, IH) , 2.11 (s, 3H)A suspension of the acetamide (2a) (53.3 g) in water (530 ml) was heated to 75 ° C until a homogeneous solution had formed. Potassium permanganate (133 g) was added in small portions over 1.25 hours (the reaction temperature inside the flask was carefully controlled). After stirring for 3 hours at 75 ° C, the reaction solution was filtered hot through celite and washed with hot water. The filtrate was concentrated to about 100 ml and conc. Hydrochloric acid added until a white precipitate formed. The white solid was filtered off, dried and afforded the desired product (32 g). 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.85 (s, IH), 8.26 (d, IH), 7.97-7.72 (m, IH), 7.73 (dd, IH), 2.11 (s, 3H )
2c) 6-Amino-pyridin-2-carbonsäuremethylester2c) 6-Amino-pyridine-2-carboxylic acid methyl ester
Säure (2b) (18 g) wurde in Methanol suspendiert, mit HCl- Gas gesättigt und über Nacht unter Rückfluss erhitzt. Nach dem Abkühlen wurde eingeengt und der Rückstand mit Wasser und Dichlormethan aufgenommen. Festes Natriumhydrogencarbonat wurde hinzugegeben und die Phasen getrennt. Die wässrige Phase wurde mit Dichlormethan extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel,Acid (2b) (18 g) was suspended in methanol, saturated with HCl gas and heated at reflux overnight. After cooling, the mixture was concentrated and the residue was taken up in water and dichloromethane. Solid sodium bicarbonate was added and the phases separated. The aqueous phase was extracted with dichloromethane. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel,
Dichlormethan/Essigester 1:1) gereinigt und lieferte das gewünschte Produkt (9.64 g) .Dichloromethane / ethyl acetate 1: 1) to afford the desired product (9.64 g).
1H NMR (300 MHz, CDCl3): δ: 7.52-7.41 (m, 2H), 6.66 (dd, IH), 5.12 (bs, 2H), 3.91 (s, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 7:52 to 7:41 (m, 2H), 6.66 (dd, IH), 5.12 (bs, 2H), 3.91 (s, 3H)
2d) 6-Amino-5-brom-pyridin-2-carbonsäuremethylester2d) 6-Amino-5-bromo-pyridine-2-carboxylic acid methyl ester
Zu einer Lösung von Ester (2c) (9.64 g) in Chloroform (408 ml) wurde eine Lösung von Brom (3.35 ml) in Chloroform (70 ml) über 60 Minuten zugetropft. Nachdem das Ganze 40 Stunden bei Raumtemperatur gerührt hatte, wurde ges. Natriumthiosulfatlösung (150 ml) zugegeben und die Phasen getrennt. Die wässrige Phase wurde mit Dichlormethan extrahiert. Die vereingten organischen Phasen wurden mit ges. Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde
mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 2:1) gereinigt und lieferte das gewünschte Produkt (1.8 g) .To a solution of ester (2c) (9.64 g) in chloroform (408 ml) was added dropwise a solution of bromine (3.35 ml) in chloroform (70 ml) over 60 minutes. After stirring at room temperature for 40 hours, sat. Sodium thiosulfate solution (150 ml) was added and the phases separated. The aqueous phase was extracted with dichloromethane. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over magnesium sulfate, filtered and concentrated. The residue became purified by flash chromatography (silica gel, hexane / ethyl acetate 2: 1) to afford the desired product (1.8 g).
1H NMR (300 MHz, CDCl3): δ: 7.73 (d, IH), 7.29 (d, IH), 5.39 (bs, 2H), 3.90 (s, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 7.73 (d, IH), 7.29 (d, IH), 5:39 (bs, 2H), 3.90 (s, 3H)
2e) 3-Oxo-3, 4-dihydro-2H-pyrido[3,2-b] [1,4] thiazin-6- carbonsäuremethylester2e) 3-Oxo-3,4-dihydro-2H-pyrido [3,2-b] [1,4] thiazine-6-carboxylic acid methyl ester
Zu einer Lösung von Methylthioglycolat (2.4 ml) in DMF (75 ml) wurde Natriumhydrid (1.1 g) gegeben. Nach einer Stunde wurde Brompyridin (2d) (5 g) zugegeben und 12 Stunden bei Raumtemperatur gerührt. Die Reaktionslösung wurde mit Wasser (150 ml) verdünnt. Der Feststoff wurde abfiltriert, mit wenig Essigester und Acetonitril gewaschen und lieferte das gewünschte Produkt (1.65 g) .To a solution of methyl thioglycolate (2.4 ml) in DMF (75 ml) was added sodium hydride (1.1 g). After one hour, bromopyridine (2d) (5 g) was added and stirred at room temperature for 12 hours. The reaction solution was diluted with water (150 ml). The solid was filtered off, washed with a little ethyl acetate and acetonitrile to afford the desired product (1.65 g).
1H NMR (300 MHz, d6-DMSO) : δ: 11.29 (s, IH), 7.97 (d, IH), 7.66 (d, IH), 3.86 (s, 3H), 3.64 (s, 2H), 3.33 (s, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 11.29 (s, IH), 7.97 (d, IH), 7.66 (d, IH), 3.86 (s, 3H), 3.64 (s, 2H), 3.33 (s, 3H)
2f) 3-Oxo-3,4-dihydro-2H-pyrido[3,2-b] [1,4] thiazin-6- carbonsäure2f) 3-Oxo-3,4-dihydro-2H-pyrido [3,2-b] [1,4] thiazine-6-carboxylic acid
Zu einer Lösung von Ester (2e) (2.33 g) in Dioxan (354 ml) und Wasser (90 ml) wurde über 2 Stunden 0.5N Natronlauge (24 ml) zugetropft und dann bei Raumtemperatur über Nacht gerührt. Die Lösung wurde eingeengt und der pH auf 4 mit 2N Salzsäure eingestellt. Der entstandene Feststoff wurde abfiltriert, mit wenig Wasser gewaschen und über Nacht unter Vakuum getrocknet und lieferte das gewünschte Produkt (1.72 g) .To a solution of ester (2e) (2.33 g) in dioxane (354 ml) and water (90 ml) was added dropwise over 2 hours 0.5N sodium hydroxide solution (24 ml) and then stirred at room temperature overnight. The solution was concentrated and the pH adjusted to 4 with 2N hydrochloric acid. The resulting solid was filtered off, washed with a little water and dried under vacuum overnight to yield the desired product (1.72 g).
MS (EI) : m/z: 211 [M+H]+
2g) 6-Hydroxymethyl-4H-pyrido[3,2-b] [1,4] thiazin-3-onMS (EI): m / z: 211 [M + H] + 2g) 6-hydroxymethyl-4H-pyrido [3,2-b] [1,4] thiazine-3-one
Zu einer Lösung der Säure (2f) (1.72 g) in THF (82 ml) wurde Triethylamin (1.4 ml) und Isobutylchloroformat (1.2 ml) bei -100C gegeben. Nach 25 Minuten wurde die Lösung durch Celit in eine eiskalte Lösung von Natriumborhydrid (1.1 g) in Wasser (28 ml) filtriert, bei dieser Temperatur 30 Minuten gerührt und der pH auf 7 mit 0.2N Salzsäure eingestellt. Nach dem Einengen wurde der entstandene Feststoff abfiltriert, mit Wasser gewaschen und getrocknet und lieferte das gewünschte Produkt (1.1 g) .To a solution of the acid (2f) (1.72 g) in THF (82 ml) was added triethylamine (1.4 ml) and isobutyl chloroformate (1.2 ml) at -10 0 C. After 25 minutes, the solution was filtered through celite into an ice-cold solution of sodium borohydride (1.1 g) in water (28 ml), stirred at this temperature for 30 minutes, and the pH adjusted to 7 with 0.2N hydrochloric acid. After concentration, the resulting solid was filtered off, washed with water and dried to afford the desired product (1.1 g).
MS (EI) : m/z: 197 [M+H]+ MS (EI): m / z: 197 [M + H] +
2h) 3-Oxo-3,4-dihydro-2H-pyrido[3,2-b] [1,4] thiazin-6- carbaldehyd2h) 3-Oxo-3,4-dihydro-2H-pyrido [3,2-b] [1,4] thiazine-6-carbaldehyde
Zu einer Lösung des Alkohols (2g) (1.1 g) in Dichlormethan (100 ml) und THF (100 ml) wurde Mangandioxid (2.5 g) gegeben. Nachdem für 90 Minuten bei Raumtemperatur gerührt worden war, wurde weiteres Mangandioxid (3 g) zugegeben, weitere 2 Stunden bei Raumtemperatur gerührt und dann durch Celit filtriert. Das Filtrat wurde eingeengt und lieferte das gewünschte Produkt (598 mg) .To a solution of the alcohol (2g) (1.1g) in dichloromethane (100ml) and THF (100ml) was added manganese dioxide (2.5g). After being stirred for 90 minutes at room temperature, additional manganese dioxide (3 g) was added, stirred for a further 2 hours at room temperature and then filtered through celite. The filtrate was concentrated to afford the desired product (598 mg).
1H NMR (300 MHz, CDCl3): δ: 9.85 (s, IH), 8.40 (bs, IH) , 7.74 (d, IH), 7.55 (d, IH) , 3.50 (s, 2H) 1 H NMR (300 MHz, CDCl 3): δ: 9.85 (s, IH), 8.40 (bs, IH), 7.74 (d, IH), 7:55 (d, IH), 3:50 (s, 2H)
2i) Titelverbindung2i) Title compound
Die Verbindung wurde wie in Beispiel Ik aus Aldehyd (2h) in 96% Ausbeute hergestellt.The compound was prepared as in Example Ik from aldehyde (2h) in 96% yield.
1H NMR (300 MHz, d6-DMSO) : δ: 10.85 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.74-7.67 (m, 2H), 7.58-7.51 (m, IH),
7.11-7.05 (m, IH), 5.50-5.36 (m, IH), 5.30-5.19 (m, IH), 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.85 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.74-7.67 (m, 2H), 7.58-7.51 (m, IH), 7.11-7.05 (m, IH), 5.50-5.36 (m, IH), 5.30-5.19 (m, IH),
3.95 (m, IH), 3.72 (s, 2H), 3.53 (s, 2H), 3.02-2.87 (m,3.95 (m, IH), 3.72 (s, 2H), 3.53 (s, 2H), 3.02-2.87 (m,
2H), 2.65-2.54 (m, 2H), 2.44-2.32 (m, IH), 2.21-2.02 (m,2H), 2.65-2.54 (m, 2H), 2.44-2.32 (m, IH), 2.21-2.02 (m,
2H), 1.86-1.70 (m, 3H), 1.42-1.13 (m, 3H)2H), 1.86-1.70 (m, 3H), 1.42-1.13 (m, 3H)
Beispiel 3: 7-Fluor-6- ( {1- [2-hydroxy-2- (3-methoxy-chinolin- 5-yl) -ethyl] -piperidin-4-ylamino}-methyl) -4H- benzo[l,4] thiazin-3-on (Enantiomer 2)Example 3: 7-Fluoro-6- ({1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [l , 4] thiazine-3-one (enantiomer 2)
3a) 2, 4-Difluorbenzoesäureethylester3a) 2, 4-Difluorbenzoesäureethylester
2 , 4-Difluorbenzoesäure (5.00 g) wurde in Ethanol (50 ml) gelöst und für 20 Minuten HCl-Gas duch die Lösung geleitet. Dann wurde für 5 Stunden unter Rückfluss erhitzt, die Lösung eingeengt und der Rückstand in Ether gelöst. Die organische Phase wurde mit IN Natronlauge und ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt und lieferte das gewünschte Produkt (3.8 g) .2,4-Difluorobenzoic acid (5.00 g) was dissolved in ethanol (50 ml) and bubbled through the solution for 20 minutes with HCl gas. The mixture was then refluxed for 5 hours, the solution was concentrated and the residue was dissolved in ether. The organic phase was washed with 1N sodium hydroxide solution and sat. Sodium chloride solution, dried over magnesium sulfate, filtered and concentrated to afford the desired product (3.8 g).
1H NMR (300 MHz, CDCl3): δ: 8.05-7.95 (m, IH), 6.99-6.82 (m, 2H), 4.40 (q, 2H), 1.22 (t, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 8.05-7.95 (m, IH), 6.99-6.82 (m, 2H), 4:40 (q, 2H), 1.22 (t, 3H)
3b) 2,4-Difluor-5-nitro-benzoesäureethylester3b) ethyl 2,4-difluoro-5-nitrobenzoate
Ethylester (3a) (3.8 g) wurde in rauchender Salpetersäure (3 ml) und konz . Schwefelsäure (3 ml) bei 00C gelöst und für 2.5 Stunden gerührt. Dann wurde mit Wasser (10 ml)
verdünnt und mit Dichlormethan (200 ml) extrahiert. Die organische Phase wurde mit ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Hexan/Essigester 6:1) gereinigt und lieferte das gewünschte Produkt (3.96 g) .Ethyl ester (3a) (3.8 g) was dissolved in fuming nitric acid (3 ml) and conc. Dissolved sulfuric acid (3 ml) at 0 0 C and stirred for 2.5 hours. Then it was washed with water (10 ml) diluted and extracted with dichloromethane (200 ml). The organic phase was washed with sat. Washed sodium chloride solution, dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 6: 1) to afford the desired product (3.96 g).
1H NMR (300 MHz, CDCl3): δ: 8.70 (m, IH), 7.05 (m, IH), 4.36 (q, 2H), 1.35 (t, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 8.70 (m, IH), 7:05 (m, IH), 4:36 (q, 2H), 1:35 (t, 3H)
3c) 2-Fluor-4-methoxycarbonylmethylsulfanyl-5-nitro- benzoesäureethylester3c) 2-fluoro-4-methoxycarbonylmethylsulfanyl-5-nitrobenzoate
Nitrobenzoesäure (3b) (3.96 g) wurde in Dichlormethan (75 ml) gelöst, mit Triethylamin (2.8 ml) versetzt und auf 00C abgekühlt. Nach der Zugabe von Methylthioglycolat (1.5 ml) wurde bei 0-50C 3.5 Stunden gerührt und die Lösung über Nacht im Kühlschrank aufbewahrt. Die Lösung wurde eingeengt und der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 6:1) gereinigt und lieferte das gewünschte Produkt (3.86 g) .Nitrobenzoic acid (3b) (3.96 g) was dissolved in dichloromethane (75 ml), added with triethylamine (2.8 ml) and cooled to 0 ° C. After the addition of methyl thioglycolate (1.5 ml) was stirred at 0-5 0 C 3.5 hours and the solution stored overnight in the refrigerator. The solution was concentrated and the residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 6: 1) to give the desired product (3.86 g).
1H NMR (300 MHz, CDCl3): δ: 8.82 (d, IH), 7.19 (d, IH), 4.35 (q, 2H), 3.72 (s, 3H), 3.70 (s, 2H), 1.35 (t, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 8.82 (d, IH), 7.19 (d, IH), 4:35 (q, 2H), 3.72 (s, 3H), 3.70 (s, 2H), 1:35 ( t, 3H)
3d) 7-Fluor-3-oxo-3,4-dihydro-2H-benzo[l,4]thiazin-6- carbonsäureethylester3d) 7-Fluoro-3-oxo-3,4-dihydro-2H-benzo [l, 4] thiazine-6-carboxylic acid ethyl ester
Verbindung (3c) (3.86 g) wurde in Essigsäure (142 ml) gelöst, mit Eisenpulver (6.8 g) versetzt und bei 6O0C 4 Stunden gerührt. Die Reaktionsmischung wurde durch Kieselgel filtriert, mit Methanol nachgewaschen und das Filtrat partiell eingeengt. Wasser und Essigester wurden zugegeben und die Phasen getrennt. Die wässrige Phase wurde
nochmals mit Essigester extrahiert. Die vereinigten organischen Phasen wurden 4 x mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt und lieferten das gewünschte Produkt (3.11 g) .Compound (3c) (3.86 g) was dissolved in acetic acid (142 ml), added with iron powder (6.8 g) and stirred for 4 hours at 6O 0 C. The reaction mixture was filtered through silica gel, washed with methanol and the filtrate partially concentrated. Water and ethyl acetate were added and the phases separated. The aqueous phase became extracted again with ethyl acetate. The combined organic phases were washed four times with water, dried over magnesium sulfate, filtered and concentrated to afford the desired product (3.11 g).
1H NMR (300 MHz, d6-DMSO) : δ: 10.71 (s, IH), 7.50-7.39 (m, 2H), 4.30 (q, 2H), 3.56 (s, 2H), 1.30 (t, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.71 (s, IH), 7.50-7.39 (m, 2H), 4.30 (q, 2H), 3.56 (s, 2H), 1.30 (t, 3H )
3e) 7-Fluor-3-oxo-3,4-dihydro-2H-benzo[l,4] thiazin-6- carbonsäure3e) 7-Fluoro-3-oxo-3,4-dihydro-2H-benzo [l, 4] thiazine-6-carboxylic acid
Thiazin (3d) (3.11 g) wurde in THF (37 ml) suspendiert, mit IN Natronlauge (37 ml) versetzt und bei Raumtemperatur über Nacht gerührt. Die Lösung wurde mit IN Salzsäure auf pH 3 angesäuert und partiell eingeengt. Der entstandene Niederschlag wurde abfiltriert und mit Wasser gewaschen.Thiazine (3d) (3.11g) was suspended in THF (37ml), added with 1N sodium hydroxide solution (37ml) and stirred at room temperature overnight. The solution was acidified to pH 3 with 1N hydrochloric acid and partially concentrated. The resulting precipitate was filtered off and washed with water.
Der Feststoff wurde bei vermindertem Druck (100 mbar, 400C) getrocknet und lieferte das gewünschte Produkt (2.49 g) .The solid was dried at reduced pressure (100 mbar, 40 ° C.) to give the desired product (2.49 g).
1H NMR (300 MHz, dδ-DMSO) : δ: 13.26 (bs, IH), 10.72 (s, IH), 7.48 (d, IH), 7.38 (d, IH), 3.57 (s, 2H) 1 H NMR (300 MHz, d δ -DMSO): δ: 13.26 (bs, IH), 10.72 (s, IH), 7.48 (d, IH), 7.38 (d, IH), 3.57 (s, 2H)
3f) 7-Fluor-6-hydroxymethyl-4H-benzo[l,4] thiazin-3-on3f) 7-Fluoro-6-hydroxymethyl-4H-benzo [l, 4] thiazine-3-one
Thiazincarbonsäure (3e) (2.49 g) wurde in trockenem THF (80 ml) suspendiert, auf 00C abgekühlt, mit Triethylamin (1.8 ml) und Isobutylchloroformat (1.6 ml) versetzt und 30Thiazincarbonsäure (3e) (2:49 g) was suspended in dry THF (80 ml), cooled to 0 0 C, treated with triethylamine (1.8 ml) and isobutyl chloroformate (1.6 ml) and 30
Minuten gerührt. Die Suspension wurde schnell durch Celit in eine eiskalte Lösung von Natriumborhydrid (1.24 g) in Wasser (24 ml) filtriert. Nach 45 Minuten wurde die Lösung mit IN Salzsäure auf pH 1 gebracht und mit Essigester extrahiert. Die organische Phase wurde mit ges .Stirred for minutes. The suspension was quickly filtered through celite into an ice-cold solution of sodium borohydride (1.24 g) in water (24 ml). After 45 minutes, the solution was brought to pH 1 with 1N hydrochloric acid and extracted with ethyl acetate. The organic phase was washed with sat.
Natriumchloridlösung gewaschen, über Magnesiumsulfat
getrocknet, filtriert und eingeengt und lieferte das gewünschte Produkt (2.29 g) .Washed with sodium chloride solution, over magnesium sulfate dried, filtered and concentrated to afford the desired product (2.29 g).
1H NMR (300 MHz, d6-DMSO) : δ: 10.61 (s, IH), 7.19 (d, IH), 7.10 (d, IH), 5.33 (m, IH), 4.47 (d, 2H), 3.26 (s, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.61 (s, IH), 7.19 (d, IH), 7.10 (d, IH), 5.33 (m, IH), 4.47 (d, 2H), 3.26 (s, 2H)
3g) 7-Fluor-3-oxo-3,4-dihydro-2H-benzo[l,4]thiazin-6- carbaldehyd3g) 7-Fluoro-3-oxo-3,4-dihydro-2H-benzo [l, 4] thiazine-6-carbaldehyde
Thiazinon (3f) (1.63 g) wurde in Dichlormethan/THF 1:1 (138 ml) gelöst, mit Mangandioxid (6.63 g) versetzt und 2 Tage bei Raumtemperatur gerührt. Mehr Mangandioxid (3.32 g) wurde hinzugefügt und weitere 3 Tage gerührt. Die Suspension wurde durch Celit filtriert und mit THF nachgewaschen. Das FiItrat wurde eingeengt und der Rückstand wurde mittels Flash-Chromatographie (Kieselgel,Thiazinone (3f) (1.63 g) was dissolved in dichloromethane / THF 1: 1 (138 ml), manganese dioxide (6.63 g) added and stirred for 2 days at room temperature. More manganese dioxide (3.32 g) was added and stirred for a further 3 days. The suspension was filtered through celite and washed with THF. The filtrate was concentrated and the residue was purified by flash chromatography (silica gel, silica gel).
Hexan/Essigester 7:3) gereinigt und lieferte das gewünschte Produkt (765 mg) .Hexane / ethyl acetate 7: 3) to afford the desired product (765 mg).
1H NMR (300 MHz, d6-DMSO) : δ: 10.80 (s, IH), 10.14 (s, IH), 7.51 (d, IH), 7.35 (d, IH), 3.60 (s, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.80 (s, IH), 10.14 (s, IH), 7.51 (d, IH), 7.35 (d, IH), 3.60 (s, 2H)
3h) Titelverbindung3h) Title compound
Die Verbindung wurde wie in Beispiel Ik aus Aldehyd (3g) in 93% Ausbeute hergestellt.The compound was prepared as in Example Ik from aldehyde (3g) in 93% yield.
1H NMR (300 MHz, d6-DMSO) : δ: 10.53 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m, IH), 7.18 (d, IH), 7.09 (d, IH), 5.49-5.38 (m, IH), 5.33-5.21 (m, IH), 3.95 (s, 3H), 3.69 (s, 2H), 3.45 (s, 2H), 3.05-2.90 (m, 2H), 2.65-2.55 (m, 2H), 2.45-2.29 (m, IH), 2.23-2.03 (m, 2H), 1.88-1.74 (m, 2H), 1.42-1.16 (m, 3H)
Beispiel 4: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl)- ethyl] -piperidin-4-ylamino}-methyl) -4H-benzo[l,4] thiazin-3- on (Enantiomer 2) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.53 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m , IH), 7.18 (d, IH), 7.09 (d, IH), 5.49-5.38 (m, IH), 5.33-5.21 (m, IH), 3.95 (s, 3H), 3.69 (s, 2H), 3.45 (s, 2H), 3.05-2.90 (m, 2H), 2.65-2.55 (m, 2H), 2.45-2.29 (m, IH), 2.23-2.03 (m, 2H), 1.88-1.74 (m, 2H ), 1.42-1.16 (m, 3H) Example 4: 6- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [l, 4] thiazine -3- on (enantiomer 2)
4a) (4-Formyl-2-nitro-phenylsulfanyl) -essigsäuremethylester4a) (4-formyl-2-nitro-phenylsulfanyl) -acetic acid methyl ester
4-Chlor-3-nitrobenzaldehyd (10 g) wurde in DMF (100 ml) gelöst, Natriumhydrid (2.35 g) hinzugegeben und für 15 Minuten bei Raumtemperatur gerührt . Dann wurde Methylthioglycolat (3.45 ml) zugetropft und 5 Stunden bei Raumtemperatur gerührt. Die Reaktionsmischung wurde mit Wasser verdünnt und mit Essigester extrahiert. Die vereinigten organischen Phasen wurden 2 x mit Wasser gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash- Chromatographie (Kieselgel, Hexan/Essigester 2:1) gereinigt und lieferte das gewünschte Produkt (5.5 g) .4-Chloro-3-nitrobenzaldehyde (10 g) was dissolved in DMF (100 ml), sodium hydride (2.35 g) added and stirred for 15 minutes at room temperature. Then methyl thioglycolate (3.45 ml) was added dropwise and stirred at room temperature for 5 hours. The reaction mixture was diluted with water and extracted with ethyl acetate. The combined organic phases were washed twice with water, dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, hexane / ethyl acetate 2: 1) to afford the desired product (5.5 g).
1H NMR (300 MHz, CDCl3): δ: 10.05 (s, IH), 8.75 (d, IH), 8.09 (dd, IH), 7.68 (d, IH), 3.84 (s, 2H), 3.81 (s, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 5.10 (s, IH), 8.75 (d, IH), 8:09 (dd, IH), 7.68 (d, IH), 3.84 (s, 2H), 3.81 ( s, 3H)
4b) 3-Oxo-3 , 4-dihydro-2H-benzo[l, 4] thiazin-6-carbaldehyd Verbindung (4a) (5.5 g) wurde in Essigsäure (115 ml) gelöst und Eisenpulver (8.42 g) hinzugegeben. Die4b) 3-Oxo-3,4-dihydro-2H-benzo [l, 4] thiazine-6-carbaldehyde Compound (4a) (5.5 g) was dissolved in acetic acid (115 ml) and iron powder (8.42 g) added. The
Reaktionsmischung wurde 15 Minuten bei Raumtemperatur, dann 3 Stunden bei 500C gerührt und durch Decalit filtriert. Der Filterkuchen wurde mit Methanol gewaschen und das Filtrat
eingeengt. Der Rückstand wurde in ges . Natriumhydrogen- carbonatlösung gelöst und mit Essigester extrahiert. Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 2:1) gereinigt und lieferte das gewünschte Produkt (1 g) .Reaction mixture was 15 minutes at room temperature, then stirred for 3 hours at 50 0 C and filtered through Decalite. The filter cake was washed with methanol and the filtrate concentrated. The residue was dissolved in sat. Dissolved sodium bicarbonate solution and extracted with ethyl acetate. The combined organic phases were dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, hexane / ethyl acetate 2: 1) to afford the desired product (1 g).
1H NMR (300 MHz, CDCl3): 5: 10.18 (bs, IH), 9.85 (S, IH), 7.45-7.34 (m, 3H), 3.39 (s, 2H) 1 H NMR (300 MHz, CDCl3) 5: 10.18 (bs, IH), 9.85 (S, IH), 7:45 to 7:34 (m, 3H), 3:39 (s, 2H)
4c) Titelverbindung4c) Title compound
Die Verbindung wurde wie in Beispiel Ik aus Aldehyd (4b) inThe compound was prepared as in Example Ik from aldehyde (4b) in
80% Ausbeute hergestellt.80% yield produced.
1H NMR (300 MHz, d6-DMSO) : δ: 10.49 (s, IH), 8.65 (d, IH) , 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m, IH), 7.23 (d, IH), 6.97-6.91 (m, 2H), 5.46-5.36 (m, IH), 5.28-5.20 (m, IH), 3.95 (s, 3H), 3.62 (s, 2H), 3.43 (s, 2H), 3.04- 2.98 (m, 2H), 2.65-2.55 (m, 2H), 2.43-2.28 (m, IH), 2.20- 2.00 (m, 2H), 1.85-1.71 (m, 2H), 1.40-1.16 (m, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.49 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m , IH), 7.23 (d, IH), 6.97-6.91 (m, 2H), 5.46-5.36 (m, IH), 5.28-5.20 (m, IH), 3.95 (s, 3H), 3.62 (s, 2H ), 3.43 (s, 2H), 3.04-2.98 (m, 2H), 2.65-2.55 (m, 2H), 2.43-2.28 (m, IH), 2.20-2.00 (m, 2H), 1.85-1.71 (m , 2H), 1.40-1.16 (m, 3H)
Beispiel 5: 2- {4- [ (2, 3-Dihydro- [l,4]dioxino[2, 3-c]pyridin- 7-ylmethyl) -amino] -piperidin-l-yl}-l- (3-methoxy-chinolin-5- yl)-ethanol (Enantiomer 2)Example 5: 2- {4- [(2,3-Dihydro- [l, 4] dioxino [2,3-c] pyridin-7-ylmethyl) -amino] -piperidin-1-yl} -1- (3 -methoxy-quinolin-5-yl) -ethanol (enantiomer 2)
5a) 5-Benzyloxy-2-hydroxymethyl-pyran-4-on 5a) 5-Benzyloxy-2-hydroxymethyl-pyran-4-one
Zu einer Lösung von Kojicsäure (10.36 g) in warmem Methanol (135 ml) wurde portionsweise Natriummethylat (4.3 g) gegeben und dann Benzylchlorid (9.6 ml) zugetropft. Das Reaktionsgemisch wurde über Nacht auf 700C erhitzt, abgekühlt und auf Eiswasser gegossen. Der Feststoff wurde abfiltriert und getrocknet und lieferte das gewünschte Produkt (6.43 g) .To a solution of kojic acid (10.36 g) in warm methanol (135 ml) was added portionwise sodium methylate (4.3 g) and then benzyl chloride (9.6 ml) was added dropwise. The reaction mixture was heated at 70 ° C. overnight, cooled and poured onto ice-water. The solid was filtered off and dried, yielding the desired product (6.43 g).
1H NMR (300 MHz, d6-DMSO) : δ: 8.18 (s, IH), 7.44-7.32 (m, 5H), 6.33 (s, IH), 5.71-5.66 (m, IH), 4.95 (s, 2H), 4.30 (d, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.18 (s, IH), 7.44-7.32 (m, 5H), 6.33 (s, IH), 5.71-5.66 (m, IH), 4.95 (s , 2H), 4.30 (d, 2H)
5b) 5-Benzyloxy-2-hydroxymethyl-lH-pyridin-4-on Eine Suspension des Pyranons (5a) (6.43 g) in konz .5b) 5-Benzyloxy-2-hydroxymethyl-1H-pyridin-4-one A suspension of the pyranone (5a) (6.43 g) in conc.
Ammoniak (67 ml) und Ethanol (14 ml) wurde über Nacht unter Rückfluss erhitzt. Die Lösung wurde abgekühlt, der Feststoff abfiltriert und getrocknet und lieferte das gewünschte Produkt (5.1 g) .Ammonia (67 ml) and ethanol (14 ml) were refluxed overnight. The solution was cooled, the solid filtered off and dried to afford the desired product (5.1 g).
1H NMR (300 MHz, de-DMSO) : δ: 11.17 (bs, IH), 7.48-7.29 (m, 5H), 6.14 (bs, IH), 5.59 (bs, IH), 5.02 (s, 2H), 4.34 (s, 2H) 1 H NMR (300 MHz, de-DMSO): δ: 11.17 (bs, IH), 7.48-7.29 (m, 5H), 6.14 (bs, IH), 5.59 (bs, IH), 5.02 (s, 2H) , 4.34 (s, 2H)
5c) (2,3-Dihydro-[l,4]dioxino[2,3-c]pyridin-7-yl)-methanol5c) (2,3-dihydro- [l, 4] dioxino [2,3-c] pyridin-7-yl) -methanol
Zu einer Lösung des Pyridinons (5b) (12.6 g) in Wasser (1.4 1) wurde Natriumhydroxid (4.36 g) und 10% Palladium auf Kohle (6.7 g) gegeben und für 2 Tage hydriert. Der Katalysator wurde abfiltriert und die Lösung lyophilisiert. Der Rückstand wurde in DMF (106 ml) gelöst, mitTo a solution of the pyridinone (5b) (12.6 g) in water (1.4 L) was added sodium hydroxide (4.36 g) and 10% palladium on carbon (6.7 g) and hydrogenated for 2 days. The catalyst was filtered off and the solution was lyophilized. The residue was dissolved in DMF (106 ml), washed with
Kaliumcarbonat (18.13 g) und 1, 2-Dibromethan (3.84 ml) versetzt und über Nacht auf 1000C erhitzt. Nach dem
Abkühlen wurde die Lösung eingeengt, der Rückstand in Wasser aufgenommen und mehrfach mit Essigester extrahiert. Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1) gereinigt und lieferte das gewünschte Produkt (1.49 g) .Potassium carbonate (18.13 g) and 1, 2-dibromoethane (3.84 ml) and heated to 100 0 C overnight. After this Cooling, the solution was concentrated, the residue taken up in water and extracted several times with ethyl acetate. The combined organic phases were dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1) to afford the desired product (1.49 g).
1H NMR (300 MHz, d6-DMSO) : δ: 8.00 (S, IH) , 6.91 (s, IH), 5.31-5.26 (m, IH), 4.41 (d, 2H), 4.36-4.33 (m, 2H), 4.29- 4.26 (m, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.00 (S, IH), 6.91 (s, IH), 5.31-5.26 (m, IH), 4.41 (d, 2H), 4.36-4.33 (m , 2H), 4.29-4.26 (m, 2H)
5d) 2 , 3-Dihydro- [1, 4] dioxino [2, 3-c] pyridin-7-carbaldehyd5d) 2, 3-Dihydro- [1,4] dioxino [2,3-c] pyridine-7-carbaldehyde
Zu einer Lösung von OxalylChlorid (2.2 ml) in Dichlormethan (22 ml) wurde bei -78°C tropfenweise eine Lösung von DMSO (2.2 ml) in Dichlormethan (22 ml) gegeben und 15 Minuten gerührt. Anschliessend wurde eine Lösung von Alkohol (5c) (1.49 g) in Dichlormethan (16 ml) zugegeben, 1 Stunde gerührt und dann eine Lösung von Triethylamin (8.7 ml) in Dichlormethan (11 ml) zugegeben. Nach 20 Minuten wurde auf 00C aufgewärmt und 30 Minuten gerührt. Dann wurde Wasser zugesetzt, die Phasen getrennt und die wässrige Phase 2 x mit Dichlormethan extrahiert. Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash- Chromatographie (Kieselgel, Dichlormethan/Methanol 19:1) gereinigt und lieferte das gewünschte Produkt (1.36 g) .To a solution of oxalyl chloride (2.2 ml) in dichloromethane (22 ml) was added dropwise at -78 ° C a solution of DMSO (2.2 ml) in dichloromethane (22 ml) and stirred for 15 minutes. Subsequently, a solution of alcohol (5c) (1.49 g) in dichloromethane (16 ml) was added, stirred for 1 hour and then a solution of triethylamine (8.7 ml) in dichloromethane (11 ml) was added. After 20 minutes, the mixture was warmed to 0 ° C. and stirred for 30 minutes. Then water was added, the phases were separated and the aqueous phase extracted twice with dichloromethane. The combined organic phases were dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, dichloromethane / methanol 19: 1) to afford the desired product (1.36 g).
1H NMR (300 MHz, CDCl3): δ: 9.91 (s, IH), 8.24 (s, IH), 7.45 (s, IH), 4.33 (s, 4H) 1 H NMR (300 MHz, CDCl 3): δ: 9.91 (s, IH), 8.24 (s, IH), 7:45 (s, IH), 4:33 (s, 4H)
5e) Titelverbindung
Die Verbindung wurde wie in Beispiel Ik aus Aldehyd (5d) in 78% Ausbeute hergestellt.5e) Title compound The compound was prepared as in Example Ik from aldehyde (5d) in 78% yield.
1H NMR (300 MHz, d6-DMSO) : δ: 8.65 (d, IH), 8.03 (s, IH), 7.87-7.81 (m, 2H), 7.68 (d, IH), 7.58-7.51 (m, IH), 6.96 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.65 (d, IH), 8.03 (s, IH), 7.87-7.81 (m, 2H), 7.68 (d, IH), 7.58-7.51 (m , IH), 6.96
(s, IH), 5.48-5.38 (m, IH), 5.36-5.19 (m, IH), 4.36-4.33(s, IH), 5.48-5.38 (m, IH), 5.36-5.19 (m, IH), 4.36-4.33
(m, 2H), 4.29-4.27 (m, 2H), 3.95 (s, 3H), 3.73 (s, 2H),(m, 2H), 4.29-4.27 (m, 2H), 3.95 (s, 3H), 3.73 (s, 2H),
3.04-2.90 (m, IH), 2.78-2.55 (m, 2H), 2.46-2.34 (m, IH),3.04-2.90 (m, IH), 2.78-2.55 (m, 2H), 2.46-2.34 (m, IH),
2.21-2.03 (m, 2H), 1.89-1.74 (m, 2H), 1.43-1.11 (m, 4H)2.21-2.03 (m, 2H), 1.89-1.74 (m, 2H), 1.43-1.11 (m, 4H)
Beispiel 6: 2-{4- [ (2,3-Dihydro-benzo[l,4]dioxin-6- ylmethyl) -amino] -piperidin-l-yl}-l- (3-methoxy-chinolin-5- yl)-ethanol (Enantiomer 2)Example 6: 2- {4- [(2,3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) amino] -piperidin-1-yl} -1- (3-methoxy-quinoline-5-) yl) -ethanol (enantiomer 2)
Die Verbindung wurde wie in Beispiel Ik aus (2 , 3-Dihydro- benzo [1,4] dioxin-6-carbaldehyd hergestellt .The compound was prepared as in Example Ik from (2,3-dihydrobenzo [1,4] dioxin-6-carbaldehyde.
MS (EI) : m/z: 450 [M+H]+ MS (EI): m / z: 450 [M + H] +
Beispiel 7: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-ylamino>-methyl) -4H-benzo[l,4]oxazin-3- on (Enantiomer 1)
Example 7: 6- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino] -methyl) -4H-benzo [1,4] oxazine -3- on (enantiomer 1)
7a) 3-Methoxy-5-oxiranyl-chinolin (Enantiomer 1)7a) 3-methoxy-5-oxiranyl-quinoline (enantiomer 1)
Die Verbindung wurde wie in Beispiel Id bis If beschrieben synthetisiert. Statt AD mix alpha wurde AD mix beta zur Herstellung des Diols (Id) verwendet.The compound was synthesized as described in Example Id to If. Instead of AD mix alpha, AD mix beta was used to prepare the diol (Id).
7b) {1- [2-Hydroxy-2-(3-methoxy-chinolin-5-yl)-ethyl]- piperidin-4-yl} -carbaminsäure-tert-butylester (Enantiomer 1)7b) tert-butyl {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-yl} -carbamate (enantiomer 1)
Die Titelverbindung wurde wie in Beispiel Ig aus Epoxid (7a) in 56% Ausbeute hergestellt.The title compound was prepared as in Example Ig from epoxide (7a) in 56% yield.
1H NMR (300 MHz, CDCl3): δ: 8.56 (d, IH), 7.92 (m, IH) , 7.64 (m, IH), 7.48-7.43 (m, IH) , 5.72 (bs, IH), 4.51 (m, IH), 3.85 (s, 3H), 3.60-3.46 (m, IH), 3.29-3.26 (m, 2H), 2.84- 2.73 (m, 2H), 2.67-2.40 (m, 2H), 2.09-1.95 (m, 2H), 1.84- 1.64 (m, 2H), 1.38 (s, 9H) 1 H NMR (300 MHz, CDCl 3): δ: 8:56 (d, IH), 7.92 (m, IH), 7.64 (m, IH), 7:48 to 7:43 (m, IH), 5.72 (bs, IH), 4.51 (m, IH), 3.85 (s, 3H), 3.60-3.46 (m, IH), 3.29-3.26 (m, 2H), 2.84-2.73 (m, 2H), 2.67-2.40 (m, 2H), 2.09-1.95 (m, 2H), 1.84- 1.64 (m, 2H), 1.38 (s, 9H)
7c) 2-(4-Amino-piperidin-l-yl)-l-(3-methoxy-chinolin-5-yl)- ethanol (Enantiomer 1)7c) 2- (4-amino-piperidin-1-yl) -1- (3-methoxy-quinolin-5-yl) -ethanol (enantiomer 1)
Die Verbindung wurde wie in Beispiel Ih aus Boc-Amin (7b) in 63% Ausbeute hergestellt.The compound was prepared from Boc-amine (7b) in 63% yield as in Example Ih.
1H NMR (300 MHz, d6-DMSO) : δ: 8.66-8.63 (m, IH), 7.87-7.82 (m, 2H), 7.67 (m, IH), 7.58-7.51 (m, IH), 5.43-5.39 (m, IH), 5.26-5.23 (m, IH), 3.95 (s, 3H), 2.99-2.85 (m, 2H), 2.62-2.55 (m, IH), 2.19-1.99 (m, 2H), 1.72-1.57 (m, 2H)
7d) Titelverbindung 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.66-8.63 (m, IH), 7.87-7.82 (m, 2H), 7.67 (m, IH), 7.58-7.51 (m, IH), 5.43 -5.39 (m, IH), 5.26-5.23 (m, IH), 3.95 (s, 3H), 2.99-2.85 (m, 2H), 2.62-2.55 (m, IH), 2.19-1.99 (m, 2H) , 1.72-1.57 (m, 2H) 7d) Title compound
Die Verbindung wurde wie in Beispiel Ik aus Amin (7c) und Aldehyd (Ij) in 86% Ausbeute hergestellt.The compound was prepared as in Example Ik from amine (7c) and aldehyde (Ij) in 86% yield.
1H NMR (300 MHz, d6-DMSO) : δ: 10.78 (s, IH), 8.66 (d, IH), 7.96 (s, IH), 7.88-7.84 (m, 2H), 7.70-7.68 (m, IH), 7.59- 7.54 (m, IH), 7.00-6.91 (m, 3H), 5.75 (s, IH), 5.49-5.46 (m, IH), 4.56 (s, 2H), 3.96 (s, 3H), 2.82 (s, 2H), 3.12- 3.03 (m, 2H), 2.72-2.60 (m, 2H), 2.30-2.10 (m, 2H), 2.00- 1.85 (m, 2H), 1.58-1.36 (m, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.78 (s, IH), 8.66 (d, IH), 7.96 (s, IH), 7.88-7.84 (m, 2H), 7.70-7.68 (m , IH), 7.59-7.54 (m, IH), 7.00-6.91 (m, 3H), 5.75 (s, IH), 5.49-5.46 (m, IH), 4.56 (s, 2H), 3.96 (s, 3H ), 2.82 (s, 2H), 3.12- 3.03 (m, 2H), 2.72-2.60 (m, 2H), 2.30-2.10 (m, 2H), 2.00- 1.85 (m, 2H), 1.58-1.36 (m , 3H)
Beispiel 8: 7-Fluor-6- ( {1- [2-hydroxy-2- (3-methoxy-chinolin- 5-yl) -ethyl] -piperidin-4-ylamino}-methyl) -4H- benzo[l,4] thiazin-3-on (Enantiomer 1)Example 8: 7-Fluoro-6- ({1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [l , 4] thiazine-3-one (enantiomer 1)
Die Verbindung wurde wie in Beispiel 7d aus Aldehyd (3g) in 78% Ausbeute hergestellt.The compound was prepared from aldehyde (3g) in 78% yield as in Example 7d.
1H NMR (300 MHz, d6-DMSO) : δ: 10.53 (s, IH) , 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m, IH), 7.18 (d, IH), 7.09 (d, IH), 5.49-5.38 (m, IH), 5.33-5.21 (m, IH), 3.95 (s, 3H), 3.69 (s, 2H), 3.45 (s, 2H), 3.05-2.90 (m, 2H), 2.65-2.55 (m, 2H), 2.45-2.29 (m, IH), 2.23-2.03 (m, 2H), 1.88-1.74 (m, 2H), 1.42-1.16 (m, 3H)
Beispiel 9: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [1,4] thiazin-3■ on (Enantiomer 1) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.53 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m , IH), 7.18 (d, IH), 7.09 (d, IH), 5.49-5.38 (m, IH), 5.33-5.21 (m, IH), 3.95 (s, 3H), 3.69 (s, 2H), 3.45 (s, 2H), 3.05-2.90 (m, 2H), 2.65-2.55 (m, 2H), 2.45-2.29 (m, IH), 2.23-2.03 (m, 2H), 1.88-1.74 (m, 2H ), 1.42-1.16 (m, 3H) Example 9: 6- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [1,4] thiazine -3 ■ on (enantiomer 1)
Die Verbindung wurde wie in Beispiel 7d aus Aldehyd (4b) in 73% Ausbeute hergestellt.The compound was prepared from aldehyde (4b) in 73% yield as in Example 7d.
1H NMR (300 MHz, d6-DMSO) : δ: 10.49 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m, IH), 7.23 (d, IH), 6.97-6.91 (m, 2H), 5.46-5.36 (m, IH), 5.28-5.20 (m, IH), 3.95 (s, 3H), 3.62 (s, 2H), 3.43 (s, 2H), 3.04- 2.98 (m, 2H), 2.65-2.55 (m, 2H), 2.43-2.28 (m, IH), 2.20- 2.00 (m, 2H), 1.85-1.71 (m, 2H), 1.40-1.16 (m, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.49 (s, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.68 (d, IH), 7.58-7.53 (m , IH), 7.23 (d, IH), 6.97-6.91 (m, 2H), 5.46-5.36 (m, IH), 5.28-5.20 (m, IH), 3.95 (s, 3H), 3.62 (s, 2H ), 3.43 (s, 2H), 3.04-2.98 (m, 2H), 2.65-2.55 (m, 2H), 2.43-2.28 (m, IH), 2.20-2.00 (m, 2H), 1.85-1.71 (m , 2H), 1.40-1.16 (m, 3H)
Beispiel 10: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ethyl] -piperidin-4-ylamino} -methyl) -4H-pyrido [3,2- b] [1,4] thiazin-3-on (Enantiomer 1)Example 10: 6- ({1- [2-Hydroxy-2- (3-methoxyquinolin-5-yl) ethyl] piperidin-4-ylamino} methyl) -4 H -pyrido [3,2-b] [1,4] thiazine-3-one (enantiomer 1)
Die Verbindung wurde wie in Beispiel 7d aus Aldehyd (2h) in 83% Ausbeute hergestellt. The compound was prepared from aldehyde (2h) in 83% yield as in Example 7d.
1H NMR (300 MHz, d6-DMSO) : δ: 10.85 (S, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.74-7.67 (m, 2H), 7.58-7.51 (m, IH), 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.85 (S, IH), 8.65 (d, IH), 7.87-7.82 (m, 2H), 7.74-7.67 (m, 2H), 7.58-7.51 (m, IH),
7.11-7.05 (m, IH), 5.50-5.36 (m, IH), 5.30-5.19 (m, IH),7.11-7.05 (m, IH), 5.50-5.36 (m, IH), 5.30-5.19 (m, IH),
3.95 (m, IH), 3.72 (s, 2H), 3.53 (s, 2H), 3.02-2.87 (m,3.95 (m, IH), 3.72 (s, 2H), 3.53 (s, 2H), 3.02-2.87 (m,
2H), 2.65-2.54 (m, 2H), 2.44-2.32 (m, IH), 2.21-2.02 (m,2H), 2.65-2.54 (m, 2H), 2.44-2.32 (m, IH), 2.21-2.02 (m,
2H), 1.86-1.70 (m, 3H), 1.42-1.13 (m, 3H)2H), 1.86-1.70 (m, 3H), 1.42-1.13 (m, 3H)
Beispiel 11 : 2- {4- [ (2 , 3-Dihydro- [ l, 4] dioxino [2 , 3-c] pyridin- 7 -ylmethyl ) -axnino] -piperidin-l-yl} -l- (3-methoxy-chinolin-5- yl ) -ethanol (Enantiomer 1)Example 11: 2- {4- [(2,3-Dihydro- [l, 4] dioxino [2,3-c] pyridine-7-ylmethyl) -axnino] -piperidin-1-yl} -1- (3 -methoxy-quinolin-5-yl) -ethanol (enantiomer 1)
Die Verbindung wurde wie in Beispiel 7d aus Aldehyd (5d) in 78% Ausbeute hergestellt.The compound was prepared from aldehyde (5d) in 78% yield as in Example 7d.
1H NMR (300 MHz, d6-DMSO) : δ: 8.65 (d, IH), 8.03 (s, IH), 7.87-7.81 (m, 2H), 7.68 (d, IH), 7.58-7.51 (m, IH), 6.96 (s, IH), 5.48-5.38 (m, IH), 5.36-5.19 (m, IH), 4.36-4.33 (m, 2H), 4.29-4.27 (m, 2H), 3.95 (s, 3H), 3.73 (s, 2H), 3.04-2.90 (m, IH), 2.78-2.55 (m, 2H), 2.46-2.34 (m, IH), 2.21-2.03 (m, 2H), 1.89-1.74 (m, 2H), 1.43-1.11 (m, 4H)
Beispiel 12 : 2- {4- [ ( 2 , 3 -Dihydro-benzo [ l, 4 ] dioxin-6- ylmethyl ) -amino] -piperidin-l-yl} -l- O-methoxy-chinolin-S- yl ) -ethanol (Enantiomer 1 ) 1 H NMR (300 MHz, d 6 -DMSO): δ: 8.65 (d, IH), 8.03 (s, IH), 7.87-7.81 (m, 2H), 7.68 (d, IH), 7.58-7.51 (m , IH), 6.96 (s, IH), 5.48-5.38 (m, IH), 5.36-5.19 (m, IH), 4.36-4.33 (m, 2H), 4.29-4.27 (m, 2H), 3.95 (s , 3H), 3.73 (s, 2H), 3.04-2.90 (m, IH), 2.78-2.55 (m, 2H), 2.46-2.34 (m, IH), 2.21-2.03 (m, 2H), 1.89-1.74 (m, 2H), 1.43-1.11 (m, 4H) Example 12: 2- {4- [(2,3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -piperidin-1-yl} -1-O-methoxy-quinolin-S-yl ) -ethanol (enantiomer 1)
Die Verbindung wurde wie in Beispiel 7d aus 2,3-Dihydro- benzo [1,4] dioxin-6-carbaldehyd hergestellt .The compound was prepared as in Example 7d from 2,3-dihydro-benzo [1,4] dioxin-6-carbaldehyde.
MS (EI): m/z: 450 [M+H] + MS (EI): m / z: 450 [M + H] +
Beispiel 13: 2-{l- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ethyl] -piperidin-4-ylamino}-N-pyridin-2-yl-acetamidExample 13: 2- {1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) ethyl] piperidin-4-ylamino} -N-pyridin-2-yl-acetamide
13a) 2-Chloro-N-pyridin-2-yl-acetaπιid13a) 2-chloro-N-pyridin-2-yl-acetaπιid
Chloracetylchlorid (1.8 ml) wurde zu einer eisgekühlten Lösung von 2-Aminopyridin (1.88 g) in THF/Pyridin (20 ml, 1:1) zugetropft. Nach 3 Stunden Rühren bei Raumtemperatur wurde die Lösung in Wasser gegossen und mit Essigester extrahiert. Die vereinigten organischen Phasen wurde über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der
Rückstand wurde aus Essigester/Ether umkristallisiert und lief erte das gewünschte Produkt (3.4 g) .Chloroacetyl chloride (1.8 ml) was added dropwise to an ice-cooled solution of 2-aminopyridine (1.88 g) in THF / pyridine (20 ml, 1: 1). After stirring for 3 hours at room temperature, the solution was poured into water and extracted with ethyl acetate. The combined organic phases were dried over magnesium sulfate, filtered and concentrated. Of the Residue was recrystallized from ethyl acetate / ether to yield the desired product (3.4 g).
MS (EI) : m/z: 171 [M+H]+ MS (EI): m / z: 171 [M + H] +
13b) Titelverbindung13b) Title compound
Zu einer Lösung von Amin (7c) (0.05 g) in DMF (1 ml) wurde Chlorid (13a) (0.034 g) und Natriumcarbonat (0.05 g) gegeben und für 2 Stunden bei 600C gerührt. Nach dem Einengen wurde das Rohprodukt mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1) gereinigt und lieferte das gewünschte Produkt.To a solution of amine (7c) (0.05 g) in DMF (1 ml) chloride (13a) (0.034 g) and sodium carbonate (0.05 g) was added and stirred for 2 hours at 60 0 C. After concentration, the crude product was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1) to afford the desired product.
MS (EI) : m/z: 436 [M+H]+ MS (EI): m / z: 436 [M + H] +
Beispiel 14: 2- {4- [ (2,3-Dihydro-benzo[l,4]dioxin-6- ylmethyl) -amino] -piperidin-l-yl}-l- (3-methoxy-chinolin-5- yl ) -ethanol (Racemat)Example 14: 2- {4- [(2,3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -piperidin-1-yl} -1- (3-methoxy-quinoline-5-) yl) ethanol (racemate)
14a) S-Methoxy-chinolin-S-carbaldehyd14a) S-methoxy-quinoline-S-carbaldehyde
Zu einer Lösung von Bromid (Ib) (2.68 g) in Ether (37 ml) und THF (37 ml) wurde bei -78°C n-Butyllithium (9.3 ml,To a solution of bromide (Ib) (2.68g) in ether (37ml) and THF (37ml) at -78 ° C was added n-butyllithium (9.3ml,
2.5M in Hexan) gegeben, 30 Minuten gerührt und mit DMF (5 ml) gequencht. Nach 15 Minuten wurde Ethanol (8 ml) und Ammoniumchloridlösung (50 ml) zugegeben und auf Raumtemperatur erwärmt. Die wässrige Phase wurde mit
Essigester extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 2:1, 1:2) gereinigt und lieferte das gewünschte Produkt (1.06 g) .2.5M in hexane), stirred for 30 minutes and quenched with DMF (5 mL). After 15 minutes, ethanol (8 ml) and ammonium chloride solution (50 ml) were added and warmed to room temperature. The aqueous phase was washed with Extracted vinegar. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 2: 1, 1: 2) to afford the desired product (1.06 g).
MS (EI): m/z: 188 [M+H]+ MS (EI): m / z: 188 [M + H] +
14b) 3-Methoxy-5-oxiranyl-chinolin14b) 3-methoxy-5-oxiranyl-quinoline
Zu einer Lösung von Aldehyd (14a) (1.06 g) in Acetonitril (17.6 ml) wurden 9 Tropfen Wasser, Trimethylsulfoniumiodid (1.19 g) und Kaliumhydroxid (2.25 g) gegeben und für 20 Minuten auf 600C erhitzt. Nach dem Abkühlen wurde die Lösung filtriert, das Filtrat mit Wasser verdünnt (10 ml) und eingeengt. Der Rückstand wurde mit Essigester extrahiert und die vereinigten organischen Phasen eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Hexan/Essigester 2:1, 1:1) gereinigt und lieferte das gewünschte Produkt (1 g) .To a solution of aldehyde (14a) (1.06g) in acetonitrile (17.6ml) was added 9 drops of water, trimethylsulfonium iodide (1.19g) and potassium hydroxide (2.25g) and heated to 60 ° C for 20 minutes. After cooling, the solution was filtered, the filtrate diluted with water (10 ml) and concentrated. The residue was extracted with ethyl acetate and the combined organic phases were concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 2: 1, 1: 1) to afford the desired product (1 g).
1H NMR (300 MHz, CDCl3): δ: 8.64 (d, IH) , 7.94 (dd, IH), 7.59 (d, IH), 7.48-7.39 (m, 2H), 4.30 (m, IH), 3.91 (s, 3H), 3.22 (dd, IH), 2.81 (dd, IH) 1 H NMR (300 MHz, CDCl 3): δ: 8.64 (d, IH), 7.94 (dd, IH), 7:59 (d, IH), 7:48 to 7:39 (m, 2H), 4.30 (m, IH), 3.91 (s, 3H), 3.22 (dd, IH), 2.81 (dd, IH)
14c) {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) -ethyl] - piperidin-4-yl}-carbaminsäure-tert-butylester (Racemat) Die Verbindung wurde wie in Beispiel Ig aus Epoxid (14b) in 65% Ausbeute hergestellt.14c) {1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-yl} -carbamic acid tert-butyl ester (racemate) The compound was obtained as in Example Ig Epoxide (14b) prepared in 65% yield.
1H NMR (300 MHz, CDCl3): δ: 8.56 (d, IH), 7.92 (m, IH), 7.64 (m, IH), 7.48-7.43 (m, IH), 5.72 (bs, IH), 4.51 (m, IH),
3.85 (s, 3H) , 3.60-3.46 (m, IH), 3.29-3.26 (m, 2H) , 2.84- 2.73 (m, 2H) , 2.67-2.40 (m, 2H), 2.09-1.95 (m, 2H) , 1.84- 1.64 (m, 2H), 1.38 (s, 9H) 1 H NMR (300 MHz, CDCl 3): δ: 8:56 (d, IH), 7.92 (m, IH), 7.64 (m, IH), 7:48 to 7:43 (m, IH), 5.72 (bs, IH), 4.51 (m, IH), 3.85 (s, 3H), 3.60-3.46 (m, IH), 3.29-3.26 (m, 2H), 2.84-2.73 (m, 2H), 2.67-2.40 (m, 2H), 2.09-1.95 (m, 2H ), 1.84- 1.64 (m, 2H), 1.38 (s, 9H)
14d) 2- (4-Amino-piperidin-l-yl) -1- (3-methoxy-chinolin-5- yl) -ethanol (Racemat)14d) 2- (4-Amino-piperidin-1-yl) -1- (3-methoxy-quinolin-5-yl) -ethanol (racemate)
Die Verbindung wurde wie in Beispiel Ih aus Boc-Amin (14c) in 78% Ausbeute hergestellt.The compound was prepared from Boc-amine (14c) in 78% yield as in Example Ih.
MS (EI): m/z: 302 [M+H]+ MS (EI): m / z: 302 [M + H] +
14e) Titelverbindung14e) title compound
Die Titelverbindung wurde wie in Beispiel Ik aus Amin (14d) und 2, 3-Dihydro-benzo[l, 4] dioxin-6-carbaldehyd in 50% Ausbeute hergestellt.The title compound was prepared as in Example Ik from amine (14d) and 2, 3-dihydro-benzo [l, 4] dioxin-6-carbaldehyde in 50% yield.
MS (EI) : m/z: 450 [M+H]+ MS (EI): m / z: 450 [M + H] +
Beispiel 15: 2- {4- [ (Benzo[l#2, 5] thiadiazol-5-ylmethyl) - amino] -piperidin-l-yl}-l- (3-methoxy-chinolin-5-yl) -ethanol (Racemat)Example 15: 2- {4- [(Benzo [l # 2, 5] thiadiazol-5-ylmethyl) -amino] -piperidin-1-yl} -1- (3-methoxy-quinolin-5-yl) -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus Benzo[l, 2,5] thiadiazol-5-carbaldehyd hergestellt
MS (EI): m/z: 450 [M+H]+ The compound was prepared as in Example 14e from benzo [l, 2,5] thiadiazole-5-carbaldehyde MS (EI): m / z: 450 [M + H] +
Beispiel 16: 1- (3-Methoxy-chinolin-5-yl) -2-{4- [ (2-methyl- benzofuran-5-ylinethyl) -amino] -piperidin-1-yl} -ethanol (Racemat)Example 16: 1- (3-Methoxy-quinolin-5-yl) -2- {4- [(2-methyl-benzofuran-5-ylin-ethyl) -amino] -piperidin-1-yl} -ethanol (racemate)
16a) 4-Prop-2-ynyloxy-benzaldehyd16a) 4-prop-2-ynyloxy-benzaldehyde
Zu einer Suspension von 4-Hydroxybenzaldehyd (5.91 g) in Toluol (80 ml) wurde Kaliumcarbonat (87.4 g) und Propargylbromid (8 ml, 80% Lösung in Toluol) gegeben und für 7 Stunden auf 1000C erhitzt. Die Suspension wurde dann filtriert und das Filtrat eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 3:1) gereinigt und lieferte das gewünschte Produkt (5 g).To a suspension of 4-hydroxybenzaldehyde (5.91 g) in toluene (80 ml) was added potassium carbonate (87.4 g) and propargyl bromide (8 ml, 80% solution in toluene) and heated at 100 ° C. for 7 hours. The suspension was then filtered and the filtrate concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 3: 1) to afford the desired product (5 g).
MS (EI): m/z: 161 [M+H]+ MS (EI): m / z: 161 [M + H] +
16b) 2-Methyl-benzofuran-5-carbaldehyd16b) 2-methyl-benzofuran-5-carbaldehyde
PEG 300 (40 ml) wurde auf 2200C erhitzt. Eine Lösung von Propynylaldehyd (16a) (5 g) in PEG 300 (10 ml) wurde hinzugegeben und bei 2200C 90 Minuten gerührt. Nach dem Abkühlen wurde die Reaktionsmischung auf Eis (200 g) gegossen und mit Dichlormethan/Ether (1:1, 2 x 300 ml) extrahiert. Die vereinigten organischen Phasen wurden eingeengt. Der Rückstand wurde mittels Flash-
Chromatographie (Kieselgel, Hexan/Essigester 9:1) gereinigt und lieferte das gewünschte Produkt (2 g) .PEG 300 (40 ml) was heated to 220 ° C. A solution of propynyl aldehyde (16a) (5g) in PEG 300 (10ml) was added and stirred at 220 ° C for 90 minutes. After cooling, the reaction mixture was poured onto ice (200 g) and extracted with dichloromethane / ether (1: 1, 2 x 300 ml). The combined organic phases were concentrated. The residue was removed by flash Chromatography (silica gel, hexane / ethyl acetate 9: 1) and gave the desired product (2 g).
1H NMR (300 MHz, CDCl3): δ: 9.93 (S, IH), 7.91 (s, IH), 7.67 (dd, IH), 7.40 (d, IH), 6.38 (s, IH), 2.39 (s, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 9.93 (S, IH), 7.91 (s, IH), 7.67 (dd, IH), 7:40 (d, IH), 6:38 (s, IH), 2:39 ( s, 3H)
16c) Titelverbindung16c) Title compound
Die Verbindung wurde wie in Beispiel 14e aus Aldehyd (16b) hergestellt.The compound was prepared from aldehyde (16b) as in Example 14e.
MS (EI) : m/z: 446 [M+H]MS (EI): m / z: 446 [M + H]
Beispiel 17: 1- (3-Methoxy-chinolin-5-yl) -2-{4- [ (chinoxalin- 2-ylmethyl) -amino] -piperidin-l-yl}-ethanol (Racemat)Example 17: 1- (3-Methoxy-quinolin-5-yl) -2- {4- [(quinoxalin-2-ylmethyl) -amino] -piperidin-1-yl} -ethanol (racemate)
17a) Chinoxalin-2-carbaldehyd Zu einer unter Rückfluss kochenden Lösung von Selendioxid (12 g) in Dioxan (120 ml) und Wasser (5 ml) wurde tropfenweise eine Lösung von 2-Methylchinoxalin (10 g) in Dioxan (20 ml) gegeben und anschliessend 4 Stunden unter Rückfluss erhitzt. Nach dem Abkühlen wurde die Suspension durch Kieselgel filtriert und das Filtrat wurde eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 2:1) gereinigt und lieferte das gewünschte Produkt (8 g) .
MS (EI) : m/z: 159 [M+H]+ 17a) Quinoxaline-2-carbaldehyde To a refluxing solution of selenium dioxide (12 g) in dioxane (120 ml) and water (5 ml) was added dropwise a solution of 2-methylquinoxaline (10 g) in dioxane (20 ml) and then heated under reflux for 4 hours. After cooling, the suspension was filtered through silica gel and the filtrate was concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 2: 1) to afford the desired product (8 g). MS (EI): m / z: 159 [M + H] +
17b) Titelverbindung Die Verbindung wurde wie in Beispiel 14e aus Aldehyd (17a) hergestellt .17b) Title compound The compound was prepared from aldehyde (17a) as in Example 14e.
MS (EI) : m/z: 445 [M+H]+ MS (EI): m / z: 445 [M + H] +
Beispiel 18: 2- [4- ( (E) -3-Furan-2-yl-allylamino) -piperidin- 1-yl] -1- (3-methoxy-chinolin-5-yl) -ethanol (Racemat)Example 18: 2- [4- ((E) -3-Furan-2-yl-allylamino) -piperidin-1-yl] -1- (3-methoxy-quinolin-5-yl) -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus (E) -3-Furan-2- yl-propenal hergestellt.The compound was prepared as in Example 14e from (E) -3-furan-2-yl-propenal.
MS (EI) : m/z: 408 [M+H]+ MS (EI): m / z: 408 [M + H] +
Beispiel 19 : 2-{4- [ (Benzofuran-2-ylmethyl) -amino] - piperidin-l-yl}-l- (3-methoxy-chinolin-5-yl) -ethanol (Racemat)
Example 19: 2- {4- [(Benzofuran-2-ylmethyl) amino] -piperidin-1-yl} -1- (3-methoxy-quinolin-5-yl) -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus Benzofuran-2- carbaldehyd hergestellt.The compound was prepared from benzofuran-2-carbaldehyde as in Example 14e.
MS (EI): m/z: 432 [M+H]+ MS (EI): m / z: 432 [M + H] +
Beispiel 20: 1- (3-Methoxy-chinolin-5-yl) -2- [4- (2-phenoxy- ethylamino) -piperidin-1-yl] -ethanol (Racemat)Example 20: 1- (3-Methoxy-quinolin-5-yl) -2- [4- (2-phenoxy-ethylamino) -piperidin-1-yl] -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus Phenoxyacetaldehyd (nach Syn. Lett., Vol. 11, 2004, S. 2010) hergestellt.The compound was prepared as in Example 14e from phenoxyacetaldehyde (according to Syn. Lett., Vol. 11, 2004, p. 2010).
MS (EI): m/z: 422 [M+H]+ MS (EI): m / z: 422 [M + H] +
Beispiel 21: 5- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ethyl] -piperidin-4-ylamino}-methyl) -3H-benzooxazol-2-on (Racemat)
Example 21: 5- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -3H-benzooxazol-2-one (racemate)
21a) 4- [l#3]Dioxan-2-yl-2-nitro-phenol21a) 4- [l # 3] dioxan-2-yl-2-nitro-phenol
Zu einer Lösung von 4-Hydroxy-3-nitro-benzaldehyd (5.54 g) in Toluol (110 ml) wurde 1, 3-Propandiol (3.80 g) und p- Toluolsulfonsäure (0.11 g) gegeben und für 3 Stunden unter Rückfluss erhitzt. Nach dem Abkühlen wurde die Lösung mit ges . Natriumhydrogencarbonatlösung gewaschen und die wässrige Phase mit Ether rückextrahiert. Die vereinigten organischen Phasen wurden mit ges. Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt und lieferten das gewünschte Produkt (3.5 g) .To a solution of 4-hydroxy-3-nitrobenzaldehyde (5.54 g) in toluene (110 ml) was added 1,3-propanediol (3.80 g) and p-toluenesulfonic acid (0.11 g) and heated at reflux for 3 hours. After cooling, the solution was washed with sat. Washed sodium bicarbonate solution and the aqueous phase back-extracted with ether. The combined organic phases were washed with sat. Sodium chloride solution, dried over magnesium sulfate, filtered and concentrated to afford the desired product (3.5 g).
1H NMR (300 MHz, CDCl3): δ: 10.63 (s, IH), 8.26 (s, IH), 7.73 (d, IH), 7.17 (d, IH) , 5.49 (s, IH) , 4.32-4.26 (m, 2H), 4.04-3.96 (m, 2H), 1.51-1.46 (m, 2H) 1 H NMR (300 MHz, CDCl 3): δ: 10.63 (s, IH), 8.26 (s, IH), 7.73 (d, IH), 7.17 (d, IH), 5:49 (s, IH), 4.32- 4.26 (m, 2H), 4.04-3.96 (m, 2H), 1.51-1.46 (m, 2H)
21b) 2-Amino-4- [l,3]dioxan-2-yl-phenol21b) 2-Amino-4- [l, 3] dioxan-2-yl-phenol
Zu einer Lösung von Nitrophenol (21a) (2 g) in THF wurde Raney Nickel gegeben und 5 Stunden unter einer Wasserstoffatmosphäre gerührt. Die Reaktionsmischung wurde filtriert und der Filterkuchen mit Essigester gewaschen. Das Filtrat wurde eingeengt und lieferte das gewünschte Produkt (1.66 g) .To a solution of nitrophenol (21a) (2 g) in THF was added Raney Nickel and stirred for 5 hours under a hydrogen atmosphere. The reaction mixture was filtered and the filter cake was washed with ethyl acetate. The filtrate was concentrated to afford the desired product (1.66 g).
MS (EI) : m/z: 196 [M+H]MS (EI): m / z: 196 [M + H]
21c) 5- [l,3]Dioxan-2-yl-3H-benzooxazol-2-on
Zu einer Lösung von Aminophenol (21b) (1.66 g) in Dichlormethan (40 ml) wurde bei 00C Triethylamin (1.72 ml) and Triphosgen (3.33 g) gegeben und 1.5 Stunden gerührt. Die Lösung wurde eingeengt und der Rückstand mittels Flash- Chromatographie (Kieselgel, Essigester/Hexan 1:1) gereinigt und lieferte das gewünschte Produkt (1.5 g) .21c) 5- [l, 3] dioxan-2-yl-3H-benzooxazol-2-one To a solution of aminophenol (21b) (1.66g) in dichloromethane (40ml) at 0 ° C was added triethylamine (1.72ml) and triphosgene (3.33g) and stirred for 1.5 hours. The solution was concentrated and the residue purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 1) to afford the desired product (1.5 g).
MS (EI): m/z: 222 [M+H]+ MS (EI): m / z: 222 [M + H] +
2Id) 2-Oxo-2,3-dihydro-benzooxazol-5-carbaldehyd2Id) 2-oxo-2,3-dihydro-benzooxazole-5-carbaldehyde
Zu einer Lösung von Benzoxazol (21c) (1.5 g) in Methanol (20 ml) wurde 3M Salzsäure (2.5 ml) gegeben und 2 Stunden gerührt. Dann wurde die Lösung partiell eingeengt und mit Essigester extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumhydrogencarbonatlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt und lieferten das gewünschte Produkt (0.84 g) .To a solution of benzoxazole (21c) (1.5 g) in methanol (20 ml) was added 3M hydrochloric acid (2.5 ml) and stirred for 2 hours. Then, the solution was partially concentrated and extracted with ethyl acetate. The combined organic phases were washed with sat. Sodium bicarbonate solution, dried over magnesium sulfate, filtered and concentrated to afford the desired product (0.84 g).
1H NMR (300 MHz, d6-DMSO) : δ: 12.00 (bs, IH) , 9.96 (S, IH) , 7.73 (d, IH), 7.54-7.50 (m, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 12.00 (bs, IH), 9.96 (S, IH), 7.73 (d, IH), 7.54-7.50 (m, 2H)
2Ie) Titelverbindung2Ie) Title compound
Die Verbindung wurde wie in Beispiel 14e aus Aldehyd (2Id) hergestellt .The compound was prepared from aldehyde (2Id) as in Example 14e.
MS (EI) : m/z: 449 [M+H]+ MS (EI): m / z: 449 [M + H] +
Beispiel 22: 2-{4- [ (2, 3-Dihydro- [l,4]dioxino[2,3-c]pyridin- 7-ylmethyl) -amino] -piperidin-l-yl}-l-(3-methoxy-chinolin-5- yl) -ethanol (Racemat)
Example 22: 2- {4- [(2,3-Dihydro- [l, 4] dioxino [2,3-c] pyridin-7-ylmethyl) -amino] -piperidin-1-yl} -1- (3 -methoxy-quinolin-5-yl) -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus Aldehyd (5d) hergestellt.The compound was prepared from aldehyde (5d) as in Example 14e.
MS (EI) : m/z: 451 [M+H]+ MS (EI): m / z: 451 [M + H] +
Beispiel 23: 2-{4- [ (3,4-Dihydro-2H-benzo[b] [l,4]dioxepin-7- ylmethyl) -amino] -piperidin-l-yl}-l- (3-methoxy-chinolin-5- yl) -ethanol (Racemat)Example 23: 2- {4- [(3,4-Dihydro-2H-benzo [b] [l, 4] dioxepin-7-ylmethyl) -amino] -piperidin-1-yl} -1- (3-methoxy -quinolin-5-yl) -ethanol (racemate)
23a) 3,4-Dihydro-2H-benzo[b] [l,4]dioxepin-7-carbaldehyd23a) 3,4-dihydro-2H-benzo [b] [1,4] dioxepine-7-carbaldehyde
Zu einer Lösung von 3 , 4-Dihydroxybenzaldehyd (1.67 g) und Kaliumcarbonat (3.34 g) in Acetonitril (15 ml) wurde 1,3- Dibrompropan (1.36 ml) gegeben und unter Rückfluss erhitzt. Dann wurde filtriert und mit Ether nachgewaschen. Das FiItrat wurde eingeengt und der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 4:1) gereinigt und lieferte das gewünschte Produkt (1.5 g) .To a solution of 3,4-dihydroxybenzaldehyde (1.67 g) and potassium carbonate (3.34 g) in acetonitrile (15 ml) was added 1,3-dibromopropane (1.36 ml) and heated to reflux. It was then filtered and washed with ether. The filtrate was concentrated and the residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 4: 1) to afford the desired product (1.5 g).
1H NMR (300 MHz, CDCl3): δ: 9.86 (s, IH) , 7.50-7.43 (m, 2H), 7.08-7.04 (m, IH), 4.39-4.21 (m, 4H), 2.31-2.23 (m, 2H)
23b) Titelverbindung 1 H NMR (300 MHz, CDCl 3): δ: 9.86 (s, IH), 7:50 to 7:43 (m, 2H), 7:08 to 7:04 (m, IH), 4:39 to 4:21 (m, 4H), 2:31 to 2:23 (m, 2H) 23b) Title compound
Die Verbindung wurde wie in Beispiel 14e aus Aldehyd (23a) hergestellt .The compound was prepared from aldehyde (23a) as in Example 14e.
MS (EI) : m/z: 464 [M+H]+ MS (EI): m / z: 464 [M + H] +
Beispiel 24: 1- (3-Methoxy-chinolin-5-yl)-2- [4- ( (E) -3- phenyl-allylamino)-piperidin-l-yl] -ethanol (Racemat)Example 24: 1- (3-Methoxy-quinolin-5-yl) -2- [4- ((E) -3-phenyl-allylamino) -piperidin-1-yl] -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus Zimtaldehyd hergestellt.The compound was prepared from cinnamic aldehyde as in Example 14e.
MS (EI) : m/z: 418 [M+H]+ MS (EI): m / z: 418 [M + H] +
Beispiel 25 : 1- (3-Methoxy-chinolin-5-yl ) -2- {4- [ ( 1-methyl- lH-indol-2-ylmethyl) -amino] -piperidin-1-yl} -ethanol (Racemat )Example 25: 1- (3-Methoxy-quinolin-5-yl) -2- {4- [(1-methyl-1H-indol-2-ylmethyl) -amino] -piperidin-1-yl} -ethanol (racemate )
Die Verbindung wurde wie in Beispiel 14e aus 1-Methyl-lH- indol-2-carbaldehyd hergestellt. The compound was prepared as in Example 14e from 1-methyl-1H-indole-2-carbaldehyde.
MS (EI) : m/z: 445 [M+H]+ MS (EI): m / z: 445 [M + H] +
Beispiel 26: 1- (3-Methoxy-chinolin-5-yl) -2- [4- (3-phenyl- propylamino) -piperidin-1-yl] -ethanol (Racemat)Example 26: 1- (3-Methoxy-quinolin-5-yl) -2- [4- (3-phenyl-propylamino) -piperidin-1-yl] -ethanol (racemate)
Die Verbindung wurde wie in Beispiel 14e aus 3- Phenylpropionaldehyd hergestellt .The compound was prepared from 3-phenylpropionaldehyde as in Example 14e.
MS (EI) : m/z: 420 [M+H]+ MS (EI): m / z: 420 [M + H] +
Beispiel 27: 7- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ■ ethyl] -piperidin-4-ylamino}-methyl) -4H-benzo[l,4]oxazin-3- on (Racemat)Example 27: 7- ({1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) ■ ethyl] piperidin-4-ylamino} -methyl) -4H-benzo [l, 4] oxazin -3- on (racemate)
27a) (5-Formyl-2-nitro-phenoxy) -essigsäureethylester
Zu einer Lösung von 3-Hydroxy-4-nitrobenzaldehyd in DMF (100 ml) wurde Ethylchloracetat (7 ml) und Kaliumcarbonat (10 g) gegeben und 2 Stunden auf 5O0C erhitzt. Wasser wurde zu der Reaktionsmischung gegeben und mit Essigester/Ether extrahiert. Die organische Phase wurde eingeengt und der27a) (5-formyl-2-nitro-phenoxy) -acetic acid ethyl ester To a solution of 3-hydroxy-4-nitrobenzaldehyde in DMF (100 ml) was added ethyl chloroacetate (7 ml) and potassium carbonate (10 g) and heated for 2 hours at 5O 0 C. Water was added to the reaction mixture and extracted with ethyl acetate / ether. The organic phase was concentrated and the
Rückstand mittels Flash-Chromatographie (Kieselgel,Residue by flash chromatography (silica gel,
Hexan/Essigester 4:1, 3:1, 2:1, 1:1) gereinigt und lieferte das gewünschte Produkt (14.2 g) .Hexane / ethyl acetate 4: 1, 3: 1, 2: 1, 1: 1) to afford the desired product (14.2 g).
1H NMR (300 MHz, CDCl3): δ: 10.04 (s, IH), 7.98 (d, IH), 7.62 (d, IH), 7.50 (s, IH), 4.87 (s, 2H), 4.29 (q, 2H), 1.31 (t, 3H) 1 H NMR (300 MHz, CDCl 3): δ: 4.10 (s, IH), 7.98 (d, IH), 7.62 (d, IH), 7.50 (s, IH), 4.87 (s, 2H), 4.29 ( q, 2H), 1.31 (t, 3H)
27b) 7-Hydroxymethyl-4H-benzo [1,4] oxazin-3-on Eine Suspension von Nitrobenzaldehyd (27a) (7 g) in27b) 7-Hydroxymethyl-4H-benzo [1,4] oxazin-3-one A suspension of nitrobenzaldehyde (27a) (7 g) in
Essigsäure (200 ml) wurde mit Eisenpulver (15.4 g) versetzt und unter Rückfluss erhitzt. Dann wurde über Celit abfiltriert und mit Essigsäure nachgewaschen. Das FiItrat wurde eingeengt, der Rückstand mit Essigester aufgenommen und mit ges . Natriumhydrogencarbonatlösung gewaschen. Die organische Phase wurde über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 1:1) gereinigt und lieferte das gewünschte Produkt (1.5 g) .Acetic acid (200 ml) was added with iron powder (15.4 g) and heated to reflux. It was then filtered through Celite and washed with acetic acid. The filtrate was concentrated, the residue taken up in ethyl acetate and washed with sat. Washed sodium bicarbonate solution. The organic phase was dried over sodium sulfate, filtered and concentrated. The crude product was purified by flash chromatography (silica gel, hexane / ethyl acetate 1: 1) to afford the desired product (1.5 g).
1H NMR (300 MHz, d6-DMSO) : δ: 10.64 (s, IH), 6.88-6.81 (m, 3H), 5.13-5.09 (m, IH), 4.54 (s, 2H), 4.38 (d, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.64 (s, IH), 6.88-6.81 (m, 3H), 5.13-5.09 (m, IH), 4.54 (s, 2H), 4.38 (i.e. , 2H)
27c) 3-Oxo-3 ,4-dihydro-2H-benzo[l, 4] oxazin-7-carbaldehyd Eine Lösung von Alkohol (27b) (1.5 g) in THF/Dichlormethan (150 ml, 1:1) wurde mit Mangandioxid (7.3 g) versetzt und 1.5 Stunden gerührt. Dann wurde über Celit abfiltriert, mit
THF nachgewaschen und das Filtrat eingeengt. Der Rückstand wurde mit Ether behandelt, der entstandene Feststoff abfiltriert und lieferte das gewünschte Produkt (1 g) .27c) 3-Oxo-3,4-dihydro-2H-benzo [l, 4] oxazine-7-carbaldehyde A solution of alcohol (27b) (1.5 g) in THF / dichloromethane (150 ml, 1: 1) was added Manganese dioxide (7.3 g) and stirred for 1.5 hours. Then it was filtered off over Celite, with THF washed and the filtrate concentrated. The residue was treated with ether, the resulting solid filtered off to afford the desired product (1 g).
1H NMR (300 MHz, d6-DMSO) : δ: 9.83 (s, IH) , 7.54 (d, IH), 7.43 (s, IH), 7.06 (d, IH), 4.68 (s, 2H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 9.83 (s, IH), 7.54 (d, IH), 7.43 (s, IH), 7.06 (d, IH), 4.68 (s, 2H)
27d) Titelverbindung27d) title compound
Die Verbindung wurde wie in Beispiel 14e aus Aldehyd (27c) hergestellt.The compound was prepared from aldehyde (27c) as in Example 14e.
MS (EI) : m/z: 464 [M+H]+ MS (EI): m / z: 464 [M + H] +
Beispiel 28: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ■ ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [1,4] oxazin-3■ on (Racemat)Example 28: 6- ({1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) ■ ethyl] piperidin-4-ylamino} -methyl) -4H-benzo [1,4] oxazin -3 ■ on (racemate)
Die Titelverbindung wurde wie in Beispiel 14e aus Aldehyd (Ij) hergestellt.The title compound was prepared from aldehyde (Ij) as in Example 14e.
1H NMR (300 MHz, d6-DMSO) : δ: 10.78 (s, IH) , 8.66 (d, IH) , 7.96 (s, IH) , 7.88-7.84 (m, 2H) , 7.70-7.68 (m, IH) , 7.59- 7.54 (m, IH) , 7.00-6.91 (m, 3H) , 5.75 (s, IH) , 5.49-5.46 (m, IH) , 4.56 (s, 2H) , 3.96 (s, 3H) , 2.82 (s, 2H) , 3.12-
3.03 (m, 2H) , 2.72-2.60 (m, 2H) , 2.30-2.10 (m, 2H) , 2.00- 1.85 (m, 2H) , 1.58-1.36 (m, 3H) 1 H NMR (300 MHz, d 6 -DMSO): δ: 10.78 (s, IH), 8.66 (d, IH), 7.96 (s, IH), 7.88-7.84 (m, 2H), 7.70-7.68 (m , IH), 7.59-7.54 (m, IH), 7.00-6.91 (m, 3H), 5.75 (s, IH), 5.49-5.46 (m, IH), 4.56 (s, 2H), 3.96 (s, 3H ), 2.82 (s, 2H), 3.12- 3.03 (m, 2H), 2.72-2.60 (m, 2H), 2.30-2.10 (m, 2H), 2.00- 1.85 (m, 2H), 1.58-1.36 (m, 3H)
Beispiel 29: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ethyl] -piperidin-4-ylainino}-methyl) -4H- pyrido[3,2b] [l,4]oxazin-3-on (Racemat)Example 29: 6- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-yl-amino} -methyl) -4 H -pyrido [3,2b] [l , 4] oxazin-3-one (racemate)
Die TitelVerbindung wurde wie in Beispiel 14e aus 3-Oxo- 3 , 4-dihydro-2H-pyrido [3 , 2-b] [1,4] oxazin-6-carbaldehyd (wurde nach WO2006/021448 hergestellt) hergestellt.The title compound was prepared as in Example 14e from 3-oxo-3,4-dihydro-2H-pyrido [3, 2-b] [1,4] oxazine-6-carbaldehyde (prepared according to WO2006 / 021448).
MS (EI): m/z: 464 [M+H]+ MS (EI): m / z: 464 [M + H] +
Beispiel 30: l-(3-Methoxy-chinolin-5-yl)-2- [4- ( (E) -3- pyridin-2-yl-allylamino) -piperidin-1-yl] -ethanol (Racemat)Example 30: 1- (3-Methoxy-quinolin-5-yl) -2- [4- ((E) -3-pyridin-2-yl-allylamino) -piperidin-1-yl] -ethanol (racemate)
Die Titelverbindung wurde wie in Beispiel 14e aus (E) -3- Pyridin-2-yl-propenal (wurde nach WO2006/021448 hergestellt) hergestellt.
MS (EI): m/z: 419 [M+H]+ The title compound was prepared as in Example 14e from (E) -3-pyridin-2-yl-propenal (prepared according to WO2006 / 021448). MS (EI): m / z: 419 [M + H] +
Beispiel 31: 2-{4- [ (E) -3- (2,5-Difluoro-phenyl)-allylamino] piperidin-1-yl} -1- (3-methoxy-chinolin-5-yl) -ethanol (Racemat)Example 31: 2- {4- [(E) -3- (2,5-Difluoro-phenyl) -allylamino] -piperidin-1-yl} -1- (3-methoxy-quinolin-5-yl) -ethanol ( racemate)
Die TitelVerbindung wurde wie in Beispiel 14e aus (E) -3- (2,5-Difluoro-phenyl) -propenal (wurde nach WO2004/087647 hergestellt) hergestellt.The title compound was prepared as in Example 14e from (E) -3- (2,5-difluoro-phenyl) -propenal (prepared according to WO2004 / 087647).
MS (EI): m/z: 454 [M+H]+ MS (EI): m / z: 454 [M + H] +
Beispiel 32: 1- (3-Methoxy-chinolin-5-yl) -2- {4- [ (naphthalin- 2-ylmethyl) -amino] -piperidin-1-yl} -ethanolExample 32: 1- (3-Methoxy-quinolin-5-yl) -2- {4- [(naphthalen-2-ylmethyl) -amino] -piperidin-1-yl} -ethanol
Die Titelverbindung wurde wie in Beispiel 14e aus Naphthalin-2-carbaldehyd hergestellt.
MS (EI) : m/z: 442 [M+H]+ The title compound was prepared from naphthalene-2-carbaldehyde as in Example 14e. MS (EI): m / z: 442 [M + H] +
Beispiel 33: 3-Oxo-3,4-dihydro-2H-benzo[l,4]oxazin-6- carbonsäure-{l- [2-hydroxy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-yl}-amid (Racemat)Example 33: 3-Oxo-3,4-dihydro-2H-benzo [l, 4] oxazine-6-carboxylic acid {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl ] -piperidin-4-yl} -amide (racemate)
Zu einer Lösung von Amin (14d) (180 mg) in einer Mischung aus Dichlormethan (6 ml) und DMF (1 ml) wurde bei Raumtemperatur 3-Oxo-3 , 4-dihydro-2H-benzo [1,4] oxazin-6- carbonsäure (116 mg), EDC (112 mg) und HOBT (98 mg) gegeben. Nach 12 Stunden Rühren bei Raumtemperatur wurde die Lösung eingeengt. Der Rückstand wurde durch Flash- Chromatographie gereinigt (Kieselgel, 2-3% Methanol in DCM + 1% Ammoniumhydroxid) und lieferte das gewünschte Produkt (111 mg) .To a solution of amine (14d) (180 mg) in a mixture of dichloromethane (6 ml) and DMF (1 ml) at room temperature was added 3-oxo-3,4-dihydro-2H-benzo [1,4] oxazine 6-carboxylic acid (116 mg), EDC (112 mg) and HOBT (98 mg). After stirring at room temperature for 12 hours, the solution was concentrated. The residue was purified by flash chromatography (silica gel, 2-3% methanol in DCM + 1% ammonium hydroxide) to give the desired product (111 mg).
MS (EI) : m/z: 477 [M+H]+ MS (EI): m / z: 477 [M + H] +
Beispiel 34: 3-Oxo-3,4-dihydro-2H-benzo[l,4] thiazin-6- carbonsäure- {1- [2-hydroxy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-yl>-amid (Racemat)
Example 34: 3-Oxo-3,4-dihydro-2H-benzo [l, 4] thiazine-6-carboxylic acid {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl ] -piperidin-4-yl> -amide (racemate)
Die Titelverbindung wurde wie in Beispiel 33 aus 3-Oxo-3,4- dihydro-2H-benzo [1,4] thiazin-6-carbonsäure hergestellt .The title compound was prepared as in Example 33 from 3-oxo-3,4-dihydro-2H-benzo [1,4] thiazine-6-carboxylic acid.
MS (EI): m/z: 493 [M+H]+ MS (EI): m / z: 493 [M + H] +
Beispiel 35: 3-Oxo-3,4-dihydro-2H-pyrido[3,2- b] [1,4] thiazin-6-carbonsäure- {1- [2-hydroxy-2- (3-methoxy- chinolin-5-yl) -ethyl] -piperidin-4-yl}-amid (Racemat)Example 35: 3-Oxo-3,4-dihydro-2H-pyrido [3,2-b] [1,4] thiazine-6-carboxylic acid {1- [2-hydroxy-2- (3-methoxy-quinoline -5-yl) -ethyl] -piperidin-4-yl} -amide (racemate)
Die TitelVerbindung wurde wie in Beispiel 33 aus 3-Oxo-3,4- dihydro-2H-pyrido[3, 2-b] [1 , 4] thiazin-6-carbonsäure (2f) hergestellt .The title compound was prepared as in Example 33 from 3-oxo-3,4-dihydro-2H-pyrido [3, 2-b] [1, 4] thiazine-6-carboxylic acid (2f).
MS (EI) : m/z: 494 [M+H]MS (EI): m / z: 494 [M + H]
Beispiel 36: 2,3-Dihydro-benzo[l,4]dioxin-6-carbonsäure-{l- [2-hydroxy-2- (3-methoxy-chinolin-5-yl) -ethyl] -piperidin-4- yl}-amid (Racemat)
Example 36: 2,3-Dihydro-benzo [1,4] dioxin-6-carboxylic acid {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidine-4- yl} -amide (racemate)
Die TitelVerbindung wurde wie in Beispiel 33 aus 2,3- Dihydro-benzo [1,4] dioxin-6-carbonsäure hergestellt .The title compound was prepared as in Example 33 from 2,3-dihydro-benzo [1,4] dioxin-6-carboxylic acid.
MS (EI): m/z: 464 [M+H]+ MS (EI): m / z: 464 [M + H] +
Beispiel 37: 3-Oxo-3,4-dihydro-2H-benzo[l#4]oxazin-6- sulfonsäure-{l- [2-hydroxy-2- (3-methoxy-chinolin-5-yl) ■ ethyl] -piperidin-4-yl}-amid (Racemat)Example 37: 3-oxo-3,4-dihydro-2H-benzo [l # 4] oxazin-6-sulfonic acid {l- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) ethyl ■ ] -piperidin-4-yl} -amide (racemate)
Zu einer Lösung von Amin (14d) (0.3 g) in trockenemTo a solution of amine (14d) (0.3 g) in dry
Dichlormethan (15 ml) wurde bei Raumtemperatur Triethylamin (0.21 ml) und 3-Oxo-3 , 4-dihydro-2H-benzo [1 , 4] oxazin-6- sulfonylchlorid (0.27 g) gegeben. Nach 24 Stunden Rühren bei Raumtemperatur wurde die Reaktionsmischung eingeengt. Der Rückstand wurde mittels Flash-ChromatographieDichloromethane (15 ml) was added at room temperature to triethylamine (0.21 ml) and 3-oxo-3,4-dihydro-2H-benzo [1,4] oxazine-6-sulfonyl chloride (0.27 g). After stirring at room temperature for 24 hours, the reaction mixture was concentrated. The residue was purified by flash chromatography
(Kieselgel, Chloroform/Methanol 9:1 + 5% Ammoniumhydroxid) gereinigt und lieferte das gewünschte Produkt (0.15 g) .
MS (EI) : m/z: 513 [M+H](Silica gel, chloroform / methanol 9: 1 + 5% ammonium hydroxide) to afford the desired product (0.15 g). MS (EI): m / z: 513 [M + H]
Beispiel 38: 3-Oxo-3,4-dihydrc—2H-benzo[l,4] thiazin-6- sulfonsäure-{l- [2-hydroxy-2-(3-methoxy-chinolin-5- yDethyl] -piperidin-4-yl}-amid (Racemat)Example 38: 3-Oxo-3,4-dihydroc-2H-benzo [l, 4] thiazine-6-sulfonic acid {1- [2-hydroxy-2- (3-methoxy-quinoline-5-y-dimethyl] -piperidine -4-yl} -amide (racemate)
Die Titelverbindung wurde wie in Beispiel 37 aus 3-Oxo-3,4- dihydro-2H-benzo [1,4] thiazin-6-sulfonylchlorid hergestelltThe title compound was prepared as in Example 37 from 3-oxo-3,4-dihydro-2H-benzo [1,4] thiazine-6-sulfonyl chloride
MS (EI) : m/z: 529 [M+H]+ MS (EI): m / z: 529 [M + H] +
Beispiel 39: 2,3-Dihydro-benzo[l,4]dioxin-6-sulfonsäure-{l- [2-hydroxy-2- (3-methoxy-chinolin-5-yl) -ethyl] -piperidin-4- yl}-amid (Racemat)Example 39: 2,3-Dihydro-benzo [1,4] dioxin-6-sulfonic acid {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidine-4- yl} -amide (racemate)
Die Titelverbindung wurde wie in Beispiel 37 aus 2 , 3 - Dihydro-benzo [ 1 , 4 ] dioxin-6-sulfonylchlorid hergestellt ,
MS ( EI ) : m/ z : 500 [M+H]The title compound was prepared as in Example 37 from 2,3-dihydro-benzo [1,4] dioxin-6-sulfonyl chloride, MS (EI): m / z: 500 [M + H]
Beispiel 40: 2- {4- [ (2,3-Dihydro-benzo[l,4]dioxin-6- ylmethyl)-amino] -3-fluor-piperidin-l-yl}-l- (3-methoxy- chinolin-5-yl)-ethanol (Enantiomer 1)Example 40: 2- {4- [(2,3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) amino] -3-fluoro-piperidin-1-yl} -1- (3-methoxy) quinolin-5-yl) ethanol (enantiomer 1)
40a) 4-Oxo-piperidin-l-carbonsäure-tert-butylester40a) tert-butyl 4-oxo-piperidine-1-carboxylate
4-Piperidonhydrochlorid Hydrat (15.00 g) wurde in IN Natronlauge (102 ml), Wasser (102 ml) und Dioxan (102 ml) gelöst. Eine Lösung aus Bocanhydrid (23.44 g) in Dioxan (102 ml) wurde bei Raumtemperatur dazugetropft und das Ganze über Nacht bei Raumtemperatur gerührt. Die Lösung wurde partiell eingeengt und mehrfach mit Essigester extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, eingeengt und lieferten das gewünschte Produkt (19.27 g) .4-piperidone hydrochloride hydrate (15.00 g) was dissolved in 1N sodium hydroxide solution (102 ml), water (102 ml) and dioxane (102 ml). A solution of bocane hydride (23.44 g) in dioxane (102 ml) was added dropwise at room temperature and the whole was stirred at room temperature overnight. The solution was partially concentrated and extracted several times with ethyl acetate. The combined organic phases were washed with sat. Washed with sodium chloride solution, dried over magnesium sulfate, concentrated and afforded the desired product (19.27 g).
MS (EI): m/z: 200 [M+H]+ MS (EI): m / z: 200 [M + H] +
40b) 4-Trimethylsilanyloxy-3#6-dihydro-2H-pyridin-l- carbonsäure-tert-butylester40b) 4-trimethylsilanyloxy-3 # 6-dihydro-2H-pyridine-1-carboxylic acid tert-butyl ester
Zu einer Lösung des Ketons (40a) (10.12 g) in DMF (20 ml) wurde Trimethylsilylchlorid (7.8 ml) und Triethylamin (17 ml) gegeben und über Nacht auf 800C erhitzt. Nach dem
Abkühlen wurde das DMF unter vermindertem Druck entfernt, der Rückstand in ges . Natriumhydrogencarbonatlösung aufgenommen und mit Hexan ausgeschüttelt. Die organische Phase wurde über Magnesiumsulfat getrocket, filtriert und eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Hexan/Essigester 9:1) gereinigt und lieferte das gewünschte Produkt (10.5 g) .To a solution of the ketone (40a) (10.12g) in DMF (20ml) was added trimethylsilyl chloride (7.8ml) and triethylamine (17ml) and heated at 80 ° C overnight. After this Cooling the DMF was removed under reduced pressure, the residue in sat. Sodium bicarbonate solution and extracted with hexane. The organic phase was dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 9: 1) to afford the desired product (10.5 g).
MS (EI): m/z: 272 [MH-H] + MS (EI): m / z: 272 [MH-H] +
40c) 3-Fluor-4-oxo-piperidin-l-carbonsäure-tert-butylester40c) tert-butyl 3-fluoro-4-oxo-piperidine-1-carboxylate
Zu einer Lösung der Silylenolethers (40b) (10.5 g) in Acetonitril (420 ml) wurde Selectfluor (15.1 g) gegeben und 75 Minuten bei Raumtemperatur gerührt. Ges. Natriumchloridlösung wurde dazugegeben und das Acetonitril unter vermindertem Druck entfernt. Der Rückstand wurde mit Essigster extrahiert und die organische Phase über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Aluminiumoxid III, Essigester, Essigester/Methanol 9:1) gereinigt und lieferte das gewünschte Produkt (8.5 g) .To a solution of the silyl enol ether (40b) (10.5 g) in acetonitrile (420 ml) was added Selectfluor (15.1 g) and stirred at room temperature for 75 minutes. Sodium chloride solution was added and the acetonitrile was removed under reduced pressure. The residue was extracted with ethyl acetate and the organic phase dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (alumina III, ethyl acetate, ethyl acetate / methanol 9: 1) to afford the desired product (8.5 g).
MS (EI) : m/z: 218 [M+H]+ MS (EI): m / z: 218 [M + H] +
40d) 4-Benzylamino-3-fluor-piperidin-l-carbonsäure-tert- butylester40d) tert-butyl 4-benzylamino-3-fluoro-piperidine-1-carboxylate
Zu einer Lösung des Fluorids (40c) (7.12 g) in 1,2- Dichlorethan (150 ml) wurde Benzylamin (4 ml) und dann Natriumtriacetoxyborhydrid (8.5 g) gegeben und über Nacht bei Raumtemperatur gerührt. Dann wurde ges.To a solution of the fluoride (40c) (7.12g) in 1,2-dichloroethane (150ml) was added benzylamine (4ml) then sodium triacetoxyborohydride (8.5g) and stirred overnight at room temperature. Then sat.
Natriumhydrogencarbonatlösung (100 ml) hinzugegeben und der pH auf 8 mit festem Natriumhydrogencarbonat eingestellt.
Die Phasen wurden getrennt und die wässrige Phase mit Dichlormethan extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan/Essigester 1:1) gereinigt und lieferte das gewünschte Produkt .Sodium bicarbonate solution (100 ml) was added and the pH adjusted to 8 with solid sodium bicarbonate. The phases were separated and the aqueous phase extracted with dichloromethane. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, hexane / ethyl acetate 1: 1) to afford the desired product.
MS (EI) : m/z: 309 [M+H]+ MS (EI): m / z: 309 [M + H] +
40e) 4-Amino-3-fluor-piperidin-1-carbonsäure-tert- butylester40e) tert-butyl 4-amino-3-fluoro-piperidine-1-carboxylate
Zu einer Lösung des Benzylamins (40d) (4 g) in Methanol (100 ml) wurde 20% Palladiumhydroxid (2.7 g) gegeben und die Reaktionsmischung unter einer Wasserstoffatmosphäre für 4 Stunden gerührt. Die Lösung wurde filtriert, unter Vakuum eingeengt und lieferte das gewünschte Produkt (2.84 g) .To a solution of the benzylamine (40d) (4 g) in methanol (100 ml) was added 20% palladium hydroxide (2.7 g) and the reaction mixture was stirred under a hydrogen atmosphere for 4 hours. The solution was filtered, concentrated in vacuo to afford the desired product (2.84 g).
MS (EI) : m/z: 219 [M+H]+ MS (EI): m / z: 219 [M + H] +
4Of) 4-Benzyloxycarbonylamino-3-fluor-piperidin-1- carbonsäure-tert-butylester4Of) 4-Benzyloxycarbonylamino-3-fluoro-piperidine-1-carboxylic acid tert-butyl ester
Zu einer Lösung des Amins (40e) (2.84 g) in Essigester (50 m) und ges. Natriumhydrogencarbonatlösung (50 ml) wurde Z- Chlorid (2 ml) gegeben und eine Stunde bei Raumtemperatur gerührt. Die beiden Phasen wurden getrennt und die wässrige mit Essigester extrahiert. Die vereinigten organischen Phasen wurden mit ges. Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel,To a solution of the amine (40e) (2.84 g) in ethyl acetate (50 m) and sat. Sodium bicarbonate solution (50 ml) was added with Z-chloride (2 ml) and stirred for one hour at room temperature. The two phases were separated and the aqueous extracted with ethyl acetate. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel,
Hexan/Essigester 2:1) gereinigt und lieferte das gewünschte Produkt .
MS ( EI ) : m/ z : 3 53 [IVM-H ] + Hexane / ethyl acetate 2: 1) to afford the desired product. MS (EI): m / z: 3 53 [IVM-H] +
40g) (3-Fluor-piperidin-4-yl) -carbaminsäurebenzylester Eine Lösung des geschützten Amins (4Of) in TFA (10 ml) wurde bei Raumtemperatur für 30 Minuten gerührt. Das Lösungsmittel wurde unter vermindertem Druck entfernt, der Rückstand mit 3N Natronlauge aufgenommen und mehrfach mit Dichlormethan/Methanol 9 : 1 extrahiert . Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert, eingeengt und lieferten das gewünschte Produkt (2.9 g) .40g) (3-Fluoro-piperidin-4-yl) -carbamic acid benzyl ester A solution of the protected amine (4Of) in TFA (10 ml) was stirred at room temperature for 30 minutes. The solvent was removed under reduced pressure, the residue was taken up in 3N sodium hydroxide solution and extracted repeatedly with dichloromethane / methanol 9: 1. The combined organic phases were washed with sat. Sodium chloride solution, dried over sodium sulfate, filtered, concentrated and afforded the desired product (2.9 g).
MS (EI) : m/z: 253 [M+H]+ MS (EI): m / z: 253 [M + H] +
40h) {3-Fluor-l- [2-hydroxy-2- (3-methoxy-chinolin-5-yl) - ethyl] -piperidin-4-yl} -carbaminsäurebenzylester (Enantiomer40h) {3-Fluoro-1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-yl} -carbamic acid benzyl ester (enantiomer
DD
Zu einer Lösung von 3-Methoxy-5-oxiranyl-chinolin (7a) (0.8 g) und Piperidin (40g) (1.01 g) in DMF (10 ml) wurdeTo a solution of 3-methoxy-5-oxiranyl-quinoline (7a) (0.8g) and piperidine (40g) (1.01g) in DMF (10ml)
Lithiumperchlorat (0.425 g) gegeben und auf 800C über Nacht erhitzt. Das Lösungsmittel wurde unter vermindertem Druck entfernt, der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester) gereinigt und lieferte das gewünschte Produkt (1.7 g) .Lithium perchlorate (0.425 g) and heated to 80 0 C overnight. The solvent was removed under reduced pressure, the residue was purified by flash chromatography (silica gel, ethyl acetate) to afford the desired product (1.7 g).
MS (EI) : m/z: 454 [M+H]+ MS (EI): m / z: 454 [M + H] +
40i) 2-(4-Amino-3-fluor-piperidin-1-yl) -1- (3-methoxy- chinolin-5-yl)-ethanol (Enantiomer 1)40i) 2- (4-amino-3-fluoro-piperidin-1-yl) -1- (3-methoxy-quinolin-5-yl) -ethanol (enantiomer 1)
Zu einer Lösung von Verbindung (40h) (1.7 g) in Essigester (50 ml) und Ethanol (10 ml) wurde 10% Palladium auf Kohle
(0.7 g) gegeben und 6 Stunden unter einerTo a solution of compound (40h) (1.7g) in ethyl acetate (50ml) and ethanol (10ml) was added 10% palladium on carbon (0.7 g) and 6 hours under a
Wasserstoffatmosphäre gerührt. Die Lösung wurde filtriert, eingeengt und lieferte das gewünschte Produkt.Stirred hydrogen atmosphere. The solution was filtered, concentrated and afforded the desired product.
MS (EI): m/z: 320 [M+H]+ MS (EI): m / z: 320 [M + H] +
4Oj) Titelverbindung4Oj) Title compound
Die Verbindung wurde wie in Beispiel 7d aus Amin (4Oi) und 2, 3-Dihydro-benzo [1, 4] dioxin-6-carbaldehyd hergestellt.The compound was prepared as in Example 7d from amine (40I) and 2, 3-dihydro-benzo [1,4] dioxine-6-carbaldehyde.
MS (EI) : m/z: 468 [M+H]+ MS (EI): m / z: 468 [M + H] +
Beispiel 41: 6- ( {3-Fluor-l- [2-hydroxy-2- (3-methoxy- chinolin-5-yl) -ethyl] -piperidin-4-ylamino}-methyl) -4H- benzo[l,4]oxazin-3-on (Enantiomer 1)Example 41: 6- ({3-Fluoro-1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [l , 4] oxazin-3-one (enantiomer 1)
Die Verbindung wurde wie in Beispiel 40j aus Aldehyd (Ij) hergestellt.The compound was prepared from aldehyde (Ij) as in Example 40j.
MS (EI) : m/z: 481 [M+H]+ MS (EI): m / z: 481 [M + H] +
Beispiel 42: 2- [3-Fluor-4- ( (E) -3-phenyl-allylamino) ■ piperidin-1-yl] -1- (3-methoxy-chinolin-5-yl) -ethanol (Enantiomer 1)
Example 42: 2- [3-fluoro-4- ((E) -3-phenyl-allylamino) ■ piperidin-1-yl] -1- (3-methoxy-quinolin-5-yl) -ethanol (enantiomer 1)
Die Verbindung wurde wie in Beispiel 40j aus Zimtaldehyd hergestellt .The compound was prepared from cinnamic aldehyde as in Example 40j.
MS (EI): m/z: 436 [M+H]+ MS (EI): m / z: 436 [M + H] +
Beispiel 43: 6- ( {3-Fluor-l- [2-hydroxy-2- (3-methoxy- chinolin-5-yl) -ethyl] -piperidin-4-ylamino}-methyl) -4H- pyrido[3#2-b] [1,4] thiazin-3-on (Enantiomer 1)Example 43: 6- ({3-Fluoro-1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4 H -pyrido [3 # 2-b] [1,4] thiazine-3-one (enantiomer 1)
Die Verbindung wurde wie in Beispiel 4Oj aus Aldehyd (2h) hergestellt .The compound was prepared from aldehyde (2h) as in Example 40j.
MS (EI) : m/z: 498 [M+H]+ MS (EI): m / z: 498 [M + H] +
Beispiel 44: 2- {4- [ (3,4-Dihydro-2H-benzo[l, 4] oxazin-6- ylmethyl) -amino] -3-fluor-piperidin-l-yl}-l- (3-methoxy- chinolin-5-yl)-ethanol (Enantiomer 1)
Example 44: 2- {4- [(3,4-Dihydro-2H-benzo [l, 4] oxazin-6-ylmethyl) -amino] -3-fluoro-piperidin-1-yl} -l- (3 methoxy-quinolin-5-yl) -ethanol (enantiomer 1)
44a) (3,4-Dihydro-2H-benzo[l,4]oxazin-6-yl) -methanol44a) (3,4-dihydro-2H-benzo [l, 4] oxazin-6-yl) -methanol
Zu einer eiskalten Lösung von Aldehyd (Ij) (1.77 g) in THF (100 ml) wurde Lithiumaluminiumhydrid (1 g) gegeben, 30 Minuten bei 00C gerührt und dann für 90 Minuten unter Rückfluss erhitzt. Nach dem Abkühlen wurde Wasser (1 ml), 15% Natronlauge (1 ml) und Wasser (3 ml) nacheinander zugegeben. Die Reaktionsmischung wurde mit THF (100 ml) verdünnt und der Niederschlag abfiltriert. Das Filtrat wurde eingeengt und der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Essigester) gereinigt und lieferte das gewünschte Produkt (1.5 g) .To an ice-cold solution of aldehyde (Ij) (1.77 g) in THF (100 ml) was added lithium aluminum hydride (1 g), stirred at 0 ° C. for 30 minutes and then heated at reflux for 90 minutes. After cooling, water (1 ml), 15% sodium hydroxide solution (1 ml) and water (3 ml) were added successively. The reaction mixture was diluted with THF (100 ml) and the precipitate filtered off. The filtrate was concentrated and the residue was purified by flash chromatography (silica gel, ethyl acetate) to give the desired product (1.5 g).
MS (EI): m/z: 166 [M+H]+ MS (EI): m / z: 166 [M + H] +
44b) 3/4-Dihydro-2H-benzo[l,4]oxazin-6-carbaldehyd44b) 3 / 4-dihydro-2H-benzo [l, 4] oxazine-6-carbaldehyde
Zu einer Lösung von Alkohol (44a) (1.5 g) in Dichlormethan (100 ml) und THF (100 ml) wurde Mangandioxid (3 g) gegeben. Nach 2 Stunden Rühren bei Raumtemperatur wurde weiteres Mangandioxid (3 g) dazugegeben und weitere 3 Stunden gerührt. Dann wurde die Reaktionsmischung durch Celit filtriert und mit THF nachgewaschen. Das Filtrat wurde eingeengt und lieferte das gewünschte Produkt (1 g) .To a solution of alcohol (44a) (1.5 g) in dichloromethane (100 ml) and THF (100 ml) was added manganese dioxide (3 g). After stirring for 2 hours at room temperature, additional manganese dioxide (3 g) was added and stirred for a further 3 hours. The reaction mixture was filtered through celite and washed with THF. The filtrate was concentrated to afford the desired product (1 g).
MS (EI) : m/z: 164 [M+H]+ MS (EI): m / z: 164 [M + H] +
44c) Titelverbindung
Die Verbindung wurde wie in Beispiel 40j aus Aldehyd (44b) hergestellt .44c) Title compound The compound was prepared from aldehyde (44b) as in Example 40j.
MS (EI): m/z: 467 [M+H]+ MS (EI): m / z: 467 [M + H] +
Beispiel 45: 2-{4- [ (2,3-Dihydro- [l,4]dioxino [2,3-c]pyridin- 7-ylmethyl) -amino] -3-fluor-piperidin-l-yl}-l- (3-methoxy- chinolin-5-yl)-ethanol (Enantiomer 1)Example 45: 2- {4- [(2,3-Dihydro- [l, 4] dioxino [2,3-c] pyridin-7-ylmethyl) amino] -3-fluoro-piperidin-1-yl} - 1- (3-methoxy-quinolin-5-yl) -ethanol (enantiomer 1)
Die Verbindung wurde wie in Beispiel 4Oj aus Aldehyd (5d) hergestellt.The compound was prepared from aldehyde (5d) as in Example 40j.
MS (EI) : m/z: 470 [M+H]+ MS (EI): m / z: 470 [M + H] +
Beispiel 46: 2-{4- [ (Benzo [1,2, 5] thiadiazol-5-ylmethyl) - amino] -3-fluor-piperidin-l-yl}-l- (3-methoxy-chinolin-5-yl) ethanol (Enantiomer 1)Example 46: 2- {4- [(Benzo [1,2,5] thiadiazol-5-ylmethyl) amino] -3-fluoro-piperidin-1-yl} -1- (3-methoxy-quinoline-5- yl) ethanol (enantiomer 1)
Die Verbindung wurde wie in Beispiel 40j aus Benzo[l, 2,5] thiadiazol-5-carbaldehyd hergestellt. The compound was prepared as in Example 40j from benzo [l, 2,5] thiadiazole-5-carbaldehyde.
MS (EI): m/z: 468 [M+H]+ MS (EI): m / z: 468 [M + H] +
Beispiel 47: 6- ( {3-Fluor-l- [2-hydroxy-2- (3-methoxy- chinolin-5-yl) -ethyl] -piperidin-4-ylamino}-methyl) -4H- benzo [1, 4] thiazin-3-on (Enantiomer 1)Example 47: 6- ({3-Fluoro-1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) -4H-benzo [1 , 4] thiazine-3-one (enantiomer 1)
Die Verbindung wurde wie in Beispiel 40j aus Aldehyd (4b) hergestellt.The compound was prepared from aldehyde (4b) as in Example 40j.
MS (EI) : m/z: 497 [M+H]+ MS (EI): m / z: 497 [M + H] +
Beispiel 48: 2- [4- [ (2, 3-Dihydro-benzo[l,4]dioxin-6- ylmethyl)-amino] -4- (2-hydroxy-ethyl) -piperidin-1-yl] -l-(3- methoxy-chinolin-5-yl) -ethanol (Racemat)Example 48: 2- [4- [(2,3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -4- (2-hydroxy-ethyl) -piperidin-1-yl] -l - (3-methoxy-quinolin-5-yl) -ethanol (racemate)
48a) 4-Amino-4-carboxymethyl-piperidin-1-carbonsäure- benzylester 48a) 4-Amino-4-carboxymethyl-piperidine-1-carboxylic acid benzyl ester
Zu einer Lösung von 4-Oxo-piperidin-l-carbonsäure- benzylester (10 g) und Ammoniumformiat (4.93 g) in Methanol (20 ml) wurde Malonsäure (4.5 g) gegeben und 3 Tage unter Rückfluss erhitzt. Nach dem Einengen wurde das Rohprodukt (12 g) ohne weitere Reinigung weiterverwendet.To a solution of 4-oxo-piperidine-1-carboxylic acid benzyl ester (10 g) and ammonium formate (4.93 g) in methanol (20 ml) was added malonic acid (4.5 g) and heated at reflux for 3 days. After concentration, the crude product (12 g) was used without further purification.
48b) 4-Amino-4-methoxycarbonylmethyl-piperidin-1-carbon- säurebenzylester48b) 4-Amino-4-methoxycarbonylmethyl-piperidine-1-carboxylic acid benzyl ester
Zu einer Lösung des Esters (48a) (5 g) in Methanol (25 ml) und Hexan (25 ml) wurde TMS-Diazomethan (2M in Hexan, 9 ml) gegeben und 3 Stunden bei Raumtemperatur gerührt. Nach dem Einengen wurde der Rückstand mit Essigester (100 ml) und IN Natronlauge (30 ml) aufgenommen. Die organische Phase wurde mit IN Natronlauge (30 ml) und ges . Natriumchloridlösung (30 ml) gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt und lieferte das gewünschte Produkt (4.9 g) .To a solution of the ester (48a) (5 g) in methanol (25 ml) and hexane (25 ml) was added TMS-diazomethane (2M in hexane, 9 ml) and stirred at room temperature for 3 hours. After concentration, the residue was taken up in ethyl acetate (100 ml) and IN sodium hydroxide solution (30 ml). The organic phase was washed with 1N sodium hydroxide solution (30 ml) and sat. Sodium chloride solution (30 ml), dried over sodium sulfate, filtered and concentrated to afford the desired product (4.9 g).
MS (EI): m/z: 307 [M+H]+ MS (EI): m / z: 307 [M + H] +
48c) 4- [ (2#3-Dihydro-benzo[l,4]dioxin-6-ylmethyl) -amino] -4- methoxycarbonylmethyl-piperidin-1-carbonsäurebenzylester48c) 4- [(2 # 3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -4-methoxycarbonylmethyl-piperidine-1-carboxylic acid benzyl ester
Zu einer Lösung von Aminopiperidin (48b) (0.86 g) und 2,3- Dihydro-benzo[l, 4] dioxin-6-carbaldehyd (0.5 g) in 1,2-To a solution of aminopiperidine (48b) (0.86 g) and 2,3-dihydro-benzo [l, 4] dioxin-6-carbaldehyde (0.5 g) in 1,2-
Dichlorethan (15 ml) wurde Natriumtriacetoxyborhydrid (0.72 g) gegeben und 16 Stunden bei Raumtemperatur gerührt. Dann wurde ges. Bicarbonatlösung (20 ml) und Dichlormethan (50 ml) zugegeben, die Phasen getrennt und die wässrige Phase mit Dichlormethan (50 ml) extrahiert. Die vereinigten organischen Phasen wurden mit ges. Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und
eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Essigester) gereinigt und lieferte das gewünschte Produkt (0.75g).Dichloroethane (15 ml) was added with sodium triacetoxyborohydride (0.72 g) and stirred at room temperature for 16 hours. Then sat. Add bicarbonate solution (20 mL) and dichloromethane (50 mL), separate the layers and extract the aqueous layer with dichloromethane (50 mL). The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate) to give the desired product (0.75 g).
MS (EI): m/z: 455 [M+H]+ MS (EI): m / z: 455 [M + H] +
48d) 4- [ (2,3-Dihydro-benzo[l,4]dioxin-6-ylmethyl)-amino] -4- (2-hydroxy-ethyl)-piperidin-l-carbonsäurebenzylester48d) 4- [(2,3-dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -4- (2-hydroxy-ethyl) -piperidine-1-carboxylic acid benzyl ester
Zu einer Lösung von Ester (48c) (0.75 g) in THF (20 ml) wurde Lithiumborhydrid (0.3 g) gegeben und 2 Stunden beiTo a solution of ester (48c) (0.75g) in THF (20ml) was added lithium borohydride (0.3g) and added for 2 hours
Raumtemperatur gerührt. Wasser (5 ml), Methanol (2 ml) und ges . Kalium-Natrium-Tartratlösung (50 ml) wurden zugegeben. Nach 20 Minuten Rühren wurde Dichlormethan (100 ml) zugegeben, die Phasen getrennt und die wässrige Phase mit Dichlormethan (3 x 50 ml) extrahiert. Die vereinigten organischen Phasen wurde eingeengt und der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester) gereinigt und lieferte das gewünschte Produkt (0.5 g) .Room temperature stirred. Water (5 ml), methanol (2 ml) and sat. Potassium-sodium tartrate solution (50 ml) was added. After stirring for 20 minutes, dichloromethane (100 ml) was added, the phases separated, and the aqueous phase extracted with dichloromethane (3 x 50 ml). The combined organic phases were concentrated and the residue was purified by flash chromatography (silica gel, ethyl acetate) to give the desired product (0.5 g).
MS (EI): m/z: 427 [M+H]+ MS (EI): m / z: 427 [M + H] +
48e) 2-{4-[(2,3-Dihydro-benzo[l,4]dioxin-6-ylmethyl)- amino] -piperidin-4-yl} -ethanol48e) 2- {4 - [(2,3-dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -piperidin-4-yl} -ethanol
Zu einer Lösung von geschütztem Piperidin (48d) (0.5 g) in THF (8 ml) und Methanol (2 ml) wurde 20% Palladiumhydroxid (0.5 g) gegeben und für 4 Stunden bei Raumtemperatur unter einer Wasserstoffatmosphäre gerührt. Die Lösung wurde filtriert, eingeengt und lieferte das gewünschte Produkt (340 mg) .To a solution of protected piperidine (48d) (0.5 g) in THF (8 ml) and methanol (2 ml) was added 20% palladium hydroxide (0.5 g) and stirred for 4 hours at room temperature under a hydrogen atmosphere. The solution was filtered, concentrated and afforded the desired product (340 mg).
MS (EI): m/z: 293 [M+H]+
48f) TitelverbindungMS (EI): m / z: 293 [M + H] + 48f) title compound
Die Titelverbindung wurde wie in Beispiel Ig aus Epoxid (14b) und Piperidin (48e) hergestellt.The title compound was prepared as in Example Ig from epoxide (14b) and piperidine (48e).
MS (EI): m/z: 494 [M+H]+ MS (EI): m / z: 494 [M + H] +
Beispiel 49: 2- [4- [ (Benzo[l,3]dioxol-5-ylπιethyl) -amino] -4- (2-hydroxy-ethyl) -piperidin-1-yl] -1- (3-methoxy-chinolin-5- yl)-ethanol (Racemat)Example 49: 2- [4- [(Benzo [1,3] dioxol-5-yl-ptiethyl) -amino] -4- (2-hydroxyethyl) -piperidin-1-yl] -1- (3-methoxy- quinoline-5-yl) ethanol (racemate)
Das Piperidin (2- {4- [ (Benzo [1, 3] dioxol-5-ylmethyl) -amino] - piperidin-4-yl} -ethanol) wurde analog zu den Schritten 48c bis 48e aus Benzo [1 , 3 ] dioxol-5-carbaldehyd hergestellt. Die TitelVerbindung wurde wie in Beispiel 48f aus Epoxid (14b) und 2- {4- [ (Benzo [1 , 3 ] dioxol-5-ylmethyl) -amino] - piperidin-4-yl} -ethanol hergestellt .The piperidine (2- {4- [(benzo [1,3-dioxol-5-ylmethyl) -amino] -piperidin-4-yl} -ethanol) was prepared analogously to steps 48c to 48e from benzo [1, 3] dioxole-5-carbaldehyde. The title compound was prepared as in Example 48f from epoxide (14b) and 2- {4- [(benzo [1,3-dioxol-5-ylmethyl) -amino] -piperidin-4-yl} -ethanol.
MS (EI) : m/z: 480 [M+H]+ MS (EI): m / z: 480 [M + H] +
Beispiel 50: 6- ({4- (2-Hydroxy-ethyl) -1- [2-hydroxy-2- (3- methoxy-chinolin-5-yl) -ethyl] -piperidin-4-ylamino}-methyl) 4H-benzo [1,4] oxazin-3-on (Racemat)
Example 50: 6- ({4- (2-Hydroxyethyl) -1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-ylamino} -methyl) 4H-benzo [1,4] oxazin-3-one (racemate)
Das Piperidin (6- { [4- (2-Hydroxy-ethyl) -piperidin-4- ylamino] -methyl} -4H-benzo [1 , 4] oxazin-3-on) wurde analog zu den Schritten 48c bis 48e aus Aldehyd (Ij) hergestellt. Die TitelVerbindung wurde wie in Beispiel 48f aus Epoxid (14b) und 6- { [4- (2-Hydroxy-ethyl ) -piperidin-4-ylamino] -methyl} - 4H-benzo [1,4] oxazin-3-on hergestellt .The piperidine (6- {[4- (2-hydroxy-ethyl) -piperidin-4-ylamino] -methyl} -4 H -benzo [1,4] oxazin-3-one) was analogous to steps 48c to 48e Aldehyde (Ij) produced. The title compound was prepared as in Example 48f from epoxide (14b) and 6- {[4- (2-hydroxy-ethyl) -piperidin-4-ylamino] -methyl} -4H-benzo [1,4] oxazin-3-one produced .
MS (EI): m/z: 507 [M+H]+ MS (EI): m / z: 507 [M + H] +
Beispiel 51 : 2- {4- [ (2 , 3-Dihydro-benzo [ l , 4 ] dioxin-6- ylmethyl ) -amino] - 3 -hydroxymethyl -piperidin- l-yl} -l- ( 3- methoxy-chinolin-5-yl ) -ethanol (Racemat )Example 51: 2- {4- [(2,3-Dihydro-benzo [l, 4] dioxin-6-ylmethyl) -amino] -3-hydroxymethyl-piperidin-1-yl} -l- (3-methoxy) quinolin-5-yl) ethanol (racemate)
51a) 1-Benzyl-3-hydroxymethyl-piperidin-4-ol Zu einer Mischung aus Natriumhydroxid (1.344 g) und 1- Benzyl-3-carbethoxy-4-piperidon Hydrochlorid (10 g) in Methanol (160 ml) wurde bei 00C Natriumborhydrid (2.543 g) gegeben und 30 Minuten gerührt. Dann wurde Wasser (150 ml)
zugetropft und die Lösung partiell eingeengt. Die wässrige Phase wurde mit Dichlormethan exrahiert (3 x 150 ml) . Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde in Ether (140 ml) aufgenommen und bei 00C51a) 1-Benzyl-3-hydroxymethyl-piperidin-4-ol To a mixture of sodium hydroxide (1344 g) and 1-benzyl-3-carbethoxy-4-piperidone hydrochloride (10 g) in methanol (160 ml) was added at 0 Add 0 C sodium borohydride (2.543 g) and stir for 30 minutes. Then water (150 ml) added dropwise and the solution partially concentrated. The aqueous phase was extracted with dichloromethane (3 x 150 ml). The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was taken up in ether (140 ml) and at 0 ° C.
Lithiumaluminiumhydrid (2.55 g) zugegeben und 1 Stunde gerührt. Dann wurde Wasser (2 ml) , 3N Natronlauge (4 ml) und Wasser (9 ml) zugegeben, auf Raumtemperatur erwärmt und Ether (150 ml) zugegeben. Der Feststoff wurde abfiltriert, das Filtrat eingeengt und lieferte das gewünschte Produkt (5.33 g) .Lithium aluminum hydride (2.55 g) was added and stirred for 1 hour. Then water (2 ml), 3N sodium hydroxide solution (4 ml) and water (9 ml) were added, warmed to room temperature and added ether (150 ml). The solid was filtered off, the filtrate concentrated and afforded the desired product (5.33 g).
MS (EI): m/z: 222 [M+H]+ MS (EI): m / z: 222 [M + H] +
51b) l-Benzyl-3- (tert-butyl-dimethyl-silanyloxymethyl) - piperidin-4-ol51b) 1-benzyl-3- (tert-butyl-dimethyl-silanyloxymethyl) -piperidin-4-ol
Zu einer Lösung von Diol (51a) (5.33 g) in Dichlormethan (47 ml) wurde bei O0C tert-Butyldimethylsilylchlorid (3.9 g) , Triethylamin (6.6 ml) and DMAP (0.287 mg) gegeben und 4 Tage bei 00C gerührt. Nach dem Einengen wurde der Rückstand mit Wasser und Essigester aufgenommen, die Phasen getrennt und die wässrige Phase mit Essigester exrahiert (3 x 100 ml) . Die vereinigten organischen Phasen wurden mit ges. Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 1:2) gereinigt und lieferte das gewünschte Produkt (5.6 g) .To a solution of diol (51) (5:33 g) in dichloromethane (47 ml) 0 C tert-butyldimethylsilyl chloride (3.9 g), triethylamine (6.6 ml) and DMAP (0.287 mg) was added at O and 4 days at 0 0 C touched. After concentration, the residue was taken up in water and ethyl acetate, the phases were separated and the aqueous phase was extracted with ethyl acetate (3 × 100 ml). The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 2) to afford the desired product (5.6 g).
MS (EI): m/z: 336 [M+H] +
51c) 3- (tert-Butyl-dimethyl-silanyloxymethyl) -piperidin-4- olMS (EI): m / z: 336 [M + H] + 51c) 3- (tert-butyl-dimethyl-silanyloxymethyl) -piperidin-4-ol
Zu einer Lösung von Benzylpiperidin (51b) (5.6 g) in THF/Methanol 1:1 (90 ml) wurde 10% Palladiumhydroxid (3.6 g) gegeben und über Nacht unter einer Wasserstoffatmosphäre gerührt. Dann wurde filtriert und das Filtrat eingeengt und lieferte das gewünschte Produkt (4.1 g) .To a solution of benzylpiperidine (51b) (5.6 g) in THF / methanol 1: 1 (90 ml) was added 10% palladium hydroxide (3.6 g) and stirred overnight under a hydrogen atmosphere. It was then filtered and the filtrate concentrated to afford the desired product (4.1 g).
MS (EI) : m/z: 246 [M+H]+ MS (EI): m / z: 246 [M + H] +
5Id) 3- (tert-Butyl-dimethyl-silanyloxymethyl) -4-hydroxy- piperidin-1-carbonsäurebenzylester5Id) 3- (tert-butyl-dimethyl-silanyloxymethyl) -4-hydroxy-piperidine-1-carboxylic acid benzyl ester
Zu einer Lösung von Piperidinol (51c) (4.1 g) in Aceton/Wasser 2:1 (87 ml) wurde Natriumbicarbonat (2.803 g) und Z-Chlorid (2.35 ml) gegeben. Nach einer Stunde Rühren bei Raumtemperatur wurde die Lösung partiell eingeengt und die wässrige Phase mit Essigester extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Magnesiumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 1:4, 1:1) gereinigt und lieferte das gewünschte Produkt (6.1 g) .To a solution of piperidinol (51c) (4.1 g) in acetone / water 2: 1 (87 ml) was added sodium bicarbonate (2,803 g) and Z-chloride (2:35 ml). After stirring for one hour at room temperature, the solution was partially concentrated and the aqueous phase extracted with ethyl acetate. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over magnesium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 4, 1: 1) to afford the desired product (6.1 g).
MS (EI): m/z: 380 [M+H]+ MS (EI): m / z: 380 [M + H] +
5Ie) 3- (tert-Butyl-dimethyl-silanyloxymethyl) -4-oxo- piperidin-1-carbonsäurebenzylester5Ie) 3- (tert-Butyl-dimethyl-silanyloxymethyl) -4-oxopiperidine-1-carboxylic acid benzyl ester
Zu einer Lösung von Alkohol (5Id) (3 g) , N-Methylmorpholin- N-Oxid (1.857 g) und pulverisiertem 4A Molsieb (3.95 g) in Dichlormethan (15 ml) wurde bei Raumtemperatur TPAP (0.139 g) gegeben. Nach einer Stunde wurde die Lösung durch
Kieselgel filtriert und das Filtrat eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 1:4) gereinigt und lieferte das gewünschte Produkt (2 g) .To a solution of alcohol (5Id) (3 g), N-methylmorpholine N-oxide (1.857 g) and powdered 4A molecular sieve (3.95 g) in dichloromethane (15 ml) was added TPAP (0.139 g) at room temperature. After one hour, the solution was through Silica gel filtered and the filtrate was concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 4) to afford the desired product (2 g).
MS (EI) : m/z: 378 [M+H]+ MS (EI): m / z: 378 [M + H] +
5If) 4-Amino-3- (tert-butyl-dimethyl-silanyloxymethyl) - piperidin-1-carbonsäurebenzylester Zu einer Lösung von Keton (5Ie) (2 g) in Methanol (50 ml) wurde Ammoniumacetat (6.13 g) und5If) Benzyl 4-amino-3- (tert-butyl-dimethyl-silanyloxymethyl) -piperidine-1-carboxylate To a solution of ketone (5Ie) (2 g) in methanol (50 ml) was added ammonium acetate (6.13 g) and
Natriumtriacetoxyborhydrid (1.69 g) gegeben und über Nacht bei Raumtemperatur gerührt . Nach dem Einengen wurde der Rückstand mit Wasser und Dichlormethan aufgenommen, die Phasen getrennt und die wässrige Phase mit Dichlormethan exrahiert (3 x 70 ml) . Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt (1 g) wurde ohne weitere Reinigung weiterverwendet.Sodium triacetoxyborohydride (1.69 g) and stirred overnight at room temperature. After concentration, the residue was taken up in water and dichloromethane, the phases were separated and the aqueous phase was extracted with dichloromethane (3 × 70 ml). The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The crude product (1 g) was used without further purification.
51g) 3-(tert-Butyl-dimethyl-silanyloxymethyl)-4-[(2,3- dihydro-benzo [1,4] dioxin-6-ylmethyl) -ainixio] -piperidin-1 -carbonsäurebenzylester Zu einer Lösung von Amin (5If) (I g) in Methanol (7 ml) und Dichlormethan (22 ml) wurde 3A Molsieb (7 g) und 2,3- Dihydro-benzo[l, 4] dioxin-6-carbaldehyd (0.434 g) gegeben und 20 Stunden bei Raumtemperatur gerührt. Dann wurde Natriumborhydrid (0.120 g) zugegeben und weitere 2 Stunden gerührt. Das Molsieb wurde abfiltriert und das Filtrat mit ges . Bicarbonatlösung und ges . Natriumchloridlösung gewaschen. Die organische Phase wurde über Magnesiumsulfat
getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1 + 1% Ammoniak) gereinigt und lieferte das gewünschte Produkt (500 mg) .51g) Benzyl 3- (tert -butyl-dimethyl-silanyloxymethyl) -4 - [(2,3-dihydro-benzo [1,4] dioxin-6-ylmethyl) -alixio] -piperidine-1-carboxylate To a solution of amine (5If) (I g) in methanol (7 mL) and dichloromethane (22 mL) was added 3A molecular sieves (7 g) and 2,3-dihydro-benzo [l, 4] dioxin-6-carbaldehyde (0.434 g) and Stirred for 20 hours at room temperature. Then, sodium borohydride (0.120 g) was added and stirred for a further 2 hours. The molecular sieve was filtered off and the filtrate with sat. Bicarbonate solution and sat. Washed sodium chloride solution. The organic phase was over magnesium sulfate dried, filtered and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1 + 1% ammonia) to give the desired product (500 mg).
MS (EI): m/z: 527 [M+H]+ MS (EI): m / z: 527 [M + H] +
51h) [3- (tert-Butyl-dimethyl-silanyloxymethyl) -piperidin-4- yl] - (2 , 3-dihydro-benzo [1,4] dioxin-6-ylmethyl) -amin Zu einer Lösung von Z-geschütztem Piperidin (51g) (500 mg) in Essigester (15 ml) wurde 10% Palladium auf Kohle (0.4 g) gegeben und für 12 Stunden unter einer51h) [3- (tert -butyl-dimethyl-silanyloxymethyl) -piperidin-4-yl] - (2,3-dihydro-benzo [1,4] dioxin-6-ylmethyl) -amine To a solution of Z-protected Piperidine (51g) (500mg) in ethyl acetate (15ml) was added 10% palladium on charcoal (0.4g) and boiled for 12 hours
Wasserstoffatmosphäre gerührt. Die Lösung wurde filtriert und eingeengt und lieferte das gewünschte Produkt (0.37 g) .Stirred hydrogen atmosphere. The solution was filtered and concentrated to afford the desired product (0.37 g).
MS (EI): m/z: 393 [M+H]+ MS (EI): m / z: 393 [M + H] +
5Ii) 2-{3-(tert-Butyl-dimethyl-silanyloxymethyl)-4-[(2,3- dihydro-benzo [1, 4] dioxin-6-ylmethyl ) -amino] -piperidin -l-yl}-l-(3-methoxy-chinolin-5-yl)-ethanol5Ii) 2- {3- (tert-Butyl-dimethyl-silanyloxymethyl) -4 - [(2,3-dihydro-benzo [1,4] dioxin-6-ylmethyl) -amino] -piperidin-1-yl} - l- (3-methoxy-quinolin-5-yl) ethanol
Zu einer Lösung von Epoxid (14b) (150 mg) und geschütztem Piperidin (51h) (293 mg) in DMF (3 ml) wurde Kaliumcarbonat (0.150 g) und Lithiumperchlorat (0.083 g) gegeben und bei 800C über Nacht gerührt. Nach dem Abkühlen wurde die Lösung filtriert und eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1) gereinigt und lieferte das gewünschte Produkt (304 mg) .To a solution of epoxide (14b) (150 mg) and protected piperidine (51h) (293 mg) in DMF (3 ml) of potassium carbonate (0.150 g) and lithium perchlorate was added (0.083 g) and stirred at 80 0 C overnight. After cooling, the solution was filtered and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1) to give the desired product (304 mg).
MS (EI) : m/z: 594 [M+H]+ MS (EI): m / z: 594 [M + H] +
51j ) Titelverbindung
Zu einer Lösung von Silylether (5Ii) (304 mg) in Acetonitril (1 ml) wurde 2.5N wässrige Flusssäure (0.62 ml) bei 00C gegeben und 1 Stunde gerührt. Danach wurde mit 3N Natronlauge (1 ml) basisch gemacht und die Lösung eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1 + 1% Ammoniak) gereinigt und lieferte das gewünschte Produkt (112 mg) .51j) Title compound To a solution of silyl ether (5ii) (304 mg) in acetonitrile (1 ml) 2.5N aqueous hydrofluoric acid (0.62 ml) was added at 0 0 C and stirred for 1 hour. It was then basified with 3N sodium hydroxide solution (1 ml) and the solution was concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1 + 1% ammonia) to afford the desired product (112 mg).
MS (EI) : m/z: 480 [M+H] + MS (EI): m / z: 480 [M + H] +
Bespiel 52: 6- ( {1- [2-Hydroxy-2- (3-methoxy-chinolin-5-yl) ethyl] -3-hydro:κymethyl-piperidin-4-ylamino} -methyl) -4H- benzo[l,4]oxazin-3-on (Racemat)Example 52: 6- ({1- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) ethyl] -3-hydro: κ-methyl-piperidin-4-ylamino} -methyl) -4 H -benzo [ l, 4] oxazin-3-one (racemate)
Das Piperidin (6-{ [3- ( tert-Butyl-dimethyl-silanyloxy- methyl) -piperidin-4-ylamino] -methyl}-4H-benzo [1 , 4]oxazin-3- on) wurde analog zu den Schritten 51g bis 51h aus AldehydThe piperidine (6- {[3- (tert-butyl-dimethyl-silanyloxymethyl) -piperidin-4-ylamino] -methyl} -4 H -benzo [1,4] oxazin-3-one) was analogous to the steps 51g to 51h from aldehyde
(Ij) hergestellt.(Ij).
Die Titelverbindung wurde wie in Beispiel 51i bis 51j ausThe title compound was as in Example 51i to 51j from
Epoxid (14b) und 6-{ [3- (tert-Butyl-dimethyl-silanyloxy- methyl) -piperidin-4-ylamino] -methyl} -4H-benzo [1 , 4]oxazin-3- on hergestellt.Epoxide (14b) and 6- {[3- (tert-butyl-dimethyl-silanyloxymethyl) -piperidin-4-ylamino] -methyl} -4 H -benzo [1,4] oxazin-3-one.
MS (EI) : m/z: 493 [M+H]+
Beispiel 53 : 1- ( 3 -Methoxy-chinolin-5-yl ) -2- {4- [3- ( thiophen- 2-ylsulfanyl ) -propyl] -piperazin-l-yl} -ethanolMS (EI): m / z: 493 [M + H] + Example 53: 1- (3-Methoxy-quinolin-5-yl) -2- {4- [3- (thiophen-2-ylsulfanyl) -propyl] -piperazin-1-yl} -ethanol
53a) 2- (3-Brom-propylsulfanyl) -thiophen53a) 2- (3-Bromo-propylsulfanyl) thiophene
Zu einer Lösung von Thiophenthiol (2.5 g) und Natriumhydroxid (2 g) in Wasser (10 ml) wurde 1,3-To a solution of thiophene thiol (2.5 g) and sodium hydroxide (2 g) in water (10 ml) was added 1.3-
Dibrompropan (6.59 ml) gegeben und über Nacht auf 800C erhitzt. Nach dem Abkühlen wurde mit Ether verdünnt, die Phasen getrennt und die wässrige Phase mit Ether extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Hexan) gereinigt und lieferte das gewünschte Produkt (2.37 g) .Optionally dibromopropane (6:59 ml) and heated overnight at 80 0C. After cooling, it was diluted with ether, the phases were separated and the aqueous phase was extracted with ether. The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, hexane) to afford the desired product (2.37 g).
MS (EI): m/z: 238 [M+H]+ MS (EI): m / z: 238 [M + H] +
53b) 4- [3- (Thiophen-2-ylsulfanyl) -propyl] -piperazin-1- carbonsäure-tert-butylester53b) tert-butyl 4- [3- (thiophen-2-ylsulfanyl) -propyl] -piperazine-1-carboxylate
Zu einer Lösung von Piperazin-1-carbonsäure-tert-butylester (0.43 g) and Bromid (53a) (0.5 g) in DMF (5 ml) wurdeTo a solution of piperazine-1-carboxylic acid tert -butyl ester (0.43 g) and bromide (53a) (0.5 g) in DMF (5 ml) was added
Kaliumcarbonat (0.4 g) gegeben und für 14 Stunden auf 600C erhitzt. Dann wurde die Lösung eingeengt und der Rückstand mittels Flash-Chromatographie (Kieselgel,
Dichlormethan/Methanol 9:1) gereinigt und lieferte das gewünschte Produkt (500 mg) .Potassium carbonate (0.4 g) and heated to 60 0 C for 14 hours. The solution was then concentrated and the residue was purified by flash chromatography (silica gel, Dichloromethane / methanol 9: 1) to afford the desired product (500 mg).
MS (EI) : m/z: 343 [M+H]+ MS (EI): m / z: 343 [M + H] +
53c) 1- [3- (Thiophen-2-ylsulfanyl) -propyl] -piperazin53c) 1- [3- (thiophen-2-ylsulfanyl) -propyl] -piperazine
Eine Lösung aus geschütztem Piperazin (53b) (0.5 g) in TFA (5 ml) wurde für 20 Minuten bei Raumtemperatur gerührt. Nach dem Einengen wurde der Rückstand in IN Natronlauge (30 ml) aufgenommen und mit Dichlormethan (3 x 30 ml) extrahiert. Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt und lieferten das gewünschte Produkt (346 mg) .A solution of protected piperazine (53b) (0.5 g) in TFA (5 ml) was stirred for 20 minutes at room temperature. After concentration, the residue was taken up in 1N sodium hydroxide solution (30 ml) and extracted with dichloromethane (3 x 30 ml). The combined organic phases were dried over sodium sulfate, filtered and concentrated to afford the desired product (346 mg).
MS (EI): m/z: 243 [M+H]+ MS (EI): m / z: 243 [M + H] +
53d) Titelverbindung53d) title compound
Zu einer Lösung von Epoxid (14b) (0.1 g) and Piperazin (53c) (0.130 g) in DMF (5 ml) wurde Lithiumperchlorat (0.06 g) und Kaliumcarbonat (0.1 g) gegeben und für 2 Stunden auf 400C erhitzt. Dann wurde die Lösung eingeengt und der Rückstand mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 19:1) gereinigt und lieferte das gewünschte Produkt.To a solution of epoxide (14b) (0.1 g) and piperazine (53c) (0.130 g) in DMF (5 ml) was added lithium perchlorate (0.06 g) and potassium carbonate (0.1 g) and heated at 40 ° C. for 2 hours. The solution was then concentrated and the residue purified by flash chromatography (silica gel, dichloromethane / methanol 19: 1) to afford the desired product.
MS (EI) : m/z: 444 [M+H]+ MS (EI): m / z: 444 [M + H] +
Beispiel 54: 6- (l-Hydroxy-2-{4- [2-hydroxy-2- (3-methoxy- chinolin-5-yl)-ethyl]-piperazin-l-yl}-ethyl)-4H- benzo[l,4]oxazin-3-on (Racemat)
Example 54: 6- (1-Hydroxy-2- {4- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperazin-1-yl} -ethyl) -4H-benzo [1,4] oxazin-3-one (racemate)
54a) 4- [2-Hydroxy-2- (3-oxo-3,4-dihydro-2H-benzo[l,4]oxazin- 6-yl) -ethyl] -piperazin-1-carbonsäurebenzylester Zu einer Löung von Piperazin-1-carbonsäurebenzylester (2.2 g) in Ethanol (20 ml) und Acetonitril (10 ml) wurde 6- (2- Chloro-acetyl) -4H-benzo[l, 4] oxazin-3-on (2.25 g) und Triethylamin (1.67 ml) gegeben und für 3 Stunden auf 65°C erhitzt. Dann wurde die Lösung eingeengt und der Rückstand in Methanol (30 ml) aufgenommen. Nach Abkühlen auf 00C wurde portionsweise Natriumborhydrid (2 g) zugegeben und für 30 Minuten gerührt. Dann wurde Wasser (20 ml) hinzugegeben und die Lösung partiell eingeengt. Der Rückstand wurde mit Essigester (3 x 100 ml) extrahiert. Die vereinigten organischen Phasen wurden mit ges .54a) 4- [2-Hydroxy-2- (3-oxo-3,4-dihydro-2H-benzo [l, 4] oxazin-6-yl) -ethyl] -piperazine-1-carboxylic acid benzyl ester To a solution of piperazine Benzyl -1-carboxylate (2.2 g) in ethanol (20 ml) and acetonitrile (10 ml) gave 6- (2-chloro-acetyl) -4 H -benzo [1,4] oxazin-3-one (2.25 g) and triethylamine (1.67 ml) and heated to 65 ° C for 3 hours. Then, the solution was concentrated and the residue was taken up in methanol (30 ml). After cooling to 0 0 C sodium borohydride in portions, was added (2 g) and stirred for 30 minutes. Then, water (20 ml) was added and the solution was partially concentrated. The residue was extracted with ethyl acetate (3 x 100 ml). The combined organic phases were washed with sat.
Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 19:1) gereinigt und lieferte das gewünschte Produkt (2 g) .Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 19: 1) to afford the desired product (2 g).
MS (EI) : m/z: 412 [M+H]+ MS (EI): m / z: 412 [M + H] +
54b) 6- (l-Hydroxy-2-piperazin-l-yl-ethyl) -4H- benzo [1,4] oxazin-3-on54b) 6- (1-Hydroxy-2-piperazin-1-yl-ethyl) -4H-benzo [1,4] oxazin-3-one
Zu einer Lösung des geschützten Piperazins (54a) (3 g) in Essigester (100 ml) wurde 10% Palladium auf Kohle (1.5 g) gegeben. Die Reaktionsmischung wurde bei Raumtemperatur über Nacht unter einer Wasserstoffatmosphäre gerührt, dann
filtriert und eingegeengt und lieferte das gewünschte Produkt (2 g) .To a solution of the protected piperazine (54a) (3 g) in ethyl acetate (100 ml) was added 10% palladium on carbon (1.5 g). The reaction mixture was stirred at room temperature overnight under a hydrogen atmosphere, then filtered and concentrated to give the desired product (2 g).
MS (EI) : m/z: 278 [M+H]+ MS (EI): m / z: 278 [M + H] +
54c) Titelverbindung54c) Title compound
Die Titelverbindung wurde wie in Beispiel 53d aus Epoxid (14b) und Piperazin (54b) hergestellt.The title compound was prepared as in Example 53d from epoxide (14b) and piperazine (54b).
MS (EI): m/z: 479 [M+H]+ MS (EI): m / z: 479 [M + H] +
Beispiel 55: 6- (l-Hydroxy-2-{4- [2-hydroxy-2- (3-methoxy- chinolin-5-yl) -ethyl] -piperazin-l-yl}-ethyl) -4H- benzo[l,4] thiazin-3-on (Racemat)Example 55: 6- (1-Hydroxy-2- {4- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperazin-1-yl} -ethyl) -4H-benzo [l, 4] thiazine-3-one (racemate)
Das Piperazin (6- (l-Hydroxy-2-piperazin-l-yl-ethyl) -4H- benzo[l, 4] thiazin-3-on) wurde analog zu den Schritten 54a bis 54b aus 6- (2-Chlor-acetyl) -4H-benzo [1, 4] thiazin-3-on hergestellt.The piperazine (6- (1-hydroxy-2-piperazin-1-yl-ethyl) -4H-benzo [l, 4] thiazine-3-one) was prepared analogously to steps 54a to 54b from 6- (2-chloro -acetyl) -4H-benzo [1, 4] thiazine-3-one.
Die Titelverbindung wurde wie in Beispiel 54c aus EpoxidThe title compound was made from epoxide as in Example 54c
(14b) und 6- (l-Hydroxy-2-piperazin-l-yl-ethyl) -4H- benzo[l, 4] thiazin-3-on hergestellt.(14b) and 6- (1-hydroxy-2-piperazin-1-yl-ethyl) -4H-benzo [l, 4] thiazine-3-one.
MS (EI): m/z: 495 [M+H]+
Beispiel 56 : 2 - {4- [ 2 - ( 2 , 3-Dihydro-benzo [ 1 , 4 ] dioxin-6-yl ) -2- hydroxy-ethyl] -piperazin-l-yl} -l- (3-methoxy-chinolin-5-yl) ■ ethanol (Enantiomer 1 )MS (EI): m / z: 495 [M + H] + Example 56: 2 - {4- [2 - (2,3-Dihydro-benzo [1,4] dioxin-6-yl) -2-hydroxy-ethyl] -piperazin-1-yl} -l- (3 methoxy-quinolin-5-yl) ■ ethanol (enantiomer 1)
Das Piperazin (1- (2 , 3-Dihydro-benzo [1, 4] dioxin-6-yl) -2- piperazin-1-yl-ethanol) wurde analog zu den Schritten 54a bis 54b aus 2-Chlor-l- (2 , 3-dihydro-benzo [1, 4] dioxin-6-yl) - ethanon hergestellt.The piperazine (1- (2,3-dihydro-benzo [1,4] dioxin-6-yl) -2-piperazin-1-yl-ethanol) was prepared analogously to steps 54a to 54b from 2-chloro-1-one (2, 3-dihydro-benzo [1, 4] dioxin-6-yl) -ethanone produced.
Die Titelverbindung wurde wie in Beispiel 54c aus Epoxid (14b) und 1- (2 , 3-Dihydro-benzo [1, 4] dioxin-6-yl) -2- piperazin-1-yl-ethanol hergestellt .The title compound was prepared as in Example 54c from epoxide (14b) and 1- (2,3-dihydro-benzo [1,4] dioxin-6-yl) -2-piperazin-1-yl-ethanol.
MS (EI): m/z: 466 [M+H]+ MS (EI): m / z: 466 [M + H] +
Beispiel 57: 5- {2- [4- (2, 3-Dihydro-benzo [1,4] dioxin-6- ylmethyl) -piperazin-1-yl] -ethoxy}-3-methoxy-chinolinExample 57: 5- {2- [4- (2,3-Dihydro-benzo [1,4] dioxin-6-ylmethyl) -piperazin-1-yl] -ethoxy} -3-methoxy-quinoline
57a) 3-Methoxy-5- (4, 4, 5, 5-tetramethyl [1,3,2] dioxaborolan-2- yl) -chinolin
Zu einer Mischung aus Bis (pinacolato) diboron (6.14 g) , 1 , 1 '-Bis (diphenylphosphino) ferrocen-palladium(II) dichlorid- Dichlormethan-Komplex (1.475 g) und Kaliumacetat (5.93 g) wurde eine Lösung von Ib (4.8 g) in DMSO (145 ml) gegeben. Die Reaktionsmischung wurde über Nacht bei 8O0C gerührt. Nach dem Abkühlen auf Raumtemperatur wurde die Reaktionsmischung mit Wasser (300 ml) und Essigester (300 ml) verdünnt. Die Phasen wurden getrennt und die wässrige Phase wurde mit Essigester extrahiert (2 x 300 ml) . Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der braune Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 1:4) gereinigt und lieferte das gewünschte Produkt (4.65 g) .57a) 3-Methoxy-5- (4, 4, 5, 5-tetramethyl [1,3,2] dioxaborolan-2-yl) -quinoline To a mixture of bis (pinacolato) diboron (6.14 g), 1,1'-bis (diphenylphosphino) ferrocene palladium (II) dichloride-dichloromethane complex (1475 g) and potassium acetate (5.93 g) was added a solution of Ib ( 4.8 g) in DMSO (145 ml). The reaction mixture was stirred at 8O 0 C overnight. After cooling to room temperature, the reaction mixture was diluted with water (300 ml) and ethyl acetate (300 ml). The phases were separated and the aqueous phase was extracted with ethyl acetate (2 x 300 ml). The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The brown residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 4) to afford the desired product (4.65 g).
MS (EI) : m/z: 286 [M+H]+ MS (EI): m / z: 286 [M + H] +
57b) 3-Methoxy-chinolin-5-ol Zu einer eisgekühlten Lösung von 57a (4.6 g) in THF (110 ml) wurde 3N Natronlauge (13 ml) getropft. Anschliessend wurde 30%ige wässrige Wasserstoffperoxid- Lösung (5.6 ml) zugetropft und die Reaktionsmischung eine Stunde bei 00C gerührt. Das Reaktionsgemisch wurde in Wasser (100 ml) aufgenommen und einmal mit Essigester57b) 3-Methoxy-quinolin-5-ol To an ice-cooled solution of 57a (4.6 g) in THF (110 ml) was added dropwise 3N sodium hydroxide solution (13 ml). Subsequently, 30% aqueous hydrogen peroxide solution (5.6 ml) was added dropwise and the reaction mixture stirred at 0 0 C for one hour. The reaction mixture was taken up in water (100 ml) and once with ethyl acetate
(200 ml) extrahiert. Der pH der wässrigen Phase wurde auf 4 mit IN Salzsäure eingestellt und anschliessend mit Essigester extrahiert (3x 100 ml) . Die organischen Phasen wurden vereinigt, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash- Chromatographie (Kieselgel, Dichlormethan/Methanol 29:1) gereinigt und lieferte das gewünschte Produkt (2.82 g) .
MS (EI) : m/z: 176 [M+H]+ (200 ml) extracted. The pH of the aqueous phase was adjusted to 4 with 1N hydrochloric acid and then extracted with ethyl acetate (3 × 100 ml). The organic phases were combined, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 29: 1) to afford the desired product (2.82 g). MS (EI): m / z: 176 [M + H] +
57c) 4- (2-Hydroxy-ethyl) -piperazin-1-carbonsäure- benzylester57c) 4- (2-hydroxy-ethyl) -piperazine-1-carboxylic acid benzyl ester
Zu einer Lösung von Hydroxyethylpiperazin (13 ml) in Aceton (200 ml) wurde unter heftigem Rühren eine 10%ige Natrium- hydrogencarbonat-Lösung (254 ml) gegeben. Anschliessend wurde auf 00C gekühlt und Benzylchloroformat (17.92 ml) zugetropft. Die Reaktionsmischung wurde 4 Stunden beiTo a solution of hydroxyethylpiperazine (13 ml) in acetone (200 ml) was added, with vigorous stirring, a 10% sodium bicarbonate solution (254 ml). Then was cooled to 0 0 C and added dropwise benzyl chloroformate (17.92 ml). The reaction mixture was allowed to stand for 4 hours
Raumtemperatur gerührt. Nach dem Entfernen des Acetons im Vakuum wurde die wässrige Phase mit Essigester (3x 250 ml) extrahiert. Die vereinigten organischen Phasen wurden einmal mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert, eingeengt und lieferten das gewünschte Produkt (28.2 g) .Room temperature stirred. After removal of the acetone in vacuo, the aqueous phase was extracted with ethyl acetate (3x 250 ml). The combined organic phases were washed once with sat. Sodium chloride solution, dried over sodium sulfate, filtered, concentrated and afforded the desired product (28.2 g).
MS (EI): m/z: 265 [M+H]+ MS (EI): m / z: 265 [M + H] +
57d) 4-(2-Methansulfonyloxy-ethyl)-piperazin-l-carbonsäure- benzylester57d) 4- (2-methanesulfonyloxy-ethyl) -piperazine-1-carboxylic acid benzyl ester
Eine Lösung von 57c (2.0 g) in Dichlormethan (10 ml) wurde auf 00C gekühlt und mit Triethylamin (1.27 ml) und Methansulfonylchlorid (706 μl) versetzt. Die Lösung wurde auf Raumtemperatur aufgetaut und dann 30 Minuten gerührt. DieA solution of 57c (2.0 g) in dichloromethane (10 ml) was cooled to 0 ° C. and treated with triethylamine (1.27 ml) and methanesulfonyl chloride (706 μl). The solution was thawed to room temperature and then stirred for 30 minutes. The
Reaktionsmischung wurde mit Dichlormethan verdünnt und dann nacheinander mit ges. Natriumhydrogencarbonatlösung, Wasser und ges. Natriumchloridlösung gewaschen. Durch Einengen wurde das gewünschte Produkt (2.57 g) erhalten.Reaction mixture was diluted with dichloromethane and then washed successively with sat. Sodium bicarbonate solution, water and sat. Washed sodium chloride solution. Concentration gave the desired product (2.57 g).
MS (EI) : m/z: 343 [M+H]+
57e) 4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] -piperazin-1- carbonsäure-benzylesterMS (EI): m / z: 343 [M + H] + 57e) 4- [2- (3-methoxy-quinolin-5-yloxy) -ethyl] -piperazine-1-carboxylic acid benzyl ester
Verbindung (57b) (350 mg) wurde in DMF (2 ml) gelöst und bei Raumtemperatur mit Natriumhydrid (87 mg) versetzt. Nach 10 Minuten Rühren wurde langsam eine Lösung von VerbindungCompound (57b) (350 mg) was dissolved in DMF (2 ml) and sodium hydride (87 mg) was added at room temperature. After stirring for 10 minutes, a solution of compound became slowly
(57d) (684 mg) in DMF (2 ml) zugetropft. Die Reaktionsmischung wurde über Nacht bei Raumtemperatur gerührt, dann in Wasser aufgenommen und mit Essigester extrahiert (3 x 5 ml) . Die vereinigten organischen Phasen wurden mehrmals mit Wasser gewaschen, über Natriumsulfat getrocknet, filtriert, eingeengt und lieferten das gewünschte Produkt(57d) (684 mg) in DMF (2 ml) was added dropwise. The reaction mixture was stirred overnight at room temperature, then taken up in water and extracted with ethyl acetate (3 x 5 ml). The combined organic phases were washed several times with water, dried over sodium sulfate, filtered, concentrated and afforded the desired product
(320 mg) .(320 mg).
MS (EI): m/z: 422 [M+H]+ MS (EI): m / z: 422 [M + H] +
57f) 3-Methoxy-5- (2-piperazin-l-yl-ethoxy) -chinolin57f) 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline
Zu einer Lösung von Verbindung (57e) (250 mg) in Essigester (25 ml) und Methanol (25 ml) wurde 10% Palladium auf Kohle (50 mg) gegeben und 4 Stunden unter einer Wasserstoff- atmosphäre gerührt. Die Lösung wurde filtriert, eingeengt und lieferte das gewünschte Produkt.To a solution of compound (57e) (250 mg) in ethyl acetate (25 ml) and methanol (25 ml) was added 10% palladium on carbon (50 mg) and stirred for 4 hours under a hydrogen atmosphere. The solution was filtered, concentrated and afforded the desired product.
MS (EI) : m/z: 288 [M+H]+ MS (EI): m / z: 288 [M + H] +
57g) Titelverbindung57g) Title compound
Die Verbindung wurde wie in Beispiel Ik aus 3-Methoxy-5- (2- piperazin-1-yl-ethoxy) -chinolin (57f) und 2,3-Dihydro- benzo [1 , 4] dioxin-6-carbaldehyd in 66% Ausbeute hergestellt.The compound was prepared as in Example Ik from 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline (57f) and 2,3-dihydro-benzo [1, 4] dioxin-6-carbaldehyde in 66 % Yield produced.
MS (EI): m/z: 436 [M+H] +
Beispiel 58: 6-{4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] piperazin-1-ylmethyl} -4H-benzo [1, 4] oxazin-3-onMS (EI): m / z: 436 [M + H] + Example 58: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) -ethyl] piperazin-1-ylmethyl} -4 H -benzo [1,4] oxazin-3-one
Die TitelVerbindung wurde wie in Beispiel 57g aus Aldehyd (Ij) in 71% Ausbeute hergestellt.The title compound was prepared as in Example 57g from aldehyde (Ij) in 71% yield.
MS (EI): m/z: 449 [M+H]+ MS (EI): m / z: 449 [M + H] +
Beispiel 59: 6-{4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] - piperazin-1-ylmethyl} -4H-benzo [1,4] thiazin-3-onExample 59: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) -ethyl] -piperazin-1-ylmethyl} -4 H -benzo [1,4] thiazine-3-one
Die Titelverbindung wurde wie in Beispiel 57g aus Aldehyd (4b) in 56% Ausbeute hergestellt.The title compound was prepared as in Example 57g from aldehyde (4b) in 56% yield.
MS (EI): m/z: 465 [M+H]+ MS (EI): m / z: 465 [M + H] +
Beispiel 60: 6-{4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] - piperazin-1-ylmethyl}-4H-pyrido[3, 2-b] [1,4] thiazin-3-on
Example 60: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) -ethyl] -piperazin-1-ylmethyl} -4 H -pyrido [3, 2-b] [1,4] thiazine one 3-
Die Titelverbindung wurde wie in Beispiel 57g aus Aldehyd (2h) in 80% Ausbeute hergestellt.The title compound was prepared as in Example 57g from aldehyde (2h) in 80% yield.
MS (EI): m/z: 466 [IYH-H] + MS (EI): m / z: 466 [IYH-H] +
Beispiel 61: 5- (2-{4- [ (E) -3- (2,5-Difluor-phenyl) -allyl] piperazin-l-yl}-ethoxy) -3-methoxy-chinolinExample 61: 5- (2- {4- [(E) -3- (2,5-Difluoro-phenyl) -allyl] -piperazin-1-yl} -ethoxy) -3-methoxy-quinoline
Die Titelverbindung wurde wie in Beispiel 57g aus (E) -3- (2,5-Difluor-phenyl)-propenal (wurde nach WO2004/087647 hergestellt) hergestellt.The title compound was prepared as in Example 57g from (E) -3- (2,5-difluoro-phenyl) -propenal (prepared according to WO2004 / 087647).
MS (EI): m/z: 440 [M+H]+ MS (EI): m / z: 440 [M + H] +
Beispiel 62: 3-Methoxy-5- [2- (4-naphthalin-2-ylmethyl- piperazin-1-yl) -ethoxy] -chinolin
Example 62: 3-Methoxy-5- [2- (4-naphthalen-2-ylmethylpiperazin-1-yl) -ethoxy] -quinoline
Die Titelverbindung wurde wie in Beispiel 57g aus Naphthalin-2-carbaldehyd hergestellt .The title compound was prepared from naphthalene-2-carbaldehyde as in Example 57g.
MS (EI): m/z: 428 [M+H]+ MS (EI): m / z: 428 [M + H] +
Beispiel 63: 3-Methoxy-5- (2-{4- [2- (thiophen-2-yl-sulfanyl) ethyl] -piperazin-l-yl}-ethoxy) -chinolinExample 63: 3-Methoxy-5- (2- {4- [2- (thiophen-2-yl-sulfanyl) -ethyl] -piperazin-1-yl} -ethoxy) -quinoline
63a) 2- (2-Brom-ethylsulfanyl) -thiophen Die Verbindung wurde wie in Beispiel 53a aus 1,2-Dibrom- ethan hergestellt.63a) 2- (2-Bromoethylsulfanyl) thiophene The compound was prepared from 1,2-dibromoethane as in Example 53a.
MS (EI) : m/z: 224 [M+H]+ MS (EI): m / z: 224 [M + H] +
63b) Titelverbindung63b) Title compound
Die Verbindung wurde wie in Beispiel 53b aus 3-Methoxy-5- (2-piperazin-l-yl-ethoxy) -chinolin (57f)und 2-(2-Brom- ethylsulfanyl) -thiophen (63a) in 86% Ausbeute hergestelltThe compound was prepared as in Example 53b from 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline (57f) and 2- (2-bromo-ethylsulfanyl) -thiophene (63a) in 86% yield
MS (EI) : m/z: 430 [M+H]+
Beispiel 64: 6-{4- [2- (3-Methoxy-chinolin-5-yloxy)-ethyl] piperazin-l-carbonyl}-4H-benzo[l,4] thiazin-3-onMS (EI): m / z: 430 [M + H] + Example 64: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) -ethyl] piperazine-1-carbonyl} -4H-benzo [l, 4] thiazine-3-one
Die TitelVerbindung wurde wie in Beispiel 33 aus 3-Methoxy- 5- (2-piperazin-l-yl-ethoxy) -chinolin (57f)und 3-Oxo-3,4- dihydro-2H-benzo[l, 4] thiazin-6-carbonsäure hergestellt.The title compound was prepared as in Example 33 from 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline (57f) and 3-oxo-3,4-dihydro-2H-benzo [l, 4] thiazine -6-carboxylic acid prepared.
MS (EI): m/z: 479 [M+H]+ MS (EI): m / z: 479 [M + H] +
Beispiel 65: 6- {4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] piperazin-1-carbonyl} -4H-benzo [1,4] oxazin-3-onExample 65: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) ethyl] piperazine-1-carbonyl} -4 H -benzo [1,4] oxazin-3-one
Die Titelverbindung wurde wie in Beispiel 33 aus 3-Methoxy- 5- (2-piperazin-l-yl-ethoxy) -chinolin (57f)und 3-Oxo-3,4- dihydro-2H-benzo[l, 4] oxazin-6-carbonsäure hergestellt.The title compound was prepared as in Example 33 from 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline (57f) and 3-oxo-3,4-dihydro-2H-benzo [1,4] oxazine -6-carboxylic acid prepared.
MS (EI) : m/z: 463 [M+H]+
Beispiel 66: 6-{4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] piperazin-l-sulfonyl}-4H-benzo[l#4] thiazin-3-onMS (EI): m / z: 463 [M + H] + Example 66: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) ethyl] piperazine-1-sulfonyl} -4H-benzo [l # 4] thiazine-3-one
Die Verbindung wurde wie in Beispiel 37 aus 3-Methoxy-5- (2- piperazin-1-yl-ethoxy) -chinolin (57f) und 3-Oxo-3,4- dihydro-2H-benzo[l, 4] thiazin-6-sulfonylchlorid hergestellt,The compound was prepared as in Example 37 from 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline (57f) and 3-oxo-3,4-dihydro-2H-benzo [l, 4] thiazine -6-sulfonyl chloride,
MS (EI) : m/z: 515 [M+H]+ MS (EI): m / z: 515 [M + H] +
Beispiel 67: 6-{4- [2- (3-Methoxy-chinolin-5-yloxy) -ethyl] piperazin-l-sulfonyl}-4H-benzo[l,4]oxazin-3-onExample 67: 6- {4- [2- (3-Methoxy-quinolin-5-yloxy) -ethyl] piperazine-1-sulfonyl} -4H-benzo [1,4-oxazin-3-one
Die Titelverbindung wurde wie in Beispiel 37 aus 3-Methoxy- 5- (2-piperazin-l-yl-ethoxy) -chinolin (57f) und 3-Oxo-3,4- dihydro-2H-benzo[l, 4] oxazin-6-sulfonylchlorid hergestellt.
MS (EI) : m/z: 499 [M+H]+ The title compound was prepared as in Example 37 from 3-methoxy-5- (2-piperazin-1-yl-ethoxy) -quinoline (57f) and 3-oxo-3,4-dihydro-2H-benzo [1,4] oxazine -6-sulfonyl chloride. MS (EI): m / z: 499 [M + H] +
Beispiel 68: 2-{4- [2- (2, 3-Dihydro-benzo[l,4]dioxin-6-yl) - ethyl] -piperazin-l-yl}-l- (3-methoxy-chinolin-5-yl) -ethanol (Enantiomer 1)Example 68: 2- {4- [2- (2,3-Dihydro-benzo [l, 4] dioxin-6-yl) -ethyl] -piperazin-1-yl} -1- (3-methoxyquinoline) 5-yl) -ethanol (enantiomer 1)
68a) 6-Vinyl-2,3-dihydro-benzo[l,4]dioxin68a) 6-vinyl-2,3-dihydrobenzo [l, 4] dioxin
Eine Lösung von Methyltriphenylphosphoniumbromid (13.2 g) in THF (120 ml) wurde auf -78°C abgekühlt, dann wurde Butyllithium (15 ml, 2.5M Lösung in Hexan) zugegeben, anschliessend 15 Minuten bei -78°C gerührt und dann 45 Minuten bei 00C. Nach Abkühlen auf -780C wurde eine Lösung von 2, 3-Dihydro-benzo[l, 4]dioxin-6-carbaldehyd (5 g) in THF (20 ml) zugegeben, auf Raumtemperatur erwärmt und 2 Stunden gerührt. Die Reaktionsmischung wurde mit Essigester (3 x 100 ml) und die vereinigten organischen Phasen mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 1:6) gereinigt und lieferte das gewünschte Produkt (3.9 g) .A solution of methyltriphenylphosphonium bromide (13.2g) in THF (120ml) was cooled to -78 ° C, then butyllithium (15ml, 2.5M solution in hexane) was added, then stirred at -78 ° C for 15 minutes and then 45 minutes at 0 0 C. After cooling to -78 0 C a solution of 2, 3-dihydro-benzo was [l, 4] dioxin-6-carbaldehyde was added (5 g) in THF (20 ml), warmed to room temperature and 2 Hours stirred. The reaction mixture was washed with ethyl acetate (3 x 100 ml) and the combined organic phases with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 6) to afford the desired product (3.9 g).
MS (EI) : m/z: 163 [M+H]+ MS (EI): m / z: 163 [M + H] +
68b) 2-(2,3-Dihydro-benzo[l,4]dioxin-6-yl)-ethanol
Zu einer Lösung der Vinylverbindung (68a) (5 g) in THF (100 ml) wurde 9-BBN (2.2 g) gegeben und 16 Stunden bei Raumtemperatur gerührt. Dann wurde auf 00C abgekühlt und Ethanol (20 ml), 3N Natronlauge (110 ml) and 30% Wasserstoffperoxidlösung (110 ml) zugegeben. Die68b) 2- (2,3-dihydro-benzo [l, 4] dioxin-6-yl) -ethanol To a solution of the vinyl compound (68a) (5 g) in THF (100 ml) was added 9-BBN (2.2 g) and stirred at room temperature for 16 hours. It was then cooled to 0 ° C. and ethanol (20 ml), 3N sodium hydroxide solution (110 ml) and 30% hydrogen peroxide solution (110 ml) were added. The
Reaktionsmischung wurde 1 Stunde bei Raumtemperatur gerührt, dann mit 10% Natriumsulfitlösung (120 ml) versetzt und weitere 30 Minuten gerührt. Die Phasen wurden getrennt und die wässrige Phase mit Essigester (2 x 100 ml) extrahiert. Die vereinigten organischen Phasen wurden mit ges . Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 2:1) gereinigt und lieferte das gewünschte Produkt (3.75 g) .The reaction mixture was stirred for 1 hour at room temperature, then treated with 10% sodium sulfite solution (120 ml) and stirred for a further 30 minutes. The phases were separated and the aqueous phase extracted with ethyl acetate (2 x 100 ml). The combined organic phases were washed with sat. Washed sodium chloride solution, dried over sodium sulfate, filtered and concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 2: 1) to afford the desired product (3.75 g).
MS (EI) : m/z: 181 [M+H]+ MS (EI): m / z: 181 [M + H] +
68c) Toluol-4-sulfonsäure-2- (2,3-dihydro-benzo[l,4]dioxin- 6-yl)-ethylester68c) toluene-4-sulfonic acid 2- (2,3-dihydro-benzo [l, 4] dioxin-6-yl) -ethyl ester
Zu einer Lösung von Alkohol (68b) (3.55 g) in Dichlormethan (70 ml) wurden bei 00C DMAP (4.2 g) und Tosylchlorid (4.13 g) gegeben. Die Lösung wurde 20 Minuten bei 00C gerührt und dann auf Raumtemperatur erwärmt. Nach 2 Stunden wurde die Lösung eingeengt, der Rückstand mittels Flash- Chromatographie (Kieselgel, Essigester/Hexan 1:3) gereinigt und lieferte das gewünschte Produkt (3.23 g) .To a solution of alcohol (68b) (3.55 g) in dichloromethane (70 ml) was added (4.13 g) at 0 0 C. DMAP (4.2 g) and tosyl chloride. The solution was stirred for 20 minutes at 0 0 C and then warmed to room temperature. After 2 hours, the solution was concentrated, the residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 1: 3) to afford the desired product (3.23 g).
MS (EI) : m/z: 335 [M+H]+ MS (EI): m / z: 335 [M + H] +
68d) 4-[2-(2,3-Dihydro-benzo[l,4]dioxin-6-yl)-ethyl]- piperazin-1-carbonsäurebenzylester
Zu einer Lösung des Tosylats (68c) (0.7 g) in DMF (10 ml) wurde Piperazin-1-carbonsäurebenzylester (0.49 g) und Triethylamin (1 ml) gegeben. Die Reaktionsmischung wurde für 16 Stunden auf 600C erhitzt und dann eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Essigester/Hexan 2:1) gereinigt und lieferte das gewünschte Produkt (0.6 g) .68d) 4- [2- (2,3-dihydro-benzo [l, 4] dioxin-6-yl) -ethyl] -piperazine-1-carboxylic acid benzyl ester To a solution of the tosylate (68c) (0.7g) in DMF (10ml) was added piperazine-1-carboxylic acid benzyl ester (0.49g) and triethylamine (1ml). The reaction mixture was heated at 60 ° C. for 16 hours and then concentrated. The residue was purified by flash chromatography (silica gel, ethyl acetate / hexane 2: 1) to afford the desired product (0.6 g).
MS (EI) : m/z: 383 [M+H]+ MS (EI): m / z: 383 [M + H] +
68e) 1- [2-(2,3-Dihydro-benzo[l,4]dioxin-6-yl)-ethyl] - piperazin68e) 1- [2- (2,3-dihydro-benzo [l, 4] dioxin-6-yl) -ethyl] -piperazine
Zu einer Lösung des geschützten Piperazins (68d) (0.180 g) in Essigester (5 ml) wurde 10% Palladium auf Kohle (0.18 g) gegeben und bei Raumtemperatur 1 Stunde unterTo a solution of the protected piperazine (68d) (0.180 g) in ethyl acetate (5 ml) was added 10% palladium on carbon (0.18 g) and allowed to sit at room temperature for 1 hour
Wasserstoffatmosphäre hydriert. Die Reaktionsmischung wurde filtriert, das FiItrat eingeengt und lieferte das gewünschte Produkt (0.13 g) .Hydrogenated hydrogen atmosphere. The reaction mixture was filtered, the filtrate concentrated and afforded the desired product (0.13 g).
MS (EI): m/z: 249 [M+H]+ MS (EI): m / z: 249 [M + H] +
68f) Titelverbindung68f) title compound
Zu einer Lösung des Epoxids (7a, Enantiomer 1) (0.1 g) und Piperazin (68e) (0.13 g) in DMF (2 ml) wurde Lithiumperchlorat (0.06 g) gegeben und dieTo a solution of the epoxide (7a, enantiomer 1) (0.1 g) and piperazine (68e) (0.13 g) in DMF (2 ml) was added lithium perchlorate (0.06 g) and the
Reaktionsmischung für 4 Stunden auf 600C erhitzt. Dann wurde die Lösung eingeengt und der Rückstand mittels Flash- Chromatographie (Kieselgel, Dichlormethan/Methanol 19:1) gereinigt und lieferte das gewünschte Produkt.Reaction mixture heated to 60 0 C for 4 hours. The solution was then concentrated and the residue purified by flash chromatography (silica gel, dichloromethane / methanol 19: 1) to afford the desired product.
MS (EI) : m/z: 450 [M+H]+
Beispiel 69: 6- (2- {4- [2-Hydroxy-2- (3-methoxy-chinolin-5- yl) -ethyl] -piperazin-l-yl}-ethyl) -4H-benzo [l,4]oxazin-3-on (Enantiomer 1)MS (EI): m / z: 450 [M + H] + Example 69: 6- (2- {4- [2-Hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperazin-1-yl} -ethyl) -4 H -benzo [l, 4 ] oxazin-3-one (enantiomer 1)
Das Piperazin (6- (2-Piperazin-l-yl-ethyl) -4H- benzo[l, 4] oxazin-3-on) wurde analog zu den Schritten 68a bis 68e aus Aldehyd (Ij) hergestellt.The piperazine (6- (2-piperazin-1-yl-ethyl) -4H-benzo [1,4-oxazin-3-one] was prepared analogously to steps 68a to 68e from aldehyde (Ij).
Die TitelVerbindung wurde wie in Beispiel 68f aus Epoxid (7a) und 1- (2 , 3-Dihydro-benzo [1, 4] dioxin-6-yl) -2-piperazin- 1-yl-ethanol hergestellt.The title compound was prepared as in Example 68f from epoxide (7a) and 1- (2,3-dihydro-benzo [1,4] dioxin-6-yl) -2-piperazin-1-yl-ethanol.
MS (EI): m/z: 463 [M+H]+ MS (EI): m / z: 463 [M + H] +
Beispiel 70: 2- [4- (2-Benzo[l,3]dioxol-5-yl-ethyl) - piperazin-1-yl] -1- (3-itιethoxy-chinolin-5-yl) -ethanol (Enantiomer 1)Example 70: 2- [4- (2-Benzo [1,3] dioxol-5-yl-ethyl) -piperazin-1-yl] -1- (3-itethoxy-quinolin-5-yl) -ethanol (enantiomer 1)
Das Piperazin (1- (2-Benzo [1, 3] dioxol-5-yl-ethyl) -piperazin) wurde analog zu den Schritten 68a bis 68e aus The piperazine (1- (2-benzo [1,3-dioxol-5-yl-ethyl) -piperazine) was analogous to steps 68a to 68e
Benzo [1,3] dioxol-5-carbaldehyd hergestellt .Benzo [1,3] dioxole-5-carbaldehyde produced.
Die Titelverbindung wurde wie in Beispiel 68f aus EpoxidThe title compound was made from epoxide as in Example 68f
(7a) und 1- (2-Benzo [1, 3 ] dioxol-5-yl-ethyl) -piperazin hergestellt.(7a) and 1- (2-benzo [1,3] dioxol-5-yl-ethyl) -piperazine.
MS (EI) : m/z: 436 [M+H]+ MS (EI): m / z: 436 [M + H] +
Beispiel 71: l-Cyclopropyl-6-fluor-7-{4- [2-hydroxy-2- (3- methoxy-chinolin-5-yl) -ethyl] -piperazin-l-yl}-4-oxo-l,4- dihydro-chinolin-3-carbonsäureExample 71: 1-Cyclopropyl-6-fluoro-7- {4- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperazin-1-yl} -4-oxo-1 4-dihydro-quinoline-3-carboxylic acid
Epoxid (14a) (50 mg) und Ciprofloxacin (91.4 mg) wurden in DMF (0.2 ml) suspendiert und Kaliumcarbonat (34.3 mg) zugegeben. Das Reaktionsgemsich wurde über Nacht bei 1000C gerührt. Nach dem Abkühlen auf Raumtemperatur wurde das Reaktionsgemsich eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol 9:1) gereinigt. Die eingeengten Fraktionen wurden aus Ether/Dichlormethan umkristallisiert .Epoxide (14a) (50 mg) and ciprofloxacin (91.4 mg) were suspended in DMF (0.2 ml) and potassium carbonate (34.3 mg) added. The Reaktionsgemsich was stirred overnight at 100 0 C. After cooling to room temperature, the reaction mixture was concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane / methanol 9: 1). The concentrated fractions were recrystallized from ether / dichloromethane.
MS (EI) : m/z: 533 [M+H]+
Beispiel 72: l-Cyclopropyl-β-fluor-V- (4-{l- [2-hydroxy-2- (3- methoxy-chinolin-5-yl) -ethyl] -piperidin-4-yl}-piperazin-l- yl) -4-oxo~l#4-dihydro-chinolin-3-carbonsäure (Racexnat)MS (EI): m / z: 533 [M + H] + Example 72: 1-Cyclopropyl-β-fluoro-V- (4- {1- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperidin-4-yl} -piperazine l- yl) -4-oxo ~ l # 4-dihydro-quinoline-3-carboxylic acid (Racexnat)
72a) 4- (4-Benzyl-piperazin-l-yl) -piperidin-1-carbonsäure- tert-butylester72a) 4- (4-Benzyl-piperazin-1-yl) -piperidine-1-carboxylic acid tert-butyl ester
N-tert-Boc-4-piperidinon (5.0 g) und 1-Benzyl-piperazin (4.43 g) wurden in Methanol (60 ml) gelöst und mitN-tert-Boc-4-piperidinone (5.0 g) and 1-benzyl-piperazine (4.43 g) were dissolved in methanol (60 ml) and washed with
Essigsäure (1.58 g) versetzt. Die Mischung wurde 7 Stunden bei Raumtemperatur gerührt. Anschliessend wurden Natrium- cyanoborhydrid (1.89 g) und Methanol (20 ml) zugegeben. Die Mischung wurde über Nacht bei Raumtemperatur gerührt. Nach der Zugabe von Wasser (250 ml) wurde die Mischung mit Essigester extrahiert (4 x 250 ml) . Die vereinigten organischen Phasen wurden über Natriumsulfat getrocknet, filtriert und eingeengt. Der Rückstand wurde mittels MPLC gereinigt und lieferte das gewünschte Produkt (4,52 g) .Acetic acid (1.58 g) was added. The mixture was stirred at room temperature for 7 hours. Subsequently, sodium cyanoborohydride (1.89 g) and methanol (20 ml) were added. The mixture was stirred at room temperature overnight. After the addition of water (250 ml), the mixture was extracted with ethyl acetate (4 x 250 ml). The combined organic phases were dried over sodium sulfate, filtered and concentrated. The residue was purified by MPLC to afford the desired product (4.52 g).
MS (EI) : m/z: 360 [M+H]+ MS (EI): m / z: 360 [M + H] +
72b) 4-Piperazin-l-yl-piperidin-l-carbonsäure-tert- butylester Zu einer Lösung des geschützten Piperazins (72a) (2.05 g) in Methanol (20 ml) wurde 10% Palladiumhydroxid (0.5 g) gegeben und bei Raumtemperatur 48 Stunden unter Wasser-
stoffatmosphäre gerührt. Die Reaktionsmischung wurde filtriert, das FiItrat eingeengt und der Rückstand mittels Flash-Chromatographie (Kieselgel, Dichlormethan/Methanol /Ammoniak 19:0.9:0.1, dann 9:0.9:0.1, dann 4:0.9:0.1, dann 3:1.8:0.2) gereinigt und lieferte das gewünschte Produkt (1.0 mg) .72b) tert-Butyl 4-piperazin-1-yl-piperidine-1-carboxylate To a solution of the protected piperazine (72a) (2.05 g) in methanol (20 ml) was added 10% palladium hydroxide (0.5 g) and at room temperature 48 hours under water stirred atmosphere. The reaction mixture was filtered, the filtrate was concentrated and the residue was purified by flash chromatography (silica gel, dichloromethane / methanol / ammonia 19: 0.9: 0.1, then 9: 0.9: 0.1, then 4: 0.9: 0.1, then 3: 1.8: 0.2). purified and provided the desired product (1.0 mg).
MS (EI): m/z: 270 [M+H] + MS (EI): m / z: 270 [M + H] +
72c) 4-{4-[2-Hydroκy-2-(3-methoxy-chinolin-5-yl)-ethyl]- piperazin-l-yl}-piperidin-l-carbonsäure-tert-butylester72c) tert-butyl 4- {4- [2-hydroxy-2- (3-methoxy-quinolin-5-yl) -ethyl] -piperazine-1-yl} -piperidine-1-carboxylate
Epoxid (14b) (0.39 g) , Piperazin (72b) (0.29 g) , Kalium- carbonat (0.29 g) und Lithiumperchlorat (0.12 g) wurden in trockenem DMF (4 ml) gelöst und unter Stickstoffatmosphäre 24 Stunden bei 1000C gerührt. Die Mischung wurde aufEpoxide (14b) (0.39 g), piperazine (72b) (0.29 g), potassium carbonate (0.29 g) and lithium perchlorate (0.12 g) were dissolved in dry DMF (4 ml) and stirred at 100 ° C. under a nitrogen atmosphere for 24 hours , The mixture was on
Raumtemperatur abgekühlt und eingeengt. Der Rückstand wurde mittels Flash-Chromatographie (Kieselgel, Dichlormethan, dann Dichlormethan/Methanol/Ammoniak 19:0.9:0.1, dann 9:0.9:0.1) gereinigt und lieferte das gewünschte Produkt (472 mg) .Room temperature cooled and concentrated. The residue was purified by flash chromatography (silica gel, dichloromethane, then dichloromethane / methanol / ammonia 19: 0.9: 0.1 then 9: 0.9: 0.1) to afford the desired product (472 mg).
MS (EI): m/z: 471 [M+H]+ MS (EI): m / z: 471 [M + H] +
72d) 1- (3-Methoxy-chinolin-5-yl) -2- (4-piperidin-4-yl- piperazin-1-yl) -ethanol72d) 1- (3-methoxy-quinolin-5-yl) -2- (4-piperidin-4-yl-piperazin-1-yl) -ethanol
Zu einer eisgekühlten Lösung von Bocpiperidin (72c) (317 mg) in Dichlormethan (10 ml) wurde TFA (1.5 ml) zugetropft. Die Mischung wurde 15 Minuten bei 00C gerührt und dann innerhalb von 45 Minuten auf Raumtemperatur aufgetaut. Die Mischung wurde eingeengt , mit Ammoniak basisch gestellt und anschliessend mit Dichlormethan/Methanol (9:1) extrahiert
(5 x 25 ml) . Die vereinigten organischen Phasen wurden eingeengt und lieferten das gewünschte Produkt (93 mg) .To an ice-cooled solution of bocpiperidine (72c) (317 mg) in dichloromethane (10 ml) was added dropwise TFA (1.5 ml). The mixture was stirred for 15 minutes at 0 0 C, and then thawed within 45 minutes to room temperature. The mixture was concentrated, basified with ammonia and then extracted with dichloromethane / methanol (9: 1) (5 x 25 ml). The combined organic phases were concentrated to afford the desired product (93 mg).
MS (EI) : m/z: 371 [M+H]+ MS (EI): m / z: 371 [M + H] +
72e) Titelverbindung72e) Title compound
Amin (72d) (80 mg) und 7-Chlor-l-cyclopropyl-6-fluor-1, 4- dihydro-4-oxo-3-chinolincarbonsäure-Bordiacetat-Komplex (101 mg) wurden in NMP (5 ml) gelöst und N-Ethyl- diisopropylamin (0.3 ml) zugetropft. Die Mischung wurde 24 Stunden bei 800C gerührt. Nach dem Abkühlen auf Raumtemperatur wurde die Reaktionsmischung eingeengt. Der Rückstand wurde 30 Minuten bei 00C in 4N Salzsäure in Methanol (10 ml) gerührt, und anschliessend noch 1 Stunde bei Raumtemperatur. Die Reaktionsmischung wurde mit Essigester (50 ml) versetzt. Der Niederschlag wurde abfiltriert, gewaschen und getrocknet. Es wurden 50 mg des gewünschten Produkts erhalten.Amine (72d) (80 mg) and 7-chloro-1-cyclopropyl-6-fluoro-1,4-dihydro-4-oxo-3-quinolinecarboxylic acid Bordiacetate complex (101 mg) were dissolved in NMP (5 ml) and N-ethyl-diisopropylamine (0.3 ml) was added dropwise. The mixture was stirred at 80 ° C. for 24 hours. After cooling to room temperature, the reaction mixture was concentrated. The residue was stirred for 30 minutes at 0 ° C. in 4N hydrochloric acid in methanol (10 ml), and then for a further 1 hour at room temperature. The reaction mixture was added with ethyl acetate (50 ml). The precipitate was filtered off, washed and dried. There were obtained 50 mg of the desired product.
MS (EI): m/z: 616 [M+H]+ MS (EI): m / z: 616 [M + H] +
Die maximale Hemmkonzentration (MHK) (μg/ml) der Beispiele gegen verschiedene Organismen wurde bestimmt: A. baumannii ATCC19606, E. cloacae ATCC23355, E. coli ATCC25922, K. pneumoniae ATCC27736, P. mirabilis ATCC29906, P. aeruginosa ATCC27853, S. maltophilia ATCC13637, S. aureus ATCC43300, S. epidermidis ATCC14990, S. haemolyticus ATCC29970, E. faecalis ATCC29212 und E. faecium ATC19434.
Die Beispiele 1-12, 14-15, 17-20, 22-26, 28-53 und 56-71 weisen eine MHK von kleiner oder gleich 4 μg/ml gegen mindestens zwei der oben genannten Organismen auf.
The maximum inhibitory concentration (MIC) (μg / ml) of the examples against various organisms was determined: A. baumannii ATCC19606, E. cloacae ATCC23355, E. coli ATCC25922, K. pneumoniae ATCC27736, P. mirabilis ATCC29906, P. aeruginosa ATCC27853, p maltophilia ATCC13637, S. aureus ATCC43300, S. epidermidis ATCC14990, S. haemolyticus ATCC29970, E. faecalis ATCC29212 and E. faecium ATC19434. Examples 1-12, 14-15, 17-20, 22-26, 28-53 and 56-71 have an MIC of less than or equal to 4 μg / ml against at least two of the above organisms.