TW202302109A - 認知損傷之治療 - Google Patents
認知損傷之治療 Download PDFInfo
- Publication number
- TW202302109A TW202302109A TW111107415A TW111107415A TW202302109A TW 202302109 A TW202302109 A TW 202302109A TW 111107415 A TW111107415 A TW 111107415A TW 111107415 A TW111107415 A TW 111107415A TW 202302109 A TW202302109 A TW 202302109A
- Authority
- TW
- Taiwan
- Prior art keywords
- patient
- schizophrenia
- compound
- impaired
- administration
- Prior art date
Links
- 208000010877 cognitive disease Diseases 0.000 title claims description 204
- 208000028698 Cognitive impairment Diseases 0.000 title claims description 203
- 238000011282 treatment Methods 0.000 title claims description 109
- 150000001875 compounds Chemical class 0.000 claims abstract description 732
- 201000000980 schizophrenia Diseases 0.000 claims abstract description 568
- 238000000034 method Methods 0.000 claims abstract description 386
- 150000003839 salts Chemical class 0.000 claims abstract description 250
- 208000009668 Neurobehavioral Manifestations Diseases 0.000 claims abstract description 188
- MTCFGRXMJLQNBG-UWTATZPHSA-N D-Serine Chemical compound OC[C@@H](N)C(O)=O MTCFGRXMJLQNBG-UWTATZPHSA-N 0.000 claims abstract description 54
- 229930195711 D-Serine Natural products 0.000 claims abstract description 54
- 230000001965 increasing effect Effects 0.000 claims abstract description 33
- 230000003956 synaptic plasticity Effects 0.000 claims abstract description 32
- 208000024891 symptom Diseases 0.000 claims description 334
- 230000001771 impaired effect Effects 0.000 claims description 324
- 208000028017 Psychotic disease Diseases 0.000 claims description 95
- 230000004044 response Effects 0.000 claims description 94
- 230000001149 cognitive effect Effects 0.000 claims description 88
- 238000012360 testing method Methods 0.000 claims description 88
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 84
- 239000003814 drug Substances 0.000 claims description 74
- 230000006870 function Effects 0.000 claims description 65
- 230000003936 working memory Effects 0.000 claims description 63
- 238000012545 processing Methods 0.000 claims description 61
- 230000003997 social interaction Effects 0.000 claims description 59
- 230000008450 motivation Effects 0.000 claims description 56
- 208000035475 disorder Diseases 0.000 claims description 52
- 206010011971 Decreased interest Diseases 0.000 claims description 51
- 239000000090 biomarker Substances 0.000 claims description 50
- 239000013543 active substance Substances 0.000 claims description 49
- 239000002131 composite material Substances 0.000 claims description 47
- 208000011580 syndromic disease Diseases 0.000 claims description 46
- 208000020925 Bipolar disease Diseases 0.000 claims description 43
- 230000016571 aggressive behavior Effects 0.000 claims description 38
- 230000008449 language Effects 0.000 claims description 37
- 230000000193 eyeblink Effects 0.000 claims description 36
- 208000022610 schizoaffective disease Diseases 0.000 claims description 34
- 230000015654 memory Effects 0.000 claims description 33
- 206010012218 Delirium Diseases 0.000 claims description 30
- 206010012335 Dependence Diseases 0.000 claims description 30
- 208000009829 Lewy Body Disease Diseases 0.000 claims description 30
- 201000002832 Lewy body dementia Diseases 0.000 claims description 30
- 208000010067 Pituitary ACTH Hypersecretion Diseases 0.000 claims description 30
- 208000020627 Pituitary-dependent Cushing syndrome Diseases 0.000 claims description 30
- 208000006011 Stroke Diseases 0.000 claims description 30
- 201000006417 multiple sclerosis Diseases 0.000 claims description 30
- 230000007497 verbal memory Effects 0.000 claims description 30
- 208000001914 Fragile X syndrome Diseases 0.000 claims description 29
- 208000011597 CGF1 Diseases 0.000 claims description 28
- 239000007941 film coated tablet Substances 0.000 claims description 28
- 230000006872 improvement Effects 0.000 claims description 28
- 230000004039 social cognition Effects 0.000 claims description 28
- 230000007659 motor function Effects 0.000 claims description 27
- 229940001470 psychoactive drug Drugs 0.000 claims description 27
- 208000012202 Pervasive developmental disease Diseases 0.000 claims description 26
- 208000029560 autism spectrum disease Diseases 0.000 claims description 26
- 201000010099 disease Diseases 0.000 claims description 26
- 230000001755 vocal effect Effects 0.000 claims description 25
- 206010071176 Impaired reasoning Diseases 0.000 claims description 24
- 206010012289 Dementia Diseases 0.000 claims description 22
- 208000019901 Anxiety disease Diseases 0.000 claims description 21
- RAPZEAPATHNIPO-UHFFFAOYSA-N risperidone Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCCC4=NC=3C)=NOC2=C1 RAPZEAPATHNIPO-UHFFFAOYSA-N 0.000 claims description 21
- 229960001534 risperidone Drugs 0.000 claims description 21
- 208000018737 Parkinson disease Diseases 0.000 claims description 20
- 230000007774 longterm Effects 0.000 claims description 20
- 229940124597 therapeutic agent Drugs 0.000 claims description 20
- 208000006096 Attention Deficit Disorder with Hyperactivity Diseases 0.000 claims description 19
- 208000036864 Attention deficit/hyperactivity disease Diseases 0.000 claims description 19
- 206010003805 Autism Diseases 0.000 claims description 19
- 208000020706 Autistic disease Diseases 0.000 claims description 19
- 208000023105 Huntington disease Diseases 0.000 claims description 19
- 208000015802 attention deficit-hyperactivity disease Diseases 0.000 claims description 19
- 230000002996 emotional effect Effects 0.000 claims description 19
- 208000035231 inattentive type attention deficit hyperactivity disease Diseases 0.000 claims description 19
- 208000024827 Alzheimer disease Diseases 0.000 claims description 18
- 208000028683 bipolar I disease Diseases 0.000 claims description 18
- 208000025307 bipolar depression Diseases 0.000 claims description 18
- 208000020016 psychiatric disease Diseases 0.000 claims description 17
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 17
- 230000019771 cognition Effects 0.000 claims description 16
- 230000010330 visuo-spatial memory Effects 0.000 claims description 16
- 239000008267 milk Substances 0.000 claims description 15
- 210000004080 milk Anatomy 0.000 claims description 15
- 235000013336 milk Nutrition 0.000 claims description 15
- 230000006735 deficit Effects 0.000 claims description 14
- CEUORZQYGODEFX-UHFFFAOYSA-N Aripirazole Chemical compound ClC1=CC=CC(N2CCN(CCCCOC=3C=C4NC(=O)CCC4=CC=3)CC2)=C1Cl CEUORZQYGODEFX-UHFFFAOYSA-N 0.000 claims description 13
- 229960004372 aripiprazole Drugs 0.000 claims description 13
- KVWDHTXUZHCGIO-UHFFFAOYSA-N olanzapine Chemical compound C1CN(C)CCN1C1=NC2=CC=CC=C2NC2=C1C=C(C)S2 KVWDHTXUZHCGIO-UHFFFAOYSA-N 0.000 claims description 13
- 229960005017 olanzapine Drugs 0.000 claims description 13
- ABFPKTQEQNICFT-UHFFFAOYSA-M 2-chloro-1-methylpyridin-1-ium;iodide Chemical compound [I-].C[N+]1=CC=CC=C1Cl ABFPKTQEQNICFT-UHFFFAOYSA-M 0.000 claims description 12
- 229960005197 quetiapine fumarate Drugs 0.000 claims description 12
- 208000007502 anemia Diseases 0.000 claims description 8
- 230000003750 conditioning effect Effects 0.000 claims description 7
- 230000006378 damage Effects 0.000 claims description 7
- 230000006399 behavior Effects 0.000 claims description 5
- 206010027175 memory impairment Diseases 0.000 claims description 5
- 206010012239 Delusion Diseases 0.000 claims description 4
- 206010013496 Disturbance in attention Diseases 0.000 claims description 4
- 230000003247 decreasing effect Effects 0.000 claims description 4
- 231100000868 delusion Toxicity 0.000 claims description 4
- 239000004089 psychotropic agent Substances 0.000 claims description 4
- 206010041243 Social avoidant behaviour Diseases 0.000 claims description 3
- 230000003400 hallucinatory effect Effects 0.000 claims description 3
- 206010002942 Apathy Diseases 0.000 claims description 2
- 208000035976 Developmental Disabilities Diseases 0.000 claims description 2
- 201000010769 Prader-Willi syndrome Diseases 0.000 claims description 2
- 230000027928 long-term synaptic potentiation Effects 0.000 abstract 1
- 230000002354 daily effect Effects 0.000 description 142
- 239000008194 pharmaceutical composition Substances 0.000 description 92
- 239000000902 placebo Substances 0.000 description 91
- 229940068196 placebo Drugs 0.000 description 91
- 230000008859 change Effects 0.000 description 88
- 238000004458 analytical method Methods 0.000 description 41
- 229940079593 drug Drugs 0.000 description 39
- 230000000694 effects Effects 0.000 description 32
- 238000012216 screening Methods 0.000 description 31
- 239000000203 mixture Substances 0.000 description 29
- 238000003745 diagnosis Methods 0.000 description 23
- 238000009472 formulation Methods 0.000 description 21
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 18
- 238000004519 manufacturing process Methods 0.000 description 18
- 230000000561 anti-psychotic effect Effects 0.000 description 17
- 239000007937 lozenge Substances 0.000 description 16
- -1 D-serine Chemical class 0.000 description 14
- 241000699666 Mus <mouse, genus> Species 0.000 description 14
- 239000003826 tablet Substances 0.000 description 13
- 230000003920 cognitive function Effects 0.000 description 12
- 210000001320 hippocampus Anatomy 0.000 description 12
- 229940031703 low substituted hydroxypropyl cellulose Drugs 0.000 description 12
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 12
- 206010010144 Completed suicide Diseases 0.000 description 11
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 10
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 10
- 239000000164 antipsychotic agent Substances 0.000 description 10
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 10
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 10
- 102000004674 D-amino-acid oxidase Human genes 0.000 description 9
- 108010003989 D-amino-acid oxidase Proteins 0.000 description 9
- 230000001154 acute effect Effects 0.000 description 9
- 235000015203 fruit juice Nutrition 0.000 description 9
- 230000036541 health Effects 0.000 description 9
- 230000003993 interaction Effects 0.000 description 9
- 230000002829 reductive effect Effects 0.000 description 9
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 8
- HOKKHZGPKSLGJE-GSVOUGTGSA-N N-Methyl-D-aspartic acid Chemical compound CN[C@@H](C(O)=O)CC(O)=O HOKKHZGPKSLGJE-GSVOUGTGSA-N 0.000 description 8
- 230000002349 favourable effect Effects 0.000 description 8
- 239000003326 hypnotic agent Substances 0.000 description 8
- 239000000843 powder Substances 0.000 description 8
- 239000003981 vehicle Substances 0.000 description 8
- 206010054089 Depressive symptom Diseases 0.000 description 7
- 241000700159 Rattus Species 0.000 description 7
- 210000001638 cerebellum Anatomy 0.000 description 7
- 230000003001 depressive effect Effects 0.000 description 7
- 231100000673 dose–response relationship Toxicity 0.000 description 7
- 230000036749 excitatory postsynaptic potential Effects 0.000 description 7
- 239000000546 pharmaceutical excipient Substances 0.000 description 7
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 6
- 208000021384 Obsessive-Compulsive disease Diseases 0.000 description 6
- 229940005529 antipsychotics Drugs 0.000 description 6
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 6
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 6
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 6
- 229960003943 hypromellose Drugs 0.000 description 6
- 230000005764 inhibitory process Effects 0.000 description 6
- JEIPFZHSYJVQDO-UHFFFAOYSA-N iron(III) oxide Inorganic materials O=[Fe]O[Fe]=O JEIPFZHSYJVQDO-UHFFFAOYSA-N 0.000 description 6
- 235000019359 magnesium stearate Nutrition 0.000 description 6
- 235000010355 mannitol Nutrition 0.000 description 6
- 229940016286 microcrystalline cellulose Drugs 0.000 description 6
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 6
- 239000008108 microcrystalline cellulose Substances 0.000 description 6
- 230000003285 pharmacodynamic effect Effects 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 238000011160 research Methods 0.000 description 6
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 5
- 208000027776 Extrapyramidal disease Diseases 0.000 description 5
- 102000004868 N-Methyl-D-Aspartate Receptors Human genes 0.000 description 5
- 108090001041 N-Methyl-D-Aspartate Receptors Proteins 0.000 description 5
- 230000002411 adverse Effects 0.000 description 5
- 238000000540 analysis of variance Methods 0.000 description 5
- 239000011230 binding agent Substances 0.000 description 5
- 210000004556 brain Anatomy 0.000 description 5
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 5
- 230000001684 chronic effect Effects 0.000 description 5
- 238000013461 design Methods 0.000 description 5
- 230000000971 hippocampal effect Effects 0.000 description 5
- 238000011056 performance test Methods 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 230000001568 sexual effect Effects 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 5
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 4
- 208000013738 Sleep Initiation and Maintenance disease Diseases 0.000 description 4
- 239000008186 active pharmaceutical agent Substances 0.000 description 4
- 230000002490 cerebral effect Effects 0.000 description 4
- 230000008451 emotion Effects 0.000 description 4
- 230000003862 health status Effects 0.000 description 4
- 230000003284 homeostatic effect Effects 0.000 description 4
- 230000013016 learning Effects 0.000 description 4
- 230000000670 limiting effect Effects 0.000 description 4
- 229940126601 medicinal product Drugs 0.000 description 4
- 239000011812 mixed powder Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 230000002441 reversible effect Effects 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 230000000638 stimulation Effects 0.000 description 4
- 239000007916 tablet composition Substances 0.000 description 4
- 239000004408 titanium dioxide Substances 0.000 description 4
- 238000010200 validation analysis Methods 0.000 description 4
- 230000000007 visual effect Effects 0.000 description 4
- 208000020401 Depressive disease Diseases 0.000 description 3
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 3
- 206010020751 Hypersensitivity Diseases 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 3
- 208000019022 Mood disease Diseases 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- 206010042464 Suicide attempt Diseases 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 230000007370 cognitive improvement Effects 0.000 description 3
- 230000003931 cognitive performance Effects 0.000 description 3
- 230000001143 conditioned effect Effects 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 230000000763 evoking effect Effects 0.000 description 3
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 206010022437 insomnia Diseases 0.000 description 3
- 230000005923 long-lasting effect Effects 0.000 description 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 3
- 235000021317 phosphate Nutrition 0.000 description 3
- 238000013439 planning Methods 0.000 description 3
- 230000036470 plasma concentration Effects 0.000 description 3
- 229960004431 quetiapine Drugs 0.000 description 3
- URKOMYMAXPYINW-UHFFFAOYSA-N quetiapine Chemical compound C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12 URKOMYMAXPYINW-UHFFFAOYSA-N 0.000 description 3
- 229960001153 serine Drugs 0.000 description 3
- 230000002459 sustained effect Effects 0.000 description 3
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 2
- 206010001540 Akathisia Diseases 0.000 description 2
- 241001489705 Aquarius Species 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 2
- 208000012239 Developmental disease Diseases 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 244000024675 Eruca sativa Species 0.000 description 2
- 235000014755 Eruca sativa Nutrition 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 206010019233 Headaches Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 229910002651 NO3 Inorganic materials 0.000 description 2
- 206010057852 Nicotine dependence Diseases 0.000 description 2
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 2
- 208000002193 Pain Diseases 0.000 description 2
- 208000001431 Psychomotor Agitation Diseases 0.000 description 2
- 206010070834 Sensitisation Diseases 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 2
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 2
- 208000025569 Tobacco Use disease Diseases 0.000 description 2
- 230000002159 abnormal effect Effects 0.000 description 2
- 238000009098 adjuvant therapy Methods 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 229940124604 anti-psychotic medication Drugs 0.000 description 2
- 230000036506 anxiety Effects 0.000 description 2
- 238000003491 array Methods 0.000 description 2
- 229940077388 benzenesulfonate Drugs 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- GZUXJHMPEANEGY-UHFFFAOYSA-N bromomethane Chemical compound BrC GZUXJHMPEANEGY-UHFFFAOYSA-N 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- FATUQANACHZLRT-KMRXSBRUSA-L calcium glucoheptonate Chemical compound [Ca+2].OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)C([O-])=O.OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)C([O-])=O FATUQANACHZLRT-KMRXSBRUSA-L 0.000 description 2
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- ZPUCINDJVBIVPJ-LJISPDSOSA-N cocaine Chemical compound O([C@H]1C[C@@H]2CC[C@@H](N2C)[C@H]1C(=O)OC)C(=O)C1=CC=CC=C1 ZPUCINDJVBIVPJ-LJISPDSOSA-N 0.000 description 2
- 238000012937 correction Methods 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 231100000517 death Toxicity 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 2
- 229940043264 dodecyl sulfate Drugs 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 239000003651 drinking water Substances 0.000 description 2
- 235000020188 drinking water Nutrition 0.000 description 2
- 238000002651 drug therapy Methods 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 239000012458 free base Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 229940050410 gluconate Drugs 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 229930195712 glutamate Natural products 0.000 description 2
- 231100000869 headache Toxicity 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- 238000009533 lab test Methods 0.000 description 2
- 229940099584 lactobionate Drugs 0.000 description 2
- JYTUSYBCFIZPBE-AMTLMPIISA-N lactobionic acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O JYTUSYBCFIZPBE-AMTLMPIISA-N 0.000 description 2
- 230000020796 long term synaptic depression Effects 0.000 description 2
- 229960003511 macrogol Drugs 0.000 description 2
- 159000000003 magnesium salts Chemical class 0.000 description 2
- 229940049920 malate Drugs 0.000 description 2
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 2
- 238000007726 management method Methods 0.000 description 2
- 230000003340 mental effect Effects 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 206010065579 multifocal motor neuropathy Diseases 0.000 description 2
- 230000001537 neural effect Effects 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 230000036407 pain Effects 0.000 description 2
- 208000019906 panic disease Diseases 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 239000008213 purified water Substances 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 230000008313 sensitization Effects 0.000 description 2
- 230000001953 sensory effect Effects 0.000 description 2
- 230000009155 sensory pathway Effects 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 208000011117 substance-related disease Diseases 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 2
- 229940095064 tartrate Drugs 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 2
- 238000011870 unpaired t-test Methods 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- 230000004584 weight gain Effects 0.000 description 2
- 235000019786 weight gain Nutrition 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical compound CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- HFVMEOPYDLEHBR-UHFFFAOYSA-N (2-fluorophenyl)-phenylmethanol Chemical compound C=1C=CC=C(F)C=1C(O)C1=CC=CC=C1 HFVMEOPYDLEHBR-UHFFFAOYSA-N 0.000 description 1
- GHOKWGTUZJEAQD-ZETCQYMHSA-N (D)-(+)-Pantothenic acid Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-ZETCQYMHSA-N 0.000 description 1
- KWTSXDURSIMDCE-QMMMGPOBSA-N (S)-amphetamine Chemical compound C[C@H](N)CC1=CC=CC=C1 KWTSXDURSIMDCE-QMMMGPOBSA-N 0.000 description 1
- GNENVASJJIUNER-UHFFFAOYSA-N 2,4,6-tricyclohexyloxy-1,3,5,2,4,6-trioxatriborinane Chemical compound C1CCCCC1OB1OB(OC2CCCCC2)OB(OC2CCCCC2)O1 GNENVASJJIUNER-UHFFFAOYSA-N 0.000 description 1
- 229940080296 2-naphthalenesulfonate Drugs 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-M 3-carboxy-2,3-dihydroxypropanoate Chemical compound OC(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-M 0.000 description 1
- ALKYHXVLJMQRLQ-UHFFFAOYSA-M 3-carboxynaphthalen-2-olate Chemical compound C1=CC=C2C=C(C([O-])=O)C(O)=CC2=C1 ALKYHXVLJMQRLQ-UHFFFAOYSA-M 0.000 description 1
- ZRPLANDPDWYOMZ-UHFFFAOYSA-N 3-cyclopentylpropionic acid Chemical compound OC(=O)CCC1CCCC1 ZRPLANDPDWYOMZ-UHFFFAOYSA-N 0.000 description 1
- XMIIGOLPHOKFCH-UHFFFAOYSA-M 3-phenylpropionate Chemical compound [O-]C(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-M 0.000 description 1
- PXRKCOCTEMYUEG-UHFFFAOYSA-N 5-aminoisoindole-1,3-dione Chemical compound NC1=CC=C2C(=O)NC(=O)C2=C1 PXRKCOCTEMYUEG-UHFFFAOYSA-N 0.000 description 1
- USSIQXCVUWKGNF-UHFFFAOYSA-N 6-(dimethylamino)-4,4-diphenylheptan-3-one Chemical compound C=1C=CC=CC=1C(CC(C)N(C)C)(C(=O)CC)C1=CC=CC=C1 USSIQXCVUWKGNF-UHFFFAOYSA-N 0.000 description 1
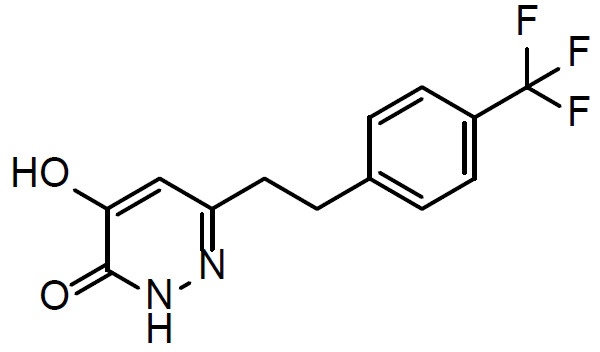
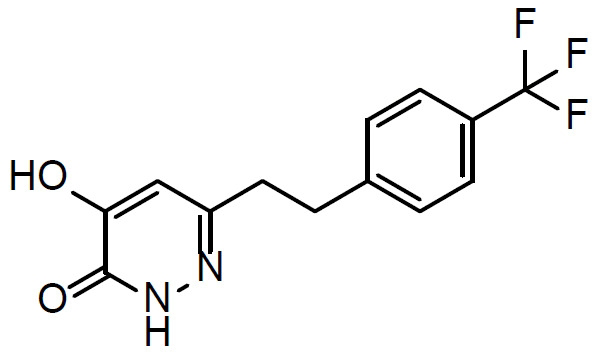
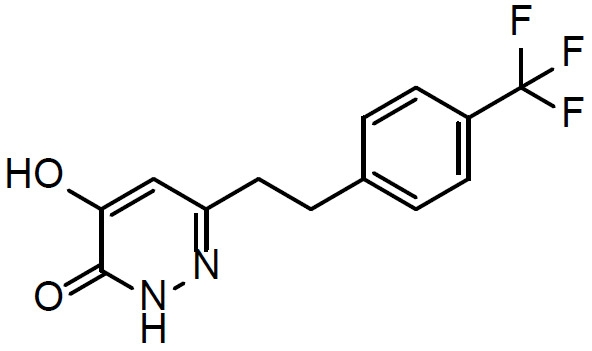
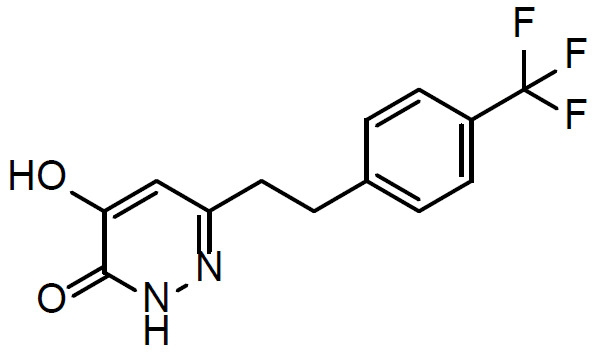
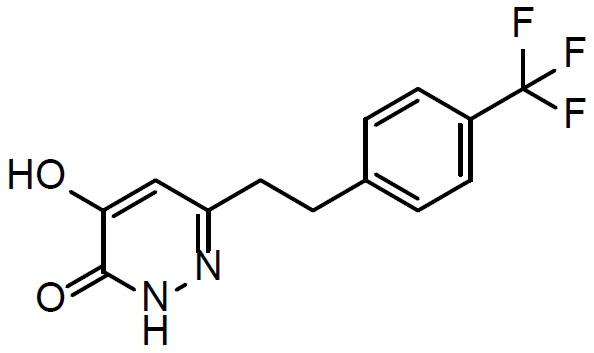
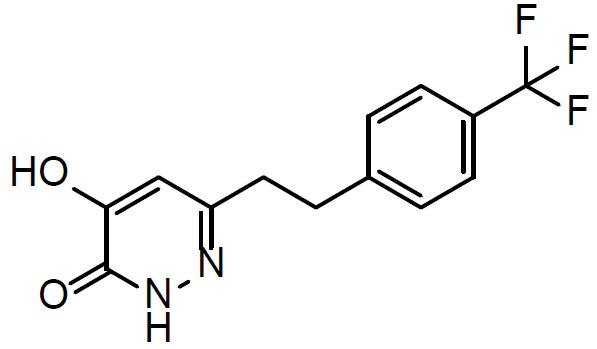
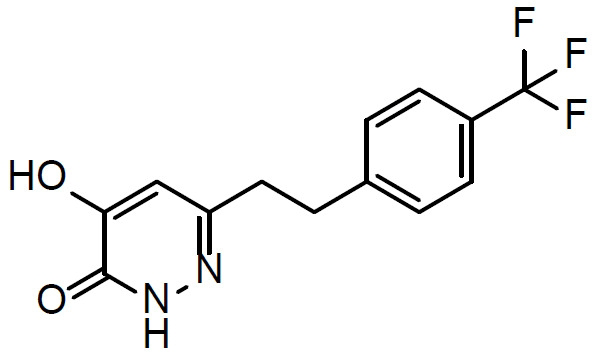
- QBQMUMMSYHUDFM-UHFFFAOYSA-N 6-[2-[4-(trifluoromethyl)phenyl]ethyl]-1,2-dihydropyridazine-3,4-dione Chemical compound N1C(=O)C(O)=CC(CCC=2C=CC(=CC=2)C(F)(F)F)=N1 QBQMUMMSYHUDFM-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- 229930000680 A04AD01 - Scopolamine Natural products 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 206010002198 Anaphylactic reaction Diseases 0.000 description 1
- 206010004146 Basal cell carcinoma Diseases 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 208000025721 COVID-19 Diseases 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- 235000012766 Cannabis sativa ssp. sativa var. sativa Nutrition 0.000 description 1
- 235000012765 Cannabis sativa ssp. sativa var. spontanea Nutrition 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 206010008617 Cholecystitis chronic Diseases 0.000 description 1
- 102000004420 Creatine Kinase Human genes 0.000 description 1
- 108010042126 Creatine kinase Proteins 0.000 description 1
- 150000008574 D-amino acids Chemical class 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- 241001069765 Fridericia <angiosperm> Species 0.000 description 1
- 102000018899 Glutamate Receptors Human genes 0.000 description 1
- 108010027915 Glutamate Receptors Proteins 0.000 description 1
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 1
- 208000004547 Hallucinations Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- STECJAGHUSJQJN-GAUPFVANSA-N Hyoscine Natural products C1([C@H](CO)C(=O)OC2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 STECJAGHUSJQJN-GAUPFVANSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 201000006347 Intellectual Disability Diseases 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 208000007811 Latex Hypersensitivity Diseases 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 1
- 208000036626 Mental retardation Diseases 0.000 description 1
- STECJAGHUSJQJN-UHFFFAOYSA-N N-Methyl-scopolamin Natural products C1C(C2C3O2)N(C)C3CC1OC(=O)C(CO)C1=CC=CC=C1 STECJAGHUSJQJN-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 1
- 102000004316 Oxidoreductases Human genes 0.000 description 1
- 108090000854 Oxidoreductases Proteins 0.000 description 1
- 206010033664 Panic attack Diseases 0.000 description 1
- 206010034010 Parkinsonism Diseases 0.000 description 1
- 229920002230 Pectic acid Polymers 0.000 description 1
- 108091036414 Polyinosinic:polycytidylic acid Proteins 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 206010039020 Rhabdomyolysis Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 206010039251 Rubber sensitivity Diseases 0.000 description 1
- 208000020186 Schizophreniform disease Diseases 0.000 description 1
- 206010039897 Sedation Diseases 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 206010040914 Skin reaction Diseases 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 206010065604 Suicidal behaviour Diseases 0.000 description 1
- 206010042458 Suicidal ideation Diseases 0.000 description 1
- 229920002253 Tannate Polymers 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 1
- 208000030886 Traumatic Brain injury Diseases 0.000 description 1
- 208000003443 Unconsciousness Diseases 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 208000021017 Weight Gain Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 229940045714 alkyl sulfonate alkylating agent Drugs 0.000 description 1
- 150000008052 alkyl sulfonates Chemical class 0.000 description 1
- 208000030961 allergic reaction Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- AEMOLEFTQBMNLQ-BKBMJHBISA-N alpha-D-galacturonic acid Chemical compound O[C@H]1O[C@H](C(O)=O)[C@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-BKBMJHBISA-N 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229940025084 amphetamine Drugs 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 230000036783 anaphylactic response Effects 0.000 description 1
- 208000003455 anaphylaxis Diseases 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000003466 anti-cipated effect Effects 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 125000005228 aryl sulfonate group Chemical group 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 229940125717 barbiturate Drugs 0.000 description 1
- HNYOPLTXPVRDBG-UHFFFAOYSA-N barbituric acid Chemical compound O=C1CC(=O)NC(=O)N1 HNYOPLTXPVRDBG-UHFFFAOYSA-N 0.000 description 1
- 231100000871 behavioral problem Toxicity 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- 229940049706 benzodiazepine Drugs 0.000 description 1
- 150000001557 benzodiazepines Chemical class 0.000 description 1
- XMIIGOLPHOKFCH-UHFFFAOYSA-N beta-phenylpropanoic acid Natural products OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- 150000004648 butanoic acid derivatives Chemical class 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 235000011148 calcium chloride Nutrition 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 210000003710 cerebral cortex Anatomy 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- VDANGULDQQJODZ-UHFFFAOYSA-N chloroprocaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1Cl VDANGULDQQJODZ-UHFFFAOYSA-N 0.000 description 1
- 229960002023 chloroprocaine Drugs 0.000 description 1
- 201000001352 cholecystitis Diseases 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Natural products OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 1
- 229960004170 clozapine Drugs 0.000 description 1
- QZUDBNBUXVUHMW-UHFFFAOYSA-N clozapine Chemical compound C1CN(C)CCN1C1=NC2=CC(Cl)=CC=C2NC2=CC=CC=C12 QZUDBNBUXVUHMW-UHFFFAOYSA-N 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 229960003920 cocaine Drugs 0.000 description 1
- 230000003930 cognitive ability Effects 0.000 description 1
- 238000009225 cognitive behavioral therapy Methods 0.000 description 1
- 238000011970 concomitant therapy Methods 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 239000003405 delayed action preparation Substances 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000001177 diphosphate Substances 0.000 description 1
- XPPKVPWEQAFLFU-UHFFFAOYSA-J diphosphate(4-) Chemical compound [O-]P([O-])(=O)OP([O-])([O-])=O XPPKVPWEQAFLFU-UHFFFAOYSA-J 0.000 description 1
- 235000011180 diphosphates Nutrition 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000002635 electroconvulsive therapy Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 229950005627 embonate Drugs 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000006274 endogenous ligand Substances 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 230000005713 exacerbation Effects 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 229940050411 fumarate Drugs 0.000 description 1
- 229960002598 fumaric acid Drugs 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- DSLZVSRJTYRBFB-DUHBMQHGSA-N galactaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O DSLZVSRJTYRBFB-DUHBMQHGSA-N 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 150000002301 glucosamine derivatives Chemical class 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 208000002672 hepatitis B Diseases 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-N heptanoic acid Chemical compound CCCCCCC(O)=O MNWFXJYAOYHMED-UHFFFAOYSA-N 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-M hexadecanoate Chemical compound CCCCCCCCCCCCCCCC([O-])=O IPCSVZSSVZVIGE-UHFFFAOYSA-M 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- WJRBRSLFGCUECM-UHFFFAOYSA-N hydantoin Chemical compound O=C1CNC(=O)N1 WJRBRSLFGCUECM-UHFFFAOYSA-N 0.000 description 1
- 229940091173 hydantoin Drugs 0.000 description 1
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical compound C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 1
- BICAGYDGRXJYGD-UHFFFAOYSA-N hydrobromide;hydrochloride Chemical compound Cl.Br BICAGYDGRXJYGD-UHFFFAOYSA-N 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 230000000147 hypnotic effect Effects 0.000 description 1
- 238000013095 identification testing Methods 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 230000010365 information processing Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 201000005391 latex allergy Diseases 0.000 description 1
- 239000011344 liquid material Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 229910003002 lithium salt Inorganic materials 0.000 description 1
- 159000000002 lithium salts Chemical class 0.000 description 1
- 238000007449 liver function test Methods 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 238000013187 longer-term treatment Methods 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 208000024714 major depressive disease Diseases 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-M mandelate Chemical compound [O-]C(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-M 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 229960003194 meglumine Drugs 0.000 description 1
- 230000004630 mental health Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 229960001797 methadone Drugs 0.000 description 1
- 229960001252 methamphetamine Drugs 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 229940102396 methyl bromide Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- LRMHVVPPGGOAJQ-UHFFFAOYSA-N methyl nitrate Chemical compound CO[N+]([O-])=O LRMHVVPPGGOAJQ-UHFFFAOYSA-N 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 230000036651 mood Effects 0.000 description 1
- PSZYNBSKGUBXEH-UHFFFAOYSA-M naphthalene-1-sulfonate Chemical compound C1=CC=C2C(S(=O)(=O)[O-])=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-M 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 1
- 230000003557 neuropsychological effect Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 239000000820 nonprescription drug Substances 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 239000003883 ointment base Substances 0.000 description 1
- 229940049964 oleate Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 229940005483 opioid analgesics Drugs 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 230000003534 oscillatory effect Effects 0.000 description 1
- 150000003891 oxalate salts Chemical class 0.000 description 1
- 229940014662 pantothenate Drugs 0.000 description 1
- 235000019161 pantothenic acid Nutrition 0.000 description 1
- 239000011713 pantothenic acid Substances 0.000 description 1
- 208000035824 paresthesia Diseases 0.000 description 1
- 230000001936 parietal effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 235000019371 penicillin G benzathine Nutrition 0.000 description 1
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical class OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 1
- JRKICGRDRMAZLK-UHFFFAOYSA-L peroxydisulfate Chemical compound [O-]S(=O)(=O)OOS([O-])(=O)=O JRKICGRDRMAZLK-UHFFFAOYSA-L 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- JTJMJGYZQZDUJJ-UHFFFAOYSA-N phencyclidine Chemical compound C1CCCCN1C1(C=2C=CC=CC=2)CCCCC1 JTJMJGYZQZDUJJ-UHFFFAOYSA-N 0.000 description 1
- 229950010883 phencyclidine Drugs 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 230000006461 physiological response Effects 0.000 description 1
- 229940075930 picrate Drugs 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-M picrate anion Chemical compound [O-]C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-M 0.000 description 1
- 229950010765 pivalate Drugs 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 229940115272 polyinosinic:polycytidylic acid Drugs 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 239000000955 prescription drug Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 229940072554 risperidone 6 mg Drugs 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 230000000698 schizophrenic effect Effects 0.000 description 1
- STECJAGHUSJQJN-FWXGHANASA-N scopolamine Chemical compound C1([C@@H](CO)C(=O)O[C@H]2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 STECJAGHUSJQJN-FWXGHANASA-N 0.000 description 1
- 229960002646 scopolamine Drugs 0.000 description 1
- 230000036280 sedation Effects 0.000 description 1
- 239000012056 semi-solid material Substances 0.000 description 1
- 230000037152 sensory function Effects 0.000 description 1
- 230000006403 short-term memory Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 231100000430 skin reaction Toxicity 0.000 description 1
- 230000035483 skin reaction Effects 0.000 description 1
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000012453 sprague-dawley rat model Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 229910021653 sulphate ion Inorganic materials 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 210000000225 synapse Anatomy 0.000 description 1
- 230000005062 synaptic transmission Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 238000012549 training Methods 0.000 description 1
- 238000012384 transportation and delivery Methods 0.000 description 1
- 230000009529 traumatic brain injury Effects 0.000 description 1
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 1
- 238000002562 urinalysis Methods 0.000 description 1
- 229940070710 valerate Drugs 0.000 description 1
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 1
- 230000031836 visual learning Effects 0.000 description 1
- 238000009528 vital sign measurement Methods 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/554—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having at least one nitrogen and one sulfur as ring hetero atoms, e.g. clothiapine, diltiazem
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Psychiatry (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本文揭示治療有需要患者中認知損傷的方法。亦揭示治療有需要患者中至少一種認知症狀(例如至少一種與精神分裂症相關之認知症狀)的方法,以及增加有需要患者中突觸可塑性及/或長效增益的方法。
精神分裂症為一種嚴重精神障礙,影響人口的大約1%,終生盛行率估計為每1000人中有5.6至11.9人。精神分裂症之特徵在於精神病、認知損傷及/或社交及動力缺陷。舉例而言,精神分裂症之特徵可在於正性症狀(例如幻覺或妄想)、負性症狀(例如失樂症狀、無意志、反應遲鈍、自發性語音減少及社交退縮)及/或與精神分裂症相關之認知損傷(CIAS)。精神分裂症之認知症狀會影響廣泛領域,包括(但不限於)注意力、工作記憶及/或執行功能。雖然精神分裂症之正性症狀易於復發及緩解,但在當今環境中,精神分裂症之負性及認知症狀通常為慢性的,且影響患者之社交活動,反映當前對症狀進展過程及可用治療之瞭解有限。
儘管負性及認知症狀對生活品質及功能恢復有高度預測性,但對於與精神分裂症相關之認知損傷,尚無經批准之治療。因此,需要對認知損傷,包括與精神分裂症相關之認知損傷的新穎治療。
D-胺基酸氧化酶(DAAO)為降解中性D-胺基酸,諸如D-絲胺酸(N-甲基-D-天冬胺酸(NMDA)受體共促效劑)之過氧化體酶。連同麩胺酸一起,D-絲胺酸介導NMDA受體傳輸、突觸可塑性及其他生理功能。另外,D-絲胺酸為德耳塔(δ)2麩胺酸受體(GluRδ2)之內源性配位體,該受體與突觸可塑性及長期抑制有關。
因此,DAAO抑制劑可適用於治療認知損傷,包括治療與精神分裂症及其他精神病症(例如,精神病性病症)及神經病症相關的認知症狀。
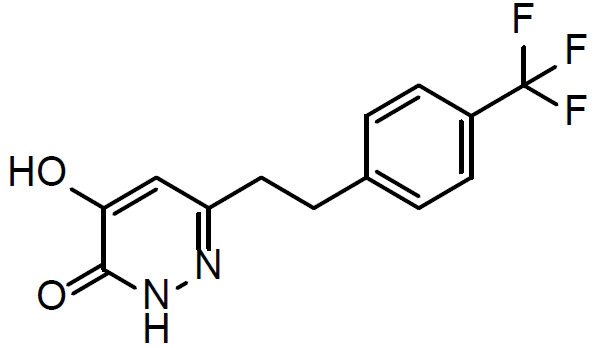
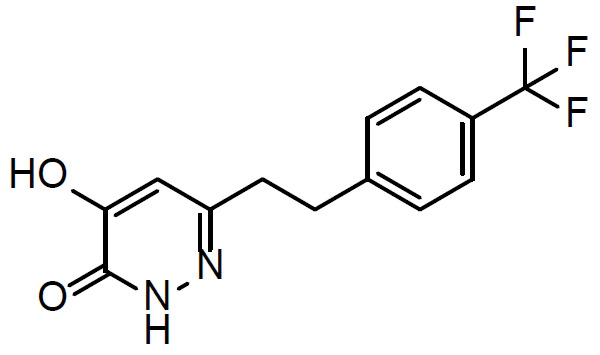
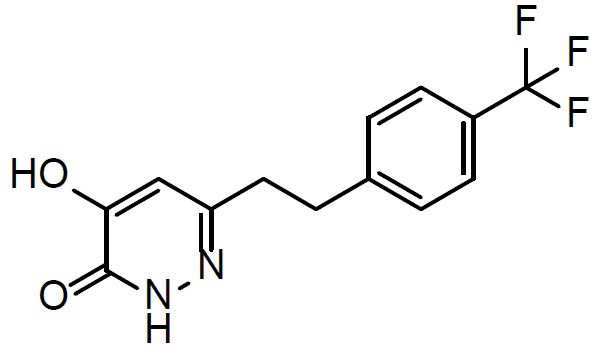
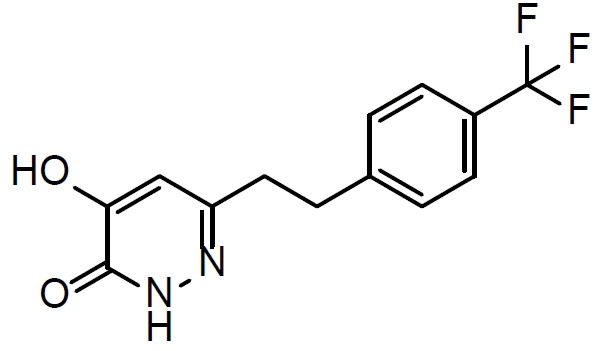
本文揭示一種治療有需要患者中與精神分裂症相關之認知損傷的方法,該方法包含向該患者投與1 mg至500 mg (例如1 mg至100 mg)至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀/域係藉由該投與治療。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於治療有需要患者中與精神分裂症相關之認知損傷的方法中,該方法包含向該患者投與1 mg至500 mg (例如1 mg至100 mg)該至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於治療有需要患者中與精神分裂症相關之認知損傷的方法中的藥劑,該方法包含向該患者投與1 mg至500 mg (例如1 mg至100 mg)該至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
在一些實施例中,該方法包含:
● 向該患者投與1 mg至500 mg (例如1 mg至100 mg;10 mg至50 mg;20 mg至50 mg;25 mg至50 mg;20 mg或50 mg;20 mg;50 mg)至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(eye-blink conditioning;EBC)反應、該患者之失配負波(mismatch negativity;MMN)幅值及該患者之聽覺穩態反應(auditory steady state response;ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg (例如1 mg至100 mg;20 mg至50 mg;20 mg或50 mg;20 mg;50 mg)至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。在一些實施例中,至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,投與改善患者在認知量測方面之表現。在一些實施例中,投與改善患者在認知域量測方面之表現。在一些實施例中,投與改善患者之認知量測總分。
在一些實施例中,相對於投與之前量測的患者之簡易精神分裂症認知評定(Brief Assessment of Cognition in Schizophrenia;BACS)綜合評分,投與改善患者之BACS綜合評分。在一些實施例中,相對於投與之前量測的患者之精神分裂症認知評分量表(Schizophrenia Cognition Rating Scale;SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。在一些實施例中,相對於投與之前的持續表現測試-相同配對(Continuous Performance Test-Identical Pairs;CPT-IP)測試,投與改善患者在CPT-IP測試方面之表現。在一些實施例中,相對於投與之前患者在簡易視覺空間記憶測試-修訂版(Brief Visuospatial Memory Test-Revised;BVMT-R)測試方面之表現,投與改善患者在BVMT-R測試方面之表現。在一些實施例中,相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(Mayer-Salovey-Caruso Emotional Intelligence Test;MSCEIT)方面之表現,投與改善患者在MSCEIT方面之表現。在一些實施例中,相對於投與之前患者在虛擬實境功能能力評定工具(Virtual Reality Functional Capacity Assessment Tool;VRFCAT)方面之表現,投與改善患者在VRFCAT方面之表現。在一些實施例中,相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(Clinical Global Impression-Severity Scale;CGI-S)評分,投與改善患者之CGI-S評分。
在一些實施例中,在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用正性及負性症候群量表(Positive and Negative Syndrome Scale;PANSS)來評定/量測。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(Brief Negative Symptom Scale;BNSS)工具來評定。
在一些實施例中,在投與之前,患者未展現出任何抑鬱或錐體外症狀。在一些實施例中,在投與之前,以2-6 mg日劑量之利培酮(risperidone)當量向患者投與穩定抗精神病治療。
在一些實施例中,在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
在一些實施例中,投與不治療至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種與精神分裂症相關之負性症狀係根據正性及負性症候群量表(PANSS)量測。
在一些實施例中,至少一種化合物係與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑(aripiprazole)、奧氮平(olanzapine)、利培酮及反丁烯二酸喹硫平(quetiapine fumarate)。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,向患者投與20 mg至50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次。在一些實施例中,向患者投與50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次持續54週。
在一些實施例中,至少一種化合物係口服投與。在一些實施例中,至少一種化合物係以至少一種錠劑形式投與。在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,患者在投與之前至少一年被診斷患有精神分裂症。在一些實施例中,患者被診斷患有如藉由精神障礙診斷與統計手冊(Diagnostic and Statistical Manual of Mental Disorders) (DSM-5)所定義之精神分裂症。在一些實施例中,患者被診斷患有如藉由MINI 7.0.2版所定義之精神分裂症。
在一些實施例中,患者處於精神藥物治療之穩定療程中。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未增加。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未降低超過25%。
在一些實施例中,患者在投與之前具有穩定症狀至少3個月。
在一些實施例中,患者在12歲的年齡之後被診斷患有精神分裂症。在一些實施例中,患者沒有接受過分裂情感性精神障礙之終身診斷、躁鬱症之終身診斷或強迫症之終身診斷。在一些實施例中,患者在投與之前未罹患抑鬱症。在一些實施例中,在投與之前,如藉由卡爾加里精神分裂症抑鬱量表評分(Calgary Depression Scale for Schizophrenia Score;CDSS)所量測,患者未罹患抑鬱症。
本文亦揭示一種治療患者之至少一種與精神分裂症相關之認知症狀的方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),其包含向該患者投與1 mg至500 mg (例如1 mg至100 mg)至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於治療患者的至少一種與精神分裂症相關之認知症狀的方法中,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1 (妄想)、P3 (幻覺行為)、P4 (興奮)、P5 (自大)及/或P6 (猜疑)的評分<5),該方法包含向該患者投與1 mg至500 mg (例如1 mg至100 mg)該至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於治療患者的至少一種與精神分裂症相關之認知症狀的方法中的藥劑,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),該方法包含向該患者投與1 mg至500 mg (例如1 mg至100 mg)該至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,該方法包含:
● 向該患者投與1 mg至500 mg (例如1 mg至100 mg;10 mg至50 mg;20 mg至50 mg;25 mg至50 mg;20 mg或50 mg;20 mg;50 mg)至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg (例如1 mg至100 mg;10 mg至50 mg;20 mg至50 mg;25 mg至50 mg;20 mg或50 mg;20 mg;50 mg)至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,投與改善患者在認知量測方面之表現。在一些實施例中,投與改善患者在認知域量測方面之表現。在一些實施例中,投與改善患者之認知量測總分。
在一些實施例中,相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。在一些實施例中,相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。在一些實施例中,相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,投與改善患者在CPT-IP測試方面之表現。在一些實施例中,相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,投與改善患者在BVMT-R測試方面之表現。在一些實施例中,相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,投與改善患者在MSCEIT方面之表現。在一些實施例中,相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,投與改善患者在VRFCAT方面之表現。在一些實施例中,相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,投與改善患者之CGI-S評分。
在一些實施例中,在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
在一些實施例中,投與不治療至少一種與精神分裂症相關之負性症狀。
在一些實施例中,在投與之前,患者未展現出任何抑鬱或錐體外症狀。在一些實施例中,在投與之前,以2-6 mg日劑量之利培酮當量向患者投與穩定抗精神病治療。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,向患者投與20 mg至50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次。在一些實施例中,向患者投與50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次持續54週。
在一些實施例中,至少一種化合物係口服投與。在一些實施例中,至少一種化合物係以至少一種錠劑形式投與。在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種額外活性劑治療患者之與精神分裂症之至少一種負性症狀相關之行為問題。在一些實施例中,至少一種症狀之嚴重程度係根據正性及負性症候群量表(PANSS)量測。
在一些實施例中,至少一種與精神分裂症相關之負性症狀為無動力症候群。在一些實施例中,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、情感淡漠、動力喪失、精力下降、社交退縮及對社交互動之興趣降低。
在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
在一些實施例中,患者在投與之前至少一年被診斷患有精神分裂症。在一些實施例中,患者被診斷患有如藉由精神障礙診斷與統計手冊(DSM-5)所定義之精神分裂症。在一些實施例中,患者被診斷患有如藉由MINI 7.0.2版所定義之精神分裂症。
在一些實施例中,患者處於精神藥物治療之穩定療程中。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未增加。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未降低超過25%。
在一些實施例中,患者在投與之前具有穩定症狀至少3個月。
在一些實施例中,患者在12歲年齡之後被診斷患有精神分裂症。在一些實施例中,患者沒有接受過分裂情感性精神障礙之終身診斷、躁鬱症之終身診斷或強迫症之終身診斷。在一些實施例中,患者在投與之前未罹患抑鬱症。在一些實施例中,在投與之前,如藉由卡爾加里精神分裂症抑鬱量表評分(CDSS)所量測,患者未罹患抑鬱症。
本文亦揭示一種治療有需要患者中與精神分裂症相關之認知損傷的方法,該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀/域係藉由該投與治療。在一些實施例中,至少一種與精神分裂症相關之認知症狀/域係由寬範圍之認知功能障礙表現。在一些實施例中,至少一種與精神分裂症相關之認知症狀/域為資訊處理能力差、專注於目標的能力受損、工作記憶及學習異常或其任何組合。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於治療有需要患者中與精神分裂症相關之認知損傷的方法中,該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀/域係藉由該投與治療。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於治療有需要患者中與精神分裂症相關之認知損傷的方法中的藥劑,該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀/域係藉由該投與治療。
在一些實施例中,該方法包含:
● 向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。在一些實施例中,至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,投與改善患者在認知量測方面之表現。在一些實施例中,投與改善患者在認知域量測方面之表現。在一些實施例中,投與改善患者之認知量測總分。
在一些實施例中,相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。在一些實施例中,相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。在一些實施例中,相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,投與改善患者在CPT-IP測試方面之表現。在一些實施例中,相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,投與改善患者在BVMT-R測試方面之表現。在一些實施例中,相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,投與改善患者在MSCEIT方面之表現。在一些實施例中,相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,投與改善患者在VRFCAT方面之表現。在一些實施例中,相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,投與改善患者之CGI-S評分。
在一些實施例中,在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS評定來評定。在一些實施例中,至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
在一些實施例中,在投與之前,患者未展現出任何抑鬱或錐體外症狀。在一些實施例中,在投與之前,以2-6 mg日劑量之利培酮當量向患者投與穩定抗精神病治療。
在一些實施例中,在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
在一些實施例中,投與不治療至少一種與精神分裂症相關之負性症狀。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與125 mg至少一種化合物每日一次。在一些實施例中,向患者投與500 mg至少一種化合物每日一次。在一些實施例中,向患者投與小於500 mg至少一種化合物每日一次。
在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,患者在投與之前至少一年被診斷患有精神分裂症。在一些實施例中,患者被診斷患有如藉由精神障礙診斷與統計手冊(DSM-5)所定義之精神分裂症。在一些實施例中,患者被診斷患有如藉由MINI 7.0.2版所定義之精神分裂症。
在一些實施例中,患者處於精神藥物治療之穩定療程中。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未增加。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未降低超過25%。
在一些實施例中,患者在投與之前具有穩定症狀至少3個月。
在一些實施例中,患者在12歲年齡之後被診斷患有精神分裂症。在一些實施例中,患者沒有接受過分裂情感性精神障礙之終身診斷、躁鬱症之終身診斷或強迫症之終身診斷。在一些實施例中,患者在投與之前未罹患抑鬱症。在一些實施例中,在投與之前,如藉由卡爾加里精神分裂症抑鬱量表評分(CDSS)所量測,患者未罹患抑鬱症。
本文亦揭示一種治療患者之至少一種與精神分裂症相關之認知症狀的方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),其包含向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於治療患者的至少一種與精神分裂症相關之認知症狀的方法中,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於治療患者的至少一種與精神分裂症相關之認知症狀的方法中的藥劑,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,該方法包含:
● 向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,投與改善患者在認知量測方面之表現。在一些實施例中,投與改善患者在認知域量測方面之表現。在一些實施例中,投與改善患者之認知量測總分。
在一些實施例中,相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。在一些實施例中,相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。在一些實施例中,相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,投與改善患者在CPT-IP測試方面之表現。在一些實施例中,相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,投與改善患者在BVMT-R測試方面之表現。在一些實施例中,相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,投與改善患者在MSCEIT方面之表現。在一些實施例中,相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,投與改善患者在VRFCAT方面之表現。在一些實施例中,相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,投與改善患者之CGI-S評分。
在一些實施例中,在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
在一些實施例中,投與不治療至少一種與精神分裂症相關之負性症狀。
在一些實施例中,在投與之前,患者未展現出任何抑鬱或錐體外症狀。在一些實施例中,在投與之前,以2-6 mg日劑量之利培酮當量向患者投與穩定抗精神病治療。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與125 mg至少一種化合物每日一次。在一些實施例中,向患者投與500 mg至少一種化合物每日一次。在一些實施例中,向患者投與小於500 mg至少一種化合物每日一次。
在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
在一些實施例中,患者在投與之前至少一年被診斷患有精神分裂症。在一些實施例中,患者被診斷患有如藉由精神障礙診斷與統計手冊(DSM-5)所定義之精神分裂症。在一些實施例中,患者被診斷患有如藉由MINI 7.0.2版所定義之精神分裂症。
在一些實施例中,患者處於精神藥物治療之穩定療程中。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未增加。在一些實施例中,患者處於精神藥物治療之療程中,其中該精神藥物治療劑量在投與之前至少2個月未降低超過25%。
在一些實施例中,患者在投與之前具有穩定症狀至少3個月。
在一些實施例中,患者在12歲年齡之後被診斷患有精神分裂症。在一些實施例中,患者沒有接受過分裂情感性精神障礙之終身診斷、躁鬱症之終身診斷或強迫症之終身診斷。在一些實施例中,患者在投與之前未罹患抑鬱症。在一些實施例中,在投與之前,如藉由卡爾加里精神分裂症抑鬱量表評分(CDSS)所量測,患者未罹患抑鬱症。
本文亦揭示一種治療有需要患者中認知損傷的方法,該方法包含向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其中該患者在該投與之前展現出至少一種認知症狀。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於治療有需要患者中認知損傷的方法中,該方法包含向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其中該患者在該投與之前展現出至少一種認知症狀。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於治療有需要患者中認知損傷的方法中的藥劑,該方法包含向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其中該患者在該投與之前展現出至少一種認知症狀。
在一些實施例中,該方法包含:
● 向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。在一些實施例中,至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
在一些實施例中,投與治療至少一種認知症狀。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,至少一種認知症狀係與精神病性病症相關。在一些實施例中,精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。在一些實施例中,精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。在一些實施例中,精神病性病症為與攻擊性不相關之精神分裂症。
在一些實施例中,患者罹患癡呆。在一些實施例中,患者罹患情緒障礙。
在一些實施例中,患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病(Alzheimer's disease)、帕金森氏病(Parkinson's disease)、亨廷頓氏病(Huntington's disease)、庫欣氏病(Cushing's disease)、路易體疾病(Lewy body disease)、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群(Prader-Willi syndrome)、躁鬱症、抑鬱症及譫妄。在一些實施例中,患者罹患選自以下之疾病:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
在一些實施例中,向患者投與1 mg至100 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次。在一些實施例中,向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg或50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次持續54週。
在一些實施例中,向患者投與50 mg至500 mg至少一種化合物每日一次。在一些實施例中,向患者投與125 mg至少一種化合物每日一次。在一些實施例中,向患者投與500 mg至少一種化合物每日一次。在一些實施例中,向患者投與小於500 mg至少一種化合物每日一次。
在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。在一些實施例中,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
本文亦揭示一種增加有需要患者中D-絲胺酸含量的方法,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於增加有需要患者中D-絲胺酸含量的方法中,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於增加有需要患者中D-絲胺酸含量的方法中的藥劑,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次。在一些實施例中,向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與125 mg至少一種化合物每日一次。
在一些實施例中,向患者投與1 mg至100 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg或50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次持續54週。
在一些實施例中,患者在投與之前展現出至少一種認知症狀。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
在一些實施例中,患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。在一些實施例中,患者罹患選自以下之疾病:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
在一些實施例中,患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
在一些實施例中,患者罹患癡呆。在一些實施例中,患者罹患情緒障礙。
本文亦揭示一種增加有需要患者中長效增益的方法,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於增加有需要患者中長效增益的方法中,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於增加有需要患者中長效增益的方法中的藥劑,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次。在一些實施例中,向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與125 mg至少一種化合物每日一次。
在一些實施例中,向患者投與1 mg至100 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg或50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次持續54週。
在一些實施例中,患者在投與之前展現出至少一種認知症狀。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
本文亦揭示一種增加有需要患者中突觸可塑性之方法,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物,其供用於增加有需要患者中突觸可塑性的方法中,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
本文亦揭示至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的用途,其用於製造供用於增加有需要患者中突觸可塑性的方法中的藥劑,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次。在一些實施例中,向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與125 mg至少一種化合物每日一次。
在一些實施例中,向患者投與1 mg至100 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg或50 mg至少一種化合物每日一次。
在一些實施例中,向患者投與20 mg至少一種化合物每日一次,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次。在一些實施例中,向患者投與20 mg至少一種化合物每日一次持續14週,且隨後向患者投與50 mg至少一種化合物每日一次持續54週。
在一些實施例中,患者在投與之前展現出至少一種認知症狀。
在一些實施例中,向患者投與至少一種化合物超過14週。在一些實施例中,向患者投與至少一種化合物超過20週。
在一些實施例中,至少一種化合物係以至少一種膜衣錠劑形式投與。在一些實施例中,至少一種化合物係以兩種膜衣錠劑形式投與。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1小時或之後1小時內不飲用果汁。
在一些實施例中,至少一種化合物係在早晨投與。在一些實施例中,至少一種化合物係與水或牛奶一起投與。
在一些實施例中,患者在投與之前1或之後1小時內不飲用果汁。
在一些實施例中,投與增加患者之D-絲胺酸含量。
在一些實施例中,投與增加患者之長效增益。
在一些實施例中,投與改善患者之眨眼制約(EBC)反應。在一些實施例中,投與改善患者之失配負波(MMN)幅值。在一些實施例中,投與改善患者之聽覺穩態反應(ASSR) γ波段功率。
在一些實施例中,至少一種化合物與至少一種額外活性劑組合投與。在一些實施例中,至少一種額外治療劑為催眠劑。在一些實施例中,至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
在一些實施例中,患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。在一些實施例中,患者罹患選自以下之疾病:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
在一些實施例中,患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
在一些實施例中,患者罹患癡呆。在一些實施例中,患者罹患情緒障礙。
應理解,本文中提及使用至少一種選自化合物(
I)及醫藥學上可接受之鹽之化合物的治療方法(例如,治療認知損傷之方法)亦應解釋為提及:
- 供用於治療例如認知損傷之方法中的至少一種選自化合物(
I)及醫藥學上可接受之鹽之化合物;及/或
- 至少一種選自化合物(
I)及醫藥學上可接受之鹽之化合物在製造用於治療例如認知損傷之藥劑中的用途。
非限制性實例實施例 1 :
非限制性地,本發明之一些實施例包括:
1. 一種治療有需要患者中與精神分裂症相關之認知損傷的方法,該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
2. 根據實施例1之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
3. 根據實施例1或2之治療與精神分裂症相關之認知損傷的方法,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
4. 根據實施例1至3中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
5. 根據實施例1至4中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
6. 根據實施例1至5中任一項之治療與精神分裂症相關之認知損傷的方法,其中在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
7. 根據實施例6之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
8. 根據實施例6之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
9. 根據實施例6或7之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
10. 根據實施例6至9中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。
11. 根據實施例1至5中任一項之治療與精神分裂症相關之認知損傷的方法,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
12. 根據實施例1至11中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種化合物係與至少一種額外活性劑組合投與。
13. 根據實施例12之治療與精神分裂症相關之認知損傷的方法,其中至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。
14. 根據實施例13之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
15. 根據實施例1至14中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與至少一種化合物超過14週。
16. 根據實施例1至15中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與至少一種化合物超過20週。
17. 根據實施例1至16中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與50 mg至少一種化合物每日一次。
18. 根據實施例1至16中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與125 mg至少一種化合物每日一次。
19. 根據實施例1至16中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與500 mg至少一種化合物每日一次。
20. 一種治療有需要患者中認知損傷的方法,該方法包含向該患者投與治療有效量之至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其中該患者在該投與之前展現出至少一種認知症狀。
21. 根據實施例20之治療認知損傷之方法,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
22. 根據實施例20或21之治療認知損傷之方法,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
23. 根據實施例20至22中任一項之治療認知損傷之方法,其中投與治療至少一種認知症狀。
24. 根據實施例20至23中任一項之治療認知損傷之方法,其中至少一種認知症狀係與精神病性病症相關。
25. 根據實施例24之治療認知損傷之方法,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
26. 根據實施例24或25之治療認知損傷之方法,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
27. 根據實施例24至26中任一項之治療認知損傷之方法,其中精神病性病症為與攻擊性不相關之精神分裂症。
28. 根據實施例20至23中任一項之治療認知損傷之方法,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
29. 根據實施例20至23中任一項之治療認知損傷之方法,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
30. 根據實施例20至29中任一項之治療認知損傷之方法,其中向患者投與50 mg至500 mg至少一種化合物每日一次。
31. 根據實施例20至30中任一項之治療認知損傷之方法,其中至少一種化合物係與至少一種額外活性劑組合投與。
32. 根據實施例31之治療認知損傷之方法,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
33. 根據實施例32之治療認知損傷之方法,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
34. 根據實施例20至33中任一項之治療認知損傷之方法,其中在投與之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
35. 根據實施例1至34中任一項之治療認知損傷之方法,其中至少一種化合物係以至少一種膜衣錠劑形式投與。
36. 一種治療患者之至少一種與精神分裂症相關之認知症狀的方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),
其包含向該患者投與50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
37. 根據實施例36之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
38. 根據實施例36或37之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
39. 根據實施例36至38中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
40. 根據實施例36至39中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中投與不治療至少一種與精神分裂症相關之負性症狀。
41. 根據實施例40之治療至少一種與精神分裂症相關之認知症狀的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
42. 根據實施例1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中投與不治療至少一種與精神分裂症相關之負性症狀。
43. 根據實施例42之治療至少一種與精神分裂症相關之認知症狀的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
44. 一種醫藥組合物,其供用於治療有需要患者中與精神分裂症相關之認知損傷,其中:
該醫藥組合物包含50 mg至500 mg至少一種選自化合物(
I:
及其醫藥學上可接受之鹽)之化合物;
該醫藥組合物供每日使用一次;及
患者之至少一種與精神分裂症相關之認知症狀係藉由該使用治療。
45. 根據實施例44之供使用之醫藥組合物,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
46. 根據實施例44或45之供使用之醫藥組合物,其中相對於使用之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,使用改善患者之BACS綜合評分。
47. 根據實施例44至46中任一項之供使用之醫藥組合物,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
48. 根據實施例44至47中任一項之供使用之醫藥組合物,其中相對於使用之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,使用改善患者之SCoRS訪問者總分。
49. 根據實施例44至48中任一項之供使用之醫藥組合物,其中在使用之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
50. 根據實施例49之供使用之醫藥組合物,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
51. 根據實施例49之供使用之醫藥組合物,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
52. 根據實施例49或50之供使用之醫藥組合物,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
53. 根據實施例49至52中任一項之供使用之醫藥組合物,其中至少一種與精神分裂症相關之穩定負性症狀在使用之前穩定持續至少一個月。
54. 根據實施例44至48中任一項之供使用之醫藥組合物,其中在使用之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
55. 根據實施例44至54中任一項之供使用之醫藥組合物,其中醫藥組合物係與至少一種額外活性劑組合使用。
56. 根據實施例55之供使用之醫藥組合物,其中至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。
57. 根據實施例56之供使用之醫藥組合物,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
58. 根據實施例44至57中任一項之供使用之醫藥組合物,其中醫藥組合物係供使用超過14週。
59. 根據實施例44至58中任一項之供使用之醫藥組合物,其中醫藥組合物係供使用超過20週。
60. 根據實施例44至59中任一項之供使用之醫藥組合物,其中該醫藥組合物包含50 mg至少一種化合物。
61. 根據實施例44至59中任一項之供使用之醫藥組合物,其中該醫藥組合物包含125 mg至少一種化合物。
62. 根據實施例44至59中任一項之供使用之醫藥組合物,其中該醫藥組合物包含500 mg至少一種化合物。
63. 根據實施例44至62中任一項之供使用之醫藥組合物,其中該使用不治療與精神分裂症相關之負性症狀。
64. 根據實施例63之供使用之醫藥組合物,其中在投與之前,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
65. 一種醫藥組合物,其供用於治療有需要患者中認知損傷,其中:
該醫藥組合物包含治療有效量之至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物;及
該患者在使用之前展現出至少一種認知症狀。
66. 根據實施例65之供使用之醫藥組合物,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
67. 根據實施例65或66之供使用之醫藥組合物,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
68. 根據實施例65至67中任一項之供使用之醫藥組合物,其中該使用治療至少一種認知症狀。
69. 根據實施例65至68中任一項之供使用之醫藥組合物,其中至少一種認知症狀係與精神病性病症相關。
70. 根據實施例69之供使用之醫藥組合物,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
71. 根據實施例69或70之供使用之醫藥組合物,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
72. 根據實施例69至71中任一項之供使用之醫藥組合物,其中精神病性病症為與攻擊性不相關之精神分裂症。
73. 根據實施例65至68中任一項之供使用之醫藥組合物,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
74. 根據實施例65至68中任一項之供使用之醫藥組合物,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
75. 根據實施例65至74中任一項之供使用之醫藥組合物,其中:
該醫藥組合物包含50 mg至500 mg至少一種化合物;
該醫藥組合物供每日使用一次。
76. 根據實施例65至75中任一項之供使用之醫藥組合物,其中醫藥組合物係與至少一種額外活性劑組合使用。
77. 根據實施例76之供使用之醫藥組合物,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
78. 根據實施例77之供使用之醫藥組合物,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
79. 根據實施例65至78中任一項之供使用之醫藥組合物,其中在使用之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
80. 根據實施例44至79中任一項之供使用之醫藥組合物,其中該醫藥組合物呈至少一種膜衣錠劑形式。
81. 一種醫藥組合物,其供用於治療患者之至少一種與精神分裂症相關之認知症狀,其中:
該醫藥組合物包含50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物;
該醫藥組合物供每日使用一次;
該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5);及
患者之至少一種與精神分裂症相關之認知症狀係藉由該使用治療。
82. 根據實施例81之供使用之醫藥組合物,其中相對於使用之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,使用改善患者之BACS綜合評分。
83. 根據實施例81或82之供使用之醫藥組合物,其中相對於使用之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,使用改善患者之SCoRS訪問者總分。
84. 根據實施例81至83中任一項之供使用之醫藥組合物,其中在使用之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
85. 根據實施例81至84中任一項之供使用之醫藥組合物,其中該使用不治療至少一種與精神分裂症相關之負性症狀。
86. 根據實施例85之供使用之醫藥組合物,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
87. 一種醫藥組合物之用途,其包含50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其用於製造供治療有需要患者中與精神分裂症相關之認知損傷的藥劑,其中:
該醫藥組合物供每日使用一次;及
患者之至少一種與精神分裂症相關之認知症狀係藉由該使用治療。
88. 根據實施例87之用途,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
89. 根據實施例87或88之用途,其中相對於使用之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,使用改善患者之BACS綜合評分。
90. 根據實施例87或89中任一項之用途,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
91. 根據實施例87或90中任一項之用途,其中相對於使用之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,使用改善患者之SCoRS訪問者總分。
92. 根據實施例87或91中任一項之用途,其中在使用之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
93. 根據實施例92之用途,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
94. 根據實施例92之用途,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
95. 根據實施例92或93之用途,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
96. 根據實施例87至95中任一項之用途,其中至少一種與精神分裂症相關之穩定負性症狀在使用之前穩定持續至少一個月。
97. 根據實施例87至91中任一項之用途,其中在使用之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
98. 根據實施例87至97中任一項之用途,其中醫藥組合物係與至少一種額外活性劑組合使用。
99. 根據實施例98之用途,其中至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。
100. 根據實施例99之用途,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
101. 根據實施例87至100中任一項之用途,其中醫藥組合物係供使用超過14週。
102. 根據實施例87至101中任一項之用途,其中醫藥組合物係供使用超過20週。
103. 根據實施例87至102中任一項之用途,其中該醫藥組合物包含50 mg至少一種化合物。
104. 根據實施例87至102中任一項之用途,其中該醫藥組合物包含125 mg至少一種化合物。
105. 根據實施例87至102中任一項之用途,其中該醫藥組合物包含500 mg至少一種化合物。
106. 根據實施例87至105中任一項之用途,其中該使用不治療與精神分裂症相關之負性症狀。
107. 根據實施例106之用途,其中投與之前,至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
108. 一種醫藥組合物之用途,其包含治療有效量之至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其用於治療有需要患者中認知損傷,其中該患者在使用之前展現出至少一種認知症狀。
109. 根據實施例108之用途,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
110. 根據實施例108或109之用途,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
111. 根據實施例108至110中任一項之用途,其中該使用治療至少一種認知症狀。
112. 根據實施例108至111中任一項之用途,其中至少一種認知症狀係與精神病性病症相關。
113. 根據實施例112之用途,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
114. 根據實施例112或113之用途,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
115. 根據實施例112至114中任一項之用途,其中精神病性病症為與攻擊性不相關之精神分裂症。
116. 根據實施例108至111中任一項之用途,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
117. 根據實施例108至111中任一項之用途,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
118. 根據實施例108至117中任一項之用途,其中:
該醫藥組合物包含50 mg至500 mg至少一種化合物;
該醫藥組合物供每日使用一次。
119. 根據實施例108至118中任一項之用途,其中醫藥組合物係與至少一種額外活性劑組合使用。
120. 根據實施例119之用途,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
121. 根據實施例120之用途,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
122. 根據實施例108至121中任一項之用途,其中在使用之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
123. 根據實施例87至122中任一項之用途,其中該醫藥組合物呈至少一種膜衣錠劑形式。
124. 一種醫藥組合物之用途,其包含50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其用於治療患者之至少一種與精神分裂症相關之認知症狀,其中:
該醫藥組合物供每日使用一次;
該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5);及
患者之至少一種與精神分裂症相關之認知症狀係藉由該使用治療。
125. 根據實施例124之用途,其中相對於使用之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,使用改善患者之BACS綜合評分。
126. 根據實施例124或125之用途,其中相對於使用之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,使用改善患者之SCoRS訪問者總分。
127. 根據實施例124至126中任一項之用途,其中在使用之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
128. 根據實施例124至127中任一項之用途,其中該使用不治療至少一種與精神分裂症相關之負性症狀。
129. 根據實施例128之用途,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
130. 一種增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性之方法,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次。
131. 根據實施例130之方法,其中向患者投與50 mg至少一種化合物每日一次。
132. 根據實施例130或131之方法,其中該方法增加患者之D-絲胺酸含量。
133. 根據實施例130至132中任一項之方法,其中該方法增加患者之長效增益。
134. 根據實施例130至133中任一項之方法,其中該方法增加患者之突觸可塑性。
135. 根據實施例130至134中任一項之方法,其中該患者在該投與之前展現出至少一種認知症狀。
136. 根據實施例135之方法,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
137. 根據實施例135之方法,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
138. 根據實施例130至137中任一項之方法,其中該投與改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
139. 根據實施例130至138中任一項之方法,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
140. 根據實施例130至138中任一項之方法,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
141. 根據實施例130至138中任一項之方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
142. 一種醫藥組合物,其供用於增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性,其中:
該醫藥組合物包含小於500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物;及
該醫藥組合物供每日使用一次。
143. 根據實施例142之供使用之醫藥組合物,其中該醫藥組合物包含50 mg至少一種化合物。
144. 根據實施例142或143之供使用之醫藥組合物,其中該使用增加患者之D-絲胺酸含量。
145. 根據實施例142至144中任一項之供使用之醫藥組合物,其中該使用增加患者之長效增益。
146. 根據實施例142至145中任一項之供使用之醫藥組合物,其中該使用增加患者之突觸可塑性。
147. 根據實施例142至146中任一項之供使用之醫藥組合物,其中該患者在使用之前展現出至少一種認知症狀。
148. 根據實施例147之供使用之醫藥組合物,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
149. 根據實施例147之供使用之醫藥組合物,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
150. 根據實施例142至149中任一項之供使用之醫藥組合物,其中該使用改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
151. 根據實施例142至150中任一項之供使用之醫藥組合物,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
152. 根據實施例142至150中任一項之供使用之醫藥組合物,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
153. 根據實施例142至150中任一項之供使用之醫藥組合物,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
154. 一種醫藥組合物之用途,其包含小於500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其用於製造用於增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性的藥劑,其中該醫藥組合物供每日使用一次。
155. 根據實施例154之用途,其中該醫藥組合物包含50 mg至少一種化合物。
156. 根據實施例154或155之用途,其中該使用增加患者之D-絲胺酸含量。
157. 根據實施例154至156中任一項之用途,其中該使用增加患者之長效增益。
158. 根據實施例154至157中任一項之用途,其中該使用增加患者之突觸可塑性。
159. 根據實施例154至158中任一項之用途,其中該患者在使用之前展現出至少一種認知症狀。
160. 根據實施例159之用途,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
161. 根據實施例159之用途,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
162. 根據實施例154至161中任一項之用途,其中該使用改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
163. 根據實施例154至162中任一項之用途,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
164. 根據實施例154至162中任一項之用途,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
165. 根據實施例154至162中任一項之用途,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
非限制性實例實施例 2 :
非限制性地,本發明之一些實施例/條項包括:
1. 一種治療有需要患者中與精神分裂症相關之認知損傷的方法,該方法包含向該患者投與50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
2. 根據條項1之治療與精神分裂症相關之認知損傷的方法,其中該方法包含:
● 向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
3. 根據條項1或2之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
4. 根據條項1至3中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
5. 根據條項1至4中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
6. 根據條項1至5中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
7. 根據條項1至6中任一項之治療與精神分裂症相關之認知損傷的方法,其中在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
8. 根據條項7之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
9. 根據條項7之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
10. 根據條項7或8之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
11. 根據條項7至10中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。
12. 根據條項1至6中任一項之治療與精神分裂症相關之認知損傷的方法,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
13. 根據條項1至12中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種化合物係與至少一種額外活性劑組合投與。
14. 根據條項13之治療與精神分裂症相關之認知損傷的方法,其中至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。
15. 根據條項14之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
16. 根據條項13之治療與精神分裂症相關之認知損傷的方法,其中至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
17. 根據條項1至16中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與至少一種化合物超過14週。
18. 根據條項1至17中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與至少一種化合物超過20週。
19. 根據條項1至18中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與50 mg至少一種化合物每日一次。
20. 根據條項1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與125 mg至少一種化合物每日一次。
21. 根據條項1至20中任一項之治療與精神分裂症相關之認知損傷的方法,其中投與不治療至少一種與精神分裂症相關之負性症狀。
22. 根據條項21之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
23. 一種治療有需要患者中認知損傷的方法,該方法包含向該患者投與治療有效量之至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其中該患者在該投與之前展現出至少一種認知症狀。
24. 根據條項23之治療認知損傷之方法,其中該方法包含:
● 向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
25. 根據條項23或24之治療認知損傷之方法,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
26. 根據條項23至25中任一項之治療認知損傷之方法,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
27. 根據條項23至26中任一項之治療認知損傷之方法,其中投與治療至少一種認知症狀。
28. 根據條項23至27中任一項之治療認知損傷之方法,其中至少一種認知症狀係與精神病性病症相關。
29. 根據條項28之治療認知損傷之方法,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
30. 根據條項28或29之治療認知損傷之方法,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
31. 根據條項28至30中任一項之治療認知損傷之方法,其中精神病性病症為與攻擊性不相關之精神分裂症。
32. 根據條項23至28中任一項之治療認知損傷之方法,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
33. 根據條項23至28中任一項之治療認知損傷之方法,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
34. 根據條項23至33中任一項之治療認知損傷之方法,其中向患者投與50 mg至少一種化合物每日一次。
35. 根據條項23至34中任一項之治療認知損傷之方法,其中至少一種化合物係與至少一種額外活性劑組合投與。
36. 根據條項35之治療認知損傷之方法,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
37. 根據條項36之治療認知損傷之方法,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
38. 根據條項23至37中任一項之治療認知損傷之方法,其中在投與之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
39. 根據條項1至38中任一項之治療認知損傷之方法,其中至少一種化合物係以至少一種膜衣錠劑形式投與。
40. 一種治療患者之至少一種與精神分裂症相關之認知症狀的方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),其包含向該患者投與50 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
41. 根據條項40之治療至少一種與精神分裂症相關之認知症狀的方法,其中該方法包含:
● 向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與50 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
42. 根據條項40或41之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
43. 根據條項40至42中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
44. 根據條項40至43中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
45. 根據條項40至44中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中投與不治療至少一種與精神分裂症相關之負性症狀。
46. 根據條項45之治療至少一種與精神分裂症相關之認知症狀的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
47. 根據條項40至46中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中向患者投與50 mg至少一種化合物每日一次。
48. 一種增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性之方法,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次。
49. 根據條項48之方法,其中向患者投與50 mg至少一種化合物每日一次。
50. 根據條項48或49之方法,其中該方法增加患者之D-絲胺酸含量。
51. 根據條項48至50中任一項之方法,其中該方法增加患者之長效增益。
52. 根據條項48至51中任一項之方法,其中該方法增加患者之突觸可塑性。
53. 根據條項48至52中任一項之方法,其中該患者在該投與之前展現出至少一種認知症狀。
54. 根條項53據之方法,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
55. 根據條項53之方法,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
56. 根據條項48至55中任一項之方法,其中該投與改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
57. 根據條項48至56中任一項之方法,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
58. 根據條項48至56中任一項之方法,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
59. 根據條項48至56中任一項之方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
非限制性實例實施例 3 :
非限制性地,本發明之一些實施例/特徵包括:
1. 一種治療有需要患者中與精神分裂症相關之認知損傷的方法,該方法包含向該患者投與1 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
2. 根據特徵1之治療與精神分裂症相關之認知損傷的方法,其中該方法包含:
● 向該患者投與1 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
3. 根據特徵1或2之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
4. 根據特徵1至3中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
5. 根據特徵1至4中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
6. 根據特徵1至5中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
7. 根據特徵1至6中任一項之治療與精神分裂症相關之認知損傷的方法,其中該投與改善至少一種選自以下之量度:
● 相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,患者在CPT-IP測試方面之表現;
● 相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,患者在BVMT-R測試方面之表現;
● 相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,患者在MSCEIT方面之表現;
● 相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,患者在VRFCAT方面之表現;及
● 相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,患者之CGI-S評分。
8. 根據特徵1至7中任一項之治療與精神分裂症相關之認知損傷的方法,其中在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
9. 根據特徵8之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
10. 根據特徵8之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
11. 根據特徵8或9之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
12. 根據特徵8至11中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。
13. 根據特徵1至7中任一項之治療與精神分裂症相關之認知損傷的方法,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
14. 根據特徵1至13中任一項之治療與精神分裂症相關之認知損傷的方法,其中至少一種化合物係與至少一種額外活性劑組合投與。
15. 根據特徵14之治療與精神分裂症相關之認知損傷的方法,其中至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。
16. 根據特徵15之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
17. 根據特徵14之治療與精神分裂症相關之認知損傷的方法,其中至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
18. 根據特徵1至17中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與至少一種化合物超過14週。
19. 根據特徵1至18中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與至少一種化合物超過20週。
20. 根據特徵1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與1 mg至100 mg至少一種化合物每日一次。
21. 根據特徵1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與20 mg或50 mg至少一種化合物每日一次。
22. 根據特徵1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與20 mg至少一種化合物每日一次。
23. 根據特徵1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向患者投與50 mg至少一種化合物每日一次。
24. 根據特徵1至23中任一項之治療與精神分裂症相關之認知損傷的方法,其中投與不治療至少一種與精神分裂症相關之負性症狀。
25. 根據特徵24之治療與精神分裂症相關之認知損傷的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
26. 根據特徵1至25中任一項之治療與精神分裂症相關之認知損傷的方法,其中患者處於精神藥物治療之穩定療程中。
27. 根據特徵1至26中任一項之治療與精神分裂症相關之認知損傷的方法,其中患者在投與之前至少一年被診斷患有精神分裂症。
28. 根據特徵1至27中任一項之治療與精神分裂症相關之認知損傷的方法,其中患者在投與之前具有穩定症狀至少3個月。
29. 一種治療有需要患者中認知損傷的方法,該方法包含向該患者投與治療有效量之至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物,其中該患者在該投與之前展現出至少一種認知症狀。
30. 根據特徵29之治療認知損傷的方法,其中該方法包含:
● 向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與治療有效量之至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
31. 根據特徵29或30之治療認知損傷的方法,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
32. 根據特徵29至31中任一項之治療認知損傷之方法,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
33. 根據特徵29至32中任一項之治療認知損傷之方法,其中投與治療至少一種認知症狀。
34. 根據特徵29至33中任一項之治療認知損傷之方法,其中至少一種認知症狀係與精神病性病症相關。
35. 根據特徵34之治療認知損傷的方法,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
36. 根據特徵34或35之治療認知損傷的方法,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
37. 根據特徵34至36中任一項之治療認知損傷之方法,其中精神病性病症為與攻擊性不相關之精神分裂症。
38. 根據特徵29至34中任一項之治療認知損傷之方法,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
39. 根據特徵29至34中任一項之治療認知損傷之方法,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
40. 根據特徵29至39中任一項之治療認知損傷之方法,其中向患者投與50 mg至少一種化合物每日一次。
41. 根據特徵29至39中任一項之治療認知損傷之方法,其中向患者投與20 mg至少一種化合物每日一次。
42. 根據特徵29至41中任一項之治療認知損傷之方法,其中至少一種化合物係與至少一種額外活性劑組合投與。
43. 根據特徵42之治療認知損傷的方法,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
44. 根據特徵43之治療認知損傷的方法,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
45. 根據特徵29至44中任一項之治療認知損傷之方法,其中在投與之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
46. 根據特徵1至45中任一項之治療認知損傷之方法,其中至少一種化合物係以至少一種膜衣錠劑形式投與。
47. 根據特徵1至46中任一項之治療認知損傷之方法,其中至少一種化合物係與水或牛奶一起投與。
48. 一種治療患者之至少一種與精神分裂症相關之認知症狀的方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),該方法包含向該患者投與1 mg至500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次,其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
49. 根據特徵48之治療至少一種與精神分裂症相關之認知症狀的方法,其中該方法包含:
● 向該患者投與1 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物每日一次。
50. 根據特徵48或49之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
51. 根據特徵48至50中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
52. 根據特徵48至51中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中該投與改善至少一種選自以下之量度:
● 相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,患者在CPT-IP測試方面之表現;
● 相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,患者在BVMT-R測試方面之表現;
● 相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,患者在MSCEIT方面之表現;
● 相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,患者在VRFCAT方面之表現;及
● 相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,患者之CGI-S評分。
53. 根據特徵48至52中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
54. 根據特徵48至53中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中投與不治療至少一種與精神分裂症相關之負性症狀。
55. 根據特徵54之治療至少一種與精神分裂症相關之認知症狀的方法,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
56. 根據特徵48至55中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中向患者投與50 mg至少一種化合物每日一次。
57. 根據特徵48至55中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中向患者投與20 mg至少一種化合物每日一次。
58. 一種增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性之方法,該方法包含向該患者投與小於500 mg至少一種選自化合物(
I):
及其醫藥學上可接受之鹽之化合物每日一次。
59. 根據特徵58之方法,其中向患者投與50 mg至少一種化合物每日一次。
60. 根據特徵58之方法,其中向患者投與20 mg至少一種化合物每日一次。
61. 根據特徵58至60中任一項之方法,其中該方法增加患者之D-絲胺酸含量。
62. 根據特徵58至61中任一項之方法,其中該方法增加患者之長效增益。
63. 根據特徵58至62中任一項之方法,其中該方法增加患者之突觸可塑性。
64. 根據特徵58至63中任一項之方法,其中該患者在該投與之前展現出至少一種認知症狀。
65. 根據特徵64之方法,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
66. 根據特徵64之方法,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
67. 根據特徵58至66中任一項之方法,其中該投與改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
68. 根據特徵58至67中任一項之方法,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
69. 根據特徵58至67中任一項之方法,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
70. 根據特徵58至67中任一項之方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
71. 一種化合物(
I):
或其醫藥學上可接受之鹽,
其供用於治療有需要患者中與精神分裂症相關之認知損傷的方法中,
該方法包含向該患者投與1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次,
其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
72. 根據特徵71之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該方法包含:
● 向該患者投與1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg化合物(
I)及其醫藥學上可接受之鹽每日一次。
73. 根據特徵71或72之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
74. 根據特徵71至73中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
75. 根據特徵71至74中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
76. 根據特徵71至75中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
77. 根據特徵71至76中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該投與改善至少一種選自以下之量度:
● 相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,患者在CPT-IP測試方面之表現;
● 相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,患者在BVMT-R測試方面之表現;
● 相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,患者在MSCEIT方面之表現;
● 相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,患者在VRFCAT方面之表現;及
● 相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,患者之CGI-S評分。
78. 根據特徵71至77中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
79. 根據特徵78之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
80. 根據特徵78之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
81. 根據特徵78或79之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
82. 根據特徵78至81中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。
83. 根據特徵71至77中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
84. 根據特徵71至83中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中化合物(
I)或其醫藥學上可接受之鹽係與至少一種額外活性劑組合投與。
85. 根據特徵84之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種額外活性劑治療患者之至少一種與精神分裂症相關之負性症狀。
86. 根據特徵85之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
87. 根據特徵84之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
88. 根據特徵71至87中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與化合物(
I)或其醫藥學上可接受之鹽超過14週。
89. 根據特徵71至88中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與化合物(
I)或其醫藥學上可接受之鹽超過20週。
90. 根據特徵71至89中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與1 mg至100 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
91. 根據特徵71至89中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與20 mg或50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
92. 根據特徵71至89中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
93. 根據特徵71至89中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
94. 根據特徵71至93中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中投與不治療至少一種與精神分裂症相關之負性症狀。
95. 根據特徵94之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
96. 根據特徵71至95中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中患者處於精神藥物治療之穩定療程中。
97. 根據特徵71至96中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中患者在投與之前至少一年被診斷患有精神分裂症。
98. 根據特徵71至97中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中患者在投與之前具有穩定症狀至少3個月。
99. 一種化合物(
I):
或其醫藥學上可接受之鹽,
其供用於治療有需要患者中認知損傷的方法中,
該方法包含向該患者投與治療有效量之化合物(
I)或其醫藥學上可接受之鹽,
其中該患者在該投與之前展現出至少一種認知症狀。
100. 根據特徵99之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該方法包含:
● 向該患者投與治療有效量之至少一種選自化合物(
I)或其醫藥學上可接受之鹽之化合物每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與治療有效量之化合物(
I)及其醫藥學上可接受之鹽每日一次。
101. 根據特徵99或100之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
102. 根據特徵99至101中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
103. 根據特徵99至102中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中投與治療至少一種認知症狀。
104. 根據特徵99至103中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係與精神病性病症相關。
105. 根據特徵104之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
106. 根據特徵104或105之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
107. 根據特徵104至106中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中精神病性病症為與攻擊性不相關之精神分裂症。
108. 根據特徵99至104中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
109. 根據特徵99至104中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
110. 根據特徵99至109中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
111. 根據特徵99至109中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
112. 根據特徵99至111中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中化合物(
I)或其醫藥學上可接受之鹽係與至少一種額外活性劑組合投與。
113. 根據特徵112之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
114. 根據特徵113之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
115. 根據特徵99至114中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中在投與之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
116. 根據特徵71至115中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中化合物(
I)或其醫藥學上可接受之鹽係以至少一種膜衣錠劑形式投與。
117. 根據特徵71至116中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中化合物(
I)或其醫藥學上可接受之鹽係與水或牛奶一起投與。
118. 一種化合物(
I):
或其醫藥學上可接受之鹽,
其供用於治療患者的至少一種與精神分裂症相關之認知症狀的方法中,
其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),
該方法包含向該患者投與供使用之1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
119. 根據特徵118之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該方法包含:
● 向該患者投與1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg化合物(
I)及其醫藥學上可接受之鹽每日一次。
120. 根據特徵118或119之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
121. 根據特徵118至120中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
122. 根據特徵118至121中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該投與改善至少一種選自以下之量度:
● 相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,患者在CPT-IP測試方面之表現;
● 相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,患者在BVMT-R測試方面之表現;
● 相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,患者在MSCEIT方面之表現;
● 相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,患者在VRFCAT方面之表現;及
● 相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,患者之CGI-S評分。
123. 根據特徵118至122中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
124. 根據特徵118至123中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中投與不治療至少一種與精神分裂症相關之負性症狀。
125. 根據特徵124之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
126. 根據特徵118至125中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
127. 根據特徵118至125中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
128. 一種化合物(
I):
或其醫藥學上可接受之鹽,
其供用於增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性的方法中,
該方法包含向該患者投與小於500 mg之化合物(
I)或其醫藥學上可接受之鹽每日一次。
129. 根據特徵128之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
130. 根據特徵128之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
131. 根據特徵128至130中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該方法增加患者之D-絲胺酸含量。
132. 根據特徵128至131中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該方法增加患者之長效增益。
133. 根據特徵128至132中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該方法增加患者之突觸可塑性。
134. 根據特徵128至133中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該患者在該投與之前展現出至少一種認知症狀。
135. 根據特徵134之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
136. 根據特徵134之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
137. 根據特徵128至136中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該投與改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
138. 根據特徵128至137中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
139. 根據特徵128至137中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
140. 根據特徵128至137中任一項之供使用之化合物(
I)或其醫藥學上可接受之鹽,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
141. 一種化合物(
I):
或其醫藥學上可接受之鹽之用途,
其用於製造供用於治療有需要患者中與精神分裂症相關之認知損傷的方法中的藥劑,
其中該方法包含向該患者投與1 mg至500 mg之化合物(
I)或其醫藥學上可接受之鹽每日一次,
其中該患者之至少一種與精神分裂症相關之認知症狀係藉由該投與治療。
142. 根據特徵141之用途,其中該方法包含:
● 向該患者投與1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg化合物(
I)及其醫藥學上可接受之鹽每日一次。
143. 根據特徵141或142之用途,其中至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
144. 根據特徵141至143中任一項之用途,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
145. 根據特徵141至144中任一項之用途,其中至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
146. 根據特徵141至145中任一項之用途,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
147. 根據特徵141至146中任一項之用途,其中該投與改善至少一種選自以下之量度:
● 相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,患者在CPT-IP測試方面之表現;
● 相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,患者在BVMT-R測試方面之表現;
● 相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,患者在MSCEIT方面之表現;
● 相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,患者在VRFCAT方面之表現;及
● 相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,患者之CGI-S評分。
148. 根據特徵141至147中任一項之用途,其中在投與之前,患者具有至少一種與精神分裂症相關之穩定負性症狀。
149. 根據特徵148之用途,其中至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
150. 根據特徵148之用途,其中該至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用PANSS來評定。
151. 根據特徵148或149之用途,其中至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(BNSS)工具來評定。
152. 根據特徵148至151中任一項之用途,其中至少一種與精神分裂症相關之穩定負性症狀在投與之前穩定持續至少一個月。
153. 根據特徵141至147中任一項之用途,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
154. 根據特徵141至153中任一項之用途,其中化合物(
I)或其醫藥學上可接受之鹽係與至少一種額外活性劑組合投與。
155. 根據特徵154之用途,其中該至少一種額外活性劑治療該患者之至少一種與精神分裂症相關之負性症狀。
156. 根據特徵155之用途,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
157. 根據特徵154之用途,其中至少一種額外治療劑係選自阿立哌唑、奧氮平、利培酮及反丁烯二酸喹硫平。
158. 根據特徵141至157中任一項之用途,其中向患者投與化合物(
I)或其醫藥學上可接受之鹽超過14週。
159. 根據特徵141至158中任一項之用途,其中向患者投與化合物(
I)或其醫藥學上可接受之鹽超過20週。
160. 根據特徵141至159中任一項之用途,其中向患者投與1 mg至100 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
161. 根據特徵141至159中任一項之用途,其中向患者投與20 mg或50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
162. 根據特徵141至159中任一項之用途,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
163. 根據特徵141至159中任一項之用途,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
164. 根據特徵141至163中任一項之用途,其中投與不治療至少一種與精神分裂症相關之負性症狀。
165. 根據特徵164之用途,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
166. 根據特徵141至165中任一項之用途,其中患者處於精神藥物治療之穩定療程中。
167. 根據特徵141至166中任一項之用途,其中患者在投與之前至少一年被診斷患有精神分裂症。
168. 根據特徵141至167中任一項之用途,其中患者在投與之前具有穩定症狀至少3個月。
169. 一種化合物(
I):
或其醫藥學上可接受之鹽之用途,
其用於製造供用於治療有需要患者中認知損傷的方法中的藥劑,
該方法包含向該患者投與治療有效量之化合物(
I)或其醫藥學上可接受之鹽,
其中該患者在該投與之前展現出至少一種認知症狀。
170. 根據特徵169之用途,其中該方法包含:
● 向該患者投與治療有效量之化合物(
I)或其醫藥學上可接受之鹽每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與治療有效量之化合物(
I)及其醫藥學上可接受之鹽每日一次。
171. 根據特徵169或170之用途,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
172. 根據特徵169至171中任一項之用途,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
173. 根據特徵169至172中任一項之用途,其中投與治療至少一種認知症狀。
174. 根據特徵169至173中任一項之用途,其中至少一種認知症狀係與精神病性病症相關。
175. 根據特徵174之用途,其中精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
176. 根據特徵174或175之用途,其中精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
177. 根據特徵174至176中任一項之用途,其中精神病性病症為與攻擊性不相關之精神分裂症。
178. 根據特徵169至174中任一項之用途,其中至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
179. 根據特徵169至174中任一項之用途,其中至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
180. 根據特徵169至179中任一項之用途,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
181. 根據特徵169至179中任一項之用途,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
182. 根據特徵169至181中任一項之用途,其中該化合物(
I)或其醫藥學上可接受之鹽係與至少一種額外活性劑組合投與。
183. 根據特徵182之用途,其中患者患有精神分裂症且該至少一種額外活性劑治療患者之至少一種負性症狀。
184. 根據特徵183之用途,其中至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
185. 根據特徵169至184中任一項之用途,其中在投與之前,患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
186. 根據特徵141至185中任一項之用途,其中化合物(
I)或其醫藥學上可接受之鹽係以至少一種膜衣錠劑形式投與。
187. 根據特徵141至186中任一項之用途,其中化合物(
I)或其醫藥學上可接受之鹽係與水或牛奶一起投與。
188. 一種化合物(
I):
或其醫藥學上可接受之鹽之用途,
其用於製造供用於治療患者的至少一種與精神分裂症相關之認知症狀的方法中的藥劑,
其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5),
該方法包含向該患者投與1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
189. 根據特徵188之用途,其中該方法包含:
● 向該患者投與1 mg至500 mg化合物(
I)或其醫藥學上可接受之鹽每日一次持續6至8天;
● 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及
● 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg化合物(
I)及其醫藥學上可接受之鹽每日一次。
190. 根據特徵188或189之用途,其中相對於投與之前量測的患者之簡易精神分裂症認知評定(BACS)綜合評分,投與改善患者之BACS綜合評分。
191. 根據特徵188至190中任一項之用途,其中相對於投與之前量測的患者之精神分裂症認知評分量表(SCoRS)訪問者總分,投與改善患者之SCoRS訪問者總分。
192. 根據特徵188至191中任一項之用途,其中該投與改善至少一種選自以下之量度:
● 相對於投與之前的持續表現測試-相同配對(CPT-IP)測試,患者在CPT-IP測試方面之表現;
● 相對於投與之前患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,患者在BVMT-R測試方面之表現;
● 相對於投與之前患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,患者在MSCEIT方面之表現;
● 相對於投與之前患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,患者在VRFCAT方面之表現;及
● 相對於投與之前量測的患者之臨床整體印象-嚴重程度量表(CGI-S)評分,患者之CGI-S評分。
193. 根據特徵188至192中任一項之用途,其中在投與之後,患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
194. 根據特徵188至193中任一項之用途,其中投與不治療至少一種與精神分裂症相關之負性症狀。
195. 根據特徵194之用途,其中至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
196. 根據特徵188至195中任一項之用途,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
197. 根據特徵188至195中任一項之用途,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
198. 一種化合物(
I):
或其醫藥學上可接受之鹽之用途,
其用於製造供用於增加有需要患者中D-絲胺酸含量、長效增益及/或突觸可塑性的方法中的藥劑,
該方法包含向該患者投與小於500 mg之化合物(
I)或其醫藥學上可接受之鹽每日一次。
199. 根據特徵198之用途,其中向患者投與50 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
200. 根據特徵198之用途,其中向患者投與20 mg化合物(
I)或其醫藥學上可接受之鹽每日一次。
201. 根據特徵198至200中任一項之用途,其中該方法增加患者之D-絲胺酸含量。
202. 根據特徵198至201中任一項之用途,其中該方法增加患者之長效增益。
203. 根據特徵198至202中任一項之用途,其中該方法增加患者之突觸可塑性。
204. 根據特徵198至203中任一項之用途,其中該患者在該投與之前展現出至少一種認知症狀。
205. 根據特徵204之用途,其中至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
206. 根據特徵204之用途,其中至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
207. 根據特徵198至206中任一項之用途,其中該投與改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
208. 根據特徵198至207中任一項之用途,其中患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
209. 根據特徵198至207中任一項之用途,其中患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
210. 根據特徵198至207中任一項之用途,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1、P3、P4、P5、P6的評分<5)。
本申請案主張2021年3月1日申請的美國臨時申請案第63/200,327號;2021年8月5日申請的美國臨時申請案第63/229,945號;2021年12月1日申請的美國臨時申請案第63/264,747號;2021年12月17日申請的美國臨時申請案第63/265,628號,該等專利之內容各自以全文引用之方式併入本文中。
定義:
除非另外陳述,否則如本文所使用,「一(a/an)」實體係指彼實體中之一或多者,例如「化合物」係指一或多種化合物或至少一種化合物。因此,術語「一」、「一或多個(種)」及「至少一個(種)」在本文中可互換地使用。
如本文所使用,術語「活性醫藥成分」(「API」)、「活性劑」或「治療劑」係指生物活性化合物。
如本文所使用,向患者「投與」API係指向患者引入或遞送API之任何途徑(例如口服遞送)。投與包括自投與及由另一者投與。
如本文所使用,「病況」、「病症」或「疾病」係關於任何不健康或異常狀態。
如本文所使用,「有效量」、「有效劑量」或「治療有效量」係指在單次或多次劑量投藥後,治療罹患病況之患者之分子的量。有效量可由主治診斷醫師經由使用已知技術及藉由在類似情形下獲得之觀測結果來確定。在確定有效量時,主治診斷醫師考慮多個因素,包括(但不限於):患者之物種;其體型、年齡及一般健康狀況;所涉及之特定病況、病症或疾病;病況、病症或疾病之涉及程度或嚴重程度;個別患者之反應;所投與之特定化合物;投與模式;所投與之製劑的生物可用性特徵;所選擇之給藥方案;伴隨藥療之使用;及其他相關情況。
如本文中所使用,就「至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物的毫克數」表述之量係以化合物(
I)之游離鹼及/或一或多種醫藥學上可接受之鹽形式存在的化合物(
I)之游離鹼之總重量計。
如本文所使用,「哺乳動物」係指馴養動物(例如,狗、貓及馬)及人類。在一些實施例中,哺乳動物為人類。
如本文所使用,術語「調節」係指正或負改變。非限制性實例調節包括1%變化、2%變化、5%變化、10%變化、25%變化、50%變化、75%變化或100%變化。
如本文所使用,術語「患者」及「個體」可互換使用且係指哺乳動物,諸如(例如)人類。
如本文所使用,「醫藥學上可接受之賦形劑」係指適用於製備醫藥組合物之載劑或賦形劑。舉例而言,醫藥學上可接受之賦形劑通常為安全的且包括通常視為可接受用於哺乳動物醫藥用途之載劑及賦形劑。作為一非限制性實例,醫藥學上可接受之賦形劑可為在聚集體中可充當活性成分之媒劑或介質之固體、半固體或液體物質。醫藥學上可接受之賦形劑之一些實例見於雷明頓氏醫藥科學(Remington's Pharmaceutical Sciences)及醫藥賦形劑之手冊(the Handbook of Pharmaceutical Excipients)中,且包括稀釋劑、媒劑、載劑、軟膏基、黏結劑、崩解劑、潤滑劑、滑動劑、甜味劑、調味劑、凝膠基、持續釋放型基質、穩定劑、防腐劑、溶劑、懸浮劑、緩衝液、乳化劑、染料、推進劑、包衣劑及其他。
如本文所使用,術語「醫藥學上可接受之鹽」係指本發明之化合物之無毒鹽形式。本發明之化合物(
I)之醫藥學上可接受之鹽包括衍生自適合的無機酸及有機酸以及無機鹼及有機鹼之醫藥學上可接受之鹽。醫藥學上可接受之鹽在此項技術中為吾人所熟知。適合醫藥學上可接受之鹽為例如揭示於Berge, S.M.等人
J . Pharma . Sci .66:1-19 (1977)中之彼等鹽。揭示於彼論文中之醫藥學上可接受之鹽的非限制性實例包括:乙酸鹽;苯磺酸鹽;苯甲酸酯;碳酸氫鹽;酒石酸氫鹽;溴化物;乙二胺四乙酸鈣;樟腦磺酸鹽;碳酸鹽;氯化物;檸檬酸鹽;二鹽酸鹽;乙二胺四乙酸鹽;乙二磺酸鹽;依託酸鹽;乙磺酸鹽;反丁烯二酸鹽;葡庚糖酸鹽;葡糖酸鹽;麩胺酸鹽;乙內醯胺苯胂酸鹽;己基間苯二酚酸鹽;海卓胺(hydrabamine);氫溴酸鹽;鹽酸鹽;羥基萘甲酸鹽;碘化物;羥乙磺酸鹽;乳酸鹽;乳糖酸鹽;蘋果酸鹽;順丁烯二酸鹽;杏仁酸鹽;甲磺酸鹽;甲基溴;甲基硝酸鹽;甲磺醯鹽;半乳糖二酸鹽;萘磺酸鹽;硝酸鹽;雙羥萘酸鹽(恩波酸鹽(embonate));泛酸鹽;磷酸鹽/二磷酸鹽;聚半乳糖醛酸鹽;水楊酸鹽;硬脂酸鹽;次乙酸鹽;丁二酸鹽;硫酸鹽;丹寧酸鹽(tannate);酒石酸鹽;茶氯酸鹽;三乙基碘;苯乍生(benzathine);氯普魯卡因(chloroprocaine);膽鹼;二乙醇胺;乙二胺;葡甲胺;普魯卡因(procaine);鋁鹽;鈣鹽;鋰鹽;鎂鹽;鉀鹽;鈉鹽;及鋅鹽。
衍生自適當酸的醫藥學上可接受之鹽之非限制性實例包括:由無機酸,諸如鹽酸、氫溴酸、磷酸、硫酸或過氯酸形成之鹽;由有機酸,諸如乙酸、草酸、順丁烯二酸、酒石酸、檸檬酸、琥珀酸或丙二酸形成之鹽;及藉由使用此項技術中所用之其他方法,諸如離子交換形成之鹽。醫藥學上可接受之鹽的非限制性實例包括己二酸鹽、褐藻酸鹽、抗壞血酸鹽、天冬胺酸鹽、苯磺酸鹽、苯甲酸鹽、硫酸氫鹽、硼酸鹽、丁酸鹽、樟腦酸鹽、樟腦磺酸鹽、檸檬酸鹽、環戊烷丙酸鹽、二葡糖酸鹽、十二烷基硫酸鹽、乙磺酸鹽、甲酸鹽、反丁烯二酸鹽、葡庚糖酸鹽、甘油磷酸鹽、葡糖酸鹽、半硫酸鹽、庚酸鹽、己酸鹽、氫碘酸鹽、2-羥基-乙磺酸鹽、乳糖酸鹽、乳酸鹽、月桂酸鹽、月桂基硫酸鹽、蘋果酸鹽、順丁烯二酸鹽、丙二酸鹽、甲磺酸鹽、2-萘磺酸鹽、菸鹼酸鹽、硝酸鹽、油酸鹽、草酸鹽、棕櫚酸鹽、雙羥萘酸鹽、果膠酸鹽、過硫酸鹽、3-苯基丙酸鹽、磷酸鹽、苦味酸鹽、特戊酸鹽、丙酸鹽、硬脂酸鹽、丁二酸鹽、硫酸鹽、酒石酸鹽、硫氰酸鹽、對甲苯磺酸鹽、十一烷酸鹽及戊酸鹽。衍生自適合鹼之醫藥學上可接受之鹽的非限制性實例包括鹼金屬鹽、鹼土金屬鹽、銨鹽及N
+(C
1 - 4烷基)
4鹽。本揭示案亦設想本文中所揭示化合物之任何鹼性含氮基團之四級銨化。鹼金屬及鹼土金屬鹽之非限制性實例包括鈉鹽、鋰鹽、鉀鹽、鈣鹽及鎂鹽。醫藥學上可接受之鹽之其他非限制性實例包括使用諸如鹵離子、氫氧根、羧酸根、硫酸根、磷酸根、硝酸根、低碳數烷基磺酸根及芳基磺酸根之相對離子形成之銨、四級銨及胺陽離子。醫藥學上可接受之鹽之其他非限制性實例包括苯磺酸鹽及葡糖胺鹽。
另外,「至少一種選自化合物(
I)及其醫藥學上可接受之鹽之化合物」可在本文中與「至少一種選自化合物(
I)及醫藥學上可接受之鹽之化合物或鹽」及「至少一種選自化合物(
I)及醫藥學上可接受之鹽的實體」互換使用。同樣,「至少一種化合物」可在本文中與「至少一種化合物或鹽」或「至少一種實體」互換使用。
如本文所使用,術語「降低」係指負改變至少5%,包括(但不限於)負改變5%、負改變10%、負改變25%、負改變30%、負改變50%、負改變75%或負改變100%。
如本文所使用,術語「治療(treat/treating/treatment)」當與病症或病況結合使用時,包括導致病症或病況改善之任何作用,例如減輕、減少、調節、緩解或消除。改善或減輕病症或病況之任何症狀的嚴重程度可易於根據此項技術中所已知的標準方法及技術予以評定。作為一非限制性實例,在一些實施例中,可使用認知成套測試(例如BACS、MCCB、CogState或Cambridge Cognition)或功能能力之量測(例如SCoRS、UPSA、UPSA-B、CAI或VRFCAT)評定投與作用。
如本文所使用,「卡爾加里精神分裂症抑鬱量表」或「CDSS」係用於評定患有精神分裂症之患者的重度抑鬱症之症狀,且具體言之,經設計以評定共存抑鬱症狀。參見例如,Addington D, Addington J, Maticka-Tyndale E. 「Assessing depression in schizophrenia: the Calgary Depression Scale.」
Br. J. Psychiatry Suppl.1993;(22):39-44。CDSS係由9項組成:抑鬱情緒、絕望、自我貶低、罪感性牽連觀念、病理性罪惡感、晨間抑鬱變重、早醒、自殺及觀測到之抑鬱表現。使用0至3分量表(0-3)對各項進行評分;CDSS評分可在0至27範圍內。CDSS上之各項為所有典型的抑鬱症狀且似乎不與精神分裂症之負性症狀重疊。CDSS將由研究者或其他合格現場人員進行。
除非相反地指示或以其他方式自上下文顯而易見,否則若一個、超過一個或所有群成員存在於給定產物或方法中、用於給定產物或方法中或以其他方式與給定產物或方法相關,則在該群組之至少一個成員之間包括「或」或「及/或」之申請專利範圍或描述視為滿足。本發明包括群組中恰好一個成員存在於、用於給定產物或方法中或另外與給定產物或方法相關之實施例。本發明包括其中超過一個或所有群組成員存在於給定產物或方法中、用於給定產物或方法中或以其他方式與給定產物或方法有關之實施例。
此外,本揭示案涵蓋其中來自所列舉之申請專利範圍中之至少一者的至少一個限制、要素、條項及描述性術語引入至另一申請專利範圍中之所有變化、組合及排列。舉例而言,依附於另一申請專利範圍之任何申請專利範圍可經修改以包括在依附於同一基本申請專利範圍之任何其他申請專利範圍中可見的至少一個限制。在要素以清單形式,諸如(例如)呈馬庫什群組(Markush group)形式呈現之情況下,亦揭示要素之各子組,且可自該組移除任何要素。應理解,一般而言,當本發明或本發明之態樣稱為包含特定要素及/或特徵時,本發明之實施例或本發明之態樣由此類要素及/或特徵組成或基本上由其組成。出於簡單之目的,彼等實施例尚未具體地以詞語闡述在本文中。除非另外指示,否則當給定範圍(諸如,例如[X]至[Y])之情況下,包括端點(諸如,例如片語「[X]至[Y]」中之[X]及[Y])。此外,除非另外指示或以其他方式自上下文及一般熟習此項技術者的理解顯而易見,否則表示為範圍之值可在本發明之不同實施例中採用所述範圍內之任何特定值或子範圍,除非上下文另外明確規定,否則達到該範圍下限之單位的十分之一。
一般熟習此項技術者將認識到或能夠僅使用常規實驗確定本文所描述之本發明之特定實施例的許多等效物。該等等效物欲由隨附申請專利範圍所涵蓋。
實例
以下實例僅意欲為說明性的且不意欲以任何方式限制本發明之範疇。
縮寫 % 百分比
aCSF 人工腦脊髓液
ANCOVA 互變異數分析
ANOVA 變異數分析
ASSR 聽覺穩態反應
ASST 注意力集中轉移任務
BACS 簡易精神分裂症認知評定
BNSS 簡易負性症狀量表
CI 信賴區間
CIAS 與精神分裂症相關之認知損傷
CR 制約反應
CS 制約刺激
CSF 腦脊髓液
d 天
DAAO D-胺基酸氧化酶
DB 雙盲
EBC 眨眼制約
ECG 心電圖
EEG 腦電圖
EPSP 興奮性突觸後電位
fEPSP 場興奮性突觸後電位
F/U 隨訪
g 公克
h 小時
HFS 高頻刺激
Hz 赫茲
kg 公斤
LS 最小平方
LTD 長期抑制
LTP 長效增益
m
2平方公尺
mg 毫克
min 分鐘
mL 毫升
mm 毫米
MMN 失配負波
NMDA N-甲基-d-天冬胺酸
ns 不顯著
PANSS NSFS 正性及負性症候群量表-負性症狀因子評分
PK 藥物動力學
PD 藥力學
qd 每日一次
s 秒
SCoRS 精神分裂症認知評分量表
SD 標準差
SE 標準誤差
STP 短效增益
TEAE 治療引發不良事件
US 非制約刺激
UR 非制約反應
實例1:小鼠中在用化合物(I)進行急性及亞慢性口服給藥之後的海馬體長效增益之臨床前評估
DAAO抑制增加D-絲胺酸(N-甲基-d-天冬胺酸(NMDA)受體之共促效劑)之含量。DAAO酶在小腦中高度表現,且因此,藉由化合物(
I)抑制DAAO應會引起小腦中之D-絲胺酸含量增加,其隨後亦可在腦脊髓液(CSF)中被量測到。經由仍有待闡明之機制,小腦中之D-絲胺酸含量增加亦可影響腦部之遠端區(諸如海馬體)或皮質區。
嚙齒動物之臨床前研究已探究化合物(
I)對認知表現任務之影響(
表 1)。在表1中,+號意謂有效,-號意謂無效,且空單元格指示未對劑量進行測試。在此等臨床前研究中,相較於急性給藥,歷時14天之化合物(
I)之亞慢性給藥在新物體識別任務之行為反應中引起敏感(亦即,最低有效劑量降低且在較高劑量下失去功效)。此等發現表明化合物(
I)在亞慢性給藥後可能影響海馬體突觸可塑性。
表 1. 化合物(
I)之亞慢性給藥後的活體內模型中之敏感反應
| 功效 / 藥力學標記物 | 物種 | 劑量(mg/kg) | |||||||||
| 0.001 | 0.003 | 0.01 | 0.03 | 0.1 | 0.3 | 1 | 3 | 10 | 30 | ||
| 單一劑量 | |||||||||||
| 新物體識別(認知) | 小鼠 | - | + | + | + | + | |||||
| ASST (執行功能) | 大鼠 | +/- | + | + | + | ||||||
| BALB/C社交互動(急性) | 小鼠 | - | + | + | |||||||
| Poly I:C社交互動(急性) | 小鼠 | - | - | + | |||||||
| 小腦中之D-絲胺酸增加(6小時) | 小鼠 | + | + | + | + | ||||||
| 10 天,每日一次(QD) | |||||||||||
| 眨眼制約(失調及精神分裂症) | 小鼠 | + | + | ||||||||
| 14 天,每日一次(QD) | |||||||||||
| 新物體識別(認知) | 小鼠 | - | + | + | + | + | - | - | - | ||
| 注意力集中轉移任務(ASST) (執行功能) | 大鼠 | +/- | + | + | + | ||||||
| BALB/C社交互動(負性症狀) | 小鼠 | - | - | + | + | + | + | + | + | ||
| 小腦中之D-絲胺酸增加(6小時) | 小鼠 | - | - | + | + | + |
在此研究中,在用化合物(
I)進行急性及亞慢性(14天)給藥之後,使用公認長效增益(LTP)範例評估海馬體突觸可塑性。
大鼠海馬體切片之製備
為了獲得大鼠海馬體切片,在無麻醉下藉由快速斷頭術使4週齡史泊格多利大鼠(Sprague Dawley rat) (由Elevage Janvier (Le Genest-Saint-Isle, France)提供)安樂死。快速移出腦部且將其浸泡於以下冰冷含氧緩衝液:2 mM KCl,1.2 mM NaH
2PO
4,7 mM MgCl
2,0.5 mM CaCl
2,26 mM NaHCO
3,11 mM葡萄糖及250 mM蔗糖。以400 μ m厚度使用McILWAIN組織切片機製備海馬體切片。使切片在室溫下在以下人工CSF (aCSF)中恢復至少1小時:126 mM NaCl,3.5 mM KCl,1.2 mM NaH
2PO
4,1.3 mM MgCl
2,2 mM CaCl
2,25 mM NaHCO
3及11 mM葡萄糖。在實驗期間,用含氧aCSF連續灌注切片。動物係根據法國及歐洲法規進行圈養及使用。
小 鼠海馬體切片之製備
給與年齡為5至6週之野生型小鼠(總計97隻;每種條件n=5至8隻)化合物(
I)之急性或亞慢性(14天)口服劑量(0.001 mg/kg至10 mg/kg,p.o.)或媒劑(1% Tween 80於0.5%甲基纖維素中)。5小時後收集海馬體切片。亦獲得小腦及血漿以量測實驗動物中達成之D-絲胺酸含量。
從置於腔室上且用aCSF以恆定速率灌注之單一海馬體切片獲得電生理學記錄。使用填充有aCSF之玻璃微量吸管記錄CA1放線層中之細胞外場興奮性突觸後電位(fEPSP)。fEPSP係用置於放線層中之玻璃刺激電極以0.1 Hz由對薛氏側枝/連合路徑進行電刺激來引起。
為測試化合物(
I)對基礎突觸傳遞之影響,在實驗開始時構組輸入/輸出(I/V)曲線。量測fEPSP之斜率且相對於不同強度之刺激(0至100 µA)進行繪製。在基線刺激強度下藉由θ脈衝串刺激方案(10個脈衝串,各脈衝串有4個脈衝,在100 Hz下,各脈衝串之間有200 ms)誘導長效增益(LTP)。在此制約刺激之後,記錄1小時測試時段,其中藉由每10秒一次之單一刺激(0.1 Hz)在相同刺激強度下再次引起反應。
結果
相較於大鼠海馬體中之對照組,D-絲胺酸之急性高劑量(1 mM)誘導海馬體突觸可塑性(短效增益及長期抑制) (
圖 1A 至圖 1C)。
圖 1A 及圖 1B中之資料標準化為10分鐘控制時間。D-絲胺酸增加興奮性突觸後電位(EPSP)幅值之增強,但此變化在統計學上並不顯著(p=0.0603,非配對t測試)。然而,D-絲胺酸顯著降低EPSP幅值之抑制(p=0.0374,非配對t測試)。
化合物(
I)之單次口服劑量未顯著影響LTP (基於單因子變異數分析[ANOVA]對比小鼠海馬體中媒劑之投與) (
圖 2)。相比之下,化合物(
I)之低亞慢性口服劑量(0.001 mg/kg及0.01 mg/kg)誘導LTP增加,而較高劑量(0.1 mg/kg及10 mg/kg)與LTP降低相關(所有劑量p<0.05對比媒劑,基於單因子ANOVA事後多重比較分析) (
圖 3),表明突觸可塑性增加。另外,在用化合物(
I)對小鼠進行亞慢性給藥之後,觀測到血漿及小腦中D-絲胺酸含量之劑量依賴性增加(
圖 4A ,圖 4B)。特定言之,化合物(
I)引起小鼠腦部(8.7 nmol/g至34 nmol/g)及小鼠血漿(213 ng/mL至490 ng/mL)中D-絲胺酸含量之劑量依賴性增加。
論述
化合物(
I)在慢性給藥時誘導活體內反應之敏感,其表明突觸可塑性之潛在變化。化合物(
I)之急性給藥未改變LTP,此為反映神經元突觸可塑性之變化的現象。D-絲胺酸含量之急劇變化不大可能在突觸中產生結構變化;然而,在D-絲胺酸含量之慢性增加之後觀測到可塑性變化,其可在用化合物(
I)進行慢性給藥之後達成。較低劑量之化合物(
I)之亞慢性給藥顯著增加LTP,表明突觸可塑性增加。較高劑量(0.1 mg/kg及10 mg/kg)誘導LTP降低,指示反向U形劑量反應。此現象可能為急性對比慢性給藥之後觀測到的行為反應(亦即,新物體識別任務)左移的基礎。此研究中所報導之劑量-反應關係左移表明低劑量在DAAO抑制劑(諸如化合物(
I))之臨床試驗中可為有效的。
實例2:10 mg包含化合物(I)之調配物(製劑1)
將羥丙基纖維素(810 g,等級L,由NIPPON SODA有限公司生產)溶解於純化水(12690 g)中以製備黏結劑溶液。將化合物(
I) (900 g)、D-甘露糖醇(19620 g,PEARLITOL 50C,由Roquette公司生產)及微晶纖維素(2700 g,CEOLUS PH-101,由Asahi Kasei公司生產)在流化床粒化機(FD-WGS-30,由Powrex公司製造)中粒化,同時噴塗黏結劑溶液,且接著乾燥以得到粒化粉末。分2批製造粒化粉末。接著研磨粒化粉末,稱量44060 g之所得研磨粉末,且添加低取代之羥丙基纖維素(4950 g,等級LH-21,由Shin-Etsu Chemical有限公司生產) (含有11%羥丙氧基(乾重)),及硬脂酸鎂(495 g,由Taihei Chemical Industrial有限公司生產)且混合以得到混合粉末。使用旋轉式製錠機(AQUARIUS 08242L2JI,由KIKUSUI SEISAKUSHO有限公司製造)將所得混合粉末製備為錠劑以得到每錠重量為300 mg且直徑為9 mm之無包衣錠劑。將40500 g所得無包衣錠劑插入至Doria塗佈機(DRC-900S,由Powrex公司製造)中,且噴塗羥丙甲纖維素、聚乙二醇6000、氧化鈦、紅氧化鐵及黃氧化鐵之水性分散液以製備每錠12.2 mg之膜衣且獲得製劑1 (膜衣錠劑)。製劑1之組成(以每錠計)示於
表 2中。
表 2.每錠製劑1之組成(10 mg調配物)
實例3:25 mg包含化合物(I)之調配物(製劑2)
| 組分 | 量(mg) |
| 化合物( I) | 10 |
| D-甘露糖醇(PEARLITOL 50C) | 218 |
| 微晶纖維素(CEOLUS PH-101) | 30 |
| 羥丙基纖維素(HPC-L) | 9 |
| 低取代之羥丙基纖維素(LH-21) | 30 |
| 硬脂酸鎂 | 3 |
| 羥丙甲纖維素(TC-5R) | 9 |
| 二氧化鈦 | 1 |
| 紅氧化鐵 | 0.1 |
| 黃氧化鐵 | 0.1 |
| 總計 | 310.2 |
將羥丙基纖維素(810 g,等級L,由NIPPON SODA有限公司生產)溶解於純化水(12690 g)中以製備黏結劑溶液。將化合物(
I) (2250 g)、D-甘露糖醇(18270 g,PEARLITOL 50C,由Roquette公司生產)及微晶纖維素(2700 g,CEOLUS PH-101,由Asahi Kasei公司生產)在流化床粒化機(FD-WGS-30,由Powrex公司製造)中粒化,同時噴塗黏結劑溶液,且接著乾燥以得到粒化粉末。分2批製造粒化粉末。接著研磨粒化粉末,稱量44060 g之所得研磨粉末,且添加低取代之羥丙基纖維素(4950 g,等級LH-21,由Shin-Etsu Chemical有限公司生產) (含有11%羥丙氧基(乾重)),及硬脂酸鎂(495 g,由Taihei Chemical Industrial有限公司生產)且混合以得到混合粉末。使用旋轉式製錠機(AQUARIUS 08242L2JI,由KIKUSUI SEISAKUSHO有限公司製造)將所得混合粉末製備為錠劑以得到每錠重量為300 mg且直徑為9 mm之無包衣錠劑。將40500 g所得無包衣錠劑插入至Doria塗佈機(DRC-900S,由Powrex公司製造)中,且噴塗羥丙甲纖維素、聚乙二醇6000、氧化鈦、紅氧化鐵及黃氧化鐵之水性分散液以製備每錠12.2 mg之膜衣且獲得製劑2 (膜衣錠劑)。製劑2之組成(以每錠計)示於
表 3中。
表 3.每錠製劑2之組成(25 mg調配物)
實例4:100 mg包含化合物(I)之調配物(製劑3)
| 組分 | 量(mg) |
| 化合物( I) | 25 |
| D-甘露糖醇(PEARLITOL 50C) | 203 |
| 微晶纖維素(CEOLUS PH-101) | 30 |
| 羥丙基纖維素(HPC-L) | 9 |
| 低取代之羥丙基纖維素(LH-21) | 30 |
| 硬脂酸鎂 | 3 |
| 羥丙甲纖維素(TC-5R) | 9 |
| 二氧化鈦 | 1 |
| 紅氧化鐵 | 0.1 |
| 黃氧化鐵 | 0.1 |
| 總計 | 310.2 |
每錠含有100 mg化合物(
I)的製劑3(膜衣錠劑)可由相似製造方法產生。製劑3之組成(以每錠計)示於
表 4中。
表 4.每錠製劑3之組成
實例5:50 mg包含化合物(I)之調配物(製劑4)
| 組分 | 量(mg) |
| 化合物(A) | 100 |
| D-甘露糖醇(PEARLITOL 50C) | 128 |
| 微晶纖維素(CEOLUS PH-101) | 30 |
| 羥丙基纖維素(HPC-L) | 9 |
| 低取代之羥丙基纖維素(LH-21) | 30 |
| 硬脂酸鎂 | 3 |
| 羥丙甲纖維素(TC-5R) | 9 |
| 二氧化鈦 | 1 |
| 紅氧化鐵 | 0.1 |
| 黃氧化鐵 | 0.1 |
| 總計 | 310.2 |
每錠含有50 mg化合物(
I)的製劑4 (膜衣錠劑)可由相似製造方法產生。製劑4之組成(以每錠計)示於
表 5中。
表 5.每錠製劑4之組成
實例6:評估化合物(I)之3個劑量在具有精神分裂症之負性症狀的成年參與者之輔助治療中的功效、安全性、耐受性及藥物動力學的研究(NCT03382639)
| 組分 | 量(mg) |
| 化合物( I) | 50 |
| D-甘露糖醇(PEARLITOL 50C) | 178 |
| 微晶纖維素(CEOLUS PH-101) | 30 |
| 羥丙基纖維素(HPC-L) | 9 |
| 低取代之羥丙基纖維素(LH-21) | 30 |
| 硬脂酸鎂 | 3 |
| 羥丙甲纖維素(TC-5R) | 9 |
| 二氧化鈦 | 1 |
| 紅氧化鐵 | 0.1 |
| 黃氧化鐵 | 0.1 |
| 總計 | 310.2 |
進行2期隨機分組、雙盲、平行組、安慰劑對照、劑量範圍探索研究臨床試驗(INTERACT)以確定附加/輔助化合物(
I)在治療具有精神分裂症之持久負性症狀的成年患者中是否優於安慰劑(ClinicalTrials.gov識別碼:NCT03382639)。此多中心試驗在美國、保加利亞、捷克共和國、意大利、波蘭、俄羅斯聯邦、塞爾維亞、西班牙及烏克蘭進行。研究在503名患者中征選256名篩選合格之患者(
表 5 , 表 6)。符合條件之參與者年齡為18至60歲,精神分裂症之症狀穩定,且基線簡易負性症狀量表(BNSS)評分為28或更高(12項,不包括第4項)。另外,符合條件之參與者以2-6 mg日劑量之利培酮當量接受穩定抗精神病治療,且若以低於治療劑量作為催眠劑使用第二抗精神病藥(受試驗委託者批准),則允許參與者用第二抗精神病藥治療。最常見之伴隨抗精神病藥物為阿立哌唑(25.4%)、奧氮平(18.8%)、利培酮(18.0%)及反丁烯二酸喹硫平(9.4%)。為克服潛在的混淆影響,不包括具有抑鬱及錐體外症狀之彼等者。
參與者在雙盲期被隨機分配(機遇,例如翻轉硬幣)至四個處理組中之一者:(1)化合物(
I) 50 mg,每日一次(5個製劑1錠劑);(2)化合物(
I) 125 mg,每日一次(5個製劑2錠劑);(3)化合物(
I) 500 mg,每日一次(5個製劑3錠劑);及(4)安慰劑,每日一次(5個口服安慰劑錠劑)。此研究之劑量選擇係基於靶佔有率及D-絲胺酸之升高。
總體而言,256名參與者係以3:2:2:2隨機分組以分別接受安慰劑、化合物(
I) 50 mg、化合物(
I) 125 mg及化合物(
I) 500 mg,其中228名(89.1%)參與者完成研究。參與者平均年齡為40歲(範圍為18-60歲),168名(65.6%)為男性,且208名(81.3%)為白人。人口資料及基線特徵均勻分佈於整個處理組中。
以錠劑形式每日一次口服投與化合物(
I),持續至多14週。化合物(I)安慰劑-匹配錠劑係同樣每日一次口服投與,持續至多14週。除非存在緊急醫療需求,否則處理組在研究期間對參與者及研究醫生/現場人員保持不被揭示。
研究之納入標準包括:
1.如精神病症診斷與統計手冊,第五版(DSM-5)的關於精神病性病症之簡明國際神經精神訪談(MINI) 7.0.2及一般精神病學評估所界定,目前有精神分裂症之診斷。
2.初始診斷必須在篩選後大於或等於(≥1)年。
3.正在接受初級背景抗精神病療法(氯氮平除外),每日總劑量在2-6 mg利培酮當量之間。若用於治療特定症狀,諸如失眠或焦慮(例如,視焦慮需要,喹硫平25-50 mg或其等效劑量),則經試驗委託者或指定人員批准,可准許用低於治療劑量之第二抗精神病藥進行伴隨治療,但若其用於難治性正性精神病症狀,則不准許。
4.用精神藥物治療之穩定療程治療,而在篩選訪視之前2個月內,處方劑量無臨床意義之變化(不增加劑量,關於耐受性之劑量降低小於或等於[≤]百分之25 [25%]),且在整個研究參與期間,直至第84天/提早終止訪視,預計沒有劑量調整。
5.BNSS總分(12項,不包括第4項) ≥28;穩定單盲安慰劑磨合期及基線BNSS總分(12項,不包括第4項)(相對於篩選評分變化≤ 20%)。
6.PANSS正性症狀項P1 (妄想)、P3 (幻覺行為)、P4 (興奮)、P5 (自大)、P6 (猜疑)及/或G9 (不尋常思考內容)的評分不超過中重度(≤5),其中此等項中最多有2項評分為『5』;P2 (概念混亂)之評分不超過中度(≤4)。
7.有跡象表明,參與者在篩選訪視之前≥3個月具有穩定症狀(例如,沒有因精神分裂症住院,沒有因精神分裂症之症狀而進急診室,沒有因精神分裂症之症狀惡化而增加精神照護程度)。
8.有一個將能夠為完成研究評分量表,包括PANSS及SCoRS提供意見的成人資訊提供者(例如,家庭成員、社會工作者、個案工作者、住宿機構工作人員,或每週與參與者相處≥4小時的護士),且被研究者認為係可靠的。資訊提供者必須能夠且願意提供書面知情同意書,且至少參與1次面談,隨後能夠藉由參加各臨床評定訪視或經由參與包括PANSS或SCoRS指標的其他研究訪視的電話訪問來提供持續的意見。
研究之排除標準包括:
1.基於MINI與一般精神病學評估之組合,終身被診斷為分裂情感性精神障礙;終身被診斷為躁鬱症;或終身被診斷為強迫症。
2.基於DSM-5之MINI及一般精神病學評估,最近(過去6個月內)發生過恐慌症、抑鬱發作或目前需要臨床關注的其他共存精神病況。
3.基於DSM-5之MINI及一般精神病學評估,在過去6個月內診斷有物質使用障礙(尼古丁依賴除外)。
4.在隨機分組之前,正在參與正式的結構化非醫藥社會心理治療性治療計劃(認知矯正、認知行為治療、重症症狀/職業康復),持續時間小於(<) 3個月。此外,在參與研究期間至第84天訪視中,不允許開始此類非醫藥治療計劃。
5.參試者展現出超過極低程度的抗精神病藥誘發之帕金森氏症症狀,如改良版辛普森-安格斯量表(Modified Simpson Angus Scale;SAS)(第10項,靜坐不能除外)之評分(>)6所記錄。
6.如藉由卡爾加里抑鬱量表評分(CDSS) > 9所量測,具有抑鬱症跡象。
7.被研究者認為有自殺或對自己、他人或財產造成傷害的迫在眉睫的風險,或參與者在篩選前的過去一年內曾試圖自殺過。在隨機分組之前,哥倫比亞-自殺嚴重程度評分量表(Columbia-Suicide Severity Rating Scale;C-SSRS)第4項或第5項有肯定答案的參與者被排除在外(基於過去一年)。
8.有與喪失意識>15分鐘相關的腦外傷史。
9.在12歲之前有精神分裂症診斷。
10.在篩選之前6個月(180天)內接受過電痙攣療法。
11.有發育性智能障礙或智力遲鈍的病史。
12.在篩選或安慰劑磨合期訪視時,參與者之初級背景抗精神病藥之抗精神病藥血漿含量低於根據抗精神病藥參考文件(Antipsychotic Reference document)中的最低可接受濃度標準。此標準不適用於服用初級背景抗精神病藥的參與者,因為其臨床分析結果不詳。
13.有治療抗性。治療抗性定義為精神分裂症之正性症狀之前對使用不同化學類別之抗精神病藥治療至少4週的2個療程沒有反應,各療程之劑量被視為有效的。
14.沒有穩定的住所或無家可歸。
該研究包含28天篩選期;14天單盲安慰劑磨合期,以預期性地評估藥物依從性及BNSS評分穩定性;及12週雙盲處理期(
圖 5)。參與研究之總時間為大約20週。完成研究之參與者通常要至門診進行11次就診,且在最後一次劑量之化合物(
I)(第98天)之後10至14天隨訪以進行安全性評定。人口資料、基線特徵及功效評定係基於全分析集,該全分析集包括在處理期間接受至少一次劑量之研究藥物的隨機參與者(
表 6)。安全性分析集包括接受至少一次劑量之研究藥物的隨機參與者。所有256名入選患者包括於全分析集及安全性分析集中。
表 6.入選INTERACT研究中之患者的基線人口資料及臨床特徵(全分析集)
BACS,簡易精神分裂症認知評定;max.,最大值;Min.,最小值;PANSS NSFS,正性及負性症候群量表-負性症狀因子評分;SCoRS,精神分裂症認知評分量表;SD,標準差。
| 安慰劑 (n = 87) | 化合物(I) 50 mg (n = 58) | 化合物(I) 125 mg (n = 56) | 化合物(I) 500 mg (n = 55) | |
| 年齡,歲 平均值(SD) Min., max. | 39.9 (11.11) 20, 60 | 39.9 (10.96) 21, 60 | 40.1 (9.80) 23, 60 | 40.1 (11.79) 18, 60 |
| 性別,n (%) 男性 女性 | 63 (72.4) 24 (27.6) | 38 (65.5) 20 (34.5) | 34 (60.7) 22 (39.3) | 33 (60.0) 22 (40.0) |
| 種族,n (%) 美洲印第安人 或阿拉斯加土著人 亞洲人 黑人或非洲裔 美國人 白人 未報導者 | 2 (2.3) 2 (2.3) 10 (11.5) 70 (80.5) 3 (3.4) | 0 0 9 (15.5) 46 (79.3) 3 (5.2) | 1 (1.8) 3 (5.4) 9 (16.1) 42 (75.0) 1 (1.8) | 0 0 5 (9.1) 50 (90.9) 0 |
| 基線處之PANSS NSFS | ||||
| 平均值(SD) Min., max. | 24.6 (4.76) 14, 41 | 24.6 (4.25) 17, 35 | 24.1 (4.36) 16, 37 | 24.3 (5.02) 16, 37 |
| 基線處之BACS 綜合評分 | ||||
| 平均值(SD) Min., max. | 33.4 (15.50) -11, 72 | 31.3 (15.61) -10, 63 | 32.6 (13.44) 0, 62 | 33.6 (12.67) 2, 62 |
| 基線處之SCoRS 訪問者總分 | ||||
| 平均值(SD) Min., max. | 39.5 (9.90) 20, 61 | 39.6 (10.63) 21, 73 | 38.5 (10.21) 20, 62 | 41.3 (9.89) 23, 60 |
所評估之主要指標為負性症狀變化,量測為正性及負性症候群量表-負性症狀因子評分(PANSS NSFS)中相對於基線之12週變化。對於負性症狀,在第12週,使用化合物(
I) 50 mg、125 mg或500 mg未觀測到PANSS NSFS相對於安慰劑有顯著改善(分別呈
p= 0.426,
p= 0.362及
p= 0.808)。自基線至第12週,使用化合物(
I) 50 mg、125 mg或500 mg,PANSS NSFS中之最小平方(LS)平均變化分別為:-3.3 (95%信賴區間[CI],-4.3至-2.2)、-3.4 (95% CI,-4.4至-2.3)及-2.5 (95% CI,-3.6至-1.5),且使用安慰劑,其為-3.1 (95% CI,-4.0至-2.3) (
圖 6)。另外,如使用BNSS所量測,負性症狀中未觀測到顯著改善。
安全性指標包括治療引發不良事件(TEAE)。總共有76名參與者(29.7%)經歷TEAE,其中23名(9%)被研究者認為與藥物有關。大部分TEAE之嚴重程度為輕度或中度(
表 7)。在超過5名參與者(大於或等於2%之研究參與者)中出現之TEAE為頭痛、失眠及體重增加,其在化合物(
I)及安慰劑組中觀測到之頻率相似。輕度、中度及重度TEAE分別出現於49名(19.1%)、24名(9.4%)及3名(1.2%)參與者中。嚴重的橫紋肌溶解症(安慰劑,n = 1)及慢性膽囊炎(化合物(
I) 50 mg,n = 1)事件不被視為與藥物相關。一名服用化合物(
I) 125 mg之參與者被報導有重度精神分裂症,且被視為與藥物相關之嚴重TEAE。安慰劑組中報導有四例嚴重TEAE;無一者被視為藥物相關。五名參與者,包括三名服用安慰劑之參與者,經歷導致中斷之TEAE (血肌酸磷酸激酶增加、肝功能測試結果增加、精神病症)。未報導有死亡,且各組在安全性、實驗室、生命體徵或心電圖評定方面未觀測到臨床上有顯著結果。
表 7.入選INTERACT研究之患者之TEAE發生率(安全性分析組)
| 安慰劑 (N = 87) | 化合物(I) 50 mg (N = 58) | 化合物(I) 125 mg (N = 56) | 化合物(I) 500 mg (N = 55) | |
| 具有任何TEAE 之患者 輕度 中度 重度 | 30 (34.5) 18 (20.7) 11 (12.6) 1 (1.1) | 13 (22.4) 10 (17.2) 2 (3.4) 1 (1.7) | 17 (30.4) 13 (23.2) 3 (5.4) 1 (1.8) | 16 (29.1) 8 (14.5) 8 (14.5) 0 |
| 與研究藥物相關之TEAE a | 12 (13.8) | 0 | 4 (7.1) | 7 (12.7) |
| 嚴重不良事件 | 4 (4.6) | 0 | 1 (1.8) | 0 |
| 死亡 | 0 | 0 | 0 | 0 |
| 導致研究中斷之TEAE | 3 (3.4) | 0 | 1 (1.8) | 1 (1.8) |
| 常見TEAE 頭痛 失眠 體重增加 | 4 (4.6) 3 (3.4) 3 (3.4) | 0 0 2 (3.4) | 5 (8.9) 2 (3.6) 0 | 2 (3.6) 2 (3.6) 0 |
為了評定與精神分裂症相關之認知損傷(CIAS)的變化,次要指標包括簡易精神分裂症認知評定(BACS)綜合評分(多個領域中之認知能力的量度)及精神分裂症認知評分量表(SCoRS)評分(日常認知功能之量度,需要成人資訊提供者之意見)相對於基線之12週變化。次要指標未針對多重性進行校正。
對於CIAS,在BACS綜合評分(
p= 0.031;效應量,0.4,未針對多重性進行校正,
圖 7)及SCoRS訪問者總分(
p= 0.011;效應量,0.4,未針對多重性進行校正,
圖 8)方面,相對於安慰劑,使用化合物(
I) 50 mg在認知評定及患者認知功能方面觀測到名義上之顯著改善,但使用化合物(
I) 125 mg或500 mg則沒有改善。對於BACS綜合評分,使用化合物(
I) 50 mg觀測到的12週LS相對於基線之平均變化為4.6 (95% CI,2.7至6.5),而使用安慰劑為2.3 (95% CI,0.7至3.9)。對於SCoRS訪問者總分,使用化合物(
I) 50 mg觀測到的12週LS相對於基線之平均變化為-3.8 (95% CI,-5.3至-2.3),而使用安慰劑為-1.6 (95% CI,-2.9至-0.3)。
BACS經特定設計以量測認知中之處理相關改善且包括替代形式。BACS為精神分裂症中認知功能之可靠及敏感量測。BACS為認知評定成套測試,其評定在精神分裂症中被發現持續受損的6個認知功能領域:語言記憶;工作記憶;運動速度;注意力;執行功能;及語言流暢性。BACS之各測試的主要量度係由產生T-評分進行標準化,其中匹配的參考健康參與者之測試階段之平均值設定為50且標準差設定為10。BACS評定之結果之初步分析概述於
表 10 至表 16中。
SCoRS為基於訪問之認知功能量測,是為了特定評估患有精神分裂症之參與者之認知功能的態樣而研發的。各項評定7個認知領域,即注意力、記憶、推理能力及問題解決能力、工作記憶、處理速度、語言功能及社會認知。SCoRS整體總評分為20項之和,且其在20至80範圍內變化,其中20為最佳結果,而80為最差結果。SCoRS評定之結果之初步分析概述於
表 17中。
在INTERACT研究中所評估之三個劑量下,化合物(
I)在精神分裂症之負性症狀之處理中並未顯示出顯著功效。然而,如分別藉由BACS綜合評分及SCoRS訪問者總分(各項之有臨床意義之效應量為0.4)所量測,化合物(
I) 50 mg顯示認知測試表現及自評分及資訊提供者評分之日常認知功能方面出現改善。對於CIAS,使用化合物(
I) 50 mg、125 mg及500 mg觀測到反向U形劑量反應。如實例1中所述,亦在與INTERACT研究並行進行之長效增益研究中的活體外模型中觀測到反向U形劑量反應。需要進行其他臨床研究以進一步評估此功效信號。與先前臨床經驗一致,化合物(
I)在INTERACT研究中通常具有良好耐受性。
表 8.個體之處置(初步分析)
附註 1:百分比係基於接受至少一次劑量之研究藥物的各處理組之分析集中之個體總數。
附註 2:中斷研究藥物/研究之原因之百分比係基於過早中斷研究藥物/研究之個體總數。
表 9.人口資料及基線特徵(初步分析)
附註 1:百分比係基於各處理組之分析集中之個體總數。
附註 2:若個體在CRF上記錄了多於一種種族類別,則該個體僅包括在多種族類別下。
附註 3:篩選時之年齡係由知情同意日期計算。
附註 4:西班牙裔種族僅在美國網站輸入。非美國網站之種族將歸類為未報導者。
表 10:藉由訪視進行的BACS綜合評分相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE –標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS綜合評分作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS綜合評分相對於基線之變化。基於隨機缺失假設(Missing at Random Assumption),此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a)基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 11:藉由訪視進行的BACS語言記憶認知域相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE -標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS語言記憶認知域作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS語言記憶認知域相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a)基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 12:藉由訪視進行的BACS工作記憶認知域相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE -標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS工作記憶認知域作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS工作記憶認知域相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a) 基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 13:藉由訪視進行的BACS運動速度相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE -標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS運動速度認知域作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS運動速度認知域相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a)基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 14:藉由訪視進行的BACS注意力認知域相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE -標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS注意力認知域作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS注意力認知域相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a) 基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 15:藉由訪視進行的BACS執行功能認知域相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE -標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS執行功能認知域作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS執行功能認知域相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a)基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 16:藉由訪視進行的BACS語言流暢性認知域相對於基線之變化之分析(初步分析)
CI -信賴區間;LS -最小平方;SE -標準誤差。
附註 1:使用重複量測混合模型(MMRM),基線BACS語言流暢性認知域作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析BACS語言流暢性認知域相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a)基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
表 17.第12週時SCoRS訪問者總分相對於基線之變化之分析(初步分析)
附註 1:使用重複量測混合模型(MMRM),基線SCoRS訪問者總分作為互變異數;彙集地點、訪視、處理及分類年齡(隨機分組因子)作為固定因子;及處理/訪視及基線/訪視相互作用來分析SCoRS訪問者總分相對於基線之變化。基於隨機缺失假設,此分析將僅使用觀測到之情況進行。P值為單側的,對立假設為化合物(
I)在臨床上有利的方向方面優於安慰劑。
附註 2:(a)基線定義為第一次劑量之研究藥物之前的最後一次觀測值。
*指示0.025水準(單側)下有統計顯著性(單側)。
實例7:評估化合物(I)之多個口服劑量在患有精神分裂症之成人中的功效、耐受性、藥力學及藥物動力學的研究(NCT03359785)
| 個體數(%) | ||||||
| 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) | 化合物( I) 總體 (N=169) | 總體 (N=256) | |
| 接受至少一次劑量之研究藥物 | 87 | 58 | 56 | 55 | 169 | 256 |
| 完成研究 | 76 (87.4) | 53 (91.4) | 52 (92.9) | 47 (85.5) | 152 (89.9) | 228 (89.1) |
| 提前中斷研究藥物 | 11 (12.6) | 5 (8.6) | 4 (7.1) | 8 (14.5) | 17 (10.1) | 28 (10.9) |
| 提前中斷研究 | 11 (12.6) | 5 (8.6) | 4 (7.1) | 8 (14.5) | 17 (10.1) | 28 (10.9) |
| 中斷研究藥物之原因 | ||||||
| 不良事件 | 3 (27.3) | 0 | 1 (25.0) | 1 (12.5) | 2 (11.8) | 5 (17.9) |
| 方案偏離 | 0 | 0 | 0 | 0 | 0 | 0 |
| 失訪 | 1 (9.1) | 0 | 0 | 0 | 0 | 1 (3.6) |
| 個體退出 | 4 (36.4) | 3 (60.0) | 2 (50.0) | 4 (50.0) | 9 (52.9) | 13 (46.4) |
| 由試驗委託者終止研究 | 0 | 0 | 0 | 0 | 0 | 0 |
| 懷孕 | 0 | 0 | 0 | 0 | 0 | 0 |
| 不令人滿意之治療反應 | 1 (9.1) | 0 | 0 | 0 | 0 | 1 (3.6) |
| 在雙盲處理期期間不順應研究藥物 | 1 (9.1) | 2 (40.0) | 1 (25.0) | 1 (12.5) | 4 (23.5) | 5 (17.9) |
| 明顯自殺風險 | 0 | 0 | 0 | 0 | 0 | 0 |
| 症狀惡化 | 0 | 0 | 0 | 0 | 0 | 0 |
| 其他 | 1 (9.1) | 0 | 0 | 2 (25.0) | 2 (11.8) | 3 (10.7) |
| 中斷研究之原因 | ||||||
| 死亡 | 0 | 0 | 0 | 0 | 0 | 0 |
| 不良事件 | 2 (18.2) | 0 | 1 (25.0) | 1 (12.5) | 2 (11.8) | 4 (14.3) |
| 方案偏離 | 0 | 0 | 0 | 0 | 0 | 0 |
| 失訪 | 1 (9.1) | 0 | 0 | 0 | 0 | 1 (3.6) |
| 個體退出 | 4 (36.4) | 3 (60.0) | 2 (50.0) | 3 (37.5) | 8 (47.1) | 12 (42.9) |
| 由試驗委託者終止研究 | 0 | 0 | 0 | 0 | 0 | 0 |
| 懷孕 | 0 | 0 | 0 | 0 | 0 | 0 |
| 不令人滿意之治療反應 | 1 (9.1) | 0 | 0 | 0 | 0 | 1 (3.6) |
| 在雙盲處理期期間不順應研究藥物 | 1 (9.1) | 2 (40.0) | 1 (25.0) | 1 (12.5) | 4 (23.5) | 5 (17.9) |
| 明顯自殺風險 | 0 | 0 | 0 | 0 | 0 | 0 |
| 症狀惡化 | 0 | 0 | 0 | 0 | 0 | 0 |
| 其他 | 2 (18.2) | 0 | 0 | 3 (37.5) | 3 (17.6) | 5 (17.9) |
| 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) | 化合物( I) 總體 (N=169) | 總體 (N=256) | |
| 年齡(歲) | ||||||
| N | 87 | 58 | 56 | 55 | 169 | 256 |
| 平均值(SD) | 39.9 (11.11) | 39.9 (10.96) | 40.1 (9.80) | 40.1 (11.79) | 40.0 (10.81) | 40.0 (10.89) |
| 中值 | 38.0 | 39.0 | 40.5 | 39.0 | 39.0 | 39.0 |
| 最小值, 最大值 | 20, 60 | 21, 60 | 23, 60 | 18, 60 | 18, 60 | 18, 60 |
| 年齡類別(n (%)) | ||||||
| 年齡< 35歲 | 30 (34.5) | 19 (32.8) | 18 (32.1) | 18 (32.7) | 55 (32.5) | 85 (33.2) |
| 年齡≥ 35歲 | 57 (65.5) | 39 (67.2) | 38 (67.9) | 37 (67.3) | 114 (67.5) | 171 (66.8) |
| 族群(n (%)) | ||||||
| 西班牙裔或拉丁裔 | 3 (3.4) | 2 (3.4) | 2 (3.6) | 1 (1.8) | 5 (3.0) | 8 (3.1) |
| 非西班牙裔或拉丁裔 | 19 (21.8) | 12 (20.7) | 18 (32.1) | 8 (14.5) | 38 (22.5) | 57 (22.3) |
| 未報導者 | 65 (74.7) | 44 (75.9) | 36 (64.3) | 46 (83.6) | 126 (74.6) | 191 (74.6) |
| 未知 | 0 | 0 | 0 | 0 | 0 | 0 |
| 性別(n (%)) | ||||||
| 男性 | 63 (72.4) | 38 (65.5) | 34 (60.7) | 33 (60.0) | 105 (62.1) | 168 (65.6) |
| 女性 | 24 (27.6) | 20 (34.5) | 22 (39.3) | 22 (40.0) | 64 (37.9) | 88 (34.4) |
| 種族(n (%)) | ||||||
| 美洲印第安人或阿拉斯加土著人 | 2 (2.3) | 0 | 1 (1.8) | 0 | 1 (0.6) | 3 (1.2) |
| 亞洲人 | 2 (2.3) | 0 | 3 (5.4) | 0 | 3 (1.8) | 5 (2.0) |
| 黑人或非洲裔美國人 | 10 (11.5) | 9 (15.5) | 9 (16.1) | 5 (9.1) | 23 (13.6) | 33 (12.9) |
| 夏威夷原住民或其他太平洋島民 | 0 | 0 | 0 | 0 | 0 | 0 |
| 白人 | 70 (80.5) | 46 (79.3) | 42 (75.0) | 50 (90.9) | 138 (81.7) | 208 (81.3) |
| 多種族 | 0 | 0 | 0 | 0 | 0 | 0 |
| 未報導者 | 3 (3.4) | 3 (5.2) | 1 (1.8) | 0 | 4 (2.4) | 7 (2.7) |
| 國家(n (%)) | ||||||
| 保加利亞 | 18 (20.7) | 12 (20.7) | 13 (23.2) | 11 (20.0) | 36 (21.3) | 54 (21.1) |
| 捷克共和國 | 5 (5.7) | 4 (6.9) | 2 (3.6) | 3 (5.5) | 9 (5.3) | 14 (5.5) |
| 意大利 | 10 (11.5) | 5 (8.6) | 2 (3.6) | 6 (10.9) | 13 (7.7) | 23 (9.0) |
| 波蘭 | 3 (3.4) | 0 | 2 (3.6) | 1 (1.8) | 3 (1.8) | 6 (2.3) |
| 俄羅斯聯邦 | 7 (8.0) | 6 (10.3) | 4 (7.1) | 5 (9.1) | 15 (8.9) | 22 (8.6) |
| 塞爾維亞 | 5 (5.7) | 1 (1.7) | 3 (5.4) | 3 (5.5) | 7 (4.1) | 12 (4.7) |
| 西班牙 | 3 (3.4) | 2 (3.4) | 1 (1.8) | 3 (5.5) | 6 (3.6) | 9 (3.5) |
| 烏克蘭 | 14 (16.1) | 14 (24.1) | 9 (16.1) | 14 (25.5) | 37 (21.9) | 51 (19.9) |
| 美國 | 22 (25.3) | 14 (24.1) | 20 (35.7) | 9 (16.4) | 43 (25.4) | 65 (25.4) |
| 身高(cm) | ||||||
| N | 87 | 58 | 56 | 55 | 169 | 256 |
| 平均值(SD) | 173.65 (8.568) | 175.11 (8.992) | 172.23 (9.884) | 171.14 (8.951) | 172.86 (9.382) | 173.13 (9.104) |
| 中值 | 174.00 | 175.60 | 173.00 | 172.00 | 174.00 | 174.00 |
| 最小值, 最大值 | 148.0, 193.0 | 154.0, 197.0 | 146.0, 193.0 | 150.0, 188.5 | 146.0, 197.0 | 146.0, 197.0 |
| 篩選時之體重(kg) | ||||||
| N | 87 | 58 | 56 | 55 | 169 | 256 |
| 平均值(SD) | 86.80 (16.474) | 84.86 (18.961) | 83.70 (16.816) | 81.96 (16.346) | 83.53 (17.374) | 84.64 (17.112) |
| 中值 | 85.00 | 81.30 | 85.50 | 82.30 | 83.00 | 84.15 |
| 最小值, 最大值 | 51.6, 135.6 | 52.0, 140.9 | 46.0, 132.9 | 47.8, 115.0 | 46.0, 140.9 | 46.0, 140.9 |
| BMI (kg/m^2) | ||||||
| N | 87 | 58 | 56 | 55 | 169 | 256 |
| 平均值(SD) | 28.70 (4.497) | 27.55 (5.061) | 28.18 (5.081) | 27.95 (5.081) | 27.89 (5.051) | 28.16 (4.876) |
| 中值 | 28.70 | 27.55 | 28.05 | 27.40 | 27.70 | 28.00 |
| 最小值, 最大值 | 18.1, 40.2 | 19.2, 37.0 | 19.3, 39.7 | 18.5, 39.6 | 18.5, 39.7 | 18.1, 40.2 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 87 34.9 (14.84) 35.0 -7, 72 | 58 33.1 (14.44) 32.5 -1, 63 | 56 33.7 (13.65) 34.0 0, 62 | 55 34.1 (12.80) 35.0 2, 62 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 34.9 (15.67) 36.0 -16, 70 | 56 35.4 (14.53) 34.0 -1, 73 | 56 35.6 (14.55) 37.0 2, 72 | 51 35.6 (13.84) 38.0 -7, 63 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 79 0.4 (5.28) 1.0 -13, 18 | 56 1.7 (5.81) 2.0 -12, 19 | 56 1.9 (4.95) 2.0 -7, 13 | 51 1.5 (7.57) 1.0 -24, 20 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | -0.4 (0.70) (-1.8, 1.0) | 0.9 (0.81) (-0.7, 2.5) | 1.4 (0.80) (-0.2, 3.0) | 0.5 (0.87) (-1.2, 2.2) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 1.3 (1.01) (-0.7, 3.3) 0.096 | 1.8 (1.02) (-0.2, 3.8) 0.038 | 0.9 (1.04) (-1.1, 3.0) 0.194 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 73 36.4 (15.31) 36.0 -3, 74 | 52 37.7 (13.30) 37.5 -8, 67 | 50 37.1 (15.02) 38.5 -8, 71 | 45 37.6 (13.86) 40.0 5, 65 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 73 1.4 (5.47) 1.0 -10, 21 | 52 3.8 (5.91) 3.0 -10, 19 | 50 2.9 (6.54) 3.5 -11, 16 | 45 3.0 (7.98) 3.0 -14, 26 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | 0.7 (0.78) (-0.8, 2.3) | 2.7 (0.92) (0.9, 4.5) | 2.3 (0.91) (0.5, 4.1) | 1.5 (0.99) (-0.5, 3.5) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 1.9 (1.15) (-0.3, 4.2) 0.046 | 1.5 (1.16) (-0.8, 3.8) 0.095 | 0.8 (1.20) (-1.6, 3.1) 0.260 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 87 43.1 (11.60) 44.0 19, 73 | 58 39.6 (11.65) 40.5 12, 64 | 56 40.6 (12.82) 40.0 5, 70 | 55 40.5 (12.53) 41.0 5, 72 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 41.8 (13.69) 42.0 3, 69 | 56 41.7 (11.59) 44.5 9, 68 | 56 42.4 (12.62) 42.0 16, 75 | 51 42.1 (12.06) 42.0 10, 72 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 79 -0.8 (7.10) 0.0 -17, 16 | 56 1.6 (7.40) 0.0 -12, 21 | 56 1.8 (7.71) 2.5 -17, 19 | 51 1.8 (8.65) 2.0 -15, 22 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | -1.3 (0.88) (-3.1, 0.4) | 0.6 (1.04) (-1.5, 2.6) | 1.2 (1.01) (-0.8, 3.2) | 0.7 (1.11) (-1.5, 2.8) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 1.9 (1.29) (-0.6, 4.4) 0.071 | 2.5 (1.29) (0.0, 5.1) 0.025 | 2.0 (1.33) (-0.6, 4.6) 0.070 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 72 42.7 (11.04) 42.0 19, 69 | 52 42.9 (12.41) 43.5 14, 70 | 50 42.3 (13.54) 42.5 -1, 72 | 45 41.8 (13.82) 41.0 5, 76 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 72 -0.1 (7.26) -0.5 -17, 23 | 52 3.2 (7.87) 4.0 -11, 26 | 50 1.6 (8.07) 1.0 -17, 23 | 45 1.6 (10.04) 0.0 -20, 33 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | -0.7 (0.98) (-2.6, 1.3) | 1.9 (1.13) (-0.3, 4.1) | 0.8 (1.13) (-1.5, 3.0) | 0.0 (1.23) (-2.4, 2.4) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 2.6 (1.43) (-0.3, 5.4) 0.038 | 1.4 (1.44) (-1.4, 4.3) 0.164 | 0.7 (1.49) (-2.3, 3.6) 0.329 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 87 39.2 (12.18) 38.0 14, 67 | 58 39.3 (14.00) 37.5 13, 66 | 56 39.5 (11.17) 40.0 15, 59 | 55 39.6 (12.95) 41.0 7, 64 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 39.8 (12.94) 39.0 4, 66 | 56 40.8 (14.10) 42.0 14, 72 | 56 41.0 (11.17) 41.0 18, 66 | 51 40.1 (13.75) 43.0 5, 60 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 79 1.2 (6.84) 2.0 -20, 28 | 56 1.0 (6.60) 0.0 -12, 15 | 56 1.5 (5.89) 2.0 -12, 14 | 51 0.5 (7.99) 0.0 -18, 18 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | 0.0 (0.79) (-1.5, 1.6) | 0.0 (0.92) (-1.8, 1.8) | 0.9 (0.90) (-0.9, 2.6) | -0.9 (0.98) (-2.8, 1.0) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 0.0 (1.15) (-2.3, 2.2) 0.507 | 0.8 (1.16) (-1.5, 3.1) 0.239 | -0.9 (1.19) (-3.3, 1.4) 0.788 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 73 40.5 (13.94) 38.0 12, 75 | 52 42.0 (13.95) 42.5 10, 63 | 50 41.7 (13.58) 40.0 10, 67 | 45 42.6 (13.20) 45.0 14, 67 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 73 2.0 (8.69) 3.0 -31, 23 | 52 2.1 (6.61) 1.0 -11, 17 | 50 1.8 (7.40) 0.0 -16, 20 | 45 1.7 (7.39) 0.0 -10, 20 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | 0.7 (0.91) (-1.1, 2.4) | 0.9 (1.06) (-1.1, 3.0) | 1.0 (1.06) (-1.1, 3.1) | 0.2 (1.15) (-2.1, 2.4) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 0.3 (1.34) (-2.3, 2.9) 0.413 | 0.3 (1.35) (-2.3, 3.0) 0.406 | -0.5 (1.40) (-3.2, 2.3) 0.637 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 86 41.7 (14.10) 40.5 -4, 73 | 58 39.6 (14.11) 37.0 13, 78 | 56 39.6 (9.64) 39.5 20, 60 | 55 40.5 (12.13) 39.0 3, 73 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 43.1 (14.70) 43.0 4, 73 | 56 40.6 (13.61) 40.0 18, 77 | 56 39.6 (10.80) 39.0 19, 68 | 51 40.7 (12.38) 41.0 1, 66 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 78 0.9 (8.44) 0.0 -29, 33 | 56 1.7 (5.73) 1.0 -10, 15 | 56 0.0 (5.97) 0.5 -10, 21 | 51 0.5 (9.53) 2.0 -33, 25 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | -0.1 (0.86) (-1.8, 1.6) | 0.1 (1.00) (-1.9, 2.1) | -1.0 (0.98) (-2.9, 1.0) | -1.3 (1.07) (-3.4, 0.9) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 0.2 (1.26) (-2.3, 2.7) 0.440 | -0.9 (1.26) (-3.4, 1.6) 0.753 | -1.1 (1.30) (-3.7, 1.4) 0.812 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 72 42.9 (14.36) 41.5 8, 71 | 52 42.0 (12.93) 41.5 9, 74 | 50 42.6 (10.35) 42.0 19, 70 | 45 41.3 (11.31) 40.0 1, 63 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 71 0.1 (6.74) 0.0 -16, 14 | 52 2.6 (6.80) 1.0 -7, 23 | 50 2.5 (7.60) 2.0 -13, 24 | 45 2.0 (6.58) 2.0 -14, 17 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | -0.5 (0.81) (-2.1, 1.1) | 1.0 (0.93) (-0.9, 2.8) | 1.3 (0.93) (-0.6, 3.1) | -0.2 (1.02) (-2.2, 1.8) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 1.5 (1.17) (-0.8, 3.8) 0.101 | 1.8 (1.18) (-0.5, 4.1) 0.067 | 0.3 (1.22) (-2.1, 2.7) 0.405 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 87 34.7 (12.64) 36.0 6, 66 | 58 34.2 (13.75) 35.5 -2, 59 | 56 34.5 (11.35) 33.5 13, 61 | 55 34.1 (11.49) 35.0 12, 63 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 35.2 (13.07) 36.0 6, 64 | 56 36.0 (14.78) 34.0 5, 94 | 56 36.7 (12.72) 37.0 12, 65 | 51 35.5 (12.68) 35.0 13, 64 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 79 1.0 (5.58) 2.0 -17, 13 | 56 0.9 (7.74) 0.0 -16, 38 | 56 2.2 (6.07) 2.0 -8, 32 | 51 0.9 (6.26) 0.0 -18, 15 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | 1.0 (0.77) (-0.5, 2.6) | 1.0 (0.90) (-0.8, 2.7) | 2.2 (0.88) (0.5, 4.0) | 1.0 (0.96) (-0.9, 2.9) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | -0.1 (1.12) (-2.3, 2.1) 0.524 | 1.2 (1.12) (-1.0, 3.4) 0.146 | 0.0 (1.15) (-2.3, 2.2) 0.516 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 71 36.7 (12.73) 37.0 6, 67 | 51 38.0 (11.83) 39.0 7, 72 | 50 36.2 (12.21) 36.0 14, 69 | 45 38.0 (14.08) 36.0 8, 84 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 71 1.7 (6.40) 2.0 -12, 25 | 51 2.2 (6.95) 2.0 -14, 21 | 50 1.2 (6.41) 2.0 -13, 21 | 45 3.1 (9.31) 2.0 -24, 39 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | 1.9 (0.87) (0.2, 3.6) | 2.3 (1.02) (0.3, 4.3) | 1.4 (1.01) (-0.6, 3.4) | 3.1 (1.09) (1.0, 5.3) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 0.4 (1.28) (-2.1, 2.9) 0.376 | -0.5 (1.29) (-3.1, 2.0) 0.659 | 1.2 (1.33) (-1.4, 3.8) 0.178 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 87 45.8 (15.63) 49.0 -21, 66 | 58 42.7 (13.98) 45.5 -8, 65 | 56 45.5 (13.88) 47.5 1, 66 | 55 45.9 (13.48) 50.0 9, 68 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 45.0 (14.77) 48.0 -17, 66 | 56 44.9 (11.66) 48.5 4, 62 | 56 46.3 (16.06) 50.0 -13, 69 | 51 47.0 (10.95) 51.0 -3, 63 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 79 -1.2 (9.79) 0.0 -48, 17 | 56 1.6 (10.55) 2.0 -29, 60 | 56 0.8 (9.01) 0.0 -32, 21 | 51 1.3 (7.62) 0.0 -13, 20 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | -1.2 (1.04) (-3.2, 0.9) | 0.9 (1.22) (-1.5, 3.3) | 0.8 (1.19) (-1.6, 3.1) | 1.1 (1.29) (-1.5, 3.6) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 2.1 (1.53) (-0.9, 5.1) 0.085 | 2.0 (1.53) (-1.0, 5.0) 0.099 | 2.3 (1.57) (-0.8, 5.4) 0.075 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 73 46.8 (12.21) 49.0 -4, 69 | 52 46.4 (10.55) 49.5 18, 63 | 50 47.6 (13.17) 51.0 11, 66 | 45 48.5 (11.88) 51.0 3, 68 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 73 0.5 (8.78) 0.0 -32, 31 | 52 2.6 (7.73) 1.0 -14, 34 | 50 2.0 (8.79) 3.0 -33, 17 | 45 2.0 (9.28) 0.0 -17, 26 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | 0.6 (0.94) (-1.3, 2.4) | 1.8 (1.09) (-0.4, 4.0) | 2.0 (1.09) (-0.2, 4.1) | 2.0 (1.19) (-0.3, 4.3) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 1.2 (1.36) (-1.5, 3.9) 0.188 | 1.4 (1.38) (-1.3, 4.1) 0.157 | 1.4 (1.42) (-1.4, 4.2) 0.160 |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) N 平均值(SD) 中值 最小值, 最大值 | 87 38.0 (10.89) 38.0 14, 69 | 57 39.7 (9.78) 39.0 19, 61 | 56 38.1 (8.46) 38.0 21, 53 | 55 38.7 (9.45) 38.0 22, 67 |
| 第6週 N 平均值(SD) 中值 最小值, 最大值 | 79 38.1 (10.88) 37.0 16, 65 | 55 39.9 (10.86) 38.0 16, 71 | 55 39.1 (8.98) 40.0 19, 58 | 51 39.6 (10.14) 40.0 20, 63 |
| 自基線至第6週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 79 0.5 (4.22) 1.0 -11, 12 | 55 -0.2 (5.57) 0.0 -22, 13 | 55 0.8 (4.53) 1.0 -13, 11 | 51 0.8 (5.87) 1.0 -17, 15 |
| 自基線至第6週之調整後變化 LS平均值(SE) 95% CI | 0.2 (0.60) (-1.0, 1.3) | -0.3 (0.70) (-1.7, 1.0) | 0.7 (0.68) (-0.6, 2.1) | 0.5 (0.74) (-1.0, 1.9) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第6週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | -0.5 (0.87) (-2.2, 1.2) 0.722 | 0.6 (0.87) (-1.1, 2.3) 0.258 | 0.3 (0.89) (-1.4, 2.1) 0.364 | |
| 第12週 N 平均值(SD) 中值 最小值, 最大值 | 73 38.9 (11.91) 38.0 13, 77 | 51 41.8 (10.41) 40.0 24, 70 | 50 40.6 (9.54) 39.0 21, 62 | 45 40.6 (10.30) 40.0 20, 63 |
| 自基線至第12週之變化(a) N 平均值(SD) 中值 最小值, 最大值 | 73 1.2 (5.53) 0.0 -11, 17 | 51 1.5 (5.87) 0.0 -12, 14 | 50 2.1 (5.59) 2.0 -11, 14 | 45 1.3 (6.95) 0.0 -11, 20 |
| 自基線至第12週之調整後變化 LS平均值(SE) 95% CI | 1.0 (0.72) (-0.4, 2.4) | 1.2 (0.85) (-0.5, 2.9) | 1.9 (0.84) (0.2, 3.6) | 0.5 (0.91) (-1.3, 2.3) |
| 訪視 統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 第12週與安慰劑之差異 LS平均值(SE) 95% CI p值(未調整) | 0.2 (1.07) (-1.9, 2.3) 0.433 | 0.9 (1.07) (-1.2, 3.0) 0.202 | -0.5 (1.11) (-2.7, 1.7) 0.668 |
| 訪視統計 | 安慰劑 (N=87) | 化合物( I) 50 mg (N=58) | 化合物( I) 125 mg (N=56) | 化合物( I) 500 mg (N=55) |
| 基線(a) | ||||
| N | 84 | 57 | 55 | 52 |
| 平均值(SD) | 39.7 (9.96) | 39.6 (10.73) | 38.5 (10.29) | 41.6 (9.98) |
| 中值 | 39.0 | 40.0 | 39.0 | 40.5 |
| 最小值, 最大值 | 20, 61 | 21, 73 | 20, 62 | 23, 60 |
| 第12週 | ||||
| N | 77 | 54 | 52 | 49 |
| 平均值(SD) | 37.8 (9.39) | 35.5 (10.91) | 36.1 (9.69) | 39.4 (9.60) |
| 中值 | 38.0 | 32.0 | 36.5 | 39.0 |
| 最小值, 最大值 | 20, 58 | 20, 72 | 20, 57 | 21, 59 |
| 自基線至第12週之變化(a) | ||||
| N | 74 | 53 | 51 | 47 |
| 平均值(SD) | -1.8 (5.14) | -4.0 (5.93) | -2.1 (5.89) | -2.4 (5.34) |
| 中值 | -1.0 | -3.0 | -2.0 | -2.0 |
| 最小值, 最大值 | -16, 14 | -20, 17 | -16, 15 | -15, 15 |
| 自基線至第12週之調整後變化 | ||||
| LS平均值(SE) | -1.4 (0.66) | -3.7 (0.77) | -2.1 (0.77) | -1.5 (0.84) |
| 95% CI | (-2.7, -0.1) | (-5.2, -2.2) | (-3.6, -0.6) | (-3.2, 0.1) |
| 第12週與安慰劑之差異 | ||||
| LS平均值(SE) | -2.4 (0.94) | -0.7 (0.96) | -0.1 (0.98) | |
| 95% CI | (-4.2, -0.5) | (-2.6, 1.2) | (-2.1, 1.8) | |
| p值(未調整) | 0.007* | 0.236 | 0.449 |
NCT03359785為隨機分組、雙盲、安慰劑對照交叉1b期臨床試驗,其在單一地點在精神分裂症患者中進行,以評估化合物(
I)之多個口服劑量之PD作用、安全性、耐受性及藥物動力學。該研究之目標為評定關於已知在精神分裂症中受影響的小腦迴路功能及NMDA藥理學相關之量測的化合物(
I)之藥力學(PD)生物標記物。
研究具有雙順序雙向交叉設計,其中參與者在由2或3週清除間隔之兩個階段內接受50或500 mg化合物(
I)及安慰劑持續8個連續日(
圖 9)。
主要指標為各處理期之第8天時,眨眼制約(EBC)測試期間的制約反應之平均百分比(
圖 10)。EBC用於評定化合物(
I)對小腦迴路功能之影響。EBC為依賴於小腦迴路之高度保守反射,其中NMDA受體起關鍵作用。相比於健康對照組,患有精神分裂症之患者之EBC受損。化合物(
I)已在臨床前研究中在逆轉莨菪鹼誘導之EBC缺陷中顯示穩健作用(參見例如WO 2015/132608之實例2)。
亦測試腦電圖中之誘發電位以評定化合物(
I)之多個口服劑量對精神分裂症中受影響之NMDA敏感性生理反應的影響。特定言之,在兩個階段中在基線及處理8天之後量測失配負波(MMN)、聽覺穩態反應(ASSR)及P300。
MMN為對NMDA受體藥理學敏感之古怪事件相關電位。MMN為事件相關電位(ERP),其回應於背景刺激中之未被關注之變化而引起且對D-絲胺酸升高有反應。有跡象表明在患有精神分裂症之患者中D-絲胺酸投與改善MMN。MMN反映了偵測偏差刺激與感覺記憶痕跡之間失配的自動過程(
圖 11A 、圖 11B)。相較於健康對照組,已在精神分裂症參與者中持續地鑑別到較小MMN幅值(效應量較大)。在此研究中,MMN幅值係在腦電圖[EEG]之中線前額電極(Fz)處量測。
P300波為ERP組分,其由新穎的行為相關靶刺激包埋於不相關刺激中的表現而引起,其方式類似於MMN,但需要參與者之積極傾聽及反應。聽覺刺激係以由1個標準音與1個目標音組成的古怪範式呈現。參與者被指示在聽到目標音時儘可能快地按下一個按鈕,而在聽到標準音時則不按。P300反映了注意力的分配及即時記憶之激活。P300幅值是指刺激環境之心理表徵被更新時的腦部動作,而P300潛伏期則指與反應選擇過程無關的刺激分類速度。P300幅值係在EEG之中線頂骨電極(Pz)處量測。
ASSR為所引起之振盪反應,其受時間調變刺激之頻率及相位影響。患有精神分裂症之個體經歷主觀感覺異常及在感覺功能之評定方面的客觀缺陷。此等缺陷可由感覺路徑及感覺皮質中之異常信號傳導或由此類輸入之認知處理中之後期階段紊亂產生。ASSR可用於評定包括皮質處理之感覺路徑之完整性。ASSR係在EEG之中線中央電極(Cz)處量測。
研究之次要指標包括:(1)各處理期之第8天時的平均失配負波(MMN)幅值;(2)各處理期之第8天時的平均聽覺穩態反應(ASSR);及(3)各處理期之第7天時的簡易精神分裂症認知評定(BACS)評分。
亦分析所有組之D-絲胺酸及L-絲胺酸含量。特定言之,其他次要結果量測包括:(1)第8天時的血漿D-絲胺酸及L-絲胺酸含量之平均濃度;(2)第8天時的平均血漿D-絲胺酸與總絲胺酸比率;及(3)化合物(
I)之平均血漿濃度。
安全性目標包括治療引發不良事件(TEAE)之發生率、實驗室測試、生命體徵及心電圖(ECG)評定。
所有指標均以同一個體中與安慰劑相比,相對於基線之變化的形式進行分析。用ANOVA模型進行統計比較,以處理順序、階段及治療作為固定效應,且以個體作為隨機效應。作為補充分析,對主要指標應用互變異數分析模型(ANCOVA),以(階段)基線作為互變異數,以治療順序、階段、處理作用及基線/處理作為固定效應,且以個體作為隨機效應。
COVID-19影響研究,引起完成者比最初計劃要少,此影響研究之影響力。因此,資料在本質上被視為探索性的,且研究的焦點為變化之方向性及效應量。
1b期研究征選31名18至60歲之患者。參與者為症狀穩定的精神分裂症患者,接受穩定的抗精神病藥物超過2個月。12名患者完成各劑量之活性物階段及安慰劑階段。患者主要為男性(26/31)及非洲裔美國人(26/31)。14名患者被隨機分至化合物(
I) 50 mg(中值年齡,45歲;11名男性),且12名完成研究。17名患者被隨機分至化合物(I) 500 mg(中值年齡,34歲;15名男性),且12名完成研究。
研究之納入標準包括:
1.在篩選訪視時,身體質量指數(BMI)大於或等於(≥) 18.5,且小於或等於(≤) 40.0 (每平方公尺之公斤數[kg/m^2])。
2.現行精神病症診斷與統計手冊,第五版(DSM-5)診斷有精神分裂症,正在接受穩定抗精神病療法(在過去2個月中劑量無增加,沒有降低超過[>]20%)。
3.正性及負性症候群量表(PANSS)負性症狀因子評分(NSFS) ≥ 15,穩定篩選及基線PANSS NSFS(變化<25%)。
4.PANSS總分≤ 90;穩定篩選及基線PANSS總分(變化小於[<]20%)。
5.正在接受穩定(在過去2個月中劑量無增加,沒有降低超過> 25%)抗精神病藥物,劑量不超過利培酮6 mg或其等效劑量。若用作催眠劑(最高喹硫平300 mg或其等效劑量,每日就寢時間一次)且根據研究者意見,個體沒有顯示出晨間鎮靜,則經試驗委託者或指定人員批准,可准許用低於治療劑量之第二抗精神病藥進行伴隨治療,但若其用於難治性正性精神病症狀,則不准許。在此例外情況下,第二抗精神病藥之每日總劑量將不必包括於6 mg/天利培酮當量限值之計算中。
研究之排除標準包括:
1.具有癌症(惡性疾病)病史,不包括經治療之基底細胞癌或經治療之0期(原位)子宮頸癌。
2.具有顯著多種及/或嚴重過敏(例如[如]食物、藥物、乳膠過敏)之病史,或已具有對處方或非處方藥物或食物之過敏性反應或顯著不耐受性。
3.在篩選訪視或登記時,使用費氏(Fridericia)校正法之QT間隔(QTcF) > 450毫秒[ms] (男性)或>470 ms (女性),經一次重複測試證實。
4.酒精或藥物篩查呈陽性,不允許使用的物質包括安非他命(amphetamine)、巴比妥酸(barbiturate)、可卡因、大麻、美沙酮、甲基安非他命、3,4-亞甲基二氧基甲安非他命、苯環利定(phencyclidine)或非處方苯并二氮呯或鴉片類。
5.B型肝炎表面抗原(HBsAg)、C型肝炎抗體呈陽性,或根據病史有HIV (允許進行確認性測試;應優先考慮最敏感測試)。
6.在研究前(篩選)訪視前4週內做過大手術,獻血或失血過250毫升[mL]。
7.對化合物(
I)之調配物的任何組分有已知的過敏反應。
8.具有對黏著劑、金屬或塑膠之顯著皮膚反應(過敏反應)的病史。
9.被研究者認為有自殺或對自己、他人或財產造成傷害的迫在眉睫的風險,或參與者在篩選前的過去一年內曾試圖自殺過。在隨機分組之前,哥倫比亞自殺嚴重程度評分量表(C-SSRS)第4項或第5項有肯定答案的參與者被排除在外(基於過去一年)。
主要指標為EBC相對於基線之變化。相較於安慰劑,使用化合物(
I) 50 mg (p = 0.109)觀測到改善趨勢,但使用化合物(
I) 500 mg (p = 0.777)則沒有(
圖 12A , 圖 12B)。化合物(
I) 50 mg及化合物(
I) 500 mg之效應量分別為0.246及−0.198 (ANCOVA)。
關於次要指標,相較於安慰劑,使用化合物(
I) 50 mg,MMN幅值得到改善(變得比基線更負),但使用化合物(
I) 500 mg則沒有(
圖 13A , 圖 13B)。LS平均值相對於基線之變化在50 mg與安慰劑之間的差異在統計學上為顯著的(50 mg:-0.239 (-0.863至0.386);安慰劑:0.669 (0.012至1.326);p=0.0497;效應量:-0.691)。500 mg劑量在相對於基線之變化方面未顯示與安慰劑有顯著差異(500 mg:0.594 (-0.245至1.432);安慰劑:-0.154 (-1.008至0.700);p=0.8517;效應量:0.389)。
相較於安慰劑,使用化合物(
I) 50 mg,ASSR γ波段功率顯示數值相對於基線增加,但化合物(
I) 500 mg則沒有(
圖 14A 、 圖 14B)。50 mg劑量顯示,相較於安慰劑,ASSR γ功率相對於基線之變化更大,但其僅顯示朝向顯著性的趨勢(50 mg:2.135 (-13.127至17.396);安慰劑:-16.282 (-32.353至-0.211);p=0.056;效應量:0.575)。500 mg劑量相對於基線之變化與安慰劑相似(500 mg:9.411 (-26.018至44.480);安慰劑:9.203 (-26.981至45.387);p=0.495;效應量:0.003)。
化合物(
I)通常具有良好耐受性。不存在死亡、嚴重不良事件(AE)或導致研究藥物中斷之TEAE。另外,安全性、實驗室或ECG評定中不存在顯著結果。在所報導之五個不良事件中,所有均為輕度的且不視為與研究藥物相關,且所有患者均恢復。
總之,化合物(
I)證明在患有精神分裂症之穩定患者中MMN幅值有統計學上顯著之改善且ASSR γ波段功率在數值上亦有改善(
圖 15)。僅在50 mg之較低劑量下觀測到此等作用,而使用500 mg則沒有。此等結果支持最近完成的2期INTERACT研究(ClinicalTRials.gov:NCT03382639)之結果,該研究顯示服用化合物(
I) 50 mg持續12週的患有精神分裂症之患者的BACS及精神分裂症認知評分量表(SCoRS)有所改善,但服用化合物(
I) 500 mg的患者則沒有。所觀測到之較低劑量之較高影響(潛在反向U形劑量反應)與化合物(
I)之臨床前資料(例如在小鼠中關於長效增益進行的化合物(
I)之臨床前研究)及一般NMDA受體藥理學一致。儘管對主要EBC指標之影響不顯著,但此可能歸因於此分析之樣本量不足。總體而言,資料表明低劑量之化合物(
I)改善神經迴路活動之結果,該神經迴路活動已與NMDA受體藥理學相關且與精神分裂症中之認知表現相關。另外,與INTERACT研究發現相結合,此研究表明MMN為在更長期處理下預測認知改善之NMDA藥理學的潛在生物標記物。
實例8:評估化合物(I)在具有與精神分裂症相關之認知損傷之個體中的功效、安全性及耐受性的隨機分組、雙盲、安慰劑對照、平行組研究,之後進行開放標記處理
將進行具有12個月開放標記延長期之2b期、隨機分組、雙盲、平行、安慰劑對照研究,以評估當每日一次作為改善與精神分裂症相關之認知損傷(CIAS)之症狀的輔助處理口服投與時,化合物(
I)處理之功效、安全性及耐受性以及藥物動力學(PK)。另外,研究將評估用50 mg化合物(
I) QD處理之長期安全性及耐受性。
2b期研究將在包括(但不限於)北美洲及歐洲之地區的大約45個研究中心進行,且將征選大約308名患有精神分裂症之成人個體。各個體之研究參與之預期持續時間為大約72週,包括4週篩選、14週雙盲處理、52週開放標記處理及2週隨訪。為了儘可能客觀地獲得在用化合物(
I)處理期間症狀嚴重程度之評定結果,研究者及與研究者互動之工作人員將對以下不知情:隨機分組時間安排;指標評定時間安排;及統計分析方法之細節。
該研究將征選年齡在18歲與50歲之間的男性及女性患者,其患有如MINI版本7.0.2所界定之精神分裂症,其中患者精神分裂症之初始診斷必須在篩選(第1次訪視)之前超過一年進行。在篩選之前,個體必須具有穩定症狀持續至少3個月,且當前必須正接受精神藥物治療之穩定療程,而在篩選之前至少2個月內,處方劑量無臨床意義之變化(不增加劑量,關於耐受性之劑量降低<25%)。另外,個體必須具有限定PANSS症狀。
個體必須符合所有以下納入標準:
1.完成書面知情同意書。
2.個體必須為18至50歲(包括端點)且能夠遵守所有方案程序。
3.有如藉由精神病症診斷與統計手冊(DSM -5)所界定的精神分裂症之診斷。
4.精神分裂症之初始診斷必須在篩選前≥1年。
5.個體當前正接受精神藥物治療之穩定療程。
6.個體在篩選訪視之前≥3個月具有穩定症狀。
7.個體必須具有成人資訊提供者。
8.體重為至少45 kg且身體質量指數(BMI)為18.0至40.5 kg/m
2(包括端點)。
另外,若個體符合以下標準中之任一者,則將該等個體自研究排除:
1.懷孕或哺乳期,或計劃在研究期間懷孕。
2.展現出超過極低程度的錐體外病徵/症狀。
3.精神分裂症診斷出現在12歲之前。
4.分裂情感性精神障礙、躁鬱症或強迫症之終身診斷。
5.最近發生過恐慌症、抑鬱發作或其他共存精神病況。
6.被研究者認為有自殺或對自己、他人或財產造成傷害的迫在眉睫的風險,或在篩選前6個月內個體曾試圖自殺過。
7.在篩選之前12個月內診斷有中度或重度物質使用障礙(尼古丁依賴除外)。
8.不允許使用的物質的藥物篩查呈陽性。
9.有可能干擾研究進行或臨床評定之任何其他醫學或精神病況或認知損傷。
篩選期 ( 第 -28 天至第 -1 天 )
在篩選訪視時,提供知情同意書且如藉由簡明國際神經精神訪談(MINI)版本7.0.2所界定,滿足精神分裂症之現行診斷的個體將進行額外篩選評定以確定合格性。此外,成人資訊提供者必須提供書面知情同意書且在篩選期(第-28天至第-1天)期間在研究點參與至少一次篩選訪問。將在整個篩選期(第-28天至第-1天)期間使用藥物依從性應用程式評定對背景每日口服抗精神病藥物之依從性;使用長效可注射抗精神病藥之個體在篩選期期間將不使用藥物依從性應用程式。
雙盲處理期 ( 第 1 天至第 98 天 )
符合條件的個體將被隨機分組(1:1:2)以在14週雙盲處理期期間口服接受化合物(
I) 20 mg、化合物(
I) 50 mg或安慰劑(QD)。隨後,完成雙盲處理期且繼續進行研究處理之所有個體將進入12個月開放標記處理期且接受化合物(
I) 50 mg QD。最後一次安全性隨訪訪視將在研究處理之最後一劑後大約2週進行(第476天[第21次訪視])。研究設計示意圖提供於
圖 16A(篩選及雙盲處理期)及
圖 16B(開放標記處理及安全性隨訪期)中。
將指示個體在晨間與水或牛奶一起服用兩種錠劑(QD)且在進行研究處理之前1小時及在進行研究處理之後1小時避免飲水。化合物(
I)將以10及25 mg之匹配錠劑劑型供應以供口服投與。對研究處理之依從性將用藥物依從性應用程式監測。
個體將進行現場及虛擬研究訪視。將努力在約相同的當日時間及在整個雙盲處理期(第1天至第98天)中利用相同的評分者進行認知及認知功能評定。
在整個雙盲處理期(第1天至第98天)期間將繼續評定對背景每日口服抗精神病藥物之依從性;使用長效可注射抗精神病藥之個體將使用藥物依從性應用程式以僅記錄研究處理攝入。
開放標記處理期 ( 第 99 天至第 462 天 )
第98天(第7次訪視)評定已進行之後,繼續進行研究處理之所有個體將進入12個月的開放標記處理期且接受化合物(
I) 50 mg QD。在此期間不准許劑量減少或調整。將指示個體在第99天晨間開始服用兩種錠劑(每種25 mg) (QD)。如同在雙盲處理期一樣,將指示個體在晨間與水或牛奶一起服用兩種錠劑且在進行研究處理之前1小時及在進行研究處理之後1小時避免飲水。個體將進行現場及虛擬研究訪視。
最後一次安全性隨訪訪視將在各個體之研究處理之最後一劑之後14天進行(第476天[第21次訪視])。
功效指標
研究之主要指標將為第98天時簡易精神分裂症認知評定(BACS)綜合評分相對於基線之變化。
關鍵次要指標將為第98天時精神分裂症認知評分量表(SCoRS)訪問者評分相對於基線之變化。
其他次要指標將包括:(1)第98天時持續表現測試-相同配對(CPT-IP)測試相對於基線之變化;(2)第98天時簡易視覺空間記憶測試-修訂版(BVMT-R)測試相對於基線之變化;(3)第98天時梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)相對於基線之變化;(4)第98天時虛擬實境功能能力評定工具(VRFCAT)相對於基線之變化;及(5)第98天時臨床整體印象-嚴重程度量表(CGI-S)評分相對於基線之變化。BACS為認知評定成套測試,其評定在精神分裂症中被發現持續受損的6個認知功能領域:語言記憶、處理速度、工作記憶、語言流暢性、運動功能及執行功能。其在科學上得到驗證且對損傷具有高可靠性及敏感性(Keefe等人, 2004)。BACS評估與認知改善相關之功能之態樣,且其總體評分可用於評定總體認知功能。參見例如,Bralet MC, Navarre M, Eskenazi AM, Lucas-Ross M, Falissard B. Intérêt d'un nouvel instrument dans l'évaluation cognitive dans la schizophrénie [Interest of a new instrument to assess cognition in schizophrenia: The Brief Assessment of Cognition in Schizophrenia (BACS)]. Encephale. 2008;34(6):557-62. French。設計BACS評定以易於投與且由非心理學家評分。其經特定設計以量測處理相關之認知改善,可用於多種語言中,且具有可用於產生標準化評分之規範性資料的較大資料庫。最初以筆紙評定形式開發,基於平板電腦之BACS版本(BAC App)已開發出來且對照原始版本進行了驗證(參見例如,Atkins AS, Tseng T, Vaughan A等人 Validation of the tablet-administered Brief Assessment of Cognition (BAC App). Schizophr Res. 2017;181:100-6)且採用自動化反應捕捉及評分。BACS評定花費大約35分鐘完成。BACS將在整個雙盲處理期(第1天至第98天)中由研究者或其他合格的現場人員管理及評分。
精神分裂症認知評分量表(SCoRS)訪問者評分為經科學驗證之基於訪問之認知功能量測。其經開發以特定評定MATRICS認知功能成套測驗(MCCB)所評定的7個認知域中之每一者中所發現的認知功能態樣,MCCB為用於改善精神分裂症認知的新型藥物臨床研究之主要結果量測。參見例如,Keefe RS, Poe M, Walker TM, Kang JW, Harvey PD. 「The Schizophrenia Cognition Rating Scale: an interview-based assessment and its relationship to cognition, real-world functioning, and functional capacity.」
Am J Psychiatry.2006;163(3):426-32。該量表旨在併入自基於其與個體之互動及瞭解個體之反應的資訊提供者獲得的資訊。SCoRS包括聚焦於認知損傷及其影響日常功能之程度的20項以及總體功能量表;在隨訪訪視時,亦存在反映自個體之處理開始之變化的總體量表,由管理員、資訊提供者及個體評分。SCoRS評定花費大約12分鐘完成。SCoRS將在整個雙盲處理期(第1天至第98天)中由研究者或其他合格的現場人員管理及評分。
持續表現測試-相同配對(CPT-IP)測試評估持續注意力及警惕性。參見例如,Keilp JG, Herrera J, Stritzke P, Cornblatt BA. 「The continuous performance test, identical pairs version (CPT-IP): III. Brain functioning during performance of numbers and shapes subtasks.」
Psychiatry Res.1997;74(1):35-45。此測試為原始CPT之變體且經設計為比原始CPT更具識別挑戰性。在此電腦化測試中,150個刺激(4位數)將依序快速閃現;每當2個相同的刺激連續出現時,個體將被要求按下一個反應按鈕。在每次測試中,存在30個相同配對及相等數目個「捕捉」試驗(非常相似但不完全相同的刺激對)。剩餘90個刺激為不同的且任意組織。CPT-IP之此版本包括一系列練習序列,其最初將使用2位數作為刺激,但隨後將發展成使用4位數,其需要更多的短期記憶來正確地執行。CPT-IP對注意力及工作記憶要求高,此係由於各刺激必須首先被處理,隨後保留於工作記憶中直至下一個刺激出現,且可進行比較。CPT-IP評定花費大約10至20分鐘完成。CPT-IP將在整個雙盲處理期(第1天至第98天)中由研究者或其他合格的現場人員管理及評分。
簡易視覺空間記憶測試-修訂版(BVMT-R)測試為視覺學習及記憶之可靠評定,經設計以用作更大的神經心理學成套測試之部分且記錄隨時間推移之變化。參見例如,Tam JW, Schmitter-Edgecombe M. 「The role of processing speed in the Brief Visuospatial Memory Test - revised.」
Clin. Neuropsychol.2013;27(6):962-72。在此測試中,將要求個體根據記憶再現6個幾何圖(以2×3陣列印出)。將進行一系列試驗。在學習試驗中,個體觀看刺激頁10秒,且隨後被要求儘可能多地在反應手冊的頁面上之正確位處再現陣列。然後以類似方式進行延遲回憶試驗,但使用25分鐘的延遲。在識別試驗中,個體將被要求鑑別12個陣列中哪些係包括在原始幾何圖中的。BVMT-R評定花費大約45分鐘(包括25分鐘延遲)完成。BVMT-R將在整個雙盲處理期(第1天至第98天)中由研究者或其他合格的現場人員管理及評分。
梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)藉由評估個體在日常情況下管理自己情緒的能力來測試情商。MSCEIT經設計以量測梅耶及薩洛維之情商模型的4個分支:感知情緒、促進思考、理解情緒及管理情緒。參見例如,Mayer JD, Salovey P, Caruso D. 「Mayer-Salovey-Caruso Emotional Intelligence Test (MSCEIT) Users Manual.」 Toronto, Ontario: Multi-Health Systems. 2002。此電腦化測試係由141項組成。MSCEIT產生15個主要評分(總情商評分、2個領域評分、4個分支評分及8個任務評分)及3個補充評分。MSCEIT評定花費大約30至45分鐘完成。MSCEIT將在整個雙盲處理期(第1天至第98天)中由研究者或其他合格的現場人員管理及評分。
虛擬實境功能能力評定工具(VRFCAT)為沉浸式的基於虛擬實境之電腦化評定,其評估以下4個領域中之功能能力:交通、財務、家庭管理及計劃。簡言之,VRFCAT係由4個小場景組成,其包括檢查廚房是否有可用物品完成食譜,及計劃去往雜貨店,乘坐公交車且支付正確的車費,在商店購物,以及回家。VRFCAT為可靠且經驗證之工具,且已展現對患有精神分裂症之患者之基本功能能力缺陷的敏感性。參見例如,Keefe RSE, Davis VG, Atkins AS等人 「Validation of a computerized test of functional capacity.」
Schizophr. Res.2016;175(1-3):90-6。VRFCAT評定花費大約20分鐘完成。
「嚴重程度之臨床整體印象」或「CGI-S」為7分量表(範圍:1=不嚴重至7=非常嚴重),將用於對精神分裂症之總體的整體嚴重程度進行評分。此量表為由美國國立心理衛生研究所之精神藥理學研究處(Psychopharmacology Research Branch of the National Institute of Mental Health)開發的量表修改而成,用於對個體之臨床病症的總體改善情況進行評分,且自臨床醫生角度對隨時間推移之改善情況進行整體評估。參見例如,Guy W.編 ECDEU Assessment Manual of Psychopharmacology(修訂版), 1976. US Department of Health, Education, and Welfare. 出版號(ADM), 76-338. Rockville (MD): National Institute of Mental Health - Clinical Global Impression - Improvement. 第217-22頁。CGI-S將由研究者或其他合格現場人員管理及評分。研究者或合格的臨床醫師被指派者將在排定時間對量表進行評分。CGI-S將在整個雙盲處理期(第1天至第98天)中由研究者或其他合格的現場人員管理及評分。
「正性及負性症狀量表」、「正性及負性症候群量表」或「PANSS」為可靠的、熟知的、普遍使用的、由臨床醫師管理的經驗證之30項量表,其經設計以評估精神分裂症之各種症狀之嚴重程度,且常用於涉及抗精神病藥之臨床研究中以量測服用抗精神病藥之患者的症狀減少。參見例如,European Medicines Agency [EMA], Committee for Medicinal Products for Human Use. Guidance on the clinical investigation of medicinal products, including depot preparations in the treatment of schizophrenia. 2012; EMA/CHMP/40072/2010 Rev 1;Lehman AF, Lieberman JA, Dixon LB等人 Treatment recommendations for patients with schizophrenia. In: Practice Guideline for the Treatment of Patients with Schizophrenia. 第二版. American Psychiatric Association; 2004: 3-35 (部分A);及Kay SR, Fiszbein A, Opler LA. 「The positive and negative syndrome scale (PANSS) for schizophrenia.」
Schizophr. Bull.1987;13(2):261-76。
PANSS之分量表及PANSS之5因子模型常用於評定精神分裂症之不同症狀領域。量表劃分成3個部分,其中有7項經設計以評估正性症狀(顯現為存在特質的疾病症狀),有7項經設計以評估負性症狀(顯現為不存在特質的症狀),且有16項涉及一般精神病理學。各項按7分嚴重程度量表評分(1=不存在;2=極小;3=輕度;4=中度;5=中重度;6=重度;7=極端)。該量表亦包括3個補充項,其構成攻擊風險概況;但是,此等項將不作評分,因為其不適用於本研究。PANSS總分源自各項之總和。
如本文所使用,「改良版辛普森-安格斯量表」或「SAS」為由臨床醫生管理的評分量表,在臨床實踐及研究環境中被廣泛用於評定抗精神病藥誘發之帕金森氏症。參見例如,Simpson GM, Angus JW. 「A rating scale for extrapyramidal side effects.」
Acta Psychiatr. Scand. Suppl.1970;212:11-9。本文中描述之研究使用改良版10項SAS (用於篩選及第1天之合格性評定),其中包括於原始版本中之「下肢搖擺」及「頭部下垂」項已替換為「頭部旋轉」及「靜坐不能」,其在精神分裂症臨床試驗中已被頻繁使用。參見例如,Moore TJ, Furberg CD. 「The harms of antipsychotic drugs: evidence from key studies.」
Drug Saf.2017;40(1):3-14。使用5分量表(0-4)對各項進行評分;改良版SAS評分可在0至40範圍內。
如本文所使用,「哥倫比亞-自殺嚴重程度評分量表」或「C-SSRS」為經驗證的有證據支持的用於自殺評定之量表且預期性地評定自殺觀念及行為。參見例如,www.cssrs.columbia.edu. C-SSRS將由研究者或合格研究現場人員管理及評分。
如本文所使用,「EuroQol 5維5級」或「EQ-5D-5L」為用於描述及評估健康之一般單一指數量測。參見例如,Herdman M, Gudex C, Lloyd A, Janssen M, Kind P, Parkin D等人 「Development and preliminary testing of the new five-level version of EQ-5D (EQ-5D-5L).」
Qual. Life Res.2011;20(10):1727-36。其在5個維度方面界定健康:活動能力、自我照護、日常活動、疼痛/不適及焦慮/抑鬱。各維度具有5個級別:無問題、輕微問題、中度問題、嚴重問題及極端問題。個體藉由選中最合適的陳述旁的框來表明他/她的健康狀態。5個維度之評分可組合成描述患者之健康狀態的5位數。個體亦可用0至100的哈希標記的垂直視覺類比量表(VAS)來對其總體健康進行評分。指標被標記為「你能想像的最佳健康狀況」及「你能想像的最差健康狀況」。
EQ-5D青年版(EQ-5D-Y)為更容易理解的工具,適合於兒童及青少年。EQ-5D-Y包含2頁:EQ-5D描述性系統及EQ視覺類比量表(EQ VAS)。EQ-5D-Y描述性系統包括以下五個維度:活動能力、自我照顧、進行日常活動、有疼痛或不適以及感到擔心、悲傷或不高興。各維度具有3個級別:無問題、有一些問題及有很多問題。較年輕患者被要求在五個維度中之每一者中對最合適的陳述旁的框標示記號來表明他/她的健康狀態。EQ VAS在一個垂直視覺類比量表上記錄個體自評的健康狀況,其中指標被標記為「你能想像的最佳健康狀況」及「你能想像的最差健康狀況」。EQ-5D-5L (個體≥18歲)及EQ-5D-Y (個體13至17歲)將由研究者或合格指定人員進行管理。
如本文所使用,「簡明國際神經精神訪談」或「MINI」為修訂後的DSM第三版、DSM第四版、DSM-5以及疾病及相關健康問題國際統計分類,第十版(ICD-10)中的主要精神病症(包括精神分裂症)的簡易結構化診斷訪問。參見例如,Sheehan DV, Lecrubier Y, Sheehan KH等人 「The Mini-International Neuropsychiatric Interview (M.I.N.I.): the development and validation of a structured diagnostic psychiatric interview for DSM-IV and ICD-10.」
J. Clin. Psychiatry.1998;59 增刊20:22-33; quiz 4-57。驗證及可靠性研究已比較MINI與其他熟知的精神診斷訪問進行。此等研究之結果顯示MINI與此等工具具有相似可靠性及有效性特性,但可以短得多的時段進行管理,且臨床醫師可在簡單的訓練階段之後使用其。參見例如,Sheehan DV, Lecrubier Y, Sheehan KH等人 「The validity of the Mini International Neuropsychiatric Interview (MINI) according to the SCID-P and its reliability.」
Eur. Psychiatry.1997;12:232-41。
精神分裂症之納入標準之評定將使用MINI版本7.0.2標準化。MINI亦將用於評估共存精神病症之存在以評定個體納入之適當性。
安全性指標
安全性指標包括不良事件(AE)、臨床實驗室測試(血液學、臨床化學及尿檢)、生命體徵量測(包括立位血壓及脈搏率)、12導聯心電圖(ECG)及哥倫比亞-自殺嚴重程度評分量表(C-SSRS)。
其他指標
將評估之其他指標包括:(1)正性及負性症候群量表(PANSS)總分相對於基線之變化;(2)5級EQ-5D版本(EQ-5D-5L)視覺類比量表(VAS)評分相對於基線之變化;及(3)第1天、第14天、第42天及第98天之化合物(
I)血漿濃度。
圖 1A為描繪相較於媒劑,D-絲胺酸投與在大鼠海馬體中之短效增益方面之結果的圖式。
圖 1B為描繪相較於媒劑,D-絲胺酸投與在大鼠海馬體中之長期抑制方面之結果的圖式。
圖 1C為顯示相較於媒劑,D-絲胺酸投與在增強及抑制方面之變化的圖表。
圖 2描繪在化合物(
I)之單次口服劑量之後,化合物(
I)對小鼠海馬體突觸可塑性之影響。
圖 3描繪在化合物(
I)之亞慢性(14天)口服劑量之後,化合物(
I)對小鼠海馬體突觸可塑性之影響。
圖 4A為描繪在用化合物(
I)亞慢性給藥之後,小鼠模型中之血漿D-絲胺酸含量之圖表。
圖 4B為描繪在用化合物(
I)亞慢性給藥之後,小鼠模型中之小腦D-絲胺酸含量之圖表。
圖 5描繪化合物(
I)作為具有持久負性症狀的患有精神分裂症之成人的輔助療法的2期INTERACT研究之研究設計(ClinicalTrials.gov識別碼:NCT03382639)
圖 6為描繪入選INTERACT研究中之患者在12週處理期期間PANSS NSFS相對於基線之最小平方(LS)平均變化的圖式。
圖 7為描繪入選INTERACT研究中之患者在12週處理期期間BACS綜合評分相對於基線之最小平方(LS)平均變化的圖式。
圖 8為描繪入選INTERACT研究中之患者在12週處理期期間SCoRS訪問者總分相對於基線之最小平方(LS)平均變化的圖表。
圖 9描繪1b期研究之研究設計,其經設計以評估化合物(
I)之多個口服劑量在患有精神分裂症之患者中的藥力學作用、安全性、耐受性及藥物動力學(ClinicalTrials.gov識別碼:NCT03359785)。
圖 10描繪在評估患有精神分裂症之患者中的化合物(
I)之多個口服劑量的1b期研究中所用的眨眼制約評定(ClinicalTrials.gov識別碼:NCT03359785)。
圖 11A及
圖 11B為描繪基線(用藥前及用安慰劑前)處之失配負波(MMN)之圖式。
圖 12A為顯示在用安慰劑或化合物(
I) 50 mg處理之後,患有精神分裂症之患者中眨眼制約之最小平方平均變化的圖表。
圖 12B為顯示在用安慰劑或化合物(
I) 500 mg處理之後,患有精神分裂症之患者中眨眼制約之最小平方平均變化的圖表。
圖 13A為顯示在用安慰劑或化合物(
I) 50 mg處理之後,患有精神分裂症之患者中MMN之最小平方平均變化的圖表。
圖 13B為顯示在用安慰劑或化合物(
I) 500 mg處理之後,患有精神分裂症之患者中MMN之最小平方平均變化的圖表。
圖 14A為顯示在用安慰劑或化合物(
I) 50 mg處理之後,患有精神分裂症之患者中ASSR之最小平方平均變化的圖表。
圖 14B為顯示在用安慰劑或化合物(
I) 500 mg處理之後,患有精神分裂症之患者中ASSR之最小平方平均變化的圖表。
圖 15概述在評估患有精神分裂症之患者中的化合物(
I)之多個口服劑量的1b期研究中所觀測到的藥力學指標變化之方向性(ClinicalTrials.gov識別碼:NCT03359785)。
圖 16A及
圖 16B為評估化合物(
I)相較於安慰劑在改善患有精神分裂症之個體之認知表現方面的安全性及功效的2b期研究的研究設計示意圖。
Claims (70)
- 如請求項1之治療與精神分裂症相關之認知損傷的方法,其中該方法包含: 向該患者投與1 mg至500 mg至少一種選自化合物( I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天; 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(eye-blink conditioning;EBC)反應、該患者之失配負波(mismatch negativity;MMN)幅值及該患者之聽覺穩態反應(auditory steady state response;ASSR) γ波段功率;及 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg至少一種選自化合物( I)及其醫藥學上可接受之鹽之化合物每日一次。
- 如請求項1或2之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
- 如請求項1至3中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於該投與之前量測的該患者之簡易精神分裂症認知評定(Brief Assessment of Cognition in Schizophrenia;BACS)綜合評分,該投與改善該患者之BACS綜合評分。
- 如請求項1至4中任一項之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
- 如請求項1至5中任一項之治療與精神分裂症相關之認知損傷的方法,其中相對於該投與之前量測的該患者之精神分裂症認知評分量表(Schizophrenia Cognition Rating Scale;SCoRS)訪問者總分,該投與改善該患者之SCoRS訪問者總分。
- 如請求項1至6中任一項之治療與精神分裂症相關之認知損傷的方法,其中該投與改善至少一種選自以下之量度: 相對於該投與之前的持續表現測試-相同配對(Continuous Performance Test-Identical Pairs;CPT-IP)測試,該患者在該CPT-IP測試方面之表現; 相對於該投與之前該患者在簡易視覺空間記憶測試-修訂版(Brief Visuospatial Memory Test-Revised;BVMT-R)測試方面之表現,該患者在該BVMT-R測試方面之表現; 相對於該投與之前該患者在梅耶-薩洛維-卡魯索情緒智力測試(Mayer-Salovey-Caruso Emotional Intelligence Test;MSCEIT)方面之表現,該患者在該MSCEIT方面之表現; 相對於該投與之前該患者在虛擬實境功能能力評定工具(Virtual Reality Functional Capacity Assessment Tool;VRFCAT)方面之表現,該患者在該VRFCAT方面之表現;及 相對於該投與之前量測的該患者之臨床整體印象-嚴重程度量表(Clinical Global Impression-Severity Scale;CGI-S)評分,該患者之CGI-S評分。
- 如請求項1至7中任一項之治療與精神分裂症相關之認知損傷的方法,其中在該投與之前,該患者具有至少一種與精神分裂症相關之穩定負性症狀。
- 如請求項8之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之穩定負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
- 如請求項8之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用正性及負性症候群量表(Positive and Negative Syndrome Scale;PANSS)來評定。
- 如請求項8或9之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之穩定負性症狀的穩定性係使用簡易負性症狀量表(Brief Negative Symptom Scale;BNSS)工具來評定。
- 如請求項8至11中任一項之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之穩定負性症狀在該投與之前穩定持續至少一個月。
- 如請求項1至7中任一項之治療與精神分裂症相關之認知損傷的方法,其中在該投與之後,該患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
- 如請求項1至13中任一項之治療與精神分裂症相關之認知損傷的方法,其中該至少一種化合物係與至少一種額外活性劑組合投與。
- 如請求項14之治療與精神分裂症相關之認知損傷的方法,其中該至少一種額外活性劑治療該患者之至少一種與精神分裂症相關之負性症狀。
- 如請求項15之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
- 如請求項14之治療與精神分裂症相關之認知損傷的方法,其中該至少一種額外治療劑係選自阿立哌唑(aripiprazole)、奧氮平(olanzapine)、利培酮(risperidone)及反丁烯二酸喹硫平(quetiapine fumarate)。
- 如請求項1至17中任一項之治療與精神分裂症相關之認知損傷的方法,其中向該患者投與該至少一種化合物超過14週。
- 如請求項1至18中任一項之治療與精神分裂症相關之認知損傷的方法,其中向該患者投與該至少一種化合物超過20週。
- 如請求項1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向該患者投與1 mg至100 mg該至少一種化合物每日一次。
- 如請求項1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向該患者投與20 mg或50 mg該至少一種化合物每日一次。
- 如請求項1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向該患者投與20 mg該至少一種化合物每日一次。
- 如請求項1至19中任一項之治療與精神分裂症相關之認知損傷的方法,其中向該患者投與50 mg該至少一種化合物每日一次。
- 如請求項1至23中任一項之治療與精神分裂症相關之認知損傷的方法,其中該投與不治療至少一種與精神分裂症相關之負性症狀。
- 如請求項24之治療與精神分裂症相關之認知損傷的方法,其中該至少一種與精神分裂症相關之負性症狀係選自社交退縮、情感淡漠、失樂症狀、精力下降、動力喪失及對社交互動之興趣降低。
- 如請求項1至25中任一項之治療與精神分裂症相關之認知損傷的方法,其中該患者處於精神藥物治療之穩定療程中。
- 如請求項1至26中任一項之治療與精神分裂症相關之認知損傷的方法,其中該患者在該投與之前至少一年被診斷患有精神分裂症。
- 如請求項1至27中任一項之治療與精神分裂症相關之認知損傷的方法,其中該患者在該投與之前具有穩定症狀至少3個月。
- 如請求項29之治療認知損傷之方法,其中該方法包含: 向該患者投與治療有效量之至少一種選自化合物( I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天; 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與治療有效量之至少一種選自化合物( I)及其醫藥學上可接受之鹽之化合物每日一次。
- 如請求項29或30之治療認知損傷之方法,其中該至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
- 如請求項29至31中任一項之治療認知損傷之方法,其中該至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
- 如請求項29至32中任一項之治療認知損傷之方法,其中該投與治療該至少一種認知症狀。
- 如請求項29至33中任一項之治療認知損傷之方法,其中該至少一種認知症狀係與精神病性病症相關。
- 如請求項34之治療認知損傷之方法,其中該精神病性病症係選自精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
- 如請求項34或35之治療認知損傷之方法,其中該精神病性病症為類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
- 如請求項34至36中任一項之治療認知損傷之方法,其中該精神病性病症為與攻擊性不相關之精神分裂症。
- 如請求項29至34中任一項之治療認知損傷之方法,其中該至少一種認知症狀係與以下相關:注意力缺乏症、癡呆、阿茲海默氏病(Alzheimer's disease)、帕金森氏病(Parkinson's disease)、亨廷頓氏病(Huntington's disease)、庫欣氏病(Cushing's disease)、路易體疾病(Lewy body disease)、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群(Prader-Willi syndrome)、躁鬱症、抑鬱症及譫妄。
- 如請求項29至34中任一項之治療認知損傷之方法,其中該至少一種認知症狀係與以下相關:庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、X脆折症候群、普威二氏症候群及譫妄。
- 如請求項29至39中任一項之治療認知損傷之方法,其中向該患者投與50 mg該至少一種化合物每日一次。
- 如請求項29至39中任一項之治療認知損傷之方法,其中向該患者投與20 mg該至少一種化合物每日一次。
- 如請求項29至41中任一項之治療認知損傷之方法,其中該至少一種化合物係與至少一種額外活性劑組合投與。
- 如請求項42之治療認知損傷之方法,其中該患者患有精神分裂症且該至少一種額外活性劑治療該患者之至少一種負性症狀。
- 如請求項43之治療認知損傷之方法,其中該至少一種負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
- 如請求項29至44中任一項之治療認知損傷之方法,其中在該投與之前,該患者具有選自失樂症狀、動力喪失及對社交互動之興趣降低的至少一種穩定負性症狀。
- 如請求項1至45中任一項之治療認知損傷之方法,其中該至少一種化合物係以至少一種膜衣錠劑形式投與。
- 如請求項1至46中任一項之治療認知損傷之方法,其中該至少一種化合物係與水或牛奶一起投與。
- 如請求項48之治療至少一種與精神分裂症相關之認知症狀的方法,其中該方法包含: 向該患者投與1 mg至500 mg至少一種選自化合物( I)及其醫藥學上可接受之鹽之化合物每日一次持續6至8天; 測定或已測定該6至8天投與是否改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率;及 若該6至8天投與改善至少一種生物標記物,則繼續向該患者投與1 mg至500 mg至少一種選自化合物( I)及其醫藥學上可接受之鹽之化合物每日一次。
- 如請求項48或49之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於該投與之前量測的該患者之簡易精神分裂症認知評定(BACS)綜合評分,該投與改善該患者之BACS綜合評分。
- 如請求項48至50中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中相對於該投與之前量測的該患者之精神分裂症認知評分量表(SCoRS)訪問者總分,該投與改善該患者之SCoRS訪問者總分。
- 如請求項48至51中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中該投與改善至少一種選自以下之量度: 相對於該投與之前的持續表現測試-相同配對(CPT-IP)測試,該患者在該CPT-IP測試方面之表現; 相對於該投與之前該患者在簡易視覺空間記憶測試-修訂版(BVMT-R)測試方面之表現,該患者在該BVMT-R測試方面之表現; 相對於該投與之前該患者在梅耶-薩洛維-卡魯索情緒智力測試(MSCEIT)方面之表現,該患者在該MSCEIT方面之表現; 相對於該投與之前該患者在虛擬實境功能能力評定工具(VRFCAT)方面之表現,該患者在該VRFCAT方面之表現;及 相對於該投與之前量測的該患者之臨床整體印象-嚴重程度量表(CGI-S)評分,該患者之CGI-S評分。
- 如請求項48至52中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中在該投與之後,該患者之與精神分裂症相關之任何負性症狀不存在統計學上顯著之改善。
- 如請求項48至53中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中該投與不治療至少一種與精神分裂症相關之負性症狀。
- 如請求項54之治療至少一種與精神分裂症相關之認知症狀的方法,其中該至少一種與精神分裂症相關之負性症狀係選自失樂症狀、動力喪失及對社交互動之興趣降低。
- 如請求項48至55中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中向該患者投與50 mg該至少一種化合物每日一次。
- 如請求項48至55中任一項之治療至少一種與精神分裂症相關之認知症狀的方法,其中向該患者投與20 mg該至少一種化合物每日一次。
- 如請求項58之方法,其中向該患者投與50 mg該至少一種化合物每日一次。
- 如請求項58之方法,其中向該患者投與20 mg該至少一種化合物每日一次。
- 如請求項58至60中任一項之方法,其中該方法增加該患者之D-絲胺酸含量。
- 如請求項58至61中任一項之方法,其中該方法增加該患者之長效增益。
- 如請求項58至62中任一項之方法,其中該方法增加該患者之突觸可塑性。
- 如請求項58至63中任一項之方法,其中該患者在該投與之前展現出至少一種認知症狀。
- 如請求項64之方法,其中該至少一種認知症狀係選自語言記憶受損、工作記憶受損、運動功能受損、注意力受損、處理速度受損、語言流暢性受損及執行功能受損。
- 如請求項64之方法,其中該至少一種認知症狀係選自注意力受損、記憶受損、推理能力受損、問題解決能力受損、工作記憶受損、處理速度受損、語言功能受損及社會認知受損。
- 如請求項58至66中任一項之方法,其中該投與改善至少一種選自以下之生物標記物:該患者之眨眼制約(EBC)反應、該患者之失配負波(MMN)幅值及該患者之聽覺穩態反應(ASSR) γ波段功率。
- 如請求項58至67中任一項之方法,其中該患者罹患選自以下之疾病:注意力缺乏症、癡呆、阿茲海默氏病、帕金森氏病、亨廷頓氏病、庫欣氏病、路易體疾病、多發性硬化症、中風、成癮症、廣泛性發展障礙、自閉症、X脆折症候群、焦慮症、普威二氏症候群、躁鬱症、抑鬱症及譫妄。
- 如請求項58至67中任一項之方法,其中該患者罹患選自以下之疾病:精神病、類精神分裂症精神障礙、分裂情感性精神障礙及與攻擊性不相關之精神分裂症。
- 如請求項58至67中任一項之方法,其中該患者具有不超過中重度的與精神分裂症相關之正性症狀(PANSS正性症狀項P1 (妄想)、P3 (幻覺行為)、P4 (興奮)、P5 (自大)及/或P6 (猜疑)的評分<5)。
Applications Claiming Priority (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202163200327P | 2021-03-01 | 2021-03-01 | |
| US63/200,327 | 2021-03-01 | ||
| US202163229945P | 2021-08-05 | 2021-08-05 | |
| US63/229,945 | 2021-08-05 | ||
| US202163264747P | 2021-12-01 | 2021-12-01 | |
| US63/264,747 | 2021-12-01 | ||
| US202163265628P | 2021-12-17 | 2021-12-17 | |
| US63/265,628 | 2021-12-17 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202302109A true TW202302109A (zh) | 2023-01-16 |
Family
ID=80780614
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW111107415A TW202302109A (zh) | 2021-03-01 | 2022-03-01 | 認知損傷之治療 |
Country Status (13)
| Country | Link |
|---|---|
| EP (1) | EP4301367A1 (zh) |
| JP (1) | JP2024508860A (zh) |
| KR (1) | KR20230154217A (zh) |
| AU (1) | AU2022228417A1 (zh) |
| CA (1) | CA3209781A1 (zh) |
| CL (1) | CL2023002558A1 (zh) |
| CO (1) | CO2023011625A2 (zh) |
| DO (1) | DOP2023000174A (zh) |
| EC (1) | ECSP23065907A (zh) |
| IL (1) | IL305210A (zh) |
| PE (1) | PE20232048A1 (zh) |
| TW (1) | TW202302109A (zh) |
| WO (1) | WO2022187127A1 (zh) |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JO3115B1 (ar) | 2011-08-22 | 2017-09-20 | Takeda Pharmaceuticals Co | مركبات بيريدازينون واستخدامها كمثبطات daao |
| GB201403944D0 (en) | 2014-03-06 | 2014-04-23 | Takeda Pharmaceutical | New use |
-
2022
- 2022-02-28 EP EP22710880.0A patent/EP4301367A1/en active Pending
- 2022-02-28 IL IL305210A patent/IL305210A/en unknown
- 2022-02-28 AU AU2022228417A patent/AU2022228417A1/en active Pending
- 2022-02-28 JP JP2023552508A patent/JP2024508860A/ja active Pending
- 2022-02-28 CA CA3209781A patent/CA3209781A1/en active Pending
- 2022-02-28 PE PE2023002471A patent/PE20232048A1/es unknown
- 2022-02-28 KR KR1020237033260A patent/KR20230154217A/ko unknown
- 2022-02-28 WO PCT/US2022/018112 patent/WO2022187127A1/en active Application Filing
- 2022-03-01 TW TW111107415A patent/TW202302109A/zh unknown
-
2023
- 2023-08-30 CL CL2023002558A patent/CL2023002558A1/es unknown
- 2023-08-30 DO DO2023000174A patent/DOP2023000174A/es unknown
- 2023-08-31 EC ECSENADI202365907A patent/ECSP23065907A/es unknown
- 2023-09-01 CO CONC2023/0011625A patent/CO2023011625A2/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| KR20230154217A (ko) | 2023-11-07 |
| AU2022228417A1 (en) | 2023-10-26 |
| CL2023002558A1 (es) | 2024-03-22 |
| CA3209781A1 (en) | 2022-09-09 |
| CO2023011625A2 (es) | 2023-12-11 |
| DOP2023000174A (es) | 2024-01-31 |
| IL305210A (en) | 2023-10-01 |
| ECSP23065907A (es) | 2023-09-29 |
| JP2024508860A (ja) | 2024-02-28 |
| PE20232048A1 (es) | 2023-12-27 |
| WO2022187127A1 (en) | 2022-09-09 |
| EP4301367A1 (en) | 2024-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Arnold et al. | Placebo-controlled pilot trial of mecamylamine for treatment of autism spectrum disorders | |
| RU2563821C2 (ru) | Применение 4-аминопиридина для улучшения состояния при нейрокогнитивном и/или нейропсихиатрическом нарушении у пациентов с демиелинизирующими и другими заболеваниями нервной системы | |
| CN110402140A (zh) | 加波沙朵在治疗耳鸣中的用途 | |
| EA022755B1 (ru) | Способы длительной терапии с применением аминопиридинов | |
| CN107835695A (zh) | 用于治疗自闭症的组合物和方法 | |
| TWI592156B (zh) | 使用胺基吡啶以治療與中風有關之感覺動作損傷之方法 | |
| KR20120050512A (ko) | 탈수초를 갖는 환자에서 4-아미노피리딘을 사용한 지속적 치료 | |
| US11826321B2 (en) | Cyclobenzaprine treatment for agitation, psychosis and cognitive decline in dementia and neurodegenerative conditions | |
| TW202102219A (zh) | 使用氘化右旋美沙芬(dextromethorphan)及奎尼丁(quinidine)治療精神分裂症之負面徵候之方法 | |
| WO2020123900A1 (en) | Deutetrabenazine for the treatment of dyskinesia in cerebral palsy | |
| TW202302109A (zh) | 認知損傷之治療 | |
| Seifert | Drugs Easily Explained | |
| CN117580576A (zh) | Luvadaxistat用于治疗认知损害的用途 | |
| WO2023250036A1 (en) | Cyclobenzaprine treatment for post-acute sequelae of (sars)-cov-2 infection (pasc) | |
| Jokwiro | Buddy Nurse | |
| TW202131910A (zh) | 使用mtorc1調節劑的治療方法 | |
| CA3219829A1 (en) | Method of treating essential tremor | |
| US20210212999A1 (en) | Use of riluzole prodrugs to treat alzheimer's disease | |
| EA044015B1 (ru) | Дейтетрабеназин для лечения дискинезии при церебральном параличе | |
| EP3243516A1 (en) | Methods for treating sensorimotor impairments associated with certain types of stroke using aminopyridines | |
| Penttilä | Own observation of an adverse reaction: delirium in an adolescent patient with the use of cephalexin | |
| Wahlroos | The impact of written information about medicinal products is limited | |
| Rajalahti et al. | The medicines treatment of tuberculosis, a challenge for the patient and the health care staff | |
| Juppo | Special challenges involved with regard to medicinal products appropriate for children |